Курс физики. Том I. Механика, акустика, молекулярная физика, термодинамика
Курс физики. Том I. Механика, акустика, молекулярная физика, термодинамика
ОглавлениеПРЕДИСЛОВИЕВВЕДЕНИЕ ЧАСТЬ ПЕРВАЯ. ФИЗИЧЕСКИЕ ОСНОВЫ МЕХАНИКИ И АКУСТИКА § 1. О взаимосвязи явлений и допустимых границах их схематизации в физике § 2. Система ориентировки. Материальная точка и ее перемещение § 3. Элементарное перемещение. Векторы скорости и ускорения § 4. Тангенциальное и центростремительное ускорения § 5. Угловая скорость и угловое ускорение § 6. Абсолютное, переносное и относительное движения § 7. Закон сложения ускорений ГЛАВА II. ЗАКОНЫ НЬЮТОНА § 9. Первый ньютонов закон механики (закон инерции) § 10. О понятиях «покоя» и «равномерности» § 11. Инерциальная система. Принцип относительности § 13. Различные понимания второго закона механики § 14. Движение под действием постоянной силы § 15. Третий ньютонов закон механики § 16. Статическое и динамическое проявления сил § 17. Силы инерции.  Центробежная сила Центробежная силаГЛАВА III. РАБОТА И ЭНЕРГИЯ § 18. Работа, энергия, мощность. Элемент и интеграл работы § 19. Кинетическая энергия и потенциальная энергия § 20. Системы мер и размерность механических величин ГЛАВА IV. ДИНАМИКА СИСТЕМЫ § 21. Механическая система. Внутренние и внешние силы. Центр масс § 22. Закон сохранения количества движения и теорема о движении центра масс § 24. Число степеней свободы и работа сил связи. Принцип возможных перемещений § 25. Принцип Даламбера и релятивистское понимание инерции ГЛАВА V. МЕХАНИЧЕСКАЯ ПЕРЕДАЧА СИЛ И ЭНЕРГИИ (ТРЕНИЕ, УДАР, ТЯГА) § 26. Трение. Тяга § 27. Удар ГЛАВА VI. ЗАКОН ВСЕМИРНОГО ТЯГОТЕНИЯ И ЭЛЕМЕНТЫ НЕБЕСНОЙ МЕХАНИКИ § 28. Законы Кеплера § 29. Ньютонов закон тяготения § 30. Зависимость веса и ускорения силы тяжести от высоты и географической широты местности § 31.  § 32. Потенциальная энергия и потенциал тяготения § 33. Некоторые теоремы о потенциале тяготения § 34. Потенциальная энергия системы частиц ГЛАВА VII. ДИНАМИКА ВРАЩАТЕЛЬНОГО ДВИЖЕНИЯ ТВЕРДЫХ ТЕЛ § 35. Момент силы § 36. Кинетическая энергия вращательного движения. Момент инерции § 37. Основное уравнение динамики вращательного движения § 38. Закон сохранения момента количества движения § 39. Проявление поворотных (кориолисовых) сил инерции ГЛАВА VIII. ЭЛЕМЕНТЫ ТЕОРИИ УПРУГОСТИ И МЕХАНИЧЕСКИЕ СВОЙСТВА ТЕЛ § 40. Упругие свойства тел § 42. Модуль объемной упругости. Сжимаемость § 43. Модуль Юнга, коэффициент Пуассона, модуль сдвига и соотношение между ними § 44. Характеристика механических свойств твердого тела по диаграмме растяжения. Явление наклепа § 45. Пластичность § 46. Прочность и твердость § 47. Механические свойства важнейших материалов ГЛАВА IX.  ОСНОВЫ ГИДРОДИНАМИКИ И АЭРОДИНАМИКИ ОСНОВЫ ГИДРОДИНАМИКИ И АЭРОДИНАМИКИ§ 48. Основные понятия и направления гидродинамики § 49. Уравнение Бернулли § 50. Гидравлическая энергия § 51. Вязкость и течение жидкости при трении § 52. Пограничный слой и вихреобразование. Строение турбулентного потока § 54. Числа Рейнольдса. Кинематическая вязкость § 55. Аэродинамические силы. Подъемная сила крыла и тяга самолета ГЛАВА X. КОЛЕБАТЕЛЬНОЕ ДВИЖЕНИЕ § 56. Гармоническое колебание § 57. Энергия и собственная частота гармонических колебаний § 58. Сложение колебаний одинаковой частоты и одинакового направления (интерференция колебаний) § 59. Другие случаи сложения колебаний § 60. Затухающие колебания § 61. Вынужденные колебания. Резонанс § 62. Связанные колебания ГЛАВА XI. УЧЕНИЕ О ВОЛНАХ § 63. Волновой процесс. Уравнение волн. Виды волн § 64. Интерференция волн. Стоячие волны § 65. Фазовая и групповая скорости волн  АКУСТИКА АКУСТИКА§ 66. Звук как физическое явление. Распространение звуковых волн § 67. Интенсивность звука § 68. Частота и состав звуков § 69. Явление Допплера § 70. Звук как психофизиологическое явление. Механизм звукового восприятия § 71. Высота и тембр звука § 72. Ультразвуки ЧАСТЬ ВТОРАЯ. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА § 73. Исторические сведения. Картина молекулярного движения § 74. Статистический метод в физике § 75. Термодинамический метод § 76. Термодинамическая характеристика состояния тел и термодинамические процессы § 78. Внутренняя энергия. Теплота и работа. Уравнение первого начала § 79. Изобарная и изотермическая работа газа § 80. Термохимические уравнения ГЛАВА XIV. ОСНОВЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ § 81. Схематизация явлений («модели» в молекулярной физике) § 82. Максвеллов закон распределения молекулярных скоростей в газе § 83. Основное уравнение кинетической теории газов § 84.  Молекулярно-кинетическое понимание абсолютной температуры Молекулярно-кинетическое понимание абсолютной температуры§ 85. Об уточненном (термодинамическом) понимании абсолютной температуры § 87. Максвеллова теория газовых теплоемкостей § 88. Молекулярно-кинетическое пояснение работы расширения газа § 89. Средний свободный пробег газовых молекул ГЛАВА XV. ТЕПЛОПЕРЕДАЧА, ДИФФУЗИЯ И ВЯЗКОСТЬ. ВАКУУМ § 90. Тепловое излучение (законы Стефана и Ньютона) § 91. Теплопроводность (закон Фурье) § 92. Диффузия (закон Фика) § 93. Молекулярная теория теплопроводности газов § 94. Молекулярная теория вязкости газов § 95. Сопоставление явлений диффузии, теплопроводности и вязкости газов § 96. Вакуум. Манометры § 97. Вакуумные насосы § 98. Термодинамическое равновесие и e-положение Больцмана § 99. Ограничения, налагаемые вторым началом термодинамики на циклические превращения тепла в работу § 100. 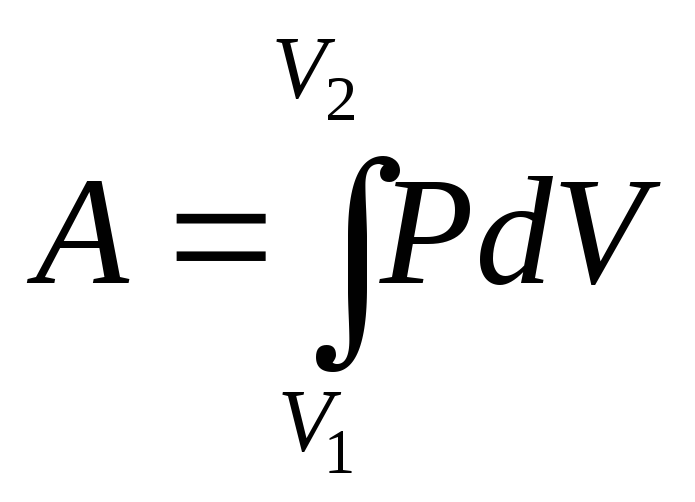 Уравнение Пуассона. Адиабатная работа газа Уравнение Пуассона. Адиабатная работа газа§ 101. Цикл Карно и теорема о сумме приведенных теплот § 102. Энтропия. Основное уравнение термодинамики § 103. Процессы обратимые и необратимые. Теорема о возрастании энтропии § 104. Статистический смысл энтропии § 105. Теоремы о термодинамическом равновесии. Свободная энергия и термодинамический потенциал § 107. Уравнения Гиббса — Гельмгольца и Клапейрона—Клаузиуса ГЛАВА XVII. ФИЗИКА РЕАЛЬНЫХ ГАЗОВ И ПАРОВ. УРАВНЕНИЕ ВАН-ДЕР-ВАЛЬСА § 108. Пары насыщенные и перегретые. Диаграмма Эндрюса § 109. Конденсация газов § 110. Уравнение Ван-дер-Вальса § 111. Учение о соответственных состояниях § 112. О качественных превращениях при тепловых процессах ГЛАВА XVIII. ФИЗИКА ЖИДКОСТЕЙ § 113. Механические и термодинамические свойства жидкостей § 114. Поверхностное натяжение § 115. Формула Лапласа. Явления капиллярности и смачивания § 116. Поверхностноактивные вещества § 117.  § 118. Кинетика испарения. Зависимость давления насыщенного пара от кривизны поверхности жидкости. Формула Томсона — Шиллера § 119. Понижение давления пара над раствором и повышение температуры кипения растворов. Законы Рауля § 120. Осмотическое давление. Закон Вант-Гоффа § 121. Электролитическая диссоциация. Закон Оствальда § 122. Абсорбция. Закон Генри § 123. О столкновении противоположных процессов в молекулярно-тепловых явлениях ГЛАВА XIX. ФИЗИКА ТВЕРДЫХ ТЕЛ § 124. Строение кристаллов § 125. Понятие о кристаллохимии § 126. Форма и рост кристаллов § 127. Теплоемкость твердых тел § 128. Сублимация твердых тел. Тройная точка § 130. Силы связи в кристаллах § 131. Адсорбция ГЛАВА XX. ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ В ДВИГАТЕЛЯХ И СВЕРХЗВУКОВОЕ ДВИЖЕНИЕ § 132. Основное уравнение газодинамики. Адиабатный теплоперепад § 133. Адиабатное течение газа § 134.  Ударные волны и скачки уплотнения. Адиабата Гюгонио Ударные волны и скачки уплотнения. Адиабата Гюгонио§ 135. Процессы в двигателях внутреннего сгорания § 136. Процессы в паровых машинах и паровых турбинах § 137. Реактивные двигатели |
Термодинамическая работа. Работа газа | Физика. Закон, формула, лекция, шпаргалка, шпора, доклад, ГДЗ, решебник, конспект, кратко
Загрузка…
В механике работа, которая выполняется силой F, равна произведению значения этой силы на перемещение x и на косинус угла между ними: A = Fx cos α.
Вычисление выполненной работы в термодинамике связывают с макропараметрами системы. Рассмотрим газ, находящийся в цилиндре под поршнем площадью S (рис. 2.1, а).
Пусть на газ действует поршень, принуждая его сжиматься. Под действием силы F̅ поршень смещается вниз на высоту Δh = h2 — h1 (рис. 2.1, б), выполняя работу A = FΔh (направление действия силы совпадает с направлением перемещения, поэтому cos α = 1). Если перемещение поршня незначительное, то давление газа можно считать постоянным (p = const). Поршень будет двигаться до тех пор, пока не уравновесятся силы F̅ и F̅’, то есть согласно третьему закону Ньютона сила F по модулю должна равняться силе давления газа F’. Приняв во внимание, что F = pS, a SΔh = ΔV, получим:
2.1, б), выполняя работу A = FΔh (направление действия силы совпадает с направлением перемещения, поэтому cos α = 1). Если перемещение поршня незначительное, то давление газа можно считать постоянным (p = const). Поршень будет двигаться до тех пор, пока не уравновесятся силы F̅ и F̅’, то есть согласно третьему закону Ньютона сила F по модулю должна равняться силе давления газа F’. Приняв во внимание, что F = pS, a SΔh = ΔV, получим:
A = pS(h2 — h1) = pAV.
Поскольку V2 < V1, следовательно, ΔV < 0, то работа внешних сил над газом будет равна:
A = —pΔV.
Рис. 2.1, а. Работа газа при уменьшении объема 2.1, а. Работа газа при уменьшении объема |
| Рис. 2.1, б. Работа газа при увеличении объема |
Если под действием силы давления F’ газ расширяется (рис. 2.1, б), то есть сам выполняет работу A’ = pS(h2 — h1), то ее значение также равно pΔV. Вместе с тем в данном случае выполненная газом работа положительная, поскольку V2 > V1 и ΔV > 0:
Загрузка…
A’ = pΔV.
Работу газа можно вычислить по графику термодинамического процесса. Так, для изобарного процесса (рис. 2.2) работа газа A’ = pΔV равна площади прямоугольника, ограниченного изобарой и осью ординат V, а также прямыми, отвечающими значениям объемов V1 и V2.
Для произвольных процессов на координатной плоскости pV работу графически вычисляют таким же способом — находят площадь фигуры, ограниченную графиком процесса (изотермой), осью V и линиями, фиксирующими изменение объема. Например, для изотермического процесса, в котором давление изменяется обратно пропорционально объему (рис. 2.3), площадь фигуры ABCD делят на небольшие участки и вычисляют площадь каждого из них. Потом складывают полученные результаты и определяют общую работу газа: A = A1 + A2 + …
При незначительных изменениях объема или постоянном давлении формулы работы A = —pΔV и A’ = pΔV справедливы не только для газов, но и для других термодинамических систем. Поскольку изменение объема при постоянном давлении сопровождается изменением температуры тела, то можно сделать вывод, что
выполнение работы в термодинамике вызывает изменение состояния тела, так как изменяются его температура T и объем V. Материал с сайта http://worldofschool.ru
Материал с сайта http://worldofschool.ru
| Рис. 2.2. Графическое вычисление работы газа для изобарного процесса |
| Рис. 2.3. Графическое вычисление работы газа для изотермического процесса |
На этой странице материал по темам:
Вопросы по этому материалу:
Как определяют работу в механике?
Почему работа газа и работа внешних сил над газом отличаются знаками?
Как можно вычислить работу по графику термодинамического процесса?
Материал с сайта http://WorldOfSchool.ru
Рассчитайте работу системы давление-объем при расширении газа с 1 литра до 2 литров при постоянном внешнем давлении 10 атмосфер.
 Выразите ответ в калориях и джоулях.
Выразите ответ в калориях и джоулях.Ответ
Проверено
291,3 тыс.+ просмотров
Подсказка : Давление – Объем выполненной работы происходит при изменении объема газа или системы. Работа, совершаемая системой, — это энергия, передаваемая от нее к окружающей среде. Выразите эту работу в джоулях и калориях, -${{P}_{external}}$$\times $$\vartriangle V$.
Полный пошаговый ответ:
Если газ нагревается, молекулы газа получают энергию. Увеличение средней кинетической энергии молекул газа можно наблюдать, измеряя, как увеличилась температура частиц газа. Молекулы газа чаще сталкиваются с поршнем из-за быстрого движения частиц газа. Эти частые столкновения передают энергию поршню и позволяют ему двигаться против внешнего давления, тем самым увеличивая полезный объем газа.
Работа, совершаемая газом, заключается именно в расширении и сжатии газа. Работу, совершаемую газами, иногда называют работой давление-объем или PV .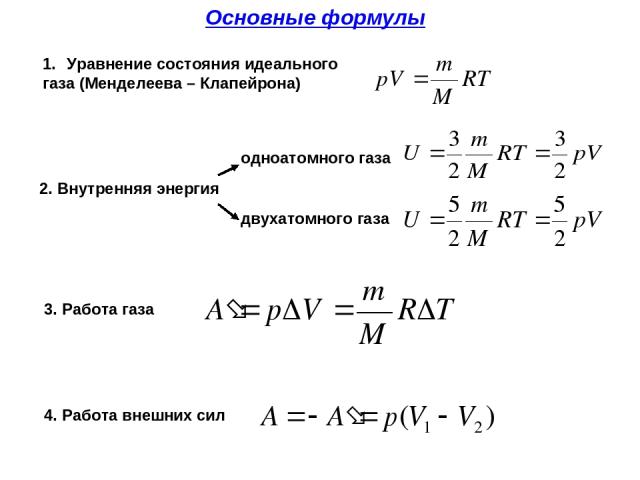
Чтобы вычислить, какую работу совершает (или совершил) газ при постоянном внешнем давлении, мы должны использовать уравнение:
РАБОТА = (w) = -${{P}_{внешнее}}$ $\times $$\vartriangle V$, где внешнее давление обозначается через ${{P}_{внешнее}}$. Внешнее давление противодействует давлению газа в системе. ∆V — изменение объема газа, которое рассчитывается как ${{V}_{final}}-{{V}_{\operatorname{in}initial}}$.
Знаковое соглашение о работе :
Когда система воздействует на окружающую среду, говорят, что произошла отрицательная работа.
Когда газ совершает работу, объем частиц газа уменьшается ($\vartriangle V$<0). Произведенная работа положительна.
Когда газ совершает работу, объем частиц газа увеличивается ($\vartriangle V$>0). Произведенная работа отрицательна.
Преобразование единиц:
Работа измеряется в ДЖОУЛЯХ.
Работа давление-объем выражается в л-атм, которые должны быть преобразованы в джоули с использованием коэффициента пересчета 101,325 Дж/1 л-атм
Для преобразования джоулей в калории коэффициент преобразования составляет 0,239 кал/1 Дж.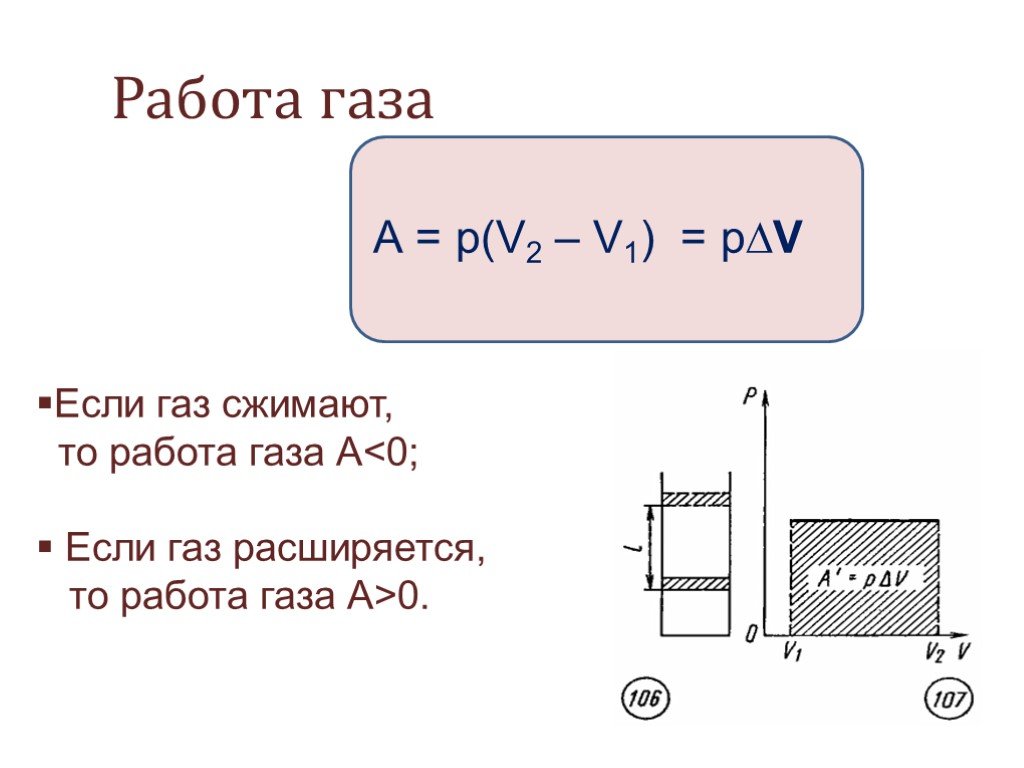
Рассчитайте работу давления-объема, выполненную газом:
Дано: ${{P}_{внешнее}}$= 10 атмосфер ${{V}_{исходное}}$= 1 литр ${{V}_{ final}}$ = 2 литра
Используйте формулу, чтобы вычислить работу, выполненную газом:
WORK= (w) = -${{P}_{external}}$$\times $$\vartriangle V$
Подставьте значения как ${{V}_{final}}-{{V}_{\operatorname{in}initial}}$
Чистая формула:
= -${{P}_{external}}$$ \times $(${{V}_{final}}-{{V}_{\operatorname{in}initial}}$)
Замените значения ${{P}_{external}}$,${{V}_{initial}}$, ${{V}_{final}}$ на 10 атмосфер, 1 литр и 2 литра.
Совершенная работа равна
= – (10 атм)$\times $(2 литра – 1 литр)
= – (10 атм)$\times $(1 литр)
= – (10 литров-атм)
Перевести литры атм в джоули с использованием коэффициента преобразования:
1 л-атм имеет 101,325 Дж, поэтому -10 л-атм имеет (-10)$\times $(101,325Дж) равно (-1013,25 Дж. )
Чтобы преобразовать джоули в калорий умножьте джоуль на коэффициент 0,239 (0,239)
$\times $(-1013,25) равно – 242,16 калорий.
Ответ на вопрос: -1013,25 Дж и -242,16 калорий.
Примечание :
(i) При подсчете выполненной работы соблюдайте правила знаков. Так как условность знаков у газа и на газе разная.
(ii) Не забудьте преобразовать, чтобы использовать коэффициент преобразования для требуемых единиц, как указано в вопросе.
Дата последнего обновления: 21 апреля 2023 г.
•
Всего просмотров: 291.3k
•
Просмотров сегодня: 4.74k
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк класс 12 химия JEE_Main
Mg может быть Ser и Mg Ba могут быть Ser и Mg Ba щелочноземельные металлы химический состав 12 класса JEE_Main
Что из следующего имеет самый высокий электродный потенциал Химический класс 12 JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 химический класс 12 JEE_Main
Какой элемент обладает наибольшим атомным радиусом А 11 класс химии JEE_Main
Фосфин получают из следующей руды Кальций 12 класс химии JEE_Main
В Индии по случаю бракосочетания фейерверки 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть расположены химический класс 12 JEE_Main
Что из следующего имеет самый высокий электродный потенциал химический класс 12 JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 химический класс 12 JEE_Main
Какой элемент обладает наибольшим атомным радиусом? Химический класс 11 JEE_Main
Фосфин получают из следующей руды. Химический класс кальция 12 JEE_Main
Химический класс кальция 12 JEE_Main
Актуальные сомнения
Закон идеального газа | Определение, формула и факты
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Этот день в истории
- Викторины
- Подкасты
- Словарь
- Биографии
- Резюме
- Популярные вопросы
- Инфографика
- Демистификация
- Списки
- #WTFact
- Товарищи
- Галереи изображений
- Прожектор
- Форум
- Один хороший факт
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Britannica объясняет
В этих видеороликах Britannica объясняет различные темы и отвечает на часто задаваемые вопросы.
- Britannica Classics
Посмотрите эти ретро-видео из архивов Encyclopedia Britannica. - Demystified Videos
В Demystified у Britannica есть все ответы на ваши животрепещущие вопросы. - #WTFact Videos
В #WTFact Britannica делится некоторыми из самых странных фактов, которые мы можем найти. - На этот раз в истории
В этих видеороликах узнайте, что произошло в этом месяце (или любом другом месяце!) в истории.
- Студенческий портал
Britannica — это главный ресурс для учащихся по ключевым школьным предметам, таким как история, государственное управление, литература и т. д. - Портал COVID-19
Хотя этот глобальный кризис в области здравоохранения продолжает развиваться, может быть полезно обратиться к прошлым пандемиям, чтобы лучше понять, как реагировать сегодня. - 100 Women
Britannica празднует столетие Девятнадцатой поправки, выделяя суфражисток и политиков, творящих историю.

