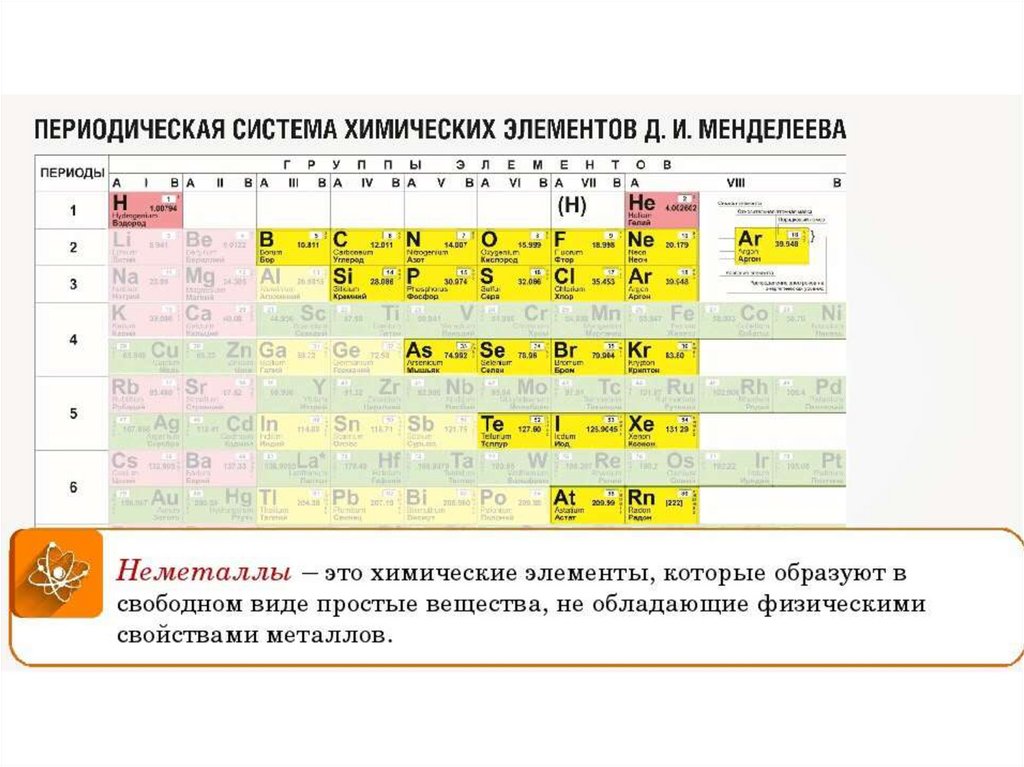
Таблица Менделеева online – Щелочные металлы
Щелочные металлы — это элементы 1-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы главной подгруппы I группы): литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щелочами.
Общая характеристика группы
В Периодической системе они следуют сразу за инертными газами, поэтому особенность строения атомов щелочных металлов заключается в том, что они содержат один электрон на внешнем энергетическом уровне: их электронная конфигурация ns1. Очевидно, что валентные электроны щелочных металлов могут быть легко удалены, потому что атому энергетически выгодно отдать электрон и приобрести конфигурацию инертного газа. Поэтому для всех щелочных металлов характерны восстановительные свойства. Это подтверждают низкие значения их потенциалов ионизации (потенциал ионизации атома цезия — самый низкий) и электроотрицательности. Как следствие, в большинстве соединений щелочные металлы присутствуют в виде однозарядных катионов. Однако существуют и соединения, где щелочные металлы представлены анионами.
Как следствие, в большинстве соединений щелочные металлы присутствуют в виде однозарядных катионов. Однако существуют и соединения, где щелочные металлы представлены анионами.
Некоторые атомные и физические свойства элементов группы
| Атомный номер |
Название, символ |
Число природных изотопов | Атомная масса | Энергия ионизации, кДж*моль−1 | Сродство к электрону, кДж*моль−1 | ЭО | ΔHдисс, кДж*моль−1 | Металл. радиус, нм | Ионный радиус (КЧ 6), нм | tпл, °C |
tкип, °C |
ρ, г/см³ |
ΔHпл, кДж*моль−1 | ΔHкип, кДж*моль−1 | ΔHобр, кДж*моль−1 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 3 | Литий Li | 2 | 6,941(2) | 520,2 | 59,8 | 0,98 | 106,5 | 0,076 | 180,6 | 1342 | 0,534 | 2,93 | 148 | 162 | |
| 11 | Натрий Na | 1 | 22,989768(6) | 495,8 | 52,9 | 0,99 | 73,6 | 0,186 | 0,102 | 97,8 | 883 | 0,968 | 2,64 | 99 | 108 |
| 19 | Калий К | 2+1а | 39,0983(1) | 418,8 | 0,82 | 57,3 | 0,227 | 0,138 | 63,07 | 759 | 0,856 | 2,39 | 79 | 89,6 | |
| 37 | Рубидий Rb | 1+1а | 85,4687(3) | 403,0 | 46,88 | 0,82 | 45,6 | 0,248 | 0,152 | 39,5 | 688 | 1,532 | 2,20 | 76 | 82 |
| 55 | Цезий Cs | 1 | 132,90543(5) | 375,7 | 45,5 | 0,79 | 44,77 | 0,265 | 0,167 | 28,4 | 671 | 1,90 | 2,09 | 67 | 78,2 |
| 87 | Франций Fr | 1а | (223) | 380 | (44,0) | 0,7 | — | — | 0,180 | 20 | 690 | 1,87 | 2 | 65 | — |
Все металлы этой подгруппы имеют серебристо-белый цвет (кроме серебристо-жёлтого цезия), они очень мягкие, их можно резать скальпелем. Литий, натрий и калий легче воды и плавают на её поверхности, реагируя с ней.
Литий, натрий и калий легче воды и плавают на её поверхности, реагируя с ней.
Группы химических элементов | это… Что такое Группы химических элементов?
Группа химических элементов — термин, используемый ИЮПАК для описания номенклатурной классификации химических элементов[1].
Содержание
|
Названия групп химических элементов, утверждённые ИЮПАК
- Щелочные металлы — металлы первой группы: Li, Na, K, Rb, Cs, Fr.
- Щелочноземельные металлы — металлы второй группы: Be, Mg, Ca, Sr, Ba, Ra.
- Пниктогены (пниктиды[2]) — элементы пятнадцатой группы: N, P, As, Sb, Bi.

- Халькогены — элементы шестнадцатой группы: O, S, Se, Te, Po.
- Галогены (галоиды
- Инертные газы — элементы восемнадцатой группы: He, Ne, Ar, Kr, Xe, Rn.
- Лантаноиды (лантаниды[2]) — элементы 57—71: La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu.
- Актиноиды (актиниды[2]) — элементы 89—103: Ac, Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr.
- Редкоземельные элементы — Sc, Y и лантаноиды.
- Переходные металлы — элементы 3—12 групп.
Другие группы химических элементов
Многие другие названия для групп элементов не утверждены ИЮПАК, но употребляются в различных областях науки. Например:
- Платиновая группа — Ru, Rh, Pd, Os, Ir, Pt.
- Благородные металлы — термин, который в основном используется для описания элементов, не подвергающихся коррозии — Au, Ag и металлы платиновой группы.
- Тяжёлые металлы — термин, использующийся для описания элементов с высокими значениями атомного веса.

- Природные металлы — металлы, находящиеся в природе; не являются искусственно полученными.
- Постпереходные металлы — металлы, у которых наблюдается полное заполнение d-подоболочки: Zn, Ga, Cd, In, Sn, Hg, Tl, Pb, Bi.
- Лёгкие металлы — термин, иногда использующийся для описания некоторых металлов p-блока: алюминий, галлий, индий, олово, таллий, свинец и висмут (иногда в эту группу включают также германий, сурьму и полоний).
- Трансурановые элементы, трансураны — элементы, следующие за ураном (атомный номер больше 92).
- Трансплутониевые элементы — элементы, следующие за плутонием (атомный номер больше 94).
- Трансфермиевые элементы — элементы, следующие за фермием (атомный номер больше 100).
- Трансактиноидные элементы, трансактиноиды — элементы, следующие за актиноидами (атомный номер больше 103).
- Суперактиноиды — гипотетически возможная группа элементов, с атомными номерами 121—153 (которые входят в g-блок).
- Тяжёлый атом — термин, используемый в компьютерной химии для описания всех элементов, кроме водорода и гелия.

- Металлы — термин, используемый в астрофизике для описания всех элементов, кроме водорода и гелия.
Геохимические группы элементов
Основная статья: Геохимические классификации элементов
Классификация Гольдшмидта
- Атмофильные элементы — склонные к накоплению в атмосфере Земли, включают в себя водород, азот и инертные газы.
- Халькофильные элементы — элементы сульфидных руд. К ним относятся S, Cu, Zn, Ga, Ge, As, Se, Ag, Cd, In, Sn, Sb, Te, Au, Hg, Tl, Pb, Bi, Po.
- Литофильные элементы — обладающие сродством к силикатным минералам и расплавам. К ним относятся Al, At, B, Ba, Be, Br, Ca, Cl, Cr, Cs, F, I, Hf, K, Li, Mg, Na, Nb, O, P, Rb, Sc, Si, Sr, Ta, Th, Ti, U, V, Y, Zr, W, лантаноиды.
- Сидерофильные элементы обладают сродством к железу. К ним относятся Au, Co, Fe, Ir, Mn, Mo, Ni, Os, Pd, Pt, Re, Rh, Ru.
Другие классификации
- Петрогенные элементы — основные элементы, составляющие породы и минералы: O, Si, Ti, Al, Mg, Fe, Ca, K, Mn, P, Na, K
- Редкие и рассеянные элементы — все остальные элементы
Биохимические группы элементов
Основная статья: Биологически значимые элементы
- Биологически значимые элементы
- Макроэлементы — суточное поступление в организм человека более 200 мг
- Биогенные (органогенные) элементы — кислород, углерод, водород и азот
- Другие макроэлементы — калий, кальций, магний, натрий, сера, фосфор, хлор
- Микроэлементы — бор, фтор, кремний, ванадий, хром, марганец, железо, кобальт, никель, медь, цинк, мышьяк, селен, молибден, иод
- Макроэлементы — суточное поступление в организм человека более 200 мг
- Биологически инертные элементы
Примечания
- ↑ IUPAC Provisional Recommendations for the Nomenclature of Inorganic Chemistry (англ.
 ) (2004). — Online draft of an updated version of the “Red Book” IR 3—6.2. Проверено 22 августа 2010.
) (2004). — Online draft of an updated version of the “Red Book” IR 3—6.2. Проверено 22 августа 2010. - ↑ 1 2 3 4 Устаревший вариант названия, не рекомендован к использованию.
Группа 1: Водород и щелочные металлы
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 589
Щелочные металлы — это химические элементы, находящиеся в группе 1 периодической таблицы. К щелочным металлам относятся: литий, натрий, калий, рубидий, цезий и франций. Хотя водород часто относят к Группе 1 из-за его электронной конфигурации, технически он не является щелочным металлом, поскольку редко проявляет подобное поведение.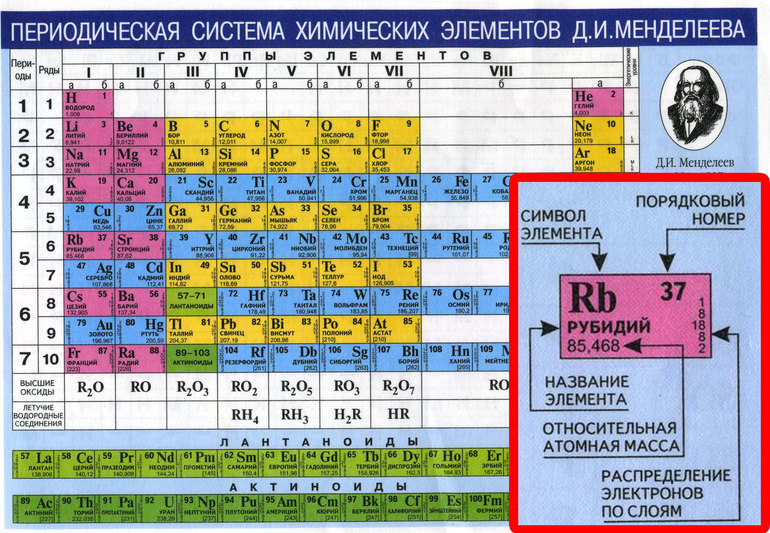
- Группа 1: Свойства щелочных металлов
- На этой странице обсуждаются тенденции изменения некоторых атомных и физических свойств элементов группы 1 – лития, натрия, калия, рубидия и цезия. Разделы ниже охватывают тенденции изменения атомного радиуса, энергии первой ионизации, электроотрицательности, температур плавления и кипения и плотности.
- Lithium Group (Группа IA) Тенденции
- Группа 1: Реакционная способность щелочных металлов
- Щелочные металлы относятся к числу наиболее реакционноспособных металлов. Частично это связано с их большими атомными радиусами и низкими энергиями ионизации. Они склонны отдавать свои электроны в реакциях и имеют степень окисления +1.
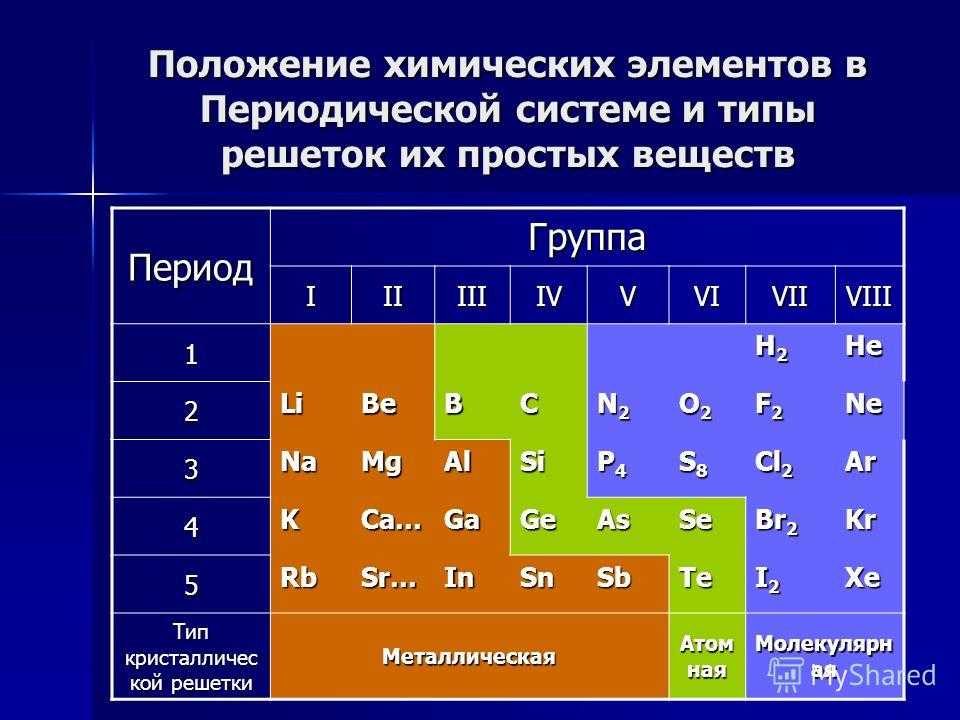 Эти металлы отличаются мягкой текстурой и серебристым цветом. Они также имеют низкие температуры кипения и плавления и менее плотны, чем большинство элементов. Все эти характеристики можно объяснить большими атомными радиусами этих элементов и слабой металлической связью.
Эти металлы отличаются мягкой текстурой и серебристым цветом. Они также имеют низкие температуры кипения и плавления и менее плотны, чем большинство элементов. Все эти характеристики можно объяснить большими атомными радиусами этих элементов и слабой металлической связью. - Flame Tests
- Group 1 Compounds
- Reactions of Group 1 Elements with Water
- Reactions of Group I Elements with Chlorine
- Reactions of Group I Elements with Oxygen
- Chemistry of Hydrogen ( Z=1)
- Водород является одним из самых важных элементов в мире. Это все вокруг нас. Он входит в состав воды (h3O), жиров, нефти, столового сахара (C6h22O6), аммиака (Nh4) и перекиси водорода (h3O2) — веществ, необходимых для жизни, какими мы их знаем. Этот модуль исследует несколько аспектов элемента и то, как они применяются в мире.

- Химия лития (Z=3)
- Перекись водорода
- Химия лития (Z=3) Считается, что он не является жизненно важным для биологических процессов человека, хотя он используется во многих лекарственных препаратах из-за его положительного воздействия на мозг человека. Из-за его реактивных свойств люди использовали литий в батареях, реакциях ядерного синтеза и термоядерном оружии.
- Химия натрия (Z=11)
- Натрий — металлический элемент, находящийся в первой группе периодической таблицы. Как шестой по распространенности элемент в земной коре, соединения натрия обычно растворяются в океанах, в минералах и даже в наших телах.
- Карбонат натрия
- Химический состав калия (Z=19)
- В чистом виде калий имеет беловато-серебристый цвет, но при контакте с воздухом быстро окисляется.
 не хранится под маслом или смазкой. Калий необходим для некоторых аспектов жизни растений, животных и человека, поэтому его добывают, производят и потребляют в огромных количествах по всему миру.
не хранится под маслом или смазкой. Калий необходим для некоторых аспектов жизни растений, животных и человека, поэтому его добывают, производят и потребляют в огромных количествах по всему миру. - Карбонат калия (Potash)
- Химический состав рубидия (Z=37)
- Рубидий (лат. rubidius = красный) по физическим и химическим характеристикам похож на калий, но гораздо более реактивен. Это семнадцатый по распространенности элемент, открытый Бунзеном и Кирхгофом по его красному спектральному излучению в 1861 году. Его температура плавления настолько низка, что его можно растопить в руке, если у вас жар (39°C). Но это не лучшая идея, потому что он будет бурно реагировать с влагой в вашей коже.
- Химия цезия (Z=55)
- Цезий настолько активен, что может взорваться даже при контакте со льдом! Он использовался в качестве «геттера» при производстве электронных ламп (т.
 Е. Он помогает удалять следовые количества оставшихся газов). В атомных часах используется изотоп цезия.
Е. Он помогает удалять следовые количества оставшихся газов). В атомных часах используется изотоп цезия.
- Химия франция (Z=87)
- Франций является последним из известных щелочных металлов и не встречается в природе в значительных количествах. Все известные изотопы радиоактивны и имеют короткий период полураспада (22 минуты — самый длинный).
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Глава
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.

- Теги
Характеристики элементов группы 1 и группы 2 периодической таблицы
Основное различие между компонентами группы 1 и группы 2 заключается в том, что каждый компонент группы 1 имеет неспаренные электроны на самой внешней орбите, тогда как компоненты группы 2 имеют спаренные электроны на внешней орбите. их крайняя орбиталь.
Компоненты блока S находятся в группах 1 и 2 периодической таблицы. Это значит; у этих частей самые внешние электроны находятся на s-орбитали. Первая и вторая группы отличаются друг от друга количеством электронов на их самой внешней орбите. Одна s-орбиталь будет содержать только 2 электрона, так как магнитное квантовое число этой орбитали равно 0.
Элементы первой группы называются щелочными металлами; группы 2 – щелочноземельные металлы; в пятнадцати — пниктогены; шестнадцать – халькогены; в семнадцати – галогены; а те, что в восемнадцати, – благородные газы.
Элементы первой группы — это химические элементы, имеющие один электрон на внешней s-орбитали. это первый столбец блока s табличного массива. Он содержит водород и щелочные металлы. Члены этой группы 1 следующие:
Водород (H)
Литий (Li)
Натрий (Na)
Калий (K)
Рубидий (Rb)
Цезий (Cs)
8 Fr)
Хотя водород принадлежит к этой группе из-за его электронной структуры, он отличается от щелочных металлов по нескольким параметрам. Например, водород существует в виде газа, в то время как другие элементы этой группы являются металлами. Все эти металлы блестящие, чрезвычайно реактивные и очень мягкие (мы будем просто резать их простым ножом).
Как правило, элементы группы 1 имеют низкую плотность, низкую температуру плавления, низкую температуру кипения и объемно-центрированную коробчатую кристаллическую структуру. Более того, им нужны отчетливые цвета пламени, поэтому мы можем просто отличить их, подставив образец к газовой горелке. Существуют периодические различия по мере прохождения группы щелочных металлов, как показано ниже.
Существуют периодические различия по мере прохождения группы щелочных металлов, как показано ниже.
Размер атома будет увеличиваться
- Температура плавления {температура замерзания|температура} и точка кипения снижаются из-за гибкости для создания прочных связей, уменьшающихся в группе (когда атом становится большим, образованная связь становится слабой).
- Плотность увеличится.
- Первая энергия ионизации уменьшается из-за массивных атомов, крайний электрон слабо связан, и он просто будет удален.
- Уменьшение электроотрицательности
- Уменьшение реактивности.
- Щелочные металлы имеют более низкое сродство к электрону, чем другие части
Каковы характеристики элементов 2-й группы Периодической таблицы
Элементы 2-й группы — это химические элементы, у которых самая внешняя электронная пара находится на s-орбитали. Поэтому их валентные электроны имеют форму ns2. Далее, эта группа является вторым столбцом блока s.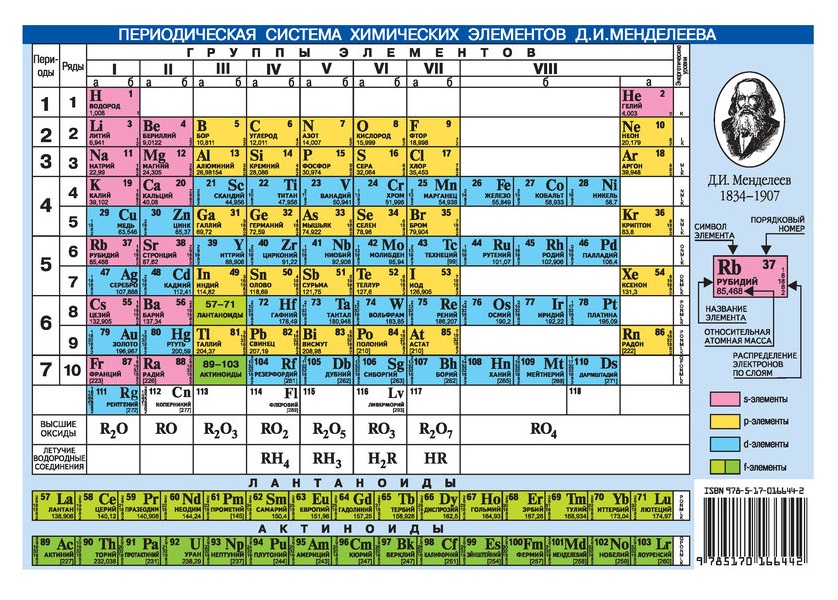 Мы называем их щелочноземельными металлами. Члены этой кластерной единицы области следующим образом:
Мы называем их щелочноземельными металлами. Члены этой кластерной единицы области следующим образом:
Бериллий (Be)
Магний (Mg)
Кальций (Ca)
Стронций (Sr)
Барий (Ba)
Радий (Ra)
Какая разница? Элементы таблицы Менделеева в группах 1 и 2
Группа 1 и пара отличаются друг от друга в зависимости от количества электронов на их внешней орбите. Ключевое различие между элементами группы 1 и группы 2 заключается в том, что все элементы группы 1 имеют непарные электроны на их самой внешней орбитали, тогда как элементы группы 2 имеют спаренные электроны на своей внешней орбитали.
Приведенная ниже инфографика показывает множество сравнений, касающихся различий между элементами группы 1 и группы 2.
Group 1 vs group 2 elements
Group 1 elements | Group 2 elements | |
Definition | Group 1 elements are chemical elements having an unpaired electron in outermost s орбитальный | Элементы группы 2 — это химические элементы, у которых самая удаленная пара элементов находится в s необязательно |
Valence electrons | One | Two |
Members | Lithium ,sodium ,potassium ,rubidium, Cesium and francium ,along with hydrogen | Бериллий, магний, кальций, стронций, барий и радий |
Другие названия | Щелочной металл вместе с водородом | Alkaline earth metal |
Reactivity | High reactive | Less reactive compared to group 1 |
Melting and boiling point | Comparatively low | Very высокая |
Натуральная | Мягкий металл | Твердый металл |
Катионы | Образование катиона путем удаления одного валентного электрона | Образование катиона путем удаления двух электронов s |
Особенности современной таблицы Менделеева.
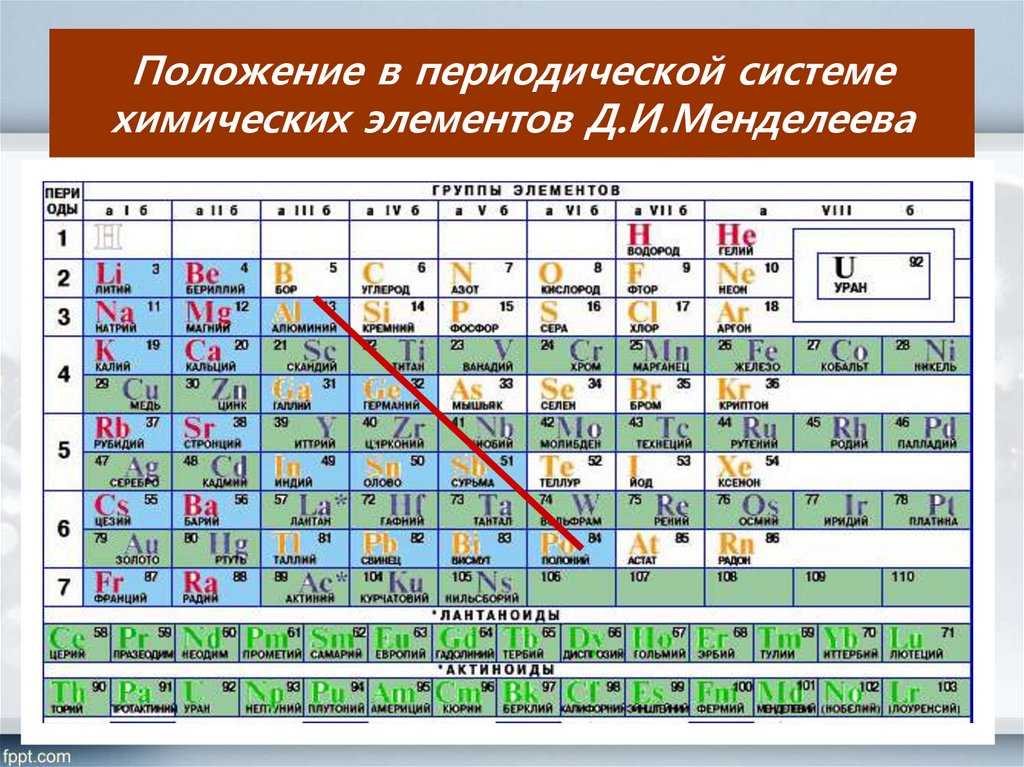
Периодическая таблица группирует элементы на основе их химических и физических свойств. В таблице есть строки и столбцы. В периодической таблице вертикальные столбцы обозначают группы. Горизонтальные строки в таблице представляют периоды. Элементы расположены в порядке возрастания их атомного номера.
В таблице семь периодов и восемнадцать групп.
Инертные газы, т.е. He, Ne, Ar и т. д. …
Все группы разделены на подгруппы A и B, кроме нулевой и VIII группы в современной табличной матрице. Три широких класса деталей: металлы, неметаллы, и металлоиды. Большинство деталей металлические. Неметаллы размещены в правой части табличного массива. Металлоиды обладают свойствами как металлов, так и неметаллов. Современный табличный массив основан на современном периодическом законе, и части расположены в порядке возрастания их атомных номеров. Современный табличный массив состоит из 18 вертикальных столбцов, известных как группы. части любой группы периодической таблицы имеют сходные физические и химические свойства.