Предложена новая форма таблицы периодических элементов
Как и в прошлый раз, идея пришла в голову российским химикам.
Российские химики Артем Оганов и Захед Аллахьяри предложили новый вариант таблицы периодических элементов, созданной в 1869 году Дмитрием Менделеевым.
В периодической таблице Менделеева, знакомой каждому из нас со школьной скамьи, элементы упорядочены по атомному номеру (количеству протонов в атомном ядре), а также по химическому сходству. Последнее следует из расположения электронов в оболочках.
Однако среди ученых по-прежнему существуют разногласия по поводу того, где следует разместить некоторые элементы, пишет The Conversation. Это зависит от того, какие именно свойства мы хотим выделить. Таблица Менделеева, которая отдает приоритет электронной структуре атомов, будет отличаться от таблиц, для которых главными критериями являются определенные химические или физические свойства. Эти версии не сильно различаются, но есть определенные элементы, например водород, которые можно расположить совершенно по-разному в зависимости от конкретного свойства, которое нужно выделить. В некоторых таблицах водород помещен в группу 1, тогда как в других он находится наверху группы 17; некоторые таблицы даже включают его в отдельную группу.
Эти версии не сильно различаются, но есть определенные элементы, например водород, которые можно расположить совершенно по-разному в зависимости от конкретного свойства, которое нужно выделить. В некоторых таблицах водород помещен в группу 1, тогда как в других он находится наверху группы 17; некоторые таблицы даже включают его в отдельную группу.
Однако Артем Оганов и Захед Аллахьяри в своей статье, опубликованной в журнале Journal of Physical Chemistry, предложили более радикальный вариант изменения принципа расстановки элементов. Их подход заключается в присвоении каждому элементу так называемого числа Менделеева (MN). Для его получения используется комбинация двух фундаментальных величин: атомного радиуса элемента и свойства, называемого электроотрицательностью, которое описывает, насколько сильно атом притягивает к себе валентные электроны других атомов.
Если упорядочить элементы по их MN, можно построить двумерную таблицу на основе MN элементов, составляющих бинарные соединения. Такой подход позволяет предсказать свойства бинарных соединений, которые еще не были созданы. Это полезно при поиске новых материалов, которые могут понадобиться как для будущих, так и для существующих технологий.
Такой подход позволяет предсказать свойства бинарных соединений, которые еще не были созданы. Это полезно при поиске новых материалов, которые могут понадобиться как для будущих, так и для существующих технологий.
Со временем принцип может быть распространен на соединения, содержащие более двух элементарных компонентов.
Изображение: Shutterstock, Артем Оганов и Захед Аллахьяри
Названы лауреаты Нобелевской премии 2020 года по химии
Неизвестный Менделеев
На сайте могут быть использованы материалы интернет-ресурсов Facebook и Instagram, владельцем которых является компания Meta Platforms Inc., запрещённая на территории Российской Федерации
Расскажите друзьям
Фрагмент рукописи
Museum of the Bible
Найдена часть утерянного древнейшего звездного каталога — 2000-летней рукописи Гиппарха
Visualization by B. MéNard & N.
 Shtarkman
Shtarkman13 млрд лет за несколько движений мышкой: опубликована крупнейшая интерактивная карта Вселенной
Космонавт Роскосмоса Анна Кикина отправилась на МКС на корабле Crew Dragon
Shutterstock
Исследование показало, как настроение матери влияет на способность ее ребенка говорить
Библиотека Кембриджского университета
Древняя грамматическая загадка решена спустя 2500 лет
Хотите быть в курсе последних событий в науке?
Оставьте ваш email и подпишитесь на нашу рассылку
Ваш e-mail
Нажимая на кнопку «Подписаться», вы соглашаетесь на обработку персональных данных
Житель Свердловской области заявляет, что открыл новый химический элемент, завершающий таблицу Менделеева
В России
время публикации: 26 сентября 2007 г.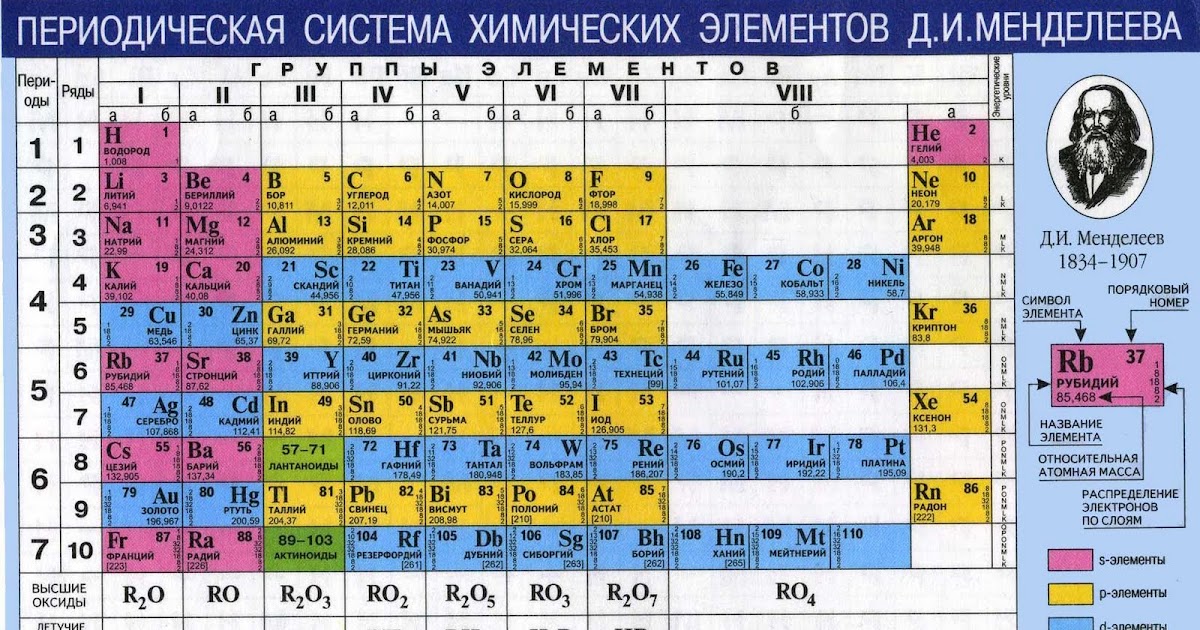 , 17:54 | последнее обновление: 06 декабря 2017 г., 14:05
, 17:54 | последнее обновление: 06 декабря 2017 г., 14:05
Архив NEWSru.com
Инженер из города Полевского Свердловской области обратился в Институт патентоведения Всероссийского общества изобретателей и рационализаторов с заявлением об открытии 119-го элемента периодической таблицы химических элементов Менделеева.
Как сообщил “Интерфаксу” руководитель института Алексей Зыков в среду, житель Полевского – не первый, кто сообщает об открытии новых составляющих таблицы, но его точка зрения достаточна интересна.
“В домашних условиях получить такой элемент невозможно, но интересен ход мысли. Он считает, что этот элемент состоит из электронного ряда всех элементов таблицы и завершает ее. Также он сообщает, что этот элемент в 299 раз тяжелее водорода”, – рассказал Зыков.
Собеседник агентства напомнил, что в настоящее время государство
отказалось от практики регистрации открытий, существовавшей в советское
время. “Теперь необходимо подтверждение опытами и признание научной
общественности. Однако инженер подал заявку на патентование способа
обнаружения 119-го элемента”, – пояснил Зыков.
“Теперь необходимо подтверждение опытами и признание научной
общественности. Однако инженер подал заявку на патентование способа
обнаружения 119-го элемента”, – пояснил Зыков.
Досье NEWSru.com :: Наука и технологии :: Химия :: Открытия
Каталог NEWSru.com :: Информационные интернет-ресурсы
ССЫЛКИ ПО ТЕМЕ
В России | 17 октября 2006 г.,
Ученые России и США получили 118-й элемент, самый тяжелый на Земле
В России | 30 мая 2006 г.,
Российские ученые подтвердили существование 112-го элемента Периодической таблицы Менделеева
В мире
|
29 сентября 2004 г.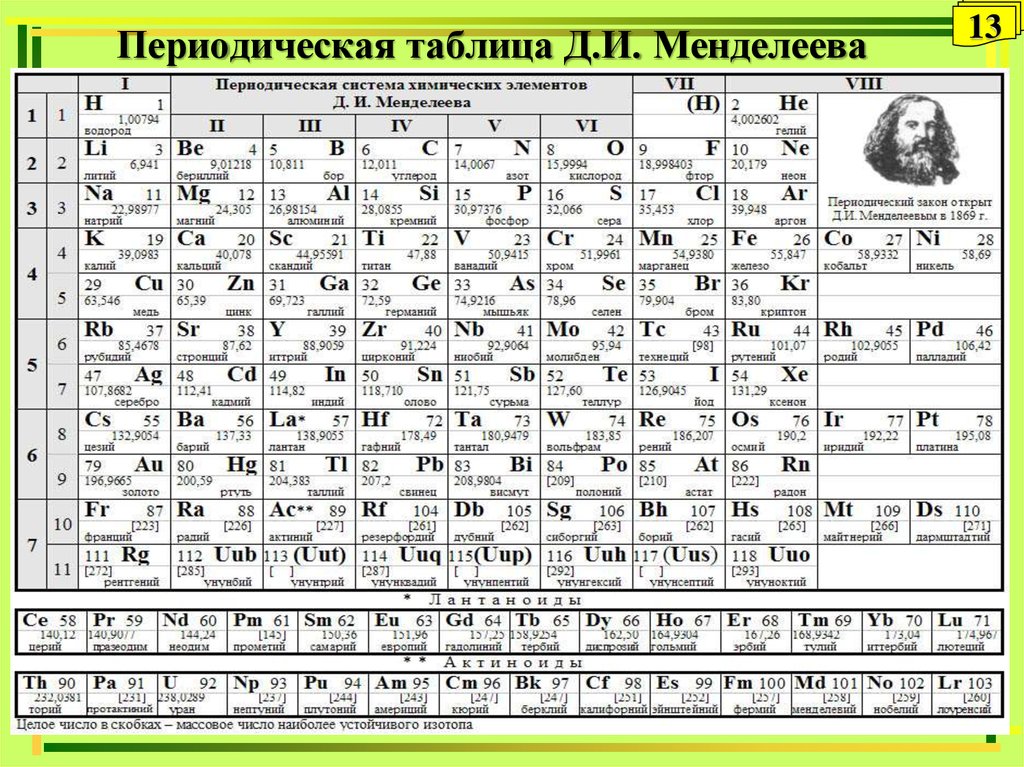
В Японии получен самый тяжелый химический элемент
В России | 17 июня 2003 г.,
Российские ученые открыли новые элементы в таблице Менделеева
В России | 07 августа 2002 г.,
Российские ученые готовятся получить 118-й элемент, ранее объявленный несуществующим
В мире | 15 июля 2002 г.,
Новые химические вещества, открытые три года назад, оказались фикцией
ПОСЛЕДНИЕ НОВОСТИ РАЗДЕЛА
09:00
Спасибо всем, кто был с нами в течение 21 года
09:00
АРХИВ NEWSru.com остается открытым: все, что было в любой день в любой год с начала века
09:00
Какой была новостная картина в этот день – 31 мая в каждый год за последние 20 лет
20:26
В Екатеринбурге мужчина открыл стрельбу с балкона, ранены девочка и сотрудник Росгвардии (ВИДЕО)
19:33
Рамзан Кадыров и министр культуры Ольга Любимова вместе снимут документальный фильм о культурных объектах Чечни
17:18
В Новосибирске скончался молодой человек, которому выстрелил в голову инспектор ДПС
13:13
Собянин объяснил рост заболеваемости COVID-19 в Москве праздниками и особенностями весеннего сезона
Галоген | Элементы, примеры, свойства, использование и факты
Таблица Менделеева
Просмотреть все СМИ
- Ключевые люди:
- Жан-Батист-Андре Дюма
- Похожие темы:
- галогенорганическое соединение йод фтор хлор бром
Просмотреть весь связанный контент →
Популярные вопросы
Что такое галогенные элементы?
Галогенные элементы представляют собой шесть элементов 17-й группы периодической таблицы. Группа 17 занимает вторую колонку справа в периодической таблице и содержит фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Астат и теннессин являются радиоактивными элементами с очень коротким периодом полураспада и поэтому не встречаются в природе.
Группа 17 занимает вторую колонку справа в периодической таблице и содержит фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Астат и теннессин являются радиоактивными элементами с очень коротким периодом полураспада и поэтому не встречаются в природе.
Каковы основные свойства галогенных элементов?
Галогенные элементы очень реакционноспособны. С натрием они производят соли, из которых наиболее известна поваренная соль (хлорид натрия, NaCl). Каждый атом галогена имеет семь валентных электронов на внешней электронной оболочке. Поэтому, когда атом галогена может получить электрон от атома другого элемента, два атома образуют очень стабильное соединение, потому что тогда самая внешняя электронная оболочка атома галогена заполнена.
В каких случаях используются галогеновые элементы?
Хлор используется для очистки воды. Кроме того, хлор входит в состав поваренной соли, хлорида натрия, который является одним из наиболее широко используемых химических соединений. Фтор используется во фторидах, которые добавляют в воду для предотвращения кариеса. Йод используется как антисептик.
Фтор используется во фторидах, которые добавляют в воду для предотвращения кариеса. Йод используется как антисептик.
Почему эти элементы называются галогенами?
При взаимодействии этих элементов с натрием образуются соли. Наиболее известным из них является хлорид натрия или обычная поваренная соль (также называемая галитом). Слово
Сводка
Прочтите краткий обзор этой темы
галоген , любой из шести неметаллических элементов, составляющих группу 17 (группа VIIa) периодической таблицы. Галогенсодержащие элементы: фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Им дали название галоген 9.0046 , от греческих корней hal – («соль») и – gen («производить»), потому что все они производят натриевые соли со схожими свойствами, из которых лучше всего подходит хлорид натрия — поваренная соль, или галит.
Свободные галогены не встречаются в природе из-за их большой реакционной способности. В комбинированной форме фтор является самым распространенным из галогенов в земной коре. Процентное содержание галогенов в изверженных породах земной коры: фтора 0,06, хлора 0,031, брома 0,00016, йода 0,00003. Астатин и теннессин не встречаются в природе, так как состоят только из короткоживущих радиоактивных изотопов.
Галогенные элементы имеют большое сходство друг с другом по своему общему химическому поведению и свойствам их соединений с другими элементами. Однако наблюдается постепенное изменение свойств от фтора через хлор, бром и йод к астату — разница между двумя последовательными элементами наиболее заметна для фтора и хлора. Фтор является наиболее реакционноспособным из галогенов и, по сути, из всех элементов, и у него есть некоторые другие свойства, которые отличают его от других галогенов.
Хлор является наиболее известным из галогенных элементов. Свободный элемент широко используется в качестве реагента для очистки воды и используется в ряде химических процессов. Поваренная соль, хлорид натрия, безусловно, является одним из самых привычных химических соединений. Фториды известны главным образом тем, что их добавляют в воду для предотвращения кариеса, но органические фториды также используются в качестве хладагентов и смазочных материалов. Йод наиболее известен как антисептик, а бром используется в основном для получения соединений брома, которые используются в антипиренах и в качестве пестицидов общего назначения. В прошлом дибромид этилена широко использовался в качестве присадки к этилированному бензину.
Поваренная соль, хлорид натрия, безусловно, является одним из самых привычных химических соединений. Фториды известны главным образом тем, что их добавляют в воду для предотвращения кариеса, но органические фториды также используются в качестве хладагентов и смазочных материалов. Йод наиболее известен как антисептик, а бром используется в основном для получения соединений брома, которые используются в антипиренах и в качестве пестицидов общего назначения. В прошлом дибромид этилена широко использовался в качестве присадки к этилированному бензину.
Вероятно, самое важное обобщение, которое можно сделать о галогенных элементах, состоит в том, что все они являются окислителями; то есть они повышают степень окисления или степень окисления других элементов – свойство, которое раньше приравнивалось к соединению с кислородом, но теперь интерпретируется в терминах переноса электронов от одного атома к другому. При окислении другого элемента восстанавливается сам галоген; т. е. степень окисления 0 свободного элемента снижается до -1. Галогены могут соединяться с другими элементами, образуя соединения, известные как галогениды, а именно фториды, хлориды, бромиды, йодиды и астатиды. Многие из галогенидов можно рассматривать как соли соответствующих галогеноводородов, которые при комнатной температуре и атмосферном давлении представляют собой бесцветные газы и (за исключением фтороводорода) образуют в водном растворе сильные кислоты. Действительно, общий термин 9Соль 0045 получают из каменной или поваренной соли (хлорида натрия). Склонность галогенных элементов к образованию солеобразных (т. е. высокоионных) соединений возрастает в следующем порядке: астат < йод < бром < хлор < фтор. Фториды обычно более стабильны, чем соответствующие хлориды, бромиды или иодиды. (Часто астат опускают из общих рассуждений о галогенах, потому что о нем известно меньше, чем о других элементах.)
Галогены могут соединяться с другими элементами, образуя соединения, известные как галогениды, а именно фториды, хлориды, бромиды, йодиды и астатиды. Многие из галогенидов можно рассматривать как соли соответствующих галогеноводородов, которые при комнатной температуре и атмосферном давлении представляют собой бесцветные газы и (за исключением фтороводорода) образуют в водном растворе сильные кислоты. Действительно, общий термин 9Соль 0045 получают из каменной или поваренной соли (хлорида натрия). Склонность галогенных элементов к образованию солеобразных (т. е. высокоионных) соединений возрастает в следующем порядке: астат < йод < бром < хлор < фтор. Фториды обычно более стабильны, чем соответствующие хлориды, бромиды или иодиды. (Часто астат опускают из общих рассуждений о галогенах, потому что о нем известно меньше, чем о других элементах.)
Окислительная сила галогенов возрастает в том же порядке, т. е. от астата к фтору. Поэтому из галогенных элементов с наибольшим трудом получается элементарный фтор, с наименьшим – йод.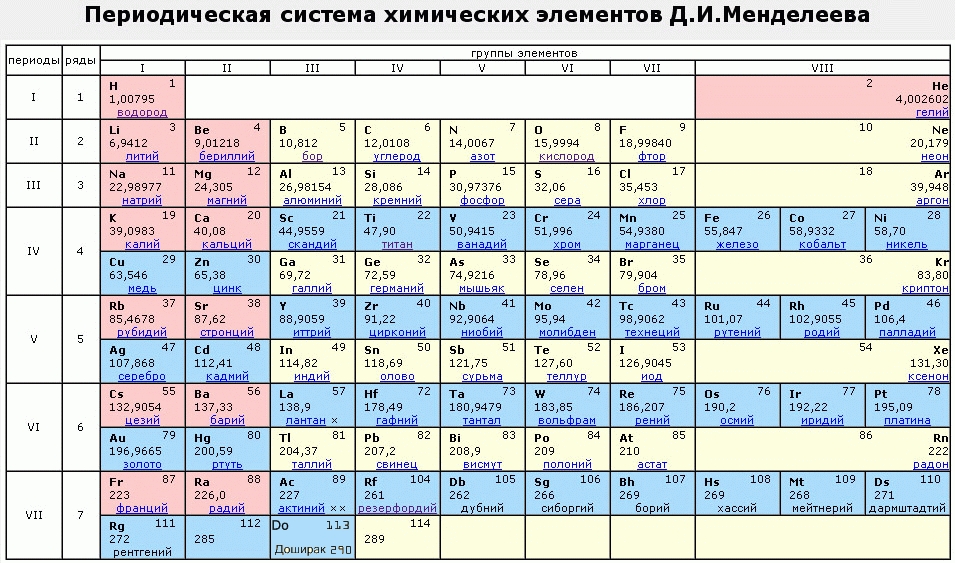 Галогенные элементы как класс относятся к неметаллам, но астат проявляет определенные свойства, напоминающие свойства металлов.
Галогенные элементы как класс относятся к неметаллам, но астат проявляет определенные свойства, напоминающие свойства металлов.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Химическое поведение галогенных элементов удобнее всего обсуждать с точки зрения их положения в периодической таблице элементов. В периодической таблице галогены составляют группу 17 (согласно системе нумерации, принятой Международным союзом теоретической и прикладной химии), группу, непосредственно предшествующую благородным газам. Атомы галогенов несут семь валентных электронов на внешней электронной оболочке. Эти семь крайних электронов находятся на двух различных орбиталях, обозначенных как 9.0045 s (с двумя электронами) и p (с пятью). Потенциально атом галогена может содержать еще один электрон (на орбитали p ), что придаст образующемуся иону галогенида такое же расположение (конфигурацию), что и благородный газ рядом с ним в периодической таблице. Эти электронные конфигурации исключительно стабильны. Эта ярко выраженная склонность галогенов приобретать дополнительный электрон делает их сильными окислителями.
Эти электронные конфигурации исключительно стабильны. Эта ярко выраженная склонность галогенов приобретать дополнительный электрон делает их сильными окислителями.
При комнатной температуре и атмосферном давлении галогенные элементы в свободном состоянии существуют в виде двухатомных молекул. В молекулярном фторе (F 2 ) атомы удерживаются вместе связью, состоящей из объединения p орбиталей каждого атома, при этом такая связь классифицируется как сигма-связь. Следует отметить, что энергия диссоциации фтора (энергия, необходимая для разрыва связи F—F) более чем на 30 % меньше, чем у хлора, но аналогична энергии йода (I 2 ). Слабость одинарной связи F—F по сравнению с хлором можно объяснить небольшим размером фтора, что приводит к уменьшению перекрывания связывающих орбиталей и увеличению отталкивания несвязывающих орбиталей. Однако в йоде p орбитали более размыты, что означает, что связь становится слабее, чем в хлоре или броме.
Галоген | Элементы, примеры, свойства, использование и факты
Таблица Менделеева
Просмотреть все СМИ
- Ключевые люди:
- Жан-Батист-Андре Дюма
- Похожие темы:
- галогенорганическое соединение йод фтор хлор бром
Просмотреть всю связанную информацию →
Самые популярные вопросы
Что такое галогенные элементы?
Галогенные элементы представляют собой шесть элементов 17-й группы периодической таблицы. Группа 17 занимает вторую колонку справа в периодической таблице и содержит фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Астат и теннессин являются радиоактивными элементами с очень коротким периодом полураспада и поэтому не встречаются в природе.
Группа 17 занимает вторую колонку справа в периодической таблице и содержит фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Астат и теннессин являются радиоактивными элементами с очень коротким периодом полураспада и поэтому не встречаются в природе.
Каковы основные свойства галогенных элементов?
Галогенные элементы очень реакционноспособны. С натрием они производят соли, из которых наиболее известна поваренная соль (хлорид натрия, NaCl). Каждый атом галогена имеет семь валентных электронов на внешней электронной оболочке. Поэтому, когда атом галогена может получить электрон от атома другого элемента, два атома образуют очень стабильное соединение, потому что тогда самая внешняя электронная оболочка атома галогена заполнена.
В каких случаях используются галогеновые элементы?
Хлор используется для очистки воды. Кроме того, хлор входит в состав поваренной соли, хлорида натрия, который является одним из наиболее широко используемых химических соединений. Фтор используется во фторидах, которые добавляют в воду для предотвращения кариеса. Йод используется как антисептик.
Фтор используется во фторидах, которые добавляют в воду для предотвращения кариеса. Йод используется как антисептик.
Почему эти элементы называются галогенами?
При взаимодействии этих элементов с натрием образуются соли. Наиболее известным из них является хлорид натрия или обычная поваренная соль (также называемая галитом). Слово галоген происходит от греческих корней hal-, что означает «соль», и -gen , что означает «производить».
Сводка
Прочтите краткий обзор этой темы
галоген , любой из шести неметаллических элементов, составляющих группу 17 (группа VIIa) периодической таблицы. Галогенсодержащие элементы: фтор (F), хлор (Cl), бром (Br), йод (I), астат (At) и теннессин (Ts). Им дали название галоген 9.0046 , от греческих корней hal – («соль») и – gen («производить»), потому что все они производят натриевые соли со схожими свойствами, из которых лучше всего подходит хлорид натрия — поваренная соль, или галит.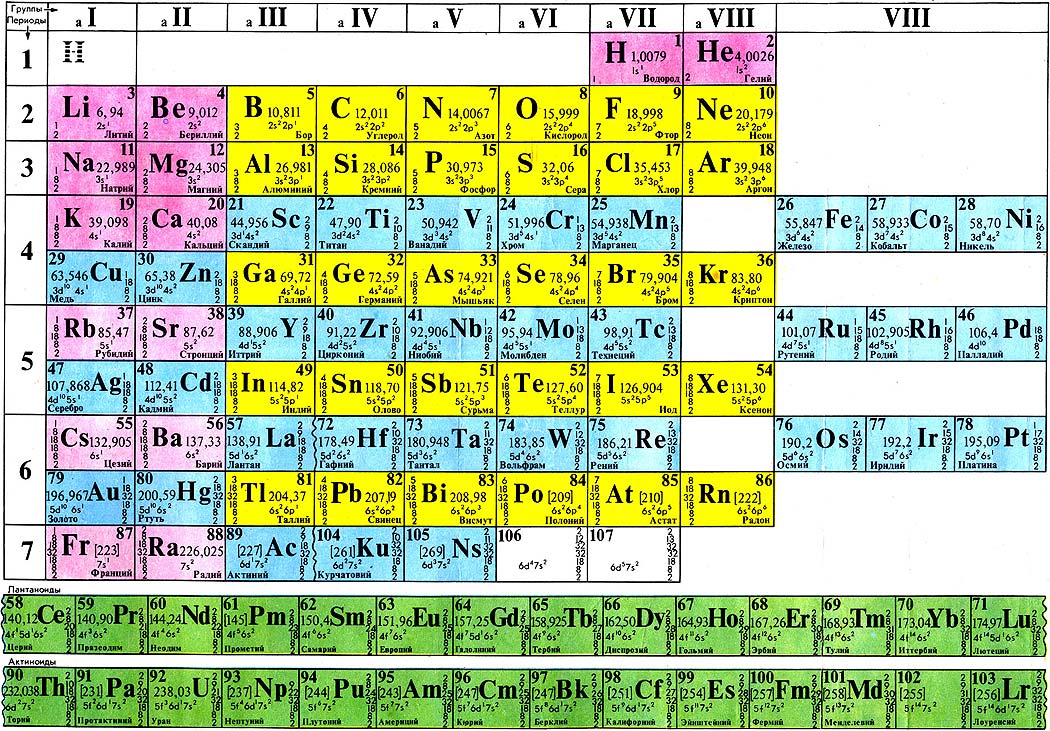 известный.
известный.
Свободные галогены не встречаются в природе из-за их большой реакционной способности. В комбинированной форме фтор является самым распространенным из галогенов в земной коре. Процентное содержание галогенов в изверженных породах земной коры: фтора 0,06, хлора 0,031, брома 0,00016, йода 0,00003. Астатин и теннессин не встречаются в природе, так как состоят только из короткоживущих радиоактивных изотопов.
Галогенные элементы имеют большое сходство друг с другом по своему общему химическому поведению и свойствам их соединений с другими элементами. Однако наблюдается постепенное изменение свойств от фтора через хлор, бром и йод к астату — разница между двумя последовательными элементами наиболее заметна для фтора и хлора. Фтор является наиболее реакционноспособным из галогенов и, по сути, из всех элементов, и у него есть некоторые другие свойства, которые отличают его от других галогенов.
Хлор является наиболее известным из галогенных элементов. Свободный элемент широко используется в качестве реагента для очистки воды и используется в ряде химических процессов. Поваренная соль, хлорид натрия, безусловно, является одним из самых привычных химических соединений. Фториды известны главным образом тем, что их добавляют в воду для предотвращения кариеса, но органические фториды также используются в качестве хладагентов и смазочных материалов. Йод наиболее известен как антисептик, а бром используется в основном для получения соединений брома, которые используются в антипиренах и в качестве пестицидов общего назначения. В прошлом дибромид этилена широко использовался в качестве присадки к этилированному бензину.
Поваренная соль, хлорид натрия, безусловно, является одним из самых привычных химических соединений. Фториды известны главным образом тем, что их добавляют в воду для предотвращения кариеса, но органические фториды также используются в качестве хладагентов и смазочных материалов. Йод наиболее известен как антисептик, а бром используется в основном для получения соединений брома, которые используются в антипиренах и в качестве пестицидов общего назначения. В прошлом дибромид этилена широко использовался в качестве присадки к этилированному бензину.
Вероятно, самое важное обобщение, которое можно сделать о галогенных элементах, состоит в том, что все они являются окислителями; то есть они повышают степень окисления или степень окисления других элементов – свойство, которое раньше приравнивалось к соединению с кислородом, но теперь интерпретируется в терминах переноса электронов от одного атома к другому. При окислении другого элемента восстанавливается сам галоген; т. е. степень окисления 0 свободного элемента снижается до -1.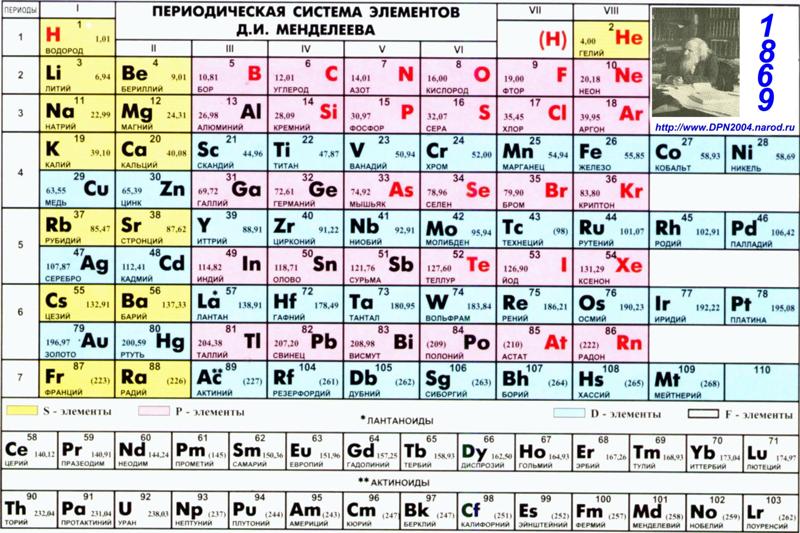 Галогены могут соединяться с другими элементами, образуя соединения, известные как галогениды, а именно фториды, хлориды, бромиды, йодиды и астатиды. Многие из галогенидов можно рассматривать как соли соответствующих галогеноводородов, которые при комнатной температуре и атмосферном давлении представляют собой бесцветные газы и (за исключением фтороводорода) образуют в водном растворе сильные кислоты. Действительно, общий термин 9Соль 0045 получают из каменной или поваренной соли (хлорида натрия). Склонность галогенных элементов к образованию солеобразных (т. е. высокоионных) соединений возрастает в следующем порядке: астат < йод < бром < хлор < фтор. Фториды обычно более стабильны, чем соответствующие хлориды, бромиды или иодиды. (Часто астат опускают из общих рассуждений о галогенах, потому что о нем известно меньше, чем о других элементах.)
Галогены могут соединяться с другими элементами, образуя соединения, известные как галогениды, а именно фториды, хлориды, бромиды, йодиды и астатиды. Многие из галогенидов можно рассматривать как соли соответствующих галогеноводородов, которые при комнатной температуре и атмосферном давлении представляют собой бесцветные газы и (за исключением фтороводорода) образуют в водном растворе сильные кислоты. Действительно, общий термин 9Соль 0045 получают из каменной или поваренной соли (хлорида натрия). Склонность галогенных элементов к образованию солеобразных (т. е. высокоионных) соединений возрастает в следующем порядке: астат < йод < бром < хлор < фтор. Фториды обычно более стабильны, чем соответствующие хлориды, бромиды или иодиды. (Часто астат опускают из общих рассуждений о галогенах, потому что о нем известно меньше, чем о других элементах.)
Окислительная сила галогенов возрастает в том же порядке, т. е. от астата к фтору. Поэтому из галогенных элементов с наибольшим трудом получается элементарный фтор, с наименьшим – йод. Галогенные элементы как класс относятся к неметаллам, но астат проявляет определенные свойства, напоминающие свойства металлов.
Галогенные элементы как класс относятся к неметаллам, но астат проявляет определенные свойства, напоминающие свойства металлов.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Химическое поведение галогенных элементов удобнее всего обсуждать с точки зрения их положения в периодической таблице элементов. В периодической таблице галогены составляют группу 17 (согласно системе нумерации, принятой Международным союзом теоретической и прикладной химии), группу, непосредственно предшествующую благородным газам. Атомы галогенов несут семь валентных электронов на внешней электронной оболочке. Эти семь крайних электронов находятся на двух различных орбиталях, обозначенных как 9.0045 s (с двумя электронами) и p (с пятью). Потенциально атом галогена может содержать еще один электрон (на орбитали p ), что придаст образующемуся иону галогенида такое же расположение (конфигурацию), что и благородный газ рядом с ним в периодической таблице.
