20 важных элементов таблицы Менделеева для блондинок
Здоровье
Это и есть Дмитрий Менделеев, которому мы обязаны многим
Водород (осветлитель для волос)
Символ: Н
Атомный номер: 1
Открыл: Генри Кавендиш (Англия)
Первый и самый главный элемент таблицы Менделеева. Из него состоит почти все, что есть во Вселенной. За редким исключением.
Но для нас важнее то, что без этого легкого и бесцветного газа блондинок было бы куда меньше. Ведь натуральных сейчас на свете всего 3 процента. Остальным помогает маскироваться перекись водорода. Она осветляет волосы, прогоняя из них естественный цвет. А потом можно как на чистый лист бумаги – любой вариант краски наносить. Или оставаться со светлой головой.
А еще водород легким движением руки химика превращается в нашатырный спирт. В былые времена считалось вполне нормальным, что красавицы падали в обморок. Постоянно. Купишь шубу? Нет! И она уже по стеночке сползает. Ну, или корсет слишком затянула, на балу не вздохнуть. Так вот, чтоб привести деву в чувства, как раз очень помогает нашатырь.
Ну, или корсет слишком затянула, на балу не вздохнуть. Так вот, чтоб привести деву в чувства, как раз очень помогает нашатырь.
Углерод (он же алмаз)
Кольцо с бриллиантом – самый желанный подарок
- Фото
- Кадр из фильма «Великий Гэтсби»
Символ: С
Атомный номер: 6
Открыл: неизвестный древний человек
Двоюродный брат водорода. Также присутствует почти во всех основных химических соединениях. Жидкость для снятия лака – вот где мы с ним встречаемся чаще всего.
Но это меркнет перед главным достоинством углерода: в своей твердой форме он называется алмазом. Дальше его красивенько шлифуют – получается бриллиант. Лучший друг каждой девушки (если верить Мэрилин Монро и группе «ВИА Гра»). Именно этот камешек с древних времен люди договорились продавать друг другу за очень большие деньги. Потому что он и сам по себе украшает. Да еще и каждая незамужняя барышня мечтает, чтоб когда прекрасный принц падет перед ней на колени прямо с белого коня и предложит стать его женой… Так вот, в этот момент на кольце должен быть именно бриллиант. Иначе не считается.
Потому что он и сам по себе украшает. Да еще и каждая незамужняя барышня мечтает, чтоб когда прекрасный принц падет перед ней на колени прямо с белого коня и предложит стать его женой… Так вот, в этот момент на кольце должен быть именно бриллиант. Иначе не считается.
А еще углерод подстерегает в кресле стоматолога. Ты же помнишь, что красота требует жертв, и раз в полгода к зубному доктору идти приходится. Насадки для бормашин покрыты алмазным напылением. Чтобы почувствовать красоту момента, когда они ж-ж-ж-ж-ж-ж.
Бериллий (изумруды и аквамарины)
Королева Елизавета в аквамаринах
Символ: Be
Атомный номер: 4
Открыл: Луи Николя Воклен (Франция)
Пока не ушли далеко от алмазов – вот вам еще немного самоцветов! Руда, из которой добывают бериллий, бывает разных цветов. Ярко-зеленые минералы встречаются редко, но именно из них делают изумруды. А из более распространенных голубых получаются аквамарины. Может быть, они и не лучшие друзья девушек, но уж точно добрые приятели.
Может быть, они и не лучшие друзья девушек, но уж точно добрые приятели.
В остальном с бериллием красавицам не по пути. Хотя он присутствует в часах и сотовых телефонах. Но когда ты опаздываешь на свидание, потому что вовремя не посмотрела на часы… Согласись, ты ведь и на звонки мобильника отвечать не будешь.
Кремний (он же силикон)
Что бы делала Памела без Менделеева?
- Фото
- Кадр из сериала «Спасатели Малибу»
Символ: Si
Атомный номер: 14
Открыл: Йенс Якоб Берцелиус (Швеция)
Вот что помогло обезьяне стать человеком. Главный тренд каменного века – из него первобытные красавицы делали самые модные копья и топоры.
А сейчас в основном грудь. Силиконовые импланты – это кремний: и оболочка-эластомер, и гель внутри. Конечно, наукой не доказано, что увеличение размера как-то влияет на привлекательность девушки. Но практика показывает: да, влияет.
Но практика показывает: да, влияет.
Не бойся – дефицита кремния не предвидится. Четверть всей планеты Земля состоит из него, хватит на всех.
А с недавних пор силикон добавляют в шампуни, чтобы обволакивал твои волосы, добавлял им блеск и – опять же – объем.
Только не вздумай ехать за красотой в Силиконовую долину. Там из кремния делают всякую заумную начинку для компьютеров. И вместо загорелых спасателей Малибу – скучные ботаны. С заниженной самооценкой.
Натрий (шампунь для волос)
За шикарные волосы спасибо натрию!
- Фото
- Shutterstock
Символ: Na
Атомный номер: 11
Открыл: Гемфри Дэви (Англия)
Лучший друг чистоты. Входит в состав практически всего, что есть у тебя в ванной. Зубная паста? Да, он оставил здесь полезный след. Шампунь? Безусловно, есть и там. Туалетное мыло? Конечно, дорогая, зачем спрашиваешь…
Туалетное мыло? Конечно, дорогая, зачем спрашиваешь…
А еще лаурилсульфаты натрия прекрасно пенятся. Поэтому его добавляют в большинство масок для волос, в пенки и лосьоны для очищения кожи. Мойдодыр – его второе имя.
Третье имя тоже тебе знакомо. Это пищевая сода (по науке – гидрокарбонат натрия). Его добавляют в тесто, чтобы кексы были пышнее. Вроде бы при чем тут красота? А вот научись печь кексы, и станешь для мужчин еще привлекательнее. Сократишь путь к сердцу любого из них. В два раза!
А еще натрий запихивают в фильтры дамских сигарет (длинных и тонких). Но с этим его проявлением лучше не знакомиться. Курение девушек уж точно не красит. Лучше брось, договорились?!
Азот (чулки и колготки)
Менделеев сделал подарок всем мужчинам
- Фото
- Shutterstock
Символ: N
Атомный номер: 7
Открыл: Даниель Резерфорд (Шотландия)
Если ты смотришь фильмы из Голливуда, то наверняка видела, как некий газ моментально замораживает какого-нибудь злодейского робота или злодейскую инопланетную тварь. А потом вражину легко разбивает на мелкие осколки Уилл Смит. Так вот этот газ – азот. И он действительно морозит все до −196°C. Но медленно. Даже на заморозку мобильника уйдет часа три. Киборг вполне успеет сбежать. Короче, врет Голливуд.
А потом вражину легко разбивает на мелкие осколки Уилл Смит. Так вот этот газ – азот. И он действительно морозит все до −196°C. Но медленно. Даже на заморозку мобильника уйдет часа три. Киборг вполне успеет сбежать. Короче, врет Голливуд.
Зато! Из азота (точнее – из полиамидов) получают капрон и нейлон. То есть за чулки в сеточку и другие модные штучки спасибо ему. А также за струны для гитары – на них достойные кабальеро играют серенады под балконами красавиц. Ну и за леску для рыбалки… Когда захочешь отдохнуть от кабальеро пару дней, подари ему удочку.
Ну и на сладкое такой факт: оксид азота помогает выдавливать взбитые сливки из баллончика.
Висмут (перламутровый лак для ногтей)
Лак для ногтей
- Фото
- С сайта O.P.I
Символ: Bi
Атомный номер: 83
Открыл: Джабир ибн Хайян (Иран)
Удивительный металл. В жидком виде он куда плотнее, чем в твердом. А еще он притягивается к обоим концам магнита.
В жидком виде он куда плотнее, чем в твердом. А еще он притягивается к обоим концам магнита.
В Средние века алхимики думали, что висмут – разновидность свинца. И именно из него пытались делать золото, очень уж приятно блестел на солнце.
Девушкам важно знать: именно оксихлорид висмута добавляют в лак для ногтей, чтобы создать перламутровый эффект. Также Его Сиятельство можно встретить в блеске для губ и тенях для век. Очень разносторонний элемент.
По натуре радиоактивен, но «фонить» начнет только через миллиарды лет. Так что пользуйся косметикой совершенно спокойно.
Цинк (красивая кожа)
Устрицы – кладезь цинка
- Фото
- Shutterstock
Символ: Zn
Атомный номер: 30
Открыл: неизвестный древний человек
Опять же металл, но местами съедобный. Принимать его внутрь в малых дозах полезно не только Терминаторам. Если у тебя, к примеру, память девичья, забываешь про важные встречи – значит, организму не хватает цинка. Срочно начинай грызть семечки, а также отруби и проростки пшеницы. Там его содержится с избытком.
Если у тебя, к примеру, память девичья, забываешь про важные встречи – значит, организму не хватает цинка. Срочно начинай грызть семечки, а также отруби и проростки пшеницы. Там его содержится с избытком.
Для красоты этот элемент полезен дважды. Во-первых, если вдруг появятся прыщи (тьфу-тьфу-тьфу), тебе поможет именно цинковая мазь. Окись цинка вообще все обеззараживает, имей в виду.
А во-вторых, немалую роль при изготовлении микрофибры играет хлорид цинка. Да что там роль, он в этом процессе важнее, чем Волочкова для русского балета. Раз в сто. А из микрофибры делают вполне себе удобное нижнее белье. Которое способно украсить любую блондинку. И брюнетку тоже.
Алюминий (зеркальце и пилочка для ногтей)
Кэтти Перри тоже ценит открытия русского ученого
Символ: Al
Атомный номер: 13
Открыл: Ханс Кристиан Эрстед (Дания)
Есть легенда, как за год до нашей эры пришел к императору Тиберию (это Древний Рим) простой кузнец. И принес тарелку из легкого, прочного и блестящего металла. Похвастал: такую красоту можем делать только я и боги. Тут Тиберий его львами и загрыз. Чтоб с богами не тягался. А секрет обработки алюминия был утрачен аж до XIX века.
И принес тарелку из легкого, прочного и блестящего металла. Похвастал: такую красоту можем делать только я и боги. Тут Тиберий его львами и загрыз. Чтоб с богами не тягался. А секрет обработки алюминия был утрачен аж до XIX века.
Много полезных изобретений для красавиц связано с этим металлом. Пожалуй, самое важное – карманные зеркала. Те что в пудреницах и просто складные. Из алюминия делали амальгаму (отражающую поверхность), а также легкий, но прочный корпус.
И это еще не все. Пилка из твоего маникюрного набора содержит оксид алюминия – мелкую крошку, которая бережно точит и натуральные ногти, и искусственные.
Железо (женское здоровье)
- Фото
- Shutterstock
Символ: Fe
Атомный номер: 26
Открыл: неизвестный древний человек
С железяками очень любят возиться мужчины (у которых руки растут откуда надо). Но зачем оно нужно девушкам? Тем более для красоты?
Но зачем оно нужно девушкам? Тем более для красоты?
А вот оказывается, просто необходимо. Без него ты просто не сможешь дышать. Железо входит в состав гемоглобина и перевозит кислород по всему организму. Вплоть до самого мозга. Но это факт, известный со школы.
Тогда новый факт: уже доказано, что суточная норма потребления железа у мужчин – 10 мг. У женщин же – в два раза больше. В период беременности даже в три раза!
Важно: нормальное (без пробок и аварий) движение кислорода по клеткам разглаживает морщинки и улучшает цвет кожи.
Так что налегай на яблоки, свеклу и гематоген. Придут здоровье и красота. А с ними жить веселее.
Хром (стройность)
Символ: Cr
Атомный номер: 24
Открыл: Луи Николя Воклен (Франция)
Все блестящее и нержавеющее, что тебя окружает, почти наверняка связано с ним. Хоть маникюрные ножницы возьми, хоть иголки для вышивания крестиком. Незаменимый в деле красоты металл.
Хром содержится в нашем организме и – на минуточку! – помогает контролировать холестерин. А также помогает женщинам похудеть – он присутствует в большинстве таблеток и пищевых добавок для избавления от лишнего веса.
Хотя порой он может быть весьма противным. Фильм про Эрин Брокович, за который Джулии Робертс дали «Оскара», основан на реальных событиях. Там алчные капиталисты травили несчастных граждан некими злодейскими разновидностями хрома. Но это нужно тонны металла в реку выбросить. А в тех дозах, которые содержатся в маникюрном наборе, нет ничего опасного.
Ртуть (фетровые шляпы)
Оливия Уайлд носит фетровые шляпы и в кино, и в жизни
- Фото
- Getty Images
Символ: Hg
Атомный номер: 80
Открыл: неизвестный древний человек
Самый жидкий из всех металлов. В таблице Менделеева обозначен как Hydrargyrum – слово древнегреческое, в переводе «серебряная вода». Но современные химики используют название Mercury. Именно под влиянием химии молодой британский певец Фредди взял себе однажды псевдоним Меркьюри. Ведь он на сцене был быстрым и подвижным, как капли ртути из разбитого термометра.
Но современные химики используют название Mercury. Именно под влиянием химии молодой британский певец Фредди взял себе однажды псевдоним Меркьюри. Ведь он на сцене был быстрым и подвижным, как капли ртути из разбитого термометра.
Кстати, только в градусниках этот элемент Периодической системы еще остался. Хотя и их стараются заменять электронными – все-таки пары ртути опасны для жизни.
Не так давно модницы изрядно рисковали – носить фетровые шляпы как в русскую рулетку играть. Головные уборы делались из пуха кроликов или шерсти бобра, а чтобы пушинки лучше сваливались и теснее обнимали друг друга, шляпки прочесывали гребешком, смоченным в ртути. Шляпники, надышавшись вредных паров, сходили с ума (вспоминаем друзей Алисы из Страны чудес). А их клиентки жаловались мужу на головную боль. Постоянно.
Но теперь все стало гораздо лучше. И фетр давно синтетический. А солист группы Queen сумел хоть немножко реабилитировать химического однофамильца. Все-таки Фредди столько прекрасных песен для девушек написал – слушай с замиранием сердца.
И не ври мужу, что голова болит.
Титан (украшения для пирсинга)
Ферджи носит украшения из титана
- Фото
- Getty Images
Символ: Ti
Атомный номер: 22
Открыл: Уильям Грегор (Англия)
Что общего у подводной лодки, бронежилета и пирсинга в твоем пупке? Украшение для пирсинга почти наверняка сделано из титана. Потому что он полезнее золота и серебра в данном вопросе.
Есть две версии, в честь кого металл получил свое имя:
- Потому что в мифах Древней Греции так называли младших богов (не таких крутых, как Зевс и его братья).
- А в комедии Шекспира королеву фей звали Титания.
Ты будешь смеяться, но на эту тему до сих пор спорят вполне солидные ученые.
Половина всего добытого в мире элемента № 22 идет на производство краски. Да, обычной белой краски. И если когда-нибудь ты захочешь покрасить спальню в голубой цвет, а потом нарисуешь облачко в изголовье кровати – то в твоей жизни станет больше титана.
И если когда-нибудь ты захочешь покрасить спальню в голубой цвет, а потом нарисуешь облачко в изголовье кровати – то в твоей жизни станет больше титана.
И романтических снов.
Серебро (серебро и есть!)
Как бы мы жили без серебра?
- Фото
- Официальный сайт Pandora
Символ: Ag
Атомный номер: 47
Открыл: неизвестный древний человек
Добро пожаловать в драгоценную часть таблицы Менделеева! Здесь благородные металлы – чем дальше, тем дороже. Кольца и браслеты, серьги и цепочки… Это классика жанра.
Все барышни любят столовое серебро: оно прибавляет понтов любому обеду или ужину. А некоторые уверены, что с такими ножами и вилками еда вкуснее и полезнее.
Йодид серебра помогает разгонять тучи-облака в праздничные дни, чтобы девушки-красавицы могли вытащить своих ленивых бойфрендов на прогулку.
Также в честь этого элемента названа страна Аргентина (там было много рудников).
Ну и на всякий пожарный запомни – серебряная пуля спасает от оборотней.
Золото
- Фото
- Shutterstock
Символ: Au
Атомный номер: 79
Открыл: неизвестный древний человек
Помнишь, мы недавно про принца, бриллиант и замуж говорили? Надеюсь, ты согласна, что идеальное колечко должно быть именно золотым?! Отлично. Тест пройден. Про золото ты и так все знаешь. Как и любая другая девушка. Это врожденное, наверное.
Поехали дальше.
Платина
Символ: Pt
Атомный номер: 78
Открыл: Антонио де Ульоа (Испания)
Когда-то давно испанские завоеватели привозили этот металл из Америки. Но в Европе все купцы крутили носом и говорили: да ну, ерунда какая-то. Даже название «платина» обидное, переводится как «серебряшка». Пираты не грабили корабли с таким грузом, зачем им эта дешевка. А потом вдруг фальшивомонетчики начали делать деньги из платины и сверху покрывать золотом. Король Испании тогда вообще запретил ее ввозить, и тонны прекрасного металла утопили в Атлантике.
Даже название «платина» обидное, переводится как «серебряшка». Пираты не грабили корабли с таким грузом, зачем им эта дешевка. А потом вдруг фальшивомонетчики начали делать деньги из платины и сверху покрывать золотом. Король Испании тогда вообще запретил ее ввозить, и тонны прекрасного металла утопили в Атлантике.
Но фальшивые деньги натолкнули ювелиров на мысль: если платина по всем показателям похожа на золото, не ржавеет, не тускнеет и не растворяется в кислоте… Значит, из нее можно делать украшения. И продавать за бешеные деньги. Раз король так вовремя создал дефицит…
Платина, кроме всего прочего, – металл, не вызывающий аллергию. То есть абсолютно.
Хлор (латекс)
Женщину-кошку без латекса трудно представить
- Фото
- Кадр из фильма «Женщина-кошка»
Символ: Cl
Атомный номер: 17
Открыл: Карл Вильгельм Шееле (Швеция)
Добрались до самого сексуального элемента Периодической системы. Мог ли старик Менделеев думать, когда рисовал табличку, что однажды в моду войдут эротические костюмы из поливинилхлорида для ролевых игр?! Согласен, думать мог. Но сделать одежду для Женщины-Кошки полтора века назад было нереально. Да и сексуальная жизнь была не настолько раскрепощенной.
Мог ли старик Менделеев думать, когда рисовал табличку, что однажды в моду войдут эротические костюмы из поливинилхлорида для ролевых игр?! Согласен, думать мог. Но сделать одежду для Женщины-Кошки полтора века назад было нереально. Да и сексуальная жизнь была не настолько раскрепощенной.
Также этому газу мы должны сказать спасибо за возможность слушать музыку с виниловых пластинок (во времена твоего папы это было круче, чем CD-диски). Много шикарной музыки перенесли они на своих дорожках. Да и звук, как признают все ценители, был по качеству лучше современного, цифрового.
А еще хлор обеззараживает воду – в кранах на твоей кухне и в бассейнах.
Литий (лечим депрессию)
- Фото
- Shutterstock
Символ: Li
Атомный номер: 3
Открыл: Иоганн Арфведсон (Швеция)
Когда тебе грустно и накатывает тоска, надо пить минеральную воду. Потому что там есть карбонат лития. А это химическое соединение прекрасно лечит депрессию. И повышает бодрость духа.
Потому что там есть карбонат лития. А это химическое соединение прекрасно лечит депрессию. И повышает бодрость духа.
С названием элемента ошибочка вышла: по-гречески «литос» – камень. А на деле литий – металл (хотя и достаточно мягкий). Но когда все эти нюансы выяснились, ученые как-то привыкли к неправильному имени. Как любой ребенок со смешным именем к окончанию второго класса уже привыкает к дурацким прозвищам и перестает на них реагировать.
Для красоты от лития тоже большая польза: с его помощью отбеливают ткани. Текстильная промышленность рулит!
Кальций (красивые зубы)
- Фото
- Shutterstock
Символ: Ca
Атомный номер: 20
Открыл: Гемфри Дэви (Англия)
Все люди и большинство животных должны сказать спасибо кальцию за крепкие кости и зубы. И если с ними все в порядке, то улыбка всегда будет украшать твое лицо.
А когда тебе нужен химический пилинг и глубокое очищение – опять же зови на помощь кальций (только хлорид). Он же способствует подтяжке кожи и разглаживанию морщин.
Фтор (лак для волос)
- Фото
- Кадр из фильма «Лак для волос»
Символ: F
Атомный номер: 9
Открыл: Анри Муассан (Франция)
Самый неприятный из всех элементов – само его имя переводится как «вред». И мы бы его даже не вспомнили сегодня. Но! Если ты пользуешься лаком для волос, значит, ты знакома с этим извергом. Без него никакой укладки не получится.
И хотя ты теперь понимаешь, что каждый пшик из аэрозольного баллончика вредит экологии, да и тебе самой…
Но красота требует жертв, да?!
Юлия Цыганкова
Строение атомов химических элементов. Состав атомного ядра. Строение электронных оболочек атомов
Билет № 3
1.
 Строение атомов химических элементов. Состав атомного ядра. Строение электронных оболочек атомов первых 20 химических
элементов периодической системы Д. И. Менделеева
Строение атомов химических элементов. Состав атомного ядра. Строение электронных оболочек атомов первых 20 химических
элементов периодической системы Д. И. МенделееваАтом — наименьшая частица вещества, неделимая химическим путем. В XX веке было выяснено сложное строение атома. Атомы состоят из положительно заряженного ядра и оболочки, образованной отрицательно заряженными электронами. Общий заряд свободного атома* равен нулю, так как заряды ядра и электронной оболочки уравновешивают друг друга. При этом величина заряда ядра равна номеру элемента в периодической таблице (атомному номеру) и равна общему числу электронов (заряд электрона равен −1).
Атомное ядро состоит из положительно заряженных протонов и нейтральных частиц — нейтронов, не имеющих заряда. Обобщенные характеристики элементарных частиц в составе атома можно представить в виде таблицы:
| Название частицы | Обозначение | Заряд | Масса |
| протон | p | +1 | 1 |
| нейтрон | n | 0 | 1 |
| электрон | e− | −1 | принимается равной 0 |
Число протонов равно заряду ядра, следовательно, равно атомному номеру. Чтобы найти число нейтронов в атоме, нужно от атомной
массы (складывающейся из масс протонов и нейтронов) отнять заряд ядра (число протонов).
Чтобы найти число нейтронов в атоме, нужно от атомной
массы (складывающейся из масс протонов и нейтронов) отнять заряд ядра (число протонов).
Например, в атоме натрия 23Na число протонов p = 11, а число нейтронов n = 23 − 11 = 12
Число нейтронов в атомах одного и того же элемента может быть различным. Такие атомы называют изотопами.
Электронная оболочка атома также имеет сложное строение. Электроны располагаются на энергетических уровнях (электронных слоях).
Номер уровня характеризует энергию электрона. Связано это с тем, что элементарные частицы могут передавать и принимать энергию не сколь угодно малыми величинами, а определенными порциями — ква́нтами. Чем выше уровень, тем большей энергией обладает электрон. Поскольку чем ниже энергия системы, тем она устойчивее (сравните низкую устойчивость камня на вершине горы, обладающего большой потенциальной энергией, и устойчивое положение того же камня внизу на равнине, когда его энергия значительно ниже), вначале заполняются уровни с низкой энергией электрона и только затем — высокие.
Максимальное число электронов, которое может вместить уровень, можно рассчитать по формуле:
N = 2n2, где N — максимальное число электронов на уровне,
n — номер уровня.
Тогда для первого уровня N = 2 · 12 = 2,
для второго N = 2 · 22 = 8 и т. д.
Число электронов на внешнем уровне для элементов главных (А) подгрупп равно номеру группы.
В большинстве современных периодических таблиц расположение электронов по уровням указано в клеточке с элементом. Очень
важно понимать, что уровни читаются снизу вверх, что соответствует их энергии. Поэтому столбик цифр в клеточке с натрием:
1
8
2
следует читать так:
на 1-м уровне — 2 электрона,
на 2-м уровне — 8 электронов,
на 3-м уровне — 1 электрон
Будьте внимательны, очень распространенная ошибка!
Распределение электронов по уровням можно представить в виде схемы:
11Na ) ) )
2 8 1
Если в периодической таблице не указано распределение электронов по уровням, можно руководствоваться:
- максимальным количеством электронов: на 1-м уровне не больше 2 e−,
на 2-м — 8 e−,
на внешнем уровне — 8 e−; - числом электронов на внешнем уровне (для первых 20 элементов совпадает с номером группы)
Тогда для натрия ход рассуждений будет следующий:
- Общее число электронов равно 11, следовательно, первый уровень заполнен и содержит 2 e−;
- Третий, наружный уровень содержит 1 e− (I группа)
- Второй уровень содержит остальные электроны: 11 − (2 + 1) = 8 (заполнен полностью)
* Ряд авторов для более четкого разграничения свободного атома и атома в составе соединения предлагают использовать термин «атом» только для обозначения свободного (нейтрального) атома, а для обозначения всех атомов, в том числе и в составе соединений, предлагают термин «атомные частицы». Время покажет, как сложится судьба этих терминов. С нашей точки зрения, атом по определению является частицей, следовательно, выражение «атомные частицы» можно рассматривать как тавтологию («масло масляное»).
Время покажет, как сложится судьба этих терминов. С нашей точки зрения, атом по определению является частицей, следовательно, выражение «атомные частицы» можно рассматривать как тавтологию («масло масляное»).
2. Задача. Вычисление количества вещества одного из продуктов реакции, если известна масса исходного вещества.
Пример:
Какое количество вещества водорода выделится при взаимодействии цинка с соляной кислотой массой 146 г?
Решение:
- Записываем уравнение реакции: Zn + 2HCl = ZnCl
- Находим молярную массу соляной кислоты: M (HCl) = 1 + 35,5 = 36,5 (г/моль)
(молярную массу каждого элемента, численно равную относительной атомной массе, смотрим в периодической таблице под знаком элемента и округляем до целых, кроме хлора, который берется 35,5) - Находим количество вещества соляной кислоты: n (HCl) = m / M = 146 г / 36,5 г/моль = 4 моль
- Записываем над уравнением реакции имеющиеся данные, а под уравнением — число моль согласно уравнению (равно коэффициенту перед веществом):
4 моль x моль
Zn + 2HCl = ZnCl2 + H2↑
2 моль 1 моль
4 моль — x моль
2 моль — 1 моль
(или с пояснением:
из 4 моль соляной кислоты получится x моль водорода,
а из 2 моль — 1 моль)- Находим x:
x = 4 моль • 1 моль / 2 моль = 2 моль
Ответ: 2 моль.
автор: Владимир Соколов
Как рождаются новые химические элементы?
Объединенный институт ядерных исследований в Дубне строит первую в мире фабрику сверхтяжелых элементов
Во второй половине XX века в Периодической таблице появилось 16 новых элементов, в XXI веке еще пять. Сейчас таблица заканчивается на оганесоне (Og 118). Его синтезировали в 2002 и 2005 годах в Объединенном институте ядерных исследований (ОИЯИ) в подмосковном городе Дубне.
Оганесон — один из так называемых сверхтяжелых элементов, следующих за ураном (U 92). Некоторые из них появились около 10 млрд лет назад в результате ядерных реакций внутри звезд. Большинство уже давно распалось. К 40-м годам XX века все существующие в природе химические элементы были найдены. Последним стал франций (Fr 87). Все последующие элементы создавались — и создаются — в лабораториях.
Сейчас ОИЯИ строит первую в мире фабрику сверхтяжелых элементов, чтобы синтезировать 119-й, 120-й, 121-й и детально изучать свойства ранее полученных элементов.
«Это просто арифметика»
Андрей Георгиевич, во-первых, почему «фабрика»? И чем она будет отличаться от, например, коллайдера?
«Фабрика» — потому что это ускоритель плюс вся инфраструктура вокруг него. Отличие от коллайдера принципиальное. В коллайдерах частицы разгоняют почти до скорости света, а потом сталкивают друг с другом. Получаются новые частицы или другие интересные события. А для синтеза сверхтяжелых элементов нельзя использовать сверхвысокие энергии. Наоборот, чем сильнее вы ударите одним ядром по другому, тем быстрее развалится система. Ничего путного вы не получите.
А что вы будете делать, чтобы получить «что-то путное»?
Надо будет сближать ядра атомов так, чтобы они коснулись друг друга. Дело в том, что, когда ядра заряжены одинаково, они отталкиваются. Для преодоления отталкивания нужно разогнать частицы до скорости, которая составляет примерно 10% от скорости света.
В дальнейшем, мы надеемся, эффективность фабрики будет примерно в десять раз выше, чем раньше. Тогда откроются уже очень большие перспективы для экспериментов. Совсем другая жизнь у нас начнется.
Так. Если очень коротко. Есть вещество, из которого сделана мишень, и есть вещества, которые через эту мишень пролетают. В результате можно получить какой-то совершенно новый химический элемент. Правильно? Все равно непонятно, как это работает.
Важно правильно подобрать комбинацию из мишенного материала и вещества, которое будет с ним сталкиваться. Условия здесь следующие: материал для мишени должен существовать в природе или может быть произведен искусственно в весовых количествах. Это первое требование. Но здесь надо смотреть не на Периодическую таблицу. Она в данном случае мало поможет. А надо смотреть на карту изотопов. Черные клеточки — это долгоживущие изотопы, существующие в природе. Теперь вы можете брать частицу, которая приводила бы к образованию желаемого элемента. Здесь действует закон сохранения электрического заряда. Например, если вам нужен 118-й элемент, вы берете для мишени изотоп, у которого заряд ядра 98 (калифорний), а для бомбардировки мишени кальций с зарядом ядра 20. 20 + 98 = 118. Все просто.
Условия здесь следующие: материал для мишени должен существовать в природе или может быть произведен искусственно в весовых количествах. Это первое требование. Но здесь надо смотреть не на Периодическую таблицу. Она в данном случае мало поможет. А надо смотреть на карту изотопов. Черные клеточки — это долгоживущие изотопы, существующие в природе. Теперь вы можете брать частицу, которая приводила бы к образованию желаемого элемента. Здесь действует закон сохранения электрического заряда. Например, если вам нужен 118-й элемент, вы берете для мишени изотоп, у которого заряд ядра 98 (калифорний), а для бомбардировки мишени кальций с зарядом ядра 20. 20 + 98 = 118. Все просто.
Можете брать любые другие комбинации, пожалуйста. Если вы хотите 120 элемент, то 120 — это два раза по 60. Берем элемент 60 — неодим. Делаем из него мишень и им же облучаем эту мишень. Получаем элемент 120. Это просто арифметика. Здесь не надо всю жизнь что-то перебирать. Плюс есть известные законы.
Карта химических элементов и их разновидностей (изотопов) (на фото Александр Карпов, учёный секретарь Лаборатории ядерных реакций). Сергей Карпухин/ТАСС
«Ядро — это не капля жидкости»
Какова вообще вероятность получить сверхтяжелый элемент?
Она складывается, как минимум, из двух частей — вероятности слияния ядер и вероятности выживания получившегося ядра в процессе остывания. Потому что ядра остывают точно так же, как, например, жидкость. Только в жидкости испаряются молекулы, а в ядрах нейтроны. Нейтроны уносят энергию из ядра, и система остывает. Это первое. Второе — ядра должны сливаться. К сожалению, чем ближе друг к другу масса мишени и масса бомбардирующей ее частицы, тем хуже они сливаются. Это только некоторые из обстоятельств, которые ограничивают получение сверхтяжелых ядер.
Какие эксперименты на «фабрике» сейчас проводятся?
Естественно, после того, как мы сделали новый ускоритель, самый верный способ показать его работоспособность, — это воспроизвести прежние результаты. Поэтому в январе этого года мы успешно провели эксперименты по синтезу 115-го элемента московия. Он был впервые получен в 2003 году.
Поэтому в январе этого года мы успешно провели эксперименты по синтезу 115-го элемента московия. Он был впервые получен в 2003 году.
Сейчас проводятся эксперименты по получению пучков ускоренных частиц, которые нужны для синтеза более тяжелых элементов.
До этого мы работали в основном с кальцием. Это элемент 20 в Периодической таблице. Им бомбардировали мишень. А самый тяжелый элемент, из которого можно сделать мишень, — это калифорний, 98. Соответственно, 98 + 20 — это 118. То есть,чтобы получить элемент 120, надо идти к следующей частице. Это, скорее всего, титан — 22 + 98 = 120.
Работы по отладке системы еще очень много. Я не хочу забегать вперед, но если получится провести успешно все модельные эксперименты, то в этом году, возможно, начнутся первые эксперименты по синтезу 120-го элемента.
А почему вообще существуют сверхтяжелые элементы? Благодаря каким законам природы?
Ядра атомов имеют структуру, которая чем-то похожа на структуру атомных оболочек. Электроны ведь удерживается на орбитах не просто так, а потому что орбиты имеет специальную сложную структуру. Примерно то же самое происходит и в ядрах. Структурные эффекты объясняют, почему существуют сверхтяжелые элементы. В обычном состоянии ядро не ведет себя подобно капле жидкости, не является аморфным телом, а имеет внутреннюю структуру. Без нее сверхтяжелые ядра вообще бы не существовали. А наличие структурных свойств ядерной материи приводит к тому, что эти ядра живут секунды, а мы надеемся, что они могут жить часы, сутки, а может быть даже миллионы лет.
Электроны ведь удерживается на орбитах не просто так, а потому что орбиты имеет специальную сложную структуру. Примерно то же самое происходит и в ядрах. Структурные эффекты объясняют, почему существуют сверхтяжелые элементы. В обычном состоянии ядро не ведет себя подобно капле жидкости, не является аморфным телом, а имеет внутреннюю структуру. Без нее сверхтяжелые ядра вообще бы не существовали. А наличие структурных свойств ядерной материи приводит к тому, что эти ядра живут секунды, а мы надеемся, что они могут жить часы, сутки, а может быть даже миллионы лет.
Бесструктурные ядра после 103-го и 104-го элемента уже не имели бы права существовать. Это открытие структурных эффектов — очень большое достижение в понимании природы ядерных сил.
«Это никогда не скучно»
Можно ли как-то использовать сверхтяжелые элементы «в народном хозяйстве»?
Это совершенно законный вопрос, но мы занимаемся фундаментальными исследованиями. Накопить хоть какое-то количество атомов 118-го, сами понимаете, совершенно невозможно. За всю историю было зарегистрировано, по-моему, пять атомов этого элемента. И живут они меньше миллисекунды.
За всю историю было зарегистрировано, по-моему, пять атомов этого элемента. И живут они меньше миллисекунды.
В частности, очень интересно, как будут эволюционировать химические свойства элементов, если двигаться дальше по таблице. Лишь две трети элементов таблицы Менделеева «вписываются» в периодический закон, который связывает зависимость свойств химических элементов с зарядами атомных ядер. А дальше начинаются нестыковки: совершенно инертных элементов — нет, элементы, которые должны быть газами, становятся твердыми, да еще и с металлическими свойствами и т.д.
Еще очень интересно, как образовались элементы в природе. Не только сверхтяжелые. Теория не исключает, что сверхтяжелые элементы могли дожить до наших времен после, скажем, образования Солнечной системы. А в таком случае их можно искать в природе.
Кроме всего прочего, открытие новых элементов демонстрирует высокий уровень науки, техники и образования, который, в свою очередь, приносит экономические и политические дивиденды.
Какие страны сейчас лидируют в поиске сверхтяжелых элементов?
В одиночку проводить такие исследования могут только две страны — Соединенные Штаты Америки и Россия. И причина здесь в том, что необходимо иметь материал для изготовления мишеней, а это тяжелые трансурановые элементы, такие как кюрий, берклий и калифорний. Чтобы эти элементы производить, требуются специальные реакторы.
Еще в поиске сверхтяжелых элементов активно участвуют Германия и Япония, но не в одиночку, а в кооперации с теми, у кого есть изотопы. Эти эксперименты очень длительные. Идет обычная работа: плановая, но интенсивная. Японцы получили три атома 113 элемента за 10 лет. Это некий мировой рекорд по настойчивости. По-моему, никто больше такого не делал и не станет делать.
Ускоритель для производства сверхтяжелых элементов. Сергей Карпухин/ТАСС
В чем конкурентные преимущества России?
Во-первых, в России существует очень давняя и плодотворная школа синтеза новых элементов, основанная Георгием Флеровым. В частности, его группе принадлежит приоритет в открытии 102-го элемента нобелия.
В частности, его группе принадлежит приоритет в открытии 102-го элемента нобелия.
Во-вторых, есть школа создания ускорителей. Как известно, первый ускоритель был построен в США, в Беркли, а второй — в Ленинграде, в Радиевом институте. И, в-третьих, мы умеем производить материал для изготовления мишеней — изотопы трансурановых элементов. Вот наши преимущества: научная школа, ускорители и изотопы. Это три составляющие успеха.
Андрей Георгиевич, вы всю жизнь занимаетесь синтезом новых элементов. Уже более полувека. Вам до сих пор это нравится?
Да. Мне все еще это нравится. Важно, что развитие методик на грани возможностей обязательно к чему-нибудь приводит. Например, к созданию новых технологий. И еще, это никогда не скучно. Поверьте, это высочайшая радость — открыть нечто, неизвестное никому. Это никогда не может надоесть.
СЛОВАРЬ
Георгий Флеров (1913–1990). Советский физик-ядерщик, один из основателей ОИЯИ и один из пионеров поиска трансуранов. Участвовал в открытии 103-го, 104-го, 105-го и 106-го элементов.
Участвовал в открытии 103-го, 104-го, 105-го и 106-го элементов.
Юрий Оганесян (р. 1933). Ученик Флерова и один из тех, кто синтезировал резерфордий, дубний и другие сверхтяжелые элементы. Академик РАН, научный руководитель лаборатории ядерных реакций ОИЯИ. В 2016 году в его честь был назван 118-й элемент — оганесон.
Изотоп — разновидность атома какого-либо химического элемента, которая имеет одинаковый с ним атомный номер, но разные массовые числа. Например, изотоп водорода Н — дейтерий 2Н, который применяется при создании термоядерного оружия.
Остров стабильности. Ядра атомов состоят из протонов и нейтронов. Но только строго определенное количество этих «кирпичиков» связано друг с другом в единое тело, которое представляет ядро атома. Комбинаций, которые «не срабатывают», оказывается больше. Поэтому, в принципе, наш мир находится в море нестабильности. Есть ядра, которые остались со времен образования Солнечной системы, они стабильны. Водород, например. Участки с такими ядрами будем называть «континентом». Он постепенно уходит в море нестабильности по мере того, как мы идем к более тяжелым элементам. Но, оказывается, если далеко уйти от суши, возникает остров стабильности, где рождаются ядра-долгожители.
Водород, например. Участки с такими ядрами будем называть «континентом». Он постепенно уходит в море нестабильности по мере того, как мы идем к более тяжелым элементам. Но, оказывается, если далеко уйти от суши, возникает остров стабильности, где рождаются ядра-долгожители.
Сверхтяжелые элементы. Элементы, которые следуют за ураном (его атомный номер 92). Некоторые из них появились около 10 млрд лет назад в результате ядерных реакций внутри звезд. Большинство уже давно распалось. Теперь лишь остается синтезировать их в лабораториях.
- #Ядерная физика
Источник: Светлана Соколова
Вам может быть интересно
10 августа
В Новосибирске состоится IX Международный форум технологического развития «Технопром-2022»
8 августа
Победитель «Лидеров России» предлагает создать команду ученых для интенсивного импортозамещения в химической промышленности
5 августа
Экскурсии «Наука рядом»: в июле школьники узнали, как создают вакцины, увидели строительство судов и сыграли роботами в лазертаг
Электронные формулы атомов химических элементов (109)
Рубрика: ЕГЭ – химия для чайников
Порядок заполнения атомных орбиталей по мере увеличения энергии: 1s
Распределение в порядке заполнения орбиталей
На 5-ege.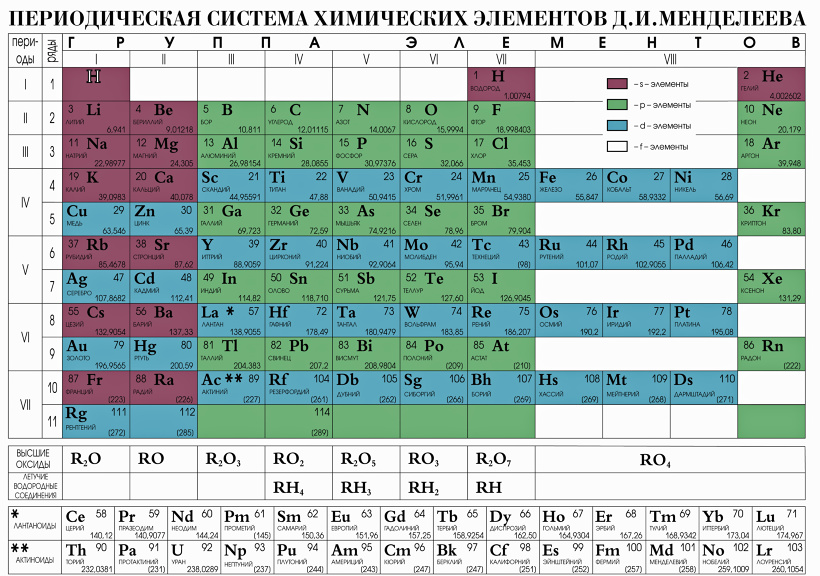 ru вы также можете открыть распределение электронов по слоям (вторая таблица, расположенная ниже).
ru вы также можете открыть распределение электронов по слоям (вторая таблица, расположенная ниже).
Электронные формулы атомов химических элементов (расположение слоев в порядке заполнения подуровней)
| № эл-та | Химический знак | Название элемента | Электронная формула |
| 1 | H | водород | 1s 1 |
| 2 | He | гелий | 1s 2 |
| II период | |||
| 3 | Li | литий | 1s 22s 1 |
| 4 | Be | бериллий | 1s 22s 2 |
| 5 | B | бор | 1s 22s 22p 1 |
| 6 | C | углерод | 1s 22s 22p 2 |
| 7 | N | азот | 1s 22s 22p 3 |
| 8 | O | кислород | 1s 22s 22p 4 |
| 9 | F | фтор | 1s 22s 22p 5 |
| 10 | Ne | неон | 1s 22s 22p 6 |
| III период | |||
| 11 | Na | натрий | 1s 22s 22p 63s 1 |
| 12 | Mg | магний | 1s 22s 22p 63s 2 |
| 13 | Al | алюминий | 1s 22s 22p 63s 23p1 |
| 14 | Si | кремний | 1s 22s 22p 63s 23p2 |
| 15 | P | фосфор | 1s 22s 22p 63s 23p3 |
| 16 | S | сера | 1s 22s 22p 63s 23p4 |
| 17 | Cl | хлор | 1s 22s 22p 63s 23p5 |
| 18 | Ar | аргон | 1s 22s 22p 63s 23p6 |
| IV период | |||
| 19 | K | калий | 1s 22s 22p 63s 23p64s 1 |
| 20 | Ca | кальций | 1s 22s 22p 63s 23p64s 2 |
| 21 | Sc | скандий | 1s 22s 22p 63s 23p64s 23d1 |
| 22 | Ti | титан | 1s 22s 22p 63s 23p64s 23d2 |
| 23 | V | ванадий | 1s 22s 22p 63s 23p64s 23d3 |
| 24 | Cr | хром | 1s 22s 22p 63s 23p64s 13d5 |
| 25 | Mn | марганец | 1s 22s 22p 63s 23p64s 23d5 |
| 26 | Fe | железо | 1s 22s 22p 63s 23p64s 23d6 |
| 27 | Co | кобальт | 1s 22s 22p 63s 23p64s 23d7 |
| 28 | Ni | никель | 1s 22s 22p 63s 23p64s 23d8 |
| 29 | Cu | медь | 1s 22s 22p 63s 23p64s 13d10 |
| 30 | Zn | цинк | 1s 22s 22p 63s 23p64s 23d10 |
| 31 | Ga | галлий | 1s 22s 22p 63s 23p64s 23d104p1 |
| 32 | Ge | германий | 1s 22s 22p 63s 23p64s 23d104p2 |
| 33 | As | мышьяк | 1s 22s 22p 63s 23p64s 23d104p3 |
| 34 | Se | селен | 1s 22s 22p 63s 23p64s 23d104p4 |
| 35 | Br | бром | 1s 22s 22p 63s 23p64s 23d104p5 |
| 36 | Kr | криптон | 1s 22s 22p 63s 23p64s 23d104p6 |
| V период | |||
| 37 | Rb | рубидий | 1s 22s 22p 63s 23p64s 23d104p65s1 |
| 38 | Sr | стронций | 1s 22s 22p 63s 23p64s 23d104p65s2 |
| 39 | Y | иттрий | 1s 22s 22p 63s 23p64s 23d104p65s24d1 |
| 40 | Zr | цирконий | 1s 22s 22p 63s 23p64s 23d104p65s24d2 |
| 41 | Nb | ниобий | 1s 22s 22p 63s 23p64s 23d104p65s14d4 |
| 42 | Mo | молибден | 1s 22s 22p 63s 23p64s 23d104p65s14d5 |
| 43 | Tc | технеций | 1s 22s 22p 63s 23p64s 23d104p65s24d5 |
| 44 | Ru | рутений | 1s 22s 22p 63s 23p64s 23d104p65s14d7 |
| 45 | Rh | родий | 1s 22s 22p 63s 23p64s 23d104p65s14d8 |
| 46 | Pd | палладий | 1s 22s 22p 63s 23p64s 23d104p65s04d10 |
| 47 | Ag | серебро | 1s 22s 22p 63s 23p64s 23d104p65s14d10 |
| 48 | Cd | кадмий | 1s 22s 22p 63s 23p64s 23d104p65s24d10 |
| 49 | In | индий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p1 |
| 50 | Sn | олово | 1s 22s 22p 63s 23p64s 23d104p65s24d105p2 |
| 51 | Sb | сурьма | 1s 22s 22p 63s 23p64s 23d104p65s224d105p3 |
| 52 | Te | теллур | 1s 22s 22p 63s 23p64s 23d104p65s24d105p4 |
| 53 | I | йод | 1s 22s 22p 63s 23p64s 23d104p65s24d105p5 |
| 54 | Xe | ксенон | 1s 22s 22p 63s 23p64s 23d104p65s24d105p6 |
| VI период | |||
| 55 | Cs | цезий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s1 |
| 56 | Ba | барий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s2 |
| 57 | La | лантан | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s25d1 |
| 58 | Ce | церий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f2 |
| 59 | Pr | празеодим | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f3 |
| 60 | Nd | неодим | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f4 |
| 61 | Pm | прометий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f5 |
| 62 | Sm | самарий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f6 |
| 63 | Eu | европий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f7 |
| 64 | Gd | гадолиний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f75d1 |
| 65 | Tb | тербий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f9 |
| 66 | Dy | диспрозий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f10 |
| 67 | Ho | гольмий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f11 |
| 68 | Er | эрбий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f12 |
| 68 | Tm | тулий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f13 |
| 70 | Yb | иттербий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f14 |
| 71 | Lu | лютеций | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d1 |
| 72 | Hf | гафний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d2 |
| 73 | Ta | тантал | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d3 |
| 74 | W | вольфрам | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d4 |
| 75 | Re | рений | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d5 |
| 76 | Os | осмий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d6 |
| 77 | Ir | иридий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d7 |
| 78 | Pt | платина | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s14f145d9 |
| 79 | Au | золото | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s14f145d10 |
| 80 | Hg | ртуть | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d10 |
| 81 | Tl | таллий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p1 |
| 82 | Pb | свинец | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p2 |
| 83 | Bi | висмут | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p3 |
| 84 | Po | полоний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p4 |
| 85 | At | астат | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p5 |
| 86 | Rn | радон | 1s 22s 22p 63s 23p64s 23d104p65s14d105p66s24f145d106p6 |
| VII период | |||
| 87 | Fr | франций | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s1 |
| 88 | Ra | радий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s2 |
| 89 | Ac | актиний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s26d1 |
| 90 | Th | торий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s26d25f0 |
| 91 | Pa | протактиний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f26d1 |
| 92 | U | уран | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f36d1 |
| 93 | Np | нептуний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f46d1 |
| 94 | Pu | плутоний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f56d1 |
| 95 | Am | америций | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f7 |
| 96 | Cm | кюрий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f76d1 |
| 97 | Bk | берклий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f86d1 |
| 98 | Cf | калифорний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f10 |
| 99 | Es | эйнштейний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f11 |
| 100 | Fm | фермий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f12 |
| 101 | Md | менделеевий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f13 |
| 102 | No | нобелий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f14 |
| 103 | Lr | лоуренсий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d1 |
| 104 | Rf | резерфордий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d2 |
| 105 | Db | дубний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d3 |
| 106 | Sg | сиборгий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d4 |
| 107 | Bh | борий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d5 |
| 108 | Hs | хассий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d6 |
| 109 | Mt | мейтнерий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d7 |
| Обозначения элементов: | |||
| s-элементы | p-элементы | d-элементы | f-элементы |
https://5-ege. ru/formuly-atomov/
ru/formuly-atomov/
Распределение электронов по слоям
Формулы элементов (распределение по подуровням)
| № эл-та | Химический знак | Название элемента | Электронная формула |
| 1 | H | водород | 1s 1 |
| 2 | He | гелий | 1s 2 |
| II период | |||
| 3 | Li | литий | 1s 22s 1 |
| 4 | Be | бериллий | 1s 22s 2 |
| 5 | B | бор | 1s 22s 22p 1 |
| 6 | C | углерод | 1s 22s 22p 2 |
| 7 | N | азот | 1s 22s 22p 3 |
| 8 | O | кислород | 1s 22s 22p 4 |
| 9 | F | фтор | 1s 22s 22p 5 |
| 10 | Ne | неон | 1s 22s 22p 6 |
| III период | |||
| 11 | Na | натрий | 1s 22s 22p 63s 1 |
| 12 | Mg | магний | 1s 22s 22p 63s 2 |
| 13 | Al | алюминий | 1s 22s 22p 63s 23p1 |
| 14 | Si | кремний | 1s 22s 22p 63s 23p2 |
| 15 | P | фосфор | 1s 22s 22p 63s 23p3 |
| 16 | S | сера | 1s 22s 22p 63s 23p4 |
| 17 | Cl | хлор | 1s 22s 22p 63s 23p5 |
| 18 | Ar | аргон | 1s 22s 22p 63s 23p6 |
| IV период | |||
| 19 | K | калий | 1s 22s 22p 63s 23p64s 1 |
| 20 | Ca | кальций | 1s 22s 22p 63s 23p64s 2 |
| 21 | Sc | скандий | 1s 22s 22p 63s 23p63d14s 2 |
| 22 | Ti | титан | 1s 22s 22p 63s 23p63d24s 2 |
| 23 | V | ванадий | 1s 22s 22p 63s 23p63d34s 2 |
| 24 | Cr | хром | 1s 22s 22p 63s 23p63d54s 1 |
| 25 | Mn | марганец | 1s 22s 22p 63s 23p63d54s 2 |
| 26 | Fe | железо | 1s 22s 22p 63s 23p63d64s 2 |
| 27 | Co | кобальт | 1s 22s 22p 63s 23p63d74s 2 |
| 28 | Ni | никель | 1s 22s 22p 63s 23p63d84s 2 |
| 29 | Cu | медь | 1s 22s 22p 63s 23p63d104s 1 |
| 30 | Zn | цинк | 1s 22s 22p 63s 23p63d104s 2 |
| 31 | Ga | галлий | 1s 22s 22p 63s 23p63d104s 24p1 |
| 32 | Ge | германий | 1s 22s 22p 63s 23p63d104s 24p2 |
| 33 | As | мышьяк | 1s 22s 22p 63s 23p63d104s 24p3 |
| 34 | Se | селен | 1s 22s 22p 63s 23p63d104s 24p4 |
| 35 | Br | бром | 1s 22s 22p 63s 23p63d104s 24p5 |
| 36 | Kr | криптон | 1s 22s 22p 63s 23p63d104s 24p6 |
| V период | |||
| 37 | Rb | рубидий | 1s 22s 22p 63s 23p63d104s 24p65s1 |
| 38 | Sr | стронций | 1s 22s 22p 63s 23p63d104s 24p65s2 |
| 39 | Y | иттрий | 1s 22s 22p 63s 23p63d104s 24p64d15s2 |
| 40 | Zr | цирконий | 1s 22s 22p 63s 23p63d104s 24p64d25s2 |
| 41 | Nb | ниобий | 1s 22s 22p 63s 23p63d104s 24p64d45s1 |
| 42 | Mo | молибден | 1s 22s 22p 63s 23p63d104s 24p64d55s1 |
| 43 | Tc | технеций | 1s 22s 22p 63s 23p63d104s 24p64d55s2 |
| 44 | Ru | рутений | 1s 22s 22p 63s 23p63d104s 24p64d75s1 |
| 45 | Rh | родий | 1s 22s 22p 63s 23p63d104s 24p64d85s1 |
| 46 | Pd | палладий | 1s 22s 22p 63s 23p63d104s 24p64d105s0 |
| 47 | Ag | серебро | 1s 22s 22p 63s 23p64s 23d104p65s14d10 |
| 48 | Cd | кадмий | 1s 22s 22p 63s 23p63d104s 24p64d105s2 |
| 49 | In | индий | 1s 22s 22p 63s 23p63d104s 24p64d105s25p1 |
| 50 | Sn | олово | 1s 22s 22p 63s 23p63d104s 24p64d105s25p2 |
| 51 | Sb | сурьма | 1s 22s 22p 63s 23p63d104s 24p64d105s25p3 |
| 52 | Te | теллур | 1s 22s 22p 63s 23p63d104s 24p64d105s25p4 |
| 53 | I | йод | 1s 22s 22p 63s 23p63d104s 24p64d105s25p5 |
| 54 | Xe | ксенон | 1s 22s 22p 63s 23p63d104s 24p64d105s25p6 |
| VI период | |||
| 55 | Cs | цезий | 1s 22s 22p 63s 23p63d104s 24p64d105s25p66s1 |
| 56 | Ba | барий | 1s 22s 22p 63s 23p63d104s 24p64d105s25p66s2 |
| 57 | La | лантан | 1s 22s 22p 63s 23p63d104s 24p64d105s25p65d16s2 |
| 58 | Ce | церий | 1s 22s 22p 63s 23p63d104s 24p64d104f25s25p66s2 |
| 59 | Pr | празеодим | 1s 22s 22p 63s 23p63d104s 24p64d104f35s25p66s2 |
| 60 | Nd | неодим | 1s 22s 22p 63s 23p63d104s 24p64d104f45s25p66s2 |
| 61 | Pm | прометий | 1s 22s 22p 63s 23p63d104s 24p64d104f55s25p66s2 |
| 62 | Sm | самарий | 1s 22s 22p 63s 23p63d104s 24p64d104f65s25p66s2 |
| 63 | Eu | европий | 1s 22s 22p 63s 23p63d104s 24p64d104f75s25p66s2 |
| 64 | Gd | гадолиний | 1s 22s 22p 63s 23p63d104s 24p64d104f75s25p65d16s2 |
| 65 | Tb | тербий | 1s 22s 22p 63s 23p63d104s 24p64d104f95s25p66s2 |
| 66 | Dy | диспрозий | 1s 22s 22p 63s 23p63d104s 24p64d104f105s25p66s2 |
| 67 | Ho | гольмий | 1s 22s 22p 63s 23p63d104s 24p64d114f75s25p66s2 |
| 68 | Er | эрбий | 1s 22s 22p 63s 23p63d104s 24p64d104f125s25p66s2 |
| 68 | Tm | тулий | 1s 22s 22p 63s 23p63d104s 24p64d104f135s25p66s2 |
| 70 | Yb | иттербий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p66s2 |
| 71 | Lu | лютеций | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d16s2 |
| 72 | Hf | гафний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d26s2 |
| 73 | Ta | тантал | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d36s2 |
| 74 | W | вольфрам | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d46s2 |
| 75 | Re | рений | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d56s2 |
| 76 | Os | осмий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d66s2 |
| 77 | Ir | иридий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d76s2 |
| 78 | Pt | платина | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d96s1 |
| 79 | Au | золото | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s1 |
| 80 | Hg | ртуть | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s2 |
| 81 | Tl | таллий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p1 |
| 82 | Pb | свинец | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p2 |
| 83 | Bi | висмут | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p3 |
| 84 | Po | полоний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p4 |
| 85 | At | астат | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p5 |
| 86 | Rn | радон | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p6 |
| VII период | |||
| 87 | Fr | франций | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p67s1 |
| 88 | Ra | радий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p67s2 |
| 89 | Ac | актиний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d106s26p66d17s2 |
| 90 | Th | торий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f06s26p66d27s2 |
| 91 | Pa | протактиний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f26s26p66d17s2 |
| 92 | U | уран | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f36s26p66d17s2 |
| 93 | Np | нептуний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f46s26p66d17s2 |
| 94 | Pu | плутоний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f56s26p66d17s2 |
| 95 | Am | америций | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f76s26p67s2 |
| 96 | Cm | кюрий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f76s26p66d17s2 |
| 97 | Bk | берклий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f86s26p66d17s2 |
| 98 | Cf | калифорний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f106s26p67s2 |
| 99 | Es | эйнштейний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f116s26p67s2 |
| 100 | Fm | фермий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f126s26p67s2 |
| 101 | Md | менделеевий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f136s26p67s2 |
| 102 | No | нобелий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p67s2 |
| 103 | Lr | лоуренсий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d17s2 |
| 104 | Rf | резерфордий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d27s2 |
| 105 | Db | дубний | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d37s2 |
| 106 | Sg | сиборгий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d47s2 |
| 107 | Bh | борий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d57s2 |
| 108 | Hs | хассий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d67s2 |
| 109 | Mt | мейтнерий | 1s 22s 22p 63s 23p63d104s 24p64d104f145s25p65d105f146s26p66d77s2 |
| Обозначения элементов: | |||
| s-элементы | p-элементы | d-элементы | f-элементы |
На 5-ege. ru есть больше материалов по химии.
ru есть больше материалов по химии.
Рекомендуем:
- Формулы по физике для ЕГЭ и 7-11 класса
- Расписание ЕГЭ 2019 (11 класс)
Обратите внимание: на главной странице есть множество материалов для подготовки к ЕГЭ по русскому языку и другим предметам.
Главная » ЕГЭ – химия для чайников » Электронные формулы атомов химических элементов (109)
Элементы 113, 115, 117 и 118: от открытия до признания
Научный руководитель Лаборатории ядерных реакций ОИЯИ, руководитель работ по синтезу сверхтяжелых элементов в Дубне, академик РАН Юрий Цолакович Оганесян, в честь которого получил название 118-й элемент, рассказал о том, как идет научный поиск в этом направлении, как новые элементы получают свои названия.
Новость о внесении в таблицу Менделеева сразу четырех новых сверхтяжелых элементов вызвала живой интерес людей даже весьма далеких от науки. Но это итог некоего пути от собственно открытия элементов до их официального признания. На основе отчетов научных групп, которым удалось синтезировать элементы с номерами 113, 115, 117 и 118, совместная комиссия международных союзов по физике (ИЮПАП) и по химии (ИЮПАК) присудила приоритеты в открытии.
На основе отчетов научных групп, которым удалось синтезировать элементы с номерами 113, 115, 117 и 118, совместная комиссия международных союзов по физике (ИЮПАП) и по химии (ИЮПАК) присудила приоритеты в открытии.
Согласно пресс-релизу от 30 декабря 2015 года ИЮПАК признал приоритет в открытии элементов: 113 – за японской группой ученых, 115, 117, 118 – за дубненской.
8 июня 2016 года ИЮПАК сообщил, что принял названия, предложенные авторами открытий. После чего в течение пяти месяцев шло обсуждение этих названий в научных сообществах всех стран мира. И 28 ноября 2016 года ИЮПАК принял решение внести в Периодическую таблицу элементы:
Нихоний (Nh) – 113,
Московий (Mc) – 115,
Теннессин (Ts) – 117,
Оганесон (Og) – 118.
Научный руководитель Лаборатории ядерных реакций ОИЯИ, руководитель работ по синтезу сверхтяжелых элементов в Дубне, академик РАН Юрий Цолакович Оганесян, в честь которого получил название 118-й элемент, в начале нынешнего года рассказывал журналистам о том, как идет научный поиск в этом направлении, как новые элементы получают свои названия и т. д.
д.
– Как реагировало научное сообщество на сообщение о признании приоритетов в открытии элементов с номерами 113, 115, 117 и 118?
– Большие дискуссии идут, причем на высоком уровне – все вдруг оживились. Хотели найти границы: насколько может быть большой Периодическая таблица элементов? Наш эксперимент показал: она может быть очень и очень большой. Все ожидали, что этих элементов не будет, а теперь, когда оказалось, что они есть, – граница отодвинулась. Вопрос: сколько вообще может быть элементов – остается открытым. С одной стороны, это говорит о том, что надо дальше работать по этой теме. С другой стороны, это оправдывает то, что мы «фабрику» делаем – для того, чтобы идти дальше.
– Есть ли сегодня представление о том, каким путем продвигаться дальше?
– На четыре новых элемента нами было потрачено 15 лет. Мы первые результаты получили в 2000 году, и за прошедшие 15 лет что-то увидели, что-то поняли. Мы не знали, есть ли вообще там какие-то элементы.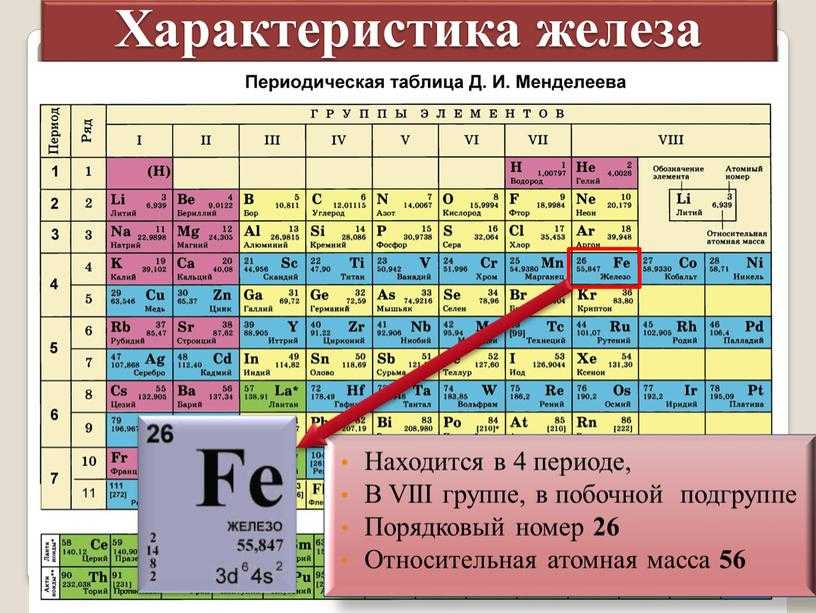 Теперь наши знания пополнились. С другой стороны – (идет) научно-технический прогресс. И если бы мы сегодня ставили такой эксперимент: с учетом того, что теперь знаем, и с техникой, которая есть сейчас, – мы могли бы в сто раз быстрее это сделать. Вот потому создается «фабрика»: она воплощает в себе все знания, которые получены здесь (в Лаборатории ядерных реакций), и весь научно-технический прогресс, который был за 15 лет.
Теперь наши знания пополнились. С другой стороны – (идет) научно-технический прогресс. И если бы мы сегодня ставили такой эксперимент: с учетом того, что теперь знаем, и с техникой, которая есть сейчас, – мы могли бы в сто раз быстрее это сделать. Вот потому создается «фабрика»: она воплощает в себе все знания, которые получены здесь (в Лаборатории ядерных реакций), и весь научно-технический прогресс, который был за 15 лет.
Тут вопрос в том, как идти дальше. Надо остановиться в какой-то момент и сказать себе: теперь надо идти по-другому. Академик Л. А. Арцимович, у которого я учился, говорил: если вы хотите какую-то установку усовершенствовать, вы можете каждый из ее узлов улучшить – здесь на 10 %, там на 20 %, где-то на 30% – и получить улучшение результата в 2–3 раза. Но если вы хотите в 10 раз лучше, надо старую установку выбросить и делать новую.
То же самое и здесь (с фабрикой сверхтяжелых элементов): если хотим получить (чувствительность эксперимента) в 100 раз больше, то нужно остановиться и сделать что-то новое – тогда получишь нужный фактор и увидишь то, чего сейчас не видишь. Это, кстати, естественное человеческое отношение к любой вещи: если вы хотите сделать серьезный скачок, надо остановиться и делать дальше по-другому.
Это, кстати, естественное человеческое отношение к любой вещи: если вы хотите сделать серьезный скачок, надо остановиться и делать дальше по-другому.
– Помогает ли в дальнейшей работе признание новых элементов?
– Нет. Это не только мое мнение, но и всех, кто занимается этим делом. Например, когда вы готовите обед – ждете, что скажут гости, или сами чувствуете, что вкусно получилось? Если ты занимаешься делом каждый день, виден тот момент, когда действительно получается. Может быть, остальные не очень верят, но ты-то это видишь: один, второй раз (новый элемент образуется), потом еще и еще раз получается – вот это первая вещь, которая вселяет уверенность.
Вторая вещь, когда в другой лаборатории другие люди на другой установке повторяют тот же эксперимент «один к одному» – тогда и они верят. Еще признания нет, но уже всё понятно, и на конференциях по-другому звучит. А когда уже официально признали и вписали (новый элемент) в Таблицу, надо понимать, что это (его существование) не сейчас стало ясно, а гораздо раньше.
Например, по 117-му элементу, который наиболее сложно нам было получить, второй эксперимент закончили в 2010 году. За 5 лет, прошедшие с тех пор, в Америке в Беркли его повторили, в Германии в Дармштадте – всё то же самое. Хочу сказать, что это довольно-таки тяжелая работа: малое количество событий (когда синтезируется новый элемент), контроль эксперимента надо делать и т. д. А когда всё подтверждается и признается приоритет – это завершающий этап.
– Как получилось, что несколько сверхтяжелых элементов даже не пытались синтезировать в Лаборатории ядерных реакций?
– В 1974 году мы здесь, в Дубне, предложили и продемонстрировали новый метод синтеза элементов. А тогда строился ускоритель в Дармштадте, коллеги из Германии посмотрели и «ухватились» за него – было такое время, когда ездили каждую неделю к нам сюда. Они построили гигантский ускоритель, сделали замечательный сепаратор и применили наш принцип, чтобы синтезировать новые элементы в Дармштадте. Более 20 лет она работали и этим способом первыми получили элементы 107, 108, 109, 110, 111 и 112. Впрочем, 112-й и мы тоже получили.
Более 20 лет она работали и этим способом первыми получили элементы 107, 108, 109, 110, 111 и 112. Впрочем, 112-й и мы тоже получили.
Меня часто спрашивают: почему вы сами этим методом не занимались? Во-первых, у нас жизнь тогда была непростая – 90-е годы. Во-вторых, не важно, главное, что они нашим методом это сделали. В-третьих, что самое главное: было ясно, что этот метод более тяжелых элементов не даст – не хватает нейтронов, чтобы подойти к этой горе, к острову стабильности. Он ведет мимо «острова стабильности». Поэтому мы начали кальцием заниматься (облучением пучками изотопов кальция-48 мишеней из трансурановых элементов).
А немецкие коллеги дошли до 112-го, и это (возможности прежнего метода) было исчерпано, тем не менее, японцы начали делать 113-й тем же методом. Они за 9 лет получили 3 события (синтеза 113-го элемента) – я называю это «из кастрюли соскребать со дна». Это неинтересно, так как не имеет выхода дальше, а просто дает еще один элемент. Поэтому мы пошли в область нейтронно-избыточных (ядер). Там получается гораздо больше. У нас был сначала 115-й элемент, затем (как результат его альфа-распада) 113-й, и это примерно одно событие в день – в тысячу раз больше.
Поэтому мы пошли в область нейтронно-избыточных (ядер). Там получается гораздо больше. У нас был сначала 115-й элемент, затем (как результат его альфа-распада) 113-й, и это примерно одно событие в день – в тысячу раз больше.
– Поэтому присуждение Японии приоритета в открытии 113-го воспринято в научных кругах неоднозначно?
– О том, что мы синтезировали 115-й элемент, а из него (после альфа-распада всегда) получается 113-й, его «дочка», – я доложил на конгрессе ИЮПАК в 2003 году в Казани. А японцы свой первый результат опубликовали через год. То есть мы и по времени раньше, и событий у нас больше, и нашим методом можно к более тяжелым элементам идти, а японский эксперимент даже никто повторять не станет – какой смысл заниматься девять лет ради трех событий, если можно (действуя, как в Дубне) получать 113-й в сотнях штук. Поэтому и физики, и химики будут пользоваться нашим методом, который дает более тяжелый изотоп 113-го.
Может быть, ИЮПАК посчитал, что «слишком много» отдавать все четыре элемента в одни руки. Может, решил отдать должное упорству японцев. Можно разные догадки строить. Плохо то, что это решение ИЮПАК ничем не подтвердил. Они должны были подготовить и опубликовать отчет, потом провести дебаты по этому поводу – а пока (на 21 января 2016 года) отчета нет: как они смогли «дочь» (113-й) от «матери» (115-го) оторвать. Это всё уже номенклатура, но мы-то знаем, что это «наше дитя».
– Как придумывают названия для новых элементов?
– По правилам мы должны предложить названия «своих» элементов, но это не значит, что номенклатурная комиссия ИЮПАК примет то, что мы скажем. Ведь потом названия и двухбуквенные символы элементов будут использоваться в учебниках, в формулах химических соединений – важно, чтобы они звучали приемлемо на всех языках мира. Так, 105-й элемент – дубний, в честь города Дубны, 114-й – флеровий, в честь Лаборатории ядерных реакций и ее основателя Георгия Николаевича Флерова, 116-й – ливерморий, в честь города в Америке (места нахождения национальной лаборатории, совместно с которой проводились эксперименты по синтезу сверхтяжелых).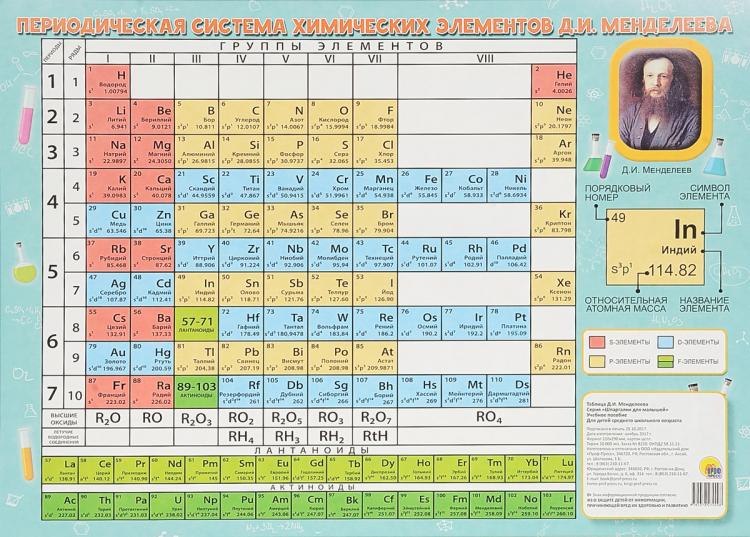
Обсуждается (для 115-го) название «московий». Важно понимать, что это в честь Московии как исторической русской древней территории. Сейчас на ней находятся Москва и Московская область, но речь не об административных единицах, а о земле Московии – той местности, в которой мы живем.
По двум другим элементам предложений пока не было, но мы должны отдать дань нашим коллегам-американцам, они внесли свой вклад. Знаете, в современном мире вообще так устроено: надо взять всё лучшее, что есть – и тогда можно чего-то достичь. Поэтому мы взяли самый мощный в мире реактор, который работает в Окридже, и самый мощный ускоритель, который работает в Дубне – и это дало такой мощный симбиоз. Вот такое сотрудничество, когда одно без второго не даст ничего, когда обе стороны являются фундаментами, – это и есть настоящее сотрудничество. У нас оно и дальше будет продолжаться. Вот сейчас у нас (в циклотроне) стоит американская мишень, на пучке облучается. И новые элементы – это наш общий результат, хотя эксперименты делаются в Дубне.
Что касается названия третьего из элементов, надо подумать – у нас есть на это время. Но, вообще говоря, мы будем следовать традиции. А по традиции принято называть элементы либо в честь планет (Плутон, Нептун, Уран), либо в честь великих ученых (Кюри, Ферми, Менделеев), либо в честь мест, где произошло их открытие (в честь немецкой земли Гессен получил название 108-й элемент, хассий). Этот вариант мне нравится больше всего, потому что когда пишешь статью по результатам эксперимента, количество авторов ограничено, хотя участвует в нем множество людей. И если элемент назван в честь места, где он открыт, все себя чувствуют упомянутыми в этом названии. Вот когда был объявлен наш приоритет по элементам 114 и 116, я предложил выписать одинаковые премии всем сотрудникам лаборатории – от директора до уборщиц, потому что все участвовали. По большому счету надо вспомнить и всех, кто работал в лаборатории раньше, ведь труд каждого здесь остался. И когда мы называем элемент в честь нашей земли, я считаю такой подход – гуманный и правильный. Не будем отходить от этой традиции.
Не будем отходить от этой традиции.
Международный год Периодической таблицы химических элементов Дмитрия Менделеева
Среда, 24 апреля 2019
В 2019 году исполняется 150 лет с открытия Д.И. Менделеевым Периодического закона. В те времена науке ничего не было известно о внутреннем строении атомов, поэтому Дмитрий Иванович столкнулся с серьезными трудностями при систематизации большого числа элементов. Несмотря на это, ему удалось установить, что свойства элементов находятся в периодической зависимости от некоторого параметра (во времена Менделеева это был атомный вес, а теперь число протонов в ядре атома) и построить свою знаменитую таблицу химических элементов. В таблице Менделеева свойства для элементов, находящихся в одном столбце (подгруппе), похожи и существенно различаются для элементов в одной строке (периоде). Химические свойства элементов определяются главным образом числом валентных (внешних) электронов, тогда как óстовные (глубоко лежащие) электроны лишь экранируют (уменьшают) действие электрического заряда ядра, определяемого числом протонов. Таким образом, элементы в одной подгруппе имеют одинаковое число валентных электронов, но различаются числом остовных, а элементы в одном периоде наоборот имеют одинаковое число остовных электронов и разное число валентных.
Таким образом, элементы в одной подгруппе имеют одинаковое число валентных электронов, но различаются числом остовных, а элементы в одном периоде наоборот имеют одинаковое число остовных электронов и разное число валентных.
В наши дни появилась возможность на достаточно мощных компьютерах рассчитывать свойства элементов (и их соединений с другими элементами) с высокой точностью. Первые численные расчеты атомов были выполнены М.И. Петрашень карандашом еще в 1934 г., но систематически такие расчеты начали выполнять только с 60-х годов, когда появились первые компьютерные программы Ch. Froese Fischer (Канада-США), уроженки Донецкой области, и В.Ф. Братцева, сотрудника ЛГУ (СПбГУ). Для более тяжелых элементов (нижней половины Таблицы Менделеева) важно учитывать релятивистские эффекты. Первые программы по методу Хартри-Фока-Дирака разработаны I.P. Grant (Англия), J.-P. Desclaux (Франция) и В.Ф. Братцевым, Г.Б. Дейнека и И.И. Тупицыным (СССР) в 70-е годы и, соответственно, в это же время стали выполняться релятивистские расчеты атомов. Однако систематические релятивистские расчеты даже двухатомных молекул стали возможными только двумя десятилетиями позже, в 90-х годах прошлого века, поскольку вычислительных мощностей для полного учета движения всех электронов не хватало уже для описания простейших молекул с тяжелыми атомами. Более того, даже для релятивистских расчетов двухатомных молекул пришлось использовать приближения, которые вытекали из Периодического закона Д.И. Менделеева, – только относительно небольшое число валентных электронов учитывалось в расчетах явным образом. В таком приближении расчет любого атома в подгруппе будет требовать близких вычислительных затрат. Остовные электроны вместе с зарядом ядра формируют электрическое поле (а при учете релятивизма – и магнитное поле), в котором движутся эти электроны. Задача точного вычисления этого поля весьма непростая, но уже в середине 30-х годов прошлого века Г. Гельман (СССР) и P. Gombas (Венгрия) предложили моделировать его с помощью некоторого приближенного псевдопотенциала.
Однако систематические релятивистские расчеты даже двухатомных молекул стали возможными только двумя десятилетиями позже, в 90-х годах прошлого века, поскольку вычислительных мощностей для полного учета движения всех электронов не хватало уже для описания простейших молекул с тяжелыми атомами. Более того, даже для релятивистских расчетов двухатомных молекул пришлось использовать приближения, которые вытекали из Периодического закона Д.И. Менделеева, – только относительно небольшое число валентных электронов учитывалось в расчетах явным образом. В таком приближении расчет любого атома в подгруппе будет требовать близких вычислительных затрат. Остовные электроны вместе с зарядом ядра формируют электрическое поле (а при учете релятивизма – и магнитное поле), в котором движутся эти электроны. Задача точного вычисления этого поля весьма непростая, но уже в середине 30-х годов прошлого века Г. Гельман (СССР) и P. Gombas (Венгрия) предложили моделировать его с помощью некоторого приближенного псевдопотенциала. Псевдопотенциал строится для фиксированного числа валентных электронов каждого атома один раз, а затем может использоваться без изменений во множестве расчетов всего многообразия химических соединений этого элемента.
Псевдопотенциал строится для фиксированного числа валентных электронов каждого атома один раз, а затем может использоваться без изменений во множестве расчетов всего многообразия химических соединений этого элемента.
Метод псевдопотенциала – приближенный, поэтому наиболее очевидное дальнейшее его развитие должно сопровождаться повышением точности расчетов с псевдопотенциалом. На первый взгляд для этого нужно просто увеличить число явно рассматриваемых в расчете с псевдопотенциалом электронов за счет добавления наиболее внешних из остовных электронов к валентным. Далее для простоты мы будем называть эти (валентные и внешние остовные) электроны – активными, а оставшиеся, внутренние остовные электроны – неактивными, поскольку последние являются наиболее инертными химически. Тогда движение бóльшего числа активных электронов будут описываться точно, а с помощью приближенного псевдопотенциала будет моделироваться меньшее число неактивных остовных электронов. В частности, для расчета химических соединений ртути с очень высокой точностью достаточно включить в расчет 20 самых внешних («активных») электронов атома, а 60 внутренних остовных («неактивных») электронов исключить из расчета, заменив их действие на активные электроны псевдопотенциалом.
Однако на практике простого увеличения числа активных электронов оказывается недостаточно, и в НИЦ «Курчатовский институт» – ПИЯФ было показано, что необходимо совершенствовать и выражение для псевдопотенциала, в частности, строить существенно разные компоненты псевдопотенциала для описания движения валентных и внешних остовных электронов данного атома. [В рамках канонического варианта псевдопотенциала – «полулокального» (или «радиально-локального») – введенного в квантовую химию еще в 1965 году И.В. Абаренковым (ЛГУ, ныне СПбГУ) и V. Heine (Кавендишская лаборатория, Англия) – этого сделать нельзя]. Для построения высокоточного псевдопотенциала данная идея была развита в рамках более сложного, «обобщенного» варианта псевдопотенциала, но на пути его реализации возникли серьезные, многочисленные трудности, на преодоление которых потребовалось почти десятилетие (1991-1999 гг., см. сайт лаборатории http://qchem.pnpi.spb.ru и [A.V. Titov, N.S. Mosyagin, Int. J. Quantum Chem., 71, 359 (1999)]). В конечном итоге разработанный в НИЦ «Курчатовский институт» – ПИЯФ метод позволил выйти на новый, более высокий уровень точности расчетов за счет более оптимального разбиения электронов на активные и неактивные для данного конкретного типа задач, а также за счет более правильного описания динамики активных электронов с использованием предложенного обобщенного варианта псевдопотенциала. Вплоть до настоящего времени, метод обобщенного псевдопотенциала позволяет добиваться наиболее точных результатов в расчетах даже двухатомных молекул, содержащих тяжелые переходные металлы, лантаноиды и актиноиды.
В конечном итоге разработанный в НИЦ «Курчатовский институт» – ПИЯФ метод позволил выйти на новый, более высокий уровень точности расчетов за счет более оптимального разбиения электронов на активные и неактивные для данного конкретного типа задач, а также за счет более правильного описания динамики активных электронов с использованием предложенного обобщенного варианта псевдопотенциала. Вплоть до настоящего времени, метод обобщенного псевдопотенциала позволяет добиваться наиболее точных результатов в расчетах даже двухатомных молекул, содержащих тяжелые переходные металлы, лантаноиды и актиноиды.
Серьезным недостатком метода псевдопотенциала долгое время считалась невозможность расчета таких свойств, которые определяются главным образом «хвостами» валентных орбиталей (одноэлектронных состояний) в óстовной области атома (вблизи атомного ядра). К таким свойствам (которые называются свойствами атомов-в-соединениях) относятся сверхтонкая структура, химические сдвиги линий мёссбауэровских и рентгеновских эмиссионных спектров. Это обусловлено сглаживанием валентных орбиталей в атóмном остове в процедуре построения псевдоорбиталей. В 90-х годах прошлого века в НИЦ «Курчатовский институт» – ПИЯФ была разработана процедура восстановления правильных валентных орбиталей (точнее, релятивистских «спиноров») после выполнения расчета молекулы (твердого тела) с псевдопотенциалом, которая успешно зарекомендовала себя в практических расчетах. Таким образом, в случае соединений тяжелых элементов трудновыполнимая задача высокоточного расчета движений всех электронов разбивается на две более мелких задачи – первоначального расчета рассматриваемой системы в валентной области с использованием псевдопотенциала, а затем – «восстановление правильной электронной структуры» в остовах тяжелых атомов. Иными словами, вместо «перемножения трудностей» расчета электронной структуры соединений тяжелых элементов, мы их складываем. Применение данного подхода в практических релятивистских молекулярных расчетах свойств «атомов-в-соединениях» с использованием двухшагового подхода (расчета методом обобщенного псевдопотенциала с последующим восстановлением электронной структуры в атомных остовах) позволило в НИЦ «Курчатовский институт» – ПИЯФ еще 20 лет назад на доступных в то время компьютерах получить такие результаты, которые только относительно недавно были получены зарубежными учеными на современных компьютерах.
Это обусловлено сглаживанием валентных орбиталей в атóмном остове в процедуре построения псевдоорбиталей. В 90-х годах прошлого века в НИЦ «Курчатовский институт» – ПИЯФ была разработана процедура восстановления правильных валентных орбиталей (точнее, релятивистских «спиноров») после выполнения расчета молекулы (твердого тела) с псевдопотенциалом, которая успешно зарекомендовала себя в практических расчетах. Таким образом, в случае соединений тяжелых элементов трудновыполнимая задача высокоточного расчета движений всех электронов разбивается на две более мелких задачи – первоначального расчета рассматриваемой системы в валентной области с использованием псевдопотенциала, а затем – «восстановление правильной электронной структуры» в остовах тяжелых атомов. Иными словами, вместо «перемножения трудностей» расчета электронной структуры соединений тяжелых элементов, мы их складываем. Применение данного подхода в практических релятивистских молекулярных расчетах свойств «атомов-в-соединениях» с использованием двухшагового подхода (расчета методом обобщенного псевдопотенциала с последующим восстановлением электронной структуры в атомных остовах) позволило в НИЦ «Курчатовский институт» – ПИЯФ еще 20 лет назад на доступных в то время компьютерах получить такие результаты, которые только относительно недавно были получены зарубежными учеными на современных компьютерах. Тем самым, была полностью подтверждена высокая эффективность развиваемого в Институте двухшагового подхода. Отметим, что несколько позднее, в 1994 г., похожую двухшаговую идею расчета реализовал P. Blöchl в методе «проектированных плоских волн», но в нерелятивистском приближении и для твердого тела в первую очередь с целью повышения точности расчетов с «ультрамягким» псевдопотенциалом.
Тем самым, была полностью подтверждена высокая эффективность развиваемого в Институте двухшагового подхода. Отметим, что несколько позднее, в 1994 г., похожую двухшаговую идею расчета реализовал P. Blöchl в методе «проектированных плоских волн», но в нерелятивистском приближении и для твердого тела в первую очередь с целью повышения точности расчетов с «ультрамягким» псевдопотенциалом.
Для обеспечения теоретической поддержки исследований электронной структуры, свойств материалов, молекул и кластеров, которые могут содержать тяжелые элементы, включая актиноиды и лантаноиды, а также с целью дальнейшего развития достижений в области моделирования электронной структуры химических соединений и их взаимодействия с электромагнитными полями, разработки соответствующих теоретических методов, компьютерных программ и создания баз данных на основе теоретической группы НИЦ «Курчатовский институт» – ПИЯФ 1 апреля 2014 года в новом Отделении перспективных разработок была создана Лаборатория квантовой химии (ЛКХ). В настоящее время ЛКХ насчитывает 5 научных групп, которые занимаются наиболее прецизионными и комбинированными методами релятивистского расчета молекул и твердых тел; теоретической поддержкой фундаментальных экспериментов по поиску Новой физики; моделированию свойств новых сверхтяжелых элементов из «острова стабильности», открытых в последние два десятилетия в Дубне, для их «химической идентификации»; лазерному охлаждению молекул; моделированию углеродных и металлоорганических структур, материалов и точечных дефектов, содержащих переходные металлы, лантаноиды и актиноиды, а также разработке неразрушающих методов контроля состояния атомов в веществе.
В настоящее время ЛКХ насчитывает 5 научных групп, которые занимаются наиболее прецизионными и комбинированными методами релятивистского расчета молекул и твердых тел; теоретической поддержкой фундаментальных экспериментов по поиску Новой физики; моделированию свойств новых сверхтяжелых элементов из «острова стабильности», открытых в последние два десятилетия в Дубне, для их «химической идентификации»; лазерному охлаждению молекул; моделированию углеродных и металлоорганических структур, материалов и точечных дефектов, содержащих переходные металлы, лантаноиды и актиноиды, а также разработке неразрушающих методов контроля состояния атомов в веществе.
Каковы первые 20 элементов? элементы периодической таблицы.
Удобно знать первые 20 элементов периодической таблицы. Около 99% массы человеческого тела состоит из шести этих элементов. Первые 20 элементов также являются хорошим обзором различных групп элементов. Они также происходят в более повседневных химических реакциях.
Список первых 20 элементов
Элементы перечислены в порядке возрастания атомного номера. Атомный номер – это количество протонов в атомах каждого элемента. Первые 20 элементов и их символы:
Атомный номер – это количество протонов в атомах каждого элемента. Первые 20 элементов и их символы:
- Водород (H)
- Гелий (He)
- Литий (Li)
- Бериллий (Be)
- Бор (B)
- Азот (C)
- N)
- Кислород (O)
- Фтор (F)
- Неон (Ne)
- Натрий (Na)
- Magnesium (Mg)
- Aluminum (Al)
- Silicon (Si)
- Phosphorus (P)
- Sulfur (S)
- Chlorine (Cl)
- Argon (Ar)
- Potassium (K)
- Кальций (Ca)
Что делает их элементами?
Как минимум, вещество должно содержать один или несколько протонов, чтобы быть элементом. Количество протонов идентифицирует элемент. Атомы элементов могут также содержать нейтроны вместе с протонами, образующими атомное ядро. Образцы с одинаковым количеством протонов, но разным количеством нейтронов — это один и тот же элемент, но разные изотопы. Атомы также имеют электроны, которые вращаются вокруг ядра. Изменение количества электронов вокруг атома делает его ионом, но не меняет его идентичности как элемента. Элементы называют строительными блоками материи, потому что их атомы нельзя разделить на более мелкие части никакими химическими средствами. Атомы элементов могут образовывать химические связи друг с другом, образуя соединения.
Изменение количества электронов вокруг атома делает его ионом, но не меняет его идентичности как элемента. Элементы называют строительными блоками материи, потому что их атомы нельзя разделить на более мелкие части никакими химическими средствами. Атомы элементов могут образовывать химические связи друг с другом, образуя соединения.
Имена и символы элементов
Элементы могут быть идентифицированы по их атомному номеру, имени элемента или символу элемента. Символ представляет собой одно- или двухбуквенное сокращение имени. Однако некоторые символы относятся к старым именам элементов. Например, символом натрия является Na. Это относится к латинскому слову natrium , которое было старым названием едкого натра. Символом калия является K, что означает латинское слово kalium , означающее щелочь или поташ. Первая буква символа элемента заглавная. Когда есть вторая буква, она в нижнем регистре.
Песня об элементах
Теперь, когда вы знаете первые 20 элементов, почему бы не выучить названия еще нескольких? Попробуйте спеть «The Element Song» или подпевайте!
Пристальный взгляд на первые 20 элементов
Вот краткое описание каждого из первых 20 элементов, включая внешний вид, состояние вещества при нормальной температуре и давлении, атомный номер, символ, атомную массу, электронную конфигурацию и элемент. группа:
группа:
Водород
Водород — первый элемент и самый распространенный во Вселенной.- Водород представляет собой неметаллический бесцветный газ при обычных условиях. Под экстремальным давлением он становится щелочным металлом. Существует три изотопа этого элемента, которые отличаются количеством нейтронов в своих атомах. Наиболее распространенным изотопом является протий. Остальные – дейтерий и тритий.
- Атомный номер: 1
- Символ: H
- Атомная масса: 1,008
- Электронная конфигурация: 1s 1
- Группа: группа 1, s-блок, неметалл
Гелий
- Гелий — легкий бесцветный газ.
- Атомный номер: 2
- Символ: HE
- Атомная масса: 4.002602 (2)
- Электронная конфигурация: 1S 2
- Группа: Группа 18, S-Block, Noble Gas
7 Lithium
777 Lithium77777 Lithium
7777777777 Lithium7777777777777 Lithium
7777777777777777777777 годы Lithium7777777777777777777777777777 гг.
 высокореактивный металл.
высокореактивный металл.- Литий представляет собой реактивный твердый металл серебра.
- Атомный номер: 3
- Символ: Li
- Атомная масса: 6,94 (6,938–6,997)
- Электронная конфигурация: [He] 2s 1
- Группа: группа 1, s-блок, щелочной металл
Бериллий
- Бериллий — блестящий серо-белый твердый металл.
- Атомный номер: 4
- Символ: Be
- Атомная масса: 9,0121831(5)
- Электронная конфигурация: [He] 2s 2
- Группа: группа 2, 9079, 9079, 90, 79, 90, 90, 90, 90, 90, 90, s-блок, 90, 90, щелочные
- Бор представляет собой твердое вещество серого цвета с металлическим блеском.
- Атомный номер: 5
- Символ: B
- Атомная масса: 10,81 (10,806–10,821)
- Электронная конфигурация: [HE] 2S 2 2P 1
- Группа: Группа 13, PLOCK, Meterloid, Methalloid, Methalloid, Methalloid, Methalloid, Methalloid, Methalloid, PLOCK 13, PLOCK.

Углерод
- Углерод представляет собой твердое вещество, которое принимает несколько форм, включая алмаз, графит и аморфный углерод. Он черный, серый или бесцветный.
- Атомный номер: 6
- Символ: C
- Атомная масса: 12,011 (12,0096–12.0116)
- Электронная конфигурация: [He] 2s 2 2p 2
- Группа: группа 14, р-блок, обычно неметалл, хотя иногда считается металлоидом
Азот бесцветный
газ. Атомный номер: 7 Символ: N Атомная масса: 14,007 Электронная конфигурация: [He] 2s 2 2p 3 Группа0017 Кислород
- Кислород — бесцветный газ. Его жидкая форма имеет синий цвет, в то время как твердая форма имеет множество цветов, включая красный, металлический и черный.
- Атомный номер: 8
- Символ: O
- Атомная масса: 15,999 или 16,00
- Электронная конфигурация: [HE] 2S 2 2P 4
- Группа: Группа 16 (Chalcogen
Фтор
- Фтор представляет собой бледно-желтый газ и жидкость и ярко-желтое твердое вещество.

- Атомный номер: 9
- Символ: F
- Атомная масса: 18,998403163 (6)
- Электронная конфигурация: [HE] 2S 2 2P 5
- Группа: Группа 17, PLOCK 5
- : Группа 17, PLOCK 5
- : Группа 17, PLOCK 5
- : Группа 17, PLOCK.
Неон
- Неон — бесцветный газ, излучающий оранжево-красное свечение при возбуждении в электрическом поле.
- Атомный номер: 10
- Символ: Ne
- Атомная масса: 20,1797(6)
- Электронная конфигурация: [He] 2s 2 2p 6
- Группа: группа 18, р-блок, благородный газ
Натрий
- Натрий — мягкий твердый металл серебристо-белого цвета.
- Atomic Number: 11
- Symbol: Na
- Atomic Mass: 22.98976928(2)
- Electron Configuration: [Ne] 3s 1
- Group: group 1, s-block, alkali metal
Magnesium
- Магний представляет собой блестящий серый твердый металл.

- Атомный номер: 12
- Обозначение: Mg
- Атомная масса: 24,305
- Электронная конфигурация: [Ne] 3s 2
- Группа: группа 2, s-блок, щелочноземельный металл
серебро, алюминий
цветной, немагнитный металл. Атомный номер: 13 Символ: Al Атомная масса: 26,9815385(7) Электронная конфигурация: [Ne] 3s 2 3p 1 группа 3 , p- группа 3 , p-блок 1
-переходный металл или иногда металлоид Кремний
- Кремний представляет собой твердое кристаллическое вещество серо-голубого цвета с металлическим блеском.
- Atomic Number: 14
- Symbol: Si
- Atomic Mass: 28.085
- Electron Configuration: [Ne] 3s 2 3p 2
- Group: group 14 (carbon group), p-block, metalloid
Фосфор
- Фосфор в обычных условиях является твердым, но принимает несколько форм.
 Наиболее распространены белый фосфор и красный фосфор.
Наиболее распространены белый фосфор и красный фосфор. - Атомный номер: 15
- Символ: P
- Атомная масса: 30,973761998 (5)
- Электронная конфигурация: [NE] 3S 2 3P 3
- Группа: Группа 15 (PN 15PGENGEG), PN-LOCKEGEN), PN-BLICTOG), PN-BLICTOG). обычно считается неметаллом, но иногда и металлоидом
Сера
Сера — желтый неметалл.- Сера представляет собой желтое твердое вещество, обычно встречающееся в виде кристаллов или порошка.
- Атомный номер: 16
- Символ: S
- Атомная масса: 32,06
- Электронная конфигурация: [Ne] 3s 2 3p 4
- Группа: группа 16 (халькогены), p-блок, неметаллический Его жидкая форма имеет ярко-желтый цвет.
- Атомный номер: 17
- Символ: Cl
- Атомная масса: 35,45
- Электронная конфигурация: [Ne] 3s 2 3p 5
группа p-блок, p-группа:- 0017
Аргон
- Аргон представляет собой бесцветный газ, жидкость и твердое вещество.
 Это газ при обычных условиях. Он излучает яркое сиренево-фиолетовое свечение при возбуждении в электрическом поле.
Это газ при обычных условиях. Он излучает яркое сиренево-фиолетовое свечение при возбуждении в электрическом поле. - Атомный номер: 18
- Символ: AR
- Атомная масса: 39,948 (1)
- Электронная конфигурация: [NE] 3S 2 3P 6
- Группа: Группа 18, P-Block, NOBLE
7777- Группа: Группа 18, P-Block, NOBLE
777777- : Группа 18, P-Block, NOBLE
777777- : Группа 18, P-Block, NOBLE
777777- .
Калий
- Калий – реактивный серебристый твердый металл.
- Атомный номер: 19
- Символ: K
- Атомная масса: 39,0983 (1)
- Электронная конфигурация: [AR] 4S 1
- Группа: Группа 1, SCLOC
- Кальций представляет собой твердый металл серебристого цвета со слабым желтоватым оттенком.
- Атомный номер: 20
- Символ: Ca
- Атомная масса: 40,078(4)
- Электронная конфигурация: [Ar] 4s 2
- Группа: группа 2, s-блок, щелочноземельный металл0017
Ссылки
- Болл, П.
 (2004). Элементы: очень краткое введение . Издательство Оксфордского университета. ISBN 978-0-19-284099-8.
(2004). Элементы: очень краткое введение . Издательство Оксфордского университета. ISBN 978-0-19-284099-8. - Эмсли, Дж. (2003). Строительные блоки природы: Путеводитель по элементам от А до Я . Издательство Оксфордского университета. ISBN 978-0-19-850340-8.
- Грей, Т. (2009). Элементы: Визуальное исследование каждого известного атома во Вселенной . ISBN Black Dog & Leventhal Publishers Inc. 978-1-57912-814-2 .
- ИЮПАК (1997). «Химический элемент». Сборник химической терминологии (2-е изд.). doi:10.1351/goldbook.C01022
3.7: Заполнение периодической таблицы из 20 элементов
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 78937
- Стэнли Э.
 Манахан
Манахан - Университет Миссури
Пока в этой главе были определены и обсуждены 10 элементов. Всего требуется еще 10, чтобы заполнить сокращенную периодическую таблицу из 20 элементов. Их имена и свойства кратко описаны здесь. Периодическая таблица представлена на рис. 3.9.
Натрий , Na , атомный номер 11, атомная масса 22,99, находится сразу после лития в периодической таблице и очень похож на литий, поскольку является мягким, химически очень активным металлом. В ядре атома есть один основной изотоп натрия, содержащий 12 нейтронов. Натрий имеет 10 электронов на внутренней оболочке, содержащихся в его первой внутренней оболочке из 2 электронов и во второй из 8 электронов. 11-й электрон в атоме натрия находится в третьей оболочке, которая является внешней оболочкой. Это показано одной точкой в символе Льюиса для Na на рис. 3.7. Электроны в натрии можно представить так, как показано на рис. 3.7.
Рисунок 3.7. Представление электронов в 2 внутренних оболочках и 1 внешней оболочке натрия и символе Льюиса натрия.
Магний , Mg , атомный номер 12, атомная масса 24,31, имеет 12 электронов на атом, поэтому он имеет 2 электрона внешней оболочки. Есть три изотопа магния, содержащие 12, 13 и 14 нейтронов. Магний — это относительно прочный и очень легкий металл, который используется в самолетах, выдвижных лестницах, переносных инструментах и других устройствах, где особенно важен легкий вес.
Алюминий , Al , атомный номер 13, атомная масса 26,98, имеет 3 электрона внешней оболочки в дополнение к 10 электронам внутренней оболочки. Алюминий — легкий металл, используемый в самолетах, автомобилях, линиях электропередач, строительстве зданий и во многих других областях. Несмотря на то, что он химически активен, оксидное покрытие, образующееся, когда алюминий на поверхности металла реагирует с кислородом воздуха, является самозащитным и предотвращает коррозию.
В некоторых важных отношениях алюминий можно рассматривать как зеленый металл. Это связано с тем, что алюминий позволяет создавать прочные легкие компоненты, которые при использовании в самолетах и автомобилях требуют относительно меньше энергии для перемещения. Таким образом, алюминий играет важную роль в энергосбережении. Алюминиевые кабели также обеспечивают эффективный способ передачи электроэнергии. Хотя руды, из которых изготавливается алюминий, являются извлекаемым ресурсом, добываемым из земли, алюминий является распространенным элементом. И есть альтернативные ресурсы, которые можно разрабатывать, в том числе алюминий в летучей золе, оставшейся от сжигания угля. Кроме того, алюминий является одним из наиболее пригодных для повторного использования металлов, а алюминиевый лом легко переплавляется и превращается в новые алюминиевые изделия.
Это связано с тем, что алюминий позволяет создавать прочные легкие компоненты, которые при использовании в самолетах и автомобилях требуют относительно меньше энергии для перемещения. Таким образом, алюминий играет важную роль в энергосбережении. Алюминиевые кабели также обеспечивают эффективный способ передачи электроэнергии. Хотя руды, из которых изготавливается алюминий, являются извлекаемым ресурсом, добываемым из земли, алюминий является распространенным элементом. И есть альтернативные ресурсы, которые можно разрабатывать, в том числе алюминий в летучей золе, оставшейся от сжигания угля. Кроме того, алюминий является одним из наиболее пригодных для повторного использования металлов, а алюминиевый лом легко переплавляется и превращается в новые алюминиевые изделия.
Если бы «элемент века» был назван в честь 1900-х годов, скромный кремний , Si , атомный номер 14, атомная масса 28,09 был бы вероятным кандидатом. Это связано с тем, что кремний является наиболее часто используемым из полупроводниковых элементов и в конце 1900-х годов стал основой для бурного развития электроники и компьютеров на основе полупроводниковых устройств, состоящих в основном из кремния. Несмотря на ценность этих продуктов на основе кремния, кремний в изобилии содержится в почве и горных породах, занимая второе место после кислорода в составе земной коры. Атом кремния имеет 4 электрона на внешней оболочке, половину октета, и это металлоид, промежуточный по поведению между металлами слева в периодической таблице и неметаллами справа.
Несмотря на ценность этих продуктов на основе кремния, кремний в изобилии содержится в почве и горных породах, занимая второе место после кислорода в составе земной коры. Атом кремния имеет 4 электрона на внешней оболочке, половину октета, и это металлоид, промежуточный по поведению между металлами слева в периодической таблице и неметаллами справа.
Значительно уменьшив объем электронных компонентов по сравнению с производительностью, кремний способствовал огромной экономии материалов, используемых в радиоприемниках, телевизорах, коммуникационном оборудовании и других электронных устройствах. Кроме того, полупроводниковые устройства на основе кремния, используемые в твердотельной электронике, потребляют лишь часть электроэнергии, которая когда-то использовалась устройствами на основе электронных ламп. Громоздкие провода из относительно редкой меди, использовавшиеся ранее для электрической передачи сигналов связи, были в значительной степени заменены оптоволоконными устройствами, состоящими из прозрачного кремнезема SiO2, которые передают информацию в виде световых импульсов. Оптическое волокно, похожее на волос, может передавать во много раз больше информации в единицу времени, чем толстый медный провод, который оно заменяет. А энергия, необходимая для передачи единицы информации по оптоволоконному кабелю, ничтожна по сравнению с энергией, необходимой для передачи той же информации электрическим импульсом по медному проводу. Таким образом, кремний — это действительно зеленый элемент, который, хотя и дешев и распространен, выполняет электронные и коммуникационные функции намного быстрее и лучше, чем медь и другие металлы, которые он заменил.
Оптическое волокно, похожее на волос, может передавать во много раз больше информации в единицу времени, чем толстый медный провод, который оно заменяет. А энергия, необходимая для передачи единицы информации по оптоволоконному кабелю, ничтожна по сравнению с энергией, необходимой для передачи той же информации электрическим импульсом по медному проводу. Таким образом, кремний — это действительно зеленый элемент, который, хотя и дешев и распространен, выполняет электронные и коммуникационные функции намного быстрее и лучше, чем медь и другие металлы, которые он заменил.
Фосфор , P , атомный номер 15, атомная масса 30,97, имеет 5 электронов на внешней оболочке. Таким образом, он находится непосредственно под азотом в периодической таблице и напоминает азот по своему химическому поведению. Чистый элементарный фосфор встречается в нескольких формах, наиболее распространенной из которых является белый фосфор. Белый фосфор является химически очень активным неметаллом, который может самовозгораться в атмосфере. Он токсичен и вызывает разрушение костей. Челюстная кость особенно восприимчива к воздействию фосфора, и у нее развивается состояние, известное как «фоссиальная челюсть», при котором кость становится пористой и слабой и может сломаться от нагрузки при жевании. Однако химически связанный фосфор является важным элементом жизни и одним из компонентов ДНК, основной молекулы, управляющей молекулярными жизненными процессами. Фосфор также является важным удобрением для растений и входит в состав многих промышленных химикатов, включая некоторые пестициды.
Он токсичен и вызывает разрушение костей. Челюстная кость особенно восприимчива к воздействию фосфора, и у нее развивается состояние, известное как «фоссиальная челюсть», при котором кость становится пористой и слабой и может сломаться от нагрузки при жевании. Однако химически связанный фосфор является важным элементом жизни и одним из компонентов ДНК, основной молекулы, управляющей молекулярными жизненными процессами. Фосфор также является важным удобрением для растений и входит в состав многих промышленных химикатов, включая некоторые пестициды.
Мышьяк находится в той же группе периодической таблицы, что и фосфор, и встречается в виде примеси с фосфором, переработанным из руды. Если этот фосфор будет использоваться в пищу, мышьяк должен быть удален.
Сера , S , атомный номер 16, атомная масса 32,06, имеет 6 электронов на внешней оболочке. Это хрупкий неметалл желтого цвета. Это важное питательное вещество для растений и животных, встречающееся в аминокислотах, из которых состоят белки. Сера является распространенным загрязнителем воздуха, выбрасываемым в атмосферу в виде двуокиси серы SO2 при сжигании ископаемого топлива, содержащего серу. Большая часть больших количеств серы, необходимых для промышленного производства серной кислоты и других серосодержащих химикатов, регенерируется из сероводорода, h3S, который загрязняет большую часть природного газа (метан, Ch5), который является таким важным топливом и сырьем. в мире сегодня. В соответствии с передовой практикой «зеленой» химии сероводород отделяется от сырого природного газа и сжигается около 1/3 его объема9.0007
Сера является распространенным загрязнителем воздуха, выбрасываемым в атмосферу в виде двуокиси серы SO2 при сжигании ископаемого топлива, содержащего серу. Большая часть больших количеств серы, необходимых для промышленного производства серной кислоты и других серосодержащих химикатов, регенерируется из сероводорода, h3S, который загрязняет большую часть природного газа (метан, Ch5), который является таким важным топливом и сырьем. в мире сегодня. В соответствии с передовой практикой «зеленой» химии сероводород отделяется от сырого природного газа и сжигается около 1/3 его объема9.0007
\[\ce{2h3S + 3O2 → 2SO2 + 2h3O} \label{3.7.1}\]
по производству диоксида серы, SO2. Затем полученный диоксид серы вступает в реакцию с оставшимся сероводородом посредством реакции Клауса, описанной ниже, с получением продукта элементарной серы, который используется для синтеза серной кислоты и других серосодержащих химических веществ.
\[\ce{2h3S + SO2 → 3S + 2h3O } \label{2.7.2}\]
Хлор , Cl , атомный номер 17, атомная масса 35,453, имеет 7 электронов на внешней оболочке, всего на 1 электрон меньше полного октета. Элементарный хлор представляет собой двухатомный газ зеленовато-желтого цвета, состоящий из молекул Cl2. В этих молекулах атомы Cl достигают стабильных октетов электронов внешней оболочки, разделяя два электрона в ковалентной связи, как показано на рис. 3.8. Атом хлора также может принять электрон для получения стабильного октета в анионе Cl-, как показано в ионном соединении хлорида натрия, NaCl, на рис. 3.8.
Элементарный хлор представляет собой двухатомный газ зеленовато-желтого цвета, состоящий из молекул Cl2. В этих молекулах атомы Cl достигают стабильных октетов электронов внешней оболочки, разделяя два электрона в ковалентной связи, как показано на рис. 3.8. Атом хлора также может принять электрон для получения стабильного октета в анионе Cl-, как показано в ионном соединении хлорида натрия, NaCl, на рис. 3.8.
Рисунок 3.8. Атомы хлора могут достигать стабильного октета электронов внешней оболочки, разделяя электроны в ковалентных связях, как показано для молекулярного двухатомного элементарного Cl2, или путем принятия электронов с образованием аниона Cl-, как показано для ионного хлорида натрия, NaCl. Элементарный хлор может быть смертельным при вдыхании и был первым военным отравляющим газом, использованным в Первой мировой войне. Несмотря на свою токсичность, газообразный хлор спас много жизней благодаря его использованию в течение примерно последних 100 лет в качестве дезинфицирующего средства для питьевой воды, которое уничтожило смертельные болезни, передающиеся через воду, такие как холера и брюшной тиф. Хлор является важным промышленным химическим веществом, которое используется для производства пластмасс и растворителей. Недостаток хлора исключен, и его можно получить даже пропусканием электрического тока через морскую воду, содержащую хлор в виде растворенного хлорида натрия.
Хлор является важным промышленным химическим веществом, которое используется для производства пластмасс и растворителей. Недостаток хлора исключен, и его можно получить даже пропусканием электрического тока через морскую воду, содержащую хлор в виде растворенного хлорида натрия.
Экологичность хлора зависит от его применения. Элементарный хлор, безусловно, представляет собой опасный материал, производства и использования которого следует по возможности избегать в практике «зеленой» химии. Но, как отмечалось выше, элементарный хлор спас много жизней благодаря его использованию для дезинфекции воды. Ряд стойких пестицидов, включая ДДТ, представляют собой органические соединения, состоящие из хлора, углерода и водорода. В дополнение к экологическому ущербу, наносимому этими пестицидами, побочные продукты их производства и производства других хлорорганических соединений являются одними из наиболее распространенных загрязнителей опасных химических отходов. Обычный пластик, поливинилхлорид (ПВХ), содержит хлор. Этот пластик широко используется в водопроводных и дренажных трубах, в первом случае заменяя относительно дефицитный и дорогой металл меди и токсичный свинец. Но материал, используемый для производства ПВХ, представляет собой летучий винилхлорид. Это один из немногих известных канцерогенов для человека, вызывающий задокументированные случаи редкой формы рака печени у рабочих, которые ранее подвергались воздействию очень высоких уровней паров винилхлорида на рабочем месте. Из-за опасности элементарного хлора и проблем, вызванных хлорорганическими соединениями, практика зеленой химии, безусловно, пытается свести к минимуму производство и использование элементарного хлора и, как правило, пытается минимизировать производство хлорорганических соединений и их рассеивание в окружающей среде.
Этот пластик широко используется в водопроводных и дренажных трубах, в первом случае заменяя относительно дефицитный и дорогой металл меди и токсичный свинец. Но материал, используемый для производства ПВХ, представляет собой летучий винилхлорид. Это один из немногих известных канцерогенов для человека, вызывающий задокументированные случаи редкой формы рака печени у рабочих, которые ранее подвергались воздействию очень высоких уровней паров винилхлорида на рабочем месте. Из-за опасности элементарного хлора и проблем, вызванных хлорорганическими соединениями, практика зеленой химии, безусловно, пытается свести к минимуму производство и использование элементарного хлора и, как правило, пытается минимизировать производство хлорорганических соединений и их рассеивание в окружающей среде.
Элемент номер 18, аргон , Ar , атомная масса 39,95, подводит нас к концу третьего периода сокращенной таблицы Менделеева. Он имеет полный октет электронов внешней оболочки и является благородным газом. Никаких истинных химических соединений аргона не было выделено, и никакие химические связи с участием этого элемента не были известны до тех пор, пока в сентябре 2000 года не было сообщено об образовании очень нестабильной переходной связи с участием атомов Ar. Аргон составляет около 1% по объему в атмосфере. Во многом из-за своей химической инертности аргон имеет некоторые применения. Он используется в качестве газа для наполнения ламп накаливания. В этом отношении он помогает предотвратить испарение раскаленных добела атомов вольфрама из нити накала лампы, что значительно продлевает срок службы лампы. Он также используется в качестве плазменной среды в приборах, используемых для атомно-эмиссионного анализа элементарных загрязнителей с индуктивно связанной плазмой. В этом приложении радиочастотный сигнал используется для преобразования аргона в газообразную плазму, которая содержит положительно заряженные ионы Ar+ и отрицательно заряженные электроны и нагревается до невероятно высокой температуры 10 000°C.
Никаких истинных химических соединений аргона не было выделено, и никакие химические связи с участием этого элемента не были известны до тех пор, пока в сентябре 2000 года не было сообщено об образовании очень нестабильной переходной связи с участием атомов Ar. Аргон составляет около 1% по объему в атмосфере. Во многом из-за своей химической инертности аргон имеет некоторые применения. Он используется в качестве газа для наполнения ламп накаливания. В этом отношении он помогает предотвратить испарение раскаленных добела атомов вольфрама из нити накала лампы, что значительно продлевает срок службы лампы. Он также используется в качестве плазменной среды в приборах, используемых для атомно-эмиссионного анализа элементарных загрязнителей с индуктивно связанной плазмой. В этом приложении радиочастотный сигнал используется для преобразования аргона в газообразную плазму, которая содержит положительно заряженные ионы Ar+ и отрицательно заряженные электроны и нагревается до невероятно высокой температуры 10 000°C.
Следующим элементом, который будет добавлен в сокращенную периодическую таблицу, является элемент номер 19. С него начинается четвертый период периодической таблицы. Этот период на самом деле содержит 18 элементов, но мы возьмем только первые два. Это связано с тем, что элемент номер 21 является первым из переходных металлов, и объяснение их положения в периодической таблице на основе входящих в них электронов становится несколько более сложным и запутанным, чем это уместно в этой книге. Читатель, нуждающийся в более подробной информации, может обратиться к другим стандартным книгам по начальной химии.2,3
Элемент с атомным номером 19 — это калий , K , имеющий атомную массу 39,10. Большая часть калия состоит из изотопа с 20 нейтронами. Однако небольшая часть встречающегося в природе К находится в форме . Это радиоактивный изотоп калия, и, поскольку у всех нас есть калий (необходимый элемент для жизни) в организме, мы все естественным образом радиоактивны! Мышечная масса содержит больше калия, чем жировая (жировая) ткань, поэтому более мускулистые люди более радиоактивны. Но не беспокойтесь, уровень радиоактивности калия в организме слишком низок, чтобы вызывать беспокойство, и его нельзя избежать ни при каких обстоятельствах. (Один из сторонников ядерной энергии указал, что сон с мускулистым человеком подвергает человека большему воздействию радиации, чем жизнь рядом с ядерным энергетическим реактором.)
Но не беспокойтесь, уровень радиоактивности калия в организме слишком низок, чтобы вызывать беспокойство, и его нельзя избежать ни при каких обстоятельствах. (Один из сторонников ядерной энергии указал, что сон с мускулистым человеком подвергает человека большему воздействию радиации, чем жизнь рядом с ядерным энергетическим реактором.)
То же, что можно сказать о натрии, элементе номер 11, в целом верно и о калии. В чистом элементарном состоянии калий является очень реакционноспособным щелочным металлом . Как важный элемент для жизни, это обычное удобрение, добавляемое в почву для хорошего роста сельскохозяйственных культур. Химически калий теряет свой единственный электрон внешней оболочки, образуя ион K+.
Кальций , Ca , атомный номер 20, атомная масса 40,08, имеет 2 электрона на внешней оболочке, два за пределами полного октета. Атом кальция легко теряет два «лишних» электрона, образуя катион Са2+. Как и другие элементы в своей группе периодической таблицы, кальций является щелочноземельным металлом. Элементарный металлический кальций химически активен, хотя и не так сильно, как калий. Кальций имеет химические свойства, очень похожие на свойства магния, щелочноземельного металла, расположенного непосредственно над кальцием в периодической таблице.
Элементарный металлический кальций химически активен, хотя и не так сильно, как калий. Кальций имеет химические свойства, очень похожие на свойства магния, щелочноземельного металла, расположенного непосредственно над кальцием в периодической таблице.
Кальций необходим для жизни, хотя большинство почв содержат достаточно кальция для оптимального роста сельскохозяйственных культур. Кальций очень важен для нашего организма, потому что, будучи твердым минералом гидроксиапатитом, Ca5OH(PO4)3, он представляет собой твердый материал в зубах и костях. Дефицит кальция может привести к формированию плохих зубов и развитию инвалидизирующего остеопороза, состояния, характеризующегося слабостью костей, которое особенно часто поражает пожилых женщин.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Стэнли Манахан
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу Содержание
- нет на странице
- Теги
На этой странице нет тегов.
Первые 20 элементов – значение, атомный номер и символ
Атомный номер и символы важны в химии. Символ элемента представляет собой одно- или двухбуквенное сокращение названия элемента. При написании длинных химических уравнений нам нужно написать краткую форму соединений и элементов, поскольку эти символы очень полезны. Атомный номер элементов дает представление об атомной структуре элементов, например о том, сколько электронов и протонов имеет этот конкретный элемент. Первые 20 элементов периодической таблицы даны на рисунке ниже.
(Изображение скоро будет загружено)
Каковы первые 20 элементов Периодической таблицы?
Первые 20 элементов таблицы Менделеева, которые имеют атомные номера 1-20, перечислены ниже.
Atomic Number
Element
Symbol
1
Hydrogen
H
2
Helium
He
3
lithium
Li
4
Beryllium
Be
5
Boron
B
6
Carbon
C
7
Nitrogen
N
8
Oxygen
O
9
Fluorine
F
10
Neon
Ne
11
Sodium
Na
12
Magnesium
Mg
13
Aluminium
Al
14
Силикон
SI
15
Phosphorus
. 0687
0687
16
Sulphur
S
17
Chlorine
Cl
18
Argon
Ar
19
Potassium
K
20
Calcium
Ca
Каждый элемент обладает различными свойствами, обусловленными его атомным номером, атомной массой, электронной конфигурацией, электроотрицательностью, энтальпией электронного усиления и т. д.
Важность атомного номера элемента в Периодической таблице
Прежде чем узнать о важности атомного числа элементов, взгляните на следующие определения.
Атомный номер. Атомный номер говорит нам, сколько протонов содержится в ядре.
Протоны – это субатомные (находящиеся внутри атома) частицы. Он имеет положительный заряд. Он находится в ядре атома элемента.
Нейтроны – это тоже субатомные частицы. Нейтроны имеют нейтральный заряд. Нейтрон весит немного больше, чем протон. Нейтроны вместе с протонами образуют ядро атома.
Электроны. Электроны также субатомны. Электроны стремятся вращаться вокруг ядра. Электроны заряжены отрицательно. Размер электрона меньше размера ядра. Электроны имеют такой же заряд, как и протон, но с отрицательным знаком. Масса электрона почти в 1/1836 раза больше массы протона.
Атомный номер элемента в периодической таблице дает нам следующую информацию:
Дает представление о количестве протонов в ядре атома
Число электронов, окружающих ядро в нейтральном атоме.
Другими словами, мы можем сказать, что атомный номер равен заряду ядра. Следовательно, оно также подобно числу протонов в ядре. Оно численно равно числу электронов в нейтральном атоме.
Попробуем разобраться дальше на примере Oxygen. Кислород имеет атомный номер 8. Это означает, что в нейтральном состоянии количество протонов в ядре равно 8. Количество электронов равно 8. Точно так же в натрии, который имеет атомный номер 11, ядро атома натрия состоит из 11 протонов. Он имеет 11 электронов, окружающих ядро. Поскольку мы знаем, что атомный номер равен количеству электронов, мы можем легко предсказать электронную конфигурацию атома, просто зная его атомный номер.
Чем полезны для нас первые 20 элементов периодической таблицы?
Некоторые из первых 20 элементов периодической таблицы очень полезны для нашей повседневной жизни, например:
Кислород (O)- Кислород играет важную роль в дыхании. Дыхание — это механизм производства энергии, который определяет метаболизм большинства живых организмов. Людям, как и многим другим существам, для дыхания требуется кислород. Кислород образуется в процессе фотосинтеза у растений и различных видов микроорганизмов.
Дыхание — это механизм производства энергии, который определяет метаболизм большинства живых организмов. Людям, как и многим другим существам, для дыхания требуется кислород. Кислород образуется в процессе фотосинтеза у растений и различных видов микроорганизмов.
Углерод (C)- Углерод на 18% состоит из человеческого тела. Белок, сахар и другие важные соединения, включая глюкозу, содержат углерод. Ископаемые виды топлива, такие как нефть, СПГ и т. д., также содержат углерод.
Алюминий (Al) — алюминий, будучи податливым и мягким, используется при изготовлении различных изделий, таких как посуда, детали самолетов, оконные рамы и т. д.
Кремний (Si) — кремний, полупроводник, используется в компьютерных чипах.
Фосфор (P) — фосфор используется в вооруженных силах для изготовления оружия (белый фосфор). Фосфор является неотъемлемой частью АТФ, энергетической валюты нашего организма.
Фосфор является неотъемлемой частью АТФ, энергетической валюты нашего организма.
Кальций (Ca) — кальций помогает поддерживать прочность костей.
Благородные газы в первых 20 элементах периодической таблицы
Во-первых, нам нужно знать, что такое благородные газы. Благородные газы также называют инертными газами. Благородные газы находятся в 18-й группе периодической таблицы. Известно, что они наименее реакционноспособны или крайне нереактивны. Благородные газы были охарактеризованы позже других элементов.
Итак, среди первых 20 элементов есть три благородных газа, а именно гелий (He), неон (Ne) и аргон (Ar). Гелий имеет атомный номер 2, неон имеет атомный номер 10, а аргон имеет атомный номер 18. все элементы. Эта статья будет развивать понимание атомных номеров и символов элементов.
Первые 20 элементов — значение, определение, примеры, периодическая таблица, часто задаваемые вопросы
Первые 20 элементов:
Любое вещество, которое нельзя разложить химически на простые молекулы, называется элементом. Элемент состоит из атомов с одинаковым атомным номером, а это означает, что каждый атом будет иметь такое же количество протонов в ядре, как и другие атомы в компоненте.
Элемент состоит из атомов с одинаковым атомным номером, а это означает, что каждый атом будет иметь такое же количество протонов в ядре, как и другие атомы в компоненте.
Первые 20 элементов периодической таблицы
Периодическая таблица — это представление элементов в порядке возрастания их атомного номера.
Первые двадцать элементов периодической таблицы с атомными номерами 1-20:
Читайте также:
- Решения NCERT для 11-го класса по химии
- NCERT Solutions для 12-го класса по химии
Атомный номер первых двадцати элементов указан в столбце 1 st , а символ названия первых 20 элементов указан в последнем столбце.
Atomic numbers 1 to 20
Element
Symbol
-
Hydrogen
H
-
Гелий
Не
-
Литий75 Li
-
Berilliyum
Be
-
Boron
B
-
Углерод
C
-
678
N
-
Oxygen
O
-
Fluorine
F
-
Неон
Ne
-
9007 Na
-
Magnesium
Mg
-
Aluminium
Al
-
Кремний
Si
-
9065 Фосфор0007
P
-
Sulfur
S
-
Chlorine
Cl
-
Аргон
Ар
-
- 07
K
-
кальций
9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068. Шесть из этих элементов составляют почти всю массу человеческого тела. Первые 20 элементов обеспечивают отличный обзор различных групп элементов. Их также можно найти в более распространенных химических процессах. Элементы даны в порядке возрастания атомного номера от 1 до 20. Атомный номер относится к числу протонов в атомах каждого элемента.
Шесть из этих элементов составляют почти всю массу человеческого тела. Первые 20 элементов обеспечивают отличный обзор различных групп элементов. Их также можно найти в более распространенных химических процессах. Элементы даны в порядке возрастания атомного номера от 1 до 20. Атомный номер относится к числу протонов в атомах каждого элемента. Название и символы элементов:
Атомный номер, имя элемента или символ элемента могут использоваться для идентификации элементов. Эмблемой служит одно- или двухбуквенное сокращение имени. С другой стороны, некоторые символы ссылаются на старые названия элементов. Символ натрия, указанный как Na. Это ссылка на латинское слово natrium, которое когда-то использовалось для обозначения каустической соды. На латыни атомное число натрия встречается как natrium. Символом калия является K, происходящее от латинского слова kalium, которое обозначало щелочь или поташ. Начальная буква символа элемента заглавная. Это нижний регистр, когда есть вторая буква.
Изучение от 1 до 20 элементов таблицы Менделеева:
Водород
В нормальных условиях водород представляет собой неметаллический бесцветный газ. Он превращается в щелочной металл под большим давлением. Этот элемент имеет три изотопа, каждый из которых имеет разное количество нейтронов в атомах. Протий является наиболее распространенным изотопом. Два других – дейтерий и тритий.
атомный номер водорода 1
H является его символом
По оценкам, он имеет значение атомной массы 1,008 а.е.м.
Гелий
Гелим — легкий газ без видимого цвета.
атомный номер гелия 2
Он его символ
It is estimatied to have an atomic mass value of 4. 002 amu
002 amu
He is assigned 1s 2 configuration
It is belonging to group 18 and s-block
Lithium
Это высокореактивный твердый металл серебристого цвета
Литий атомный номер 3
Li его символ
По оценкам, он имеет атомную массу 6,94 а.е.м.
Li присвоен [He] 2s 1 конфигурация
Это щелочной металл, относящийся к группе 1 и s-блоку.
Berilliyium
Это твердый материал с блестящим гери-белым. значение атомной массы 9,012 а.е.м.
Be назначается [He] 2s 2 конфигурация
Это щелочноземельный металл, принадлежащий к группе 2 и s-блоку.
BORON
Атомный номер бора. [He] 2s 2 2p 1 конфигурация
Это металлоид, относящийся к группе 13 и р-блоку.
углерод
Атомный номер углерода 6
C – его символ
. Символ
Металлоид группы 14 и р-блок
Подробнее:
- NCERT отмечает Химия класса 11 Глава 3 Классификация элементов и периодичность свойств
- Решения NCERT для химии класса 11 Глава 3 Классификация элементов и периодичность свойств
NCERT3 9107 Глава 3 Классификация элементов и периодичность свойств
Азот
атомный номер азота 7
N is its symbol
It is estimatied to have an atomic mass value of 14. 007 amu
007 amu
N is assigned [He] 2s 2 2p 3 configuration
It is belonging к группе 15 и p-блоку.
кислород:
Атомное количество кислорода 8
O Символ
.0007
O is assigned [He] 2s 2 2p 4 configuration
It is belonging to group 16 and p-block
Fluorine
:
atomic число фтора равно 9
F его символ
По оценкам, он имеет значение атомной массы 18,989 а.е.м.5 Конфигурация
Он принадлежит группе 17 и P-блока
NEON:
Atomic NEOON 9007
ATOMIC NEOON 9007
. по оценкам, имеет значение атомной массы 20,179 а.е.м.
по оценкам, имеет значение атомной массы 20,179 а.е.м.
N присваивается [He] 2s 2 2p 6 конфигурация
Он принадлежит к группе 18 и p-блоку
натрия:
Атомальный номер натрия
Na является символом натрия
latin naимен значение атомной массы 22,989 а.е.м.
F присваивается [Ne] 3s 1 конфигурация
Принадлежит к группе 1 и s-блоку
Магний: Атомное количество магния составляет 12
мг – его символ
. По оценкам, является атомическая масса 24.309 9007 9007 9107 3 9107 3 9107 3 9107 3 9107 3 9107. 2 Конфигурация
2 Конфигурация
Она принадлежит группе 2 и S-блоке
Алюминий:
Ат.1073
AL – его символ
. Оценка атомной массы составляет 26,968 AMU
AL назначается [NE] 3S 2 3P 1 Конфигурация
- 9090 3P 1 . 13 и P-Block
Кремний
Атомальное число кремния 14 9007
SI-это символ
- 9073
SI Symbol
9073999.0007 Si назначен [Ne] 3s 2 3p 2 конфигурация
Принадлежит к группе 14 и p-блоку.
Фосфор:
Атомное количество фосфора составляет 15
PIS. [Ne] 3s 2 3p 3 Конфигурация
[Ne] 3s 2 3p 3 Конфигурация
Он принадлежит к группе 15 и P-блоке
Sulfer:
ATOMIC IS SULFE по оценкам, имеет значение атомной массы 32,09 а.е.м.
S присваивается [Ne] 3s 2 3p 4 конфигурация
Принадлежит к группе 16 и р-блоку
0017
Хлор
Атомный номер хлора 17.
Cl – его символ
. [NE] 3S 2 3P 5 Конфигурация
Он принадлежит группе 17 и P-блока
NCERT Chemistry Notes:
- NCERT NATE0017
- NCERT Notes Class 12th Chemistry
- NCERT Примечания для всех субъектов
Аргон
ASMOMIC ASPER 9007
 ASSIS9. ASSIS77. ASSIS
ASSIS9. ASSIS77. ASSIS7. ASSIS97. ASSIS97. ASSIS97. ASSIS97.SIS. ASSIS
97. 9077. значение атомной массы 39,948 а.е.м. Ar присвоен [Ne] 3s 2 3p 6 конфигурация
Принадлежит к группе 18 и p-блоку
770056 Калий:
Атомное количество калия составляет 19
Имя латинского калия. значение атомной массы 39,093 а.е.м.
K присваивается [Ar] 4s 1 конфигурация
Принадлежит к группе 1 и s-блоку
1 Calcium:
atomic number of Calcium is 20.
Ca is its symbol
It is estimatied to have an atomic mass value of 40. 10 amu
10 amu
Ca is assigned [Ar] 4S 1 Конфигурация
Она принадлежит группе 14 и S-блока
Также проверьте
- NCERT Imemancer Class Solutions
- NCERT Exempring Exempring Exempring Exempring Exempring Exempring Exempring Exempring Exempormare Exempormare.0017
- Примеры решений NCERT для всех предметов
Часто задаваемые вопросы (FAQ) – Первые 20 элементов – значение, определение, примеры, периодическая таблица, часто задаваемые вопросы
Вопрос: Какой элемент является первым и 20-м элементом периодическая таблица? Ответ:
Первым элементом периодической таблицы является водород, а 20-м элементом периодической системы является кальций.
Вопрос: Какой атомный номер натрия и калия? Ответ:
Атомный номер натрия 11, калия 19.
Вопрос: Какое латинское название натрия? Ответ:
На латыни натрий встречается как натрий.
Вопрос: Какой элемент носит латинское название калий? Ответ:
Калиум — это латинское название калия.
Вопрос: Какой элемент имеет химический символ Al? Ответ:
Алюминий имеет химический символ Al.
Первые 20 элементов периодической таблицы с обозначением, атомным номером и массой
Первые 20 элементов периодической таблицы: При изучении вещества в химии электрон, протон и нейтрон играют жизненно важную роль в определении элемента . Материя обязательно должна иметь в своем ядре один или несколько протонов, чтобы сформировать элемент. Элемент идентифицируется по количеству протонов, присутствующих в его ядре. Элементы в химии обычно считаются строительными блоками материи . Ядра атомов элементов могут иметь нейтроны наряду с протонами. Атомы элементов также имеют электроны, которые движутся вокруг атомного ядра. Когда количество электронов изменяется, он образует ион (положительный или отрицательный), но не меняет идентичности или свойств элемента. Соединения образуются путем установления химической связи, чтобы сделать атомы одного элемента ближе к атомам другого элемента. Всегда рекомендуется запоминать первые 20 элементов периодической таблицы для лучшего понимания концепций химии. Эти первые 20 элементов периодической таблицы также доступны в повседневной жизни. В этой статье вы узнаете больше о списке первых 20 элементов периодической таблицы с их символами, атомным номером и атомной массой.
Ядра атомов элементов могут иметь нейтроны наряду с протонами. Атомы элементов также имеют электроны, которые движутся вокруг атомного ядра. Когда количество электронов изменяется, он образует ион (положительный или отрицательный), но не меняет идентичности или свойств элемента. Соединения образуются путем установления химической связи, чтобы сделать атомы одного элемента ближе к атомам другого элемента. Всегда рекомендуется запоминать первые 20 элементов периодической таблицы для лучшего понимания концепций химии. Эти первые 20 элементов периодической таблицы также доступны в повседневной жизни. В этой статье вы узнаете больше о списке первых 20 элементов периодической таблицы с их символами, атомным номером и атомной массой.
Список первых 20 элементов периодической таблицы
Здесь следует отметить, что около 99% массы тела человека состоит из 6 элементов этих первых 20 элементов периодической таблицы . Первые 20 элементов всегда помогают составить представление о различных группах элементов. Первые 20 элементов периодической таблицы 90 515 присутствуют в нашем окружении 90 516, и они также химически реагируют в нашей повседневной жизни. Литий, бериллий, натрий, магний, алюминий, калий и кальций являются металлическими элементами в первых 20 элементах периодической таблицы, в то время как водород, гелий, углерод, азот, кислород, фтор, неон, фосфор, сера, хлор и аргон являются неметаллическими элементами в первых 20 элементах периодической таблицы. . Среди первых 20 элементов периодической таблицы есть только 3 элемента в виде благородных газов. Эти 3 благородных газа — это гелий (He), неон (Ne) и аргон (Ar) . Здесь список первых 20 элементов периодической таблицы с их атомным номером, символами и атомной массой приведен ниже в табличной форме.
Первые 20 элементов периодической таблицы 90 515 присутствуют в нашем окружении 90 516, и они также химически реагируют в нашей повседневной жизни. Литий, бериллий, натрий, магний, алюминий, калий и кальций являются металлическими элементами в первых 20 элементах периодической таблицы, в то время как водород, гелий, углерод, азот, кислород, фтор, неон, фосфор, сера, хлор и аргон являются неметаллическими элементами в первых 20 элементах периодической таблицы. . Среди первых 20 элементов периодической таблицы есть только 3 элемента в виде благородных газов. Эти 3 благородных газа — это гелий (He), неон (Ne) и аргон (Ar) . Здесь список первых 20 элементов периодической таблицы с их атомным номером, символами и атомной массой приведен ниже в табличной форме.
Atomic Number Element Symbol Atomic Mass (u) 1 Hydrogen H 1. 008
008 2 Helium He 4.0026 3 Lithium Li 6.94 4 Beryllium Be 9.0122 5 Boron B 10.81 6 Carbon C 12.011 7 Nitrogen N 14.007 8 Oxygen O 15.999 9 Fluorine F 18.998 10 Neon Ne 20.18 11 Sodium Na 22.99 12 Magnesium Mg 24.305 13 Aluminium Al 26.982 14 Кремний SI 28. 085
085 15 Phosphorus P 30.974 P 30.974 P 30.974 P 30.974 .0678 S 32.06 17 Chlorine Cl 35.45 18 Argon Ar 39.948 19 Potassium K 39.098 20 Кальций Ca 40,078
Атомный номер элемента0516 . Атомный номер элемента обычно известен как число
конкретного элемента . Он дает информацию о количестве протонов, присутствующих внутри атомных ядер определенного элемента. Он также говорит о количестве электронов, вращающихся вокруг ядра атома. Например, атомный номер элемента с названием натрий равен 11. Это означает, что атомное ядро элемента натрия имеет 11 протонных частиц, а вокруг ядра вращаются 11 электронов. Следует отметить, что атомный номер эквивалентен количеству электронов. Проверив атомные номера, электронная конфигурация любого элемента может быть оценена . Количество нейтронов, присутствующих в атомном ядре, не может быть измерено атомным номером этого элемента.
Следует отметить, что атомный номер эквивалентен количеству электронов. Проверив атомные номера, электронная конфигурация любого элемента может быть оценена . Количество нейтронов, присутствующих в атомном ядре, не может быть измерено атомным номером этого элемента. Атомная масса элемента
Атомная масса определяется как общая масса одного атома определенного элемента . Единицей атомной массы является единая атомная единица массы (а.е.м.) и равна , символизируемая u . Стандартный атомный вес элемента дает среднее значение атомных масс в объединенном наборе изотопов.
Первые 20 элементов периодической таблицы: часто задаваемые вопросы
Ответ. Атомный номер определяется как количество протонов, имеющихся в атомном ядре элемента.
Ответ. Атомная масса определяется как общая масса одного атома определенного элемента.
Ответ. Около 99% массы тела человека состоит из 6 элементов из этих первых 20 элементов периодической таблицы. Первые 20 элементов всегда помогают составить представление о различных группах элементов.
Первые 20 элементов всегда помогают составить представление о различных группах элементов.
Ответ. Литий, бериллий, натрий, магний, алюминий, калий и кальций являются металлическими элементами в первых 20 элементах периодической таблицы, в то время как водород, гелий, углерод, азот, кислород, фтор, неон, фосфор, сера, хлор и аргон неметаллические элементы в первых 20 элементах таблицы Менделеева.
Ответ. Среди первых 20 элементов периодической таблицы есть только 3 элемента в виде благородных газов. Эти 3 благородных газа — гелий (He), неон (Ne) и аргон (Ar).
Важные ссылки
Символы, атомный номер и примеры вопросов
Первые 20 элементов периодической таблицы дают отличный обзор различных групп элементов . Первые 20 элементов встречаются в более распространенных химических процессах. Литий, бериллий, натрий , магний, алюминий , калий и кальций – это металлов , обнаруженных в первых двадцати элементах. Водород , Гелий, Углерод , Азот, Кислород, Фтор, Неон, Фосфор, Сера, Хлор и Аргон являются неметаллами , найденными в первых двадцати элементах.
Водород , Гелий, Углерод , Азот, Кислород, Фтор, Неон, Фосфор, Сера, Хлор и Аргон являются неметаллами , найденными в первых двадцати элементах.
Подробнее: Периодическая классификация элементов
Содержание
- Что такое элементы?
- Первые 20 элементов периодической таблицы
- Мнемоника для запоминания первых 20 элементов
- Важность первых 20 элементов периодической таблицы
- NOBLE GASES В первых 20 элементах
- Важные термины, связанные с элементами
- . Предыдущие
- . Вопросы
Ключевые термины: Первые 20 элементов, периодическая таблица, металлы, неметаллы, элементы, атомный номер, атомная масса
Что такое Элементы?
[Щелкните здесь, чтобы просмотреть примеры вопросов]
Элемент определяется как чистое вещество, состоящее только из атомов одного типа . Элементы не могут быть разделены на два или более простых вещества физическими или химическими средствами.
Элементы не могут быть разделены на два или более простых вещества физическими или химическими средствами.
- На данный момент открыто 118 элементов.
- Из общего числа элементов первые 94 встречаются в природе, а остальные 24 – искусственные.
- Все элементы представлены своими специальными символами, присвоенными IUPAC. Например, водород представлен H, кислород представлен O и т. д.
- Число 90 515 протонов 90 516 в 90 515 атомных ядрах 90 516 каждого элемента используется для определения его идентичности.
- Добавляя дополнительные протоны к атому, можно получить новый элемент.
Современная периодическая таблица
Подробнее:
Первые 20 элементов периодической таблицы
[Нажмите здесь, чтобы просмотреть вопросы за предыдущие годы]
В таблице ниже приведены первые 20 элементов периодической таблицы вместе с их атомными номерами и символами.
Element Atomic Number Symbol Hydrogen 1 H Helium 2 He Lithium 3 Li Beryllium 4 Be Boron 5 B Carbon 6 C Nitrogen 7 N Oxygen 8 O Fluorine 9 F Neon 10 Ne Sodium 11 Na Magnesium 12 Mg Aluminum 13 Al Silicon 14 SI Фосфор . 0678
0678 17 Cl Argon 18 Ar Potassium 19 K Calcium 20 Ca
Read More: Important Примечания к современной периодической таблице
Мнемоника для запоминания первых 20 элементов
[Щелкните здесь, чтобы просмотреть примеры вопросов]
Предоставляя средства для запоминания каждого слова, мнемонические слова значительно облегчают изучение и запоминание слов и их значений. Вот мнемоника для первых 20 элементов периодической таблицы:
Element Name Symbols Mnemonic Hydrogen H Hi Helium Hi Hello Lithium Li Listen Бериллий Be B Бор B B0678 Carbon C C Nitrogen N News Oxygen O O Fluorine F F Neon Ne Новая Зеландия Натрий Na Nagaland Магний Mg Meghaya 906 Aluminum Al All Silicon Si Senior Phosphorous P Public Sulfur S Schools Chlorine Cl Закрытый Аргон Ar Около Калий K Kargil Calcium CA CA
Важность первых 20 Элементов.
 ПЕРИОДА. быть наиболее важными элементами и иметь глубокое применение в повседневной жизни. Ниже приведена важность некоторых из первых 20 элементов:
ПЕРИОДА. быть наиболее важными элементами и иметь глубокое применение в повседневной жизни. Ниже приведена важность некоторых из первых 20 элементов:- Кислород (O): Мы все знаем, что кислород играет решающую роль в дыхании, и нам нужен кислород для дыхание . Кислород высвобождается в процессе фотосинтеза в растениях.
- Углерод (C): 18% человеческого тела состоит из углерода. Все основные соединения, такие как белок , сахар и глюкоза, содержат углерод. Углерод также присутствует в ископаемом топливе , таком как нефть и СПГ.
- Алюминий (Al): Алюминий широко используется в нашей повседневной жизни, поскольку он податлив и мягок, поэтому его используют при изготовлении деталей самолетов, посуды и т. д.
- Кальций (Ca): Кальций является очень важным компонентом, помогающим поддерживать прочность костей.

- Кремний (Si): Кремний действует как полупроводник и используется в компьютерных чипах.
- Фосфор (P): Фосфор является важным компонентом АТФ , который является энергетической валютой тела. Белый фосфор также используется в вооруженных силах для изготовления оружия.
Читайте также:
Благородные газы в первых 20 элементах
[Нажмите здесь, чтобы просмотреть примеры вопросов]
Благородные газы , также известные как инертные газы, являются наименее реакционноспособными или крайне нереакционноспособными элементами. Благородные газы были обнаружены позже, чем другие элементы.
В первые 20 элементов входят три благородных газа, а именно:
- Гелий (He) с атомным номером 2
- Неон (Ne) с атомным номером 10
- Аргон (Ar) с атомным номером 18
8 9 Важно Термины, относящиеся к элементам [Нажмите здесь, чтобы просмотреть вопросы прошлых лет]
- Атомная масса: Каждая частица материи, независимо от того, насколько она мала или велика, имеет связанную с ней массу.
 Атомная масса — это масса атомной частицы. Это часто указывается в терминах единой атомной единицы массы (а.е.м.) в соответствии с международным соглашением.
Атомная масса — это масса атомной частицы. Это часто указывается в терминах единой атомной единицы массы (а.е.м.) в соответствии с международным соглашением. - Атомный номер: Количество протонов в ядре атома или количество электронов в электрически нейтральном атоме равно атомному номеру. Число протонов в атоме называется его 9.0515 атомный номер .
- Протоны: Это субатомные частицы с положительным зарядом, находящиеся в ядре атома элемента.
- Нейтроны: Это субатомные частицы с нейтральным зарядом. Нейтроны и протоны вместе образуют ядро атома.
- Электроны: Это субатомные частицы, которые заряжены отрицательно. Обычно они вращаются вокруг ядра.
Подробнее: Элементы блоков d и f
Что следует помнить
- Элемент — это вещество, которое нельзя расщепить или преобразовать в другое вещество химическими методами.

- В настоящее время известно 118 элементов, из которых первые 94 элемента являются естественными, а остальные 24 созданы человеком.
- Первые 20 элементов периодической таблицы очень важны и являются неотъемлемой частью нашей повседневной жизни.
- Символы элементов происходят от первой буквы их имен, иногда добавляется вторая буква их имен.
- Атомный номер элемента относится к порядку, в котором они появляются в периодической таблице.
Вопросы прошлых лет (PYQ)
- Символ IUPAC для элемента с атомным номером… (JEE Main 2019)
- Какая из следующих пар имеет оба члена из одного и того же… Количество элементов, представленных в пятом периоде…
- Все элементы группы IIIA имеют…
- Что из следующего имеет самую высокую энергию ионизации… (DUET 2008)
- Укажите неправильное утверждение в следующем… (NEET 2012)
- В периодической таблице слева направо в периоде… (NEET 1993)
- Правильный порядок 1-го потенциала ионизации (IP) среди следующих элементов… (NEET 2001)
- Значение электроотрицательности /атомов А и… (DUET 2009)
5 Какой из 90 следующие ионы имеют наибольшее значение… (ДУЭТ 2008)
Примеры вопросов
Вопросы. Что такое элементы? Назовите элемент. (2 балла)
Что такое элементы? Назовите элемент. (2 балла)
Отв. Элемент – это вещество, которое нельзя расщепить или превратить в другое вещество химическими методами. Водород является примером элемента.
Вопросы. Что такое атомный номер? (2 балла)
Отв. Число протонов в ядре атома или количество электронов в электрически нейтральном атоме называется атомным номером.
Вопрос. Что вы подразумеваете под атомной массой элементов? (3 балла)
Отв. Атомная масса элемента относится к общей массе одного атома определенного элемента. Атомная масса эквивалентна количеству протонов и нейтронов в атоме. Атомная масса выражается через единую атомную единицу массы (а.е.м.).
Вопросы. Каково использование элементов лития, фосфора, магния, неона и аргона периодической таблицы? (5 баллов)
Ответ. Эти элементы периодической таблицы используются следующим образом:
- Литий – Литий наиболее известен благодаря своему применению в батареях.
 Он также используется в алюминиевых сплавах, чтобы сделать посуду более прочной, и, что самое странное, в качестве стабилизатора настроения в психиатрических препаратах.
Он также используется в алюминиевых сплавах, чтобы сделать посуду более прочной, и, что самое странное, в качестве стабилизатора настроения в психиатрических препаратах. - Неон — Элемент неон является четвертым по распространенности элементом во Вселенной. Рекламные вывески на сегодняшний день являются наиболее распространенным применением элемента. Стекло обычно загорается при искушении электричеством, что приводит к его использованию в секторе вывесок, а также в высоковольтных индикаторах и лазерах. Неон широко используется в криогенных жидких хладагентах.
- Магний — соли Эпсома, магнезиальное молоко, хлорид и цитрат — все это примеры медицинского применения магния. Магний также необходим для выживания как животных, так и растений. Его часто сплавляют с алюминием для использования в самолетах и автомобильных конструкциях из-за его меньшей плотности, чем у алюминия. Он также используется для удаления серы из расплавленного железа и стали.

- Фосфор – Сигнальные ракеты и зажигательные устройства содержат белый фосфор, а спичечные коробки содержат красный фосфор в веществе, прикрепленном сбоку. С другой стороны, соединения фосфора чаще всего используются в удобрениях. Фосфор также используется в производстве стали.
- Аргон – Аргон используется в качестве защитного слоя, окружающего нить накаливания в лампах накаливания и люминесцентных лампах, для предотвращения ее коррозии кислородом. Дуговая сварка и полупроводниковые кристаллы используют его в качестве защитного экрана.
Вопрос. Назовите благородные газы, входящие в состав первых 20 элементов периодической таблицы. (3 балла)
Отв. В первые 20 элементов периодической таблицы входят в основном три инертных газа:
- Гелий (He)
- Неон (Ne)
- Аргон (Ar)
Атомные номера гелия, неона и аргона равны 2, 10 и 18 соответственно.
Вопросы. Каковы химические формулы первых 20 элементов? (5 баллов)
Отв. Двухатомные элементы включают водород, азот, кислород, фтор и хлор. H 2 , N 2 , O 2 , F 2 , Cl 2 — их химические формулы соответственно.
Следующие элементы имеют символ и химическую формулу:
- Гелий-H,
- Литий-Li,
- Бериллий-Be,
- Бор-B,
- Углерод-C,
Неон-Ne,- Натрий-Na,
- Магний-Mg,
- Алюминий-Al,
- Кремний-Si,
- Аргон-Ar,
- Кальций-Ca
- Сера имеет1 химическую формулу химическая формула P 4 .
Вопрос. Какую всю информацию мы можем получить из атомного номера элемента? (3 балла)
Отв. Атомный номер элемента предоставляет следующую информацию об элементе:
- Атомный номер говорит нам о количестве протонов в ядре атома
- Количество электронов, окружающих ядро в нейтральном атоме.

7777777777777 Lithium
7777777777777777777777 годы Lithium7777777777777777777777777777 гг.
 высокореактивный металл.
высокореактивный металл.- Литий представляет собой реактивный твердый металл серебра.
- Атомный номер: 3
- Символ: Li
- Атомная масса: 6,94 (6,938–6,997)
- Электронная конфигурация: [He] 2s 1
- Группа: группа 1, s-блок, щелочной металл
Бериллий
- Бериллий — блестящий серо-белый твердый металл.
- Атомный номер: 4
- Символ: Be
- Атомная масса: 9,0121831(5)
- Электронная конфигурация: [He] 2s 2
- Группа: группа 2, 9079, 9079, 90, 79, 90, 90, 90, 90, 90, 90, s-блок, 90, 90, щелочные
- Бор представляет собой твердое вещество серого цвета с металлическим блеском.
- Атомный номер: 5
- Символ: B
- Атомная масса: 10,81 (10,806–10,821)
- Электронная конфигурация: [HE] 2S 2 2P 1
- Группа: Группа 13, PLOCK, Meterloid, Methalloid, Methalloid, Methalloid, Methalloid, Methalloid, Methalloid, PLOCK 13, PLOCK.

Углерод
- Углерод представляет собой твердое вещество, которое принимает несколько форм, включая алмаз, графит и аморфный углерод. Он черный, серый или бесцветный.
- Атомный номер: 6
- Символ: C
- Атомная масса: 12,011 (12,0096–12.0116)
- Электронная конфигурация: [He] 2s 2 2p 2
- Группа: группа 14, р-блок, обычно неметалл, хотя иногда считается металлоидом
Азот бесцветный
газ.Кислород
- Кислород — бесцветный газ. Его жидкая форма имеет синий цвет, в то время как твердая форма имеет множество цветов, включая красный, металлический и черный.
- Атомный номер: 8
- Символ: O
- Атомная масса: 15,999 или 16,00
- Электронная конфигурация: [HE] 2S 2 2P 4
- Группа: Группа 16 (Chalcogen
Фтор
- Фтор представляет собой бледно-желтый газ и жидкость и ярко-желтое твердое вещество.

- Атомный номер: 9
- Символ: F
- Атомная масса: 18,998403163 (6)
- Электронная конфигурация: [HE] 2S 2 2P 5
- Группа: Группа 17, PLOCK 5
- : Группа 17, PLOCK 5
- : Группа 17, PLOCK 5
- : Группа 17, PLOCK.
Неон
- Неон — бесцветный газ, излучающий оранжево-красное свечение при возбуждении в электрическом поле.
- Атомный номер: 10
- Символ: Ne
- Атомная масса: 20,1797(6)
- Электронная конфигурация: [He] 2s 2 2p 6
- Группа: группа 18, р-блок, благородный газ
Натрий
- Натрий — мягкий твердый металл серебристо-белого цвета.
- Atomic Number: 11
- Symbol: Na
- Atomic Mass: 22.98976928(2)
- Electron Configuration: [Ne] 3s 1
- Group: group 1, s-block, alkali metal
Magnesium
- Магний представляет собой блестящий серый твердый металл.

- Атомный номер: 12
- Обозначение: Mg
- Атомная масса: 24,305
- Электронная конфигурация: [Ne] 3s 2
- Группа: группа 2, s-блок, щелочноземельный металл
, p-блок 1
Кремний
- Кремний представляет собой твердое кристаллическое вещество серо-голубого цвета с металлическим блеском.
- Atomic Number: 14
- Symbol: Si
- Atomic Mass: 28.085
- Electron Configuration: [Ne] 3s 2 3p 2
- Group: group 14 (carbon group), p-block, metalloid
Фосфор
- Фосфор в обычных условиях является твердым, но принимает несколько форм.
 Наиболее распространены белый фосфор и красный фосфор.
Наиболее распространены белый фосфор и красный фосфор. - Атомный номер: 15
- Символ: P
- Атомная масса: 30,973761998 (5)
- Электронная конфигурация: [NE] 3S 2 3P 3
- Группа: Группа 15 (PN 15PGENGEG), PN-LOCKEGEN), PN-BLICTOG), PN-BLICTOG). обычно считается неметаллом, но иногда и металлоидом
Сера
Сера — желтый неметалл.- Сера представляет собой желтое твердое вещество, обычно встречающееся в виде кристаллов или порошка.
- Атомный номер: 16
- Символ: S
- Атомная масса: 32,06
- Электронная конфигурация: [Ne] 3s 2 3p 4
- Группа: группа 16 (халькогены), p-блок, неметаллический Его жидкая форма имеет ярко-желтый цвет.
- Атомный номер: 17
- Символ: Cl
- Атомная масса: 35,45
- Электронная конфигурация: [Ne] 3s 2 3p 5 группа p-блок, p-группа:
- 0017
Аргон
- Аргон представляет собой бесцветный газ, жидкость и твердое вещество.
 Это газ при обычных условиях. Он излучает яркое сиренево-фиолетовое свечение при возбуждении в электрическом поле.
Это газ при обычных условиях. Он излучает яркое сиренево-фиолетовое свечение при возбуждении в электрическом поле. - Атомный номер: 18
- Символ: AR
- Атомная масса: 39,948 (1)
- Электронная конфигурация: [NE] 3S 2 3P 6
- Группа: Группа 18, P-Block, NOBLE 7777
- Группа: Группа 18, P-Block, NOBLE 777777
- : Группа 18, P-Block, NOBLE 777777
- : Группа 18, P-Block, NOBLE 777777
- .
Калий
- Калий – реактивный серебристый твердый металл.
- Атомный номер: 19
- Символ: K
- Атомная масса: 39,0983 (1)
- Электронная конфигурация: [AR] 4S 1
- Группа: Группа 1, SCLOC
- Кальций представляет собой твердый металл серебристого цвета со слабым желтоватым оттенком.
- Атомный номер: 20
- Символ: Ca
- Атомная масса: 40,078(4)
- Электронная конфигурация: [Ar] 4s 2
- Группа: группа 2, s-блок, щелочноземельный металл0017
Ссылки
- Болл, П.
 (2004). Элементы: очень краткое введение . Издательство Оксфордского университета. ISBN 978-0-19-284099-8.
(2004). Элементы: очень краткое введение . Издательство Оксфордского университета. ISBN 978-0-19-284099-8. - Эмсли, Дж. (2003). Строительные блоки природы: Путеводитель по элементам от А до Я . Издательство Оксфордского университета. ISBN 978-0-19-850340-8.
- Грей, Т. (2009). Элементы: Визуальное исследование каждого известного атома во Вселенной . ISBN Black Dog & Leventhal Publishers Inc. 978-1-57912-814-2 .
- ИЮПАК (1997). «Химический элемент». Сборник химической терминологии (2-е изд.). doi:10.1351/goldbook.C01022
3.7: Заполнение периодической таблицы из 20 элементов
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 78937
- Стэнли Э.
 Манахан
Манахан - Университет Миссури
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Стэнли Манахан
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу Содержание
- нет на странице
- Теги

Атомный номер. Атомный номер говорит нам, сколько протонов содержится в ядре.
Протоны – это субатомные (находящиеся внутри атома) частицы. Он имеет положительный заряд. Он находится в ядре атома элемента.
Нейтроны – это тоже субатомные частицы. Нейтроны имеют нейтральный заряд. Нейтрон весит немного больше, чем протон. Нейтроны вместе с протонами образуют ядро атома.
Электроны. Электроны также субатомны. Электроны стремятся вращаться вокруг ядра. Электроны заряжены отрицательно. Размер электрона меньше размера ядра. Электроны имеют такой же заряд, как и протон, но с отрицательным знаком. Масса электрона почти в 1/1836 раза больше массы протона.
Дает представление о количестве протонов в ядре атома
Число электронов, окружающих ядро в нейтральном атоме.

Другими словами, мы можем сказать, что атомный номер равен заряду ядра. Следовательно, оно также подобно числу протонов в ядре. Оно численно равно числу электронов в нейтральном атоме.
Попробуем разобраться дальше на примере Oxygen. Кислород имеет атомный номер 8. Это означает, что в нейтральном состоянии количество протонов в ядре равно 8. Количество электронов равно 8. Точно так же в натрии, который имеет атомный номер 11, ядро атома натрия состоит из 11 протонов. Он имеет 11 электронов, окружающих ядро. Поскольку мы знаем, что атомный номер равен количеству электронов, мы можем легко предсказать электронную конфигурацию атома, просто зная его атомный номер.
Кислород (O)- Кислород играет важную роль в дыхании.
 Дыхание — это механизм производства энергии, который определяет метаболизм большинства живых организмов. Людям, как и многим другим существам, для дыхания требуется кислород. Кислород образуется в процессе фотосинтеза у растений и различных видов микроорганизмов.
Дыхание — это механизм производства энергии, который определяет метаболизм большинства живых организмов. Людям, как и многим другим существам, для дыхания требуется кислород. Кислород образуется в процессе фотосинтеза у растений и различных видов микроорганизмов.Углерод (C)- Углерод на 18% состоит из человеческого тела. Белок, сахар и другие важные соединения, включая глюкозу, содержат углерод. Ископаемые виды топлива, такие как нефть, СПГ и т. д., также содержат углерод.
Алюминий (Al) — алюминий, будучи податливым и мягким, используется при изготовлении различных изделий, таких как посуда, детали самолетов, оконные рамы и т. д.
Кремний (Si) — кремний, полупроводник, используется в компьютерных чипах.
Фосфор (P) — фосфор используется в вооруженных силах для изготовления оружия (белый фосфор).
 Фосфор является неотъемлемой частью АТФ, энергетической валюты нашего организма.
Фосфор является неотъемлемой частью АТФ, энергетической валюты нашего организма.Кальций (Ca) — кальций помогает поддерживать прочность костей.
- Решения NCERT для 11-го класса по химии
- NCERT Solutions для 12-го класса по химии
Атомный номер первых двадцати элементов указан в столбце 1 st , а символ названия первых 20 элементов указан в последнем столбце.
Atomic numbers 1 to 20
Element
Symbol
Hydrogen
H
Гелий
Не
Литий75 Li
Berilliyum
Be
Boron
B
Углерод
C
70675 678
N
Oxygen
O
Fluorine
F
Неон
Ne
Na
Magnesium
Mg
Aluminium
Al
Кремний
Si
9065 Фосфор0007
P
Sulfur
S
Chlorine
Cl
Аргон
Ар
-
- 07
K
кальций
9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068 9068.  Шесть из этих элементов составляют почти всю массу человеческого тела. Первые 20 элементов обеспечивают отличный обзор различных групп элементов. Их также можно найти в более распространенных химических процессах. Элементы даны в порядке возрастания атомного номера от 1 до 20. Атомный номер относится к числу протонов в атомах каждого элемента.
Шесть из этих элементов составляют почти всю массу человеческого тела. Первые 20 элементов обеспечивают отличный обзор различных групп элементов. Их также можно найти в более распространенных химических процессах. Элементы даны в порядке возрастания атомного номера от 1 до 20. Атомный номер относится к числу протонов в атомах каждого элемента.Название и символы элементов:
Атомный номер, имя элемента или символ элемента могут использоваться для идентификации элементов. Эмблемой служит одно- или двухбуквенное сокращение имени. С другой стороны, некоторые символы ссылаются на старые названия элементов. Символ натрия, указанный как Na. Это ссылка на латинское слово natrium, которое когда-то использовалось для обозначения каустической соды. На латыни атомное число натрия встречается как natrium. Символом калия является K, происходящее от латинского слова kalium, которое обозначало щелочь или поташ. Начальная буква символа элемента заглавная. Это нижний регистр, когда есть вторая буква.

Изучение от 1 до 20 элементов таблицы Менделеева:
Водород
В нормальных условиях водород представляет собой неметаллический бесцветный газ. Он превращается в щелочной металл под большим давлением. Этот элемент имеет три изотопа, каждый из которых имеет разное количество нейтронов в атомах. Протий является наиболее распространенным изотопом. Два других – дейтерий и тритий.
атомный номер водорода 1
H является его символом
По оценкам, он имеет значение атомной массы 1,008 а.е.м.
Гелий
Гелим — легкий газ без видимого цвета.
атомный номер гелия 2
Он его символ
It is estimatied to have an atomic mass value of 4.
 002 amu
002 amuHe is assigned 1s 2 configuration
It is belonging to group 18 and s-block
Lithium
Это высокореактивный твердый металл серебристого цвета
Литий атомный номер 3
Li его символ
По оценкам, он имеет атомную массу 6,94 а.е.м.
Li присвоен [He] 2s 1 конфигурация
Это щелочной металл, относящийся к группе 1 и s-блоку.
Berilliyium
Это твердый материал с блестящим гери-белым. значение атомной массы 9,012 а.е.м.
Be назначается [He] 2s 2 конфигурация
Это щелочноземельный металл, принадлежащий к группе 2 и s-блоку.

BORON
Атомный номер бора. [He] 2s 2 2p 1 конфигурация
Это металлоид, относящийся к группе 13 и р-блоку.
углерод
Атомный номер углерода 6
C – его символ
. Символ
. [He] 2s 2 2p 2 конфигурацияМеталлоид группы 14 и р-блок
Подробнее:
- NCERT отмечает Химия класса 11 Глава 3 Классификация элементов и периодичность свойств
- Решения NCERT для химии класса 11 Глава 3 Классификация элементов и периодичность свойств NCERT3 9107 Глава 3 Классификация элементов и периодичность свойств
Азот
атомный номер азота 7
N is its symbol
It is estimatied to have an atomic mass value of 14.
 007 amu
007 amuN is assigned [He] 2s 2 2p 3 configuration
It is belonging к группе 15 и p-блоку.
кислород:
Атомное количество кислорода 8
O Символ
.0007
O is assigned [He] 2s 2 2p 4 configuration
It is belonging to group 16 and p-block
Fluorine
:
atomic число фтора равно 9
F его символ
По оценкам, он имеет значение атомной массы 18,989 а.е.м.5 Конфигурация
Он принадлежит группе 17 и P-блока
NEON:
Atomic NEOON 9007
ATOMIC NEOON 9007
.
 по оценкам, имеет значение атомной массы 20,179 а.е.м.
по оценкам, имеет значение атомной массы 20,179 а.е.м.N присваивается [He] 2s 2 2p 6 конфигурация
Он принадлежит к группе 18 и p-блоку
натрия:
Атомальный номер натрия
Na является символом натрия
latin naимен значение атомной массы 22,989 а.е.м.
F присваивается [Ne] 3s 1 конфигурация
Принадлежит к группе 1 и s-блоку
Магний: Атомное количество магния составляет 12
мг – его символ
. По оценкам, является атомическая масса 24.309 9007 9007 9107 3 9107 3 9107 3 9107 3 9107 3 9107.
 2 Конфигурация
2 КонфигурацияОна принадлежит группе 2 и S-блоке
Алюминий:
Ат.1073
AL – его символ
. Оценка атомной массы составляет 26,968 AMU
AL назначается [NE] 3S 2 3P 1 Конфигурация
- 9090 3P 1 . 13 и P-Block
Кремний
Атомальное число кремния 14 9007
SI-это символ
- 9073
SI Symbol
9073999.0007 Si назначен [Ne] 3s 2 3p 2 конфигурация
Принадлежит к группе 14 и p-блоку.
Фосфор:
Атомное количество фосфора составляет 15
PIS.
 [Ne] 3s 2 3p 3 Конфигурация
[Ne] 3s 2 3p 3 КонфигурацияОн принадлежит к группе 15 и P-блоке
Sulfer:
ATOMIC IS SULFE по оценкам, имеет значение атомной массы 32,09 а.е.м.
S присваивается [Ne] 3s 2 3p 4 конфигурация
Принадлежит к группе 16 и р-блоку
0017
Хлор
Атомный номер хлора 17.
Cl – его символ
. [NE] 3S 2 3P 5 Конфигурация
Он принадлежит группе 17 и P-блока
NCERT Chemistry Notes:
- NCERT NATE0017
- NCERT Notes Class 12th Chemistry
- NCERT Примечания для всех субъектов
Аргон
ASMOMIC ASPER 9007
7.Ar присвоен [Ne] 3s 2 3p 6 конфигурация
Принадлежит к группе 18 и p-блоку
770056Калий:
Атомное количество калия составляет 19
Имя латинского калия. значение атомной массы 39,093 а.е.м.
K присваивается [Ar] 4s 1 конфигурация
Принадлежит к группе 1 и s-блоку
1 Calcium:
 ASSIS9. ASSIS77. ASSIS
ASSIS9. ASSIS77. ASSIS- 7. ASSIS97. ASSIS97. ASSIS97. ASSIS97.SIS
. ASSIS
97. 9077. значение атомной массы 39,948 а.е.м.atomic number of Calcium is 20.
Ca is its symbol
It is estimatied to have an atomic mass value of 40.
 10 amu
10 amuCa is assigned [Ar] 4S 1 Конфигурация
Она принадлежит группе 14 и S-блока
Также проверьте
- NCERT Imemancer Class Solutions
- NCERT Exempring Exempring Exempring Exempring Exempring Exempring Exempring Exempring Exempormare Exempormare.0017
- Примеры решений NCERT для всех предметов
Часто задаваемые вопросы (FAQ) – Первые 20 элементов – значение, определение, примеры, периодическая таблица, часто задаваемые вопросы
Вопрос: Какой элемент является первым и 20-м элементом периодическая таблица?Ответ:
Первым элементом периодической таблицы является водород, а 20-м элементом периодической системы является кальций.
Вопрос: Какой атомный номер натрия и калия?Ответ:
Атомный номер натрия 11, калия 19.
Вопрос: Какое латинское название натрия?
Ответ:
На латыни натрий встречается как натрий.
Вопрос: Какой элемент носит латинское название калий?Ответ:
Калиум — это латинское название калия.
Вопрос: Какой элемент имеет химический символ Al?Ответ:
Алюминий имеет химический символ Al.
Первые 20 элементов периодической таблицы с обозначением, атомным номером и массой
Первые 20 элементов периодической таблицы: При изучении вещества в химии электрон, протон и нейтрон играют жизненно важную роль в определении элемента . Материя обязательно должна иметь в своем ядре один или несколько протонов, чтобы сформировать элемент. Элемент идентифицируется по количеству протонов, присутствующих в его ядре. Элементы в химии обычно считаются строительными блоками материи .
 Ядра атомов элементов могут иметь нейтроны наряду с протонами. Атомы элементов также имеют электроны, которые движутся вокруг атомного ядра. Когда количество электронов изменяется, он образует ион (положительный или отрицательный), но не меняет идентичности или свойств элемента. Соединения образуются путем установления химической связи, чтобы сделать атомы одного элемента ближе к атомам другого элемента. Всегда рекомендуется запоминать первые 20 элементов периодической таблицы для лучшего понимания концепций химии. Эти первые 20 элементов периодической таблицы также доступны в повседневной жизни. В этой статье вы узнаете больше о списке первых 20 элементов периодической таблицы с их символами, атомным номером и атомной массой.
Ядра атомов элементов могут иметь нейтроны наряду с протонами. Атомы элементов также имеют электроны, которые движутся вокруг атомного ядра. Когда количество электронов изменяется, он образует ион (положительный или отрицательный), но не меняет идентичности или свойств элемента. Соединения образуются путем установления химической связи, чтобы сделать атомы одного элемента ближе к атомам другого элемента. Всегда рекомендуется запоминать первые 20 элементов периодической таблицы для лучшего понимания концепций химии. Эти первые 20 элементов периодической таблицы также доступны в повседневной жизни. В этой статье вы узнаете больше о списке первых 20 элементов периодической таблицы с их символами, атомным номером и атомной массой.Список первых 20 элементов периодической таблицы
Здесь следует отметить, что около 99% массы тела человека состоит из 6 элементов этих первых 20 элементов периодической таблицы . Первые 20 элементов всегда помогают составить представление о различных группах элементов.
 Первые 20 элементов периодической таблицы 90 515 присутствуют в нашем окружении 90 516, и они также химически реагируют в нашей повседневной жизни. Литий, бериллий, натрий, магний, алюминий, калий и кальций являются металлическими элементами в первых 20 элементах периодической таблицы, в то время как водород, гелий, углерод, азот, кислород, фтор, неон, фосфор, сера, хлор и аргон являются неметаллическими элементами в первых 20 элементах периодической таблицы. . Среди первых 20 элементов периодической таблицы есть только 3 элемента в виде благородных газов. Эти 3 благородных газа — это гелий (He), неон (Ne) и аргон (Ar) . Здесь список первых 20 элементов периодической таблицы с их атомным номером, символами и атомной массой приведен ниже в табличной форме.
Первые 20 элементов периодической таблицы 90 515 присутствуют в нашем окружении 90 516, и они также химически реагируют в нашей повседневной жизни. Литий, бериллий, натрий, магний, алюминий, калий и кальций являются металлическими элементами в первых 20 элементах периодической таблицы, в то время как водород, гелий, углерод, азот, кислород, фтор, неон, фосфор, сера, хлор и аргон являются неметаллическими элементами в первых 20 элементах периодической таблицы. . Среди первых 20 элементов периодической таблицы есть только 3 элемента в виде благородных газов. Эти 3 благородных газа — это гелий (He), неон (Ne) и аргон (Ar) . Здесь список первых 20 элементов периодической таблицы с их атомным номером, символами и атомной массой приведен ниже в табличной форме.Atomic Number Element Symbol Atomic Mass (u) 1 Hydrogen H 1.  008
0082 Helium He 4.0026 3 Lithium Li 6.94 4 Beryllium Be 9.0122 5 Boron B 10.81 6 Carbon C 12.011 7 Nitrogen N 14.007 8 Oxygen O 15.999 9 Fluorine F 18.998 10 Neon Ne 20.18 11 Sodium Na 22.99 12 Magnesium Mg 24.305 13 Aluminium Al 26.982 14 Кремний SI 28.  085
08515 Phosphorus P 30.974 P 30.974 P30.974 P30.974 .0678S 32.06 17 Chlorine Cl 35.45 18 Argon Ar 39.948 19 Potassium K 39.098 20 Кальций Ca 40,078 Атомный номер элемента0516 . Атомный номер элемента обычно известен как число
конкретного элемента . Он дает информацию о количестве протонов, присутствующих внутри атомных ядер определенного элемента. Он также говорит о количестве электронов, вращающихся вокруг ядра атома. Например, атомный номер элемента с названием натрий равен 11. Это означает, что атомное ядро элемента натрия имеет 11 протонных частиц, а вокруг ядра вращаются 11 электронов. Следует отметить, что атомный номер эквивалентен количеству электронов. Проверив атомные номера, электронная конфигурация любого элемента может быть оценена . Количество нейтронов, присутствующих в атомном ядре, не может быть измерено атомным номером этого элемента.
Следует отметить, что атомный номер эквивалентен количеству электронов. Проверив атомные номера, электронная конфигурация любого элемента может быть оценена . Количество нейтронов, присутствующих в атомном ядре, не может быть измерено атомным номером этого элемента.Атомная масса элемента
Атомная масса определяется как общая масса одного атома определенного элемента . Единицей атомной массы является единая атомная единица массы (а.е.м.) и равна , символизируемая u . Стандартный атомный вес элемента дает среднее значение атомных масс в объединенном наборе изотопов.
Первые 20 элементов периодической таблицы: часто задаваемые вопросы
Ответ. Атомный номер определяется как количество протонов, имеющихся в атомном ядре элемента.
Ответ. Атомная масса определяется как общая масса одного атома определенного элемента.
Ответ. Около 99% массы тела человека состоит из 6 элементов из этих первых 20 элементов периодической таблицы.
 Первые 20 элементов всегда помогают составить представление о различных группах элементов.
Первые 20 элементов всегда помогают составить представление о различных группах элементов.Ответ. Литий, бериллий, натрий, магний, алюминий, калий и кальций являются металлическими элементами в первых 20 элементах периодической таблицы, в то время как водород, гелий, углерод, азот, кислород, фтор, неон, фосфор, сера, хлор и аргон неметаллические элементы в первых 20 элементах таблицы Менделеева.
Ответ. Среди первых 20 элементов периодической таблицы есть только 3 элемента в виде благородных газов. Эти 3 благородных газа — гелий (He), неон (Ne) и аргон (Ar).
Важные ссылки
Символы, атомный номер и примеры вопросов
Первые 20 элементов периодической таблицы дают отличный обзор различных групп элементов . Первые 20 элементов встречаются в более распространенных химических процессах. Литий, бериллий, натрий , магний, алюминий , калий и кальций – это металлов , обнаруженных в первых двадцати элементах.
 Водород , Гелий, Углерод , Азот, Кислород, Фтор, Неон, Фосфор, Сера, Хлор и Аргон являются неметаллами , найденными в первых двадцати элементах.
Водород , Гелий, Углерод , Азот, Кислород, Фтор, Неон, Фосфор, Сера, Хлор и Аргон являются неметаллами , найденными в первых двадцати элементах.Подробнее: Периодическая классификация элементов
Содержание
- Что такое элементы?
- Первые 20 элементов периодической таблицы
- Мнемоника для запоминания первых 20 элементов
- Важность первых 20 элементов периодической таблицы
- NOBLE GASES В первых 20 элементах
- Важные термины, связанные с элементами
- . Предыдущие
- . Вопросы
Ключевые термины: Первые 20 элементов, периодическая таблица, металлы, неметаллы, элементы, атомный номер, атомная масса
Что такое Элементы?
[Щелкните здесь, чтобы просмотреть примеры вопросов]
Элемент определяется как чистое вещество, состоящее только из атомов одного типа .
 Элементы не могут быть разделены на два или более простых вещества физическими или химическими средствами.
Элементы не могут быть разделены на два или более простых вещества физическими или химическими средствами.- На данный момент открыто 118 элементов.
- Из общего числа элементов первые 94 встречаются в природе, а остальные 24 – искусственные.
- Все элементы представлены своими специальными символами, присвоенными IUPAC. Например, водород представлен H, кислород представлен O и т. д.
- Число 90 515 протонов 90 516 в 90 515 атомных ядрах 90 516 каждого элемента используется для определения его идентичности.
- Добавляя дополнительные протоны к атому, можно получить новый элемент.
Современная периодическая таблица
Подробнее:
Первые 20 элементов периодической таблицы
[Нажмите здесь, чтобы просмотреть вопросы за предыдущие годы]
В таблице ниже приведены первые 20 элементов периодической таблицы вместе с их атомными номерами и символами.
Element Atomic Number Symbol Hydrogen 1 H Helium 2 He Lithium 3 Li Beryllium 4 Be Boron 5 B Carbon 6 C Nitrogen 7 N Oxygen 8 O Fluorine 9 F Neon 10 Ne Sodium 11 Na Magnesium 12 Mg Aluminum 13 Al Silicon 14 SI Фосфор .  0678
067817 Cl Argon 18 Ar Potassium 19 K Calcium 20 Ca Read More: Important Примечания к современной периодической таблице
Мнемоника для запоминания первых 20 элементов
[Щелкните здесь, чтобы просмотреть примеры вопросов]
Предоставляя средства для запоминания каждого слова, мнемонические слова значительно облегчают изучение и запоминание слов и их значений. Вот мнемоника для первых 20 элементов периодической таблицы:
Element Name Symbols Mnemonic Hydrogen H Hi Helium Hi Hello Lithium Li Listen Бериллий Be B Бор B B0678 Carbon C C Nitrogen N News Oxygen O O Fluorine F F Neon Ne Новая Зеландия Натрий Na Nagaland Магний Mg Meghaya 906 Aluminum Al All Silicon Si Senior Phosphorous P Public Sulfur S Schools Chlorine Cl Закрытый Аргон Ar Около Калий K Kargil Calcium CA CA Важность первых 20 Элементов.
 ПЕРИОДА. быть наиболее важными элементами и иметь глубокое применение в повседневной жизни. Ниже приведена важность некоторых из первых 20 элементов:
ПЕРИОДА. быть наиболее важными элементами и иметь глубокое применение в повседневной жизни. Ниже приведена важность некоторых из первых 20 элементов:- Кислород (O): Мы все знаем, что кислород играет решающую роль в дыхании, и нам нужен кислород для дыхание . Кислород высвобождается в процессе фотосинтеза в растениях.
- Углерод (C): 18% человеческого тела состоит из углерода. Все основные соединения, такие как белок , сахар и глюкоза, содержат углерод. Углерод также присутствует в ископаемом топливе , таком как нефть и СПГ.
- Алюминий (Al): Алюминий широко используется в нашей повседневной жизни, поскольку он податлив и мягок, поэтому его используют при изготовлении деталей самолетов, посуды и т. д.
- Кальций (Ca): Кальций является очень важным компонентом, помогающим поддерживать прочность костей.

- Кремний (Si): Кремний действует как полупроводник и используется в компьютерных чипах.
- Фосфор (P): Фосфор является важным компонентом АТФ , который является энергетической валютой тела. Белый фосфор также используется в вооруженных силах для изготовления оружия.
Читайте также:
Благородные газы в первых 20 элементах
[Нажмите здесь, чтобы просмотреть примеры вопросов]
Благородные газы , также известные как инертные газы, являются наименее реакционноспособными или крайне нереакционноспособными элементами. Благородные газы были обнаружены позже, чем другие элементы.
В первые 20 элементов входят три благородных газа, а именно:
- Гелий (He) с атомным номером 2
- Неон (Ne) с атомным номером 10
- Аргон (Ar) с атомным номером 18
[Нажмите здесь, чтобы просмотреть вопросы прошлых лет]
- Атомная масса: Каждая частица материи, независимо от того, насколько она мала или велика, имеет связанную с ней массу.
 Атомная масса — это масса атомной частицы. Это часто указывается в терминах единой атомной единицы массы (а.е.м.) в соответствии с международным соглашением.
Атомная масса — это масса атомной частицы. Это часто указывается в терминах единой атомной единицы массы (а.е.м.) в соответствии с международным соглашением. - Атомный номер: Количество протонов в ядре атома или количество электронов в электрически нейтральном атоме равно атомному номеру. Число протонов в атоме называется его 9.0515 атомный номер .
- Протоны: Это субатомные частицы с положительным зарядом, находящиеся в ядре атома элемента.
- Нейтроны: Это субатомные частицы с нейтральным зарядом. Нейтроны и протоны вместе образуют ядро атома.
- Электроны: Это субатомные частицы, которые заряжены отрицательно. Обычно они вращаются вокруг ядра.
Подробнее: Элементы блоков d и f
Что следует помнить
- Элемент — это вещество, которое нельзя расщепить или преобразовать в другое вещество химическими методами.

- В настоящее время известно 118 элементов, из которых первые 94 элемента являются естественными, а остальные 24 созданы человеком.
- Первые 20 элементов периодической таблицы очень важны и являются неотъемлемой частью нашей повседневной жизни.
- Символы элементов происходят от первой буквы их имен, иногда добавляется вторая буква их имен.
- Атомный номер элемента относится к порядку, в котором они появляются в периодической таблице.
Вопросы прошлых лет (PYQ)
- Символ IUPAC для элемента с атомным номером… (JEE Main 2019)
- Какая из следующих пар имеет оба члена из одного и того же… Количество элементов, представленных в пятом периоде…
- Все элементы группы IIIA имеют…
- Что из следующего имеет самую высокую энергию ионизации… (DUET 2008)
- Укажите неправильное утверждение в следующем… (NEET 2012)
- В периодической таблице слева направо в периоде… (NEET 1993)
- Правильный порядок 1-го потенциала ионизации (IP) среди следующих элементов… (NEET 2001)
- Значение электроотрицательности /атомов А и… (DUET 2009) 5 Какой из 90 следующие ионы имеют наибольшее значение… (ДУЭТ 2008)
Примеры вопросов
Вопросы.
 Что такое элементы? Назовите элемент. (2 балла)
Что такое элементы? Назовите элемент. (2 балла) Отв. Элемент – это вещество, которое нельзя расщепить или превратить в другое вещество химическими методами. Водород является примером элемента.
Вопросы. Что такое атомный номер? (2 балла)
Отв. Число протонов в ядре атома или количество электронов в электрически нейтральном атоме называется атомным номером.
Вопрос. Что вы подразумеваете под атомной массой элементов? (3 балла)
Отв. Атомная масса элемента относится к общей массе одного атома определенного элемента. Атомная масса эквивалентна количеству протонов и нейтронов в атоме. Атомная масса выражается через единую атомную единицу массы (а.е.м.).
Вопросы. Каково использование элементов лития, фосфора, магния, неона и аргона периодической таблицы? (5 баллов)
Ответ. Эти элементы периодической таблицы используются следующим образом:
- Литий – Литий наиболее известен благодаря своему применению в батареях.
 Он также используется в алюминиевых сплавах, чтобы сделать посуду более прочной, и, что самое странное, в качестве стабилизатора настроения в психиатрических препаратах.
Он также используется в алюминиевых сплавах, чтобы сделать посуду более прочной, и, что самое странное, в качестве стабилизатора настроения в психиатрических препаратах. - Неон — Элемент неон является четвертым по распространенности элементом во Вселенной. Рекламные вывески на сегодняшний день являются наиболее распространенным применением элемента. Стекло обычно загорается при искушении электричеством, что приводит к его использованию в секторе вывесок, а также в высоковольтных индикаторах и лазерах. Неон широко используется в криогенных жидких хладагентах.
- Магний — соли Эпсома, магнезиальное молоко, хлорид и цитрат — все это примеры медицинского применения магния. Магний также необходим для выживания как животных, так и растений. Его часто сплавляют с алюминием для использования в самолетах и автомобильных конструкциях из-за его меньшей плотности, чем у алюминия. Он также используется для удаления серы из расплавленного железа и стали.

- Фосфор – Сигнальные ракеты и зажигательные устройства содержат белый фосфор, а спичечные коробки содержат красный фосфор в веществе, прикрепленном сбоку. С другой стороны, соединения фосфора чаще всего используются в удобрениях. Фосфор также используется в производстве стали.
- Аргон – Аргон используется в качестве защитного слоя, окружающего нить накаливания в лампах накаливания и люминесцентных лампах, для предотвращения ее коррозии кислородом. Дуговая сварка и полупроводниковые кристаллы используют его в качестве защитного экрана.
Вопрос. Назовите благородные газы, входящие в состав первых 20 элементов периодической таблицы. (3 балла)
Отв. В первые 20 элементов периодической таблицы входят в основном три инертных газа:
- Гелий (He)
- Неон (Ne)
- Аргон (Ar)
Атомные номера гелия, неона и аргона равны 2, 10 и 18 соответственно.

Вопросы. Каковы химические формулы первых 20 элементов? (5 баллов)
Отв. Двухатомные элементы включают водород, азот, кислород, фтор и хлор. H 2 , N 2 , O 2 , F 2 , Cl 2 — их химические формулы соответственно.
Следующие элементы имеют символ и химическую формулу:
- Гелий-H,
- Литий-Li,
- Бериллий-Be,
- Бор-B,
- Углерод-C, Неон-Ne,
- Натрий-Na,
- Магний-Mg,
- Алюминий-Al,
- Кремний-Si,
- Аргон-Ar,
- Кальций-Ca
- Сера имеет1 химическую формулу химическая формула P 4 .
Вопрос. Какую всю информацию мы можем получить из атомного номера элемента? (3 балла)
Отв. Атомный номер элемента предоставляет следующую информацию об элементе:
- Атомный номер говорит нам о количестве протонов в ядре атома
- Количество электронов, окружающих ядро в нейтральном атоме.

-
Пока в этой главе были определены и обсуждены 10 элементов. Всего требуется еще 10, чтобы заполнить сокращенную периодическую таблицу из 20 элементов. Их имена и свойства кратко описаны здесь. Периодическая таблица представлена на рис. 3.9.
Натрий , Na , атомный номер 11, атомная масса 22,99, находится сразу после лития в периодической таблице и очень похож на литий, поскольку является мягким, химически очень активным металлом. В ядре атома есть один основной изотоп натрия, содержащий 12 нейтронов. Натрий имеет 10 электронов на внутренней оболочке, содержащихся в его первой внутренней оболочке из 2 электронов и во второй из 8 электронов. 11-й электрон в атоме натрия находится в третьей оболочке, которая является внешней оболочкой. Это показано одной точкой в символе Льюиса для Na на рис. 3.7. Электроны в натрии можно представить так, как показано на рис. 3.7.
Рисунок 3.7. Представление электронов в 2 внутренних оболочках и 1 внешней оболочке натрия и символе Льюиса натрия.
Магний , Mg , атомный номер 12, атомная масса 24,31, имеет 12 электронов на атом, поэтому он имеет 2 электрона внешней оболочки. Есть три изотопа магния, содержащие 12, 13 и 14 нейтронов. Магний — это относительно прочный и очень легкий металл, который используется в самолетах, выдвижных лестницах, переносных инструментах и других устройствах, где особенно важен легкий вес.
Алюминий , Al , атомный номер 13, атомная масса 26,98, имеет 3 электрона внешней оболочки в дополнение к 10 электронам внутренней оболочки. Алюминий — легкий металл, используемый в самолетах, автомобилях, линиях электропередач, строительстве зданий и во многих других областях. Несмотря на то, что он химически активен, оксидное покрытие, образующееся, когда алюминий на поверхности металла реагирует с кислородом воздуха, является самозащитным и предотвращает коррозию.
В некоторых важных отношениях алюминий можно рассматривать как зеленый металл. Это связано с тем, что алюминий позволяет создавать прочные легкие компоненты, которые при использовании в самолетах и автомобилях требуют относительно меньше энергии для перемещения. Таким образом, алюминий играет важную роль в энергосбережении. Алюминиевые кабели также обеспечивают эффективный способ передачи электроэнергии. Хотя руды, из которых изготавливается алюминий, являются извлекаемым ресурсом, добываемым из земли, алюминий является распространенным элементом. И есть альтернативные ресурсы, которые можно разрабатывать, в том числе алюминий в летучей золе, оставшейся от сжигания угля. Кроме того, алюминий является одним из наиболее пригодных для повторного использования металлов, а алюминиевый лом легко переплавляется и превращается в новые алюминиевые изделия.
Это связано с тем, что алюминий позволяет создавать прочные легкие компоненты, которые при использовании в самолетах и автомобилях требуют относительно меньше энергии для перемещения. Таким образом, алюминий играет важную роль в энергосбережении. Алюминиевые кабели также обеспечивают эффективный способ передачи электроэнергии. Хотя руды, из которых изготавливается алюминий, являются извлекаемым ресурсом, добываемым из земли, алюминий является распространенным элементом. И есть альтернативные ресурсы, которые можно разрабатывать, в том числе алюминий в летучей золе, оставшейся от сжигания угля. Кроме того, алюминий является одним из наиболее пригодных для повторного использования металлов, а алюминиевый лом легко переплавляется и превращается в новые алюминиевые изделия.
Если бы «элемент века» был назван в честь 1900-х годов, скромный кремний , Si , атомный номер 14, атомная масса 28,09 был бы вероятным кандидатом. Это связано с тем, что кремний является наиболее часто используемым из полупроводниковых элементов и в конце 1900-х годов стал основой для бурного развития электроники и компьютеров на основе полупроводниковых устройств, состоящих в основном из кремния. Несмотря на ценность этих продуктов на основе кремния, кремний в изобилии содержится в почве и горных породах, занимая второе место после кислорода в составе земной коры. Атом кремния имеет 4 электрона на внешней оболочке, половину октета, и это металлоид, промежуточный по поведению между металлами слева в периодической таблице и неметаллами справа.
Несмотря на ценность этих продуктов на основе кремния, кремний в изобилии содержится в почве и горных породах, занимая второе место после кислорода в составе земной коры. Атом кремния имеет 4 электрона на внешней оболочке, половину октета, и это металлоид, промежуточный по поведению между металлами слева в периодической таблице и неметаллами справа.
Значительно уменьшив объем электронных компонентов по сравнению с производительностью, кремний способствовал огромной экономии материалов, используемых в радиоприемниках, телевизорах, коммуникационном оборудовании и других электронных устройствах. Кроме того, полупроводниковые устройства на основе кремния, используемые в твердотельной электронике, потребляют лишь часть электроэнергии, которая когда-то использовалась устройствами на основе электронных ламп. Громоздкие провода из относительно редкой меди, использовавшиеся ранее для электрической передачи сигналов связи, были в значительной степени заменены оптоволоконными устройствами, состоящими из прозрачного кремнезема SiO2, которые передают информацию в виде световых импульсов. Оптическое волокно, похожее на волос, может передавать во много раз больше информации в единицу времени, чем толстый медный провод, который оно заменяет. А энергия, необходимая для передачи единицы информации по оптоволоконному кабелю, ничтожна по сравнению с энергией, необходимой для передачи той же информации электрическим импульсом по медному проводу. Таким образом, кремний — это действительно зеленый элемент, который, хотя и дешев и распространен, выполняет электронные и коммуникационные функции намного быстрее и лучше, чем медь и другие металлы, которые он заменил.
Оптическое волокно, похожее на волос, может передавать во много раз больше информации в единицу времени, чем толстый медный провод, который оно заменяет. А энергия, необходимая для передачи единицы информации по оптоволоконному кабелю, ничтожна по сравнению с энергией, необходимой для передачи той же информации электрическим импульсом по медному проводу. Таким образом, кремний — это действительно зеленый элемент, который, хотя и дешев и распространен, выполняет электронные и коммуникационные функции намного быстрее и лучше, чем медь и другие металлы, которые он заменил.
Фосфор , P , атомный номер 15, атомная масса 30,97, имеет 5 электронов на внешней оболочке. Таким образом, он находится непосредственно под азотом в периодической таблице и напоминает азот по своему химическому поведению. Чистый элементарный фосфор встречается в нескольких формах, наиболее распространенной из которых является белый фосфор. Белый фосфор является химически очень активным неметаллом, который может самовозгораться в атмосфере. Он токсичен и вызывает разрушение костей. Челюстная кость особенно восприимчива к воздействию фосфора, и у нее развивается состояние, известное как «фоссиальная челюсть», при котором кость становится пористой и слабой и может сломаться от нагрузки при жевании. Однако химически связанный фосфор является важным элементом жизни и одним из компонентов ДНК, основной молекулы, управляющей молекулярными жизненными процессами. Фосфор также является важным удобрением для растений и входит в состав многих промышленных химикатов, включая некоторые пестициды.
Он токсичен и вызывает разрушение костей. Челюстная кость особенно восприимчива к воздействию фосфора, и у нее развивается состояние, известное как «фоссиальная челюсть», при котором кость становится пористой и слабой и может сломаться от нагрузки при жевании. Однако химически связанный фосфор является важным элементом жизни и одним из компонентов ДНК, основной молекулы, управляющей молекулярными жизненными процессами. Фосфор также является важным удобрением для растений и входит в состав многих промышленных химикатов, включая некоторые пестициды.
Мышьяк находится в той же группе периодической таблицы, что и фосфор, и встречается в виде примеси с фосфором, переработанным из руды. Если этот фосфор будет использоваться в пищу, мышьяк должен быть удален.
Сера , S , атомный номер 16, атомная масса 32,06, имеет 6 электронов на внешней оболочке. Это хрупкий неметалл желтого цвета. Это важное питательное вещество для растений и животных, встречающееся в аминокислотах, из которых состоят белки. Сера является распространенным загрязнителем воздуха, выбрасываемым в атмосферу в виде двуокиси серы SO2 при сжигании ископаемого топлива, содержащего серу. Большая часть больших количеств серы, необходимых для промышленного производства серной кислоты и других серосодержащих химикатов, регенерируется из сероводорода, h3S, который загрязняет большую часть природного газа (метан, Ch5), который является таким важным топливом и сырьем. в мире сегодня. В соответствии с передовой практикой «зеленой» химии сероводород отделяется от сырого природного газа и сжигается около 1/3 его объема9.0007
Сера является распространенным загрязнителем воздуха, выбрасываемым в атмосферу в виде двуокиси серы SO2 при сжигании ископаемого топлива, содержащего серу. Большая часть больших количеств серы, необходимых для промышленного производства серной кислоты и других серосодержащих химикатов, регенерируется из сероводорода, h3S, который загрязняет большую часть природного газа (метан, Ch5), который является таким важным топливом и сырьем. в мире сегодня. В соответствии с передовой практикой «зеленой» химии сероводород отделяется от сырого природного газа и сжигается около 1/3 его объема9.0007
\[\ce{2h3S + 3O2 → 2SO2 + 2h3O} \label{3.7.1}\]
по производству диоксида серы, SO2. Затем полученный диоксид серы вступает в реакцию с оставшимся сероводородом посредством реакции Клауса, описанной ниже, с получением продукта элементарной серы, который используется для синтеза серной кислоты и других серосодержащих химических веществ.
\[\ce{2h3S + SO2 → 3S + 2h3O } \label{2.7.2}\]
Хлор , Cl , атомный номер 17, атомная масса 35,453, имеет 7 электронов на внешней оболочке, всего на 1 электрон меньше полного октета. Элементарный хлор представляет собой двухатомный газ зеленовато-желтого цвета, состоящий из молекул Cl2. В этих молекулах атомы Cl достигают стабильных октетов электронов внешней оболочки, разделяя два электрона в ковалентной связи, как показано на рис. 3.8. Атом хлора также может принять электрон для получения стабильного октета в анионе Cl-, как показано в ионном соединении хлорида натрия, NaCl, на рис. 3.8.
Элементарный хлор представляет собой двухатомный газ зеленовато-желтого цвета, состоящий из молекул Cl2. В этих молекулах атомы Cl достигают стабильных октетов электронов внешней оболочки, разделяя два электрона в ковалентной связи, как показано на рис. 3.8. Атом хлора также может принять электрон для получения стабильного октета в анионе Cl-, как показано в ионном соединении хлорида натрия, NaCl, на рис. 3.8.
Элементарный хлор может быть смертельным при вдыхании и был первым военным отравляющим газом, использованным в Первой мировой войне. Несмотря на свою токсичность, газообразный хлор спас много жизней благодаря его использованию в течение примерно последних 100 лет в качестве дезинфицирующего средства для питьевой воды, которое уничтожило смертельные болезни, передающиеся через воду, такие как холера и брюшной тиф. Хлор является важным промышленным химическим веществом, которое используется для производства пластмасс и растворителей. Недостаток хлора исключен, и его можно получить даже пропусканием электрического тока через морскую воду, содержащую хлор в виде растворенного хлорида натрия.
Хлор является важным промышленным химическим веществом, которое используется для производства пластмасс и растворителей. Недостаток хлора исключен, и его можно получить даже пропусканием электрического тока через морскую воду, содержащую хлор в виде растворенного хлорида натрия.
Экологичность хлора зависит от его применения. Элементарный хлор, безусловно, представляет собой опасный материал, производства и использования которого следует по возможности избегать в практике «зеленой» химии. Но, как отмечалось выше, элементарный хлор спас много жизней благодаря его использованию для дезинфекции воды. Ряд стойких пестицидов, включая ДДТ, представляют собой органические соединения, состоящие из хлора, углерода и водорода. В дополнение к экологическому ущербу, наносимому этими пестицидами, побочные продукты их производства и производства других хлорорганических соединений являются одними из наиболее распространенных загрязнителей опасных химических отходов. Обычный пластик, поливинилхлорид (ПВХ), содержит хлор. Этот пластик широко используется в водопроводных и дренажных трубах, в первом случае заменяя относительно дефицитный и дорогой металл меди и токсичный свинец. Но материал, используемый для производства ПВХ, представляет собой летучий винилхлорид. Это один из немногих известных канцерогенов для человека, вызывающий задокументированные случаи редкой формы рака печени у рабочих, которые ранее подвергались воздействию очень высоких уровней паров винилхлорида на рабочем месте. Из-за опасности элементарного хлора и проблем, вызванных хлорорганическими соединениями, практика зеленой химии, безусловно, пытается свести к минимуму производство и использование элементарного хлора и, как правило, пытается минимизировать производство хлорорганических соединений и их рассеивание в окружающей среде.
Этот пластик широко используется в водопроводных и дренажных трубах, в первом случае заменяя относительно дефицитный и дорогой металл меди и токсичный свинец. Но материал, используемый для производства ПВХ, представляет собой летучий винилхлорид. Это один из немногих известных канцерогенов для человека, вызывающий задокументированные случаи редкой формы рака печени у рабочих, которые ранее подвергались воздействию очень высоких уровней паров винилхлорида на рабочем месте. Из-за опасности элементарного хлора и проблем, вызванных хлорорганическими соединениями, практика зеленой химии, безусловно, пытается свести к минимуму производство и использование элементарного хлора и, как правило, пытается минимизировать производство хлорорганических соединений и их рассеивание в окружающей среде.
Элемент номер 18, аргон , Ar , атомная масса 39,95, подводит нас к концу третьего периода сокращенной таблицы Менделеева. Он имеет полный октет электронов внешней оболочки и является благородным газом. Никаких истинных химических соединений аргона не было выделено, и никакие химические связи с участием этого элемента не были известны до тех пор, пока в сентябре 2000 года не было сообщено об образовании очень нестабильной переходной связи с участием атомов Ar. Аргон составляет около 1% по объему в атмосфере. Во многом из-за своей химической инертности аргон имеет некоторые применения. Он используется в качестве газа для наполнения ламп накаливания. В этом отношении он помогает предотвратить испарение раскаленных добела атомов вольфрама из нити накала лампы, что значительно продлевает срок службы лампы. Он также используется в качестве плазменной среды в приборах, используемых для атомно-эмиссионного анализа элементарных загрязнителей с индуктивно связанной плазмой. В этом приложении радиочастотный сигнал используется для преобразования аргона в газообразную плазму, которая содержит положительно заряженные ионы Ar+ и отрицательно заряженные электроны и нагревается до невероятно высокой температуры 10 000°C.
Никаких истинных химических соединений аргона не было выделено, и никакие химические связи с участием этого элемента не были известны до тех пор, пока в сентябре 2000 года не было сообщено об образовании очень нестабильной переходной связи с участием атомов Ar. Аргон составляет около 1% по объему в атмосфере. Во многом из-за своей химической инертности аргон имеет некоторые применения. Он используется в качестве газа для наполнения ламп накаливания. В этом отношении он помогает предотвратить испарение раскаленных добела атомов вольфрама из нити накала лампы, что значительно продлевает срок службы лампы. Он также используется в качестве плазменной среды в приборах, используемых для атомно-эмиссионного анализа элементарных загрязнителей с индуктивно связанной плазмой. В этом приложении радиочастотный сигнал используется для преобразования аргона в газообразную плазму, которая содержит положительно заряженные ионы Ar+ и отрицательно заряженные электроны и нагревается до невероятно высокой температуры 10 000°C.
Следующим элементом, который будет добавлен в сокращенную периодическую таблицу, является элемент номер 19. С него начинается четвертый период периодической таблицы. Этот период на самом деле содержит 18 элементов, но мы возьмем только первые два. Это связано с тем, что элемент номер 21 является первым из переходных металлов, и объяснение их положения в периодической таблице на основе входящих в них электронов становится несколько более сложным и запутанным, чем это уместно в этой книге. Читатель, нуждающийся в более подробной информации, может обратиться к другим стандартным книгам по начальной химии.2,3
Элемент с атомным номером 19 — это калий , K , имеющий атомную массу 39,10. Большая часть калия состоит из изотопа с 20 нейтронами. Однако небольшая часть встречающегося в природе К находится в форме . Это радиоактивный изотоп калия, и, поскольку у всех нас есть калий (необходимый элемент для жизни) в организме, мы все естественным образом радиоактивны! Мышечная масса содержит больше калия, чем жировая (жировая) ткань, поэтому более мускулистые люди более радиоактивны. Но не беспокойтесь, уровень радиоактивности калия в организме слишком низок, чтобы вызывать беспокойство, и его нельзя избежать ни при каких обстоятельствах. (Один из сторонников ядерной энергии указал, что сон с мускулистым человеком подвергает человека большему воздействию радиации, чем жизнь рядом с ядерным энергетическим реактором.)
Но не беспокойтесь, уровень радиоактивности калия в организме слишком низок, чтобы вызывать беспокойство, и его нельзя избежать ни при каких обстоятельствах. (Один из сторонников ядерной энергии указал, что сон с мускулистым человеком подвергает человека большему воздействию радиации, чем жизнь рядом с ядерным энергетическим реактором.)
То же, что можно сказать о натрии, элементе номер 11, в целом верно и о калии. В чистом элементарном состоянии калий является очень реакционноспособным щелочным металлом . Как важный элемент для жизни, это обычное удобрение, добавляемое в почву для хорошего роста сельскохозяйственных культур. Химически калий теряет свой единственный электрон внешней оболочки, образуя ион K+.
Кальций , Ca , атомный номер 20, атомная масса 40,08, имеет 2 электрона на внешней оболочке, два за пределами полного октета. Атом кальция легко теряет два «лишних» электрона, образуя катион Са2+. Как и другие элементы в своей группе периодической таблицы, кальций является щелочноземельным металлом. Элементарный металлический кальций химически активен, хотя и не так сильно, как калий. Кальций имеет химические свойства, очень похожие на свойства магния, щелочноземельного металла, расположенного непосредственно над кальцием в периодической таблице.
Элементарный металлический кальций химически активен, хотя и не так сильно, как калий. Кальций имеет химические свойства, очень похожие на свойства магния, щелочноземельного металла, расположенного непосредственно над кальцием в периодической таблице.
Кальций необходим для жизни, хотя большинство почв содержат достаточно кальция для оптимального роста сельскохозяйственных культур. Кальций очень важен для нашего организма, потому что, будучи твердым минералом гидроксиапатитом, Ca5OH(PO4)3, он представляет собой твердый материал в зубах и костях. Дефицит кальция может привести к формированию плохих зубов и развитию инвалидизирующего остеопороза, состояния, характеризующегося слабостью костей, которое особенно часто поражает пожилых женщин.
Первые 20 элементов – значение, атомный номер и символ
Атомный номер и символы важны в химии. Символ элемента представляет собой одно- или двухбуквенное сокращение названия элемента. При написании длинных химических уравнений нам нужно написать краткую форму соединений и элементов, поскольку эти символы очень полезны. Атомный номер элементов дает представление об атомной структуре элементов, например о том, сколько электронов и протонов имеет этот конкретный элемент. Первые 20 элементов периодической таблицы даны на рисунке ниже.
(Изображение скоро будет загружено)
Каковы первые 20 элементов Периодической таблицы?
Первые 20 элементов таблицы Менделеева, которые имеют атомные номера 1-20, перечислены ниже.
Atomic Number | Element | Symbol | |||||||||||||
1 | Hydrogen | H | |||||||||||||
2 | Helium | He | |||||||||||||
3 | lithium | Li | |||||||||||||
4 | Beryllium | Be | |||||||||||||
5 | Boron | B | |||||||||||||
6 | Carbon | C | |||||||||||||
7 | Nitrogen | N | |||||||||||||
8 | Oxygen | O | |||||||||||||
9 | Fluorine | F | |||||||||||||
10 | Neon | Ne | |||||||||||||
11 | Sodium | Na | |||||||||||||
12 | Magnesium | Mg | |||||||||||||
13 | Aluminium | Al | |||||||||||||
14 | Силикон | SI | |||||||||||||
15 | Phosphorus | . | |||||||||||||
16 | Sulphur | S | |||||||||||||
17 | Chlorine | Cl | |||||||||||||
18 | Argon | Ar | |||||||||||||
19 | Potassium | K | |||||||||||||
20 | Calcium | Ca |
Каждый элемент обладает различными свойствами, обусловленными его атомным номером, атомной массой, электронной конфигурацией, электроотрицательностью, энтальпией электронного усиления и т. д.
Важность атомного номера элемента в Периодической таблице
Прежде чем узнать о важности атомного числа элементов, взгляните на следующие определения.
Атомный номер элемента в периодической таблице дает нам следующую информацию:
Чем полезны для нас первые 20 элементов периодической таблицы?
Некоторые из первых 20 элементов периодической таблицы очень полезны для нашей повседневной жизни, например:
Благородные газы в первых 20 элементах периодической таблицы
Во-первых, нам нужно знать, что такое благородные газы. Благородные газы также называют инертными газами. Благородные газы находятся в 18-й группе периодической таблицы. Известно, что они наименее реакционноспособны или крайне нереактивны. Благородные газы были охарактеризованы позже других элементов.
Итак, среди первых 20 элементов есть три благородных газа, а именно гелий (He), неон (Ne) и аргон (Ar). Гелий имеет атомный номер 2, неон имеет атомный номер 10, а аргон имеет атомный номер 18. все элементы. Эта статья будет развивать понимание атомных номеров и символов элементов.
Первые 20 элементов — значение, определение, примеры, периодическая таблица, часто задаваемые вопросы
Первые 20 элементов:
Любое вещество, которое нельзя разложить химически на простые молекулы, называется элементом. Элемент состоит из атомов с одинаковым атомным номером, а это означает, что каждый атом будет иметь такое же количество протонов в ядре, как и другие атомы в компоненте.
Элемент состоит из атомов с одинаковым атомным номером, а это означает, что каждый атом будет иметь такое же количество протонов в ядре, как и другие атомы в компоненте.
Первые 20 элементов периодической таблицы
Периодическая таблица — это представление элементов в порядке возрастания их атомного номера.
Первые двадцать элементов периодической таблицы с атомными номерами 1-20:
Читайте также:
