Содержание.
Министерство здравоохранения Российской Федерации
Государственное бюджетное образовательное учреждение
высшего профессионального образования
Первый Московский государственный
Медицинский университет имени И. М. Сеченова.
Кафедра общей химии.
Тема: «Химия элементов VIII B группы»
Выполнила: студентка III курса
Педиатрического факультета 9 гр
Мирзалиева Гюнель Шахлар кызы
Проверила: Филипова А.А.
Москва 2015
Общая характеристика_______________________________________________2 стр.
Краткие сведения об истории открытия элементов данной подгруппы и распространённости в природе_______________________________________3-7 стр.
Изменения в подгруппах железа, кобальта и никеля величины радиусов атомов и ионов, потенциала ионизации ________________________________________8 стр.

Химические свойства простых веществ______________________________8-11 стр.
Свойства пентакарбонилжелеза ______________________________________________11 стр.
Цис-, транс-изомерия комплексных соединений платины_________________12 стр.
Медико-биологическое значение элементов VIII Б группы_____________12-13 стр.
Список литературы_________________________________________________14 стр.
Общая характеристика
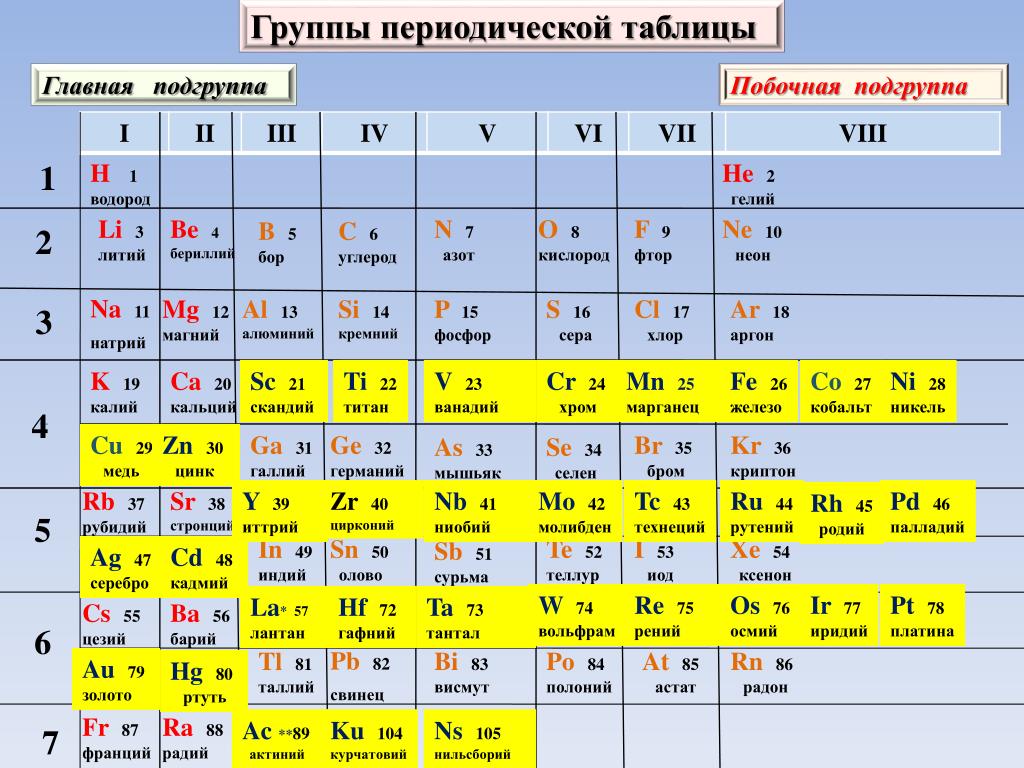
В короткой форме Периодической таблицы Менделеева каждая группа элементов подразделяется на главную подгруппу (А или а ) и побочную подгруппу ( B или b ). В главную подгруппу входят s- и p-элементы, в побочную – d-элементы.
Элементы
побочных подгрупп (d-элементы) называют
“ переходными “ элементами или
переходными металлами (все d-элементы
– металлы).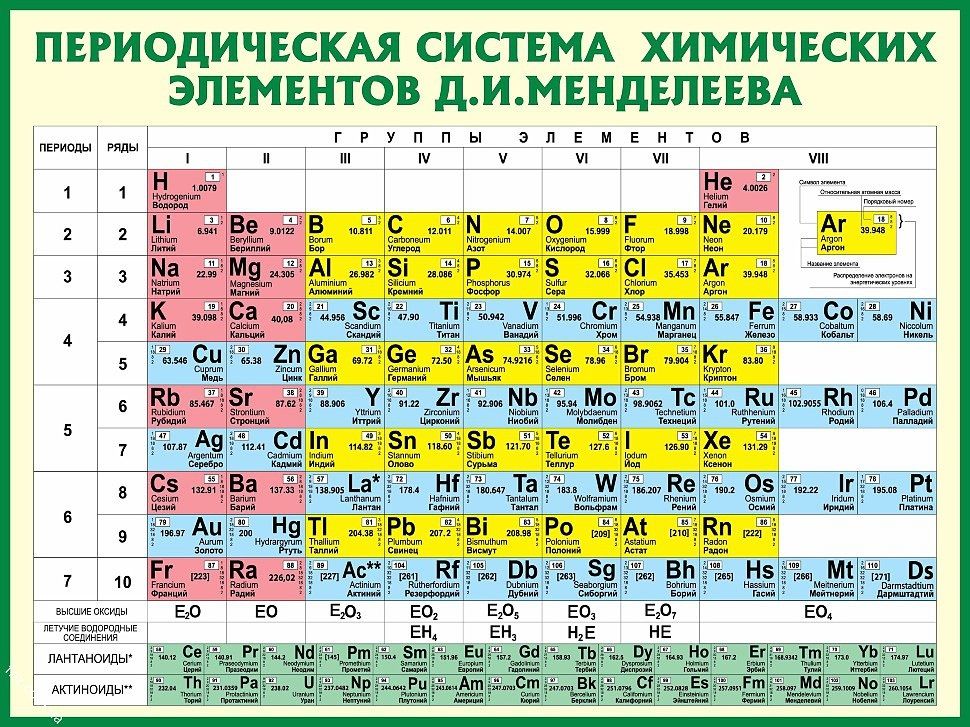 Термин “переходные металлы”
возник вследствие того, что все d-элементы
в периодах (строчках таблицы) служат
как бы “переходным мостиком” от
металлических s-элементов к p-элементам,
среди которых уже много неметаллов.
Термин “переходные металлы”
возник вследствие того, что все d-элементы
в периодах (строчках таблицы) служат
как бы “переходным мостиком” от
металлических s-элементов к p-элементам,
среди которых уже много неметаллов.
Соответственно VIII B подгруппа относится к побочным d-элементам.
Все d-элементы VIIIВ группы – металлы. В образовании связей участвуют ē подуровня и ē предпоследнего (n-1)d подуровня.
Соединения d-элементов легко вступают в ОВ-реакции. С увеличением атомного номера повышается стабильность более высоких С.О. например, OS и Ru образуют соединения со С.О. +8. Для Fе более устойчива С.О. + 3, соединения Fe с С.О. +6 неустойчивы и сильные окислители, а соединения Fe со С.О. +8 не получены.
Все
металлы VIII В – катализаторы, большей
или меньшей степени способны поглощать
водород и активизировать его; все
образуют окрашенные ионы (соединения,
и склонны к комплексообразванию).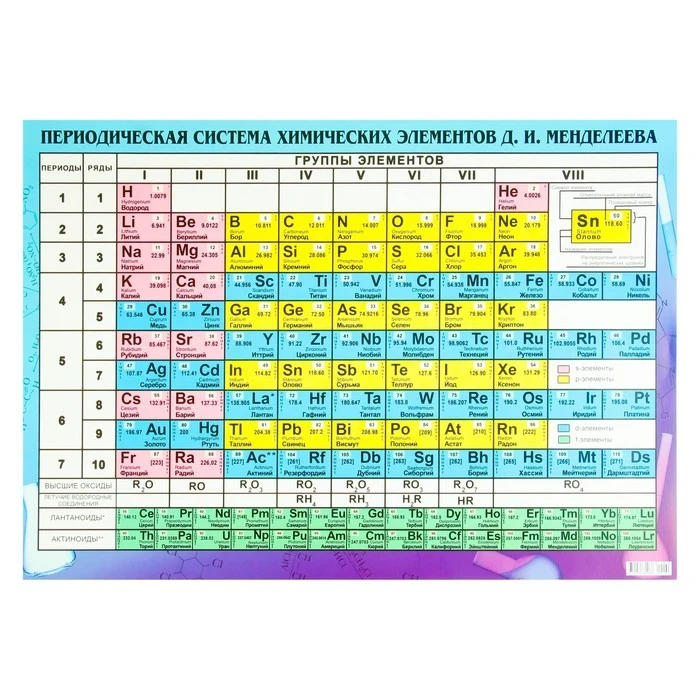
2. Краткие сведения об истории открытия элементов данной подгруппы и распространённости в природе.
2.1. Fe (железо)- элемент 8 группы, 4 периода с атомным номером 26. Один из самых распространённых в земной коре металлов.
История открытия
Предположительно,
что железо, которое попало впервые в
руки человека, было метеоритного
происхождения. Первым упоминания об
использовании железа около пяти тысяч
лет. Железо в те времена было очень
дорогим, ценилось оно дороже золота,
первого металла, который стал использовать
человек. Затем стали получать нагреванием
руд с углем, делая это на ветреных местах.
Но, полученное таким способом железо
было губчатым, с большим содержанием
шлаков и хрупким. Важнейшим шагом в
технологии получения железа стало
появление горна, который был открыт
сверху и обложен изнутри огнеупорными
материалами. Используя данный способ,
получалось относительно качественное
железо. Далее, люди заметили, что из
чугуна, который они считали отходами,
можно получить качественный металл,
при этом требовалось значительно меньше
угля, и качество металла было значительно
лучше.
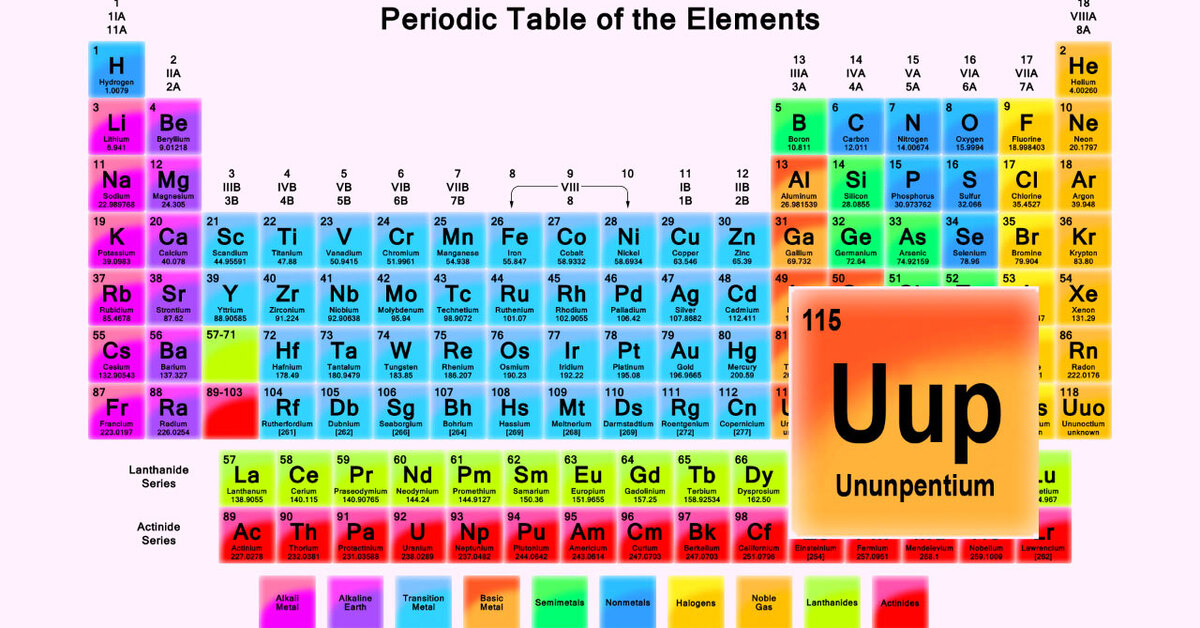
Периодическая система химических элементов Д. И. Менделеева. Знаки химических элементов
Часть 1
1. По горизонтали таблица Д.И. Менделеева делится на периоды, которые подразделяются на
а) малые, это периоды – 1, 2, 3
б) большие, это периоды – 4, 5, 6, 7
2. По вертикали таблица Д.И. Менделеева делится на группы, каждая из которых подразделяется на:
а) главную, или А группу
б) побочную, или В группу
3. Допишите
IA группа – это группа щелочных металлов
IIA группа – это группа щелчноземельных металлов
VIIA группа – это группа галогенов
VIIIA группа – это группа благородных или инертных газов
4. Аналогии языка химии с русским языком.
Аналогии языка химии с русским языком.
Русский язык Химический язык Буквы Химические знаки (символы) Слова Названия веществ Предложения Уравнения химических реакций
5. Дополните таблицу “Названия и знаки элементов”.
6. Примеры названий химических элементов (в скобках укажите химический знак) в соответствии с этимологическими источниками.
1) Свойства простых веществ
Водород (H), Кислород (O), Фтор (F)
2) Астрономия
Селен (Se), Теллур (Te), Уран (U)
3) География
Германий (Ge), Галлий (Ga), Полоний (Po)
4) Древнегреческие мифы
Тантар (Ta), Прометий (Pm), Лютеций (Lu)
5) Великие ученые
Кюрий (Cm), Менделевий (Md), Резерфордий (Rt)
Часть 2
1. Установите соответствие между положением химического элемента в Периодической системе Д.И. Менделеева и химическим знаком.
Установите соответствие между положением химического элемента в Периодической системе Д.И. Менделеева и химическим знаком.
Ответ: А-5, Б-1, В-2, Г-4
2. Выберите символы или названия химических элементов одного большого периода. Из букв, соответствующих правильным ответам, вы составите названия металла, который используется для изготовления бенгальских огней: магний.
3. Впишите в соответствующие столбцы названия следующих химических элементов: Cl, He, Br, Ne, Li, I, K, Ba, Ca, Na, Xe, Sr.
Щелочные металлы Щелочноземельный металлы Галогены Благородные газы Литий Барий Хлор Гелий Калий Кальций Бром Неон Натрий Стронций Йод Ксенон
4.
Химический элемент (H, O) – химическая реакция (H2O) – химическое получение (2H2O = 2H2 + O2)
5. Сделайте обощение:
Химические элементы – углерод, кремний, олово, свинец – относятся к IVA группе.
6. В левую колонку таблицы запишите, по какому признаку химические элементы разделены на две группы.
Металлы Цинк, медь, натрий, золото, серебро, железо Неметаллы Хлор, фтор, водород, кремний, углерод, азот
7. Установите соответствие между произношением и химическим знаком (символом).
Ответ: А-4, Б-6, В-2, Г-7, Д-5, Е-1
8. Вычеркните лишнее:
кюрий, менделевий, бром, эйнштейний
9. Общий этимологический источник названий химических элементов:
Общий этимологический источник названий химических элементов:
U, Te, Se – это планетарий
10. В честь различных государств или частей света названы элементы:
Германий, галлий, франций, дубний
Части периодической таблицы
Группа 2A (или IIA ) периодической таблицы являются щелочными
земные металлы : бериллий (Be), магний (Mg), кальций (Ca),
стронций (Sr), барий (Ba) и радий (Ra). Они тяжелее и
менее реакционноспособны, чем щелочные металлы группы 1А. Имя приходит
от того, что оксиды этих металлов давали основные растворы
при растворении в воде и оставались твердыми при температурах
доступны древним алхимикам. Как и элементы группы 1А,
Щелочноземельные металлы слишком реакционноспособны, чтобы их можно было найти в природе. элементарная форма.
Щелочноземельные металлы имеют два валентных электрона на орбиталях с наивысшей энергией. ( нс 2 ). Они меньше, чем щелочные металлы тот же период и, следовательно, имеют более высокие энергии ионизации. В большинстве случаев щелочноземельные металлы ионизируются. для формирования заряда 2+.
Щелочноземельные металлы имеют гораздо более высокую температуру плавления, чем щелочные металлы: бериллий плавится при 1287С, магний при 649С, кальций при 839С, стронций при 768°С, барий при 727°С и радий при 700°С. Они есть более твердые металлы, чем элементы группы 1А, но мягкие и легкие по сравнению со многими переходными металлами.
Соли металлов 2А группы менее растворимы в воде, чем соли
Группа 1А из-за более высокой плотности заряда на катионах 2+;
тем не менее, многие соли группы 2А, по крайней мере, умеренно растворимы.
Некоторые соли группы 2А прочно связываются с молекулами воды и кристаллизуются в виде гидраты ;
среди них английская соль, MgSO 4 7H 2 O и гипс,
CaSO 4 2H 2 О.
Бериллий (Be, Z=4).
Бериллий — серебристо-белый мягкий металл. Его название происходит от греческое слово, обозначающее минерал берилл, beryllo . Он находится в земной коры с концентрацией 2,6 промилле, что делает ее 47-й по величине обильный элемент. Первичные руды бериллия – это берилл [алюмосиликат бериллия, Be 3 Al 2 (SiO 3 ) 6 ] и бертрандит [гидроксид силиката бериллия, Be 4 Si 2 O 7 (OH) 2 ]. Бериллы драгоценного качества включают изумруды и аквамарины; зеленый цвет этих драгоценных камней происходит из следовых количеств хрома.
Из-за небольшого размера и высокой плотности заряда бериллий через ковалентную связь вместо ионной связи. Элементаль бериллий очень инертен по отношению к воздуху и воде даже при высоких температурах. температуры.
Бериллий используется для изготовления окон для рентгеновских трубок (это
прозрачен для рентгеновских лучей) и используется в сплавах с другими металлами, такими как
медь и никель для изготовления искробезопасных инструментов и часовых пружин. Бериллий также используется в корпусах ядерного оружия и в атомной промышленности.
электростанции из-за его способности отражать нейтроны. Бериллий
накапливается в костях; Длительное воздействие бериллия приводит к
воспаление в легких и одышка (состояние, называемое бериллиозом).
Бериллий также используется в корпусах ядерного оружия и в атомной промышленности.
электростанции из-за его способности отражать нейтроны. Бериллий
накапливается в костях; Длительное воздействие бериллия приводит к
воспаление в легких и одышка (состояние, называемое бериллиозом).
Магний (Mg, Z=12).
Магний — относительно мягкий металл серебристо-белого цвета. Название элемента происходит от Магнезия, район в Фессалии в центральной Греции. Он находится в земная кора с концентрацией 2,3%, что делает ее 7-й по величине обильный элемент. Большое количество магния также содержится в полезных ископаемых в мантии Земли. Получают из морской воды, карналита [MgKCl 3 6H 2 O], доломит [смесь карбонатов кальция и магния, CaMg(CO 3 ) 2 ], и магнезит [карбонат магния, MgCO 3 ].
Магний, легированный алюминием и следами других металлов, используется в
автомобилестроение и авиастроение; магниевые сплавы также используются в других
легкие устройства, такие как лестницы, камеры, велосипедные рамы, жесткий диск
диски и т. д. Магний легче окисляется, чем железо, и
используется в жертвенные аноды для защиты железных труб и других
структуры, которые легко подвергаются коррозии.
д. Магний легче окисляется, чем железо, и
используется в жертвенные аноды для защиты железных труб и других
структуры, которые легко подвергаются коррозии.
Магний горит на воздухе ярко белое пламя, и используется в фейерверках и зажигательных бомбах. (Это было используется в одноразовых лампах-вспышках, но это использование было вытеснено другими виды освещения.) Магниевые костры очень трудно зажечь наружу, так как даже в отсутствие воздуха горящий магний вступает в реакцию с азот с образованием нитрида магния (Mg 3 N 2 ), и с водой для получения гидроксида магния и газообразного водорода.
Магний содержится в ряде известных соединений. Магний
оксид MgO используется в огнеупорных кирпичах, способных
выдерживать высокие температуры в каминах и печах (магниевый
оксид плавится при 2800 С). Гептагидрат сульфата магния, MgSO 4 7H 2 O,
более известная как английская соль, является
миорелаксант и мягкое слабительное. Гидроксид магния, Mg(OH) 2 ,
также известный как молоко магнезии, является слабительным и антацидом.
(«Молоко» в «молоке магнезии» относится к тому факту, что, поскольку магний
гидроксид плохо растворяется в воде, имеет тенденцию образовывать известковую, белую
суспензия, похожая на молоко, но со значительно
физиологические эффекты.)
Гидроксид магния, Mg(OH) 2 ,
также известный как молоко магнезии, является слабительным и антацидом.
(«Молоко» в «молоке магнезии» относится к тому факту, что, поскольку магний
гидроксид плохо растворяется в воде, имеет тенденцию образовывать известковую, белую
суспензия, похожая на молоко, но со значительно
физиологические эффекты.)
Зеленые растения содержат молекулу под названием хлорофилл, состоящий из плоского кольца атомов углерода и азота с большим открытым пространством посередине, в котором связан ион магния, удерживается на месте атомами азота. молекула хлорофилла поглощает солнечный свет, и в процессе фотосинтеза, энергия света превращается в химическую энергии, которую завод может использовать для питания множества процессов.
В органической химии магний реагирует с бромалканами.
(углеводороды, содержащие бромуглеродные связи) с образованием магнийорганических соединений
известны как реактивы Гриньяра (в честь их первооткрывателя Виктора
Гриньяр, получивший Нобелевскую премию по химии в 1912 г. ). Эти соединения чрезвычайно полезны при формировании
новый углерод-углерод
связи и часто используются в синтезе органических соединений. Известно, что реактивы Гриньяра чувствительны к воде, поэтому необходимо соблюдать осторожность.
удостовериться, что аппарат, в котором идет реакция,
проведено очень сухо.
). Эти соединения чрезвычайно полезны при формировании
новый углерод-углерод
связи и часто используются в синтезе органических соединений. Известно, что реактивы Гриньяра чувствительны к воде, поэтому необходимо соблюдать осторожность.
удостовериться, что аппарат, в котором идет реакция,
проведено очень сухо.
Кальций (Ca, Z=20).
Кальций — относительно мягкий металл серебристого цвета. Название элемента происходит от Латинское слово, обозначающее известь, calx . Он находится в земная кора с концентрацией 4,1%, что делает ее пятой по величине обильный элемент. Основными источниками кальция являются кальцит и известняк. [карбонат кальция, CaCO 3 ], ангидрит [кальций сульфат, CaSO 4 ], гипс [дигидрат сульфата кальция, CaSO 4 2H 2 O], и доломит [смесь карбонатов кальция и магния, CaMg(CO 3 ) 2 ].
Соли кальция образуют твердые части тела большинства живых существ. существ, из раковин морских организмов и кораллов кораллов
рифы (в виде кальция
карбонат, CaCO 3 ) к костям и зубам наземных
существ (в виде гидроксиапатита
кристаллы, Са 3 (PO 4 ) 2 ] 3 Ca(OH) 2 ).
существ, из раковин морских организмов и кораллов кораллов
рифы (в виде кальция
карбонат, CaCO 3 ) к костям и зубам наземных
существ (в виде гидроксиапатита
кристаллы, Са 3 (PO 4 ) 2 ] 3 Ca(OH) 2 ).
Поскольку кальций образует такие твердые минералы, он полезен в строительстве.
материалов, таких как гипс, раствор и цемент. Раствор изготавливается из оксида кальция CaO, также известного как известь или негашеная известь. При взаимодействии оксида кальция с водой образуется гидроксид кальция.
Ca(OH) 2 или гашеная известь, которая поглощает углекислый газ из
воздух и постепенно образует карбонат кальция CaCO 3 .
Известь, нагретая водородом, горящим в кислороде, горит ярко-белым цветом.
свет, который можно сфокусировать в узкий пучок, видимый на большой
расстояния. Такое освещение использовалось на маяках, в
съемки, а в театрах производить прожекторы (оставляя актера «в
в центре внимания”).
Хлорид кальция расплывается (он поглощает достаточное количество воды из воздух, который он растворяет в растворе), и используется для удаления влаги с воздуха в сырых подвалах. (Потребуется более сильный человек что я не могу назвать только что открытую коробку с хлоридом кальция, не вел себя должным образом как «несовершеннолетний распутник».)
«Жесткая вода» содержит растворенные минералы, имеющие 2+ или 3+ заряда, такие как кальций и магний; эти соли вызывают некоторые мыла и моющие средства, выпадающие в осадок в виде «мыльной пены»; эти минералы осаждаются со временем образует «накипь» в воде обогреватели и кастрюли. Кальций можно удалить водой умягчители, которые обменивают ионы кальция на ионы натрия, которые имеют 1+ заряжается и не выпадает в осадок.
Стронций (Sr, Z=38).
Стронций — блестящий, относительно мягкий металл. Название элемента происходит от
Стронтиан — город в Шотландии, где добывали минерал стронтианит. открыт, из которого впервые был выделен стронций. Он находится в
земная кора с концентрацией 370 частей на миллион, что делает ее 16-й по величине
обильный элемент. Встречается в рудах целестита [стронция
сульфат, SrSO 4 ] и стронцианит [карбонат стронция, SrCO 3 ].
открыт, из которого впервые был выделен стронций. Он находится в
земная кора с концентрацией 370 частей на миллион, что делает ее 16-й по величине
обильный элемент. Встречается в рудах целестита [стронция
сульфат, SrSO 4 ] и стронцианит [карбонат стронция, SrCO 3 ].
Соли стронция при нагревании окрашиваются в ярко-красный цвет. по этой причине используется в фейерверках и сигнальных ракетах. Радиоактивный стронций-90 (бета-излучатель) образуется при ядерных взрывах; поскольку он химически похож на кальций, он включается в кости у людей, подвергающихся его воздействию. Стронций-90 является бета-излучателем, и препятствует выработке эритроцитов.
Барий (Ba, Z=56).
Барий — блестящий мягкий металл. Название элемента происходит от
греческое слово barys , означающее «тяжелый», по отношению к
высокая плотность некоторых минералов бария. Он находится в
земная кора с концентрацией 500 частей на миллион, что делает ее 14-й по величине
обильный элемент. Встречается в баритовых рудах [сульфат бария,
БаСО 4 ] и витерит [карбонат бария, BaCO 3 ].
Он находится в
земная кора с концентрацией 500 частей на миллион, что делает ее 14-й по величине
обильный элемент. Встречается в баритовых рудах [сульфат бария,
БаСО 4 ] и витерит [карбонат бария, BaCO 3 ].
Барий был обнаружен в 1500-х годов в виде «болонских камней» (теперь известных как бариевые сульфат, BaSO 4 ), обнаруженный недалеко от Болоньи, Италия. Эти камни светились в присутствии света, а также при нагревании. Соли бария при нагревании окрашиваются в зеленый цвет и используются в фейерверки (в форме нитрата бария, Ba(NO 3 ) 2 ).
Сульфат бария, BaSO 4 , ядовит, но это так
нерастворимым, что он проходит через тело до любого поглощения
может иметь место барий. Используется в диагностике некоторых
проблемы с кишечником в виде «бариевых клизм»: сульфат бария
непрозрачен для рентгеновских лучей и может быть использован для рентгенографии пищеварительного тракта.
тракт.
Радий (Ra, Z=88).
Радий — мягкий, блестящий, радиоактивный металл. Название элемента произошло от латинского слова «луч» 9.0013 радиус , из-за его способность светиться в темноте слабым голубым светом. Он находится в земной коры с концентрацией 0,6 ppt (частей на триллион), что делает ее 84-й самый распространенный элемент. Он содержится в следовых количествах в урановых руд, но коммерчески используемый радий легче получить из отработавшее ядерное топливо.
Открыт радий
Пьером и Марией Кюри в 1898 году; они извлекли миллиграмм радия
из трех тонн урановой руды. Радий производится в
радиоактивный распад урана-235, урана-238, тория-232 и
плутоний-241. После его открытия и до опасностей
радиация была понята, радий использовался во многих шарлатанских лекарствах и
патентованные лекарства. Радий использовался для изготовления часов, светящихся в темноте.
лица в начале 1900-е годы; альфа-частицы, испускаемые радием
ударил частицы сульфида цинка, заставив их светиться, но был остановлен
по корпусу часов по стеклу циферблата. Многие из
рабочие, расписывавшие эти циферблаты, заболели или умерли от
лучевая болезнь.
Многие из
рабочие, расписывавшие эти циферблаты, заболели или умерли от
лучевая болезнь.
Джон Эмсли, Элементы , 3-е издание. Оксфорд: Clarendon Press, 1998.
.Джон Эмсли, Строительные блоки природы: Путеводитель по элементам от А до Я . Оксфорд: Оксфордский университет Пресс, 2001.
Дэвид Л. Хейзерман, Исследование Химические элементы и их соединения . Нью-Йорк: TAB Книги, 1992.
Группы IIA, IIIA и IVA
Группы IIA, IIIA и IVA
| Группа IIA: Щелочно-земельные металлы | Группа IIIA: Химия из алюминия | Группа IVA: олово и свинец |
Группа IIA: Щелочно-земельные металлы
Все элементы группы IIA (Be, Mg, Ca, Sr, Ba и Ra)
металлы, и все, кроме Be и Mg, являются активными металлами. Эти элементы
часто называют щелочноземельных металлов. Терм щелочной отражает тот факт, что многие соединения этих металлов являются основными
или щелочной. Срок земля исторически использовалась для
описывают тот факт, что многие из этих соединений нерастворимы в
вода. Большая часть химии щелочноземельных металлов (группа
IIA) можно предсказать по поведению щелочных металлов (группа IA). Три точки должны быть
однако имейте в виду.
Эти элементы
часто называют щелочноземельных металлов. Терм щелочной отражает тот факт, что многие соединения этих металлов являются основными
или щелочной. Срок земля исторически использовалась для
описывают тот факт, что многие из этих соединений нерастворимы в
вода. Большая часть химии щелочноземельных металлов (группа
IIA) можно предсказать по поведению щелочных металлов (группа IA). Три точки должны быть
однако имейте в виду.
- Щелочноземельные металлы имеют тенденцию терять два электрона, чтобы форма M 2+ ионы (Be 2+ , Mg 2+ , Ка 2+ и так далее).
- Эти металлы менее реакционноспособны, чем соседние щелочной металл. Магний менее активен, чем натрий; кальций менее активен, чем калий; и так далее.
- Эти металлы становятся более активными по мере продвижения вниз по колонке.
Магний более активен, чем бериллий; кальций больше
активнее магния; и так далее.

Щелочноземельные металлы реагируют с неметаллами с образованием продукты, ожидаемые от электронных конфигураций элементы.
Mg( с ) + Cl 2 ( г ) MgCl 2 ( с )
3 Mg( с ) + N 2 ( г ) Mg 3 N 2 ( s )
Ca( s ) + H 2 ( g ) CaH 2 ( s )
Поскольку они не так активны, как щелочные металлы, большинство эти элементы образуют оксиды.
2 Мг( с ) + О 2 ( г ) 2 MgO( s )
Кальций, стронций и барий также могут образовывать пероксиды.
Ва( с ) + О 2 ( г ) BaO 2 ( s )
Более активные представители группы IIA (Ca, Sr и Ba) реагируют
с водой комнатной температуры. Продукты этих реакций
то, что мы могли бы ожидать. Кальций, например, теряет два
электроны с образованием ионов Ca 2+ при взаимодействии с водой.
Кальций, например, теряет два
электроны с образованием ионов Ca 2+ при взаимодействии с водой.
Ca Ca 2+ + 2 e –
Эти электроны подхватываются молекулами воды с образованием H 2 газ и ионы ОН – .
2 + 2 OH сохраняется, дает следующий результат.Ca( с ) + 2 Н 2 О( л ) Ca 2+ ( водный раствор ) + 2 OH – ( водный раствор ) + H 2 ( г )
Хотя Mg не реагирует с водой при комнатной температуре, он будет реагировать с паром. Продукция этого реакция не может быть водной Mg 2+ и ионы OH – потому что вокруг нет жидкой воды, чтобы стабилизировать эти ионы. Продуктами этой реакции являются газ H 2 и магний. оксид, MgO.
Mg( с ) + H 2 O( г ) MgO( с ) + H 2 ( г )
Практическая задача 2: Магний реагирует с водородом с образованием соединения A , которое представляет собой белое твердое вещество при комнатной температуре. Он также реагирует с соляной кислоты с образованием газа B и водного раствор соединения C . Определить продукты из этих реакций и написать сбалансированные уравнения для каждой реакция.
Нажмите здесь, чтобы проверить свой ответ на практическое задание 2
Группа IIIA: Химия Алюминий
Элементы группы IIIA (B, Al, Ga, In и Tl) могут быть разделены на три класса.
- Бор — единственный элемент в этой группе, который не является металл. Он ведет себя как полуметалл или даже неметалл.
- Алюминий является третьим наиболее распространенным элементом в мире. земной коры. Он лишь немного менее реактивен, чем активные металлы.
- Остальные три элемента этой группы являются активными металлами. но их так мало, что они представляют ограниченный интерес. Галлий, индий и таллий вместе взятые менее 10 -10 % земной коры.
Таким образом, обсуждение металлов группы IIIA вращается вокруг химия алюминия, которую можно понять, предположив что металл реагирует с образованием соединений, в которых он имеет степень окисления +3.
2 Al( s ) + 3 Br 2 ( l ) Al 2 Br 6 ( s )
4 Al( s ) + 3 O 2 ( g ) 2 Ал 2 О 3 ( с )
16 Ал( с ) + 3 С 8 ( с ) 8 Al 2 S 3 ( s )
Алюминий реагирует с концентрированными кислотами с образованием Al 3+ ионы и газ H 2 .
2 Al( s ) + 6 H + ( aq ) 2 Al 3+ ( водный раствор ) + 3 H 2 ( г )
Он также реагирует с концентрированными основаниями с образованием H 2 газ и ион алюмината, Al(OH) 4 – , в алюминий находится в степени окисления +3.
2 Al( s ) + 2 OH – ( aq ) + 6 H 2 O ( L ) 2 AL (OH) 4 – ( AQ ) + 3 H 2 ( G )
6994444444. и свинец
Элементы группы IVA можно разделить на три класса:
- углерод, который является неметаллом;
- кремний и германий, которые являются полуметаллами; и
- олово и свинец, которые являются металлами.
Олово и свинец входят в число древнейшие известные металлы.
Олово и свинец гораздо менее реакционноспособны, чем любая из групп IA, Металлы IIA или IIIA. Согласно утверждению, что элементы стать более металлическим а значит более активно по мере того, как мы спускаемся по столбцу таблицы Менделеева, свинца должно быть больше реактивнее олова.
Свинец реагирует с воздухом с образованием тонкого покрытия из PbO и/или PbCO 3 , который защищает металл от дальнейшей реакции.
2 Pb( с ) + O 2 ( г ) 2 PbO( s )
PbO( s ) + CO 2 ( г ) PbCO 3 ( s )
В мелкодисперсном состоянии свинец пирофорен он воспламеняется в присутствии кислорода.
Олово не вступает в реакцию ни с воздухом, ни с водой при комнатной температуре температура. При нагревании до белого каления олово вступает в реакцию с воздухом.
образуют SnO 2 .
Sn( с ) + O 2 ( г ) SnO 2 ( s )
При высоких температурах он также реагирует с паром с образованием SnO 2 .
Sn( s ) + 2 H 2 O( г ) SnO 2 ( s ) + 2 H 2 ( г )
Олово и свинец менее активны, чем алюминий. Ни металл реагирует либо с разбавленной соляной кислотой, либо с разбавленной серной кислоты при комнатной температуре. Олово при нагревании реагирует либо с концентрированная соляная кислота или концентрированная серная кислота.
Sn( с ) + 2 H + ( aq ) Sn 2+ ( водный раствор ) + H 2 ( г )
Свинец медленно реагирует с соляной кислотой при комнатной температуре и концентрированной серной кислотой при температуре выше 200С.
Pb( s ) + 2 H + ( aq ) Pb 2+ ( aq ) + H 2 ( г )
Олово и свинец являются металлами основной группы, которые образуют соединения в более чем одна степень окисления.






 образуют SnO 2 .
образуют SnO 2 .