Периодическая система химических элементов. Большая российская энциклопедия
Научные законы, утверждения, уравнения
- Области знаний:
- Общие вопросы химии, Основные понятия и законы
- Другие наименования:
- Таблица Менделеева
Периоди́ческая систе́ма хими́ческих элеме́нтов, упорядоченное множество химических элементов и их естественная классификация. Является табличным представлением периодического закона, открытого Д. И. Менделеевым. Прообразом периодической системы химических элементов служит таблица «Опыт системы элементов, основанной на их атомном весе и химическом сходстве», составленная Менделеевым в 1869 г. По мере совершенствования этой таблицы Менделеев развил представления о периодах и группах элементов и о месте каждого элемента в системе. К 1871 г. в книгу «Основы химии» Менделеевым была включена «Естественная система элементов Д. Менделеева» – первая классическая короткая форма периодической системы химических элементов. Опираясь на неё, Менделеев выполнил впоследствии оправдавшийся прогноз существования и свойств неизвестных в то время элементов (Ga, Sc, Ge).
Опираясь на неё, Менделеев выполнил впоследствии оправдавшийся прогноз существования и свойств неизвестных в то время элементов (Ga, Sc, Ge).
Таблица, составленная Дмитрием Менделеевым. 1869. БРЭ. Т. 25.Физический смысл периодичности в свойствах элементов стал ясен после появления планетарной модели атома (Э. Резерфорд, 1911), и было показано (А. ван ден Брук и Г. Мозли, 1913–1914), что порядковый номер элемента в периодической системе химических элементов равен положительному заряду (Z) ядра атома. Теория периодической системы в основном создана Н. Бором (1913–1921) на базе квантовой модели атома. Бор разработал схему построения электронных конфигураций атомов по мере возрастания Z, опирающуюся на определённую последовательность заполнения электронами оболочек и подоболочек в атомах с ростом числа
Современная периодическая система химических элементов включает более ста химических элементов. Наиболее тяжёлые элементы получены ядерным синтезом. Порядок заполнения электронами уровней в атомах определяется правилами, совокупность которых называют «принципом построения»: заполнение атомных орбиталей (АО) происходит в порядке увеличения энергии орбиталей: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 6d и т.
Согласно (n+l)-правилу Клечковского, построение электронных конфигураций главным образом происходит в соответствии с последовательным увеличением суммы (n+l). При этом в пределах каждой такой суммы сначала заполняются подоболочки с бóльшими l и меньшими n, затем с меньшими l и бóльшими
Опубликовано свыше 500 вариантов периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем её структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Д. И. Менделеевым, усовершенствована в 1905 А. Вернером). В структуре периодической системы химических элементов выделяют периоды (горизонтальные ряды) и группы (вертикальные столбцы) элементов.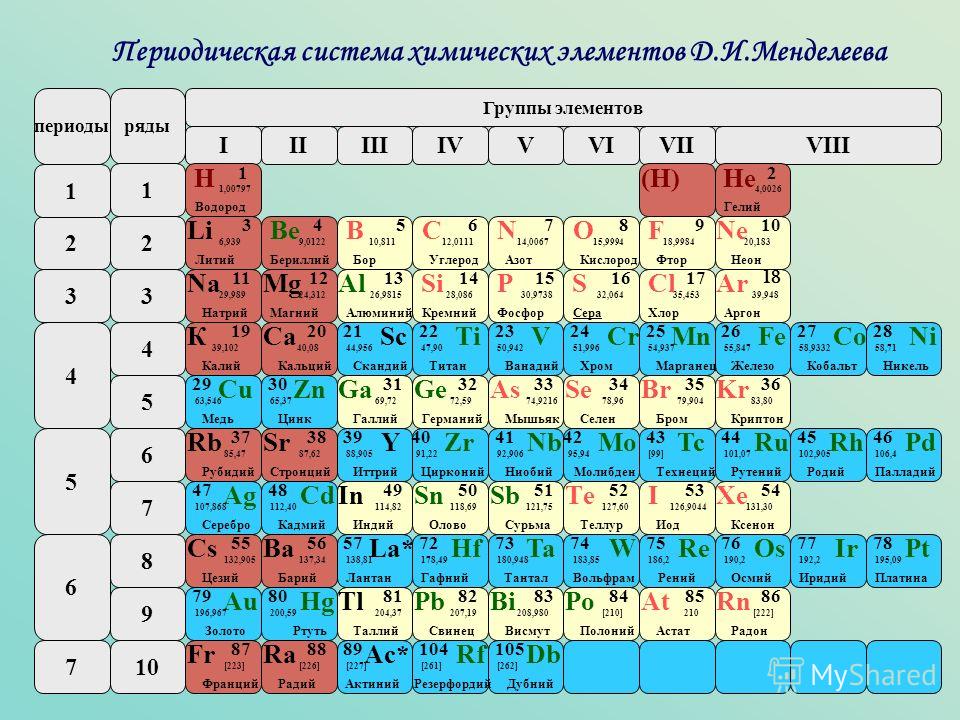
Короткая форма периодической системы химических элементов.
Архив БРЭ.Современная форма периодической системы химических элементов (в 1989 ИЮПАК рекомендована длинная форма) состоит из 7 периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма – из 8 групп. Число элементов в периодах, начиная со второго, попарно повторяется: 8, 8, 18, 18, 32, 32,… (первый период содержит два элемента). Номер группы элементов короткого варианта соответствует числу валентных электронов во внешней электронной оболочке атомов. В длиннопериодном варианте номер группы в бoльшей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам, их атомы характеризуются одинаковым строением внешних электронных оболочек. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы), щёлочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18).
Первый период содержит два элемента – Н и Не. Водород имеет некоторое сходство как со щелочными элементами, так и с галогенами. В связи с этим символ Н помещают либо в подгруппу Iа, либо в подгруппу VIIa короткого варианта, либо в обе одновременно.
Второй и третий периоды (Li – Ne; Na – Ar) содержат по 8 элементов, причём характер изменения химических свойств вертикальных аналогов во многом близок. Элементы первых трёх периодов относятся к главным подгруппам короткого варианта периодической системы химических элементов.
Элементы групп 1 и 2 длинной формы называются s-элементами, групп 13–18 – p-элементами, групп 3–12 – d-элементами; d-элементы (за исключением цинка, кадмия и ртути) называют также переходными элементами.
Четвёртый период (K – Kr) содержит 18 элементов. После K и Са (s-элементы) следует ряд из десяти (Sc – Zn) 3d
 Переходные элементы проявляют высшие степени окисления, в основном равные номеру группы короткого варианта периодической системы химических элементов (исключая Co, Ni и Cu). Элементы от Ga до Kr относятся к главным подгруппам (р-элементы).
Переходные элементы проявляют высшие степени окисления, в основном равные номеру группы короткого варианта периодической системы химических элементов (исключая Co, Ni и Cu). Элементы от Ga до Kr относятся к главным подгруппам (р-элементы).Пятый период (Rb – Xe) построен аналогично четвёртому; в нём также имеется «вставка» из десяти переходных 4d-элементов (Y – Cd). Особенности изменения свойств в этом периоде: в триаде Ru – Rh – Pd рутений проявляет максимальную степень окисления +8, родий +6, палладий +5; все элементы главных подгрупп, включая Хе, проявляют высшие степени окисления, равные номеру группы.
Шестой период (Сs – Rn) содержит 32 элемента. В него, помимо десяти 5d-элементов (La, Hf – Hg), входит семейство из четырнадцати 4f-элементов – лантаноидов (лантанидов, Ln). В степени окисления +3, +4 они являются химическими аналогами актиноидов, в степени окисления +2 – щёлочноземельных элементов. Лантаноиды размещены в группе 3 длинной формы, клетка La, и для удобства вынесены под таблицу.
Седьмой период, подобно шестому, содержит 32 элемента. Актиний – аналог лантана. После Ас следует семейство из четырнадцати 5f-элементов – актиноидов (актинидов, An) (Z= 90–103). В периодической системе химических элементов их размещают в клетке Ас и, подобно Ln, записывают отдельной строкой под таблицей. Этот приём предполагает наличие существенного химического сходства элементов двух f-семейств. Именно на этом основывалась «актинидная концепция» Г. Сиборга (1944), сыгравшая ведущую роль при разработке методов разделения продуктов деления урана и поиске новых элементов. Однако эта концепция справедлива лишь для трёх- и четырёхвалентных An. Актиноиды же проявляют степени окисления от +2 до +7 (последняя характерна для Np, Pu, Am) и +8 (для плутония). Для наиболее тяжёлых An характерна стабилизация низших степеней окисления (+2 или даже +1 для Md).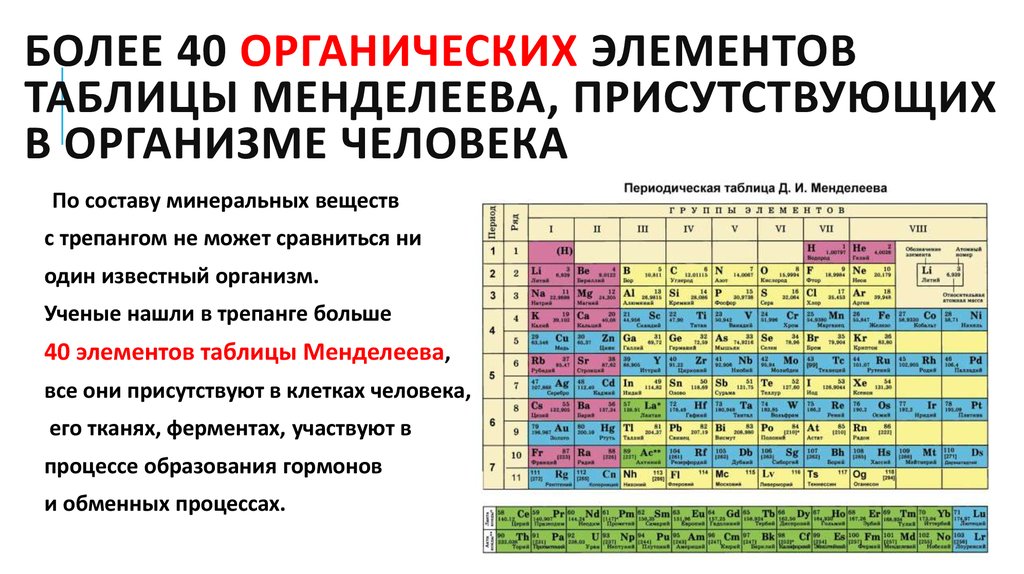
Экспериментальные оценки химии элементов с Z=104 (резерфордий) и Z=105 (дубний) позволили заключить, что они являются аналогами соответственно Hf и Та, т. е. 6d-элементами (должны располагаться в IVб и Vб подгруппах короткой формы). Химическая идентификация элементов с Z=
Памятник-таблица «Периодическая система элементов Д. И. Менделеева». Авторы: Владимир Фролов, Давид Кричевский.Периодическая система химических элементов является важным звеном эволюции атомно-молекулярного учения, способствует уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов.
Дата публикации: 1 августа 2022 г. в 14:10 (GMT+3)
Московий и оганессон официально включили в таблицу Менделеева
28 ноября собрание Международного союза по теоретической и прикладной химии (IUPAC) утвердило официальные названия 113, 115, 117 и 118 элементов таблицы Менделеева. За ними закрепили наименования, предложенные в июне 2016 года — нихоний (Nh), московий (Mc), теннессин (Ts) и оганессон (Og). Об этом сообщает пресс-релиз союза.
За ними закрепили наименования, предложенные в июне 2016 года — нихоний (Nh), московий (Mc), теннессин (Ts) и оганессон (Og). Об этом сообщает пресс-релиз союза.
Для внесения элемента в таблицу Менделеева необходимо пройти через несколько формальных этапов. Среди них доказательство получения элементов в чистом виде, определение приоритета в открытии, определение названия для элемента его первооткрывателями и признание названия международным сообществом.
IUPAC признал синтез элементов 113,115, 117 и 118 и определил приоритет в их открытии в январе 2016 года. Согласно решению комиссии, приоритет в выборе названия для 113 элемента получил институт RIKEN, а 115, 117 и 118 элементы были открыты совместно российско-американской группой из Объединенного института ядерных исследований в Дубне (ОИЯИ), Ливерморской национальной лаборатории в Калифорнии (LLNL) и Национальной лаборатории Оак-Ридж в Теннесси (ORNL).
До июня 2016 года научные группы предложили названия и IUPAC порекомендовал их для включения в таблицу Менделеева. На протяжении пяти месяцев союз принимал комментарии и апелляции к названиям. Среди них комиссия выделила касавшиеся краткого сокращения для теннессина — Ts. Традиционно это обозначение используется в органической химии для тозильных групп (остатков толуолсульфокислоты). Эксперты отметили, что аналогичный вопрос возникал при наименовании коперниция (112 элемент, Cn) — первооткрыватели предлагали для него аббревиатуру Cp, также «занятую» органиками. Тогда апелляция была принята. Однако для теннессина двухбуквенное обозначение осталось неизменным — комиссия отметила, что обозначения для актиния (Ac) и празеодима (Pr) тоже «заняты» органиками (ацетил, пропил), а контекст использования названия тенессина не позволит спутать его с другими вариантами прочтения.
На протяжении пяти месяцев союз принимал комментарии и апелляции к названиям. Среди них комиссия выделила касавшиеся краткого сокращения для теннессина — Ts. Традиционно это обозначение используется в органической химии для тозильных групп (остатков толуолсульфокислоты). Эксперты отметили, что аналогичный вопрос возникал при наименовании коперниция (112 элемент, Cn) — первооткрыватели предлагали для него аббревиатуру Cp, также «занятую» органиками. Тогда апелляция была принята. Однако для теннессина двухбуквенное обозначение осталось неизменным — комиссия отметила, что обозначения для актиния (Ac) и празеодима (Pr) тоже «заняты» органиками (ацетил, пропил), а контекст использования названия тенессина не позволит спутать его с другими вариантами прочтения.
Интересно, что оганессон стал вторым элементом таблицы Менделеева, прижизненно названным в честь ученого — Юрия Цолаковича Оганесяна, научного руководителя лаборатории ядерных реакций ОИЯИ и соавтора открытий 104-107 элементов периодической системы. Московий получил свое название в честь Московской области, где располагается ОИЯИ. Нихоний стал первым из элементов, название которого связано с Японией.
Московий получил свое название в честь Московской области, где располагается ОИЯИ. Нихоний стал первым из элементов, название которого связано с Японией.
Необычные окончания в названиях оганессона и тенессина связаны с их положением в таблице Менделеева. Оганессон относится к благородным газам: гелию, неону, аргону, криптону, ксенону и радону. Теннессин — к галогенам: фтору, хлору, брому, иоду и астату, чьи англоязычные названия оканчиваются на -ine (fluorine, chlorine, bromine, iodine, astatine). Возможно, следуя традиции, более правильным русскоязычным названием для элемента могло бы быть «теннесс».
Владимир Королёв
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Что означает номер группы в периодической таблице элементов?
Химия
Наука
- Анатомия и физиология
- астрономия
- Астрофизика
- Биология
- Химия
- наука о планете Земля
- Наука об окружающей среде
- Органическая химия
- Физика
Математика
- Алгебра
- Исчисление
- Геометрия
- Преалгебра
- Предварительный расчет
- Статистика
- Тригонометрия
Гуманитарные науки
- Английская грамматика
- История США
- Всемирная история
- Сократическая мета
- Избранные ответы
.
 .. и не только
.. и не толькоТемы
Видео с вопросами: Вспомним значение группы в периодической таблице
Стенограмма видео
Что из следующего лучше всего описывает группу в таблице Менделеева? (A) все неметаллы, (B) набор элементов в одной строке, (C) набор элементов в одном столбце, (D) набор элементов в одной диагонали или (E) все элементы с определенное число нейтронов в их ядрах.
Периодическая таблица представляет собой диаграмму, на которой показаны все 118 известных элементов, организованных в определенном порядке. Расположение каждого элемента в периодической таблице дает много полезной информации об этом элементе. Чтобы ответить на этот вопрос, нам нужно определить, какое из предоставленных утверждений лучше всего описывает группу в периодической таблице. Группа может быть определена как совокупность элементов со схожими химическими или электронными свойствами. Атомы элементов, которые находятся в одной и той же группе, обычно имеют одинаковое количество валентных или самых удаленных электронов. Давайте увеличим часть периодической таблицы и посмотрим, сможем ли мы определить взаимосвязь между положением некоторых элементов и количеством валентных электронов, которые имеет атом каждого элемента.
Чтобы ответить на этот вопрос, нам нужно определить, какое из предоставленных утверждений лучше всего описывает группу в периодической таблице. Группа может быть определена как совокупность элементов со схожими химическими или электронными свойствами. Атомы элементов, которые находятся в одной и той же группе, обычно имеют одинаковое количество валентных или самых удаленных электронов. Давайте увеличим часть периодической таблицы и посмотрим, сможем ли мы определить взаимосвязь между положением некоторых элементов и количеством валентных электронов, которые имеет атом каждого элемента.
Чтобы помочь нам найти взаимосвязь, мы можем нарисовать боровскую модель атома для каждого элемента. В модели Бора каждый круг вокруг ядра представляет собой электронную оболочку. Каждая электронная оболочка может содержать определенное количество электронов. Первая электронная оболочка может содержать максимум два электрона. Вторая электронная оболочка может содержать максимум восемь электронов.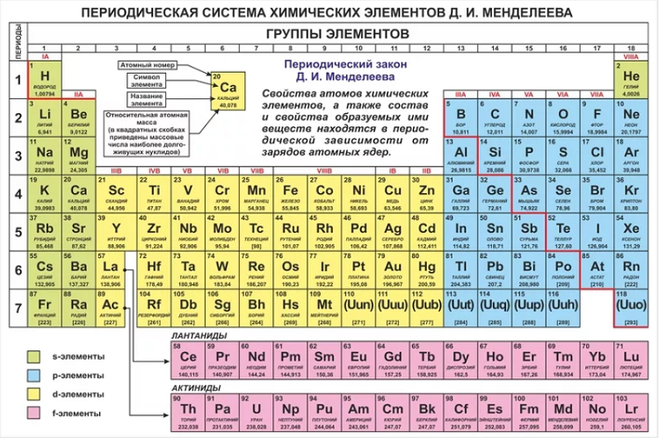 А третья электронная оболочка может содержать максимум 18 электронов. Однако 10 из этих электронов добавляются к этой электронной оболочке только тогда, когда атомы становятся больше. Поэтому мы иногда говорим, что третья электронная оболочка может содержать максимум восемь электронов.
А третья электронная оболочка может содержать максимум 18 электронов. Однако 10 из этих электронов добавляются к этой электронной оболочке только тогда, когда атомы становятся больше. Поэтому мы иногда говорим, что третья электронная оболочка может содержать максимум восемь электронов.
На диаграмме электроны представлены синими точками, а электроны, находящиеся на самой внешней электронной оболочке, являются валентными электронами. Чтобы нарисовать боровскую модель атома из этих шести элементов, нам нужно знать, сколько электронов имеет каждый атом. Атомный номер, написанный над каждым химическим символом, указывает количество протонов во всех атомах и ионах этого элемента. Он также указывает количество электронов в нейтральном атоме. Имея это в виду, построим модель Бора для атома кислорода, имеющего восемь электронов. Первые два электрона займут самую внутреннюю электронную оболочку, а оставшиеся шесть электронов займут вторую оболочку. Атом серы имеет 16 электронов. Два электрона занимают первую электронную оболочку, восемь электронов занимают вторую электронную оболочку и шесть электронов занимают третью электронную оболочку.
