Четыре новых элемента таблицы Менделеева получили официальные названия / Хабр
Эти элементы дополнили седьмой период таблицы
Источник изображения: Wikimedia Commons
Сегодня стали известны официальные названия четырех новых химических элементов, открытых ранее. Названия присвоил Международный союз теоретической и прикладной химии (ИЮПАК). Речь идет о химических элементах 115, 117, 118 и 113. Их открытие было официально подтверждено Международным союзом теоретической и прикладной химии в декабре прошлого года.
115 и 117 элементы таблицы были открыты Российским Объединенным институтом ядерных исследований (ОИЯИ), Ливерморской национальной лабораторией (США) и Окриджской национальной лабораторией (США). Первооткрывателями 118 элемента названы ОИЯИ и Ливерморская национальная лаборатория. 113 элемент открыли специалисты из японского института RIKEN (хотя на его открытие претендовала та же международная исследовательская группа, которая открыла 115 и 117 элементы).
Что касается названий, то 113 элемент получил название нихоний (Nihonium, Nh), 115 — московий (Moscovium, Mc), 117 — теннесин (Tennessine, Ts), 118 — оганессоном (Oganesson, Og).
Почему выбраны именно такие наименования? Дело в том, что на японском языке Nihon означает «Страна восходящего солнца». А поскольку элемент 113 был открыт японскими учеными, то он и получил такое название. Это первый химический элемент, который был синтезирован и обнаружен в азиатской стране. Московий и теннесин получили названия в соответствии с географическим положением мест, где эти элементы были впервые синтезированы. Ну а Оганессон назвали в честь Юрия Оганесяна — ученого из России, который ведет активные исследования в сфере синтеза новых элементов. Сразу после открытия три из четырех элементов получили другие названия: японий, флеровий и ливерморий.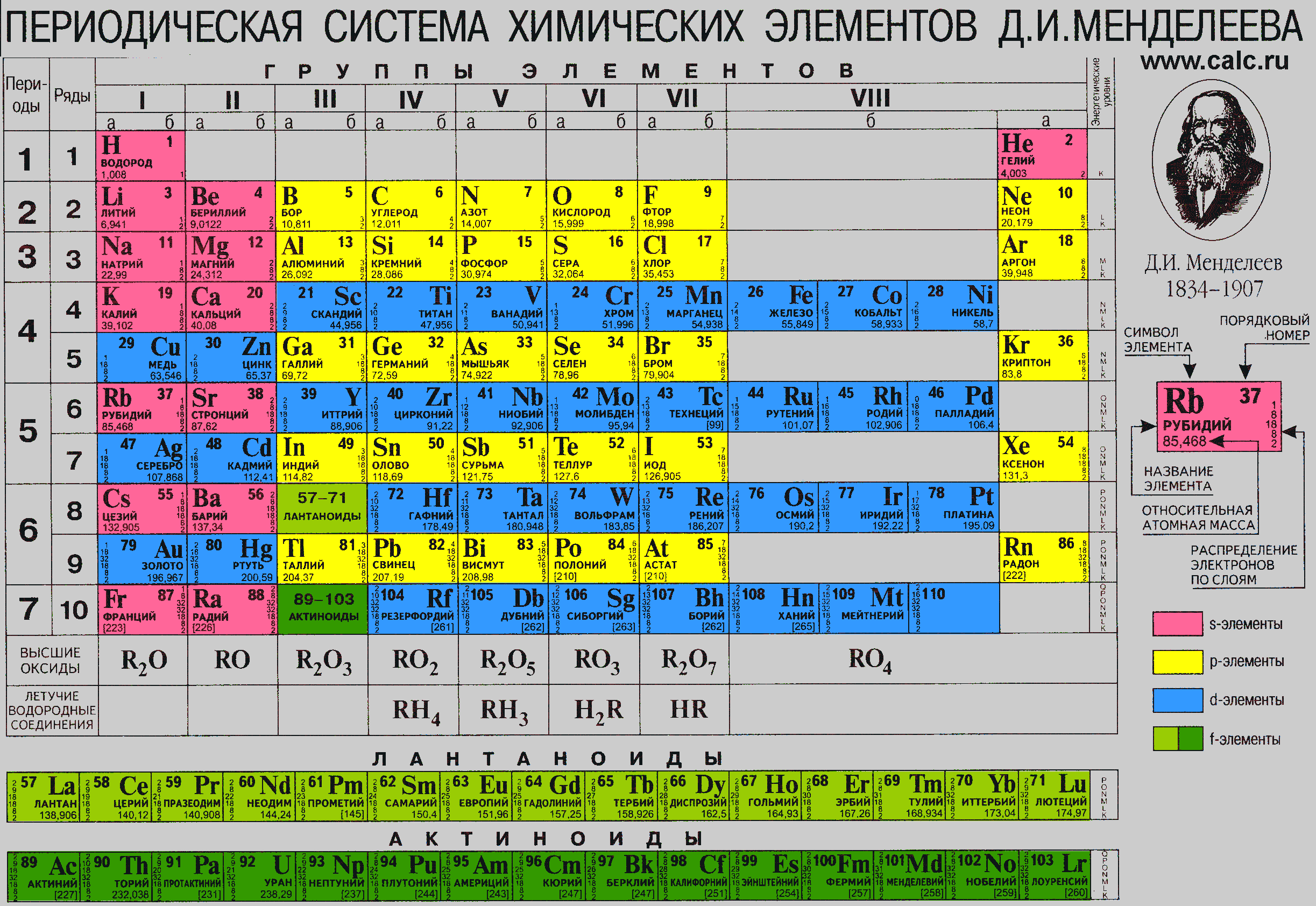
«Приятно видеть, что различные места, названия и имена (страна, штат, город и ученый), имеющие отношения к новым элементам, были отражены в этих четырех наименованиях. Хотя выбор может выглядеть несколько эгоистичным в глазах некоторых людей, все наименования полностью соответствуют правилам ЮИПАК», — прокомментировал присвоение названий элементам Ян Редейк (Jan Reedijk), представитель ИЮПАК. Он также добавил, что названия уже одобрены руководством, но в таблицу элементов «новички» с присвоенными названиями попадут в ноябре этого года. Сейчас в таблице до сих пор значатся предварительные наименования элементов.
Уже сейчас многие научные организации со всего мира работают над синтезированием элементов из 8 периода таблицы. Также ученые планируют в скором времени закрепить наименование «коперниций» (112-й элемент, впервые синтезирован 9 февраля 1996 года в Институте тяжёлых ионов) и более тяжелых элементов.
Последний раз таблица химических элементов пополнялась в 2011 году, когда в нее добавили элементы 114 и 116.
Номер периода в периодической системе менделеева показывает. Периодическая система Д
Состоит из вертикальных рядов (групп) и горизонтальных рядов (периодов). Для лучшего понимания принципов объединения элементов в группы и периоды, рассмотрим нескольких элементов, скажем, первой, четвертой и седьмой групп.
Из приведенных выше электронных конфигураций видно, что внешние (самые высокие по энергии) электронные оболочки атомов одной группы заполнены электронами одинаково. К одной группе принадлежат элементы, расположенные в одном вертикальном столбце таблицы. Элементы IVA группы периодической системы имеет два электрона на s-орбитали и два электрона на р-орбиталях. Конфигурация внешней электронной оболочки атомов фтора F, хлора Сl и брома Вг также одинакова (два s- и пять р-электронов). И эти элементы относятся к одной группе (VIIA). Атомы элементов одной группы имеют одинаковое строение внешней электронной оболочки. Именно поэтому такие элементы имеют сходные химические свойства.
Номер группы периодической системы соответствует числу электронов на внешней электронной оболочке атомов элементов этой группы. Номер периода (горизонтального ряда периодической таблицы) совпадает с номером высшей занятой электронной орбитали. Например, натрий и хлор — оба элементы 3-го периода и у обоих типов атомов высший, заполненный электронами,уровень – третий.
Строго говоря, число электронов на внешней электронной оболочке определяет номер группы только для так называемых непереходных элементов, расположенных в группах с буквенным индексом А.
Электронное строение атомов определяет химические и физические свойства элементов. А т.к электронное строение атомов повторяется через период, то и свойства элементов также повторяются периодически.
Периодический закон Д. И. Менделеева имеет следующую формулировку: «свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов» .
Размеры атомов
Нам следует остановиться еще на двух видах информации, получаемой из периодической системы. Первый из них — вопрос о размере (радиусе) атомов. Если двигаться вниз в пределах данной группы, переход к каждому следующему элементу означает заполнение электронами следующего, все более высокого уровня. В группе IA внешний электрон атома натрия находится на Зs-орбитали, калия — на 4s-орбитали, рубидия – 5s-орбитали и т. д. Поскольку 4s-орбиталь больше по размеру, чем Зs-орбиталь, атом калия имеет большие размеры, чем атом натрия. По этой же причине
При движении направо по периоду атомные массы возрастают, но размеры атомов, как правило, уменьшаются.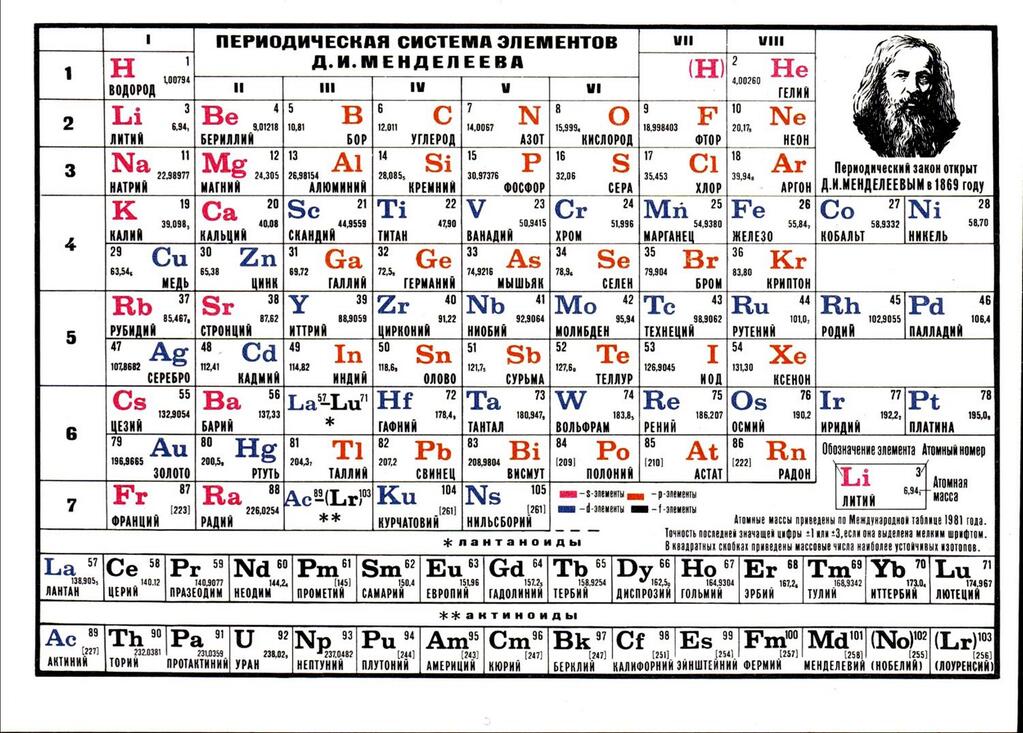 Во 2-м периоде, например, атом неона Ne имеет меньший размер, чем атом фтора, который, в свою очередь, меньше атома кислорода.
Во 2-м периоде, например, атом неона Ne имеет меньший размер, чем атом фтора, который, в свою очередь, меньше атома кислорода.
Электроотрицательность
Другая тенденция, выявляемая с помощью периодической таблицы,- закономерное изменение злектроотрицательности элементов, т. е. относительной способности атомов притягивать электроны, образующие связи с другими атомами. Например, атомы инертных газов не склонны приобретать или терять электроны, тогда как атомы металлов легко отдают электроны, а атомы неметаллов охотно их принимают.
Фтор F, расположенный в правом верхнем углу периодической системы, – наиболее электроотрицательный элемент, а франций Fr, находящийся в левом нижнем углу, наименее электроотрицателен. Изменение электроотрицательности также показано стрелками на рисунке.
Первая и широко известная шкала относительных атомных электроотрицательностей Полинга охватывает значения от 0,7 для атомов франция до 4,0 для атомов фтора.
Электронное строение инертных газов
Элементы последней группы периодической системы называются инертными (благородными) газами. В атомах этих элементов, кроме гелия Не, на внешней электронной оболочке имеется восемь электронов. Инертные газы не вступают в химические реакции и не образуют никаких соединений с другими элементами (кроме очень немногих исключений). Это связано с тем, что конфигурация из восьми электронов на внешней электронной оболочке чрезвычайно стабильна.
Атомы других элементов образуют химические связи таким образом, чтобы на их внешней оболочке оказалось восемь электронов.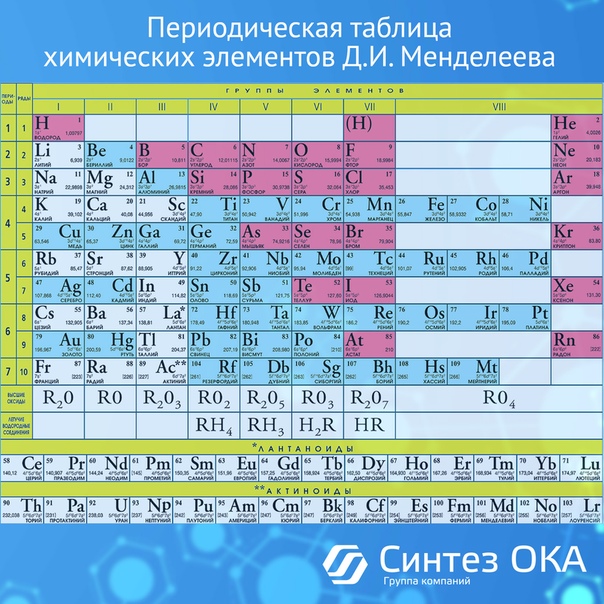 Это положение часто называют правилом октета .
Это положение часто называют правилом октета .
Группа периодической системы химических элементов последовательность атомов по возрастанию заряда ядра, обладающих однотипным электронным строением. Номер группы определяется количеством электронов на внешней оболочке атома (валентных электронов) … Википедия
К четвёртому периоду периодической системы относятся элементы четвёртой строки (или четвёртого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических)… … Википедия
К первому периоду периодической системы относятся элементы первой строки (или первого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
Ко второму периоду периодической системы относятся элементы второй строки (или второго периода) периодической системы химических элементов.
К пятому периоду периодической системы относятся элементы пятой строки (или пятого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
К третьему периоду периодической системы относятся элементы третьей строки (или третьего периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов … Википедия
К седьмому периоду периодической системы относятся элементы седьмой строки (или седьмого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов … Википедия
К шестому периоду периодической системы относятся элементы шестой строки (или шестого периода) периодической системы химических элементов. Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
Строение периодической таблицы основано на строках для иллюстрации повторяющихся (периодических) трендов в… … Википедия
Короткая форма таблицы Менделеева основана на параллелизме степеней окисления элементов главных и побочных подгрупп: например, максимальная степень окисления ванадия равна +5, как у фосфора и мышьяка, максимальная степень окисления хрома равна +6 … Википедия
Сюда перенаправляется запрос «Группировка». На эту тему нужна отдельная статья … Википедия
Если таблица Менделеева кажется вам сложной для понимания, вы не одиноки! Хотя бывает непросто понять ее принципы, умение работать с ней поможет при изучении естественных наук. Для начала изучите структуру таблицы и то, какую информацию можно узнать из нее о каждом химическом элементе. Затем можно приступить к изучению свойств каждого элемента. И наконец, с помощью таблицы Менделеева можно определить число нейтронов в атоме того или иного химического элемента.
Шаги
Часть 1
Структура таблицыКак видно, каждый следующий элемент содержит на один протон больше, чем предшествующий ему элемент. Это очевидно, если посмотреть на атомные номера. Атомные номера возрастают на один при движении слева направо. Поскольку элементы расположены по группам, некоторые ячейки таблицы остаются пустыми.
- Например, первая строка таблицы содержит водород, который имеет атомный номер 1, и гелий с атомным номером 2. Однако они расположены на противоположных краях, так как принадлежат к разным группам.
Узнайте о группах, которые включают в себя элементы со схожими физическими и химическими свойствами.
 Элементы каждой группы располагаются в соответствующей вертикальной колонке. Как правило, они обозначаются одним цветом, что помогает определить элементы со схожими физическими и химическими свойствами и предсказать их поведение. Все элементы той или иной группы имеют одинаковое число электронов на внешней оболочке.
Элементы каждой группы располагаются в соответствующей вертикальной колонке. Как правило, они обозначаются одним цветом, что помогает определить элементы со схожими физическими и химическими свойствами и предсказать их поведение. Все элементы той или иной группы имеют одинаковое число электронов на внешней оболочке.- Водород можно отнести как к группе щелочных металлов, так и к группе галогенов. В некоторых таблицах его указывают в обеих группах.
- В большинстве случаев группы пронумерованы от 1 до 18, и номера ставятся вверху или внизу таблицы. Номера могут быть указаны римскими (например, IA) или арабскими (например,1A или 1) цифрами.
- При движении вдоль колонки сверху вниз говорят, что вы «просматриваете группу».
Узнайте, почему в таблице присутствуют пустые ячейки. Элементы упорядочены не только в соответствии с их атомным номером, но и по группам (элементы одной группы обладают схожими физическими и химическими свойствами).
 Благодаря этому можно легче понять, как ведет себя тот или иной элемент. Однако с ростом атомного номера не всегда находятся элементы, которые попадают в соответствующую группу, поэтому в таблице встречаются пустые ячейки.
Благодаря этому можно легче понять, как ведет себя тот или иной элемент. Однако с ростом атомного номера не всегда находятся элементы, которые попадают в соответствующую группу, поэтому в таблице встречаются пустые ячейки.- Например, первые 3 строки имеют пустые ячейки, поскольку переходные металлы встречаются лишь с атомного номера 21.
- Элементы с атомными номерами с 57 по 102 относятся к редкоземельным элементам, и обычно их выносят в отдельную подгруппу в нижнем правом углу таблицы.
Каждая строка таблицы представляет собой период. Все элементы одного периода имеют одинаковое число атомных орбиталей, на которых расположены электроны в атомах. Количество орбиталей соответствует номеру периода. Таблица содержит 7 строк, то есть 7 периодов.
- Например, атомы элементов первого периода имеют одну орбиталь, а атомы элементов седьмого периода – 7 орбиталей.
- Как правило, периоды обозначаются цифрами от 1 до 7 слева таблицы.

- При движении вдоль строки слева направо говорят, что вы «просматриваете период».
Научитесь различать металлы, металлоиды и неметаллы. Вы лучше будете понимать свойства того или иного элемента, если сможете определить, к какому типу он относится. Для удобства в большинстве таблиц металлы, металлоиды и неметаллы обозначаются разными цветами. Металлы находятся в левой, а неметаллы – в правой части таблицы. Металлоиды расположены между ними.
Часть 2
Обозначения элементовКаждый элемент обозначается одной или двумя латинскими буквами. Как правило, символ элемента приведен крупными буквами в центре соответствующей ячейки. Символ представляет собой сокращенное название элемента, которое совпадает в большинстве языков. При проведении экспериментов и работе с химическими уравнениями обычно используются символы элементов, поэтому полезно помнить их.
- Обычно символы элементов являются сокращением их латинского названия, хотя для некоторых, особенно недавно открытых элементов, они получены из общепринятого названия.
 К примеру, гелий обозначается символом He, что близко к общепринятому названию в большинстве языков. В то же время железо обозначается как Fe, что является сокращением его латинского названия.
К примеру, гелий обозначается символом He, что близко к общепринятому названию в большинстве языков. В то же время железо обозначается как Fe, что является сокращением его латинского названия.
- Обычно символы элементов являются сокращением их латинского названия, хотя для некоторых, особенно недавно открытых элементов, они получены из общепринятого названия.
Обратите внимание на полное название элемента, если оно приведено в таблице. Это «имя» элемента используется в обычных текстах. Например, «гелий» и «углерод» являются названиями элементов. Обычно, хотя и не всегда, полные названия элементов указываются под их химическим символом.
- Иногда в таблице не указываются названия элементов и приводятся лишь их химические символы.
Найдите атомный номер. Обычно атомный номер элемента расположен вверху соответствующей ячейки, посередине или в углу. Он может также находиться под символом или названием элемента. Элементы имеют атомные номера от 1 до 118.
- Атомный номер всегда является целым числом.
Помните о том, что атомный номер соответствует числу протонов в атоме.
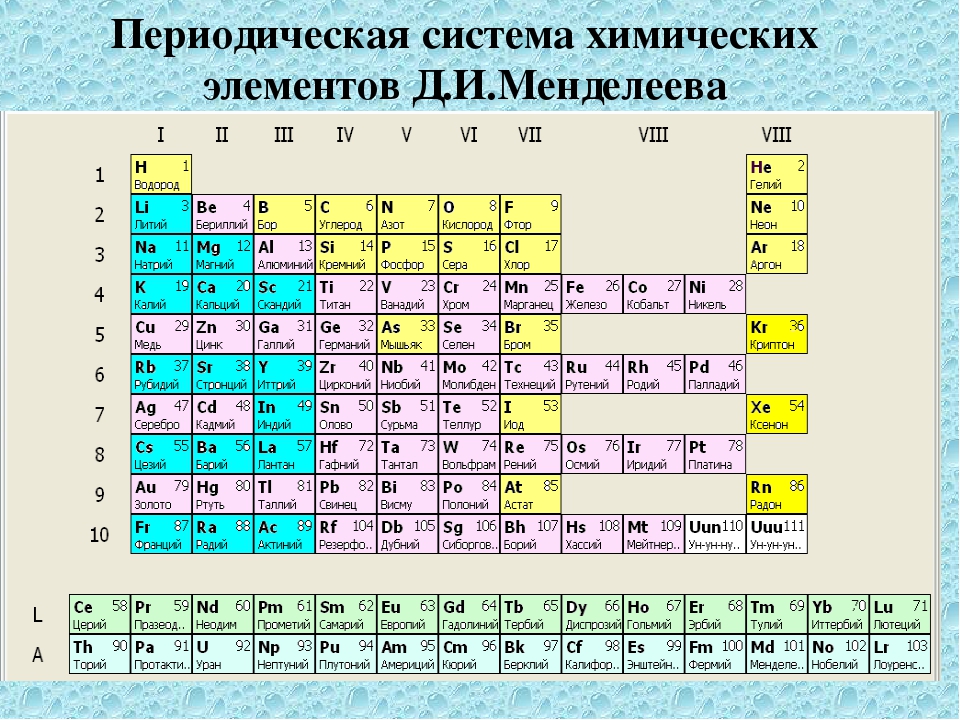 Все атомы того или иного элемента содержат одинаковое количество протонов. В отличие от электронов, количество протонов в атомах элемента остается постоянным. В противном случае получился бы другой химический элемент!
Все атомы того или иного элемента содержат одинаковое количество протонов. В отличие от электронов, количество протонов в атомах элемента остается постоянным. В противном случае получился бы другой химический элемент!- По атомному номеру элемента можно также определить количество электронов и нейтронов в атоме.
Обычно количество электронов равно числу протонов. Исключением является тот случай, когда атом ионизирован. Протоны имеют положительный, а электроны – отрицательный заряд. Поскольку атомы обычно нейтральны, они содержат одинаковое количество электронов и протонов. Тем не менее, атом может захватывать электроны или терять их, и в этом случае он ионизируется.
- Ионы имеют электрический заряд. Если в ионе больше протонов, то он обладает положительным зарядом, и в этом случае после символа элемента ставится знак «плюс». Если ион содержит больше электронов, он имеет отрицательный заряд, что обозначается знаком «минус».
- Знаки «плюс» и «минус» не ставятся, если атом не является ионом.
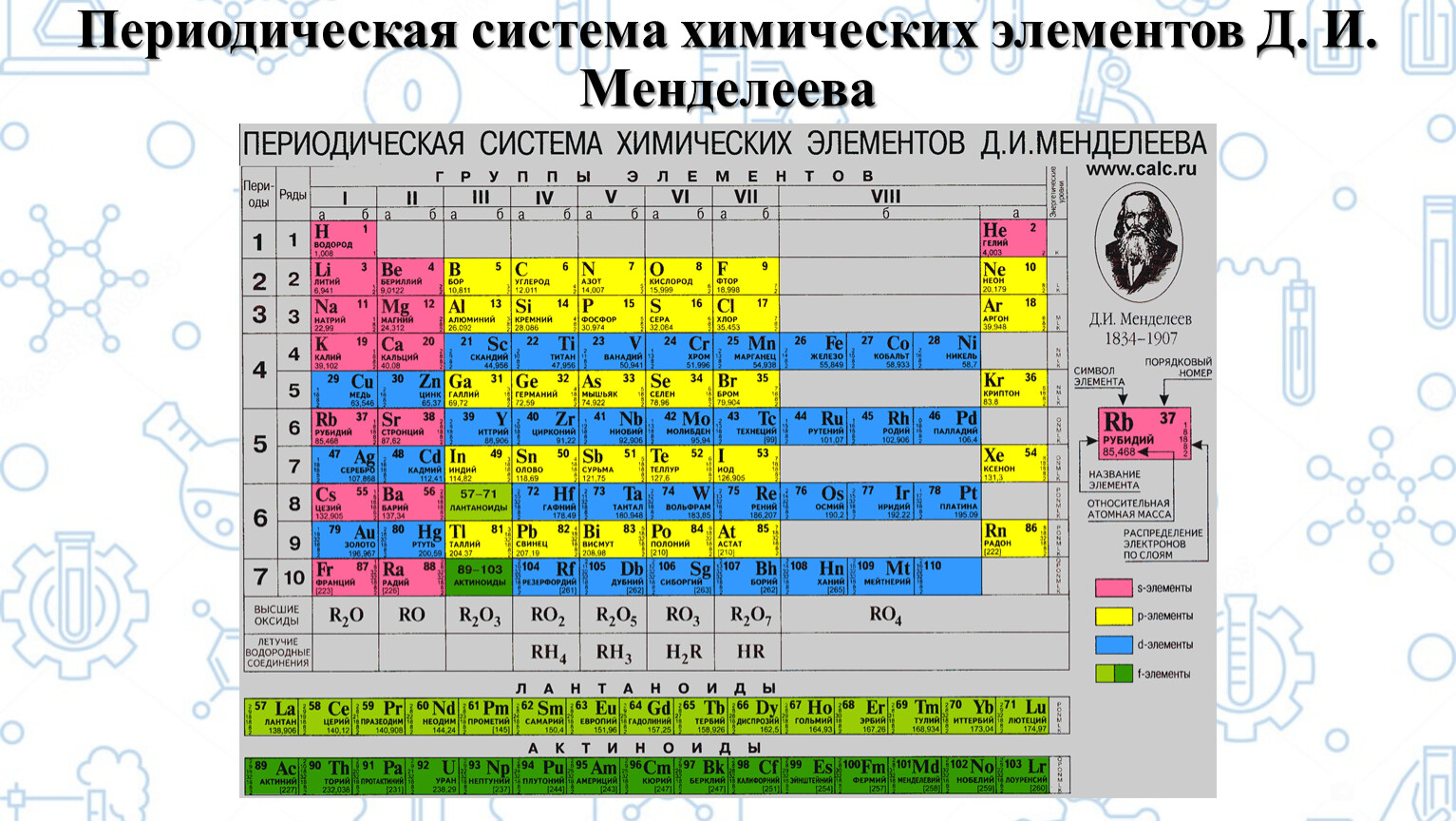
1. Номер периода в Периодической системе Д. И. Менделеева соответствует
1) числу энергетических уровней в атоме
2) числу валентных электронов в атоме
3) числу неспаренных электронов в атоме
4) общему числу электронов в атоме2. Число электронов в электронной оболочке атома определяется
1) числом протонов
2) числом нейтронов
3) числом энергетических уровней
4) величиной относительной атомной массы3. В ряду химических элементов кремний → фосфор → сера уменьшается
1) способность атома принимать электроны
2) высшая степень окисления
3) низшая степень окисления
4) радиус атома4. У элементов А групп с увеличением атомного номера уменьшается
1) атомный радиус
2) заряд ядра атома
3) число валентных электронов в атомах
4) электроотрицательность5. В главных подгруппах Периодической системы Д. И. Менделеева снизу вверх основные свойства гидроксидов металлов
1) увеличиваются
2) уменьшаются
3) не изменяются
4) изменяются периодически6.
 Среди элементов IVA группы максимальный радиус атома имеет
Среди элементов IVA группы максимальный радиус атома имеет 1) германий
2) углерод
3) олово
4) кремний7. Наиболее выражены металлические свойства у элемента
1) Na
2) Mg
3) К
4) Са8. Менее выраженные неметаллические свойства, чем кремний, имеет элемент
1) углерод
2) германий
3) фосфор
4) азот9. Наиболее сильное основание соответствует элементу
Таблица Менделеева, или периодическая система химических элементов, начинается в левом верхнем углу и заканчивается в конце последней строки таблицы (в нижнем правом углу). Элементы в таблице расположены слева направо в порядке возрастания их атомного номера. Атомный номер показывает, сколько протонов содержится в одном атоме. Кроме того, с увеличением атомного номера возрастает и атомная масса. Таким образом, по расположению того или иного элемента в таблице Менделеева можно определить его атомную массу.
Элементы в таблице расположены слева направо в порядке возрастания их атомного номера. Атомный номер показывает, сколько протонов содержится в одном атоме. Кроме того, с увеличением атомного номера возрастает и атомная масса. Таким образом, по расположению того или иного элемента в таблице Менделеева можно определить его атомную массу.
Элементы: ядовитый полуметалл – сурьма
Первые производства сурьмы появились на древнем Востоке 5 тысяч лет назад. Сурьмяная бронза (сплав меди и олова с добавлением сурьмы) использовалась в период Вавилонского царства во втором тысячелетии до н.э. Исторически сложилось так, что в русской химической терминологии у этого элемента три названия. Химический элемент называется «сурьма», в формулах произносится «стибиум», а соединения сурьмы с металлами называются антимонидами». В 1789 г. Лавуазье включил сурьму в список простых веществ, дав ей название antimoine от лат. «antimonium». Оно и сейчас остается французским названием элемента № 51. Другое латинское название элемента, «stibium», встречается в сочинениях Плиния Старшего в первом веке н. э. и стало международным. Русское слово «сурьма» родом из турецкого языка. Так и сейчас на Востоке называется порошок для чернения бровей. По другим данным, «сурьма» — от персидского «сурме» — металл. Итак, сурьма (символ — Sb) имеет атомный номер 51 в Таблице Менделеева с атомной массой 121, 760 а.е.м. и относится к группе полуметаллов.
«antimonium». Оно и сейчас остается французским названием элемента № 51. Другое латинское название элемента, «stibium», встречается в сочинениях Плиния Старшего в первом веке н. э. и стало международным. Русское слово «сурьма» родом из турецкого языка. Так и сейчас на Востоке называется порошок для чернения бровей. По другим данным, «сурьма» — от персидского «сурме» — металл. Итак, сурьма (символ — Sb) имеет атомный номер 51 в Таблице Менделеева с атомной массой 121, 760 а.е.м. и относится к группе полуметаллов.
Сурьма в Таблице Менделеева.
Существуют четыре аллотропные разновидности сурьмы: кристаллическая, взрывчатая, чёрная и жёлтая. Наиболее устойчивая, и поэтому самая распространённая – кристаллическая сурьма. Взрывчатая – взрывается при любом соприкосновении. Чёрная и жёлтая – неустойчивы и при пониженных температурах переходят в кристаллическую.
Кристаллическая сурьма по внешнему виду напоминает металл серебристо-белого цвета с синеватым оттенком, довольно хрупкий (легко истирается в порошок).
Кристаллическая сурьма.
Cурьма токсична и относится к ядовитым веществам. Пыль и пары этого элемента вызывают носовое кровотечение, сурьмяную лихорадку. Французский термин сурьмы «antimoine»
переводится буквально: «против монахов». Такое название, возможно, возникло из легенды 15 века, в которой настоятель одного мужского монастыря заметил, что свиньи быстро жиреют, потребляя сурьму. Решив, что этот рецепт набора веса сгодится и для людей, он добавил в кашу истощённой братии монастыря сурьму. На следующий день все кто ел – были мертвы. Эту легенду подробно описал Ярослав Гашек в рассказе «Камень жизни» в 1910 году. Отсюда происходит и русское название главного рудного минерала – антимонит с формулой Sb2S3, где содержание сурьмы составляет 72 %. Антимонитовые руды являются основным источником для получения сурьмы и её соединений.
Антимонит Sb2S3, кристаллы до 5 см. Месторождение Кадамджай, Киргизия.
Месторождение Кадамджай, Киргизия.
Мировая добыча сурьмы по итогам 2015 года составила около 145 тысяч тонн. Основные объемы добычи приходятся на Китай (47%), Россию (17%), Боливию (15%) и Таджикистан (12%).
Мировая добыча сурьмы, 2015 г.
В Китае основная добыча ведется в провинции Хунань, где расположено крупнейшее в мире сурьмяное месторождение Сикуаньшань. В России главный регион по добыче антимонитовых руд – Республика Саха (Якутия), где расположены крупные месторождения Сарылах и Сентачан.
Сурьма применяется при производстве диодов и инфракрасных детекторов. Является компонентом свинцовых сплавов, увеличивающим их твёрдость и механическую прочность.
Периодическая система химических элементов (таблица Менделеева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Открытие, сделанное Русским химиком Менделеевым, сыграло (безусловно) наиболее важную роль в развитии науки, а именно в развитии атомно-молекулярного учения. Это открытие позволило получить наиболее понятные, и простые в изучении, представления о простых и сложных химических соединениях. Только благодаря таблице мы имеем те понятия об элементах, которыми пользуемся в современном мире. В ХХ веке проявилась прогнозирующая роль периодической системы при оценке химических свойств, трансурановых элементов, показанная еще создателем таблицы.
Это открытие позволило получить наиболее понятные, и простые в изучении, представления о простых и сложных химических соединениях. Только благодаря таблице мы имеем те понятия об элементах, которыми пользуемся в современном мире. В ХХ веке проявилась прогнозирующая роль периодической системы при оценке химических свойств, трансурановых элементов, показанная еще создателем таблицы.
Разработанная в ХIХ веке, периодическая таблица Менделеева в интересах науки химии, дала готовую систематизацию типов атомов, для развития ФИЗИКИ в ХХ веке (физика атома и ядра атома). В начале ХХ века, ученые физики, путем исследований установили, что порядковый номер, (он же атомный), есть и мера электрического заряда атомного ядра этого элемента. А номер периода (т.е. горизонтального ряда), определяет число электронных оболочек атома. Так же выяснилось, что номер вертикального ряда таблицы определяет квантовую структуру внешней оболочки элемента, (этим самым, элементы одного ряда, обязаны сходством химических свойств).
Открытие Русского ученого, ознаменовало собой, новую эру в истории мировой науки, это открытие позволило не только совершить огромный скачек в химии, но так же было бесценно для ряда других направлений науки. Таблица Менделеева дала стройную систему сведений об элементах, на основе её, появилась возможность делать научные выводы, и даже предвидеть некоторые открытия.
Таблица МенделееваОдна из особенностей периодической таблицы Менделеева, состоит в том, что группа (колонка в таблице), имеет более существенные выражения периодической тенденции, чем для периодов или блоков. В наше время, теория квантовой механики и атомной структуры объясняет групповую сущность элементов тем, что они имеют одинаковые электронные конфигурации валентных оболочек, и как следствие, элементы которые находятся в пределах одой колонки, располагают очень схожими, (одинаковыми), особенностями электронной конфигурации, со схожими химическими особенностями. Так же наблюдается явная тенденция стабильного изменения свойств по мере возрастания атомной массы. Надо заметить, что в некоторых областях периодической таблицы, (к примеру, в блоках D и F), сходства горизонтальные, более заметны, чем вертикальные.
Надо заметить, что в некоторых областях периодической таблицы, (к примеру, в блоках D и F), сходства горизонтальные, более заметны, чем вертикальные.
Таблица Менделеева содержит группы, которым присваиваются порядковые номера от 1 до 18 (с лева, на право), согласно международной системе именования групп. В былое время, для идентификации групп, использовались римские цифры. В Америке существовала практика ставить после римской цифры, литер «А» при расположении группы в блоках S и P, или литер «В» – для групп находящихся в блоке D. Идентификаторы, применявшиеся в то время, это то же самое, что и последняя цифра современных указателей в наше время (на пример наименование IVB, соответствует элементам 4 группы в наше время, а IVA – это 14 группа элементов). В Европейских странах того времени, использовалась похожая система, но тут, литера «А» относилась к группам до 10, а литера «В» – после 10 включительно. Но группы 8,9,10 имели идентификатор VIII, как одна тройная группа. Эти названия групп закончили свое существование после того как в 1988 году вступила в силу, новая система нотации ИЮПАК, которой пользуются и сейчас.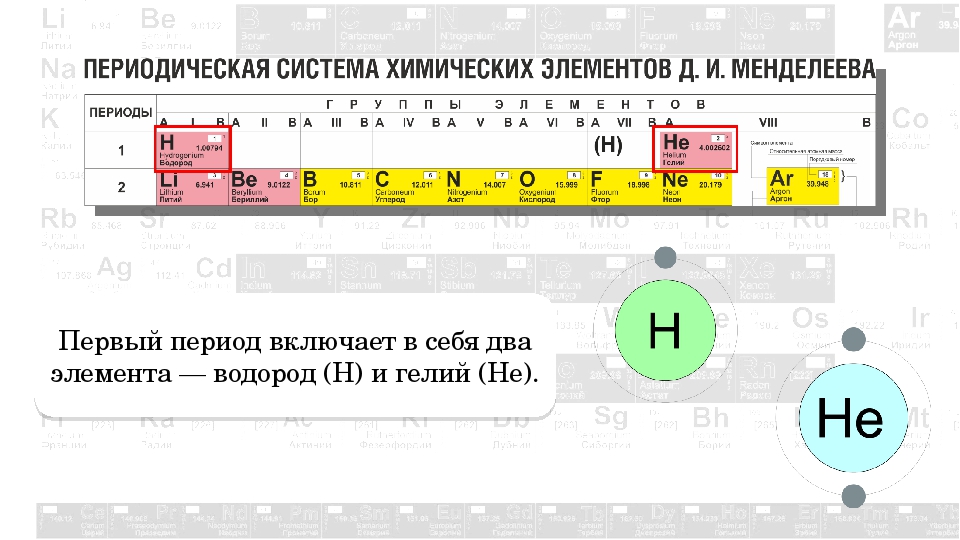
Многие группы получили несистематические названия травиального характера, (к примеру – «щелочноземельные металлы», или «галогены», и другие подобные названия). Таких названий не получили группы с 3 по 14, из за того что они в меньшей степени схожи между собой и имеют меньшее соответствие вертикальным закономерностям, их обычно, называют либо по номеру, либо по названию первого элемента группы (титановая, кобальтовая и тому подобно).
Химические элементы относящиеся к одной группе таблицы Менделеева проявляют определенные тенденции по электроотрицательности, атомному радиусу и энергии ионизации. В одной группе, по направлению сверху вниз, радиус атома возрастает, по мере заполнения энергетических уровней, удаляются, от ядра, валентные электроны элемента, при этом снижается энергия ионизации и ослабевают связи в атоме, что упрощает изъятие электронов. Снижается, так же, электроотрицательность, это следствие того, что возрастает расстояние между ядром и валентными электронами. Но из этих закономерностей так же есть исключения, на пример электроотрицательность возрастает, вместо того чтобы убывать, в группе 11, в направлении сверху вниз. В таблице Менделеева есть строка, которая называется «Период».
Но из этих закономерностей так же есть исключения, на пример электроотрицательность возрастает, вместо того чтобы убывать, в группе 11, в направлении сверху вниз. В таблице Менделеева есть строка, которая называется «Период».
Среди групп, есть и такие у которых более значимыми являются горизонтальные направления (в отличии от других, у которых большее значение имеют вертикальные направления), к таким группам относится блок F, в котором лантаноиды и актиноиды формируют две важные горизонтальные последовательности.
Элементы показывают определенные закономерности в отношении атомного радиуса, электроотрицательности, энергии ионизации, и в энергии сродства к электрону. Из-за того, что у каждого следующего элемента количество заряженных частиц возрастает, а электроны притягиваются к ядру, атомный радиус уменьшается в направлении слева направо, вместе с этим увеличивается энергия ионизации, при возрастании связи в атоме – возрастает сложность изъятия электрона. Металлам, расположенным в левой части таблицы, характерен меньший показатель энергии сродства к электрону, и соответственно, в правой части показатель энергии сродства к электрону, у не металлов, этот показатель больше, (не считая благородных газов).
Разные области периодической таблицы Менделеева, в зависимости от того на какой оболочке атома, находится последний электрон, и в виду значимости электронной оболочки, принято описывать как блоки.
В S-блок, входит две первые группы элементов, (щелочные и щелочноземельные металлы, водород и гелий).
В P-блок, входят шест последних групп, с 13 по 18 (согласно ИЮПАК, или по системе принятой в Америке – с IIIA до VIIIA), этот блок так же включает в себя все металлоиды.
Блок – D, группы с 3 по 12 (ИЮПАК, или с IIIB до IIB по-американски), в этот блок включены все переходные металлы.
Блок – F, обычно выносится за пределы периодической таблицы, и включает в себя лантаноиды и актиноиды.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Построение периодической таблицы химических элементов Менделеева отвечает характерным периодам теории чисел и ортогональных базисов. Дополнение матриц Адамара матрицами четных и нечетных порядков создает структурный базис вложенных матричных элементов: матриц первого (Odin), второго (Euler), третьего (Mersenne), четвертого (Hadamard) и пятого (Fermat) порядков.
Несложно заметить, что порядкам 4k матриц Адамара соответствуют инертные элементы с атомной массой, кратной четырем: гелий 4, неон 20, аргон 40 (39.948) и т.п., но также и основы жизни и цифровой техники: углерод 12, кислород 16, кремний 28, германий 72.
Такое впечатление, что с матрицами Мерсенна порядков 4k –1, напротив, связано все активное, ядовитое, разрушительное и разъедающее. Но это также радиоактивные элементы – источники энергии, и свинец 207 (конечный продукт, ядовитые соли). Фтор, это, конечно, 19. Порядкам матриц Мерсенна отвечает последовательность радиоактивных элементов, называемая рядом актиния: уран 235, плутоний 239 (изотоп, который является более мощным источником атомной энергии, чем уран) и т.п. Это также щелочные металлы литий 7, натрий 23 и калий 39.
Галлий – атомный вес 68
Порядкам 4k –2 матриц Эйлера (сдвоенный Мерсенн) соответствует азот 14 (основа атмосферы). Поваренная соль образована двумя “мерсенноподобными” атомами натрия 23 и хлора 35, вместе это сочетание характерно, как раз, для матриц Эйлера. Более массивный хлор с весом 35.4 немногим не добирает до адамаровой размерности 36. Кристаллы поваренной соли: куб (! т.е. характер смирный, адамаров) и октаэдр (более вызывающий, это несомненный Эйлер).
Более массивный хлор с весом 35.4 немногим не добирает до адамаровой размерности 36. Кристаллы поваренной соли: куб (! т.е. характер смирный, адамаров) и октаэдр (более вызывающий, это несомненный Эйлер).
В атомной физике переход железо 56 – никель 59, это рубеж между элементами, дающими энергию при синтезе более крупного ядра (водородная бомба) и распаде (урановая). Порядок 58 знаменит тем, что для него нет не только аналогов матриц Адамара в виде матриц Белевича с нулями на диагонали, для него нет и многих взвешенных матриц – ближайшая ортогональная W(58,53) имеет 5 нулей в каждом столбце и строке (глубокий разрыв).
В ряду, соответствующем матрицам Ферма и их замещениям порядков 4k +1, стоит волею судьбы фермий 257. Ничего не скажешь, точное попадание. Здесь же золото 197. Медь 64 (63.547) и серебро 108 (107.868), символы электроники, недотягивают, как видно, до золота и соответствуют более скромным матрицам Адамара. Медь, с ее недалеко ушедшим от 63 атомным весом, химически активна – ее зеленые окислы хорошо известны.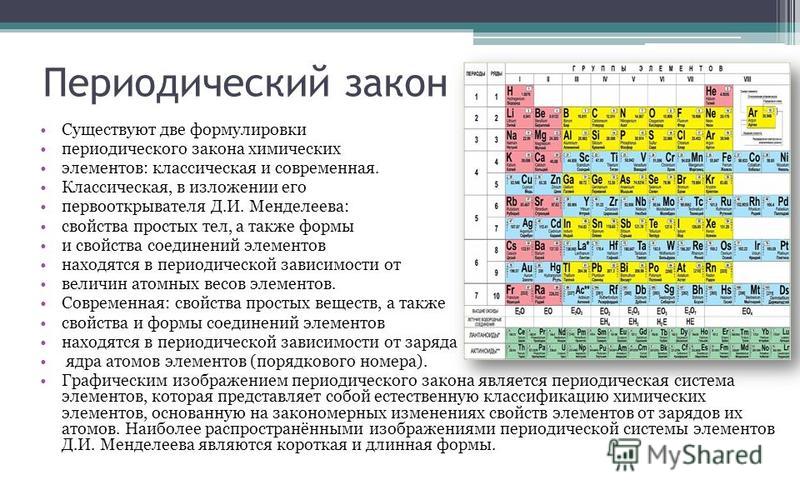
Кристаллы бора под сильным увеличением
С золотым сечением связан бор – атомная масса среди всех прочих элементов наиболее близка к 10 (точнее 10.8, близость атомного веса к нечетным числам тоже сказывается). Бор – достаточно сложный элемент. Бор играет запутанную роль в истории самой жизни. Строение каркаса в его структурах гораздо сложнее, чем в алмазе. Уникальный тип химической связи, которая позволяет бору поглощать любую примесь, очень плохо изучен, хотя за исследования, связанные с ним, большое количество ученых уже получили Нобелевские премии. Форма кристалла бора – икосаэдр, пять треугольников образуют вершину.
Загадка Платины. Пятый элемент, это, без сомнения, благородные металлы, такие, как золото. Надстройка над адамаровой размерностью 4k , на 1 большие.
Стабильный изотоп уран 238
Вспомним, все же, что числа Ферма встречаются редко (ближайшее – 257). Кристаллы самородного золота имеют форму, близкую к кубу, но и пентаграмма просверкивает.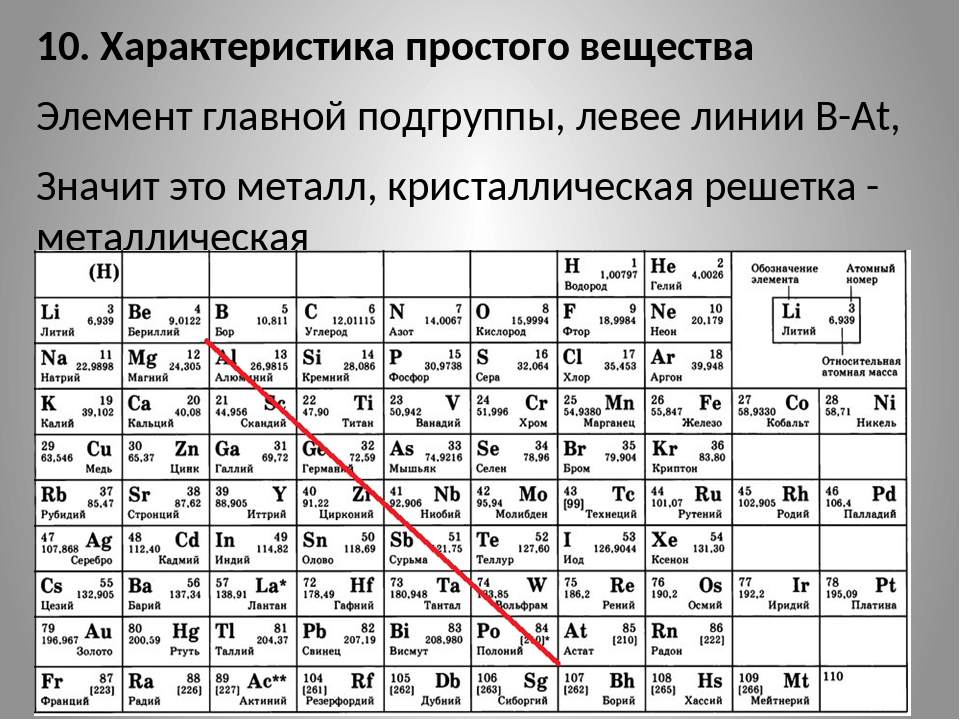 Его ближайший сосед, платина, благородный металл, отстоит от золота 197 по атомному весу меньше, чем на 4. Платина имеет атомный вес не 193, а несколько повышенный, 194 (порядок матриц Эйлера). Мелочь, но это переносит ее в стан несколько более агрессивных элементов. Стоит вспомнить, в связи, что при ее инертности (растворяется, разве, в царской водке), платину используют как активный катализатор химических процессов.
Его ближайший сосед, платина, благородный металл, отстоит от золота 197 по атомному весу меньше, чем на 4. Платина имеет атомный вес не 193, а несколько повышенный, 194 (порядок матриц Эйлера). Мелочь, но это переносит ее в стан несколько более агрессивных элементов. Стоит вспомнить, в связи, что при ее инертности (растворяется, разве, в царской водке), платину используют как активный катализатор химических процессов.
Губчатая платина при комнатной температуре воспламеняет водород. Характер у платины вовсе не мирный, смирнее себя ведет иридий 192 (смесь изотопов 191 и 193). Это, скорее, медь, но с весом и характером золота.
Между неоном 20 и натрием 23 нет элемента с атомным весом 22. Конечно, атомные веса – интегральная характеристика. Но среди изотопов, в свою очередь, тоже наблюдается любопытная корреляция свойств со свойствами чисел и соответствующих им матриц ортогональных базисов. В качестве ядерного топлива наибольшее применение имеет изотоп уран 235 (порядок матриц Мерсенна), в котором возможна самоподдерживающаяся цепная ядерная реакция. В природе этот элемент распространен стабильной форме уран 238 (порядок матриц Эйлера). Элемент с атомным весом 13 отсутствует. Что касается хаоса, то ограниченное количество устойчивых элементов таблицы Менделеева и сложность нахождения уровневых матриц высоких порядков ввиду замеченного у матриц тринадцатого порядка барьера коррелируют.
Изотопы химических элементов, островок стабильности
Таблица Менделеева является одним из величайших открытий человечества, позволившим упорядочить знания об окружающем мире и открыть новые химические элементы . Она является необходимой для школьников, а так же для всех, кто интересуется химией. Кроме того, данная схема является незаменимой и в других областях науки.
Данная схема содержит все известные человеку элементы, причем они группируются в зависимости от атомной массы и порядкового номера . Эти характеристики влияют на свойства элементов. Всего в коротком варианте таблицы имеется 8 групп, элементы, входящие в одну группу, обладают весьма сходными свойствами.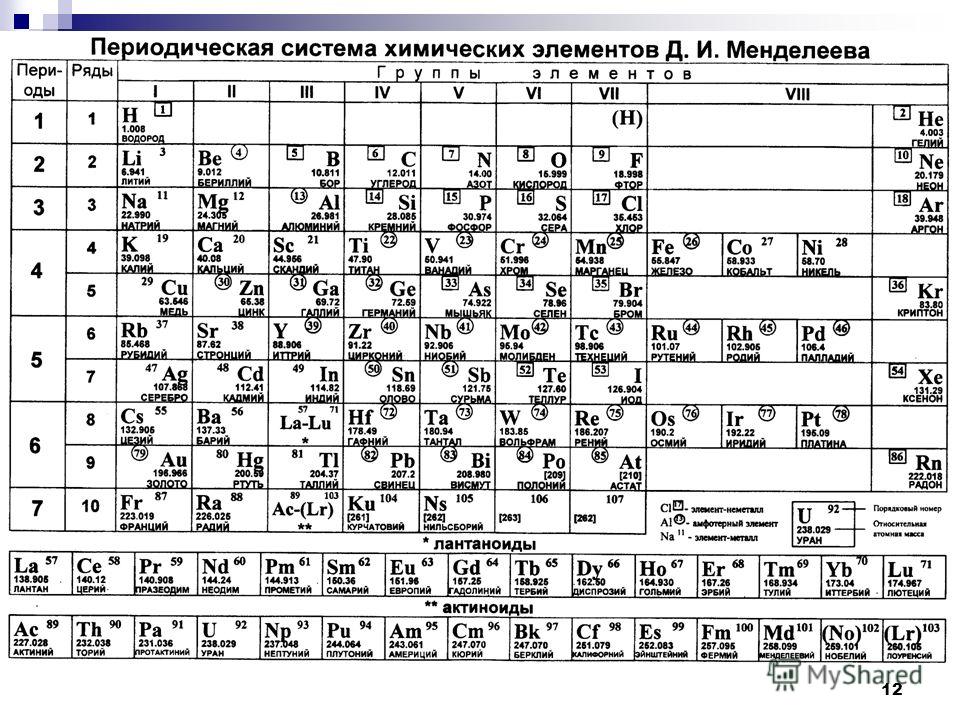 Первая группа содержит водород, литий, калий, медь, латинское произношение на русском которой купрум. А так же аргентум — серебро, цезий, золото — аурум и франций. Во второй группе расположены бериллий, магний, кальций, цинк, за ними идут стронций, кадмий, барий, заканчивается группа ртутью и радием.
Первая группа содержит водород, литий, калий, медь, латинское произношение на русском которой купрум. А так же аргентум — серебро, цезий, золото — аурум и франций. Во второй группе расположены бериллий, магний, кальций, цинк, за ними идут стронций, кадмий, барий, заканчивается группа ртутью и радием.
В состав третьей группы вошли бор, алюминий, скандий, галлий, потом следуют иттрий, индий, лантан, завершается группа таллием и актинием. Четвертая группа начинается с углерода, кремния, титана, продолжается германием, цирконием, оловом и завершается гафнием, свинцом и резерфордием. В пятой группе имеются такие элементы, как азот, фосфор, ванадий, ниже расположены мышьяк, ниобий, сурьма, потом идут тантал висмут и завершает группу дубний. Шестая начинается с кислорода, за которым лежат сера, хром, селен, потом следуют молибден, теллур, далее вольфрам, полоний и сиборгий.
В седьмой группе первый элемент – фтор, потом следует хлор, марганец, бром, технеций, за ним находится йод, потом рений, астат и борий. Последняя группа является самой многочисленной . В нее входят такие газы, как гелий, неон, аргон, криптон, ксенон и радон. Так же к данной группе относятся металлы железо, кобальт, никель, родий, палладий, рутений, осмий, иридий, платина. Далее идут ханний и мейтнерий. Отдельно расположены элементы, которые образуют ряд актиноидов и ряд лантаноидов . Они обладают сходными свойствами с лантаном и актинием.
Последняя группа является самой многочисленной . В нее входят такие газы, как гелий, неон, аргон, криптон, ксенон и радон. Так же к данной группе относятся металлы железо, кобальт, никель, родий, палладий, рутений, осмий, иридий, платина. Далее идут ханний и мейтнерий. Отдельно расположены элементы, которые образуют ряд актиноидов и ряд лантаноидов . Они обладают сходными свойствами с лантаном и актинием.
Данная схема включает в себя все виды элементов, которые делятся на 2 большие группы – металлы и неметаллы , обладающие разными свойствами. Как определить принадлежность элемента к той или иной группе, поможет условная линия, которую необходимо провести от бора к астату. Следует помнить, что такую линию можно провести только в полной версии таблицы. Все элементы, которые находятся выше этой линии, и располагаются в главных подгруппах считаются неметаллами. А которые ниже, в главных подгруппах – металлами. Так же металлами являются вещества, находящиеся в побочных подгруппах . Существуют специальные картинки и фото, на которых можно детально ознакомиться с положением этих элементов. Стоит отметить, что те элементы, которые находятся на этой линии, проявляют одинаково свойства и металлов и неметаллов.
Существуют специальные картинки и фото, на которых можно детально ознакомиться с положением этих элементов. Стоит отметить, что те элементы, которые находятся на этой линии, проявляют одинаково свойства и металлов и неметаллов.
Отдельный список составляют и амфотерные элементы, которые обладают двойственными свойствами и могут образовывать в результате реакций 2 вида соединений. При этом у них проявляются одинаково как основные, так и кислотные свойства . Преобладание тех или иных свойств зависит от условий реакции и веществ, с которыми амфотерный элемент реагирует.
Стоит отметить, что данная схема в традиционном исполнении хорошего качества является цветной. При этом разными цветами для удобства ориентирования обозначаются главные и побочные подгруппы . А так же элементы группируются в зависимости от схожести их свойств.
Однако в настоящее время наряду с цветной схемой очень распространенной является периодическая таблица Менделеева черно белая. Такой ее вид используется для черно-белой печати. Несмотря на кажущуюся сложность, работать с ней так же удобно, если учесть некоторые нюансы. Так, отличить главную подгруппу от побочной в таком случае можно по отличиям в оттенках, которые хорошо заметны. К тому же в цветном варианте элементы с наличием электронов на разных слоях обозначаются разными цветами .
Такой ее вид используется для черно-белой печати. Несмотря на кажущуюся сложность, работать с ней так же удобно, если учесть некоторые нюансы. Так, отличить главную подгруппу от побочной в таком случае можно по отличиям в оттенках, которые хорошо заметны. К тому же в цветном варианте элементы с наличием электронов на разных слоях обозначаются разными цветами .
Стоит отметить, что в одноцветном исполнении ориентироваться по схеме не очень трудно. Для этого будет достаточно информации, указанной в каждой отдельной клеточке элемента.
Егэ сегодня является основным видом испытания по окончанию школы, а значит, подготовке к нему необходимо уделять особое внимание. Поэтому при выборе итогового экзамена по химии , необходимо обратить внимание на материалы, которые могут помочь в его сдаче. Как правило, школьникам на экзамене разрешено пользоваться некоторыми таблицами, в частности, таблицей Менделеева в хорошем качестве. Поэтому, чтобы она принесла на испытаниях только пользу, следует заблаговременно уделить внимание ее строению и изучению свойств элементов, а так же их последовательности. Необходимо научиться, так же пользоваться и черно-белой версией таблицы , чтобы на экзамене не столкнуться с некоторыми трудностями.
Необходимо научиться, так же пользоваться и черно-белой версией таблицы , чтобы на экзамене не столкнуться с некоторыми трудностями.
Помимо основной таблицы, характеризующей свойства элементов и их зависимость от атомной массы, существуют и другие схемы, которые могут оказать помощь при изучении химии. Например, существуют таблицы растворимости и электроотрицательности веществ . По первой можно определить, насколько растворимо то или иное соединение в воде при обычной температуре. При этом по горизонтали располагаются анионы – отрицательно заряженные ионы, а по вертикали – катионы, то есть положительно заряженные ионы. Чтобы узнать степень растворимости того, или иного соединения, необходимо по таблице найти его составляющие. И на месте их пересечения будет нужное обозначение.
Если это буква «р», то вещество полностью растворимо в воде в нормальных условиях. При наличии буквы «м» — вещество малорастворимое, а при наличии буквы «н» — оно почти не растворяется. Если стоит знак «+», — соединение не образует осадок и без остатка реагирует с растворителем. Если присутствует знак «-», это означает, что такого вещества не существует. Иногда так же в таблице можно увидеть знак «?», тогда это обозначает, что степень растворимости этого соединения доподлинно не известна. Электроотрицательность элементов может варьироваться от 1 до 8, для определения этого параметра так же существует специальная таблица.
Если стоит знак «+», — соединение не образует осадок и без остатка реагирует с растворителем. Если присутствует знак «-», это означает, что такого вещества не существует. Иногда так же в таблице можно увидеть знак «?», тогда это обозначает, что степень растворимости этого соединения доподлинно не известна. Электроотрицательность элементов может варьироваться от 1 до 8, для определения этого параметра так же существует специальная таблица.
Еще одна полезная таблица – ряд активности металлов. В нем располагаются все металлы по увеличении степени электрохимического потенциала. Начинается ряд напряжения металлов с лития, заканчивается золотом. Считается, что чем левее занимает место в данном ряду металл, тем он более активен в химических реакциях. Таким образом, самым активным металлом считается металл щелочного типа литий. В списке элементов ближе к концу так же присутствует водород. Считается, что металлы, которые расположены после него, являются практически неактивными. Среди них такие элементы, как медь, ртуть, серебро, платина и золото.
Среди них такие элементы, как медь, ртуть, серебро, платина и золото.
Таблица Менделеева картинки в хорошем качестве
Данная схема является одним из крупнейших достижений в области химии. При этом существует немало видов этой таблицы – короткий вариант, длинный, а так же сверхдлинный. Самой распространенной является короткая таблица, так же часто встречается и длинная версия схемы. Стоит отметить, что короткая версия схемы в настоящее время не рекомендуется ИЮПАК для использования.
Всего было разработано больше сотни видов таблицы , отличающихся представлением, формой и графическим представлением. Они используются в разных областях науки, либо совсем не применяются. В настоящее время новые конфигурации схемы продолжают разрабатываться исследователями. В качестве основного варианта используется либо короткая, либо длинная схема в отличном качестве.
Вероятно, все вы видели периодическую таблицу элементов. Возможно, что она и по сей день преследует вас в ваших снах, а может быть, она пока для вас всего лишь визуальный фон, украшающий стенку школьного класса.
 Однако в этой, казалось бы, случайной коллекции клеток кроется значительно больше, чем это кажется на первый взгляд.
Однако в этой, казалось бы, случайной коллекции клеток кроется значительно больше, чем это кажется на первый взгляд.Периодическая таблица (или ПТ, как мы будем периодически называть её в этой статье), а также те элементы, которые входят в неё, обладают чертами, о которых вы, возможно, никогда не догадывались. Вот десять фактов, начиная от создания таблицы и до внесения в неё последних элементов, которые большинству людей не известны.
10. Менделееву помогали
Периодическая таблица стала использоваться, начиная с 1869 года, когда она была составлена заросшим густой бородой Димитрием Менделеевым. Большинство людей думает, что Менделеев был единственным, кто работал над этой таблицей, и благодаря этому он стал самым гениальным химиком столетия. Однако его усилиям помогали несколько европейских учёных, которые внесли важный вклад в завершение этого колоссального набора элементов.
Менделеев широко известен как отец периодической таблицы, но, когда он её составлял, ещё не все элементы таблицы были уже открыты. Как такое стало возможно? Учёные славятся своим безумием…
Как такое стало возможно? Учёные славятся своим безумием…
9. Последние добавленные элементы
Верьте или нет, периодическая таблица не сильно менялась с 1950-х годов. Однако 2 декабря 2016 года было добавлено сразу четыре новых элемента: нихоний (элемент №113), московий (элемент №115), тенессин (элемент №117) и оганесон (элемент №118). Эти новые элементы получили свои названия только в июне 2016 года, так как потребовалась пятимесячная экспертиза, прежде чем их официально добавили в ПТ.
Три элемента получили свои названия в честь городов или государств, в которых их удалось получить, а оганесон был назван в честь российского физика-ядерщика Юрия Оганесяна за его вклад в получение этого элемента.
8. Какой буквы нет в таблице?
В латинском алфавите есть 26 букв, и каждая из них важна. Однако Менделеев решил этого не замечать. Взгляните на таблицу и скажите, какой букве не повезло? Подсказка: ищите по порядку и загибайте при этом пальцы после каждой найденной буквы.
 В итоге вы найдёте «пропавшую» букву (если у вас на руках присутствуют все десять пальцев). Догадались? Это буква под номером 10, буква «J».
В итоге вы найдёте «пропавшую» букву (если у вас на руках присутствуют все десять пальцев). Догадались? Это буква под номером 10, буква «J».Говорят, что «единица» – это цифра одиноких. Так, может, стоило бы назвать букву «J» буквой одиноких? Но вот забавный факт: большинство мальчиков, родившихся в США в 2000 году, получили имена, начинавшиеся с этой буквы. Таким образом, эта буква не осталась без должного внимания.
7. Синтезированные элементы
Как вы, возможно, уже знаете, на сегодняшний день в периодической таблице присутствует 118 элементов. Можете ли вы догадаться, сколько элементов из этих 118 были получены лабораторным путём? Из всего общего списка в природных условиях можно найти лишь 90 элементов.
Вам кажется, что 28 искусственно созданных элементов – это много? Ну, просто поверьте на слово. Их синтезируют, начиная с 1937 года, и учёные продолжают это делать и сейчас. Все эти элементы вы можете найти в таблице. Посмотрите на элементы с 95 по 118, все эти элементы отсутствуют на нашей планете и были синтезированы в лабораториях.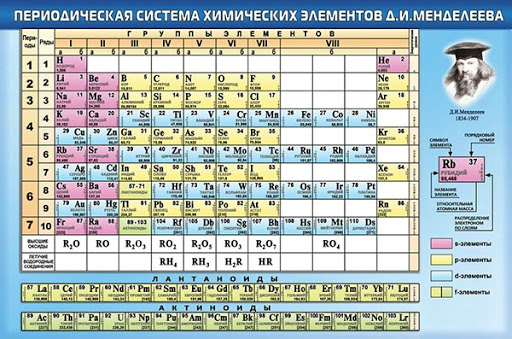 То же касается и элементов под номерами 43, 61, 85 и 87.
То же касается и элементов под номерами 43, 61, 85 и 87.
6. 137-й элемент
В середине 20-го века известный учёный по имени Ричард Фейнман сделал довольно громкое заявление, которое повергло в изумление весь научный мир нашей планеты. По его словам, если мы когда-нибудь обнаружим 137-й элемент, то мы не сможем определить количество в нём протонов и нейтронов. Число 1/137 примечательно тем, что это значение константы тонкой структуры, которая описывает вероятность поглощения или излучения электроном фотона. Теоретически элемент №137 должен иметь 137 электронов и 100-процентную вероятность поглощения фотона. Его электроны будут вращаться со скоростью света. Ещё более невероятно, что электроны элемента 139, чтобы существовать, должны вращаться быстрее, чем скорость света.
Вы ещё не устали от физики? Возможно, вам будет интересно узнать, что число 137 объединяет три важнейших области физики: теорию о скорости света, квантовую механику и электромагнетизм. С начала 1900-х годов физики предполагают, что цифра 137 может быть основой Великой единой теории, в которую войдут все три вышеуказанных области. По общему признанию, это звучит так же невероятно, как легенды о НЛО и о Бермудском треугольнике.
По общему признанию, это звучит так же невероятно, как легенды о НЛО и о Бермудском треугольнике.
5. Что можно сказать о названиях?
Почти все названия элементов имеют какой-то смысл, хотя он и не сразу понятен. Названия новым элементам даются не произвольно. Я бы назвал элемент просто первым пришедшим мне в голову словом. Например, «керфлумп». По-моему, неплохо.
Как правило, названия элементов относятся к одной из пяти основных категорий. Первая – это имена известных учёных, классический вариант – эйнштейний. Кроме того, элементы могут получить свои имена в зависимости от тех мест, где они были впервые зарегистрированы, например, германий, америций, галлий и т. д. В качестве дополнительной опции используются названия планет. Элемент уран был впервые обнаружен вскоре после того, как была открыта планета Уран. Элементы могут носить имена, связанные с мифологией, например, существует титан, названный так в честь древнегреческих титанов, и торий, названный по имени скандинавского бога-громовержца (или звёздного «мстителя», в зависимости от того, что вы предпочитаете).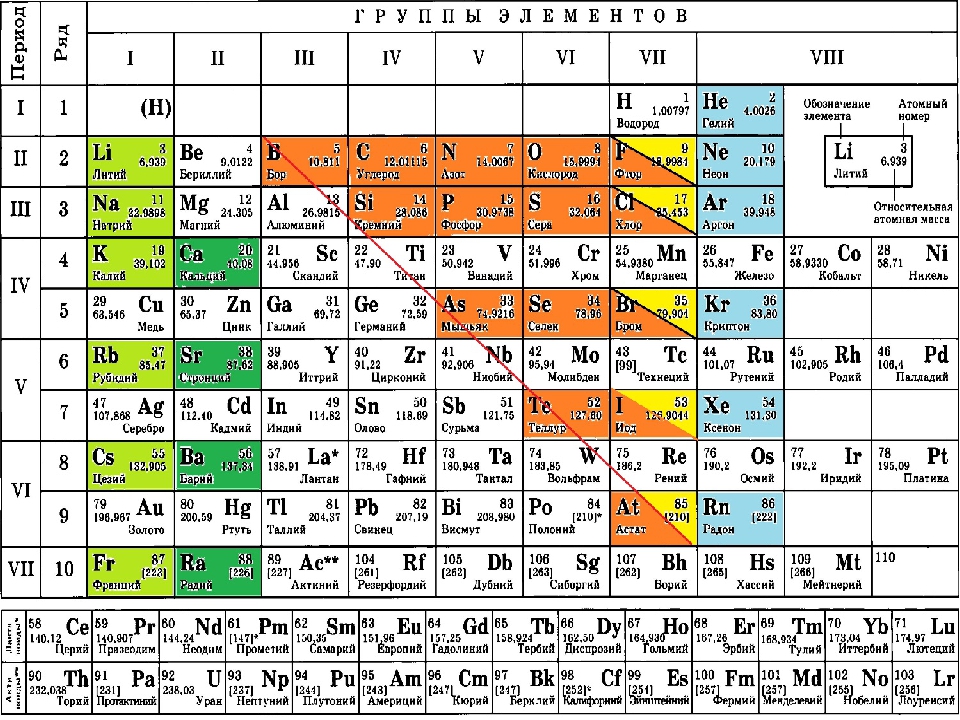
И, наконец, есть названия, описывающие свойства элементов. Аргон происходит от греческого слова «аргос», что означает «ленивый» или «медленный». Из названия следует предположение, что этот газ не отличается активностью. Бром – это ещё один элемент, название которого происходит от греческого слова. «Бромос» означает «зловоние», и это довольно точно описывает запах брома.
4. Было ли создание таблицы «озарением»
Если вы любите карточные игры, то этот факт для вас. Менделееву требовалось каким-то образом упорядочить все элементы и найти систему для этого. Естественно, что для создания таблицы по категориям он обратился к пасьянсу (ну, а к чему же ещё?) Менделеев записал атомный вес каждого элемента на отдельной карточке, а затем приступил к раскладке своего передового пасьянса. Он укладывал элементы в соответствии с их специфическими свойствами, а затем упорядочивал их в каждом столбце в соответствии с их атомным весом.
Многие не могут сложить и обычный пасьянс, так что этот пасьянс впечатляет.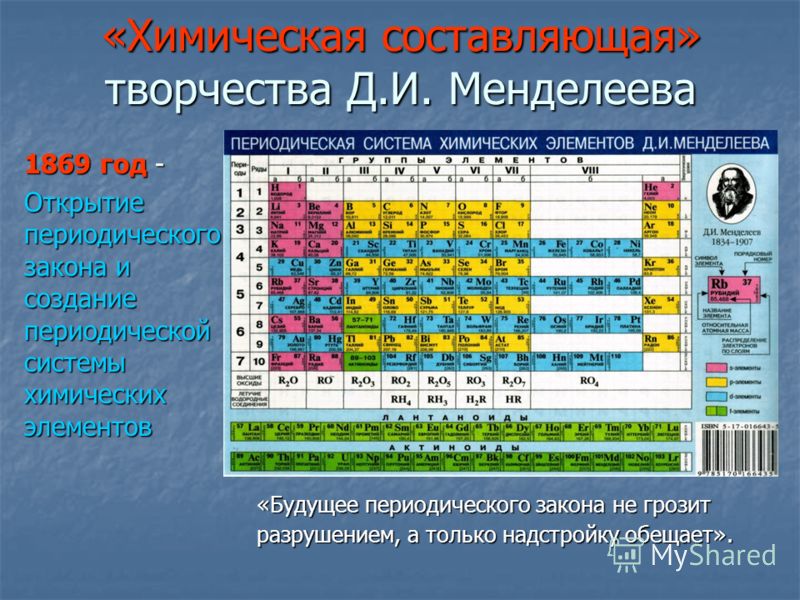 Что будет дальше? Наверное, кто-нибудь с помощью шахмат сделает переворот в астрофизике или создаст ракету, способную долететь до окраин галактики. Представляется, что в этом не будет ничего необычного, если учесть, что Менделеев сумел получить такой гениальный результат всего лишь с помощью колоды обычных игральных карт.
Что будет дальше? Наверное, кто-нибудь с помощью шахмат сделает переворот в астрофизике или создаст ракету, способную долететь до окраин галактики. Представляется, что в этом не будет ничего необычного, если учесть, что Менделеев сумел получить такой гениальный результат всего лишь с помощью колоды обычных игральных карт.
3. Невезучие инертные газы
Помните, как мы классифицировали аргон как самый «ленивый» и «медленный» элемент в истории нашей вселенной? Похоже, что Менделеевым овладели такие же чувства. Когда в 1894 году впервые удалось получить чистый аргон, он не вписывался ни в один из столбцов таблицы, поэтому, вместо того чтобы заняться поисками решения, учёный решил просто отрицать его существование.
Ещё более поразительно, что аргон был не единственным элементом, который изначально постигла эта судьба. Помимо аргона, без классификации остались ещё пять других элементов. Это коснулось радона, неона, криптона, гелия и ксенона – и все отрицали их существование просто потому, что Менделеев не смог найти для них места в таблице. После нескольких лет перегруппировки и переклассификации этим элементам (названных инертными газами) всё-таки посчастливилось присоединиться к достойному клубу признанных реально существующими.
После нескольких лет перегруппировки и переклассификации этим элементам (названных инертными газами) всё-таки посчастливилось присоединиться к достойному клубу признанных реально существующими.
2. Атомная любовь
Совет для всех тех, кто считает себя романтиком. Возьмите бумажную копию периодической таблицы и вырежьте из неё все сложные и относительно ненужные средние столбцы так, чтобы у вас осталось 8 колонок (вы получите «короткую» форму таблицы). Сложите её посредине IV группы – и вы узнаете, какие элементы могут образовывать соединения друг с другом.
Элементы, которые «целуются» при складывании, способны образовывать стабильные соединения. Эти элементы имеют комплементарные электронные структуры, и они будут сочетаться друг с другом. И, если это не настоящая любовь, как у Ромео с Джульеттой или у Шрека с Фионой – тогда я не знаю, что такое любовь.
1. Углерод рулит
Углерод пытается быть в центре игры. Вы думаете, что всё знаете об углероде, но это не так, он занимает намного более важное место, чем вы это себе представляете.
 Знаете ли вы, что он присутствует более чем в половине всех известных соединений? И как насчёт того факта, что 20 процентов веса всех живых организмов приходится на углерод? Это действительно странно, но приготовьтесь: каждый атом углерода в вашем теле был когда-то частью фракции углекислого газа в атмосфере. Углерод является не только суперэлементом нашей планеты, он четвёртый по численности элемент во всей Вселенной.
Знаете ли вы, что он присутствует более чем в половине всех известных соединений? И как насчёт того факта, что 20 процентов веса всех живых организмов приходится на углерод? Это действительно странно, но приготовьтесь: каждый атом углерода в вашем теле был когда-то частью фракции углекислого газа в атмосфере. Углерод является не только суперэлементом нашей планеты, он четвёртый по численности элемент во всей Вселенной.Если периодическую таблицу сравнить с вечеринкой, то углерод – её главный ведущий. И кажется, что он единственный знает, как нужно всё правильно организовать. Ну и, помимо прочего, это основной элемент всех бриллиантов, так что при всей своей назойливости он ещё и блестит!
Как всё начиналось?
Многие известные именитые химики на рубеже XIX-XX веков уже давно заметили, что физические и химические свойства многих химических элементов очень похожи друг на друга. Так например Калий, Литий и Натрий – все являются активными металлами, которые при взаимодействии с водой образают активные гидроксиды этих металлов; Хлор, Фтор, Бром в своих соединениях с водородом проявляли одинаковую валентность равную I и все эти соединения являются сильными кислотами. Из этой похожести давно напрашивался вывод, что все известные химические элементы можно объединить в группы, причём так чтобы у элементов каждой группы был определённый набор физико-химических характеристик. Однако часто такие группы были неверно составлены из разных элементов различными учёными и долгое время многими игнорировалась одна из главных характеристик элементов – это их атомная масса. Игнорировалась она потому, что была и есть разная у различных элементов, а значит её не могли использовать в качестве параметра для объединения в группы. Исключение составил лишь франзуский химик Александр Эмиль Шанкуртуа, он попытался расположить все элементы в трёхмерной модели по винтовой линии, но его работа не была признана научным сообществом, а модель получилась громоздкая и неудобная.
Из этой похожести давно напрашивался вывод, что все известные химические элементы можно объединить в группы, причём так чтобы у элементов каждой группы был определённый набор физико-химических характеристик. Однако часто такие группы были неверно составлены из разных элементов различными учёными и долгое время многими игнорировалась одна из главных характеристик элементов – это их атомная масса. Игнорировалась она потому, что была и есть разная у различных элементов, а значит её не могли использовать в качестве параметра для объединения в группы. Исключение составил лишь франзуский химик Александр Эмиль Шанкуртуа, он попытался расположить все элементы в трёхмерной модели по винтовой линии, но его работа не была признана научным сообществом, а модель получилась громоздкая и неудобная.
В отличие от многих учёных, Д.И. Менделеев взял атомную массу (в те времена ещё “Атомный вес”) как ключевой параметр при классификации элементов. В своём варианте Дмитрий Иванович расположил элементы по возрастанию их атомных весов и вот тут обозначилась закономерность, что через определённые промежутки элементов их свойства периодически повторяются. Правда пришлось сделать и исключения: некоторые элементы были поменяны местами и не соответствовали возрастанию атомных масс (например, теллур и йод), но зато соответствовали свойствам элементов. Дальнейшее развитие атомно-молекулярного учения оправдало такие подвижки и показало справедливость этой расстановки. Подробнее об этом вы можете прочесть в статье “В чём открытие Менделеева”
Правда пришлось сделать и исключения: некоторые элементы были поменяны местами и не соответствовали возрастанию атомных масс (например, теллур и йод), но зато соответствовали свойствам элементов. Дальнейшее развитие атомно-молекулярного учения оправдало такие подвижки и показало справедливость этой расстановки. Подробнее об этом вы можете прочесть в статье “В чём открытие Менделеева”
Как мы можем видеть, расположение элементов в этом варианте совсем не такое, какое мы видим в совремнном виде. Во первых, группы и периоды поменяны местами: группы по горизонтали, периоды по вертикали, а во-вторых, самих групп в нём как-то многовато – девятнадцать, вместо принятых на сегодня восемнадцати.
Однако, спустя всего год, в 1870-м Менделеев сформировал новый вариант таблицы, который уже более узнаваем нами: подобные элементы выстроены по вертикали, образуя группы, а 6 периодов расположены по горизонтали. Особенно примечательно то, что и в первом и во втором варианте таблицы виднеются существенные достижения, коих не было у его предшественников: в таблице заботливо оставлены места под элементы которые, по мнению Менделеева, ещё предстояло открыть.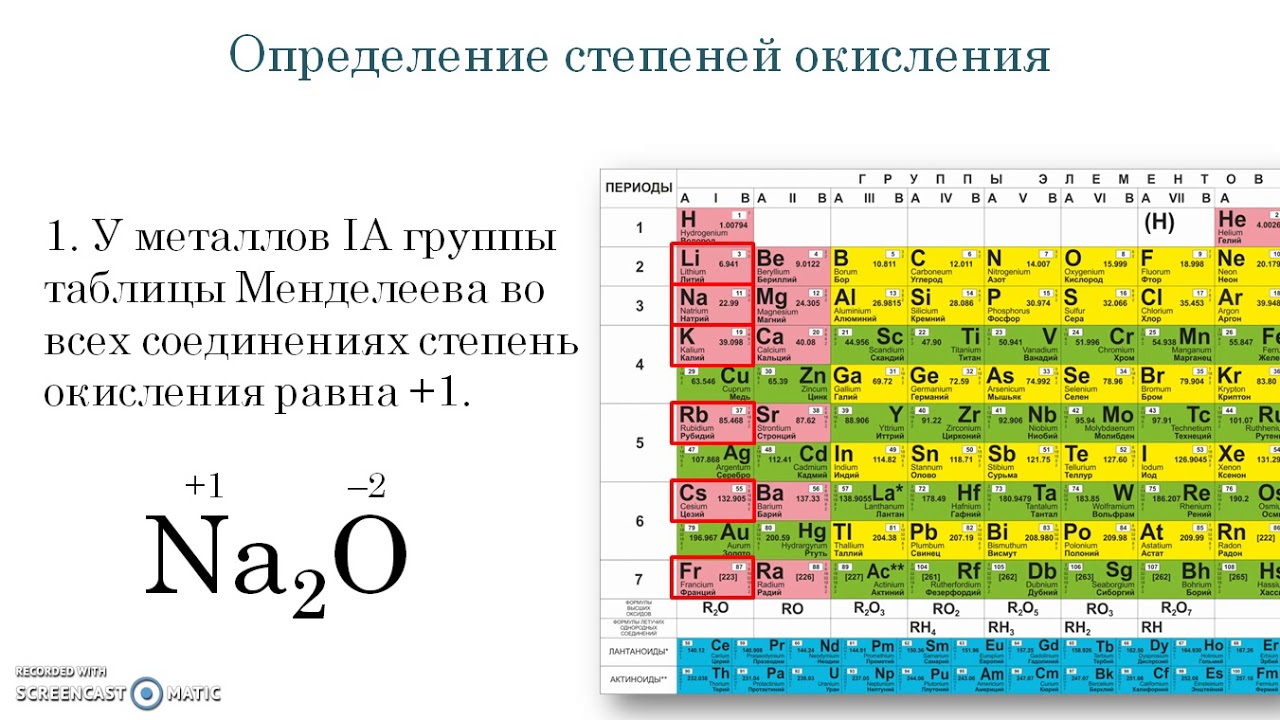 Соответствующие вакантные места обозначены им знаком вопроса и вы можете видеть их на рисунке выше. В дальнейшем были действительно открыты соответствующие элементы: Галий, Германий, Скандий. Таким образом Дмитрий Иванович не только систематезировал элементы в группы и периоды, но и предсказал открытие новых, ещё не известных, элементов.
Соответствующие вакантные места обозначены им знаком вопроса и вы можете видеть их на рисунке выше. В дальнейшем были действительно открыты соответствующие элементы: Галий, Германий, Скандий. Таким образом Дмитрий Иванович не только систематезировал элементы в группы и периоды, но и предсказал открытие новых, ещё не известных, элементов.
В дальнейшем, после разрешения многих актуальных загадок химии того времени – открытие новых элементов, выделение группы благородных газов совместно с участием Уильяма Рамзая, установления того факта, что Дидимий вовсе не является самостоятельным элементом, а является смесью двух других, – были опубликованы всё новые и новые варианты таблицы, подчас имеющих даже вовсе и не табличный вид. Но не будем приводить здесь их все, а приведём лишь конечный вариант, сформировавшийся ещё при жизни великого учёного.
Переход от атомных весов к заряду ядра.
К сожалению, Дмитрий Иванович не дожил до планетарной теории строения атома и не видел триумф опытов Резерфорда, хотя именно с его открытиями начинается новая эпоха в развитии периодического закона и всей периодической системы. Напомню что из опытов, проводимых Эрнестом Резерфордом, следовало, что атомы элементов состоят из положительно-заряженного атомного ядра и обращающихся вокруг ядра отрицательно-заряженных электронов. После определения зарядов атомных ядер всех, известных на тот момент, элементов, выяснилось, что в периодической системе они располагаются в соответствии с зарядом ядра. А периодический закон приобрёл новый смысл, теперь он стал звучать так:
Напомню что из опытов, проводимых Эрнестом Резерфордом, следовало, что атомы элементов состоят из положительно-заряженного атомного ядра и обращающихся вокруг ядра отрицательно-заряженных электронов. После определения зарядов атомных ядер всех, известных на тот момент, элементов, выяснилось, что в периодической системе они располагаются в соответствии с зарядом ядра. А периодический закон приобрёл новый смысл, теперь он стал звучать так:
“Свойства химических элементов, а также формы и свойства, образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов”
Теперь стало понятно, почему некоторые более лёгкие элементы были поставлены Менделеевым позади их более тяжёлых предшественников, – всё дело в том, что так они стоят по порядку зарядов их ядра. Например, теллур тяжелее йода, однако стоит в таблице раньше него, ибо заряд ядра его атома и количество электронов равняется 52, а у йода – 53. Можете посмотреть на таблицу и убедиться в этом сами.
После открытия строения атома и атомного ядра, периодическая система претерпевала ещё несколько изменений, пока, наконец, не достигла вида, уже знакомого нам со школы, короткопериодного варианта таблицы Менделеева.
В этой таблице нам знакомо уже всё: 7 периодов, 10 рядов, побочные и главные подгруппы. Также со временем открытия новых элементов и наполнения ими таблицы, пришлось вынести в отдельные ряды элементы подобные Актинию и Лантану, все они соответственно были названы Актиноидами и Лантаноидами. Эта версия системы просуществовала очень долго – в мировом научном сообществе практически до конца 80х, начала 90х, а в нашей стране и того дольше – до 10х годов нынешнего столетия.
Современный вариант таблицы Менделеева.
Однако, тот вариант, которые многие из нас проходили в школе на деле оказывается весьма запутанным, а путаница выражается в разделении подгрупп на главные и побочные и запоминание логики отображения свойств элементов становится достаточно сложным.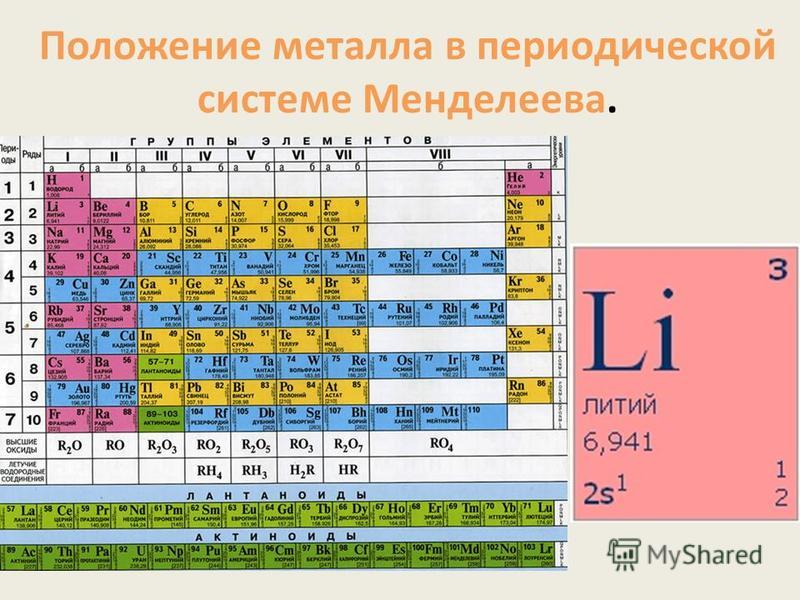 Конечно, несмотря на это, многие по нему учились, становились докторами химических наук, но всё же в современности ему на смену пришёл новый вариант – длиннопериодный. Отмечу, что именно этот вариант является одобренным IUPAC (международным союзом теоретической и прикладной химии). Давайте взглянем на него.
Конечно, несмотря на это, многие по нему учились, становились докторами химических наук, но всё же в современности ему на смену пришёл новый вариант – длиннопериодный. Отмечу, что именно этот вариант является одобренным IUPAC (международным союзом теоретической и прикладной химии). Давайте взглянем на него.
На смену восьми группам пришли восемнадцать, среди которых нет уже никакого разделения на главные и побочные, а все группы продиктованы расположением электронов в атомной оболочке. Заодно избавились и от двухрядных и однорядных периодов, теперь все периоды содержат только один ряд. Чем же удобен такой вариант? Теперь периодичность свойств элементов просматривается более наглядно. Номер группы, по сути, обозначает количество электронов во внешнем уровне, в связи с чем все главные подгруппы старого варианта расположились в первой, второй и с тринадцатой по восемнадцатую группу, а все “бывшие побочные” группы разместились в середине таблицы. Тем самым теперь из таблицы хорошо видно, что если это первая группа – то это щелочные металлы и никаких вам меди или серебра, и видно, что все транзитные металлы хорошо демонстрируют схожесть их свойств в связи с заполнением d-подуровня, в меньшей степени влияющим на внешние свойства, также как и лантаноиды и актиноиды проявляют подобные свойства по причине разного лишь f-подуровня. Таким образом, вся таблица разбита на следующие блоки: s-блок, на котором заполняются s-электроны, d-блок, p-блок и f-блок, с заполнением d, p, и f-электронов соответственно.
Таким образом, вся таблица разбита на следующие блоки: s-блок, на котором заполняются s-электроны, d-блок, p-блок и f-блок, с заполнением d, p, и f-электронов соответственно.
К сожалению, в нашей стране этот вариант включился в школьные учебники лишь в последние 2-3 года, да и то не во все. И очень напрасно. С чем это связано? Ну во-первых, с застойными временами в лихие 90-е, когда в стране не было вообще никакого развития, не говоря уж о сфере образования, а именно в 90е годы мировое химическое сообщество перешло на этот вариант. Во-вторых, с лёгкой инертностью и тяжестью восприятия всего нового, ведь нашим преподавателям привычен именно старый, короткопериодный вариант таблицы, несмотря на то, что при изучении химии он гораздо сложнее и менее удобен.
Расширенный вариант периодической системы.
Но время не стоит на месте, наука и технологии тоже. Уже открыт 118 элемент периодической системы, а значит скоро придётся открывать следующий, восьмой, период таблицы. Кроме того, появится новый энергетический подуровень: g-подуровень. Элементы его составляющие придётся вынести вниз таблицы, подобно лантаноидам или актиноидам, либо расширить эту таблицу ещё в два раза, так что она перестанет помещаться на лист формата A4. Здесь я приведу лишь ссылку на википедию (см. Расширенная периодическая система) и не буду лишний раз повторять описание этого варианта. Кому станет интересно – сможет пройти по ссылке и ознакомиться.
Элементы его составляющие придётся вынести вниз таблицы, подобно лантаноидам или актиноидам, либо расширить эту таблицу ещё в два раза, так что она перестанет помещаться на лист формата A4. Здесь я приведу лишь ссылку на википедию (см. Расширенная периодическая система) и не буду лишний раз повторять описание этого варианта. Кому станет интересно – сможет пройти по ссылке и ознакомиться.
В этом варианте ни f-элементы (лантаноиды и актиноиды) ни g-элементы (“элементы будущего” с №№ 121-128) не вынесены отдельно, а делают таблицу шире на 32 клетки. Также элемент Гелий помещён во вторую группу, так как он входит в s-блок.
В целом, же вряд ли будущие химики будут пользоваться этим вариантом, скорее всего на смену таблице Менделеева придёт одна из альтернатив, которые уже выдвигаются смелыми учёными: система Бенфея, “Химическая галактика” Стьюарта или иной вариант. Но это будет уже только после достижения второго острова стабильности химических элементов и, скорее всего, нужно будет больше для наглядности в ядерной физике, чем в химии, ну а нам пока хватит старой доброй периодической системы Дмитрия Ивановича.
– EnchantedLearning.com
Таблица Менделеева – EnchantedLearning.com Рекламное объявление. EnchantedLearning.com – это сайт, поддерживаемый пользователями.
В качестве бонуса участники сайта получают доступ к версии сайта без баннерной рекламы и страниц, удобных для печати.
Щелкните здесь, чтобы узнать больше.
Периодическая таблица элементов
Атомный номер
Периодическая таблица элементов показывает типы элементов, из которых состоит Вселенная, и относительные свойства атомов.В нем элементы расположены по возрастанию атомного номера (количества протонов в ядре атома).
Каждый из элементов в группе (столбце) имеет общие качества. Например, группа 18 (или 8a) – это инертные газы, которые практически не взаимодействуют химически с другими элементами, потому что у них нет валентных электронов. Каждый из элементов периода (ряда) имеет одинаковое количество электронных оболочек; количество электронов в этих оболочках (атомный номер элемента) увеличивается слева направо.
Каждый из элементов периода (ряда) имеет одинаковое количество электронных оболочек; количество электронов в этих оболочках (атомный номер элемента) увеличивается слева направо.
Таблица Менделеева была изобретена Дмитрием И. Менделеевым, а позже была переработана Генри Дж. Дж. Мозли.
| Период | Группа | ||||||||||||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1A | 2A | 3B | 4B | 5Б | 6B | 7B | 8B | 1Б | 2B | 3A | 4A | 5A | 6A | 7A | 8A | ||||
| 1 | H 1 | He 2 | |||||||||||||||||
| 2 | Ли 3 | Be 4 | B 5 | С 6 | № 7 | О 8 | Ф 9 | Ne 10 | |||||||||||
| 3 | Na 11 | мг 12 | Al 13 | Si 14 | П 15 | Ю 16 | Класс 17 | Ар 18 | |||||||||||
| 4 | К 19 | Ca 20 | сбн 21 | Ti 22 | В 23 | Кр 24 | млн 25 | Fe 26 | Co 27 | Ni 28 | Cu 29 | Zn 30 | Ga 31 | Ge 32 | As 33 | SE 34 | руб. 35 | Кр 36 | |
| 5 | руб. 37 | Sr 38 | Я 39 | Zr 40 | Nb 41 | Пн 42 | Тс 43 | Ру 44 | Rh 45 | Pd 46 | Ag 47 | Кд 48 | В 49 | Sn 50 | Сб 51 | Te 52 | Я 53 | Xe 54 | |
| 6 | CS 55 | Ba 56 | . .. .. | Hf 72 | Ta 73 | Вт 74 | Re 75 | Ос 76 | Ir 77 | Pt 78 | Au 79 | рт. Ст. 80 | Тл 81 | Пб 82 | Би 83 | По 84 | по адресу 85 | Rn 86 | |
| 7 | Пт 87 | Ra 88 | … | Rf 104 | Дб 105 | Sg 106 | Bh 107 | HS 108 | млн т 109 | Уун 110 | Ууу 111 | Ууб 112 | |||||||
| Лантаноиды | Ла 57 | CE 58 | Pr 59 | Nd 60 | пм 61 | см 62 | Eu 63 | Gd 64 | Тб 65 | Dy 66 | Ho 67 | Er 68 | Тм 69 | Yb 70 | Лю 71 | ||||
| Актиниды | Ac 89 | Чт 90 | Па 91 | U 92 | НП 93 | Pu 94 | Am 95 | см 96 | Bk 97 | Cf 98 | Es 99 | Фм 100 | мкр 101 | № 102 | Лр 103 | ||||
Цветной ключ:
| Серия | Имя | Недвижимость |
|---|---|---|
| группа 1 или 1a | Щелочные металлы | Один валентный электрон |
| 2 или 2a | Металлы щелочноземельные | Два валентных электрона |
| 3 или 3b | Переходные элементы | |
| Бедные металлы | ||
| Неметаллы | ||
| Металлоиды | ||
| 17 или 7a | Галогены | Семь валентных электронов |
| 18 или 8A | Благородные (инертные) газы | Нет валентных электронов |
| Серия лантанидов | Редкие земли | |
| Серия актинидов | Радиоактивные редкоземельные элементы |
Enchanted Learning ®
Более 35 000 веб-страниц
Примеры страниц для потенциальных подписчиков или щелкните ниже
Нажмите, чтобы прочитать нашу Политику конфиденциальности
Зачарованный поиск обучения
| Найдите на веб-сайте Enchanted Learning: |
Рекламное объявление.
 Рекламное объявление. Рекламное объявление.
Рекламное объявление. Рекламное объявление.Авторские права © 2001-2018 EnchantedLearning.com —— Как процитировать веб-страницу
Сколько периодов в периодической таблице
Здравствуйте, друзья! Как известно, таблица Менделеева – важное понятие в химии и науке. Итак, сегодня мы поговорим о , сколько периодов находится в Периодической таблице. Точка в периодической таблице – это горизонтальный ряд, изображающий элементы с аналогичными химическими свойствами.
В периодической таблице 7 периодов.По мере прохождения каждого периода слева направо элементы демонстрируют схожие химические и физические свойства, а атомный номер элементов увеличивается.
Группы и периоды периодической таблицы
В химии периоды и группы – это два способа классификации элементов. Группы – это вертикальные столбцы в периодической таблице, а периоды – это горизонтальные строки в периодической таблице. Группы и периоды подчиняются определенным правилам в отношении свойств элементов.По мере того, как вы опускаетесь в группе, атомный номер увеличивается. Когда вы перемещаетесь по группе слева направо, атомный номер тоже увеличивается.
Группы и периоды подчиняются определенным правилам в отношении свойств элементов.По мере того, как вы опускаетесь в группе, атомный номер увеличивается. Когда вы перемещаетесь по группе слева направо, атомный номер тоже увеличивается.
Что означают группа и период в периодической таблице
Группы – это вертикальные столбцы в периодической таблице, а периоды – это горизонтальные строки в периодической таблице. Правило, которому следует группа, состоит в том, что все элементы, принадлежащие к одной группе, имеют одинаковую валентность. И все элементы в периоде имеют одинаковое количество атомных орбиталей.
Разница между группой и периодом в таблице Менделеева
Как группами, так и периодами атомный номер увеличивается по мере движения вниз или вправо. В периодической таблице 18 групп, а количество периодов – 8.
Через некоторое время, если двигаться слева направо, элемент теряет свои металлические свойства и становится менее металлическим, чем его предшественник. В то время как группы используются химиками для определения семейства элементов, поскольку они имеют схожие химические свойства и одинаковое количество электронов во внешней оболочке.Например, первая группа (Группа 1) относится к щелочным металлам.
В то время как группы используются химиками для определения семейства элементов, поскольку они имеют схожие химические свойства и одинаковое количество электронов во внешней оболочке.Например, первая группа (Группа 1) относится к щелочным металлам.
Периодическая таблица – Руководство по таблице Менделеева
Руководство по периодической таблице
Автостопом по таблице Менделеева
Внимательно посмотрите на таблицу Менделеева, любимое творение Менделеева. Шутки в сторону. Обратите внимание на цвета, строки, столбцы и символы. Вы когда-нибудь задумывались, почему таблица – это , а – это ? О чем думал старый добрый Дмитрий, когда помещал одни элементы в один ряд, а другие – в другой? Поначалу это может показаться беспорядочным набором цифр и букв, но, действительно, есть средство от безумия.Фактически, можно сказать, что это элементарно, мой дорогой Ватсон.
Организовывать вещи – это человеческая природа. Библиотекари организуют книги. Повара устраивают свои кухни. Кто не тратил время на то, чтобы организовать свои Skittles так, чтобы они точно отражали радугу? Химики ничем не отличаются от всех нас. Ладно, может они немного другие.
Повара устраивают свои кухни. Кто не тратил время на то, чтобы организовать свои Skittles так, чтобы они точно отражали радугу? Химики ничем не отличаются от всех нас. Ладно, может они немного другие.
Периодическая таблица – это инструмент, придуманный химиками для организации всех элементов , которые представляют собой вещества (такие как углерод или водород), которые не могут разлагаться на более простые вещества.Вы могли заметить, что таблица Менделеева выглядит как большая прямоугольная сетка. У каждого элемента есть своя шпаргалка с химической информацией, которая находится в определенном месте в сетке.
Не беспокойтесь, если таблица Менделеева, к которой вы привыкли, не выглядит точно на , как приведенная выше. Каждая таблица Менделеева уникальна. Некоторые содержат больше информации, некоторые меньше. Если навороты модного стола вам не нравятся, остановитесь на более простом столе, таком как этот.
Рассмотрим подробнее индивидуальный ящик таблицы Менделеева. Выберите свой любимый элемент. Кобальт, говорите? Это не было бы нашим первым выбором, но если вы настаиваете. (Шучу. Мы одинаково любим все элементы.)
Выберите свой любимый элемент. Кобальт, говорите? Это не было бы нашим первым выбором, но если вы настаиваете. (Шучу. Мы одинаково любим все элементы.)
Одна часть информации, которую можно найти в каждой периодической таблице, – это атомный номер (расположенный в правом верхнем углу в приведенном выше примере). Это значение, уникальное для каждого элемента, указывает количество протонов, присутствующих в ядре атома. Для кобальта атомный номер 27, потому что все атомы кобальта имеют 27 протонов. Умно, не правда ли?
Все периодические таблицы также содержат химических символа для каждого элемента.Эти символы представляют собой простые двухбуквенные сокращения названий элементов. Для многих элементов символом являются только первые две буквы его названия, например Co для кобальта. Для других элементов символы не так очевидны. Например, химический символ ртути – Hg. Если вам интересно, Hg происходит от латинского слова «hydrargyrum», что означает «жидкое серебро». Очень подходит, если вы спросите нас.
Очень подходит, если вы спросите нас.
Последняя информация, которую можно найти в элементарной ячейке большинства периодических таблиц, – это атомный вес .Как следует из названия, это масса одного атома элемента. Эта информация очень полезна при решении всевозможных задач по химии на экзаменах и викторинах.
Элементы помещаются в определенные места на сетке таблицы Менделеева в соответствии с тем, как они выглядят и действуют. Это создает шаблоны в таблице, называемые периодичностью (подробнее об этом позже). Внутри сетки есть строки и столбцы, которые помогают организовать элементы с похожими свойствами вместе. Итак, было методом безумия Менделеева.
Горизонтальные ряды таблицы Менделеева называются периодами.
Горизонтальные строки периодической таблицы называются периодами . Несмотря на то, что некоторые поля отсутствуют, все строки идут слева направо, пропуская любые пустые области. Каждый элемент в тот же период имеет одинаковое количество атомных орбиталей . Эти орбитали (s, p, d и f) представляют собой область вокруг атома, где с наибольшей вероятностью будут обнаружены его электроны.
Каждый элемент в тот же период имеет одинаковое количество атомных орбиталей . Эти орбитали (s, p, d и f) представляют собой область вокруг атома, где с наибольшей вероятностью будут обнаружены его электроны.
Запутались? Давайте рассмотрим подробнее.
Элементы первого ряда периодической таблицы (одиночные изолированные квадраты в верхнем левом и верхнем правом углах) имеют орбиталь в 1 с, на которой их электроны могут сидеть – все это удобно и уютно. Элементы второй строки периодической таблицы, которая хитроумно названа вторым периодом, имеют одну 1s и три 1p-орбитали, доступные для их валентных электронов . Это электроны, находящиеся на последней оболочке или энергетическом уровне атома. Для элементов пятого периода доступны одна 5s, три 5p и пять 5d орбиталей.
Вертикальные столбцы в периодической таблице называются группами (или семействами).
Вертикальные столбцы в периодической таблице называются группами или семьями (в зависимости от того, кого вы спросите). Самый левый столбец называется первой группой. Следующая группа называется второй. Угадайте, как называется третий столбец? Подсказка: он начинается с группы и заканчивается тремя.
Самый левый столбец называется первой группой. Следующая группа называется второй. Угадайте, как называется третий столбец? Подсказка: он начинается с группы и заканчивается тремя.
Каждый элемент в определенной группе имеет одинаковое количество валентных электронов на своей внешней орбитали.Например, литий (Li) и натрий (Na) являются членами одного клуба. Литий имеет конфигурацию валентных электронов из 2s 1 , в то время как натрий имеет конфигурацию 3s 1 . Это сходство важно, потому что валентные электроны образуют химические связи с другими элементами. Другими словами, элементы одной группы, как правило, проявляют схожую реактивность, не говоря уже о музыкальном вкусе.
Периодическая таблица также разделена на четыре блока: s = красный, p = зеленый, d = желтый и f = синий.
Чтобы еще больше усложнить ваши исследования, таблица Менделеева также разбита на четыре блока . Ознакомьтесь с таблицей выше. Серьезно, проверьте это. Будем ждать.
Серьезно, проверьте это. Будем ждать.
Первые два столбца (показаны красным) составляют s-блок. Следующие 10 столбцов (показаны желтым цветом) составляют d-блок. Мы позволим вам использовать ваши сверхспособности дедукции для определения местоположения p-блока и f-блока. Электроны с самой высокой энергией каждого элемента в блоке принадлежат к одному и тому же атомному орбитальному типу.Другими словами, элементы в s-блоке имеют электроны с наивысшей энергией на s-орбитали, а элементы в d-блоке имеют электроны с наивысшей энергией на d-орбитали.
Элементы главной группы и переходные элементы периодической таблицы Менделеева.
Вы когда-нибудь думали, что одну таблицу можно разделить на столько классификаций? Что ж, мы еще не закончили. Наша любимая таблица также может быть в общих чертах разделена на элемента основной группы и переходных элементов (или переходных металлов ).Элементы основной группы показаны красным в таблице выше, и их свойства легко предсказать, основываясь на их положении в периодической таблице. Элементы перехода показаны желтым цветом, и их свойства не так легко предсказать.
Элементы перехода показаны желтым цветом, и их свойства не так легко предсказать.
Элементы периодической таблицы также можно разделить на металлов, неметаллов и металлоидов . Мы рассмотрим мельчайшие детали каждой колонки в следующих нескольких разделах, но давайте сейчас упростим наш путь в это приключение.
Периодическая таблица Менделеева на металлы, неметаллы и металлоиды.
Металлы занимают левую часть таблицы Менделеева. Обратите внимание на коробки, заштрихованные этими теплыми желтыми и оранжевыми оттенками в таблице выше. Не забудьте и два длинных ряда внизу. Бум. Металлы.
Эти ребята хорошие проводники тепла и электричества, что является причудливым способом сказать, что тепло или электроны могут легко протекать через кусок металла. Другой термин, который обычно используют, когда говорят о металлах, – это пластичность , что означает, что металлы можно измельчать в плоские листы или различные формы. Хорошими примерами металлов, с которыми мы все знакомы, являются железо (Fe), серебро (Ag) и натрий (Na).
Хорошими примерами металлов, с которыми мы все знакомы, являются железо (Fe), серебро (Ag) и натрий (Na).
В правой части таблицы Менделеева расположены неметаллы с хитроумными названиями, сияющие в своих голубых, розовых и пурпурных тонах. Эти элементы обладают более разнообразными свойствами, чем их металлические собратья. Некоторые из них представляют собой твердые вещества при комнатной температуре, например углерод (C), в то время как другие, такие как гелий (He) и кислород (O), являются газами. Неметаллы обычно плохо проводят тепло и электричество.
Элементы, расположенные в этом причудливом зигзаге, называются металлоидами.В приведенной выше таблице Менделеева они заштрихованы зеленым. Эти элементы не являются ни металлами, ни неметаллами, но обладают некоторыми общими свойствами с обеими группами. Например, металлоиды могут проводить электричество, как металлы. Кремний (Si) – превосходный пример металлоидного элемента.
Кремний (Si) представляет собой металлоид. Изображение отсюда.
Изображение отсюда.
Мы не будем вдаваться в подробности о f-блоке в этом модуле, но вам важно знать, что здесь расположены два типа соединений.Первый ряд f-блока содержит лантаноиды. Во втором ряду находятся актиниды.
Brain Snack
Единственная буква, которой нет нигде в периодической таблице, – это J.
Периодическая таблица: это элементарно!
Издание 1963 года «Периодической диаграммы атомов» Генри Хаббарда и Уильяма Меггерса из NIST. Обратите внимание, что он включает нейтрон, который сейчас не считается атомом.
Кредит: Смитсоновский национальный музей американской истории
Из всего множества полезных и интересных периодических таблиц в Интернете – периодических таблиц животных, овощей и минералов – и U.S. Presidents, приправы для хот-догов в стиле Vienna® в чикагском стиле, объекты динамического управления SQL-сервером и палео-еда – исходная Периодическая таблица элементов остается моим фаворитом.
Кодировку TIFF NIST SP 966 можно легко преобразовать в инструкции для жаккардового ткацкого станка для производства тканого хлопкового одеяла, изображенного здесь со стандартным домашним котом для измерения размеров.
Кредит: К. В. Кларк / NIST
Есть даже новая игра «Морской бой с периодической таблицей», которая была разработана, чтобы научить детей свойствам элементов.Вы можете загрузить специальную публикацию NIST 966, чтобы получить для этого игровые доски. Код NIST SP 966 также может быть отправлен непосредственно производителям из частного сектора для создания множества полезных вещей, таких как Periodic Blanket of the Elements.
Это не только мое. В то время как таблица умножения и таблицы логарифмов в значительной степени забыты, мем, который предпочитают поставщики приправ для хот-догов или SQL-DMO, – это Периодическая таблица элементов!
УчастиеNIST в Периодической таблице началось в первые дни существования Национального бюро стандартов (NBS), под которым, за исключением короткого периода, когда мы были просто Бюро стандартов, NIST был известен как с 1901 по 1988 год.Тем не менее, первый секретарь NBS, Генри Д. Хаббард, проявил личный интерес к этой теме и разработал представление «Периодической диаграммы атомов». Таблица Хаббарда, отредактированная пионером в области спектроскопии NIST Уильямом Меггерсом, позже была широко распространена компанией Welch Scientific Company, и ее до сих пор можно найти в университетских лекционных залах и лабораториях по всему миру.
За прошедшие годы названия некоторых элементов изменились, были добавлены новые элементы, а иногда и отзывались.(Что значит, вы никогда не слышали о мазуриуме, колумбиуме, иллинии, алабамине или виргинии?)
Нейтрон сохраняет свое полюсное положение на Карте радионуклидов, показанной здесь с Магдаленой Наварро и Биллом Гадзуком.
Кредит: К. В. Кларк / NIST
ИЮПАК все еще занят, подтвердив существование элементов 113, 115, 117 и 118 в конце 2015 года. В то же время он рассматривает изменение правил именования, которое открыто для комментариев до конца. этого месяца.Новые правила требуют, чтобы имена только 113 и 115 заканчивались на ium. Это дало бы толпе Беркли только один шанс на то, что им нужно для «Lawrencium Berkelium Laboratorium».
Элементы, недавно названные Международным союзом теоретической и прикладной химии (IUPAC), – это флеровий (114) и ливерморий (116). Крупными победителями в целом, похоже, являются области залива Сан-Франциско – берклий, калифорний, лоуренсий, сиборгий и ливерморий – и Швеция – иттрий, нобелий и целая куча редкоземельных элементов.
Другая табличная структура элементов – Карта радионуклидов – имеет свой впечатляющий памятник в кампусе NIST в Гейтерсбурге. По форме похожая на Лонг-Айленд, диаграмма должна быть разрезана на три части, чтобы ее можно было удобно отображать даже на большой странице (на фотографии показан только ее бруклинский конец).
Может быть, это – или тот факт, что большинство его записей радиоактивны – поэтому он еще не захватил общественное воображение, как Периодическая таблица.
И, пока я не забыл, поздравляю всех с (запоздалым) Днем Национальной таблицы Менделеева!
Разрушение Периодической таблицы
Периодическая таблица Менделеева является важным ресурсом для всех студентов-химиков, поскольку она предоставляет вам жизненно важную информацию, которая понадобится вам для решения множества задач.Следовательно, вам необходимо ознакомиться с ним и научиться читать его быстро и точно. Чем лучше вы будете извлекать информацию из таблицы Менделеева, тем лучше вы станете разбираться в химии в целом.
Таблица Менделеева содержит более сотни различных элементов, и на первый взгляд не всегда легко найти закономерности. К счастью, периодическая таблица Менделеева разработана так, чтобы быть систематизированной, и вы можете быстро научиться читать ее, используя несколько распространенных стратегий.
Но сначала важно понять, что такое таблица Менделеева, и ознакомиться с некоторыми ее ключевыми характеристиками.
Периодическая таблица Менделеева, также известная как Периодическая таблица элементов, представляет собой диаграмму, которая отображает все известные химические элементы в организованном и систематическом виде. В настоящее время в периодической таблице представлены 118 различных элементов, каждый со своей структурой, свойствами и характеристиками.
Строки периодической таблицы известны как периоды, всего их 7 периодов, каждый из которых содержит разное количество элементов.
Первый период содержит только два: водород (H) и гелий (He). Второй и третий периоды содержат по 8 элементов каждый, а четвертый и пятый периоды содержат по 18 элементов.
Последние два периода в некоторой степени уникальны, потому что они содержат ряды лантанидов и актинидов. Ряд лантанидов включает элементы с атомными номерами от 57 до 71 и находится между барием и лютецием в шестом периоде. Точно так же ряд актинидов включает элементы с атомными номерами от 89 до 102 и находится между радием и лоуренсием в седьмом периоде.
Ряды лантанидов и актинидов
Ряды лантанидов и актинидов обычно представлены в виде двух отдельных строк под основной периодической таблицей и представляют собой внутренние переходные металлы. Ряд лантанидов включает такие элементы, как лантан (La), европий (Eu) и иттербий (Yb), а ряд актинидов включает такие элементы, как уран (U), плутоний (Pu) и даже эйнштейний (Es)!
Все элементы одного периода имеют одинаковое количество электронных оболочек.Здесь хранятся электроны внутри элемента. Номер строки соответствует количеству электронных оболочек внутри каждого элемента в этой строке. Например, водород и гелий имеют по одной электронной оболочке, в то время как литий, углерод и фтор во втором ряду имеют по две электронные оболочки.
По мере того, как вы перемещаетесь по периоду слева направо, количество протонов (субатомных частиц с положительным зарядом) увеличивается. Это называется «чтением за период».
Столбцы в периодической таблице известны как группы, всего их 18 групп.Элементы одной группы обладают рядом физических и химических свойств.
Элементы одной группы имеют одинаковое количество электронов на внешней электронной оболочке. Это означает, что их ионы будут иметь одинаковый положительный или отрицательный заряд. Например, натрий (Na) и калий (K) входят в группу 1, имеют 1 электрон на своей внешней оболочке и теряют 1 электрон, образуя катион. Следовательно, они станут ионами Na + и K + с зарядом +1.
Элементы в одной группе также одинаково реагируют на вещи. Например, элементы группы 1 известны как «щелочные металлы» и, как известно, взрываются при контакте с водой. Возможно, вы видели, как ваш учитель химии проводил этот эксперимент в лаборатории: когда вы бросаете кусок металлического лития, натрия или калия в ванну с водой, они вызывают взрывоопасную реакцию.
Это связано с тем, что электроны из металла текут в окружающую воду, образуя гидроксид и газообразный водород, в чрезвычайно быстрой реакции, которая производит значительное количество тепла.Другие эксперименты покажут, что элементы в других группах также обладают похожими друг на друга свойствами.
Чтение отдельных элементов
У каждого отдельного элемента есть свой блок элементов, который содержит важную информацию о нем, которая отличает его от других элементов. Вы также можете сформировать свои собственные выводы на основе информации, приведенной в этом поле. Как правило, в каждую ячейку элемента включены четыре важных элемента информации.
Это небольшое число в верхней части поля, обозначающее количество протонов или электронов в атоме. Каждый атом содержит одинаковое количество протонов и электронов, пока он не ионизируется за счет увеличения или уменьшения количества электронов.
Буква или пара букв непосредственно под атомным номером является химическим символом элемента. Обычно это сокращенная форма имени элемента; например, химический символ лития – Li. Однако некоторые химические символы вообще не являются производными от общепринятого названия элемента; например, химический символ вольфрама – W (первая буква латинского названия элемента «Вольфрам»).Следовательно, важно ознакомиться с химическими символами наиболее часто встречающихся элементов.
Это полное название элемента, расположенного под химическим символом. Это имя, которым обычно называют элемент.
Наконец, атомная масса – это небольшое число в нижней части прямоугольника элемента, указывающее среднюю массу всех изотопов элемента (атомов и ионов). Из-за различий в процентном содержании изотопов каждого элемента это обычно десятичное число, а не целое.Это приблизительная оценка количества протонов и нейтронов в ядре атома.
Периодическая таблица Менделеева организована систематически, чтобы вы могли быстро собирать информацию. Вот несколько важных шаблонов, которые помогут вам быстрее и проще обращаться к таблице.
Металлы, металлоиды и неметаллы
За исключением водорода, элементы, расположенные ближе к левой части таблицы Менделеева, являются металлами, а элементы ближе к правой стороне – неметаллами.Металлоиды, которые служат переходом между ними, включают бор (B), кремний (Si) и сурьму (Sb).
Шесть благородных газов находятся в группе 18, самом последнем столбце периодической таблицы. Это гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn). Они образуют группу, потому что все они без запаха, цвета и низкой реакционной способности.
5 галогенов входят в группу 17 и включают фтор (F), хлор (Cl), бром (Br), йод (I) и астат (At).Название «галоген» означает «солеобразование», а 5 галогенов образуют широкий спектр солей, когда они реагируют с металлами.
Элементы с атомными номерами от 1 до 94 считаются встречающимися в природе; то есть их можно найти в природе без необходимости синтеза. Элементы с атомными номерами от 95 до 118 не встречаются в природе, а существуют, потому что они были успешно синтезированы в лабораториях, ядерных реакторах и ядерных взрывах.
Эти стратегии дают хороший обзор того, как читать таблицу Менделеева.Однако дополнительную информацию можно получить из таблицы Менделеева, которая может служить непосредственным наглядным руководством для других глав, дополнительно помогая учащимся применять информацию во время экзаменов. Если вы все еще не знаете, как это разбить, Академия наук найдет для вас решение. Наши курсы химии O Level классов помогли бесчисленному количеству студентов овладеть этим предметом, а также развить глубокую страсть к химии.
Обладая более чем 20-летним совместным опытом, наши опытные преподаватели по естествознанию стремятся помочь нашим студентам получить максимальную отдачу от естественнонаучного образования и привить им страсть к общим наукам, физике, химии и биологии.
Периодический закон
Периодический закон – Почему ученые и химики используют Периодический закон?
Периодический закон используется учеными и химиками во всем мире для систематического упорядочивания физической и химической информации о химических элементах.
Периодический закон – Что такое периодический закон?
Определение: Периодический закон – это принцип, согласно которому определенные свойства элементов встречаются периодически при упорядочении по атомному номеру .
Происхождение периодического закона – Как возникло периодическое право?
В 1869 году русский химик Дмитрий Менделеев разработал совершенно новый метод классификации элементов, который он назвал «периодической таблицей». В том же году немецкий ученый Лотар Мейер независимо предложил те же идеи. Эта договоренность пролила свет на большое обобщение, известное теперь как Периодический закон.Дмитрий Менделеев включил все 65 элементов, известных в его эпоху по их атомному весу и химической валентности. Такие закономерности очень упрощают изучение химии. Тщательное изучение одного элемента в группе элементов значительно упрощает изучение других членов группы, поскольку многие свойства и химические реакции элементов схожи.
Дмитрий Менделеев (1834-1907), разработавший Периодический закон
Происхождение периодического закона – Генри Мозли изменяет Периодический закон
В 1913 году английский ученый Генри Мозли (1887-1915) определил атомный номер каждого из элементов и соответственно изменил «Периодический закон».Мозли понял, что когда атомы располагаются в соответствии с возрастающим атомным номером, некоторые проблемы с периодической таблицей, разработанной Дмитрием Менделеевым, исчезают. Благодаря работе Генри Мозли, современная таблица Менделеева основана на атомных номерах элементов.
Генри Мозли (1887-1915), который изменил Периодический закон
Что такое атомный номер? Периодический закон
Периодический закон гласит, что физические и химические свойства элементов повторяются периодически в систематическом и предсказуемом порядке , когда элементы расположены в порядке возрастания атомного номера.Таким образом, Периодическая таблица расположена на в порядке возрастания атомных номеров в соответствии с Периодическим законом после модификации Генри Мозли. Далее Периодический закон можно объяснить, сравнивая химические и физические свойства элементов.
Периодическая таблица и периодический закон исправляют ошибки
Физические константы многих элементов сначала не согласовывались с требуемыми периодическим законом, и дальнейшее изучение многих таких случаев показало, что были допущены ошибки.Таким образом, Периодический закон оказал большую услугу в указании вероятных ошибок.
Периодический закон – Современные применения Периодического закона
Когда периодический закон был впервые сформулирован, когда Дмитрий Менделеев развивал свою теорию, в таблице было несколько свободных мест, которые, очевидно, принадлежали элементам, которые в то время были неизвестны. По их положению в таблице Дмитрий Менделеев предсказал с большой точностью свойства элементов, которые, как он был уверен, однажды будут обнаружены, чтобы заполнить эти места.В таблице все еще есть свободные места, особенно среди более тяжелых элементов. Периодический закон позволяет современным ученым включать вновь открытые элементы в Периодическую таблицу.
Периодический закон – процесс разработки научной теории
Следующая блок-схема иллюстрирует процесс разработки научной теории. Этому процессу следуют все ученые и химики, включая Дмитрия Менделеева и Генри Мозли, которые сформулировали Периодический закон.

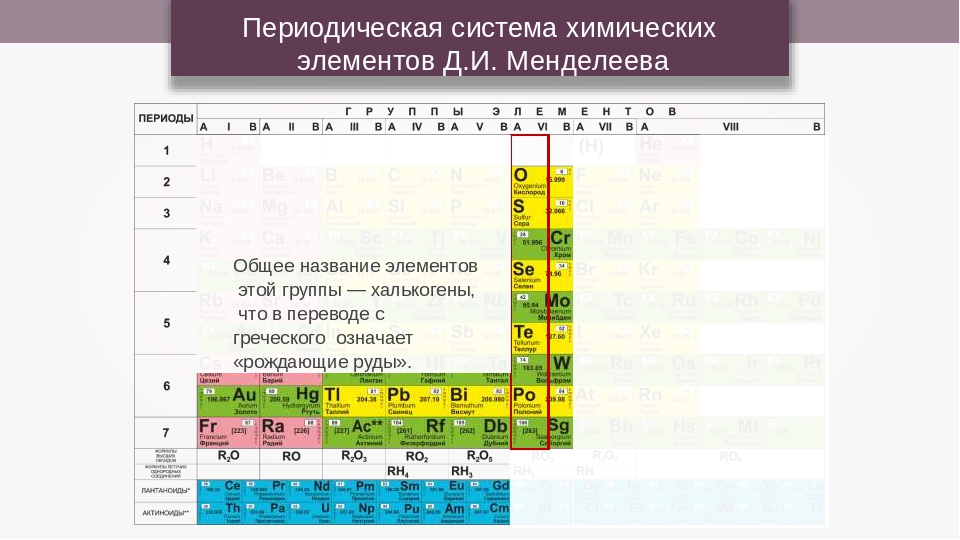 Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). Всего предложено несколько сотен вариантов изображения периодической системы (аналитических кривых, таблиц, геометрических фигур и т. п.). В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). Всего предложено несколько сотен вариантов изображения периодической системы (аналитических кривых, таблиц, геометрических фигур и т. п.). В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.