Порядковый номер элемента в таблице Д. И. Менделеева равен 35. Химия. 8 класс. Габриелян. ГДЗ. § 7. Глава 1. Вопрос 4. – Рамблер/класс
Порядковый номер элемента в таблице Д. И. Менделеева равен 35. Химия. 8 класс. Габриелян. ГДЗ. § 7. Глава 1. Вопрос 4. – Рамблер/классИнтересные вопросы
Школа
Подскажите, как бороться с грубым отношением одноклассников к моему ребенку?
Новости
Поделитесь, сколько вы потратили на подготовку ребенка к учебному году?
Школа
Объясните, это правда, что родители теперь будут информироваться о снижении успеваемости в школе?
Школа
Когда в 2018 году намечено проведение основного периода ЕГЭ?
Новости
Будет ли как-то улучшаться система проверки и организации итоговых сочинений?
Вузы
Подскажите, почему закрыли прием в Московский институт телевидения и радиовещания “Останкино”?
Помогите с вопросом.
ответы
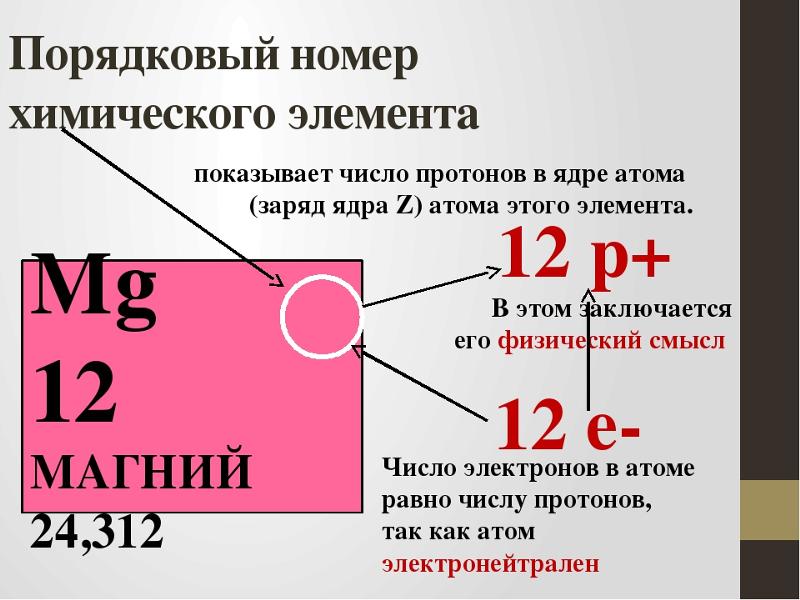
Элемент с порядковым номером 35 — это бром (Вг). Заряд ядра его
атома равен 35. Атом брома содержит 35 протонов, 35 электронов и 45 нейтронов.
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
Психология
ЕГЭ
10 класс
9 класс
похожие вопросы 5
Попробуйте провести следующий опыт. Влияние воздуха на горение свечи.
Вставьте стеклянную трубку с оттянутым концом в резиновую (Подробнее. ..)
..)
ГДЗШкола8 классХимияГабриелян О.С.
Приготовление раствора сахара и расчёт его массовой доли в растворе. Химия. 8 класс. Габриелян. ГДЗ. Хим. практикум № 1. Практ. работа № 5.
Попробуйте провести следующий опыт. Приготовление раствора
сахара и расчёт его массовой доли в растворе.
ГДЗШкола8 классХимияГабриелян О.С.
Здравствуйте.
(Подробнее…)
Химия
Это правда, что будут сокращать иностранные языки в школах?
Хочется узнать, когда собираются сократить иностранные языки в школе? Какой в итоге оставят? (Подробнее…)
ШколаНовостиИностранные языки
11. Выпишите слово, в котором на месте пропуска пишется буква Е. Русский язык ЕГЭ-2017 Цыбулько И. П. ГДЗ. Вариант 12.
11.
Выпишите слово, в котором на месте пропуска пишется буква Е.
произнос., шь (Подробнее.
ГДЗЕГЭРусский языкЦыбулько И.П.
АТОМНЫЙ НОМЕР – это что такое АТОМНЫЙ НОМЕР
Значение слова “АТОМНЫЙ НОМЕР” найдено в 28 источниках
найдено в “Большой Советской энциклопедии”
порядковый номер химического элемента в периодической системе элементов (См. Периодическая система элементов) Д. И. Менделеева. А. н. равен числу протонов в атомном ядре, которое, в свою очередь, равно числу электронов в электронной оболочке соответствующего нейтрального атома. А. н. обозначается через Z. Заряд ядра равен
найдено в “Большой советской энциклопедии”
АТОМНЫЙ НОМЕР, порядковый
номер хим. элемента в периодической системе элементов Д. И. Менделеева.
А. н. равен числу протонов в атомном ядре, к-рое, в свою очередь, равно
числу электронов в электронной оболочке соответствующего нейтрального атома. А. н. обозначается через Z. Заряд ядра равен Ze, где е – положит. элементарный
электрич, заряд, равный по абс. значению заряду электрона.
А. н. обозначается через Z. Заряд ядра равен Ze, где е – положит. элементарный
электрич, заряд, равный по абс. значению заряду электрона.
найдено в “Научно-техническом энциклопедическом словаре”
АТОМНЫЙ НОМЕР (обозначение Z), число протонов в ядре атома элемента, равное числу электронов, движущихся вокруг этого ядра. Атомный номер ставят в виде нижнего индекса перед символом элемента; например, атомный номер углерода записывается как 6С. Атомный номер определяет химические свойства элемента и его положение в периодической таблице. У всех изотопов элемента один и тот же атомный номер, но разные атомные массы, поскольку число нейтронов у них различно.
найдено в “Физической энциклопедии”
(порядковый номер) номер элемента в периодической системе элементов. Равен числу протонов в ат. ядре. Определяет химические и большинство физических св-в атома.
Физический энциклопедический словарь. — М.: Советская энциклопедия.Главный редактор А. М. Прохоров.1983.
Прохоров.1983.
найдено в “Большом энциклопедическом политехническом словаре”
порядковый номер Z хим. элемента в периодической системе элементов Менделеева. Определяет число протонов в атомном ядре и его электрич. заряд, равный Ze, где е – заряд протона (численно равный заряду электрона), а также число электронов в нейтральном атоме.
найдено в “Метеорологическом словаре”
Число элементарных положительных зарядов (протонов) в ядре атома; равно числу электронов в нейтральном атоме этого элемента. А. Н. определяет место элемента в периодической системе Менделеева.
Синоним: атомное число.
найдено в “Современном энциклопедическом словаре”
АТОМНЫЙ НОМЕР (порядковый номер), Z, номер химического элемента в периодической системе элементов. Равен числу протонов в атомном ядре и определяет химические и большинство физических свойств атома.
найдено в “Большом Энциклопедическом словаре”
АТОМНЫЙ НОМЕР (порядковый номер) – Z, номер химического элемента в периодической системе элементов.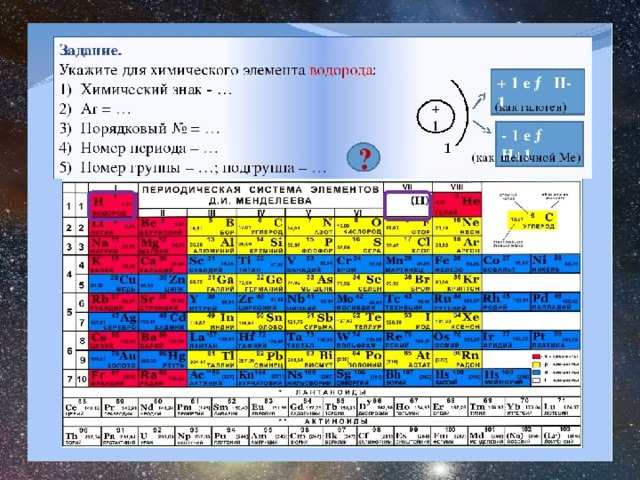
найдено в “Современной энциклопедии”
АТОМНЫЙ НОМЕР, порядковый номер химического элемента в периодической системе элементов. Равен числу протонов в атомном ядре, определяет химические и большинство физических свойств атома.
найдено в “Иллюстрированном энциклопедическом словаре”
НОМЕР, порядковый номер химического элемента в периодической системе элементов. Равен числу протонов в атомном ядре, определяет химические и большинство физических свойств атома.
найдено в “Большом энциклопедическом словаре”
– (порядковый номер) – Z, номер химического элемента впериодической системе элементов. Равен числу протонов в атомном ядре иопределяет химические и большинство физических свойств атома.
найдено в “Естествознании. Энциклопедическом словаре”
(порядковый номер), Z, номер хим. элемента в периодич. системе элементов. Равен числу протонов в атомном ядре и определяет хим. и большинство физ. свойств атома.
системе элементов. Равен числу протонов в атомном ядре и определяет хим. и большинство физ. свойств атома.
найдено в “Терминах атомной энергетики”
Atomic number
номер химического элемента в периодической системе элементов; равен числу протонов в атомном ядре.
Термины атомной энергетики. – Концерн Росэнергоатом,2010
АБВГДЕЁЖЗИЙКЛМНОПРСТУФХЦЧШЩЪЫЬЭЮЯ
ABCDEFGHIJKLMNOPQRSTUVWXYZ
электронных конфигураций
электронных конфигураций Следующее содержание является сутью лекции по общей химии 26. В этой лекции мы продолжаем обсуждение квантовых чисел и их использования в электронных конфигурациях, а также отношения электронной конфигурации к периодическим свойствам элементов.
Электронная конфигурация
Конфигурации электронов — это сводка того, где электроны находятся вокруг ядра. Как мы узнали ранее, каждый нейтральный атом имеет количество электронов, равное количеству его протонов. Теперь мы поместим эти электроны в такое расположение вокруг ядра, которое укажет на их энергию и форму орбитали, на которой они расположены. Вот краткое изложение типов орбиталей и количества электронов, которые каждая из них может содержать:
Итак, основываясь на том, что мы знаем о квантовых числах, и используя приведенную выше таблицу, вам нужно 2 электрона, чтобы заполнить s-орбиталь, 6 электронов, чтобы заполнить p-орбиталь, 10 электронов, чтобы заполнить d-орбиталь, и 14 электронов, чтобы заполнить f-орбиталь. НО то, что мы не обсуждали, так это то, как эти орбитали заполняются… порядок заполнения.
Порядок заполнения
Порядок, в котором электроны размещаются на орбиталях, основан на порядке их энергии. Это называется принципом Ауфбау. Первыми заполняются самые низкоэнергетические орбитали. Как и сами квантовые числа, этот порядок был определен расчетным путем и представлен следующей диаграммой:
Это называется принципом Ауфбау. Первыми заполняются самые низкоэнергетические орбитали. Как и сами квантовые числа, этот порядок был определен расчетным путем и представлен следующей диаграммой:
или вы можете просто использовать периодическую таблицу:
Как написать электронную конфигурацию
Символы, используемые для записи электронной конфигурации, начинаются с номера оболочки (n), за которым следует тип орбитали, и, наконец, верхний индекс указывает, сколько электронов находится на орбитали.
Например:
Глядя на периодическую таблицу, вы видите, что кислород имеет 8 электронов. Основываясь на приведенном выше порядке заполнения, эти 8 электронов заполнили бы следующий порядок 1s, 2s и затем 2p. Таким образом, электронная конфигурация кислорода будет O 1s 2 2s 2 2p 4 .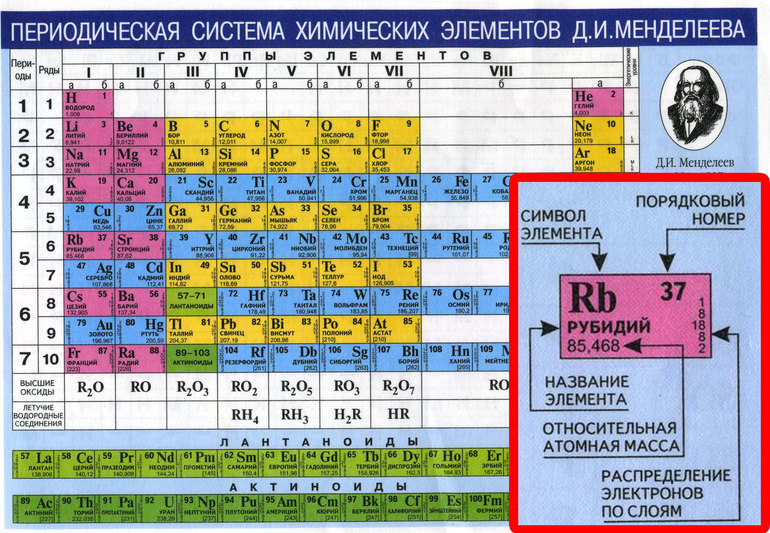
Особые случаи
Конфигурации ионов представляют собой частный случай электронной конфигурации, а также в первую очередь демонстрируют причину образования этих ионов.
Если вам нужно записать полную электронную конфигурацию для аниона , то вы просто добавляете дополнительные электроны, и конфигурация просто продолжается.
Например, мы знаем, что кислород всегда образует 2-ионы, когда он образует ион. Это добавит 2 электрона к его нормальной конфигурации, создав новую конфигурацию: O 2- 1с 2 2с 2 2п 6 . Следует отметить, что с 10 электронами электронная конфигурация кислорода теперь точно такая же, как у неона. Мы говорили о том, что ионы образуются, потому что они могут стать более стабильными с присоединением или потерей электронов, чтобы стать похожими на благородные газы, и теперь вы можете увидеть, как они становятся такими же.
Электронные конфигурации катионов также основаны на количестве электронов, но есть небольшая разница в способе их конфигурации. Сначала вы должны написать их нормальную электронную конфигурацию, а затем, когда вы удаляете электроны, вы должны брать их с самой внешней оболочки. Обратите внимание, что это не всегда тот же способ, которым они были добавлены.
Вот пример того, что я имею в виду:
Железо имеет 26 электронов, поэтому его нормальная электронная конфигурация будет следующей: Fe 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6
Когда мы создаем ион 3+ для железа, нам нужно сначала взять электроны из самой внешней оболочки, чтобы это была оболочка 4s, а не оболочка 3d: Fe 3+ 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5
Еще одно замечание по записи электронных конфигураций: короткий путь. При написании некоторых конфигураций нижних таблиц общая конфигурация может быть довольно длинной. В этих случаях вы можете использовать предыдущий благородный газ для сокращения конфигурации, как показано ниже. Вам просто нужно закончить конфигурацию, откуда выходит благородный газ:
При написании некоторых конфигураций нижних таблиц общая конфигурация может быть довольно длинной. В этих случаях вы можете использовать предыдущий благородный газ для сокращения конфигурации, как показано ниже. Вам просто нужно закончить конфигурацию, откуда выходит благородный газ:
Исключения
Как и в случае с любой другой темой, которую мы рассмотрели на сегодняшний день, существуют исключения из порядка заполнения. Но, исходя из генерируемых электронных конфигураций, эти исключения легко понять.
В блоке d, особенно в группах, содержащих хром и медь, есть исключение в том, как они заполняются.
Вот актуальные конфигурации:
В этих столбцах 4s и 3d
Практика, Практика, Практика
Здесь есть множество викторин по электронным конфигурациям, с которыми вы можете попрактиковаться
Орбитальные диаграммы
Еще один способ представить порядок заполнения атома — использовать орбитальную диаграмму, которую часто называют «маленькими квадратиками»:
Прямоугольники используются для представления орбиталей и для отображения размещенных на них электронов.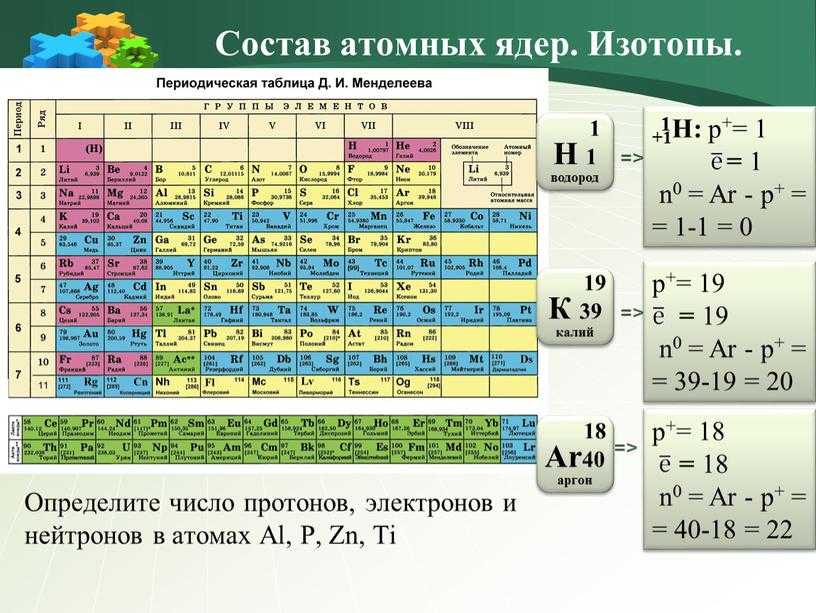 Порядок заполнения тот же, но, как вы можете видеть сверху, электроны помещаются в ящики по одному, прежде чем заполнить их обоими электронами. Это называется правилом Хунда: «Заполните наполовину, прежде чем заполнить полностью», и снова это правило было установлено на основе расчетов энергии, которые показали, что именно так атомы фактически распределяют свои электроны по орбиталям.
Порядок заполнения тот же, но, как вы можете видеть сверху, электроны помещаются в ящики по одному, прежде чем заполнить их обоими электронами. Это называется правилом Хунда: «Заполните наполовину, прежде чем заполнить полностью», и снова это правило было установлено на основе расчетов энергии, которые показали, что именно так атомы фактически распределяют свои электроны по орбиталям.
Периодические свойства
Одна из действительно крутых особенностей электронных конфигураций — их связь с периодической таблицей. В основном периодическая таблица была построена таким образом, чтобы элементы с одинаковыми электронными конфигурациями были выровнены в одни и те же группы (столбцы).
Периодическая таблица, показывающая последнюю заполненную орбиту для каждого элемента
Периодическая таблица, показанная выше, демонстрирует, как конфигурация каждого элемента была выровнена так, чтобы последняя заполненная орбиталь была такой же, за исключением оболочки.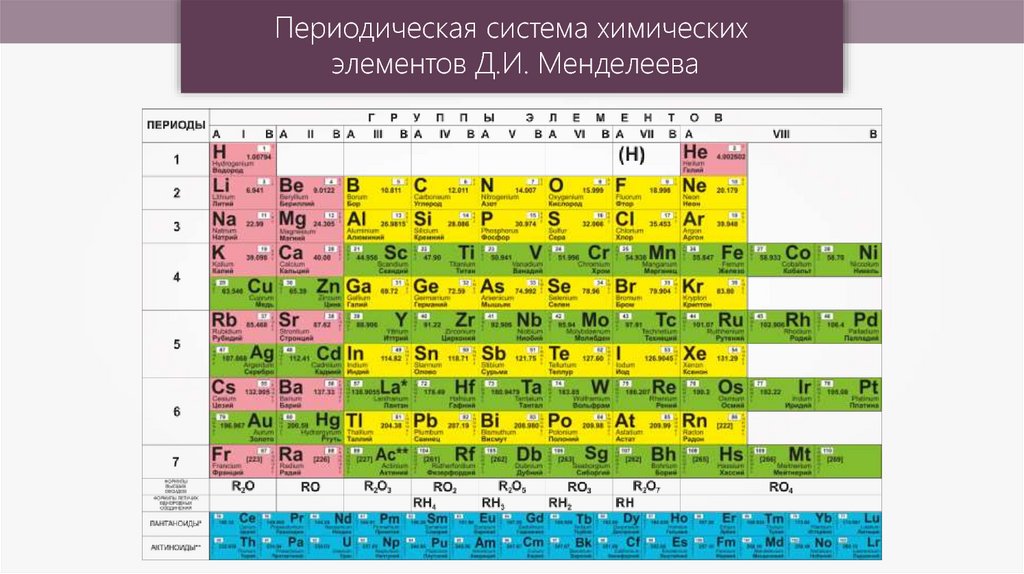 Причина, по которой это было сделано, заключается в том, что конфигурация элемента придает элементу его свойства, а аналогичные конфигурации дают аналогичные свойства.
Причина, по которой это было сделано, заключается в том, что конфигурация элемента придает элементу его свойства, а аналогичные конфигурации дают аналогичные свойства.
Давайте рассмотрим некоторые периодические свойства, на которые напрямую влияет электронная конфигурация:
Размер атома
Размер атомов увеличивается вниз по таблице Менделеева. Это должно быть интуитивно понятно, поскольку с каждой строкой таблицы вы добавляете оболочку (n). Что не так интуитивно понятно, так это то, почему размер уменьшается слева направо. Но опять же построение электронной конфигурации дает нам ответ. Что вы делаете, просматривая периодическую таблицу? Ответить, добавляя протоны к ядру и добавляя электроны к валентной оболочке элемента. Что не меняется, когда вы пересекаете период? Ответ: электроны внутренней оболочки. Подумайте об этом так: электроны внутренней оболочки являются защитой от притяжения ядра. Так, например, сила притяжения Sulphur будет равна Z Eff = 16 – 10 = +6 |
Электроотрицательность
Электроотрицательность может быть самым важным из периодических свойств, которые вы можете изучить и понять, так как многие другие свойства зависят от его значения. Электроотрицательность — это способность атомов притягивать к себе электроны.
Электроотрицательность — это способность атомов притягивать к себе электроны.
Электроотрицательность обычно выражается по шкале Полинга, и значения были определены экспериментально. В таблице ниже показаны значения шкалы для элементов.
Значения электроотрицательности увеличиваются слева направо и снизу вверх в периодической таблице, за исключением благородных газов. Наиболее электроотрицательным элементом является фтор.
Из этих значений электроотрицательности мы можем вывести модели двух других периодических свойств: энергии ионизации и сродства к электрону.
Энергия ионизации Энергия ионизации — это количество энергии, необходимое для отрыва электрона от атома. Все энергии ионизации являются положительными значениями, потому что все эти удаления (даже для элементов, образующих положительные ионы) требуют ввода энергии. Чем более электроотрицательный элемент, тем выше энергия ионизации. | |
Электронное сродствоЭлектронное сродство элемента — это количество энергии, полученное или высвобожденное при добавлении электрона. Электроотрицательность и сродство к электрону увеличиваются по той же схеме в периодической таблице. Слева направо и снизу вверх. |
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА АРОМАТОВ Торговая марка
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА АРОМАТОВ — Сведения о торговой марке
Статус: 602 – Отказ от ответа или поздний ответ
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА ВКУСОВ
Статус
602 – Заброшенный -Отказ от ответа или поздний ответ
Дата статуса
18.03.2015
Дата подачи
30.08.2013
90 002 Маркировка Чертеж3000 – Иллюстрация: рисунок или дизайн, который также включает слово(а)/букву(а)/цифру(а) Typeset
Design Searches
200308 – Миллиметровая бумага, диаграммы, чертежи, таблица Менделеева.
Имя адвоката
Benjamin C. Armitage
Код присвоенного местонахождения адвокатского бюро
L20
Имя сотрудника 9 0003
БУЛТОН, КЕЛЛИ Ф
Классификационная информация
Международный класс
043 – Услуги по обеспечению продуктами питания и напитками; временное проживание. – услуги по обеспечению едой и питьем; временное проживание.
Коды классов США
100, 101
Код статуса класса
6 – Активный
Класс Статус Дата
10.09.2013
Основной код
043
Дата первого использования в любом месте
16.12.2011
Дата первого использования в коммерческих целях
16.12.2011 9 0003
Корреспонденция
Имя
БЕНДЖАМИН С АРМИТИДЖ
Адрес
Пожалуйста, войдите в свою учетную запись Justia, чтобы увидеть этот адрес.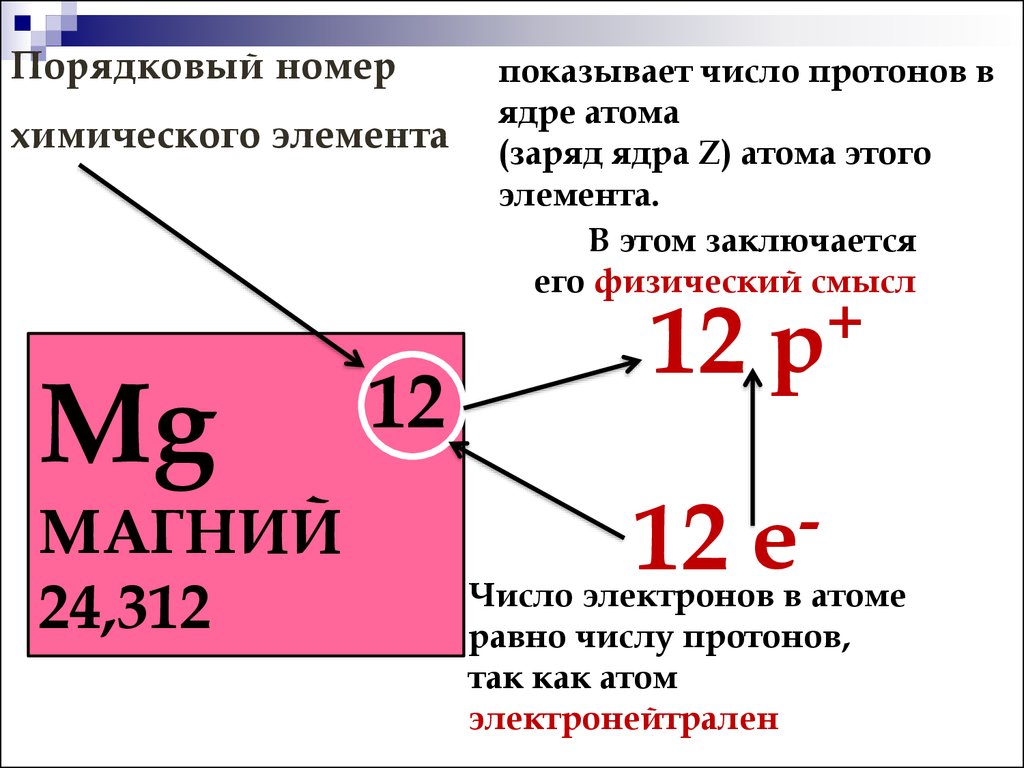
События товарных знаков
| Дата события | Описание события |
| 03.09.2013 | НОВАЯ ЗАЯВКА В ТРАМВАЙ |
| 10.09.2013 | 9015 2 НОВЫЙ ЗАЯВИТЕЛЬНЫЙ ОФИС ДАННЫЕ, ПРЕДОСТАВЛЕННЫЕ В TRAM|
| 2013-09-11 | УВЕДОМЛЕНИЕ О ПРОЕКТЕ КОД ПОИСКА ПО ЭЛЕКТРОННОЙ ПОЧТЕ |
| 13.12.2013 | НАЗНАЧЕН ЭКСПЕРТУ |
| 19.12.2013 | 9 0152 НЕЗАКОНЧИТЕЛЬНОЕ ДЕЙСТВИЕ НАПИСАНО|
| 2013-12-19 | НЕОКОНЧАТЕЛЬНОЕ РЕШЕНИЕ ОТПРАВЛЯЕТСЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ |
| 19.12.2013 | УВЕДОМЛЕНИЕ О НЕОКОНЧАТЕЛЬНОМ РЕШЕНИИ ПО ЭЛЕКТРОННОЙ ПОЧТЕ |
| 2014-0 4-23 | TEAS ОТВЕТ НА ПОЛУЧЕННЫЙ ДЕЙСТВИЕ ОФИСА |
| 23.04.2014 | ПЕРЕПИСКА, ПОЛУЧЕННАЯ В ЮРИДИЧЕСКОЙ КОНТОРЕ |
| 24.04.2014 | TEAS/ПОЧТОВАЯ ПЕРЕПИСКА ПОЛУЧЕНА |
| НЕОКОНЧАТЕЛЬНОЕ РЕШЕНИЕ ПИСЬМЕННО | |
| 2014- 05-02 | НЕОКОНЧАТЕЛЬНОЕ РЕШЕНИЕ ПО ЭЛЕКТРОННОЙ ПОЧТЕ |
02. |

 Когда вы пересекаете период и увеличиваете количество протонов в ядре, вы увеличиваете его притяжение, но поскольку вы только добавляете электроны в новую оболочку, экран не увеличивается, а остается неизменным на всем протяжении. Это означает, что притяжение электронов, добавляемых к валентной оболочке, неуклонно увеличивается на всем протяжении. Что произойдет, если вы потянете электроны сильнее? Ну, они приближаются к ядру и размер атома уменьшается. Эффект притяжения ядра на электроны, добавляемые за период, называется эффективным зарядом ядра и рассчитывается как Z Eff = #протоны – Ядро # Электроны.
Когда вы пересекаете период и увеличиваете количество протонов в ядре, вы увеличиваете его притяжение, но поскольку вы только добавляете электроны в новую оболочку, экран не увеличивается, а остается неизменным на всем протяжении. Это означает, что притяжение электронов, добавляемых к валентной оболочке, неуклонно увеличивается на всем протяжении. Что произойдет, если вы потянете электроны сильнее? Ну, они приближаются к ядру и размер атома уменьшается. Эффект притяжения ядра на электроны, добавляемые за период, называется эффективным зарядом ядра и рассчитывается как Z Eff = #протоны – Ядро # Электроны. 