Термодинамика: что это такое, характеристики и принципы
В мире физики есть раздел, который отвечает за изучение преобразований, производимых теплом и работой в системе. Это о термодинамика. Это раздел физики, который отвечает за изучение всех преобразований, которые являются только результатом процессов, которые включают изменения в переменных состояния температуры и энергии на макроскопическом уровне.
В этой статье мы расскажем вам все, что вам нужно знать о термодинамике и принципах термодинамики.
Индекс
- 1 Características principales
- 2 Leyes
- 2.1 Нулевой закон
- 2.2 Первый закон термодинамики
- 2.3 Второй закон термодинамики
- 2.4 Третий закон термодинамики
Características principales
Если мы проведем анализ классической термодинамики, то увидим, что она основана на концепции макроскопической системы. Эта система – не что иное, как часть физической или концептуальной массы, отделенная от внешней среды. Чтобы лучше изучить термодинамические системы, всегда предполагается, что это физическая масса, которая не нарушается обменом энергии с внешней экосистемой.
Эта система – не что иное, как часть физической или концептуальной массы, отделенная от внешней среды. Чтобы лучше изучить термодинамические системы, всегда предполагается, что это физическая масса, которая не нарушается обменом энергии с внешней экосистемой.
Состояние макроскопической системы, что есть в условиях равновесия он определяется величинами, называемыми термодинамическими переменными. Все эти переменные нам известны и включают температуру, давление, объем и химический состав. Все эти переменные определяют системы и их равновесие. Основные обозначения, которые используются в химической термодинамике, были установлены благодаря международному прикладному союзу. С этими единицами можно работать и лучше объяснять закон термодинамики.
Однако есть раздел термодинамики, который не изучает равновесие, но отвечает за анализ термодинамических процессов, которые в основном характеризуются отсутствие возможности стабильно достигать условий равновесия.
Leyes
Эти принципы были осуждены в XNUMX веке Иса тех, кто Они несут ответственность за регулирование всех преобразований и их прогресса. Они также анализируют реальные пределы, чтобы иметь истинное представление. Это аксиомы, которые нельзя доказать, но нельзя доказать на основе опыта. Каждая теория термодинамики основана на этих принципах. Мы можем выделить 3 основных принципа плюс принцип, но именно он определяет температуру и подразумевается в остальных 3 принципах.
Нулевой закон
Мы собираемся описать, что такое этот нулевой закон, который первым описывает температуру, которая неявно присутствует в остальных принципах. Когда две системы взаимодействуют друг с другом и находятся в тепловом равновесии, они разделяют некоторые свойства. Эти свойства, которые они разделяют друг с другом, можно измерить и дать численное значение. В результате, если две системы находятся в равновесии с третьей, они будут в равновесии друг с другом, а общим свойством является температура.
Следовательно, этот принцип просто утверждает, что если тело A находилось в равновесии с телом B, и это тело B будет в тепловом равновесии с телом C, тогда тела A и C также будут в равновесии термический. Этот принцип объясняет тот факт, что два тела при разных температурах могут обмениваться теплом друг с другом. Рано или поздно оба тела достигают одинаковой температуры, поэтому они находятся в полном равновесии.
Первый закон термодинамики
Когда тело соприкасается с более холодным телом, происходит преобразование, которое приводит к состоянию равновесия. Это состояние равновесия основано на том факте, что температуры двух тел равны, так как передача энергии между горячим телом и холодным телом усиливается. Чтобы объяснить это явление, ученые предположили, что горячее вещество, которое присутствует в больших количествах, прошло через более холодное тело. Это была жидкость, которая могла перемещаться через массу для обмена теплом.
Этот принцип отвечает за определение тепла как формы энергии. Это не материальная субстанция. Таким образом, можно показать, что тепло, измеряемое в калориях, и работа, измеряемая в джоулях, эквивалентны. Поэтому сегодня мы знаем, что 1 калория составляет примерно 4,186 XNUMX джоулей.
Это не материальная субстанция. Таким образом, можно показать, что тепло, измеряемое в калориях, и работа, измеряемая в джоулях, эквивалентны. Поэтому сегодня мы знаем, что 1 калория составляет примерно 4,186 XNUMX джоулей.
Можно сказать, что первый принцип термодинамики – это принцип сохранения энергии. Количество энергии в тепловом двигателе преобразуется в работу и может быть замечено любой машиной, которая может производить такую работу, не потребляя энергии. Мы можем установить этот первый принцип следующим образом: изменение внутренней энергии замкнутой термодинамической системы равно разнице, которая существует между теплом, подаваемым в систему, и работой, выполняемой указанной системой в окружающей среде.
Второй закон термодинамики
Вначале говорится, что невозможно создать циклическую машину, которая приводит только к передаче тепла от холодного тела к теплому. Можно сказать, что невозможно выполнить преобразование, результатом которого будет только преобразование тепла, которое мы извлекаем из единственного источника, в механическую работу.
Этот принцип отвечает за отрицание возможности существования известного вечного движения второго вида. Мы знаем, что энтропия системы остается изолированной без изменений, когда происходит обратимое преобразование. Мы также знаем, что он увеличивается, когда происходит необратимое преобразование.
Третий закон термодинамики
Этот последний принцип тесно связан со вторым и рассматривается как его следствие. Этот принцип утверждает, что абсолютное бытие не может быть достигнуто в цвете с помощью конечного числа преобразований. Мы знаем, что абсолютный ноль – это не больше минимальной температуры, которую можно достичь. В единицах Кельвин, мы знаем, что это 0, но в градусах Цельсия он имеет значение -273.15 градуса.
Он также утверждает, что энтропия для твердого тела, которое является идеально кристаллическим с температурой 0 кельвинов, равна 0. Это означает, что энтропии не будет, поэтому система будет полностью стабильной. Энергия освобождения, перемещения и вращения составляющих его частиц была бы ничем при температуре 0 кельвинов.
Я надеюсь, что с этой информацией вы сможете больше узнать о термодинамике и основных принципах.
Термодинамика. Определение, законы, применение и процессы
Что такое термодинамика? Это раздел физики, который занимается изучением свойств макроскопических систем. При этом под изучение также попадают способы превращения энергии и методы ее передачи. Термодинамика – это раздел физики, который изучает процессы, происходящие в системах, и их состояния. О том, что еще попадает в список изучаемых ей вещей, мы сегодня и поговорим.
Определение
На картинке ниже можно увидеть пример термограммы, полученной при изучении кувшина с горячей водой.
Термодинамика – это наука, которая опирается на обобщенные факты, полученные опытным путем. Происходящие в термодинамических системах процессы описываются при помощи использования макроскопических величин. В их список входят такие параметры, как концентрация, давление, температура и тому подобные. Понятное дело, что к отдельным молекулам они неприменимы, а сводятся к описанию системы в общем ее виде (в отличие от тех величин, которые используются в электродинамике, например).
Термодинамика – это раздел физики, который также имеет и свои законы. Они, подобно остальным, носят общий характер. Конкретные детали строения того или иного выбранного нами вещества не окажут значительного влияния на характер законов. Именно поэтому говорят, что данный раздел физики является одним из наиболее применимых (или, вернее сказать, успешно применимых) в науке и технике.
Применение
Перечислять примеры можно очень долго. Например, много решений, основанных на термодинамических законах, можно встретить в области тепловой техники или электроэнергетики. Что и говорить об описании и понимании химических реакций, фазовых переходов, явлений переноса. В некотором роде термодинамика “сотрудничает” с квантовой динамикой. Сфера их соприкосновения – это описание явления черных дыр.
Законы
Картинка выше демонстрирует суть одного из термодинамических процессов – конвекции. Теплые слои вещества поднимаются наверх, холодные – опускаются вниз.
Альтернативное название законов, которое, кстати, употребляется не в пример чаще, это начала термодинамики. На сегодняшний день их известно три (плюс одно “нулевое“, или “общее”). Но перед тем как говорить о том, что предполагает каждый из законов, попытаемся ответить на вопрос о том, что такое начала термодинамики.
На сегодняшний день их известно три (плюс одно “нулевое“, или “общее”). Но перед тем как говорить о том, что предполагает каждый из законов, попытаемся ответить на вопрос о том, что такое начала термодинамики.
Они представляют собой совокупность определенных постулатов, которые ложатся в основу понимания происходящих в макросистемах процессов. Положения начал термодинамики устанавливались эмпирическим путем по мере проведения целых серий опытов и научных исследований. Таким образом, существуют определенные доказательства, позволяющие нам взять постулаты на вооружение без единого сомнения в их точности.
Некоторые люди задаются вопросом о том, зачем термодинамике нужны эти самые законы. Ну, можно сказать, что необходимость их использования обусловлена тем, что в данном разделе физики макроскопические параметры описываются в общем виде, без какого-либо намека на рассмотрения их микроскопической природы или особенностей того же плана. Это сфера не термодинамики, а уже статистической физики, если говорить конкретнее. Еще одной важной вещью является тот факт, что начала термодинамики не зависят друг от друга. То есть одно из второго вывести не получится.
Еще одной важной вещью является тот факт, что начала термодинамики не зависят друг от друга. То есть одно из второго вывести не получится.
Применение
Применение термодинамики, как было сказано ранее, идет по многим направлениям. За основу берется, кстати, одно из ее начал, которое иначе интерпретируется в форме закона сохранения энергии. Термодинамические решения и постулаты успешно внедряются в такие отрасли, как энергетическая промышленность, биомедицина, химия. Вот в биологической энергетике повсеместно используется закон сохранения энергии и закон вероятности и направленности термодинамического процесса. Наряду с этим, там используются три наиболее распространенных понятия, на которых базируется вся работа и ее описание. Это термодинамическая система, процесс и фаза процесса.
Процессы
Процессы в термодинамике имеют разную степень сложности. Их насчитывается семь штук. Вообще, под процессом в таком случае следует понимать не что иное, как изменение макроскопического состояния, в которое система была приведена ранее. Следует понимать, что разница между условным начальным состоянием и конечным результатом может быть ничтожной.
Следует понимать, что разница между условным начальным состоянием и конечным результатом может быть ничтожной.
Если разница бесконечно мала, то произошедший процесс мы вполне можем назвать элементарным. Если мы будем обсуждать процессы, то придется прибегнуть к упоминанию дополнительных терминов. Один из них – это “рабочее тело”. Рабочим телом называется система, в которой происходит один тепловой процесс или несколько.
Условно процессы подразделяются на неравновесные и равновесные. В случае с последним все состояния, через которые предстоит пройти термодинамической системе, являются, соответственно, неравновесными. Зачастую изменение состояний идет в таких случаях быстрыми темпами. А вот равновесные процессы близки к квазистатическим. В них изменения проходят на порядок медленнее.
Тепловые процессы, происходящие в термодинамических системах, могут быть как обратимыми, так и необратимыми. Для того чтобы понять суть, разобьем в своем представлении последовательность действий на определенные промежутки. Если мы можем сделать тот же процесс в обратном направлении с теми же “промежуточными станциями”, то его можно назвать обратимым. В противном случае сделать это не получится.
Если мы можем сделать тот же процесс в обратном направлении с теми же “промежуточными станциями”, то его можно назвать обратимым. В противном случае сделать это не получится.
Что такое термодинамика. Механический эквивалент теплоты. Следствие из закона Гесса
В продолжение нашего курса «Физика для чайников» начнем рассматривать основы такого важнейшего раздела как термодинамика .
Активное развитие термодинамики началось в девятнадцатом веке. Именно тогда люди начали строить первые паровые машины, а потом активно внедрять их в производство. Началась промышленная революция, и, естественно, всем хотелось увеличить коэффициент полезного действия машин, чтобы произвести больше продукции, доехать подальше и в конце-концов получить больше денег. Все это очень хорошо стимулировало развитие науки и наоборот. Но давайте ближе к сути вопроса.
Термодинамика – раздел физики, изучающий макроскопические системы, их наиболее общие свойства, способы передачи и превращения энергии в таких системах.
Что такое макроскопические системы? Это системы, состоящие из очень большого числа частиц. Например, баллон с газом или воздушный шар. Описание таких систем методами классической механики просто невозможно – ведь мы не можем измерить скорость, энергию и другие параметры каждой молекулы газа в отдельности. Тем не менее, поведение всей совокупности частиц подчиняется статистическим закономерностям. По сути любой видимый нами (невооруженным глазом) предмет может быть определен как термодинамическая система.
– реально или мысленно выделяемая макроскопическая физическая система, состоящая из большого числа частиц, не требующая для своего описания привлечения микроскопических характеристик отдельных частиц. Соответственно, для описания термодинамической системы используются макроскопические параметры, не относящиеся к каждой частице, но описывающие систему целиком. Это температура, давление, объем, масса системы и проч.
Важно отметить, что термодинамические системы могут быть замкнутыми и незамкнутыми .
Система может находится в разных состояниях. Например, мы взяли баллон с газом и начали его нагревать. Тем самым мы изменили энергию молекул газа, они стали двигаться быстрее, и система перешла в какое-то новое состояние с более высокой температурой. Но что будет, если систему оставить в покое? Тогда система через какое-то время придет в состояние термодинамического равновесия .
Что это значит?
Термодинамическое равновесие – это состояние системы, в котором ее макроскопические параметры (температура, объем и др.) остаются неизменными с течением времени.
Термодинамика стоит на трех своих столпах. Существуют три основных постулата или три закона термодинамики. Они называются соответственно первым, вторым и третьим началами термодинамики. Рассмотрим первое начало или первый закон термодинамики.
Первое начало термодинамики
Первое начало термодинамики гласит:
В любой изолированной системе запас энергии остается постоянным.
К слову, у данного постулата есть еще несколько эквивалентных формулировок. Приведем их ниже:
Количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил.
Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Запишем также математическое выражение первого начала термодинамики:
Здесь Q – количество теплоты, дельта U – изменение внутренней энергии, A – работа против внешних сил. Для различных термодинамических процессов в силу их особенностей запись первого начала будет выглядеть по-разному.
Почему невозможен вечный двигатель первого рода?
Людей издревле привлекала ее величество Халява. Философский камень, превращающий любой металл в золото, скатерть самобранка, с которой не нужно готовить, джин, исполняющий любые желания.
Вечный двигатель невозможен, потому что так устроен мир . Об этом говорят нам законы термодинамики. Согласно первому началу термодинамики, количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил. Например, газ, помещенный в цилиндр с поршнем, получая определенное количество теплоты, увеличивает свою внутреннюю энергию, молекулы движутся быстрее, газ занимает больший объем и толкает поршень (работа против внешних сил). Иными словами, если работа совершается без внешнего притока энергии, она может совершаться лишь за счет внутренней энергии системы, которая рано иди поздно иссякнет, преобразовавшись в совершенную работу, на чем все закончится и система придет к состоянию термодинамического равновесия. Ведь энергия в мире никуда не уходит и не приходит, ее количество остается постоянным, а меняется лишь форма. Конечно, Вы обратили внимание на то, что речь идет о так называемом вечном двигателе первого рода (который может совершать работу без энергии).
Надеемся, знакомство с термодинамикой прошло для Вас приятно и Вы полюбите ее всем сердцем. Если же этого не произойдет, Вы всегда можете поручить выполнение задач по термодинамике , пока сами занимаетесь более приятными делами.
Термодинамика (греч. θέρμη – «тепло», δύναμις – «сила») – раздел физики, изучающий наиболее общие свойства макроскопических систем и способы передачи и превращения энергии в таких системах.
В термодинамике изучаются состояния и процессы, для описания которых можно ввести понятие температуры. Термодинамика (Т.) – это феноменологическая наука, опирающаяся на обобщения опытных фактов. Процессы, происходящие в термодинамических системах, описываются макроскопическими величинами (температура, давление, концентрации компонентов), которые вводятся для описания систем, состоящих из большого числа частиц, и не применимы к отдельным молекулам и атомам, в отличие, например, от величин, вводимых в механике или электродинамике.
Современная феноменологическая термодинамика является строгой теорией, развиваемой на основе нескольких постулатов. Однако связь этих постулатов со свойствами и законами взаимодействия частиц, из которых построены термодинамические системы, даётся статистической физикой. Статистическая физика позволяет выяснить также и границы применимости термодинамики.
Законы термодинамики носят общий характер и не зависят от конкретных деталей строения вещества на атомарном уровне. Поэтому термодинамика успешно применяется в широком круге вопросов науки и техники, таких как энергетика, теплотехника, фазовые переходы, химические реакции, явления переноса и даже чёрные дыры. Термодинамика имеет важное значение для самых разных областей физики и химии, химической технологии, аэрокосмической техники, машиностроения, клеточной биологии, биомедицинской инженерии, материаловедения и находит своё применение даже в таких областях, как экономика.
Важные годы в истории термодинамики
- Зарождение термодинамики как науки связано с именем Г.
 Галилея (G. Galilei), корый ввёл понятие температуры и сконструировал первый прибор, реагирующий на изменения температуры окружающей среды (1597).
Галилея (G. Galilei), корый ввёл понятие температуры и сконструировал первый прибор, реагирующий на изменения температуры окружающей среды (1597). - Вскоре Г. Д. Фаренгейт (G. D. Fahrenheit, 1714), Р. Реомюр (R. Reaumur, 1730} и А. Цельсий (A. Celsius, 1742) создали температурные шкалы в соответствии с этим принципом.
- Дж.Блэк (J. Black) в 1757 году уже ввёл понятия скрытой теплоты плавления и теплоемкости (1770). А Вильке (J. Wilcke, 1772) ввёл определение калории как количества тепла, необходимого для нагревания 1 г воды на 1 °С.
- Лавуазье (A. Lavoisier) и Лаплас (P. Laplace) в 1780 сконструировали калориметр (см. Калориметрия) и впервые экспериментально определили уд. теплоёмкости ряда веществ.
- В 1824 С. Карно (N. L, S. Carnot) опубликовал работу, посвящённую исследованию принципов работы тепловых двигателей.
- Б. Клапейрон (В. Clapeyron) ввёл графическое представление термодинамических процессов и развил метод бесконечно малых циклов (1834).
- Г.
 Хельмгольц (G. Helmholtz) отметил универсальный характер закона сохранения энергии (1847). Впоследствии Р. Клаузиус (R. Clausius) и У. Томсон (Кельвин; W. Thomson) систематически развили теоретический аппарат термодинамики, в основу которого положены первое начало термодинамики и второе начало термодинамики.
Хельмгольц (G. Helmholtz) отметил универсальный характер закона сохранения энергии (1847). Впоследствии Р. Клаузиус (R. Clausius) и У. Томсон (Кельвин; W. Thomson) систематически развили теоретический аппарат термодинамики, в основу которого положены первое начало термодинамики и второе начало термодинамики. - Развитие 2-го начала привело Клаузиуса к определению энтропии (1854) и формулировке закона возрастания энтропии (1865).
- Начиная с работ Дж. У. Гиббса (J. W. Gibbs, 1873), предложившего метод термодинамических потенциалов, развивается теория термодинамического равновесия.
- Во 2-й пол. 19 в. проводились исследования реальных газов. Особую роль сыграли эксперименты Т. Эндрюса (Т. Andrews), который впервые обнаружил критическую точку системы жидкость-пар (1861), её существование предсказал Д. И. Менделеев (1860).
- К концу 19 в. были достигнуты большие успехи в получении низких температур, в результате чего были ожижены О2, N2 и Н2.
- В 1902 Гиббс опубликовал работу, в которой все основные термодинамические соотношения были получены в рамках статистической физики.

- Связь между кинетич. свойствами тела и его термодинамич. характеристиками была установлена Л. Онсагером (L. Onsager, 1931).
- В 20 в. интенсивно исследовали термодинамику твёрдых тел, а также квантовых жидкостей и жидких кристаллов, в которых имеют место многообразные фазовые переходы.
- Л. Д. Ландау (1935-37) развил общую теорию фазовых переходов, основанную на концепции спонтанного нарушения симметрии.
Разделы термодинамики
Современную феноменологическую термодинамику принято делить на равновесную (или классическую) термодинамику, изучающую равновесные термодинамические системы и процессы в таких системах, и неравновесную термодинамику, изучающую неравновесные процессы в системах, в которых отклонение от термодинамического равновесия относительно невелико и ещё допускает термодинамическое описание.
Равновесная (или классическая) термодинамика
В равновесной термодинамике вводятся такие переменные, как внутренняя энергия, температура, энтропия, химический потенциал. Все они носят название термодинамических параметров (величин). Классическая термодинамика изучает связи термодинамических параметров между собой и с физическими величинами, вводимыми в рассмотрение в других разделах физики, например, с гравитационным или электромагнитным полем, действующим на систему. Химические реакции и фазовые переходы также входят в предмет изучения классической термодинамики. Однако изучение термодинамических систем, в которых существенную роль играют химические превращения, составляет предмет химической термодинамики, а техническими приложениями занимается теплотехника.
Все они носят название термодинамических параметров (величин). Классическая термодинамика изучает связи термодинамических параметров между собой и с физическими величинами, вводимыми в рассмотрение в других разделах физики, например, с гравитационным или электромагнитным полем, действующим на систему. Химические реакции и фазовые переходы также входят в предмет изучения классической термодинамики. Однако изучение термодинамических систем, в которых существенную роль играют химические превращения, составляет предмет химической термодинамики, а техническими приложениями занимается теплотехника.
Классическая термодинамика включает в себя следующие разделы:
- начала термодинамики (иногда также называемые законами или аксиомами)
- уравнения состояния и свойства простых термодинамических систем (идеальный газ, реальный газ, диэлектрики и магнетики и т. д.)
- равновесные процессы с простыми системами, термодинамические циклы
- неравновесные процессы и закон неубывания энтропии
- термодинамические фазы и фазовые переходы
Кроме этого, современная термодинамика включает также следующие направления:
- строгая математическая формулировка термодинамики на основе выпуклого анализа
- неэкстенсивная термодинамика
В системах, не находящихся в состоянии термодинамического равновесия, например, в движущемся газе, может применяться приближение локального равновесия, в котором считается, что соотношения равновесной термодинамики выполняются локально в каждой точке системы.
Неравновесная термодинамика
В неравновесной термодинамике переменные рассматриваются как локальные не только в пространстве, но и во времени, то есть в её формулы время может входить в явном виде. Отметим, что посвящённая вопросам теплопроводности классическая работа Фурье «Аналитическая теория тепла» (1822) опередила не только появление неравновесной термодинамики, но и работу Карно «Размышления о движущей силе огня и о машинах, способных развивать эту силу» (1824), которую принято считать точкой отсчёта в истории классической термодинамики.
Основные понятия термодинамики
Термодинамическая система – тело или группа тел, находящихся во взаимодействии, мысленно или реально обособленные от окружающей среды.
Гомогенная система – система, внутри которой нет поверхностей, разделяющих отличающиеся по свойствам части системы (фазы).
Гетерогенная система – система, внутри которой присутствуют поверхности, разделяющие отличающиеся по свойствам части системы.
Фаза – совокупность гомогенных частей гетерогенной системы, одинаковых по физическим и химическим свойствам, отделённая от других частей системы видимыми поверхностями раздела.
Изолированная система – система, которая не обменивается с окружающей средой ни веществом, ни энергией.
Закрытая система – система, которая обменивается с окружающей средой энергией, но не обменивается веществом.
Открытая система – система, которая обменивается с окружающей средой и веществом, и энергией.
Совокупность всех физических и химических свойств системы характеризует её термодинамическое состояние . Все величины, характеризующие какое-либо макроскопическое свойство рассматриваемой системы – параметры состояния . Опытным путем установлено, что для однозначной характеристики данной системы необходимо использовать некоторое число параметров, называемых независимыми ; все остальные параметры рассматриваются как функции независимых параметров. В качестве независимых параметров состояния обычно выбирают параметры, поддающиеся непосредственному измерению, например температуру, давление, концентрацию и т.д. Всякое изменение термодинамического состояния системы (изменения хотя бы одного параметра состояния) есть термодинамический процесс .
В качестве независимых параметров состояния обычно выбирают параметры, поддающиеся непосредственному измерению, например температуру, давление, концентрацию и т.д. Всякое изменение термодинамического состояния системы (изменения хотя бы одного параметра состояния) есть термодинамический процесс .
Обратимый процесс – процесс, допускающий возможность возвращения системы в исходное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Равновесный процесс – процесс, при котором система проходит через непрерывный ряд равновесных состояний.
Энергия – мера способности системы совершать работу; общая качественная мера движения и взаимодействия материи. Энергия является неотъемлемым свойством материи. Различают потенциальную энергию, обусловленную положением тела в поле некоторых сил, и кинетическую энергию, обусловленную изменением положения тела в пространстве.
Внутренняя энергия системы – сумма кинетической и потенциальной энергии всех частиц, составляющих систему. Можно также определить внутреннюю энергию системы как её полную энергию за вычетом кинетической и потенциальной энергии системы как целого.
Можно также определить внутреннюю энергию системы как её полную энергию за вычетом кинетической и потенциальной энергии системы как целого.
Формы перехода энергии
Формы перехода энергии от одной системы к другой могут быть разбиты на две группы.
- В первую группу входит только одна форма перехода движения путем хаотических столкновений молекул двух соприкасающихся тел, т.е. путём теплопроводности (и одновременно путём излучения). Мерой передаваемого таким способом движения является теплота. Теплота есть форма передачи энергии путём неупорядоченного движения молекул.
- Во вторую группу включаются различные формы перехода движения, общей чертой которых является перемещение масс, охватывающих очень большие числа молекул (т.е. макроскопических масс), под действием каких-либо сил. Таковы поднятие тел в поле тяготения, переход некоторого количества электричества от большего электростатического потенциала к меньшему, расширение газа, находящегося под давлением и др.
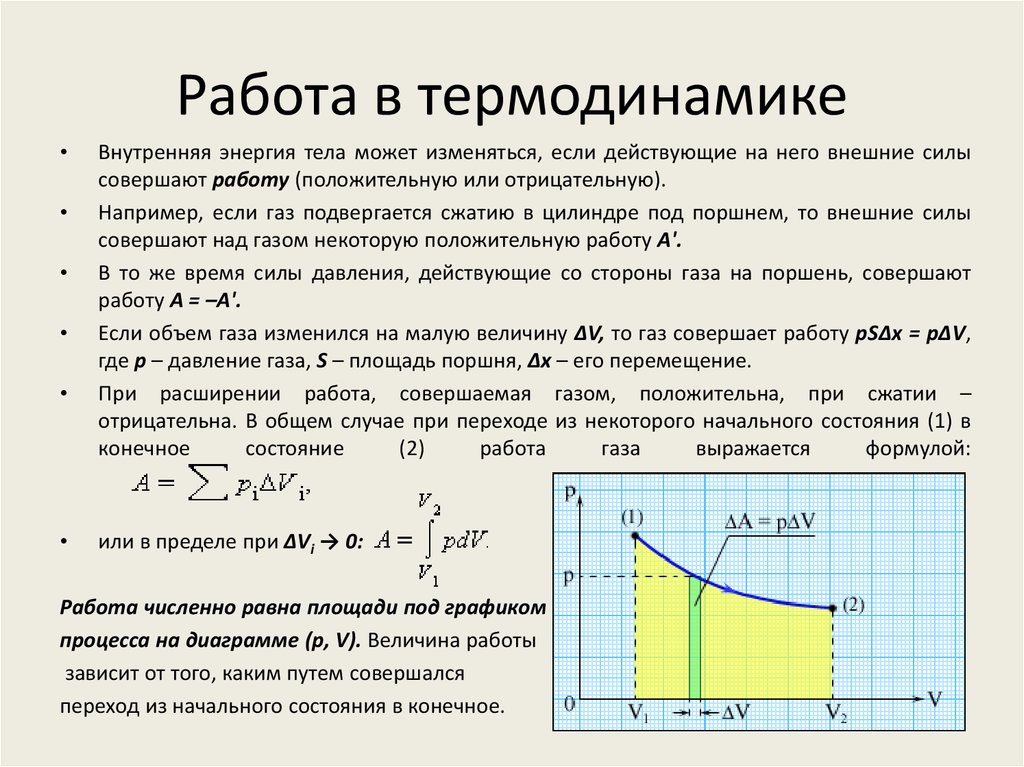 Общей мерой передаваемого такими способами движения является работа – форма передачи энергии путём упорядоченного движения частиц.
Общей мерой передаваемого такими способами движения является работа – форма передачи энергии путём упорядоченного движения частиц.
Теплота и работа характеризуют качественно и количественно две различные формы передачи движения от данной части материального мира к другой. Теплота и работа не могут содержаться в теле. Теплота и работа возникают только тогда, когда возникает процесс, и характеризуют только процесс. В статических условиях теплота и работа не существуют. Различие между теплотой и работой, принимаемое термодинамикой как исходное положение, и противопоставление теплоты работе имеет смысл только для тел, состоящих из множества молекул, т.к. для одной молекулы или для совокупности немногих молекул понятия теплоты и работы теряют смысл. Поэтому термодинамика рассматривает лишь тела, состоящие из большого числа молекул, т.е. так называемые макроскопические системы.
Три начала термодинамики
Начала термодинамики – совокупность постулатов, лежащих в основе термодинамики. Эти положения были установлены в результате научных исследований и были доказаны экспериментально. В качестве постулатов они принимаются для того, чтобы термодинамику можно было построить аксиоматически.
Эти положения были установлены в результате научных исследований и были доказаны экспериментально. В качестве постулатов они принимаются для того, чтобы термодинамику можно было построить аксиоматически.
Необходимость начал термодинамики связана с тем, что термодинамика описывает макроскопические параметры систем без конкретных предположений относительно их микроскопического устройства. Вопросами внутреннего устройства занимается статистическая физика.
Начала термодинамики независимы, то есть ни одно из них не может быть выведено из других начал. Аналогами трех законов Ньютона в механике, являются три начала в термодинамике, которые связывают понятия «тепло» и «работа»:
- Нулевое начало термодинамики говорит о термодинамическом равновесии.
- Первое начало термодинамики – о сохранении энергии.
- Второе начало термодинамики – о тепловых потоках.
- Третье начало термодинамики – о недостижимости абсолютного нуля.
Общее (нулевое) начало термодинамики
Общее (нулевое) начало термодинамики гласит, что два тела находятся в состоянии теплового равновесия, если они могут передавать друг другу теплоту, но этого не происходит.
Нетрудно догадаться, что два тела не передают друг другу теплоту в том случае, если их температуры равны. Например, если измерить температуру человеческого тела при помощи термометра (в конце измерения температура человека и температура градусника будут равны), а затем, этим же термометром измерить температуру воды в ванной, и при этом окажется, что обе температуры совпадают (наблюдается тепловое равновесие человека с термометром и термометра с водой), можно говорить о том, что человек находится в тепловом равновесии с водой в ванной.
Из сказанного выше, можно сформулировать нулевое начало термодинамики следующим образом: два тела, находящиеся в тепловом равновесии с третьим, также находятся в тепловом равновесии между собой.
С физической точки зрения нулевое начало термодинамики устанавливает точку отсчета, поскольку, между двумя телами, которые имеют одинаковую температуру, тепловой поток отсутствует. Другими словами, можно сказать, что температура есть не что иное, как индикатор теплового равновесия.
Первое начало термодинамики
Первое начало термодинамики есть закон сохранения тепловой энергии, утверждающий, что энергия никуда не девается бесследно.
Система может либо поглощать, либо выделять тепловую энергию Q, при этом система выполняет над окружающими телами работу W (или окружающие тела выполняют работу над системой), при этом внутренняя энергия системы, которая имела начальное значение Uнач, будет равна Uкон:
Uкон-Uнач = ΔU = Q-W
Тепловая энергия, работа и внутренняя энергия определяют общую энергию системы, которая является постоянной величиной. Если системе передать (забрать) некое кол-во тепловой энергии Q, при отсутствии работы кол-во внутренней энергии системы U, увеличится (уменьшится) на Q.
Второе начало термодинамики
Второе начало термодинамик гласит, что тепловая энергия может переходить только в одном направлении – от тела с более высокой температурой, к телу, с более низкой температурой, но не наоборот.
Третье начало термодинамики
Третье начало термодинамики гласит, что любой процесс, состоящий из конечного числа этапов, не позволит достичь температуры абсолютного нуля (хотя к нему можно существенно приблизиться).
Термодинамика – раздел прикладной физики или теоретической теплотехники, в котором исследуется превращение движения в теплоту и наоборот. В термодинамике рассматриваются не только вопросы распространения теплоты, но и физические и химические изменения, связанные с поглощением теплоты веществом, а также, наоборот, выделение теплоты в ходе физических и химических превращений.
Необходимость термодинамики
Термодинамика исторически возникла как эмпирическая наука об основных способах преобразования внутренней энергии нагретых тел в механическую. Однако в процессе своего развития термодинамика проникла во все разделы физики, где возможно ввести понятие «внутренняя энергия» и позволила теоретически предсказать многие явления задолго до появления строгой теории этих явлений.
* 2-й закон термодинамики: Второй закон термодинамики исключает возможность создания вечного двигателя второго рода. Имеется несколько различных, но в тоже время эквивалентных формулировок этого закона. 1 – Постулат Клаузиуса. Процесс, при котором не происходит других изменений, кроме передачи теплоты от горячего тела к холодному, является необратимым, то есть теплота не может перейти от холодного тела к горячему без каких либо других изменений в системе. Это явление называют рассеиванием или дисперсией энергии. 2 – Постулат Кельвина. Процесс, при котором работа переходит в теплоту без каких либо других изменений в системе, является необратимым, то есть невозможно превратить в работу всю теплоту, взятую от источника с однородной температурой, не проводя других изменений в системе.
1 – Постулат Клаузиуса. Процесс, при котором не происходит других изменений, кроме передачи теплоты от горячего тела к холодному, является необратимым, то есть теплота не может перейти от холодного тела к горячему без каких либо других изменений в системе. Это явление называют рассеиванием или дисперсией энергии. 2 – Постулат Кельвина. Процесс, при котором работа переходит в теплоту без каких либо других изменений в системе, является необратимым, то есть невозможно превратить в работу всю теплоту, взятую от источника с однородной температурой, не проводя других изменений в системе.
* 3-й закон термодинамики: Теорема Нернста: Энтропия любой системы при абсолютном нуле температуры всегда может быть принята равной нулю
Законы термодинамики
Термодинамика основывается на трёх законах, которые сформулированы на основе экспериментальных данных и поэтому могут быть приняты как постулаты.
* 1-й закон термодинамики. Представляет собой формулировку обобщённого закона сохранения энергии для термодинамических процессов. В наиболее простой форме его можно записать как δQ = δA + d”U, где dU есть полный дифференциал внутренней энергии системы, а δQ и δA есть элементарное количество теплоты и элементарная работа, совершенная над системой соответственно. Нужно учитывать, что δA и δQ нельзя считать дифференциалами в обычном смысле этого понятия. С точки зрения квантовых представлений этот закон можно интерпретировать следующим образом: dU есть изменение энергии данной квантовой системы, δA есть изменение энергии системы, обусловленное изменением заселённости энергетических уровней системы, а δQ есть изменение энергии квантовой системы, обусловленное изменением структуры энергетических уровней.
В наиболее простой форме его можно записать как δQ = δA + d”U, где dU есть полный дифференциал внутренней энергии системы, а δQ и δA есть элементарное количество теплоты и элементарная работа, совершенная над системой соответственно. Нужно учитывать, что δA и δQ нельзя считать дифференциалами в обычном смысле этого понятия. С точки зрения квантовых представлений этот закон можно интерпретировать следующим образом: dU есть изменение энергии данной квантовой системы, δA есть изменение энергии системы, обусловленное изменением заселённости энергетических уровней системы, а δQ есть изменение энергии квантовой системы, обусловленное изменением структуры энергетических уровней.
В термодинамике изучают самые общие законы и физические процессы преобразований внутренней энергии. При этом считается, что любое материальное тело имеет тепловую энергию $U$, которая зависит от его температур.
Перед тем, как рассмотреть основные термодинамические формулы необходимо дать определение термодинамике.
Определение 1
Термодинамика – это обширный раздел физики, который исследует и описывает процессы, происходящие в системах, а также их состояния.
Указанное научное направление опирается на обобщенные факты, которые были получены опытным путем. Происходящие в термодинамических концепциях явления описываются посредством использования макроскопических величин.
В их список входят такие параметры, как:
- давление;
- температура;
- концентрация;
- энергия;
- объем.
К отдельным молекулам данные параметры неприменимы, а сводятся к детальному описанию системы в общем ее виде. Много решений, которые основаны на термодинамических законах, можно встретить в сфере электроэнергетики и тепловой техники. Что и свидетельствует о понимании фазовых переходов, химических процессов и явлений переноса. В некотором роде термодинамика тесно “сотрудничает” с квантовой динамикой.
Уравнение идеального газа в термодинамике
Рисунок 1. Работа в термодинамике. Автор24 – интернет-биржа студенческих работ
Работа в термодинамике. Автор24 – интернет-биржа студенческих работ
Определение 2
Идеальный газ – это некая идеализация, такая же, как и материальная точка.
Молекулы такого элемента являются материальными точками, а соударения частиц – абсолютно упругие и постоянные. В задачах по термодинамике реальные газы зачастую принимаются за идеальные. Так гораздо легче составлять формулы, и не нужно иметь дела с огромным количеством новых величин в уравнениях.
Итак, молекулы идеального газа движутся, а вот чтобы узнать с какой скоростью и массой, необходимо использовать уравнение состояния идеального газа, или формулу Клапейрона-Менделеева: $PV = \frac{m}{M}RT$. Здесь $m$ – масса исследуемого газа, $M$ – его изначальная молекулярная масса, $R$ – универсальная постоянная, равная 8,3144598 Дж/(моль*кг).
В этом аспекте массу идеального газа также можно вычислить, как произведение объема и плотности $m = pV$. Существует некая связь между средней кинетической энергией $E$ и давлением газа. Эта взаимосвязь называется в физике основным уравнением молекулярно-кинетической теории и имеет вид: $p = \frac{2}{3}nE$, где $n$ – концентрация движущихся молекул по отношению к общему объему, $E$ – коэффициент средней кинетической энергии.
Эта взаимосвязь называется в физике основным уравнением молекулярно-кинетической теории и имеет вид: $p = \frac{2}{3}nE$, где $n$ – концентрация движущихся молекул по отношению к общему объему, $E$ – коэффициент средней кинетической энергии.
Первое начало термодинамики. Формулы для изопроцессов
Рисунок 2. Уравнение состояния идеального газа. Автор24 – интернет-биржа студенческих работ
Первый термодинамический закон гласит: количество внутренней теплоты, переданное газу, идёт только на изменение общей энергии газа $U$ и на совершение веществом работы $A$. Формула первого начала термодинамики записывается так: $Q = ΔU + A$.
как известно, с газом в системе всегда что-то происходит, ведь его можно сжать или нагреть. В данном случае необходимо рассмотреть такие процессы, которые протекают при одном стабильном параметре. Первое начало термодинамики в изотермическом случае, который протекает при постоянной температуре, задействует закон Бойля-Мариотта.
В результате изотермического процесса давление газа обратно пропорционально его изначальному объёму: $Q = A. $
$
Изохорный – наблюдается при постоянном объеме. Для этого явление применим закон Шарля, согласно которому, давление прямо пропорционально общей температуре. В изохорном процессе все подведенное к газу тепло идет на изменение его внутренней энергии и записывается в таком виде: $Q = ΔA.$
Изобарный процесс – происходит при постоянном давлении. Закон Гей-Люссака предполагает, что при неизменном давлении идеального газа его начальный объём прямо пропорционален итоговой температуре. При изобарном процессе тепло идет на совершение газом работы и на изменение внутреннего энергетического потенциала: $Q = \Delta U+p\Delta V.$
Формула теплоемкости и главная формула КПД в термодинамике
Замечание 1
Удельная теплоемкость в термодинамической системе всегда равна количеству теплоты, которое выделяется для нагревания одного килограмма действующего вещества на один градус Цельсия.
Уравнение теплоемкости записывается таким образом: $c = \frac{Q}{m\Delta t}$. Помимо указанного параметра, существует и молярная теплоемкость, которая работает при постоянном объеме и давлении.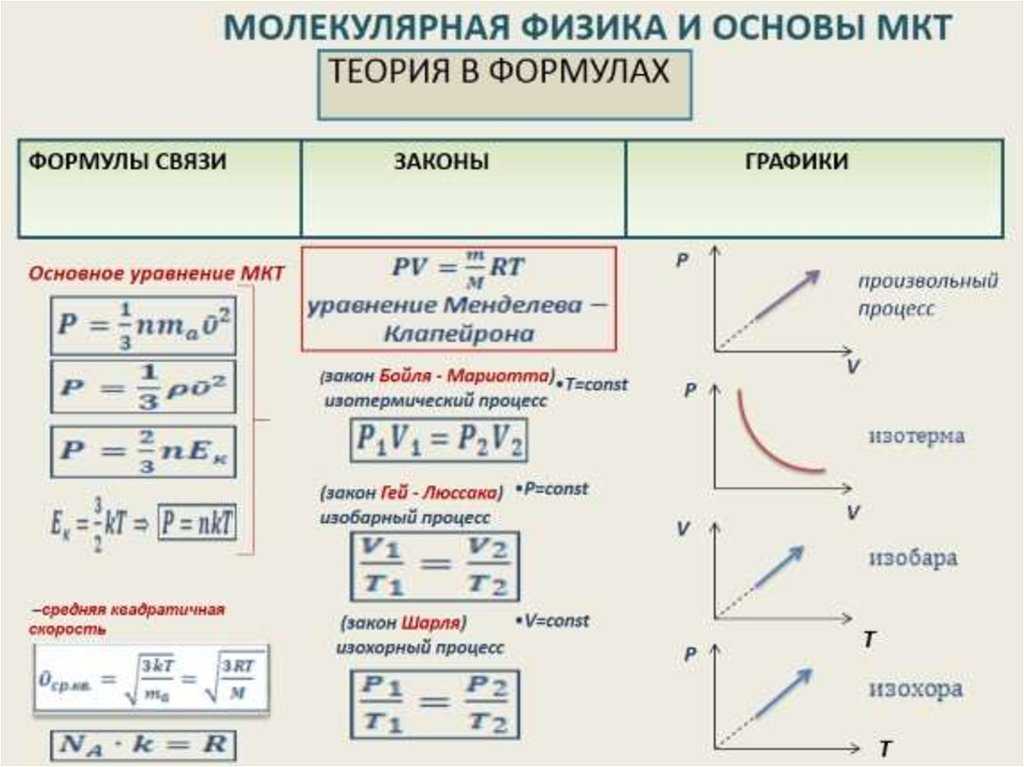
Ее действия видно в следующей формуле: $C_v = \frac {i}{2}R$ где $i$ – количество степеней свободы молекул газа.
Тепловая машина, в самом простейшем случае, состоит из холодильника, нагревателя и рабочего материального тела. Нагреватель изначально сообщает тепло физическому веществу и совершает определенную работу, а затем постепенно охлаждается холодильником, и все повторяется по кругу. Типичным примером тепловой машины выступает двигатель внутреннего сгорания.
Коэффициент полезного действия теплового устройства вычисляется по формуле: $n = \frac {Q_h-Q_x }{Q_h }.$
При изучении основ и уравнений термодинамики следует понять, что на сегодняшний день существует два метода описания физических процессов, происходящих в макроскопических материальных телах: статистический и термодинамический.
Методы термодинамики и ее формулы позволяет раскрыть и описать смысл экспериментальных закономерностей в виде закона Менделеева-Клапейрона. Важно понять, что в термодинамических концепциях, в отличие от систем молекулярной физики, не изучаются конкретные взаимодействия, происходящие с определенными молекулами или атомами, а рассматривается постоянные взаимопревращения и связь разнообразных видов теплоты, энергии и работы.
Уравнение состояния и его функции
Рисунок 4. Термодинамические уравнения состояния. Автор24 – интернет-биржа студенческих работ
При исследовании макросостояний применяются функции состояния, которые предполагают показатель, демонстрирующий определённые состояния термодинамического равновесия, независящий от предыстории концепции и метода её перехода в абсолютное состояние.
Основными функциями состояния при грамотном построении термодинамики являются:
- внутренняя энергия;
- энтропия;
- температура;
- термодинамические потенциалы.
Однако функции состояния в термодинамики не являются полностью независимыми, и для однородной системы любой термодинамический принцип может быть записан как выражение двух самостоятельных переменных. Такие функциональные взаимосвязи называются уравнениями общего состояния.
На сегодняшний день различают такие виды уравнений:
- термическое уравнение состояние – определяющее связь между давлением, температурой и объёмом;
- калорическое уравнение – выражающее внутренний энергетический потенциал, как функцию от объёма и температуры;
- каноническое уравнение состояние – записываемое в качестве термодинамического потенциала в соответствующих переменных.

Знание уравнения состояния очень важно для использования на практике общих принципов термодинамики. Для каждой конкретной термодинамической концепции такие выражения определяются из опыта или способами статистической механики, и в пределах термодинамики оно считается заданным при изначальном определении системы.
Что такое термодинамика
Определение
Термодинамика — важнейшая часть физики. Ее выводы используются в гиро- и аэродинамике, оптике, физической химии многих других науках и прикладных разработках.
Возникла термодинамика в начале XIX века. В то время начала свое развитие теплотехника. Термодинамика стала ее теоретической основой. Ее целью в то время было изучение закономерностей, которые определяют процессы превращения тепла в механическую работу с помощью тепловых двигателей и поиск условий, при которых максимальна эффективность таких превращений. Основы термодинамики заложил в своих работах Саади Карно, французский инженер и физик, который и исследовал тепловые двигатели. Тогда еще теплота рассматривалась как некоторое вещество — теплород, которое не имеет массы и не может быть создано или уничтожено. Впоследствии термодинамика вышла за границы узкой технической задачи. Основным содержанием современной термодинамики стало изучение законов тепловой формы движения материи и связанных с этим явлений.
Тогда еще теплота рассматривалась как некоторое вещество — теплород, которое не имеет массы и не может быть создано или уничтожено. Впоследствии термодинамика вышла за границы узкой технической задачи. Основным содержанием современной термодинамики стало изучение законов тепловой формы движения материи и связанных с этим явлений.
Какие процессы изучает термодинамика
Термодинамика изучает макроскопические процессы, которые происходят в телах, системах тел. Эта наука не использует специальных гипотез и представлений о строении вещества. Не задает вопросы о природе теплоты. Выводы термодинамики основаны на общих принципах (началах), которые получены обобщением эмпирических данных.
Термодинамика изучает только термодинамически равновесные состояния систем или очень медленные процессы, которые могут быть представлены совокупностью равновесных. Эта наука также изучает законы перехода от одного равновесного состояния к другому.
Выводы термодинамики весьма общие, так как получают их без использования упрощенных моделей. Термодинамика многие уравнения берет из опыта, или молекулярно — кинетической теории. Но здесь необходимо отметить, что практика показала, что аксиомы термодинамики имеют границы применимости. Так классическая термодинамика плохо применима в системах с малыми размерами, так как не рассматривает флуктуации состояния, которые в микромире имеют существенное значение.
Термодинамика многие уравнения берет из опыта, или молекулярно — кинетической теории. Но здесь необходимо отметить, что практика показала, что аксиомы термодинамики имеют границы применимости. Так классическая термодинамика плохо применима в системах с малыми размерами, так как не рассматривает флуктуации состояния, которые в микромире имеют существенное значение.
Итак, основную идею термодинамики определим так:
Основная идея термодинамики
Макроскопические системы состоят из большого количества частиц. Состояния системы характеризуются вполне конкретными параметрами. Каждая система подчиняется закону сохранения энергии.
В термодинамике закон сохранения энергии формулируется как начала термодинамики. Поведение макросистемы описывается исходя из начал термодинамики. В термодинамике сформулированы три начала. Первое начало — следствие закона сохранения энергии:
Первое начало термодинамики
\[\delta Q=dU+\delta A\ \left(1\right),\]
где $\delta Q$- элемент тепла (или бесконечно малое количество) подводимое к термодинамической системе. Изучение движение и превращений этой формы энергии является предметом термодинамики, $dU$- изменение внутренней энергии системы, $\delta A$ — элементарная работа. Бесконечно малые величины здесь обозначены разными символами (d и $\delta $), это сделано намерено. С целью подчеркнуть, что свойства этих малых величин различны. Первое начало термодинамики не дает понятия о направлении прохождения процесса. Поэтому необходимо второе начало. Именно оно характеризует направление процессов в термодинамике. Существую несколько формулировок второго начала термодинамики. По форме они отличаются, но по смыслу он эквивалентны. Приведем одну из формулировок, ее дал Томпсон (лорд Кельвин):
Изучение движение и превращений этой формы энергии является предметом термодинамики, $dU$- изменение внутренней энергии системы, $\delta A$ — элементарная работа. Бесконечно малые величины здесь обозначены разными символами (d и $\delta $), это сделано намерено. С целью подчеркнуть, что свойства этих малых величин различны. Первое начало термодинамики не дает понятия о направлении прохождения процесса. Поэтому необходимо второе начало. Именно оно характеризует направление процессов в термодинамике. Существую несколько формулировок второго начала термодинамики. По форме они отличаются, но по смыслу он эквивалентны. Приведем одну из формулировок, ее дал Томпсон (лорд Кельвин):
Второе начало термодинамики
«Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет уменьшения внутренней энергии теплового резервуара».
Третье накладывает ограничение на процессы. Его сформулируем:
Третье начало термодинамики
«Абсолютный нуль недостижим посредством конечного числа операций». +$- количество теплоты, подведенное газу от нагревателя.
+$- количество теплоты, подведенное газу от нагревателя.
Круговой процесс (цикл), который изображен на рис.1, состоит из четырех последовательных процессов. Определим, в каких процессах тепло подводится. Очевидно, что это процессы AB и BC.
Процесс AB — изобарный. Запишем первое начало термодинамики и найдем количество теплоты, пущенное газом в этом процессе.
\[\triangle Q=\triangle U+A\ \left(1.2\right).\]
Работа в изобарном процессе может быть найдена как:
Следовательно, для процесса AB мы получим:
Изменение внутренней энергии газа в процессе AB, имеет формулу:
\[\triangle U_{AB}=\frac{i}{2}\nu R\left(T_2-T_1\right)\left(1.5\right).\]
Для того, чтобы найти $\left(T_2-T_1\right)$, используем уравнение Менделеева – Клайперона для идеального газа. Запишем его для двух состояний (точек A и B):
\ \
Найдем разность (1.7) и (1.6), получим:
Подставим (1.8) в (1.5), получим:
\[\triangle U_{AB}=\frac{i}{2}p_1\left(V_2-V_1\right)\left(1.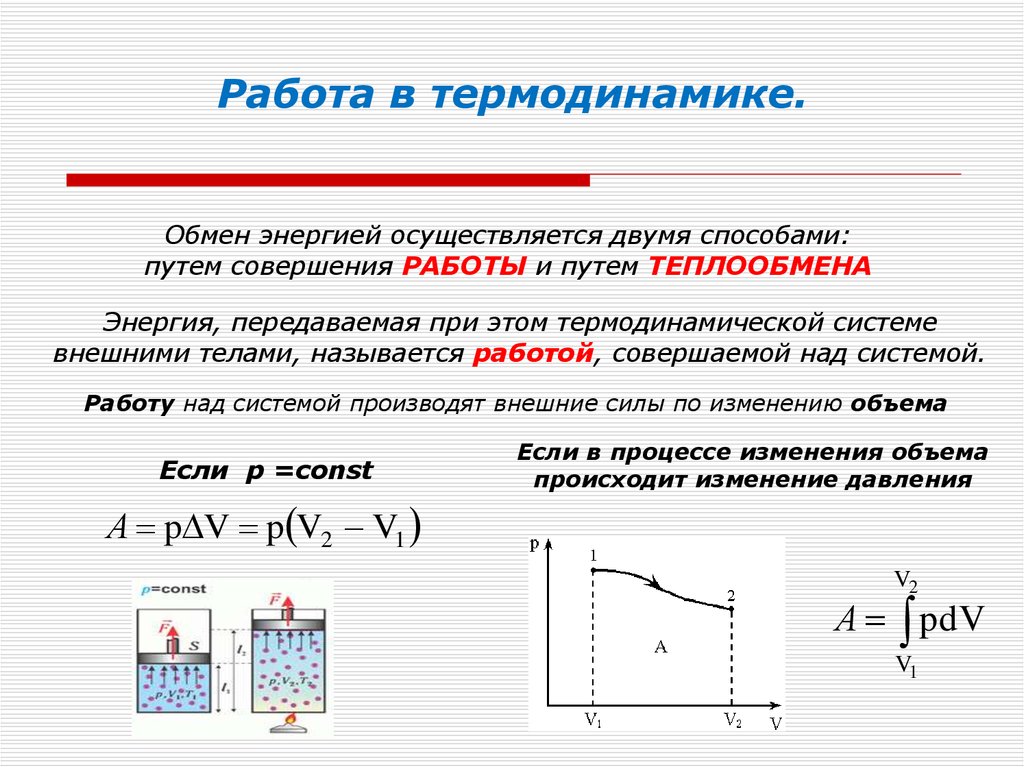 +:$
+:$
Найдем работу, которую совершает газ в круговом процессе. Она равна из геометрического смысла интегралов площади прямоугольника ABCD, соответственно запишем:
\[\eta =\frac{{(p}_2-\ p_1)\left(V_2-V_1\right)}{{\frac{i}{2}(p}_2V_2-p_1V_1)+p_1{(V}_2-V_1)}\ \left(1.18\right).\]
Ответ: КПД цикла заданного процесса выражается формулой: $\eta =\frac{{(p}_2-\ p_1)\left(V_2-V_1\right)}{{\frac{i}{2}(p}_2V_2-p_1V_1)+p_1{(V}_2-V_1)}$.
Задание: На рис. 2 изображены изотермы AB и CD. Сравните количества теплоты, получаемые газом, в процессах I и II.
Если AB и СВ — изотермы, изменения внутренней энергии газа процессах I и II одинаковы: \[\triangle U_I=\triangle U_{II}\left(2.1\right).\]
Работа в процессе I равна нулю, так как процесс изохорный, следовательно количество теплоты получаемое газом в процессе I:
\[\triangle Q_I=\triangle U_I\ \left(2.2\right).\]
В процессе II работа газом совершается и она больше 0 ($A_I>0).\ $
\[\triangle Q_{II}=\triangle U_{II}+A=\triangle U_I+A\ \to \triangle Q_{II}>\triangle Q_I\left(2. 3\right).\]
3\right).\]
Ответ: Количества теплоты получаемое газом в процессе II больше, чем количество теплоты, получаемое газом в процессе I.
Что такое термодинамика? | Живая наука
Инженер осматривает лопатки паровой турбины. (Изображение предоставлено: Монти Ракусен через Getty Images)Термодинамика — это раздел физики, изучающий взаимосвязь между теплом и другими формами энергии. В частности, он описывает, как тепловая энергия преобразуется в другие формы энергии и из них, а также как тепловая энергия влияет на материю.
Тепловая энергия — это энергия, которой вещество или система обладает благодаря своей температуре — другими словами, энергия движущихся или вибрирующих молекул — по данным Университета Кентукки . Термодинамика включает в себя измерение этой энергии, что может быть «чрезвычайно сложным», сказал Live Science Дэвид Макки, профессор физики Южного государственного университета штата Миссури. «Системы, которые мы изучаем в термодинамике… состоят из очень большого числа атомов или молекул, взаимодействующих сложным образом. Но если эти системы соответствуют правильным критериям, которые мы называем равновесием, их можно описать с помощью очень небольшого числа измерений или числа. Часто это идеализируется как масса системы, давление системы и объем системы или какой-либо другой эквивалентный набор чисел».
Но если эти системы соответствуют правильным критериям, которые мы называем равновесием, их можно описать с помощью очень небольшого числа измерений или числа. Часто это идеализируется как масса системы, давление системы и объем системы или какой-либо другой эквивалентный набор чисел».
Теплота
Таким образом, термодинамика занимается несколькими свойствами материи; в первую очередь это тепло. По данным Университета штата Джорджия, тепло — это энергия, передаваемая между веществами или системами из-за разницы температур между ними . Как форма энергии тепло сохраняется — его нельзя создать или уничтожить. Однако его можно перенести из одного места в другое. Тепло также может быть преобразовано в другие формы энергии и обратно. Например, паровая турбина может преобразовывать тепло в кинетическую энергию для запуска генератора, который преобразует кинетическую энергию в электрическую. Лампочка может преобразовывать эту электрическую энергию в электромагнитное излучение (свет), которое при поглощении поверхностью снова преобразуется в тепло. В ходе этого процесса часть энергии теряется в энтропию.
В ходе этого процесса часть энергии теряется в энтропию.
Температура
Сравнение температур замерзания и плавления воды (в градусах Цельсия). (Изображение предоставлено: Why Design через Shutterstock)Количество тепла, передаваемого веществом, зависит от скорости и количества атомов или молекул этого вещества в движении, по данным Университета штата Джорджия (открывается в новой вкладке). Чем быстрее движутся атомы или молекулы, тем выше температура, и чем больше атомов или молекул находятся в движении, тем большее количество тепла они передают.
Температура — это «мера средней кинетической энергии частиц в образце вещества, выраженная в единицах или градусах по стандартной шкале», согласно Словарю американского наследия . Наиболее часто используемой температурной шкалой является шкала Цельсия, которая основана на температурах замерзания и кипения воды, присваивая соответствующие значения 0 C и 100 C. Шкала Фаренгейта также основана на температурах замерзания и кипения воды, которым присвоены значения. 32 градуса по Фаренгейту и 212 градусов по Фаренгейту соответственно.
32 градуса по Фаренгейту и 212 градусов по Фаренгейту соответственно.
Ученые во всем мире, однако, используют шкалу Кельвина (К без знака градуса), названную в честь Уильяма Томсона, 1-го барона Кельвина, потому что она основана на общей тепловой энергии, а не на температурах замерзания и кипения воды, по данным Национальной библиотеки. Шотландии (откроется в новой вкладке). В этой шкале используются те же приращения, что и в шкале Цельсия; например, изменение температуры на 1 C равно 1 K. Однако шкала Кельвина начинается с абсолютного нуля, температуры, при которой полностью отсутствует тепловая энергия и прекращается всякое молекулярное движение. Температура 0 К равна минус 459.67 F или минус 273,15 C.
Удельная теплоемкость
Количество теплоты, необходимое для повышения температуры определенной массы вещества на определенную величину, называется удельной теплоемкостью, или удельной теплоемкостью, согласно Wolfram Research (opens в новой вкладке). Условной единицей для этого являются калории на грамм на кельвин. Калория определяется как количество тепловой энергии, необходимое для повышения температуры 1 грамма воды при 4 градусах Цельсия на 1 градус.
Калория определяется как количество тепловой энергии, необходимое для повышения температуры 1 грамма воды при 4 градусах Цельсия на 1 градус.
Удельная теплоемкость металла почти полностью зависит от количества атомов в образце и способа их связи, а не от массы образца. Например, килограмм алюминия может поглотить примерно в семь раз больше тепла, чем килограмм свинца. Однако данная масса воды может поглотить почти в пять раз больше тепла, чем такая же масса алюминия, благодаря сильным силам, связывающим молекулы воды, согласно данным Университета Юго-Восточной Луизианы .
Теплопроводность
Центральный процессор (ЦП) является неотъемлемой частью аппаратных компонентов компьютера. (Изображение предоставлено: Нарумон Бовонкитванчай через Getty Images) Теплопроводность ( k ) — это «скорость, с которой тепло проходит через определенное поперечное сечение определенного материала», согласно «Термосеткам» Дебдатты Ратны (открывается в новой вкладке). ) (Woodhead Publishing limited, 2012 г.). Единицей для k является ватт (Вт) на метр (м) на кельвин (K), согласно Swarthmore College . Значения k для таких металлов, как медь и серебро, относительно высоки и составляют 380 и 420 Вт/м·К соответственно. Это свойство делает эти материалы полезными для автомобильных радиаторов и ребер охлаждения компьютерных микросхем, поскольку они могут быстро отводить тепло и обмениваться им с окружающей средой. Согласно исследованию 2009 года, опубликованному в журнале «Материалы» (открывается в новой вкладке), наивысшее значение k для любого природного вещества имеет алмаз при 2200 Вт/м·К.
) (Woodhead Publishing limited, 2012 г.). Единицей для k является ватт (Вт) на метр (м) на кельвин (K), согласно Swarthmore College . Значения k для таких металлов, как медь и серебро, относительно высоки и составляют 380 и 420 Вт/м·К соответственно. Это свойство делает эти материалы полезными для автомобильных радиаторов и ребер охлаждения компьютерных микросхем, поскольку они могут быстро отводить тепло и обмениваться им с окружающей средой. Согласно исследованию 2009 года, опубликованному в журнале «Материалы» (открывается в новой вкладке), наивысшее значение k для любого природного вещества имеет алмаз при 2200 Вт/м·К.
Полезны и другие материалы, поскольку они крайне плохо проводят тепло; это свойство называется термическим сопротивлением, или R -значение, которое описывает скорость, с которой тепло передается через материал. Эти материалы, такие как стекловолокно, гусиный пух и пенополистирол, используются для изоляции наружных стен зданий, зимних пальто и термокружек для кофе. R – значение дано в квадратных футах, умноженных на градусы Фаренгейта, умноженные на часы на одну британскую тепловую единицу (открывается в новой вкладке) (фут2·°F·ч/БТЕ), согласно OpenStax (открывается в новой вкладке), открытая -исходный учебник.
R – значение дано в квадратных футах, умноженных на градусы Фаренгейта, умноженные на часы на одну британскую тепловую единицу (открывается в новой вкладке) (фут2·°F·ч/БТЕ), согласно OpenStax (открывается в новой вкладке), открытая -исходный учебник.
Закон охлаждения Ньютона
В 1701 году сэр Исаак Ньютон впервые сформулировал свой Закон охлаждения в короткой статье под названием «Scala graduum Caloris» («Шкала степеней тепла») в Philosophical Transactions of the Royal Society. Формулировка закона Ньютоном переводится с оригинальной латыни как «избыток степеней тепла … находился в геометрической прогрессии, тогда как времена находятся в арифметической прогрессии». Вустерский политехнический институт предлагает более современную версию этого научного закона: «скорость изменения температуры пропорциональна разнице между температурой объекта и окружающей среды».
Это приводит к экспоненциальному спаду (откроется в новой вкладке) разницы температур. Например, если теплый предмет поместить в холодную ванну, в течение определенного промежутка времени разница между двумя температурами уменьшится вдвое. Затем за тот же промежуток времени оставшаяся разница снова уменьшится вдвое. Это повторяющееся уменьшение разницы температур вдвое будет продолжаться через равные промежутки времени, пока она не станет слишком малой для измерения. В этот момент система находится в тепловом равновесии.
Затем за тот же промежуток времени оставшаяся разница снова уменьшится вдвое. Это повторяющееся уменьшение разницы температур вдвое будет продолжаться через равные промежутки времени, пока она не станет слишком малой для измерения. В этот момент система находится в тепловом равновесии.
Теплопередача
Схема, показывающая, как работает теплопередача. (Изображение предоставлено blueringmedia через Getty Images)Тепло может передаваться от одного тела к другому или между телом и окружающей средой тремя различными способами: проводимостью, конвекцией и излучением. Проводимость — это передача энергии через твердое тело. Проводимость между телами возникает, когда они находятся в непосредственном контакте, и молекулы передают свою энергию через поверхность раздела.
Конвекция – это передача тепла к текучей среде или от нее. Молекулы в газе или жидкости, соприкасающиеся с твердым телом, передают или поглощают тепло к этому телу или от него, а затем удаляются, позволяя другим молекулам жидкости перемещаться на место и повторять процесс.
Излучение – это излучение энергии посредством электромагнитного (ЭМ) излучения, особенно фотонов инфракрасного излучения, переносящих тепловую энергию. Вся материя излучает и поглощает некоторое количество электромагнитного излучения, чистое количество которого определяет, вызывает ли это потерю или увеличение тепла, согласно данным Северо-Западного университета .
Цикл Карно
В 1824 году Николя Леонар Сади Карно предложил модель тепловой машины, основанную на так называемом цикле Карно, согласно данным Американского общества инженеров-механиков . в новой вкладке). Цикл использует взаимосвязь между давлением, объемом и температурой газов, а также то, как подводимая энергия может изменять форму и выполнять работу вне системы.
Первым этапом цикла Карно является изотермическое расширение, при котором газ в цилиндре под давлением поршня поддерживается при постоянной температуре, но источник тепла контактирует с цилиндром. Чтобы поддерживать ту же температуру, газ должен расширяться. Затем адиабатическое расширение, или расширение без передачи тепла в окружающую среду, снимает вес с поршня, позволяя газу расширяться дальше, что помогает ему толкать цилиндр для выполнения работы. Затем газ охлаждается при постоянной температуре и сжимается за счет добавления веса к поршню для повышения давления в газе, после чего тепло передается от газа обратно к источнику тепла. И, наконец, адиабатическое сжатие увеличивает вес поршня, чтобы еще больше увеличить давление газа и, следовательно, повысить его температуру. Затем цикл повторяется, сообщает НАСА (откроется в новой вкладке). По данным Университета штата Джорджия, это основной принцип тепловых насосов, используемых для отопления, кондиционирования и охлаждения .
Затем адиабатическое расширение, или расширение без передачи тепла в окружающую среду, снимает вес с поршня, позволяя газу расширяться дальше, что помогает ему толкать цилиндр для выполнения работы. Затем газ охлаждается при постоянной температуре и сжимается за счет добавления веса к поршню для повышения давления в газе, после чего тепло передается от газа обратно к источнику тепла. И, наконец, адиабатическое сжатие увеличивает вес поршня, чтобы еще больше увеличить давление газа и, следовательно, повысить его температуру. Затем цикл повторяется, сообщает НАСА (откроется в новой вкладке). По данным Университета штата Джорджия, это основной принцип тепловых насосов, используемых для отопления, кондиционирования и охлаждения .
Энтропия
Все термодинамические системы генерируют отработанное тепло. Эти потери приводят к увеличению энтропии, которая является мерой беспорядка в системе. Согласно Britannica, поскольку работа возникает в результате упорядоченного молекулярного движения, энтропия является мерой энергии, недоступной для выполнения работы . Энтропия в любой закрытой системе всегда возрастает; это никогда не убывает . Кроме того, движущиеся части производят отработанное тепло из-за трения, и из системы неизбежно происходит утечка лучистого тепла.
Энтропия в любой закрытой системе всегда возрастает; это никогда не убывает . Кроме того, движущиеся части производят отработанное тепло из-за трения, и из системы неизбежно происходит утечка лучистого тепла.
Это делает невозможным создание так называемых вечных двигателей. Сиабал Митра, профессор физики в Университете штата Миссури, сказал Live Science: «Вы не можете построить двигатель, который будет эффективен на 100%, а это значит, что вы не сможете построить вечный двигатель. Не поверите, и есть люди, которые до сих пор пытаются строить вечные двигатели».
Энтропия также определяется как «мера беспорядка или случайности в замкнутой системе», которая также неумолимо возрастает. Вы можете смешивать горячую и холодную воду, но поскольку большая чашка теплой воды более беспорядочна, чем две меньшие чашки, содержащие горячую и холодную воду, вы никогда не сможете снова разделить ее на горячую и холодную, не добавляя энергии в систему. Иными словами, вы не сможете разбить яйцо или удалить сливки из кофе. Таким образом, энтропия дает нам стрелу времени: вперед — это направление увеличения энтропии.
Таким образом, энтропия дает нам стрелу времени: вперед — это направление увеличения энтропии.
Четыре закона термодинамики
Фундаментальные принципы термодинамики первоначально были выражены в трех законах. Позже ученые выяснили, что более фундаментальный закон был проигнорирован, по-видимому, потому, что он казался настолько очевидным, что его не нужно было формулировать явно. Чтобы сформировать полный набор правил, ученые решили, что необходимо включить этот самый фундаментальный закон. Проблема, однако, заключалась в том, что первые три закона уже были установлены и были хорошо известны по присвоенным им номерам. Столкнувшись с перспективой перенумерации существующих законов, что вызвало бы значительную путаницу, или помещения основного закона в конец списка, что не имело бы логического смысла, британский физик Ральф Х. Фаулер предложил альтернативу, которая решил дилемму: он назвал новый закон «Законом Зерота», согласно Колледж Святого Ансельма . Вот краткое изложение всех четырех законов:
Нулевой закон термодинамики гласит, что если два тела находятся в тепловом равновесии с каким-то третьим телом, то они также находятся в равновесии друг с другом. Это устанавливает температуру как фундаментальное и измеримое свойство материи.
Это устанавливает температуру как фундаментальное и измеримое свойство материи.
Первый закон термодинамики гласит, что общее увеличение энергии системы равно увеличению тепловой энергии плюс работа, совершенная системой. В нем говорится, что тепло является формой энергии и, следовательно, подчиняется принципу сохранения, то есть оно не может быть ни создано, ни уничтожено.
Второй закон термодинамики гласит, что тепловая энергия не может передаваться от тела с более низкой температурой к телу с более высокой температурой без добавления энергии. Вот почему кондиционер стоит денег.
Третий закон термодинамики гласит, что энтропия идеального кристалла — то есть вещества, состоящего из атомов, расположенных в идеально упорядоченном симметричном порядке — при абсолютном нуле равна нулю. Как объяснялось выше, энтропию иногда называют «бесполезной энергией» или энергией, которая не может выполнять работу; а поскольку при абсолютном нуле нет никакой тепловой энергии, не может быть и ненужной энергии. Энтропия также является мерой беспорядка в системе, и хотя идеальный кристалл по определению идеально упорядочен, любое положительное значение температуры означает, что внутри кристалла есть движение, вызывающее беспорядок. По этим причинам не может быть физической системы с меньшей энтропией, поэтому энтропия всегда имеет положительное значение.
Энтропия также является мерой беспорядка в системе, и хотя идеальный кристалл по определению идеально упорядочен, любое положительное значение температуры означает, что внутри кристалла есть движение, вызывающее беспорядок. По этим причинам не может быть физической системы с меньшей энтропией, поэтому энтропия всегда имеет положительное значение.
Наука термодинамика развивалась веками, и ее принципы применимы почти ко всем когда-либо изобретенным устройствам. Его значение в современной технике невозможно переоценить.
Автор Live Science Эшли Хамер обновила эту статью 28 января 2022 г. его наиболее заметные моменты и фигуры. Университет Кентукки Факультет физики и астрономии, «Температура и тепло — тепловая энергия», https://www.pa.uky.edu/~straley/THE/heat/then4.htm (открывается в новом вкладка) Карл Нав, «Тепло», Гиперфизика, Университет штата Джорджия, 2017 г. http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/heat.html (открывается в новой вкладке) Более общий взгляд на температуру», Гиперфизика, Университет штата Джорджия, 2017 г. Температура». 2022. https://www.ahdictionary.com/word/search.html?q=temperature (открывается в новой вкладке) Шотландский Зал славы науки, «Лорд Кельвин (1824–1819 гг.)07)». 2009 г. https://digital.nls.uk/scientists/biographies/lord-kelvin/ (открывается в новой вкладке) Wolfram Research, «Specific Heat». 2007 г. https://scienceworld.wolfram. com/physics/SpecificHeat.html (открывается в новой вкладке) Университет Юго-Восточной Луизианы, «Термодинамика, часть 1: работа, теплота, внутренняя энергия и энтальпия», 2000 г. Дебдатта Ратна, «3 — Термические свойства реактопластов», Реактопласты: структура, свойства и применение, 2012 г. https://www.sciencedirect.com/science/article/ пий/B9780857090867500031 (открывается в новой вкладке) Эрик Чивер, «Элементы тепловых систем», Swarthmore College, 2021. https://lpsa.swarthmore.edu/Systems/Thermal/SysThermalElem.html (открывается в новой вкладке) Сергей Кидалов В. и Шахов Федор М., «Теплопроводность алмазных композитов», Материалы (Базель), декабрь 2009 г. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5513588/ (открывается в новой вкладке ) Пол Питер Урон и Роберт Хинрикс, «Физика в колледже». OpenStax, 22 августа 2016 г. https://pressbooks.online.ucf.edu/algphysics/chapter/conduction/ (открывается в новой вкладке) Исаак Ньютон, “VII. Scala graduum caloris”, Philosophical Transactions of the Royal Society, 1701. Вустерский политехнический институт, “Закон охлаждения Ньютона”, 1996 г. http://www.math.wpi.edu/Course_Materials /MA1022A96/lab2/node5.html (открывается в новой вкладке) Северо-Западный университет, “Как движется тепло?” https://www.qrg.northwestern.edu/projects/vss/docs/thermal/1-how-does-heat-move.html (открывается в новой вкладке) Карл Нэйв, «Цикл Карно», Гиперфизика, Джорджия Государственный университет, 2017 г. http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/carnot.html (открывается в новой вкладке) НАСА, «Цикл Карно», 2021 г. https://www.grc.nasa.gov/www/k-12/airplane/carnot.html (открывается в новой вкладке) Карл Нейв, «Тепловой насос», Гиперфизика, Университет штата Джорджия, 2017 г. http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/heatpump.html (открывается в новой вкладке) Словарь американского наследия, «Энтропия», 2022 г. https:/ /www.ahdictionary.com/word/search.html?q=entropy Ян Т. Дарем, «Ральф Фаулер», Колледж Св. Джим Лукас — автор статей для Live Science. Он охватывает физику, астрономию и инженерное дело. Джим окончил Университет штата Миссури, где получил степень бакалавра наук в области физики, а также астрономию и техническое письмо. После окончания университета он работал в Лос-Аламосской национальной лаборатории системным администратором, техническим писателем-редактором и специалистом по ядерной безопасности. Помимо написания статей, он редактирует статьи в научных журналах по различным тематическим направлениям. При участии Термодинамика — это раздел физики, изучающий взаимосвязь между теплом и другими формами энергии. Тепловая энергия — это энергия, которой вещество или система обладает благодаря своей температуре — другими словами, энергия движущихся или вибрирующих молекул — по данным Университета Кентукки . Термодинамика включает в себя измерение этой энергии, что может быть «чрезвычайно сложным», сказал Live Science Дэвид Макки, профессор физики Южного государственного университета штата Миссури. «Системы, которые мы изучаем в термодинамике… состоят из очень большого числа атомов или молекул, взаимодействующих сложным образом. Но если эти системы соответствуют правильным критериям, которые мы называем равновесием, их можно описать с помощью очень небольшого числа измерений или числа. Часто это идеализируется как масса системы, давление системы и объем системы или какой-либо другой эквивалентный набор чисел». Таким образом, термодинамика занимается несколькими свойствами материи; в первую очередь это тепло. Количество тепла, передаваемого веществом, зависит от скорости и количества атомов или молекул этого вещества в движении, по данным Университета штата Джорджия (открывается в новой вкладке). Температура — это «мера средней кинетической энергии частиц в образце вещества, выраженная в единицах или градусах по стандартной шкале», согласно Словарю американского наследия . Наиболее часто используемой температурной шкалой является шкала Цельсия, которая основана на температурах замерзания и кипения воды, присваивая соответствующие значения 0 C и 100 C. Шкала Фаренгейта также основана на температурах замерзания и кипения воды, которым присвоены значения. 32 градуса по Фаренгейту и 212 градусов по Фаренгейту соответственно. Ученые во всем мире, однако, используют шкалу Кельвина (К без знака градуса), названную в честь Уильяма Томсона, 1-го барона Кельвина, потому что она основана на общей тепловой энергии, а не на температурах замерзания и кипения воды, по данным Национальной библиотеки. Шотландии (откроется в новой вкладке). Количество теплоты, необходимое для повышения температуры определенной массы вещества на определенную величину, называется удельной теплоемкостью, или удельной теплоемкостью, согласно Wolfram Research (opens в новой вкладке). Условной единицей для этого являются калории на грамм на кельвин. Калория определяется как количество тепловой энергии, необходимое для повышения температуры 1 грамма воды при 4 градусах Цельсия на 1 градус. Удельная теплоемкость металла почти полностью зависит от количества атомов в образце и способа их связи, а не от массы образца. Например, килограмм алюминия может поглотить примерно в семь раз больше тепла, чем килограмм свинца. Теплопроводность ( k ) — это «скорость, с которой тепло проходит через определенное поперечное сечение определенного материала», согласно «Термосеткам» Дебдатты Ратны (открывается в новой вкладке). ) (Woodhead Publishing limited, 2012 г.). Единицей для k является ватт (Вт) на метр (м) на кельвин (K), согласно Swarthmore College . Значения k для таких металлов, как медь и серебро, относительно высоки и составляют 380 и 420 Вт/м·К соответственно. Это свойство делает эти материалы полезными для автомобильных радиаторов и ребер охлаждения компьютерных микросхем, поскольку они могут быстро отводить тепло и обмениваться им с окружающей средой. Полезны и другие материалы, поскольку они крайне плохо проводят тепло; это свойство называется термическим сопротивлением, или R -значение, которое описывает скорость, с которой тепло передается через материал. Эти материалы, такие как стекловолокно, гусиный пух и пенополистирол, используются для изоляции наружных стен зданий, зимних пальто и термокружек для кофе. R – значение дано в квадратных футах, умноженных на градусы Фаренгейта, умноженные на часы на одну британскую тепловую единицу (открывается в новой вкладке) (фут2·°F·ч/БТЕ), согласно OpenStax (открывается в новой вкладке), открытая -исходный учебник. В 1701 году сэр Исаак Ньютон впервые сформулировал свой Закон охлаждения в короткой статье под названием «Scala graduum Caloris» («Шкала степеней тепла») в Philosophical Transactions of the Royal Society. Это приводит к экспоненциальному спаду (откроется в новой вкладке) разницы температур. Например, если теплый предмет поместить в холодную ванну, в течение определенного промежутка времени разница между двумя температурами уменьшится вдвое. Затем за тот же промежуток времени оставшаяся разница снова уменьшится вдвое. Это повторяющееся уменьшение разницы температур вдвое будет продолжаться через равные промежутки времени, пока она не станет слишком малой для измерения. В этот момент система находится в тепловом равновесии. Тепло может передаваться от одного тела к другому или между телом и окружающей средой тремя различными способами: проводимостью, конвекцией и излучением. Проводимость — это передача энергии через твердое тело. Проводимость между телами возникает, когда они находятся в непосредственном контакте, и молекулы передают свою энергию через поверхность раздела. Конвекция – это передача тепла к текучей среде или от нее. Молекулы в газе или жидкости, соприкасающиеся с твердым телом, передают или поглощают тепло к этому телу или от него, а затем удаляются, позволяя другим молекулам жидкости перемещаться на место и повторять процесс. Излучение – это излучение энергии посредством электромагнитного (ЭМ) излучения, особенно фотонов инфракрасного излучения, переносящих тепловую энергию. Вся материя излучает и поглощает некоторое количество электромагнитного излучения, чистое количество которого определяет, вызывает ли это потерю или увеличение тепла, согласно данным Северо-Западного университета . В 1824 году Николя Леонар Сади Карно предложил модель тепловой машины, основанную на так называемом цикле Карно, согласно данным Американского общества инженеров-механиков . в новой вкладке). Цикл использует взаимосвязь между давлением, объемом и температурой газов, а также то, как подводимая энергия может изменять форму и выполнять работу вне системы. Первым этапом цикла Карно является изотермическое расширение, при котором газ в цилиндре под давлением поршня поддерживается при постоянной температуре, но источник тепла контактирует с цилиндром. Чтобы поддерживать ту же температуру, газ должен расширяться. Затем адиабатическое расширение, или расширение без передачи тепла в окружающую среду, снимает вес с поршня, позволяя газу расширяться дальше, что помогает ему толкать цилиндр для выполнения работы. Затем газ охлаждается при постоянной температуре и сжимается за счет добавления веса к поршню для повышения давления в газе, после чего тепло передается от газа обратно к источнику тепла. Все термодинамические системы генерируют отработанное тепло. Эти потери приводят к увеличению энтропии, которая является мерой беспорядка в системе. Согласно Britannica, поскольку работа возникает в результате упорядоченного молекулярного движения, энтропия является мерой энергии, недоступной для выполнения работы . Энтропия в любой закрытой системе всегда возрастает; это никогда не убывает . Кроме того, движущиеся части производят отработанное тепло из-за трения, и из системы неизбежно происходит утечка лучистого тепла. Это делает невозможным создание так называемых вечных двигателей. Энтропия также определяется как «мера беспорядка или случайности в замкнутой системе», которая также неумолимо возрастает. Вы можете смешивать горячую и холодную воду, но поскольку большая чашка теплой воды более беспорядочна, чем две меньшие чашки, содержащие горячую и холодную воду, вы никогда не сможете снова разделить ее на горячую и холодную, не добавляя энергии в систему. Иными словами, вы не сможете разбить яйцо или удалить сливки из кофе. Таким образом, энтропия дает нам стрелу времени: вперед — это направление увеличения энтропии. Фундаментальные принципы термодинамики первоначально были выражены в трех законах. Позже ученые выяснили, что более фундаментальный закон был проигнорирован, по-видимому, потому, что он казался настолько очевидным, что его не нужно было формулировать явно. Нулевой закон термодинамики гласит, что если два тела находятся в тепловом равновесии с каким-то третьим телом, то они также находятся в равновесии друг с другом. Это устанавливает температуру как фундаментальное и измеримое свойство материи. Первый закон термодинамики гласит, что общее увеличение энергии системы равно увеличению тепловой энергии плюс работа, совершенная системой. Второй закон термодинамики гласит, что тепловая энергия не может передаваться от тела с более низкой температурой к телу с более высокой температурой без добавления энергии. Вот почему кондиционер стоит денег. Третий закон термодинамики гласит, что энтропия идеального кристалла — то есть вещества, состоящего из атомов, расположенных в идеально упорядоченном симметричном порядке — при абсолютном нуле равна нулю. Как объяснялось выше, энтропию иногда называют «бесполезной энергией» или энергией, которая не может выполнять работу; а поскольку при абсолютном нуле нет никакой тепловой энергии, не может быть и ненужной энергии. Энтропия также является мерой беспорядка в системе, и хотя идеальный кристалл по определению идеально упорядочен, любое положительное значение температуры означает, что внутри кристалла есть движение, вызывающее беспорядок. Наука термодинамика развивалась веками, и ее принципы применимы почти ко всем когда-либо изобретенным устройствам. Его значение в современной технике невозможно переоценить. Автор Live Science Эшли Хамер обновила эту статью 28 января 2022 г. его наиболее заметные моменты и фигуры. Университет Кентукки Факультет физики и астрономии, «Температура и тепло — тепловая энергия», https://www.pa.uky.edu/~straley/THE/heat/then4. Карл Нав, «Тепло», Гиперфизика, Университет штата Джорджия, 2017 г. http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/heat.html (открывается в новой вкладке) Более общий взгляд на температуру», Гиперфизика, Университет штата Джорджия, 2017 г. Температура». 2022. https://www.ahdictionary.com/word/search.html?q=temperature (открывается в новой вкладке) Шотландский Зал славы науки, «Лорд Кельвин (1824–1819 гг.)07)». 2009 г. https://digital.nls.uk/scientists/biographies/lord-kelvin/ (открывается в новой вкладке) Wolfram Research, «Specific Heat». 2007 г. https://scienceworld.wolfram. com/physics/SpecificHeat.html (открывается в новой вкладке) Университет Юго-Восточной Луизианы, «Термодинамика, часть 1: работа, теплота, внутренняя энергия и энтальпия», 2000 г. https://www2.southeast.edu/Academics/Faculty/ wparkinson/help/thermochemistry/ (открывается в новой вкладке) Дебдатта Ратна, «3 — Термические свойства реактопластов», Реактопласты: структура, свойства и применение, 2012 г. Эрик Чивер, «Элементы тепловых систем», Swarthmore College, 2021. https://lpsa.swarthmore.edu/Systems/Thermal/SysThermalElem.html (открывается в новой вкладке) Сергей Кидалов В. и Шахов Федор М., «Теплопроводность алмазных композитов», Материалы (Базель), декабрь 2009 г. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5513588/ (открывается в новой вкладке ) Пол Питер Урон и Роберт Хинрикс, «Физика в колледже». OpenStax, 22 августа 2016 г. https://pressbooks.online.ucf.edu/algphysics/chapter/conduction/ (открывается в новой вкладке) Исаак Ньютон, “VII. Scala graduum caloris”, Philosophical Transactions of the Royal Society, 1701. Вустерский политехнический институт, “Закон охлаждения Ньютона”, 1996 г. http://www.math.wpi.edu/Course_Materials /MA1022A96/lab2/node5.html (открывается в новой вкладке) Северо-Западный университет, “Как движется тепло?” https://www. Карл Нэйв, «Цикл Карно», Гиперфизика, Джорджия Государственный университет, 2017 г. http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/carnot.html (открывается в новой вкладке) НАСА, «Цикл Карно», 2021 г. https://www.grc.nasa.gov/www/k-12/airplane/carnot.html (открывается в новой вкладке) Карл Нейв, «Тепловой насос», Гиперфизика, Университет штата Джорджия, 2017 г. http://hyperphysics.phy-astr.gsu.edu/hbase/thermo/heatpump.html (открывается в новой вкладке) Словарь американского наследия, «Энтропия», 2022 г. https:/ /www.ahdictionary.com/word/search.html?q=entropy Ян Т. Дарем, «Ральф Фаулер», Колледж Св. Ансельма. 2001. https://mathshistory.st-andrews.ac.uk/Biographies/Fowler/ (открывается в новой вкладке) Джим Лукас — автор статей для Live Science. Он охватывает физику, астрономию и инженерное дело. Джим окончил Университет штата Миссури, где получил степень бакалавра наук в области физики, а также астрономию и техническое письмо. При участии ? A. Термодинамика: определение Слово термодинамика происходит от греческого слова thermos , что означает тепло, и dynamis , что означает мощность. Вместо того, чтобы быть сгруппированным в семье химии, термодинамика является частью семьи физики. По сути, термодинамика — это наука, изучающая изменения температуры, давления и объема физических систем в макроскопическом масштабе путем анализа коллективного движения их частиц с помощью наблюдений и статистики. Поскольку тепло означает энергию в пути и динамику связано с движением; термодинамика изучает движение энергии и то, как энергия создает движение. B. Термодинамика и тепло: история До 19-го века было распространено мнение, что степень, в которой объект ощущается горячим или холодным, зависит от количества тепла, содержащегося в нем. В то время тепло представлялось жидкостью, перетекающей от горячего объекта к холодному. В это время невесомая жидкость называлась «калорийной». Так оставалось до тех пор, пока Джозеф Блэк (1728-1799) не обнаружил связь между количеством (калорией) и интенсивностью (температурой) тепла, в отличие от отсутствия разницы между теплом и температурой. В конце концов, в 1847 году Дж. П. Джоуль опубликовал окончательную статью , которая подтвердила идею о том, что тепло является формой энергии. В термодинамике есть четыре закона. Широкие возможности применения, они могут быть полезны для всех типов систем, если функциональный элемент связан с балансом энергии и переносом материи. Далекие примеры таких применений включают на рубеже 20–20 9 гг.0366 й век, Теория Эйнштейна о спонтанном излучении, а также текущие исследования, которые проводятся в области термодинамики черных дыр. Нулевой закон термодинамики. Термодинамическое равновесие является отношением эквивалентности. Нулевой закон объясняется следующим образом: если две термодинамические системы находятся в тепловом равновесии с третьей, они также находятся в тепловом равновесии друг с другом. Вышеупомянутые эксперименты Джоуля, посредством которых он подтвердил представление о том, что тепло действительно является формой энергии, были предпосылкой первого закона термодинамики (также известного как закон преобразования энергии) Первый закон термодинамики (сохранение энергии). При преобразовании тепла в любую другую форму энергии или при преобразовании других форм энергии в тепло общее количество энергии (тепло плюс другие формы) в системе остается постоянным. В частности, в отношении того, как работают машины (исторически термодинамика была разработана из-за необходимости повышения эффективности промышленных паровых двигателей), второй закон термодинамики объясняет, что циклическая машина не может преобразовывать тепловую энергию сама по себе в другие формы энергии. . Второй закон термодинамики (энтропия). Полная энтропия (измерение внутренней энергии) любой изолированной термодинамической системы имеет тенденцию к увеличению со временем, приближаясь к максимальному значению. Второй закон термодинамики предполагает, что некоторые процессы приводят к необратимым результатам. Например, процесс преобразования тепла в механическую энергию нельзя обратить вспять; вы не можете преобразовать механическую энергию в тепло после того, как тепловая энергия была преобразована в механическую энергию. Третий закон термодинамики фокусируется на температуре абсолютного нуля. Третий закон термодинамики (температура абсолютного нуля). Хотите узнать больше? Почему бы не пройти онлайн-курс по физике? При асимптотическом приближении системы к абсолютному нулю температуры все процессы практически прекращаются и энтропия системы асимптотически приближается к минимальному значению. Третий закон термодинамики подкрепляет представление о том, что при достижении измерения абсолютного нуля система теряет всякую ценность и способность функционировать. В соответствии с третьим законом термодинамики, помимо того, что она состоит из всех основных принципов термодинамики, термодинамическая шкала температуры (также известная как абсолютная шкала или шкала Кельвина) считается абсолютной мерой температуры. Это абсолютная шкала не только потому, что она используется для измерения температуры или тепла, но и потому, что она измеряет фундаментальное свойство, лежащее в основе температуры, нулевую или нулевую точку на термодинамической температурной шкале. По определению, абсолютный ноль — это самая низкая возможная температура, при которой ничто не может быть холоднее и из вещества больше нельзя извлечь тепловую энергию. Термодинамическая шкала температур представлена идентичной шкале температур газа. Это основано на микроскопической (детальной) интерпретации температуры, которая предполагает, что макроскопическая (широкая) измеримая величина, известная как температура , является результатом случайных движений отдельных частиц, составляющих систему. Важным понятием в термодинамике является система . Система — это область Вселенной, которая считается изучаемой . Система отделена от остальной Вселенной либо воображаемой, либо реальной границей. Эта граница помогает выделить определенную область, а также указать определенный объем. Через очерченную границу происходит обмен работой, теплом и/или веществом между системой и ее окружением. В термодинамике выделяют пять основных классов систем: 1. Изолированные системы. Где материя и энергия не пересекают границу. 2. Адиабатические системы . Где тепло не переходит границы. 3. Диатермические системы. Там, где тепло может пересечь границу. 4. Закрытые системы. Где материя не переходит границы. 5. Открытые системы. Там, где тепло, работа и материя могут пересечь границу. В изолированных системах общие внутренние различия в системе со временем сглаживаются; давления, температуры и плотности имеют тенденцию уравновешиваться. И, наконец, термодинамические процессы, протекающие с невероятно медленной скоростью, когда каждая промежуточная стадия считается равновесной, классифицируются как обратимые процессы. F. Термодинамика: параметры Центральная концепция термодинамики вращается вокруг идеи энергии, т. е. способности совершать работу. Согласно первому закону, энергетический уровень всей системы, а также ее окружения сохраняется. Энергия может быть передана телу с помощью таких средств, как нагревание, сжатие или добавление большего количества вещества. Для сравнения, в механике передача энергии является результатом сил, вызывающих перемещение. Таким образом, произведение двух равно общему количеству передаваемой энергии. В аналогичном смысле термодинамические системы влекут за собой передачу энергии, производимой общей силой, которая вызывает общее смещение. Таким образом, произведение двух равно общему количеству передаваемой энергии. В частности, термодинамические пары сила-перемещение называются «сопряженными переменными». Наиболее распространены: давление-объем (механические параметры), температура-энтропия (тепловые параметры) и химический потенциал-число частиц (материальные параметры). G. Термодинамика: состояния При определенном наборе условий, когда система находится в равновесии, говорят, что она существует в определенном состоянии . Состояние системы может быть описано как интенсивными, так и экстенсивными переменными. Состояние можно рассматривать как непосредственное количественное описание системы, в которой заданное число переменных поддерживается постоянным. H. Термодинамика: процессы Определение термодинамического процесса – это энергосодержащее преобразование термодинамической системы, посредством которого она переходит из начального состояния в конечное. По большей части каждый термодинамический процесс отличается от других процессов. Фиксированные примеры некоторых конкретных отличительных характеристик, которые отделяют друг от друга, включают: количество энергии, параметры процесса, температуру, давление и объем материала. Примечание: Было сочтено полезным сгруппировать эти процессы в пары, в которых каждая переменная, сохраняемая постоянной, является одним членом сопряженной пары.
Библиография
 https://www2.southeast.edu/Academics/Faculty/ wparkinson/help/thermochemistry/ (открывается в новой вкладке)
https://www2.southeast.edu/Academics/Faculty/ wparkinson/help/thermochemistry/ (открывается в новой вкладке) 
 Ансельма. 2001. https://mathshistory.st-andrews.ac.uk/Biographies/Fowler/ (открывается в новой вкладке)
Ансельма. 2001. https://mathshistory.st-andrews.ac.uk/Biographies/Fowler/ (открывается в новой вкладке) Что такое термодинамика? | Живая наука
Инженер осматривает лопатки паровой турбины.
(Изображение предоставлено: Монти Ракусен через Getty Images) В частности, он описывает, как тепловая энергия преобразуется в другие формы энергии и из них, а также как тепловая энергия влияет на материю.
В частности, он описывает, как тепловая энергия преобразуется в другие формы энергии и из них, а также как тепловая энергия влияет на материю. Теплота
 По данным Университета штата Джорджия, тепло — это энергия, передаваемая между веществами или системами из-за разницы температур между ними . Как форма энергии тепло сохраняется — его нельзя создать или уничтожить. Однако его можно перенести из одного места в другое. Тепло также может быть преобразовано в другие формы энергии и обратно. Например, паровая турбина может преобразовывать тепло в кинетическую энергию для запуска генератора, который преобразует кинетическую энергию в электрическую. Лампочка может преобразовывать эту электрическую энергию в электромагнитное излучение (свет), которое при поглощении поверхностью снова преобразуется в тепло. В ходе этого процесса часть энергии теряется в энтропию.
По данным Университета штата Джорджия, тепло — это энергия, передаваемая между веществами или системами из-за разницы температур между ними . Как форма энергии тепло сохраняется — его нельзя создать или уничтожить. Однако его можно перенести из одного места в другое. Тепло также может быть преобразовано в другие формы энергии и обратно. Например, паровая турбина может преобразовывать тепло в кинетическую энергию для запуска генератора, который преобразует кинетическую энергию в электрическую. Лампочка может преобразовывать эту электрическую энергию в электромагнитное излучение (свет), которое при поглощении поверхностью снова преобразуется в тепло. В ходе этого процесса часть энергии теряется в энтропию. Температура
Сравнение температур замерзания и плавления воды (в градусах Цельсия). (Изображение предоставлено: Why Design через Shutterstock) Чем быстрее движутся атомы или молекулы, тем выше температура, и чем больше атомов или молекул находятся в движении, тем большее количество тепла они передают.
Чем быстрее движутся атомы или молекулы, тем выше температура, и чем больше атомов или молекул находятся в движении, тем большее количество тепла они передают. В этой шкале используются те же приращения, что и в шкале Цельсия; например, изменение температуры на 1 C равно 1 K. Однако шкала Кельвина начинается с абсолютного нуля, температуры, при которой полностью отсутствует тепловая энергия и прекращается всякое молекулярное движение. Температура 0 К равна минус 459.67 F или минус 273,15 C.
В этой шкале используются те же приращения, что и в шкале Цельсия; например, изменение температуры на 1 C равно 1 K. Однако шкала Кельвина начинается с абсолютного нуля, температуры, при которой полностью отсутствует тепловая энергия и прекращается всякое молекулярное движение. Температура 0 К равна минус 459.67 F или минус 273,15 C. Удельная теплоемкость
 Однако данная масса воды может поглотить почти в пять раз больше тепла, чем такая же масса алюминия, благодаря сильным силам, связывающим молекулы воды, согласно данным Университета Юго-Восточной Луизианы .
Однако данная масса воды может поглотить почти в пять раз больше тепла, чем такая же масса алюминия, благодаря сильным силам, связывающим молекулы воды, согласно данным Университета Юго-Восточной Луизианы . Теплопроводность
Центральный процессор (ЦП) является неотъемлемой частью аппаратных компонентов компьютера. (Изображение предоставлено: Нарумон Бовонкитванчай через Getty Images) Согласно исследованию 2009 года, опубликованному в журнале «Материалы» (открывается в новой вкладке), наивысшее значение k для любого природного вещества имеет алмаз при 2200 Вт/м·К.
Согласно исследованию 2009 года, опубликованному в журнале «Материалы» (открывается в новой вкладке), наивысшее значение k для любого природного вещества имеет алмаз при 2200 Вт/м·К. Закон охлаждения Ньютона
 Формулировка закона Ньютоном переводится с оригинальной латыни как «избыток степеней тепла … находился в геометрической прогрессии, тогда как времена находятся в арифметической прогрессии». Вустерский политехнический институт предлагает более современную версию этого научного закона: «скорость изменения температуры пропорциональна разнице между температурой объекта и окружающей среды».
Формулировка закона Ньютоном переводится с оригинальной латыни как «избыток степеней тепла … находился в геометрической прогрессии, тогда как времена находятся в арифметической прогрессии». Вустерский политехнический институт предлагает более современную версию этого научного закона: «скорость изменения температуры пропорциональна разнице между температурой объекта и окружающей среды». Теплопередача
Схема, показывающая, как работает теплопередача. (Изображение предоставлено blueringmedia через Getty Images)
(Изображение предоставлено blueringmedia через Getty Images)
Цикл Карно
 И, наконец, адиабатическое сжатие увеличивает вес поршня, чтобы еще больше увеличить давление газа и, следовательно, повысить его температуру. Затем цикл повторяется, сообщает НАСА (откроется в новой вкладке). По данным Университета штата Джорджия, это основной принцип тепловых насосов, используемых для отопления, кондиционирования и охлаждения .
И, наконец, адиабатическое сжатие увеличивает вес поршня, чтобы еще больше увеличить давление газа и, следовательно, повысить его температуру. Затем цикл повторяется, сообщает НАСА (откроется в новой вкладке). По данным Университета штата Джорджия, это основной принцип тепловых насосов, используемых для отопления, кондиционирования и охлаждения . Энтропия
 Сиабал Митра, профессор физики в Университете штата Миссури, сказал Live Science: «Вы не можете построить двигатель, который будет эффективен на 100%, а это значит, что вы не сможете построить вечный двигатель. Не поверите, и есть люди, которые до сих пор пытаются строить вечные двигатели».
Сиабал Митра, профессор физики в Университете штата Миссури, сказал Live Science: «Вы не можете построить двигатель, который будет эффективен на 100%, а это значит, что вы не сможете построить вечный двигатель. Не поверите, и есть люди, которые до сих пор пытаются строить вечные двигатели». Четыре закона термодинамики
 Чтобы сформировать полный набор правил, ученые решили, что необходимо включить этот самый фундаментальный закон. Проблема, однако, заключалась в том, что первые три закона уже были установлены и были хорошо известны по присвоенным им номерам. Столкнувшись с перспективой перенумерации существующих законов, что вызвало бы значительную путаницу, или помещения основного закона в конец списка, что не имело бы логического смысла, британский физик Ральф Х. Фаулер предложил альтернативу, которая решил дилемму: он назвал новый закон «Законом Зерота», согласно Колледж Святого Ансельма . Вот краткое изложение всех четырех законов:
Чтобы сформировать полный набор правил, ученые решили, что необходимо включить этот самый фундаментальный закон. Проблема, однако, заключалась в том, что первые три закона уже были установлены и были хорошо известны по присвоенным им номерам. Столкнувшись с перспективой перенумерации существующих законов, что вызвало бы значительную путаницу, или помещения основного закона в конец списка, что не имело бы логического смысла, британский физик Ральф Х. Фаулер предложил альтернативу, которая решил дилемму: он назвал новый закон «Законом Зерота», согласно Колледж Святого Ансельма . Вот краткое изложение всех четырех законов:  В нем говорится, что тепло является формой энергии и, следовательно, подчиняется принципу сохранения, то есть оно не может быть ни создано, ни уничтожено.
В нем говорится, что тепло является формой энергии и, следовательно, подчиняется принципу сохранения, то есть оно не может быть ни создано, ни уничтожено. По этим причинам не может быть физической системы с меньшей энтропией, поэтому энтропия всегда имеет положительное значение.
По этим причинам не может быть физической системы с меньшей энтропией, поэтому энтропия всегда имеет положительное значение. Библиография
 htm (открывается в новом вкладка)
htm (открывается в новом вкладка) https://www.sciencedirect.com/science/article/ пий/B9780857090867500031 (открывается в новой вкладке)
https://www.sciencedirect.com/science/article/ пий/B9780857090867500031 (открывается в новой вкладке) qrg.northwestern.edu/projects/vss/docs/thermal/1-how-does-heat-move.html (открывается в новой вкладке)
qrg.northwestern.edu/projects/vss/docs/thermal/1-how-does-heat-move.html (открывается в новой вкладке) После окончания университета он работал в Лос-Аламосской национальной лаборатории системным администратором, техническим писателем-редактором и специалистом по ядерной безопасности. Помимо написания статей, он редактирует статьи в научных журналах по различным тематическим направлениям.
После окончания университета он работал в Лос-Аламосской национальной лаборатории системным администратором, техническим писателем-редактором и специалистом по ядерной безопасности. Помимо написания статей, он редактирует статьи в научных журналах по различным тематическим направлениям. Что такое термодинамика?

 После серии экспериментов, проведенных Джоулем и др. al., Гельмгольц смог наглядно продемонстрировать, как различные формы энергии могут быть преобразованы из одной в другую.
После серии экспериментов, проведенных Джоулем и др. al., Гельмгольц смог наглядно продемонстрировать, как различные формы энергии могут быть преобразованы из одной в другую.
C. Термодинамика: законы 

D. Термодинамика: шкала температур  .
.
E. Термодинамика: Системы 
 Когда система имеет площади, почти все равные, считается, что она находится в состоянии термодинамического равновесия. В термодинамическом равновесии, по определению, свойства системы не меняются со временем. В принципе, системы в равновесии намного проще и легче для понимания, чем системы, которые не находятся в равновесии. В большинстве случаев при анализе термодинамического процесса можно предположить, что каждое промежуточное состояние находится в равновесии. Это также помогает упростить измерение процесса.
Когда система имеет площади, почти все равные, считается, что она находится в состоянии термодинамического равновесия. В термодинамическом равновесии, по определению, свойства системы не меняются со временем. В принципе, системы в равновесии намного проще и легче для понимания, чем системы, которые не находятся в равновесии. В большинстве случаев при анализе термодинамического процесса можно предположить, что каждое промежуточное состояние находится в равновесии. Это также помогает упростить измерение процесса. Его можно извлечь путем: охлаждения, расширения или извлечения вещества.
Его можно извлечь путем: охлаждения, расширения или извлечения вещества. В свою очередь, свойства системы могут быть описаны уравнением состояния, которое определяет характер взаимосвязи, существующей между переменными.
В свою очередь, свойства системы могут быть описаны уравнением состояния, которое определяет характер взаимосвязи, существующей между переменными.

