Таблица Менделеева online – Co
Co
27
2
15
8
2
58.9332±1
3d74s2
Кобальт
| Относительная электроотрицательность (по Полингу): | 1,75 |
| Температура плавления: | 1663°C |
| Температура кипения: | 3402°C |
| Теплопроводность: | 23 |
| Плотность: | 9,85 г/см3 |
| Открыт: | Г. Урбеин |
| Цвет в твёрдом состоянии: | Серебристо-белый |
| Тип: | Редкоземельный |
| Орбитали: | 1s22s22p63s23p63d104s24p64d104f145s25p65d15f06s2 |
| Электронная формула: |
Co – 1s2 2s2 2p6 3s2 3p Co – [Ar] 4s2 3d7 |
| Валентность: | +2, +3, (+4) |
| Степени окисления: | 0, +II, III |
| Сверхпроводящее состояние при температуре: | 0 К |
| Потенциалы ионизации: | 13,888 В 20,957 В |
Электропроводность в тв. фазе: фазе: |
1,47*106 при 298K |
| Ковалентный радиус: | 1,56 Å |
| Атомный объем: | 17,78 см3/моль |
| Атомный радиус: | 2,25 Å |
| Теплота распада: | 18,6 Кдж/моль |
| Теплота парообразования: | 355,9 Кдж/моль |
| Кристаллическая структура: | Гексагональная. Радиус описанной вокруг основания окружности не равен высоте фигуры. Боковая сторона перпендикулярна основанию |
Реклама
Изотопы
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
полураспада (T1/2) |
Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 47Co | 27 | 20 | 47,01149 | 7/2- | |
| 48Co | 27 | 21 | 48,00176 | 6+ | |
| 49Co | 27 | 22 | 48,98972 | 35 нс | 7/2- |
| 50Co | 27 | 23 | 49,98154 | 44 мс | 6+ |
| 51Co | 27 | 24 | 50,97072 | 60 мс | 7/2- |
| 52Co | 27 | 25 | 51,96359 | 115 мс | 6+ |
| 52mCo | 380 кэВ | 104 мс | 2+ | ||
| 53Co | 27 | 26 | 52,954219 | 242 мс | 7/2- |
| 53mCo | 3,197 МэВ | 247 мс | 19/2- | ||
| 54Co | 27 | 27 | 53,9484596 | 193,28 мс | 0+ |
| 54mCo | 197,4 кэВ | 1,48 мин | 7+ | ||
| 55Co | 27 | 28 | 54,9419990 | 17,53 ч | 7/2- |
| 56Co | 27 | 29 | 55,9398393 | 77,233 сут | 4+ |
| 57Co | 27 | 30 | 56,9362914 | 271,74 сут | 7/2- |
| 58Co | 27 | 31 | 57,9357528 | 70,86 сут | 2+ |
| 58m1Co | 24,95 кэВ | 9,04 ч | 5+ | ||
| 58m2Co | 53,15 кэВ | 10,4 мкс | 4+ | ||
| 59Co | 27 | 32 | 58,9331950 | стабилен | 7/2- |
| 60Co | 27 | 33 | 59,9338171 | 5,2713 г. |
5+ |
| 60mCo | 58,59 кэВ | 10,467 мин | 2+ | ||
| 61Co | 27 | 34 | 60,9324758 | 1,650 ч | 7/2- |
| 62Co | 27 | 35 | 61,934051 | 1,50 мин | 2+ |
| 62mCo | 22 кэВ | 13,91 мин | 5+ | ||
| 63Co | 27 | 36 | 62,933612 | 26,9 с | 7/2- |
| 64Co | 27 | 37 | 63,935810 | 300 мс | 1+ |
| 65Co | 27 | 64,936478 | 1,20 с | 7/2- | |
| 66Co | 27 | 39 | 65,93976 | 180 мс | 3+ |
| 66m1Co | 175 кэВ | 1,21 мкс | 5+ | ||
| 66m2Co | 642 кэВ | 100 мкс | 8- | ||
| 67Co | 27 | 40 | 66,94089 | 425 мс | 7/2- |
| 68Co | 27 | 41 | 67,94487 | 199 мс | 7- |
| 68mCo | 150 кэВ | 1,6 с | 3+ | ||
| 69Co | 27 | 42 | 68,94632 | 227 мс | 7/2- |
| 70Co | 27 | 43 | 69,9510 | 119 мс | 6- |
| 70mCo | 200 кэВ | 500 мс | 3+ | ||
| 71Co | 27 | 44 | 70,9529 | 97 мс | 7/2- |
| 72Co | 27 | 71,95781 | 62 мс | 6- | |
| 73Co | 27 | 46 | 72,96024 | 41 мс | 7/2- |
| 74Co | 27 | 47 | 73,96538 | 50 мс | 0+ |
| 75Co | 27 | 48 | 74,96833 | 40 мс | 7/2- |
Химический элемент кобальт Co в таблице Менделеева
Кобальт — серебристо-белый, с некоторым желтоватым оттенком, металл. В таблице Менделеева кобальт обозначается символом Co.
В таблице Менделеева кобальт обозначается символом Co.
История кобальта
Искусные стекольные и гончарные мастера древности при выделке своих художественных изделий пользовались синей краской. В витринах Британского национального музея в Лондоне хранятся уникальные коллекции синих стекол, найденные археологами при раскопках памятников древней культуры в Египте и Ассиро-Вавилонии.
Ученых уже давно интересовал вопрос о природе этой любопытной синей краски, которая не утратила своих сильнокрасящих свойств в течение тысячелетий. Ряд специальных исследований, произведенных химиками, показал, что синие стекла, происходящие из Египта и Ассиро-Вавилонии, содержат соединения редкого элемента кобальта. Однако ученым так и не удалось окончательно разгадать, была ли известна древним мастерам способность окиси кобальта давать глубокое синее окрашивание, или они пользовались этим красящим материалом случайно, как и многими другими стойкими красками.
Неоднократно делались также попытки раскрыть тайну античных мастеров путем самого тщательного изучения синих стекол более позднего происхождения — александрийских, византийских и римских — в надежде найти в них присутствие кобальта. Но каково было удивление исследователей, когда они установили, что синяя краска этих стекол обусловлена наличием в них не кобальта, а меди. Не найдено было также кобальта в роскошных стеклянных и глиняных художественных изделиях, окрашенных в синий цвет, доставленных прославленным путешественником Марко Поло в Европу из стран азиатского материка.
Но каково было удивление исследователей, когда они установили, что синяя краска этих стекол обусловлена наличием в них не кобальта, а меди. Не найдено было также кобальта в роскошных стеклянных и глиняных художественных изделиях, окрашенных в синий цвет, доставленных прославленным путешественником Марко Поло в Европу из стран азиатского материка.
Ремесленники средневековья совсем не применяли кобальта для окраски в синий цвет разнообразных изделий из стекла. В то время слово кобальт было ругательным именем для различных минералов, сопровождающих серебряные руды старинных месторождений в районе Саксонско-Богемского кряжа. Ненависть горняков и плавильщиков к кобальтy историки горного дела и металлурги объясняют тем, что его присутствие в шихте значительно затрудняло и удорожало проплавку серебряных руд.
Окраска стеклянной посуды с помощью кобальтаПередовые ученые своей эпохи Агрикола, Парацельс и Василий Валентин упоминают, что «Cobold» — имя злого духа, который якобы обитает в недрах земли, расстраивает труд горняков и причиняет им всевозможные бедствия.
«Дух» ненавистного кобальта много столетий веял над рудниками Германии, и именем злого духа называли даже минералы, не содержащие кобальта, например, мышьяковистые руды, неблагоприятные свойства которых усугублялись, выделением ядовитых газов при их добыче и металлургической обработке.
Только в XVI столетии, когда добыча серебра из месторождений Саксонско-Богемского кряжа получила значительное развитие, были обнаружены сильные красящие свойства окиси кобальта. Но это новое интересное открытие около двух столетий держали в строжайшем секрете. Лишь узкий круг избранных владел секретом полезного использования красящих свойств кобальта.
Сохранились указания, что в 1533 году стекольный мастер Шюрер, проживавший в Богемии, успешно приготовлял кобальтовую синюю краску для окраски керамических изделий. Скоро голландские купцы заинтересовались новой красивой краской и с помощью Шюрера организовали ее производство у себя на родине. Первая саксонская мельница для размола кобальтовой краски была построена близ Аннаберга в 1649 году.
Теперь, когда кобальту была открыта широкая дорога в промышленность, его соединения начали быстро внедряться в качестве ценных красок для стекол, глазури, фарфора, эмалей и ряда других продуктов керамики.
Химические свойства кобальта
Но какова же природа кобальта, и не является ли он смесью некоторых «земель», к которым пионеры теоретической химии относили большинство известных им минеральных видов?
Над научной расшифровкой этой задачи много потрудился швед Брандт, который в своей диссертации (написанной в 1735 г.) «О полуметаллах» впервые сообщил, что висмут, полученный из кобальто-висмутовых руд, не чист, а содержит кобальт, который может быть отделен механическим путем. Эта первая попытка разгадать природу кобальтовых руд была подхвачена учеными в различных странах.
На рубеже XIX в. продукция соединений кобальта исчислялась уже сотнями тонн в год. В науку вошли исследования Бергмана, составившего в 1787 году довольно полное описание химических свойств кобальта, отличающих его от никеля.
Из таблицы периодической системы элементов можно узнать, что порядковое число кобальта равно 27, а его атомный вес 58,94. В этой таблице кобальт стоит между железом и никелем, что соответствует непрерывному закономерному изменению свойств элементов в периодической системе Д. И. Менделеева. Постепенно ученым удалось установить, что по своим физическим и химическим свойствам кобальт больше приближается к никелю, чем к железу.
КобальтНекоторые характерные химические свойства кобальта как бы заранее предопределили его практическое использование в технике.
Кобальт — металл, который достаточно устойчив против разрушительного действия атмосферных агентов. При обыкновенной температуре он мало поддается действию воды и воздуха. Значительно легче окисляется мелкораздробленный кобальт, но и в этом случае образующаяся на поверхности металла пленка окислов предохраняет его от дальнейшего окисления. Однако с повышением температуры этот процесс заметно активизируется. Единственной кислотой, быстро растворяющей кобальт при комнатной температуре, является азотная.
В своей автобиографии Генри Бессемер пространно рассказывает, что он переплавил не одну сотню мешков русских медных монет. Это было еще тогда, когда все помыслы молодого и инициативного Генри были сосредоточены на том, чтобы получить тончайший пылевидный материал (так называемый «китайский порошок») для позолоты различных предметов. Бессемер установил, что лучшее сырье для получения «золотой» пыли, дающей сверкающие золотистые оттенки и искристые переливы – русская медная монета. В русских копейках, привлекших внимание предприимчивого Бессемера присутствовал кобальт.
Применение кобальта
Многочисленны по составу и оттенкам технические сорта, изготовляемых в наши дни, красок из кобальта. Широким распространением пользуются красивые и очень прочные краски под названием смальта и окислы кобальта. Это незаменимый материал для окраски некоторых стекол, эмалей и изделий из керамики. Особенность синих кобальтовых стекол заключается в том, что они прозрачны для красного света. Именно на этом свойстве и основано их применение в химическом анализе в качестве световых фильтров для определения окраски пламени. Получила широкое распространение турецкая зелень, которую применяют для окраски фарфора.
Именно на этом свойстве и основано их применение в химическом анализе в качестве световых фильтров для определения окраски пламени. Получила широкое распространение турецкая зелень, которую применяют для окраски фарфора.
В малярном деле и в производстве керамике применяется небесно-голубая краска, единственная краска, обладающая хорошей кроющей способностью. Для акварельных и малярных красок в керамике применяется желтая краска, или соль Фишера. Окислы кобальта приобрели большое значение в технике эмалирования жести и в производстве лаков.
Выдающаяся роль принадлежит кобальту в новейших сверхтвердых и магнитных сплавах. Кобальтовые твердые сплавы (сюда относятся кобальтовые легированные стали) завоевали важные области применения в металлообрабатывающей промышленности. Ценные свойства обеспечивают им распространение в разных отраслях индустрии. Вот далеко не полный арсенал изделий, содержащих кобальт: фрезы, сверла, измерительные приборы, штампы, части молотов, шестеренки, зубчатки, валы, подшипники и т. д.
д.
Кобальт
- Главная
- Статьи
- Периодическая система элементов — Периодическая система химических элементов, периодическая система элементов Менделеева
- Кобальт
+++++
| Кобальт | |
|---|---|
| Атомный номер | 27 |
| Внешний вид простого вещества | |
| Свойства атома | |
(молярная масса) |
58,9332 а.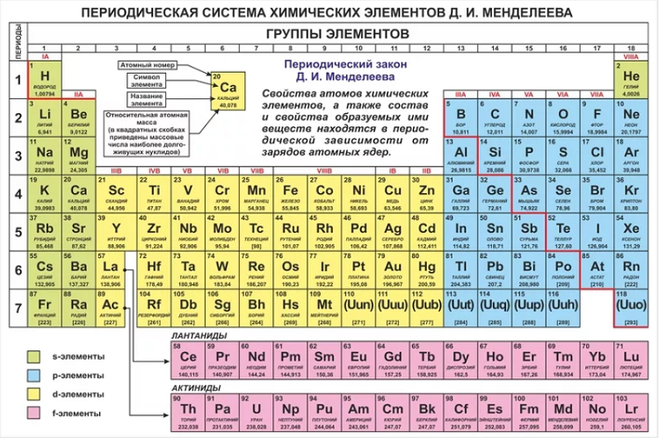 е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | 125 пм |
|
Энергия ионизации (первый электрон) |
758,1 (7,86) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 3d7 4s2 |
| Химические свойства | |
| Ковалентный радиус | 116 пм |
| Радиус иона | (+3e) 63 (+2e) 72 пм |
|
Электроотрицательность (по Полингу) |
1,88 |
| Электродный потенциал | 0 |
| Степени окисления | 3, 2, 0, -1 |
| Термодинамические свойства простого вещества | |
| Плотность | 8,9 г/см³ |
| Молярная теплоёмкость | 24,8[1]Дж/(K·моль) |
| Теплопроводность | 100 Вт/(м·K) |
| Температура плавления | 1 768 K |
| Теплота плавления | 15,48 кДж/моль |
| Температура кипения | 3143 K |
| Теплота испарения | 389,1 кДж/моль |
| Молярный объём | 6,7 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Параметры решётки | a=2,505 c=4,089 Å |
| Отношение c/a | 1,632 |
| Температура Дебая | 385 K |
| Co | 27 |
| 58,9332 | |
| [Ar]3d74s2 | |
| Кобальт | |
Кобальт — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, атомный номер 27. Обозначается символом Co (лат. Cobaltum). Простое вещество кобальт (CAS-номер: 7440-48-4) — серебристо-белый, слегка желтоватый металл с розоватым или синеватым отливом. Существует в двух кристаллических модификациях: α-Co с гексагональной плотноупакованной решёткой, β-Co с кубической гранецентрированной решёткой, температура перехода α↔β 427 °C.
И. Менделеева, атомный номер 27. Обозначается символом Co (лат. Cobaltum). Простое вещество кобальт (CAS-номер: 7440-48-4) — серебристо-белый, слегка желтоватый металл с розоватым или синеватым отливом. Существует в двух кристаллических модификациях: α-Co с гексагональной плотноупакованной решёткой, β-Co с кубической гранецентрированной решёткой, температура перехода α↔β 427 °C.
Схема атома кобальта
Название химического элемента кобальт происходит от нем. Kobold — домовой, гном. При обжиге содержащих мышьяк кобальтовых минералов выделяется летучий ядовитый оксид мышьяка. Руда, содержащая эти минералы, получила у горняков имя горного духа Кобольда. Древние норвежцы приписывали отравления плавильщиков при переплавке серебра проделкам этого злого духа. Вероятно, имя злого духа восходит к греческому «кобалос» — дым. Этим же словом греки называли лживых людей. В 1735 году шведский минералог Георг Бранд сумел выделить из этого минерала неизвестный ранее металл, который и назвал кобальтом. Он выяснил также, что соединения именно этого элемента окрашивают стекло в синий цвет — этим свойством пользовались ещё в древних Ассирии и Вавилоне.
Он выяснил также, что соединения именно этого элемента окрашивают стекло в синий цвет — этим свойством пользовались ещё в древних Ассирии и Вавилоне.
Нахождение в природе
Массовая доля кобальта в земной коре 4·10−3%. Кобальт входит в состав минералов: каролит CuCo2S4, линнеит Co3S4, кобальтин CoAsS, сферокобальтит CoCO3, смальтит CoAs2 и других. Всего известно около 30 кобальтосодержащих минералов. Кобальту сопутствуют железо, никель, марганец и медь. Содержание в морской воде приблизительно (1,7)·10−10%.
Получение
Кобальт получают в основном из никелевых руд, обрабатывая их растворами серной кислоты или аммиака. Также используется методы пирометаллургии. Для отделения от близкого по свойствам никеля используется хлор, хлорат кобальта (Co(ClO3)2) выпадает в осадок, а соединения никеля остаются в растворе.
Кобальт имеет только один стабильный изотоп — 59Co (изотопная распространённость 100[2] %). Известны еще 22 радиоактивных изотопа кобальта.
Известны еще 22 радиоактивных изотопа кобальта.
Физические свойства
Кобальт — твердый металл, существующий в двух модификациях. При температурах от комнатной до 427 °C устойчива α-модификация. При температурах от 427 °C до температуры плавления (1494 °C) устойчива β-модификация кобальта (решетка кубическая гранецентрированная). Кобальт — ферромагнетик, точка Кюри 1121 °C.
Желтоватый оттенок ему придает тонкий слой оксидов.
Химические свойства
Оксиды
- На воздухе кобальт окисляется при температуре выше 300 °C.
- Устойчивый при комнатной температуре оксид кобальта состоит из смеси оксидов CoO и Co2O3, поэтому в справочниках можно встретить брутто формулу Co3O4.
- При высоких температурах можно получить α-форму или β-форму оксида CoO
-
Все оксиды кобальта восстанавливаются водородом. Со3О4 + 4Н2 → 3Со + 4Н2О.
- Оксид кобальта (II) можно получить, прокаливая соединения кобальта (II), например: 2Со(ОН)2 + O2 → Co2O3 + Н2O.
Другие соединения
- При нагревании, кобальт реагирует с галогенами, причём соединения кобальта (III) образуются только с фтором. Co + 3F → CoF3, но, Co + 2Cl → CoCl2
- С серой кобальт образует 2 различных модификации CoS. Серебристо-серую α-форму (при сплавлении порошков) и черную β-форму (выпадает в осадок из растворов).
- При нагревании CoS в атмосфере сероводорода получается сложный сульфид Со9S8
- С другими окисляющими элементами, такими как углерод, фосфор, азот, селен, кремний, бор. кобальт тоже образует сложные соединения, являющиеся смесями где присутствует кобальт со степенями окисления 1, 2, 3.
-
Кобальт способен растворять водород, не образуя химических соединений.
 Косвенным путем синтезированы два стехиометрических гидрида кобальта СоН2 и СоН.
Косвенным путем синтезированы два стехиометрических гидрида кобальта СоН2 и СоН. - Растворы солей кобальта CoSO4, CoCl2, Со(NO3)2 придают воде бледно-розовую окраску. Растворы солей кобальта в спиртах темно-синие. Многие соли кобальта нерастворимы.
- Кобальт создаёт комплексные соединения. Чаще всего на основе аммиака.
Наиболее устойчивыми комплексами являются лутеосоли [Co(NH3)6]3+ желтого цвета и розеосоли [Co(NH3)5H2O]3+ красного или розового цвета.
- Также кобальт создаёт комплексы на основе CN−, NO2− и многих других.
- Хлорид кобальта
- Ионные комплексы кобальта
Применение
-
Легирование кобальтом стали повышает её жаропрочность, улучшает механические свойства.
 Из сплавов с применением кобальта создают обрабатывающий инструмент: свёрла, резцы, и.т.п.
Из сплавов с применением кобальта создают обрабатывающий инструмент: свёрла, резцы, и.т.п. - Магнитные свойства сплавов кобальта находят применение в аппаратуре магнитной записи, а также сердечниках электромоторов и трансформаторов.
- Для изготовления постоянных магнитов иногда применяется сплав, содержащий около 50 % кобальта, а также ванадий или хром.
- Кобальт применяется как катализатор химических реакций.
- Кобальтат лития применяется в качестве высокоэффективного положительного электрода для производства литиевых аккумуляторов.
- Силицид кобальта отличный термоэлектрический материал и позволяет производить термоэлектрогенераторы с высоким КПД.
- Радиоактивный кобальт-60 (период полураспада 5,271 года) применяется в гамма-дефектоскопии и медицине.
- 60Со используется в качестве топлива в радиоизотопных источниках энергии.
Биологическая роль
Кобальт, один из микроэлементов, жизненно важных организму. Он входит в состав витамина В12 (кобаламин). Кобальт задействован при кроветворении, функциях нервной системы и печени, ферментативных реакциях. Потребность человека в кобальте 0,007-0,015 мг, ежедневно. В теле человека содержится 0,2 мг кобальта на каждый килограмм массы человека. При отсутствии кобальта развивается акобальтоз.
Он входит в состав витамина В12 (кобаламин). Кобальт задействован при кроветворении, функциях нервной системы и печени, ферментативных реакциях. Потребность человека в кобальте 0,007-0,015 мг, ежедневно. В теле человека содержится 0,2 мг кобальта на каждый килограмм массы человека. При отсутствии кобальта развивается акобальтоз.
Токсикология
Избыток кобальта для человека вреден.
ПДК пыли кобальта в воздухе 0,5 мг/м³, в питьевой воде допустимое содержание солей кобальта 0,01 мг/л.
Токсическая доза (LD50 для крыс) — 50 мг. Особенно токсичны пары октакарбонила кобальта Со2(СО)8.
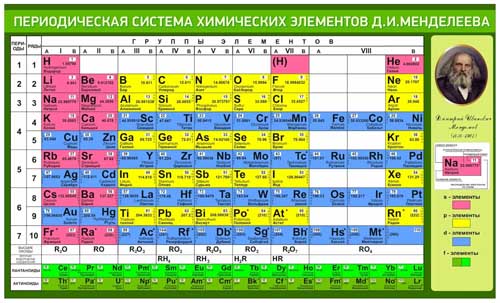
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
| IA | IIA | IIIB | IVB | VB | VIB | VIIB | —- | VIIIB | —- | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |
| Период | ||||||||||||||||||
| 1 |
1 H Водород |
2 He Гелий |
||||||||||||||||
| 2 |
3 Li Литий |
4 Be Бериллий |
5 B Бор |
6 C Углерод |
7 N Азот |
8 O Кислород |
9 F Фтор |
10 Ne Неон |
||||||||||
| 3 |
11 Na Натрий |
12 Mg Магний |
13 Al Алюминий |
14 Si Кремний |
15 P Фосфор |
16 S Сера |
17 Cl Хлор |
18 Ar Аргон |
||||||||||
| 4 |
19 K Калий |
20 Ca Кальций |
21 Sc Скандий |
22 Ti Титан |
23 V Ванадий |
24 Cr Хром |
25 Mn Марганец |
26 Fe Железо |
27 Co Кобальт |
28 Ni Никель |
29 Cu Медь |
30 Zn Цинк |
31 Ga Галлий |
32 Ge Германий |
33 As Мышьяк |
34 Se Селен |
35 Br Бром |
36 Kr Криптон |
| 5 |
37 Rb Рубидий |
38 Sr Стронций |
39 Y Иттрий |
40 Zr Цирконий |
41 Nb Ниобий |
42 Mo Молибден |
(43) Tc Технеций |
44 Ru Рутений |
45 Rh Родий |
46 Pd Палладий |
47 Ag Серебро |
48 Cd Кадмий |
49 In Индий |
50 Sn Олово |
51 Sb Сурьма |
52 Te Теллур |
53 I Иод |
54 Xe Ксенон |
| 6 |
55 Cs Цезий |
56 Ba Барий |
* |
72 Hf Гафний |
73 Ta Тантал |
74 W Вольфрам |
75 Re Рений |
76 Os Осмий |
77 Ir Иридий |
78 Pt Платина |
79 Au Золото |
80 Hg Ртуть |
81 Tl Таллий |
82 Pb Свинец |
83 Bi Висмут |
(84) Po Полоний |
(85) At Астат |
86 Rn Радон |
| 7 |
87 Fr Франций |
88 Ra Радий |
** |
(104) Rf Резерфордий |
(105) Db Дубний |
(106) Sg Сиборгий |
(107) Bh Борий |
(108) Hs Хассий |
(109) Mt Мейтнерий |
(110) Ds Дармштадтий |
(111) Rg Рентгений |
(112) Cp Коперниций |
(113) Uut Унунтрий |
(114) Uuq Унунквадий |
(115) Uup Унунпентий |
(116) Uuh Унунгексий |
(117) Uus Унунсептий |
(118) Uuo Унуноктий |
| 8 |
(119) Uue Унуненний |
(120) Ubn Унбинилий |
||||||||||||||||
| Лантаноиды * |
57 La Лантан |
58 Ce Церий |
59 Pr Празеодим |
60 Nd Неодим |
(61) Pm Прометий |
62 Sm Самарий |
63 Eu Европий |
64 Gd Гадолиний |
65 Tb Тербий |
66 Dy Диспрозий |
67 Ho Гольмй |
68 Er Эрбий |
69 Tm Тулий |
70 Yb Иттербий |
71 Lu Лютеций |
|||
| Актиноиды ** |
89 Ac Актиний |
90 Th Торий |
91 Pa Протактиний |
92 U Уран |
(93) Np Нептуний |
(94) Pu Плутоний |
(95) Am Америций |
(96) Cm Кюрий |
(97) Bk Берклий |
(98) Cf Калифорний |
(99) Es Эйнштейний |
(100) Fm Фермий |
(101) Md Менделевий |
(102) No Нобелей |
(103) Lr Лоуренсий |
|||
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
кобальт | Использование, свойства и факты
кобальт
Посмотреть все СМИ
- Ключевые люди:
- Георг Брандт
- Похожие темы:
- химический элемент переходный металл обработка кобальта витамин В12 кобальт-60
Просмотреть весь соответствующий контент →
Резюме
Прочтите краткий обзор этой темы
кобальт (Co) , химический элемент, ферромагнитный металл группы 9 (VIIIb) периодической таблицы, используемый в основном для жаропрочных и магнитных сплавов.
Металл был выделен (ок. 1735 г.) шведским химиком Георгом Брандтом, хотя соединения кобальта веками использовались для придания синего цвета глазури и керамике. Кобальт был обнаружен в египетских статуэтках и персидских бусинах для ожерелий 3-го тысячелетия до н.07 г. н.э.), а затем и в голубом фарфоре династии Мин (1368–1644). Название кобольд было впервые применено (16 век) к рудам, которые, как считалось, содержали медь, но в конечном итоге оказалось, что это ядовитые кобальтовые руды, содержащие мышьяк. В конце концов Брандт определил (1742 г.), что синий цвет этих руд обусловлен присутствием кобальта.
Britannica Викторина
118 Названий и символов периодической таблицы Викторина
Периодическая таблица состоит из 118 элементов. Насколько хорошо вы знаете их символы? В этом тесте вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них.
| atomic number | 27 |
|---|---|
| atomic weight | 58. 933194 933194 |
| melting point | 1,495 °C (2,723 °F) |
| boiling point | 2,870 °C (5,198 °F) |
| density | 8.9 gram/cm 3 at 20 °C (68 °F) |
| oxidation states | +2, +3 |
| electron configuration | [AR] 3 D 7 4 S 2 |
ВКЛЮЧЕНИЕ, Свойства и использование Земли
КОЛОДА, хотя широко рассеянный, придает только 0,001 процента. Он содержится в небольших количествах в земном и метеоритном самородном никелевом железе, на Солнце и в атмосферах звезд, а в сочетании с другими элементами в природных водах, в железомарганцевых корках на глубинах океанов, в почвах, в растениях и животных, в минералы, такие как кобальтит, линнеит, скуттерудит, смальтит, гетерогенит и эритрит. У животных кобальт является микроэлементом, необходимым для питания жвачных животных (крупный рогатый скот, овцы) и для созревания эритроцитов человека в форме витамина В 12 , единственный известный витамин, содержащий такой тяжелый элемент.
За некоторыми исключениями, кобальтовая руда обычно не добывается из-за содержания кобальта. Скорее, его часто извлекают как побочный продукт добычи руд железа, никеля, меди, серебра, марганца, цинка и мышьяка, которые содержат следы кобальта. Для концентрирования и извлечения кобальта из этих руд требуется сложная переработка. Ко второму десятилетию 21 века Демократическая Республика Конго (ДРК), Китай, Канада и Россия были ведущими мировыми производителями добываемого кобальта. Однако крупнейшим производителем рафинированного кобальта был Китай, который импортировал огромные дополнительные объемы полезных ископаемых кобальта из ДРК. (Дополнительную информацию о добыче, переработке и извлечении кобальта см. в см. обработка кобальта.)
Полированный кобальт серебристо-белого цвета со слабым голубоватым оттенком. Известны два аллотропа: гексагональная плотноупакованная структура, стабильная ниже 417 ° C (783 ° F), и гранецентрированная кубическая, стабильная при высоких температурах. Он является ферромагнитным при температуре до 1121 ° C (2050 ° F, самая высокая известная точка Кюри для любого металла или сплава) и может найти применение там, где необходимы магнитные свойства при повышенных температурах.
Он является ферромагнитным при температуре до 1121 ° C (2050 ° F, самая высокая известная точка Кюри для любого металла или сплава) и может найти применение там, где необходимы магнитные свойства при повышенных температурах.
Кобальт — один из трех металлов, обладающих ферромагнитными свойствами при комнатной температуре. Он медленно растворяется в разбавленных минеральных кислотах, не соединяется непосредственно ни с водородом, ни с азотом, но при нагревании соединяется с углеродом, фосфором или серой. Кобальт также подвергается воздействию кислорода и водяного пара при повышенных температурах, в результате чего образуется оксид кобальта CoO (с металлом в состоянии +2).
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Природный кобальт полностью состоит из стабильного изотопа кобальта-59, из которого методом нейтронного облучения в ядерном реакторе производится самый долгоживущий искусственный радиоактивный изотоп кобальт-60 (период полураспада 5,3 года). Гамма-излучение кобальта-60 использовалось вместо рентгеновского или альфа-излучения радия при проверке промышленных материалов для выявления внутренней структуры, дефектов или посторонних предметов. Он также использовался в терапии рака, в исследованиях по стерилизации, а также в биологии и промышленности в качестве радиоактивного индикатора.
Гамма-излучение кобальта-60 использовалось вместо рентгеновского или альфа-излучения радия при проверке промышленных материалов для выявления внутренней структуры, дефектов или посторонних предметов. Он также использовался в терапии рака, в исследованиях по стерилизации, а также в биологии и промышленности в качестве радиоактивного индикатора.
Большая часть производимого кобальта используется для специальных сплавов. Относительно большой процент мирового производства приходится на магнитные сплавы, такие как Alnicos для постоянных магнитов. Значительные количества используются для сплавов, которые сохраняют свои свойства при высоких температурах, и суперсплавов, которые используются вблизи их точек плавления (где стали стали бы слишком мягкими). Кобальт также используется для твердосплавных сплавов, инструментальных сталей, сплавов с низким коэффициентом расширения (для уплотнений стекло-металл) и сплавов с постоянным модулем (упругих) (для прецизионных пружин). Кобальт является наиболее подходящей матрицей для цементированных карбидов.
Мелкодисперсный кобальт самовозгорается. Более крупные куски относительно инертны на воздухе, но при температуре выше 300 ° C (570 ° F) происходит интенсивное окисление.
В своих соединениях кобальт почти всегда проявляет степень окисления +2 или +3, хотя известны состояния +4, +1, 0 и -1. Соединения, в которых кобальт проявляет степень окисления +2 (Co 2+ , ион устойчив в воде), называются кобальтовыми, а в которых кобальт проявляет степень окисления +3 (Co 3+ ) называются кобальтовыми.
Как Co 2+ , так и Co 3+ образуют многочисленные координационные соединения или комплексы. Co 3+ образует больше известных комплексных ионов, чем любой другой металл, кроме платины. Координационное число комплексов обычно равно шести.
Кобальт образует с кислородом два четко определенных бинарных соединения: оксид кобальта, CoO, и текстроксид трикобальта, или оксид кобальта-кобальта, Co 3 O 4 . Последний содержит кобальт как в +2, так и в +3 степени окисления и составляет до 40% товарного оксида кобальта, используемого в производстве керамики, стекла и эмали, а также в приготовлении катализаторов и порошка металлического кобальта.
Последний содержит кобальт как в +2, так и в +3 степени окисления и составляет до 40% товарного оксида кобальта, используемого в производстве керамики, стекла и эмали, а также в приготовлении катализаторов и порошка металлического кобальта.
Одной из наиболее важных солей кобальта является сульфат CoSO 4 , который используется в гальванике, при приготовлении осушающих средств и для подкормки пастбищ в сельском хозяйстве. Другие соли кобальта находят широкое применение в производстве катализаторов, осушителей, порошков металлического кобальта и других солей. Хлорид кобальта (CoCl 2 ∙ 6H 2 O в коммерческой форме), твердое вещество розового цвета, которое при обезвоживании становится синим, используется при приготовлении катализатора и в качестве индикатора влажности. Фосфат кобальта, Co 3 (PO 4 ) 2 ∙8H 2 O, используется для росписи фарфора и окрашивания стекла.
Эта статья была недавно отредактирована и обновлена Эриком Грегерсеном.
Кобальт Информация об элементе: факты, свойства, тенденции, использование и сравнение – Периодическая таблица элементов
Кристаллическая структура кобальта
Твердотельная структура кобальта Простая гексагональная .
Кристаллическая структура может быть описана с точки зрения ее элементарной ячейки. Единичные Клетки повторяются в трехмерном пространстве, образуя структуру.
Параметры элементарной ячейки
Элементарная ячейка представлена параметрами решетки, которые являются длинами ребер ячейки Постоянные решетки (a, b и c)
| a | b | c |
|---|---|---|
| 250,71 пм | 250,71 пм | 406,95 пм |
и углы между ними Углы решетки (альфа, бета и гамма).
| альфа | бета | Gamma |
|---|---|---|
| π/2 | π/2 | 2 π/3 |
Положения атомов внутри единичной клетки описаны по набору атт -позиций (x 9002.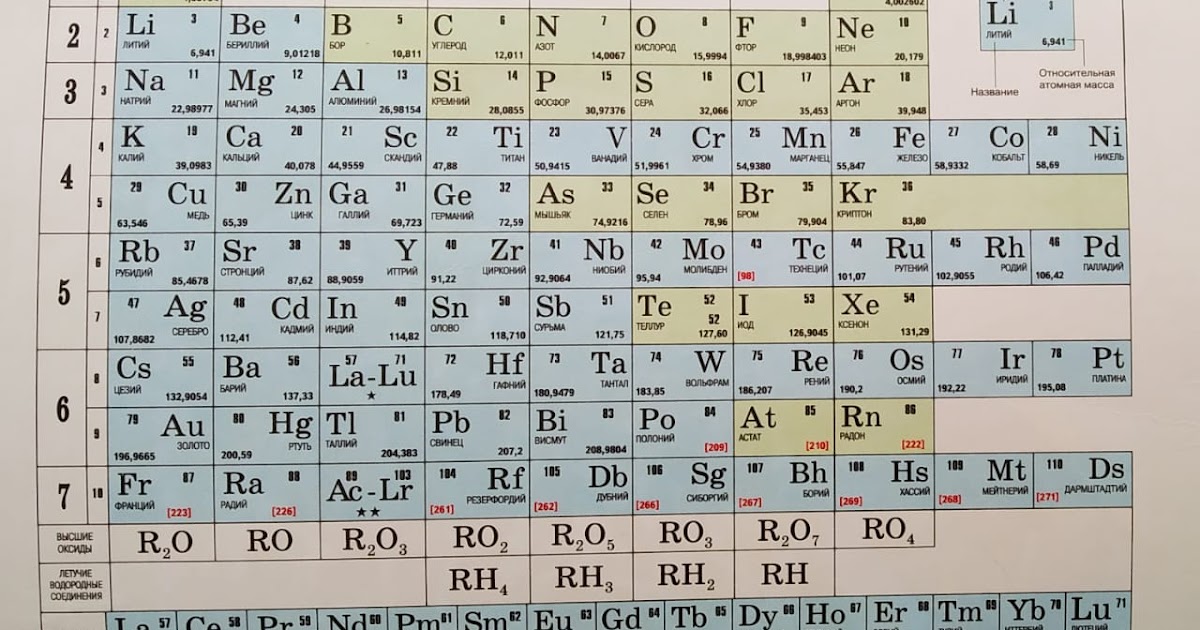 , y i , z i ), измеренные от опорной точки решетки.
, y i , z i ), измеренные от опорной точки решетки.
Свойства симметрии кристалла описываются концепцией пространственных групп. Все возможные симметричные расположения частиц в трехмерном пространстве описываются 230 пространственными группами (219различные типы или 230, если хиральные копии считаются различными.
| Space Group Name | P63/mmc | |
| Oxidation States | Space Group Number | 194 |
| Crystal Structure | Simple Hexagonal |
Cobalt Atomic and Orbital Properties
Атомы кобальта имеют 27 электронов и структуру электронной оболочки [2, 8, 15, 2] с символом атомного термина (квантовые числа) 4 F 9/2 .
| Atomic Number | 27 |
| Number of Electrons (with no charge) | 27 |
| Number of Protons | 27 |
| Mass Number | 59 |
| Number нейтронов | 32 |
| Структура оболочки (электронов на энергетический уровень) | 2, 8, 15, 2 |
| Электронная конфигурация | [Ar] 3d7 4s2 |
| Valence Electrons | 3d7 4s2 |
| Valence (Valency) | 4 |
| Main Oxidation States | 2, 3 |
| Oxidation States | -3 , -1, 0, 1, 2, 3, 4, 5 |
| Atomic Term Symbol (Quantum Numbers) | 4 F 9/2 |
Bohr Atomic Model of Cobalt – Электронов на энергетический уровень
Электронная конфигурация основного состояния кобальта – нейтральный атом кобальта
Сокращенная электронная конфигурация кобальта
Сокращенная электронная конфигурация основного состояния нейтрального атома кобальта [Ar] 3d7 4s2. Часть конфигурации кобальта, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 3d7 4s2, электроны в самой внешней оболочке, определяют химические свойства элемента.
Часть конфигурации кобальта, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 3d7 4s2, электроны в самой внешней оболочке, определяют химические свойства элемента.
Полная электронная конфигурация нейтрального кобальта
Полная электронная конфигурация основного состояния атома кобальта, Полная электронная конфигурация
1s2 2s2 2p6 3s2 3p6 3d7 4s2
Электроны заполняют атомные орбитали в порядке, определяемом принципом Ауфбау, Принцип запрета Паули и правило Хунда.
 …
…Атомная структура кобальта
Атомный радиус кобальта составляет 152 пм, а его ковалентный радиус равен 126 пм.
| Вычисленный атомный радиус | 152 пм (1,52 Å) |
| Атомный радиус Эмпирический | 135 вечера (1,35 Å) |
| 6,62 CM3/Мол | |
| . 6,62 CM3/Мол | |
| .6.62 CM3/MOL | |
| COVLENT 6.62/Мол | |
| COVLENT 6.62/Мол | |
| COVLENT. Waals Radius | – |
| Нейтронный сечение | 37,2 |
| Абсорбция массы нейтроны | 0,021 |
Atomic Spectrum
Atomic Spectrum из кобола
Atomic Spectrum
Atomic Spect.
 0169
0169Химические свойства кобальта: Энергия ионизации кобальта и сродство к электрону
Сродство кобальта к электрону составляет 63,7 кДж/моль.
| Valence | 4 |
| Electronegativity | 1.88 |
| ElectronAffinity | 63.7 kJ/mol |
Ionization Energy of Cobalt
Refer to table below for Ionization energies of Cobalt
| Ionization energy number | Enthalpy – kJ/mol | ||||
|---|---|---|---|---|---|
| 1st | 760.4 | ||||
| 2nd | 1648 | ||||
| 3rd | 3232 | ||||
| 4th | 4950 | ||||
| 5th | 7670 | ||||
| 6th | 9840 | ||||
| 7th | 12440 | ||||
| 8th | 15230 | ||||
| 9th | 17959 | ||||
| 10th | 26570 | ||||
| 11th | 29400 | ||||
| 12th | 32400 | ||||
| 13th | 36600 | ||||
| 14th | 39700 | ||||
| 15th | 42800 | ||||
| 16th | 49396 | ||||
| 17th | 52737 | ||||
| 18th | 1348797 | ||||
| 18th | 1111097 | . 0043 0043 | 19th | 145170 | |
| 20th | 154700 | ||||
| 21st | 167400 | ||||
| 22nd | 178100 | ||||
| 23rd | 189300 | ||||
| 24th | 204500 | ||||
| 25 -й | 214100 | ||||
| 26th | 920870 | ||||
| 27th | 966023 |
Физические свойства
.0099
Refer to below table for Cobalt Physical Properties
| Density | 8.9 g/cm3(when liquid at m.p density is $7.75 g/cm3) |
| Molar Volume | 6.62 cm3/mol |
Elastic Properties
| Young Modulus | 209 |
| Shear Modulus | 75 GPa |
| Bulk Modulus | 180 GPa |
| Poisson Ratio | 0. 31 31 |
Hardness of Cobalt – Tests to Measure of Hardness of Element
| Mohs Hardness | 5 MPa |
| Vickers Hardness | 1043 MPa |
| Brinell Hardness | 700 МПа |
Кобальт Электрические свойства
Кобальт является проводником электричества. Обратитесь к таблице ниже для получения информации об электрических свойствах кобальта 9.0003
| Electrical Conductivity | 17000000 S/m |
| Resistivity | 6e-8 m Ω |
| Superconducting Point | – |
Cobalt Heat and Conduction Properties
| Thermal Проводимость | 100 Вт/(м·К) |
| Тепловое расширение | 0,000013 /K |
Магнитные свойства кобальта
| Magnetic Type | Ferromagnetic |
| Curie Point | 1394 K |
| Mass Magnetic Susceptibility | – |
| Molar Magnetic Susceptibility | – |
| Volume Magnetic Susceptibility | – |
Оптические свойства кобальта
| Показатель преломления | – |
Акустические свойства Cobalt
| Скорость звука | 4720 м/с |
Кобальтовые термические свойства – энтелпий и термодики
Спрание таблицы ниже для термических.
Enthalpies of Cobalt
| Heat of Fusion | 16.2 kJ/mol |
| Heat of Vaporization | 375 kJ/mol |
| Heat of Горение | – |
Изотопы кобальта. Ядерные свойства кобальта
Кобальт состоит из 29 изотопов, содержащих от 47 до 75 нуклонов. Кобальт имеет 1 стабильный природный изотоп.
Изотопы кобальта – Встречающиеся в природе стабильные изотопы: 59Co.
| Isotope | Z | N | Isotope Mass | % Abundance | T half | Decay Mode |
|---|---|---|---|---|---|---|
| 47Co | 27 | 20 | 47 | Synthetic | ||
| 48Co | 27 | 21 | 48 | Синтетика | ||
| 49Co | 27 | 22 | 49 | Synthetic | ||
| 50Co | 27 | 23 | 50 | Synthetic | ||
| 51Co | 27 | 24 | 51 | Synthetic | ||
| 52Co | 27 | 25 | 52 | Synthetic | ||
| 53Co | 27 | 26 | 53 | Synthetic | ||
| 54Co | 27 | 27 | 54 | Synthetic | ||
| 55Co | 27 | 28 | 55 | Synthetic | ||
| 56Co | 27 | 29 | 56 | Synthetic | ||
| 57Co | 27 | 30 | 57 | Synthetic | ||
| 58Co | 27 | 31 | 58 | Synthetic | ||
| 59Co | 27 | 32 | 59 | 100% | Stable | |
| 60Co | 27 | 33 | 60 | Synthetic | ||
| 61Co | 27 | 34 | 61 | Synthetic | ||
| 62Co | 27 | 35 | 62 | Synthetic | ||
| 63Co | 27 | 36 | 63 | Synthetic | ||
| 64Co | 27 | 37 | 64 | Synthetic | ||
| 65Co | 27 | 38 | 65 | Synthetic | ||
| 66Co | 27 | 39 | 66 | Synthetic | ||
| 67Co | 27 | 40 | 67 | Synthetic | ||
| 68Co | 27 | 41 | 68 | Synthetic | ||
| 69Co | 27 | 42 | 69 | Synthetic | ||
| 70Co | 27 | 43 | 70 | Synthetic | ||
| 71Co | 27 | 44 | 71 | Synthetic | ||
| 72Co | 27 | 45 | 72 | Synthetic | ||
| 73Co | 27 | 46 | 73 | Synthetic | ||
| 74Co | 27 | 47 | 74 | Synthetic | ||
| 75Co | 27 | 48 | 75 | Synthetic |
Cobalt Facts – Atomic Number 27 or Co
This entry was posted on by Anne Гельменстин (обновлено )
Чистый элементарный кобальт. (Alchemist-hp)
Кобальт — атомный номер 27 в периодической таблице и символ элемента Co. Этот твердый серо-голубой переходный металл используется в сплавах и придает стеклу синий цвет. Вот факты о кобальте, включая его свойства, использование и воздействие на здоровье.
Факты о кобальте
Кобальт — это атомный номер 27 с символом элемента Co в периодической таблице.
Открытие : Соединения кобальта использовались с бронзового века для придания синего цвета стеклу. Шведский химик Георг Брандт открыл этот элемент около 1735 года.
Название : Название элемента кобальт происходит от немецкого слова кобольд , что означает «гоблин». Горняки называли кобальтовую руду кобольдом, имея в виду токсичные пары, выделяемые во время плавки, и то, как кобальтовая руда мешала процессу выплавки никеля или меди. Кобальтовая руда обычно содержит оксид мышьяка, отравляющий шахтеров и плавильщиков.
Кобальтовая руда обычно содержит оксид мышьяка, отравляющий шахтеров и плавильщиков.
Свойства : Кобальт – твердый, хрупкий переходный металл, напоминающий железо или никель. Его наиболее распространенные степени окисления +2 или +3. Элемент является магнитным, с магнитной проницаемостью примерно в две трети от магнитной проницаемости железа. Металл образует две аллотропы. При 400°C преобладает бета-форма. Альфа-форма чаще встречается при температуре выше 400°C. Температура плавления кобальта 1495°С, температура кипения 2870°С. Его удельный вес составляет 8,9 при 20°C.
Кобальтовое стекло используется из-за его цвета и для защиты светочувствительных жидкостей. (Юрий)
Использование : Синий цвет стекла и глазури, которые использовались в Древнем Египте, Помпеях, династии Тан и династии Мин, произошли от использования соединений кобальта. Сегодня синий кобальт остается популярным красителем для стекла и красок.
Кобальт добавляется в сплавы для повышения твердости и коррозионной стойкости. Он также используется для изготовления магнитов. Изотоп кобальт-60 используется в качестве индикатора, источника гамма-излучения и радиотерапевтического агента. Он также используется для стерилизации продуктов питания.
Изотопы : Единственный стабильный изотоп — кобальт-59. Известно двадцать шесть изотопов, от Co-50 до Co-75. Кобальт-60 является важным радиоизотопом для исследовательских, коммерческих и медицинских целей. Его период полураспада составляет 5,27 года. Кобальт также используется для изготовления «грязной» бомбы, известной как кобальтовая бомба.
Биологическая роль : Кобальт является важным микроэлементом для питания человека, животных и растений. Он является частью молекулы витамина B-12. Однако, как и железо, чрезмерное воздействие кобальта может вызвать потенциально смертельные заболевания. Подобно никелю и хрому, кобальт вызывает контактный дерматит при попадании на кожу. При вдыхании вызывает дыхательную недостаточность. Является естественным компонентом табачного дыма. В 1966, соединения кобальта, используемые для стабилизации пивной пены, вызывали состояние, известное как «кардиомиопатия любителей пива». LD 50 для солей кобальта колеблется от 150 мг/кг до 500 кг/мг.
При вдыхании вызывает дыхательную недостаточность. Является естественным компонентом табачного дыма. В 1966, соединения кобальта, используемые для стабилизации пивной пены, вызывали состояние, известное как «кардиомиопатия любителей пива». LD 50 для солей кобальта колеблется от 150 мг/кг до 500 кг/мг.
Источники : Кобальт образуется в сверхновых посредством r-процесса. Элемент существует во многих соединениях, но не в чистом (нативном) виде. Источники кобальта включают минералы смальтит, эритрит и кобальтит. Кобальт встречается с никелевыми, медными, серебряными, железными и свинцовыми рудами. Этот элемент также содержится во многих метеоритах.
Атомные данные кобальта
Электронная конфигурация атома кобальта.
Вот периодическая дата таблицы для кобальта, как это принято IUPAC:
- Символ элемента : CO
- Атомный номер : 27
- .
 : Кобальт — блестящий, твердый металл серо-голубого цвета.
: Кобальт — блестящий, твердый металл серо-голубого цвета. - Группа : Группа 9 (Переходные металлы)
- Период : Период 4
- Блок : элемент D-блока
- Электронная конфигурация : [AR] 3D 7 4S 2
- Pope at STP : SOLID 962629292929292929292929292929292929291 29002 2TINGIT C, 2723 ° F)
- Точка кипячения : 3200 K (2927 ° C, 5301 ° F)
- Плотность : 8,90 г/см 3
- . −1, +1, +2 , +3 , +4, +5
- Электроотрицательность : 1,88 (шкала Полинга)
- Энергии ионизации : 1-й: 760,4 кДж/моль; 2-й: 1648 кДж/моль; 3-й: 3232 кДж/моль
- Атомный радиус : 125 вечера (эмпирические данные)
- Кристаллическая структура : Hexagonal Close Packed (HCP)
- Discovery : Georg).

