Таблица Менделеева. Такая разная. : moris_levran — LiveJournal
1 марта 1869 года Менделеев закончил свою работу “Опыт системы элементов, основанной на их атомном весе и химическом сходстве”. Этот день считается днём открытия периодического закона элементов Д.М. Менделеева. “Открытие Д.И. Менделеева относится к фундаментальным законам мироздания, таким как закон всемирного тяготения Ньютона или теория относительности Эйнштейна, а Д.М. Менделеев стоит в одном ряду с именами этих великих физиков”. Академик А.И. Русанов.“Периодическая система как была, так и осталась в самых новейших решениях проблемы о веществе главной путеводной звездой”. Проф. А. Н. Реформатский.
“Когда подходишь к оценке личностей, подобных Д. И. Менделееву, к анализу их научного творчества, невольно является желание отыскать в этом творчестве элементы, всего более отмеченные печатью гения. Из всех признаков, отличающих гениальность и ее проявление, два, кажется, являются наиболее показательными: это, во-первых, способность охватывать и объединять широкие области знания и, во-вторых, способность к резким скачкам мысли, к неожиданному сближению фактов и понятий, которые для обыкновенного смертного кажутся далеко стоящими друг от друга и ничем не связанными, по крайнем мере до того момента, когда такая связь будет обнаружена и доказана”. Л. А. Чугаев, профессор химии.
Л. А. Чугаев, профессор химии.
Да и сам Менделеев понимал огромное значение открытого им закона для науки. И верил в его дальнейшее развитие. “По видимому, периодическому закону будущее не грозит разрушением, а только надстройки и развитие обещает”. Д.И. Менделеев.
Первоначальный вид таблицы, написанный рукой Д.И. Менделеева.
Если бы все научные знания мира пропали бы, из-за какого либо катаклизма, то для возрождения цивилизации одним из главных законов стал бы периодический закон Д.И. Менделеева. Успехи атомной физики, включая ядерную энергетику и синтез искусственных элементов, стали возможными лишь благодаря Периодическому закону. В свою очередь, они расширили и углубили сущность закона Менделеева.
Периодический закон сыграл огромную роль в развитии химии и других естественных наук. Была открыта взаимная связь между всеми элементами, их физическими и химическими свойствами. Это поставило перед естествознанием научно-философскую проблемы огромной важности: эта взаимная связь должно получить объяснение.![]()
Открытию периодического закона предшествовало 15 лет напряженной работы. Ко времени открытия периодического закона было известно 63 химических элемента, существовало около 50 различных классификаций. Большинство ученых сравнивали между собой только сходные по свойствам элементы, поэтому не смогли открыть закон. Менделеев же сравнивал между собой все, в том числе и несходные элементы. Менделеев выписал на карточки все известные сведения об открытых и изученных в то время химических элементах и их соединениях, расположил их в порядке возрастания их относительных атомных масс и всесторонне проанализировал всю эту совокупность, пытаясь найти в ней определенные закономерности. В результате напряженного творческого труда он обнаружил в этой цепочке отрезки, в которых свойства химических элементов и образованных ими веществ изменялись сходным образом – периодически – периоды. С развитием учения о строении электронной оболочки атомов стало ясно, почему свойства атомов показывают периодичность с возрастанием атомной массы. Атомы с одинаковой внешней сферой составляют одну группу. Атомы с одинаковым числом внешних сфер — составляют один ряд. Атомы с ядрами, имеющими одинаковые заряды, но разные массы, обладают одинаковыми химическими свойствами, но разными атомными весами и представляют собой изотопы одного и того же химического элемента. По существу свойства атомов отражают свойства внешних электронных оболочек, которые тесно связанны с законами квантовой физики.
Атомы с одинаковой внешней сферой составляют одну группу. Атомы с одинаковым числом внешних сфер — составляют один ряд. Атомы с ядрами, имеющими одинаковые заряды, но разные массы, обладают одинаковыми химическими свойствами, но разными атомными весами и представляют собой изотопы одного и того же химического элемента. По существу свойства атомов отражают свойства внешних электронных оболочек, которые тесно связанны с законами квантовой физики.
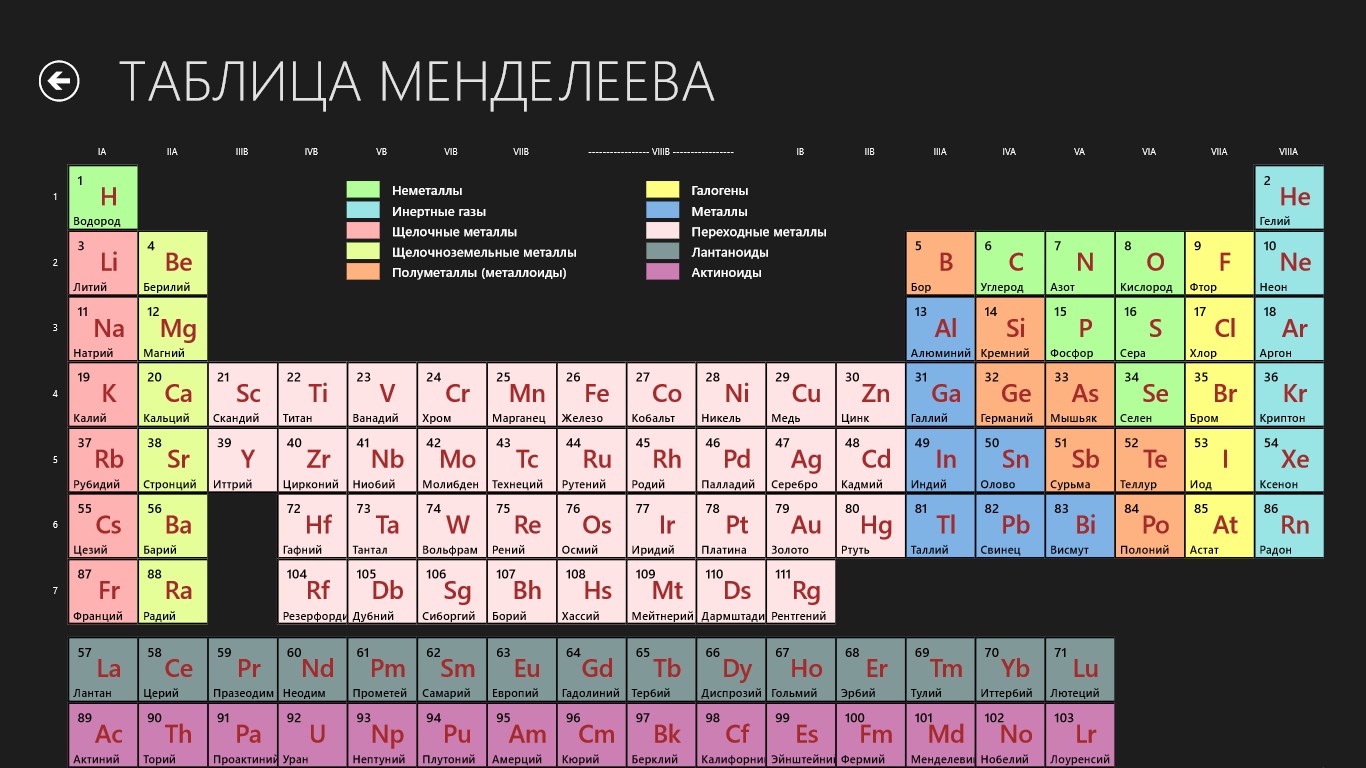
Сама таблица Менделеева много раз трансформировалась, отображая разную информацию о свойствах атомов. Встречаются и курьёзные таблицы.
Так называемая короткопериодная или короткая форма ТМ
Длиннопериодная или длинная форма ТМ
Сверхдлинная.
Флаги государств, обозначающие страну, где впервые открыли данный элемент.
Названия элементов, которые были отменены или оказались ошибочными, как например, история с дидимом Di — оказался в дальнейшем смесью двух вновь открытых элементов празеодима и неодима.
Здесь синим цветом обозначены элементы, образованные во время Большого Взрыва, голубым – синтезированные во время первичного нуклеосинтеза, жёлтые и зелёные цвета обозначают элементы, синтезированные соответственно в недрах “малых” и “больших” звёзд. Розовым цветом – вещества (ядра), синтезируемые во время вспышек сверхновых звёзд. Кстати, золото (Au) ещё синтезируется во время столкновений нейтронных звёзд. Фиолетовые – созданные в лабораториях искусственно. Но это ещё не вся история…
Здесь разными цветами обозначены органические, неорганические и незаменимые элементы, необходимые для построения тел живых существ, в том числе и нас.
Таблица-башня
Предложена в 2006-ом Виталием Циммерманом на основе идей Чарльза Джанета. Он изучал орбитальное заполнение атомов — то, как располагаются электроны относительно ядра. И на основе этого разделил все элементы в четыре группы, рассортировав их по конфигурациям положения электронов. Таблица предельно проста и функциональна.
Таблица предельно проста и функциональна.
Таблица – спираль.
В 1964-ом Теодор Бенфей предложил поставить в центр таблицы водород (H), а прочие элементы разместить вокруг него по спирали, которая раскручивается по часовой стрелке. Уже на втором витке спираль вытягивается в петли, который соответствуют переходным металлам и лантаноидам с актиноидами, предусмотрено место для неизвестных пока суперактинидов. Это придает таблице вид экстравагантного дизайнерского решения.
Таблица – радужная спираль.
Изобретена в 1975 химиком Джеймсом Хайдом. Он увлекался кремнийорганическими соединениями, поэтому в основание таблицы попал именно кремень, так как у него большое число связей с другими элементами. Различные категории элементов так же объединены по секторам и отмечены нужным цветом. Таблица красивее аналогов, но из-за криволинейной формы пользоваться ею непросто.
Эти таблицы отображают последовательность заполнения электронных оболочек. Во всяком случае некоторые из них. Все эти таблицы выглядят весьма экзотично.
Во всяком случае некоторые из них. Все эти таблицы выглядят весьма экзотично.
Таблица изотопов. Здесь отображено время “жизни” различных изотопов, их стабильность в зависимости от массы ядра. Впрочем, это уже не таблица Менделеева, это совсем другая (ядерная физика) история…
российские химики записали в кварцевом стекле миниатюрное цветное изображение Таблицы Менделеева
Ученые РХТУ им. Д.И. Менделеева создали микроизображение Таблицы Менделеева в кварцевом стекле, которое переживет пожар и другие внешние воздействия. Для этого использовали метод фемтосекундной лазерной записи, на основе которого разрабатывают технологии сверхплотного хранения данных в стекле. Размер созданной Таблицы 3,6х2,4 мм и она выдерживает температурное воздействие до 900°С. Работа опубликована в специальном номере журнала Frontiers in Chemistry, посвященном Таблице Менделеева и напоминает, что стекло может включать в себя почти все элементы Таблицы.
Мы используем стекла уже больше 5000 лет, и встретить их можно не только в привычной посуде, окнах и смартфонах, но и в стоматологии, ракетостроении, волоконно-оптической связи и других областях промышленности. Несмотря на такую распространённость, стекла до сих пор изучены не так хорошо, как кажется, и появляются всё новые их составы и методы обработки.
Несмотря на такую распространённость, стекла до сих пор изучены не так хорошо, как кажется, и появляются всё новые их составы и методы обработки. К примеру, в составе красных стекол Кремлевских звезд есть кадмий и селен, а из стекла с оксидом урана раньше производили бокалы и столовую посуду.
В новой работе, опубликованной в журнале Frontiers in Chemistry, ученые записали в стекле миниатюрную Таблицу Менделеева. «В этой работе мы показали, насколько близки две, на первый взгляд никак не связанные между собой вещи – стекло и Таблица Менделеева», – комментирует ассистент кафедры стекла и ситаллов РХТУ им.
Лазерные операции на стеклах
“Для многих стекол метод прямой лазерной записи приводит к ожидаемым результатам, но тут не обходится и без алхимических превращений” – рассказывает Владимир Сигаев, заведующий кафедрой стекла и ситаллов РХТУ и один из авторов работы, “в прозрачном стекле выделяются наночастицы золота
или серебра, область стекла превращается в нелинейный кристалл
или внезапно возникают зоны
со строго повторяющейся периодической структурой (нанорешетки)”.
Картинка с Таблицами
При этом цветом можно управлять, меняя интенсивность лазерного излучения и записывая несколько нанорешеточных слоев друг на другом. Ученые варьировали эти параметры от одной ячейки таблицы к другой, и в результате они стали цветными. Правда в обычном оптическом микроскопе эти цвета не видны, и все ячейки окрашены только в разные оттенки коричневого цвета, но если в микроскоп вставить скрещенные поляризаторы, тогда она становится цветной (это связано с тем, что прохождение света через нанорешетки также меняет поляризацию излучения).
Сделано на века
Общий размер Таблицы получился 3.6 на 2.4 мм, уместится на кончике ногтя, а каждая ячейка с химическим элементом вышла размером всего 200*200 микрон – не больше диаметра иглы шприца. Кроме того, Таблица устойчива перед температурой. Эксперименты показали, что нагрев до 900°С (температура бытового пожара) и резкое охлаждение стекла не влияет на изображение записанной Таблицы. Это делает созданное в РХТУ стекло с нанорешетками самым надежным хранилищем для Таблицы Менделеева.
Любая картинка процесса на твой вкус
“Ученые погружены в узкую научную тематику, читают статьи и обзоры в области своих исследований и редко выходят далеко за ее границы.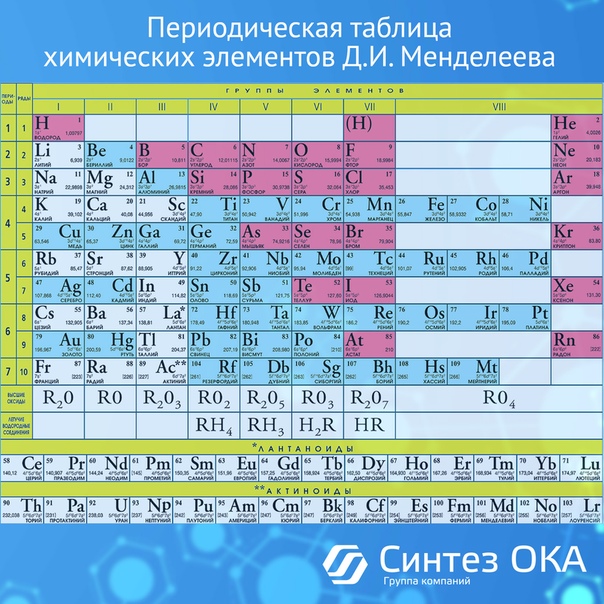
Кроме того, использованный учеными метод формирования нанорешеток в стекле подходит для записи данных. “Исследования нашей кафедры в области лазерной записи в стеклах привели к запуску в РХТУ первого в мире проекта по созданию технологии оптической памяти
на основе стекла” – рассказывает профессор Сигаев. “Эту идею подхватила компания Microsoft
и тоже работает в данном направлении. Технология лазерной записи массивов данных в стекле пока имеет ряд ограничений, но в случае их преодоления нами или другими научными группами, будут созданы носители данных с неограниченным сроком службы”.
Домашнее задание “ТАБЛИЦА МЕНДЕЛЕЕВА” | Парк научных развлечений NEWTON
Это случилось! Ты получил подарок и знания, необходимые, чтобы приступить к выполнению домашнего задания!
Хром в каждый дом
Это домашнее задание – не простое. Если ты сфотографируешь пять пробирок с растворами разных цветов, которые должны получиться, и пришлёшь фотографии на e-mail [email protected], то на нашей следующей программе мы выдадим тебе приз – защитные очки для дальнейших опытов и экспериментов.
Техника безопасности (прочитай этот раздел вместе с кем-то из взрослых, с которыми ты живешь)
Применяемые тобой реактивы и вещества, которые из них получаются в опытах, практически безопасны для здоровья. Некоторые из них даже используются как пищевые добавки или входят в состав лекарств.
Даже хромат и дихромат, про которые можно прочитать много страшного в Интернете, опасны только в чистом виде или при ежедневной работе с ними в течение многих лет. В виде очень разбавленных растворов, которые получаются у нас – они практически безвредны.
В виде очень разбавленных растворов, которые получаются у нас – они практически безвредны.
Но все химические реактивы не стоит употреблять в пищу – мало того, что они невкусные, так ещё и живот заболеть может. Поэтому для приготовления растворов нельзя использовать пищевую посуду, а работать лучше в защитных перчатках.
Для приготовления раствора стиральной соды (описано ниже) можно использовать пищевую посуду – стиральная сода входит в состав стиральных порошков и средств для мытья посуды. Но это исключение из общего правила.
Если вдруг какой-то реактив или капли раствора попали в глаз – тщательно промой глаз водой, пока не перестанет щипать. Если у тебя есть возможность, работай в защитных очках (или в своих, если носишь очки).
Некоторые вещества, с которыми ты будешь работать, сильно пахнут. Работай с ними при открытой форточке и ни в коем случае не нюхай специально. Пробирки после опытов с такими веществами мой только холодной водой.
Пробирки после опытов с такими веществами мой только холодной водой.
Мы будем получать разные соединения элемента хрома. Хром – это металл, которым часто покрывают железные предметы и детали для защиты от ржавчины. Такие вещи так и называют – хромированные. Ещё хром обязательно входит в состав нержавеющей стали.
Название “хром” происходит от древнегреческого слова “хромос”, которое означает “цвет”. И действительно, все-все-все соединения хрома окрашены в разные цвета. В какие? Сейчас узнаем!
У тебя в наборе:
- Реактив – хромокалиевые квасцы
- Шпатель
- Пипетка Пастера
- Пробирки – 3 штуки
- Резиновая пробка
Если у тебя есть ещё какое-то лабораторное оборудование (например, стеклянный стакан или колба), то его тоже можно использовать. Скажем, в стакан удобно ставить пробирки, чтобы они не падали, а в колбе можно готовить растворы.
Тебе также понадобятся:
- Пищевая сода (продается в супермаркетах)
- Уксусная эссенция (продается в супермаркетах, иногда её называют 70% уксусом).
 Внимание! Обычный столовый уксус не подойдёт.
Внимание! Обычный столовый уксус не подойдёт. - Перекись водорода, 3% раствор (продается в аптеке).
- Нашатырный спирт (иногда его называют 10% раствор аммиака) (продается в аптеке).
- Чашка или стакан для приготовления раствора стиральной соды.
- Чашка или стакан, в которые ты будешь ставить пробирку для нагревания.
Тебе часто будет нужна очень горячая вода (кипяток), поэтому заранее поставь кипятиться чайник (или попроси взрослых это сделать).
Опыт 1. Приготовление раствора стиральной соды
Возьми чашку или стакан и положи в неё 3 полные чайные ложки пищевой соды. Нагрей в чайнике воду до кипения, налей в стакан с содой кипяток до половины высоты (осторожно!) и перемешай ложкой. При этом ты увидишь, как сода растворится, а из раствора выделится газ, как будто ты налил(а) газировку. Это пищевая сода от действия горячей воды превратилась в так называемую стиральную соду (её кладут в стиральные порошки) и выделился углекислый газ.
Часть соды может не раствориться – это не страшно.
Опыт 2. Зелёный цвет
- Возьми пробирку и насыпь в неё ⅓ шпателя хромокалиевых квасцов.
- Налей примерно половину пробирки тёплой воды, плотно закрой пробирку пробкой и переворачивай пробирку вниз головой до тех пор, пока всё вещество не растворится. У тебя получится синевато-фиолетовый раствор.
- Разлей полученный тобой раствор примерно поровну в 3 пробирки. Дальше тебе понадобится одна пробирка, а остальные сохрани для других экспериментов.
- Поставь пробирку в маленькую стеклянную банку или стакан, чтобы было удобно наблюдать.
- Возьми пипетку Пастера и уксусную эссенцию. Аккуратно добавь в пробирку 1-2 миллилитра уксусной эссенции с помощью пипетки и перемешай.
- Нагрей в чайнике воду до кипения, осторожно налей кипяток в стакан, в котором стоит пробирка с приготовленным тобой раствором, и оставь стоять на 10-15 минут (можешь в это время делать другие эксперименты).

- Через 10-15 минут вытащи пробирку из горячей воды. Ты увидишь, что цвет раствора изменился на тёмно-зелёный.
Что произошло
Хромокалиевые квасцы в растворе могут быть в двух разных формах: фиолетовой и зелёной. Когда мы добавили кислоту и нагрели, фиолетовая форма превратилась в зелёную.
Совет
Если обернуть кружку полотенцем, вода в ней будет остывать медленнее.
Опыт 3. Сиреневый цвет
- Возьми пробирку с раствором хромокалиевых квасцов и с помощью пипетки добавь в неё 2 миллилитра раствора стиральной соды. При этом из раствора выделится газ и выпадет серый осадок.
- Промой пипетку водой и с помощью пипетки добавь в неё 3 миллилитра нашатырного спирта.
- Поставь пробирку в маленькую стеклянную банку или стакан.
- Нагрей в чайнике воду до кипения, осторожно налей кипяток в стакан, в котором стоит пробирка с приготовленным тобой раствором.

- Оставь пробирку стоять на 10-15 минут (можешь в это время делать другие эксперименты).
- Через 10-15 минут вытащи пробирку из горячей воды. Ты увидишь, что осадок станет голубым, а раствор окрасится в красивый сиреневый цвет.
Что произошло
При добавлении соды к раствору хромокалиевых квасцов сначала выпадает серый осадок – гидроксид хрома. При нагревании он взаимодействует с аммиаком (который содержится в нашатырном спирте), и образуются соединения хрома голубого и сиреневого цвета.
Совет
Если заткнуть пробирку кусочком ваты, пахнуть будет меньше.
- Возьми пробирку с раствором хромокалиевых квасцов и с помощью пипетки добавь в неё 2-3 миллилитра раствора стиральной соды. При этом из раствора выделится газ и выпадет серый осадок.
- Промой пипетку водой и добавь в пробирку 2 миллилитра перекиси водорода.
 Раствор сразу станет зеленовато-коричневым.
Раствор сразу станет зеленовато-коричневым. - Поставь пробирку в маленькую стеклянную банку или стакан.
- Нагрей в чайнике воду до кипения, осторожно налей кипяток в стакан, в котором стоит пробирка с приготовленным тобой раствором.
- Ты увидишь, как раствор станет ярко-жёлтым, и из него начнут выделяться пузырьки газа. Оставь пробирку в горячей воде до тех пор, пока газ не перестанет выделяться (можешь в этой время делать другие эксперименты).
- Вытащи пробирку из горячей воды. Ты получил(а) ярко-жёлтый раствор.
- С помощью пипетки по каплям добавляй в пробирку уксусную эссенцию. При этом снова начнёт выделяться газ, а раствор станет ярко-оранжевым.
- С помощью пипетки добавь в пробирку с оранжевым раствором ещё 1,5 миллилитра уксусной эссенции. Закрой пробирку пробкой и тщательно встряхни, чтобы всё перемешалось.
- Промой пипетку водой и по каплям добавляй перекись водорода. Ты увидишь, как верхний слой раствора станет тёмно-фиолетовым.
- Через 1-2 минуты фиолетовый цвет изменится на коричневый.
 Добавь ещё несколько капель перекиси водорода и наблюдай образование цветных слоёв – коричневый сверху, тёмно-фиолетовый в середине и оранжевый снизу.
Добавь ещё несколько капель перекиси водорода и наблюдай образование цветных слоёв – коричневый сверху, тёмно-фиолетовый в середине и оранжевый снизу. - После того, как весь раствор в пробирке станет коричневым, оставь её стоять на 10-15 минут. При этом коричневый цвет сменится на синевато-фиолетовый, такой же, как цвет исходного раствора хромокалиевых квасцов.
Что произошло
Произошло много чего.
При добавлении соды к раствору хромокалиевых квасцов сначала выпадает серый осадок – гидроксид хрома. Это вещество при нагревании с перекисью водорода превращается в новое соединение хрома – хромат, который ярко-жёлтого цвета. Хромат при взаимодействии с кислотой переходит в оранжевый дихромат. Дихромат реагирует с кислотой и перекисью водорода и превращается в перекись хрома, которая имеет фиолетовый цвет.
Перекись хрома быстро разлагается сначала с образованием различных соединений хрома коричневого цвета, а потом переходит обратно в хромокалиевые квасцы.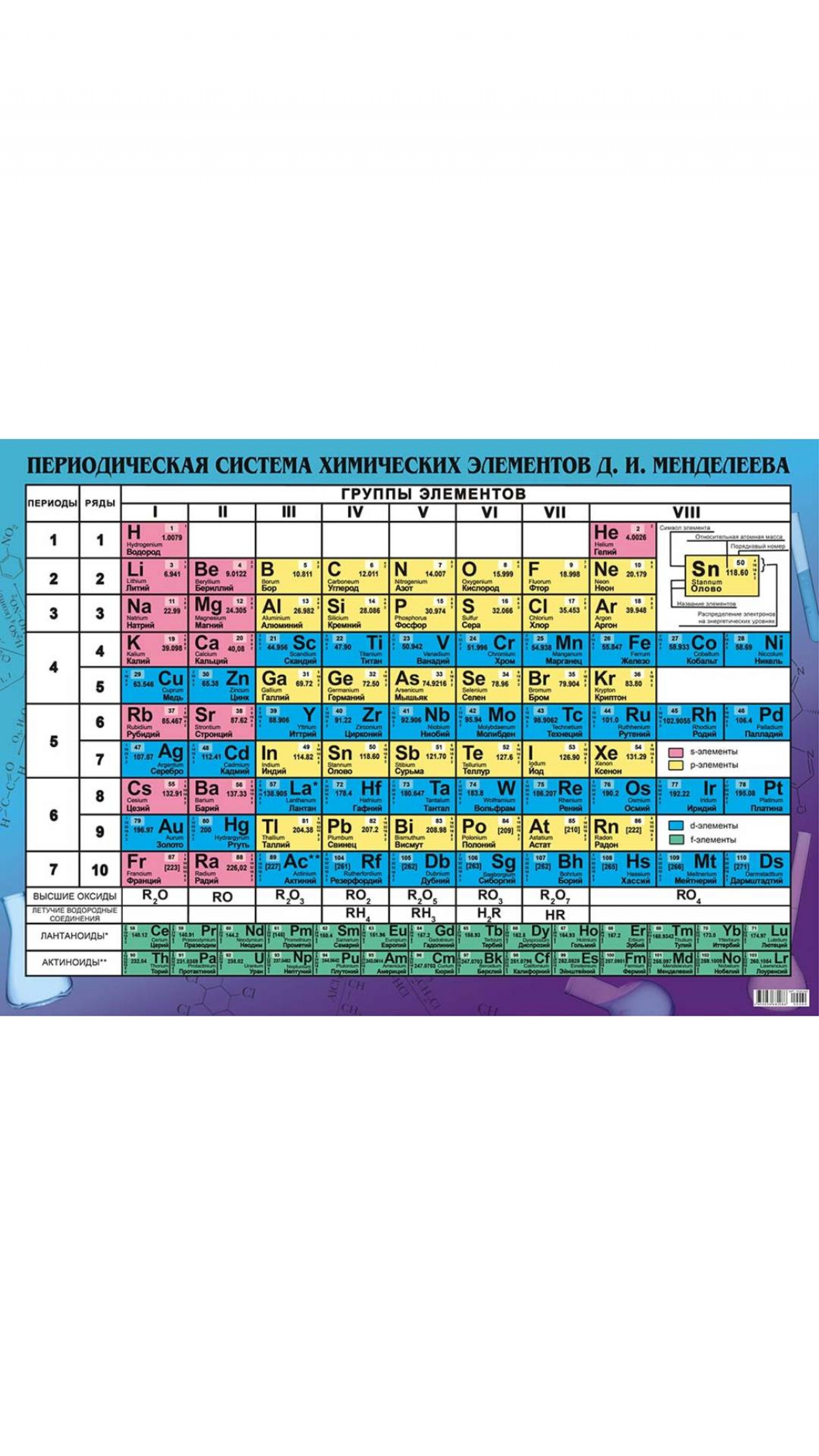
То есть элемент хром совершил несколько химических превращений, а потом снова вернулся в исходное состояние. Круто?
Совет
Если при добавлении растворов пробирку неудобно держать в руках, поставь её в пустой стакан или чашку.
У тебя все получилось? Если не все прошло гладко, не отчаивайся, ты всегда можешь задать вопрос нашим ведущим в группе Умный Екатеринбург
В кварцевом стекле записали таблицу Менделеева
Исследователи из РХТУ им. Д. И. Менделеева создали изображение таблицы Менделеева размером 3,6 х 2,4 мм в кварцевом стекле. Для этого использовали метод фемтосекундной лазерной записи, перспективный для технологий сверхплотного хранения данных в стекле. Работа ученых опубликована в специальном номере журнала Frontiers in Chemistry.
Стекла используются человеком уже более пяти тысяч лет, и за это время успели прочно войти в нашу жизнь. Но несмотря на такую распространенность, этот класс материалов до сих пор пополняется новыми представителями, у которых открываются новые свойства.
Почти 95% всех стекол — силикатные. Они изготавливаются из сырья, главный компонент которого — оксид кремния. Но кроме него в стеклах встречается почти вся таблица Менделеева. Для придания стеклу нужных свойств (например, прочности, химической стойкости или цвета) в него включают оксиды натрия, алюминия, бора, кальция, хрома и так далее.
Новое исследование российских ученых отражает это богатство элементов в виде миниатюрной таблицы Менделеева, выгравированной в толще стекла. Сделать это удалось благодаря использованию фемтосекундных лазеров, которые испускают очень короткие импульсы света. Такие импульсы, хоть и длятся очень мало, но имеют высокую интенсивность излучения, что позволяет точечно менять структуру материала. В операциях на глазах врачи используют фемтосекундные лазеры, чтобы аккуратно разрезать и сшивать живые ткани. Применение этой технологии в стеклах позволяет создавать внутри них миниатюрные оптические элементы: волноводы, каналы, переключатели.
Авторы новой работы воспользовались фемтосекундным лазером для создания внутри кварцевого стекла нанорешеток, обладающих свойством двулучепреломления. Это значит, что луч, проходящий через область с такой периодической структурой, разделяется на две компоненты, которые идут через материал разными путями и с разной скоростью, а затем соединяются на выходе из него. Благодаря этому внутри стекла и появляется интерференционная окраска.
Это значит, что луч, проходящий через область с такой периодической структурой, разделяется на две компоненты, которые идут через материал разными путями и с разной скоростью, а затем соединяются на выходе из него. Благодаря этому внутри стекла и появляется интерференционная окраска.
150 лет Периодической таблице химических элементов Д.И.Менделеева
Внеклассное мероприятие
«Д.И.Менделеев – великий сын России»
(посвящено 150-летию открытия периодического закона химических элементов»
Сегодняшнюю нашу встречу мы посвящаем знаменательной дате – 150- летию создания периодической таблицы. 1 марта 2019 года ей исполнится150 и 185-летию со дня рождения Д.И.Менделеева.
Поэтому все наши вопросы будут посвящены элементам периодической таблицы и ее создателю Дмитрию Ивановичу Менделееву- этому великому сыну России, ученому-энциклопедисту.
Презентация(Д.И.Менделеев и его периодическая таблица)
.
Путешествие по таблице
Сейчас мы будем путешествовать по периодической таблице
Сегодня в таблице 118 химических элементов.
О некоторых из них мы сейчас поговорим.
Видеофильм (Элементы в природе)
Викторина:
1.По городам и селам
Назовите элементы в названиях, которых зашифровано название страны или города (скандий (Скандинавия – Sn) германий (Германия – Ge), рутений (Россия – Ru), франций (Франция – Fr), полоний (Польша – Ро), индий (Индия- In), дубний (Дублин – Db), самарий (Самара – Sm), европий – (Европа – Eu), америций (Америка – Am), калифорний (Калифорния – Cf)).
2.Химия и космос
Назовите химические элементов, в названии которых упоминаются космические объекты.
Интересные факты из жизниМенделеева
Ученик 1.Семнадцатый ребёнок в семье.
Дмитрий Менделеев был семнадцатым ребёнком в семье Ивана Павловича Менделеева, который занимал должность директора Тобольской гимназии. На то время многодетная семья была нетипичной для русской интеллигенции, даже в деревнях такие семьи редко встречались. Впрочем, ко времени рождения будущего великого учёного в семье Менделеевых осталось в живых трое мальчиков и пять девочек, восемь детей умерли ещё в младенческом возрасте, и троим из них родители не успели дать даже имени
Продолжим нашу игру.
3.Ученые элементы
Назовите элементы, в названии которых упоминается фамилия ученого (резерфордий (Резерфорд – Rf), борий (Bh), мейтнерий (Mt), кюрий(Cm), берклий (Bk), энштейний (Еs), фермий (Fm), менделевий (Md), нобелий (No), лоуренсий (Lr).
4. Цветные элементы
Назовите элементы, в которых зашифровано название цвета (рубидий – красный, аурум – желтый, аргентум – серебряный, иод – фиолетовый, цвет фиалки, радий – розовый)
5. Попробуй, угадай
Попробуй, угадай
Заменив первую букву в названии элемента первой группы, получите название избыточно увлажненного участка земли, заросшего растениями (золото – болото).
Интересные факты из жизниМенделеева
Ученик2: Двоечник и золотой медалист
В гимназии Дмитрий Менделеев учился плохо, не любил латынь и Закон Божий. Во время обучения в Главном педагогическом институте Петербурга будущий учёный остался на второй год. На первом курсе института он умудрился по всем предметам, кроме математики, получить неудовлетворительные отметки. Да и по математике он имел всего лишь «удовлетворительно»… Но на старших курсах дело пошло по-другому: среднегодовой балл у Менделеева был равен 4,5 при единственной тройке — по Закону Божьему. Менделеев окончил институт в 1855 году с золотой медалью и был назначен старшим учителем гимназии в Симферополь, но из-за подорванного во время учёбы здоровья и начавшейся Крымской войны перевёлся в Одессу, где работал учителем в Ришельевском лицее.
Продолжим нашу игру.
6.Герои древних мифов
Этот элемент назван в честь мифического героя, подарившего людям огонь. Отцом его был титан Иапет, а матерью великая Фемида, богиня справедливости и правосудия. Радиоактивный элемент семейства лантаноидов (прометий)
7. Самый распространенный элемент космоса
8. Самый распространенный элемент на Земле.
9.В таблице Менделеева большинство металлов или неметаллов
10.Какой химический элемент есть в каждой аптечке, в водоросли ламинарии и необходим организму человека.
Интересные факты из жизни Менделеева
Ученик3: «Менделеевский» порох Россия покупала у американцев
В 1893 году Дмитрий Менделеев наладил производство изобретённого им бездымного пороха, но российское правительство, возглавляемое тогда Петром Столыпиным, не успело его запатентовать, и изобретением воспользовались за океаном. В 1914 году Россия купила у США несколько тысяч тонн этого пороха за золото. Сами американцы, смеясь, не скрывали, что продают русским «менделеевский порох».
В 1914 году Россия купила у США несколько тысяч тонн этого пороха за золото. Сами американцы, смеясь, не скрывали, что продают русским «менделеевский порох».
Продолжим нашу игру.
11. Самый распространенный на земле металл
12. Элемент, обеспечивающий цвет нашей крови
.13. А какой элемент обеспечивает крепость наших костей и зубов
14. Элемент, который принимает участие в изготовлении грузел для удочек
15. Элемент входит в состав спичечной головки
Интересные факты из жизни Менделеева
Ученик4: Признанный мастер чемоданных дел
Менделеев любил переплетать книги, клеить рамки для портретов, а также изготовлять чемоданы. В Петербурге и в Москве его знали как лучшего в России чемоданных дел мастера. «От самого Менделеева», — говорили купцы. Его изделия были добротными и качественными. Учёный изучил все известные в то время рецепты приготовления клея и придумал свою особую клеевую смесь. Способ её приготовления Менделеев держал в секрете.
Учёный изучил все известные в то время рецепты приготовления клея и придумал свою особую клеевую смесь. Способ её приготовления Менделеев держал в секрете.
Продолжим нашу игру.
16. Название какого элемента V группы не соответствует действительности
17. ) Какой металл при обычных условиях жидкость
18.Элемент с порядковым номером101
Интересные факты из жизниМенделеева
Ученик5: « О сне, которого не было»
Очень распространено мнение, о том, что таблица приснилась Менделееву однажды во сне. Однако ученый отверг эту легенду, ответив следующее: «Я над ней, может быть, двадцать лет думал, а вы: сидел, заснул и вдруг …готово» Периодический закон был открыт в феврале 1869 года. В то время было изучено около 63 элементов
Учитель
Круг интересов его был настолько широк, что не ограничивался исключительно химией.
(слайд) К примеру, в 1863 г. он первым выдвинул идею использовать трубопровод при перекачке нефти и нефтепродуктов. Разработка этой идеи имела огромное значение для российской промышленности, в которой стала стремительно развиваться нефтяная отрасль.
он первым выдвинул идею использовать трубопровод при перекачке нефти и нефтепродуктов. Разработка этой идеи имела огромное значение для российской промышленности, в которой стала стремительно развиваться нефтяная отрасль.
(слайд) Задолго до создания герметической гондолы покорителем стратосферы Огюстом Пиккаром Менделеев в одной из своих статей выдвинул идею «прикреплять к аэростату герметически закрытый, оплетенный, упругий прибор для помещения наблюдателя, который тогда будет обеспечен сжатым воздухом и может безопасно для себя управлять шаром».
(слайд) В 1887 г. Менделеев самостоятельно поднялся на воздушном шаре, чтобы наблюдать солнечное затмение. Стартовав возле Клина, он приземлился в Тверской губернии. Этот полет обсуждался во всем мире, а Французская Академия метеорологического воздухоплавания присудила ему диплом «За проявленное мужество при полете для наблюдения солнечного затмения».
(слайд)В 1892 г. Менделеев принял предложение премьер-министра Витте занять должность «ученого хранителя» при депо образцовых мер и весов. Свою деятельность он начал с воссоздания новых «прототипов» основных мер длины и веса и их копий, а также тщательной их сверки с уже существовавшими европейскими эталонами. В результате в 1899 г. в России был введен Закон о мерах и весах.
Свою деятельность он начал с воссоздания новых «прототипов» основных мер длины и веса и их копий, а также тщательной их сверки с уже существовавшими европейскими эталонами. В результате в 1899 г. в России был введен Закон о мерах и весах.
( слайд) Менделеев обладал уникальной системностью мышления, любое дело он разрабатывал до мелочей – от размера шахт в Донбассе до книжек, какие надо читать детям шахтеров. Он был выдающимся экономистом, горячим сторонником протекционизма и хозяйственной самостоятельности России. В своих работах «Письма о заводах», «Толковый тариф…» он стоял на позициях защиты русской промышленности от конкуренции со стороны западных стран, связывая развитие промышленности России с общей таможенной политикой. Ученый отмечал экономическую несправедливость, позволяющую странам, перерабатывающим сырье, пожинать плоды труда стран-поставщиков этого сырья. Этот порядок, по его мнению, «имущему отдает весь перевес над неимущим».
Именем Д. И.Менделеева названы
И.Менделеева названы
(Слайды) В честь Д.И.Менделеева учреждены премии АН России за выдающиеся заслуги в области работ по физике и математике. Его имя носят учебные заведения, научные общества: в том числе Российское химическое общество, ВНИИ метрологии, Санкт-Петербургский химико-технологический институт, учебный институт в Москве, гигантский, в полторы тысячи километров протяжённости, подводный хребет в Северном Ледовитом океане, город на Каме, посёлок под Москвой, улица в Москве, вулкан на Курильских островах, лунный кратер, станция московского метрополитена, научно-исследовательское судно для
океанографических исследований, 101-й химический элемент и минерал – менделеевит.
Д.И.Менделеев – великий сын России!!!
«Сам удивляюсь — чего только я ни делывал
на своей научной жизни. И сделано, думаю, недурно» писал
Д.И. Менделеев
Стране нужен металл Как таблица Менделеева пополнилась шестью новыми элементами: Достижения: 69-я параллель: Lenta.
Недавно в таблицу Менделеева добавили сразу четыре новых элемента: три из них были открыты российскими учеными. Прежде подобные открытия происходили чаще и процесс этот был куда хаотичнее. «Лента.ру» решила рассказать историю шести металлов, которые добывают в России, чтобы доказать это утверждение.
Медный демон
Металл никель был открыт шведским химиком и минералогом Акселем Кронштедтом в 1751 году. Уже в XX веке ученые выяснили, что примеси никеля содержатся в бронзовых предметах, датированных 3,5 тысячи лет до н.э. В них было до двух процентов никеля. В Китае купферникель, то есть соединение меди, никеля и железа, применялся за 1,7 тысячи лет до н.э.
Своему названию металл обязан сленговому выражению немецких шахтеров. Иногда вместо меди им попадалась внешне похожая руда, из которой не получалось извлечь желаемое. Тогда горняки говорили, что шалит «Старый Ник», а слово Nickolaus означало двуличного человека или бездельника.
Кронштедт не дожил до признания своего открытия — он умер в 1765 году.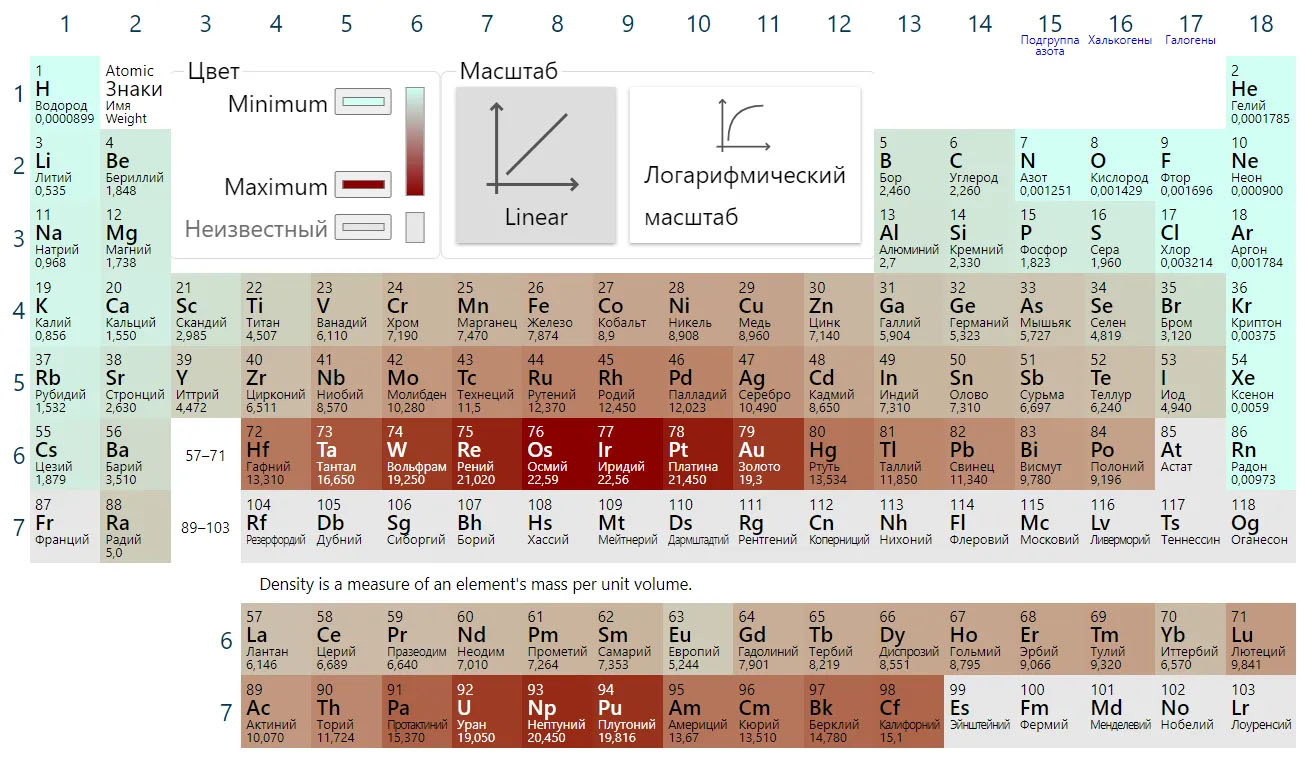 Только в 1804 году немецкий химик Иеремия Рихтер получил чистейший никель. Это был серебристый металл, который обладал полезнейшими свойствами — он мог противостоять агрессивным средам. Для того чтобы полностью воспользоваться достоинствами никеля, потребовалось еще много времени. Металл был очень хрупким и плохо поддавался ковке. Причина заключалась в примесях серы.
Только в 1804 году немецкий химик Иеремия Рихтер получил чистейший никель. Это был серебристый металл, который обладал полезнейшими свойствами — он мог противостоять агрессивным средам. Для того чтобы полностью воспользоваться достоинствами никеля, потребовалось еще много времени. Металл был очень хрупким и плохо поддавался ковке. Причина заключалась в примесях серы.
Первым крупным производителем никеля еще в XIX веке стала Норвегия. Затем его месторождения были открыты в Канаде, России и Южной Африке. Полезные свойства никеля в полной мере раскрылись в конце XIX века. Тогда его начали использовать в сплавах с железом. Выяснилось, что это значительно повышало коррозийную устойчивость. Обычные люди познакомились с никелем, когда из него стали делать монеты. Первопроходцем в этом стали Соединенные Штаты. С середины XIX века они применяли никель для чеканки. Монета в пять центов в США до сих пор известна как nickel.
Никель
Фото: Павел Смертин / «Коммерсантъ»
Настоящий успех к никелю пришел в эпоху научно-технической революции. Без никеля было бы невозможно создание лопастей турбин реактивных двигателей. Сплав стали и никеля способен выдержать температуру в 700-1000 градусов. В качестве альтернативы при их производстве может применяться титан, но он слишком дорог. В электротехнике никель используется в аккумуляторах.
Без никеля было бы невозможно создание лопастей турбин реактивных двигателей. Сплав стали и никеля способен выдержать температуру в 700-1000 градусов. В качестве альтернативы при их производстве может применяться титан, но он слишком дорог. В электротехнике никель используется в аккумуляторах.
Сейчас крупнейшим производителем никеля в мире является «Норильский никель». На него приходится 13 процентов мирового производства. В 2015 году компания произвела 266 тысяч тонн этого металла.
Водка помогла
Крупнейшее в мире месторождение палладия находится в Норильске. Палладий представляет собой пластичный переходный металл серебристо-белого цвета и относится в платиновой группе. С открытием этого элемента связана интересная история.
Еще в конце XVII века бразильские горняки обнаружили «сплав платины и золота». В 1803 году английский химик Уильям Волластон добрался до платиновой руды из Латинской Америки и даже выделил новый металл. Тогда исследователь экспериментировал с царской водкой, в которой и попытался растворить руду. В результате изысканий был получен новый элемент, который химик назвал в честь астероида Паллада, открытого годом ранее.
В результате изысканий был получен новый элемент, который химик назвал в честь астероида Паллада, открытого годом ранее.
При этом Волластон не торопился рассказывать о своем открытии. Вместо этого он распространил в Лондоне анонимную рекламу, в которой рассказал о том, что в магазине его товарища — торговца минералами Форстера — продается «новое серебро». Волею случая приобрести необычный товар решил ирландский химик Ричард Ченевикс. Проведя опыты, он решил, что металл является не чем иным, как сплавом ртути с платиной, который открыл российский химик Аполлос Мусин-Пушкин. Это породило дискуссию в научном сообществе, в результате которой Волластон спешно заявил об открытии палладия и описал его свойства
В природе этот драгоценный металл существует в основном в виде соединений и входит в состав около 30 минералов, в чистом виде он встречается крайне редко. Чаще его извлекают как побочный элемент при добыче меди и никеля. Кроме того, найти палладий можно и в космосе и на других небесных телах: в железных метеоритах на тонну вещества приходится до 7,7 грамма палладия, а в каменных — до 3,5 грамма. Кроме того, этот металл есть на Солнце.
Кроме того, этот металл есть на Солнце.
Палладий выглядит совсем как платина или белое золото, однако весит значительно меньше. Физические и химические свойства металла способствовали широкому применению палладия в промышленности и электронике, в особенности он славился в сфере приборостроения во времена СССР: многие радиоэлектронные компоненты советских приборов изготавливались с помощью палладия. Также он с успехом используется в качестве ювелирного сырья: палладию можно легко придать любую форму и его сложно поцарапать. Тем не менее небольшие ювелирные мастерские не могут заниматься переплавкой этого металла, так как для этого требуется особая дорогостоящая печь.
Палладий
Фото: Павел Лисицын / РИА Новости
Химик Уильям Волластон не остановился на палладии и открыл еще один металл — родий. Это произошло в 1804 году, когда ученый растворял сырую платину в царской водке. В результате он получил порошок, при прокаливании которого в токе водорода и получился новый металл. Слово «родий» является производным от греческих слов «роза» и «розовый» и было выбрано вследствие цвета раствора солей металла в воде.
Слово «родий» является производным от греческих слов «роза» и «розовый» и было выбрано вследствие цвета раствора солей металла в воде.
Родий является очень редким и рассеянным элементом, не имеющим собственного минерала. Каждый год во всем мире добывается менее 30 тонн этого металла, основные месторождения находятся на территории ЮАР и России. По стойкости к коррозии родий превосходит платину, также он обладает высоким коэффициентом отражения электромагнитных лучей.
Окисления этого металла можно добиться лишь при температуре свыше 600 градусов Цельсия. Родий используется в качестве катализатора для различных химических производств, широко применяется в производстве поверхностных зеркал и стекол для жидкокристаллических экранов, в ювелирном деле с помощью родия делают более крепкими и долговечными изделия из платины и палладия.
Родий
Фото: Purpy Pupple / Wikipedia
Все цвета радуги
Еще один металл — иридий — был открыт английским химиком Смитсоном Теннантом в 1804 году. Как и его коллега Волластон, ученый работал с самородками платины и царской водкой. После растворения в ней платины он обнаружил черный порошок, изучив который открыл два новых элемента. Соли одного из них буквально играли всеми цветами радуги, поэтому новый металл и был назван «иридием» от греческого слова «радужный».
Как и его коллега Волластон, ученый работал с самородками платины и царской водкой. После растворения в ней платины он обнаружил черный порошок, изучив который открыл два новых элемента. Соли одного из них буквально играли всеми цветами радуги, поэтому новый металл и был назван «иридием» от греческого слова «радужный».
Теннант весной 1804 года представил доклад Британскому королевскому обществу, в котором сообщил, что в черном порошке содержатся два новых химических элемента. Этими элементами оказались иридий и осмий. Черный порошок, вероятно, представлял из себя сплав осмия с иридием. Осмий хорошо растворяется в царской водке, а иридий в ней не растворяется. Эти свойства способствовали быстрому их разделению.
Иридий
Изображение: pse-mendelejew.de
Иридий относится к наиболее редким элементам, встречающимся на Земле, его количество в земной коре значительно меньше по сравнению с количеством золота или платины, при этом он довольно часто встречается в метеоритах. Из-за своей стойкости иридий плохо поддается обработке, однако он с успехом используется в производстве топливных баков для космических кораблей, а его ядерный изомер 192m2, имеющий период полураспада 241 год, представляет большой интерес в качестве источника электроэнергии. Иридий применяется в производстве наиболее долговечных свечей зажигания автомобиля, его свойства используются для придания жароустойчивости покрытиям, иридий также применяется в производстве электрических стимуляторов сердечной деятельности.
Иридий применяется в производстве наиболее долговечных свечей зажигания автомобиля, его свойства используются для придания жароустойчивости покрытиям, иридий также применяется в производстве электрических стимуляторов сердечной деятельности.
Русский металл
В 1844 году русский химик, профессор Казанского университета Карл Клаус открыл еще один новый элемент — рутений. Получив из Петербургского монетного двора около 15 фунтов платиновых руд, он сплавил их остатки с селитрой и извлек растворимую в воде часть, содержащую осмий, хром и другие металлы. Нерастворимый в воде остаток он поместил в царскую водку и перегнал досуха. Обработав получившееся соединение кипящей водой и добавив избыток поташа, Клаус отделил осадок гидроокиси железа, в котором обнаружил присутствие неизвестного элемента. Его химик предложил назвать рутением в честь России (от латинского Ruthenia — Россия). Это название впервые было использовано еще в 1828 году немецким химиком Готтфридом Вильгельмом Озанном. Тогда при анализе нижнетагильской платиновой руды он заявил, что обнаружил сразу три новых металла: рутений, плуран (сокращение от «платина Урала») и полин (от греческого «седой»). Позднее шведский ученый Йенс Якоб Берцелиус опроверг открытия Озанна. Однако Карл Клаус полагал, что окись рутения впервые обнаружил именно его немецкий коллега.
Тогда при анализе нижнетагильской платиновой руды он заявил, что обнаружил сразу три новых металла: рутений, плуран (сокращение от «платина Урала») и полин (от греческого «седой»). Позднее шведский ученый Йенс Якоб Берцелиус опроверг открытия Озанна. Однако Карл Клаус полагал, что окись рутения впервые обнаружил именно его немецкий коллега.
Рутений
Изображение: pse-mendelejew.de
Сегодня рутений является побочным продуктом при очищении платины и других благородных металлов. Он также применяется при производстве износостойких и жаропрочных материалов и конструкций, что особенно ценно в космической промышленности. Кроме того, рутений является единственным металлом платиновой группы, который обнаруживается в живых организмах (преимущественно в мышечной ткани). Ежегодно в мире добывают около 17 тонн рутения, а общие запасы этого металла оцениваются примерно в пять тысяч тонн.
Прямиком из Древнего Египта
В 1735 году шведскому химику Георгу Бранду удалось выделить из минералов новый металл серебристо-белого, иногда слегка желтоватого оттенка. Ученый назвал его кобальтом, поскольку древние саксонцы объясняли смерти плавильщиков серебра проделками злого гнома Кобольда. В реальности они умирали от ядовитых выделений оксида мышьяка из кобальтовых минералов.
Ученый назвал его кобальтом, поскольку древние саксонцы объясняли смерти плавильщиков серебра проделками злого гнома Кобольда. В реальности они умирали от ядовитых выделений оксида мышьяка из кобальтовых минералов.
Некоторые свойства этого металла были известны людям с незапамятных времен. Так, изготовленный древними египтянами в ХV веке до нашей эры стеклянный кувшин был окрашен солями кобальта, его же обнаружили в составе голубых стекловидных кирпичей в гробницах фараонов. В древней Ассирии и Вавилоне из кобальта изготовляли лазурит — голубую краску, которой затем обливали керамические изделия. Исходным материалом для получения кобальтовых соединений тогда служил содержащий металл сапфир цаффер. Вероятно, оттуда и произошли названия красок сафлор и шафран.
Кобальт
Фото: Wikipedia
В средние века горняки часто натыкались на кобальтовую «землю». Иногда она была похожа на серебряную руду, но не содержала драгоценного металла. Примесь кобальтовой земли к другим рудам часто мешала выплавке, ведь из-за образующегося в процессе густого дыма из сульфидов и арсенидов часть выплавляемого металла терялась.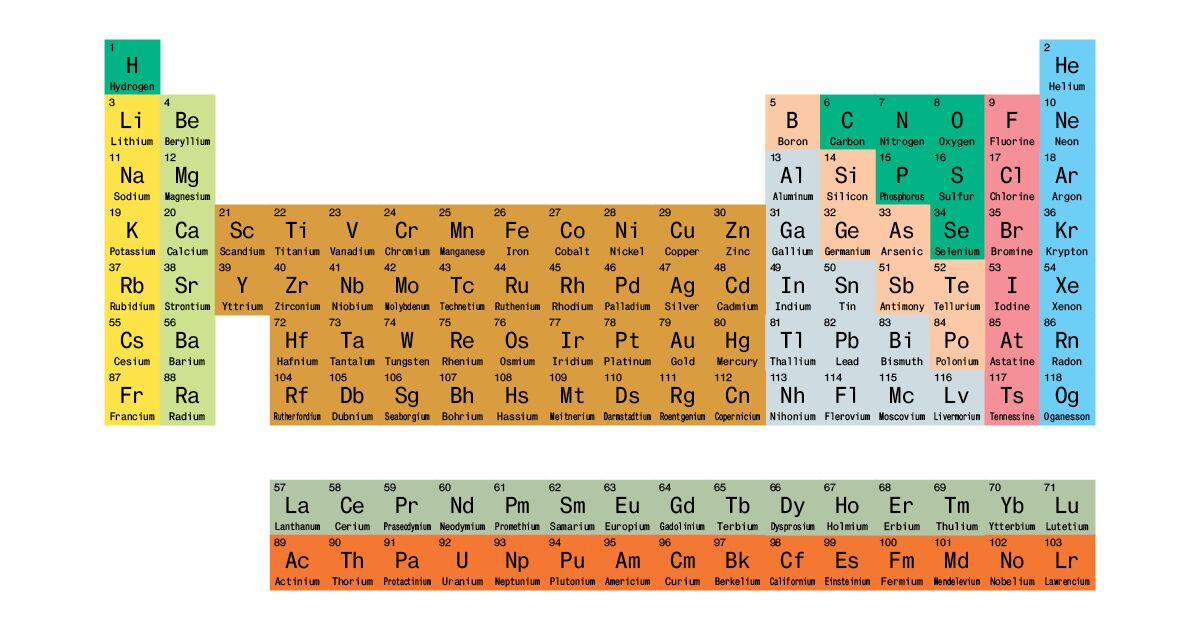
Об этом еще в IV веке нашей эры писал Псевдо-Демокрит, а позже немецкие горняки стали называть пары от кобальтовых земель коб-ольд или кобельт — как звали плутоватого подземного гнома, насмехавшегося над шахтерами. В древнерусском языке также имеются близкие по смыслу слова кобение (гадание) и кобь — гадание по птичьему полету.
Кобальт также упоминается у Бирингуччо, Василия Валентина, Парацельса и других авторов XV-XVII веков. В «Алхимическом лексиконе» Руланда (1612 год) о кобальте говорится: «Кобол кобальт или коллет — металлическая материя, чернее свинца и железа, растягивающаяся при нагревании. Кобальт — черная, немного похожая по цвету на золу материя, которую можно ковать и лить. Но она не обладает металлическим блеском и представляет собой вредную взвесь, уводящую (при плавке) вместе с дымом хорошую руду».
Металлический кобальт впервые был описан в 1735 году упсальским профессором Брандтом. В диссертации «О полуметаллах» он рассказывает, что получаемый из руд металлический висмут не представляет собой чистого металла, а содержит «кобальтовый королек», то есть металлический кобальт. Он же выяснил, что соли кобальта окрашивают стекла в синий цвет. В чистом виде металлический кобальт был впервые получен Верцелиусом.
Гелий – Что такое Гелий?
Гелий – это химический элемент с атомным номером 2 и атомной массой 4,0026; относится к инертным газам.Гелий добывается из природного газа процессом низкотемпературного разделения – так называемой фракционной перегонкой.
Физические свойства гелия:
- нетоксичный,
- не имеет цвета, запаха и вкуса,
- при нормальных условиях представляет собой одноатомный газ,
- при атмосферном давлении не переходит в твердую фазу даже при крайне близких к абсолютному нулю температурах,
- теплопроводность (0,1437 Вт/(м·К) при н. у.) больше, чем у других газов за исключением водорода;
- коэффициент преломления ближе к 1, чем у любого другого газа,
- менее растворим в воде, чем любой другой известный газ (при 20 °C около 8,8 мл/л),
- скорость диффузии сквозь твердые материалы в 3 раза выше, чем у воздуха, и приблизительно на 65 % выше, чем у водорода,
-
при пропускании тока через заполненную гелием трубку наблюдаются разряды различных цветов, зависящих главным образом от давления газа в трубке.

- наименее химически активный элемент 8й группы таблицы Менделеева,
- в газовой фазе может образовывать (при действии электрического разряда или ультрафиолетового излучения) так называемые эксимерные молекулы, у которых устойчивы возбужденные электронные состояния и неустойчиво основное состояние: двухатомные молекулы He2, фторид HeF, хлорид HeCl,
- в отличие от многих других газов не образует клатратов (соединения, в которых молекулы одного сорта («гости») заключены в полости, образованной молекулами другого сорта («хозяевами»)), т. к. маленькие атомы гелия «ускользают» из слишком больших для них пустот в структуре воды.
Например, в нефтегазовой промышленности его используют для поиска мест утечек в подземных газопроводах – для этого гелий вводят в рабочий объем тестируемого объекта.
В атомной энергетике он применяется в качестве теплоносителя в некоторых типах ядерных реакторов.

В металлургии гелий используется в качестве защитного инертного газа для выплавки чистых металлов.
В пищевой промышленности гелий известен как пищевая добавка E939 – он применяется в качестве пропеллента и упаковочного газа.
Кроме того, данный газ служит хладагентом для получения сверхнизких температур.
Периодическая таблица с цветами элементов
Периодическая таблица с цветами элементовСредней длины формы периодической таблицы с цветами элементов.
Ограниченный поиск таблицы Менделеева с цветами
из элементов еще не располагалась таблица такого типа. Однако Теодор Грей
изготовил множество замечательных таблиц, в том числе одну с изображениями аутентичных
образцы элементов (http://periodictable.com/) и коммерчески
доступная модель, содержащая образцы большинства элементов (http: // www.periodictable.co.uk/). Хотя приведенные ниже таблицы не совсем такие
увлекательные или интересные, как таблицы Грея, таблицы, представленные ниже, были спроектированы
чтобы зрители могли сосредоточиться на свойстве цвета. Большинство цветов имеют
был извлечен с https://www.chemicool.com/ в первую очередь потому, что он часто
включает описание цвета из двух слов. Другие упомянутые сайты были
Http://periodictable.com/Properties/A/Color.html Теодора Грея и Марк
Зимний https://www.webelements.com/. Для некоторых элементов цвета, указанные на
Интернет-сайты не всегда согласны.Рене Вернон, автор статьи
по металлоидам https://pubs.acs.org/doi/pdfplus/10.1021/ed3008457 имеет
внес ценные комментарии о цветах бора, фосфора, йода,
цезий и астатин. Некоторые из этих проблем с цветом связаны с тем, что самый стабильный
аллотроп (например, фосфор) не всегда является наиболее распространенным аллотропом.
Большинство цветов имеют
был извлечен с https://www.chemicool.com/ в первую очередь потому, что он часто
включает описание цвета из двух слов. Другие упомянутые сайты были
Http://periodictable.com/Properties/A/Color.html Теодора Грея и Марк
Зимний https://www.webelements.com/. Для некоторых элементов цвета, указанные на
Интернет-сайты не всегда согласны.Рене Вернон, автор статьи
по металлоидам https://pubs.acs.org/doi/pdfplus/10.1021/ed3008457 имеет
внес ценные комментарии о цветах бора, фосфора, йода,
цезий и астатин. Некоторые из этих проблем с цветом связаны с тем, что самый стабильный
аллотроп (например, фосфор) не всегда является наиболее распространенным аллотропом.
бор – наиболее стабильный аллотроп бора – бета-ромбоэдрический кристаллический государство. Цвета, указанные для этого состояния, варьируются от блестящего серебристо-серого до серого и от темного к черному.В таблице он обозначен темно-серым цветом.
фосфор – наиболее стабильный аллотроп – черный, но наиболее распространенной формой является
описывается как от белого до бледно-желтого. Очень светло-желтый был использован ниже с
черная вставка.
йод – хотя иногда упоминается серебро, подавляющее большинство согласны с тем, что кристаллы йода фиолетового или пурпурного цвета.
астат – хотя астат наблюдался из-за его временного существования, его цвет, видимо, определить не удалось.Некоторые веб-сайты сделать вывод, что он должен иметь некоторые металлические свойства и, как результат, иметь серебристый цвет. Другие веб-сайты предполагают, что прогрессирование замедляется по группе 7А. (17), цвет непрерывно темнеет, предполагая, что астатин должен быть рядом с черным. В этих таблицах он оставлен неизвестным, как франций и его элементы. с атомными номерами выше 99.
Таблицы выше были разработаны таким образом, чтобы содержать элементы, раскрашенные так, чтобы они напоминали актуальные цвета элементов.Периодические таблицы с цветами элементов могут также можно найти на нескольких сайтах:
http://murov.info/timelines.htm
http://murov.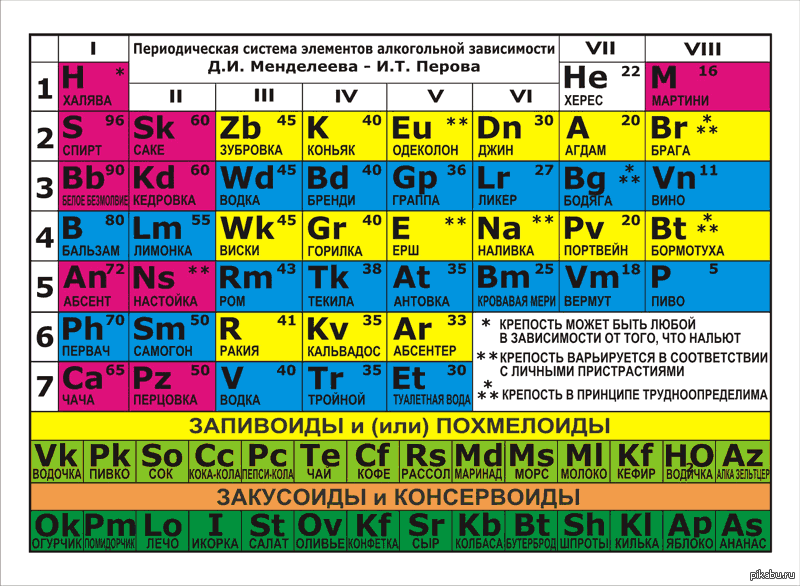 info/periodictables.htm
info/periodictables.htm
http://murov.info/pertabcol1.pdf
http://murov.info/pertabcol2.pdf
http://murov.info/timeline.pptx
Пожалуйста, присылайте комментарии и предложения Стиву Мурову, [email protected]
счетчик посещений запущен 21.05.18, последняя редакция 19.06.20 уникальных посетителей начат 21.05.18
Что обозначают разные цвета в периодической таблице? – Restaurantnorman.com
Что обозначают разные цвета в таблице Менделеева?
В периодической таблице элементов с цветовой кодировкой прямоугольник для каждого элемента окрашен. Этот цвет представляет классы элементов, которые включают металлы, металлоиды и неметаллы. Обычно синий цвет используется для металлов, оранжевый – для металлоидов, а зеленый – для неметаллов.
Какие цвета есть в таблице Менделеева?
Периодическая таблица Менделеева также разделена на четыре блока: s = красный, p = зеленый, d = желтый и f = синий.
Какого цвета или цветов представляют элементы, являющиеся металлами?
Цветовая маркировка: желтый, металл; серый с подчеркнутым символом – металлоиды; синий жирным курсивом, неметаллический; белый, элементы с неизвестной классификацией.
Какие символы в периодической таблице?
Элементы таблицы Менделеева, отсортированные по символу
| Обозначение | Название химического элемента |
|---|---|
| К | Калий |
| Kr | Криптон |
| La | Лантан |
| Li | Литий |
Какие 9 элементов природы?
Девять Элементов являются жизненно важными компонентами вселенной и являются продуктом магии, используемой ее обитателями.Они известны как Нуль, Свет, Тьма, Луна, Космос, Пламя, Мороз, Земля и Буря и естественным образом связаны с каждым существом или объектом во вселенной.
Все элементы существуют на земле?
Элементы с 1 по 92 (за исключением элементов 43 и 61) встречаются на Земле в естественных условиях, хотя некоторые из них присутствуют только в очень малых количествах. Элементы, следующие за ураном в периодической таблице, производятся только искусственно и известны как трансурановые или трансурановые элементы.
Элементы, следующие за ураном в периодической таблице, производятся только искусственно и известны как трансурановые или трансурановые элементы.
Где его можно найти на Земле?
Гелий – второй по распространенности элемент во Вселенной, но здесь, на Земле, он довольно редок. Большинство людей предполагают, что мы добываем гелий из воздуха, но на самом деле мы выкапываем его из земли. Гелий можно найти в некоторых частях мира, особенно в Техасе, в качестве второстепенного компонента в некоторых источниках природного газа.
Какой элемент чаще всего встречается в звездах?
гелий
Каковы два основных элемента звезд?
Звезды сделаны из очень горячего газа.Этот газ состоит в основном из водорода и гелия, двух самых легких элементов. Звезды сияют, превращая водород в гелий в своих ядрах, а позже в своей жизни создают более тяжелые элементы.
Какого цвета самая горячая звезда?
синий
Гигантская периодическая таблица с цветовой кодировкой
Положения и условия
Спасибо, что посетили наш сайт. Эти условия использования применимы к веб-сайтам США, Канады и Пуэрто-Рико (далее «Веб-сайт»), которыми управляет VWR («Компания»).Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Все пользователи веб-сайта подчиняются следующим условиям использования веб-сайта (эти «Условия использования»). Пожалуйста, внимательно прочтите эти Условия использования перед доступом или использованием любой части веб-сайта. Заходя на веб-сайт или используя его, вы соглашаетесь с тем, что прочитали, поняли и соглашаетесь соблюдать настоящие Условия использования с поправками, которые время от времени вносятся, а также Политику конфиденциальности компании, которая настоящим включена в настоящие Условия. использования. Если вы не желаете соглашаться с настоящими Условиями использования, не открывайте и не используйте какие-либо части Веб-сайта.
Эти условия использования применимы к веб-сайтам США, Канады и Пуэрто-Рико (далее «Веб-сайт»), которыми управляет VWR («Компания»).Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Все пользователи веб-сайта подчиняются следующим условиям использования веб-сайта (эти «Условия использования»). Пожалуйста, внимательно прочтите эти Условия использования перед доступом или использованием любой части веб-сайта. Заходя на веб-сайт или используя его, вы соглашаетесь с тем, что прочитали, поняли и соглашаетесь соблюдать настоящие Условия использования с поправками, которые время от времени вносятся, а также Политику конфиденциальности компании, которая настоящим включена в настоящие Условия. использования. Если вы не желаете соглашаться с настоящими Условиями использования, не открывайте и не используйте какие-либо части Веб-сайта.
Компания может пересматривать и обновлять настоящие Условия использования в любое время без предварительного уведомления, разместив измененные условия на веб-сайте. Продолжение использования вами веб-сайта означает, что вы принимаете и соглашаетесь с пересмотренными Условиями использования. Если вы не согласны с Условиями использования (в которые время от времени вносятся поправки) или недовольны Веб-сайтом, ваше единственное и исключительное средство правовой защиты – прекратить использование Веб-сайта.
Использование сайта
Информация, содержащаяся на этом веб-сайте, предназначена только для информационных целей. Хотя считается, что информация верна на момент публикации, вам следует самостоятельно определить ее пригодность для вашего использования. Не все продукты или услуги, описанные на этом веб-сайте, доступны во всех юрисдикциях или для всех потенциальных клиентов, и ничто в настоящем документе не предназначено как предложение или ходатайство в какой-либо юрисдикции или какому-либо потенциальному покупателю, где такое предложение или продажа не соответствует требованиям.
Покупка товаров и услуг
Настоящие Условия и положения распространяются только на использование веб-сайта. Обратите внимание, что условия, касающиеся обслуживания, продаж продуктов, рекламных акций и других связанных мероприятий, можно найти по адресу https://us.vwr.com/store/content/externalContentPage.jsp?path=/en_US/about_vwr_terms_and_conditions.jsp , и эти условия регулируют любые покупки продуктов или услуг у Компании.
Интерактивные функции
Веб-сайт может содержать службы досок объявлений, области чата, группы новостей, форумы, сообщества, личные веб-страницы, календари и / или другие средства сообщения или связи, предназначенные для того, чтобы вы могли общаться с общественностью в целом или с группой ( вместе “Функция сообщества”).Вы соглашаетесь использовать функцию сообщества только для публикации, отправки и получения сообщений и материалов, которые являются надлежащими и относятся к конкретной функции сообщества. Вы соглашаетесь использовать веб-сайт только в законных целях.
Вы соглашаетесь использовать веб-сайт только в законных целях.
A. В частности, вы соглашаетесь не делать ничего из следующего при использовании функции сообщества:
1. Оскорблять, оскорблять, преследовать, преследовать, угрожать или иным образом нарушать законные права (например, право на неприкосновенность частной жизни и гласность) других.
2. Публиковать, размещать, загружать, распространять или распространять любую неуместную, непристойную, дискредитирующую, нарушающую авторские права, непристойную, непристойную или незаконную тему, название, материал или информацию.
3. Загружайте файлы, содержащие программное обеспечение или другие материалы, защищенные законами об интеллектуальной собственности (или правами на неприкосновенность частной жизни), если вы не владеете или не контролируете права на них или не получили всех необходимых разрешений.
4. Загрузите файлы, содержащие вирусы, поврежденные файлы или любое другое подобное программное обеспечение или программы, которые могут повредить работу чужого компьютера.
5. Перехватить или попытаться перехватить электронную почту, не предназначенную для вас.
6. Рекламировать или предлагать продавать или покупать какие-либо товары или услуги для любых деловых целей, если такая функция сообщества специально не разрешает такие сообщения.
7. Проводите или рассылайте опросы, конкурсы, финансовые пирамиды или письма счастья.
8. Загрузите любой файл, опубликованный другим пользователем функции сообщества, который, как вы знаете или разумно должен знать, не может распространяться на законных основаниях таким образом или что у вас есть договорное обязательство сохранять конфиденциальность (несмотря на его доступность на веб-сайте).
9. Подделывать или удалять любые ссылки на автора, юридические или другие надлежащие уведомления, обозначения собственности или ярлыки происхождения или источника программного обеспечения или других материалов, содержащихся в загружаемом файле.
10. Предоставление ложной информации о принадлежности к какому-либо лицу или организации.
11. Участвовать в любых других действиях, которые ограничивают или препятствуют использованию веб-сайта кем-либо или которые, по мнению Компании, могут нанести вред Компании или пользователям веб-сайта или подвергнуть их ответственности.
12. Нарушать любые применимые законы или постановления или нарушать любой кодекс поведения или другие правила, которые могут быть применимы к какой-либо конкретной функции Сообщества.
13. Собирать или иным образом собирать информацию о других, включая адреса электронной почты, без их согласия.
B. Вы понимаете и признаете, что несете ответственность за любой контент, который вы отправляете, вы, а не Компания, несете полную ответственность за такой контент, включая его законность, надежность и уместность. Если вы публикуете сообщения от имени или от имени вашего работодателя или другого юридического лица, вы заявляете и гарантируете, что у вас есть на это право. Загружая или иным образом передавая материалы в любую область веб-сайта, вы гарантируете, что эти материалы являются вашими собственными или находятся в общественном достоянии или иным образом свободны от проприетарных или иных ограничений, и что вы имеете право размещать их на веб-сайте.
Кроме того, загружая или иным образом передавая материалы в любую область веб-сайта, вы предоставляете Компании безотзывное, бесплатное, всемирное право на публикацию, воспроизведение, использование, адаптацию, редактирование и / или изменение таких материалов любым способом, в любые и все средства массовой информации, известные в настоящее время или обнаруженные в будущем во всем мире, в том числе в Интернете и World Wide Web, для рекламных, коммерческих, торговых и рекламных целей, без дополнительных ограничений или компенсации, если это не запрещено законом, и без уведомления, проверки или одобрения.
C. Компания оставляет за собой право, но не принимает на себя никакой ответственности (1) удалить любые материалы, размещенные на веб-сайте, которые Компания по своему собственному усмотрению сочтет несовместимыми с вышеуказанными обязательствами или иным образом неприемлемыми по любой причине. ; и (2) прекратить доступ любого пользователя ко всему или к части веб-сайта.
Однако Компания не может ни просмотреть все материалы до их размещения на веб-сайте, ни обеспечить быстрое удаление нежелательных материалов после их размещения.Соответственно, Компания не несет ответственности за какие-либо действия или бездействие в отношении передач, сообщений или контента, предоставленных третьими сторонами. Компания оставляет за собой право предпринимать любые действия, которые она сочтет необходимыми для защиты личной безопасности пользователей этого веб-сайта и общественности; тем не менее, Компания не несет ответственности перед кем-либо за выполнение или невыполнение действий, описанных в этом параграфе.
D. Несоблюдение вами положений пунктов (A) или (B) выше может привести к прекращению вашего доступа к веб-сайту и может подвергнуть вас гражданской и / или уголовной ответственности.
Особое примечание о содержании функций сообщества
Любой контент и / или мнения, загруженные, выраженные или отправленные с помощью любой функции сообщества или любого другого общедоступного раздела веб-сайта (включая области, защищенные паролем), а также все статьи и ответы на вопросы, кроме контента, явно разрешенного Компания, являются исключительно мнениями и ответственностью лица, представляющего их, и не обязательно отражают мнение Компании. Например, любое рекомендованное или предлагаемое использование продуктов или услуг, доступных от Компании, которое публикуется через функцию сообщества, не является признаком одобрения или рекомендации со стороны Компании. Если вы решите следовать какой-либо такой рекомендации, вы делаете это на свой страх и риск.
Например, любое рекомендованное или предлагаемое использование продуктов или услуг, доступных от Компании, которое публикуется через функцию сообщества, не является признаком одобрения или рекомендации со стороны Компании. Если вы решите следовать какой-либо такой рекомендации, вы делаете это на свой страх и риск.
Ссылки на сторонние сайты
Веб-сайт может содержать ссылки на другие веб-сайты в Интернете. Компания не несет ответственности за контент, продукты, услуги или методы любых сторонних веб-сайтов, включая, помимо прочего, сайты, связанные с Веб-сайтом или с него, сайты, созданные внутри Веб-сайта, или стороннюю рекламу, и не делает заявлений относительно их качество, содержание или точность.Наличие ссылок с веб-сайта на любой сторонний веб-сайт не означает, что мы одобряем, поддерживаем или рекомендуем этот веб-сайт. Мы отказываемся от всех гарантий, явных или подразумеваемых, в отношении точности, законности, надежности или действительности любого контента на любых сторонних веб-сайтах. Вы используете сторонние веб-сайты на свой страх и риск и в соответствии с условиями использования таких веб-сайтов.
Вы используете сторонние веб-сайты на свой страх и риск и в соответствии с условиями использования таких веб-сайтов.
Права собственности на контент
Вы признаете и соглашаетесь с тем, что все содержимое веб-сайта (включая всю информацию, данные, программное обеспечение, графику, текст, изображения, логотипы и / или другие материалы) и его дизайн, выбор, сбор, расположение и сборка являются являются собственностью Компании и защищены законами США и международными законами об интеллектуальной собственности.Вы имеете право использовать содержимое веб-сайта только в личных или законных деловых целях. Вы не можете копировать, изменять, создавать производные работы, публично демонстрировать или исполнять, переиздавать, хранить, передавать, распространять, удалять, удалять, дополнять, добавлять, участвовать в передаче, лицензировать или продавать какие-либо материалы в Интернете. Сайт без предварительного письменного согласия Компании, за исключением: (а) временного хранения копий таких материалов в ОЗУ, (б) хранения файлов, которые автоматически кэшируются вашим веб-браузером в целях улучшения отображения, и (в) печати разумного количество страниц веб-сайта; в каждом случае при условии, что вы не изменяете и не удаляете какие-либо уведомления об авторских правах или других правах собственности, включенные в такие материалы.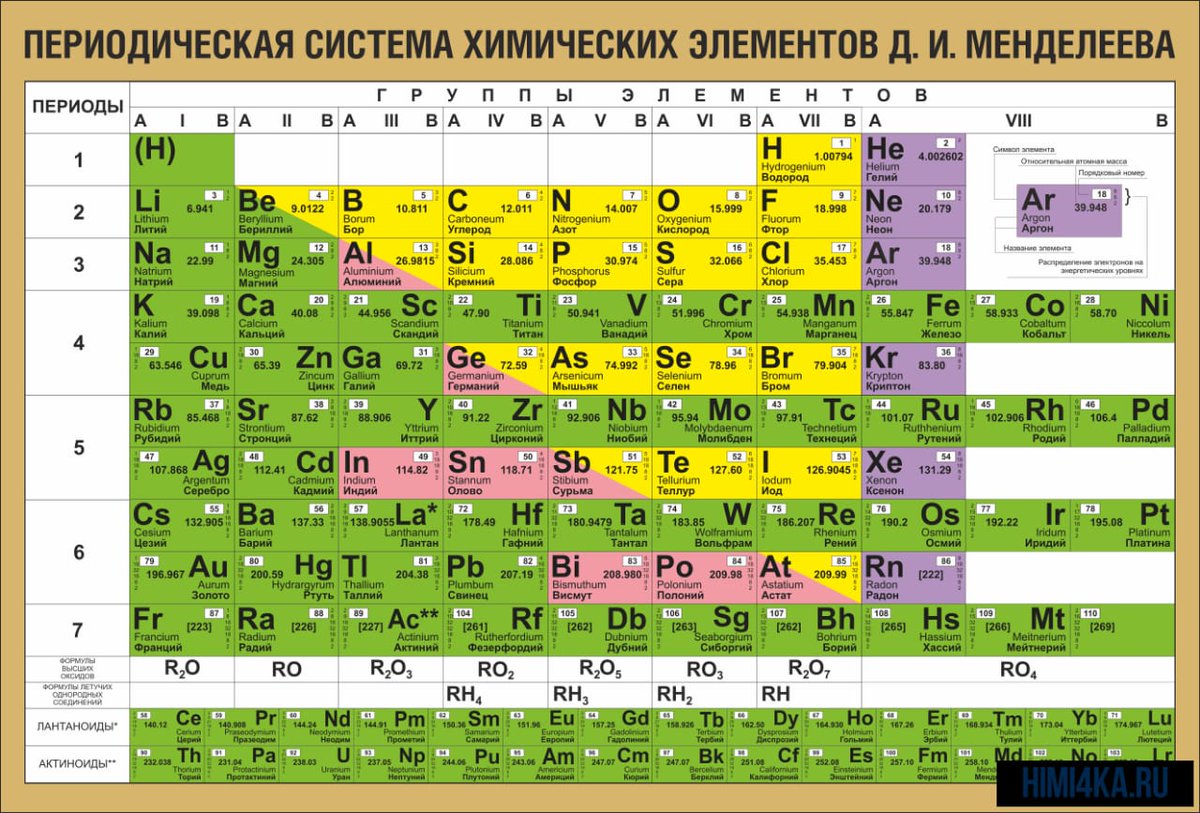 Ни название, ни какие-либо права интеллектуальной собственности на любую информацию или материалы на веб-сайте не передаются вам, а остаются за Компанией или соответствующим владельцем такого контента.
Ни название, ни какие-либо права интеллектуальной собственности на любую информацию или материалы на веб-сайте не передаются вам, а остаются за Компанией или соответствующим владельцем такого контента.
Товарные знаки
Название и логотип компании, а также все связанные названия, логотипы, названия продуктов и услуг, появляющиеся на веб-сайте, являются товарными знаками компании и / или соответствующих сторонних поставщиков. Их нельзя использовать или повторно отображать без предварительного письменного согласия Компании.
Отказ от ответственности
Компания не несет никакой ответственности за материалы, информацию и мнения, предоставленные или доступные через Веб-сайт («Контент сайта»). Вы полагаетесь на Контент сайта исключительно на свой страх и риск. Компания не несет никакой ответственности за травмы или убытки, возникшие в результате использования любого Контента Сайта.
ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА И ПРОДУКТЫ И УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ ИЛИ ДОСТУПНЫЕ ЧЕРЕЗ САЙТ, ПРЕДОСТАВЛЯЮТСЯ НА УСЛОВИЯХ «КАК ЕСТЬ» И «ПО ДОСТУПНОСТИ», СО ВСЕМИ ОШИБКАМИ. КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ДАЕТ НИКАКИХ ГАРАНТИЙ ИЛИ ЗАЯВЛЕНИЙ В ОТНОШЕНИИ КАЧЕСТВА, ТОЧНОСТИ ИЛИ ДОСТУПНОСТИ ВЕБ-САЙТА. В частности, НО БЕЗ ОГРАНИЧЕНИЯ ВЫШЕИЗЛОЖЕННОГО, НИ КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ГАРАНТИРУЕТ ИЛИ ЗАЯВЛЯЕТ, ЧТО ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА ИЛИ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА САЙТЕ ИЛИ С ПОМОЩЬЮ САЙТА, БУДУТ ТОЧНЫМИ, НАДЕЖНЫМИ ИЛИ БЕСПЛАТНЫМИ ИЛИ БЕСПЛАТНЫМИ ЧТО ДЕФЕКТЫ БУДУТ ИСПРАВЛЕНЫ; ЧТО ВЕБ-САЙТ ИЛИ СЕРВЕР, КОТОРЫЙ ДЕЛАЕТ ЕГО ДОСТУПНЫМ, НЕ СОДЕРЖИТ ВИРУСОВ ИЛИ ДРУГИХ ВРЕДНЫХ КОМПОНЕНТОВ; ИЛИ ЧТО ВЕБ-САЙТ ИНАЧЕ ОТВЕЧАЕТ ВАШИМ ПОТРЕБНОСТЯМ ИЛИ ОЖИДАНИЯМ.КОМПАНИЯ ОТКАЗЫВАЕТСЯ ОТ ВСЕХ ГАРАНТИЙ, ЯВНЫХ ИЛИ ПОДРАЗУМЕВАЕМЫХ, ВКЛЮЧАЯ ЛЮБЫЕ ГАРАНТИИ КОММЕРЧЕСКОЙ ЦЕННОСТИ, ПРИГОДНОСТИ ДЛЯ ОПРЕДЕЛЕННОЙ ЦЕЛИ И НЕ НАРУШЕНИЯ.
КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ДАЕТ НИКАКИХ ГАРАНТИЙ ИЛИ ЗАЯВЛЕНИЙ В ОТНОШЕНИИ КАЧЕСТВА, ТОЧНОСТИ ИЛИ ДОСТУПНОСТИ ВЕБ-САЙТА. В частности, НО БЕЗ ОГРАНИЧЕНИЯ ВЫШЕИЗЛОЖЕННОГО, НИ КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ГАРАНТИРУЕТ ИЛИ ЗАЯВЛЯЕТ, ЧТО ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА ИЛИ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА САЙТЕ ИЛИ С ПОМОЩЬЮ САЙТА, БУДУТ ТОЧНЫМИ, НАДЕЖНЫМИ ИЛИ БЕСПЛАТНЫМИ ИЛИ БЕСПЛАТНЫМИ ЧТО ДЕФЕКТЫ БУДУТ ИСПРАВЛЕНЫ; ЧТО ВЕБ-САЙТ ИЛИ СЕРВЕР, КОТОРЫЙ ДЕЛАЕТ ЕГО ДОСТУПНЫМ, НЕ СОДЕРЖИТ ВИРУСОВ ИЛИ ДРУГИХ ВРЕДНЫХ КОМПОНЕНТОВ; ИЛИ ЧТО ВЕБ-САЙТ ИНАЧЕ ОТВЕЧАЕТ ВАШИМ ПОТРЕБНОСТЯМ ИЛИ ОЖИДАНИЯМ.КОМПАНИЯ ОТКАЗЫВАЕТСЯ ОТ ВСЕХ ГАРАНТИЙ, ЯВНЫХ ИЛИ ПОДРАЗУМЕВАЕМЫХ, ВКЛЮЧАЯ ЛЮБЫЕ ГАРАНТИИ КОММЕРЧЕСКОЙ ЦЕННОСТИ, ПРИГОДНОСТИ ДЛЯ ОПРЕДЕЛЕННОЙ ЦЕЛИ И НЕ НАРУШЕНИЯ.
НИ ПРИ КАКИХ ОБСТОЯТЕЛЬСТВАХ КОМПАНИЯ ИЛИ ЕЕ ЛИЦЕНЗИАРЫ ИЛИ ПОДРЯДЧИКИ НЕ НЕСЕТ ОТВЕТСТВЕННОСТИ ЗА ЛЮБЫЕ УБЫТКИ ЛЮБОГО РОДА, ПРИ КАКИХ-ЛИБО ЮРИДИЧЕСКИХ ТЕОРИЯХ, ВЫЗВАННЫЕ ИЛИ В СВЯЗИ С ИСПОЛЬЗОВАНИЕМ ВАМИ ИЛИ НЕВОЗМОЖНОСТЬЮ ИСПОЛЬЗОВАТЬ ВЕБ-САЙТ, СОДЕРЖИМОЕ САЙТА, ЛЮБЫЕ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА САЙТЕ ИЛИ ЧЕРЕЗ ВЕБ-САЙТ ИЛИ ЛЮБОЙ САЙТ, ВКЛЮЧАЮЩИЙ ПРЯМЫЕ, КОСВЕННЫЕ, СЛУЧАЙНЫЕ, СПЕЦИАЛЬНЫЕ, КОСВЕННЫЕ ИЛИ КАРАТНЫЕ УБЫТКИ, ВКЛЮЧАЯ, НО НЕ ОГРАНИЧИВАЯСЯ, ЛИЧНЫЕ ТРАВМЫ, ПОТЕРЯ ФАКТОВ ИЛИ УБЫТКОВ , ВИРУСЫ, УДАЛЕНИЕ ФАЙЛОВ ИЛИ ЭЛЕКТРОННЫХ СООБЩЕНИЙ, ИЛИ ОШИБКИ, УПУЩЕНИЯ ИЛИ ДРУГИЕ НЕТОЧНОСТИ НА ВЕБ-САЙТЕ ИЛИ СОДЕРЖАНИИ САЙТА ИЛИ УСЛУГАХ, ИЛИ ИЛИ НЕ ИСПОЛЬЗУЕТСЯ КОМПАНИЯ, И ПРЕДОСТАВЛЯЛА ЛИ КОМПАНИЯ ВОЗМОЖНОСТЬ ЛЮБЫЕ ТАКИЕ УБЫТКИ, ЕСЛИ НЕ ЗАПРЕЩЕНЫ ПРИМЕНИМЫМ ЗАКОНОДАТЕЛЬСТВОМ.
Компенсация
Вы соглашаетесь возместить и обезопасить Компанию и ее должностных лиц, директоров, агентов, сотрудников и других лиц, участвующих в работе Веб-сайта, от любых обязательств, расходов, убытков и издержек, включая разумные гонорары адвокатам, возникающих в результате любое нарушение вами настоящих Условий использования, использование вами Веб-сайта или любых продуктов, услуг или информации, полученных с Веб-сайта или через него, ваше подключение к Веб-сайту, любой контент, который вы отправляете на Веб-сайт через любые Функция сообщества или нарушение вами каких-либо прав другого лица.
Применимое право; Международное использование
Настоящие условия регулируются и толкуются в соответствии с законами штата Пенсильвания без учета каких-либо принципов коллизионного права. Вы соглашаетесь с тем, что любые судебные иски или иски, вытекающие из настоящих Условий использования или связанные с ними, будут подаваться исключительно в суды штата или федеральные суды, расположенные в Пенсильвании, и вы тем самым соглашаетесь и подчиняетесь личной юрисдикции таких судов для цели судебного разбирательства по любому подобному действию.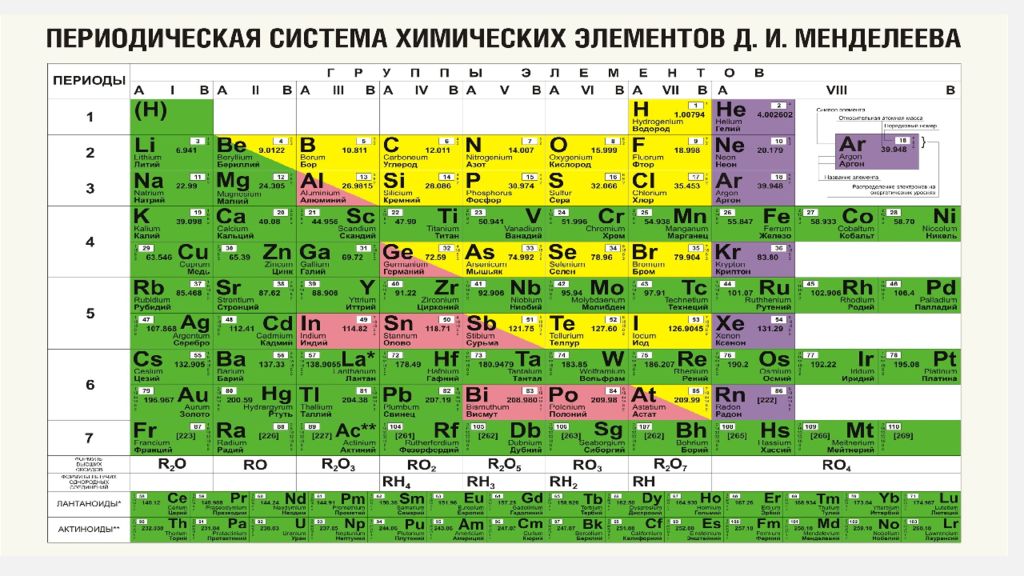
Настоящие Условия использования применимы к пользователям в США, Канаде и Пуэрто-Рико. Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Если вы решите получить доступ к этому веб-сайту из-за пределов указанных юрисдикций, а не использовать доступные международные сайты, вы соглашаетесь с настоящими Условиями использования и тем, что такие условия будут регулироваться и толковаться в соответствии с законами США и штата. Пенсильвании и что мы не делаем никаких заявлений о том, что материалы или услуги на этом веб-сайте подходят или доступны для использования в этих других юрисдикциях.В любом случае все пользователи несут ответственность за соблюдение местных законов.
Общие условия
Настоящие Условия использования, в которые время от времени могут вноситься поправки, представляют собой полное соглашение и понимание между вами и нами, регулирующее использование вами Веб-сайта. Наша неспособность реализовать или обеспечить соблюдение какого-либо права или положения Условий использования не означает отказ от такого права или положения. Если какое-либо положение Условий использования будет признано судом компетентной юрисдикции недействительным, вы, тем не менее, соглашаетесь с тем, что суд должен попытаться реализовать намерения сторон, отраженные в этом положении и других положениях Положения и условия использования остаются в полной силе.Ни ваши деловые отношения, ни поведение между вами и Компанией, ни какая-либо торговая практика не может считаться изменением настоящих Условий использования. Вы соглашаетесь с тем, что независимо от какого-либо закона или закона об обратном, любые претензии или основания для иска, возникающие из или связанные с использованием Сайта или Условий использования, должны быть поданы в течение одного (1) года после такой претензии или причины. иска возникла или будет навсегда запрещена. Любые права, прямо не предоставленные в настоящем документе, сохраняются за Компанией.
Наша неспособность реализовать или обеспечить соблюдение какого-либо права или положения Условий использования не означает отказ от такого права или положения. Если какое-либо положение Условий использования будет признано судом компетентной юрисдикции недействительным, вы, тем не менее, соглашаетесь с тем, что суд должен попытаться реализовать намерения сторон, отраженные в этом положении и других положениях Положения и условия использования остаются в полной силе.Ни ваши деловые отношения, ни поведение между вами и Компанией, ни какая-либо торговая практика не может считаться изменением настоящих Условий использования. Вы соглашаетесь с тем, что независимо от какого-либо закона или закона об обратном, любые претензии или основания для иска, возникающие из или связанные с использованием Сайта или Условий использования, должны быть поданы в течение одного (1) года после такой претензии или причины. иска возникла или будет навсегда запрещена. Любые права, прямо не предоставленные в настоящем документе, сохраняются за Компанией. Мы можем прекратить ваш доступ или приостановить доступ любого пользователя ко всему сайту или его части без предварительного уведомления за любое поведение, которое мы, по нашему собственному усмотрению, считаем нарушением любого применимого законодательства или наносящим ущерб интересам другого пользователя. , стороннего поставщика, поставщика услуг или нас. Любые вопросы, касающиеся настоящих Условий использования, следует направлять по адресу [email protected].
Мы можем прекратить ваш доступ или приостановить доступ любого пользователя ко всему сайту или его части без предварительного уведомления за любое поведение, которое мы, по нашему собственному усмотрению, считаем нарушением любого применимого законодательства или наносящим ущерб интересам другого пользователя. , стороннего поставщика, поставщика услуг или нас. Любые вопросы, касающиеся настоящих Условий использования, следует направлять по адресу [email protected].
Жалобы на нарушение авторских прав
Мы уважаем чужую интеллектуальную собственность и просим наших пользователей поступать так же.Если вы считаете, что ваша работа была скопирована и доступна на Сайте способом, который представляет собой нарушение авторских прав, вы можете уведомить нас, предоставив нашему агенту по авторским правам следующую информацию:
электронная или физическая подпись лица, уполномоченного действовать от имени правообладателя;
описание работы, защищенной авторским правом, в отношении которой были нарушены ваши претензии;
идентификация URL-адреса или другого конкретного места на Сайте, где находится материал, который, по вашему мнению, нарушает авторские права;
ваш адрес, номер телефона и адрес электронной почты;
ваше заявление о том, что вы добросовестно полагаете, что спорное использование не разрешено владельцем авторских прав, его агентом или законом; и
ваше заявление, сделанное под страхом наказания за лжесвидетельство, о том, что приведенная выше информация в вашем уведомлении является точной и что вы являетесь владельцем авторских прав или уполномочены действовать от имени владельца авторских прав.

С нашим агентом для уведомления о жалобах на нарушение авторских прав на Сайте можно связаться по адресу: [email protected].
Урок в девятом классе Цветовое кодирование периодической таблицы
Учащиеся сразу же ощетиниваются и спрашивают: «Как мне узнать, где находятся щелочные металлы?» Я обычно использую легкий сарказм, отсылая их к инструкциям по использованию компьютера (или мобильного устройства, если они предпочитают). Студенты могут быть очень сбиты с толку из-за того, что нет прямого веб-сайта, на который можно было бы перейти, и кажутся очень неуверенными в том, что делать дальше.
Я прошу сбитых с толку студентов выделить слова в каждой строке инструкций, которые они не знают. Как только они это сделают, я показываю им, как они только что определили, что они будут искать, и направляю их в поисковую систему по их выбору. Я предупреждаю их, что информация в их периодической таблице может быть более актуальной, чем на многих веб-сайтах, поэтому им следует расширять любые закономерности, которые они замечают.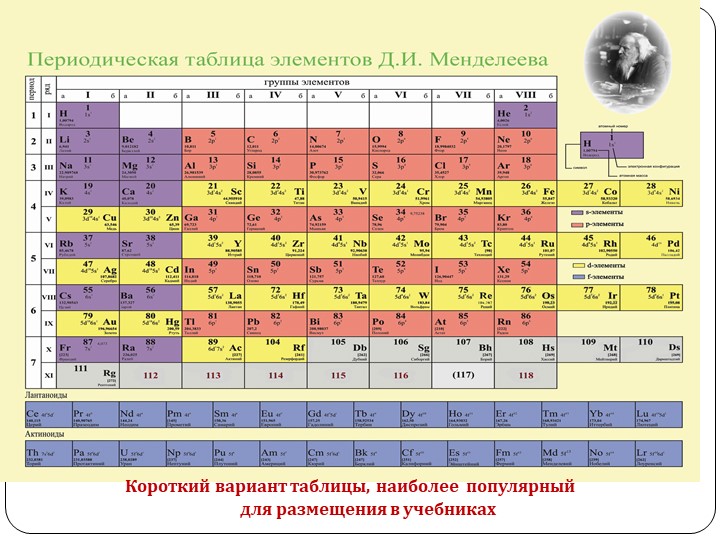
Последняя часть, которую я подчеркиваю каждой группе, – это сделать хороший ключ. Многие студенты просто копируют образец ключа, что для них мало что дает.Студенты, которые изначально делают хороший ключ, имеют огромное преимущество. Обычно это выравнивается в течение следующей недели, так как учащиеся понимают, что им нужен ключ получше, и возвращаются, пересматривают и улучшают свои собственные.
Перед тем, как уйти, студенты сдают цветные таблицы Менделеева, чтобы я мог оценить их, используя контрольный список на странице инструкций, и вернуть их на следующий день.
Хотя это задание может показаться пустым занятием, оно очень помогает моим ученикам с визуальным восприятием. Студенты могли использовать периодическую таблицу в младших классах средней школы или нет, и это служит для них ориентиром.Он также служит источником ресурсов при выполнении нашей деятельности в будущем. Мы не обязываем студентов запоминать названия групп или различать элементы основной группы и переходные металлы. Тем не менее, многие из наших действий могут по-прежнему использовать эти ярлыки.
Тем не менее, многие из наших действий могут по-прежнему использовать эти ярлыки.
Студенты могут ориентироваться в этих занятиях с помощью хорошо обозначенной таблицы с цветовой кодировкой. Это уменьшает мою потребность вычеркивать все имена из уже существовавших ранее занятий и предоставляет безопасный ресурс для укрепления уверенности, когда учащиеся знакомятся с периодической таблицей.
Какое значение имеет цвет в Периодической таблице?
Что такое металл? – Урок для детей
Если что-то блестящее и привлекло ваше внимание, скорее всего, оно было металлическим! В этом уроке вы узнаете о различных типах металлов и их особых характеристиках.
Атомный радиус: определение, формула и пример
Атомный радиус – это просто половина диаметра самого атома, но это не так интуитивно понятно, как может показаться, поскольку увеличение атомной массы не всегда соответствует большему радиусу или размеру.Изучите эти нюансы, научившись вычислять формулу атомных радиусов.
Реакции кислот: металлов, карбонатов и гидроксидов
Когда вы думаете о химии, вам, вероятно, приходит на ум смешивание разных вещей. В этом уроке будет обсуждаться, что происходит, когда кислоты смешиваются с металлами, карбонатами и гидроксидами, и приведены сбалансированные уравнения и уравнения ионов для протекающих реакций.
В этом уроке будет обсуждаться, что происходит, когда кислоты смешиваются с металлами, карбонатами и гидроксидами, и приведены сбалансированные уравнения и уравнения ионов для протекающих реакций.
Атмосфера Земли: компоненты и структура
Атмосфера Земли состоит из газовой смеси, окружающей планету.Изучите компоненты и структуру атмосферы Земли и откройте для себя ее слои, включая тропосферу, стратосферу, мезосферу, термосферу и экзосферу.
Химический символ: определение и примеры
Химический символ – это упрощенное письменное представление элемента, использующее одну или две буквы для единообразия.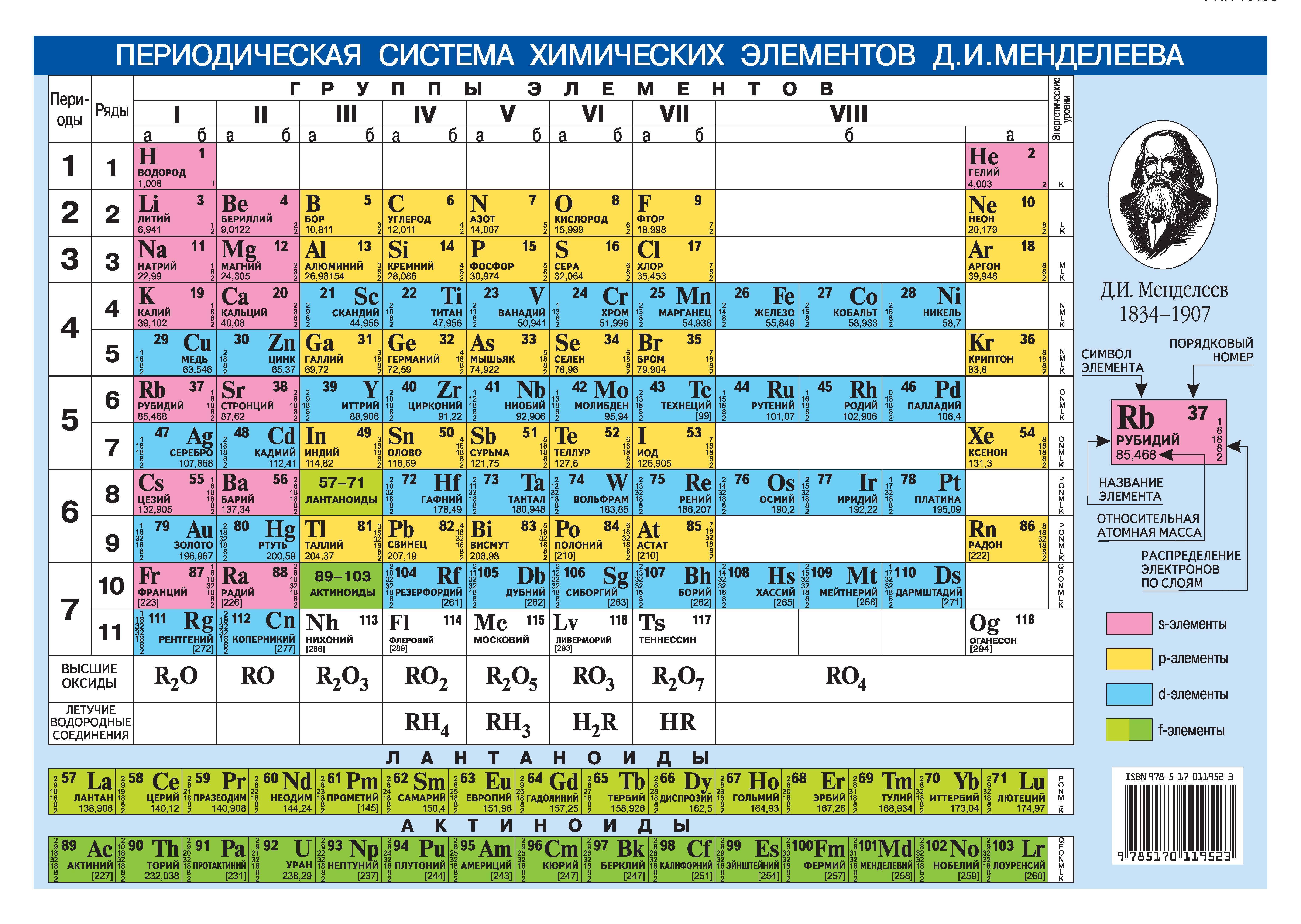 Узнайте происхождение этих символов и примеры того, как они используются химиками в дополнение к таблице Менделеева.
Узнайте происхождение этих символов и примеры того, как они используются химиками в дополнение к таблице Менделеева.
Реакции металлов: разбавленные кислоты, вода и кислород
Есть несколько категорий металлов.Некоторые из них очень реактивны, а некоторые вообще не очень реактивны. В этом уроке мы рассмотрим различные металлы и то, как они реагируют с кислотами, водой и кислородом.
Раскрасьте и узнайте о периодической таблице
Это исследование для детей от 10 лет, как показывают цветные смайлы. Узнать о периодической таблице элементов можно с детьми с 5 по 12 класс!
Узнать о периодической таблице элементов можно с детьми с 5 по 12 класс!
Урок «Периодическая таблица элементов» – это химическое исследование, посвященное элементам из разделов Уровни обучения 1–13.В Layers of Learning есть практические эксперименты в каждом разделе этой семейной учебной программы. Узнайте больше о слоях обучения.
Периодическая таблица элементов – это визуальный способ организации элементов Вселенной, который разработали химики. С помощью этого метода элементы группируются рядом с другими похожими элементами. По мере разработки таблицы Менделеева появилось много неоткрытых элементов, присутствие которых было предсказано на основе пустого места в таблице. Таблица Менделеева – одно из свидетельств того, что Вселенная упорядочена и предсказуема.
Шаг 1. Библиотечные исследования
Перед тем, как начать исследование, прочтите пару книг о периодической таблице элементов. Вот несколько советов, но если вы не можете их найти, поищите в своей библиотеке книги о движении, физике, гравитации и трении. Цветные смайлы над каждой книгой подскажут, для какого возраста они рекомендованы.
Вот несколько советов, но если вы не можете их найти, поищите в своей библиотеке книги о движении, физике, гравитации и трении. Цветные смайлы над каждой книгой подскажут, для какого возраста они рекомендованы.
Как аффилированные лица Amazon, рекомендуемые книги и продукты ниже возвращают нам крошечный процент от вашей покупки.Это не влияет на ваши расходы и помогает нам управлять нашим веб-сайтом. Мы благодарим Вас!
Шаг 2: Исследование периодической таблицы
Вам понадобятся печатные и цветные карандаши, цветные карандаши, цветные ручки или краски для таблицы Менделеева.
Нажмите на это изображение, чтобы получить периодическую таблицу элементов для печати.Начните с раскраски семейств элементов, как показано в примере ниже. Семейства – это элементы со схожими свойствами. Они ведут себя одинаково физически и химически.
Прочтите о наборах элементов в книгах, которые вы получили из библиотеки.Некоторые правила Периодической таблицы
Далее выучите некоторые правила таблицы Менделеева.
Периоды проходят горизонтально по таблице строками, а атомный номер увеличивается на единицу при перемещении слева направо. Атомный номер – это количество протонов в атоме. Атомный номер – это большое число в верхней части поля для определенного элемента.
Группы располагаются вертикально вниз по таблице, и все элементы в определенной группе имеют одинаковое количество электронов во внешней оболочке, поэтому они ведут себя одинаково.Первая группа, щелочные металлы, имеет один электрон на внешней оболочке. Во второй группе их двое. Затем мы пропускаем выпадающий раздел и переходим к группе, которая начинается с Boron. Группа бора состоит из трех электронов и так далее, вплоть до благородных газов, которые имеют восемь электронов во внешней оболочке.
Буквы в каждой ячейке являются символом химического вещества. Обозначение углерода – C, свинца – Pb, происходящее от латинского слова “свинец” – свинец.
Число в нижней части прямоугольника элемента – это атомный вес или общий вес протонов, нейтронов и электронов этого элемента.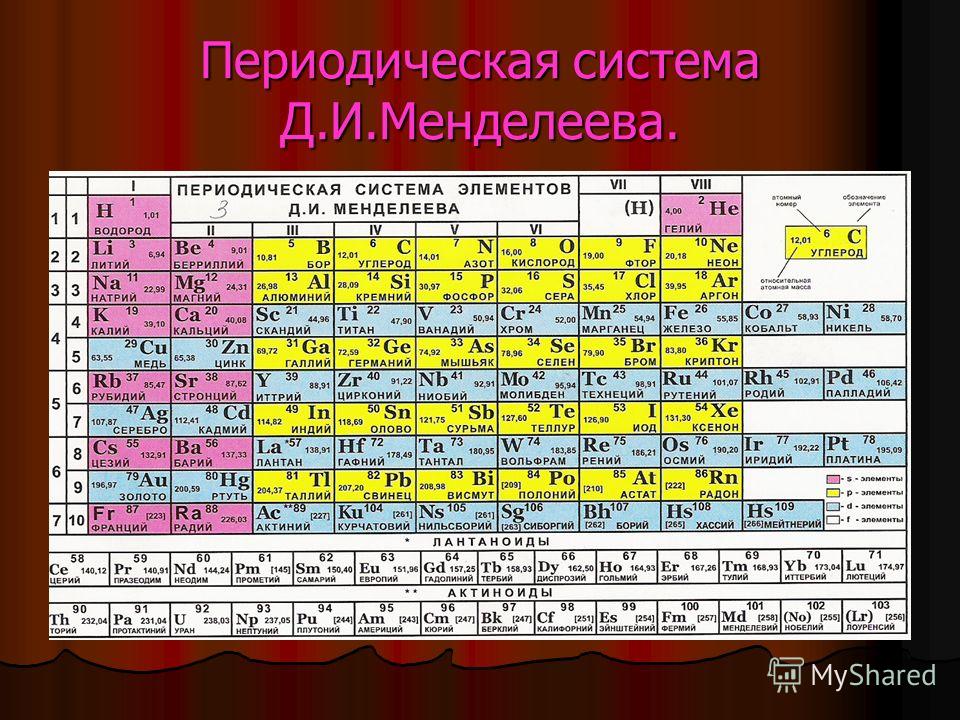 Водород, который имеет один протон и один электрон, имеет вес 1. (Вес электронов по сравнению с протонами и нейтронами незначителен и не учитывается.)
Водород, который имеет один протон и один электрон, имеет вес 1. (Вес электронов по сравнению с протонами и нейтронами незначителен и не учитывается.)
Изучая периодическую таблицу Менделеева, вы также можете играть в эту интерактивную игру «Построить атом», чтобы попрактиковаться в построении атомов на основе элементов в периодической таблице.
Шаг 3. Покажите, что вы знаете
После того, как вы объяснили основные правила таблицы Менделеева, задайте вопросы детям, которые награждают их за хорошую успеваемость.
- К какому семейству принадлежит ксенон (Xe)?
- Какой химический символ у золота?
- Сколько электронов находится во внешней оболочке бора (B)?
- Назовите элемент в той же группе, что и Углерод.
- Какой элемент имеет химический символ Na?
- Сколько электронов находится во внешней оболочке галогенных газов?
Вы уловили идею. Это упражнение не предназначено для того, чтобы помочь детям запомнить периодическую таблицу Менделеева, а скорее для того, чтобы узнать, что означают символы и как их интерпретировать, чтобы они могли ссылаться на таблицу, когда им понадобится информация позже.
Дополнительные слои
дополнительных слоев – это дополнительные действия, которые вы можете выполнять, или касательные, которые вы можете использовать. Вы найдете их на боковых панелях каждого модуля Layers of Learning. Они не являются обязательными, поэтому просто выберите то, что вас интересует.
Дополнительный слой
Люди предложили множество альтернативных способов организации таблицы Менделеева. Вот одна идея.
Узнайте больше об альтернативных предложенных таблицах Менделеева.
В Интернете
В каталоге Layers of Learning для каждого раздела есть список веб-сайтов для дальнейшего изучения тем.
Чтобы узнать больше о периодической таблице элементов, посетите https://www.ptable.com/, где вы можете щелкнуть элементы, чтобы узнать больше о них один за другим.
Знаменитые люди
Русский химик и изобретатель Дмитрий Менделеев создал первую таблицу Менделеева в том виде, в котором мы ее знаем сегодня.
Он даже предсказал существование элементов, которые еще не были обнаружены.
Начните домашнее обучение в семейном стиле прямо сейчас с помощью бесплатного модуля Layers of Learning при подписке.Храните устройство навсегда, без вопросов.
Мы очень рады, что вы присоединились к семье Layers of Learning.
Проверьте свою электронную почту, чтобы получить инструкции по загрузке бесплатного устройства. Письмо должно прийти в течение 15 минут.
Что-то пошло не так. Пожалуйста, проверьте свои записи и попробуйте еще раз.
% PDF-1.7 % 7 0 объект > / Метаданные 4 0 R / Страницы 3 0 R / Тип / Каталог / PageLabels 1 0 R >> эндобдж 4 0 объект > поток PScript5.dll Версия 5.22011-05-28T14: 55: 46-06: 002011-05-28T14: 54: 51-06: 002011-05-28T14: 55: 46-06: 00application / pdf
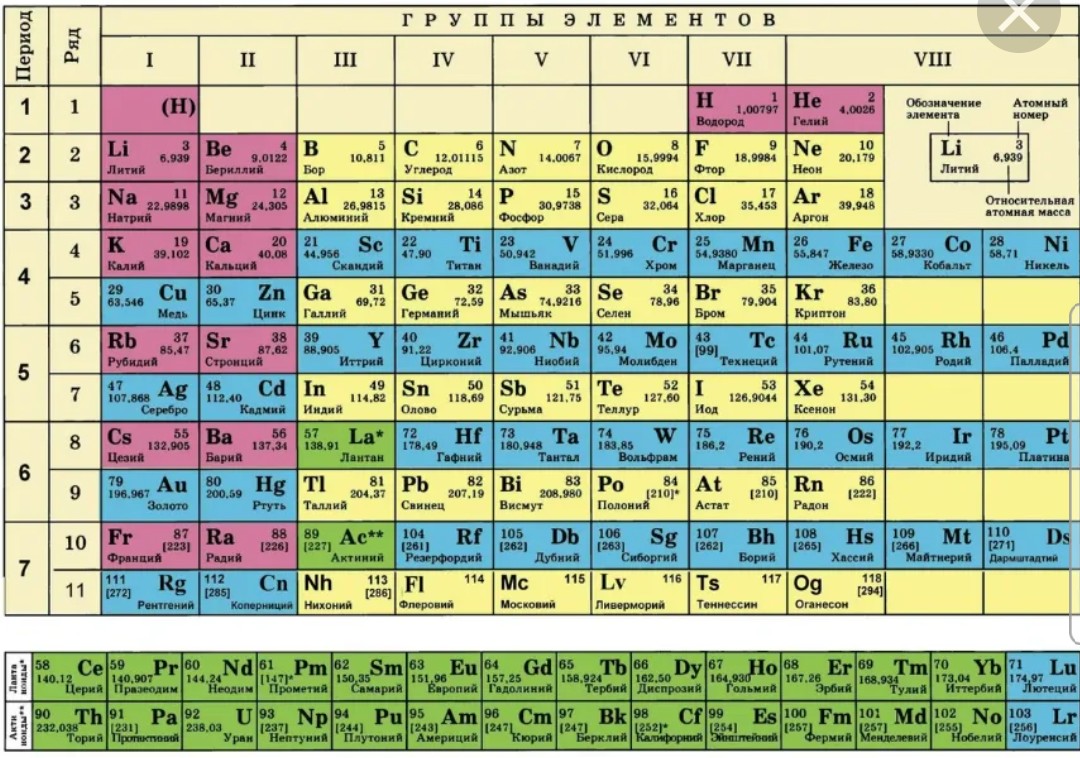 vertex42.com/mlPpersonalruse.EUL конечный поток
эндобдж
3 0 obj
>
эндобдж
1 0 объект
>
эндобдж
2 0 obj
>
эндобдж
8 0 объект
>
эндобдж
9 0 объект
> / ColorSpace> / Font> / ProcSet [/ PDF / Text / ImageC / ImageI] / ExtGState >>>
эндобдж
55 0 объект
>
эндобдж
21 0 объект
>
эндобдж
10 0 объект
>
эндобдж
11 0 объект
>
эндобдж
12 0 объект
>
эндобдж
16 0 объект
>
эндобдж
22 0 объект
>
эндобдж
23 0 объект
>
эндобдж
54 0 объект
> поток
hTP = o [u.
vertex42.com/mlPpersonalruse.EUL конечный поток
эндобдж
3 0 obj
>
эндобдж
1 0 объект
>
эндобдж
2 0 obj
>
эндобдж
8 0 объект
>
эндобдж
9 0 объект
> / ColorSpace> / Font> / ProcSet [/ PDF / Text / ImageC / ImageI] / ExtGState >>>
эндобдж
55 0 объект
>
эндобдж
21 0 объект
>
эндобдж
10 0 объект
>
эндобдж
11 0 объект
>
эндобдж
12 0 объект
>
эндобдж
16 0 объект
>
эндобдж
22 0 объект
>
эндобдж
23 0 объект
>
эндобдж
54 0 объект
> поток
hTP = o [u.
