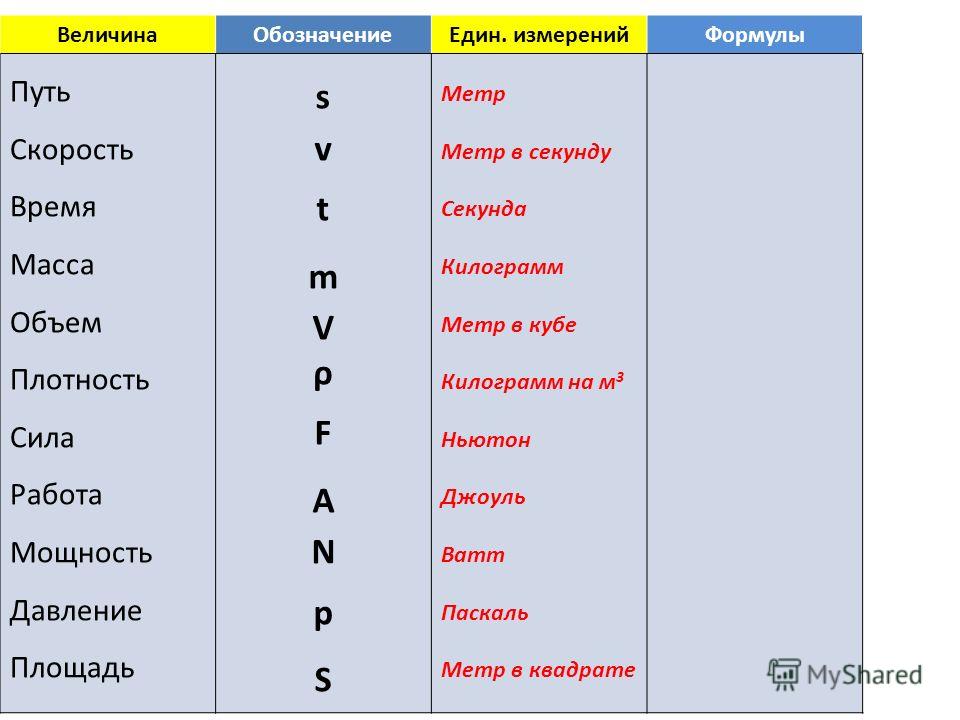
Объем, масса, плотность, удельный объем. Приведение к нормальным и стандартным условиям и пересчет
Главная / Справочник / Приложения / Единицы физических величин, физико-химические понятия, соотношения, состав и характеристики газов / Объем, масса, плотность, удельный объем. Приведение к нормальным и стандартным условиям и пересчет
Приведение к нормальным и стандартным условиям
Единицей измерения объема газа является кубический метр (м³). Измеренный объем приводится к нормальным физическим условиям.
Нормальные физические условия: давление 101 325 Па, температура 273,16 К (0 °С).
Стандартные условия: давление 101 325 Па, температура 293,16 К (+20 °С).
В настоящее время эти обозначения выходят из употребления. Поэтому в дальнейшем следует указывать те условия, к которым относятся объемы и другие параметры газа. Если эти условия не указываются, то это значит, что параметры газа даны при 0 °С (273,16 °К) и 760 мм рт. ст. (1,033 кгс/см²). Иногда объем газа (особенно в иностранной литературе и нормах) при пользовании системой СИ приводится к 288,16 °К (+15 °С) и давлению 1 бар (105 Па).
ст. (1,033 кгс/см²). Иногда объем газа (особенно в иностранной литературе и нормах) при пользовании системой СИ приводится к 288,16 °К (+15 °С) и давлению 1 бар (105 Па).
Если известен объем газа при одних условиях, то пересчитать его в объемы при других условиях можно с помощью коэффициентов, приведенных следующей таблице.
Коэффициенты для пересчета объемов газа из одних условий в другие
| Температура и даление газа | 0 °С и 760 мм рт. ст. | 15 °С и 760 мм рт. ст. | 20 °С и 760 мм рт. ст. | 15 °С (288,16 °К) и 1 бар |
| 0 °С и 760 мм рт. ст. (норм. условия) | 1 | 1,055 | 1,073 | 1,069 |
| 15 °С и 760 мм рт. ст. (в зар. литературе) | 0,948 | 1,019 | 1,013 | |
| 20 °С и 760 мм рт. ст. (ст. условия) | 0,932 | 0,983 | 1 | 0,966 |
| 15 °С (288,16 °К) и 1 бар (СИ) | 0,936 | 0,987 | 1,003 | 1 |
Для приведения объемов газа к 0 °С (273,16 °К) и 760 мм рт. ст. (1,033 кгс/см²), а также к 20 °С (293,16 °К) и 760 мм рт. ст. (1,033 кгс/см²) могут быть применены следующие формулы:
ст. (1,033 кгс/см²), а также к 20 °С (293,16 °К) и 760 мм рт. ст. (1,033 кгс/см²) могут быть применены следующие формулы:
где V0 °С и 760 мм рт. ст. — объем газа при 0 °С и 760 мм рт. ст., м³;
VP — объем газа в рабочих условиях, м³;
р — абсолютное давление газа в рабочих условиях, мм рт. ст.;
Т — абсолютная температура газа в рабочих условиях, °К.
Пересчет объемов газа, приведенных к 0 °С и 760 мм рт. ст., а также к 20 °С и 760 мм рт. ст., в объемы при других (рабочих) условиях можно производить по формулам:
Любой газ способен расширяться. Следовательно, знание объема, который занимает газ, недостаточно для определения его массы, так как в любом объеме, целиком заполненном газом, его масса может быть различной.
Масса — это мера вещества какого-либо тела (жидкости, газа) в состоянии покоя; скалярная величина, характеризующая инерционные и гравитационные свойства тела.
Плотность, или масса единицы объема, обозначаемая буквой p, — это отношение массы тела m, кг, к его объему, V, м³:
p = m/V
или с учетом химической формулы газа:
p = M/VМ = M/22,4,
где M — молекулярная масса,
VМ — молярный объем.
Единица плотности в СИ — килограмм на кубический метр (кг/м³).
Зная состав газовой смеси и плотность ее компонентов, определяем по правилу смешения среднюю плотность смеси:
pсм = (p1V1 + p2V2 + … + pnVn)/100,
где p1, p2, …, pn — плотность компонентов газового топлива, кг/м³;
V1, V2, …, Vn — содержание компонента, об. %.
%.
Величину, обратную плотности, называют удельным, или массовым, объемом (ν) и измеряют в кубических метрах на килограмм (м³/кг).
Как правило, на практике, чтобы показать, на сколько 1 м³ газа легче или тяжелее 1 м³ воздуха, используют понятие относительная плотность d, которая представляет собой отношение плотности газа к плотности воздуха:
d = p/1,293
и
d = M/(22,4×1,293).
Азот (Nitrogene, N) – Актуальные публикации на сайте компании «НИИ КМ»
Азот — химический элемент, который известен каждому. Его обозначают буквой N. Он, можно сказать, основа неорганической химии, и поэтому его начинают изучать еще в восьмом классе. В этой статье мы подробно рассмотрим азот, а также его характеристики и свойства.
История открытия элемента
Такие соединения, как аммиак, селитра, азотная кислота, были известны и применялись на практике задолго до получения чистого азота в свободном состоянии.
Во время эксперимента, проведенного в 1772 году, Даниель Резерфорд сжигал фосфор и прочие вещества в колоколе из стекла. Он выяснил, что газ, остающийся после сгорания соединений, не поддерживает горения и дыхания, и назвал его «удушливым воздухом».
В 1787 году Антуан Лавуазье установил, что газы, входящие в состав обычного воздуха, — это простые химические элементы, и предложил название «Азот». Чуть позже (в 1784 г.) физик Генри Кавендиш доказал, что это вещество входит в состав селитры (группы нитратов). Отсюда происходит латинское название азота (от позднелатинского nitrum и греческого gennao), предложенное Ж. А. Шапталем в 1790 году.
К началу XIX века учеными были выяснены химическая инертность элемента в свободном состоянии и его исключительная роль в соединениях с другими веществами. С этого момента «связывание» азота воздуха стало важнейшей технической проблемой химии.
Физические свойства
Азот немного легче воздуха. Его плотность составляет 1,2506 кг/м³ (0 °С, 760 мм рт. ст.), температура плавления — -209,86 °С, кипения — -195,8 °С. Азот с трудом сжижается. Его критическая температура относительно низка (-147,1 °С), при этом критическое давление довольно высоко — 3,39 Мн/м². Плотность в жидком состоянии — 808 кг/м³. В воде этот элемент менее растворим, чем кислород: в 1 м³ (при 0 °С) Н₂О может раствориться 23,3 г N. Этот показатель выше при работе с некоторыми углеводородами.
ст.), температура плавления — -209,86 °С, кипения — -195,8 °С. Азот с трудом сжижается. Его критическая температура относительно низка (-147,1 °С), при этом критическое давление довольно высоко — 3,39 Мн/м². Плотность в жидком состоянии — 808 кг/м³. В воде этот элемент менее растворим, чем кислород: в 1 м³ (при 0 °С) Н₂О может раствориться 23,3 г N. Этот показатель выше при работе с некоторыми углеводородами.
Химические свойства азота
При нагревании до невысоких температур этот элемент взаимодействует только с активными металлами. Например, с литием, кальцием, магнием. С большинством других веществ азот вступает в реакцию в присутствии катализаторов и/или при высокой температуре.
Хорошо изучены соединения N с О₂ (кислородом) N₂O₅, NO, N₂O₃, N₂O, NO₂. Из них при взаимодействии элементов (t — 4000 °С) образуется оксид NO. Далее в процессе охлаждения он окисляется до NO₂. Оксиды азота образуются в воздухе при прохождении атмосферных разрядов. Их можно получить действием ионизирующих излучений на смесь N с О₂.
При растворении в воде N₂O₃ и N₂O₅ соответственно получаются кислоты HNO₂ и HNO₂, образующие соли — нитраты и нитриты. Азот соединяется с водородом исключительно в присутствии катализаторов и при высокой температуре, образуя NH₃ (аммиак). Кроме того, известны и другие (они довольно многочисленны) соединения N с H₂, к примеру диимид HN = NH, гидразин H₂N-NH₂, октазон N₈H₁₄, кислота HN₃ и другие.
Стоит сказать, что большинство соединений водород + азот выделены исключительно в виде органических производных. Этот элемент не взаимодействует (непосредственно) с галогенами, поэтому все его галогениды получают только косвенным путем. К примеру, NF₃ образуется при взаимодействии аммиака с фтором.
Большинство галогенидов азота — малостойкие соединения, более устойчивы оксигалогениды: NOBr, NO₂F, NOF, NOCl, NO₂Cl. Непосредственного соединения N с серой также не происходит, N₄S₄ получается в процессе реакции аммиак + жидкая сера. Во время взаимодействия раскаленного кокса с N образуется циан (CN)₂. В процессе нагревания ацетилена С₂Н₂ с азотом до 1500 °С можно получить цианистый водород HCN. При взаимодействии N с металлами при относительно высоких температурах образуются нитриды (к примеру, Mg₃N₂).
В процессе нагревания ацетилена С₂Н₂ с азотом до 1500 °С можно получить цианистый водород HCN. При взаимодействии N с металлами при относительно высоких температурах образуются нитриды (к примеру, Mg₃N₂).
При воздействии на обычный азот электроразрядов [при давлении 130–270 н/м² (соответствует 1–2 мм рт. cт.)] и при разложении Mg₃N₂, BN, TiNx и Ca₃N₂, а также при электроразрядах в воздухе может быть образован активный азот, обладающий повышенным запасом энергии. Он, в отличие от молекулярного, весьма энергично взаимодействует с водородом, парами серы, кислородом, некоторыми металлами и фосфором.
Азот входит в состав довольно многих важнейших органических соединений, в том числе — аминокислот, аминов, нитросоединений и прочих.
Получение азота
В лаборатории этот элемент может быть легко получен в процессе нагревания концентрированного раствора нитрита аммония (формула: NH₄NO₂ = N₂ + 2H₂O). Технический метод получения N основан на разделении заранее сжиженного воздуха, который в дальнейшем подвергается разгонке.
Область применения
Основная часть получаемого свободного азота используется при промышленном производстве аммиака, который потом в довольно больших количествах перерабатывается на удобрения, взрывчатые вещества и т. п.
Кроме прямого синтеза NH₃ из элементов, применяется разработанный в начале прошлого века цианамидный метод. Он основан на том, что при t = 1000 °С карбид кальция (образованный накаливанием смеси угля и извести в электропечи) реагирует со свободным азотом (формула: СаС₂ + N₂ = CaCN₂ + С). Полученный цианамид кальция под действием разогретого водяного пара разлагается на CaCO₃ и 2NH₃.
В свободном виде данный элемент применяется во многих отраслях промышленности: в качестве инертной среды при разнообразных металлургических и химических процессах, при перекачке горючих жидкостей, для заполнения пространства в ртутных термометрах и т. д. В жидком состоянии он используется в различных холодильных установках. Его транспортируют и хранят в стальных сосудах Дьюара, а сжатый газ — в баллонах.
Широко применяют и многие соединения азота. Их производство стало усиленно развиваться после Первой мировой войны и на данный момент достигло поистине огромных масштабов.
Роль азота в биологии
Это вещество является одним из основных биогенных элементов и входит в состав важнейших элементов живых клеток — нуклеиновых кислот и белков. Однако количество азота в живых организмах невелико (примерно 1–3 % на сухую массу). Имеющийся в атмосфере молекулярный материал усваивают лишь сине-зеленые водоросли и некоторые микроорганизмы.
Довольно большие запасы этого вещества сосредоточены в почве в виде различных минеральных (нитраты, аммонийные соли) и органических соединений (в составе нуклеиновых кислот, белков и продуктов их распада, включая еще не полностью разложившиеся остатки флоры и фауны).
Растения отлично усваивают азот из грунта в виде органических и неорганических соединений. В природных условиях большое значение имеют особые почвенные микроорганизмы (аммонификаторы), которые способны минерализировать органический N почвы до солей аммония.
Нитратный азот грунта образуется в процессе жизнедеятельности нитрифицирующих бактерий, открытых С. Виноградским в 1890 году. Они окисляют аммонийные соли и аммиак до нитратов. Часть усвояемого флорой и фауной вещества теряется из-за воздействия денитрифицирующих бактерий.
Микроорганизмы и растения отлично усваивают как нитратный, так и аммонийный N. Они активно превращают неорганический материал в различные органические соединения — аминокислоты и амиды (глутамин и аспарагин). Последние входят в состав многих белков микроорганизмов, растений и животных. Синтез аспарагина и глутамина путем амидирования (ферментативного) аспарагиновой и глутаминовой кислот осуществляется многими представителями флоры и фауны.
Производство аминокислот происходит при помощи восстановительного аминирования ряда кетокислот и альдегидокислот, возникающих путем ферментативного переаминирования, а также в результате окисления различных углеводов. Конечными продуктами усвоения аммиака (NH₃) растениями и микроорганизмами являются белки, которые входят в состав ядра клеток, протоплазмы, а также откладываются в виде так называемых запасных белков.
Человек и большинство животных могут синтезировать аминокислоты лишь в довольно ограниченной мере. Они не способны производить восемь незаменимых соединений (лизин, валин, фенилаланин, триптофан, изолейцин, лейцин, метионин, треонин), и потому для них главным источником азота являются потребляемые с пищей белки, то есть, в конечном счете, — собственные белки микроорганизмов и растений.
9.12: Закон парциальных давлений Дальтона
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 49453
- Эд Витц, Джон В. Мур, Джастин Шорб, Ксавьер Прат-Ресина, Тим Вендорф и Адам Хан
- Цифровая библиотека химического образования (ChemEd DL)
Закон об идеальном газе также можно изменить, чтобы показать, что давление газа пропорционально количеству газа:
\[P=\frac{RT}{V}\,n\label{1} \]
Таким образом, коэффициент RT/V можно использовать для взаимного преобразования количества вещества и давления в контейнере определенного объема и температуры.
Уравнение \(\ref{1}\) также полезно при работе с ситуацией, когда два или более газа находятся в одном и том же контейнере (т. е. в одном и том же объеме). Предположим, например, что у нас имеется 0,010 моль газа в сосуде объемом 250 мл при температуре 32°С. Давление будет 9{-\text{1}}\,\times \text{ 305 K}}{\text{0}\text{.250 литров}}\,\times \text{ 0}\text{.006 моль}= \text{0}\text{0,60 атм} \номер\]
Теперь предположим, что мы поместили 0,004 моль H 2 и 0,006 моль N 2 в одну и ту же колбу вместе. Какое будет давление? Поскольку закон идеального газа не зависит от того, какой -й газ у нас есть, а только от количества -го любого -го газа, давление (0,004 + 0,006) моль, или 0,010 моль, будет именно таким, какое мы получили в нашем первом опыте. расчет. Но это всего лишь сумма давлений, которые H  То есть
То есть
\[P_{всего} = p_{\text{H}_{2}} + p_{\text{N}_{2}} \nonumber \]
Рисунок ниже демонстрирует понятие парциального давления в более конкретных терминах, показывая давление каждого газа отдельно в контейнере, а затем показывая комбинированное давление газов после их смешивания.
Рисунок \(\PageIndex{1}\): На приведенном выше рисунке показано, как работает закон Дальтона для парциального давления. Один только водород имеет давление 0,4 атм, а азот – 0,6 атм. При помещении в один и тот же контейнер общее давление составляет 1 атм, при этом каждый газ вносит свое парциальное давление. Кредиты изображения: Колледж OpenStax
Закон Дальтона для парциальных давлений чаще всего встречается, когда газ собирается путем вытеснения воды, как показано на рис. 2.9.0032 Рисунок \(\PageIndex{2}\): Общее давление влажного газа равно сумме парциального давления самого газа + давления паров воды при данной температуре. (При 20°С давление паров воды составляет 17,3 мм рт. ст.) Изображение тонкой узкой трубки, погруженной в воду и подведенной к дну измерительной трубки. Видны пузырьки, выходящие из горловины трубки.
Поскольку газ барботируется через воду, он содержит некоторое количество молекул воды и называется «влажным». Полное давление этого влажного газа представляет собой сумму парциального давления самого газа и парциального давления содержащегося в нем водяного пара. Последнее парциальное давление называется давление пара воды. Он зависит только от температуры эксперимента и может быть получен из справочника или из таблицы 1.
| Температура (°C) | Давление паров (мм рт.ст.) | Давление пара (кПа) |
|---|---|---|
| 0 | 4,6 | 0,61 |
| 5 | 6,5 | 0,87 |
| 10 | 9,2 | 1,23 |
| 15 | 12,8 | 1,71 |
| 20 | 17,5 | 2,33 |
| 25 | 23,8 | 3,17 |
| 30 | 31,8 | 4,24 |
| 50 | 92,5 | 12. 33 33 |
| 70 | 233,7 | 31.16 |
| 75 | 289,1 | 38,63 |
| 80 | 355.1 | 47,34 |
| 85 | 433,6 | 57,81 |
| 90 | 525,8 | 70.10 |
| 95 | 633,9 | 84,51 |
| 100 | 760,0 | 101,32 |
Пример \(\PageIndex{1}\): Объем водорода
Предположим, что 0,321 г металлического цинка реагируют с избытком соляной кислоты (водный раствор газообразного HCl) в соответствии с уравнением
\[\text{Zn} (s) + 2 \text{HCL} (aq) \ rightarrow \text{Zn} \text{Cl}_{2} (водн. ) + \text{H}_{2} (g) \nonumber \]
) + \text{H}_{2} (g) \nonumber \]
Полученный газообразный водород собирают над водой при 25°C, в то время как барометрическое давление составляет 745,4 мм рт. Какой объем влажного водорода будет собран?
Раствор Из таблицы 1 находим, что при 25°С давление паров воды составляет 23,8 мм рт.ст. Соответственно
p H 2 = p всего – p H 2 O = 754 мм рт.ст. – 23,8 мм рт.ст. = 721,6 мм рт.ст.
Необходимо перевести в совместимые единицы измерения R :
\[p_{\text{H}_{\text{2}}}=\text{721}\text{0,6 мм рт. \frac{\text{1 атм}}{\text{760 мм рт.ст.}}=\text{0}\text{0,949 атм} \nonumber \]
Дорожная карта для этой проблемы:
\[m_{ \text{Zn}}\xrightarrow{M_{\text{Zn}}}n_{\text{Zn}}\xrightarrow{S\left( \text{H}_{\text{2}}\text{/ Zn} \right)}n_{\text{H}_{\text{2}}}\xrightarrow{RT/P}V_{\text{H}_{\text{2}}} \nonumber \]
Таким образом,
\[\begin{align}V_{\text{H}_{\text{2}}} & =\text{0}\text{0,321 г Zn}\times \,\frac{ \text{1 моль Zn}}{\text{65}\text{0,38 г Zn}}\,\times \,\frac{\text{1 моль H}_{\text{2}}}{\ text{2 моль Zn}}\,\times \,\frac{\text{0}\text{0,0820 л атм}}{\text{1 К моль H}_{\text{2}}}\, \times \,\frac{\text{293}\text{0,15 K}}{\text{0}\text{0,987 атм}}\\ & =\text{0}\text{0,126 литра}\ end{align} \nonumber \]
Эта страница под названием 9. 12: Закон Дальтона о парциальных давлениях распространяется под лицензией CC BY-NC-SA 4.0, ее авторами, ремиксами и/или кураторами являются Эд Витц, Джон У. Мур, Джастин Шорб, Ксавье Прат-Ресина, Тим Вендорф и Адам Хан.
12: Закон Дальтона о парциальных давлениях распространяется под лицензией CC BY-NC-SA 4.0, ее авторами, ремиксами и/или кураторами являются Эд Витц, Джон У. Мур, Джастин Шорб, Ксавье Прат-Ресина, Тим Вендорф и Адам Хан.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Автор
- ХимПРАЙМ
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.
- Теги
- Дальтон
- Закон Дальтона о парциальном давлении
- парциальное давление
- давление пара
ChemTeam: четыре переменных газового закона
ChemTeam: Четыре переменных газового законаПеременные закона четырех газов:
объем, температура, давление и количество
Вернуться в меню KMT & Gas Laws
I. Том
Все газы должны быть помещены в контейнер, который при наличии отверстий можно закрыть без утечек. Трехмерное пространство, ограниченное стенками контейнера, называется объемом. Когда обсуждается обобщенная переменная объема, используется символ V.
Объем в химии обычно измеряется в литрах (символ = л) или миллилитрах (символ = мл). Литр также называют кубическим дециметром (дм 3 ).
Литр также называют кубическим дециметром (дм 3 ).
Существуют и другие единицы измерения объема, такие как кубические футы (куб. фут или фут 3 ) или кубические сантиметры (куб.см или см 3 ). Главное помнить: какие бы единицы объема не использовались, используйте их на протяжении всей задачи. Если вам необходимо преобразовать одну единицу измерения в другую, убедитесь, что вы делаете это правильно.
ChemTeam обсуждает различные газовые законы, в которых объем является переменной величиной. Наиболее распространенный способ визуализировать это — представить контейнер, участвующий в эксперименте, с подвижной стенкой. Когда громкость увеличивается, эта стена выдвигается. Когда объем уменьшается, стена скользит внутрь. Представьте, что уплотнение подвижной стенки идеально, так что газ не выходит.
Если объем постоянный, то контейнер сделан с жесткими стенками, которые не могут двигаться. В пределах любого обсуждаемого эксперимента стенки остаются неподвижными, а объем остается постоянным. Другими словами, стенки контейнера никогда не двигаются (и не ломаются) во время эксперимента.
Другими словами, стенки контейнера никогда не двигаются (и не ломаются) во время эксперимента.
II. Температура
Все газы имеют температуру, обычно измеряемую в градусах Цельсия (символ = °C). Обратите внимание, что Цельсий пишется с заглавной буквы, поскольку это имя человека (Андерс Цельсий). Когда обсуждается обобщенная переменная температуры, используется символ T.
Существует еще одна температурная шкала, которая очень важна для поведения газа. Она называется шкалой Кельвина (символ = К). Обратите внимание, что у K нет знака градуса, а Кельвин написан с большой буквы, потому что это был титул человека (лорд Кельвин, его имя было Уильям Томсон).
Все проблемы с газовым законом будут решаться с температурой Кельвина. Если бы вы использовали градусы Цельсия в любом из ваших расчетов, ВЫ БЫЛИ бы НЕПРАВЫ. Ваш учитель может попытаться сбить вас с толку в этом вопросе.
Вы можете конвертировать градусы Цельсия в кельвины следующим образом:
Кельвин = Цельсий + 273,15
Часто вместо 273,15 используется значение 273. Проконсультируйтесь с вашим учителем по этому вопросу. В большинстве примеров, выполненных ChemTeam, будет использоваться число 273. Например, 25 °C = 298 K, потому что 25 + 273 = 29.8.
Проконсультируйтесь с вашим учителем по этому вопросу. В большинстве примеров, выполненных ChemTeam, будет использоваться число 273. Например, 25 °C = 298 K, потому что 25 + 273 = 29.8.
Я буду использовать 273 K (ноль градусов Цельсия) в качестве стандартной температуры.
Температура газа по шкале Кельвина прямо пропорциональна его кинетической энергии. (Например, удвоив температуру по Кельвину, вы удвоите кинетическую энергию.) Время от времени эта взаимосвязь будет проявляться.
III. Давление
Давление газа создается молекулами газа, ударяющимися о стенки сосуда. Эта концепция очень важна для понимания поведения газа. Твердо держите это в уме. Эта идея о том, что молекулы газа ударяются о стену, будет часто использоваться. Когда обсуждается обобщенная переменная давления, используется символ P.
В химии используются три различные единицы измерения давления. Это неприятная ситуация, но мы не можем ее изменить. Вы должны уметь использовать все три в расчетах, а также уметь конвертировать одно в другое. Вот они:
Вот они:
- атмосферы (символ = атм)
- миллиметра ртутного столба (обозначение = мм рт. ст.)
- Паскали (обозначение = Па) или, чаще, килоПаскали (обозначение = кПа)
Более подробную информацию о преобразовании единиц давления можно найти здесь.
Стандартное давление определяется как 1000 атм, или 760,0 мм рт.ст., или 101,325 кПа.
Давайте остановимся на секунду. Убедитесь, что вы запомнили значения стандартного давления. Повторяю: советую запомнить приведенные выше стандартные значения!! Во многих задачах будет просто указано «стандартное давление», и вы уже должны знать его значение. Вот они снова:
Единица давления Стандартное значение атм 1.000 мм рт.ст. 760,0 кПа 101,325
Стандартная температура и давление — это очень распространенная фраза в химии, поэтому она была сокращена до STP.