Первый способ создания структурированной воды
Итак, готовим дома структурированную воду. Для этого можно использовать воду для кулера, которую можно купить или заказать. Чтобы не просто получить ее, а и понять, что и почему приходится выполнять, для начала нужно вспомнить кое-что из школьного курса.
Чуть-чуть из урока химии
Вы, конечно же, слышали слово «дейтерий». Напомним, что таким термином обозначают тяжелый водород. Он представляет собой изотоп водорода с атомной массой ядра равной 2. Изотоп – это разновидность атома, который в таблице Менделеева имеет такой же порядковый номер, но содержит более тяжелое ядро элемента. А вот обычный водород хоть и занимает такое же, 1 место в таблице химических элементов, но имеет атомную массу 1.
Отдельно нужно сказать, что благодаря дейтерию образуется так называемая тяжёлая вода, которая замерзает при температуре + 4 градуса и является самой вредной для всего живого. Дейтерий относится к тяжелым изомерам водорода.
Сверхлегкие же замерзают при -1 градусе. Но в школе мы учили, что вода переходит в твердое состояние при 0. Да, все правильно, именно последняя вода, которая нам нужна для нормального пополнения биожидкости.
Но в школе мы учили, что вода переходит в твердое состояние при 0. Да, все правильно, именно последняя вода, которая нам нужна для нормального пополнения биожидкости.
Как получить структурированную воду
Вообще-то говоря, существует два способа получения структурированной воды, которая абсолютно подходит для восполнения биожидкости, постоянно выходящей из организма.
Как из испорченных продуктов невозможно приготовить качественное блюдо, так и для создания структурированной воды подойдет только очищенная вода. Причем, чем лучше ее качество, тем совершеннее получится конечный продукт.
Для проведения таких процедур, можно заказать питьевую воду «КАНЬОН», которая по степени очистки и антибактериальным свойствам ничем не уступает глубинной артезианской воде, находящейся в недрах земли на глубине 100 м.
Для приготовления структурированной воды нельзя брать металлические ёмкости, поскольку ионы металла перейдут в воду. Стеклянная посуда тоже не подойдет – вода во время замерзания расширяется и может разорвать сосуд.
Поэтому очищенную воду нужно налить в эмалированную кастрюлю и поставить в морозильную камеру. Как только появится первый лед в виде кромки, его нужно немедленно удалить с помощью шумовки (с дырочками). Этот лед представляет собой тот самый дейтерий, о котором говорилось выше, т. е. представляет собой самую «вредную» воду для живого организма.
Кстати, время образования кромки зависит от температуры в камере и от объема кастрюли. Поэтому первые разы придется поэкспериментировать, чтобы в дальнейшем четко знать, когда удалять первый лед. На 1 л воды это может быть от 1 до 2 часов.
Итак, лед удалили, а вот воду придется перелить в другую кастрюлю, которую вновь загружаем в морозильник. После того, как вода в кастрюльке промерзнет приблизительно на 2/3 (что хорошо видно), в середине кастрюли останется незамерзшая вода.
Это и есть те самые сверхлегкие изомеры, о которых говорилось в начале. Поскольку они замерзают при температуре -1 градус, не мудрено, что вода в центре не замерзла. Так вот от этой жидкой водицы нужно также избавиться – ее просто слейте.
Так вот от этой жидкой водицы нужно также избавиться – ее просто слейте.
А оставшийся лед как раз и есть структурированная вода, которую Вы и хотели получить. Нужно сказать, что в среднем весь процесс займет 7-8 часов. В дальнейшем лед можно разморозить и употреблять в пищу и питье эту талую воду.
Без чего не создать структурированную воду
Только не забывайте, что для её создания потребуется хорошая вода, например можно использовать бутилированную воду. Ведь чистота исходной жидкости – очень важное условие для качественного продукта, получаемого после разморозки.
И еще помните, что все манипуляции с аква витой делайте с чистым сердцем и при хороших мыслях. Ведь воду многие считают живым существом. С этим можно спорить, но отрицать чудодейственную силу, которой наполняется водичка в кранах и в реках в Крещение, согласитесь, бессмысленно. Поэтому постарайтесь к процессу создания структурированной воды подходить благоговейно.
Но если у Вас нет времени возиться с моментом «ловли» ледовых кромок из дейтерия или незамерзших вод легких изотопов, тогда воспользуйтесь вторым способом приготовления структурированной воды.
Но об этом подробнее читайте в следующей статье.
На дне Тихого океана нашли вещество внеземного происхождения
Почему оно внеземное
Фото © Wikipedia
Это первый в истории человечества взрыв атомной бомбы. Он произошёл 16 июля 1945 года в США — в пустыне недалеко от города Аламогордо, штат Нью-Мексико. Снимок сделан через 16 тысячных секунды после детонации. Бомба называлась Gadget (“Штучка”). Чуть позже точно такую же обернули в оболочку, назвали “Толстяком” и сбросили на Нагасаки. То есть это были две практически одинаковые бомбы.
Фото © Wikipedia
Они были плутониевые. В основе — реакция распада плутония-239. Это один из известных изотопов этого вещества. Изотоп — это то же вещество, но с немного другим составом субатомных частиц. У плутония-239 в ядре 145 нейтронов. А протонов — 94. Поэтому в таблице Менделеева плутоний 94-й. Это его атомный номер. Соответственно, 94 плюс 145 равно 239.
Открыл плутоний-239 ещё в 1934 году создатель первого в мире ядерного реактора итальянский физик Энрико Ферми, но экспериментально получить плутоний впервые удалось в 1940-м в Калифорнии.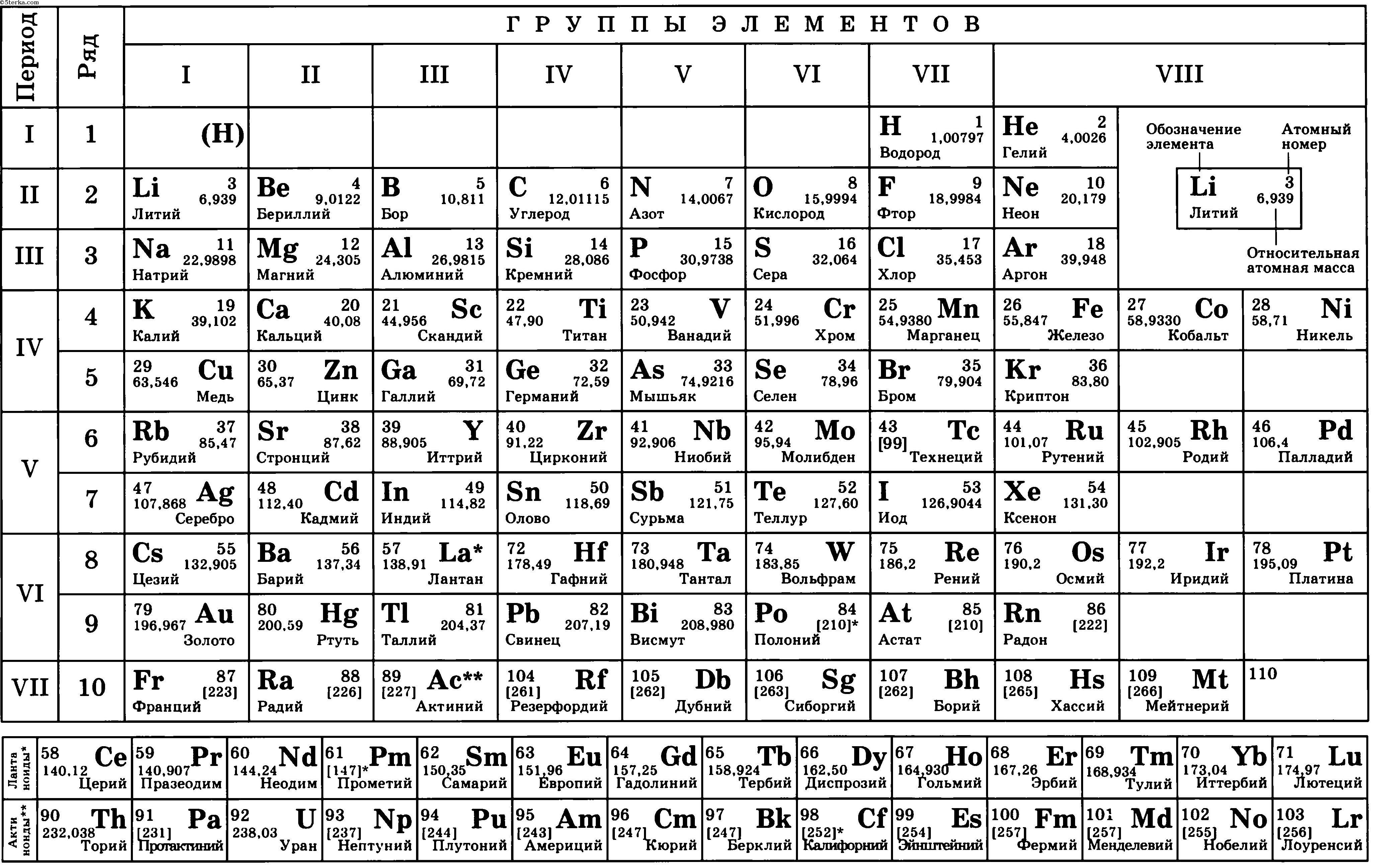 Американские учёные синтезировали его в циклотроне, то есть в коллайдере: бомбардировали окись урана ядрами дейтерия (это тяжёлый изотоп водорода, у него помимо протона в ядре имеется ещё и нейтрон). Позже плутоний-239 обнаруживали в урановых рудниках, он там в очень малых количествах образуется естественным путём в ходе природных ядерных реакций.
Американские учёные синтезировали его в циклотроне, то есть в коллайдере: бомбардировали окись урана ядрами дейтерия (это тяжёлый изотоп водорода, у него помимо протона в ядре имеется ещё и нейтрон). Позже плутоний-239 обнаруживали в урановых рудниках, он там в очень малых количествах образуется естественным путём в ходе природных ядерных реакций.
Так вот.
В Тихом океане найден плутоний, но только совершенно другой — плутоний-244. Протонов столько же, но нейтронов — все 150. Извлекли удивительное вещество с полуторакилометровой глубины из образца, взятого со дна недалеко от экватора.
Физики уверяют, что ничего подобного в земной природе само собой получиться не может. Можно было бы подумать, что это вещество сопровождает нас с самого рождения планеты — прилипло, так сказать, от протопланетного облака. Но нет, это тоже невозможно. Земле 4,5 миллиарда лет. Период полураспада плутония-244 — 80,6 миллиона лет. Значит, за 161 миллион лет он распадается совсем. Вывод: он когда-то прибыл к нам из космоса.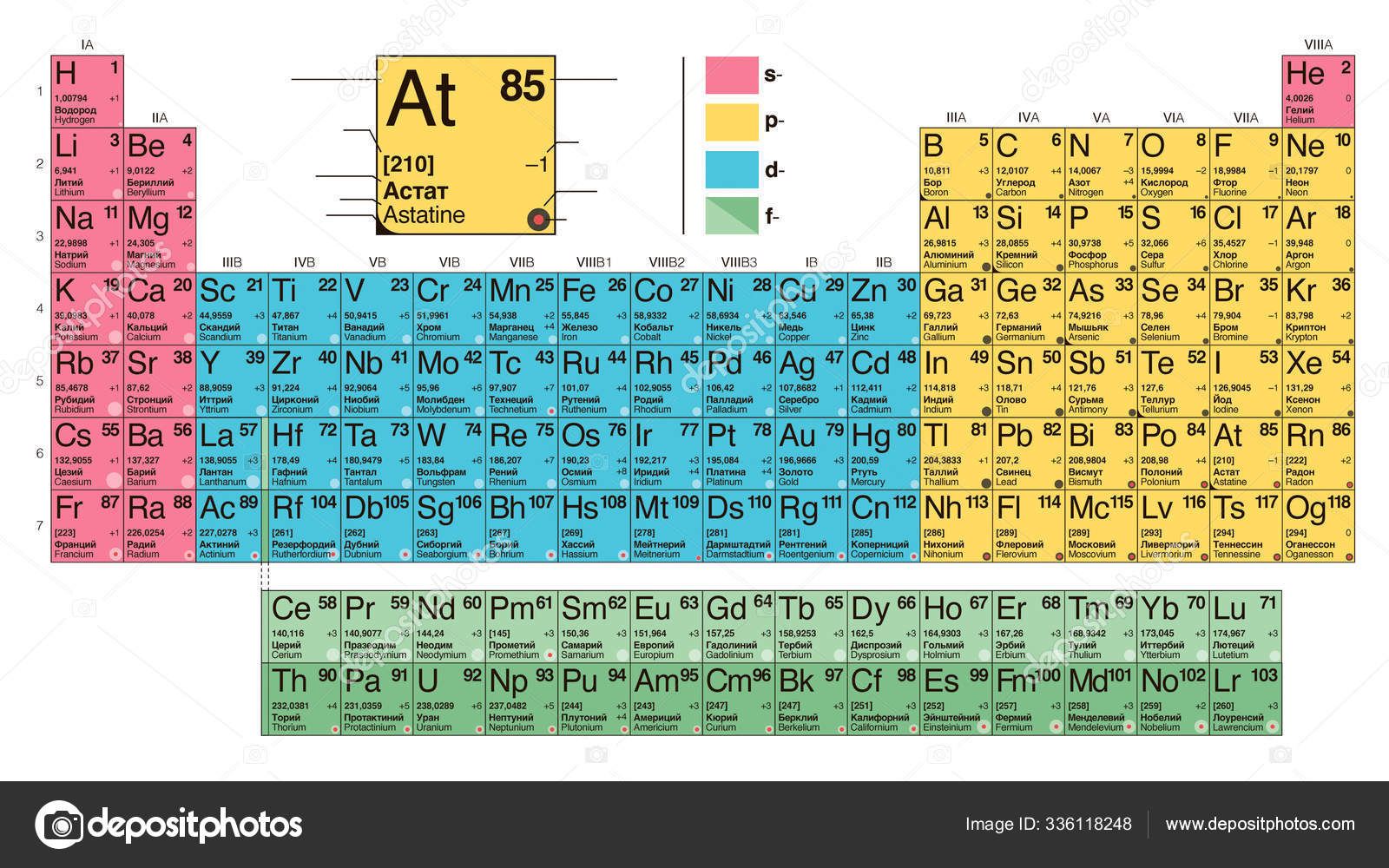 Поскольку взятому со дна образцу примерно 10 миллионов лет, стало быть, прибыл внеземной плутоний в этом временном промежутке.
Поскольку взятому со дна образцу примерно 10 миллионов лет, стало быть, прибыл внеземной плутоний в этом временном промежутке.
Версии происхождения
Первая — взрыв сверхновой звезды. Часто это событие называют её смертью, но в масштабах Вселенной о смерти говорить трудно: звезда трансформируется. Она эффектно сбрасывает бренную оболочку, поскольку внутри заканчивается водород для превращения в гелий. Астрофизики установили, что во время этой вспышки в выброшенной мешанине образуется очень много тяжёлых элементов. Их атомы — конструктор из порой поистине фантастического количества деталей: протонов, нейтронов, электронов. Учёные говорят, что если этот плутоний возник именно так, то это должна была быть вспышка, по яркости сравнимая с полной луной.
© giphy, NASA
От самой звезды при этом остаётся одно ядро. И оно сжимается так, что в лучшем случае получается адски плотный комок даже не ядер, а в основном свободных нейтронов. Этот комок может быть в диаметре меньше Москвы и при этом раза в полтора тяжелее Солнца. Он называется нейтронной звездой. Или пульсаром, потому что очень быстро вращается и испускает со своих полюсов радиосигналы, так что астрономы наблюдают в телескопы пульсацию.
Он называется нейтронной звездой. Или пульсаром, потому что очень быстро вращается и испускает со своих полюсов радиосигналы, так что астрономы наблюдают в телескопы пульсацию.
© giphy, NASA
Да, в худшем случае — если звезда была особо массивной — ядро превращается не в нейтронный шарик, а в чёрную дыру. То есть коллапсирует так, что проглатывает вообще всё вместе с фотонами.
Но это, кстати, не единственный способ “приготовления” чёрной дыры. Её можно получить путём столкновения двух нейтронных звёзд. Когда же они сливаются, тоже происходит взрыв. И при этом тоже образуются тяжеловесные химические элементы, которые с огромной скоростью вылетают в окружающее пространство.
© giphy
Отсюда вторая версия происхождения плутония-244. Причём, по мнению исследователей, несколько более предпочтительная. Дело в том, что вместе с этим плутонием в образце нашли тяжёлые изотопы железа (железо-60), которые возникают при взрывах сверхновых. Но его как-то маловато по сравнению с количеством плутония.
Детство Вселенной. Что было после Большого взрыва и как это увидеть в телескоп
Таблица Менделеева глазами астрономов
Пользуясь таким великолепным случаем, самое время рассказать о составленной недавно “астрономической таблице Менделеева”. Из неё следует, что абсолютно всё, с чем мы имеем дело, так или иначе космического происхождения.
Университет Огайо. Фото © astronomy.ohio-state.edu
Например, водород (чего проще, протон да электрон) образовался в результате Большого взрыва. Кстати, из него состоит 73% всей видимой материи во Вселенной. Ещё 25% — это гелий, а всё остальное, что есть в периодической таблице, составляет 2%.
Углерод и азот в основном родом из умирающих маломассивных звёзд вроде нашего Солнца. Они тоже сбрасывают оболочки, но ядро становится просто белым карликом. Рано или поздно он тоже взорвётся и выбросит в космос в том числе серу, хлор, аргон, железо, никель, цинк. А вот, например, кислород, по мнению астрофизиков, мог появиться только после действительно мощной вспышки сверхновой. И обратите внимание на номер 94 — плутоний в оранжевой категории, этим цветом обозначены элементы, возникающие при слиянии нейтронных звёзд.
И обратите внимание на номер 94 — плутоний в оранжевой категории, этим цветом обозначены элементы, возникающие при слиянии нейтронных звёзд.
Загадочная звезда стала за два месяца ярче в 50 раз
23 мая 2021, 04:38
“Роскосмос” начнёт использовать виртуальную реальность для разработки техники
22 мая 2021, 08:38
Обнаружена галактика с древнейшей спиралью
22 мая 2021, 02:38
Дейтерий | Определение, символ, производство и факты
- Ключевые люди:
- Гилберт Н. Льюис Гарольд С. Юри Морис Гольдхабер
- Похожие темы:
- водород дейтрон
См. все связанные материалы →
дейтерий , (D, или 2 H), также называемый тяжелым водородом , изотоп водорода с ядром, состоящим из одного протона и одного нейтрона, что в два раза больше, чем масса ядра обычного водорода (один протон).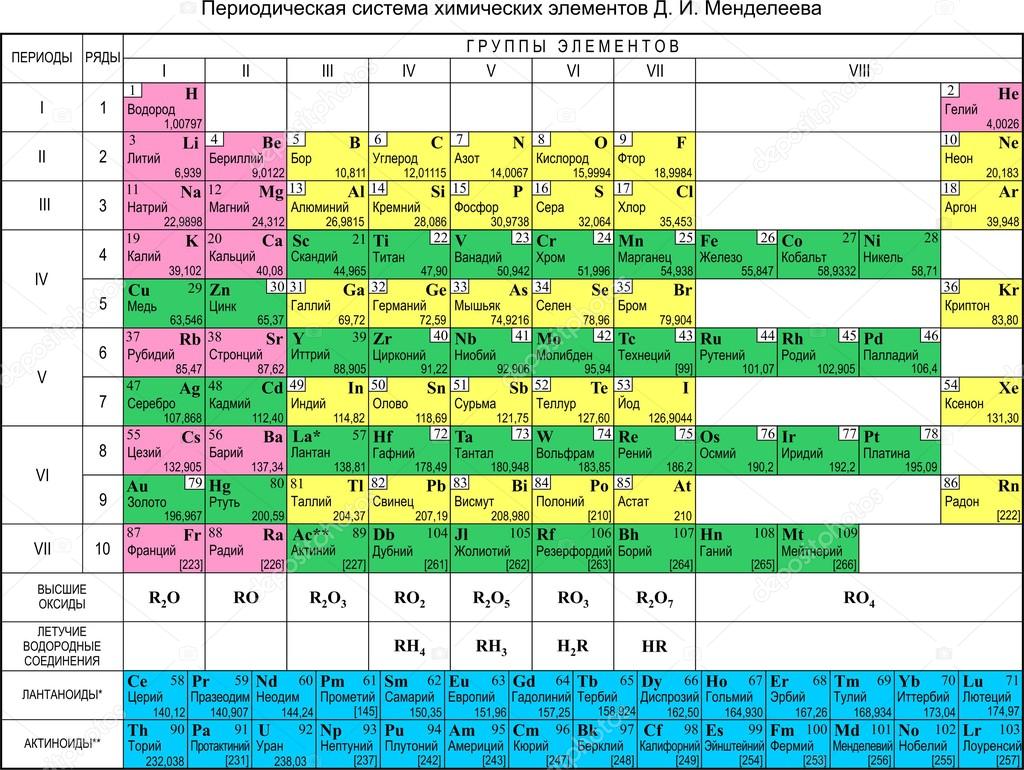 Дейтерий имеет атомный вес 2,014. Это стабильный атомный вид, содержащийся в природных соединениях водорода в количестве около 0,0156 процента.
Дейтерий имеет атомный вес 2,014. Это стабильный атомный вид, содержащийся в природных соединениях водорода в количестве около 0,0156 процента.
Дейтерий был открыт (1931 г.) американским химиком Гарольдом К. Юри (за что он был удостоен Нобелевской премии по химии в 1934 г.) и его соратниками Фердинандом Г. Брикведдом и Джорджем М. Мерфи. Юри предсказал разницу между давлениями паров молекулярного водорода (H 
Викторина “Британника”
Викторина “Наука”
Дейтерий вступает во все химические реакции, характерные для обычного водорода, образуя эквивалентные соединения. Однако дейтерий реагирует медленнее, чем обычный водород, и этот критерий отличает две формы водорода. Из-за этого свойства, среди прочего, дейтерий широко используется в качестве изотопного индикатора в исследованиях химических и биохимических реакций с участием водорода.
Ядерный синтез атомов дейтерия или дейтерия и более тяжелого изотопа водорода, трития, при высокой температуре сопровождается выделением огромного количества энергии; такие реакции использовались в термоядерном оружии. С 1953 года вместо дейтерия и трития используется стабильное твердое вещество дейтерид лития (LiD).
Физические свойства молекулярной формы изотопа дейтерия (D 2 ) и молекул дейтерида водорода (HD) сравниваются со свойствами молекул обычного водорода (H 2 ) в табл.
| обычный водород | дейтерид водорода | дейтерий | |
|---|---|---|---|
| * При 20,39 К. | |||
| ** При 22,54 К. | |||
| *** При 23,67 К. | |||
| грамм молекулярный объем твердого вещества в тройной точке (куб см) | 23.25 | 21,84 | 20.48 |
| тройная точка (К) | 13,96 | 16. 60 60 | 18,73 |
| давление пара в тройной точке (мм рт. ст.) | 54,0 | 92,8 | |
| температура кипения (К) | 20.39 | 22.13 | 23,67 |
| теплота плавления в тройной точке (кал/моль) | 28,0 | 38.1 | 47,0 |
| теплота парообразования (кал/моль) | 216* | 257** | 293*** |
Редакторы Британской энциклопедии Эта статья была недавно отредактирована и обновлена Адамом Августином.
WebElements Periodic Table » Hydrogen » изотопные данные
1 H
Доступные свойства водорода…
Изотоп водорода H-2, также известный как дейтерий, используется в различных областях. Дейтерий широко используется в органической химии для изучения химических реакций. Он также используется в исследованиях витаминов. Дейтерий в форме H 2 O, известный как тяжелая вода, используется в качестве замедлителя в ядерных реакторах CANDU, в исследованиях ЯМР и в исследованиях метаболизма человека. Тяжелая вода также применяется в нейтринной обсерватории Садбери, где она используется для изучения поведения нейтрино.
Природные изотопы
| Изотоп | Масса/Да | Естественное содержание (атомов %) | Ядерный спин (I) | Магнитный момент (мк/мк |
|---|---|---|---|---|
| 1 Н | 1.007825032 1(4) | 99,9885 (70) | 1 1 2 | 2.7928456 |
| 2 Н | 2.014101778 0(4) | 0,0115 (70) | 0,8574376 |
Радиоизотопные данные
| Изотоп | Масса/Да | Период полураспада | Режим распада | Ядерный спин | Магнитный момент ядра |
|---|---|---|---|---|---|
| 3 Н | 3.0160492675(11) | 12.33 г | β – до 3 | 1 / 2 | 2,978960 |
Каталожные номера
- Содержание изотопов в природе: отчет Комиссии по атомным весам и изотопному содержанию для Международного союза теоретической и прикладной химии в Изотопные составы элементов 1989 , Pure and Applied Chemistry, 1998, 70 , 217. [Copyright 1998 IUPAC]
- Для получения дополнительной информации о радиоизотопах см. Таблицу нуклидов Jonghwa Chang (Корейский научно-исследовательский институт атомной энергии)
- Массы, ядерные спины и магнитные моменты: И.
 Миллс, Т. Квитас, К. Хоманн, Н. Каллай и К. Кучицу в
Миллс, Т. Квитас, К. Хоманн, Н. Каллай и К. Кучицу в
ЯМР Свойства водорода
Общее эталонное соединение: Si(CH 3 ) 4 /CDCl 3 (1%) для 1 H, Si(C 2 H 3 ) для 4 ) 2 H и Si(CH 3 ) 3 (CH 2 3 H)/C 6 D 6 для 3 H 3 Изотоп 1 Изотоп 2 Изотоп 3 Изотоп 1 Н 2 Н 3 Н Естественное обилие /% 99,9885 0,0115 0 Спин (I) 1 / 2 1 1 / 2 Частота относительно 1 H = 100 (МГц) 100.  000000
000000 15.350609 106.663974 Восприимчивость, D P , относительно 1 H = 1,00 1.000 0,00000111 – Восприимчивость, D C , относительно 13 C = 1,00 5870 0,00652 – Магнитогирическое отношение, γ (10 7 рад Т ‑1 с -1 ) 26.7522128 4.10662791 28.5349779 Магнитный момент, мк (мк Н ) 4.837353570 1.21260077 5.159714367 Ядерный квадрупольный момент, Q/миллибарн – 2.860(15) – Коэффициент ширины линии, 10 56 л (м 4 ) – 0,41 –
Каталожные номера
- Р.К.



 Эта таблица дает информацию о некоторых радиоизотопах водорода, их массах, периодах полураспада, способах их распада, их ядерных спинах и их ядерных магнитных моментах.
Эта таблица дает информацию о некоторых радиоизотопах водорода, их массах, периодах полураспада, способах их распада, их ядерных спинах и их ядерных магнитных моментах.