Таблица Менделеева
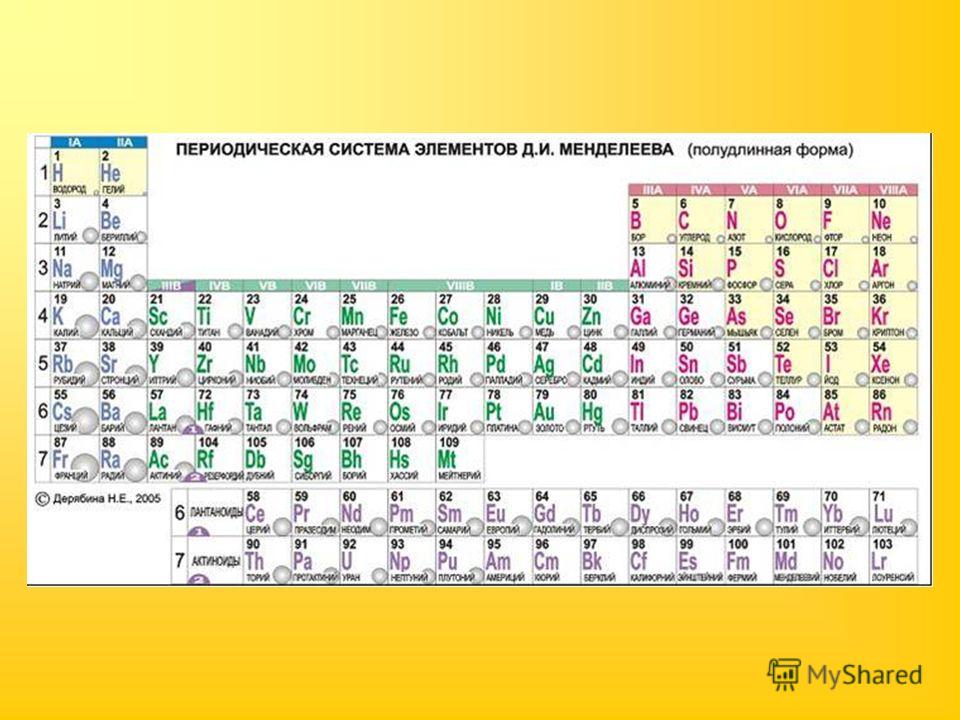
В этом году исполняется 170 лет со дня рождения выдающегося российского химика Дмитрия Ивановича Менделеева и 135 лет со дня создания им периодической системы элементов. За истекшее время таблица, наглядно демонстрирующая периодический закон, неоднократно дополнялась и расширялась. До последнего времени в научной и учебной литературе приводилась так называемая короткая форма таблицы. Современный, расширенный вариант таблицы Менделеева составлен авторами статьи на основании последних решений ИЮПАК – Междунаpодного союза теоpетической и пpикладной химии (International Union of Pure and Applied Chemistry – IUPAC). Эта оpганизация, созданная в 1919 году, кооpдиниpует исследования, тpебующие междунаpодного согласования, контpоля и стандаpтизации, pекомендует и утверждает химическую теpминологию, включая названия элементов. Россия, будучи полноправным членом союза, выполняет его решения и рекомендации. Новая форма таблицы была одобрена XVII Менделеевским съездом в сентябре 2003 года.
ИЗ ИСТОРИИ СОЗДАНИЯ И РАЗВИТИЯ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
Первого марта 1869 года Д. И. Менделеев обнародовал периодический закон и его следствие – таблицу элементов. В 1870 году он назвал систему “естественной”, а спустя год – “периодической”. Таблица (далекий прообраз современной), демонстрирующая закон, была представлена Менделеевым под названием “Опыт системы элементов, основанный на их атомном весе и химическом сходстве”. Им же была дана формулировка закона: “Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, находятся в периодической зависимости от их атомного веса”. Таблица состояла из шести вертикальных групп, предшественниц будущих периодов. По горизонтали прослеживались еще не полные ряды элементов, прообразов будущих подгрупп (сегодня – групп) элементов.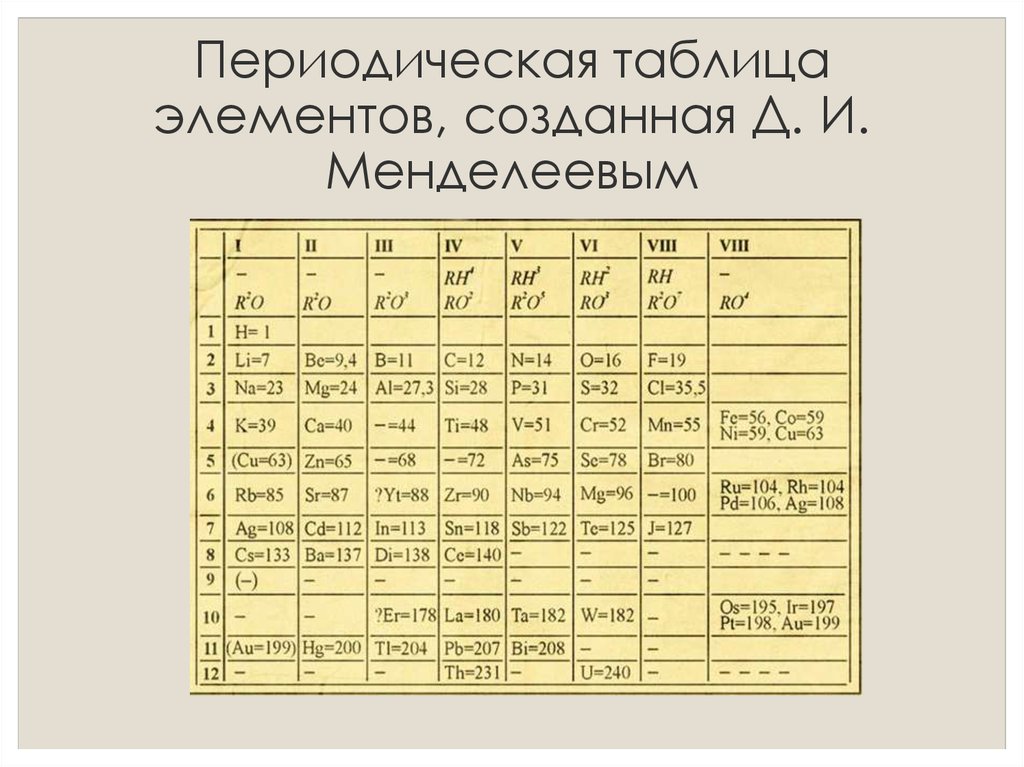
Естественно, первая таблица была несовершенной, и в последующие годы Менделеев многократно дополнял ее и вносил в ее структуру изменения. В момент представления первого варианта таблицы (март 1869 года) не были еще известны благородные (“инертные”) газы (Не, Ne, Ar, Kr, Xe, Rn) и отсутствовали сведения о внутреннем строении атомов. Лишь в двадцатых годах прошлого столетия, после революционных открытий в физике, применения рентгеновских лучей и обнаружения благородных газов, стало возможным дать современное определение закона о периодической зависимости свойств элементов от порядкового номера элемента, а не от атомного веса, как было вначале отмечено Д. Менделеевым. Иными словами, в трактовке закона понятие “атомный вес” элемента было заменено словами “порядковый (или атомный) номер”, что отвечает числу протонов в ядре атома и, соответствен но, числу электронов у нейтрального атома.

Так выглядел первый вариант таблицы элементов, составленный Менделеевым в 1869 году.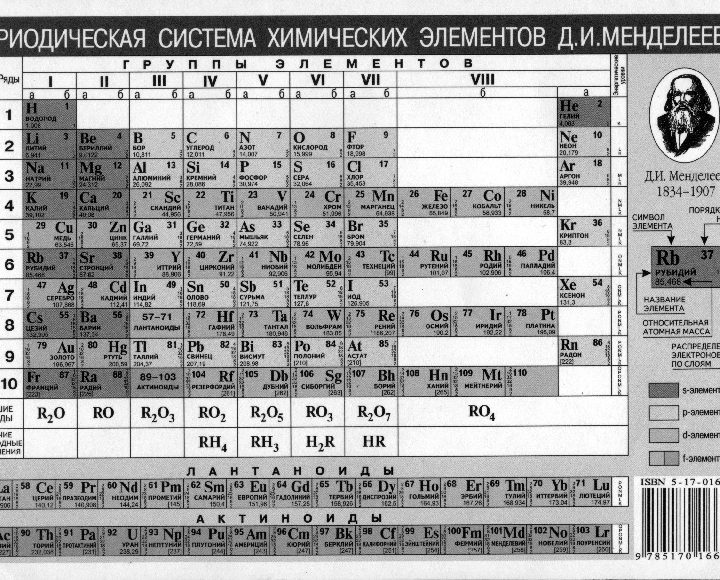
Таким образом, число элементов в семи известных периодах составляет 2, 8, 8, 18, 18, 32, 32. В соответствии с указанными числами будут наполняться элементами все периоды в порядке возрастания их порядковых номеров. При этом один и тот же элемент может оказаться в различных по номеру группах, что заметно при сравнении двух таблиц.
Рассмотренные цифры позволяют создать таблицы, состоящие из 2, 8, 18 или 32 групп элементов в трех вариантах – из (2+6), (2+6+10) или (2+6+10+14) групп. Исторически, как наиболее удобные, распространение получили в первую очередь таблицы, состоящие из 8 или 18 вертикальных групп:
а) Короткая форма таблицы. Она, к сожалению, до сих пор приводится в большинстве российских справочников и учебных пособий, хотя официально отменена ИЮПАК в 1989 году. Таблица состояла из VIII (+0) групп “типических” элементов, подгрупп (иногда и рядов) и периодов элементов. В современной зарубежной литературе эта форма таблицы заменена длинной формой.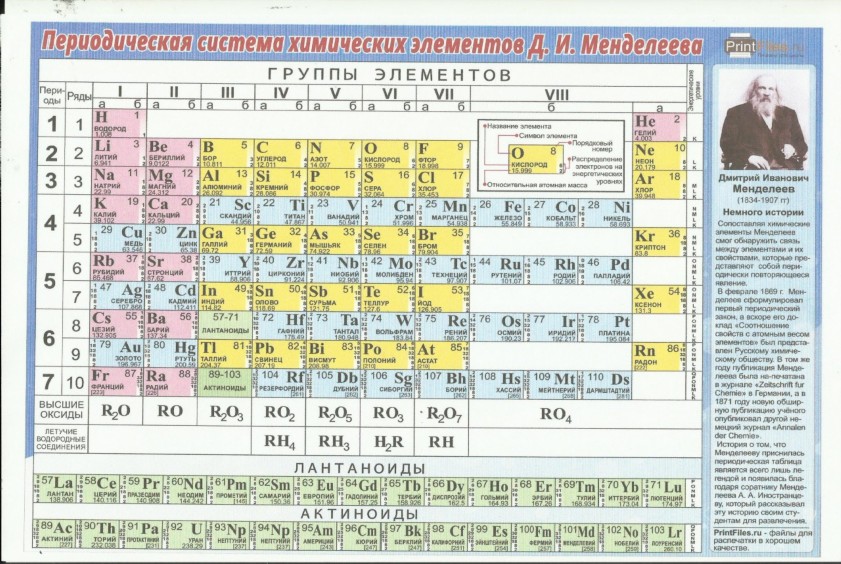
б) Длинная (реже называемая длиннопериодной или полудлинной) форма таблицы. Она была утверждена ИЮПАК в 1989 году, состоит из 18 групп, обозначенных арабскими (вместо римских) цифрами, и не содержит “типических” элементов, подгрупп, рядов и семейств. Ее упрощенные варианты появлялись гораздо раньше, но чаще всего с одним отличием – групп, обозначенных римскими цифрами, было восемь (с их растяжкой до восемнадцати за счет приставок а и b и искусственным созданием триад элементов).
в) Сверхдлинная (реже именуемая длинной) форма таблицы состояла бы из 32 групп элементов. Официально она вряд ли будет принята в предвидимом будущем, так как каждая из 14 дополнительных групп (сверх 18) содержала бы лишь два элемента (один лантаноид и один актиноид), близкие по свойствам ко всем остальным тринадцати элементам периода.
До 80-90-х годов прошлого века были распространены две первые формы таблицы. Первая – архаичная короткая форма с “насильственной” упаковкой элементов в восемь (I-VIII), иногда девять (+0) групп, подразделенных дополнительно еще на ряды (8 или 10) и подгруппы, содержавшие два или три “типических” элемента, предшествующих, в свою очередь, двум спорным по названиям (A, B или a, b, “главная” или “побочная”).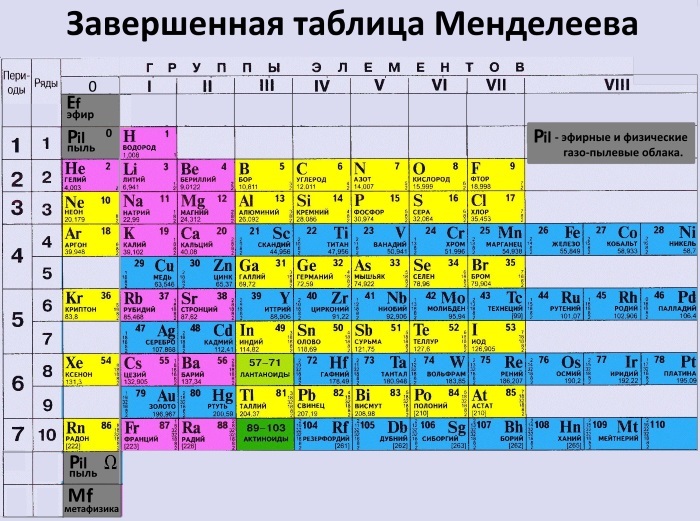
При выборе и утверждении длинного варианта таблицы были соблюдены “интересы” большинства элементов и принцип “золотой середины” без нарушения основы закона Менделеева – периодичности в свойствах элементов. Сорок элементов (по 10 d-элементов в каждом из периодов с 4 по 7), относимые ранее к “переходным”, или “вставным” (между s- и p-элементами), и называемые “побочными”, после 1989 года перестали быть таковыми. Они стали полноправными компонентами своих новых десяти групп.
Современный вариант таблицы Менделеева, составленный по форме, утвержденной ИЮПАК в 1989 году и принятой международным научным сообществом. В нем приведены уточненные в 1995 году значения атомных масс и утвержденные в 1997 году названия девяти полученных искусственно элементов №№ 101-109.
С официальным принятием новой формы таблицы исчезли, став лишними, надуманные или принятые вынужденно термины: “типические элементы”, “подгруппа” (главная и побочная), “триада”, “ряды”, “семейства” (железа или платиновых металлов). Все элементы одной группы (кроме водорода и гелия – они всегда на особом положении), расположенные вертикально в один ряд, имеют в принципе одинаковые две наружные (определяющие степень окисления) s- + p- или s- + d-орбитали электронов. Лантаноиды и актиноиды (f-элементы), как и раньше, остаются в третьей группе в соответствии с наличием в их электронных орбиталях условно s2d1-электронов. Различия в электронной структуре атомов актиноидов здесь не обсуждаются.
Все элементы одной группы (кроме водорода и гелия – они всегда на особом положении), расположенные вертикально в один ряд, имеют в принципе одинаковые две наружные (определяющие степень окисления) s- + p- или s- + d-орбитали электронов. Лантаноиды и актиноиды (f-элементы), как и раньше, остаются в третьей группе в соответствии с наличием в их электронных орбиталях условно s2d1-электронов. Различия в электронной структуре атомов актиноидов здесь не обсуждаются.
Периодическая система элементов, предложенная Нильсом Бором в 1921 году. Она отражает и строение электронных оболочек, и химические свойства атомов.
Длинная форма таблицы лишена несоответствий, недостатков и очевидных противоречий, присущих ее короткой форме, заметных при первом же взгляде на свойства элементов, искусственно собранных в одну и ту же группу. Так, например, в I группу короткой таблицы попали и металлы Cu, Ag, Au,и противоположные по активности щелочные металлы Na, K, Rb, Cs. Несовместимость свойств “одногрупповых” элементов прослеживается и по всем остальным группам.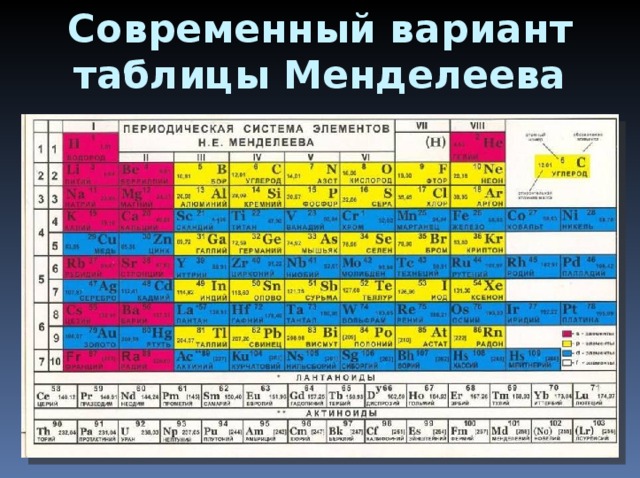 Обратим внимание лишь на бывшие конечные (VI-VIII) группы. Это – соседство в VI группе двух “типических” элементов – O и S и их аналогов Se, Te, Po с тугоплавкими металлами – Cr, Mo, W; в VII группе – элементов, отвечающих агрессивным летучим галогенам F, Cl, Br, I, с не менее тугоплавкими металлами Mn, Tc, Re.
Обратим внимание лишь на бывшие конечные (VI-VIII) группы. Это – соседство в VI группе двух “типических” элементов – O и S и их аналогов Se, Te, Po с тугоплавкими металлами – Cr, Mo, W; в VII группе – элементов, отвечающих агрессивным летучим галогенам F, Cl, Br, I, с не менее тугоплавкими металлами Mn, Tc, Re.
Д. Менделеев и Д. Коновалов на закладке химической лаборатории Санкт-Петербургского университета. 1892.
Максимально противоречива структура VIII группы. В нее включены подгруппа VIIIb с “триадой” (“семейство железа” – Fe, Co, Ni) и “семейство платиновых металлов” (Ru, Rh, Pd, Os, Ir, Pt), куда, естественно, должны входить в виде трех вертикальных рядов и только что полученные элементы 108-110, которые никогда не относились к платиновым. В эту же группу входит, противореча здравому смыслу, и подгруппа VIIIa, куда отнесены благородные газы (He, Ne и другие).С уверенностью можно утверждать, что исторически эти триады-семейства были “втиснуты” в прокрустово ложе последней (VIII) группы вынужденно, вопреки логике, так как эта группа, согласно электронной структуре атомов, предназначена природой только для указанных газовых элементов. Причина образования такого “Ноева ковчега” проста: четырем триадам из 3(4) декад в каждом периоде при компоновке таблицы из восьми групп не хватило места в ее предшествующих семи группах.
Причина образования такого “Ноева ковчега” проста: четырем триадам из 3(4) декад в каждом периоде при компоновке таблицы из восьми групп не хватило места в ее предшествующих семи группах.
Группа русских ученых, обследовавших уральские заводы в 1899 году. Слева направо: С. Вуколов, К. Егоров, Д. Менделеев, П. Земятченский.
В официально принятой длинной форме таблицы понятия “семейство железа” и “семейство платиновых металлов” исчезают логически, так как к ним, согласно их свойствам, совместному распространению в природе, изоморфизму и последовательному изменению электронной структуры, можно было бы присоединить соседей по таблице и справа и слева. Иными словами, первое семейство можно расширить, например, до ванадия и цинка включительно, а во второе – поместить другие благородные металлы – серебро, золото, ртуть; старые понятия надуманы искусственно, будучи привязаны к структуре бывшей VIII группы.
В предложенную таблицу для каждого элемента введены также две альтернативные величины относительной электроотрицательности (ОЭО) атомов (их способности в молекуле притягивать электроны, участвующие в образовании химических связей) и основные физические параметры соответствующих простых веществ. Использовать значения ОЭО важно, в частности, для исключения и исправления устаревших ошибочных названий и написания химических формул бинарных соединений. Например, водородные соединения элементов второго периода Н4С, Н3N, h3О, НF согласно значениям ОЭО (для водорода около 2,0, для других элементов – от 2,5 для углерода до 4,0 для фтора) называются соответственно карбидом, нитридом, оксидом и фторидом водорода. В соответствии с этим приведенные написания формул аммиака и метана более справедливы, нежели традиционные (NH3 и СН4).
Использовать значения ОЭО важно, в частности, для исключения и исправления устаревших ошибочных названий и написания химических формул бинарных соединений. Например, водородные соединения элементов второго периода Н4С, Н3N, h3О, НF согласно значениям ОЭО (для водорода около 2,0, для других элементов – от 2,5 для углерода до 4,0 для фтора) называются соответственно карбидом, нитридом, оксидом и фторидом водорода. В соответствии с этим приведенные написания формул аммиака и метана более справедливы, нежели традиционные (NH3 и СН4).
Д. И. Менделеев с братом Павлом. 1890.
Однако, несмотря на справедливое разрешение ИЮПАК давно назревшей проблемы и принятие новой системы во всем мире, ее использование в российском образовании и науке неоправданно запаздывает. Вместе с тем есть и отрадные исключения из этого. Помимо ряда изданий нового варианта таблицы, предложенного авторами настоящей статьи, можно отметить публикации простых вариантов длинной формы таблицы рядом передовых российских издательств, а современной таблицы на двух языках – в новом семитомном справочном издании. В отличие от российских, зарубежное образование и наука приняли к исполнению решение ИЮПАК 1989 года незамедлительно. Интернет также сообщает только о наличии длинной формы таблицы.
В отличие от российских, зарубежное образование и наука приняли к исполнению решение ИЮПАК 1989 года незамедлительно. Интернет также сообщает только о наличии длинной формы таблицы.
Д. И. Менделеев в мантии доктора прав Эдинбургского университета. Акварельный портрет работы И. Е. Репина. 1885 год.
Д. И. Менделеев в своем рабочем кабинете. 1904 год. Фото Ф. Блумбаха.
Современный вариант периодической системы, первый в российских публикациях, был создан в 1999 году. Новая форма таблицы Менделеева учебно-справочного назначения отвечает международным стандартам. Кроме русских и латинских названий элементов в ней приводятся английские и американские формы их написания. Чтобы сохранить преемственность таблиц и упростить использование ее длинной формы, новые номера групп в ней согласованы со старыми (римскими) номерами групп (I – VIII) и подгрупп (a, b), хотя зарубежные источники прежние обозначения уже не указывают. Упрощенные варианты рациональной длинной таблицы были распространены еще задолго до 1989 года, в том числе в СССР, с одним отличием – номеров групп было восемь (они обозначались римскими цифрами), но они “растягивались” до восемнадцати за счет приставок а и b и искусственного создания триад элементов. В новой таблице приведены исправленные атомные массы элементов, утвержденные ИЮПАК в 1995 году, и новые названия десяти последних элементов, окончательно утвержденные, также этой организацией, в 1997-м. Аналоги такой системы, в основном англоязычные, широко распространены в зарубежной литературе.
В новой таблице приведены исправленные атомные массы элементов, утвержденные ИЮПАК в 1995 году, и новые названия десяти последних элементов, окончательно утвержденные, также этой организацией, в 1997-м. Аналоги такой системы, в основном англоязычные, широко распространены в зарубежной литературе.
Тобольская губернская классическая гимназия, в которой в 1841-1849 годах учился Д. И. Менделеев.
Авторы благодарныпрофессорам С. Г. Дьяконову,Н. В. Коровину, А. М. Кочневу, А. М. Кузнецову, Г. В. Лисичкину, А. И. Михайличенко, Ю. И. Сальникову, С. Н. Соловьеву, Н. А. Улаховичу, А. И. Хацринову и др., поддержавшим высказанные идеи или давшим полезные советы при оформлении современной таблицы Д. И. Менделеева.
Доктор технических наук Р. Сайфуллин, профессор, действительный член Академии наук Республики Татарстан; кандидат химических наук А. САЙФУЛЛИН.
ЛИТЕРАТУРА
Лидин Р. А. и др. Химия в помощь абитуриенту. – М.: Дрофа, 2001. 576 с.
576 с.
Никольский А. Б., Суворов А. В. Химия. – СПб.: Химиздат, 2001. 512 с.
Новый справочник химика и технолога. – СПб.: НПО “Мир и семья”, 2002. Т. 1, 954 с. Т. 2, 1276 с.
Сайфуллин Р. С., Сайфуллин А. Р. Универсальный лексикон: химия, физика и технология; R.S.Saifullin, A.R.Saifullin. Universal Concise Dictionary: Chemistry, Physics andTechnology. – М.: Логос, 2001, 2002. 548 с.
Хаускрофт К., Констебле Э.. Современный курс общей химии/ Пер. с англ. – М.: Мир, 2002. Т. 1, 252 с. Т. 2, 250 с.
Химия, справочник школьника и студента / Коллектив авторов. Пер. с нем. Изд. 2-е. – М.: Дрофа, 2000. 384 с.
Хисамиев Г. Г. Общая химия, задачи и упражнения (для вузов). – Казань: Магариф, 1999. 368 с.
Эмсли Дж. Элементы. – М.: Мир, 1993. 258 с.
Oxford Dictionary of Science / Ed. Isaacs A., Daintith J., Martin E. Oxford University Press, Oxford, New York, 1999. 858 p.
The New Encyclopedia Britannica, 15-th Ed., Encyclopedia Britannica, Inc. Chicago, 1974-1994.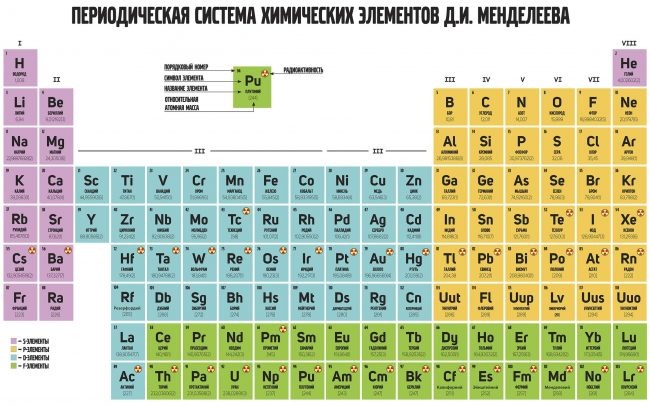
Hawley’s Condensed Chemical Dictionary, 11-nd Ed Rev. N.I. Sax, R.J. Lewis, Sr. Van Nostrand Rheinhold Co., N.Y., 1987. 1303 p.
WebElementsTM Periodic table (professional edition) (http://www.webelements.com/. 1993-2003).
Krzysztof M. Pazdro, Chemia dla licealistov (Budowa materii w ochach chemika), Wyd. II. Oficyna Edukacyjna, Warszawa, 1996. 246 p.
Новые книги
НЕИЗВЕСТНЫЙ МЕНДЕЛЕЕВ
В представлении большинства людей Менделеев – великий химик. Но оказывается, из всего количества его трудов собственно химии посвящено лишь 9%. С гораздо большим основанием Дмитрия Ивановича можно было бы назвать физико-химиком, физиком или технологом, ибо каждой из этих областей он посвятил примерно 20% своих работ. Наконец, немалая доля его исследований приходится на геофизику (5%) и экономику (8%).
Общественный фонд “Возрождение Тобольска” выпустил к 170-летию со дня рождения Дмитрия Ивановича Менделеева (1834-1907) избранные произведения ученого в двух томах (“Тобольский гений России”. Тобольск, 2003).
Тобольск, 2003).
Менделеев родился в Тобольске, первой столице сибирского края. Здесь жили его предки. Первые книги, изданные в Сибири в XVIII веке, были напечатаны в Тобольске в типографии прадеда Дмитрия Ивановича – В. Я. Корнильева. Детство и юность, проведенные в Сибири, определили во многом последующие увлечения ученого.
Юбилейное издание готовили к печати Надежда Полунина и Герман Смирнов. Из огромного количества произведений, оставленных Менделеевым (более 500), им предстояло отобрать для двухтомника наиболее интересные и значимые работы. В последнее время сочинения Менделеева издаются очень редко. А между тем многие “заветные мысли”, высказанные ученым, актуальны до сих пор. Вот, например: “Велико заблуждение тех, которые думают, что предстоящее России можно выполнить легко и просто, одним мановением руки или одними пламенными речами…”
Первый том издатели назвали “Неизвестный Менделеев”. Книгу открывают отрывки из последних работ ученого – “Заветные мысли” (1903-1905) и “К познанию России” (1906).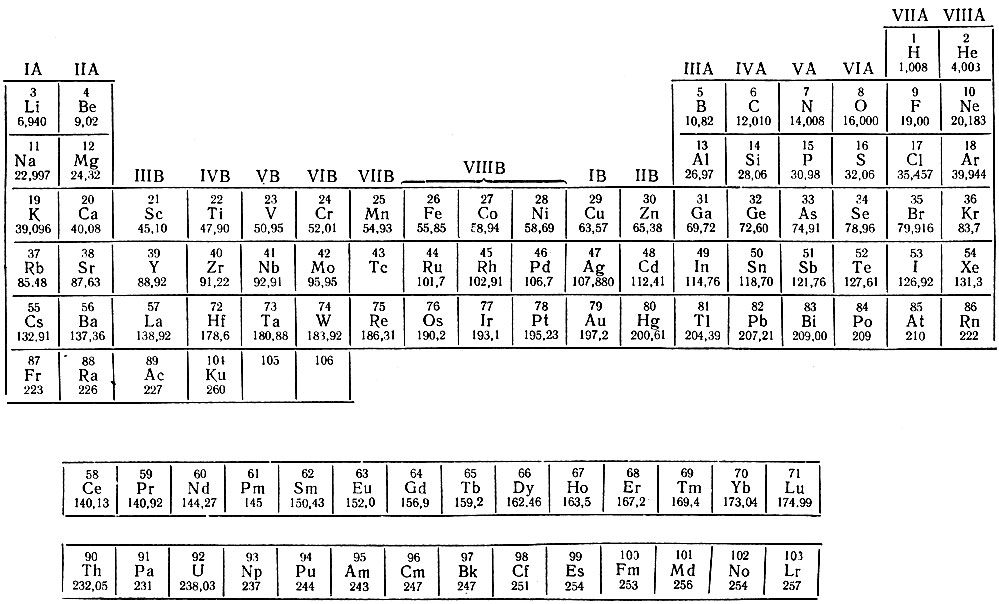 Вот как сформулировал автор те задачи, что ставил перед собой при написании “Заветных мыслей”: “Вся предлагаемая книга для того, между прочим, и писана, чтобы увеличить существующую у нас меру понимания условий для возможности увеличения средних народных достатков”. Составители книги выделили на полях некоторые мысли – заповеди ученого: “… надо еще немало поработать мозгами в Государственной Думе, чтобы законами поощрить труд и вызвать порывы долга перед Родиной”. И вновь о том же: “… нужно развивать мысли о накоплении в народе личной инициативы и трудолюбия…” Развитие образования, науки всегда волновало ученого: “Затраты на науку окупаются тем, что она видит многое зараньше, предупреждает, разбирает возможное, отбирает существенное из кучи практических подробностей”.
Вот как сформулировал автор те задачи, что ставил перед собой при написании “Заветных мыслей”: “Вся предлагаемая книга для того, между прочим, и писана, чтобы увеличить существующую у нас меру понимания условий для возможности увеличения средних народных достатков”. Составители книги выделили на полях некоторые мысли – заповеди ученого: “… надо еще немало поработать мозгами в Государственной Думе, чтобы законами поощрить труд и вызвать порывы долга перед Родиной”. И вновь о том же: “… нужно развивать мысли о накоплении в народе личной инициативы и трудолюбия…” Развитие образования, науки всегда волновало ученого: “Затраты на науку окупаются тем, что она видит многое зараньше, предупреждает, разбирает возможное, отбирает существенное из кучи практических подробностей”.
Каких только проблем не коснулся ученый: тончайшие химические исследования и сыроварение, пульсирующий насос и действие удобрений, температура верхних слоев атмосферы и наиболее удобные конструкции керосиновых ламп. Он летал на воздушном шаре и интересовался проблемами мореходства и судостроения, занимался выработкой таможенного тарифа, работал в Главной палате мер и весов. Менделеев писал о мировом эфире и о картине Куинджи, о ледоколе “Ермак” и о разработке донецких углей…
Он летал на воздушном шаре и интересовался проблемами мореходства и судостроения, занимался выработкой таможенного тарифа, работал в Главной палате мер и весов. Менделеев писал о мировом эфире и о картине Куинджи, о ледоколе “Ермак” и о разработке донецких углей…
Сохранилось письмо Дмитрия Ивановича, адресованное министру финансов С. Ю. Витте. Письмо написано за несколько месяцев до смерти автора и не отправлено адресату. Вот что ученый говорит о себе, подводя итоги прожитой жизни: “Начав (1855) с учительства в Симферопольской гимназии, я выслужил 48 лет Родине и Науке. Плоды моих трудов, прежде всего, в научной известности, составляю щей гордость – не одну мою личную, но и общую русскую, так как все главнейшие научные академии, начиная с Лондонской, Римской, Бельгийской, Парижской, Берлинской и Бостонской, избрали меня своим сочленом, как и многие ученые общества России, Западной Европы и Америки, всего более 50-ти обществ и учреждений.
Лучшее время жизни и ее главную силу взяло преподавательство во 2-ом кадетском корпусе, в Инженерной академии, в Институте путей сообщения, в Технологическом институте и в Университете.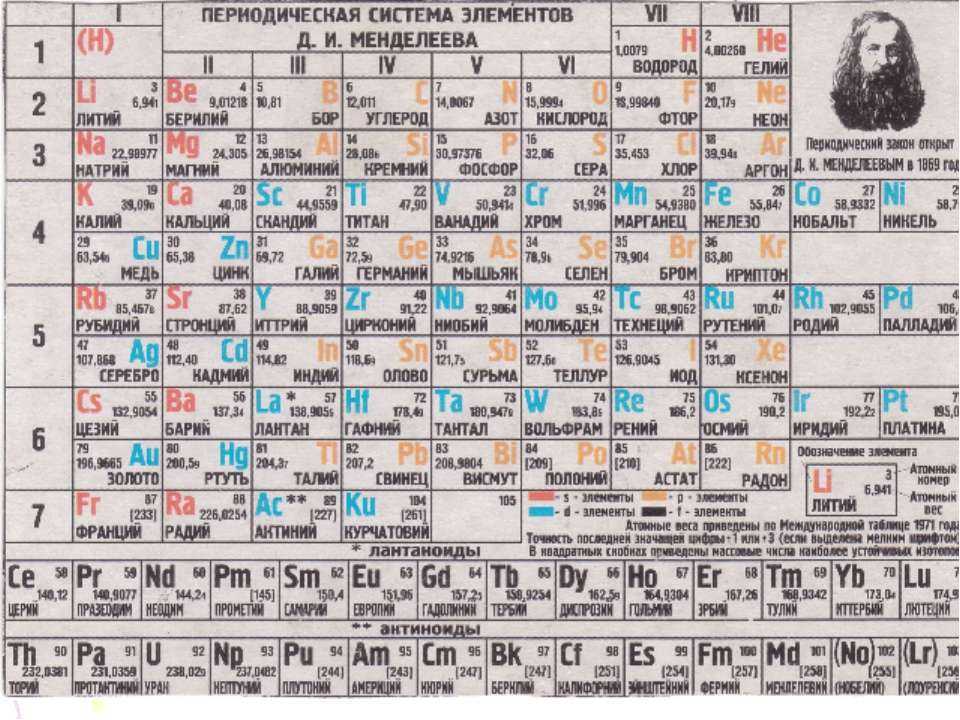 Из тысяч моих учеников много теперь повсюду видных деятелей, профессоров, администраторов, и, встречая их, всегда слышал, что доброе в них семя полагал, а не простую отбывал повинность.
Из тысяч моих учеников много теперь повсюду видных деятелей, профессоров, администраторов, и, встречая их, всегда слышал, что доброе в них семя полагал, а не простую отбывал повинность.
Третья служба моя Родине наименее видна, хотя заботит меня с юных лет до сих пор. Эта служба, по мере сил и возможности, на пользу роста русской промышленности, начиная с сельскохозяйственной, в которой лично действовал, показав на деле возможность и выгодность еще в 60-х годах интенсивного хозяйства и организовав первые у нас опытные исследования по разведению хлебов. Личные усилия убедили меня, однако, очень скоро в том, что с одним земледелием Россия не двинется к надобным ей прогрессу, богатству и силе, останется страною бедною, что настоятельнее всего рост других видов промышленности: горного дела, фабрик, заводов, путей сообщения и торговли. Мои, так сказать, теоретические усилия начались с настойчивой пропаганды в пользу возможности развития – при определенных условиях – выработки бакинской нефти в эпоху, когда к нам ввозились миллионы пудов американского керосина”.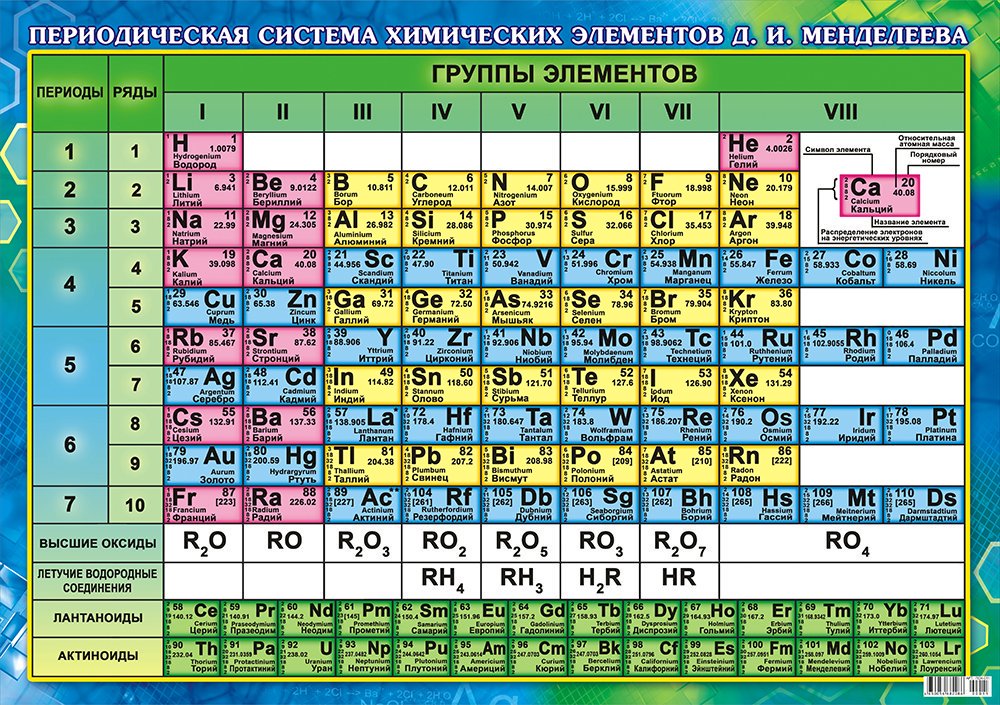
“Сам удивляюсь – чего только я не делывал на своей научной жизни. И сделано, думаю, неплохо”, – заметил как-то ученый.
Составители двухтомника использовали воспоминания людей, близко знавших Дмитрия Ивановича. “Если в какой-нибудь специальности достигнешь сути дела, – говорил Менделеев своей племяннице, – взберешься по лестнице всех предварительных знаний, а потом самостоятельно поработаешь сам, то и достигнешь того, что все легко будет даваться и сущность всякой науки будет легко усваивать”.
А вот как видел Менделеева Александр Блок, имевший возможность наблюдать ученого в непринужденной домашней обстановке: “Он давно ВСЕ знает, что бывает на свете. Во все проник. Не скрывается от него ничего. Его знание самое полное. Оно происходит от гениальности, у простых людей такого не бывает… При нем вовсе не страшно, но всегда – неспокойно, это оттого, что он все и давно знает, без рассказов, без намеков, даже не видя и не слыша. Это всепознание лежит на нем очень тяжело. Когда он вздыхает и охает, он каждый раз вздыхает обо всем вместе; ничего отдельного или отрывочного у него нет – все неразделимо. То, что другие говорят, ему почти всегда скучно, потому что он все знает лучше всех…”
То, что другие говорят, ему почти всегда скучно, потому что он все знает лучше всех…”
З. КОРОТКОВА.
Периодическая система элементов — Периодическая система химических элементов, периодическая система элементов Менделеева
Периодическая система химических элементов. – систематизированные названия хим элементов, основнаые показатели, значения и свойства хим. элементов. Chemical family of elements of the periodic table. Ниже приведён длинный вариант (длиннопериодная форма), утверждённый Международным союзом теоретической и прикладной химии (IUPAC) в качестве основного.
| IA | IIA | IIIB | IVB | VB | VIB | VIIB | —- | VIIIB | —- | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |
| Период | ||||||||||||||||||
| 1 |
1 H Водород |
2 He Гелий |
||||||||||||||||
| 2 |
3 Li Литий |
4 Be Бериллий |
5 B Бор |
6 C Углерод |
7 N Азот |
8 O Кислород |
9 F Фтор |
10 Ne Неон |
||||||||||
| 3 |
11 Na Натрий |
12 Mg Магний |
13 Al Алюминий |
14 Si Кремний |
15 P Фосфор |
16 S Сера |
17 Cl Хлор |
18 Ar Аргон |
||||||||||
| 4 |
19 K Калий |
20 Ca Кальций |
21 Sc Скандий |
22 Ti Титан |
23 V Ванадий |
24 Cr Хром |
25 Mn Марганец |
26 Fe Железо |
27 Co Кобальт |
28 Ni Никель |
29 Cu Медь |
30 Zn Цинк |
31 Ga Галлий |
32 Ge Германий |
33 As Мышьяк |
34 Se Селен |
35 Br Бром |
36 Kr Криптон |
| 5 |
37 Rb Рубидий |
38 Sr Стронций |
39 Y Иттрий |
40 Zr Цирконий |
41 Nb Ниобий |
42 Mo Молибден |
(43) Tc Технеций |
44 Ru Рутений |
45 Rh Родий |
46 Pd Палладий |
47 Ag Серебро |
48 Cd Кадмий |
49 In Индий |
50 Sn Олово |
51 Sb Сурьма |
52 Te Теллур |
53 I Иод |
54 Xe Ксенон |
| 6 |
55 Cs Цезий |
56 Ba Барий |
* |
72 Hf Гафний |
73 Ta Тантал |
74 W Вольфрам |
75 Re Рений |
76 Os Осмий |
77 Ir Иридий |
78 Pt Платина |
79 Au Золото |
80 Hg Ртуть |
81 Tl Таллий |
82 Pb Свинец |
83 Bi Висмут |
(84) Po Полоний |
(85) At Астат |
86 Rn Радон |
| 7 |
87 Fr Франций |
88 Ra Радий |
** |
(104) Rf Резерфордий |
(105) Db Дубний |
(106) Sg Сиборгий |
(107) Bh Борий |
(108) Hs Хассий |
(109) Mt Мейтнерий |
(110) Ds Дармштадтий |
(111) Rg Рентгений |
(112) Cp Коперниций |
(113) Uut Унунтрий |
(114) Uuq Унунквадий |
(115) Uup Унунпентий |
(116) Uuh Унунгексий |
(117) Uus Унунсептий |
(118) Uuo Унуноктий |
| 8 |
(119) Uue Унуненний |
(120) Ubn Унбинилий |
||||||||||||||||
| Лантаноиды * |
57 La Лантан |
58 Ce Церий |
59 Pr Празеодим |
60 Nd Неодим |
(61) Pm Прометий |
62 Sm Самарий |
63 Eu Европий |
64 Gd Гадолиний |
65 Tb Тербий |
66 Dy Диспрозий |
67 Ho Гольмй |
68 Er Эрбий |
69 Tm Тулий |
70 Yb Иттербий |
71 Lu Лютеций |
|||
| Актиноиды ** |
89 Ac Актиний |
90 Th Торий |
91 Pa Протактиний |
92 U Уран |
(93) Np Нептуний |
(94) Pu Плутоний |
(95) Am Америций |
(96) Cm Кюрий |
(97) Bk Берклий |
(98) Cf Калифорний |
(99) Es Эйнштейний |
(100) Fm Фермий |
(101) Md Менделевий |
(102) No Нобелей |
(103) Lr Лоуренсий |
|||
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
Идея организовать элементы в порядке возрастания веса их атомов. Химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом.
Химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом.
Закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме.
Сейчас используем понятие атомного числа (количества протонов) для того, чтобы правильно упорядочить систему элементов, это решает техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
Короткая форма таблицы, содержащая восемь групп элементов, была официально отменена ИЮПАК в 1989 году. Несмотря на рекомендацию использовать длинную форму, короткая форма продолжила приводиться в большом числе российских справочников и пособий и после этого времени. Из современной иностранной литературы короткая форма исключена полностью, вместо неё используется длинная форма. Такую ситуацию некоторые исследователи связывают в том числе с кажущейся рациональной компактностью короткой формы таблицы, а также с инерцией, стереотипностью мышления и невосприятием современной международной информации.
Из современной иностранной литературы короткая форма исключена полностью, вместо неё используется длинная форма. Такую ситуацию некоторые исследователи связывают в том числе с кажущейся рациональной компактностью короткой формы таблицы, а также с инерцией, стереотипностью мышления и невосприятием современной международной информации.
Периодический закон Дмитрия Ивановича Менделеева является фундаментальным законом описывающим периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Менделеевым в марте 1869 года при сопоставлении свойств всех известных в то время элементов и величин их атомных масс (весов).
Термин «периодический закон» Менделеев впервые употребил в ноябре 1870, а в октябре 1871 дал окончательную формулировку Периодического закона: «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса». Графическое табличное выражение периодического закона — периодическая система элементов разработанна Дмитрием Ивановичем Менделеевым.
Графическое табличное выражение периодического закона — периодическая система элементов разработанна Дмитрием Ивановичем Менделеевым.
Проекты
ИНТЕРАКТИВНАЯ ПЛАТФОРМА ДЛЯ МОБИЛЬНЫХ УСТРОЙСТВ
VERIMAG
SK
Участник
+7 (925) 771 12 16
НАУКА
НЕЗАВИСИМЫЕ ГИПОТЕЗЫ И ПРОЕКТЫ
ЦВЕТОК МЕНДЕЛЕЕВА
Verimag представляет проект программы, популяризирующей малоизвестные работы Д.И.Менделеева, опубликованные
в последние годы его жизни. В программе визуализированы пространственные модели Периодической системы, предложенные российскими и зарубежными исследователями, основные сведения о химических элементах.
Идея создания проекта возникла на прошедшем Фестивале науки 2015. Детально сам проект обсуждался на кафедре Химического факультета МГУ с Игорем Николаевичем Бекманом доктором химических наук, профессором, Георгием Борисовичем Рязанцевым и Максимом Александровичем Хасковым, на основе предложенной ими пространственной модели.
Подлинная Таблица Д. И. Менделеева (1906 г.)
Периодическая таблица Д. И. Менделеева (короткая форма)
Периодическая таблица Д. И. Менделеева (длинная форма)
Основная концепция проекта заключается в том, чтобы использовать 3D-интерпретацию для представления таблицы элементов. Соединить современный научный подход русской химической школы МГУ и идеи Дмитрия Ивановича Менделеева с возможностями мультимедийной платформы Verimag.
Приглашаем
к сотрудничеству всех, КОМУ МОЖЕТ БЫТЬ ИНТЕРЕСЕН ЭТОТ ПРОЕКТ химиков, физиков, разработчиков ПО, 3D-дизайнеров, аниматоров,
операторов и, конечно, ИНВЕСТОРОВ!
С древнейших времён открытия первого химического элемента по настоящее время мировому научному сообществу известно более 116 элементов, при этом попытка их систематизировать на основании Закона предпринималась многими известнейшими учёными со всего мира. Общепринятой сейчас считается систематизация, предложенная Д.И.Менделеевым
в его первых работах.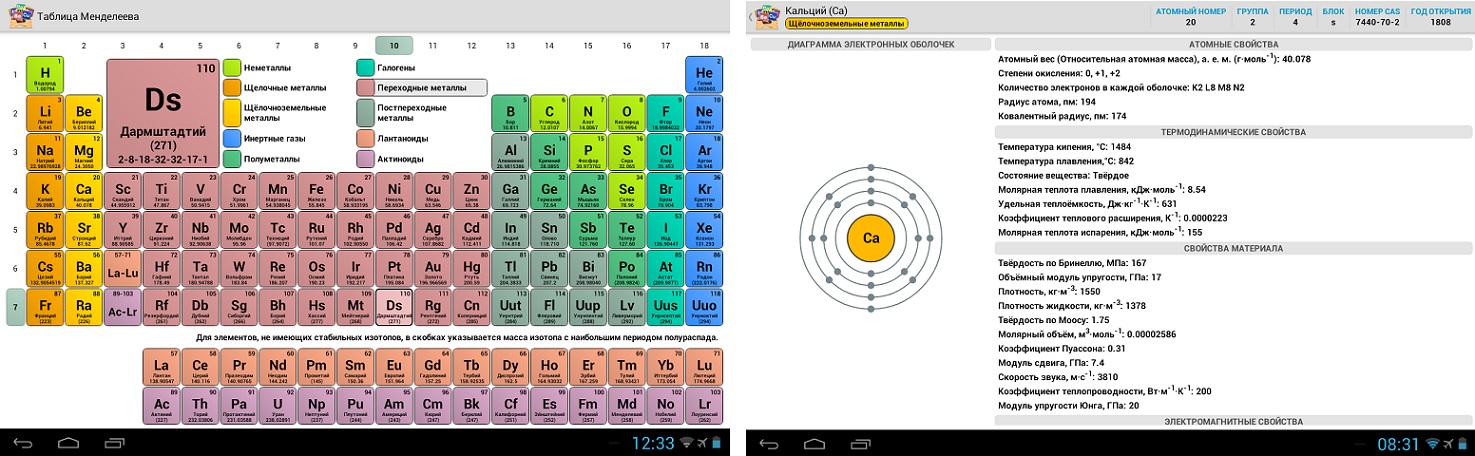
Однако даже при жизни Д.И.Менделеева в связи с открытием новых элементов (в частности некоторых лантаноидов, актиноидов и инертных газов), его не удовлетворяла выстраивающаяся система того времени, известная нам сейчас короткопериодная форма периодической таблицы (ПТ).
Предлагаемая нами концепция систематизации периодических элементов основана на забытых идеях Д.И.Менделеева
о доводородных элементах, нулевых группе и периоде.
Преимуществом предлагаемой систематизации является соблюдение принципов, предсказанных Д.И.Менделеевым,
о необходимости непрерывности и последовательности представления элементов в Периодической системе, что позволит
не выделять из таблицы лантаноиды и актиноиды, рассматривая их как обособленных представителей ПТ, а представлять все элементы в виде целостной, гармоничной и научно-обоснованной последовательности.
Сочетание использования объёмной съёмки образцов материалов, доступных на кафедре Химического факультета МГУ с 3D моделями позволит создать современный мультимедийный продукт, полезный с точки зрения использования как учебной практики в России так и по всему миру. Проект мобильного приложения «Интерактивная
Проект мобильного приложения «Интерактивная
3D таблица Д. И. Менделеева» позволит популяризировать русскую научную школу Московского Государственного Университета.
По степени сложности планируем версии: для школьников, для студентов и для специалистов.
читать об образовательных программах
и системе построения курсов Verimag
Институт мобильных образовательных систем (ИМОС). Данную проблему считает актуальной научный уководитель авторского коллектива ФГОС общего образования, д.п.н., член–корр. РАО А.М. КОНДАКОВ особеено для малокомплектных сельских школ Дагестана и других российских регионов. Мобильный класс на планшетах (без внешней точки доступа и интернет) в ноябре 2015 был продемонстрирован
в автономной работе на 33 планшетах и вызвал живой интерес особенно в части быстрой реакции на команды учителя и показом статистики в реальном времени. Основное конкурентное преимущество Verimag – мобильный класс на планшетах (без внешней точки доступа и интернет) в том, что на сегодняшний момент подобное решение на базе штатных возможностей планшетов с iOS и им подобных не реализовано.
Основное конкурентное преимущество Verimag – мобильный класс на планшетах (без внешней точки доступа и интернет) в том, что на сегодняшний момент подобное решение на базе штатных возможностей планшетов с iOS и им подобных не реализовано.
http://mobiledu.ru
ЛАНИТ Образование Направление: ИНДИГОС Корнеева О.А. руководитель проектов ИНДИГОС считает данную проблему актуальной. Мобильный класс на планшетах (без внешней точки доступа и интернет) в ноябре 2015 был продемонстрирован
в автономной работе на 33 планшетах и вызвал живой интерес особенно в части быстрой реакции на команды учителя и показом статистики в реальном времени.
http://www.lanitedu.ru/business/indigos/
читать дальше
© 2016, ООО «Веримаг». Все права защищены. Полное или частичное копирование запрещено,без согласования с правообладателями. +7 (925) 771-12-16
Полная форма периодической таблицы
Периодическая таблица представляет собой табличное представление химических элементов. Она также известна как периодическая таблица (химических) элементов. Он широко используется в химии, физике и других науках и считается символом химии. Это графическое представление периодического закона, согласно которому свойства химических элементов периодически зависят от их атомных номеров. Таблица разделена на четыре блока, каждый прямоугольный. Строки таблицы называются периодами, а ее столбцы — группами. Элементы в одной и той же группе столбцов периодической таблицы имеют сходные химические свойства. Неметаллический характер (сохранение своих электронов) увеличивается слева направо по периоду и снизу вверх по группе.
Она также известна как периодическая таблица (химических) элементов. Он широко используется в химии, физике и других науках и считается символом химии. Это графическое представление периодического закона, согласно которому свойства химических элементов периодически зависят от их атомных номеров. Таблица разделена на четыре блока, каждый прямоугольный. Строки таблицы называются периодами, а ее столбцы — группами. Элементы в одной и той же группе столбцов периодической таблицы имеют сходные химические свойства. Неметаллический характер (сохранение своих электронов) увеличивается слева направо по периоду и снизу вверх по группе.
Напротив, металлический характер (отдача электронов другим атомам) увеличивается в противоположном направлении. Основной причиной этих тенденций являются атомные электронные конфигурации. С развитием науки периодическая таблица продолжает развиваться. В природе существуют только элементы до атомного номера 94; чтобы пойти дальше, новые элементы должны были быть синтезированы в лаборатории. На сегодняшний день известны все 118 элементов, составляющих первые семь строк таблицы. Однако химическая характеристика самых тяжелых элементов по-прежнему требуется, чтобы подтвердить соответствие их свойств их положению. Неизвестно, как далеко таблица выйдет за пределы этих семи строк и сохранятся ли закономерности известной области в этой неизвестной области. Некоторые научные дебаты также бушуют о том, правильно ли расположены некоторые элементы в сегодняшней таблице. Только во втором десятилетии двадцатого века стало понятно, что порядок периодической системы определяется ее атомными номерами, целые числа которых равны положительным электрическим зарядам атомных ядер, выраженным в электронных единицах. За прошедшие годы были достигнуты большие успехи в объяснении периодического закона электронной структуры атомов и молекул. Это уточнение повысило ценность закона, который и сегодня так же широко используется, как и на рубеже двадцатого века, когда он выражал единственную известную связь между элементами.
На сегодняшний день известны все 118 элементов, составляющих первые семь строк таблицы. Однако химическая характеристика самых тяжелых элементов по-прежнему требуется, чтобы подтвердить соответствие их свойств их положению. Неизвестно, как далеко таблица выйдет за пределы этих семи строк и сохранятся ли закономерности известной области в этой неизвестной области. Некоторые научные дебаты также бушуют о том, правильно ли расположены некоторые элементы в сегодняшней таблице. Только во втором десятилетии двадцатого века стало понятно, что порядок периодической системы определяется ее атомными номерами, целые числа которых равны положительным электрическим зарядам атомных ядер, выраженным в электронных единицах. За прошедшие годы были достигнуты большие успехи в объяснении периодического закона электронной структуры атомов и молекул. Это уточнение повысило ценность закона, который и сегодня так же широко используется, как и на рубеже двадцатого века, когда он выражал единственную известную связь между элементами.
Присоединяйтесь к программе регулярных занятий Infinity Learn!
Загрузите БЕСПЛАТНО PDF-файлы, решенные вопросы, работы за предыдущий год, викторины и головоломки!
+91
Проверьте код OTP (обязательно)
класс
— Класс 6CLASS 7CLASS 9CLASS 9CLASS 10CLASS 11CLASS 12
КУРС
— CBSEIIT-JEENEET
ШКОЛА/Колледж название
SRI CHITANEA?
НетДа
Я согласен с условиями и политикой конфиденциальности.
ОбзорСовременная периодическая таблица, также известная как полная форма, основана на современном периодическом законе. Таблица представляет собой расположение элементов в порядке возрастания атомного номера. В своем нынешнем виде периодическая таблица известна как современная периодическая таблица. Он состоит из 18 вертикальных столбцов и 7 горизонтальных рядов.
- 1,2,3,…18 — названия или номера 18 вертикальных столбцов. Поскольку элементы каждой группы имеют одинаковое количество валентных электронов, их свойства идентичны.
 Только самая внешняя оболочка пуста; все внутренние оболочки заполнены.
Только самая внешняя оболочка пуста; все внутренние оболочки заполнены. - Состоит из групп 1 и 2 (щелочные металлы) и 13 и 17 (щелочноземельные металлы).
- Отсутствует самая внешняя оболочка (рядом с самой внешней предпоследней оболочкой) и вторая самая внешняя оболочка (следующая за внешней предпоследней оболочкой). Состоит из элементов с 3 по 12 группы.
- Лантаниды — это элементы с атомными номерами от 58 до 71, и эта серия известна как серия лантанидов. Он спрятан под основным столом.
- Актиниды — это элементы с атомными номерами в диапазоне от 90 до 103, и эта серия известна как серия актинидов. Он также указан отдельно с серией лантанидов в нижней части основной таблицы.
- Инертные газы, часто называемые благородными газами, представляют собой элементы с полностью заполненными валентными оболочками.
- Количество оболочек атомов элемента определяет его номер периода.
 Например, в элементе третьего периода (K, L, M) присутствуют три оболочки.
Например, в элементе третьего периода (K, L, M) присутствуют три оболочки. - Все элементы имеют различную электронную конфигурацию с течением времени. Отсюда и разные их характеристики.
Текущая версия таблицы Менделеева — это длинная версия, которая широко используется во всем мире. В периодической таблице этого типа горизонтальные строки называются периодами, а вертикальные столбцы — группами. Группы образованы элементами, атомы которых имеют сходную электрическую структуру внешней оболочки. Ранее группы обозначались как IA,…VIIIA, VIII, IB…VIIB и 0. Однако теперь они известны как 1, 2, 3,…18. Семь горизонтальных строк текущей периодической таблицы известны как периоды. Период элемента определяется квантовым числом «n». Одно из четырех квантовых чисел является главным квантовым числом (n) (n, l, m и s). Он предоставляет информацию о фундаментальной электронной оболочке. Например, если n=3, основная оболочка будет обозначена как 3.
- Периоды — это горизонтальные строки в современной или длинной форме периодической таблицы.

- Периодическая таблица состоит из семи периодов, пронумерованных 1, 2, 3, 4, 5, 6 и 7 сверху вниз. Начальный период состоит всего из двух элементов: водорода и гелия. В каждом из второго и третьего периодов по восемь элементов. В каждом из четвертого и пятого периодов по 18 элементов.
- С другой стороны, шестой период состоит из 32 элементов.
- Седьмой период периодической таблицы теперь содержит четыре новых элемента.
- Элементы: 113-нихоний, 115-московий, 117-теннессин и 118-оганесон. С этим добавлением в 7-м периоде теперь 32 элемента. Кроме того, длинная форма таблицы Менделеева имеет отдельную панель внизу.
- Он состоит из 14 элементов шестого периода, известных как лантаноиды. В седьмом периоде насчитывается 14 элементов, известных как актиноиды.
- Каждая точка представляет собой количество оболочек или энергетических уровней в атоме элемента.

Работа Мозли, несомненно, продемонстрировала, что свойства элементов хорошо объясняются и что большинство аномалий и изъянов в периодической таблице Менделеева исчезают, когда основа классификации меняется с атомных масс на атомные числа. Это приводит к Периодическому современному закону, который гласит:
Физические и химические свойства элементов являются постоянной функцией их атомных номеров. Для устранения недостатков периодической таблицы Менделеева был предложен ряд таблиц классификации элементов на основе современного периодического закона. Полная периодическая таблица, также известная как таблица Бора, является наиболее широко используемой из этих различных таблиц.
Поскольку периодическая таблица основана на схеме Бора, разделяющей элементы на четыре типа в зависимости от их электронной конфигурации, она представляет собой табличное расположение элементов в строках и столбцах в порядке возрастания атомного номера, подчеркивая регулярное повторение свойств элементов. . Базовая структура периодической таблицы состоит в ее разделении на строки и столбцы.
. Базовая структура периодической таблицы состоит в ее разделении на строки и столбцы.
Получите ответы на самые важные вопросы по физике, химии, математике и биологии.
Полная форма периодической таблицы элементовФизические и химические свойства элементов являются периодическими функциями их атомных номеров в соответствии с текущим периодическим законом. Элементы расположены в порядке возрастания атомного номера. Связанные атрибуты элементов группируются. Более фундаментальное свойство определяет расположение элементов, атомный номер. Положение элемента в этой периодической таблице связано с электронной конфигурацией его атома. Он объясняет сходства и различия свойств элементов с точки зрения электронных конфигураций и долгосрочные тенденции в химических свойствах.
Они расположены в порядке возрастания атомного номера. Точность может быть достигнута при предсказании свойств элементов и их соединений. Когда элементы расположены в порядке возрастания атомных номеров, все недостатки периодической таблицы Менделеева устраняются. Они имеют сходные химические свойства, поскольку имеют одинаковую внешнюю электронную конфигурацию, т. е. одинаковое число валентных электронов. Они имеют градации из-за различного притяжения ядра и внешних валентных электронов по мере продвижения вниз по группе.
Они имеют сходные химические свойства, поскольку имеют одинаковую внешнюю электронную конфигурацию, т. е. одинаковое число валентных электронов. Они имеют градации из-за различного притяжения ядра и внешних валентных электронов по мере продвижения вниз по группе.
- Первый период: Он состоит из двух элементов, H и He. Он известен как самый короткий период.
- Второй период: Он состоит из восьми элементов от Li до Ne. Его называют коротким периодом. Элементы второго периода также называют элементами моста.
- Третий период, также известный как короткий период, содержит восемь элементов в диапазоне от Na до Ar. Элементы этого периода также называют типичными элементами.
- Четвертый период: содержит 18 элементов от K до Kr и известен как длинный период.
- Пятый период: также содержит 18 элементов от Rb до Xe. Это называется долгим периодом.
- Шестой период содержит 32 элемента от Cs до Kr. Это самый длительный период.
- Седьмой период: Это неполный период с 29 элементами от Fr до Uuo.

Осуществите свою мечту об ИИТ с Infinity Learn.
Преодолейте NEET с помощью программы обучения, ориентированной на результат, от Infinity Learn.
Часто задаваемые вопросы
Что такое полная таблица Менделеева?
Современная периодическая таблица, также известная как полная форма, основана на современном периодическом законе. Таблица представляет собой расположение элементов в порядке возрастания атомного номера.
Как расположены элементы в полной форме таблицы Менделеева?
Элементы расположены в длинной форме периодической таблицы, чтобы увеличить их атомный номер. Элементы каждой группы имеют одинаковое количество валентных электронов, поэтому их свойства схожи.
В чем разница между полной формой таблицы Менделеева и современной таблицей Менделеева?
Нет, нет никакой разницы между полной формой периодической таблицы и современной периодической таблицей. Менделеев предложил первую концепцию таблицы Менделеева. Эта новая версия периодической таблицы известна как длинная форма периодической таблицы, которую мы теперь называем современной периодической таблицей.
Менделеев предложил первую концепцию таблицы Менделеева. Эта новая версия периодической таблицы известна как длинная форма периодической таблицы, которую мы теперь называем современной периодической таблицей.
Теперь вы можете найти ответы на все интересующие вас вопросы и подготовиться к экзаменам на нашем Образовательное приложение – Infinity Learn.
Похожие материалы
Каковы характеристики полной формы периодической таблицы?
Химические сомнения
1. 18 вертикальных столбцов длинной формы таблицы Менделеева называются группами.
2. Некоторые группы имеют типичные названия.
а. Элементы 1 группы называются щелочными металлами.
б. Элементы 2 группы называются щелочноземельными металлами
в. Элементы группы 15 называются пникогенами 9.0005
д. Элементы 16 группы называются халькогенами
е. Элементы 17 группы называются галогенами
Элементы 17 группы называются галогенами
ф. Элементы группы 18 называются благородными газами.
грамм. Элементы группы 11 называются чеканными металлами.
3. 7 горизонтальных строк или столбцов длинной формы периодической таблицы называются периодами. то есть
а) Первый период: Он содержит два элемента, т. е. Н и Не. Это называется кратчайшим периодом
b) Второй период : содержит восемь элементов e. Ли к Не. Его называют коротким периодом. Элементы второго периода также известны как мостовые элементы.
c) Третий период : Он также содержит 8 элементов, то есть от Na до Ar, и известен как короткий период. Элементы этого периода также известны как типичные элементы.
d) Четвертый период : Он содержит 18 элементов, от K до Kr, и это называется долгим периодом.
e) Пятый период : Он также содержит 18 элементов, от Rb до Xe. Это называется долгим периодом.
f) Шестой период : Он состоит из 32 элементов, от Cs до Kr. Этот период является самым продолжительным периодом.
g) Седьмой период : Это неполный период, состоящий из 29 элементов, от Fr до Uuo.
4. Элементы группы 1, 2 и с 13 по 17 называются элементами главной группы. Их также называют репрезентативными или нормальными элементами.
5. Элементы групп с 3 по 12 называются переходными элементами.
6. Элементы с атомным номером от 58 до 71 называются лантаноидами, тогда как элементы с атомным номером от 90 до 103 называются актинидами. Эти элементы также известны как элементы f-блока или элементы внутреннего перехода.
7. Лантаниды (серия 4f) и актиноиды (серия 5f) размещены в двух отдельных строках под основной таблицей Менделеева, чтобы избежать ненужного бокового расширения таблицы Менделеева.
Таблица : Период и уровни энергии в периодической таблице
Страница Physics Wallah Chemistry Doubts состоит из дополнительных вопросов для справки.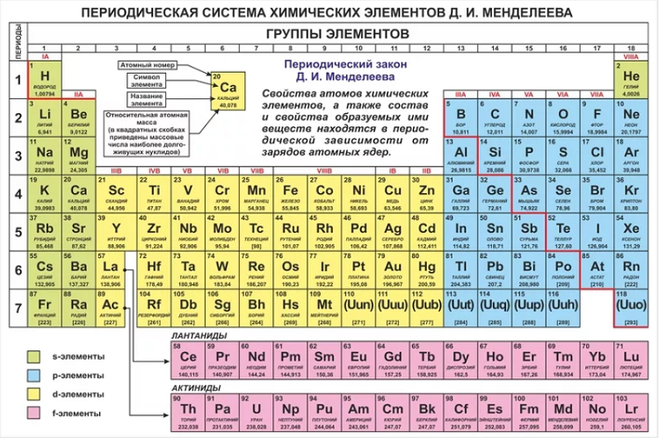
Периоды | Уровень энергии | Количество элементов | Общее название |
1 ст | 1с | 2 (от H до He) | Кратчайший период |
2 и | 2с, 2п | 8 (от Li до Ne) | Короткий период |
3 рд | 3с, 3п | 8 (от Na до Ar) | |
4 -й | 4с 3д 4п | 18 (от К до Кр) | Длительный период |
5 -й | 5с, 4д 5п | 18 (Rb в Xe) | |
6 -й | 6с 4ф 5д 6п | 32 (от Cs до Rn) | самый длинный период |
7 -й | 7с 5ф 6д 7п | 29 | Неполный, вмещает до 32 элементов |
Преимущество длинной формы периодической таблицы:
1. Он основан на более фундаментальном свойстве, т. е. на атомном номере и электронной конфигурации.
Он основан на более фундаментальном свойстве, т. е. на атомном номере и электронной конфигурации.
2. Полностью разделяет металлы и неметаллы.
3. Из-за разделения двух подгрупп разнородные элементы не попадают вместе.
4. Четко соотносит положение элементов с их электронной конфигурацией.
5. Завершение каждого периода более логично.
6. Периодичность свойств можно легко визуализировать.
7. Самым большим преимуществом этой периодической таблицы является то, что ее можно разделить на четыре блока, а именно элементы s, p, d и f-блоков.
8. Такое расположение элементов легко запомнить и воспроизвести.
9. Удаляет аномалии периодической таблицы Манделеева, т.е. K 39 прецедент Ar 40 .
Дефекты полной формы периодической таблицы:
1. Положение Водорода до сих пор не зафиксировано
2. Положение гелия не вполне обосновано, так как его ЭК оправдывает включение его в s-блок.
3. Внутри таблицы не указано положение лантаноидов и актиноидов.
4. Он не отражает точного распределения электронов среди всех орбиталей атомов всего элемента.
Каковы характеристики полной формы периодической таблицы? pdf
Формы периодической таблицы | Периодическая таблица: очень краткое введение
Фильтр поиска панели навигации Oxford AcademicThe Periodic Table: A Very Short Introduction (2nd edn)Very Short IntroductionsChemistryQuantum PhysicsBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Periodic Table: A Very Short Introduction (2nd edn)Very Short IntroductionsChemistryQuantum PhysicsBooksJournals Термин поиска на микросайте
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Еще
Cite
Шерри, Эрик Р.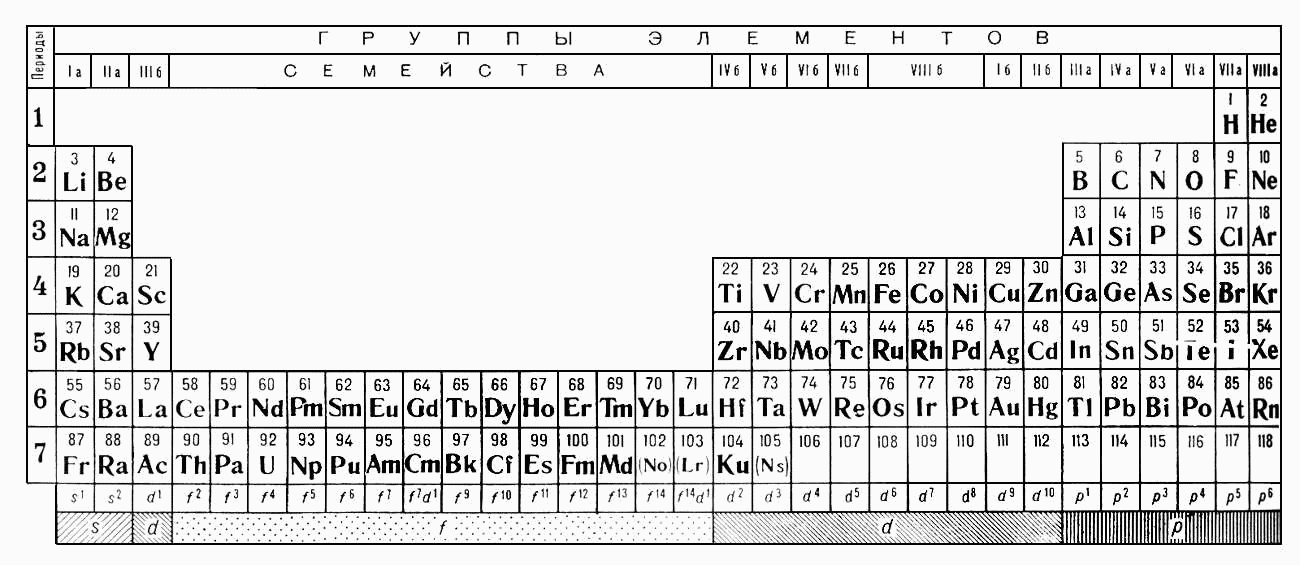 ,
,
‘Формы периодической таблицы’
,
Периодическая таблица: очень короткое введение
, 2 -е изд.
, очень короткие введения
(
Oxford,
2019;
Online EDN,
Oxford Academic
, 25 июля 2019 г.
), https://doi.org/10.1093/actrade/9780198842323.003.0010,
, по состоянию на 6 октября 2022 г.
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Periodic Table: A Very Short Introduction (2nd edn)Very Short IntroductionsChemistryQuantum PhysicsBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Periodic Table: A Very Short Introduction (2nd edn)Very Short IntroductionsChemistryQuantum PhysicsBooksJournals Термин поиска на микросайте
Advanced Search
Abstract
В разделе «Формы периодической таблицы» обсуждаются некоторые из опубликованных периодических таблиц и задается вопрос, существует ли «оптимальная» периодическая таблица.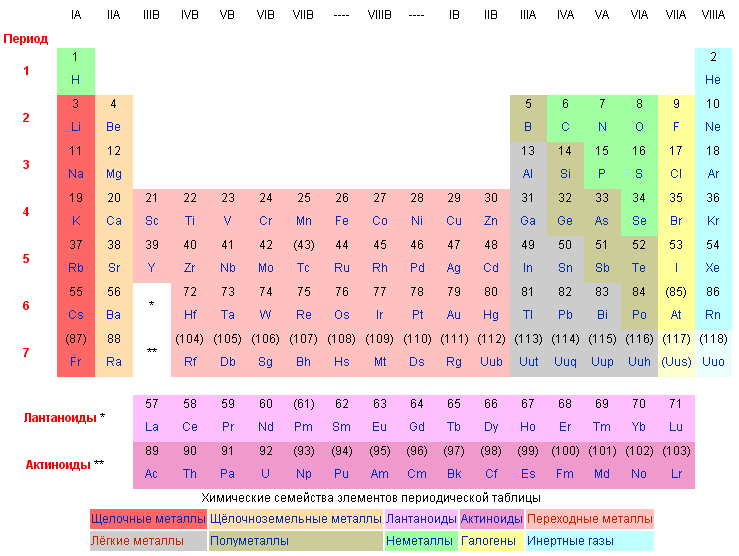 Значимые различия возникают только при изменении порядка элементов. Примеры включают изменение положения водорода и гелия, чтобы лучше отразить их химические свойства, или смещение элементов для формирования триад с аналогичным поведением. Существование оптимальной периодической таблицы в конечном счете зависит от философии человека. Реалисты считают повторение химических свойств объективным фактом и поэтому стремятся к наиболее точному его изображению. Инструменталисты считают, что такие изображения – просто человеческая конструкция и не имеют решающего значения.
Значимые различия возникают только при изменении порядка элементов. Примеры включают изменение положения водорода и гелия, чтобы лучше отразить их химические свойства, или смещение элементов для формирования триад с аналогичным поведением. Существование оптимальной периодической таблицы в конечном счете зависит от философии человека. Реалисты считают повторение химических свойств объективным фактом и поэтому стремятся к наиболее точному его изображению. Инструменталисты считают, что такие изображения – просто человеческая конструкция и не имеют решающего значения.
Ключевые слова: актиний, атомный номер, химия, гелий, водород, ИЮПАК, лоуренсий, лютеций, периодическая таблица, квантовая механика, симметрия
Предмет
ХимияКвантовая физика
СерияКраткие сведения
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Нажмите Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- При посещении сайта учреждения используйте учетные данные, предоставленные вашим учреждением.
 Не используйте личную учетную запись Oxford Academic.
Не используйте личную учетную запись Oxford Academic. - После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Войти с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом.
 Не используйте личную учетную запись Oxford Academic.
Не используйте личную учетную запись Oxford Academic. - После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Вход через личный кабинет
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр учетных записей, вошедших в систему
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.

