Презентация по химии на тему 150 лет периодической таблице Менделеева доклад, проект
150 ЛЕТ ПЕРИОДИЧЕСКОЙ ТАБЛИЦЕ МЕНДЕЛЕЕВА Д.И.
1869-2019
Интересные факты
о периодической таблице Менделеева Д.И.
Периодическая система химических элементов – это классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра.
Интересные факты
о периодической таблице Менделеева Д.И.
Основная идея к 1869 году уже была сформирована Менделеевым, но оформить её в какую-либо упорядоченную систему, наглядно отображающую, что к чему, он долго не мог. Согласно данным биографов Менделеева, он приступил к кропотливой работе над своей таблицей, которая продолжалась трое суток без перерывов на сон.
Перебирались всевозможные способы организации элементов в таблицу.
Периодическая таблица не сильно менялась с 1950-х годов. Однако 2 декабря 2016 года было добавлено сразу четыре новых элемента: нихоний (элемент №113), московий (элемент №115), тенессин (элемент №117) и оганесон (элемент №118). Эти новые элементы получили свои названия только в июне 2016 года, так как потребовалась пятимесячная экспертиза, прежде чем их официально добавили в ПТ.
Интересные факты
о периодической таблице Менделеева Д.И.
Три элемента получили свои названия в честь городов или государств, в которых их удалось получить, а оганесон был назван в честь российского физика-ядерщика Юрия Оганесяна за его вклад в получение этого элемента.
Как правило, названия элементов относятся к одной из пяти основных категорий:
Интересные факты
о периодической таблице Менделеева Д.И.
1. Имена известных учёных, классический вариант – эйнштейний.
2. Место открытия или регистрации. Например, германий, америций, галлий и т. д.
3. Названия планет. Элемент уран был впервые обнаружен вскоре после того, как была открыта планета Уран.
4. Мифология. Титан, названный так в честь древнегреческих титанов, и торий, названный по имени скандинавского бога-громовержца.
Интересные факты
о периодической таблице Менделеева Д.И.
5. Названия, описывающие свойства элементов. Аргон происходит от греческого слова «аргос», что означает «ленивый» или «медленный». Из названия следует предположение, что этот газ не отличается активностью. Бром – это ещё один элемент, название которого происходит от греческого слова.
В периодической таблице присутствует 118 элементов.
Из всего общего списка в природных условиях можно найти лишь 90 элементов.
Оставшиеся 28 элементов синтезируют, начиная с 1937 года. Все эти элементы вы можете найти в таблице. Посмотрите на элементы с 95 по 118, все эти элементы отсутствуют на нашей планете и были синтезированы в лабораториях. То же касается и элементов под номерами 43, 61, 85 и 87.
Интересные факты
о периодической таблице Менделеева Д.И.
Элемент 115 живет меньше секунды.
Большинство изотопов сверхтяжелых элементов (элементов с порядковым номером >100) являются нестабильными и подвергаются распадам в течение очень короткого промежутка времени.
Интересные факты
о периодической таблице Менделеева Д.И.
Так, недавно открытый унунпентий, также известный как элемент 115 и эка-висмут, имеет период полураспада всего около 220-ти миллисекунд.
Радиоактивные элементы двигаются по таблице.
К сожалению, у Менделеева не было возможности встроить в периодическую систему часы, а ведь изменение некоторых элементов во времени — самое обычное дело.
Интересные факты
о периодической таблице Менделеева Д.И.
Так, своей нестабильностью отличаются ядра атомов радиоактивных элементов. Благодаря ней, претерпевая цепочки распадов, эти элементы могут «гулять» по таблице. В продуктах деления урана-235, обнаружено около 300 изотопов различных элементов: от цинка до гадолиния
Некоторые атомы могут «любить друг друга»
Если взять современную периодическую таблицу, вырезать из ее середины столбцы и сложить их пополам группами по 4 элемента, то группы, которые соприкоснутся («поцелуются»), в химическом смысле могут «любить друг друга», то есть взаимодействовать.
Интересные факты
о периодической таблице Менделеева Д. И.
И.
Элементы из этих групп будут иметь комплиментарные (т.е. дополняющие друг друга) структуры, что и делает возможными реакции между ними.
В честь Менделеева назван 101-й элемент Периодической системы – менделевий. Он обозначается символом Md.
Интересные факты
о периодической таблице Менделеева Д.И.
В 1969 году Теодор Сиборг предложил расширенную периодическую таблицу элементов. Нильсом Бором разрабатывалась лестничная (пирамидальная) форма периодической системы.
Интересные факты
о периодической таблице Менделеева Д.И.
Существует и множество других, редко или вовсе не используемых, но весьма оригинальных способов графического отображения Периодической таблицы, при этом учёные предлагают всё новые варианты…
Самая большая таблица Менделеева была установлена на стенах химического факультета в Университете Мурсии в Испании.
Интересные факты
о периодической таблице Менделеева Д.И.
В общей сложности инсталляция занимает в общей сложности около 150 кв. м и состоит из 118 металлических квадратов размером 75х75 см. В периодическую систему включены все известные на сегодняшний день химические элементы
B 2006 году в административном центре города Чикаго из отдельных плакатов была собрана огромная таблица Менделеева, которая простиралась на восемь этажей.
Интересные факты
о периодической таблице Менделеева Д.И.
Не менее удивительной по размерам получилась периодическая система химических элементов в городе Сан-Антонио. В 2016 году ученики более ста школ собрались на стадионе и выложили громадную таблицу Менделеева из отдельных квадратных элементов размером 3,5х4,5 м. Общая площадь составила 2000 кв.м.
Интересные факты
о периодической таблице Менделеева Д. И.
И.
В Санкт-Петербурге Периодическая таблица Менделеева была создана в 1935 году на Московском проспекте, дом 19. Памятник представляет собой выполненную мозаикой на стене дома таблицу химических элементов, которая соответствовала состоянию её при жизни Менделеева и была приведена в последнем прижизненном 8 издании, опубликованном в 1906 году. На ней элементы, открытые при жизни учёного, изображены красным цветом, а элементы, открытые с 1907 года по 1934 год – синим цветом. Выполнен памятник в 1935 году по инициативе Сталина. Ранее, в 1932 году, здесь был установлен памятник Дмитрию Ивановичу Менделееву.
Интересные факты
о периодической таблице Менделеева Д.И.
Интересные факты
о периодической таблице Менделеева Д.И.
Интересный памятник Дмитрию Менделееву есть в Челябинской области в городе Верхний Уфалей. Ученый заезжал сюда в 1899 году. Осмотрев здешнее производство и разработки, он воскликнул: «Да у вас тут вся моя таблица!». В честь этого поставлен памятник Менделееву на фоне его таблицы.
Ученый заезжал сюда в 1899 году. Осмотрев здешнее производство и разработки, он воскликнул: «Да у вас тут вся моя таблица!». В честь этого поставлен памятник Менделееву на фоне его таблицы.
Интересные факты
о периодической таблице Менделеева Д.И.
Памятник Менделееву и его таблице есть в Словакии. Находится он перед химическим факультетом Словацкого технологического университета в Братиславе.
Интересные факты
о периодической таблице Менделеева Д.И.
в 2017 году памятник Менделееву украсил бульвар Менделеева в Мурино Ленинградской области. Памятник «Сон Менделеева» напоминает о знаменитом сне ученого, в котором он увидел периодическую таблицу элементов. Футуристическая скульптура изображает химические элементы, над которыми парит фигура Дмитрия Менделеева.
Интересные факты
о периодической таблице Менделеева Д. И.
И.
СПАСИБО ЗА ВНИМАНИЕ!
Любите химию – это наша жизнь!
Периодическая таблица Д.И. Менделеева Своя игра презентация, доклад, проект
Периодическая таблица Д.И. Менделеева
Своя игра
10
10
10
20
20
20
30
30
30
40
40
40
50
50
50
Факты из жизни
Д.И. Менделеева
Названия химических элементов
Факты о таблице Менделеева
Факты из жизни Д.И. Менделеева – 10
Сколько детей было в семье Менделеевых?
17 детей
Факты из жизни Д. И. Менделеева – 20
И. Менделеева – 20
Какова причина обучения в течении двух лет на первом курсе ВУЗа?
Болезнь
Факты из жизни Д.И. Менделеева – 30
Сколько было детей у ученого?
5 детей: 3 сына и 2 дочери
Факты из жизни Д.И. Менделеева – 40
В каком году была опубликована первая научная работа Д. И. Менделеева?
1854 год
Факты из жизни Д.И. Менделеева – 50
Что в детском возрасте привлекало Митю и послужило формированию интереса к знаниям в период жизни в Аремзянке?
Наблюдение за стеклодувным мастерством на стекольном заводе Василия Корнильева, дяди Менделеева
Названия химических элементов – 10
Какие химические элементы названы в честь частей света?
Европий(№63) и Америций(№95)
Названия химических элементов – 20
Перечислите минимум 4 элемента, названных в честь ученых
Резерфордий №104, Кюрий №96, Эйнштейний №99, Фермий №100, Менделевий №101, Нобелий №102
Названия химических элементов – 30
Химический элемент, названный в честь
Солнца –
Луны-
Земли –
Гелий
Селен
Теллур
Названия химических элементов – 40
Этот химический элемент назван по имени мифологических существ (в переводе с немецкого – домовой, гном), проделками которых в Средние века считался ядовитый дым, который выделялся при обжигании руды.
Кобальт: существа Кобольды
Названия химических элементов – 50
Перечислите химические элементы, названные в честь столиц
Гольмий назван в честь столицы Швеции.
Гафний назван в честь столицы Дании.
Лютеций назван в честь столицы Франции, латинское название Парижа.
Факты о таблице Менделеева – 10
Из скольки элементов изначально состояла таблица?
Из 56-ти элементов
Факты о таблице Менделеева – 20
Что из перечисленного не относится к металлам: щелочные металлы, щелочноземельные, полуметаллы, переходные металлы, постпереходные, лантаноиды, актиноиды ?
Полуметаллы
Факты о таблице Менделеева – 30
Сколько лет в этом году исполняется Периодической таблице Д. И. Менделеева и ее автору?
И. Менделеева и ее автору?
150 и 185 лет
Факты о таблице Менделеева – 40
Перечислите минимум 5 закономерностей в группах (с увеличением порядкового номера)
увеличивается заряд ядра
увеличивается радиус атомов (только в А-группах)
уменьшается электроотрицательность (только в А-группах)
ослабевают окислительные свойства простых веществ ( в А-гр.)
усиливаются восстановительные свойства простых веществ ( в А-гр.)
возрастает основный характер гидроксидов и соответствующих оксидов ( в А-гр.)
снижается устойчивость водородных соединений (в А-группах).
…
Факты о таблице Менделеева – 50
Перечислите минимум 5 закономерностей в периодах (с увеличением порядкового номера)
увеличивается заряд ядра
увеличивается число внешних электронов
уменьшается радиус атомов
увеличивается прочность связи электронов с ядром (энергия ионизации)
увеличивается электроотрицательность
усиливаются окислительные свойства простых веществ (“неметалличность”)
ослабевают восстановительные свойства простых веществ
Скачать презентацию
В Париже состоялась церемония открытия Международного года Периодической таблицы химических элементов
2019 год провозглашен Генеральной ассамблеей ООН Международным
годом Периодической таблицы химических элементов. Это масштабное
событие посвящено 150-летию открытия Периодического закона
химических элементов великим русским ученым Д.И.
Менделеевым.
Это масштабное
событие посвящено 150-летию открытия Периодического закона
химических элементов великим русским ученым Д.И.
Менделеевым.
Участниками и гостями открытия Международного года Периодической таблицы в штаб-квартире ЮНЕСКО в Париже стали более 1300 человек из 80 стран мира. Среди них – ученые, политики, руководители международных, научных, образовательных организаций, представители бизнес-компаний и общественных объединений.
В торжественной церемонии приняли участие: Министр науки и высшего образования РФ Михаил Котюков, президент Российской академии наук Александр Сергеев, президент Академии наук Франции Пьер Корволь, генеральный директор ЮНЕСКО Одри Азуле.
Генеральным партнером Международного года Периодической таблицы химических элементов в России выступает Благотворительный Фонд Алишера Усманова «Искусство, наука и спорт».
«Во всем мире Периодическая таблица химических элементов
ассоциируется с именем Дмитрия Ивановича Менделеева, что является
признанием феноменального открытия, которое стало единым языком
всех естественных наук. И именно поэтому ученые разных
специальностей – химики, физики, астрономы, геологи, медики,
биологи и географы – считают эту таблицу своей. Роль сделанного
150 лет назад открытия не только не стирается временем, но и
продолжает расти. Гигантская работа ученого по осмыслению всего
доступного на тот период времени пласта знаний привела к созданию
единой стройной системы, не только объясняющей взаимную связь
между элементами, но и позволяющей предсказывать существование
новых химических элементов», – сказал Михаил
Котюков.
И именно поэтому ученые разных
специальностей – химики, физики, астрономы, геологи, медики,
биологи и географы – считают эту таблицу своей. Роль сделанного
150 лет назад открытия не только не стирается временем, но и
продолжает расти. Гигантская работа ученого по осмыслению всего
доступного на тот период времени пласта знаний привела к созданию
единой стройной системы, не только объясняющей взаимную связь
между элементами, но и позволяющей предсказывать существование
новых химических элементов», – сказал Михаил
Котюков.
Президент Российской академии наук РАН Александр Сергеев
добавил: «Сегодня очень важный день для России.
Важный, во-первых, благодаря Дмитрию Ивановичу Менделееву и его
открытию. Во-вторых, важно то, что наша страна выступила
инициатором Международного года Таблицы химических элементов, и
это предложение было единогласно поддержано международным
сообществом. И наконец, мы видим большой вклад в организацию и
проведение Международного года, который внесли со своей стороны
наша власть и наш бизнес.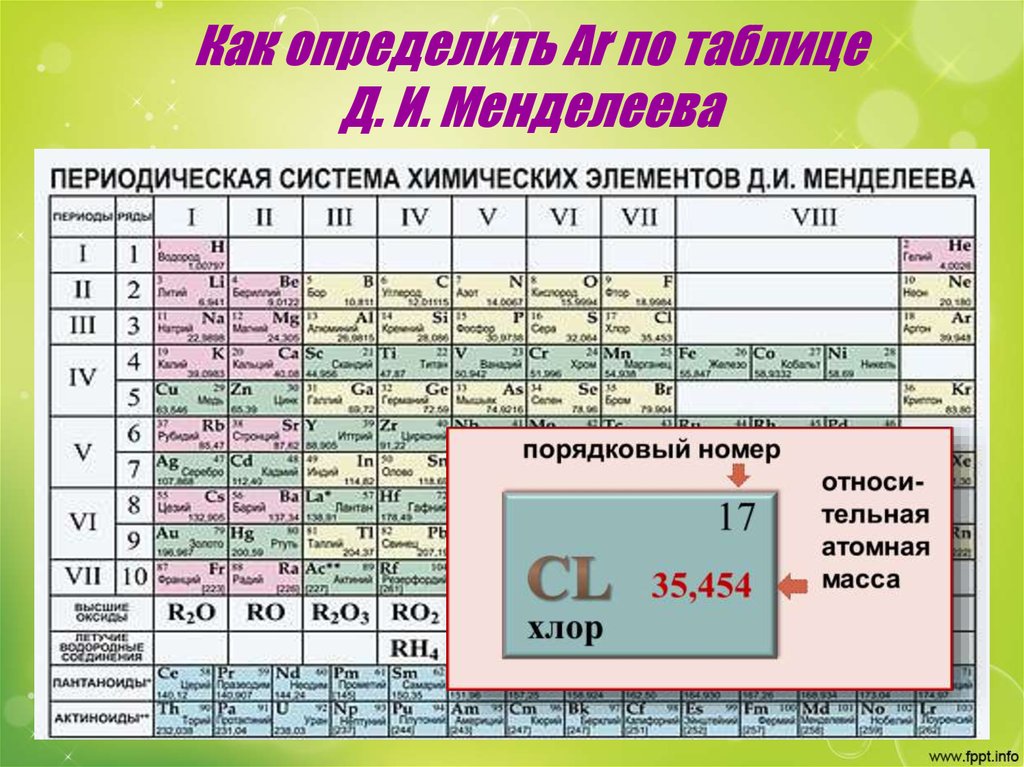 Поэтому роль и значение России в
проведении Международного года Таблицы чрезвычайно
велики».
Поэтому роль и значение России в
проведении Международного года Таблицы чрезвычайно
велики».
В рамках церемонии состоялись выступления всемирно известных ученых. Так, Нобелевский лауреат по химии 2016 года, профессор Бен Феринга представил свой доклад на тему «Периодическая таблица для общества и будущего». Научный руководитель Лаборатории ядерных реакций имени Г.Н. Флерова, профессор Юрий Оганесян, именем которого был назван 118-й элемент Таблицы «оганесон», выступил с лекцией о новых элементах Периодической таблицы. Вице-президент Лондонского королевского общества, автор серии «Видео о периодической таблице», сэр Мартин Полякофф в своей лекции на тему «Менделеев – подарок для образования» отметил роль Периодической таблицы в популяризации науки и образования.
Большой интерес представляли выступления известных ученых на тему
космоса и происхождения химических элементов. Так, профессор РАН,
заместитель директора Института космических исследований РАН
Александр Лутовинов прочел лекцию «Звезды: от колыбели до
могилы», а лауреат премии Кавли 2018 Эвина Ван Дисхук рассказала
о происхождении элементов в космическом пространстве. Также с
докладами и лекциями о Таблице Менделеева выступили молодые
талантливые ученые из Европы, Африки, Азии, Латинской Америки и
стран Востока. Дополнили программу научные шоу и музыкальные
спектакли.
Также с
докладами и лекциями о Таблице Менделеева выступили молодые
талантливые ученые из Европы, Африки, Азии, Латинской Америки и
стран Востока. Дополнили программу научные шоу и музыкальные
спектакли.
В рамках мероприятий, приуроченных к церемонии открытия Международного года Периодической таблицы химических элементов, в Париже с 28 января начала свою работу международная выставка, посвященная химии и современным достижениям в области химической науки. Свои уникальные экспозиции на выставке представили: Россия, Великобритания, Франция, Нидерланды, США, Швейцария, Китай, Япония и Шотландия.
Самой масштабной частью международной выставки стала экспозиция России, где в увлекательной форме продемонстрированы не только достижения ведущих российских научно-исследовательских групп в области химии и материаловедения, но и интерактивная Периодическая таблица химических элементов.
Участниками российской экспозиции стали ведущие вузы и
инновационные, научно-исследовательские и образовательные
организации страны, такие как – МГУ имени М. В. Ломоносова,
Российский химико-технологический университет имени Д.И.
Менделеева, Объединенный Институт Ядерных Исследований (в знак
признания заслуг учёных этого института названы новые элементы
Таблицы – дубний, флеровий, московий и оганесон), компания
«ФосАгро» и многие другие. На каждом из стендов посетители
выставки могут поучаствовать в экспериментах по созданию и
применению различных материалов и химических элементов, а также
пообщаться с учеными-исследователями в области синтетической
химии и современного материаловедения.
В. Ломоносова,
Российский химико-технологический университет имени Д.И.
Менделеева, Объединенный Институт Ядерных Исследований (в знак
признания заслуг учёных этого института названы новые элементы
Таблицы – дубний, флеровий, московий и оганесон), компания
«ФосАгро» и многие другие. На каждом из стендов посетители
выставки могут поучаствовать в экспериментах по созданию и
применению различных материалов и химических элементов, а также
пообщаться с учеными-исследователями в области синтетической
химии и современного материаловедения.
Всероссийский фестиваль науки NAUKA 0+ разместил в международной
экспозиции свою Интерактивную химическую выставку – с зоной
виртуальной реальности и новейшими технологиями образования,
зоной научных экспериментов, IT-зоной с возможностью создания
своей собственной Таблицы элементов, зоной «зеленой химии», а
также зоной научного искусства, где представлены художественные
работы на тему химии. Кроме того, посетители этой выставки могут
сделать сэлфи с Д. И. Менделеевым в химической лаборатории 19
века, выпить коктейль в молекулярном баре и протестировать
химических роботов.
И. Менделеевым в химической лаборатории 19
века, выпить коктейль в молекулярном баре и протестировать
химических роботов.
Международная химическая выставка в рамках открытия Года Периодической таблицы в Париже продлится до 30 января. Затем экспозиция переместится в Москву и продолжит свою работу в дни открытия Международного года Периодической таблицы в России.
Церемония открытия Международного года Периодической таблицы химических элементов в России состоится 6 февраля 2019 года в Москве и будет приурочена ко Дню российской науки и одновременно Дню рождения Д.И. Менделеева.
Официальным оператором церемоний открытия Международного года Периодической таблицы химических элементов в Париже и Москве выступает Всероссийский фестиваль науки NAUKA 0+. Главной темой Фестиваля науки в 2019 году объявлена Периодическая таблица Менделеева.
В рамках Международного года во всех регионах России планируется
проведение более 500 научно-популярных и образовательных
мероприятий, посвященных 150-летию выдающегося открытия Д. И.
Менделеева и направленных на привлечение внимания школьников,
студентов и молодежи в целом к науке и ее достижениям.
И.
Менделеева и направленных на привлечение внимания школьников,
студентов и молодежи в целом к науке и ее достижениям.
Проведение в 2019 году Международного года Периодической таблицы химических элементов имеет особое значение для России. Это событие будет способствовать международному признанию заслуг великого русского ученого Д.И. Менделеева, а также укреплению престижа и популяризации отечественной науки.
Периодический закон Менделеева, система химических элементов, современная формулировка
4.6
Средняя оценка: 4.6
Всего получено оценок: 770.
4.6
Средняя оценка: 4.6
Всего получено оценок: 770.
В 1871 году был сформулирован периодический закон Менделеева. К этому времени науке было известно 63 элемента, и Дмитрий Иванович Менделеев упорядочил их на основе относительной атомной массы. Современная периодическая таблица значительно расширилась.
История
В 1869 году, работая над учебником химии, Дмитрий Менделеев столкнулся с проблемой систематизации материала, накопленного за много лет разными учёными – его предшественниками и современниками. Ещё до работы Менделеева предпринимались попытки систематизировать элементы, что послужило предпосылками разработки периодической системы.
Ещё до работы Менделеева предпринимались попытки систематизировать элементы, что послужило предпосылками разработки периодической системы.
Поиски классификации элементов кратко описаны в таблице.
Год | Учёный | Что сделано |
1829 | Иоганн Дёберейнер | Объединил элементы со схожими химическими свойствами в триады. Например, одну триаду составили Li, Na, K. Таблица включала пять триад |
1862 | Александр Шанкуртуа | Создал «земную спираль», расположив 50 элементов по спирали |
1864 | Джон Ньюлендс | Расположил элементы в порядке возрастания атомных масс и выявил сходство между каждым восьмым элементом. Закономерность была названа законом октав |
1864 | Лотар Мейер | Распределил 28 элементов по шести столбцам в соответствии с их валентностью |
Менделеев упорядочил элементы по относительной атомной массе, расположив их в порядке возрастания.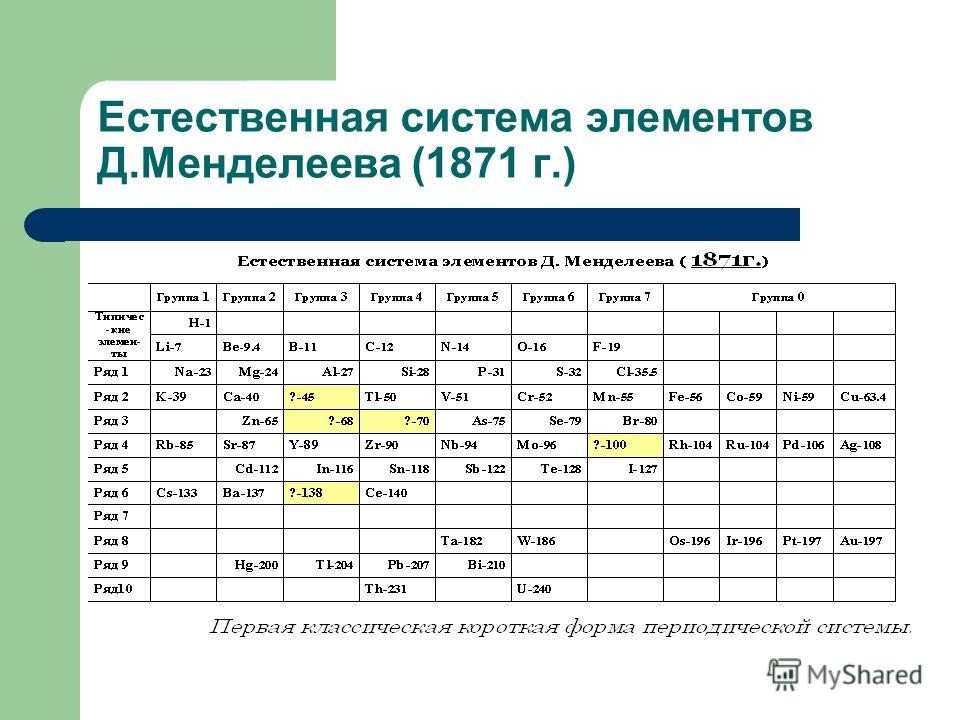 Всего получилось девятнадцать горизонтальных и шесть вертикальных рядов. Это была первая редакция периодической таблицы элементов. С этого начинается история открытия периодического закона.
Всего получилось девятнадцать горизонтальных и шесть вертикальных рядов. Это была первая редакция периодической таблицы элементов. С этого начинается история открытия периодического закона.
Учёному понадобилось почти три года, чтобы создать новую, более совершенную таблицу. Шесть столбцов элементов превратились в горизонтальные периоды, каждый из которых начинался щелочным металлом, а заканчивался неметаллом (инертные газы ещё не были известны). Горизонтальные ряды образовали восемь вертикальных групп.
В отличие от своих коллег Менделеев использовал два критерия распределения элементов:
- атомную массу;
- химические свойства.
Оказалось, что между двумя этими критериями прослеживается закономерность. После определённого количества элементов с возрастающей атомной массой, свойства начинают повторяться.
Рис. 2. Таблица, составленная Менделеевым.Изначально теория не выражалась математически и не могла полностью подтвердиться экспериментально. Физический смысл закона стал понятен только после создания модели атома. Смысл заключается в повторении структуры электронных оболочек при последовательном увеличении зарядов ядер, что отражается на химических и физических свойствах элементов.
Физический смысл закона стал понятен только после создания модели атома. Смысл заключается в повторении структуры электронных оболочек при последовательном увеличении зарядов ядер, что отражается на химических и физических свойствах элементов.
Закон
Установив периодичность изменений свойств с увеличением атомной массы, Менделеев в 1871 году сформулировал периодический закон, ставший основополагающим в химической науке.
Дмитрий Иванович определил, что свойства простых веществ находятся в периодической зависимости от относительных атомных масс.
Наука XIX века не обладала современными знаниями об элементах, поэтому современная формулировка закона несколько отличается от менделеевской. Однако суть остаётся прежней.
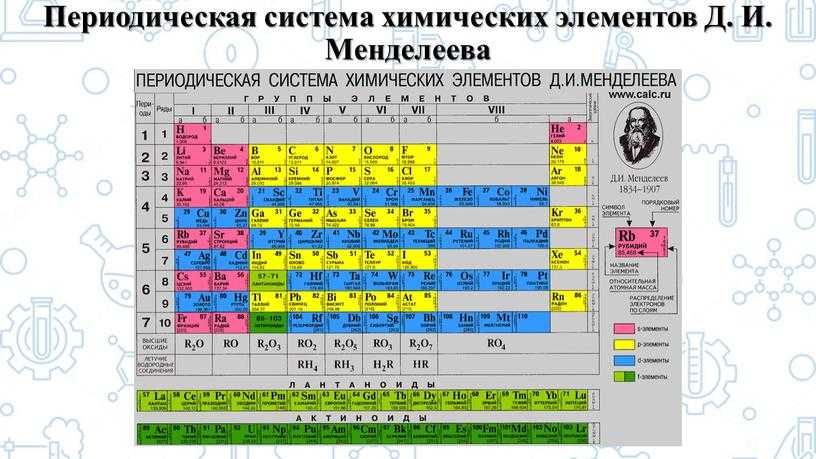
С дальнейшим развитием науки было изучено строение атома, что повлияло на формулировку периодического закона. Согласно современному периодическому закону свойства химических элементов зависят от зарядов атомных ядер.
Таблица
Со времён Менделеева созданная им таблица значительно преобразилась и стала отражать практически все функции и характеристики элементов.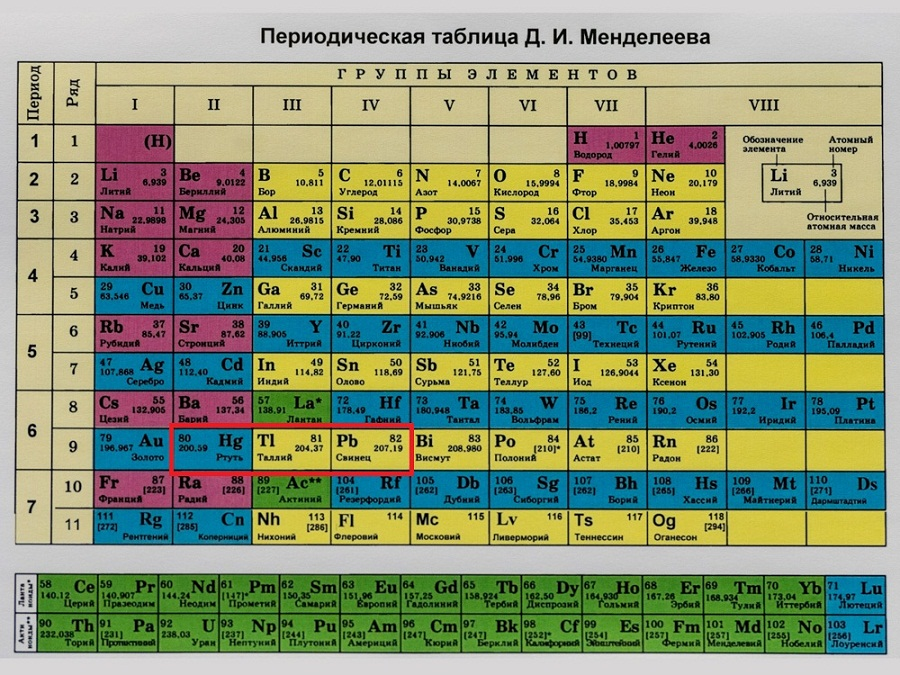 Умение пользоваться таблицей необходимо для дальнейшего изучения химии. Современная таблица представлена в трёх формах:
Умение пользоваться таблицей необходимо для дальнейшего изучения химии. Современная таблица представлена в трёх формах:
- короткая – периоды занимают по две строчки, а водород часто относят к 7 группе;
- длинная – изотопы и радиоактивные элементы вынесены за пределы таблицы;
- сверхдлинная – каждый период занимает отдельную строку.
Короткая таблица – наиболее устаревший вариант, который был отменён в 1989 году, но по-прежнему используется во многих учебниках. Длинная и сверхдлинная формы признаны международным сообществом и используются по всему миру. Несмотря на установленные формы, учёные продолжают совершенствовать периодическую систему, предлагая новейшие варианты.
Что мы узнали?
Периодический закон и периодическая система Менделеева были сформулированы в 1871 года. Менделеев выявил закономерности свойств элементов и упорядочил их на основе относительной атомной массы.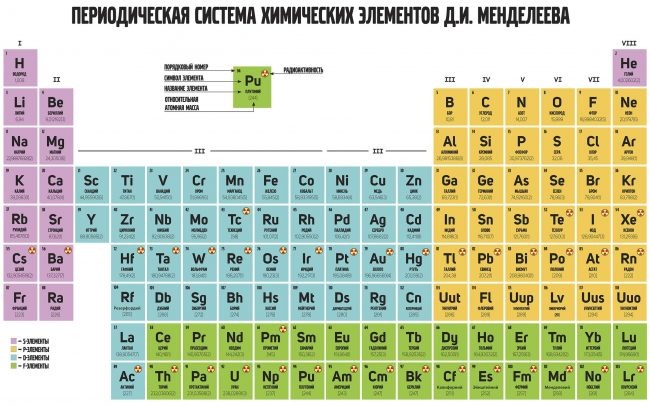 С возрастанием массы менялись, а затем повторялись свойства элементов. Впоследствии таблица была дополнена, а закон скорректирован в соответствии с современными знаниями.
С возрастанием массы менялись, а затем повторялись свойства элементов. Впоследствии таблица была дополнена, а закон скорректирован в соответствии с современными знаниями.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
Никита Губский
8/10
Александр Котков
10/10
Александр Котков
10/10
Александр Котков
10/10
Сергей Макаров
7/10
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 770.
А какая ваша оценка?
Дмитрий Менделеев – биография, фото, личная жизнь, интересные факты
Биография
Менделеев Дмитрий Иванович – русский ученый, гениальный химик, физик, исследователь в области метрологии, гидродинамики, геологии, глубокий знаток промышленности, приборостроитель, экономист, воздухоплаватель, педагог, общественный деятель и оригинальный мыслитель.
Детство и юность
Великий ученый родился в 1834 году, 8 февраля, в Тобольске. Отец Иван Павлович был директором окружных училищ и Тобольской гимназии, происходил из рода священника Павла Максимовича Соколова, русского по национальности.
Дмитрий Менделеев в детстве и молодостиФамилию Иван поменял в детстве, будучи учащимся Тверской семинарии. Предположительно, это было сделано в честь его крестного отца, помещика Менделеева. Позднее неоднократно затрагивался вопрос о национальной принадлежности фамилии ученого. По одним сведениям, она свидетельствовала о еврейских корнях, по другим – о немецких. Сам Дмитрий Менделеев рассказывал о том, что фамилию присвоил Ивану его педагог из семинарии. Юноша произвел удачный обмен и тем прославился среди однокашников. По двум словам – «мену делать» – Иван Павлович был вписан в учебную ведомость.
Родители Дмитрия МенделееваМать Мария Дмитриевна (в девичестве Корнильева) занималась воспитанием детей и домашним хозяйством, имела репутацию интеллигентной и умной женщины. Дмитрий был в семье самым младшим, последним из четырнадцати детей (по другой информации – последним из семнадцати детей). В 10-летнем возрасте мальчик лишился отца, который ослеп и вскоре умер.
Дмитрий был в семье самым младшим, последним из четырнадцати детей (по другой информации – последним из семнадцати детей). В 10-летнем возрасте мальчик лишился отца, который ослеп и вскоре умер.
Во время учебы в гимназии способностей Дмитрий не проявил, сложнее всего ему давалась латынь. Любовь к науке прививала мать, она же участвовала в формировании его характера. Мария Дмитриевна увезла сына учиться в Петербург.
Дмитрий Менделеев в молодостиВ 1850 году в Петербурге юноша поступает в Главный пединститут на отделение естественных наук физмата. Его преподавателями были профессора Э. Х. Ленц, А. А. Воскресенский и Н. В. Остроградский.
Во время учебы в институте (1850-1855 годы) Менделеев демонстрирует незаурядные способности. Будучи студентом, он публикует статью «Об изоморфизме» и ряд химических анализов.
Наука
В 1855-м Дмитрий получает диплом с золотой медалью и направление в Симферополь. Здесь он работает старшим учителем гимназии. С началом Крымской войны Менделеев перебирается в Одессу и получает должность преподавателя в лицее.
В 1856-м он снова в Петербурге. Учится в университете, защищает диссертацию, преподает химию. Осенью защищает еще одну диссертацию и назначается приват-доцентом университета.
В 1859-м Менделеева отправляют в командировку в Германию. Работает в университете Гейдельберга, обустраивает лабораторию, исследует капиллярные жидкости. Здесь им были написаны статьи «О температуре абсолютного кипения» и «О расширении жидкостей», открыто явление «критическая температура».
Дмитрий МенделеевВ 1861-м ученый возвращается в Петербург. Создает учебник «Органическая химия», за что удостаивается Демидовской премии. В 1864-м он уже профессор, а спустя два года возглавляет кафедру, преподает и работает над «Основами химии».
В 1869-м представляет периодическую систему элементов, совершенствованию которой посвятил всю жизнь. В таблице Менделеев представил атомную массу девяти элементов, позднее добавил в свод группу благородных газов и оставил место для элементов, которые еще предстояло открыть. В 90-е годы Дмитрий Менделеев внес свой вклад в открытие явления радиоактивности. Периодический закон включал в себя доказательства связи свойств элементов и их атомного объема. Теперь рядом с каждой таблицей химических элементов находится фото первооткрывателя.
В 90-е годы Дмитрий Менделеев внес свой вклад в открытие явления радиоактивности. Периодический закон включал в себя доказательства связи свойств элементов и их атомного объема. Теперь рядом с каждой таблицей химических элементов находится фото первооткрывателя.
В 1865–1887 годах разрабатывает гидратную теорию растворов. В 1872-м начинает изучать упругость газов, спустя два года выводит уравнение идеального газа. Среди достижений Менделеева этого периода – создание схемы дробной перегонки нефтепродуктов, применение цистерн и трубопровода. При содействии Дмитрия Ивановича сжигание черного золота в топках полностью прекратилось. Фраза ученого «Сжигать нефть — все равно, что топить печку ассигнациями» стала афоризмом.
Портрет Д.И. Менделеева в мантии доктора права Эдинбургского университета. Илья РепинЕще одной сферой деятельности ученого стали географические исследования. В 1875 году Дмитрий Иванович побывал на Парижском международном географическом конгрессе, где представил на суд свое изобретение – дифференциальный барометр-высотомер. В 1887 году ученый участвовал в путешествии на аэростате в верхние слои атмосферы для наблюдения полного солнечного затмения.
В 1887 году ученый участвовал в путешествии на аэростате в верхние слои атмосферы для наблюдения полного солнечного затмения.
В 1890-м ссора с высокопоставленным чиновником стала причиной ухода Менделеева из университета. В 1892-м химик изобретает методику получения бездымного пороха. Одновременно с этим его назначают хранителем Депо образцовых мер и весов. Здесь он возобновляет прототипы фунта и аршина, занимается вычислениями по сравнению русских и английских эталонов мер.
Прототипы фунта и аршинаПо инициативе Менделеева в 1899 году факультативно вводится метрическая система мер. В 1905, 1906 и 1907 годах ученого выдвигают кандидатом на Нобелевскую премию. В 1906-м году Нобелевским комитетом премия присуждается Менделееву, но Королевская академия наук Швеции это решение не подтвердила.
Менделеев, являющийся автором более чем полутора тысяч трудов, имел огромный научный авторитет в мире. За свои заслуги ученый был удостоен многочисленных научных званий, российских и зарубежных наград, был почетным членом ряда научных обществ на родине и за границей.
Личная жизнь
В юности с Дмитрием случился неприятный случай. Ухаживания за девушкой Соней, с которой тот был знаком с детства, закончились помолвкой. Но изнеженная красавица к венцу так и не пошла. Накануне свадьбы, когда подготовка уже шла полным ходом, выходить замуж Сонечка отказалась. Девушка посчитала, что нет смысла что-то менять, если жизнь и так хороша.
Дмитрий МенделеевДмитрий болезненно переживал разрыв с невестой, но жизнь шла своим чередом. От тяжких дум его отвлекла поездка за границу, чтение лекций и верные друзья. Возобновив отношения с Феозвой Никитичной Лещевой, с которой был знаком ранее, стал с ней встречаться. Девушка была старше Дмитрия на 6 лет, но выглядела молодо, поэтому разница в возрасте была незаметной.
Дмитрий Менделеев с первой женой ФеозвойВ 1862-м они стали мужем и женой. Первая дочь Маша родилась в 1863 году, но прожила только несколько месяцев. В 1865-м родился сын Володя, спустя три года – дочь Оля. К детям Дмитрий Иванович был привязан, но времени им уделял мало, так как жизнь была посвящена научной деятельности. В браке, заключенном по принципу «стерпится-слюбится», он не был счастлив.
В браке, заключенном по принципу «стерпится-слюбится», он не был счастлив.
В 1877-м Дмитрий знакомится с Анной Ивановной Поповой, которая стала для него человеком, способным в трудную минуту поддержать умным словом. Девушка оказалась творчески одаренным человеком: училась в консерватории игре на фортепиано, позже в Академии художеств.
Дмитрий Иванович устраивал у себя молодежные «пятницы», где и познакомился с Анной. «Пятницы» трансформировались в литературно-художественные «среды», завсегдатаями которых были талантливые художники и профессора. Среди них были Илья Репин, Иван Крамской, Архип Куинджи, Иван Шишкин, Николай Вагнер, Николай Бекетов и другие.
Дочь ученого – Любовь МенделееваЖенитьба Дмитрия и Анны состоялась в 1881 году. Вскоре у них родилась дочь Люба, сын Иван появился в 1883-м, близнецы Василий и Мария – в 1886-м. Во втором браке личная жизнь ученого сложилась счастливо. Позднее зятем Дмитрия Ивановича стал поэт Александр Блок, женившись на дочери ученого Любови.
Смерть
В начале 1907 года в Палате мер и весов проходила встреча Дмитрия Менделеева и нового министра промышленности Дмитрия Философова. После обхода палаты ученый заболел простудой, которая вызвала воспаление легких. Но даже будучи сильно больным, Дмитрий продолжал работу над рукописью «К познанию России», последними написанными им словами в которой стала фраза:
«В заключение считаю необходимым, хоть в самых общих чертах, высказать…».Могила Дмитрия Менделеева
Смерть наступила в пять часов утра 2 февраля по причине паралича сердца. Могила Дмитрия Менделеева находится на Волковом кладбище Санкт-Петербурга.
Память Дмитрия Менделеева увековечена рядом монументов, документальных фильмов, книгой «Дмитрий Менделеев. Автор великого закона».
Интересные факты
- С именем Дмитрия Менделеева связано множество интересных фактов биографии. Помимо деятельности ученого, Дмитрий Иванович занимался промышленной разведкой. В 70-е годы в США начался расцвет нефтяной промышленности, появились технологии, которые удешевили производство нефтепродуктов.
 Российские производители стали терпеть убытки на международном рынке из-за неспособности конкурировать по цене.
Российские производители стали терпеть убытки на международном рынке из-за неспособности конкурировать по цене. - В 1876 году по ходатайству министерства финансов России и «Русского технического общества», сотрудничавшего с военным ведомством, Менделеев отправился за океан на выставку технических новинок. На месте химик изучил новаторские принципы изготовления керосина и других нефтепродуктов. А по заказанным отчетам железнодорожных служб Европы Дмитрий Иванович попытался расшифровать метод изготовления бездымного пороха, что ему и удалось.
- У Менделеева было хобби – изготавливать чемоданы. Ученый шил себе одежду.
- Ученому приписывают изобретение водки и самогонного аппарата. Но на самом деле Дмитрий Иванович в теме докторской диссертации «Рассуждение о соединении спирта с водою» изучил вопрос уменьшения объема смешиваемых жидкостей. В работе ученого не было и слова о водке. А стандарт в 40° был установлен в царской России еще в 1843 году.

- Придумал герметические отсеки для пассажиров и пилотов.
- Существует легенда, что открытие периодической системы Менделеева произошло во сне, но это миф, созданный самим ученым.
- Сам скручивал папиросы, используя дорогой табак. Говорил, что никогда не бросит курить.
Открытия
- Создал управляемый аэростат, который стал неоценимым вкладом в воздухоплавание.
- Разработал периодическую таблицу химических элементов, ставшую графическим выражением закона, установленного Менделеевым в ходе работы над «Основами химии».
- Создал пикнометр – прибор, способный определять плотность жидкости.
- Открыл критическую температуру кипения жидкостей.
- Создал уравнение состояния идеального газа, устанавливающее зависимость между абсолютной температурой идеального газа, давлением и молярным объемом.
- Открыл Главную палату мер и весов – центральное учреждение Министерства финансов, заведовавшее поверочной частью Российской империи, подчинявшееся отделу торговли.

Новый взгляд на таблицу Менделеева: ученые ЮУрГУ систематизируют взаимодействия молекул
Размер шрифта
Межбуквенный интервал
Семейство шрифтов
- Новость
- 2018
- марта
- 05
- Новый взгляд на таблицу Менделеева: ученые ЮУрГУ систематизируют взаимодействия молекул
05.03.2018
Трансформация современных взглядов на физико-химические основы строения вещества — одна из наиболее важных современных тенденций в химии. В этом прорывном направлении работают ученые Южно-Уральского государственного университета. Новые фундаментальные знания в химии станут отправной точкой для следующего этапа развития материаловедения, а цифровые химические технологии ускорят воплощение практически значимых идей.
Один из главных проектов международной лаборатории «Многомасштабного моделирования многокомпонентных функциональных материалов» ЮУрГУ — междисциплинарное исследование свойств химических связей и межмолекулярных взаимодействий, находящееся на стыке химии, физики и информатики. О проделанной работе рассказала заведующий лабораторией, доктор химических наук Екатерина Барташевич.
О проделанной работе рассказала заведующий лабораторией, доктор химических наук Екатерина Барташевич.
От молекул к межмолекулярным взаимодействиям
«Еще в конце ХХ века ученые-химики утверждали, что молекула определяет свойства вещества. Это утверждение не исчерпывает, однако, проблему микроскопической природы физико-химических свойств. Сталкиваясь с многообразием строения кристаллических и полимерных материалов, конденсированных сред, мы понимаем, что эти свойства будут определяться не только набором молекул, но и тем, как они связаны между собой. Поэтому научное сообщество стремится систематизировать информацию о химических связях, чтобы перейти к алгоритмам, прогнозирующим строение многокомпонентных соединений. Этому способствует и интерес к материалам на основе органических соединений, к компонентам солнечных батарей, электрооптическим свойствам жидких кристаллов, лекарствам. Чтобы вырабатывать рекомендации к синтезу новых функциональных материалов, нужно, прежде всего, систематизировать знания о том, как могут взаимодействовать между собой частицы в веществе, и научиться использовать эти данные».

2019 год объявлен Международным годом периодической таблицы химических элементов. В настоящее время в области исследования межмолекулярных взаимодействий происходит выстраивание собственной периодической системы. Эта систематизация опирается на общность свойств элементов в рядах и определяет, как будут взаимодействовать между собой молекулы в веществе. Практический взгляд с позиций химии на физико-химические основы строения вещества являются основой таких исследований.
На пути к мировоззренческим изменениям в химии
«В основе выстраиваемой научным сообществом новой системы межмолекулярных взаимодействий — периодическая таблица Менделеева, которая является «фундаментом» базы знаний в химии, — подчеркивает Екатерина Владимировна. — В настоящее время для более крупных структурных единиц формируется своя система. Ее составляющие — уже не химические элементы, а связи между молекулами и их агломератами. В терминах новой классификации выделяют галогенную, халькогенную, пниктогенную, тетрельную связь и т.
д. По силе, устойчивости и влиянию на свойства вещества их можно сравнивать с водородной связью, влияние которой на свойства жизненно важных соединений (например, белков и нуклеиновых кислот) хорошо известно даже из школьной программы. Галогенные связи обеспечивают пластичность некоторых кристаллических материалов, а халькогенные — низкотемпературную проводимость. Изучение и систематизация свойств межмолекулярных связей открывают путь к объективным прогнозам: когда известны закономерности строения, становится понятным, чего следует ожидать от той или иной комбинации свойств».
Новая система знаний в химии — путь к новым материалам
Деление межмолекулярных взаимодействия на галогенные, халькогенные, пниктогенные и тетрельные связи — это новый взгляд на периодическую систему. Официальное определение IUPAC (Международный союз по чистой и прикладной химии) галогенной связи было дано совсем недавно, в 2013 году. Ученые Южно-Уральского государственного университета одними из первых стали работать в этом направлении. Они принимали участие в I Международном симпозиуме по галогенным связям, ISXB-1, который проходил в Италии. Через два года, на ISXB-2 в Швеции, доклад Екатерины Барташевич вызвал серьезный интерес и получил признание в международном научном сообществе. Сегодня один из проектов лаборатории «Многомасштабного моделирования многокомпонентных функциональных материалов» поддерживается Российским фондом фундаментальных исследований.
Они принимали участие в I Международном симпозиуме по галогенным связям, ISXB-1, который проходил в Италии. Через два года, на ISXB-2 в Швеции, доклад Екатерины Барташевич вызвал серьезный интерес и получил признание в международном научном сообществе. Сегодня один из проектов лаборатории «Многомасштабного моделирования многокомпонентных функциональных материалов» поддерживается Российским фондом фундаментальных исследований.
«Безусловно, задачи моделирования свойств вещества носят междисциплинарный характер. Если химические знания дополняются знаниями, например, из области квантовой кристаллографии и опираются на суперкомпьютерные вычисления, это помогает завладеть научными приоритетами. В феврале 2018 года в высокорейтинговом научном издании «Journal of Computational Chemistry» по теме характеризации химических связей опубликована наша совместная работа с профессором Владимиром Цирельсоном из Российского химико-технологического университета им.
Д. И. Менделеева. Исследования молекулярных кристаллов с галогенными связями и поиск среди них новых структур с нелинейно-оптическими свойствами ведется совместно с профессором Артёмом Масуновым из Университета Центральной Флориды (США). Наша научная группа, в которую входят молодые ученые ЮУрГУ, Ирина Юшина и Александр Дьяков, ставит перед собой задачу обработать максимальный объем информации, используя эволюционные алгоритмы. В этой новой области очень много как проблем, так и возможностей».
Углубленное изучение свойств химических связей невозможно без цифровых технологий и неразрывно связано с введением результатов в практику. Фактически, на данном этапе в химии закладываются фундаментальные основы, которые уже востребованы в конструировании новых материалов.
Виктория Матвейчук
периодическая таблица | Определение, элементы, группы, сборы, тенденции и факты
Таблица Менделеева
Просмотреть все СМИ
- Ключевые люди:
- Дмитрий Менделеев Лотар Мейер Поль-Эмиль Лекок де Буабодран
- Похожие темы:
- химический элемент атом группа период периодический закон
Просмотреть весь связанный контент →
Популярные вопросы
Что такое периодическая таблица?
Периодическая таблица представляет собой табличный массив химических элементов, упорядоченных по атомному номеру, от элемента с наименьшим атомным номером, водорода, до элемента с наибольшим атомным номером, оганесона. Атомный номер элемента — это число протонов в ядре атома этого элемента. У водорода 1 протон, а у оганесона 118.
Атомный номер элемента — это число протонов в ядре атома этого элемента. У водорода 1 протон, а у оганесона 118.
Что общего у групп периодической таблицы?
Группы периодической таблицы отображаются в виде вертикальных столбцов, пронумерованных от 1 до 18. Элементы в группе имеют очень похожие химические свойства, которые возникают из-за количества присутствующих валентных электронов, то есть количества электронов в внешняя оболочка атома.
Откуда взялась периодическая таблица?
Расположение элементов в периодической таблице определяется электронной конфигурацией элементов. Из-за принципа запрета Паули не более двух электронов могут занимать одну и ту же орбиталь. Первый ряд периодической таблицы состоит всего из двух элементов, водорода и гелия. Чем больше у атомов электронов, тем больше у них орбит, доступных для заполнения, и, таким образом, строки содержат больше элементов в нижней части таблицы.
Почему таблица Менделеева делится?
Периодическая таблица имеет две строки внизу, которые обычно отделены от основной части таблицы. Эти ряды содержат элементы лантаноидного и актиноидного рядов, обычно от 57 до 71 (от лантана до лютеция) и от 89 до 103 (актиний до лоуренсия) соответственно. Для этого нет никаких научных оснований. Это просто сделано для того, чтобы сделать таблицу более компактной.
Эти ряды содержат элементы лантаноидного и актиноидного рядов, обычно от 57 до 71 (от лантана до лютеция) и от 89 до 103 (актиний до лоуренсия) соответственно. Для этого нет никаких научных оснований. Это просто сделано для того, чтобы сделать таблицу более компактной.
Сводка
Прочтите краткий обзор этой темы
периодическая таблица , полностью периодическая таблица элементов , в химии систематизированный массив всех химических элементов в порядке возрастания атомного номера, т. е. общее количество протонов в атомном ядре. Когда химические элементы расположены таким образом, в их свойствах возникает повторяющаяся закономерность, называемая «периодическим законом», при которой элементы в одном столбце (группе) обладают сходными свойствами. Первоначальное открытие, которое сделал Д.И. Менделеев в середине 19ХХ века, сыграл неоценимую роль в развитии химии.
Изучите периодический закон химии, чтобы понять свойства элементов и то, как они связаны друг с другом их атомных номеров, целые числа которых равны положительным электрическим зарядам атомных ядер, выраженным в электронных единицах.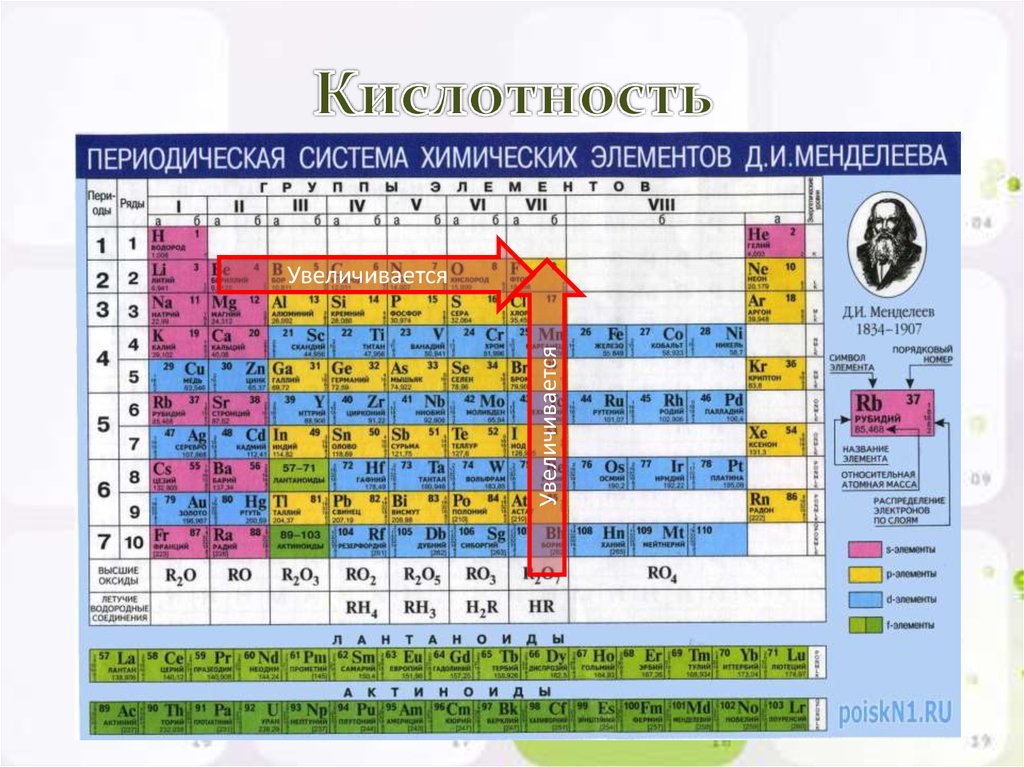 В последующие годы был достигнут большой прогресс в объяснении периодического закона с точки зрения электронной структуры атомов и молекул. Это разъяснение повысило ценность закона, который сегодня используется так же часто, как и в начале 20-го века, когда он выражал единственную известную взаимосвязь между элементами.
В последующие годы был достигнут большой прогресс в объяснении периодического закона с точки зрения электронной структуры атомов и молекул. Это разъяснение повысило ценность закона, который сегодня используется так же часто, как и в начале 20-го века, когда он выражал единственную известную взаимосвязь между элементами.
История периодического закона
Узнайте, как устроена таблица Менделеева
Просмотреть все видео к этой статье В первые годы XIX века наблюдалось бурное развитие аналитической химии — искусства различать различные химические вещества — и, как следствие, накопление обширных знаний о химических и физических свойствах как элементов, так и соединений. Это быстрое распространение химических знаний вскоре потребовало классификации, ибо на классификации химических знаний основана не только систематизированная литература по химии, но и лабораторное искусство, с помощью которого химия передается как живая наука от одного поколения химиков к другому. Отношения между соединениями обнаруживались легче, чем между элементами; так получилось, что классификация элементов на много лет отставала от классификации соединений. Фактически, среди химиков не было достигнуто общего согласия относительно классификации элементов в течение почти полувека после того, как системы классификации соединений стали общеупотребительными.
Фактически, среди химиков не было достигнуто общего согласия относительно классификации элементов в течение почти полувека после того, как системы классификации соединений стали общеупотребительными.
Дж.В. Доберейнер в 1817 году показал, что совокупный вес, то есть атомный вес, стронция находится посередине между весами кальция и бария, а несколько лет спустя он показал, что существуют и другие подобные «триады» (хлор, бром и йод [галогены] и литий, натрий и калий [щелочные металлы]). Ж.-Б.-А. Дюма, Л. Гмелин, Э. Ленссен, Макс фон Петтенкофер и Дж. П. Кук расширили предположения Доберейнера между 1827 и 1858 гг., показав, что подобные отношения простираются дальше, чем триады элементов: фтор добавляется к галогенам, а магний — к щелочноземельным. металлы, в то время как кислород, сера, селен и теллур были отнесены к одному семейству, а азот, фосфор, мышьяк, сурьма и висмут – к другому семейству элементов.
Викторина “Британника”
Периодическая таблица элементов
Проверьте свою связь с периодической таблицей элементов в этой викторине по всем 118 химическим элементам и их символам. Вы можете быть знакомы с химическими символами водорода и кислорода, но можете ли вы сопоставить такие низкопрофильные элементы, как гадолиний и эрбий, с соответствующими символами?
Вы можете быть знакомы с химическими символами водорода и кислорода, но можете ли вы сопоставить такие низкопрофильные элементы, как гадолиний и эрбий, с соответствующими символами?
Позднее были предприняты попытки показать, что атомные массы элементов могут быть выражены арифметической функцией, и в 1862 г. А.-Э.-Б. де Шанкуртуа предложил классификацию элементов, основанную на новых значениях атомных весов, данных системой Станислао Канниццаро 1858 года. Де Шанкуртуа нанес атомные веса на поверхность цилиндра с окружностью 16 единиц, что соответствует приблизительному атомному весу кислород. Получившаяся винтовая кривая перенесла тесно связанные элементы в соответствующие точки цилиндра, расположенные выше или ниже друг друга, и, следовательно, он предположил, что «свойства элементов — это свойства чисел» — замечательное предсказание в свете современных знаний.
Классификация элементов
В 1864 г. Я.А.Р. Ньюлендс предложил классифицировать элементы в порядке увеличения атомного веса, при этом элементам присваивались порядковые номера от единицы и вверх, и они были разделены на семь групп, обладающих свойствами, тесно связанными с первыми семью из известных тогда элементов: водород, литий, бериллий, бор, углерод. , азот и кислород. Это соотношение было названо законом октав по аналогии с семью интервалами музыкальной гаммы.
, азот и кислород. Это соотношение было названо законом октав по аналогии с семью интервалами музыкальной гаммы.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подписаться сейчас
Затем, в 1869 г., в результате обширной корреляции свойств и атомных весов элементов с особым вниманием к валентности (т. е. числу одинарных связей, которые может образовать элемент), Менделеев предложил периодическую закон, согласно которому «элементы, расположенные по величине атомного веса, обнаруживают периодическое изменение свойств». Лотар Мейер независимо пришел к аналогичному заключению, опубликованному после выхода статьи Менделеева.
периодическая таблица | Определение, элементы, группы, сборы, тенденции и факты
Таблица Менделеева
Просмотреть все СМИ
- Ключевые люди:
- Дмитрий Менделеев Лотар Мейер Поль-Эмиль Лекок де Буабодран
- Похожие темы:
- химический элемент атом группа период периодический закон
Просмотреть весь связанный контент →
Популярные вопросы
Что такое периодическая таблица?
Периодическая таблица представляет собой табличный массив химических элементов, упорядоченных по атомному номеру, от элемента с наименьшим атомным номером, водорода, до элемента с наибольшим атомным номером, оганесона. Атомный номер элемента — это число протонов в ядре атома этого элемента. У водорода 1 протон, а у оганесона 118.
Атомный номер элемента — это число протонов в ядре атома этого элемента. У водорода 1 протон, а у оганесона 118.
Что общего у групп периодической таблицы?
Группы периодической таблицы отображаются в виде вертикальных столбцов, пронумерованных от 1 до 18. Элементы в группе имеют очень похожие химические свойства, которые возникают из-за количества присутствующих валентных электронов, то есть количества электронов в внешняя оболочка атома.
Откуда взялась периодическая таблица?
Расположение элементов в периодической таблице определяется электронной конфигурацией элементов. Из-за принципа запрета Паули не более двух электронов могут занимать одну и ту же орбиталь. Первый ряд периодической таблицы состоит всего из двух элементов, водорода и гелия. Чем больше у атомов электронов, тем больше у них орбит, доступных для заполнения, и, таким образом, строки содержат больше элементов в нижней части таблицы.
Почему таблица Менделеева делится?
Периодическая таблица имеет две строки внизу, которые обычно отделены от основной части таблицы. Эти ряды содержат элементы лантаноидного и актиноидного рядов, обычно от 57 до 71 (от лантана до лютеция) и от 89 до 103 (актиний до лоуренсия) соответственно. Для этого нет никаких научных оснований. Это просто сделано для того, чтобы сделать таблицу более компактной.
Эти ряды содержат элементы лантаноидного и актиноидного рядов, обычно от 57 до 71 (от лантана до лютеция) и от 89 до 103 (актиний до лоуренсия) соответственно. Для этого нет никаких научных оснований. Это просто сделано для того, чтобы сделать таблицу более компактной.
Сводка
Прочтите краткий обзор этой темы
периодическая таблица , полностью периодическая таблица элементов , в химии систематизированный массив всех химических элементов в порядке возрастания атомного номера, т. е. общее количество протонов в атомном ядре. Когда химические элементы расположены таким образом, в их свойствах возникает повторяющаяся закономерность, называемая «периодическим законом», при которой элементы в одном столбце (группе) обладают сходными свойствами. Первоначальное открытие, которое сделал Д.И. Менделеев в середине 19ХХ века, сыграл неоценимую роль в развитии химии.
Изучите периодический закон химии, чтобы понять свойства элементов и то, как они связаны друг с другом их атомных номеров, целые числа которых равны положительным электрическим зарядам атомных ядер, выраженным в электронных единицах. В последующие годы был достигнут большой прогресс в объяснении периодического закона с точки зрения электронной структуры атомов и молекул. Это разъяснение повысило ценность закона, который сегодня используется так же часто, как и в начале 20-го века, когда он выражал единственную известную взаимосвязь между элементами.
В последующие годы был достигнут большой прогресс в объяснении периодического закона с точки зрения электронной структуры атомов и молекул. Это разъяснение повысило ценность закона, который сегодня используется так же часто, как и в начале 20-го века, когда он выражал единственную известную взаимосвязь между элементами.
История периодического закона
Узнайте, как устроена таблица Менделеева
Просмотреть все видео к этой статье В первые годы XIX века наблюдалось бурное развитие аналитической химии — искусства различать различные химические вещества — и, как следствие, накопление обширных знаний о химических и физических свойствах как элементов, так и соединений. Это быстрое распространение химических знаний вскоре потребовало классификации, ибо на классификации химических знаний основана не только систематизированная литература по химии, но и лабораторное искусство, с помощью которого химия передается как живая наука от одного поколения химиков к другому. Отношения между соединениями обнаруживались легче, чем между элементами; так получилось, что классификация элементов на много лет отставала от классификации соединений..jpg) Фактически, среди химиков не было достигнуто общего согласия относительно классификации элементов в течение почти полувека после того, как системы классификации соединений стали общеупотребительными.
Фактически, среди химиков не было достигнуто общего согласия относительно классификации элементов в течение почти полувека после того, как системы классификации соединений стали общеупотребительными.
Дж.В. Доберейнер в 1817 году показал, что совокупный вес, то есть атомный вес, стронция находится посередине между весами кальция и бария, а несколько лет спустя он показал, что существуют и другие подобные «триады» (хлор, бром и йод [галогены] и литий, натрий и калий [щелочные металлы]). Ж.-Б.-А. Дюма, Л. Гмелин, Э. Ленссен, Макс фон Петтенкофер и Дж. П. Кук расширили предположения Доберейнера между 1827 и 1858 гг., показав, что подобные отношения простираются дальше, чем триады элементов: фтор добавляется к галогенам, а магний — к щелочноземельным. металлы, в то время как кислород, сера, селен и теллур были отнесены к одному семейству, а азот, фосфор, мышьяк, сурьма и висмут – к другому семейству элементов.
Britannica Викторина
118 Названий и символов периодической таблицы Викторина
Периодическая таблица состоит из 118 элементов. Насколько хорошо вы знаете их символы? В этом тесте вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них.
Насколько хорошо вы знаете их символы? В этом тесте вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них.
Позднее были предприняты попытки показать, что атомные массы элементов могут быть выражены арифметической функцией, и в 1862 г. А.-Э.-Б. де Шанкуртуа предложил классификацию элементов, основанную на новых значениях атомных весов, данных системой Станислао Канниццаро 1858 года. Де Шанкуртуа нанес атомные веса на поверхность цилиндра с окружностью 16 единиц, что соответствует приблизительному атомному весу кислород. Получившаяся винтовая кривая перенесла тесно связанные элементы в соответствующие точки цилиндра, расположенные выше или ниже друг друга, и, следовательно, он предположил, что «свойства элементов — это свойства чисел» — замечательное предсказание в свете современных знаний.
Классификация элементов
В 1864 г. Я.А.Р. Ньюлендс предложил классифицировать элементы в порядке увеличения атомного веса, при этом элементам присваивались порядковые номера от единицы и вверх, и они были разделены на семь групп, обладающих свойствами, тесно связанными с первыми семью из известных тогда элементов: водород, литий, бериллий, бор, углерод. , азот и кислород. Это соотношение было названо законом октав по аналогии с семью интервалами музыкальной гаммы.
, азот и кислород. Это соотношение было названо законом октав по аналогии с семью интервалами музыкальной гаммы.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подписаться сейчас
Затем, в 1869 г., в результате обширной корреляции свойств и атомных весов элементов с особым вниманием к валентности (т. е. числу одинарных связей, которые может образовать элемент), Менделеев предложил периодическую закон, согласно которому «элементы, расположенные по величине атомного веса, обнаруживают периодическое изменение свойств». Лотар Мейер независимо пришел к аналогичному заключению, опубликованному после выхода статьи Менделеева.
Периодическая таблица | CPD
Источник: © Getty Images
От мобильных телефонов до одежды, которую мы носим, все состоит из одного или нескольких из 118 известных химических элементов. Так как же ученые узнают, с чего начать при разработке новых или существующих материалов?
Химики часто начинают с наблюдений, а затем ищут закономерности. Они будут использовать периодическую таблицу, поскольку она занимает центральное место в нашем понимании и классификации окружающего мира. Он упорядочивает и классифицирует все элементы в соответствии с их физическими и химическими свойствами.
Они будут использовать периодическую таблицу, поскольку она занимает центральное место в нашем понимании и классификации окружающего мира. Он упорядочивает и классифицирует все элементы в соответствии с их физическими и химическими свойствами.
Все известные элементы перечислены в периодической таблице. Особенности таблицы:
- строк, называемых периодами.
- столбцов называются группами.
- металлов слева.
- неметаллов справа.
- химически активные металлы, называемые щелочными металлами группы 1.
- центральный блок металлов, называемый переходными металлами.
- неметаллов, называемых галогенами в группе 7.
- нереакционноспособные газы, называемые благородными газами группы 0.
Элементы в группе демонстрируют закономерности в своих физических свойствах, таких как температура плавления или кипения, теплопроводность и плотность. У них сходные химические реакции, например, с кислородом.
У них сходные химические реакции, например, с кислородом.
Положение элемента в периодической таблице помогает химикам решить, будет ли он полезен для конкретной работы.
Загрузите этот
Загрузите сборник идей и мероприятий в формате MS Powerpoint или pdf.
В вашем классе
Загрузите подборку идей и заданий с веб-сайта «Образование по химии»: rsc.li/2Z81sap
Идеи для вашего класса
Аналогии — это эффективный способ помочь учащимся понять сложности химии. Мы можем использовать различные системы классификации из повседневной жизни, чтобы помочь учащимся понять, как периодическая таблица классифицирует элементы.
Начните с аналогий, с которыми учащиеся, вероятно, знакомы, прежде чем переходить к менее знакомым примерам. Планировка супермаркетов — хорошее место для начала. В супермаркете продукты сгруппированы по разным проходам в соответствии с характеристиками и свойствами продуктов, например: фрукты и овощи, выпечка, мясо, молочные продукты, крупы.
Итак, если вы хотите купить масло, вам нужно знать, что это молочный продукт, и идти в молочный отдел.
Познакомьте учащихся с рядом различных элементов в таблице, попросив их классифицировать их как металлы или неметаллы. Затем попросите их найти символ в периодической таблице. Повторив это с рядом элементов, они вскоре начнут строить картину и обнаружат, что металлы находятся в левой части таблицы, а неметаллы — в правой.
Раздайте учащимся чистую таблицу Менделеева. По мере того, как ключевые слова, идеи и элементы встречаются на каждом уроке, учащиеся добавляют их в свою таблицу. Со временем это поможет им составить собственное представление о периодической таблице, в котором будут подчеркнуты ключевые моменты.
Источник: © Shutterstock. и собственность. Хорошим примером является струнная часть оркестра, в которой есть инструменты разного размера. Самые маленькие инструменты расположены с одной стороны и играют самые высокие ноты, а самые большие — с другой стороны и играют самые низкие ноты.
Теперь взгляните на группу металлов или неметаллов, таких как щелочные металлы или галогены. Продемонстрируйте, как свойства меняются по мере продвижения вниз по группе. Это можно сделать путем поиска таких данных, как точки плавления и плотность, и/или с помощью практических демонстраций. Предложите учащимся искать закономерности в реактивности и сравнивать эту реактивность с положением элемента в периодической таблице.
Вы также можете использовать периодическую таблицу для развития у учащихся навыков исследования и презентации. Назначьте каждому учащемуся отдельный элемент и попросите их найти и представить группе ключевую информацию. Вместе вы можете построить периодическую таблицу класса с этой работой. Интерактивная периодическая таблица RSC — хорошее место для начала исследований.
Существует множество других ресурсов, доступных для консолидации и пересмотра, таких как бинго Периодической таблицы, Elemental Su Duko, Elemental top trumps и игра Periodic table.
Распространенные заблуждения
Распространенное заблуждение состоит в том, что все элементы в современной периодической таблице расположены в порядке возрастания атомного веса. Хотя это было отправной точкой для многих разработчиков периодических таблиц, при ближайшем рассмотрении обнаруживаются заметные исключения. В современной периодической таблице элементы расположены в порядке атомного номера, который представляет собой количество протонов в атоме, тогда как атомная масса основана на всей массе атома. Чтобы помочь преодолеть эту альтернативную теорию, предложите своим ученикам внимательно посмотреть на таблицу и выяснить для себя, как увеличиваются числа. Подчеркните, что они должны использовать ключ, чтобы отличить относительную атомную массу от атомного номера.
Положение водорода часто может привести к путанице, так как разные версии периодической таблицы помещают его по-разному: вверху группы 1 или 7 или где-то посередине. Здесь следует подчеркнуть, что водород — это аномалия. Это неметалл с электронной структурой, подобной металлам группы 1. Поэтому химикам иногда трудно понять, куда его поместить.
Это неметалл с электронной структурой, подобной металлам группы 1. Поэтому химикам иногда трудно понять, куда его поместить.
Обычно в классе используется определение и цветовая кодировка элементов, которые являются жидкостями и газами при комнатной температуре. Хотя это помогает учащимся ознакомиться с положением определенных элементов, это может привести к неправильному пониманию того, что другие элементы не могут существовать в виде газов и жидкостей. Чтобы оспорить эту идею, попросите учащихся назвать щелочной металл, находящийся в жидком состоянии при 100°C.
Понимание концепции элементарной природы элементов необходимо для понимания того, как работает периодическая таблица. Студенты могут бороться с этим, и это обсуждается в разделе «Как преподавать состояния материи и теории частиц».
Источник: © Shutterstock
Игра в лишнее дает вам представление о мышлении учащихся. Например, назовите элемент символом He или Какой символ обозначает калий? Ответы могут быть записаны на мини-доске.
Упражнения «Выпадение одного» требуют от учащихся обоснования своего выбора, что дает вам представление об их мышлении. Например, попросите их посмотреть на изображения выше и решить, какое из них не подходит.
Повышение до 14–16 лет
По мере того, как учащиеся продвигаются в учебе, они должны описывать этапы разработки периодической таблицы. Они должны быть в состоянии объяснить, как положение элемента в периодической таблице связано с расположением электронов в его атомах и, следовательно, с его атомным номером. Кроме того, они должны уметь объяснять различия между металлами и неметаллами на основе их характерных физических и химических свойств. По положению элементов в таблице они должны быть в состоянии предсказать возможные реакции и возможную реакционную способность. Ожидается, что они объяснят, как и почему реактивность группы элементов изменяется по мере того, как вы спускаетесь по группе.
Забрать домой баллы
- Учащиеся должны ознакомиться с макетом и ключевыми словами, связанными с периодической таблицей, но не должны запоминать их.

- Использование ряда начальных заданий и игр поможет учащимся в изучении символов.
- Убедитесь, что учащиеся хорошо понимают основные химические концепции, такие как модель частиц, физические и химические свойства, прежде чем просить их определить тенденции в группах элементов.
- Понимание учащимися наблюдаемых тенденций в периодической таблице будет развиваться по мере того, как они будут изучать и применять идеи об атомной структуре.
Таблица Менделеева: очень краткое введение [Обзор книги] | Периодическая таблица
Современная периодическая таблица является основой науки и настолько знакома, что о ней даже сложены популярные песни. Но, возможно, удивительно, что даже многие профессиональные химики мало что знают об истории того, как он был открыт, помимо вклада Менделеева.
В своей новейшей книге Периодическая таблица: очень краткое введение [Oxford University Press; 2012: Амазонка Великобритания; Amazon US], преподаватель университета и писатель Эрик Шерри отправляет нас в увлекательное и увлекательное путешествие в то, как появилась современная таблица Менделеева. Эта небольшая книга представляет собой удивительно большой обзор многих открытий, разработок и отдельных людей, которые определили этот универсальный закон природы, периодический закон, и все это свернуто в увлекательное и познавательное повествование.
Эта небольшая книга представляет собой удивительно большой обзор многих открытий, разработок и отдельных людей, которые определили этот универсальный закон природы, периодический закон, и все это свернуто в увлекательное и познавательное повествование.
В этой книге мы знакомимся с интересным набором международных персонажей, включая физиков, химиков, геологов, учителей, торговцев и дворян, всех, кто сыграл роль в открытии и эволюции периодической таблицы. Примечательно, что мы встречаемся с шотландским врачом Уильямом Праутом, чье предположение о том, что вся материя состоит из атомов водорода, побудило ученых того времени получить еще более точные веса для каждого атома в их стремлении доказать, верна ли его гипотеза. Мы встречаем датско-американского чудака Густава Хинрихса, который увидел связь между частотами спектров, излучаемых элементами, и внутренним строением их атомов. Мы также встречаем немецкого физико-химика Юлиуса Лотара Мейера, которого некоторые историки считают одним из первооткрывателей периодической таблицы, вместе с русским ученым Дмитрием Менделеевым, который набросал свою периодическую таблицу на обратной стороне приглашения местная сыроварня.
Но помимо простого пересказа истории, Шерри также обсуждает, как более глубокое значение структуры периодической таблицы постепенно стало очевидным для ученых и послужило укреплению растущего перекрестного опыления между химией и физикой, способствуя развитию атомной теории и квантовой теории. механика. Далее есть глава, посвященная искусственному синтезу сверхтяжелых элементов помимо урана (элемент 92). Меня особенно увлекло обсуждение множества альтернативных форм периодической таблицы — от деревьев до спиралей — как с научной, так и с философской точки зрения. Я не уверен, что автор сделал это намеренно, но, рассказывая многогранную историю периодической таблицы, читатель получает представление о научном методе и о том, как наука устроена.0290 действительно сделано.
Эта книга понравится исследователям, ученым, преподавателям естественных наук и студентам, а также любителям науки и истории науки. Эта небольшая книга в мягкой обложке состоит из 147 страниц и включает черно-белые фотографии, таблицы и диаграммы, список дополнительной литературы и предметный указатель. Главы включают:
Главы включают:
– Хотя разработан и написан, есть одно небольшое дополнение, которое, возможно, улучшит его: временная шкала, в которой отмечается, когда были сделаны соответствующие открытия в химии и физике, чтобы дать читателю краткий мысленный образ того, как вся эта информация сочетается в связную историю.
Эта небольшая книга в мягкой обложке является частью растущей коллекции книг “Очень краткое введение” Оксфорда, которые были проданы тиражом более трех миллионов экземпляров по всему миру. Написанные экспертами в своих областях и прошедшие рецензирование перед публикацией, эти книги достаточно малы, чтобы поместиться в кармане, дамской сумочке или рюкзаке. Основываясь на названиях, которые я прочитал до сих пор, я нашел эти тонкие тома интересными, информативными и очень удобочитаемыми, и я с нетерпением жду каждую новую книгу.
Основываясь на названиях, которые я прочитал до сих пор, я нашел эти тонкие тома интересными, информативными и очень удобочитаемыми, и я с нетерпением жду каждую новую книгу.
.. .. .. .. .. .. .. .. .. .. .. ..
Эрик Шерри — преподаватель химии, истории и философии науки в Калифорнийском университете в Лос-Анджелесе. . Он написал и опубликовал более 100 исследовательских статей, множество глав в книгах, представлен во многих онлайн-видео- и аудиолекциях, является редактором академического журнала Foundations of Chemistry , а также отредактировал или написал шесть книг. Его книга 2007 года « История периодической системы: ее развитие и значение» принес ему награду Герберта Ньюби Маккоя Калифорнийского университета в Лос-Анджелесе, которая отмечает значительный вклад в науку о химии. Периодическая таблица: очень краткое введение — шестая книга доктора Шерри. Посетите веб-сайт доктора Шерри.
.. .. .. .. .. .. .. .. .. .. .. ..
twitter: @GrrlScientist
facebook: grrlscientist
evil google+: grrlscientist
электронная почта: grrlscientist@gmail. com
com
Периодическая таблица — Химия для старших классов
Все ресурсы по химии для старших классов
6 Диагностические тесты 143 практических теста Вопрос дня Карточки Learn by Concept
← Предыдущая 1 2 3 4 5 6 Следующая →
Химия в старших классах Справка » Периодическая таблица
Какой из следующих атомов самый большой?
Возможные ответы:
Калий
Кислород
Азот
Литий
Бром
Правильный ответ:
Калий
Пояснение:
Размер атома определяется количеством оболочек и количеством протонов и электронов в атоме. Любой атом в периоде с более высоким номером (ряд) больше, чем любой атом в периоде с более низким номером, поскольку количество электронных оболочек увеличивается по мере увеличения номера периода. В течение того же периода атомы становятся меньше, когда вы двигаетесь вправо. Это происходит потому, что атомный номер увеличивается, увеличивая количество протонов в ядре. Эти протоны притягивают окружающие электроны, притягивая их ближе и уменьшая общий размер атома.
В течение того же периода атомы становятся меньше, когда вы двигаетесь вправо. Это происходит потому, что атомный номер увеличивается, увеличивая количество протонов в ядре. Эти протоны притягивают окружающие электроны, притягивая их ближе и уменьшая общий размер атома.
Обычно атомный радиус увеличивается при движении вниз и влево. Это делает гелий самым маленьким атомом, а франций — самым большим.
Сообщить об ошибке
Какой ион азота самый большой?
Возможные ответы:
Правильный ответ:
Пояснение:
Ионы атомов различаются по размеру. Когда атом получает электроны, размер атома увеличивается, а когда атом теряет электроны, размер атома уменьшается. Азот с формальным зарядом минус три будет иметь наибольший размер, потому что у него больше всего электронов. Помните, что добавление электронов создаст отрицательный ион, а удаление электронов вызовет положительный ион.
Сообщить об ошибке
Какое из следующих значений будет уменьшаться при перемещении слева направо в периоде таблицы Менделеева?
Возможные ответы:
Атомный радиус
Электронегативность
Атомный номер
Электронный сродство
Правильный ответ:
Atomic Radius
7 Пояснение:
Движение слева направо в периодической таблице приводит к увеличению атомного номера (количества протонов), а также сродства к электрону и электроотрицательности.
Однако радиус атома будет уменьшаться при движении слева направо. Чем больше протонов добавляется к ядру, тем сильнее они притягиваются к электронам. Это притягивает электроны ближе к ядру, что приводит к уменьшению атомного радиуса.
Сообщить об ошибке
Элементы со схожими свойствами будут иметь одинаковые __________ в периодической таблице.
Возможные ответы:
период
атомный радиус
атомный заряд
атомная масса
группа
Правильный ответ:
группа
Пояснение:
Таблица Менделеева устроена таким образом, чтобы мы могли быстро определить, какие элементы будут реагировать сходным химическим образом. Элементы из одной группы, то есть одного столбца, будут иметь схожие свойства. Это связано с одинаковым количеством валентных электронов во внешней оболочке.
Сообщить об ошибке
Элементы какой группы периодической таблицы будут иметь самые низкие энергии первой ионизации?
Possible Answers:
Alkali metals
Group III
Alkaline earth metals
Halogens
Noble gases
Correct answer:
Alkali metals
Пояснение:
Энергия ионизации — это количество энергии, необходимое для отрыва электрона от атома. Щелочным металлам нужно всего лишь потерять один электрон, чтобы получить октет стабильного благородного газа. В результате потеря этого электрона требует очень мало энергии, поскольку образующийся ион достаточно стабилен. Это свойство приводит к тому, что щелочные металлы (находящиеся в группе I) имеют самые низкие энергии первой ионизации.
Щелочным металлам нужно всего лишь потерять один электрон, чтобы получить октет стабильного благородного газа. В результате потеря этого электрона требует очень мало энергии, поскольку образующийся ион достаточно стабилен. Это свойство приводит к тому, что щелочные металлы (находящиеся в группе I) имеют самые низкие энергии первой ионизации.
Сообщить об ошибке
Какой из этих элементов имеет наименьший атомный радиус?
Возможные ответы:
азот
Phosphorus
Bismuth
Arsenic
Ответ
Правильный ответ:
NITRONGE
7 Объяснение:
Тенденция для радиуса атома следующая: радиус атома увеличивается справа налево в строке и сверху вниз в группе периодической таблицы.
Сообщить об ошибке
Какой из этих элементов является наиболее электроотрицательным?
Возможные ответы:
азот
Boron
Кислород
Флуорин
Углерод
Правильный ответ:
Флуор
7777. Пояснение:
Пояснение:
Фтор — самый электроотрицательный элемент. Тенденция электроотрицательности следующая: электроотрицательность увеличивается слева направо в пределах строки и снизу вверх в пределах группы таблицы Менделеева.
Сообщить об ошибке
Какой из этих элементов является наименее электроотрицательным?
Возможные ответы:
Rubidium
Francium
Цезий
Калий
натрия
Правильный ответ:
Francium
7771 Пояснение:
Франций является наименее электроотрицательным элементом. Тенденция электроотрицательности следующая: электроотрицательность увеличивается слева направо в пределах строки и снизу вверх в пределах группы таблицы Менделеева.
Сообщить об ошибке
Какой из этих элементов имеет наибольший атомный радиус?
Возможные ответы:
Кремний
Phosphorus
Chlorine
Sulfur
Алюминий
Правильный ответ:
Алюминий
Объяснение:
Тенденция для атомного радиуса следующая: атомный радиус увеличивается справа налево в строке и сверху вниз в группе периодической таблицы.
Сообщить об ошибке
Какой из этих элементов имеет наибольшую энергию ионизации?
Возможные ответы:
Калий
Рубидий
Литий
Натрий
Цезий
Правильный ответ:
Литий
7777. Пояснение:
Литий обладает наибольшей энергией ионизации, потому что это наименьший из доступных вариантов. Чем меньше элемент/атом, тем ближе к ядру атома находятся валентные электроны. Чем ближе валентные электроны к центру атома, тем труднее их отобрать, потому что они сильно притягиваются к протонам в центре атома. Тенденция к энергии ионизации следующая: энергия ионизации увеличивается слева направо в ряду и снизу вверх внутри группы периодической таблицы 9.0003
Сообщить об ошибке
← Назад 1 2 3 4 5 6 Далее →
Уведомление об авторских правах
Все ресурсы по химии для средней школы
6 Диагностические тесты 143 практических теста Вопрос дня Карточки Учитесь по концепции
NYTimes
ПЕРИОДИЧЕСКИЙ СТОЛ
По Примо Леви . Перевод Раймонда Розенталя. 233 стр. Нью-Йорк: Schocken Books. 16,95 долларов США.
Перевод Раймонда Розенталя. 233 стр. Нью-Йорк: Schocken Books. 16,95 долларов США.
Начинающему студенту-химику периодическая таблица может показаться не более чем шахматной доской с элементами, атомные символы, веса и числа которых представляют собой множество шифров, которые нужно запомнить. Посвященным, однако, как можно узнать из Primo Levi ”The Periodic Table , менделеевская система есть поэзия, возможный мост между миром слов и миром вещей, а потому неожиданная средства познания Вселенной и самих себя.
Поскольку г-н Леви , итальянский писатель и химик, выделяет эти средства, они бесконечно метафоричны, какими они должны быть, чтобы обеспечить соответствие, которое он ищет между иначе несопоставимыми мирами физической и человеческой природы.
21 произведение в «The Periodic 9»0640 Таблицы , каждая из которых названа в честь элемента, являются, таким образом, в одно и то же время строгими «конфронтациями с Матерью-Материей» и ярко нарисованными портретами. человеческих типов – аналитические «рассказы о воинствующей химии» и образное исследование личного, социального и политического опыта. Редко можно встретить такие разнообразные цели в сочетании, и еще реже можно найти их
так удачно интегрирована в современное литературное произведение. Тем не менее, это то, что мы имеем в этой прекрасно оформленной книге, самой последней и во многих отношениях самой оригинальной из «Мистера 9».0640 Леви , три тома автобиографических
отражение.
человеческих типов – аналитические «рассказы о воинствующей химии» и образное исследование личного, социального и политического опыта. Редко можно встретить такие разнообразные цели в сочетании, и еще реже можно найти их
так удачно интегрирована в современное литературное произведение. Тем не менее, это то, что мы имеем в этой прекрасно оформленной книге, самой последней и во многих отношениях самой оригинальной из «Мистера 9».0640 Леви , три тома автобиографических
отражение.
Текст:
Примо Леви известен американским читателям, если вообще известен, как автор книги «Выживание в Освенциме». Эта книга, подтверждающая ясный, гуманный разум перед лицом нацистского варварства, является одним из поистине выдающихся произведений о Холокосте.
литературы и стал чем-то вроде классики. За ним последовало «Пробуждение», в котором автор описал свой долгий и причудливый путь домой после освобождения из Освенцима. В родной Италии
эти тома, наряду с несколькими другими, снискали г-ну Леви значительную репутацию, но, поскольку так мало его работ было доступно английским читателям, он остался почти неизвестным здесь. Эта ситуация теперь счастливо
изменился благодаря замечательному переводу «Периодической таблицы» Раймонда Розенталя.
В родной Италии
эти тома, наряду с несколькими другими, снискали г-ну Леви значительную репутацию, но, поскольку так мало его работ было доступно английским читателям, он остался почти неизвестным здесь. Эта ситуация теперь счастливо
изменился благодаря замечательному переводу «Периодической таблицы» Раймонда Розенталя.
Первая часть книги, «Аргон» (названный в честь газа, «настолько инертного, настолько удовлетворяющего (своему) состоянию», что он «не сочетается ни с каким другим элементом»), является данью уважения еврейскому учению автора.
предки, сами по себе порода друг от друга. Намереваясь вернуть своих бесчисленных тетушек и дядей из легендарного прошлого, г-н Леви в то же время спасает для потомков обрывки их утерянного языка, местного варианта иудео-итальянского, который
сочетал еврейские корни с пьемонтскими окончаниями и флексиями — «скептическая, добродушная речь». . . наполнен нежной и достойной близостью с Богом». Возрождение этого жаргона (который г.
Леви в другом месте называет своего рода «средиземноморским идишем»), и для некоторых людей, которые когда-то говорили, это значительное достижение, и его лингвистическая точность и остроумие задают тон и направление.
для следующих частей.
. . наполнен нежной и достойной близостью с Богом». Возрождение этого жаргона (который г.
Леви в другом месте называет своего рода «средиземноморским идишем»), и для некоторых людей, которые когда-то говорили, это значительное достижение, и его лингвистическая точность и остроумие задают тон и направление.
для следующих частей.
Подобно «Аргону», они построены на аналогиях между стихиями и различными человеческими типами и развивают способ воображения реальности, поразительный в своем слиянии физических, химических и моральных истин. Мистеру Леви
нет таких вещей, как эмоционально нейтральные элементы, как нет эмоционально нейтральных мужчин и женщин. Таким образом, независимо от того, сосредоточена ли данная история на дружбе, альпинизме, ранних встречах с любовью или беспокойных
статус еврея в муссолиниевской Италии, автор может установить подходящую корреляцию с одним из элементов. Меркьюри, «всегда Элвин Х. Розенфельд преподает на факультете английского языка в Университете Индианы. Его
«Воображение Гитлера» будет опубликовано в апреле. беспокойный», — «постоянный и изменчивый дух». Цинк, напротив, — «скучный металл», «не элемент
что говорит многое для воображения» (для реакции требуется наличие примеси, и в фашистской Италии, как воображение г-на Леви ухватывается за аналогию, еврей должен был быть примесью — в его случае, почти гордо
так). Есть элементы, такие как железо и медь, «легкие и прямые, неспособные к сокрытию»; другие, такие как висмут и кадмий, «обманчивы и неуловимы».
эти образы призваны возродить «тысячелетний диалог между элементами и человеком» и показать, что ни в одном из своих аспектов природа не непроницаема для разума.
Меркьюри, «всегда Элвин Х. Розенфельд преподает на факультете английского языка в Университете Индианы. Его
«Воображение Гитлера» будет опубликовано в апреле. беспокойный», — «постоянный и изменчивый дух». Цинк, напротив, — «скучный металл», «не элемент
что говорит многое для воображения» (для реакции требуется наличие примеси, и в фашистской Италии, как воображение г-на Леви ухватывается за аналогию, еврей должен был быть примесью — в его случае, почти гордо
так). Есть элементы, такие как железо и медь, «легкие и прямые, неспособные к сокрытию»; другие, такие как висмут и кадмий, «обманчивы и неуловимы».
эти образы призваны возродить «тысячелетний диалог между элементами и человеком» и показать, что ни в одном из своих аспектов природа не непроницаема для разума.
Разум, проявленный в этой книге, неустанно любознателен и посвящен постижению самых тонких измерений материи и человека. Одновременно аналитический и романистический, это интеллект писателя, который смог
выковать необычный синтез научного знания и поэтической чувствительности, рациональных процедур и моральных восприятий. Его цель, следовательно, состоит в том, чтобы одновременно постигать и творить, и тем самым уберечься от того, чтобы стать жертвой всего внешнего.
нападения, как духовные, так и материальные.
Одновременно аналитический и романистический, это интеллект писателя, который смог
выковать необычный синтез научного знания и поэтической чувствительности, рациональных процедур и моральных восприятий. Его цель, следовательно, состоит в том, чтобы одновременно постигать и творить, и тем самым уберечься от того, чтобы стать жертвой всего внешнего.
нападения, как духовные, так и материальные.
Следуя г-ну Леви в его поисках элементов, можно увидеть, как прозрения аналитика служат для освещения широкого спектра личного и исторического опыта, включая опыт автора как антифашистского партизана и его
последующий арест и заключение в Освенциме. Читателям более ранней работы «Цинк», «Золото», «Церий», «Хром» и «Ванадий».
будут представлять особый интерес, поскольку они дополняют или иным образом расширяют эпизоды, описанные в «Выживании в Освенциме».
один, например, живо описывает сверхъестественную переписку Леви после войны с доктором Мюллером, немецким химиком, который, как оказалось, был начальником лаборатории в Освенциме, где в 1944, автор раб
остаться в живых. Конфронтация в этой истории затрагивает самую суть предмета мистера Леви и показывает его в лучшем его созерцательном состоянии: он ставит вопросы, обдумывает их многообразные последствия и достигает решения, которое
и строго, и гуманно.
Конфронтация в этой истории затрагивает самую суть предмета мистера Леви и показывает его в лучшем его созерцательном состоянии: он ставит вопросы, обдумывает их многообразные последствия и достигает решения, которое
и строго, и гуманно.
В самом деле, несмотря на все размышления о загадках материи, «Периодическую таблицу» лучше всего читать как исторически связанную книгу, и она будет иметь наибольшее значение для тех читателей, которые бдительны к взаимодействию ума с моральными, а также физическими аспектами.
истины. Таким образом, «Железо», посвященное Сандро Дельмастро, однокурснику-химику (и первому бойцу Сопротивления, убитому в Пьемонте), в первую очередь рассказывает о благородстве дружбы, как и «Фосфор».
это скорее рассказ о сексуальном влечении, чем анатомия жизни в лаборатории. Обе части, установленные в 1940-х, имеют гораздо больше общего с капризами человеческих отношений по итальянским расовым законам, чем с законами
химии.
Таким образом, реальная привлекательность «Периодической таблицы» заключается в способности автора исследовать человеческие события с такой же различительной способностью, с какой он исследует природу, и в его отказе отказаться от суверенитета независимых исследование либо бесстрастной материи, либо глупой и дикой политики. Если смотреть на книгу таким образом, то нетрудно понять, как химия стала для г-на Леви в такой же степени «политической школой», как и ремеслом и ремеслом. как его термины могут быть восприняты как «противоядие от фашизма». . . потому что они были четкими, отчетливыми и проверяемыми на каждом шагу, а не тканью лжи и пустоты».
ПРИ всем своем погружении в самые мучительные исторические обстоятельства «Периодическая таблица» не является гневной или задумчивой книгой. Наоборот, это исцеляющая работа спокойного, даже жизнерадостного воображения. Медитативный
сила «Выживания в Освенциме» и «Пробуждения» полностью очевидна, но к ней присоединяется недавно обретенная сила радостной изобретательности. Без сомнения, каждый химик немного волшебник (как и каждый
хочет быть писателем) и надеется извлечь золото из пустой породы, хотя немногим удается это сделать. Спустившись глубоко в матрицу как физической, так и человеческой природы, Примо Леви, кажется, узнал секреты таких трансформаций.
и он написал то, что можно назвать только освобождающей книгой.
Медитативный
сила «Выживания в Освенциме» и «Пробуждения» полностью очевидна, но к ней присоединяется недавно обретенная сила радостной изобретательности. Без сомнения, каждый химик немного волшебник (как и каждый
хочет быть писателем) и надеется извлечь золото из пустой породы, хотя немногим удается это сделать. Спустившись глубоко в матрицу как физической, так и человеческой природы, Примо Леви, кажется, узнал секреты таких трансформаций.
и он написал то, что можно назвать только освобождающей книгой.
Чтобы увидеть, насколько это освобождает, прочитайте «Углерод», заключительную историю, чудесную историю об одном атоме углерода, который пересекает вселенную, проходит через сложные процессы фотосинтеза и останавливается почти волшебным образом.
на кончике авторского пера. То, что это перо привнесло в эти истории благодаря этому неуловимому, но жизненно важному элементу, стало новым открытием жизни, и тем, что подтверждает точку зрения еврейской пословицы, используемой в качестве источника. эпиграф к книге: «Ибергекумене цорес из гут цу дерцейлин» («О преодоленных бедах хорошо рассказывать»).
эпиграф к книге: «Ибергекумене цорес из гут цу дерцейлин» («О преодоленных бедах хорошо рассказывать»).
НЕОЖИДАННОЕ ПРИНУЖДАЕТ НАПИСАТЬ Примо Леви говорит, что он «химик по убеждению» и никогда не думал, что станет писателем. Что побудило его написать, так это время, проведенное в Освенциме. «После Освенцима у меня была острая потребность писать»
он говорит. «Не только как моральный долг, но и как физиологическая потребность». Г-на Леви отправили в Освенцим после того, как он был арестован в итальянском регионе Пьемонт за деятельность Сопротивления и оказался евреем. Он подчеркивает
что преследование евреев в Италии в значительной степени было навязано нацистами, вторгшимися в страну после падения Муссолини, и что собственные антисемитские законы Муссолини часто нарушались. «Итальянцы никогда не любили
законов, либо тогда, либо сейчас», — вспоминал 65-летний автор в телефонном интервью из своего дома в Турине. «Итак, в период расовых законов для христианина стало делом славы иметь друга-еврея».
«Выживание в Освенциме» не имело большого успеха, пока не было переиздано в 1957. «После успеха, — отмечает г-н Леви, — я последовал совету нескольких друзей, которые сказали:
‘почему бы не продолжить свой рассказ?’ «Пробуждение» описывает то, что для него последовало за Освенцимом. «Меня освободили русские, которые спасли мне жизнь. Но после спасения моей жизни (они)
депортировал меня в Россию вместе с другими заключенными». По иронии судьбы два научно-фантастических произведения г-на Леви были переведены только на два языка — немецкий и русский. Через все это автор придерживался своей химии.
Но он говорит, что смог написать «Периодическую таблицу» только после того, как ушел из поля. «Я хотел объяснить непрофессионалу, что значит быть химиком», — говорит он. ”Каждый
элемент приносит мне своего рода «щелчок».
«Итак, в период расовых законов для христианина стало делом славы иметь друга-еврея».
«Выживание в Освенциме» не имело большого успеха, пока не было переиздано в 1957. «После успеха, — отмечает г-н Леви, — я последовал совету нескольких друзей, которые сказали:
‘почему бы не продолжить свой рассказ?’ «Пробуждение» описывает то, что для него последовало за Освенцимом. «Меня освободили русские, которые спасли мне жизнь. Но после спасения моей жизни (они)
депортировал меня в Россию вместе с другими заключенными». По иронии судьбы два научно-фантастических произведения г-на Леви были переведены только на два языка — немецкий и русский. Через все это автор придерживался своей химии.
Но он говорит, что смог написать «Периодическую таблицу» только после того, как ушел из поля. «Я хотел объяснить непрофессионалу, что значит быть химиком», — говорит он. ”Каждый
элемент приносит мне своего рода «щелчок».
