Электродвижущая сила аккумулятора
Можно ли по ЭДС точно судить о степени заряженности аккумулятора?
Электродвижущей силой (ЭДС) аккумулятора называется разность его электродных потенциалов, измеренная при разомкнутой внешней цепи:
Е = φ+ – φ–
где φ+ и φ– – соответственно потенциалы положительного и отрицательного электродов при разомкнутой внешней цепи.
ЭДС батареи, состоящей из n последовательно соединённых аккумуляторов:
Еб = n · Е
В свою очередь, электродный потенциал при разомкнутой цепи в общем случае состоит из равновесного электродного потенциала, характеризующего равновесное (стационарное) состояние электрода (при отсутствии переходных процессов в электрохимической системе), и потенциала поляризации.
Этот потенциал в общем случае определяется как разность между потенциалом электрода при разряде или заряде и его потенциалом в равновесном состоянии в отсутствии тока. Однако следует отметить, что состояние аккумулятора сразу после выключения зарядного или разрядного тока не является равновесным вследствие различия концентрации электролита в порах электродов и межэлектродном пространстве.
Химическая активность реагентов, собранных в электрохимическую систему аккумулятора, и, следовательно, изменение ЭДС аккумулятора весьма незначительно зависит от температуры. При изменении температуры от –30°С до+50°С (в рабочем диапазоне для АКБ) электродвижущая сила каждого аккумулятора в батарее изменяется всего на 0,04 В и при эксплуатации аккумуляторов им можно пренебречь.
С повышением плотности электролита ЭДС повышается. При температуре +18°С и плотности 1,28 г/см3 аккумулятор (имеется в виду одна банка) обладает ЭДС равной2,12 В. Аккумуляторная батарея из шести элементов обладает ЭДС равной 12,72 В(6 ? 2,12 В = 12,72 В).
Аккумуляторная батарея из шести элементов обладает ЭДС равной 12,72 В(6 ? 2,12 В = 12,72 В).
По ЭДС нельзя точно судить о степени заряженности аккумулятора.
ЭДС разряженного аккумулятора с большей плотностью электролита будет выше, чем ЭДС заряженного аккумулятора, но имеющего меньшую плотность электролита. Величина ЭДС исправного аккумулятора зависит от плотности электролита (степени его заряженности) и изменяется от 1,92 до 2,15 В.
При эксплуатации аккумуляторных батарей путём измерения ЭДС можно обнаружить серьёзную неисправность аккумуляторной батареи (замыкание пластин в одной или нескольких банках, обрыв соединительных проводников между банками и тому подобное).
ЭДС измеряют высокоомным вольтметром (внутреннее сопротивление вольтметране менее 300 Ом/В). В ходе выполнения измерений вольтметр присоединяют к выводам аккумулятора или батареи. При этом через аккумулятор (батарею) не должен протекать зарядный или разрядный ток!
***
Электродвижущая сила (ЭДС) – скалярная физическая величина, характеризующая работу сторонних сил, то есть любых сил неэлектрического происхождения, действующих в квазистационарных цепях постоянного или переменного тока.
ЭДС так же, как и напряжение, в Международной системе единиц (СИ) измеряется в вольтах.
ЭДС и внутреннее сопротивление источника тока
19 мая, 2022
1 мин
Физ 🔬
ЭДС (электродвижущая сила) — физическая величина, равная отношению работы сторонних сил по перемещению положительного заряда от отрицательного полюса источника к положительному к величине этого заряда q.
Была открыта Майклом Фарадеем.
Измеряется в вольтах [B].
Внутреннее сопротивление цепи r — определяет количество потерь энергии при прохождении тока через источник тока. Как правило, достаточно мало по сравнению с сопротивлением внешней цепи.
📌 Следствие: разность потенциалов U между полюсами источника тока (напряжение), приложенная к подключённому к полюсам проводнику, меньше ЭДС.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите  Мы обязательно поправим!
Мы обязательно поправим!
Редакция Без Сменки
Честно. Понятно. С душой.
45 подписчиков
+ Подписаться
Редакция Без Сменки
06 июня, 2022
1 мин
Англ 🇬🇧
Strong adjectives
Strong, very strong. Звучит почти как «Бонд. Джеймс Бонд» 😎
Позвольте представиться, strong…
Звучит почти как «Бонд. Джеймс Бонд» 😎
Позвольте представиться, strong…
29 июня, 2022
1 мин
Ист 🤴
Советы перед экзаменом
👉🏻 ЗА НЕДЕЛЮ – постарайся восстановить режим и ложиться в течение недели пораньше, чтобы легко…
Редакция Без Сменки
06 июня, 2022
1 мин
Англ 🇬🇧
Что почитать на английском?
🔸https://www.newsinlevels.com/- на этом сайте можно читать одну и ту же статью/новость на разных…
Редакция Без Сменки
31 октября, 2022
1 мин
Гомологичные и аналогичные органы
В этой подборке собрана подборка гомологичных и аналогичных органов. Гомологичные органы …
Редакция Без Сменки
26 апреля, 2022
1 мин
Физ 🔬
Линза. Фокусное расстояние линзы
Прозрачное для света тело, ограниченное двумя сферическими поверхностями (одна из которых может…
Редакция Без Сменки
03 августа, 2022
1 мин
В этой шпаргалке рассказываем о частых ошибках, которые допускают выпускники во время выполнения. ..
..
Как измеряется ЭДС?
Дата последнего обновления: 18 апреля 2023 г.
Подсказка: E.M.F. это полная энергия, обеспечиваемая ячейкой для прохождения единицы заряда через всю цепь, или она описывается как электрический потенциал, создаваемый либо гальванической ячейкой, либо изменением магнитного поля. ЭМП измеряется в вольтах, что соответствует разности потенциалов.
Полный ответ:
Электродвижущая сила описывается как электрический потенциал, создаваемый либо гальваническим элементом, либо регулированием магнитного поля. ЭДС – это обычно используемая аббревиатура для электродвижущей силы.
Батарея или генератор используются для преобразования энергии из одного режима в другой. В этих устройствах один конец становится положительно заряженным, а противоположный — отрицательным. Соответственно, электродвижущая сила – это работа, совершаемая над единицей электрического заряда.
В электромагнитном расходомере используется электродвижущая сила, что соответствует закону Фарадея. ЭДС численно обозначается как количество джоулей мощности, отдаваемой источником, общим для каждого кулона, чтобы позволить единичному электрическому заряду течь по цепи.
ЭДС численно обозначается как количество джоулей мощности, отдаваемой источником, общим для каждого кулона, чтобы позволить единичному электрическому заряду течь по цепи.
Э.М.Ф. измеряется в вольтах, что равно разности потенциалов. Один вольт равен одному джоулю на кулон.
Примечание: ЭДС отличается от напряжения на клеммах тем, что напряжение на клеммах описывается как разность потенциалов на концах нагрузки, когда цепь включена. Для сравнения, ЭДС определяется как максимальная разность потенциалов, создаваемая батареей, когда ток отсутствует. Вольтметр используется для измерения напряжения на клеммах, тогда как потенциометр используется для измерения ЭДС.
Недавно обновленные страницы
Большинство эубактериальных антибиотиков получено из биологии ризобий класса 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологии класса 12 А 002 Сточные воды или муниципальные канализационные трубы не должны быть непосредственно 12 класса биологии NEET_UG
Очистка сточных вод выполняется микробами A B Удобрения 12 класса биологии NEET_UG
Иммобилизация фермента – это конверсия активного фермента класса 12 биологии NEET_UG
Большинство эубактериальных антибиотиков получают из биологического класса Rhizobium 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологического класса А 12 NEET_UG
12 класс биологии NEET_UG
Канализационные или городские канализационные трубы не должны быть напрямую 12 класс биологии NEET_UG
Очистка сточных вод выполняется микробами A B Удобрения 12 класс биологии NEET_UG
Иммобилизация фермента — это преобразование активного фермента класса 12 биологии NEET_UG
Тенденции сомнений
Студенты также читают
Измерение ЭДС: применение, устройство и единицы измерения твой стакан.
 Что ж, мы не Гарри Поттер, чтобы выполнить эту задачу с помощью магии. Нам нужно вложить свою энергию, чтобы выполнить некоторую работу по подъему и наклону бутылки, чтобы жидкость попала в ваш стакан. Но так не должно происходить. Жидкость может оставаться в бутылке, не вытекайте в стакан. Это все еще происходит, почему? Внутри баллона есть давление. Таким образом, жидкость падает из области высокого давления внутри бутылки (и, конечно, под действием силы тяжести) в область низкого давления в ваш стакан.
Что ж, мы не Гарри Поттер, чтобы выполнить эту задачу с помощью магии. Нам нужно вложить свою энергию, чтобы выполнить некоторую работу по подъему и наклону бутылки, чтобы жидкость попала в ваш стакан. Но так не должно происходить. Жидкость может оставаться в бутылке, не вытекайте в стакан. Это все еще происходит, почему? Внутри баллона есть давление. Таким образом, жидкость падает из области высокого давления внутри бутылки (и, конечно, под действием силы тяжести) в область низкого давления в ваш стакан.Точно так же электроны перемещаются из области высокого потенциала в область низкого потенциала. Если разница в давлении — это то, что направляет воду из верхних резервуаров для воды в ваши краны, то разница потенциалов на двух электродах переводит электроны из высокого потенциала в низкий. Этот поток электронов представляет собой электричество/ток.
Здесь, в этой статье, мы собираемся исследовать ЭДС, которая представляет собой не что иное, как максимальную разность потенциалов между электродами.
- Эта статья о измерении ЭДС .
- Мы познакомим вас с определением ЭДС с точки зрения химии и простейшей формой выражения, используемой для ее расчета, на примере.
- Мы пройдемся по единицам ЭДС.
- Затем мы расскажем о устройствах , которые измеряют ЭДС.
- Затем мы объясним вам еще одно явление – обратную ЭДС .
- Мы закончим к приложений измерения ЭДС в химии.
Определение ЭДС
ЭДС — это сокращение от электродвижущей силы . Хотя в названии есть сила , на самом деле не сила, а форма энергии. Давайте посмотрим на определение ЭДС с точки зрения химии.
Электродвижущая сила определяется как максимальная разность электродных потенциалов 9{+2} = -076V \)
Решение:
Уравнение из определения:
\( E_{cell} = E_{Cathode} – E_{Anode} \)
Поскольку происходит окисление на аноде восстановительный потенциал цинка представляет собой анодную полуреакцию, при которой цинк окисляется от \(Zn(0)\) до \(Zn(+2)\). Точно так же восстановительный потенциал Ag представляет собой полуреакцию восстановления.
Точно так же восстановительный потенциал Ag представляет собой полуреакцию восстановления.
Подстановка значений,
\( E_{ячейка} = 0,80 – (-0,76) \)
Получаем,
\( E_{cell} = 1,56 В\)
Что такое электродный потенциал?
Чтобы понять, что это такое, давайте сначала повторим процессы, происходящие на каждом электроде.
Рис. 1: Ячейка Даниэля.
На приведенном выше рисунке показан элемент Daniel , пример элемента voltaic . Вы уже знаете из статьи – Электрохимические элементы, что происходит и как вырабатывается электричество. Давайте рассмотрим основные моменты, чтобы понять электродный потенциал. 9{+2}\) . Это полуреакция окисления. (Эти катионы цинка переходят в электролит.)
Когда цинк окисляется до катионов цинка, между электродом и электролитом происходит разделение заряда. Это разделение заряда приводит к разности потенциалов этого электрода, которая называется потенциалом одиночного электрода. Таким образом, тенденция электрода создавать разность потенциалов между собой и электролитом называется потенциалом одиночного электрода полуэлемента ( \(Zn\) в \(ZnSO_4\) ).
Таким образом, тенденция электрода создавать разность потенциалов между собой и электролитом называется потенциалом одиночного электрода полуэлемента ( \(Zn\) в \(ZnSO_4\) ).
Точно так же ионы меди (+2) восстанавливаются до атомов меди (0), что является полуреакцией восстановления . (Теперь восстановленная медь осаждается на медном электроде.) Это приведет к разности потенциалов в этой полуэлементе катода между электродом и электролитом.
Проще говоря,
Склонность металла e l электрода к окислению или восстановлению, приводящему к разнице потенциалов между электродом и электролитом, называется электродным потенциалом/ потенциал одного электрода этой полуэлемента.
Склонность металла на аноде к окислению называется потенциалом окисления , а тенденция металла на катоде к восстановлению называется потенциалом восстановления . Если электродный потенциал измеряется в стандартных условиях, он называется стандартным электродным потенциалом .
Если электродный потенциал измеряется в стандартных условиях, он называется стандартным электродным потенциалом .
Чтобы избежать путаницы, IUPAC просто дал нам все эти значения потенциалов отдельных электродов в виде их единых стандартных восстановительных потенциалов. Например, цинк имеет потенциал окисления 9{+2} | Zn} \) \( +0,76 В = -0,76 В \)
Этот восстановительный потенциал является стандартным восстановительным потенциалом. Стандартные восстановительные потенциалы рассчитываются путем размещения половины ячейки с неизвестным восстановительным потенциалом напротив электрода сравнения, восстановительный потенциал которого считается равным нулю. Стандартный водородный электрод (SHE) является наиболее часто используемым электродом сравнения.
Этот стандартный электродный потенциал равен ЭДС этого полуэлемента . Разность электродных потенциалов полуячеек равна общая ЭДС клетки, также называемая потенциалом клетки, E или \( \эпсилон \)
ЭДС, движущая сила потока электронов
Чтобы электроны могли течь, должна быть некоторая энергия, которая толкает их вперед. Разность электродных потенциалов – Разность потенциалов, или полная ЭДС ячейки, заставляет течь электроны.
Разность электродных потенциалов – Разность потенциалов, или полная ЭДС ячейки, заставляет течь электроны.
Как ЭДС заставляет электроны течь?
Электроны имеют в себе потенциальную энергию . По мере увеличения числа электронов общая потенциальная энергия увеличивается, что делает анодная полуячейка как область с высокой потенциальной энергией (ПЭ). [2] Также накопление электронов приводит к отталкиванию и электроны просто хотят оттуда уйти. В то время как, с другой стороны, в области катода мало электронов, следовательно, мало потенциальной энергии, таким образом, катод представляет собой область с низкой потенциальной энергией. [2]
Теперь эта разность потенциалов (высокий и низкий) заставляет электроны двигаться от анода (высокий PE) к катоду (низкий PE), точно так же, как в водопаде, где вода под высоким давлением стекает в область пониженного давления. Этот поток электронов генерирует электричество, как обсуждалось во введении.
Этот поток электронов генерирует электричество, как обсуждалось во введении.
Эта разность потенциалов является движущей силой движения электронов и генерации электричества. ЭДС представляет собой разницу в индивидуальных разностях потенциалов (потенциалы электродов/восстановительные потенциалы) двух электродов. Точно так же, как разница в массах снова является массой и измеряется в граммах, разница в индивидуальных разностях потенциалов снова является разностью потенциалов, измеряемой в вольтах.
Следовательно, \(E_{Катод} – E_{Анод\} \) дает нам ЭДС этой ячейки.
Путешествие электронов с точки зрения восстановительного потенциала
Эту концепцию потенциальной энергии не следует путать с электродными потенциалами. Анод имеет низкий потенциал электрода , что означает низкий потенциал восстановления, и по этой причине металл на аноде не хочет восстанавливаться, а хочет окисляться. Следовательно, хочет пнуть электроны. С другой стороны, катод имеет высокий электродный потенциал — означает высокий восстановительный потенциал, поэтому он захватывает входящие электроны.
Рис. 2: Изображение анода и катода.
Чтобы представить путь электронов с точки зрения восстановительного потенциала , мы можем сказать, что в гальваническом элементе электроны перемещаются из области с низким потенциалом (анод) в область с высоким потенциалом (катод) – [из области, где тенденция
Полуэлемент представляет собой металлический стержень (называемый электродом), погруженный в раствор ионов металла (называемый электролитом). Важно отметить, что невозможно измерить абсолютный потенциал отдельного электрода/восстановительный потенциал электрода. Он всегда измеряется относительно, что означает использование стандартного электрода сравнения, такого как SHE.
Единицы измерения ЭДС
ЭДС измеряется в вольтах (единица СИ). В физике ЭДС также описывается как проделанная работа, измеряемая в джоулях для перемещения единичного заряда в кулонах из одной точки в другую.
Таким образом, Вольт, \(V = \frac{W} {Q} \)
Где:
- Вт = выполненная работа = Дж
- Q = заряд единицы = кулон
$$V=\frac {J}{C}$$
Вольт также является единицей стандартного восстановительного потенциала.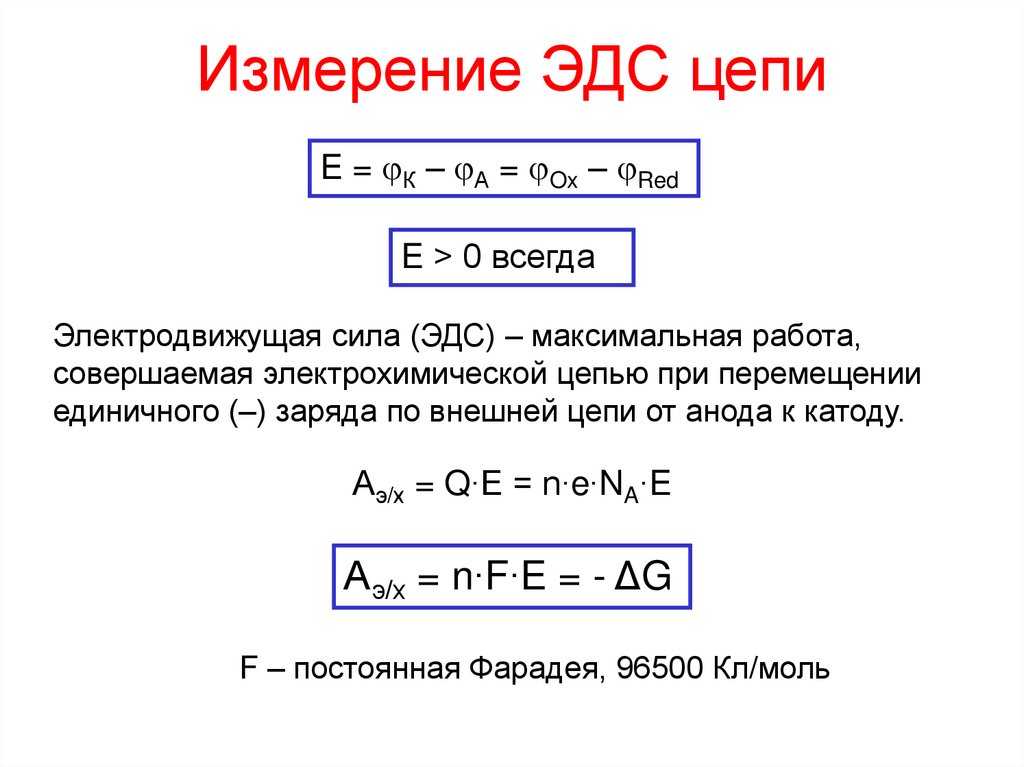
Приборы для измерения электромагнитного поля
Для измерения ЭДС используются два устройства: потенциометр и вольтметр.
Обычно потенциометр предпочтительнее вольтметра, потому что потенциометр не потребляет ток из цепи для измерения ЭДС и, таким образом, не возмущает цепь. Вольтметр, с другой стороны, будет потреблять некоторый ток из цепи для измерения ЭДС. Поэтому потенциометр более надежен и точен по сравнению с вольтметром, но в то же время дороже вольтметра, что является его недостатком.
Рис. 3: Фото вольтметра | Wikimedia Commons
Измерение обратной ЭДС
Само название дает нам некоторую информацию об этом типе ЭДС. Обратная ЭДС или задняя ЭДС — это разность потенциалов, которая работает против приложенного напряжения/фактической ЭДС, которая может быть определена как:
«Противодействующая ЭДС, которая генерируется в электролите при адсорбции продуктов электролиза (газов или газообразных ионов). на поверхность электродов называется обратной ЭДС, задней ЭДС или противоЭДС». [3]
[3]
Лучшим примером для объяснения обратной ЭДС является электролитическая ячейка, содержащая платиновые электроды, погруженные в раствор серной кислоты. Мы знаем, что происходит при электролизе подкисленной воды. На катоде выделяется газообразный водород, а на аноде выделяется газообразный кислород. Некоторое внешнее напряжение (ЭДС через батарею) применяется для запуска этой реакции, поскольку она не является самопроизвольной.
Через некоторое время электролиз останавливается из-за адсорбции газов на поверхности электродов. Это вызывает обратную ЭДС, которая, когда превышает приложенное внешнее напряжение, приводит к остановке электролиза. Чтобы преодолеть эту контратаку, мы должны медленно увеличивать внешнее напряжение. Когда эта внешняя ЭДС снова превышает противоЭДС, электролиз протекает гладко.
Применение измерения ЭДС
Существует несколько применений измерения ЭДС. Здесь мы даем вам список нескольких важных приложений:
- Константа равновесия для реакции полуэлемента может быть определена путем измерения ЭДС.

- Свободная энергия Гибба .
- Можно определить произведение растворимости малорастворимой соли.
- Можно определить валентность числа электронов, переданных в реакции полуэлемента. 9H\) решения можно вычислить.
- Самопроизвольность электрохимической реакции можно определить. Если потенциал ячейки положительный, это спонтанная реакция (гальванического элемента). Если потенциал ячейки отрицателен, это несамопроизвольная реакция (электролитической ячейки).
На этом тема измерения ЭДС завершена. В этой статье мы объяснили, что такое ЭДС и как она отвечает за поток электронов и, в свою очередь, за генерацию электричества. Теперь вы, возможно, поняли концепцию батарей, которые вы используете в своей повседневной жизни.
Измерение ЭДС – основные выводы
- Электродвижущая сила определяется как максимальная разность электродных потенциалов [1] двух электродов ячейки.
 ЭДС обозначается буквой E. ЭДС иногда называют напряжением.
ЭДС обозначается буквой E. ЭДС иногда называют напряжением.\( E_{cell} = E_{Cathode} – E_{Anode} \)
Электроны текут от анода с (низким восстановительным потенциалом) к катоду (с высоким восстановительным потенциалом).
ЭДС – это разность потенциалов, возникающая из-за разделения зарядов. Эта разница потенциалов является движущей силой движения электронов.
Разность потенциалов, возникающая на границе раздела электрод/электролит, дает ЭДС этого полуэлемента, который также называется потенциалом электрода или восстановительным потенциалом этого полуэлемента. Потенциал ячейки представляет собой разность электродных потенциалов двух полуячеек.
ЭДС можно измерить с помощью двух устройств, называемых потенциометром и вольтметром.
Единицами ЭДС являются Вольты или Джоуль/Кулон.
«Противодействующая ЭДС, которая генерируется в электролите, когда продукты электролиза (газы или газообразные ионы) адсорбируются на поверхности электродов, известна как обратная ЭДС, задняя ЭДС или противоЭДС».

