Таблица Менделеева online – Fr
Fr
87
1
8
18
32
18
18
8
2
223.0197
7s1
Франций
Изотопы
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
Период полураспада (T1/2) |
Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 199Fr | 87 | 112 | 199,00726 | 16 мс | 1/2+ |
| 200Fr | 87 | 113 | 200,00657 | 24 мс | 3+ |
| 200mFr | 60 кэВ | 650 мс | 10- | ||
| 201Fr | 87 | 114 | 201,00386 | 67 мс | 9/2- |
| 202Fr | 87 | 115 | 202,00337 | 290 мс | 3+ |
| 202mFr | 330 кэВ | 340 мс | 10- | ||
| 203Fr | 87 | 116 | 203,000925 | 550 мс | 9/2- |
| 204Fr | 87 | 117 | 204,000653 | 1,7 с | 3+ |
| 204m1Fr | 50 кэВ | 2,6 с | 7+ | ||
| 204m2Fr | 326 кэВ | 1,7 с | 10- | ||
| 205Fr | 87 | 118 | 204,998594 | 3,80 с | 9/2- |
| 206Fr | 87 | 119 | 205,99867 | 16 с | 2+ |
| 206m1Fr | 190 кэВ | 15,9 с | 7+ | ||
| 206m2Fr | 730 кэВ | 700 мс | 10- | ||
| 207Fr | 87 | 120 | 206,99695 | 14,8 с | 9/2- |
| 208Fr | 87 | 121 | 207,99714 | 59,1 с | 7+ |
| 209Fr | 87 | 122 | 208,995954 | 50,0 с | 9/2- |
| 210Fr | 87 | 123 | 209,996408 | 3,18 мин | 6+ |
| 211Fr | 87 | 124 | 210,995537 | 3,10 мин | 9/2- |
| 212Fr | 87 | 125 | 211,996202 | 20,0 мин | 5+ |
| 213 |
87 | 126 | 212,996189 | 34,6 с | 9/2- |
| 214Fr | 87 | 127 | 213,998971 | 5,0 мс | 1- |
| 214m1Fr | 123 кэВ | 3,35 мс | 8- | ||
| 214m2Fr | 638 кэВ | 103 нс | 11+ | ||
| 214m3Fr | 6,477 МэВ | 108 нс | 33+ | ||
| 215Fr | 87 | 128 | 215,000341 | 9/2- | |
| 216Fr | 87 | 129 | 216,003198 | 700 нс | 1- |
| 217Fr | 87 | 130 | 217,004632 | 16,8 мкс | 9/2- |
| 218Fr | 87 | 131 | 218,007578 | 1,0 мс | 1- |
| 218m1Fr | 86 кэВ | 22,0 мс | |||
| 218m2Fr | 200 кэВ | high | |||
| 219Fr | 87 | 132 | 219,009252 | 20 мс | 9/2- |
| 220Fr | 87 | 133 | 220,012327 | 27,4 с | 1+ |
| 221Fr | 87 | 134 | 221,014255 | 4,9 мин | 5/2- |
| 222Fr | 87 | 135 | 222,017552 | 14,2 мин | 2- |
| 223Fr | 87 | 136 | 223,0197359 | 22,00 мин | 3/2- |
| 224Fr | 87 | 137 | 224,02325 | 1- | |
| 225Fr | 87 | 138 | 225,02557 | 4,0 мин | 3/2- |
| 226Fr | 87 | 139 | 226,02939 | 49 с | 1- |
| 227Fr | 87 | 140 | 227,03184 | 2,47 мин | 1/2+ |
| 228Fr | 87 | 141 | 228,03573 | 38 с | 2- |
| 229Fr | 87 | 142 | 229,03845 | 50,2 с | 1/2+ |
| 230Fr | 87 | 143 | 230,04251 | 19,1 с | |
| 231Fr | 87 | 144 | 231,04544 | 17,6 с | 1/2+ |
| 232Fr | 87 | 145 | 232,04977 | 5 с | |
описание и свойства элемента, способ получения и сферы применения
Описание этого элемента идет в превосходной степени: самый массивный в своем семействе, самый неустойчивый, второй по редкости. Назван в честь одной из самых романтичных стран Европы. Однако о франции известно мало, ученые изучают его до сих пор.
Назван в честь одной из самых романтичных стран Европы. Однако о франции известно мало, ученые изучают его до сих пор.
Содержание
- Что представляет собой
- Как был открыт
- Присутствие в природе
- Технология получения
- Физико-химические характеристики
- Где используется
- Биологическое воздействие
- Стоимость
Что представляет собой
Франций – это элемент №87 таблицы Менделеева. Радиоактивный, относится к щелочным металлам.
Международное обозначение и формула вещества – Fr (Francium).
Как был открыт
Существование франция предсказал Дмитрий Менделеев. На основе предполагаемых свойств он классифицировал элемент как эка-цезий.
Физическое открытие случилось в парижском Институте радия почти семьдесят лет спустя, в 1939 году.
«Неуловимость» элемента обусловлена уникальным тандемом характеристик: микроскопическая ядерная устойчивость на фоне высокой химической активности.
Обнаружить элемент удалось благодаря феномену радиоактивности. Неизвестное излучение заметила Маргарита Пере, работавшая с изотопом актиния.
Она же – автор имени. С 1946 года новооткрытый элемент вошел в историю как франций, по названию родной страны первооткрывательницы.
-50%
Большой выбор украшений из натуральных камней и минералов со скидкой -50%
Show Less
Присутствие в природе
Элемент – второй по редкости на планете. Его опережает только астат.
В природе на 1 атом франция приходится три триллиона атомов урана.
По составу это конгломерат трех десятков изотопов.
- Это свойство (радиогенность) уравновешивается: распавшиеся атомы сменяются новыми. Они представляют собой транзитный продукт распада изотопов тория (232) и урана (235).
- На планете выявлены изотопы вещества 223 и 224.
 Они «исчезают», соответственно, за 22 минуты 18 секунд и 175 секунд.
Они «исчезают», соответственно, за 22 минуты 18 секунд и 175 секунд. - Франций-223 – результат распада актиния-227 (отсюда его старое название «актиний К»), 224-й получается в реакциях с участием тория.
Микродозы вещества присутствуют в ториевых и урановых рудах.
Запасы франция-223 в земной коре не превышают трети килограмма, изотопа-224 – полуграмма.
Технология получения
Нанодозы франция-223 и -224 выделяют из актиния, ториевого и уранового сырья.
Способ получения базируется на экстракции либо хроматографии.
Другие изотопы синтезируются ядерными установками. В реакциях задействовано золото.
Физико-химические характеристики
Из-за сроков полураспада ученым доступны образцы с долей франция в одну стомиллионную грамма.
Информацию получают расчетным, а не опытным путем. Базой служат данные для рядовых щелочных металлов. Также задействуется оборудование Европейского центра по ядерным исследованиям (ЦЕРНа).
| Свойства атома | |
|---|---|
| Название, символ, номер | Франций / Francium (Fr), 87 |
| Атомная масса | 223,0197 а. е. м. (г/моль) |
| Электронная конфигурация | [Rn] 7s1 |
| Радиус атома | 290 пм |
| Химические свойства | |
| Радиус Ван-дер-Ваальса | 348 пм |
| Радиус иона | (+1e) 179 пм |
| Электроотрицательность | 0,7 (шкала Полинга) |
| Электродный потенциал | Fr←Fr+ −2,92 В |
| Степени окисления | 0; +1 |
| Энергия ионизации (первый электрон) | 392,96 (4,0727) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
Плотность (при н. у.) у.) | 2,3—2,5 г/см³ |
| Температура плавления | 18—21 °C; 291—294 K |
| Температура кипения | 640—660 °C (910—930 К) расчётная: 598 °C, 871 K |
| Критическая точка | (расчётная) 1980 ± 50 К, ? МПа |
| Уд. теплота плавления | ~2 кДж/моль |
| Уд. теплота испарения | ~65 кДж/моль |
| Молярная теплоёмкость | 31,6 Дж/(K·моль) |
| Структура решётки | кубическая, объёмноцентрированая |
| Номер CAS | 7440-73-5 |
Поэтому за почти столетие со дня открытия элемента полной ясности о его свойствах нет. Например, о цвете, сплавах.
Однако некоторые характеристики франция как металла установлены:
- Структура кристаллической решетки – куб.
- Самая малая устойчивость.
- Самая малая электроотрицательность среди известных элементов.
- Самая высокая масса, химическая активность в сегменте щелочных металлов.
- Образует два десятка соединений разной степени растворимости водой.
Признаки 2-4 позволяют отличить франций от других элементов.
По химическим свойствам, физическим параметрам активный металл сродни цезию: бурно реагирует с водой, присутствует в цезиевых соединениях.
Более 8000 видов товара из 500 разновидностей натурального камня. Ежедневное обновление!
Show Less
Где используется
Учеными используется 223-й изотоп франция, чтобы оперативно выявить в природных объектах актиний-227.
Недостатки металла – малый период полураспада плюс радиоактивность – делают его непригодным для практического применения. О промышленном производстве речи нет.
Хлорид вещества распознает онкологию, но дороговизна обнуляет это достоинство.
Франций представляет интерес только для ученых-теоретиков.
Биологическое воздействие
Франций аккумулируется почками, печенью, слюной, раковыми структурами.
Поэтому изотопы 212 и 223 – инструмент исследователей биологических организмов и онкодиагностики.
Стоимость
На общедоступном рынке продукция на основе радиоактивного элемента не представлена. Цена за грамм не озвучивается.
Франций – Информация об элементе, свойства и использование
Перейти к основному содержанию
У вас не включен JavaScript.
Пожалуйста, включите JavaScript, чтобы получить доступ ко всем функциям сайта.
Перейти к радию >
| Группа | 1 | Температура плавления | 21°С, 70°F, 294 К |
| Период | 7 | Температура кипения | 650°С, 1202°F, 923 К |
| Блок | с | Плотность (г см −3 ) | Неизвестный |
| Атомный номер | 87 | Относительная атомная масса | [223] |
| Состояние при 20°С | Твердый | Ключевые изотопы | 223 Пт |
| Электронная конфигурация | [Рн] 7с 1 | КАС номер | 7440-73-5 |
| ChemSpider ID | 4886484 | ChemSpider — бесплатная база данных химической структуры. | |
Изображение отражает древнюю культурную «галльскую» иконографию Франции, страны, давшей название элементу.
Сильно радиоактивный металл.
Франций бесполезен, его период полураспада составляет всего 22 минуты.
Франций не играет известной биологической роли. Он токсичен из-за своей радиоактивности.
Франций получают бомбардировкой радия нейтронами в ядерном реакторе. Его также можно получить путем бомбардировки тория протонами.
Элементы и история периодической таблицы
Менделеев сказал, что должен существовать такой элемент, как цезий, ожидающий своего открытия. Следовательно, были претензии, опровержения и встречные претензии со стороны ученых, которые утверждали, что нашли его. В течение 1920-х и 30-х годов, эти утверждения были сделаны на основе необъяснимой радиоактивности минералов или новых линий в их рентгеновских спектрах, но в конечном итоге все они не оказались доказательством наличия элемента 87.
Франций был наконец обнаружен в 1939 году Маргаритой. Перей в Институте Кюри в Париже. Она очистила образец актиния от всех известных радиоактивных примесей, но его радиоактивность по-прежнему указывала на присутствие другого элемента, который, как она правильно сделала, был отсутствующим элементом 87. Другие тоже оспаривали ее результаты, и только после мировой войны II, что она была признана законным первооткрывателем в 1946.
| Атомный радиус, несвязанный (Å) | 3,48 | Ковалентный радиус (Å) | 2,42 |
| Сродство к электрону (кДж моль −1 ) | 44,38 | Электроотрицательность (шкала Полинга) | 0,7 |
| Энергии ионизации (кДж моль −1 ) | 1 ст 392,96 | ||
| Общие степени окисления | 1 | ||||
| Изотопы | Изотоп | Атомная масса | Естественное изобилие (%) | Период полураспада | Режим распада |
| 223 Пт | 223. 020 020 | – | 22,0 м | β- | |
| | α | ||||
| Удельная теплоемкость (Дж кг -1 К -1 ) | Неизвестный | Модуль Юнга (ГПа) | Неизвестный | |||||||||||
| Модуль сдвига (ГПа) | Неизвестный | Объемный модуль (ГПа) | Неизвестный | |||||||||||
| Давление пара | ||||||||||||||
| Температура (К) |
| |||||||||||||
| Давление (Па) |
| |||||||||||||
| Слушайте подкаст Francium |
Стенограмма: (Промо) Вы слушаете Химию в ее стихии, представленную вам Chemistry World , журналом Королевского химического общества. (Конец промо) Крис Смит На этой неделе мы ищем химическое вещество, названное в честь Франции. Но вам понадобится очень хорошее зрение, потому что на всей земле его меньше килограмма. Знаете, что это еще? Вот Питер Уотерс. Питер Уотерс В 1929 году мадам Кюри наняла недавно получившую квалификацию двадцатилетнюю лаборантку Маргерит Катрин Перей в качестве ее лаборанта. Десять лет спустя эта выдающаяся женщина открыла столь популярный элемент франций. В результате ей было предложено учиться на степень, а затем и на докторскую степень. Несмотря на то, что ее мать была убеждена, что она потерпит неудачу, в марте 1946 года Перей успешно защитила диссертацию об элементе 87. Шестнадцать лет спустя она стала первой женщиной, избранной членом Французской академии наук, а эта честь даже не была присуждена. своей наставнице мадам Кюри. Но история элемента 87 начинается намного раньше, чем дата его открытия в 1939 году. Более 40 лет спустя было высказано предположение, что каждый элемент имеет уникальную пронумерованную позицию в периодической таблице, известную как его атомный номер. Физик Генри Мозли доказал существование «атомного числа», а также предположил, что оно представляет собой количество положительно заряженных протонов в ядре атома. Как только были присвоены атомные номера всем известным элементам, стало ясно, что в периодической таблице отсутствуют семь элементов между водородом с атомным номером 1 и ураном с номером 9.2. Франций под номером 87 был последним из этих элементов, открытых в природе. Из его положения в таблице было ясно, что элемент 87 будет химически активным щелочным металлом, самым тяжелым членом семейства лития, натрия, калия, рубидия и цезия. Два простых правила определяют, какие элементы образуются при распаде. Для каждой альфа-частицы, испускаемой радиоактивным образцом, атомный номер образовавшегося элемента-продукта на два меньше, чем элемент, из которого он образовался. Для каждой испущенной бета-частицы атомный номер продукта увеличивается на единицу. Элемент с атомным номером 89, на два знака правее нашего 87, — это актиний, открытый в 1899 году. она могла наблюдать только выбросы этого элемента. В конце концов она поняла, что большая часть актиния (почти 99% на самом деле) медленно распадается с испусканием бета-частицы, образуя элемент 90, торий. Затем он распадается, испуская альфа-частицу с образованием элемента 88, радия. Во время этих первоначальных исследований Перей назвала свой элемент актинием-К; ссылка на маршрут, по которому он формируется. Однако ей нужно было правильное имя для своего элемента. Во время своего докторского экзамена она предложила название «катий», поскольку думала, что это металл, который легче всего теряет электрон с образованием катиона. К счастью, это имя было встречено без особого энтузиазма — один из ее экзаменаторов даже предположил, что англоязычные люди могут подумать, что оно названо в честь кошки. Затем Перей предложила имя Francium в честь ее родной страны, и это имя было принято. Несмотря на то, что он встречается в природе, или, если быть более точным, естественным образом образуется, хотя и ненадолго, при радиоактивном распаде других элементов, количество франция на Земле ничтожно мало. Примечательно, что, учитывая его короткий период полураспада, стало возможным экспериментально измерить энергию, необходимую для удаления электрона из франция с образованием положительно заряженного катиона франция. Крис Смит Так что эксперимент, который мы все хотели провести в школе и бросить туда кусок франция, в конце концов, не был бы таким впечатляющим. Тогда я просто остановлюсь на цезии. На следующей неделе вы говорите помидор, я говорю помидор, но когда дело доходит до элемента номер 13, кто на самом деле прав? Кира Вайсман Сэр Хамфри Дэви, химик из Корнуолла, открывший этот металл, назвал его «алюминием» в честь одного из исходных соединений — квасцов. Однако вскоре после этого вмешался Международный союз теоретической и прикладной химии (или IUPAC), стандартизировавший суффикс до более традиционного «ium». Крис Смит И вы можете догнать историю о веществе, которое дало нам сверхлегкие самолеты и одноименную банку с напитком, на следующей неделе Химия в своей стихии. Я Крис Смит, спасибо за внимание и до свидания. (Промо) Химия в ее стихии представлена вам Королевским химическим обществом и произведена thenakedscientists.com. Дополнительную информацию и другие эпизоды химии в ее стихии можно найти на нашем веб-сайте chemistryworld.org/elements. (окончание акции) |
Нажмите здесь, чтобы посмотреть видео о Francium
Learn Chemistry: ваш единственный путь к сотням бесплатных учебных ресурсов по химии.
Изображения и видео Visual Elements
© Murray Robertson 1998-2017.
W. M. Haynes, ed., CRC Handbook of Chemistry and Physics , CRC Press/Taylor and Francis, Boca Raton, FL, 95th Edition, Internet Version 2015, по состоянию на декабрь 2014 г.1 903 & Chemical Constants, Kaye & Laby Online, 16-е издание, 1995 г. Версия 1.0 (2005 г.), по состоянию на декабрь 2014 г.
Дж. С. Курси, Д. Дж. Шваб, Дж. Дж. Цай и Р. А. Драгосет, Атомные веса и изотопные композиции (версия 4.1) , 2015 г., Национальный институт стандартов и технологий, Гейтерсберг, Мэриленд, по состоянию на ноябрь 2016 г.
TL Cottrell, The Strengths of Chemical Bonds , Butterworth, London, 1954.
John Emsley, Nature’s Building Blocks: An AZ Guide to the Elements , Oxford University Press, New York, 2nd, New York, 2nd. Издание 2011 г.
Издание 2011 г.
Национальный ускорительный центр Томаса Джефферсона — Управление научного образования, It’s Elemental — The Periodic Table of Elements, по состоянию на декабрь 2014 г.
Периодическая таблица видео, по состоянию на декабрь 2014 г.
Частично получены из материалов, предоставленных Британской геологической службой © NERC.
Исторический текст
Элементы 1-112, 114, 116 и 117 © Джон Эмсли 2012. Элементы 113, 115, 117 и 118 © Королевское общество химии 2017.
Podccasts
. .
Создано видеожурналистом Брэди Хараном, работающим с химиками Ноттингемского университета.
Загрузите наше бесплатное приложение Периодической таблицы для мобильных телефонов и планшетов.
Исследуйте все элементы
Франций
Зона данных | Открытие | Факты | Внешний вид и характеристики | Использование | Изобилие и изотопы | Ссылки
87
Fr
(223)
Химический элемент франций относится к щелочным металлам. Он был открыт в 1939 году Маргаритой Перей.
Он был открыт в 1939 году Маргаритой Перей.
Зона данных
| Классификация: | Франций – щелочной металл |
| Цвет: | серебристо-серый металлик (предположительно) |
| Атомный вес: | (223), без стабильных изотопов |
| Состояние: | твердый |
| Температура плавления: | 27 или С, 300 К |
| Точка кипения: | 677 или С, 950 К |
| Электроны: | 87 |
| Протоны: | 87 |
| Нейтроны в наиболее распространенном изотопе: | 136 |
| Электронные оболочки: | 2,8,18,32,18,8,1 |
| Электронная конфигурация: | [Rn] 7s 1 |
| Плотность @ 20 o C: | 1,873 г/см 3 |
Показать больше, в том числе: Теплота, Энергия, Окисление,
Реакции, Соединения, Радиусы, Проводимости
| Атомный объем: | 71,07 см 3 /моль |
| Структура: | считается bcc: объемно-центрированный куб |
| Твердость: | – |
| Удельная теплоемкость | – |
| Теплота плавления | 2 кДж моль -1 |
| Теплота распыления | 73 кДж моль -1 |
| Теплота парообразования | 64 кДж моль -1 |
| 1 st энергия ионизации | 384 кДж моль -1 |
| 2 -й энергия ионизации | – |
| 3 rd энергия ионизации | – |
| Сродство к электрону | – |
| Минимальная степень окисления | 0 |
Мин. общее окисление нет. общее окисление нет. | 0 |
| Максимальная степень окисления | 1 |
| Макс. общее окисление нет. | 1 |
| Электроотрицательность (шкала Полинга) | 0,7 |
| Объем поляризуемости | 48,7 Å 3 |
| Реакция с воздухом | – |
| Реакция с 15 M HNO 3 | – |
| Реакция с 6 М HCl | энергичный, ⇒ H 2 , FrCl |
| Реакция с 6 М раствором NaOH | энергичный, ⇒ H 2 , FrOH |
| Оксид(ы) | – |
| Гидрид(ы) | – |
| Хлорид(ы) | – |
| Атомный радиус | – |
| Ионный радиус (1+ ион) | 194 вечера |
| Ионный радиус (2+ ион) | – |
| Ионный радиус (3+ ион) | – |
| Ионный радиус (1-ион) | – |
| Ионный радиус (2-ион) | – |
| Ионный радиус (3-ионный) | – |
| Теплопроводность | 3,61 Вт·м -1 К -1 |
| Электропроводность | – |
| Температура замерзания/плавления: | 27 или С, 300 К |
Этот образец урановой руды содержит около 100 000 атомов франция-223 (3,3 x 10 -20 г). Франций радиоактивен; менее 30 г его существует на Земле в любой момент времени. Изображение № (1)
Франций радиоактивен; менее 30 г его существует на Земле в любой момент времени. Изображение № (1)
Открытие франция
Доктор Дуг Стюарт
Франций был открыт Маргерит Перей в 1939 году, когда она исследовала радиоактивный распад актиния-227.
Открытие произошло в Институте Кюри в Париже. Элемент получил свое название от страны его открытия – Франции.
Открытие началось в 1935 лет, когда Перею было 26 лет, он прочитал исследовательскую работу, в которой утверждалось, что американские ученые обнаружили бета-частицы, испускаемые актинием, который имеет более высокое количество энергии, чем обычно.
Перей заинтересовалась этим открытием, и, уже будучи экспертом по работе, связанной с актинием, она решила провести свои собственные эксперименты с актинием. Она изготовила сверхчистый образец актиния и изучила его излучение. Перей обнаружил, что около 1% радиоактивности актиния было вызвано тем, что он испускал альфа-, а не бета-частицы.
Перей обнаружил, что актиний-227 может распадаться, испуская ядро гелия (также называемое альфа-частицей) из собственного ядра. Образовавшееся дочернее ядро представляло собой ранее не открытый элемент, который она решила назвать францием в честь своей родины, Франции.
227 Ac → 223 Fr + 4 He
С 87 протонами новый элемент относился к группе 1 периодической таблицы, присоединяясь к другим пяти щелочным металлам: литию, натрию, калию, рубидию и цезию.
Открытие франция завершило открытие человечеством природных элементов.
Все элементы, обнаруженные с тех пор, были обнаружены, когда элемент был произведен в лаборатории.
Щелочные металлы – свойства и реакции.
Ядро испускает бета-частицу (электрон) и антинейтрино. В результате нейтрон в ядре превращается в протон. Когда это делает элемент 87 периодической таблицы (франций), лишний протон означает, что он становится элементом 88 (радий).
Внешний вид и характеристики
Вредное воздействие:
Франций высокорадиоактивен.
Характеристики:
Франций — тяжелый, нестабильный, радиоактивный металл с максимальным периодом полураспада всего 22 минуты. Он имеет низкую температуру плавления (27 o C, 81 o F) и, если бы его можно было накопить в достаточном количестве, он был бы жидким в теплой комнате.
Франций — второй по редкости элемент в земной коре после астата. В любой момент времени на Земле существует менее тридцати граммов франция.
Франций является наименее электроотрицательным из всех элементов, поэтому он должен быть наиболее химически активным щелочным металлом. К сожалению, его нет в достаточном количестве, чтобы показать, как он реагирует с водой — его производят в крошечных количествах в ускорителях частиц. Теоретически его реакция с водой должна быть более бурной, чем у цезия, и гораздо более бурной, чем у натрия.
Франций совсем недавно изучался в Университете Стоуни-Брук в Нью-Йорке. Ученые улавливали до десяти тысяч атомов франция одновременно, используя лазерные лучи в магнитном поле, чтобы измерить их свойства.
Использование франция
В коммерческих целях франций не используется из-за его редкости и нестабильности. Он используется только в исследовательских целях.
Распад франция
Изотопы франция с массовыми числами от 200 до 232 чаще всего подвергаются альфа- или бета-распаду.
Вот лишь несколько примеров путей распада франция:
Франций-223 — самый долгоживущий изотоп элемента. Период полувыведения составляет 22 минуты. Он может испускать альфа-частицу (ядро гелия) с образованием астата-219.или бета-частица с образованием радия-223. (Бета-частица — это электрон, испускаемый ядром при превращении нейтрона в протон.)
Франций-221 имеет период полураспада 5 минут. Он может испускать альфа-частицу, образуя астат-217, или бета-частицу, превращаясь в радий-221.
Франций-216 имеет период полураспада 0,7 микросекунды. Он может испускать альфа-частицу с образованием астата-212 или позитрон с образованием радона-216.
Франций-212 имеет период полураспада 19 минут. Он может испускать альфа-частицу с образованием астата-208 или захватывать орбитальный электрон с образованием радона-212. (2) (Во время орбитального захвата электрона ядро захватывает один из собственных электронов атома и испускает нейтрино.)
Изобилие и изотопы
Изобилие в земной коре: ~ 0 частей на миллион, ~ 0 частей на миллион
Изобилие в солнечной системе: ~ 0 частей на миллиард по весу, ~ 0 частей на миллиард по молям
Стоимость в чистом виде: $ за 100 г
Стоимость в массе: $ за 100 г
Источник: Франций встречается в природе в результате альфа радиоактивный распад актиния.
Изотопы: Франций имеет 33 изотопа с известным периодом полураспада и массовыми числами от 200 до 232. Ни один из них не является стабильным.


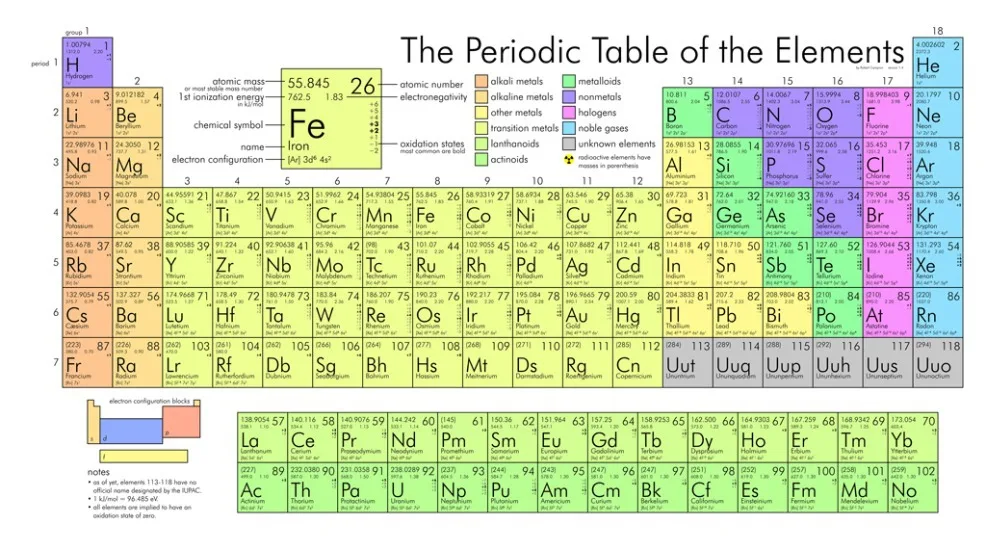
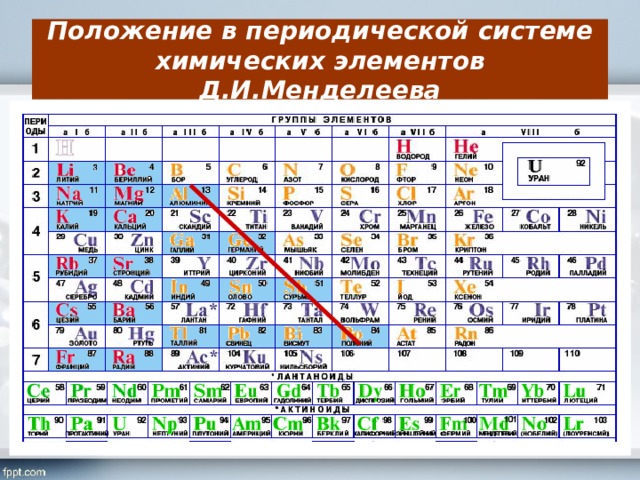
 Когда Менделеев впервые предложил свою периодическую таблицу в 1869 году, он оставил пробелы для еще не открытых элементов, существование которых он предсказывал. Один из таких пробелов находился под цезием, положение, которое, как позже выяснилось, принадлежало францию.
Когда Менделеев впервые предложил свою периодическую таблицу в 1869 году, он оставил пробелы для еще не открытых элементов, существование которых он предсказывал. Один из таких пробелов находился под цезием, положение, которое, как позже выяснилось, принадлежало францию. Следовательно, многие исследователи начали искать новый металл в рудах, содержащих эти родственные элементы. Было сделано много ложных заявлений, прежде чем стало понятно, что отсутствующий элемент будет радиоактивным без стабильной формы. Затем поиск сосредоточился на изучении последовательностей распада других радиоактивных элементов.
Следовательно, многие исследователи начали искать новый металл в рудах, содержащих эти родственные элементы. Было сделано много ложных заявлений, прежде чем стало понятно, что отсутствующий элемент будет радиоактивным без стабильной формы. Затем поиск сосредоточился на изучении последовательностей распада других радиоактивных элементов.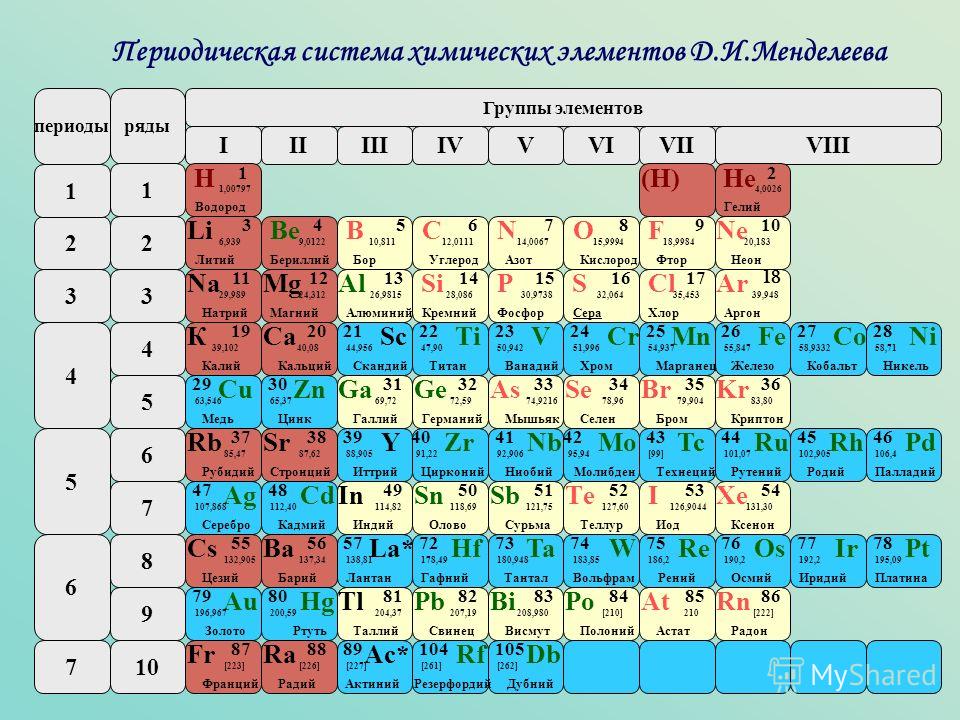 Однако около 1% актиния этого не делает, а вместо этого испускает альфа-частицу, образуя отсутствующий элемент щелочного металла 87. Это стало еще труднее обнаружить из-за того факта, что период полураспада франция составляет всего 21 минуту, потому что он быстро испускает бета-частицу, чтобы снова сформировать радий.
Однако около 1% актиния этого не делает, а вместо этого испускает альфа-частицу, образуя отсутствующий элемент щелочного металла 87. Это стало еще труднее обнаружить из-за того факта, что период полураспада франция составляет всего 21 минуту, потому что он быстро испускает бета-частицу, чтобы снова сформировать радий. Было подсчитано, что в любой момент времени во всей земной коре содержится менее килограмма этого элемента. Более того, к удивлению большинства химиков и вопреки известным тенденциям таблицы Менделеева, оказывается, что франций является , а не самым реакционноспособным металлом. Спускаясь по группе в периодической таблице, в среднем самые внешние электроны удаляются все дальше и дальше от ядра, и в результате их становится легче удалить из атома. Это тенденция для элементов лития, натрия, калия, рубидия и цезия. Однако для действительно тяжелых элементов наличие такого количества положительно заряженных протонов в ядре приводит к тому, что электроны движутся с невероятно высокой скоростью, приближающейся к звуку света. Как понял Эйнштейн, на таких скоростях происходят странные вещи. Электроны становятся немного ближе к ядру, чем ожидалось, и их также становится немного труднее удалить, чем ожидалось.
Было подсчитано, что в любой момент времени во всей земной коре содержится менее килограмма этого элемента. Более того, к удивлению большинства химиков и вопреки известным тенденциям таблицы Менделеева, оказывается, что франций является , а не самым реакционноспособным металлом. Спускаясь по группе в периодической таблице, в среднем самые внешние электроны удаляются все дальше и дальше от ядра, и в результате их становится легче удалить из атома. Это тенденция для элементов лития, натрия, калия, рубидия и цезия. Однако для действительно тяжелых элементов наличие такого количества положительно заряженных протонов в ядре приводит к тому, что электроны движутся с невероятно высокой скоростью, приближающейся к звуку света. Как понял Эйнштейн, на таких скоростях происходят странные вещи. Электроны становятся немного ближе к ядру, чем ожидалось, и их также становится немного труднее удалить, чем ожидалось. Требуемая энергия составляет 393 кДж моль-1, что примерно на 17 кДж моль-1 больше, чем для цезия. Это означает, что франций представляет собой 90 390, а не 90 391 металл, который легче всего образует катион, как предложила Перей, предложив название катий; эта честь достается более легкому члену семьи франция, цезию.
Требуемая энергия составляет 393 кДж моль-1, что примерно на 17 кДж моль-1 больше, чем для цезия. Это означает, что франций представляет собой 90 390, а не 90 391 металл, который легче всего образует катион, как предложила Перей, предложив название катий; эта честь достается более легкому члену семьи франция, цезию.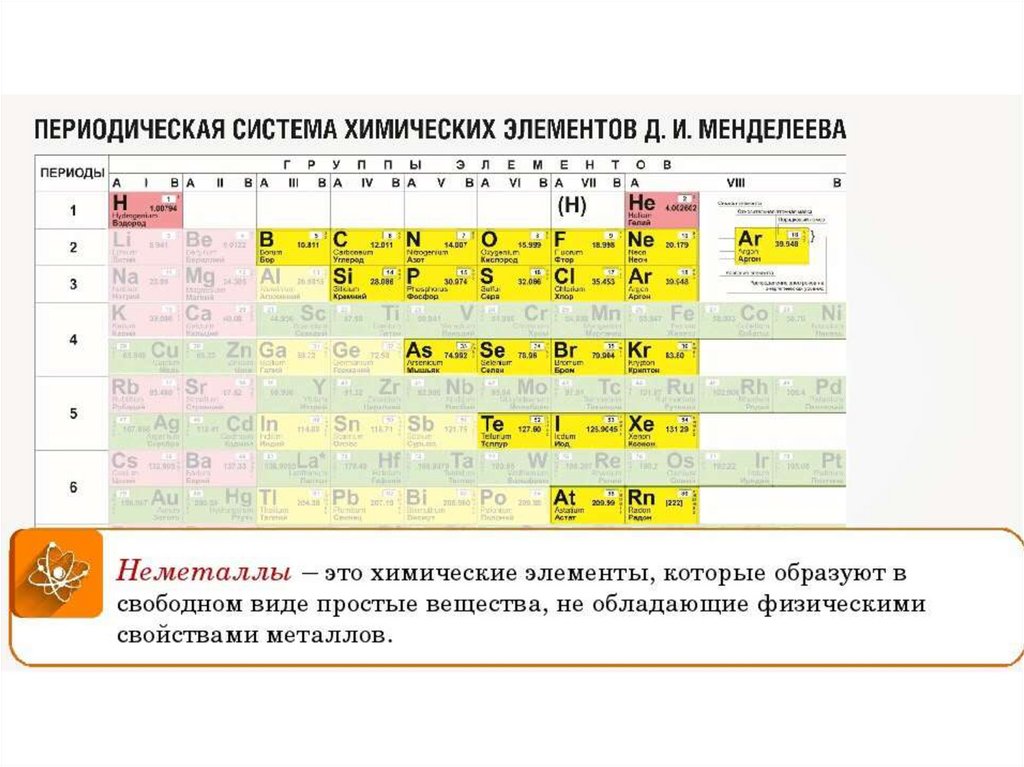 Еще одним поворотом в истории номенклатуры стало то, что Американское химическое общество воскресило первоначальное написание в 1925, и по иронии судьбы именно американцы, а не британцы произносят название элемента так, как намеревался Дэви.
Еще одним поворотом в истории номенклатуры стало то, что Американское химическое общество воскресило первоначальное написание в 1925, и по иронии судьбы именно американцы, а не британцы произносят название элемента так, как намеревался Дэви.