Таблица Менделеева online – Cd
Cd
48
2
18
18
8
2
112.41±1
4d105s2
Кадмий
| Относительная электроотрицательность (по Полингу): | 1,46 |
| Температура плавления: | 700°C |
| Температура кипения: | 1140°C |
| Теплопроводность: | 18 |
| Плотность: | 5 г/см3 |
| Открыт: | немецким профессором Ф. Штромейером в 1817 |
| Цвет в твёрдом состоянии: | Металлический блестящий |
| Тип: | Щелочно-земельный металл |
| Орбитали: | 1s22s22p63s23p63d104s24p64d104f145s25p65d105f06s26p66d07s2 |
| Электронная формула: |
Cd – 1s Cd – [Kr] 4d10 5s2 |
| Валентность: | (+1), +2 |
| Степени окисления: | 0, + II |
| Сверхпроводящее состояние при температуре: | 0 К |
| Потенциалы ионизации: | 5,277 В 10,148 В |
Электропроводность в тв. фазе: фазе: |
|
| Ковалентный радиус: | 148 пм |
| Атомный объем: | 45,2 см3/моль |
| Атомный радиус: | 154 пм |
| Теплота распада: | |
| Теплота парообразования: | |
| Кристаллическая структура: | гексагональная |
Реклама
Изотопы
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
Период полураспада (T1/2) | Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 95Cd | 48 | 47 | 94,94987 | 5 мс | 9/2+ |
| 96Cd | 48 | 48 | 95,93977 | 1 с | 0+ |
| 97Cd | 48 | 49 | 96,93494 | 2,8 с | 9/2+ |
| 98Cd | 48 | 50 | 97,92740 | 9,2 с | 0+ |
| 98mCd | 190 нс | 8+ | |||
| 99Cd | 48 | 51 | 98,92501 | 16 с | 5/2+ |
| 100Cd | 48 | 52 | 99,92029 | 49,1 с | 0+ |
| 101Cd | 48 | 53 | 100,91868 | 1,36 мин | 5/2+ |
| 102Cd | 48 | 54 | 101,91446 | 5,5 мин | 0+ |
| 103Cd | 48 | 55 | 102,913419 | 7,3 мин | 5/2+ |
| 104Cd | 48 | 56 | 103,909849 | 57,7 мин | 0+ |
| 105Cd | 48 | 57 | 104,909468 | 55,5 мин | 5/2+ |
| 106Cd | 48 | 58 | 105,906459 | стабилен | 0+ |
| 107Cd | 48 | 59 | 106,906618 | 6,50 ч | 5/2+ |
| 108Cd | 48 | 60 | 107,904184 | стабилен | 0+ |
| 109Cd | 48 | 61 | 108,904982 | 461,4 сут | 5/2+ |
| 109m1Cd | 59,6 кэВ | 12 мкс | 1/2+ | ||
| 109m2Cd | 463,0 кэВ | 10,9 мкс | 11/2- | ||
| 110Cd | 48 | 62 | 109,9030021 | стабилен | 0+ |
| 111Cd | 48 | 63 | 110,9041781 | стабилен | 1/2+ |
| 111mCd | 48,50 мин | 11/2- | |||
| 112Cd | 48 | 64 | 111,9027578 | стабилен | 0+ |
| 113Cd | 48 | 65 | 112,9044017 | 7,7·1015 лет | 1/2+ |
| 113mCd | 263,54 кэВ | 14,1 лет | 11/2- | ||
| 114Cd | 48 | 66 | 113,9033585 | стабилен | 0+ |
| 115Cd | 48 | 67 | 114,9054310 | 53,46 ч | 1/2+ |
| 115mCd | 181,0 кэВ | 44,56 сут | 11/2- | ||
| 116Cd | 48 | 68 | 115,904756 | 3,1·1019 лет | 0+ |
| 117Cd | 48 | 69 | 116,907219 | 2,49 ч | 1/2+ |
| 117mCd | 136,4 кэВ | 3,36 ч | 11/2- | ||
| 118Cd | 48 | 70 | 117,906915 | 50,3 мин | 0+ |
| 119Cd | 48 | 71 | 118,90992 | 2,69 мин | 3/2+ |
| 119mCd | 146,54 кэВ | 2,20 мин | 11/2- | ||
| 120Cd | 48 | 72 | 119,90985 | 50,80 с | 0+ |
| 121Cd | 48 | 73 | 120,91298 | 13,5 с | 3/2+ |
| 121mCd | 214,86 кэВ | 8,3 с | 11/2- | ||
| 122Cd | 48 | 74 | 121,91333 | 5,24 с | 0+ |
| 123Cd | 48 | 75 | 122,91700 | 2,10 с | 3/2+ |
| 123mCd | 316,52 кэВ | 1,82 с | 11/2- | ||
| 124Cd | 48 | 76 | 123,91765 | 1,25 с | 0+ |
| 125Cd | 48 | 77 | 124,92125 | 650 мс | 3/2+ |
| 125mCd | 50 кэВ | 11/2- | |||
| 126Cd | 48 | 78 | 125,92235 | 515 мс | 0+ |
| 127Cd | 48 | 79 | 126,92644 | 370 мс | 3/2+ |
| 128Cd | 48 | 80 | 127,92776 | 280 мс | 0+ |
| 129Cd | 48 | 81 | 128,93215 | 242 мс | 3/2+ |
| 129mCd | 0 кэВ | 104 мс | 11/2- | ||
| 130Cd | 48 | 82 | 129,9339 | 162 мс | 0+ |
| 131Cd | 48 | 83 | 130,94067 | 68 мс | 7/2- |
| 132Cd | 48 | 84 | 131,94555 | 97 мс | 0+ |
Кадмий
| Кадмий | |
|---|---|
| Атомный номер | 48 |
| Внешний вид простого вещества | мягкий ковкий металл, серебристо-белого цвета |
| Свойства атома | |
|
Атомная масса (молярная масса) |
112,411 а.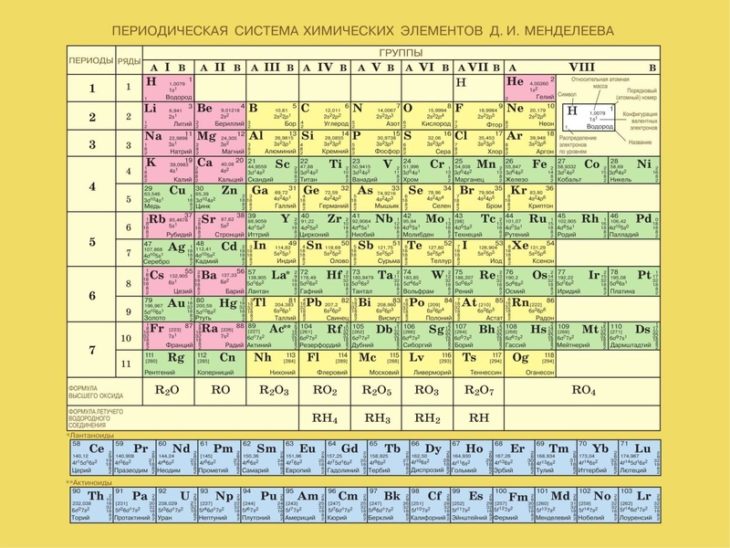 е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | 154 пм |
|
Энергия ионизации (первый электрон) |
867,2 (8,99) кДж/моль (эВ) |
| Электронная конфигурация | [Kr] 4d10 5s2 |
| Химические свойства | |
| Ковалентный радиус | 148 пм |
| Радиус иона | (+2e) 97 пм |
|
Электроотрицательность (по Полингу) |
1,69 |
| Электродный потенциал | −0,403 |
| Степени окисления | 2 |
| Термодинамические свойства простого вещества | |
| Плотность | 8,65 г/см³ |
| Молярная теплоёмкость | 26,0[1]Дж/(K·моль) |
| Теплопроводность | 96,9 Вт/(м·K) |
| Температура плавления | 594,1 K |
| Теплота плавления | 6,11 кДж/моль |
| Температура кипения | 1 038 K |
| Теплота испарения | 59,1 кДж/моль |
| Молярный объём | 13,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Параметры решётки | a=2,979 c=5,618 Å |
| Отношение c/a | 1,886 |
| Температура Дебая | 209 K |
| Cd | 48 |
| 112,411 | |
| [Kr]4d105s2 | |
| Кадмий | |
Кадмий — элемент побочной подгруппы второй группы, пятого периода периодической системы химических элементов Д.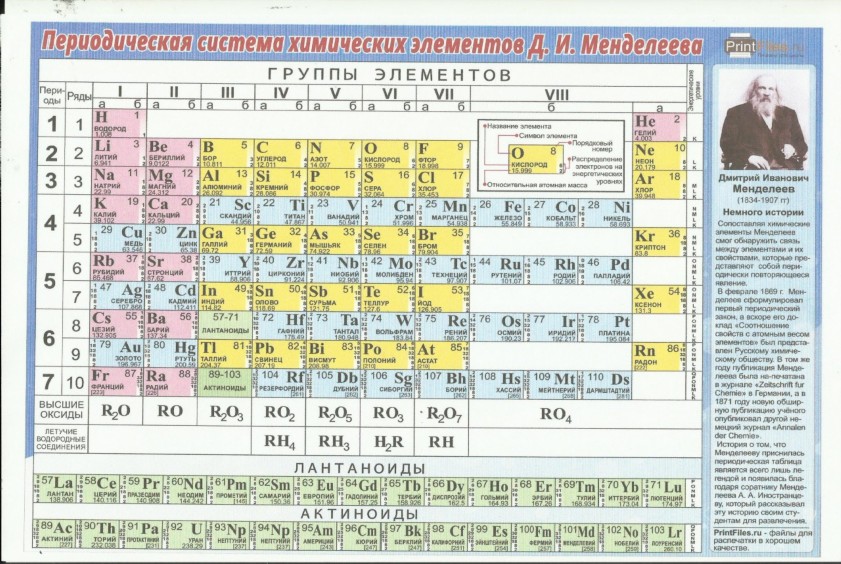 И. Менделеева, с атомным номером 48. Обозначается символом Cd (лат. Cadmium). Простое вещество кадмий (CAS-номер: 7440-43-9) при нормальных условиях — мягкий ковкий тягучий переходный металл серебристо-белого цвета. Устойчив в сухом воздухе, во влажном на его поверхности образуется плёнка оксида, препятствующая дальнейшему окислению металла.
И. Менделеева, с атомным номером 48. Обозначается символом Cd (лат. Cadmium). Простое вещество кадмий (CAS-номер: 7440-43-9) при нормальных условиях — мягкий ковкий тягучий переходный металл серебристо-белого цвета. Устойчив в сухом воздухе, во влажном на его поверхности образуется плёнка оксида, препятствующая дальнейшему окислению металла.
Открыт немецким профессором Ф. Штромейером в 1817. Провизоры Магдебурга при изучении оксида цинка ZnO заподозрили в нём примесь мышьяка. Штромейер выделил из ZnO коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий.
Происхождение названия
Штромейер назвал кадмий по греческому названию руды, из которой в Германии добывали цинк, — καδμεία. В свою очередь, руда получила своё название в честь Кадма, героя древнегреческой мифологии.
Нахождение в природе
Кадмий относится к редким, рассеянным элементам: он содержится в виде изоморфной примеси во многих минералах и всегда в минералах цинка. Весьма редкими минералами кадмия являются гринокит CdS, отавит CdCO3, монтемпонит CdO и кадмоселит CdSe.
Весьма редкими минералами кадмия являются гринокит CdS, отавит CdCO3, монтемпонит CdO и кадмоселит CdSe.
Получение
Единственный минерал, который представляет интерес в получении кадмия — гринокит, так называемая «кадмиевая обманка». Его добывают вместе с фаеритом при разработке цинковых руд. В ходе переработки кадмий концентрируется в побочных продуктах процесса, откуда его потом извлекают. В настоящее время производится свыше 10³ тонн кадмия в год.
Физические свойства
Кадмий — серебристо-белый мягкий металл с гексагональной решёткой. Если кадмиевую палочку изгибать, то можно услышать слабый треск — это трутся друг о друга микрокристаллы металла (так же трещит и пруток олова).
Химические свойства
Кадмий расположен в одной группе периодической системы с цинком и ртутью, занимая промежуточное место между ними, поэтому некоторые химические свойства этих элементов сходны. Так, сульфиды и оксиды этих элементов практически нерастворимы в воде.
Применение
Сплавы
Кадмий используется как компонент твёрдых припоев (сплавов на основе серебра, меди, цинка) для снижения их температуры плавления. Около 10 % производимого кадмия — компонент ювелирных и легкоплавких сплавов. Сплав кадмия с золотом — единственный металлический сплав зелёного цвета. Сплав кадмия с вольфрамом, рением и 0,15 % урана 235 — небесно-голубого цвета был получен испанскими учеными в 1998 году.
Защитные покрытия
40 % производимого кадмия используется для нанесения антикоррозионных покрытий на металлы.
Химические источники тока
Около 20 % кадмия идет на изготовление кадмиевых электродов, применяемых в аккумуляторах (никель-кадмиевых и серебряно-кадмиевых), нормальных элементах Вестона, в резервных батареях (свинцово-кадмиевый элемент, ртутно-кадмиевый элемент и др.
Пигменты
Около 20 % кадмия используется для производства неорганических красящих веществ (сульфиды и селениды, смешанные соли, например, сульфид кадмия — кадмий лимонный).
Медицина
- Иногда кадмий применяется в экспериментальной медицине.
Кадмий используется в гомеопатической медицине
- В последние годы кадмий стал применяться при создании новых противоопухолевых нано-медикаментов. В России в начале 1950-х годов были проведены первые успешные эксперименты, связанные с разработкой противоопухолевых медикаментов на основе соединений кадмия.
Другие сферы применения
- Сульфид кадмия применяется для производства плёночных солнечных батарей с КПД около 10—16 %, а также как очень хороший термоэлектрический материал.
- Кадмий используется как компонент полупроводниковых материалов и люминофоров.
- Кадмий очень хорошо захватывает тепловые нейтроны и служит для изготовления регулирующих стержней для атомных реакторов и в качестве защиты от нейтронов. Иногда эти свойства используются в экспериментальных моделях противоопухолевой терапии Neutron Capture Therapy
-
Фтороборат кадмия — важный флюс, применяемый для пайки алюминия и других металлов.

- Теплопроводность кадмия вблизи абсолютного нуля наивысшая среди всех металлов, поэтому кадмий иногда применяется для криогенной техники.
Физиологическое действие
Острая токсичность
Пары кадмия, все его соединения токсичны, что связано, в частности, с его способностью связывать серосодержащие ферменты и аминокислоты.
Симптомы острого отравления солями кадмия — рвота и судороги.
Хроническая токсичность
Кадмий — кумулятивный яд (способен накапливаться в организме).
Санитарно-экологические нормативы
В питьевой воде ПДК для кадмия 0,001 мг/дм3 (СанПиН 2.1.4.1074-01).
Механизм токсического действия
Растворимые соединения кадмия после всасывания в кровь поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей.
Кадмий в норме в небольших количествах присутствуют в организме здорового человека. Кадмий легко накапливается в быстроразмножающихся клетках (например в опухолевых или половых). Он связывается с цитоплазматическим и ядерным материалом клеток и повреждает их. Он изменяет активность многих гормонов и ферментов. Это обусловлено его способностью связывать сульфгидрильные (-SH) группы.
Кадмий легко накапливается в быстроразмножающихся клетках (например в опухолевых или половых). Он связывается с цитоплазматическим и ядерным материалом клеток и повреждает их. Он изменяет активность многих гормонов и ферментов. Это обусловлено его способностью связывать сульфгидрильные (-SH) группы.
Изотопы
Из восьми природных изотопов кадмия шесть стабильны, для двух изотопов обнаружена слабая радиоактивность. Это 113Cd (изотопная распространённость 12,22 %, бета-распад с периодом полураспада 7,7×1015 лет) и 116Cd (изотопная распространённость 7,49 %, двойной бета-распад с периодом полураспада 3,0×1019 лет).
что это, история открытия, применения, физические, химические свойства, место в природе и таблице Менделеева, строение атома
Кадмий – вещество, без которого невозможно представить производство аккумуляторов. Металл известен еще с времен Средневековья. Сегодня же обладает спросом во многих отраслях промышленности.
История открытия
Металл был открыт в 1817 году профессором университета из Геттингена – Штромейером. Во время ревизии аптек он обнаружил, что при прокаливании отдельных экземпляров карбоната цинка образуется окись ярко-желтого или коричневого цвета. Однако при анализе было обнаружено, что химическое соединение не содержит в своем составе железа.
Химик предположил, что окраска оксида появляется из-за присутствия в нем неизвестного химического элемента. Его удалось получить путем восстановления водородом оксида.
Вместе с Штромейером новое вещество открыли К. Херман и И. Ролофф, а также берлинские химики В. Мейсснер и С. Карстен. Штромейер предложил назвать новый элемент кадмий по названию цинковой руды, которую во времена Гомера добавляли при выплавке латуни.
Кадмий в таблице Менделеева
Это элемент 5 периода 12 группы (или побочной подгруппы 2-й группы) периодической системы. Обозначение – Cd. Атомный (порядковый) номер – 48. Атомная масса – 112.
Принадлежит к группе переходных металлов. Кадмий – это представитель d-элементов.
Строение атома
Конфигурация электронного облака – 1s22s22p63s23p63d104s24p64d105s2. По орбиталям электроны распределяются так: +48Cd)2)8)18)18)2.
Схематическое строение атома кадмия
Валентные электроны – те, которые располагаются на 4d и 5s электронных орбиталях. В основном состоянии энергетическая диаграмма имеет такой вид:
Ион этого элемента имеет вид 1s22s22p63s23p64s23d104p65s24d9.
Физические характеристики
Кадмий – это серебристо-белый мягкий металл. Плавится при температуре 321 градусов, кипит – при 770. Удельная теплота плавления – 6,1 кДж/моль, испарения – 59,1 кДж/моль. Простое вещество имеет гексагональную кристаллическую решетку. Удельная плотность металла – 8,65 г /куб. см.
Благодаря ковкости, тягучести и мягкости этот металл легко протянуть в тонкий лист. Изделия из вещества хорошо полируются.
При сгибании кадмиевой палочки слышен треск (он исчезает, если в металл добавить примеси).
Химические свойства
Атомы этого элемента в соединениях имеют степени окисления 1, 2. Проявляют валентность II, I.
Главные химические характеристики кадмия такие:
- Реакция с кислородом с получением оксида.
- Реакция с водой – образуется оксид и водород.
- Образование солей при реакции с кислотами.
- Окисление солями двухвалентной меди или трехвалентного железа.
- В жидком состоянии реагирует с галогенами (при воздействии хлора образуется гигроскопичный хлорид кадмия).
- Не реагирует со щелочами, водородом, бором, азотом, углеродом, инертными газами. Гидроокись практически не растворяется в щелочах.
Кадмий в природе
Нахождение самородного металла в земной коре незначительно. Однако химический элемент находится в составе руд, из которых добывают цинк, свинец и медь. Так что его могут добывать как побочный продукт при выплавке этих металлов. В цинковом концентрате находится до 0,5% кадмия.
Основная масса простого вещества находится примерно в составе 50 минералов. В 1 кг почвы может содержаться до 60 мкг Cd. Граничное содержание вещества в питьевой воде – 1 мкг в 1 л.
В 1 кг почвы может содержаться до 60 мкг Cd. Граничное содержание вещества в питьевой воде – 1 мкг в 1 л.
Токсичен ли кадмий
Этот химический элемент может попасть в организм с табачным дымом, дорожной пылью. Он находится в дыме теплоэлектростанций, дыме, образующегося после сжигания дров. Любители пива рискуют получить некоторую дозу элемента, потому что его добавляют в напиток для повышения пенообразования.
Японские ученые доказали, что у людей, которые проживают на территориях, загрязненных солями Cd, обнаруживается высокая ломкость костей. Впервые эта болезнь была замечена у фермеров, которые применяли воду с цинковой шахты для орошения рисового поля. Поразительно, но с рисом каждую неделю в организм человека поступало до 4 мг металла (в 8 раз больше предельной нормы).
Вещество угнетает активность ферментов, поражает нервную систему, печень, почки. Хроническая интоксикация приводит к развитию анемии. Пары оксидов и чистого металла токсичны: вдыхание на протяжении полуминуты воздуха с концентрацией паров 5 граммов на кубический метр оказывает смертельное влияние на организм. Острое отравление сопровождается рвотой и судорогами.
Острое отравление сопровождается рвотой и судорогами.
Применение
Директива RoHS, принятая в Евросоюзе, ограничивает использование кадмия в промышленности при производстве:
- бытовой техники;
- осветительной аппаратуры;
- электроники;
- игрушек;
- товаров для досуга;
- лампах накаливания и проч.
Почти 40% всего кадмия расходуется на антикоррозионные покрытия. Кадмированные поверхности устойчивы в морской воде.
Это вещество применяется для изготовления никель-кадмиевых аккумуляторов. Подобные устройства выдерживают в несколько раз больше циклов зарядки и разрядки, нежели их конкуренты. Несмотря на высокую цену, никель-кадмиевые аккумуляторы имеют большие перспективы для использования в электромобилях. Срок их службы превышает 30 лет, они быстро заряжаются и так же быстро отдают накопленную энергию.
Указанные аккумуляторы применяются всюду, где нужен ток большой плотности: в троллейбусах, электрокарах, трамваях, троллейбусах. Эти устройства могут хранить до 6,5 мегаватт-час электрической энергии.
Эти устройства могут хранить до 6,5 мегаватт-час электрической энергии.
Химический элемент имеет перспективы в производстве солнечных батарей: соединение металла с теллуром эффективно превращает свет в электрический ток.
Соединения этого металла могут применяться как краситель. Получая определенными способами сульфокислую соль, можно сделать краску разных цветов и оттенков – от лимонно-желтого до оранжевого. Кадмиевый желтый цвет подходит для художественной росписи керамики. При смешивании сульфата кадмия с ультрамарином получается краска красивого зеленого цвета.
Вещество используется в пиротехнике – во время горения его соли дают синий оттенок. Раствор кадмия хлорида применяется в фотореактивах.
Cd относится к редким элементам, находящимся в большом количестве руд. Соединения кадмия токсичны. Вещество ограниченно используется в промышленности. Как считаете вы, может стоит больше использовать в промышленности этот элемент? Напишите свое мнение в комментариях. Поделитесь статьей в социальных сетях с друзьями и сохраните ее в закладках, чтобы не потерять полезную информацию.
Как получают кадмий можно узнать из видео:
Еще одно познавательное видео: Кадмий — токсичный металл из старых батареек!
Кадмий – информация об элементе, свойства и использование
Перейти к основному содержанию
У вас не включен JavaScript. Пожалуйста, включите JavaScript, чтобы получить доступ ко всем функциям сайта.
Перейти в Индию >
| Группа | 12 | Температура плавления | 321. 069° С, 609,924 ° F, 594,219 К 069° С, 609,924 ° F, 594,219 К |
| Период | 5 | Точка кипения | 767°С, 1413°F, 1040 К |
| Блок | д | Плотность (г см −3 ) | 8,69 |
| Атомный номер | 48 | Относительная атомная масса | 112. 414 414 |
| Состояние при 20°C | Твердый | Ключевые изотопы | 114 CD |
| Электронная конфигурация | [Кр] 4d 1 0 5s 2 | Номер КАС | 7440-43-9 |
| ChemSpider ID | 22410 | ChemSpider — бесплатная база данных химической структуры. | |
Кадмий в природе встречается в земной коре. Изображение включает в себя алхимический символ, когда-то использовавшийся для обозначения «земных» элементов, на фоне проекции Земли.
Кадмий — серебристый металл с голубоватым оттенком на поверхности.
Кадмий является ядом и, как известно, вызывает врожденные дефекты и рак. В результате предпринимаются шаги по ограничению его использования.
80% производимого в настоящее время кадмия используется в перезаряжаемых никель-кадмиевых батареях. Тем не менее, они постепенно выводятся из эксплуатации и заменяются никель-металлгидридными батареями.
Кадмий часто использовался для гальванического покрытия стали и защиты ее от коррозии. Он до сих пор используется для защиты важных компонентов самолетов и нефтяных платформ.
Другие прошлые применения кадмия включали люминофоры в цветных телевизорах с электронно-лучевой трубкой, а также желтые, оранжевые и красные пигменты.
Кадмий поглощает нейтроны и поэтому используется в стержнях ядерных реакторов для управления атомным делением.
Кадмий токсичен, канцерогенен и тератогенен (нарушает развитие эмбриона или плода). В среднем мы потребляем всего 0,05 миллиграмма в день. Но он накапливается в организме, и поэтому в среднем мы запасаем около 50 миллиграммов.
До того, как опасность кадмия была полностью осознана, сварщики и другие рабочие-металлисты подвергались риску заболеть. В 1966 некоторым сварщикам, работавшим на мосту через Северн-Роуд, стало плохо от вдыхания паров кадмия.
Единственным минералом, содержащим значительное количество кадмия, является гринокит (сульфид кадмия). Он также присутствует в небольших количествах в сфалерите. Почти весь промышленно производимый кадмий получается как побочный продукт рафинирования цинка.
История элементов и периодической таблицы
В начале 1800-х годов аптекари Ганновера, Германия, получили оксид цинка путем нагревания встречающейся в природе формы карбоната цинка, называемой кадмием. Иногда продукт обесцвечивался вместо того, чтобы быть чисто белым, и когда Фридрих Штромейер из Геттингенского университета изучил проблему, он проследил изменение цвета до компонента, который он не мог идентифицировать и который, как он сделал вывод, должен быть неизвестным элементом. Он выделил его в виде коричневого оксида и, нагревая его с сажей (углеродом), получил образец сине-серого металла, который он назвал кадмием по названию минерала. Это было в 1817 году. Тем временем два других немца, Карл Мейснер в Галле и Карл Карстен в Берлине, работали над той же проблемой и в следующем году объявили об открытии кадмия.
Иногда продукт обесцвечивался вместо того, чтобы быть чисто белым, и когда Фридрих Штромейер из Геттингенского университета изучил проблему, он проследил изменение цвета до компонента, который он не мог идентифицировать и который, как он сделал вывод, должен быть неизвестным элементом. Он выделил его в виде коричневого оксида и, нагревая его с сажей (углеродом), получил образец сине-серого металла, который он назвал кадмием по названию минерала. Это было в 1817 году. Тем временем два других немца, Карл Мейснер в Галле и Карл Карстен в Берлине, работали над той же проблемой и в следующем году объявили об открытии кадмия.
| Атомный радиус, несвязанный (Å) | 2.18 | Ковалентный радиус (Å) | 1,40 |
| Сродство к электрону (кДж моль −1 ) | Нестабильный | Электроотрицательность (шкала Полинга) | 1,69 |
| Энергии ионизации (кДж моль −1 ) | 1 ст 867,772 2 -й 1631. 3 рд 3616,27 | ||
| Общие степени окисления | 2 | ||||
| Изотопы | Изотоп | Атомная масса | Естественное изобилие (%) | Период полураспада | Режим распада |
| 106 CD | 105. 906 906 | 1,25 | > 1,9 х 10 19 г | ЕС, ЕС | |
| 108 CD | 107.904 | 0,89 | > 4,1 х 10 17 г | ЕС ЕС | |
| 110 CD | 109. 903 903 | 12.49 | – | – | |
| 111 CD | 110.904 | 12,8 | – | – | |
| 112 CD | 111. 903 903 | 24.13 | – | – | |
| 113 CD | 112.904 | 12.22 | 8,04 х 10 15 г | β-β- | |
| 114 CD | 113,903 | 28,73 | > 1,3 х 10 18 г | β-β- | |
| 116 CD | 115. 905 905 | 7,49 | 3,8 х 10 19 г | β-β- | |
|
|
| Удельная теплоемкость (Дж кг -1 К -1 ) | 231 | Модуль Юнга (ГПа) | 49,9 | |||||||||||
| Модуль сдвига (ГПа) | 19. 2 2 | Объемный модуль (ГПа) | 41,6 | |||||||||||
| Давление пара | ||||||||||||||
| Температура (К) |
| |||||||||||||
| Давление (Па) |
| |||||||||||||
| Слушайте подкаст кадмия | ||||||||||||||
Стенограмма: (Промо) Вы слушаете Химию в ее стихии, представленную вам Chemistry World , журналом Королевского химического общества. (Конец промо) Крис Смит Привет, на этой неделе мы получаем очень болезненный урок о хэви-метале Стив Майлон Я не могу себе представить, что это все, что кто-то мог бы сказать, если бы им не повезло заболеть одноименной болезнью. Правильно, ай-ай-болезнь. Судя по описанию, боль будет достаточно сильной, чтобы я мог сказать гораздо больше, чем просто ой-ой. Итай-Итай — это оригинальное японское слово «ай-ай». Заболевание возникает в результате чрезмерного отравления кадмием и впервые было зарегистрировано в небольшом городке примерно в 200 милях к северо-западу от Токио. Там рис, выращенный на загрязненных кадмием почвах, содержал в 10 раз больше кадмия, чем обычный рис. Избыток кадмия стал мешать отложению кальция в костях. Ох-о-о-о-о-о-о-о-о-о-сть этой болезни была следствием слабых и ломких костей, подверженных разрушению из-за высокой пористости. Удивительно, что кадмий способен накапливаться до таких высоких уровней, что он может подавить и без того сильную защиту человеческого организма от него. Это коварный маленький, я имею в виду, хэви-метал. Кадмий находится сразу после цинка в таблице Менделеева и, следовательно, обладает многими схожими химическими свойствами. В окружающей среде он распространен почти везде, где мы находим цинк, и поэтому, когда мы добываем цинк, мы, следовательно, добываем кадмий. Когда мы гальванизируем (покрываем цинком) гвоздь или какой-либо другой кусок стали, в процессе появляется немного кадмия. Задумайтесь на минуту о том, насколько важна гальванизация для промышленно развитого мира. Если вы не знаете, поверьте мне, это действительно важно, и, таким образом, это небольшое количество кадмия, которое появляется вместе с вами, становится большим потенциальным воздействием кадмия. Добавьте к этому другие пути воздействия, такие как шахты и металлообработка, а также легкость поглощения кадмия сельскохозяйственными культурами, и нам действительно повезло, что наш организм разработал систему для ослабления воздействия кадмия в нашем рационе. Я, конечно, не хочу внушать вам, что у кадмия очень пестрое прошлое. Чтобы по достоинству оценить кадмий, вы должны знать, что некоторые из самых ярких цветов и красок получаются из солей кадмия, и художники пользуются этим в течение многих лет. Никель-кадмиевые аккумуляторы перспективны благодаря более высокой эффективности, что продемонстрирует их важность в электромобилях следующего поколения. Кадмий является важным элементом во многих формах нового класса полупроводников, известных как квантовые точки. Эти передовые материалы демонстрируют перспективность в области электроники, фотогальваники и медицинской визуализации. И, наконец, в природе группа из Принстонского университета несколько лет назад показала, что некоторые морские диатоны могут заменять цинк кадмием в важном ферменте карбоангидразе. Это продемонстрировало, что кадмий также может быть питательным веществом. Однако мы, люди, не рассчитываем на питательную ценность кадмия, оставим это диетам. Крис Смит Итак, главное: не ешьте аккумуляторы. Это был Стив Майлон с историей о кадмии, химическом веществе, благодаря которому мир выглядит в приятной цветовой гамме. На следующей неделе от раскрашивания мира к его изменению. Кэтрин Холт Жестяные банки, оловянная фольга, оловянные свистки, оловянные солдатики… вот что приходит на ум, когда мы думаем о жести. К сожалению, жестяные банки на самом деле сделаны из стали; оловянная фольга сделана из алюминия и оловянных свистков …. ну вы поняли. Быть связанным со списком устаревших расходных материалов особенно неудачно для олова, если учесть, что оно было ответственно за буквальное изменение цивилизации! Вы слышали о бронзовом веке? Крис Смит Что ж, если нет, присоединяйтесь к Кэтрин Холт, чтобы узнать, как олово заставило все это произойти на следующей неделе Химия в ее стихии. (Промо) Химия в ее стихии представлена вам Королевским химическим обществом и произведена thenakedscientists.com. Дополнительную информацию и другие эпизоды химии в ее стихии можно найти на нашем веб-сайте chemistryworld.org/elements. (окончание акции) Нажмите здесь, чтобы посмотреть видео о кадмии Learn Chemistry: ваш единственный путь к сотням бесплатных учебных ресурсов по химии. Изображения и видео Visual Elements Загрузите наше бесплатное приложение Периодической таблицы для мобильных телефонов и планшетов. Исследуйте все элементы
кадмий | Использование, свойства и фактыкадмий См.
Просмотреть весь связанный контент → Резюме Прочтите краткий обзор этой темыкадмий (Cd) , химический элемент, металл группы 12 (IIb, или группы цинка) периодической таблицы.
Свойства, происхождение и применение Серебристо-белый и хорошо полируемый кадмий почти так же мягок, как олово, и, подобно олову, издает треск при сгибании; его можно раскатать в листы. Britannica Викторина 118 Названий и символов периодической таблицы Викторина Периодическая таблица состоит из 118 элементов. Насколько хорошо вы знаете их символы? В этом тесте вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них. Редкий элемент (около 0,2 грамма на тонну в земной коре), кадмий встречается в нескольких минералах и в небольших количествах в других рудах, особенно в цинковых рудах, из которых он производится как побочный продукт. Большая часть производимого кадмия наносится гальванопокрытием на сталь, железо, медь, латунь и другие сплавы для защиты от коррозии. Важным применением кадмия является его использование в качестве анода с оксидом никеля или серебра в качестве катода и электролитом с едким кали в перезаряжаемых электрических аккумуляторных батареях для использования, в которых меньший вес, более длительный срок службы и стабильность при хранении в разряженном состоянии желательно как в самолетах. Кадмий соединяется со многими тяжелыми металлами с образованием сплавов; важнейшее значение имеют подшипниковые сплавы и легкоплавкие сплавы, применяемые для пайки. Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас Природный кадмий представляет собой смесь восьми изотопов: 106 Cd (1,2 процента), 108 Cd (0,9 процента), 110 Cd (12,4 процента), 111 Cd (12,82 процента), 112 Cd (24,0 процента), 113 Cd (12,3 процента), 114 Cd (28,8 процента) и 116 Cd (7,6 процента). Соединения В своих соединениях кадмий проявляет почти исключительно степень окисления +2, как в бесцветном Cd 2+ , который образует ряд устойчивых комплексных ионов, особенно галогенидных комплексов. Наиболее важным соединением кадмия является оксид кадмия CdO. Это коричневый порошок, полученный путем сжигания паров кадмия на воздухе, и он является удобным исходным материалом для производства большинства других солей кадмия. Другим соединением, имеющим некоторую экономическую ценность, является сульфид кадмия, CdS. Обычно получаемый путем обработки раствора кадмия растворимым сульфидом, это ярко-желтый пигмент, известный как желтый кадмий, который используется в высококачественных красках и пигментах для художников из-за его цветовой стабильности и устойчивости к сере и окислению. Еще одно известное соединение, селенид кадмия (CdSe), обычно осаждается селенидом водорода или щелочными селенидами из растворов солей кадмия. Редакторы Британской энциклопедии Эта статья была недавно отредактирована и дополнена Эриком Грегерсеном. Химия кадмия – Химия LibreTexts
Этот модуль создан для предоставления информации о кадмии, которую может быть очень полезно знать, поскольку этот переходный металл ядовит и может нанести вред тем, кто не обращается с ним осторожно. Введение Кадмий, переходный металл, имеет химический символ Cd. Общие свойства кадмия
Атомная структураElectron Configuration of CadmiumElectron Configuration of CadmiumЭлектрон. 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s2 4d 10 or [Kr] 4d 10 5s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s2 4d 10 or [Kr] 4d 10 5s 2
Common IsotopesКадмий имеет в общей сложности восемь встречающихся в природе изотопов. Это 106 CD, 108 CD, 110 CD, 111 CD, 112 CD, 113 CD, 114 CD, 116 CD. Из этих восьми изотопов 114 Cd и 112 Cd являются наиболее распространенными с содержанием 29% и 24% соответственно. Металлические характеристики Металлический кадмий мягкий и ковкий в чистом виде и используется в основном для гальванического покрытия стали (коррозионная стойкость) и в производстве подшипников. Соединения кадмия также встречаются в масляных красках, где они обеспечивают яркие цвета (например, «желтый кадмий»). В твердом состоянии этот металл имеет серебристо-серый цвет. Подобно цинку и олову, металлический кадмий “плачет” или издает высокий звук при быстром сгибании. Большая часть кадмия сегодня извлекается как побочный продукт процесса рафинирования цинка. Встречающиеся в природеКадмий никогда не встречается в природе в чистом виде. Он всегда находится в соединении с другим элементом. Наиболее распространенными природными соединениями кадмия являются сульфид кадмия, карбонат кадмия и оксид углерода. Сероуглерод, также известный как минерал гринокит, является наиболее известным источником кадмия. Кадмий также содержится в земной коре в количестве от 0,1 до 0,2 частей на миллион, что является очень небольшим количеством. Большая часть кадмия получается в процессе, известном как рафинирование цинка, в котором используются разные температуры плавления. Общие реакции с кадмиемКадмий образует несколько важных соединений в природе:
Эти три соединения наиболее широко используются в обществе; однако в природе существуют еще несколько соединений: цианид кадмия, хлорид кадмия, карбонат кадмия и нитрат кадмия. Общее применение Кадмий наиболее известен тем, что используется в никель-кадмиевых или никель-кадиевых перезаряжаемых батареях, которые являются вторыми наиболее широко используемыми батареями, используемыми в самолетах, телефонах, электроинструментах, проигрывателях компакт-дисков, компьютерах и даже радиолокационных станциях. Опасности и токсичность Кадмий — очень токсичный металл, поэтому с ним следует обращаться очень осторожно. Кадмий может попасть в организм человека при курении сигарет, загрязненной воде из-за свалок, некоторых пищевых продуктах, таких как моллюски, и в основном при обращении с самим металлом. Этот металл при вдыхании или переваривании может вызвать множество проблем со здоровьем, включая рвоту, тошноту, диарею, сухость в горле и головные боли. Более серьезные последствия все еще исследуются, но считается, что они вызывают высокое кровяное давление, рак, болезни сердца и печени. Ссылки
Проблемы
Solutions to Problems
|

 404
404 1
1
 Если нет, многие из нас могли бы сказать «Ой-ой».
Если нет, многие из нас могли бы сказать «Ой-ой». Одна из вещей, которая делает кадмий таким интересным, — это его многочисленные полезные свойства.
Одна из вещей, которая делает кадмий таким интересным, — это его многочисленные полезные свойства. Потребление кадмия через зараженные продукты или даже курение табака может привести ко всем видам проблем, некоторые из которых даже хуже, чем болезнь ай-ай.
Потребление кадмия через зараженные продукты или даже курение табака может привести ко всем видам проблем, некоторые из которых даже хуже, чем болезнь ай-ай. Я Крис Смит, спасибо за внимание и до свидания.
Я Крис Смит, спасибо за внимание и до свидания.
 все СМИ
все СМИ Кадмий плавится и кипит при относительно низких температурах; его пар темно-желтый и одноатомный. Металл устойчив в сухом воздухе, во влажном воздухе покрывается оксидом, при нагревании сгорает до покраснения, хорошо растворяется в минеральных кислотах. Отравление происходит при вдыхании паров или пыли кадмия. Фридрих Штромейер, немецкий химик, открыл этот элемент (1817 г.) в образце карбоната цинка, и в том же году К.С.Л. Германн и Дж.Ч.Х. Ролофф обнаружил кадмий в образце оксида цинка. Оба соединения цинка были исследованы, потому что их чистота как фармацевтических препаратов была сомнительной.
Кадмий плавится и кипит при относительно низких температурах; его пар темно-желтый и одноатомный. Металл устойчив в сухом воздухе, во влажном воздухе покрывается оксидом, при нагревании сгорает до покраснения, хорошо растворяется в минеральных кислотах. Отравление происходит при вдыхании паров или пыли кадмия. Фридрих Штромейер, немецкий химик, открыл этот элемент (1817 г.) в образце карбоната цинка, и в том же году К.С.Л. Германн и Дж.Ч.Х. Ролофф обнаружил кадмий в образце оксида цинка. Оба соединения цинка были исследованы, потому что их чистота как фармацевтических препаратов была сомнительной. Основная цинковая руда — цинковая обманка или сфалерит — состоит в основном из сульфида цинка, содержащего от 0,1 до 0,3% кадмия. Все методы производства цинка начинаются с превращения сульфида в оксид цинка путем обжига: кадмий концентрируется в дымовых газах, которые обрабатываются в несколько этапов до получения продукта, содержащего более 99,9% кадмия. Некоторые свинцовые руды также содержат небольшое количество кадмия, и, если он присутствует в достаточном количестве, его извлекают с помощью цикла операций, аналогичного тому, который используется на цинковых заводах. Производители цинка, использующие электролитический процесс, извлекают кадмий несколько иным способом, но опять же принцип тот же, начиная с обжига сульфида цинка с последующей обработкой колошниковой пыли. Большая часть кадмия извлекается в одном из этих трех процессов. Китай, Южная Корея, Канада, Япония и Казахстан лидировали в мире по переработке кадмия в начале 21 века.
Основная цинковая руда — цинковая обманка или сфалерит — состоит в основном из сульфида цинка, содержащего от 0,1 до 0,3% кадмия. Все методы производства цинка начинаются с превращения сульфида в оксид цинка путем обжига: кадмий концентрируется в дымовых газах, которые обрабатываются в несколько этапов до получения продукта, содержащего более 99,9% кадмия. Некоторые свинцовые руды также содержат небольшое количество кадмия, и, если он присутствует в достаточном количестве, его извлекают с помощью цикла операций, аналогичного тому, который используется на цинковых заводах. Производители цинка, использующие электролитический процесс, извлекают кадмий несколько иным способом, но опять же принцип тот же, начиная с обжига сульфида цинка с последующей обработкой колошниковой пыли. Большая часть кадмия извлекается в одном из этих трех процессов. Китай, Южная Корея, Канада, Япония и Казахстан лидировали в мире по переработке кадмия в начале 21 века. Кадмирование особенно устойчиво к воздействию щелочи. Кадмий физически подобен цинку, но более плотный и мягкий. Кадмий с гальванопокрытием имеет меньший размер зерна, чем электроцинковые покрытия, а отложения имеют тенденцию быть более однородными и гладкими. Следовательно, хорошую защиту обеспечивают тонкие покрытия из кадмия, поэтому, несмотря на его высокую цену, его часто используют для защиты прецизионных деталей. Его устойчивость к морской атмосфере также выше, чем у цинка.
Кадмирование особенно устойчиво к воздействию щелочи. Кадмий физически подобен цинку, но более плотный и мягкий. Кадмий с гальванопокрытием имеет меньший размер зерна, чем электроцинковые покрытия, а отложения имеют тенденцию быть более однородными и гладкими. Следовательно, хорошую защиту обеспечивают тонкие покрытия из кадмия, поэтому, несмотря на его высокую цену, его часто используют для защиты прецизионных деталей. Его устойчивость к морской атмосфере также выше, чем у цинка. Небольшие количества кадмия, добавляемые к тяжелым металлам, укрепляют их. Один процент, добавленный к меди, увеличивает ее прочность и твердость при небольшом снижении электропроводности. В сплаве с цинком кадмий образует припои с хорошей прочностью на сдвиг. Поскольку он эффективно поглощает тепловые нейтроны, он используется в регулирующих стержнях некоторых ядерных реакторов.
Небольшие количества кадмия, добавляемые к тяжелым металлам, укрепляют их. Один процент, добавленный к меди, увеличивает ее прочность и твердость при небольшом снижении электропроводности. В сплаве с цинком кадмий образует припои с хорошей прочностью на сдвиг. Поскольку он эффективно поглощает тепловые нейтроны, он используется в регулирующих стержнях некоторых ядерных реакторов. Несколько соединений со степенью окисления +1 были получены путем растворения металлического кадмия в расплавленных двухзарядных галогенидах кадмия (Cd 2+ ). Образовавшийся двухатомный ион кадмия Cd 2 2+ (где кадмий находится в степени окисления +1) нестабилен в воде и немедленно диспропорционирует в металлический кадмий и Cd 2+ .
Несколько соединений со степенью окисления +1 были получены путем растворения металлического кадмия в расплавленных двухзарядных галогенидах кадмия (Cd 2+ ). Образовавшийся двухатомный ион кадмия Cd 2 2+ (где кадмий находится в степени окисления +1) нестабилен в воде и немедленно диспропорционирует в металлический кадмий и Cd 2+ . Изменяя условия осаждения, можно получить устойчивые цвета от желтого до ярко-красного. Сам по себе или в смеси с сульфидом кадмия он широко используется в качестве высококачественного пигмента.
Изменяя условия осаждения, можно получить устойчивые цвета от желтого до ярко-красного. Сам по себе или в смеси с сульфидом кадмия он широко используется в качестве высококачественного пигмента. Кадмий расположен в d-блоке и 12 группе периодической таблицы, имеет атомный номер 48 и атомную массу 112,411 г. Кадмий был открыт в Германии в 1817 году немецким ученым Фридрихом Штромейером. Этот элемент очень часто использовался в качестве расходуемого анода для защиты железа и стали от коррозии, а также используется в никель-кадмиевых батареях. Кадмий очень токсичен, поэтому с ним следует обращаться с большой осторожностью.
Кадмий расположен в d-блоке и 12 группе периодической таблицы, имеет атомный номер 48 и атомную массу 112,411 г. Кадмий был открыт в Германии в 1817 году немецким ученым Фридрихом Штромейером. Этот элемент очень часто использовался в качестве расходуемого анода для защиты железа и стали от коррозии, а также используется в никель-кадмиевых батареях. Кадмий очень токсичен, поэтому с ним следует обращаться с большой осторожностью. Кадмий является очень хорошим проводником электричества, а также очень устойчив к коррозии, что делает его отличным расходуемым анодом для таких металлов, как железо и сталь.
Кадмий является очень хорошим проводником электричества, а также очень устойчив к коррозии, что делает его отличным расходуемым анодом для таких металлов, как железо и сталь. Кислотный раствор.
Кислотный раствор. . В этой батарее кадмий принимает форму гидроксида кадмия. Кадмий также используется в покрытиях, пигментах, пластмассах и сплавах. Наиболее часто образуются сплавы с серебром, медью и цинком, главным образом потому, что кадмий снижает температуру плавления, что делает их подходящими для твердой пайки металлов. В прошлые годы кадмий использовался при гальванике стали для защиты от коррозии; однако это не так часто.
. В этой батарее кадмий принимает форму гидроксида кадмия. Кадмий также используется в покрытиях, пигментах, пластмассах и сплавах. Наиболее часто образуются сплавы с серебром, медью и цинком, главным образом потому, что кадмий снижает температуру плавления, что делает их подходящими для твердой пайки металлов. В прошлые годы кадмий использовался при гальванике стали для защиты от коррозии; однако это не так часто.
