Вопрос ученому: есть ли предел у таблицы Менделеева?
Depositphotos/Albert Tica
«Флеровий, ливерморий, дармштадтий, рентгений — то и дело в лентах новостей в Интернете появляются любопытные имена «новоселов» в периодической таблице Менделеева. Говорят, что она содержит уже гораздо больше ста химических элементов. Часть из них обнаружили в природе, остальные искусственно получены в результате ядерных реакций», — пишет посетитель нашего портала Евгений. Так есть ли предел у таблицы Менделеева? Этот вопрос мы адресовали кандидату химических наук, директору центра коллективного пользования сорбционных и каталитических исследований ТГУ Олегу Магаеву. Напоминаем, если вам есть, что спросить у ученых, пишите в комментарии или на почту [email protected]. Ваши вопросы мы зададим экспертам в самых разных областях науки и опубликуем на портале.Олег Магаев, кандидат химических наук, директор центра коллективного пользования сорбционных и каталитических исследований ТГУ:
— Всем известно, что таблица химических элементов была составлена выдающимся русским ученым Дмитрием Ивановичем Менделеевым, который прославился не только как химик, но и как экономист, геолог, педагог, плотник и во многих других сферах деятельности. Тем не менее, периодический закон химических элементов, как один из основных законов мироздания, стал, безусловно, наиболее известным открытием Менделеева.
Тем не менее, периодический закон химических элементов, как один из основных законов мироздания, стал, безусловно, наиболее известным открытием Менделеева.
Таблица представляет собой классификацию химических элементов, устанавливающую зависимость свойств элементов от заряда атомного ядра. По сути, это графическое выражение периодического закона, установленного Менделеевым. Первоначально таблица строилась так, что отображала свойства элемента от его атомного веса. Впоследствии было предложено множество ее различных начертаний. Современный вариант представляет собой двухмерную таблицу, в которой столбцы определяют основные физико-химические свойства, а строки — периоды, подобные друг другу.
К моменту создания таблицы было открыто 63 химических элемента. Со временем все пробелы были устранены, и, казалось, система элементов приобрела завершенный вид. Однако прогресс в области ядерной физики открыл новые горизонты: искусственно синтезируемые химические элементы начали отодвигать границу периодической системы в область все больших значений атомных номеров.
На данный момент в таблице официально зарегистрировано 118 элементов. Но проблема в том, что элементы с большими атомными номерами нестабильны и имеют малый срок существования. Поэтому элементы с номерами больше 90 — фактически лабораторные, в природе они не встречаются. Срок жизни некоторых их них не превышает долей секунды!
Прийти к единому мнению о том, как далеко может зайти этот процесс, ученые, разумеется, не могут — есть как ярые сторонники, настаивающие на существовании предела, как и те, кто полагает, что границ познания нет. Что касается практической стороны вопроса, то в современном научном мире сложно уловить ориентир. Элементы, открытые лет десять назад, вполне реальны — сейчас же, гипотетически, мы можем открывать новые элементы еще сколько угодно. Но здесь встает самый главный вопрос — для чего? Если с целью пополнить таблицу и показать, что мы развиваем ядерный синтез, — это одно. А если мы хотим, чтобы это можно было применить и использовать в реальной практике, — то уже совсем другая история.
Если говорить об официальных таблицах элементов, используемых в европейских странах, сейчас в них фигурирует не больше 104-106 элементов — это максимум. Кстати, в последнее время в российских школьных учебниках химии все чаще встречаются довольно модернизированные таблицы, систематизация которых весьма далека от классического варианта. В дальнейшем, когда ребята становятся студентами и приходят обучаться в стены высших учебных заведений, у них возникает большая путаница.
Сама же процедура признания нового элемента довольна сложна. Одним из ключевых требований является то, что открытие должно быть перепроверено, экспериментально подтверждено двумя-тремя независимыми научными группами. В мире есть не так много лабораторий, сотрудникам которых удалось синтезировать один или даже несколько новых элементов. И в первую очередь, одну из лидирующих позиций здесь занимают российские исследователи — ученые объединенного института ядерных исследований в Дубне.
основные свойства и области применения
Европий – химический элемент в таблице Менделеева. Он используется в энергетике, медицине и электронике и является самым дорогим представителем лантаноидов. Каковы свойства и характеристики европия?
Он используется в энергетике, медицине и электронике и является самым дорогим представителем лантаноидов. Каковы свойства и характеристики европия?
Элемент 63
Впервые химический элемент европий был обнаружен англичанином Уильямом Круксом в 1886 году. Но его свойства стали известны далеко не сразу. Неоднократно Крукс и другие учёные видели лишь спектральные линии неизвестного им вещества. Открытие же его приписывается французу Эжену Демарсе, который не просто обнаружил элемент, но и выделил его из минерала, описал и дал название.
Европий – это металл с атомным числом 63. Он не встречается в самостоятельном виде и присутствует в природе в составе редкоземельных минералов, например, монаците и ксенотиме. Количество химического элемента европия в земной коре составляет 1,2 *10-4 %. Для промышленного производства металл добывают из монацита, так как в этом минерале его содержание доходит до 1 %.
Крупнейшие месторождения европия находятся в Кении. Он также встречается на территории США, Бразилии, Австралии, Скандинавских стран, России, Казахстана и т. д.
д.
Основные характеристики
Химический элемент европий представляет собой металл серебристо-белого цвета. Его атомная масса составляет 151,964 (1) г/моль. Он мягкий и легко поддаётся механическому воздействию, но только при инертной атмосфере, так как является достаточно активным веществом.
Температура плавления металла составляет 826 градусов Цельсия, кипит европий при температуре 1529 градусов. Он может становиться сверхпроводящим (приобретает способность к нулевому электрическому сопротивлению) при давлении в 80 ГПа и температуре -271,35 Цельсия (1,8 К).
Существует два природных изотопа элемента европий 153 и европий 151 с разным содержанием нейтронов в ядре. Первый достаточно стабилен и распространён в природе чуть больше. Второй изотоп нестабилен и обладает альфа-распадом. Период химического элемента европия 151 составляет 5×1018 лет. Кроме этих изотопов, существует ещё 35 искусственных. Самым длинным периодом полураспада обладает Eu 150 (полураспад 36,9 лет), а одним из наиболее быстрых – Eu 152m3 (полураспад 164 наносекунды).
Химические свойства
Состоит химический элемент европий в группе лантаноидов, вместе с Лантаном, Церием, Гадолинием, Прометием и другими. Он самый легкий и самый активный из всех своих «одногруппников». Европий быстро вступает в реакцию с воздухом, окисляясь и покрываясь плёнкой. Из-за этого его обычно хранят в парафине или керосине в специальных контейнерах и колбах.
Активен европий и в других реакциях. В соединениях он обычно трёхвалентный, но иногда бывает и двухвалентным. При нагреве в атмосфере кислорода он образует соединение Eu2O3 в виде бело-розового порошка. При небольшом нагревании он легко вступает в реакцию с азотом, водородом и галогенами. Многие его соединения имеют белый цвет со светлыми оттенками оранжевого и розового.
Катионы европия (III) получают разложением растворов солей сульфата, оксалата, нитрата. В промышленности металл получают при помощи углерода или лантана путём восстановления его окиси или электролизом его сплава EuCl3.
Из всех лантаноидов только спектр излучения ионов европия (III) может быть уловимы для человеческого глаза. При использовании для генерации лазерного излучения, цвет его луча оранжевый.
Применение
Применение химический элемент европий нашёл в сфере электроники. В цветном телевидении его используют для активации люминофоров красного или синего цвета. Его соединение с кремнием EuSi2 образует тонкие пленки и используется для изготовления микросхем.
Элемент применяют для производства люминесцентных ламп и флуоресцентного стекла. В медицине с его помощью проводились лечения некоторых форм раковых заболеваний. Его искусственный изотоп европий 152 служит в химических исследованиях индикатором, а изотоп с номером 155 применяют для медицинской диагностики.
Он сильнее других лантаноидов поглощает тепловые нейтроны, что очень пригождается в ядерной энергетике. Для этих целей используют его окись, соединение с борной кислотой (борат европия) и бинарное соединение с бором (гексаборид европия). Элемент применяют и в атомно-водородной энергетике во время термохимического разложения воды.
Элемент применяют и в атомно-водородной энергетике во время термохимического разложения воды.
Вред и влияние на человека
В небольших количествах европий содержится в организме человека. Он также может содержаться в воде, попадая в неё в районах месторождения минералов, в состав которых он входит. Промышленное производство также снабжает воды этим элементом.
Действие элемента на организм и здоровье человека не изучено. Доверяя распространённой информации, он не представляет особой опасности, так как его концентрации, как правило, слишком малы.
Европий имеет совсем небольшую токсичность, а содержание его в воде обычно настолько незначительно, что не способно существенно повлиять на её качество. В пресных и малосолёных водах его количество доходит до 1 мкг/л, морской воде этот показатель составляет 1,1*10-6 мг/л.
Менделееву и не снилось. Получен новый элемент
Начало большого пути
Когда Дмитрий Менделеев сформулировал свой периодический закон, ему было известно 63 химических элемента. Известно, что окружающий нас мир состоит из 83 химических элементов, самый легкий из них – водород (его атомный номер – Z=1), самый тяжелый – уран (Z=92).
Известно, что окружающий нас мир состоит из 83 химических элементов, самый легкий из них – водород (его атомный номер – Z=1), самый тяжелый – уран (Z=92).
В Солнечной системе и на нашей планете сохранились лишь те элементы, время жизни которых больше возраста Земли (4,5 млрд лет). Другие распались и не дожили до наших дней. Радиоактивный элемент уран, у которого период полураспада около 4,5×108 лет, еще распадается. Однако в середине прошлого века люди научились получать элементы, которых нет в природе, например, нарабатываемый в ядерных реакторах плутоний (Z=94). Плутоний производится сотнями тонн и служит одним из мощнейших источников энергии. Его время жизни ничтожно мало, но в масштабе микромира это огромная величина, сообщает издание “В мире науки”.
К 1940 г. таблица Менделеева была практически полностью заполнена, до номера 92 – урана включительно. (Кроме элемента 61 – прометия, открытого в 1945 г.). Все последующие 18 трансурановых элементов в буквальном смысле – творение рук человеческих. В природе их нет, – сообщает “НГ-Наука”.
В начале 70-х в Лаборатории ядерных реакций был разработан метод холодного слияния ядер. Собственно, именно этим занимались еще средневековые алхимики, пытаясь превратить железо в золото. Но у них не было молотка, двигающегося с релятивистскими скоростями (близкими к скорости света), а для холодного слияния элементов нужно, чтобы один из них имел скорость лишь в 10 раз меньшую, чем скорость света. В Лаборатории ядерных реакций (ЛЯР, как зовут ее сами сотрудники Объединенного института ядерных исследований) такой “релятивистский молоток” имеется – ускоритель тяжелых ионов – циклотрон У-400. Именно с его помощью в этом году был поставлен уникальный эксперимент, готовившийся три года.
Эксперименты ученых в этой области не всегда увенчивались успехом. Семь лет назад в американском городе Беркли лаборатория имени Лоуренса заявила об удачном синтезе 118-го элемента, который был назван “унуноктикум”. По американским технологиям аналогичные опыты пытались повторить физики из Германии и Японии, однако успеха не добились, после чего унуноктикум прозвали “элементом-невидимкой”. Однако три года спустя американские ученые аннулировали открытие, публично заявив о научном мошенничестве одного из членов группы, проводившей опыт, сообщает газета “Взгляд”.
Через распад к стабильности
Впервые в мире выйти на остров стабильности химическим маршрутом удалось в Дубне, в лаборатории, которой руководит академик Юрий Оганесян. Мишень из плутония-242 облучалась ускоренными до 0,1 скорости света ионами кальция-48. В реакции образовывался изотоп элемента 114 и проникал в камеру со смесью гелия и аргона при атмосферном давлении. Через полсекунды изотоп после альфа-распада превращался в изотоп элемента 112 (химический аналог ртути), который газовой струей переносился в новую криогенную камеру с золотыми детекторами, на которых были зарегистрированы распады ядер элемента 112. Как разъяснил академик Оганесян, похожий эффект использовали мастера в старину, когда золотили купола: покрывали их ртутью, а затем наносили на нее листы золота, которые прилипали намертво, на века.
28 мая был завершен эксперимент по химической идентификации элементов 115 и 113 по конечному продукту распада – элементу, названному “Дубний-105” и теперь российские ученые смело могут заявить, что открыли элементы в таблице с атомарными номерами 112, 113, 114, 115 и 116.
Дубненский эксперимент по-своему уникален: чтобы наблюдать распад дочернего ядра – изотопа 114-го элемента – в отсутствие всякого искажающего фона, в ЛЯРе использовали систему мгновенной остановки циклотрона У-400 после регистрации нового атома №116.
Чрезвычайно дорогой изотоп кальция-48 (1 грамм стоит 250 тыс. долларов), по решению министра по атомной энергии РФ Евгения Адамова, для дубненских физиков наработали на комбинате “Электрохимприбор” города Лесной. Производительность комбината – 4,5 грамма кальция-48 в год. Учитывая это обстоятельство, в Лаборатории ядерных реакций разработали такую методику эксперимента, при которой кальция-48 расходуется 0,3 мг в час. “Мы считаем, одним из больших наших достижений, – подчеркивает Юрий Оганесян, – то, что это уникальное вещество нам удалось перевести в разряд рутинных. Это позволило нам вести эксперименты продолжительностью полгода. В США, например, попытались это сделать, но у них меньше 40 миллиграмм не получилось”.
Это позволило нам вести эксперименты продолжительностью полгода. В США, например, попытались это сделать, но у них меньше 40 миллиграмм не получилось”.
В настоящее время, как сообщает “НГ-Наука”, физики-теоретики уже обсуждают свойства элемента с порядковым номером 400 и числом нейтронов в ядре – 900, так называемые bubble-nuclear (центр ядра пустой).
Материал подготовлен интернет-редакцией www.rian.ru на основе информации Агентства РИА Новости и других источников
Европий
| Европий | |
|---|---|
| Атомный номер | 63 |
| Внешний вид простого вещества | мягкий серебристо-белый металл |
| Свойства атома | |
|
Атомная масса (молярная масса) |
151,965 а. е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | 199 пм |
|
Энергия ионизации (первый электрон) |
546,9 (5,67) кДж/моль (эВ) |
| Электронная конфигурация | [Xe] 4f7 6s2 |
| Химические свойства | |
| Ковалентный радиус | 185 пм |
| Радиус иона | (+3e) 95 (+2e) 109 пм |
|
Электроотрицательность (по Полингу) |
1,2 |
| Электродный потенциал |
Eu←Eu3+ -1,99 В Eu←Eu2+ -2,80 В |
| Степени окисления | 3, 2 |
| Термодинамические свойства простого вещества | |
| Плотность | 5,243 г/см³ |
| Молярная теплоёмкость | 27,656 Дж/(K·моль) |
| Теплопроводность | 13,9 Вт/(м·K) |
| Температура плавления | 1 095 K |
| Теплота плавления | n/a кДж/моль |
| Температура кипения | 1 870 K |
| Теплота испарения | 176 кДж/моль |
| Молярный объём | 28,9 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки |
кубическая объёмноцентрированая |
| Параметры решётки | 4,610 Å |
| Отношение c/a | n/a |
| Температура Дебая | n/a K |
| Eu | 63 |
| 151,965 | |
| 4f76s2 | |
| Европий | |
История
Элемент был выделен в 1886 году из смеси редкоземельных элементов французским химиком Э.
Происхождение названия
После подтверждения существования нового элемента Демарсе дал ему название европий — в честь Европы.
Получение
Металлический европий получают восстановлением Eu2O3 в вакууме лантаном или углеродом, а также электролизом расплава EuCl3.
Цены
Цена на оксид европия чистотой 99,9 % в 2008 году составляет $400-$600 долларов США за килограмм.
Цена на металлический европий чистотой 99,99 % в 2008 году составляет $1600-$2500 за килограмм
Физические свойства
В чистом виде — мягкий серебристо-белый металл, легко поддаётся механической обработке в инертной атмосфере. Приобретает сверхпроводящие свойства при температуре 1,8 К и давлении 80 ГПа.
Химические свойства
На воздухе быстро окисляется, поэтому его хранят в банках или ампулах под слоем жидкого парафина. Очень активный и может вытеснять из растворов солей почти все металлы.
Очень активный и может вытеснять из растворов солей почти все металлы.
В соединениях, как и большинство РЗЭ, проявляет преимущественно валентность +3, при определённых условиях (например, электрохимическим восстановлением, восстановлением амальгамой цинка и др.) можно получить степень окисления +2.
Применение
Ядерная энергетика
Европий используется в качестве поглотителя нейтронов (в основном окись европия, гексаборид и борат европия) в атомных реакторах, но окись постепенно «выгорает», и по срокам эксплуатации уступает карбиду бора в 1,5 раза (хотя имеет преимущество в почти полном отсутствии газовыделения и распухания в мощном потоке нейтронов, например реактор БН-600). Сечение захвата тепловых нейтронов европием (природной смесью изотопов) составляет около 4500 барн, самым активным в отношении захвата нейтронов является европий-151 (9200 барн).
Атомно-водородная энергетика
Оксид европия применяется при термохимическом разложении воды в атомно-водородной энергетике (европий-стронций-йодидный цикл).
Лазерные материалы
Ионы европия служат для генерации лазерного излучения в видимой области спектра с длиной волны 0,61 мк (оранжевые лучи), поэтому оксид европия используется для создания твердотельных, и менее распространённых жидкостных лазеров.
Электроника
Европий является легирующей примесью в моносульфиде самария (термоэлектрогенераторы), а так же как легирующий компонент для синтеза алмазоподобного (сверхтвердого) нитрида углерода. Силицид европия в виде тонких пленок находит применение в интегральной микроэлектронике.
Моноокись европия а так же сплав моноокиси европия и моноокиси самария применяются в виде тонких пленок в качестве магнитных полупроводниковых материалов для стремительно развивающейся функциональной электроники, и в частности МДП — электроники.
Люминофоры
- Вольфрамат европия практически очень важный используемый микроэлектроникой люминофор.
-
Легированный европием борат стронция используется как люминофор в лампах чёрного света.

Европий в медицине
Катионы европия давно и успешно используются в медицине в качестве флуоресцентных зондов. Радиоактивные изотопы европия применяются при лечении некоторых форм рака.
Другие сферы применения европия
- Светочувствительные соединения европия с бромом, хлором и йодом интенсивно изучаются.
- Европий-154 обладает большой мощностью тепловыделения при радиоактивном распаде и предложен в качестве топлива в радиоизотопных источниках энергии.
Влияние на качество воды
В своих реакциях с водой европий химически ведет себя как кальций. При уровнях рН ниже 6 европий способен мигрировать в воде в ионном виде. При более высоких уровнях рН европий образует плохо растворимые и, соответственно, менее подвижные гидроксиды. При контакте с кислородом воздуха происходит дальнейшее окисление до Eu Влияние на качество воды при таких концентрациях представляется незначительным. Очевидно поэтому предельно допустимая концентрация (ПДК) в воде нормируется только российскими нормами и равна (для питьевой воды) 0.3 мг/л.
Влияние на качество воды при таких концентрациях представляется незначительным. Очевидно поэтому предельно допустимая концентрация (ПДК) в воде нормируется только российскими нормами и равна (для питьевой воды) 0.3 мг/л.
Пути поступления в организм
Вероятность попадания европия в организм человека представляется незначительной. Возможно поступление европия в организм с водой в микроскопических количествах. Нельзя исключать вероятности и других путей попадания в организм у людей, сталкивающихся с соединениями европия на производстве.
Потенциальная опасность для здоровья
Европий относится к малотоксичным элементам. По крайней мере, не удалось добыть какой-либо информации о последствиях воздействия европия на организм человека. Единственное, что можно с большой степенью достоверности утверждать, так это то, что в силу своих химических свойств, европий (как и другие лантаноиды) может замещать в биологических системах кальций.
Физиологическое значение
На данный момент нет данных о какой-либо биологической роли европия в организме человека.
Самая большая в Европе таблица Менделеева
23 июля в рамках мероприятий, посвященных 65-летнему юбилею ОИЯИ и города Дубны, состоится торжественное открытие панно «Периодическая таблица Д. И. Менделеева». Ее площадь составляет более 284 кв. м, что делает ее самой большой в Европе.
Таблица расположена на стене плавательного бассейна «Архимед» на набережной Волги и будет хорошо видна как жителям и гостям города, так и пассажирам многочисленных круизных теплоходов, проплывающих по реке. Таблица отражает выдающийся вклад ученых подмосковной Дубны в открытие новых химических элементов и призвана способствовать повышению интереса общества к достижениям современной науки.
Об идее создания панно мы побеседовали с Юрием Цолаковичем Оганесяном – специалистом в области экспериментальной ядерной физики, академиком РАН, научным руководителем Лаборатории ядерных реакций имени Г. Н. Флерова в Объединенном институте ядерных исследований. Под руководством Юрия Цолаковича в Дубне получены все известные к настоящему времени сверхтяжелые элементы от 113-го до 118-го, последний из которых назван в честь ученого – оганесон.
— Юрий Цолакович, в день рождения нашего наукограда состоится знаковое событие – открытие в Дубне самой большой в мире таблицы Менделеева на фасаде бассейна «Архимед».
— Да, это панно станет новой достопримечательностью нашего города. У Дубны славная история: когда построили канал, то здесь установили памятник Ленину работы великого скульптора С. Д. Меркурова, затем был снят кинофильм «Волга-Волга» с Любовью Орловой – часть съемок прошла на канале Москва-Волга и Московском море, а теперь на набережной будет столь знаменательный объект – панно «Периодическая таблица Менделеева».
— Панно – не просто украшение, это прежде всего популяризация науки, своеобразный рассказ дубненцам и гостям города о достижениях ОИЯИ.
— Именно так. Здесь, в Дубне, великое открытие Менделеева имело продолжение – учеными ОИЯИ синтезированы новые химические элементы. Таблица, которую будет видно пассажирам всех проплывающих по Волге теплоходов, отражает выдающийся вклад ученых нашего города в развитие науки и, надеюсь, будет способствовать повышению интереса прежде всего молодежи к новым научным достижениям.
Достопримечательность всегда имеет много граней. На панно можно смотреть с архитектурной, документальной, познавательной, с глубоко научной точек зрения. Мы увидим, как Таблица будет меняться, какие элементы еще будут появляться и так далее.
— На Ваш взгляд, наступит ли время, когда Периодическая таблица Менделеева заполнится и замкнется?
— Вообще, ядерной физике сто с небольшим лет. Говоря об элементах, следует вспомнить, что, когда в марте 1869 года Менделеев отдал свой труд в печать, считалось, что элементы, сколько бы их ни было, являются кирпичиками мироздания, и мир построен из этих элементов. И они, эти кирпичики, неделимы. Их еще Демокрит за 400 лет до нашей эры назвал атомами, тогда это было чисто философское понятие.
А у великого ученого Дальтона – 1808 год, когда было известно всего 36 элементов, – кирпичики соединяются в молекулы, далее в более сложные формы – кристаллы. Всего 36 элементов, как буквы алфавита. И этими буквами вы можете описать все что угодно.
И этими буквами вы можете описать все что угодно.
Но, когда Менделеев начал исследовать свойства этих элементов, их было уже 63, он заметил, что свойства этих элементов периодически повторяются. Однако такое поведение явно не согласуется с понятием «кирпичики мироздания». Буквы в алфавите не должны быть похожи друг на друга! А если они похожи, подчиняясь какой-то закономерности, то это значит, что они сами имеют сложную структуру, которая, собственно, и дает эту периодичность…
Менделеев понял, что рассматриваемый набор элементов – это не кирпичики мироздания. Он стал искать эфир, в котором рождаются элементы, и был целиком поглощен поисками этих истоков материального мира. А таблица осталась. И теперь, как ни странно, 150 лет спустя, мы стали задаваться теми же вопросами: что такое таблица и как толкуется периодичность, что будет дальше, могут ли быть какие-то элементы более тяжелыми, можно ли считать элементы, которые созданы искусственно, настоящими?
Если мы пойдем дальше, то сам закон будет видоизменяться, потому что, согласно теории относительности, если электроны будут двигаться вокруг этого ядра со скоростью, близкой к скорости света, то станет расти их масса, и это должно быть учтено. По этой причине орбиты будут уплотняться, и тогда самая последняя орбита, где крутится тот самый электрон, который ответственен за химические свойства, изменит свои характеристики.
По этой причине орбиты будут уплотняться, и тогда самая последняя орбита, где крутится тот самый электрон, который ответственен за химические свойства, изменит свои характеристики.
Благодаря этим открытиям весь научный мир еще раз убедился, что можно сделать то, что раньше казалось невозможным. Большой прогресс случится, когда начнут строить квантовые компьютеры, это уже мы говорим о технике, а вот как это будет выглядеть… Есть разные сценарии, они зависят от указанного взаимодействия и эффектов теории относительности. Этим мы будем заниматься, это большой путь, сейчас пока мы поняли, что те средства, которые использовали для открытия новых элементов, не годятся, чтобы идти дальше. Сейчас все развивается очень быстро: то, что на данный момент считается передним краем науки, через 10 лет будет обычным делом.
— То есть процесс поиска новых элементов бесконечен…
— Таблица сама по себе неисчерпаема. Она продолжает жить в научном мире, будут добавляться элементы, открываться новые ее формы, строиться новые лаборатории по поиску элементов.
— Юрий Цолакович, любопытно, при каких обстоятельствах возникла сама идея? С чем связан выбор пространства для размещения панно?
— Подобные таблицы уже есть в мире, в Испании, например, она занимает площадь 150 квадратных метров – наша будет больше! Я показал эту таблицу Виктору Анатольевичу Матвееву в 2017 году, тогда мы обсуждали возможность ее появления на заднем фасаде Дома культуры «Мир». Я иногда гуляю по этому парку, сажусь на скамейку как раз напротив. И однажды подходит ко мне Андрей Владимирович Тамонов, и мы обсуждаем, что бы такое монументальное сделать на этой стене. И я посвящаю его в свою идею. А когда я поделился мыслями с Григорием Владимировичем Трубниковым, то он уже имел это в планах, только имел в виду фасад бассейна, чтобы было видно с Волги.
— Если говорить о деталях создания панно – как разрабатывался дизайн, почему он именно такой? Познавательный аспект превыше остального и главенствует в данном объекте?
— Если Вы поищете таблицу Менделеева в интернете – там их огромное количество, по-моему, 1500 видов. Таблица имеет разные формы, из всех мы с Сергеем Николаевичем Дмитриевым выбрали ту, которая имеет научное содержание. Панно «Периодическая таблица имени Д. И. Менделеева» сделано не просто декоративно, но и содержательно с точки зрения науки.
Таблица имеет разные формы, из всех мы с Сергеем Николаевичем Дмитриевым выбрали ту, которая имеет научное содержание. Панно «Периодическая таблица имени Д. И. Менделеева» сделано не просто декоративно, но и содержательно с точки зрения науки.
Наша Таблица будет очень хорошо смотреться ночью, с подсветкой. Кроме того, рядом слева есть свободное поле, на нем можно транслировать лекции, рассказывать об истории открытия элементов, об их химических свойствах, а на правой стороне демонстрировать различные элементы Таблицы.
— Юрий Цолакович, круг Ваших научных интересов описан не в одной статье. А что помогает Вам отвлекаться от рабочего процесса, от науки. Может быть, театральное, музыкальное искусство?
— Все, о чем Вы сейчас сказали, – это все духовное: и мышление, и творчество связаны с духовностью человека. Вы знаете, мне часто задают вопрос, на который сложно отвечать. Меня спрашивают о пользе открытия элементов. Это неосязаемое понимание, которое нельзя купить или продать, оно приходит как открытие, ты вдруг по-новому видишь мир.
— Насколько, на Ваш взгляд, взаимосвязаны наука и культура?
— Одно без другого очень бедно, и, безусловно, они взаимосвязаны. Поэтому своим ученикам я говорю – оставьте ваши книги, забудьте о них на некоторое время, идите в театр, послушайте музыку, посмотрите, что делается вокруг. Это так важно, это расширяет горизонты.
— После соприкосновения с искусством ученые возвращаются к работе уже другими людьми?
— Именно так: я им говорю, что могу все простить, но не могу простить того, если они ничего не знают, кроме своей области. Тогда они и в будущем мало что узнают и откроют.
Если посмотреть на ученых прошлого, они были многогранны. Тот же Менделеев – он не был членом Академии наук, а был членом Академии художеств! Он жил в квартире, выделенной петербургским университетом, и в ней по субботам принимал гостей, накрывая стол белой скатертью. А потом, когда они собирались расходиться, Дмитрий Иванович просил, чтобы они на этой скатерти расписались. А дальше его жена вышивала эти подписи – Репин, Мусоргский, кто только там не был! Это потрясающе. Он устраивал на Соловках раз в месяц семинары. И один из них был посвящен цвету. Приглашал физиков, химиков, артистов, художников, театральных деятелей, и каждый из них выступал на этом семинаре, рассказывал, что он понимает под словом «цвет».
А дальше его жена вышивала эти подписи – Репин, Мусоргский, кто только там не был! Это потрясающе. Он устраивал на Соловках раз в месяц семинары. И один из них был посвящен цвету. Приглашал физиков, химиков, артистов, художников, театральных деятелей, и каждый из них выступал на этом семинаре, рассказывал, что он понимает под словом «цвет».
Физик говорит, что это излучение, химик – что это смешение таких-то компонентов, художник рассуждал, как красный цвет напоминает ему кровь и он не может спокойно смотреть на красные полотнища. И это все интересно людям. В этом смысле, конечно, то что в Дубне будет такая достопримечательность – панно «Периодическая таблица Менделеева» – это замечательно. Будут разные люди смотреть на нее со своей точки зрения, по-разному воспринимать – это очень хорошо!
Беседовала Элеонора Ямалеева
Фотографии Елены Пузыниной
Источник – еженедельник ОИЯИ «Дубна: Наука. Содружество. Прогресс»
Таблица Менделеева пополнится 115-м элементом // Смотрим
Шведские исследователи заявили о том, что обнаружили новый, 115 элемент таблицы Менделеева. Возможно, школьникам понадобятся новые учебники по химии.
Возможно, школьникам понадобятся новые учебники по химии.
Школьникам, возможно, вскоре придётся запомнить название и свойства ещё одного элемента периодической системы химических элементов Менделеева. Исследователи из Лундского университета в Швеции (Lund University) обнаружили новый, сверхтяжёлый элемент с атомным номером 115.
Как сообщается в пресс-релизе, этот элемент крайне радиоактивен и существует всего секунду, прежде чем распадается на более лёгкие атомы. Нужно сказать, что само открытие этого вещества принадлежит русским учёным: они получили его ещё в 2004 году в Дубне. Однако Шведам удалось подтвердить существование нового химического элемента.
“Эксперимент прошёл успешно, и я с уверенностью могу сказать, что это открытие является одним из важнейших за последнее время в нашей сфере исследования”, — говорит ведущий автор исследования, физик-ядерщик Дирк Рудольф (Dirk Rudolph).
После открытия нового элемента, необходимо было определить его точное протонное число. Для этого Рудольф и его коллеги прибегли к нестандартным технологиям: они создали изотоп нового элемента, который затем распался на другие частицы посредством так называемого альфа-распада.
Для этого Рудольф и его коллеги прибегли к нестандартным технологиям: они создали изотоп нового элемента, который затем распался на другие частицы посредством так называемого альфа-распада.
Далее физики изучали внутреннее строение сверхтяжёлого атома. Для этого они взяли мишень из 95-протонного америция (очень тонкую плёнку) бомбардировали её ионами кальция, состоящими из 20 протонов каждый. Это позволило им измерить количество фотонов, связанных с альфа-распадом нового элемента. Удельная энергия частиц света соответствовала предполагаемой энергии рентгеновского излучения, которое учёные назвали “отпечатком пальца” химического элемента.
Прежде чем новый элемент получит своё название, открытие должен подтвердить Международный союз теоретической и прикладной химии.
Статья об открытии вышла в журнале Physical Review Letters.
Также по теме:
113-й элемент таблицы Менделеева: кому присудят открытие?
Японские ученые синтезируют несуществующие элементы таблицы Менделеева
118-й элемент назовут по-русски
Учёные дали названия 114 и 116 элементам таблицы Менделеева
Российские физики впервые получили элемент-117 таблицы Менделеева
Почему мы решили провести акцию Mendeleev Lab?
За полвека до Менделеева периодическая таблица элементов приснилась Пушкину, но он в ней ничего не понял. Это изящный анекдот для тех, кто понимает. Ведь таблицу Менделеева вполне мог «открыть» (на самом деле, конечно, «создать») не Менделеев. Рискнем предположить, что в этом случае она и называлась бы по-другому.
Это изящный анекдот для тех, кто понимает. Ведь таблицу Менделеева вполне мог «открыть» (на самом деле, конечно, «создать») не Менделеев. Рискнем предположить, что в этом случае она и называлась бы по-другому.
2019 год объявлен годом Периодической таблицы химических элементов. «Лаба» решила разобраться: что все-таки сделал Менделеев? И, что не менее важно, – что он не сделал?
Кто же создал таблицу?
Сама идея выстроить известные химические элементы – 63 к середине XIX века – в соответствии с некой закономерностью в то время была совершенно очевидной. Попытки предпринимались уже с начала века. Да и закономерность напрашивалась – атомный вес, работы по измерению которого активно велись с начала века.
Первым ввел понятие «атомный вес», рассчитал атомные массы ряда элементов и составил первую таблицу английский естествоиспытатель Джон Далтон. У нас он в первую очередь ассоциируется с названной в его честь цветовой слепотой – дальтонизмом (у Далтона была эта особенность, которую он исследовал и подробно описал).
Остроумную систему попытался выстроить его соотечественник Джон Александр Ньюлендс, уловивший, как ему казалось, закономерность. «Номера аналогичных элементов, как правило, отличаются или на целое число семь, или на кратное семи, – писал он. – Другими словами, члены одной и той же группы соотносятся друг с другом в том же отношении, как и крайние точки одной или больше октав в музыке».
Однако коллеги «таблицу Ньюлендса» не оценили, ехидно прокомментировав его чрезмерное увлечение музыкой. Фактически, ему в достаточно обидной форме посоветовали быть посерьезнее.
Позже заслуги британца в том, что Менделеев определил как «некоторые зародыши периодического закона», были все-таки подтверждены.
Ньюлендса наградили той же почетной наградой, что и ранее Менделеева и Мейера, – медалью Дэви, присуждаемой Лондонским королевским обществом «за чрезвычайно важные открытия в любой области химии». Но осадочек остался, приоритет «уплыл».
А вот куда он приплыл – вопрос до сих пор в некоторой степени открытый. Честь создания периодической системы элементов, помимо Менделеева, приписывается также немецкому химику Юлиусу Лотару Мейеру, который впервые опубликовал свою таблицу в 1864 году. Она содержала 28 элементов (число было ограничено, чтобы продемонстрировать закономерность), размещённые в шесть столбцов согласно их валентностям.
Менделеев свой первый вариант продемонстрировал в 1869-м. Однако надо понимать, что первые опыты как Мейера, так и Менделеева достаточно далеки от нынешней таблицы. Но при этом труд российского ученого к ней гораздо ближе. Собственно, та закономерность, которую Дмитрий Иванович назвал «периодической закономерностью химических элементов», у Мейера появится позже, чем у Менделеева.
40 градусов внутрь. Это тоже Менделеев?
За свою таблицу Дмитрий Иванович народом глубоко уважаем, а вот подлинно любим за «изобретение водки», что, разумеется, является мифом; но мифом чрезвычайно устойчивым.
Любому человеку, знакомому даже не с историей вопроса, а хотя бы поверхностно – с великой русской литературой, – известно, что водка употреблялась на Руси задолго до появления Менделеева на свет. На ее изобретение претендует несколько кулинарных культур, наилучшие шансы – у русской и польской, но дискуссия еще далека от завершения.
Большинство «верующих в водку Менделеева» полагают: его заслуга состоит не в открытии принципа смешения дистиллированного или ректификованного спирта с водой, а в вычислении идеального соотношения, образующего в итоге «идеальную» крепость в 40 объемных процентов.
Адепты убеждены, что именно Дмитрию Ивановичу принадлежит научное обоснование неких выдающихся свойств 40-градусного напитка, делающих его воздействие на организм не только приятным, но и полезным (вариант: почти безвредным). Те же люди относят печальную реальность на счет злокозненной деятельности производителей, государства или мировой закулисы, скрытно этот золотой принцип нарушающих с разнообразными целями (варианты: для увеличения прибыли, для одурманивания электората, для изведения народа российского под корень).
Наконец, как и положено любому иррациональному учению, имеются раскольники. Те учат, что Менделеев работал не один, а в составе специального комитета по стандартизации, выработавшего идеальный рецепт и превратившего его в государственный стандарт. В любом случае, подавляющее большинство заинтересованных лиц («А кто не пьет? Назови! Нет, я жду!») убеждены в неразрывной связи великого ученого и великого напитка.
Не будем трогать верующих, дабы не оскорбить их чувств. А для остальных поясним: Дмитрий Менделеев практически никакого отношения к водке не имеет. Практически – ибо две его работы могли быть опосредованно использованы для развития водочного производства. Он действительно написал докторскую диссертацию «О соединении спирта с водою», защита которой состоялась 31 января (12 февраля по новому стилю) 1865 года в Санкт-Петербургском университете, и которая носила строго метрологический характер. В ней он исследовал удельный вес водно-спиртовых растворов, содержащих от 50 до 100 весовых процентов спирта, и контракцию (явление уменьшения объёма при смешивании жидкостей) растворов, содержащих от 40 до 55 весовых процентов спирта.
Иными словами, водочные 38-40% остались на нижней границе научных интересов диссертанта.
Менделеев также входил в технический отдел Комитета для пересмотра Положения о питейном сборе, учреждённого в 1863 году при Министерстве финансов, где занимал пост главы подкомиссии по упорядочению производства и продажи слабых (!) алкогольных напитков. Ученый имел также некоторое отношение к учрежденной Сергеем Витте в 1895 году «Комиссии для изыскания способов к упорядочению производства и торгового обращения напитков, содержащих в себе алкоголь», но выступал на её заседаниях всего несколько раз и только по вопросу об акцизах. То есть по предмету экономическому, а не технологическому.
Что же до 40-градусного «золотого сечения», то оно сложилось еще в детстве великого ученого, напрочь минуя при этом науку, исключительно на основе замечательного принципа «государственной пользы». Опытным путем было установлено, что данный стандарт существенно упрощает расчет акциза, взимаемого с производителей. То есть решение имело отношение к наполнению казны деньгами, а не к наполнению сердец подданных российского императора радостью.
То есть решение имело отношение к наполнению казны деньгами, а не к наполнению сердец подданных российского императора радостью.
Сны Менделеева. Что с ними не так?
История с увиденной во сне таблицей тоже, увы, из разряда баек. Откуда она взялась, точно установить не удается.
По одной из версий, в ней «повинен» сам Менделеев, который якобы на сто первый вопрос про происхождение периодического закона раздраженно ответил: «Во сне увидел».
Более вероятно, что мы имеем дело с проекцией куда более достоверной истории. Немецкий химик Фридрих Август Кекуле, один из авторов теории валентности, сам рассказывал, что строение бензольного кольца было навеяно ему сном, в котором он увидел змею, держащую себя за хвост. Впрочем, до сих пор не утихают споры о том, следует ли воспринимать его слова серьезно или известный своим превосходным чувством юмора ученый просто был в хорошем расположении духа. Это, кстати, более чем вероятно: дело было на праздновании 25-летия первой работы Кекуле по бензолу, организованном в его честь Германским химическим обществом.
Вообще «открытие, сделанное во сне» является своеобразным «штампом» истории науки.
Его приписывают Рене Декарту, которого целых три сна навели на мысль о значении дедуктивного метода как универсального в науке. Похожую историю рассказывают о швейцарце Агассисе, который якобы в подробностях увидел кистеперую рыбу, объект его пристального научного интереса. То же рассказывают и о юном Эйнштейне, который вроде бы увидел и запомнил сон, который впоследствии помог обосновать предельность скорости света. Рассказывают и о Нильсе Боре, и о канадце Бантинге – одном из первооткрывателей инсулина, и о целом ряде других ученых.
Пожалуй, в этом, как мало в чем ином, прослеживается старая, как мир, мечта человечества о том, чтобы все устраивалось само собой, увековеченная наблюдением: «Солдат спит – служба идет». Но наука, как известно, сама себя не двигает. Именно за это мы должны быть благодарны и Менделееву, и его многочисленными коллегам.
Европий Eu (элемент) 63 периодической таблицы
63 Eu (Европиум)
Карточка европия
Европий — это мягкий серебристый металл , твердый, как свинец, и достаточно пластичный.
Это самый реактивный металл , быстро окисляется на воздухе и похож на кальций в реакции с водой.
Он Быстро воспламеняется на воздухе при температуре от 150 o C до 180 o C. годы.
Металлическая деталь из европия
Идентификационный номер
Номер CAS: CAS7440-53-1
Номер CID: CID23981
Произношение: Yoor-oh-pee-am
Внешний вид: серебристо-белый, с бледно-желтым оттенком (но редко наблюдается без окислительного обесцвечивания)
Массовый номер: 152
Стандарт Атомный вес: 151,964 г/моль
Атомный номер (Z) : 63
Электроны: 63
Протоны: 63
Нейтроны: 89
Период: 6
Блок: f
Категория элемента: Лантанид
Электроны на оболочке: K2, L8, M18, N25, O8, P2
Электронная конфигурация: 0 17 1s 90 2 2S 2 2P 6 3P 6 3P 6 3P 6 3D 10 4S 2 4P 6 4D 10 5s 2 5p 6 4f 7 6s 2
Электронная конфигурация европия
Термические свойства европия Фаза: Твердое
Температура плавления: 1099 K (826 o C, 1519 o F)
Температура кипения: 1802 K (1529 o C, 2784 o C, 2784 o Fusion) 1 плавление8: 1 плавление821 кДж/моль
Теплота испарения: 176 кДж/моль
Молярная теплоемкость: 27,66 Дж/(моль. К)
К)
Термическое расширение: поли: 35,0 мкм/(м∙K)
Теплопроводность: оценочная 13,9 Вт/(м ∙K)
Точка Нееля (температура магнитного упорядочения) T N : 90,5 K (температура, выше которой антиферромагнитный материал становится парамагнитным)
Электропроводность: 1,1×10 6 См/м
a Удельное электрическое сопротивление: поли: 0.900 мкОм∙м
a Электрический тип: Проводник
Критическая точка (сверхпроводящая точка): 1,8 К (значение измерено при 80 ГПа)
Магнитный Тип: Paramagnetic
Магнитная восприимчивость (x MOL ): + 34 000 × 10 -6 см 3 / моль
Громкость Магнитная восприимчивость: 0.0014473
Массовая магнитная восприимчивость: 276 × 10 -9 м 3 /кг
Молярная магнитная восприимчивость: 41.942×10 -9 м 3 /моль
Плотность: 5. 264 г / см 3 (в солидном) 5.13 г / см 3 (в жидкости)
264 г / см 3 (в солидном) 5.13 г / см 3 (в жидкости)
молярный объем: 0.00002898 м 3 / моль
Модуль молодых: 18.2 GPA
Модуль сдвига: 7,9 GPA
модуль: 8,3 ГПа
Коэффициент Пуассона: 0,152
Твердость по Моосу: 3,7
Твердость по Виккеру: 165-200 МПа
Скорость звука: 2680 м/с
Степени окисления: 3, 2
Валентные электроны: 4f 7 6s 2
Заряд иона: Eu 3+ Eu 2+
Энергии ионизации: 1.1 кДж.моль 2-й: 1085 кДж/моль 3-й: 2404 кДж/моль
Ионный радиус: 94,7 пм
Атомный радиус: 233 пм (Ван-дер-Ваальс)
Ковалентный радиус: 198±6 пм
Заполняющая орбита: 4f 7 Кристаллическая структура: Объемно-центрированная кубическая
Углы решетки: π/2, π/2, π/2
Постоянная решетки: 458,1, 458,1, 458,1 пм
Параметры сетки: 4,581 Å
Название пространственной группы: lm_3m
Номер пространственной группы: 229
Объемно-центрированный куб (BCC)
Реакционная способность европия Электроотрицательность: шкала Полинга: 1. 2
2
Валентность: +3
Сродство к электрону: 50 кДж/моль
Период полураспада: стабильный (бесконечность)
Срок службы: стабильный (бесконечность)
Квантовое число: 8 S 7/2
Нейтронное сечение (Бранс): 4450
Поглощение массы нейтронов: 0,6 203
1150 Eu Изотопы: 151 Евро 152 Евро 153 Евро 154 Евро 155 Евро
| Изотоп | Численность (%) | Атомная масса г/моль | Период полувыведения (т 1/2 ) |
| 150 ЕС | Син | – | 36.9 лет |
| 151 ЕС | 47,8 | 150,920 | 5×10 18 г |
| 152 ЕС | Син | – | 13. 54 г 54 г |
| 153 ЕС | 52,2 | 152,921 | Стабильный |
| 154 ЕС | Эйн | – | 8,59 г |
| 155 ЕС | Син | – | 4.76 лет |
европий горит легко на 150 O C , чтобы сформировать EURUPIUM (LLL) Оксид :
4 EU + 3 O 2 → 2 EU 2 o 3
реагирует с водой:
2 EU ( s) + 6 H 2 O (г) → 2 Eu(OH) 3 (водн.) + 3 H 2 (г)
Металл реагирует со всеми галогенами с образованием галогенидов европия (lll) :
2 Eu (т) + 3 F 2 (г) → 2 EuF 3 (т) [белый] (Европия (lll) фторид)
2 Eu (т) + 3 Cl 2 (г ) → 2 EuCl 3 (т) [желтый] (Европия (III) хлорид)
2 Eu (т) + 3 Br 2 (г) → 2 EuBr 3 (т) 9000 3 (Европия (lll) бромид)
2 Eu (s) + 3 I 2 (g) → 2 EuI 3 (s) (Европия (lll) йодид)
Легко растворяется в разбавленной серной кислоте гидратированный европий (lll) (бледно-розовый раствор):
2 Eu + 3 H 2 SO 4 + 18 H 2 O → 2 [ЕС (H 2 O) 9 ] 3+ + 3 SO 4 2- + 3 ч 2
Наименование: После Европы
Открытие: Эжен-Анатоль Демарсе (1896, 1901)
Европий является отличным поглотителем нейтронов , Он используется в регулирующих стержнях ядерных реакторов.
Он светится красным в ультрафиолетовом свете.
Для мощного уличного освещения, Лампы с низким энергопотреблением (ртутные лампы) содержат немного европия, чтобы дать более естественный свет, уравновешивая синий (холодный) свет небольшим количеством красного (теплого) света.
A Соль (оксид) европия используется для более новых фосфоресцирующих порошков (светящихся в темноте) и красок . Пластмасса
, легированная европием, использовалась в качестве лазерного материала .
Биологическая роль: Малотоксичен, но с ним следует обращаться осторожно.
Обилие европия Европий в основном содержится в минералах , монаците, и , бастнезите.
Получают смешиванием оксида европия (III) (Eu 2 O 3 ) с 10%-ным избытком металлического лантана и нагреванием смеси в высоком вакууме в танталовом тигле , и его собирают в виде серебристо-белого металлического осадка на стенке тигля.
Ежегодное мировое производство составляет около 400 тонн.
5 × 10 -8 % (в Universe )
5,9 × 10 -6 % (в Meteorites )
5 × 10 -8 % (в Sun )
0,00018% В Земная кора )
1,3×10 -11 % (В океанах )
1) Китай
2) Россия
3) Малайзия
1) Китай
2) Страны СНГ (вкл.Россия)
3) США
#Европиум
Карточки с дополнительными элементами
Объяснение Периодической таблицы элементов
Просмотров: 19307 Просмотров
Обновлено 26 января 2022 г.
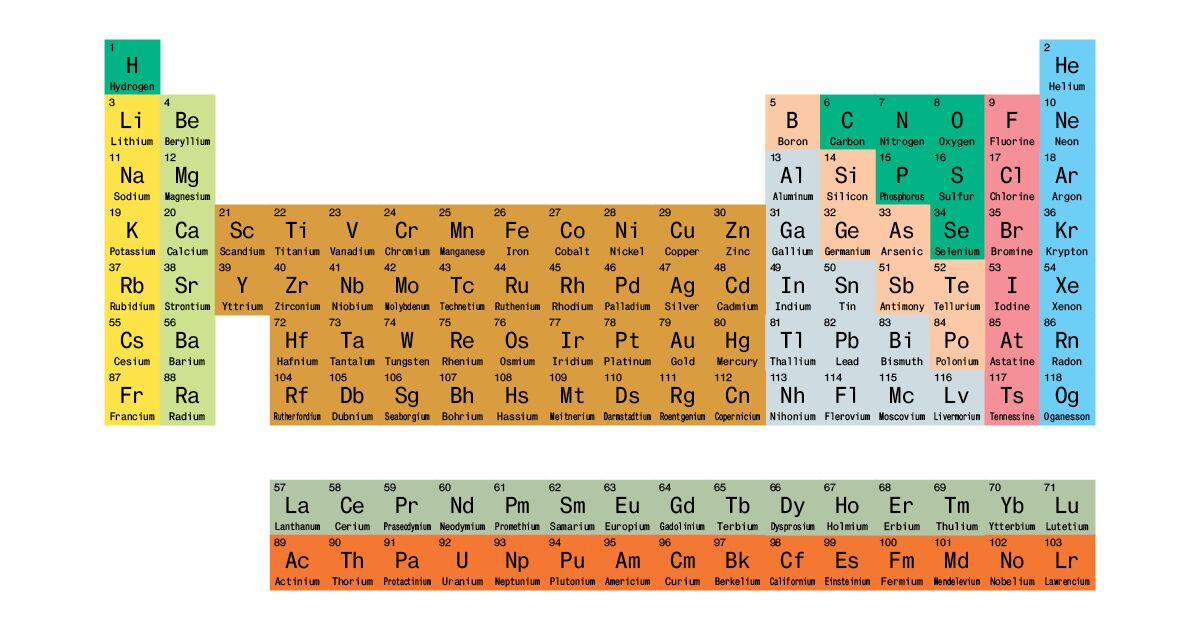
Периодическая таблица элементов 1 представляет собой упорядоченную систему всех идентифицированных элементов. Эти элементы составляют все в нашей вселенной.
Эти элементы составляют все в нашей вселенной.
Химические элементы таблицы Менделеева являются строительными блоками всего в природе.Эти элементы также создают продукты и технологии, которые бесчисленным образом сформировали современное общество — чистая питьевая вода, эффективные лекарства и технологии, начиная от солнечных батарей и заканчивая компонентами электроники.
Вам не нужно быть химиком, чтобы понимать периодическую таблицу. Читайте дальше, чтобы узнать больше об этом.
Почему была разработана таблица Менделеева:
В 1869 году русский химик Дмитрий Менделеев хотел выяснить, существует ли закономерность в химических свойствах известных ему элементов.Он нашел закономерность, упорядочив элементы по возрастанию атомного номера и расположив их на диаграмме, создав первую периодическую таблицу. Эта структура помогла Менделееву и другим ученым определить сходства и различия между элементами, чтобы предсказать будущие химические реакции.
Периодическая таблица Менделеева включала 63 элемента. Он ожидал, что в один прекрасный день будут обнаружены и другие, поэтому он оставил свободное место в своей таблице для дополнений. Сегодня 118 химических элементов, идентифицированных в периодической таблице, включают материалы, из которых состоят все известные объекты во Вселенной.
Он ожидал, что в один прекрасный день будут обнаружены и другие, поэтому он оставил свободное место в своей таблице для дополнений. Сегодня 118 химических элементов, идентифицированных в периодической таблице, включают материалы, из которых состоят все известные объекты во Вселенной.
Знаете ли вы? Наиболее распространенным элементом (по массе), составляющим Землю4, является железо (Fe). 2 Кислород (O) является наиболее распространенным элементом в земной коре. 3
Как элементы организованы в периодической таблице:
Элементы организованы в горизонтальные ряды по возрастанию атомного номера. 4 Атомный номер, расположенный в верхнем левом углу символа элемента, означает количество протонов в ядре атома.
Под символом элемента стоит атомный вес, представляющий собой средний вес протонов и нейтронов в атоме. Поскольку в природе атомы имеют разное количество нейтронов (известных как изотопы), атомная масса представляет собой среднее значение всех весов всех изотопов для данного атома.
Что такое периоды?
Горизонтальные ряды периодической таблицы называются периодами. Периодическая таблица содержит семь периодов 5 (девять, если считать ряды лантаноидов и актиноидов).В каждом периоде атомные номера элементов увеличиваются слева направо. Все элементы одного и того же периода имеют одинаковое количество электронных оболочек, но разное количество электронов и протонов.
Зная количество электронов химического элемента, вы можете рассчитать его валентность. 6 Способность атома или группы атомов образовывать химические связи с другими атомами. Валентность является важным аспектом расчета химических формул для студентов и химиков.
Что такое семьи?
«Семейства» — это группы элементов, представленные в девяти из 18 вертикальных столбцов периодической таблицы. 7 Семейства химических элементов имеют схожие свойства, например, их электронные конфигурации. 8 Например, элементы со свойствами, сходными с натрием (Na), такие как литий (Li) и калий (K), входят в одно и то же семейство.
Как элементы добавляются в таблицу?
Международный союз теоретической и прикладной химии (IUPAC) ведет периодическую таблицу и устанавливает критерии для новых дополнений. 9 Последний раз ИЮПАК обновлял периодическую таблицу в 2016 году, добавляя четыре новых элемента: нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). 10
Как читать и интерпретировать периодическую таблицу:
Периодическая таблица помогает химикам классифицировать элементы по свойствам и сходству. Один из способов сортировки элементов состоит в том, чтобы разделить их на три категории: металлы, неметаллы и металлоиды:
- Большинство элементов в периодической таблице считаются металлами .У них схожие характеристики — большинство из них твердые, блестящие, хорошо проводят электричество и податливы.
- Неметаллы обладают свойствами, противоположными металлам – они хрупкие, не гибкие и плохо проводят тепло или электричество.
 Некоторые неметаллы являются жидкостями, некоторые газообразными.
Некоторые неметаллы являются жидкостями, некоторые газообразными. - Металлоиды или полуметаллы считаются чем-то средним между металлами и неметаллами. Металлоиды обладают уникальными свойствами проводимости, что делает их полезными в производстве полупроводников и компьютерных микросхем. 11
Периодическая таблица элементов помогает нам лучше понять химические элементы и их связь друг с другом. Продукты, материалы и технологии, формирующие нашу жизнь, создаются элементами и тем, как они взаимодействуют друг с другом.
1 Периодическая таблица элементов – PubChem (nih.gov)
2 Ион железа | Fe+3 – PubChem (nih.gov)
3 Самый распространенный элемент во Вселенной, Земле и Теле (thinkco.ком)
4 Как устроена Периодическая таблица сегодня? (thinkco.com)
5 Разница между группой элементов и периодом (thoughtco.com)
6 Что такое валентность или валентность в химии? (thinkco. com)
com)
7 Семейства элементов периодической таблицы (thightco.com)
8 Периодическая таблица: семьи и периоды – макеты
9 Международный союз теоретической и прикладной химии (iupac.орг)
10 ИЮПАК дает названия четырем новым элементам: нихоний, московий, теннессин и оганесон – ИЮПАК
11 Периодическая таблица: металлы, неметаллы и металлоиды – макеты
150 лет гениальному сотворению Дмитрия Менделеева
Таблица Менделеева смотрит вниз со стен почти каждой химической лаборатории. Заслуга в его создании обычно принадлежит Дмитрию Менделееву, русскому химику, который в 1869 году записал известные элементы (которых в то время было 63) на карточках, а затем расположил их в столбцы и ряды в соответствии с их химическими и физическими свойствами.В ознаменование 150-летия этого поворотного момента в науке ООН провозгласила 2019 год Международным годом Периодической таблицы.
Но на самом деле периодическая таблица началась не с Менделеева. Многие возились с расположением элементов. За несколько десятилетий до этого химик Джон Дальтон попытался создать таблицу, а также несколько довольно интересных символов для элементов (они не прижились). А всего за несколько лет до того, как Менделеев сел за свою колоду самодельных карт, Джон Ньюлендс также создал таблица, сортирующая элементы по их свойствам.
Гениальность Менделеева заключалась в том, что он упустил из своей таблицы. Он признал, что некоторые элементы отсутствуют, но их еще предстоит обнаружить. Так что там, где Дальтон, Ньюлендс и другие изложили известное, Менделеев оставил место для неизвестного. Что еще более удивительно, он точно предсказал свойства недостающих элементов.
Таблица Дмитрия Менделеева с недостающими элементами. Викисклад Обратите внимание на вопросительные знаки в его таблице выше? Например, рядом с Al (алюминием) есть место для неизвестного металла.Менделеев предсказал, что у него будет атомная масса 68, плотность шесть граммов на кубический сантиметр и очень низкая температура плавления. Шесть лет спустя Поль Эмиль Лекок де Буабодран выделил галлий и, конечно же, он попал прямо в щель с атомной массой 69,7, плотностью 5,9 г/см³ и температурой плавления настолько низкой, что он становится жидким в вашей руке. Менделеев сделал то же самое для скандия, германия и технеция (который был открыт только в 1937 году, через 30 лет после его смерти).
Шесть лет спустя Поль Эмиль Лекок де Буабодран выделил галлий и, конечно же, он попал прямо в щель с атомной массой 69,7, плотностью 5,9 г/см³ и температурой плавления настолько низкой, что он становится жидким в вашей руке. Менделеев сделал то же самое для скандия, германия и технеция (который был открыт только в 1937 году, через 30 лет после его смерти).
На первый взгляд таблица Менделеева не очень похожа на знакомую нам.Во-первых, в современной таблице есть множество элементов, которые Менделеев упустил из виду (и не оставил для них места), в первую очередь благородные газы (такие как гелий, неон, аргон). И таблица ориентирована иначе, чем наша современная версия, с элементами, которые мы теперь размещаем вместе в столбцах, расположенных в строках.
Но стоит повернуть таблицу Менделеева на 90 градусов, как становится очевидным сходство с современной версией. Например, галогены — фтор (F), хлор (Cl), бром (Br) и йод (I) (символ J в таблице Менделеева) — располагаются рядом друг с другом. Сегодня они расположены в 17-й колонке таблицы (или в 17-й группе, как ее предпочитают называть химики). для элементов. Еще до того, как стол получил свое постоянное переворачивание под прямым углом, люди предложили несколько странных и замечательных поворотов.
Сегодня они расположены в 17-й колонке таблицы (или в 17-й группе, как ее предпочитают называть химики). для элементов. Еще до того, как стол получил свое постоянное переворачивание под прямым углом, люди предложили несколько странных и замечательных поворотов.
Одним из особенно ярких примеров является спираль Генриха Баумхауэра, опубликованная в 1870 году, с водородом в ее центре и элементами с возрастающей атомной массой, раскручивающимися по спирали наружу. Элементы, попадающие на каждую из спиц колеса, имеют общие свойства, как и элементы в столбце (группе) в сегодняшней таблице. Была также довольно странная формулировка Генри Бассета «гантели» 1892 года.
Тем не менее, к началу 20-го века таблица приняла знакомый горизонтальный формат с поразительно современной версией Генриха Вернера в 1905 году. Впервые благородные газы появились в привычном для них положении на крайняя правая часть стола. Вернер также попытался вырвать листок из книги Менделеева, оставив пробелы, хотя он несколько переборщил с предположениями относительно элементов, более легких, чем водород, и еще одного элемента, находящегося между водородом и гелием (ни одного из которых не существует).)
Впервые благородные газы появились в привычном для них положении на крайняя правая часть стола. Вернер также попытался вырвать листок из книги Менделеева, оставив пробелы, хотя он несколько переборщил с предположениями относительно элементов, более легких, чем водород, и еще одного элемента, находящегося между водородом и гелием (ни одного из которых не существует).)
Несмотря на то, что таблица выглядела довольно современно, предстояло еще кое-что переставить. Особенно влиятельной была версия Чарльза Джанет. Он подошёл к таблице с точки зрения физики и использовал недавно открытую квантовую теорию для создания макета на основе электронных конфигураций. Полученная в результате таблица «левого шага» до сих пор предпочитается многими физиками. Интересно, что Джанет также предоставила место для элементов вплоть до номера 120, несмотря на то, что в то время было известно только 92 (сейчас у нас только 118).
Современный стол на самом деле представляет собой прямую эволюцию версии Джанет.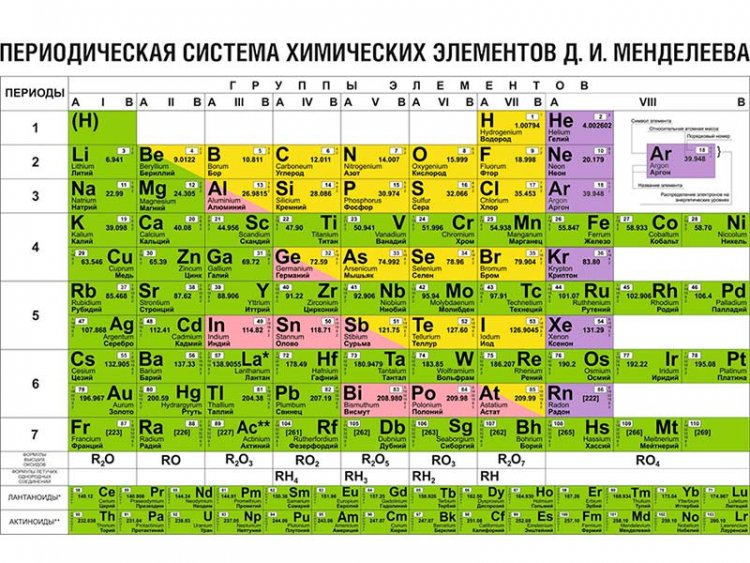 Щелочные металлы (группа, возглавляемая литием) и щелочноземельные металлы (возглавляемая бериллием) сместились из крайнего правого положения в крайнее левое, чтобы создать очень широкую (длинную форму) периодическую таблицу. Проблема с этим форматом заключается в том, что он плохо помещается на странице или плакате, поэтому в основном из эстетических соображений элементы f-блока обычно вырезаются и размещаются под основной таблицей. Вот как мы пришли к таблице, которую мы знаем сегодня.
Щелочные металлы (группа, возглавляемая литием) и щелочноземельные металлы (возглавляемая бериллием) сместились из крайнего правого положения в крайнее левое, чтобы создать очень широкую (длинную форму) периодическую таблицу. Проблема с этим форматом заключается в том, что он плохо помещается на странице или плакате, поэтому в основном из эстетических соображений элементы f-блока обычно вырезаются и размещаются под основной таблицей. Вот как мы пришли к таблице, которую мы знаем сегодня.
Это не значит, что люди не возились с макетами, часто пытаясь выделить корреляции между элементами, которые не очевидны в обычной таблице. Существуют буквально сотни вариаций (ознакомьтесь с базой данных Марка Лича), особенно популярны спирали и 3D-версии, не говоря уже о более насмешливых вариантах.
Как насчет моего собственного слияния двух знаковых рисунков, таблицы Менделеева и карты лондонского метро Генри Бека ниже?
Авторская подземная карта стихий.Марк Лорх Или головокружительный набор имитаций, которые призваны дать научное ощущение категоризации всего, от пива до персонажей Диснея, и моей любимой «иррациональной чепухи». Все это показывает, как периодическая таблица элементов стала культовым символом науки.
Все это показывает, как периодическая таблица элементов стала культовым символом науки.
Марк Лорч — профессор научной коммуникации и химии Университета Халла, Великобритания.
Прочитайте оригинальную статью.
Европий Факты, Символ, Открытие, Свойства, Использование
Что такое европий
Принадлежность к семейству лантаноидов, европий (произносится как yoo-RO-pee-em) представляет собой редкоземельный металл, обозначаемый химическим символом Eu [1] . Он состоит из тридцати изотопов с массовыми числами от 131 до 162, из которых европий-151 и европий-153 стабильны и встречаются в природе [3] .
Символ европия
Где найти
Поскольку этот элемент не встречается в природе свободно, он встречается в минералах монаците и бастназите [1] .Его добывают в Австралии, США, Индии, России и Китае [6] .
История
Происхождение его названия: Он назван в честь континента, Европа [1] .
Кто открыл: Открыт французским химиком Эженом-Анатолем Демарсе [1] .
Когда и где был открыт европий
В 1839 году, после открытия церия, Карл Мосандер выделил два новых элемента, лантан и дидим, где последний содержал смесь празеодима и неодима, обнаруженную позднее в 1879 году Карлом Ауэром.После этого Поль-Эмиль Лекок де Буабодран выделил еще один новый элемент, самарий, но обнаружил, что он нечист, а затем Жан Шарль Галиссар де Мариньяк, который извлек гадолиний в 1886 году. Наконец, в 1901 году Демарсе провел серию кристаллизаций нитрата магния самария для выделения другой новый элемент под названием европий [1] .
Европий Металл
Европий Идентификация | |||
| Атомный номер | 63 [1] | ||
| Номер CAS | 7440-53-1 [1] | ||
| Позиция в таблице Менделеева [1] | Группа | Период | Блок |
| Лантаниды | 6 | ф | |
Место европия в периодической таблице
Свойства и характеристики европия
Общие свойства | ||
| Относительная атомная масса | 151. 964 [1] 964 [1] | |
| Атомная масса | 151,964 атомных единиц массы [5] | |
Физические свойства | ||
| Цвет/внешний вид | Серебро [1] | |
| Точка плавления/замерзания | 822°C (1521°F) [1] | |
| Температура кипения | 1529°C (2784°F) [1] | |
| Плотность | 5.24 г/см 3 [1] | |
| Комнатная температура при нормальной фазе (твердое/жидкое/газообразное) | сплошной [1] | |
| Твердость (по Виккерсу) | 3,07 Мооса [5] | |
| Электропроводность | 1,6×10 6 Ш/м | |
Химические свойства | ||
| Степени окисления | 3, 2 [1] | |
Атомные данные европия (элемент 63)
| Валентные электроны | 3 [5] | ||||||
| Кристаллическая структура | Объемно-центрированная кубическая решетка [5] | ||||||
| Квантовые числа [7] | |||||||
| – № | 4 | ||||||
| – ℓ | 3 | ||||||
| – м ℓ | 3 | ||||||
| – м с | +1/2 | ||||||
| Электронная конфигурация (конфигурация благородных газов) | [Xe] 4f 7 6s 2 [1] | ||||||
| Атомная структура [3] | |||||||
| – Количество электронов | 63 | ||||||
| — Количество нейтронов | 90 | ||||||
| — Количество протонов | 63 | ||||||
| Радиус атома | |||||||
| – Атомный радиус | 2. 35 Å [1] 35 Å [1] | ||||||
| – Ковалентный радиус | 1,83 Å [1] | ||||||
| Энергия ионизации [1] (кДжмоль -1 ) | 1-й | 2-й | 3-й | 4-й | 5-й | 6-й | 7-й |
| 547,109 | 1085,46 | 2404.41 | 4119,9 | – | – | – | |
Атомная структура европия (модель Бора)
Для чего используется европий
- Люминофоры, легированные европием, используются в качестве флуоресцентных маркеров безопасности на банкнотах евро, поскольку они светятся красным в ультрафиолетовом свете и, следовательно, помогают в обнаружении подделок [1, 2, 8] .
- Он используется при изготовлении лампочек с низким энергопотреблением для получения мягкого света, как в лампах накаливания, за счет поддержания баланса между синим (холодным) светом и мягким красным (теплым) светом [1, 9] .

- Пластмассы, легированные европием, являются хорошими лазерными материалами и сверхпроводящими сплавами [1] .
Европий
Токсичность европия
Металл может оказывать слабое токсическое воздействие, поэтому при обращении с ним следует соблюдать крайние меры предосторожности.
Интересные факты
- Способность европия поглощать нейтроны может быть использована в ядерных реакторах в будущем [2] .
- Наиболее реакционноспособен среди всех редкоземельных металлов [2] .
Сколько стоит европий
Цена металла в чистом виде может варьироваться от 2300 до 2500 долларов за килограмм.
Ссылки
- http://www.rsc.org/periodic-table/element/63/europium
- https://образование.jlab.org/itselemental/ele063.html
- https://pubchem.ncbi.nlm.nih.gov/compound/europium#section=Computed-Properties
- https://www.
 chemicool.com/elements/europium.html
chemicool.com/elements/europium.html - http://periodictable.com/Elements/063/data.html
- https://mineralseducationcoalition.org/elements/europium/
- http://chemistry-reference.com/q_elements.asp?Symbol=Eu&language=en
- файл:///C:/Users/LENOVO/Downloads/Европий-допированные_люминофоры_для_освещения_the_past_the.пдф
- https://eic.rsc.org/elements/europium/2020007.article
ЭниГ. Периодическая таблица элементов
ПЕРЕХОДНЫЙ ЭЛЕМЕНТ: ЛАНТАНИД
| Number | |
| 63 | 63 |
| Количество номеров: | 3 |
| Период: | |
| Период: | 6 |
| Электронная конфигурация: | [XE] 4F 7 6s 2 |
| Формальная степень окисления: | +2 +3 |
| Электроотрицательности: | – |
| Атомный радиус / пм: | 199. |
| Относительная атомная масса: | 151,964(1) |
Европий был обнаружен Эженом-Анатолем Демарсе (Франция) в 1896 году. Назван в честь континента Европа . Это мягкий серебристо-белый металл, который чрезвычайно активно реагирует с кислородом и водой. Европий получают из монацитового песка, представляющего собой смесь фосфатов кальция, тория, церия и большинства других редкоземельных элементов. Он используется с оксидом иттрия для изготовления красных люминофоров для цветных телевизоров.Цена слитка европия чистотой 99,9% составляет 254,30 € за 5 г.
| Плотность / г DM -3 : | :5243 | (293 K) |
| Молровый объем / см 3 Mol -1 : | 28.98 | (293 K) |
| Удельное электрическое сопротивление / мкОм·см: | 90 | (20 °C) |
| Теплопроводность / Вт·м -1 К -1 : | 13. 9 9 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Pointing Point / ° C: | 822 | 822 | 822 | ||||||||||||||||||||||||||||||||||||||||||||||
| Тонкость кипения / ° C: | 1529 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое тепло / KJ Mol -1 : | 10.5 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Тепло теплоты испарения / кДж моль -1 : | 176 | ||||||||||||||||||||||||||||||||||||||||||||||||
|


 Это легирующая примесь в некоторых типах стекла в лазерах и других оптоэлектронных устройствах. Оксид европия (Eu 2 O 3 ) широко используется в качестве красного люминофора в телевизорах и люминесцентных лампах, а также в качестве активатора люминофоров на основе иттрия. Экраны цветных телевизоров содержат от 0,5 до 1 г оксида европия.
Это легирующая примесь в некоторых типах стекла в лазерах и других оптоэлектронных устройствах. Оксид европия (Eu 2 O 3 ) широко используется в качестве красного люминофора в телевизорах и люминесцентных лампах, а также в качестве активатора люминофоров на основе иттрия. Экраны цветных телевизоров содержат от 0,5 до 1 г оксида европия.


 Эти реакторы представляют собой месторождения урана, которые естественным образом подверглись устойчивым ядерным реакциям в Габоне, западная Африка, около 1,9 миллиарда лет назад.
Эти реакторы представляют собой месторождения урана, которые естественным образом подверглись устойчивым ядерным реакциям в Габоне, западная Африка, около 1,9 миллиарда лет назад.