происхождение и характеристика Номер железа в таблице менделеева
Если таблица Менделеева кажется вам сложной для понимания, вы не одиноки! Хотя бывает непросто понять ее принципы, умение работать с ней поможет при изучении естественных наук. Для начала изучите структуру таблицы и то, какую информацию можно узнать из нее о каждом химическом элементе. Затем можно приступить к изучению свойств каждого элемента. И наконец, с помощью таблицы Менделеева можно определить число нейтронов в атоме того или иного химического элемента.
Шаги
Часть 1
Структура таблицы
Как видно, каждый следующий элемент содержит на один протон больше, чем предшествующий ему элемент. Это очевидно, если посмотреть на атомные номера. Атомные номера возрастают на один при движении слева направо. Поскольку элементы расположены по группам, некоторые ячейки таблицы остаются пустыми.
- Например, первая строка таблицы содержит водород, который имеет атомный номер 1, и гелий с атомным номером 2. Однако они расположены на противоположных краях, так как принадлежат к разным группам.
Узнайте о группах, которые включают в себя элементы со схожими физическими и химическими свойствами.
 Все элементы той или иной группы имеют одинаковое число электронов на внешней оболочке.
Все элементы той или иной группы имеют одинаковое число электронов на внешней оболочке.- Водород можно отнести как к группе щелочных металлов, так и к группе галогенов. В некоторых таблицах его указывают в обеих группах.
- В большинстве случаев группы пронумерованы от 1 до 18, и номера ставятся вверху или внизу таблицы. Номера могут быть указаны римскими (например, IA) или арабскими (например,1A или 1) цифрами.
- При движении вдоль колонки сверху вниз говорят, что вы «просматриваете группу».
Узнайте, почему в таблице присутствуют пустые ячейки. Элементы упорядочены не только в соответствии с их атомным номером, но и по группам (элементы одной группы обладают схожими физическими и химическими свойствами). Благодаря этому можно легче понять, как ведет себя тот или иной элемент. Однако с ростом атомного номера не всегда находятся элементы, которые попадают в соответствующую группу, поэтому в таблице встречаются пустые ячейки.
- Например, первые 3 строки имеют пустые ячейки, поскольку переходные металлы встречаются лишь с атомного номера 21.

- Элементы с атомными номерами с 57 по 102 относятся к редкоземельным элементам, и обычно их выносят в отдельную подгруппу в нижнем правом углу таблицы.
- Например, первые 3 строки имеют пустые ячейки, поскольку переходные металлы встречаются лишь с атомного номера 21.
Каждая строка таблицы представляет собой период. Все элементы одного периода имеют одинаковое число атомных орбиталей, на которых расположены электроны в атомах. Количество орбиталей соответствует номеру периода. Таблица содержит 7 строк, то есть 7 периодов.
- Например, атомы элементов первого периода имеют одну орбиталь, а атомы элементов седьмого периода – 7 орбиталей.
- Как правило, периоды обозначаются цифрами от 1 до 7 слева таблицы.
- При движении вдоль строки слева направо говорят, что вы «просматриваете период».
Научитесь различать металлы, металлоиды и неметаллы. Вы лучше будете понимать свойства того или иного элемента, если сможете определить, к какому типу он относится. Для удобства в большинстве таблиц металлы, металлоиды и неметаллы обозначаются разными цветами.
 Металлы находятся в левой, а неметаллы – в правой части таблицы. Металлоиды расположены между ними.
Металлы находятся в левой, а неметаллы – в правой части таблицы. Металлоиды расположены между ними. Часть 2
Обозначения элементовКаждый элемент обозначается одной или двумя латинскими буквами. Как правило, символ элемента приведен крупными буквами в центре соответствующей ячейки. Символ представляет собой сокращенное название элемента, которое совпадает в большинстве языков. При проведении экспериментов и работе с химическими уравнениями обычно используются символы элементов, поэтому полезно помнить их.
- Обычно символы элементов являются сокращением их латинского названия, хотя для некоторых, особенно недавно открытых элементов, они получены из общепринятого названия. К примеру, гелий обозначается символом He, что близко к общепринятому названию в большинстве языков. В то же время железо обозначается как Fe, что является сокращением его латинского названия.
Обратите внимание на полное название элемента, если оно приведено в таблице.
 Это «имя» элемента используется в обычных текстах. Например, «гелий» и «углерод» являются названиями элементов. Обычно, хотя и не всегда, полные названия элементов указываются под их химическим символом.
Это «имя» элемента используется в обычных текстах. Например, «гелий» и «углерод» являются названиями элементов. Обычно, хотя и не всегда, полные названия элементов указываются под их химическим символом.- Иногда в таблице не указываются названия элементов и приводятся лишь их химические символы.
Найдите атомный номер. Обычно атомный номер элемента расположен вверху соответствующей ячейки, посередине или в углу. Он может также находиться под символом или названием элемента. Элементы имеют атомные номера от 1 до 118.
- Атомный номер всегда является целым числом.
Помните о том, что атомный номер соответствует числу протонов в атоме. Все атомы того или иного элемента содержат одинаковое количество протонов. В отличие от электронов, количество протонов в атомах элемента остается постоянным. В противном случае получился бы другой химический элемент!
- По атомному номеру элемента можно также определить количество электронов и нейтронов в атоме.

- По атомному номеру элемента можно также определить количество электронов и нейтронов в атоме.
Обычно количество электронов равно числу протонов. Исключением является тот случай, когда атом ионизирован. Протоны имеют положительный, а электроны – отрицательный заряд. Поскольку атомы обычно нейтральны, они содержат одинаковое количество электронов и протонов. Тем не менее, атом может захватывать электроны или терять их, и в этом случае он ионизируется.
- Ионы имеют электрический заряд. Если в ионе больше протонов, то он обладает положительным зарядом, и в этом случае после символа элемента ставится знак «плюс». Если ион содержит больше электронов, он имеет отрицательный заряд, что обозначается знаком «минус».
- Знаки «плюс» и «минус» не ставятся, если атом не является ионом.
Таблица Менделеева, или периодическая система химических элементов, начинается в левом верхнем углу и заканчивается в конце последней строки таблицы (в нижнем правом углу).
Элементы в таблице расположены слева направо в порядке возрастания их атомного номера. Атомный номер показывает, сколько протонов содержится в одном атоме. Кроме того, с увеличением атомного номера возрастает и атомная масса.
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов.
Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.
Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс “Таблица Менделеева для чайников”. В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе , который с радостью поделится с вами своими знаниями и опытом.
Инструкция
Периодическая система представляет собой многоэтажный «дом», в котором располагается большое количество квартир. Каждый «жилец» или в своей собственной квартире под определенным номером, который является постоянным. Помимо этого элемент имеет «фамилию» или название, например кислород, бор или азот. Кроме этих данных в каждой «квартире» или указана такая информация, как относительная атомная масса, которая может иметь точные или округленные значения.
Кроме этих данных в каждой «квартире» или указана такая информация, как относительная атомная масса, которая может иметь точные или округленные значения.
Как в любом доме, здесь имеются «подъезды», а именно группы. Причем в группах элементы располагаются слева и справа, образуя . В зависимости от того, с какой стороны их больше, та называется главной. Другая подгруппа, соответственно, будет побочной. Также в таблице имеются «этажи» или периоды. Причем периоды могут быть как большими (состоят из двух рядов) так и малыми (имеют только один ряд).
По таблице можно показать строение атома элемента, каждый из которых имеет положительно заряженное ядро, состоящее из протонов и нейтронов, а также вращающихся вокруг него отрицательно заряженных электронов. Число протонов и электронов численно совпадает и определяется в таблице по порядковому номеру элемента. Например, химический элемент сера имеет №16, следовательно, будет иметь 16 протонов и 16 электронов.
Чтобы определить количество нейтронов (нейтральных частиц, также расположенных в ядре) вычтите из относительной атомной массы элемента его порядковый номер. Например, железо имеет относительную атомную массу равную 56 и порядковый номер 26. Следовательно, 56 – 26 = 30 протонов у железа.
Например, железо имеет относительную атомную массу равную 56 и порядковый номер 26. Следовательно, 56 – 26 = 30 протонов у железа.
Электроны находятся на разном расстоянии от ядра, образуя электронные уровни. Чтобы определить число электронных (или энергетических) уровней, нужно посмотреть на номер периода, в котором располагается элемент. Например, алюминий находится в 3 периоде, следовательно, у него будет 3 уровня.
По номеру группы (но только для главной подгруппы) можно определить высшую валентность. Например, элементы первой группы главной подгруппы (литий, натрий, калий и т.д.) имеют валентность 1. Соответственно, элементы второй группы (бериллий, магний, кальций и т.д.) будут иметь валентность равную 2.
Также по таблице можно проанализировать свойства элементов. Слева направо металлические свойства ослабевают, а неметаллические усиливаются. Это хорошо видно на примере 2 периода: начинается щелочным металлом натрием, затем щелочноземельный металл магний, после него амфотерный элемент алюминий, затем неметаллы кремний, фосфор, сера и заканчивается период газообразными веществами – хлором и аргоном. В следующем периоде наблюдается аналогичная зависимость.
В следующем периоде наблюдается аналогичная зависимость.
Сверху вниз также наблюдается закономерность – металлические свойства усиливаются, а неметаллические ослабевают. То есть, например, цезий гораздо активнее по сравнению с натрием.
Fe (лат. Ferrum), химический элемент VIII группы периодической системы, атомный номер 26, атомная масса 55,847. Блестящий серебристо-белый металл. Образует полиморфные модификации; при обычной температуре устойчиво a – Fe (кристаллическая решетка кубическая объемноцентрированная) с плотностью 7,874 г./см?. a – Fe вплоть до 769°С (точка Кюри) ферромагнитно; tпл 1535°С.
На воздухе окисляется покрывается рыхлой ржавчиной. По распространенности элементов в природе железо находится на 4-м месте; образует ок. 300 минералов. На долю сплавов железа с углеродом и другими элементами приходится около 95% всей металлической продукции (чугун, сталь, ферросплавы). В чистом виде практически не используется (в быту железными часто называются стальные или чугунные изделия). Необходимо для жизнедеятельности животных организмов; входит в состав гемоглобина.
Необходимо для жизнедеятельности животных организмов; входит в состав гемоглобина.
Желемзо – элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д.И. Менделеева, с атомным номером 26. Обозначается символом Fe (лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия).
Простое вещество железо (CAS-номер: 7439-89-6) – ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро коррозирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе.
На самом деле железом обычно называют его сплавы с малым содержанием примесей (до 0,8%), которые сохраняют мягкость и пластичность чистого металла. Но на практике чаще применяются сплавы железа с углеродом: сталь (до 2,14 вес.% углерода) и чугун (более 2,14 вес.% углерода), а также нержавеющая (легированная) сталь с добавками легирующих металлов (хром, марганец, никель и др. ). Совокупность специфических свойств железа и его сплавов делают его «металлом №1» по важности для человека.
). Совокупность специфических свойств железа и его сплавов делают его «металлом №1» по важности для человека.
В природе железо редко встречается в чистом виде, чаще всего оно встречается в составе железо-никелевых метеоритов. Распространённость железа в земной коре – 4,65% (4-е место после O, Si, Al). Считается также, что железо составляет бомльшую часть земного ядра.
Железо в трудах ученых
O том, что древние люди пользовались вначале именно железом метеоритного происхождения, свидетельствуют и распространенные у некоторых народов мифы о богах или демонах, сбросивших с неба железные предметы и орудия, – плуги, топоры и пр.
Интересен также факт, что к моменту открытия Америки индейцы и эскимосы Северной Америки не были знакомы со способами получения железа из руд, но умели обрабатывать метеоритное железо.
В древности и в средние века семь известных тогда металлов сопоставляли с семью планетами, что символизировало связь между металлами и небесными телами и небесное происхождение металлов. Такое сопоставление стало обычным более 2000 лет назад и постоянно встречается в литературе вплоть до XIX в.
Такое сопоставление стало обычным более 2000 лет назад и постоянно встречается в литературе вплоть до XIX в.
Во II в. н.э. железо сопоставлялось с Меркурием и называлось меркурием, но позднее его стали сопоставлять с Марсом и называть марс (Mars), что, в частности, подчеркивало внешнее сходство красноватой окраски Марса с красными железными рудами.
Впрочем, некоторые народы не связывали название железа с небесным происхождением металла. Так, у славянских народов железо называется по «функциональному» признаку.
Русское железо (южнославянское зализо, польское zelaso, литовское gelesis и т.д.) имеет корень «лез» или «рез» (от слова лезо – лезвие). Такое словообразование прямо указывает на функцию предметов, изготовлявшихся из железа, – режущих инструментов и оружия.
Приставка «же», по-видимому, смягчение более древнего «зе» или «за»; она сохранилась в начальном виде у многих славянских народов (у чехов – zelezo).
Старые немецкие филологи – представители теории индоевропейского, или, как они его называли, индогерманского праязыка – стремились произвести славянские названия от немецких и санскритских корней.
Например, Фик сопоставляет слово железо с санскритским ghalgha (расплавленный металл, от ghal – пылать). Но вряд ли это соответствует действительности: ведь древним людям была недоступна плавка железа. С санскритским ghalgha скорее можно сопоставить греческое название меди, но не славянское слово железо.
Функциональный признак в названиях железа нашел отражение и в других языках. Так, на латинском языке наряду с обычным названием стали (chalybs), происходящим от наименования племени халибов, жившего на южном побережье Черного моря, употреблялось название acies, буквально обозначающее лезвие или острие.
Это, слово в точности соответствует древнегреческому, применявшемуся в том же самом смысле.
Упомянем в нескольких словах о происхождении немецкого и английского названий железа. Филологи обычно принимают, что немецкое слово Eisen имеет кельтское происхождение, так же как и английское Iron. В обоих терминах отражены кельтские названия рек (Isarno, Isarkos, Eisack), которые затем трансформировались) isarn, eisarn) и превратились в Eisen. Существуют, впрочем, и другие точки зрения.
Существуют, впрочем, и другие точки зрения.
Некоторые филологи производят немецкое Eisen от кельтского isara, означающего «крепкий, сильный». Существуют также теории, утверждающие, что Eisen происходит от ayas или aes (медь), а также от Eis (лед) и т.д. Староанглийское название железа (до 1150 г.) – iren; оно употреблялось наряду с isern и isen и перешло в средние века. Современное Iron вошло в употребление после 1630 г.
Заметим, что в «Алхимическом лексиконе» Руланда (1612) в качестве одного из старых названий железа приведено слово Iris, означающее «радуга» и созвучное Iron.
Ставшее международным, латинское название Ferrum принято у романских народов. Оно, вероятно, связано с греколатинским fars (быть твердым), которое происходит от санскритского bhars (твердеть). Возможно сопоставление и с ferreus, означающим у древних писателей «нечувствительный, непреклонный, крепкий, твердый, тяжкий», а также с ferre (носить). Алхимики наряду с Ferrum yпoтребляли и многие другие названия, например Iris, Sarsar, Phaulec, Mineraи др.
Железные изделия из метеоритного железа найдены в захоронениях, относящихся к очень давним временам (IV-V тысячелетиях до н.э.), в Египте и Месопотамии. Однако железный век в Египте начался лишь с ХIIв. до н.э., а в других странах еще позднее. В древнерусской литературе слово железо фигурирует в древнейших памятниках (с XI в.) под названиями желъзо, железо, железо.
МЕТАЛЛЫ ПОБОЧНЫХ ПОДГРУПП
Характеристика переходных элементов – меди, хрома, железа по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов.
Понятие переходный элемент обычно используется для обозначения любого из d- или f-элементов. Эти элементы занимают переходное положение между электроположительными s-элементами и электроотрицательными p-элементами. d-Элементы образуют три переходных ряда – в 4-м, 5-м и 6-м периодах соответственно. Первый переходный ряд включает 10 элементов, от скандия до цинка. Он характеризуется внутренней застройкой 3d-орбиталей. Хром и медь имеют на 4s-орбиталях всего по одному электрону. Дело в том, что полузаполненные или заполненные d-подоболочки обладают большей устойчивостью, чем частично заполненные. В атоме хрома на каждой из пяти 3d-орбиталей, образующих 3d-подоболочку, имеется по одному электрону. Такая подоболочка является полузаполненной. В атоме меди на каждой из пяти 3d-орбиталей находится по паре электронов (аналогичным образом объясняется аномалия серебра). Все d-элементы являются металлами. Большинство из них имеет характерный металлический блеск. По сравнению с s-металлами их прочность в целом значительно выше. В частности, для них характерны свойства: высокий предел прочности на разрыв; тягучесть; ковкость (их можно расплющить ударами в листы). d-элементы и их соединения обладают рядом характерных свойств: переменные состояния окисления; способность к обра зованию комплексных ионов; образование окрашенных соединений. d-Элементы характеризуются также более высокой плотностью по сравнению с другими металлами.
Хром и медь имеют на 4s-орбиталях всего по одному электрону. Дело в том, что полузаполненные или заполненные d-подоболочки обладают большей устойчивостью, чем частично заполненные. В атоме хрома на каждой из пяти 3d-орбиталей, образующих 3d-подоболочку, имеется по одному электрону. Такая подоболочка является полузаполненной. В атоме меди на каждой из пяти 3d-орбиталей находится по паре электронов (аналогичным образом объясняется аномалия серебра). Все d-элементы являются металлами. Большинство из них имеет характерный металлический блеск. По сравнению с s-металлами их прочность в целом значительно выше. В частности, для них характерны свойства: высокий предел прочности на разрыв; тягучесть; ковкость (их можно расплющить ударами в листы). d-элементы и их соединения обладают рядом характерных свойств: переменные состояния окисления; способность к обра зованию комплексных ионов; образование окрашенных соединений. d-Элементы характеризуются также более высокой плотностью по сравнению с другими металлами. Это объясняется сравнительно малыми радиусами их атомов. Атомные радиусы этих металлов мало изменяются в этом ряду. d-Элементы – хорошие проводники электрического тока, особенно те из них, в атомах которых имеется только один внешний s-электрон сверх полузаполненной или заполненной d-оболочки. Например, медь.
Это объясняется сравнительно малыми радиусами их атомов. Атомные радиусы этих металлов мало изменяются в этом ряду. d-Элементы – хорошие проводники электрического тока, особенно те из них, в атомах которых имеется только один внешний s-электрон сверх полузаполненной или заполненной d-оболочки. Например, медь.
Химические свойства .
Электроотрицательность металлов первого переходного ряда возрастают в направлении от хрома к цинку. Это означает, что металлические свойства элементов первого переходного ряда постепенно ослабевают в указанном направлении. Такое изменение их свойств проявляется и в последовательном возрастании окислительно-восстановительных потенциалов с переходом от отрицательных к положительным значениям.
Характеристика хрома и его соединений
Хром – твердый, голубовато-белый металл.ρ = 7,2г/см 3 , t плавл = 1857 0 С СО: +1,+2,+3,+4,+5,+6
Химические свойства.
- При обычных условиях хром реагирует только со фтором.
 При высоких температурах (выше 600 0 C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором.
При высоких температурах (выше 600 0 C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором.4Cr + 3O 2 2Cr 2 O 3
2Cr + 3Cl 2 2CrCl 3
2Cr + 3S Cr 2 S 3
- В раскалённом состоянии реагирует с парами воды:
2Cr + 3H 2 O Cr 2 O 3 + 3H 2
- Хром растворяется в разбавленных сильных кислотах (HCl, H 2 SO 4). В отсутствии воздуха образуются соли Cr 2+ , а на воздухе – соли Cr 3+ .
Cr + 2HCl → CrCl 2 + H 2 –
2Cr + 6HCl + O 2 → 2CrCl 3 + 2H 2 O + H 2 –
- Наличие защитной окисной плёнки на поверхности металла объясняет его пассивность по отношению к холодным концентрированным кислотам – окислителям. Однако при сильном нагревании эти кислоты растворяют хром:
2 Сr + 6 Н 2 SО 4 (конц) Сr 2 (SО 4) 3 + 3 SО 2 + 6 Н 2 О
Сr + 6 НNО 3 (конц) Сr(NО 3) 3 + 3 NO 2 + 3 Н 2 О
Получение.
Соединения хрома
Соединения двухвалентного хрома
Оксид хрома (II ) CrO
Физические свойства: твердое нерастворимое в воде вещество ярко-красного или коричнево- красного цвета. Химические свойства. CrO – основной оксид.
Химические свойства. CrO – основной оксид.
Получение.
Cr 2 O 3 + 3Н 2 2Cr + 3H 2 O Гидроксид хрома (II ) Сr(ОН) 2 Физические свойства: твердое нерастворимое в воде вещество желтого цвета . Химические свойства. Сr(ОН) 2 – слабое основание.
- Взаимодействует с кислотами: Cr(OH) 2 + 2HCl → CrCl 2 + 2H 2 O Легко окисляется в присутствии влаги кислородом воздуха в Сr(ОН) 3:
4Cr(OH) 2 + O 2 + 2H 2 O → 4Cr(OH) 3
- При прокаливании разлагается:
а) без доступа воздуха: Сr(ОН) 2 CrO + H 2 O б) в присутствии кислорода: 4Сr(ОН) 2 2 Cr 2 O 3 + 4H 2 O Получение.
- Действием щелочи на растворы солей Cr(II): СrСl 2 + 2 NaОН = Сr(ОН) 2 ↓ + 2 NaСl.
Соединения трёхвалентного хрома
Оксид хрома (III ) Cr 2 O 3 Физические свойства: темно-зеленое тугоплавкое вещество, нерастворимое в воде. Химические свойства. Cr 2 O 3 – амфотерный оксид.
Химические свойства. Cr 2 O 3 – амфотерный оксид.
Хромит натрия
- При высокой температуре восстанавливается водородом, кальцием, углеродом до хрома:
Cr 2 O 3 + 3Н 2 2Cr + 3H 2 O
Получение.
Гидроксид хрома (III ) Cr (OH ) 3 Физические свойства: нерастворимое в воде вещество зелёного цвета. Химические свойства. Сr(ОН) 3 – амфотерный гидроксид
2Cr(OH) 3 + 3H 2 SO 4 →Cr 2 (SO 4) 3 + 6H 2 O
Cr(OH) 3 + KOH → KCrO 2 + 2H 2 O
(хромит калия) Получение.
- При действии щелочей на соли Сr 3+ выпадает студнеобразный осадок гидроксида хрома (III) зеленого цвета:
Сr 2 (SО 4) 3 + 6NaОН → 2 Сr(ОН) 3 ↓ + 3 Na 2 SО 4 ,
Соединения шестивалентного хрома
Оксид хрома (VI ) CrO 3 Физические свойства: твердое вещество темно-красного цвета, хорошо растворимое в воде.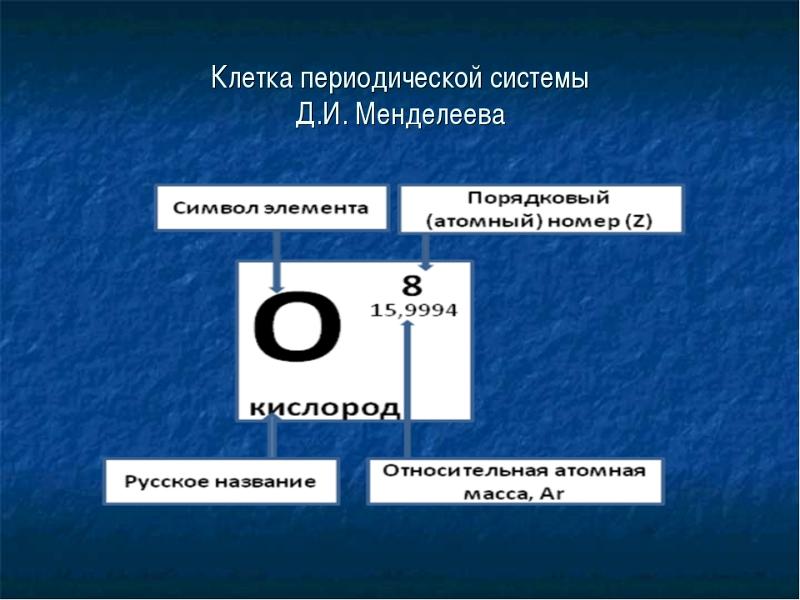 Ядовит! Химические свойства. CrO 3 – кислотный оксид.
Ядовит! Химические свойства. CrO 3 – кислотный оксид.
- Взаимодействует со щелочами, образуя соли желтого цвета-хроматы:
CrO 3 + 2KOH → K 2 CrO 4 + H 2 O
- Взаимодействует с водой, образуя кислоты: CrO 3 + H 2 O → H 2 CrO 4 хромовая кислота
2 CrO 3 + H 2 O → H 2 Cr 2 O 7 дихромовая кислота
- Термически неустойчив: 4 CrO 3 → 2Cr 2 O 3 + 3O 2
Получение.
- Получают из хромата (или дихромата) калия действием H 2 SO 4 (конц.).
K 2 CrO 4 + H 2 SO 4 → CrO 3 + K 2 SO 4 + H 2 O
K 2 Cr 2 O 7 + H 2 SO 4 → 2CrO 3 + K 2 SO 4 + H 2 O
Гидроксиды хрома (VI) H 2 CrO 4 – хромовая кислота , H 2 Cr 2 O 7 – дихромовая кислота Обе кислоты неустойчивы, при попытке их выделения в чистом виде распадаются на воду и оксид хрома (VI). Однако соли их вполне устойчивы. Соли хромовой кислоты называют хроматами, они окрашены в желтый цвет, а соли дихромовой кислоты – дихроматами, они окрашены в оранжевый цвет.
Однако соли их вполне устойчивы. Соли хромовой кислоты называют хроматами, они окрашены в желтый цвет, а соли дихромовой кислоты – дихроматами, они окрашены в оранжевый цвет.
Железо и его соединения
Железо – сравнительно мягкий ковкий металл серебристого цвета, пластичный, намагничивается. T плавл =1539 0 С. ρ = 7,87г/см 3 . СО: +2 – со слабыми окислителями – растворы кислот, солей, неметаллы, кроме кислорода и галогенов +3 – с сильными окислителями – концентрированные кислоты, кислород, галогены.
Химические свойства.
- Горит в кислороде, образуя окалину – оксид железа (II,III): 3Fe + 2O 2 → Fe 3 O 4 Железо реагирует с неметаллами при нагревании:
- При высокой температуре (700–900C) железо реагирует с парами воды:
3Fe + 4H 2 O Fe 3 O 4 + 4H 2 –
- На воздухе в присутствии влаги ржавеет: 4Fе + 3O 2 + 6Н 2 О → 4Fе(ОН) 3 . Железо легко растворяется в соляной и разбавленной серной кислотах, проявляя СО +2:
Fe + 2HCl → FeCl 2 + H 2 –
Fe + H 2 SO 4 (разб. ) → FeSO 4 + H 2 –
) → FeSO 4 + H 2 –
- В концентрированных кислотах–окислителях железо растворяется только при нагревании, проявляя СО +3:
2Fe + 6H 2 SO 4 (конц.) Fe 2 (SO 4) 3 + 3SO 2 – + 6H 2 O
Fe + 6HNO 3 (конц.) Fe(NO 3) 3 + 3NO 2 – + 3H 2 O
(на холоде концентрированные азотная и серная кислоты пассивируют железо).
- Железо вытесняет металлы, стоящие правее его в ряду напряжений из растворов их солей.
Fe + CuSO 4 → FeSO 4 + Cu↓
Получение.
- Восстановлением из оксидов углём или оксидом углерода (II)
Fe 2 O 3 + 3CO 2Fe + 3CO 2
Соединения двухвалентного железа
О ксид железа (II ) FeOФизические свойства: твердое вещество черного цвета, нерастворимое в воде. Химические свойства: FeО – основной оксид 6 FeО + O 2 2Fe 3 О 4
- Восстанавливается водородом, углеродом, оксидом углерода(II) до железа:
Получение. Fe 3 О 4 + H 2 – 3 FeО + H 2 O
Fe 3 О 4 + H 2 – 3 FeО + H 2 O
Гидроксид железа (II ) Fe (OH ) 2
Физические свойства: порошок белого цвета, нерастворимый в воде. Химические свойства: Fe(OH) 2 – слабое основание. Получение.
- Образуется при действии растворов щелочей на соли железа (II) без доступа воздуха:
FeCl 2 + 2KOH → 2KCl + Fе(OH) 2 ↓
Качественная реакция на Fe 2+
При действии гексацианоферрата (III) калия K 3 (красной кровяной соли) на растворы солей двухвалентного железа образуется синий осадок (турнбулева синь):
3FeSO 4 + 2K 3 Fe 3 2 + 3K 2 SO 4
Соединения трёхвалентного железа
Оксид железа (III ) Fe 2 O 3Физические свойства: твердое вещество красно-коричневого цвета. Химические свойства: Fe 2 O 3 – амфотерный оксид. феррит натрия Fe 2 О 3 + 3H 2 – 2 Fe + 3H 2 O Получение.
Химические свойства: Fe 2 O 3 – амфотерный оксид. феррит натрия Fe 2 О 3 + 3H 2 – 2 Fe + 3H 2 O Получение.
Физические свойства: твердое вещество красно-бурого цвета. Химические свойства: Fe(OH) 3 – амфотерный гидроксид.
- Взаимодействует с кислотами, как нерастворимое основание:
2Fe(OH) 3 + 3H 2 SO 4 →Fe 2 (SO 4) 3 + 6H 2 O
- Взаимодействует со щелочами, как нерастворимая кислота:
Fe(OH) 3 + KOH (тв) → KFeO 2 + 2H 2 O
Fе(ОН) 3 + 3КОН (конц) → К 3
Получение.
- Образуется при действии растворов щелочей на соли трёхвалентного железа: выпадает в виде красно–бурого осадка:
Fe(NO 3) 3 + 3KOH Fe(OH) 3 + 3KNO 3
Качественные реакции на Fe 3+- При действии гексацианоферрата (II) калия K 4 (жёлтой кровяной соли) на растворы солей трёхвалентного железа образуется синий осадок (берлинская лазурь):
4FeCl 3 +3K 4 Fe 4 3 + 12KCl
- При добавлении к раствору, содержащему ионы Fe 3+ роданистого калия или аммония появляется интенсивная кроваво-красная окраска роданида железа(III):
FeCl 3 + 3KCNS 3КCl + Fe(CNS) 3
Медь и её соединения
Медь – довольно мягкий металл красно-желтого цвета, ковкий, пластичный, обладает высокой тепло- и электропроводностью. T плавл = 1083 0 С. ρ = 8,96г/см 3 . СО: 0,+1,+2
T плавл = 1083 0 С. ρ = 8,96г/см 3 . СО: 0,+1,+2
Химические свойства.
- Взаимодействие с простыми веществами.
- Взаимодействие со сложными веществами.
Медь стоит в ряду напряжений правее водорода, поэтому не реагирует с разбавленными соляной и серной кислотами, но растворяется в кислотах – окислителях:
3Cu + 8HNO 3 (разб.) → 3Cu(NO 3) 2 + 2NO- + 2H 2 O
Cu + 4HNO 3 (конц.) → Cu(NO 3) 2 + 2NO 2 -+ 2H 2 O
Cu + 2H 2 SO 4 (конц.) → CuSO 4 + SO 2 -+2H 2 O
Получение .
CuO + CO Cu + CO 2
- При электролизе солей меди: 2CuSO 4 + 2H 2 O → 2 Cu + O 2 – + 2H 2 SO 4
Соединения одновалентной меди
Оксид меди(I ) С u 2 O Физические свойства: твердое вещество красного цвета, нерастворимое в воде. Химические свойства: Сu 2 O – основной оксид. Получение.
- Получают восстановлением соединений меди (II), например, глюкозой в щелочной среде:
2CuSO 4 + C 6 H 12 O 6 + 5NaOH → Cu 2 O↓ + 2Na 2 SO 4 + C 6 H 11 O 7 Na + 3H 2 O Гидроксид меди(I ) CuOH Физические свойства: неустойчивое, плохо растворимое в воде вещество желтого цвета, в свободном состоянии не выделен. Химические свойства: CuOH – слабое основание.
Химические свойства: CuOH – слабое основание.
- Взаимодействует с кислотами: CuOH + HCl → CuCl + H 2 O На воздухе легко окисляется до Cu(OH) 2: 4CuOH + О 2 + 2H 2 O → 4 Cu(OH) 2
Получение.
Соединения двухвалентной меди
Железо (символ Fe) − химический элемент восьмой группы, четвертого периода. Железо в периодической системе химических элементов расположено под номером 26.
В подгруппе Железа содержится 4 элемента: Fe железо, рутений Ru, осмий Os, Hs хасмий.
Характеристика химического элемента Железо
Ferrum – латинское слово, оно означает не только железо, а также твёрдость и оружие. От него произошли названия железа и в некоторых европейских языках: французском fer, итальянском ferro, испанском hierro и такие термины, как ферриты, ферромагнетизм. Похожие названия этого металла в славянских и балтийских языка: литовском gelezis, польском zelazo, болгарском желязо, украинском залiзо и белорусском жалеза. Английское название Iron, немецкое Eisen, голландское ijzer имеют происхождение от санскритского isira (крепкий, сильный).
Английское название Iron, немецкое Eisen, голландское ijzer имеют происхождение от санскритского isira (крепкий, сильный).
Распространение Железа в природе
Железо 26 элемент таблицы Менделеева
Железо – первый на земном шаре и второй по распространённости металл в земной коре, очень важный металл для человека. Ещё с незапамятных времён люди встречали железо в виде железных метеоритов. Обычно в метеоритном железе содержится от 5 до 30 % никеля, почти 0,5 % кобальта и до 1 % других элементов. На территории Африки 80 тысяч лет назад упал самый крупный метеорит Гоба, он весил 66 тонн. Он содержит 84 % железа и 16 % никеля. В метеоритном музее Российской академии наук, хранятся два осколка железного метеорита, которые весят 256 кг, упавшего на Дальнем Востоке. В 1947 г. в Приморском крае на площади 35 км 2 «железным дождём» выпали тысячи осколков (массой от 60 до 100 тонн) железного метеорита. Очень редкий минерал – самородное железо земного происхождения, встречается в виде мелких зёрен и содержит 2% никеля и десятые доли процента других металлов. На Луне было найдено самородное железо в раздробленном состоянии.
На Луне было найдено самородное железо в раздробленном состоянии.
В 13- 12 веках до н.э. происходит распад и смена культур на всём пространстве Евразии от Атлантики до Тихого океана, и в течение нескольких веков – до 10-8 веков до н.э. происходят переселения народов. Этот период получил название катастрофы бронзового века и начало перехода к железному веку.
Железа в земной коре очень много, но добывать его тяжело. Этот металл прочно связан в рудах с кислородом, а иногда с серой. Древние печи не могли дать нужной температуры, при которой плавится чистое железо и получалось железо в виде губки с примесями из руды, называемой крицей. При ковке крицы, железо частично отделялось от руды.
Во многих минералах содержится железо. Магнитный железняк, содержащий 72,3% железа – самый богатый железом минерал. Древнегреческий философ Фалес Милетский более 2500 лет назад изучил образцы чёрного металла, которые притягивают железо. Дал ему название magnetis lithos – камень из Магнесии, так произошло название магнита. Теперь известно, что это был магнитный железняк – чёрный оксид железа.
Теперь известно, что это был магнитный железняк – чёрный оксид железа.
Роль Железа в живом организме
Важнейшей рудой железа является гематит. Он содержит 69,9% железа. Гематит ещё называют красный железняк, а старинное название – кровавик. От греческого haima, что означает кровь. Появились и другие слова, связанные с кровью, такие как гемоглобин. Гемоглобин служит переносчиком кислорода от органов дыхания к тканям организма, а в обратном направлении переносит диоксид углерода. Недостаток железа в организме приводит к тяжёлому заболеванию – железодефицитной анемии . При этом заболевании происходят нарушения скелета, функции центральной нервной и сосудистой систем , наблюдается недостаток кислорода в тканях. Железо необходимо живым организмам. Оно содержится также в мышцах, селезёнке и печени. У взрослого человека железа около 4 г, оно присутствует в каждой клетке организма. Человек каждый день с пищей должен получать 15 миллиграммов железа. При недостатке железа врачи назначают специальные препараты, в которых железо находится в легко усвояемом виде.
Применение Железа
Если в выплавляемом железе больше 2% углерода, то получается чугун, его плавят на сотни градусов ниже, чем чистое железо. Так как чугун хрупкий, из него можно только отливать различные изделия, ковать его нельзя. Из железной руды в доменных печах выплавляют большое количество чугуна, который используют для отливки памятников, решёток и тяжёлых станин для станков. Основную массу чугуна перерабатывают в сталь. Для этого в конвертерах или в мартеновских печах из чугуна «выжигают» часть углерода и других примесей.
Из стали с разным содержанием углерода сделаны все предметы от рельсов до гвоздей. Если в железе мало углерода, получается мягкая низкоуглеродистая сталь, а вводя в сталь легирующие примеси других элементов, получаются разные сорта специальных сталей. Известно огромное множество сталей и каждая имеет своё применение.
Самая известная – нержавеющая сталь, которая содержит никель и хром. Из этой стали делают аппаратуру для химических заводов и столовую посуду. А если в сталь ввести 18% вольфрама, 1% ванадия и 4% хрома, получится быстрорежущая сталь, из неё делают свёрла и наконечники резцов. Если сплавить железо с 1,5% углерода и 15% марганца, получается такая твёрдая сталь, из которой делают ножи бульдозеров и зубья экскаваторов. Сталь содержащая 36% никеля, 0,5 % углерода и 0,5% марганца называется инваром, из неё делают точные приборы и некоторые детали для часов. Сталь, которую называют платинитом, содержит 46% никеля и 15% углерода расширяется при нагревании так же как и стекло. Спай платинита со стеклом не растрескивается и поэтому его используют при изготовлении электрических ламп.
А если в сталь ввести 18% вольфрама, 1% ванадия и 4% хрома, получится быстрорежущая сталь, из неё делают свёрла и наконечники резцов. Если сплавить железо с 1,5% углерода и 15% марганца, получается такая твёрдая сталь, из которой делают ножи бульдозеров и зубья экскаваторов. Сталь содержащая 36% никеля, 0,5 % углерода и 0,5% марганца называется инваром, из неё делают точные приборы и некоторые детали для часов. Сталь, которую называют платинитом, содержит 46% никеля и 15% углерода расширяется при нагревании так же как и стекло. Спай платинита со стеклом не растрескивается и поэтому его используют при изготовлении электрических ламп.
Нержавеющая сталь не намагничивается и к магниту не притягивается. Намагнитить можно только углеродистую сталь. Чистое железо само не намагничивается, а притягивается магнитом, такое железо подходит для изготовления сердечников электромагнитов.
В мире ежегодно выплавляется более миллиарда тонн железа. Но коррозия, которая является страшным врагом металла, не только уничтожает сам металл, на выплавку которого были затрачены огромные усилия , ещё и выводит из строя готовые изделия, которые стоят дороже самого металла. Она ежегодно уничтожает десятки миллионов тонн выплавляемого металла. Железо при коррозии реагирует с кислородом и водой, превращаясь в ржавчину.
Она ежегодно уничтожает десятки миллионов тонн выплавляемого металла. Железо при коррозии реагирует с кислородом и водой, превращаясь в ржавчину.
Железо, его положение в периодической системе химических элементов Д. И. Менделеева, взаимодействие с серой, хлороводородной кислотой, растворами солей.
ПЛАН ОТВЕТА:
положение в п. с. и строение атома физические свойства химические свойства Химический элемент железо находится в 4-ом периоде 8-ой группе побочной подгруппе. В атоме железа четыре электронных слоя. Электронами заполняется d–подуровень третьего слоя, на нём находится 6 электронов, а на четвёртом слое s–подуровне находится 2 электрона. В соединениях железо проявляет степени окисления +2 и +3.
| IV период VIII группа побочная подгруппа | Fe)))) | +2 | +3 | ||
| +26 2 8 8+6 2 | 4s | ?? | |||
| 3d | ?? | ? | ? | ? | ? |
Простое вещество железо – серебристо-белый металл с температурой плавления 15390С, плотностью 7,87 г/см3, обладает магнитными свойствами. Железо – химически активный металл. При нагревании оно взаимодействует с серой с образованием сульфида железа(II): Fe0 + S0 = Fe+2S-2. Железо вытесняет водород из растворов кислот, при этом образуются соли железа(II), например, при действии на железо соляной кислоты образуется хлорид железа(II): Fe0 + 2H+1Cl-1 = Fe+2Cl2-1 + h30. Железо может вытеснять менее активные металлы из растворов их солей, например, при действии железа на раствор сульфата меди(II) образуются металлическая медь и сульфат железа(II): Fe0 + Cu+2SO4 = Cu0 + Fe+2SO4.
Железо – химически активный металл. При нагревании оно взаимодействует с серой с образованием сульфида железа(II): Fe0 + S0 = Fe+2S-2. Железо вытесняет водород из растворов кислот, при этом образуются соли железа(II), например, при действии на железо соляной кислоты образуется хлорид железа(II): Fe0 + 2H+1Cl-1 = Fe+2Cl2-1 + h30. Железо может вытеснять менее активные металлы из растворов их солей, например, при действии железа на раствор сульфата меди(II) образуются металлическая медь и сульфат железа(II): Fe0 + Cu+2SO4 = Cu0 + Fe+2SO4.
Во всех реакциях железо проявляет свойства восстановителя. Более сильные окислители – хлор, кислород, концентрированные кислоты – окисляют железо до степени окисления +3.
Если домашнее задание на тему: » Железо, его положение в периодической системе химических элементов Д И Менделеева, взаимодействие оказалось вам полезным, то мы будем вам признательны, если вы разместите ссылку на эту сообщение у себя на страничке в вашей социальной сети.
Соединения железа – свойства, валентность железа в реакциях с веществами
Железо (Fe) — это один из наиболее распространенных химических элементов. Соединения железа массово используются в химической промышленности, народном хозяйстве. Сплавы железа с другими элементами стали основой большинства строительных материалов или деталей автомобилей и другой техники.
Но о применении железа поговорим позже. Сначала обозначим характеристики этого необыкновенного элемента.
Содержание
- Fe — строение, признаки, расположение в таблице Менделеева
- Свойства Fe
- Физические свойства
- Химические свойства
- Соединения Fe (+2)
- Оксид железа II — FeO
- Гидроксид железа II — Fe(OH)2
- Соли Fe (+2): FeSO4, FeCl2
- Соль Мора — FeSO4*(Nh5)2SO4*6h3O
- Соединения Fe (+3)
- Оксид железа III — Fe2O3
- Гидроксид железа III — Fe(OH)3
- Соли Fe (+3): FeCl3, Fe2(SO4)3
- Соединения Fe (+2, +3)
- Оксид железа II, III — Fe3O4, железная окалина.
- Турнбулева синь или берлинская лазурь — KFe{Fe(CN)6}
- Оксид железа II, III — Fe3O4, железная окалина.
- Соединения Fe (+6)
- Ферраты: K2FeO4, Na2FeO4
- Органические вещества, содержащие Fe
- Применение Fe и его соединений
Fe — строение, признаки, расположение в таблице Менделеева
Железо (Fe) — элемент 8б группы 4 периода. Порядковый номер в периодической системе — 26. Отметим, что кобальт (Co) и никель (Ni), входящие в 8б группу таблицы Менделеева, включены в семейство железа. Строение электронной оболочки атома Fe таково:
1s22s22p63s23p63d64s2
Электронное строение атома данного элемента обусловливает характерные степени окисления: +2 и + 3. Железо также может находиться в степени +6. О некоторых исключениях и интересных веществах, где этот элемент проявляет необычные свойства, поговорим чуть позже.
Рис. 1. Характеристика железа
1. Характеристика железа
Свойства Fe
Перед тем, как начать ознакомление со всеми соединениями железа, необходимо иметь представление о его физических и химических свойствах. Нельзя сказать, чтобы химические способности данного элемента выделялись среди ему подобных, но физические свойства обусловливают его ценность и уникальность.
Важно! Этот химический элемент в немалом количестве содержится в горах. Огромные залежи располагаются на Урале, в Сибири и других регионах России. Богаты железными рудами Украина, Прибалтика и т.д.
Физические свойства
Железо — ковкий и довольно прочный металл серебристо-белого цвета. На воздухе поддается коррозии с появлением желто-оранжевого налета — ржавчины. В чистом кислороде железо горит, а в обычных условиях кристаллизуется. Если брать только чистое железо, то оно является мягким и пластичным.
Химические свойства
Fe является химически активным элементом и чаще всего играет роль восстановителя. Итак, рассмотрим основные химические взаимодействия различных веществ с данным элементом:
Итак, рассмотрим основные химические взаимодействия различных веществ с данным элементом:
- Железо с легкостью вступает в реакции с соляной и разбавленной серной кислотами, образуя на выходе водород и соответствующие соли.
- Также взаимодействует с концентрированной серной кислотой, но по иному механизму. Здесь происходит образование кислотного оксида, соли и воды.
- Удачно реагирует с разбавленной азотной кислотой, а в аналогичной кислоте высокой концентрации железо пассивируется. Оксидная пленка покрывает поверхность металла, вследствие чего замедляется процесс коррозии.

Теперь перейдем к детальному изучению способностей соединений железа.
Соединения Fe (+2)
Начнем с тех веществ, где железо проявляет наименьшую окислительную степень после нуля — + 2. Данную степень этот химический элемент способен проявлять в различных бинарных соединениях, а также в сложных и комплексных солях.
Оксид железа II — FeO
Получить его возможно, если восстанавливать с помощью водорода оксид железа III. В целом FeO можно считать амфотерным оксидом, но в нем больше преобладают основные свойства. Представляет собой черный порошок, который невозможно растворить в воде. Ценится за свое быстрое окисление и восстановление до изначального вещества.
Гидроксид железа II — Fe(OH)2
Данный гидроксид также имеет основный характер и легко растворяется в кислотах. Это соединение является белым осадком, получаемым при взаимодействиях солей железа и щелочей. Такие реакции должны проходить в бескислородной среде, иначе может образоваться другой гидроксид, о котором будем говорить далее. Fe(OH)2 способен к активному окислению на воздухе с получением соединений, где Fe находится в степени окисления +3.
Fe(OH)2 способен к активному окислению на воздухе с получением соединений, где Fe находится в степени окисления +3.
Соли Fe (+2): FeSO4, FeCl2
Соли данного элемента можно получить путем большого количества реакций. Большинство из них будут иметь светло-зеленоватую окраску в растворах. Превращаются в соли железа III, окисляясь на воздухе. При этом они имеют коричнево-бурую окраску. Также благодаря солям можно получить оксиды и гидроксиды, содержащие Fe.
Соль Мора — FeSO4*(Nh5)2SO4*6h3O
Это вещество широко распространено в фармацевтике и медицине. Применяется для поставки недостающего железа в организм человека. Также противодействует гниению в дереве и деревянных изделиях. Участвует в обнаружении соединений хрома и ванадия.
Соединения Fe (+3)
Крупная группа веществ, в которой содержится трехвалентное железо. Эти соединения отличаются по своим свойствам по сравнению с предыдущими. Рассмотрим их подробнее.
Оксид железа III — Fe2O3
Проявляет амфотерные качества, соответственно — реагирует с кислотами и щелочами, образуя при этом средние, комплексные и другие соли. В обычных условиях является кристаллическим порошком коричнево-красного цвета, нерастворимым в воде.
В обычных условиях является кристаллическим порошком коричнево-красного цвета, нерастворимым в воде.
Гидроксид железа III — Fe(OH)3
Так же, как и соответствующий ему оксид, проявляет амфотерные свойства. Имеет темно-коричневый цвет. Получают вещество в ходе реакций щелочей с солями трехвалентного железа. В результате образуется бурый, темноватый осадок — Fe(OH)3. Если это основание прокалить, то получим Fe2O3.
Соли Fe (+3): FeCl3, Fe2(SO4)3
Растворы солей трехвалентного железа имеют желтый окрас и являются слабыми окислителями. При воздействии восстановителей переходят в те вещества, где железо имеет степень окисления +2.
Важно! Солей данного типа открыто достаточно много, и все они используются в промышленных, медицинских отраслях, а также в повседневной жизни.
Соединения Fe (+2, +3)
В некоторых веществах этот химический элемент имеет целых две степени окисления. Подробнее изучим сами соединения и их свойства.
Оксид железа II, III — Fe3O4, железная окалина.
Данное вещество является смесью двух оксидов железа: II и III. Железо не может быть в степени +4, поэтому такое соединение записывается как: FeO*Fe2O3. Получают данный оксид путем взаимодействия железа с водой и кислородом, которое проходит при наличии высокой температуры.
Турнбулева синь или берлинская лазурь — KFe{Fe(CN)6}
Это необычное соединение является осадком темного и чуть синеватого цвета, получаемым в ходе реакции между FeSO4 и красной кровяной солью. Здесь один атом Fe имеет степень окисления +2, а другой — +3. Чтобы обнаружить ионы трехвалентного железа, применяют желтую кровяную соль K4{Fe(CN)6}.
Рис. 2. Железо и его соединения
Соединения Fe (+6)
Химические вещества, где окислительная степень железа равна +6, называются ферратами.
Ферраты: K2FeO4, Na2FeO4
Ферраты являются мощными восстановителями и сходными по всем остальным способностям. Немаловажным является наличие в них бактерицидных способностей. Это обусловливает их ценность в качестве средств, обеззараживающих воду в крупных количествах.
Немаловажным является наличие в них бактерицидных способностей. Это обусловливает их ценность в качестве средств, обеззараживающих воду в крупных количествах.
Органические вещества, содержащие Fe
Железо и его свойства крайне важны и полезны в повседневной жизни людей, хозяйственной и промышленной деятельности. Но еще соединения железа выполняют значимые функции в теле человека. Чаще всего биологическую роль выполняют именно органические вещества, содержащие Fe. Пожалуй, самым важным веществом в теле человека, содержащим железо, является гемоглобин. Гемоглобин является белком, который осуществляет транспортировку кислорода по крови и обеспечивает постоянный газообмен. Fe входит в состав многих ферментов и белков нашего тела. Этот элемент также влияет и на наш иммунитет. Не зря при нехватке железа человек чувствует себя уставшим и сонным. При снижении концентрации Fe повышается вероятность заражения инфекционными заболеваниями. Поэтому важно следить за тем, чтобы в рационе было достаточно продуктов, содержащих железо — бобы, крупы, орехи, сухофрукты, морская капуста.
Применение Fe и его соединений
В конце стоит сказать и о неизмеримом вкладе Fe в современную жизнь и ее сферы. В статье уже встречались строки об использовании железа в различных областях, но разберемся в этом вопросе подробнее:
- Вещества, включающие в себя Fe, широко применяются в хозяйственной деятельности. Повсеместно в качестве строительных материалов используются сплавы железа — чугун, стали и т.д. Ковкость и прочность делают Fe незаменимой деталью в громоздких и массивных сооружениях.
- Часто этот элемент применяют и в химической промышленности. Железо играет роль катализатора во многих реакциях органического и неорганического синтеза. Пириты (соединения железа и серы) применяют для выделения серы и ее производных.
- С помощью Fe2O3 производят краски, цемент, материалы, обладающие магнитными свойствами.
- Железный купорос используется в качестве защиты урожая от вредных насекомых, также он нашел применение и в гальванотехнике.

Предыдущая
ХимияТипы химических связей – структурные особенности молекул
Следующая
ХимияАлканы – химические и физические свойства
Железо и его характеристики
Онлайн калькуляторы
На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.
Справочник
Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!
Заказать решение
Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Общая характеристика железа
Железо – самый распространенный после алюминия металл на земном шаре: оно составляет 4% (масс. ) земной коры. Встречается железо в виде различных соединений: оксидов, сульфидов, силикатов. В свободном состоянии железо находят только в метеоритах.
) земной коры. Встречается железо в виде различных соединений: оксидов, сульфидов, силикатов. В свободном состоянии железо находят только в метеоритах.
К важнейшим рудам железа относятся магнитный железняк Fe3O4, красный железняк Fe2O3, бурый железняк 2Fe2O3×3H2O и шпатовый железняк FeCO3.
Железо – серебристый (рис. 1) пластичный металл. Оно хорошо поддается ковке, прокатке и другим видам механической обработки. Механические свойства железа сильно зависят от его чистоты – от содержания в нем даже весьма малых количеств других элементов.
Рис. 1. Железо. Внешний вид.
Атомная и молекулярная масса железа
Относительной молекулярная масса вещества (Mr) – это число, показывающее, во сколько раз масса данной молекулы больше 1/12 массы атома углерода, а относительная атомная масса элемента (Ar) — во сколько раз средняя масса атомов химического элемента больше 1/12 массы атома углерода.
Поскольку в свободном состоянии железо существует в виде одноатомных молекул Fe значения его атомной и молекулярной масс совпадают. Они равны 55,847.
Аллотропия и аллотропные модификации железа
Железо образует две кристаллические модификации: α-железо и γ-железо. Первая из них имеет кубическую объемноцентрированную решетку, вторая – кубическую гранецентрированную. α-Железо термодинамически устойчиво в двух интервалах температур: ниже 912oС и от 1394oС до температуры плавления. Температура плавления железа равна 1539 ± 5oС. Между 912oС и от 1394oС устойчиво γ-железо.
Температурные интервалы устойчивости α- и γ-железа обусловлены характером изменения энергии Гиббса обеих модификаций при изменении температуры. При температурах ниже 912oС и выше 1394oС энергия Гиббса α-железа меньше энергии Гиббса γ-железа, а в интервале 912 — 1394oС – больше.
Изотопы железа
Известно, что в природе железо может находиться в виде четырех стабильных изотопов 54Fe, 56Fe, 57Fe и 57Fe. Их массовые числа равны 54, 56, 57 и 58 соответственно. Ядро атома изотопа железа 54Fe содержит двадцать шесть протонов и двадцать восемь нейтронов, а остальные изотопы отличаются от него только числом нейтронов.
Их массовые числа равны 54, 56, 57 и 58 соответственно. Ядро атома изотопа железа 54Fe содержит двадцать шесть протонов и двадцать восемь нейтронов, а остальные изотопы отличаются от него только числом нейтронов.
Существуют искусственные изотопы железа с массовыми числами от 45-ти до 72-х, а также 6 изомерных состояний ядер. Наиболее долгоживущим среди вышеперечисленных изотопов является 60Fe с периодом полураспада равным 2,6 млн. лет.
Ионы железа
Электронная формула, демонстрирующая распределение по орбиталям электронов железа выглядит следующим образом:
1s22s22p63s23p63d64s2.
В результате химического взаимодействия железо отдает свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион:
Fe0 -2e → Fe2+;
Fe0 -3e → Fe3+.
Молекула и атом железа
В свободном состоянии железо существует в виде одноатомных молекул Fe. Приведем некоторые свойства, характеризующие атом и молекулу железа:
|
Энергия ионизации атома, эВ |
7,87 |
|
Относительная электроотрицательность |
1,83 |
|
Радиус атома, нм |
0,117 |
Сплавы железа
До XIX века из сплавов железа были известны в основном его сплавы с углеродом, получившие названия стали и чугуна. Однако в дальнейшем были созданы новые сплавы на основе железа, содержащие хром, никель и другие элементы. В настоящее время сплавы железа подразделяют на углеродистые стали, чугуны, легированные стали и стали с особыми свойствами.
В технике сплавы железа принято называть черными металлами, а их производство – черной металлургией.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
Железо (элемент) – факты, история, где оно встречается и как используется
Живая наука поддерживается аудиторией. Когда вы покупаете по ссылкам на нашем сайте, мы можем получать партнерскую комиссию. Вот почему вы можете доверять нам.
Железная руда окисляется или ржавеет при контакте с кислородом. (Изображение предоставлено: Денис Селиванов | Шаттерсток)От того, что является важнейшим строительным блоком стали до питания растений и переноса кислорода в кровь — железо всегда занято, помогая поддерживать жизнь на Земле.
Железо — хрупкое твердое вещество, относящееся к группе 8 Периодической таблицы элементов. Самый распространенный из всех металлов, в чистом виде быстро подвергается коррозии под воздействием влажного воздуха и высоких температур. Железо также является четвертым наиболее распространенным элементом в земной коре по весу, и считается, что большая часть ядра Земли состоит из железа. По данным Лос-Аламосской национальной лаборатории, помимо того, что он обычно встречается на Земле, его много на Солнце и в звездах. По данным лаборатории Джефферсона, железо имеет решающее значение для выживания живых организмов. В растениях он играет роль в производстве хлорофилла. У животных он является компонентом гемоглобина — белка в крови, который переносит кислород от легких к тканям организма.
Железо также является четвертым наиболее распространенным элементом в земной коре по весу, и считается, что большая часть ядра Земли состоит из железа. По данным Лос-Аламосской национальной лаборатории, помимо того, что он обычно встречается на Земле, его много на Солнце и в звездах. По данным лаборатории Джефферсона, железо имеет решающее значение для выживания живых организмов. В растениях он играет роль в производстве хлорофилла. У животных он является компонентом гемоглобина — белка в крови, который переносит кислород от легких к тканям организма.
По данным Королевского химического общества, девяносто процентов всех металлов, перерабатываемых в наши дни, составляет железо. Большая его часть используется для производства стали — сплава железа и углерода, которая, в свою очередь, используется в производстве и гражданском строительстве, например, для производства железобетона. Нержавеющая сталь, содержащая не менее 10,5% хрома, обладает высокой устойчивостью к коррозии. Он используется в кухонных столовых приборах, бытовой технике и посуде, такой как сковороды и сковороды из нержавеющей стали. Добавление других элементов может придать стали другие полезные качества. Например, никель повышает его прочность и делает более устойчивым к воздействию тепла и кислот; По данным Jefferson Lab, марганец делает его более прочным, а вольфрам помогает ему сохранять твердость при высоких температурах.
Добавление других элементов может придать стали другие полезные качества. Например, никель повышает его прочность и делает более устойчивым к воздействию тепла и кислот; По данным Jefferson Lab, марганец делает его более прочным, а вольфрам помогает ему сохранять твердость при высоких температурах.
Только факты
- Атомный номер (количество протонов в ядре): 26
- Символ атома (в Периодической таблице элементов): Fe
- Атомный вес (средняя масса атома): 55,845
- Плотность : 7,874 г на кубический сантиметр
- Фаза при комнатной температуре: Твердая
- Температура плавления: 2 800,4 градуса по Фаренгейту (1 538 градусов по Цельсию)
- Температура кипения: 5 181,8 F (2 861 C)
- разное количество нейтронов): (укажите, сколько стабильных изотопов): 33 Стабильные изотопы: 4
- Наиболее распространенные изотопы: железо-56 (естественное содержание: 91,754 процента)
По оценкам археологов, люди используют железо более 5000 лет, по данным лаборатории Джефферсона. На самом деле получается, что часть самого древнего железа, известного человеку, буквально упала с неба. В исследовании, опубликованном в 2013 году в Journal of Archeological Science, исследователи изучили древние египетские железные бусы, которые датируются примерно 3200 годом до нашей эры. и обнаружил, что они сделаны из железных метеоритов. По данным Национальной лаборатории Лос-Аламоса, в Ветхом Завете в Библии также несколько раз упоминается железо.
На самом деле получается, что часть самого древнего железа, известного человеку, буквально упала с неба. В исследовании, опубликованном в 2013 году в Journal of Archeological Science, исследователи изучили древние египетские железные бусы, которые датируются примерно 3200 годом до нашей эры. и обнаружил, что они сделаны из железных метеоритов. По данным Национальной лаборатории Лос-Аламоса, в Ветхом Завете в Библии также несколько раз упоминается железо.
Железо в основном получают из минералов гематита и магнетита. По данным Jefferson Lab, в меньших количествах его также можно получить из минералов таконита, лимонита и сидерита. По данным Лос-Аламосской национальной лаборатории, железо имеет четыре различные аллотропные формы, а это означает, что оно имеет четыре различные структурные формы, в которых атомы связываются по разным схемам. Эти формы называются ферритами, известными как альфа (магнитные), бета, гамма и омега.
Железо является важным питательным веществом в нашем рационе. Дефицит железа, наиболее распространенный дефицит питательных веществ, может вызывать анемию и усталость, которые влияют на способность выполнять физическую работу у взрослых. По данным Центров по контролю и профилактике заболеваний, это также может ухудшить память и другие психические функции у подростков. Центры по контролю и профилактике заболеваний предупреждают, что у женщин с дефицитом железа во время беременности повышен риск рождения маловесных и ранних детей.
Дефицит железа, наиболее распространенный дефицит питательных веществ, может вызывать анемию и усталость, которые влияют на способность выполнять физическую работу у взрослых. По данным Центров по контролю и профилактике заболеваний, это также может ухудшить память и другие психические функции у подростков. Центры по контролю и профилактике заболеваний предупреждают, что у женщин с дефицитом железа во время беременности повышен риск рождения маловесных и ранних детей.
Существует два типа пищевого железа: гемовое железо и негемовое железо. Гемовое железо, которое легче усваивается, содержится в мясе, рыбе и птице, тогда как негемовое железо, которое также усваивается, но в меньшей степени, чем гемовое, содержится в обеих растительных продуктах (таких как шпинат, капуста и брокколи) и мясо, по данным Американского Красного Креста. Люди усваивают до 30 процентов гемового железа по сравнению с 2-10 процентами негемового железа, сообщает ARC, добавляя, что продукты, богатые витамином С, такие как помидоры или цитрусовые, могут помочь людям усваивать негемовое железо.
Кто знал?
- Кровь имеет красный цвет из-за взаимодействия между железом и кислородом, по данным Калифорнийского университета в Санта-Барбаре. Кровь выглядит красной из-за того, как химические связи между двумя элементами отражают свет.
- Чистое железо на самом деле мягкое и податливое, по данным Университета Денвера.
- В 2007 году исследователи обнаружили огромный шлейф богатой железом воды, исходящий из гидротермальных источников в южной части Атлантического океана.
- Железо необходимо для роста фитопланктона — крошечных морских бактерий, которые используют углекислый газ из атмосферы для фотосинтеза. Поэтому некоторые исследователи утверждают, что удобрение океанов дополнительным железом может помочь поглотить избыток углекислого газа. Но исследование, опубликованное в Интернете в ноябре 2010 года в Proceedings of the National Academy of Sciences, показало, что это может быть не такой уж хорошей идеей, поскольку все это дополнительное железо может фактически вызвать рост токсинообразующих водорослей, которые способствуют загрязнению морской среды.
 дикая природа.
дикая природа. - По данным Королевского химического общества, около 90 процентов всех металлов, перерабатываемых сегодня, составляют железо.
- Согласно данным Лос-Аламосской национальной лаборатории, железо является важнейшим компонентом класса метеоритов, известного как сидериты.
- Согласно данным Лос-Аламосской национальной лаборатории, железный столб, датируемый примерно 400 годом нашей эры, до сих пор стоит в Дели, Индия. Столб имеет высоту около 23,75 футов (7,25 метра) и диаметр 15,75 дюймов (40 сантиметров). Несмотря на воздействие погодных условий, столб не подвергся сильной коррозии благодаря уникальному составу металлов.
- Примеры продуктов, богатых железом, включают мясо, такое как говядина, индейка, курица и свинина; морепродукты, такие как креветки, моллюски, устрицы и тунец; овощи, такие как шпинат, горох, брокколи, сладкий картофель и стручковая фасоль; хлеб и злаки, такие как отруби, цельнозерновой хлеб и обогащенный рис; другие продукты, такие как бобы, чечевица, томатная паста, тофу и патока, по данным американского Красного Креста.
- Поверхность Марса красная из-за большого количества оксида железа (ржавчины) на его поверхности, согласно Nature . В коре Марса в два раза больше оксида железа, чем на Земле.
- Твердое внутреннее и жидкое внешнее ядра Земли в основном состоят из железа (приблизительно 85 процентов и 80 процентов по весу соответственно). По данным НАСА, электрический ток, генерируемый жидким железом, создает магнитное поле, защищающее Землю. Железо также содержится в ядрах всех планет Солнечной системы.
- Согласно данным JPL, железо является самым тяжелым элементом, образующимся в ядрах звезд. Элементы тяжелее железа могут быть созданы только при взрыве звезд большой массы (сверхновых).
- Латинское название железа — ferrum, что является источником его атомного символа Fe.
- Слово «железо» происходит от англо-саксонского слова iren. Слово «железо», возможно, произошло от более ранних слов, означающих «священный металл», потому что оно использовалось для изготовления мечей, используемых в крестовых походах, согласно WebElements.
Текущие исследования
Железо было предметом многочисленных медицинских исследований, некоторые из которых показывают, что высокий уровень железа в крови может фактически быть связан с повышенным риском сердечно-сосудистых заболеваний. «Есть некоторые исследования, показывающие, что люди, у которых больше ферритина в системе крови и маркеров более высокого уровня железа в организме, могут быть более подвержены риску некоторых сердечно-сосудистых заболеваний», — сказала Джудит Уайли-Розетт, профессор кафедры эпидемиологии. и здоровье населения и медицинский факультет Медицинского колледжа Альберта Эйнштейна Университета Йешива в Нью-Йорке. «И является ли это причиной риска или биомаркером чего-то еще, неясно», — сказал Уайли-Розетт Live Science. (Ферритин — это тип белка, в котором хранится железо, а тест на ферритин измеряет количество железа в крови.)
В исследовании более 1900 финских мужчин в возрасте от 42 до 60 лет, опубликованном в 1992 году в журнале Circulation, исследователи обнаружили связь между высоким уровнем железа и повышенным риском сердечного приступа. В более позднем исследовании, опубликованном онлайн в январе 2014 года в Journal of Nutrition, исследователи обнаружили, что гемовое железо, содержащееся в мясе, увеличивает риск ишемической болезни сердца на 57 процентов, но такой связи между негемовым железом и риск ишемической болезни сердца.
В более позднем исследовании, опубликованном онлайн в январе 2014 года в Journal of Nutrition, исследователи обнаружили, что гемовое железо, содержащееся в мясе, увеличивает риск ишемической болезни сердца на 57 процентов, но такой связи между негемовым железом и риск ишемической болезни сердца.
Интересно, что недавние исследования также связывают накопление железа в мозге с болезнью Альцгеймера. В исследовании, опубликованном в августе 2013 года в Журнале болезни Альцгеймера, исследователи обнаружили, что количество железа в гиппокампе — области мозга, связанной с формированием воспоминаний, — было увеличено и связано с повреждением тканей в области гиппокампа у людей. с болезнью Альцгеймера, но не у здоровых пожилых людей.
«На накопление железа в мозге могут влиять модифицирующие факторы окружающей среды, такие как количество красного мяса и пищевых добавок с железом, которые мы потребляем, а также наличие у женщин гистерэктомии до менопаузы», — автор исследования доктор Джордж Барцокис, профессор. психиатрии Семельского института неврологии и поведения человека Калифорнийского университета в Лос-Анджелесе, говорится в заявлении.
психиатрии Семельского института неврологии и поведения человека Калифорнийского университета в Лос-Анджелесе, говорится в заявлении.
Дефицит железа также был связан с депрессией, согласно исследованию 2017 года, опубликованному в Журнале психиатрических исследований группой австралийских исследователей, которые пытались найти связь между генетикой, уровнем железа и депрессией, особенно у подростков. Исследователи обнаружили, что, хотя существует связь между уровнем железа в крови и степенью депрессии, нет никаких доказательств генетической связи между ними. Исследователи использовали данные, полученные в результате исследований близнецов, и рассмотрели множество факторов при сравнении близнецов-подростков со взрослыми близнецами. Связь между уровнем железа и депрессией чаще всего наблюдается в периоды времени, когда организму требуется большее количество железа, например, во время всплесков роста.
В статье 2017 года , опубликованной в Европейском журнале питания исследовательской группой из Ирана, описано исследование, в котором добавки железа давали новым матерям без анемии с послеродовой депрессией (ППД). Группа из 70 женщин начала двойное слепое исследование через неделю после родов, а через шесть недель сравнили симптомы ППД. В группе, принимавшей добавку железа, наблюдалось значительно большее улучшение симптомов ПРЛ, чем в группе, принимавшей плацебо.
Группа из 70 женщин начала двойное слепое исследование через неделю после родов, а через шесть недель сравнили симптомы ППД. В группе, принимавшей добавку железа, наблюдалось значительно большее улучшение симптомов ПРЛ, чем в группе, принимавшей плацебо.
Дополнительный отчет Рэйчел Росс, автора Live Science
Элемент железа, история, свойства, факты, использование, функция
Элемент железа
Железо — это химический элемент, серебристо-белый, блестящий, ковкий и пластичный металл группы 8 (VIIIB) периодической таблицы с символ Fe и атомный номер 26. Это самый удобный и дешевый металл, который используется человеческой цивилизацией намного позже, чем медь, серебро и золото.
При изучении химии химический элемент железо включается в семейство переходных металлов из-за наличия не полностью заполненных d-орбиталей в их атомарном или ионном состоянии.
Название происходит от древнеанглийского слова iren, а символ железа происходит от латинского слова Ferrum.
Физические и химические свойства
Физические свойства железа
Железо имеет четыре аллотропные кристаллические решетки,
- α-Fe (ферромагнитный ОЦК)
- β-Fe (парамагнитный ОЦК)
- γ-Fe (парамагнитный ГЦК)
- δ-Fe (ОЦК парамагнитный)
Это самое магнитное вещество среди всех элементов и умеренно химически активный металл в земной среде.
| Железо | |||
| Символ | Фе | ||
| Дискавери | около 3500 г. до н.э. | ||
| Название производное от | Англосаксонское название iren и символ железа происходит от латинского слова Ferrum 9.0130 | ||
| Обычный изотоп | 26 Fe 56 | ||
| Степени окисления | +6, +3 , +2 , 0, −2 | ||
| Номер CAS | 7439-89-6 | ||
| Периодические свойства | |||
| Атомный номер | 26 | ||
| Относительная атомная масса | 55. 845 845 | ||
| Электрон на ячейку | 2, 8, 14, 2 | ||
| Электронная конфигурация | [Ар] 3d 6 4s 2 | ||
| Блок | крестовина | ||
| Группа | 8 | ||
| Период | 4 | ||
| Физические свойства | |||
| Состояние при 20 °C | Твердый | ||
| Температура плавления | 1538 °С, 2800 °F, 1811 К | ||
| Температура кипения | 2861 °С, 5182 °F, 3134 К | ||
| Молярная теплоемкость | 25,10 Дж моль −1 К − 1 | ||
| Кристаллическая структура | объемно-центрированная кубическая (ОЦК) или гранецентрированная кубическая (ГЦК) | ||
| Плотность | 7,87 г/см 3 | ||
| Удельное электрическое сопротивление | 96,1 нОм·м | ||
| Атомные свойства | |||
| Атомный радиус (несвязанный) | 2,04 Å | ||
| Ковалентный радиус | 1,24 Å | ||
| Электроотрицательность | 1,83 (шкала Полинга) | ||
| Сродство к электрону | 14,569 кДж моль −1 | ||
| Энергия ионизации (кДж/моль) | 1-й | 2-й | 3-й |
| 762,47 | 1561,88 | 2957,47 | |
Химические свойства железа
Второй по распространенности металл, железо, имеет валентную электронную конфигурацию [Ar] 3d 6 4s 2 и общую степень окисления +2 и +3.
Железо в периодической таблице
Железо находится в группе 8 и периоде 4 периодической таблицы. Это переходный металл, который находится между марганцем и кобальтом.
История железа
Он участвовал в гонке человеческой цивилизации раньше меди, серебра и золота. Впервые его использовали наши предки около 4000 г. до н.э. Знания об извлечении железа из разных видов руд развивались в разных странах на протяжении длительного промежутка времени.
В Египте и Месопотамии процесс был обнаружен около 2000 г. до н.э. Ранние методы нагревания руды углем на ветреных участках давали губчатый металл, сформированный длительной ковкой. Техника изготовления металла хорошего качества была разработана с использованием печи.
В наше время хорошо развиты плавильные печи. Повышение механической прочности за счет производства стали из железной руды началось в девятнадцатом веке.
Где содержится железо?
Железо является вторым наиболее распространенным металлом после алюминия. Это четвертый по распространенности химический элемент после кислорода, кремния и алюминия в земной коре, встречающийся в количестве более 5 процентов или 50 000 частей на миллион.
Это четвертый по распространенности химический элемент после кислорода, кремния и алюминия в земной коре, встречающийся в количестве более 5 процентов или 50 000 частей на миллион.
В земной коре свободный металл встречается редко, земное железо в базальтовых породах встречается в Гренландии. Углеродистые отложения встречаются в США (штат Миссури).
Около 0,5 процента лунного грунта состоит из металлического железа, а это означает, что на поверхности Луны присутствует большое количество Fe.
Руды железа и их формула
Наиболее распространенные оксидные руды и минералы, встречающиеся в земной коре, могут включать:
- красный гематит (Fe 2 О 3 )
- коричневый гематит или лимонит (2F 2 O 3 , 3H 2 O)
- магнетит (Fe 2 O 3 ),
- сидерит (FeCO 3 )
- пирит (FeS 2 )
Пирит не может быть экономически выгодным для производства железа, поэтому пирит не считается железной рудой.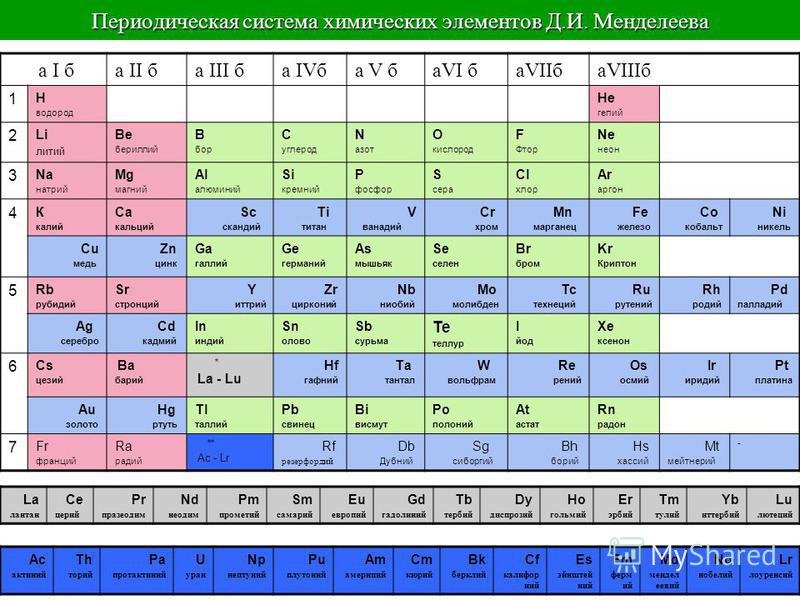
Руды находятся в разных странах, таких как Китай, Бразилия, Австралия, США и Индия.
Ежегодно в мире производится 1000 миллионов тонн железа. Производство нерафинированной стали после 1996 года в мире составляет около 700 миллионов тонн.
Изотопы
Железо встречается в природе в виде четырех стабильных изотопов, таких как 54 Fe (5,845 процента), 56 Fe (91,754 процента), 57 Fe (2,119 процента) и 57 58 Fe 90,15 процента (2,119 процента) .
Производственный процесс
Железо извлекается путем восстановления углерода в доменной печи.
- Руда, кокс и известняк (обычно в соотношении 8:4:1) поступают в верхнюю часть печи, в то время как струя предварительно нагретого воздуха при температуре около 900 °C проходит через отверстия в нижней части печи.
- При сжигании кокса выделяется тепло у основания с температурой около 2000 °C, которая постепенно падает к верхней части печи (400 °C).
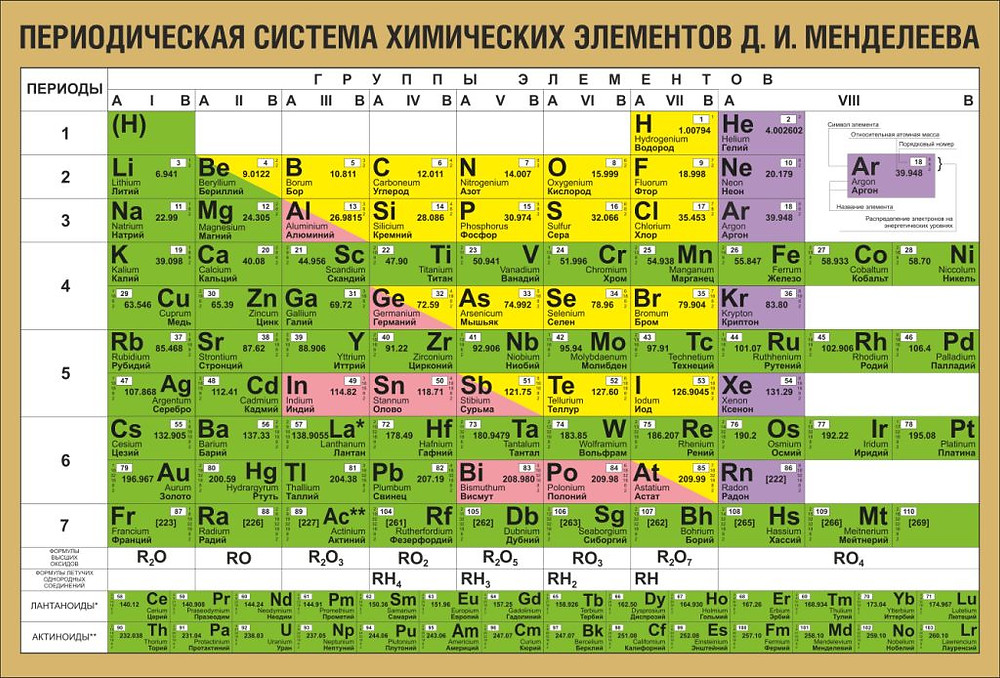
- При сжигании углерода при температуре выше 700 °C образуется монооксид углерода, который поднимается вверх и восстанавливает Fe 2 O 3 и FeO. Некоторое восстановление осуществляется углеродом.
- Известняк разлагается при температуре около 900 °C с образованием CaO, который соединяется с кремнеземом с образованием шлака (CaSiO 3 ).
Что такое чугун?
Расплавленный шлак и сырой металл собираются в основании доменной печи, где они образуют отдельные слои, а шлак плавает на расплавленном металле, предотвращая его окисление. Их заливают через отдельные отверстия и дают затвердеть в песчаной форме с образованием чугуна или чугуна, которые содержат такие примеси, как углерод, кремний, фосфор, сера и марганец.
Когда большая часть примесей, присутствующих в чугуне, удаляется, образуется чистая коммерческая форма металла, известная как кованое железо.
Интересные факты о железе
- Чистое железо – химически умеренно активный, серебристо-белый блестящий, ковкий, пластичный металл, самое магнитное вещество среди всех элементов таблицы Менделеева.
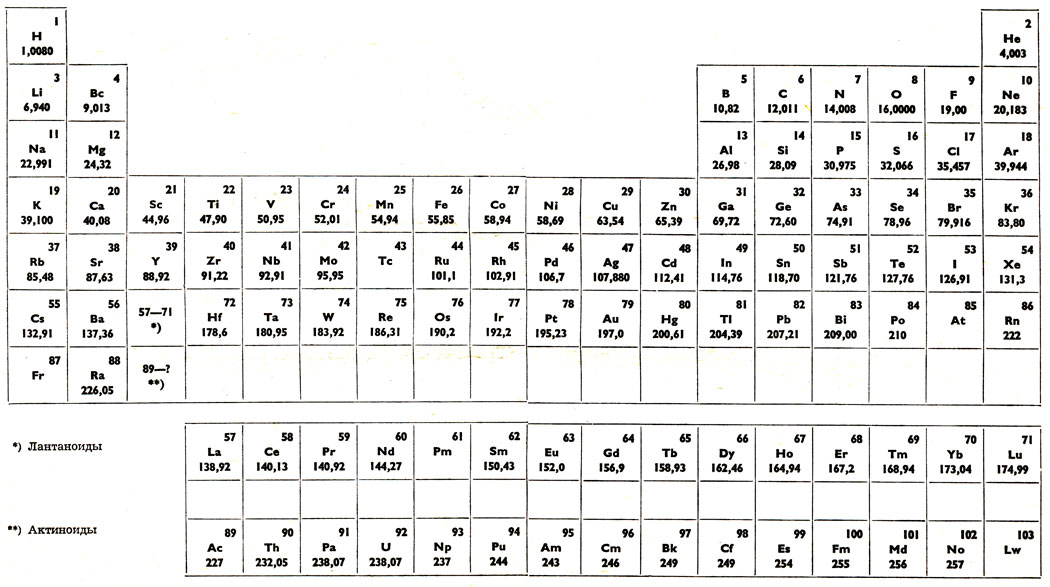
- Мелкодисперсный металл пирофорен на воздухе при комнатной температуре.
- Вода может вступать в реакцию при температуре выше 500 °C с выделением водорода и образованием Fe 2 O 3 и FeO.
- В нагретом мелкоизмельченном состоянии реагирует со всеми неметаллами (углеродом, кремнием, азотом, фосфором и водородом) с образованием твердых металлоподобных соединений Fe 3 C, Fe 3 Si, Fe 3 P, Fe 4 N, FeN или бинарные ионно-ковалентные соединения, такие как FeF 3 , FeCl 3 , FeS.
- Твердый кристаллический твердый карбид Fe 3 C (цементит) в основном отвечает за изменение свойств стали.
- В отсутствие кислорода железо реагирует с минеральными кислотами (серной, соляной или азотной кислотой) с образованием в растворе иона Fe(II).
- Разбавленные растворы щелочей и вода без воздуха почти не воздействуют на Fe, но горячие концентрированные гидроксиды щелочных металлов воздействуют на него.

Химические соединения
В химии железо обладает характерными свойствами переходных металлов с различными степенями окисления и различными типами координации и металлоорганическими химическими соединениями при различных типах химической связи.
Степени окисления +2 (железо) и +3 (железо) являются основными степенями окисления Fe с образованием большого количества соединений в химии.
В Fe (II) он образует простые соединения, такие как оксиды, галогениды (кроме йода ) и другие соли, а также большое количество сложных соединений. FeF 3 , FeCl 3 и FeBr 3 представляют собой галогениды Fe, образованные прямой реакцией металлов с соответствующими галогенами, такими как фтор, хлор и бром.
Fe (II) восстанавливается в природе с образованием большого количества простых и сложных соединений, достаточно стабильных в состоянии +2. Галогениды, нитраты, перхлораты и сульфаты растворимы в воде, а гидроксиды, карбонаты, фосфаты и оксалаты растворимы мало.
Встречается в высшей степени окисления в пурпурном феррате калия (KFeO 4 ) со степенью окисления +6, полученном окислением Fe (III) соляной кислотой.
Для чего используется железо?
Железо и сталь используются в основном в различных типах структурных единиц в современной цивилизации и гражданском строительстве. Существуют разные виды стали с разными свойствами и назначением, изготавливаемые из легированного железа с углеродом и другими химическими элементами.
- Мягкая сталь наиболее широко используется в мостах, опорах линий электропередач, велосипедных цепях, режущих инструментах и винтовочных стволах.
- Он также используется в качестве химического катализатора в процессе Габера для производства аммиака.
- В мелкосерийном производстве водорода используется в качестве восстановителя. Нержавеющая сталь
- — это важный сплав железа, который содержит не менее 12–15 процентов хрома и других металлов, таких как никель, молибден, титан и медь, которые устойчивы к коррозии и действию кислот.
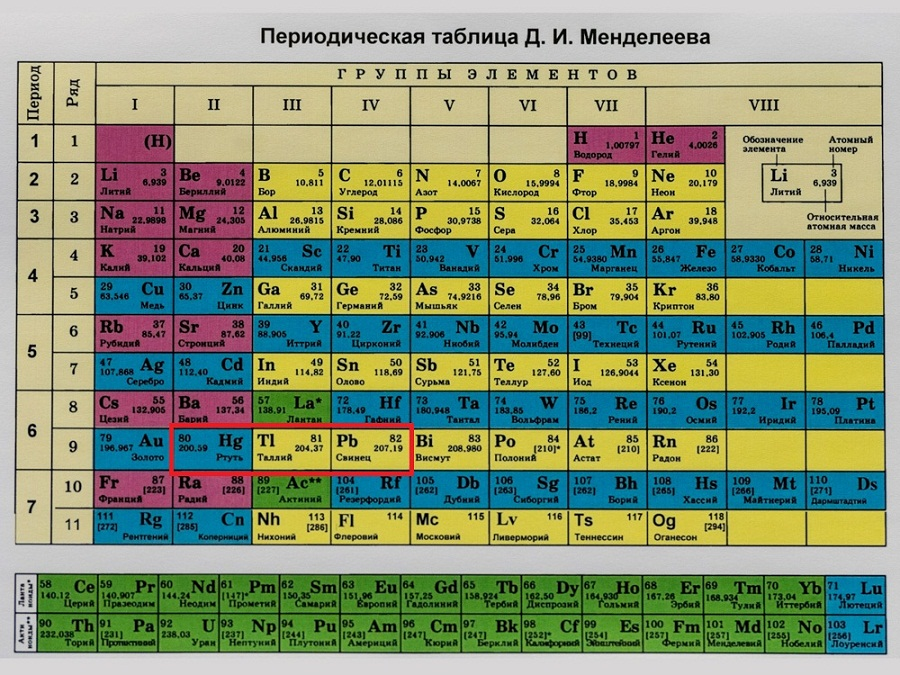 Он широко используется в архитектуре, подшипниках, столовых приборах, медицинских хирургических инструментах и ювелирных изделиях.
Он широко используется в архитектуре, подшипниках, столовых приборах, медицинских хирургических инструментах и ювелирных изделиях. - Чугун — еще один сплав, содержащий от 3 до 5 процентов углерода, широко используемый в трубах, клапанах, насосах и производстве магнитов.
Функция железа в организме
Это нетоксичный элемент, необходимый для всех форм жизни (растений и животных). Много ионов железа присутствует в гемоглобине крови, который переносит кислород от легких к клетке для дыхания организма.
Дефицит железа
Дефицит железа в организме человека вызывает анемию, которая является наиболее распространенным расстройством нейтрализации во всем мире, как в развитых, так и в слаборазвитых странах.
Хроническая кровопотеря, повторная беременность и инфаркт анкилостомы могут вызвать анемию в организме человека. Анемия характеризуется более низкой концентрацией железа в гемоглобине крови (<12 мг/л), что вызывает замедление роста, потерю аппетита, вялость метаболической активности и вялость или малоподвижность.
Железо – Энергетическое образование
Энергетическое образованиеМеню навигации
ИСТОЧНИКИ ЭНЕРГИИ
ИСПОЛЬЗОВАНИЕ ЭНЕРГИИ
ЭНЕРГЕТИЧЕСКОЕ ВОЗДЕЙСТВИЕ
ИНДЕКС
Поиск
Рис. 1. Железо с атомным номером 26 и атомным весом 55,845. [1]
Железо ( Fe ) является 26-м -м -м элементом в периодической таблице и используется людьми более 5000 лет. [1] Это один из самых распространенных металлов на Земле, составляющий 5,6% земной коры и почти все ядро Земли.
Некоторые полезные свойства железа включают: [1]
| Атомный вес | 55.845 |
| Плотность (при 0 o С) | 7,874 г/см 3 |
| Температура кипения | 3134 К |
| Температура плавления | 1811 К |
| Воплощенная энергия [2] | 20-25 МДж/кг |
Железо сыграло ключевую роль в истории человечества, поскольку те, кто мог использовать его для изготовления оружия, инструментов и других материалов, получали экономическую и политическую власть. [3] В современном обществе железо является самым важным из всех металлов, так как оно используется для изготовления различных типов стали, которая используется в самых разных областях. Сталь используется для изготовления скрепок, небоскребов и всего, что между ними. [1]
[3] В современном обществе железо является самым важным из всех металлов, так как оно используется для изготовления различных типов стали, которая используется в самых разных областях. Сталь используется для изготовления скрепок, небоскребов и всего, что между ними. [1]
Железо также является важным элементом в жизни растений и животных. У растений он играет роль в создании хлорофилла, а у человека играет решающую роль в сосудистой системе.
Энергетическое использование железа в обществе
Рисунок 2. Арматура, сокращение от «арматурный стержень», изготавливается из железа (не чистого железа, а его сплава, стали), используется для армирования бетона. [4]
Железо составляет 95% всего тоннажа металла, производимого в мире, при этом ежегодно производится более 500 миллионов тонн нового железа и 300 миллионов тонн переработанного железа. [5] Такой выпуск железа возможен благодаря огромным запасам железа на Земле, превышающим 100 миллиардов тонн. Большая часть добычи ведется в Китае, Бразилии, Австралии, России и Украине.
Большая часть добычи ведется в Китае, Бразилии, Австралии, России и Украине.
Около 18% мирового промышленного энергопотребления приходится на добычу, переработку и производство изделий из железа и стали. [6] С точки зрения фактической энергии, он использует около 19 из 106 эксаджоулей (10 19 джоулей), вводимых в промышленный сектор каждый год.
Железо имеет воплощенную энергию 20-25 мегаджоулей на килограмм (МДж/кг), [2] , что соответствует энергии, необходимой для его извлечения, очистки и обработки. Таким образом, годовое потребление энергии для получения железа составляет примерно 10 эксаджоулей.
Чтобы узнать больше о том, что происходит с железом после его добычи, см.: Сталь
Магнитные свойства
Железо — один из немногих элементов, проявляющих ферромагнетизм . Молекулярная структура железа такова, что существует 90 547 доменов 90 548 электронов, которые выстраивают свои спины, что приводит к сильно локализованным магнитным полям. Однако эти домены часто ориентированы случайным образом, поэтому объемный материал не проявляет магнитных свойств. Интересная характеристика материала возникает, когда к железу прикладывается внешнее магнитное поле, в результате чего эти домены выстраиваются в линию друг с другом, и говорят, что материал намагничивается. [7]
Однако эти домены часто ориентированы случайным образом, поэтому объемный материал не проявляет магнитных свойств. Интересная характеристика материала возникает, когда к железу прикладывается внешнее магнитное поле, в результате чего эти домены выстраиваются в линию друг с другом, и говорят, что материал намагничивается. [7]
Ферромагнитные материалы, такие как железо, очень полезны в повседневной жизни, а также в специальных приложениях. Обычное использование включает электродвигатели, генераторы, трансформаторы, телефоны и динамики. [8]
Стабильность ядер
Группа железа (от хрома до никеля) содержит наиболее стабильные изотопы всех элементов, имеющих самую высокую энергию связи на нуклон. [9] Значение этого имеет решающее значение для изобилия этих металлов во Вселенной, а также для производства всех более тяжелых элементов, которые образуются из сверхновых. Эти стабильные элементы останавливают ядерный синтез в тяжелых звездах, поскольку процесс синтеза больше не может выделять больше энергии, вызывая звездный коллапс и вызывая сверхновые.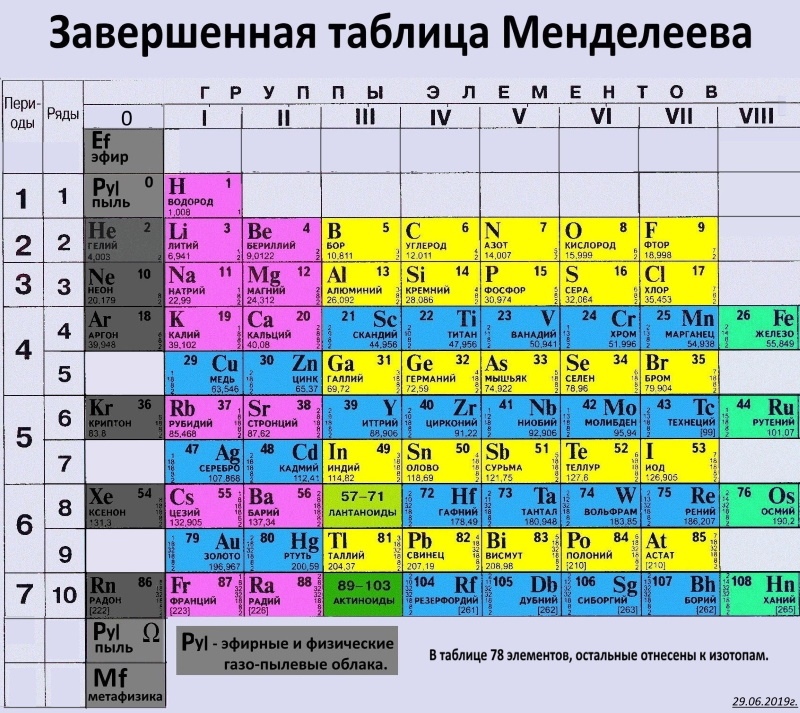 [10]
[10]
Видео
Приведенное ниже видео взято из проекта периодических видеороликов Ноттингемского университета. [11] Они создали полный набор коротких видеороликов о каждом элементе периодической таблицы элементов.
Ссылки
- ↑ 1,0 1,1 1,2 1,3 Jefferson Labs. (По состоянию на 17 февраля 2016 г.). The Element Iron [онлайн], доступно: http://education.jlab.org/itselemental/ele026.html
- ↑ 2,0 2,1 ЮНЕП. (19 августа 2015 г.). Экологические риски и проблемы антропогенных потоков и циклов металлов [Онлайн]. Доступно: https://d396qusza40orc.cloudfront.net/metals/3_Environmental_Challenges_Metals-Full%20Report_36dpi_130923.pdf#96
- ↑ Королевское химическое общество. (По состоянию на 17 февраля 2016 г.) [В сети], Доступно: http://www.
 rsc.org/periodic-table/element/26/iron.
rsc.org/periodic-table/element/26/iron. - ↑ Wikimedia Commons [в сети], доступно: https://commons.wikimedia.org/wiki/File:US_Navy_060616-N-9712C-009_Steelworker_3rd_Class_Robert_Sprague_ties_together_rebar_before_a_concrete_placement_on_a_bridge_project.jpg
- ↑ Лентех. (По состоянию на 17 февраля 2016 г.). Железо (Fe) [Онлайн], доступно: http://www.lenntech.com/periodic/elements/fe.htm
- ↑ МЭА (2014), « Мировые энергетические балансы », Мировая энергетическая статистика и балансы МЭА (база данных). DOI: http://dx.doi.org/10.1787/data-00512-en (По состоянию на февраль 2015 г.)
- ↑ Гиперфизика. (По состоянию на 12 марта 2016 г.). Ферромагнетизм [Онлайн], Доступно: http://hyperphysics.phy-astr.gsu.edu/hbase/solids/ferro.html
- ↑ Британская энциклопедия. (По состоянию на 12 марта 2016 г.). ферромагнетизм [онлайн], доступно: http://www.britannica.com/science/ferromagnetism
- ↑ Гиперфизика. (По состоянию на 12 марта 2016 г.


