| Код и классификация направлений подготовки | Код группы образовательной программы | Наименование групп образовательных программ | Количество мест |
| 8D01 Педагогические науки | |||
| 8D011 Педагогика и психология | D001 | Педагогика и психология | 45 |
| 8D012 Педагогика дошкольного воспитания и обучения | D002 | Дошкольное обучение и воспитание | 5 |
| 8D013 Подготовка педагогов без предметной специализации | D003 | Подготовка педагогов без предметной специализации | 22 |
| 8D014 Подготовка педагогов с предметной специализацией общего развития | D005 | Подготовка педагогов физической культуры | 7 |
| 8D015 Подготовка педагогов по естественнонаучным предметам | D010 | Подготовка педагогов математики | 30 |
| D011 | Подготовка педагогов физики (казахский, русский, английский языки) | 23 | |
| D012 | Подготовка педагогов информатики (казахский, русский, английский языки) | 35 | |
| D013 | Подготовка педагогов химии (казахский, русский, английский языки) | 22 | |
| D014 | Подготовка педагогов биологии (казахский, русский, английский языки) | 18 | |
| D015 | Подготовка педагогов географии | 18 | |
| 8D016 Подготовка педагогов по гуманитарным предметам | D016 | Подготовка педагогов истории | 17 |
| 8D017 Подготовка педагогов по языкам и литературе | D017 | Подготовка педагогов казахского языка и литературы | 37 |
| D018 | Подготовка педагогов русского языка и литературы | 24 | |
| D019 | Подготовка педагогов иностранного языка | 37 | |
| 8D018 Подготовка специалистов по социальной педагогике и самопознанию | D020 | Подготовка кадров по социальной педагогике и самопознанию | 10 |
| 8D019 Cпециальная педагогика | D021 | Cпециальная педагогика | 20 |
| Всего | 370 | ||
| 8D02 Искусство и гуманитарные науки | |||
| 8D022 Гуманитарные науки | D050 | Философия и этика | 20 |
| D051 | Религия и теология | 11 | |
| D052 | Исламоведение | 6 | |
| D053 | История и археология | 33 | |
| D054 | Тюркология | 7 | |
| D055 | Востоковедение | 10 | |
| 8D023 Языки и литература | D056 | Переводческое дело, синхронный перевод | 16 |
| D057 | Лингвистика | 15 | |
| D058 | Литература | 26 | |
| D059 | Иностранная филология | 19 | |
| D060 | Филология | 42 | |
| Всего | 205 | ||
| 8D03 Социальные науки, журналистика и информация | |||
| 8D031 Социальные науки | D061 | Социология | 20 |
| D062 | Культурология | 12 | |
| D063 | Политология и конфликтология | 25 | |
| D064 | Международные отношения | 13 | |
| D065 | Регионоведение | 16 | |
| D066 | Психология | 17 | |
| 8D032 Журналистика и информация | D067 | Журналистика и репортерское дело | 12 |
| D069 | Библиотечное дело, обработка информации и архивное дело | 3 | |
| Всего | 118 | ||
| 8D04 Бизнес, управление и право | |||
| 8D041 Бизнес и управление | D070 | Экономика | 39 |
| D071 | Государственное и местное управление | 28 | |
| D072 | Менеджмент и управление | 12 | |
| D073 | Аудит и налогообложение | 8 | |
| D074 | Финансы, банковское и страховое дело | ||
| D075 | Маркетинг и реклама | 7 | |
| 8D042 Право | D078 | Право | 30 |
| Всего | 145 | ||
| 8D05 Естественные науки, математика и статистика | |||
| 8D051 Биологические и смежные науки | D080 | Биология | 40 |
| D081 | Генетика | ||
| D082 | Биотехнология | 19 | |
| D083 | Геоботаника | 10 | |
| 8D052 Окружающая среда | D084 | География | 10 |
| D085 | Гидрология | 8 | |
| D086 | Метеорология | 5 | |
| D087 | Технология охраны окружающей среды | 15 | |
| D088 | Гидрогеология и инженерная геология | 7 | |
| 8D053 Физические и химические науки | D089 | Химия | 50 |
| D090 | Физика | 70 | |
| 8D054 Математика и статистика | D092 | Математика и статистика | 50 |
| D093 | Механика | 4 | |
| Всего | 292 | ||
| 8D06 Информационно-коммуникационные технологии | |||
| 8D061 Информационно-коммуникационные технологии | D094 | Информационные технологии | 80 |
| 8D062 Телекоммуникации | D096 | Коммуникации и коммуникационные технологии | 14 |
| 8D063 Информационная безопасность | D095 | Информационная безопасность | 26 |
| Всего | 120 | ||
| 8D07 Инженерные, обрабатывающие и строительные отрасли | |||
| 8D071 Инженерия и инженерное дело | D097 | Химическая инженерия и процессы | 46 |
| D098 | Теплоэнергетика | 22 | |
| D099 | Энергетика и электротехника | 28 | |
| D100 | Автоматизация и управление | 32 | |
| D101 | Материаловедение и технология новых материалов | 10 | |
| D102 | Робототехника и мехатроника | 13 | |
| D103 | Механика и металлообработка | 35 | |
| D104 | Транспорт, транспортная техника и технологии | 18 | |
| D105 | Авиационная техника и технологии | 3 | |
| D107 | Космическая инженерия | 6 | |
| D108 | Наноматериалы и нанотехнологии | 21 | |
| D109 | Нефтяная и рудная геофизика | 6 | |
| 8D072 Производственные и обрабатывающие отрасли | D111 | Производство продуктов питания | 20 |
| D114 | Текстиль: одежда, обувь и кожаные изделия | 9 | |
| D115 | Нефтяная инженерия | 15 | |
| D116 | Горная инженерия | 19 | |
| D117 | Металлургическая инженерия | 20 | |
| D119 | Технология фармацевтического производства | 13 | |
| D121 | Геология | 24 | |
| 8D073 Архитектура и строительство | D122 | Архитектура | 15 |
| D123 | Геодезия | 16 | |
| D124 | Строительство | 12 | |
| D125 | Производство строительных материалов, изделий и конструкций | 13 | |
| D128 | Землеустройство | 14 | |
| 8D074 Водное хозяйство | D129 | Гидротехническое строительство | 5 |
| 8D075 Стандартизация, сертификация и метрология (по отраслям) | D130 | Стандартизация, сертификация и метрология (по отраслям) | 11 |
| Всего | 446 | ||
| 8D08 Сельское хозяйство и биоресурсы | |||
| 8D081 Агрономия | D131 | Растениеводство | 22 |
| 8D082 Животноводство | D132 | Животноводство | 12 |
| 8D083 Лесное хозяйство | D133 | Лесное хозяйство | 6 |
| 8D084 Рыбное хозяйство | D134 | Рыбное хозяйство | 4 |
| 8D087 Агроинженерия | D135 | Энергообеспечение сельского хозяйства | 5 |
| D136 | Автотранспортные средства | 3 | |
| 8D086 Водные ресурсы и водопользование | D137 | Водные ресурсы и водопользования | 11 |
| Всего | 63 | ||
| 8D09 Ветеринария | |||
| 8D091 Ветеринария | D138 | Ветеринария | 21 |
| Всего | 21 | ||
| 8D11 Услуги | |||
| 8D111 Сфера обслуживания | D143 | Туризм | 11 |
| 8D112 Гигиена и охрана труда на производстве | D146 | Санитарно-профилактические мероприятия | 5 |
| 8D113 Транспортные услуги | D147 | Транспортные услуги | 5 |
| D148 | Логистика (по отраслям) | 4 | |
| 8D114 Социальное обеспечение | D142 | Социальная работа | 10 |
| Всего | 35 | ||
| Итого | 1815 | ||
| АОО “Назарбаев Университет” | 65 | ||
| Стипендиальная программа на обучение иностранных граждан, в том числе лиц казахской национальности, не являющихся гражданами Республики Казахстан | 10 | ||
| Всего | 1890 | ||
Количество теплоты и тепловая мощность.
 Расчет в Excel.
Расчет в Excel.Опубликовано 13 Окт 2013
Рубрика: Теплотехника | 106 комментариев
Человечеству известно немного видов энергии – механическая энергия (кинетическая и потенциальная), внутренняя энергия (тепловая), энергия полей (гравитационная, электромагнитная и ядерная), химическая. Отдельно стоит выделить энергию взрыва,…
…энергию вакуума и еще существующую только в теории – темную энергию. В этой статье, первой в рубрике «Теплотехника», я попытаюсь на простом и доступном языке, используя практический пример, рассказать о важнейшем виде энергии в жизни людей — о тепловой энергии и о рождающей ее во времени тепловой мощности.
Несколько слов для понимания места теплотехники, как раздела науки о получении, передаче и применении тепловой энергии. Современная теплотехника выделилась из общей термодинамики, которая в свою очередь является одним из разделов физики. Термодинамика – это дословно «теплый» плюс «силовой». Таким образом, термодинамика – это наука об «изменении температуры» системы.
Воздействие на систему извне, при котором изменяется ее внутренняя энергия, может являться результатом теплообмена. Тепловая энергия, которая приобретается или теряется системой в результате такого взаимодействия с окружающей средой, называется количеством теплоты и измеряется в системе СИ в Джоулях.
Если вы не инженер-теплотехник, и ежедневно не занимаетесь теплотехническими вопросами, то вам, столкнувшись с ними, иногда без опыта бывает очень трудно быстро в них разобраться. Трудно без наличия опыта представить даже размерность искомых значений количества теплоты и тепловой мощности. Сколько Джоулей энергии необходимо чтобы нагреть 1000 метров кубических воздуха от температуры -37˚С до +18˚С?.. Какая нужна мощность источника тепла, чтобы сделать это за 1 час?.. На эти не самые сложные вопросы способны сегодня ответить «сходу» далеко не все инженеры. Иногда специалисты даже помнят формулы, но применить их на практике могут лишь единицы!
Прочитав до конца эту статью, вы сможете легко решать реальные производственные и бытовые задачи, связанные с нагревом и охлаждением различных материалов. Понимание физической сути процессов теплопередачи и знание простых основных формул – это главные блоки в фундаменте знаний по теплотехнике!
Понимание физической сути процессов теплопередачи и знание простых основных формул – это главные блоки в фундаменте знаний по теплотехнике!
Количество теплоты при различных физических процессах.
Большинство известных веществ могут при разных температуре и давлении находиться в твердом, жидком, газообразном или плазменном состояниях. Переход из одного агрегатного состояния в другое происходит при постоянной температуре (при условии, что не меняются давление и другие параметры окружающей среды) и сопровождается поглощением или выделением тепловой энергии. Не смотря на то, что во Вселенной 99% вещества находится в состоянии плазмы, мы в этой статье не будем рассматривать это агрегатное состояние.
Рассмотрим график, представленный на рисунке. На нем изображена зависимость температуры вещества Т от количества теплоты Q, подведенного к некой закрытой системе, содержащей определенную массу какого-то конкретного вещества.
1. Твердое тело, имеющее температуру T1, нагреваем до температуры Tпл, затрачивая на этот процесс количество теплоты равное Q1.
Твердое тело, имеющее температуру T1, нагреваем до температуры Tпл, затрачивая на этот процесс количество теплоты равное Q1.
2. Далее начинается процесс плавления, который происходит при постоянной температуре Тпл (температуре плавления). Для расплавления всей массы твердого тела необходимо затратить тепловой энергии в количестве Q2— Q1.
3. Далее жидкость, получившаяся в результате плавления твердого тела, нагреваем до температуры кипения (газообразования) Ткп, затрачивая на это количество теплоты равное Q3–Q2.
4. Теперь при неизменной температуре кипения Ткп жидкость кипит и испаряется, превращаясь в газ. Для перехода всей массы жидкости в газ необходимо затратить тепловую энергию в количестве Q4–Q3.
5. На последнем этапе происходит нагрев газа от температуры Ткп до некоторой температуры Т2. При этом затраты количества теплоты составят Q5–Q4. (Если нагреем газ до температуры ионизации, то газ превратится в плазму.)
При этом затраты количества теплоты составят Q5–Q4. (Если нагреем газ до температуры ионизации, то газ превратится в плазму.)
Таким образом, нагревая исходное твердое тело от температуры Т1 до температуры Т2 мы затратили тепловую энергию в количестве Q5, переводя вещество через три агрегатных состояния.
Двигаясь в обратном направлении, мы отведем от вещества то же количество тепла Q5, пройдя этапы конденсации, кристаллизации и остывания от температуры Т2 до температуры Т1. Разумеется, мы рассматриваем замкнутую систему без потерь энергии во внешнюю среду.
Заметим, что возможен переход из твердого состояния в газообразное состояние, минуя жидкую фазу. Такой процесс именуется возгонкой, а обратный ему процесс – десублимацией.
Итак, уяснили, что процессы переходов между агрегатными состояниями вещества характеризуются потреблением энергии при неизменной температуре.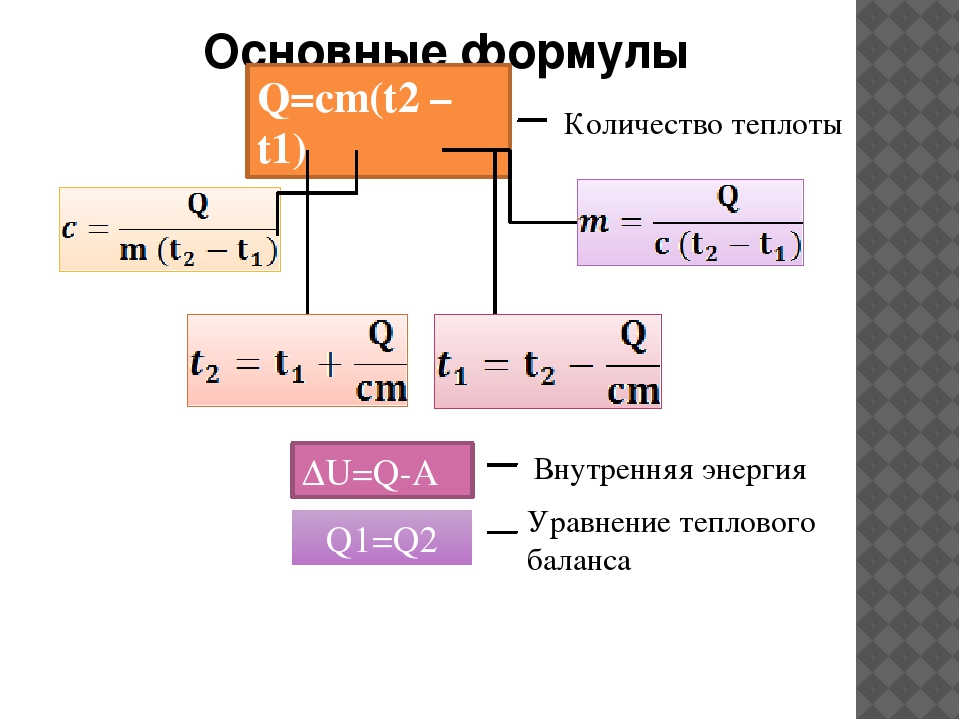 При нагреве вещества, находящегося в одном неизменном агрегатном состоянии, повышается температура и также расходуется тепловая энергия.
При нагреве вещества, находящегося в одном неизменном агрегатном состоянии, повышается температура и также расходуется тепловая энергия.
Главные формулы теплопередачи.
Формулы очень просты.
Количество теплоты Q в Дж рассчитывается по формулам:
1. Со стороны потребления тепла, то есть со стороны нагрузки:
1.1. При нагревании (охлаждении):
Q=m*c*(Т2-Т1)
Здесь и далее:
m – масса вещества в кг
с – удельная теплоемкость вещества в Дж/(кг*К)
1.2. При плавлении (замерзании):
Q=m*λ
λ – удельная теплота плавления и кристаллизации вещества в Дж/кг
1.3. При кипении, испарении (конденсации):
Q=m*r
r – удельная теплота газообразования и конденсации вещества в Дж/кг
2. 2
2
t – время в с
I – действующее значение тока в А
U – действующее значение напряжения в В
R – сопротивление нагрузки в Ом
Делаем вывод – количество теплоты прямо пропорционально массе вещества при всех фазовых превращениях и при нагреве дополнительно прямо пропорционально разности температур. Коэффициенты пропорциональности (c, λ, r, q) для каждого вещества имеют свои значения и определены опытным путем (берутся из справочников).
Тепловая мощность N в Вт – это количество теплоты переданное системе за определенное время:
N=Q/t
Чем быстрее мы хотим нагреть тело до определенной температуры, тем большей мощности должен быть источник тепловой энергии – все логично.
Расчет в Excel прикладной задачи.
В жизни бывает часто необходимо сделать быстрый оценочный расчет, чтобы понять – имеет ли смысл продолжать изучение темы, делая проект и развернутые точные трудоемкие расчеты. Сделав за несколько минут расчет даже с точностью ±30%, можно принять важное управленческое решение, которое будет в 100 раз более дешевым и в 1000 раз более оперативным и в итоге в 100000 раз более эффективным, чем выполнение точного расчета в течение недели, а то и месяца, группой дорогостоящих специалистов…
Сделав за несколько минут расчет даже с точностью ±30%, можно принять важное управленческое решение, которое будет в 100 раз более дешевым и в 1000 раз более оперативным и в итоге в 100000 раз более эффективным, чем выполнение точного расчета в течение недели, а то и месяца, группой дорогостоящих специалистов…
Условия задачи:
В помещение цеха подготовки металлопроката размерами 24м х 15м х 7м завозим со склада на улице металлопрокат в количестве 3т. На металлопрокате есть лед общей массой 20кг. На улице -37˚С. Какое количество теплоты необходимо, чтобы нагреть металл до +18˚С; нагреть лед, растопить его и нагреть воду до +18˚С; нагреть весь объем воздуха в помещении, если предположить, что до этого отопление было полностью отключено? Какую мощность должна иметь система отопления, если все вышесказанное необходимо выполнить за 1час? (Очень жесткие и почти не реальные условия – особенно касающиеся воздуха!)
Расчет выполним в программе MS Excel или в программе OOo Calc.
С цветовым форматированием ячеек и шрифтов ознакомьтесь на странице «О блоге».
Исходные данные:
1. Названия веществ пишем:
в ячейку D3: Сталь
в ячейку E3: Лед
в ячейку F3: Лед/вода
в ячейку G3: Вода
в ячейку G3: Воздух
2. Названия процессов заносим:
в ячейки D4, E4, G4, G4: нагрев
в ячейку F4: таяние
3. Удельную теплоемкость веществ c в Дж/(кг*К) пишем для стали, льда, воды и воздуха соответственно
в ячейку D5: 460
в ячейку E5: 2110
в ячейку G5: 4190
в ячейку H5: 1005
4. Удельную теплоту плавления льда λ в Дж/кг вписываем
в ячейку F6: 330000
5. Массу веществ m в кг вписываем соответственно для стали и льда
Массу веществ m в кг вписываем соответственно для стали и льда
в ячейку D7: 3000
в ячейку E7: 20
Так как при превращении льда в воду масса не изменяется, то
в ячейках F7 и G7: =E7=20
Массу воздуха находим произведением объема помещения на удельный вес
в ячейке H7: =24*15*7*1,23=3100
6. Время процессов t в мин пишем только один раз для стали
в ячейку D8: 60
Значения времени для нагрева льда, его плавления и нагрева получившейся воды рассчитываются из условия, что все эти три процесса должны уложиться в сумме за такое же время, какое отведено на нагрев металла. Считываем соответственно
в ячейке E8: =E12/(($E$12+$F$12+$G$12)/D8)=9,7
в ячейке F8: =F12/(($E$12+$F$12+$G$12)/D8)=41,0
в ячейке G8: =G12/(($E$12+$F$12+$G$12)/D8)=9,4
Воздух также должен прогреться за это же самое отведенное время, читаем
в ячейке H8: =D8=60,0
7. Начальную температуру всех веществ T1 в ˚C заносим
Начальную температуру всех веществ T1 в ˚C заносим
в ячейку D9: -37
в ячейку E9: -37
в ячейку F9: 0
в ячейку G9: 0
в ячейку H9: -37
8. Конечную температуру всех веществ T2 в ˚C заносим
в ячейку D10: 18
в ячейку E10: 0
в ячейку F10: 0
в ячейку G10: 18
в ячейку h20: 18
Думаю, вопросов по п.7 и п.8 быть недолжно.
Результаты расчетов:
9. Количество теплоты Q в КДж, необходимое для каждого из процессов рассчитываем
для нагрева стали в ячейке D12: =D7*D5*(D10-D9)/1000=75900
для нагрева льда в ячейке E12: =E7*E5*(E10-E9)/1000= 1561
для плавления льда в ячейке F12: =F7*F6/1000= 6600
для нагрева воды в ячейке G12: =G7*G5*(G10-G9)/1000= 1508
для нагрева воздуха в ячейке h22: =H7*H5*(h20-H9)/1000= 171330
Общее количество необходимой для всех процессов тепловой энергии считываем
в объединенной ячейке D13E13F13G13h23: =СУММ(D12:h22) = 256900
В ячейках D14, E14, F14, G14, h24, и объединенной ячейке D15E15F15G15h25 количество теплоты приведено в дугой единице измерения – в ГКал (в гигакалориях).
10. Тепловая мощность N в КВт, необходимая для каждого из процессов рассчитывается
для нагрева стали в ячейке D16: =D12/(D8*60)=21,083
для нагрева льда в ячейке E16: =E12/(E8*60)= 2,686
для плавления льда в ячейке F16: =F12/(F8*60)= 2,686
для нагрева воды в ячейке G16: =G12/(G8*60)= 2,686
для нагрева воздуха в ячейке h26: =h22/(H8*60)= 47,592
Суммарная тепловая мощность необходимая для выполнения всех процессов за время t рассчитывается
в объединенной ячейке D17E17F17G17h27: =D13/(D8*60) = 71,361
В ячейках D18, E18, F18, G18, h28, и объединенной ячейке D19E19F19G19h29 тепловая мощность приведена в дугой единице измерения – в Гкал/час.
На этом расчет в Excel завершен.
Выводы:
Обратите внимание, что для нагрева воздуха необходимо более чем в два раза больше затратить энергии, чем для нагрева такой же массы стали.
При нагреве воды затраты энергии в два раза больше, чем при нагреве льда. Процесс плавления многократно больше потребляет энергии, чем процесс нагрева (при небольшой разности температур).
Нагрев воды в десять раз затрачивает больше тепловой энергии, чем нагрев стали и в четыре раза больше, чем нагрев воздуха.
Для получения информации о выходе новых статей и для скачивания рабочих файлов программ прошу вас подписаться на анонсы в окне, расположенном в конце статьи или в окне вверху страницы.
После ввода адреса своей электронной почты и нажатия на кнопку «Получать анонсы статей» НЕ ЗАБУДЬТЕ ПОДТВЕРДИТЬ ПОДПИСКУ кликом по ссылке в письме, которое тут же придет к вам на указанную почту (иногда — в папку «Спам»)!
Мы вспомнили понятия «количество теплоты» и «тепловая мощность», рассмотрели фундаментальные формулы теплопередачи, разобрали практический пример. Надеюсь, что мой язык был прост, понятен и интересен.
Надеюсь, что мой язык был прост, понятен и интересен.
Жду вопросы и комментарии на статью!
Прошу УВАЖАЮЩИХ труд автора скачать файл ПОСЛЕ ПОДПИСКИ на анонсы статей.
Ссылка на скачивание файла: raschet-teplovoy-moshchnosti (xls 19,5KB).
Другие статьи автора блога
На главную
Статьи с близкой тематикой
Отзывы
Формула нахождения количества теплоты в физике. Как рассчитать количество теплоты, тепловой эффект и теплоту образования
Что быстрее нагреется на плите – чайник или ведро воды? Ответ очевиден – чайник. Тогда второй вопрос – почему?
Ответ не менее очевиден – потому что масса воды в чайнике меньше. Отлично. А теперь вы можете проделать самостоятельно самый настоящий физический опыт в домашних условиях. Для этого вам понадобится две одинаковые небольшие кастрюльки, равное количество воды и растительного масла, например, по пол-литра и плита. На одинаковый огонь ставите кастрюльки с маслом и водой. А теперь просто наблюдайте, что быстрее будет нагреваться. Если есть градусник для жидкостей, можно применить его, если нет, можно просто пробовать температуру время от времени пальцем, только осторожно, чтобы не обжечься. В любом случае вы вскоре убедитесь, что масло нагревается значительно быстрее воды. И еще один вопросик, который тоже можно реализовать в виде опыта. Что быстрее закипит – теплая вода или холодная? Все снова очевидно – теплая будет на финише первой. К чему все эти странные вопросы и опыты? К тому, чтобы определить физическую величину, называемую «количеством теплоты».
На одинаковый огонь ставите кастрюльки с маслом и водой. А теперь просто наблюдайте, что быстрее будет нагреваться. Если есть градусник для жидкостей, можно применить его, если нет, можно просто пробовать температуру время от времени пальцем, только осторожно, чтобы не обжечься. В любом случае вы вскоре убедитесь, что масло нагревается значительно быстрее воды. И еще один вопросик, который тоже можно реализовать в виде опыта. Что быстрее закипит – теплая вода или холодная? Все снова очевидно – теплая будет на финише первой. К чему все эти странные вопросы и опыты? К тому, чтобы определить физическую величину, называемую «количеством теплоты».
Количество теплоты
Количество теплоты – это энергия, которую тело теряет или приобретает при теплопередаче. Это понятно и из названия. При остывании тело будет терять некое количество теплоты, а при нагревании – поглощать. А ответы на наши вопросы показали нам, от чего зависит количество теплоты? Во-первых, чем больше масса тела, тем большее количество теплоты надо затратить на изменение его температуры на один градус. Во-вторых, количество теплоты, необходимое для нагревания тела, зависит от того вещества, из которого оно состоит, то есть от рода вещества. И в-третьих, разность температур тела до и после теплопередачи также важна для наших расчетов. Исходя из всего вышесказанного, мы можем определить количество теплоты формулой:
Во-вторых, количество теплоты, необходимое для нагревания тела, зависит от того вещества, из которого оно состоит, то есть от рода вещества. И в-третьих, разность температур тела до и после теплопередачи также важна для наших расчетов. Исходя из всего вышесказанного, мы можем определить количество теплоты формулой:
где Q – количество теплоты,
m – масса тела,
(t_2-t_1) – разность между начальной и конечной температурами тела,
c – удельная теплоемкость вещества, находится из соответствующих таблиц.
По этой формуле можно произвести расчет количества теплоты, которое необходимо, чтобы нагреть любое тело или которое это тело выделит при остывании.
Измеряется количество теплоты в джоулях (1 Дж), как и всякий вид энергии. Однако, величину эту ввели не так давно, а измерять количество теплоты люди начали намного раньше. И пользовались они единицей, которая широко используется и в наше время – калория (1 кал). 1 калория – это такое количество теплоты, которое потребуется для нагреванияь 1 грамма воды на 1 градус Цельсия. Руководствуясь этими данными, любители подсчитывать калории в съедаемой пище, могут ради интереса подсчитать, сколько литров воды можно вскипятить той энергией, которую они потребляют с едой в течение дня.
Руководствуясь этими данными, любители подсчитывать калории в съедаемой пище, могут ради интереса подсчитать, сколько литров воды можно вскипятить той энергией, которую они потребляют с едой в течение дня.
Внутренняя энергия тела изменяется при совершении работы или теплопередаче. При явлении теплопередачи внутренняя энергия передается теплопроводностью, конвекцией или излучением.
Каждое тело при нагревании или охлаждении (при теплопередаче) получает или теряет какое-то количество энергии. Исходя из этого, принято это количество энергии назвать количеством теплоты.
Итак, количество теплоты – это та энергия, которую отдает или получает тело в процессе теплопередачи.
Какое количество теплоты необходимо для нагревания воды? На простом примере можно понять, что для нагревания разного количества воды потребуется разное количество теплоты. Допустим, возьмем две пробирки с 1 литром воды и с 2-мя литрами воды. В каком случае потребуется большее количество теплоты? Во втором, там, где в пробирке 2 литра воды. Вторая пробирка будет нагреваться дольше, если мы подогреваем их одинаковым источником огня.
Вторая пробирка будет нагреваться дольше, если мы подогреваем их одинаковым источником огня.
Таким образом, количество теплоты зависит от массы тела. Чем больше масса, тем большее количество теплоты требуется для нагрева и, соответственно, на охлаждение тела требуется большее время.
От чего еще зависит количество теплоты? Естественно, от разности температур тел. Но это еще не все. Ведь если мы попытаемся нагреть воду или молоко, то нам потребуется разное количество времени. Т.е получается, что количество теплоты зависит от вещества, из которого состоит тело.
В итоге получается, что количество теплоты, которое нужно для нагревания или количество теплоты, которое выделяется при остывании тела, зависит от его массы, от изменения температуры и от вида вещества, из которого состоит тело.
В чем измеряется количество теплотыЗа единицу количества теплоты принято считать 1 Джоуль . До появления единицы измерения энергии ученые считали количество теплоты калориями.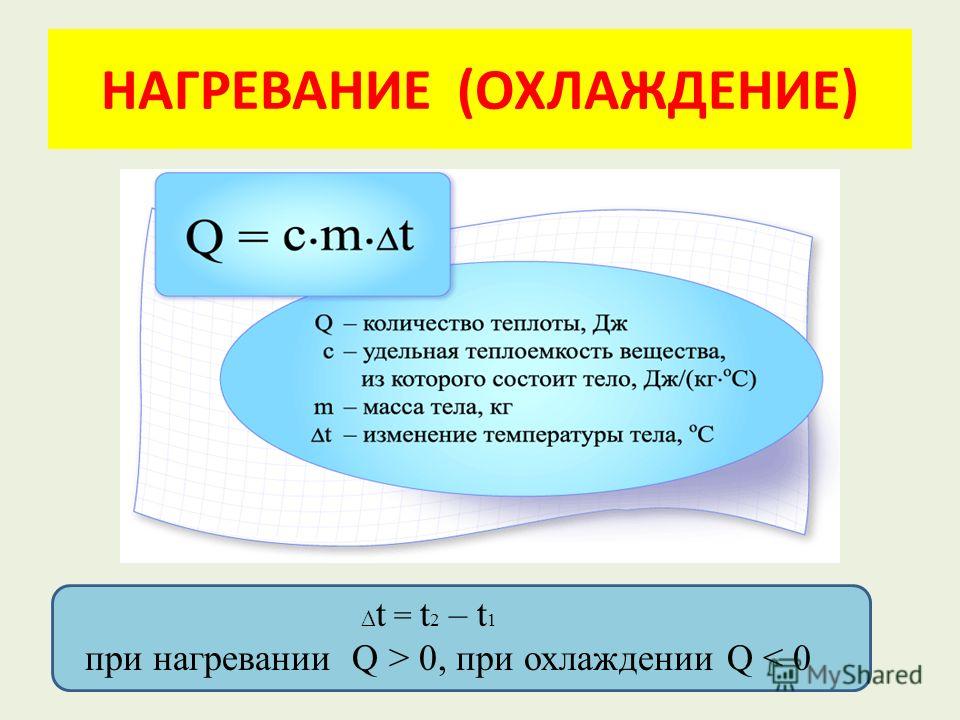 Сокращенно эту единицу измерения принято писать – “Дж”
Сокращенно эту единицу измерения принято писать – “Дж”
Калория – это количество теплоты, которое необходимо для того, чтобы нагреть 1 грамм воды на 1 градус Цельсия. Сокращенно единицу измерения калории принято писать – “кал”.
1 кал = 4,19 Дж.
Обратите внимание, что в этих единицах энергии принято отмечать пищевую ценность продуктов питания кДж и ккал.
1 ккал = 1000 кал.
1 кДж = 1000 Дж
1 ккал = 4190 Дж = 4,19 кДж
Что такое удельная теплоемкостьКаждое вещество в природе имеет свои свойства, и для нагрева каждого отдельного вещества требуется разное количество энергии, т.е. количества теплоты.
Удельная теплоемкость вещества – это величина, равная количеству теплоты, которое нужно передать телу с массой 1 килограмм, чтобы нагреть его на температуру 1 0 C
Удельная теплоемкость обозначается буквой c и имеет величину измерения Дж/кг*
Например, удельная теплоемкость воды равна 4200 Дж/кг*
0
C. То есть это то количество теплоты, которое нужно передать 1 кг воды, чтобы нагреть ее на 1
0
C
То есть это то количество теплоты, которое нужно передать 1 кг воды, чтобы нагреть ее на 1
0
C
Следует помнить, что удельная теплоемкость веществ в разных агрегатных состояниях различна. То есть для нагревания льда на 1 0 C потребуется другое количество теплоты.
Как рассчитать количество теплоты для нагревания телаНапример, необходимо рассчитать количество теплоты, которое нужно потратить для того, чтобы нагреть 3 кг воды с температуры 15 0 С до температуры 85 0 С. Нам известна удельная теплоемкость воды, то есть количество энергии, которое нужно для того, чтобы нагреть 1 кг воды на 1 градус. То есть для того, чтобы узнать количество теплоты в нашем случае, нужно умножить удельную теплоемкость воды на 3 и на то количество градусов, на которое нужно увеличить температуры воды. Итак, это 4200*3*(85-15) = 882 000.
В скобках мы рассчитываем точное количество градусов, отнимая от конечного необходимого результата начальное
Итак, для того, чтобы нагреть 3 кг воды с 15 до 85
0
С, нам потребуется 882 000 Дж количества теплоты.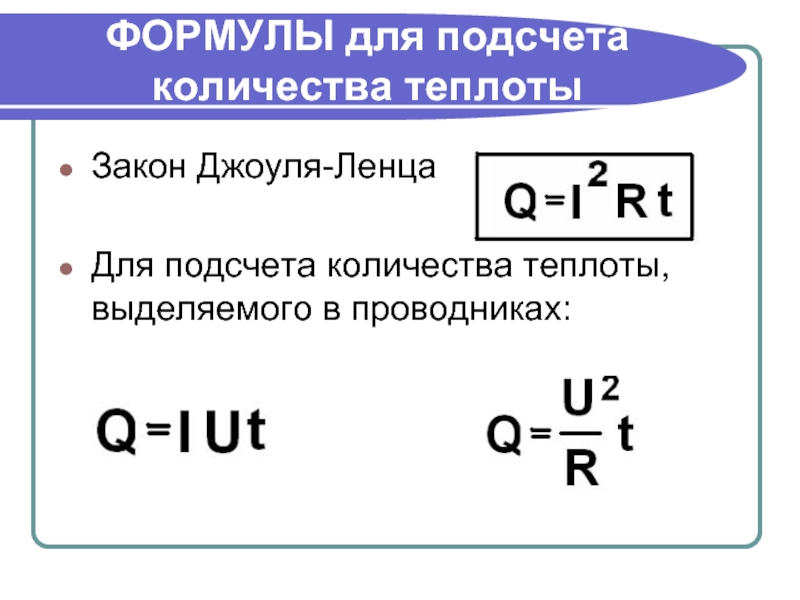
Количество теплоты обозначается буквой Q, формула для его расчета выглядит следующим образом:
Q=c*m*(t 2 -t 1).
Разбор и решение задачЗадача 1 . Какое количество теплоты потребуется для нагрева 0,5 кг воды с 20 до 50 0 С
Дано:
m = 0,5 кг.,
с = 4200 Дж/кг* 0 С,
t 1 = 20 0 С,
t 2 = 50 0 С.
Величину удельной теплоемкость мы определили из таблицы.
Решение:
2 -t 1 ).
Подставляем значения:
Q=4200*0,5*(50-20) = 63 000 Дж = 63 кДж.
Ответ: Q=63 кДж.
Задача 2. Какое количество теплоты потребуется для нагревания алюминиевого бруска массой 0,5 кг на 85 0 С?
Дано:
m = 0,5 кг.,
с = 920 Дж/кг* 0 С,
t 1 = 0 0 С,
t 2 = 85 0 С.
Решение:
количество теплоты определяется по формуле Q=c*m*(t 2 -t 1 ).
Подставляем значения:
Q=920*0,5*(85-0) = 39 100 Дж = 39,1 кДж.
Ответ: Q= 39,1 кДж.
ТЕПЛООБМЕН.
1.Теплообмен.
Теплообмен или теплопередача – это процесс передачи внутренней энергии одного тела другому без совершения работы.
Существуют три вида теплообмена.
1) Теплопроводность – это теплообмен между телами при их непосредственном контакте.
2) Конвекция – это теплообмен, при котором перенос тепла осуществляется потоками газа или жидкости.
3) Излучение – это теплообмен посредством электромагнитного излучения.
2.Количество теплоты.
Количество теплоты – это мера изменения внутренней энергии тела при теплообмене. Обозначается буквой Q .
Единица измерения количества теплоты = 1 Дж.
Количество теплоты,
полученное телом от другого тела в
результате теплообмена, может тратиться
на увеличение температуры (увеличение
кинетической энергии молекул) или на
изменение агрегатного состояния
(увеличение потенциальной энергии).
3.Удельная теплоёмкость вещества.
Опыт показывает, что количество теплоты, необходимое для нагревания тела массой m от температуры Т 1 до температуры Т 2 пропорционально массе тела m и разности температур (Т 2 – Т 1), т.е.
Q = cm (Т 2 – Т 1 ) = с m Δ Т,
с называется удельной теплоёмкостью вещества нагреваемого тела.
Удельная теплоёмкость вещества равна количеству теплоту, которое необходимо сообщить 1 кг вещества, чтобы нагреть его на 1 К.
Единица измерения удельной теплоёмкости =.
Значения теплоёмкости различных веществ можно найти в физических таблицах.
Точно такое же количество теплоты Q будет выделяться при охлаждении тела на ΔТ.
4.Удельная теплота парообразования.
Опыт показывает, что количество теплоты, необходимое для превращения жидкости в пар, пропорционально массе жидкости, т.е.
Q = Lm ,
где коэффициент
пропорциональности L называется
удельной теплотой парообразования.
Удельная теплота парообразования равна количеству теплоты, которое необходимо для превращения в пар 1 кг жидкости, находящейся при температуре кипения.
Единица измерения удельной теплоты парообразования .
При обратном процессе, конденсации пара, теплота выделяется в том же количестве, которое затрачено на парообразование.
5.Удельная теплота плавления.
Опыт показывает, что количество теплоты, необходимое для превращения твёрдого тела в жидкость, пропорционально массе тела, т.е.
Q = λ m ,
где коэффициент пропорциональности λ называется удельной теплотой плавления.
Удельная теплота плавления равна количеству теплоты, которое необходимо для превращения в жидкость твёрдого тела массой 1 кг при температуре плавления.
Единица измерения удельной теплоты плавления .
При обратном процессе, кристаллизации жидкости, теплота выделяется в том же количестве, которое затрачено на плавление.
6. Удельная теплота
сгорания.
Удельная теплота
сгорания.
Опыт показывает, что количество теплоты, выделяемое при полном сгорании топлива, пропорционально массе топлива, т.е.
Q = q m ,
Где коэффициент пропорциональности q называется удельной теплотой сгорания.
Удельная теплота сгорания равна количеству теплоты, которое выделяется при полном сгорании 1 кг топлива.
Единица измерения удельной теплоты сгорания.
7.Уравнение теплового баланса.
В теплообмене участвуют два или более тела. Одни тела отдают теплоту, а другие принимают. Теплообмен происходит до тех пор, пока температуры тел не станут равными. По закону сохранения энергии, количество теплоты, которое отдаётся, равно количеству, которое принимается. На этом основании записывается уравнение теплового баланса.
Рассмотрим пример.
Тело массой m 1 ,
теплоёмкость которого с 1 ,
имеет температуру Т 1 ,
а тело массой m 2 ,
теплоёмкость которого с 2 ,
имеет температуру Т 2 . Причём Т 1
больше Т 2 .
Эти тела приведены в соприкосновение.
Опыт показывает, что холодное тело (m 2)
начинает нагреваться, а горячее тело
(m 1)
– охлаждаться. Это говорит о том, что
часть внутренней энергии горячего тела
передаётся холодному, и температуры
выравниваются. Обозначим конечную общую
температуру θ.
Причём Т 1
больше Т 2 .
Эти тела приведены в соприкосновение.
Опыт показывает, что холодное тело (m 2)
начинает нагреваться, а горячее тело
(m 1)
– охлаждаться. Это говорит о том, что
часть внутренней энергии горячего тела
передаётся холодному, и температуры
выравниваются. Обозначим конечную общую
температуру θ.
Количество теплоты, переданной горячим телом холодному
Q передан. = c 1 m 1 (Т 1 – θ )
Количество теплоты, полученной холодным телом от горячего
Q получен. = c 2 m 2 (θ – Т 2 )
По закону сохранения энергии Q передан. = Q получен. , т.е.
c 1 m 1 (Т 1 – θ )= c 2 m 2 (θ – Т 2 )
Раскроем скобки
и выразим значение общей установившейся
температуры θ.
Значение температуры θ в данном случае получим в кельвинах.
Однако, так как в выражениях для Q передан. и Q получен. стоит разность двух температур, а она и в кельвинах, и в градусах Цельсия одинакова, то расчёт можно вести и в градусах Цельсия. Тогда
В этом случае значение температуры θ получим в градусах Цельсия.
Выравнивание температур в результате теплопроводности можно объяснить на основании молекулярно-кинетической теории как обмен кинетической энергией между молекулами при сталкивании в процессе теплового хаотического движения.
Этот пример можно проиллюстрировать графиком.
Внутреннюю энергию термодинамической системы можно изменить двумя способами:
- совершая над системой работу,
- при помощи теплового взаимодействия.
Передача тепла телу не связана с совершением над телом макроскопической работы. В данном случае изменение внутренней энергии вызвано тем,
что отдельные молекулы тела с большей температурой совершают работу над некоторыми молекулами тела, которое имеет меньшую температуру.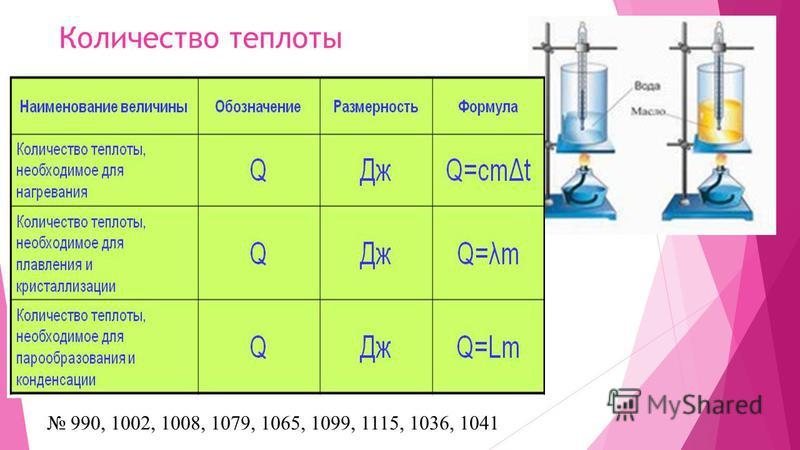 В этом
случае тепловое взаимодействие реализуется за счет теплопроводности. Передача энергии также возможна при помощи излучения. Система
микроскопических процессов (относящихся не ко всему телу, а к отдельным молекулам) называется теплопередачей. Количество энергии,
которое передается от одного тела к другому в результате теплопередачи, определяется количеством теплоты, которое предано от одного тела другому.
В этом
случае тепловое взаимодействие реализуется за счет теплопроводности. Передача энергии также возможна при помощи излучения. Система
микроскопических процессов (относящихся не ко всему телу, а к отдельным молекулам) называется теплопередачей. Количество энергии,
которое передается от одного тела к другому в результате теплопередачи, определяется количеством теплоты, которое предано от одного тела другому.
Определение
Теплотой называют энергию, которая получается (или отдается) телом в процессе теплообмена с окружающими телами (средой). Обозначается теплота, обычно буквой Q.
Это одна из основных величин в термодинамике. Теплота включена в математические выражения первого и второго начал термодинамики. Говорят, что теплота – это энергия в форме молекулярного движения.
Теплота может сообщаться системе (телу), а может забираться от нее. Считают, что если тепло сообщается системе, то оно положительно.
Формула расчета теплоты при изменении температуры
Элементарное количество теплоты обозначим как . Обратим внимание,
что элемент тепла, которое получает (отдает) система при малом изменении ее состояния не является полным дифференциалом.
Причина этого состоит в том, что теплота является функцией процесса изменения состояния системы.
Обратим внимание,
что элемент тепла, которое получает (отдает) система при малом изменении ее состояния не является полным дифференциалом.
Причина этого состоит в том, что теплота является функцией процесса изменения состояния системы.
Элементарное количество тепла, которое сообщается системе, и температура при этом меняется от Tдо T+dT, равно:
где C – теплоемкость тела. Если рассматриваемое тело однородно, то формулу (1) для количества теплоты можно представить как:
где – удельная теплоемкость тела, m – масса тела, – молярная теплоемкость, – молярная масса вещества, – число молей вещества.
Если тело однородно, а теплоемкость считают независимой от температуры, то количество теплоты (), которое получает тело при увеличении его температуры на величину можно вычислить как:
где t 2 , t 1 температуры тела до нагрева и после. Обратите внимание, что температуры при нахождении разности
() в расчетах можно подставлять как в градусах Цельсия, так и в кельвинах.
Формула количества теплоты при фазовых переходах
Переход от одной фазы вещества в другую сопровождается поглощением или выделением некоторого количества теплоты, которая носит название теплоты фазового перехода.
Так, для перевода элемента вещества из состояния твердого тела в жидкость ему следует сообщить количество теплоты () равное:
где – удельная теплота плавления, dm – элемент массы тела. При этом следует учесть, что тело должно иметь температуру, равную температуре плавления рассматриваемого вещества. При кристаллизации происходит выделение тепла равного (4).
Количество теплоты (теплота испарения), которое необходимо для перевода жидкости в пар можно найти как:
где r – удельная теплота испарения. При конденсации пара теплота выделяется. Теплота испарения равна теплоте конденсации одинаковых масс вещества.
Единицы измерения количества теплоты
Основной единицей измерения количества теплоты в системе СИ является: [Q]=Дж
Внесистемная единица теплоты, которая часто встречается в технических расчетах. [Q]=кал (калория). 1 кал=4,1868 Дж.
[Q]=кал (калория). 1 кал=4,1868 Дж.
Примеры решения задач
Пример
Задание. Какие объемы воды следует смешать, чтобы получить 200 л воды при температуре t=40С, если температура одной массы воды t 1 =10С, второй массы воды t 2 =60С?
Решение. Запишем уравнение теплового баланса в виде:
где Q=cmt – количество теплоты приготовленной после смешивания воды; Q 1 =cm 1 t 1 – количество теплоты части воды температурой t 1 и массой m 1 ; Q 2 =cm 2 t 2 – количество теплоты части воды температурой t 2 и массой m 2 .
Из уравнения (1.1) следует:
При объединении холодной (V 1) и горячей (V 2) частей воды в единый объем (V) можно принять то, что:
Так, мы получаем систему уравнений:
Решив ее получим:
Как записывается формула для вычисления энергии топлива
Всем известно, что в нашей жизни огромную роль играет использование топлива. Топливо применяют практически в любой отрасли современной промышленности. Особенно часто применяется топливо, полученное из нефти: бензин, керосин, соляр и другие. Также применяют горючие газы (метан и другие).
Особенно часто применяется топливо, полученное из нефти: бензин, керосин, соляр и другие. Также применяют горючие газы (метан и другие).
Откуда берется энергия у топлива
Известно, что молекулы состоят из атомов. Для того, чтобы разделить какую либо молекулу (например, молекулу воды) на составляющие её атомы, требуется затратить энергию (на преодоление сил притяжения атомов). Опыты показывают, что при соединении атомов в молекулу (это и происходит при сжигании топлива) энергия, напротив, выделяется.
Как известно, существует ещё и ядерное топливо, но мы не будем здесь говорить о нём.
При сгорании топлива выделяется энергия. Чаще всего это тепловая энергия. Опыты показывают, что количество выделившейся энергии прямо пропорционально количеству сгоревшего топлива.
Удельная теплота сгорания
Для расчёта этой энергии используют физическую величину, называемую удельная теплота сгорания топлива. Удельная теплота сгорания топлива показывает, какая энергия выделяется при сгорании единичной массы топлива.
Её обозначают латинской буквой q. В системе СИ единица измерения этой величины Дж/кг. Отметим, что каждое топливо имеет собственную удельную теплоту сгорания. Эта величина измерена практически для всех видов топлива и при решении задач определяется по таблицам.
Например, удельная теплота сгорания бензина 46 000 000 Дж/кг, керосина такая же, этилового спирта 27 000 000 Дж/кг. Нетрудно понять, что энергия, выделившаяся при сгорании топлива, равна произведению массы этого топлива и удельной теплоты сгорания топлива:
Q = q*m
Рассмотрим примеры
Рассмотрим пример. 10 граммов этилового спирта сгорело в спиртовке за 10 минут. Найдите мощность спиртовки.
Решение. Найдём количество теплоты, выделившееся при сгорании спирта:
Q = q*m; Q = 27 000 000 Дж/кг * 10 г = 27 000 000 Дж/кг * 0,01 кг = 270 000 Дж.
Найдём мощность спиртовки:
N = Q / t = 270 000 Дж / 10 мин = 270 000 Дж / 600 с = 450 Вт.
Рассмотрим более сложный пример.Алюминиевую кастрюлю массой m1, заполненную водой массой m2, нагрели с помощью примуса от температуры t1 до температуры t2 (00С
Предыдущая тема: Удельная теплоёмкость: расчет количества теплоты
Следующая тема:   Студент или преподаватель? Кого выбрать? — Nado5.ru
Все неприличные комментарии будут удаляться.
«Чтобы согреть других, свеча должна сгореть»
Цель: Изучить вопросы использования внутренней энергии топлива, выделения тепла при сгорании топлива.
Задачи урока:
- повторить и закрепить знания по пройденному материалу,;
- ввести понятие об энергии топлива, удельной теплоты сгорания топлива;
- продолжить развитие навыков решения расчётных задач.
- развивать аналитическое мышление;
- развивать умения работать с таблицами и делать выводы;
- развивать способности учащихся выдвигать гипотезы, аргументировать их, грамотно выражать свои мысли вслух;
- развивать наблюдательность и внимание.

- воспитывать бережное отношение к использованию топливных ресурсов;
- воспитывать интерес к предмету через показ связи изучаемого материала с реальной жизнью;
- воспитывать навыки коммуникативного общения.
Предметные результаты:
Обучающиеся должны знать:
- удельная теплота сгорания топлива — это физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг;
- при сгорании топлива выделяется значительная энергия, которую используют в быту, промышленности, сельском хозяйстве, на электростанциях, в автомобильном транспорте;
- единицу измерения удельной теплоты сгорания топлива.
Обучающиеся должны уметь:
- объяснять процесс выделения энергии при сгорании топлива;
- пользоваться таблицей удельной теплоты сгорания топлива;
- сравнивать удельную теплоту сгорания топлива различных веществ и энергию, выделяющуюся при сгорании различных видов топлива.

Обучающиеся должны применять:
- формулу для вычисления энергии, которая выделилась при сгорании топлива.
Тип урока: урок изучения нового материала.
Оборудование: свеча, тарелка, стакан, листок растения, сухое горючее, 2 спиртовки, бензин, спирт, 2 пробирки с водой.
Ход урока
1. Оргмомент.
Приветствие учащихся, проверка готовности к уроку.
Известно, что великий ученый М. В. Ломоносов ещё в 1744 г работал над трактатом «Размышления о причине теплоты и холода». Тепловые явления играют огромную роль в окружающем нас мире, в жизни человека, растений, животных, а также в технике.
Давайте проверим, насколько хорошо вы усвоили эти знания.
2. Мотивация к учебной деятельности.
Есть ли у вас вопросы по домашнему заданию? Давайте проверим, как вы справились с ним:
- двое учащихся представляют решение домашних задач на доске.
1) Определите абсолютную влажность воздуха в кладовке объемом 10 м 3 , если в нем содержится водяной пар массой 0,12 кг.
2) Давление водяного пара в воздухе равно 0,96 кПа, относительная влажность воздуха 60 %. Чему равно давление насыщенного водяного пара при той же температуре?
- 1 ученик (Дима) на доске заполняет схему;
задание: подпишите около каждой стрелки название процессов и формулу для расчета количества теплоты в каждом из них
- А пока ребята работают у доски, мы с вами выполним другое задание.
Посмотрите на текст, изображенный на слайде, и найдите в нем физические ошибки, которые допустил автор (предложите правильный ответ):
1) В яркий солнечный день ребята отправились в поход. Чтобы было не так жарко, ребята оделись в темные костюмы. К вечеру стало свежо, но после купания стало теплее. Ребята налили себе горячий чай в железные кружки и с удовольствием пили его, не обжигаясь. Было очень здорово.
Ответ: темное больше поглощает тепла; при испарении температура тела понижается; теплопроводность металлов больше, поэтому он нагревается сильнее.
2) Проснувшись раньше обычного, Вася сразу вспомнил, что на восемь утра договорился с Толей идти на речку смотреть ледоход. Вася выбежал на улицу, Толя был уже там. «Вот погодка сегодня! – вместо приветствия восхищённо произнёс он. – Солнце какое, а температура с утра -2 градуса по Цельсию.» «Нет, -4», возразил Вася. Мальчики заспорили, потом сообразили, в чём дело. «У меня термометр на ветру, а у тебя в укромном месте, поэтому твой и показывает больше», – догадался Толя. И ребята побежали, шлёпая по лужам.
Ответ: при наличии ветра испарение происходит интенсивнее, поэтому первый термометр должен показывать температуру ниже; при температуре ниже 00С вода замерзает.
Молодцы, все ошибки нашли верно.
Давайте проверим правильность решения задач (ученики, решавшие задачи, комментируют свое решение).
А теперь давайте проверим, как Дима справился со своим заданием.
Все ли фазовые переходы Дима назвал верно? А что произойдет, если в пламя поместить деревянную палочку? (Она будет гореть)
Вы верно заметили, что происходит процесс горения.
Наверное, вы уже догадались, о чем мы сегодня с вами будем говорить (выдвигают гипотезы).
Как вы думаете, на какие вопросы мы сможем ответить в конце урока?
- понять физический смысл процесса сгорания;
- узнать, от чего зависит количество теплоты, выделяющееся при сгорании;
- выяснить применение данного процесса в жизни, в быту и т.д.
3. Новый материал.
Каждый день мы можем наблюдать, как сгорает природный газ в горелке плиты. Это и есть процесс сгорания топлива.
Опыт №1. Свеча закреплена на дне тарелки с помощью пластилина. Зажжём свечу, затем закроем её банкой. Несколько мгновений спустя пламя свечи погаснет.
Создаётся проблемная ситуация, при решение которой учащиеся делают вывод: свеча горит при наличии кислорода.
Вопросы к классу:
— Чем сопровождается процесс горения?
— Почему свеча гаснет? Каковы условия, при которых идет процесс горения?
— За счёт чего выделяется энергия?
Для этого вспомним строение вещества.
— Из чего состоит вещество? (из молекул, молекулы из атомов)
— Какими видами энергии обладает молекула? (кинетической и потенциальной)
— А можно ли молекулу разделить на атомы? (да)
Чтобы разделить молекулы на атомы, необходимо преодолеть силы притяжения атомов, а значит, совершить работу, то есть затратить энергию.
При соединении атомов в молекулу энергия, наоборот, выделяется. Такое соединение атомов в молекулы происходит и при сжигании топлива. Обычное топливо содержит углерод. Вы верно определили, что без доступа воздуха горение невозможно. При горении атомы углерода соединяются с атомами кислорода, которые содержатся в воздухе, при этом образуется молекула углекислого газа и выделяется энергия в виде тепла.
А теперь давайте проведем опыт и посмотрим одновременное горение нескольких видов топлива: бензина, сухого горючего, спирта и парафина (Опыт №2).
Что общего и чем отличается горение каждого вида топлива?
Да, при сгорании любых веществ образуются другие вещества-продукты сгорания. Например ,при сгорании дров остается зола и выделяется углекислый ,угарный и другие газы.
Например ,при сгорании дров остается зола и выделяется углекислый ,угарный и другие газы.
Но, главное предназначение топлива – давать тепло!
Давайте рассмотрим еще один опыт.
Опыт №3: (на двух одинаковых спиртовках: одна заполнена бензином, другая спиртом, нагревается одинаковое количество воды).
Вопросы по опыту:
— За счет какой энергии нагревается вода?
— А как определить количество теплоты, которое пошло на нагревание воды?
— В каком случае вода быстрее закипела?
— Какой вывод можно сделать из опыта?
— Какое топливо, спирт или бензин, выделило больше тепла при полном сгорании? (бензин больше тепла, чем спирт).
Учитель: Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется удельной теплотой сгорания топлива, обозначается буквой q. Единица измерения Дж/кг.
Удельную теплоту сгорания определяют на опыте довольно сложными приборами.
Результаты опытных данных приведены в таблице учебника (стр.128) .
Давайте поработаем с этой таблицей.
Вопросы по таблице:
- Чему равна удельная теплота сгорания бензина? (44 МДж/кг)
- Что это означает? (Это значит, что при полном сгорании бензина массой 1 кг выделяется 44 МДж энергии).
- У какого вещества наименьшая удельная теплота сгорания? (дрова).
- Какое топливо при сгорании дает больше всего количества теплоты? (водород, т.к. его удельная теплота сгорания больше остальных).
- Сколько выделяется количества теплоты при сгорании 2 кг спирта? Как вы это определили?
- Что же нужно знать, чтобы рассчитать количество теплоты, выделяющееся при сгорании?
Делают вывод, что для нахождения количества теплоты нужно знать не только удельную теплоту сгорания топлива, но и его массу.
Значит, общее количество теплоты Q (Дж), выделяемое при полном сгорании m (кг) топлива, вычисляется по формуле: Q = q · m
Запишем в тетрадь.
А как найти из этой формулы массу сгораемого топлива?
Выразите из формулы удельную теплоту сгорания. (Можно вызвать ученика к доске для записи формул)
Физкультминутка
Мы устали. Давайте немного разомнемся. Выпрямите спину. Расправьте плечи. Я буду называть топливо, а вы если считаете, что оно твердое, опускаете голову вниз, если жидкое, то поднимаете руки вверх, а если газообразное — тянете руки вперед.
Природный газ – газообразное.
Коксовальный газ – газообразное.
Молодцы! Самый внимательный и спортивный у нас… Садитесь.
Учитель: Ребята! Давайте подумаем над вопросом: «Процесс сгорания человеку друг или враг?»
Опыт №4. Повторим опыт с горящей свечей, но теперь рядом со свечей положим листок растения.
Посмотрите, что произошло с растением рядом с пламенем свечи?
Т.о. при использовании топлива не нужно забывать и про вред продуктов сгорания для живых организмов.
4. Закрепление.

Ребята, а скажите мне пожалуйста, а что для нас с вами является топливом? В человеческом организме роль горючего играет пища. Разные виды пищи, как и разные виды топлива, содержат различный запас энергии. (Показать таблицу на компьютере “Удельная теплота сгорания пищевых продуктов”).
Удельная теплота сгорания топлива q, МДж/кг
Для расчёта этой энергии используют физическую величину, называемую удельная теплота сгорания топлива. Удельная теплота сгорания топлива показывает, какая энергия выделяется при сгорании единичной массы топлива.
Её обозначают латинской буквой q. В системе СИ единица измерения этой величины Дж/кг. Отметим, что каждое топливо имеет собственную удельную теплоту сгорания. Эта величина измерена практически для всех видов топлива и при решении задач определяется по таблицам.
Например, удельная теплота сгорания бензина 46 000 000 Дж/кг, керосина такая же, этилового спирта 27 000 000 Дж/кг. Нетрудно понять, что энергия, выделившаяся при сгорании топлива, равна произведению массы этого топлива и удельной теплоты сгорания топлива:
Задачи на расчет количества теплоты с решениями
Есть тут те, кто хочет научиться решать задачи и щелкать их, как орешки? Наш совет: практикуйтесь с различными заданиями побольше! А мы поможем и в этой статье дадим вам несколько примеров решения задач на тему «расчет количества теплоты».
Подписывайтесь на наш телеграм-канал, чтобы не только решать задачи, но и просто быть в курсе актуальных новостей студенческой жизни.
Задачи на количество теплоты
Для начала, запомним, что количество теплоты обозначается буквой Q. Кроме того, не забываем держать под рукой общую памятку по решению физических задач и список полезных формул. Но сначала, конечно же, читаем теорию в старых советских учебниках или в нашем отдельном материале по термодинамике.
Задача №1. Нахождение количества теплоты
Условие
Водород массой 20 г был нагрет на 100 градусов Цельсия при постоянном давлении. Найти количество теплоты, переданное газу.
Решение
Будем использовать первое начало термодинамики, согласно которому:
Изменение внутренней энергии дельта U вычисляется по формуле (газ считаем двухатомным):
Работа газа при изобарном процессе равна:
Теперь можно вычислить количество теплоты:
Ответ: 29085 Дж.
Задача №2. Количество теплоты, пример цикла Карно
Условие
В ходе цикла Карно рабочее вещество совершает работу, равную 113333 Дж. Температуры нагревателя и холодильника соответственно равны 450 К и 280 К. Какое количество теплоты рабочее тело получает от нагревателя в ходе цикла?
Решение
По определению, КПД цикла Карно:
Можно записать:
Ответ: 300 кДж.
Задача №3. Расчет количества теплоты, теплоемкость
Условие
Определить количество теплоты, необходимое для нагревания 4 литров воды в алюминиевой кастрюле массой 500 г от 30 градусов Цельсия до кипения.
Решение
Это типичная задача на вычисление количества теплоты. Искомое количество теплоты складывается из количества теплоты для нагревания кастрюли и количества теплоты, которое пойдет на нагревание воды. Запишем уравнение теплового баланса:
Запишем выражения для количества теплоты и массы воды:
Вычислим, пользуясь табличными значениями для теплоемкостей:
Ответ: 1380,8 кДж
Задача №4.
 Молярная теплоемкость вещества
Молярная теплоемкость вещества Условие
Вычислить молярные теплоёмкости газа, масса киломоля которого равна M = 30 г/моль, а отношение теплоёмкостей (Cp/Cv) = γ = 1,4.
Решение
Молярная теплоёмкость газа при p = const находится из уравнения Майера:
Молярная теплоёмкость газа при V = const находится из выражения:
Первое выражение можно переписать в виде:
Здесь R – универсальная газовая постоянная, R=8,31 Дж/(К* моль).
Ответ: 29,085 Дж/(К*моль); 20,775 Дж/(К*моль).
Задача №5. Количество теплоты
Условие
На сколько градусов изменилась температура чугунной детали массой 12 кг, если при остывании она отдала 648 кДж теплоты?
Решение
Это простая задача, которая решается в одно действие:
Ответ: 100 градусов Цельсия.
Кстати! Для всех наших читателей действует скидка 10% на решение задач по физике на количество теплоты и любые другие виды работ.
Вопросы по теме «количество теплоты»
Вопрос 1. В чем измеряется количество теплоты?
Ответ. В системе СИ единицей измерения количества теплоты является 1 Джоуль.
Теплота – это мера энергии, которая передается при теплообмене, поэтому она измеряется в тех же единицах.Существуют также внесистемные и широко применяемые единицы измерения количества теплоты:
- калория;
- килокалория.
1 калория равна 4,19 Дж.
Объясним на примере, как рассчитывают количество теплоты. Допустим, есть брусок из какого-то вещества, который нагревают от температуры Т1 до температуры Т2. Количество теплоты, которое для этого нужно, можно определить по формуле:
Здесь с – удельная теплоемкость вещества
Вопрос 2. Что такое теплоемкость?
Что такое теплоемкость?
Ответ. По определению:
Теплоемкость – это скалярная физическая величина, которая показывает, какое количество теплоты нужно сообщить телу, чтобы нагреть его на один градус.
Удельная теплоемкость – это теплоемкость, отнесенная к единице массы. Именно значения удельной теплоемкости указаны в таблицах. Например, удельная теплоемкость воды равна 4200 Дж/(К*кг). Это значит, что для нагрева одного килограмма воды на один градус понадобится 4200 Джоулей.
Вопрос 3. Какие есть единицы измерения температуры?
Ответ. В системе СИ температура измеряется в Кельвинах. В быту мы привыкли к шкале Цельсия, которая наряду со шкалой Кельвина применяется в системе СИ. Также широко известна температурная шкала Фаренгейта, используемая в Англии и США.
Связь между температурой в Кельвинах и Цельсиях можно выразить формулой:
Температура кипения воды по шкале Фаренгейта равна 212 градусам, а лед тает при 32 градусах по Фаренгейту. Один градус Фаренгейта равен 1/180 разности этих температур.
Один градус Фаренгейта равен 1/180 разности этих температур.Вопрос 4. Дайте определение температуры:
Ответ. Температура – это физическая величина, характеристика термодинамической системы, описывающая степень нагретости тел.
Вопрос 5. Какие виды теплопередачи вы знаете?
Ответ. Есть следующие виды теплопередачи:
- Теплопроводность – переход теплоты от более нагретых участков твердых тел к более холодным.
- Конвекция – передача теплоты потоками газа или жидкости.
- Излучение – теплота передается посредством электромагнитных волн.
Кстати, если у вас есть какой-то вопрос, вы всегда можете задать его в комментариях или обратиться за помощью к специалистам профессионального студенческого сервиса, которые всегда смогут вычислить удельную теплоемкость и рассчитать количество теплоты при теплообмене.
8 класс. Конспект урока №07/07.
 Расчёт количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении.
Расчёт количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении.Физика.
8 класс.
Урок №07/07.
Расчёт количества теплоты, необходимого для нагревания тела
или выделяемого им при охлаждении.
Цель урока. Вывести формулу для расчёта количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении.
Демонстрация. Устройство калориметра.
Содержание нового материала. Формула для расчёта количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении. Единицы количества теплоты. Устройство и применение калориметра.
Планируемые результаты обучения.
Метапредметные: овладеть регулятивными универсальными учебными действиями при решении задач на нахождение количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении; развивать монологическую и диалогическую речь; применять теоретические знания о количестве теплоты при решении задач; оценивать результаты своих действий; излагать информацию в словесной и символической форме; работать в парах.
Личностные: осознать необходимость самостоятельного приобретения знаний о количестве теплоты и практической значимости изученного материала; сформировать познавательный интерес; развивать творческие способности и практические умения при нахождении количества теплоты, уважительное отношение друг к другу, к учителю.
Общие предметные: применять знания об удельной теплоемкости при решении задач на расчет количества теплоты; обнаруживать зависимость изменения внутренней энергии нагревающих тел и внутренней энергии остывающих тел при теплообмене; кратко и чётко отвечать на вопросы; объяснять полученные результаты и делать выводы; использовать знания для объяснения принципа работы калориметра при решении практических задач.
Частные предметные: объяснять явление теплообмена, рассчитывать количество теплоты; использовать знания о количестве теплоты в повседневной жизни.
Ход урока.
1. Опрос.
1. Что понимают под внутренней энергией тела?
(Кинетическая энергия всех молекул, из которых состоит тело, и потенциальная энергия их взаимодействия составляют внутреннюю энергию тела.
)
2. Каким образом можно изменить внутреннюю энергию тела?
(1. Путём совершения механической работы.
2. Путём теплопередачи.)
3. Что такое количество теплоты?
(Энергия, которую получает или теряет тело при теплопередаче, называется количеством теплоты.)
4. Что понимают под удельной теплоёмкостью вещества?
(Физическая величина, численно равная количеству теплоты, которое необходимо передать телу массой 1кг для того, чтобы его температура изменилась на 1°C, называется удельной теплоёмкостью вещества.)
5. Удельная теплоёмкость растительного масла равна 700Дж/(кг•°С). Что это означает?
(Для нагревания растительного масла массой 1кг на 1°C, необходимо количество теплоты, равное 700Дж.)
(При охлаждении растительного масла массой 1кг на 1°C, выделится количество теплоты, равное 700Дж.)
2. Упражнение 7.
1. Удельная теплоёмкость свинца равна . Что это означает?
(Для нагревания свинца массой 1кг на 1°C, необходимо количество теплоты, равное 140Дж.)
(При охлаждении свинца массой 1кг на 1°C, выделится количество теплоты, равное 140Дж.)
2. Для нагревания 1кг золота на 1°С требуется 130Дж. Какова удельная теплоёмкость золота?
)
3. Изучение нового материала.
1. Учащимся известно, что количество теплоты, необходимое для нагревания (или выделяющееся при остывании тела), зависит от массы тела, разности температур и рода вещества, из которого изготовлено тело. Вывод формулы следует сделать на примере.
После проведённых рассуждений можно дать задание одному из учащихся подставить данные в формулу и рассчитать количество теплоты.
2. Далее для закрепления материала учащиеся в парах анализируют примеры решения задач из учебника, один из учеников у доски (по желанию) записывает её условие и объясняет решение.
Притер 1.
В железный котёл массой 5кг налита вода массой 10кг. Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10°С до 100°С?
Пример 2.
Смешали воду массой 0,8кг, имеющую температуру 25°С, и воду при температуре 100°С массой 0,2кг. Температуру полученной смеси измерили, и она оказалась равной 40°С. Вычислите, какое количество теплоты отдала горячая вода при остывании и получила холодная вода при нагревании. Сравните эти количества теплоты.
При смешивании горячей и холодной воды происходит теплообмен не только с холодной водой, но и с окружающей средой — сосудом, подставкой, термометром, воздухом. На практике не всю внутреннюю энергию, отдаваемую горячей водой, получает холодная. Чтобы устранить такие потери или свести их хотя бы к минимуму, применяют специальный прибор — калориметр (от лат. color — тепло и meter — измерять).
Учитель знакомит учащихся с этим прибором, принципом его действия, основными элементами и способом использования в предстоящей лабораторной работе.
Калориметр состоит из двух сосудов, разделённых воздушным промежутком. Дно внутреннего сосуда отделено от внешнего пластмассовой подставкой. Такое устройство позволяет уменьшать теплообмен содержимого внутреннего сосуда с внешней средой.
Вывод:
«Количество теплоты, отданное горячей водой, и количество теплоты, полученное холодной водой, равны между собой.
Если между телами происходит теплообмен, то внутренняя энергия всех нагревающихся тел увеличивается на столько, на сколько уменьшается внутренняя энергия остывающих тел.»
4. Закрепление материала.
1. Что такое «количество теплоты»?
Энергия, которую получает или теряет тело при теплопередаче, называется количеством теплоты.
2. В каких единицах выражают количество теплоты?
[Q]=1Дж
3. От чего зависит количество теплоты, выделяемое телом при охлаждении?
Количество теплоты, выделяемое телом при охлаждении, зависит от разности температур тела.
Q~(°t2-°t1)
Количество теплоты, выделяемое телом при охлаждении, зависит от его массы.
Q~m
Количество теплоты, выделяемое телом при охлаждении, зависит от того, из какого вещества оно состоит, то есть от рода вещества.
Q~c
4. Формула для расчёта количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении.
Q=cm(°t2-°t1)
5. Для чего служит калориметр?
Калориметр состоит из двух сосудов, разделённых воздушным промежутком. Дно внутреннего сосуда отделено от внешнего пластмассовой подставкой. Такое устройство позволяет уменьшать теплообмен содержимого внутреннего сосуда с внешней средой.
5. Домашнее задание.
§9.
Упражнение 8.
Подготовиться к лабораторной работе 1 (тетрадь для лабораторных работ).
Глава 14. Термодинамика
Изучение энергетических превращений в молекулярных системах составляет содержание термодинамики. Для решения задач на термодинамику необходимо знать определения внутренней энергии, количества теплоты, теплоемкости и ряда других величин. Необходимо также понимать и уметь использовать в простейших случаях первый закон термодинамики как балансовое соотношение, описывающее процессы превращения энергии из одних форм в другие. Также нужно знать основные свойства процессов перехода вещества из одних агрегатных состояний в другие. Рассмотрим эти вопросы.
Внутренней энергией тела называется сумма кинетической энергии молекул и потенциальной энергии их взаимодействия друг с другом. Для жидкостей и твердых тел из-за сильного взаимодействия молекул друг с другом вычислить внутреннюю энергию не удается. Внутреннюю энергию можно вычислить только для идеальных газов, в которых можно пренебречь энергией взаимодействия молекул друг с другом и считать, что внутренняя энергия равна сумме кинетических энергий молекул. Для одноатомного газа (т.е. газа, каждая молекула которого состоит из одного атома) внутренняя энергия определяется соотношением
(14.1) |
где — количество вещества газа (число молей), — универсальная газовая постоянная, — абсолютная температура. Заметим, что с помощью закона Клапейрона-Менделеева формула (14.1) может быть преобразована к виду
(14.2) |
где — давление, — объем газа.
Внутренняя энергия тела может измениться при теплообмене, когда молекулы тела сталкиваются с более быстрыми или более медленными молекулами других тел и получают от них или отдают им энергию, или в процессе совершения механической работы над этим телом внешними силами. В связи с эти вводят следующие определения. Количеством теплоты, переданным некоторому телу, называют энергию, переданную этому телу в процессе хаотических столкновений молекул. Процесс передачи энергии в виде теплоты называют процессом теплопередачи. Если внешние силы не совершают над телом работы, для процесса теплопередачи справедливо следующее балансовое соотношение
(14.3) |
где — изменение внутренней энергии тела, — количество переданной этому телу теплоты. Поскольку изменение внутренней энергии тела может быть и положительным , и отрицательным , из закона (14.3) следует, что количеству теплоты следует придать алгебраический смысл: если энергия передается телу, количество переданной этому телу теплоты нужно считать положительным , если забирается — отрицательным .
Внутренняя энергия тела изменяется при сжатии тела, трении и ряде других механических процессах. В этом случае на изменение внутренней энергии расходуется работа , совершаемая над телом внешними силами
(14.4) |
(конечно, здесь подразумевается, что работа не расходуется на энергию движения тела как целого, а только на изменение внутреннего движения, т.е. все перемещения тела как целого или его макроскопических частей должны происходить бесконечно медленно). Очевидно, работа внешних сил положительна, если эти силы сжимают тело и его объем уменьшается, и отрицательна — если объем тела увеличивается. В первом случае, как это следует из (14.4), внутренняя энергия тела возрастает (), во втором убывает ().
Одновременно с внешними силами при сжатии или расширении тел совершают работу и сами эти тела. Рассмотрим, например, газ, находящийся в цилиндрическом сосуде и отделенный от атмосферы поршнем (см. рисунок). И при сжатии, и при расширении газа силы, действующие на поршень со стороны газа, совершают над ним работу (в первом случае отрицательную, во втором положительную). При этом, поскольку поршень перемещается бесконечно медленно, силы, действующие на него со стороны газа и внешние силы практически равны друг другу как при сжатии, так и при расширении газа (в противном случае в балансе энергии необходимо было учитывать кинетическую энергию, приобретенную поршнем). Поэтому работа, совершенная газом и внешними силами над газом равны по величине, но отличаютсязнаком1. Очевидно, работа газа положительна, если газ расширяется, и отрицательна, если газ сжимается.
При решении задач на термодинамику следует помнить одно важное свойство работы газа, которое во многих случаях позволяет ее легко вычислить. Работа газа в некотором процессе численно равна площади фигуры под графиком зависимости давления от объема в этом процессе. В частности в изобарическом процессе при давлении , в котором объем газа изменился от значения до значения , газ совершает работу (см. рисунок; площадь графика, соответствующая работе, выделена):
(14.5) |
где — количество вещества газа, — изменение температуры в рассматриваемом процессе.
Если газ участвует в процессе, в котором одновременно имеет место и теплообмен, и совершается работа, то справедливо соотношение
(14.6) |
которое называется первым законом термодинамики (здесь — работа газа).
Закон (14.6) позволяет найти одну из входящих в него величин, если заданы две других. Если задается только одна из величин, входящих в закон (14.6), но как-то определяется процесс, происходящий с газом, то две остальные величины могут быть определены. Например, в изохорическом процессе не совершается работа, поэтому
(14.7) |
В изотермическом процессе не меняется внутренняя энергия газа, поэтому
(14.8) |
В адиабатическом процессе (процессе без теплообмена с окружающей средой) , поэтому
(14.9) |
В изобарическом процессе есть связь между изменением внутренней энергии газа и его работой. Из формул (14.1) и (14.5) заключаем, что работа одноатомного идеального газа и изменение его внутренней энергии в изобарическом процессе связаны соотношением
(14.10) |
Для характеристики процессов нагрева-остывания тела вводят понятие теплоемкости тела , которая определяется как
(14.11) |
где — количество теплоты, сообщенное телу в некотором процессе, — изменение его температуры в этом процессе. Подчеркнем, что и в формуле (14.11) не независимы, а связаны друг с другом: — это то изменение температуры, которое происходит благодаря сообщению телу количества теплоты . Поэтому теплоемкость (14.11) не зависит от и , а зависит от свойств тела и происходящего с ним процесса.
Если тело однородно, то его теплоемкость пропорциональна его массе . Поэтому отношение является характеристикой вещества тела и называется его удельной теплоемкостью. Удельная теплоемкость представляет собой экспериментально измеряемую (табличную) характеристику веществ. Из определения удельной теплоемкости следует, что если телу массой , изготовленному из вещества с удельной теплоемкостью , сообщить количество теплоты , то будет справедливо соотношение
(14.12) |
где — изменение температуры тела.
Приведем теперь решения данных в первой части задач.
В задаче 14.1.1 внутренняя энергии газа увеличится согласно формуле (14.1) — ответ 1.
Для ответа на вопрос задачи 14.1.2 удобно использовать формулу для внутренней энергии газа в виде (14.2). По этой формуле находим, что внутренняя энергия увеличилась в 3/2 раза (ответ 2). Обратим внимание читателя, что причина изменения давления и объема может быть любой — ответ от этого не зависит. Может измениться или температура газа, или количество вещества, или и то и другое одновременно.
Поскольку температура и количество вещества газа не изменялись в рассматриваемом в задаче 14.1.3 процессе, внутренняя энергия газа не изменилась (ответ 3).
В задаче 14.1.4 следует воспользоваться определением теплоемкости (14.11). Для этого рассмотрим, например, ин-тервал времени , выделенный жирным на оси времени (см. рисунок). За этот интервал оба тела получили одинаковое количество теплоты , поскольку нагреватели одинаковы. Изменение температур тел и можно определить по графику — эти величины отмечены фигурными скобками на оси температур. Поскольку из формулы (14.11) заключаем, что — ответ 2.
В задаче 14.1.5 следует воспользоваться определением удельной теплоемкости. По формуле (14.12) находим
(ответ 1).
Для совершения работы необходимо механическое движение. Поскольку объем газа в задаче 14.1.6 не меняется, механическое движение отсутствует, работа газа равна нулю (ответ 4).
Применяя к рассматриваемому в задаче 14.1.7 процессу первый закон термодинамики (14.6) и учитывая, что в изохорическом процессе работа газа равна нулю, заключаем, что (ответ 3).
В изотермическом процессе не меняется внутренняя энергия идеального газа. Поэтому , и работа , совершенная над газом, определяется соотношением (14.4), (14.6): (задача 14.1.8 — ответ 2).
Адиабатический процесс происходит без теплообмена с окружающими телами: . Поэтому из первого закона термодинамики (14.6) получаем в задаче 14.1.9 для работы газа (ответ 2).
Применяя первый закон термодинамики (14.6) к процессу, происходящему с газом в задаче 14.1.10, найдем, что внутренняя энергия газа увеличилась на 10 Дж (ответ 2).
Для решения задачи 14.2.1 можно использовать то обстоятельство, что работа газа численно равна площади фигуры, ограниченной графиком зависимости давления от объема и осью объемов. Из рисунка следует, что наибольшей является площадь под графиком процесса 1. Поэтому бóльшую работу газ совершает в процессе 1 (ответ 1).
В задаче 14.2.2 следует применить ко всем трем процессам, графики которых даны на рисунке к решению предыдущей задачи, первый закон термодинамики (14.6) . Учитывая, что начальная и конечная температура газа во всех трех процессах одинакова, и, следовательно, одинаковы изменения внутренней энергии газа , а работа наибольшая в процессе 1 (см. решение предыдущей задачи), заключаем, что газ получил большее количество теплоты в процессе 1 (ответ 1).
Работа газа положительна, если газ расширяется. Для доказательства этого утверждения представим газ в сосуде, ограниченном подвижным поршнем. Если газ расширяется, то и перемещение поршня и сила, действующая на него со стороны газа, направлены одинаково, поэтому работа газа положительна. При сжатии газа его работа отрицательна. Поэтому в задаче 14.2.3 работа газа положительна в процессе 3 (ответ 3).
Так как графики процессов 1–2 и 3–4 в задаче 14.2.4 — прямые, проходящие через начало координат, эти процессы — изохорические, и газ не совершает в них работу. А поскольку изменение внутренней энергии газа в этих процессах одинаково, то одинаковы и количества теплоты, сообщенные газу в этих процессах (ответ 3).
Задача 14.2.5 аналогична предыдущей. Рассматриваемый процесс — изохорический, поэтому изменение внутренней энергии газа равно сообщенному количеству теплоты = 100 кДж (ответ 2).
Вычисляя площадь под графиком процесса в задаче 14.2.6, находим работу газа (ответ 2).
В условии задачи 14.2.7 дано количество теплоты , которое забрали у газа. Первый закон термодинамики, в который входит эта величина, имеет вид
где — работа, совершенная над газом в рассматриваемом процессе. Подставляя в эту формулу данные в условии величины, находим = –5 Дж (ответ 1).
Чтобы понять, расширялся или сжимался газ в рассматриваемом в задаче 14.2.8 процессе, из первого закона термодинамики найдем работу газа: если она окажется положительной, газ расширялся, если отрицательной — сжимался. Из закона (14.6) находим
Поэтому газ сжимался (ответ 1).
Чтобы найти долю количества теплоты, которая пошла на увеличение внутренне энергии газа в изобарическом процессе (задача 14.2.9) воспользуемся формулой (14.5) для работы газа в этом процессе . Поскольку изменение внутренней энергии одноатомного идеального газа равно , заключаем, что изменение внутренней энергии газа составляет 3/2 от его работы. Поэтому 2/5 количества теплоты, сообщенного газу в изобарическом процессе тратится на работу, 3/5 — на изменение внутренней энергии газа (ответ 3).
Чтобы найти теплоемкость газа в изотермическом процессе (задача 14.2.10), применим к этому процессу определение теплоемкости (14.11)
Поскольку в изотермическом процессе при ненулевом количестве сообщенной теплоты, то теплоемкость газа равна бесконечности. Это означает следующее — в изотермическом процессе газу сообщают теплоту, а он не нагревается, что и означает бесконечную теплоемкость газа (теплота расходуется только на совершение работы).
Удельная теплоемкость – Концепция – Видео по химии от Brightstorm
Хорошо, давайте поговорим об удельной теплоемкости, которую мы будем обозначать буквой c. Это количество тепла, необходимое для повышения температуры 1 грамма вещества на 1 градус Цельсия или 1 Кельвин. Причина, по которой они могут быть заменены местами, заключается в том, что они имеют одинаковые значения приращения, которые они могут переключать. Итак, когда мы говорим о тепле, мы на самом деле измеряем тепло и энергию, и давайте поговорим о числах, которые вы на самом деле будете видеть в единицах измерения, поэтому мы измеряем энергию в калориях или джоулях.Итак, 1 калория равна 4,184 джоулей, но это не та калория, которую вы видите на этикетке продукта, это на самом деле калория с заглавной буквой C, что на самом деле 1 килограмм калорий, а это – тысяча калорий или 4 184 джоулей. Итак, понимая, что означают эти числа, когда говорят о тепле, давайте вернемся к разговору об удельной теплоемкости, которая измеряется в джоулях на грамм градусов Цельсия.
Давайте поговорим об удельной теплоемкости воды, вода имеет удельную теплоемкость 4,184 джоулей на грамм градусов Цельсия и что это значит? Это означает, что на каждый грамм воды, которую вы хотите поднять на 1 градус по Цельсию, требуется 4.184 джоулей энергии. На самом деле это относительно много по сравнению с остальными данными в этой таблице и с большинством веществ. Это потому, что для нагрева воды требуется много энергии, если вы думаете о том, когда вы кипятите воду на плите или о чем-то, что на самом деле требуется много времени и много тепла, чтобы она действительно поднялась, перешла из жидкого состояния в до достижения газообразного состояния. Удельная теплоемкость льда на самом деле различается для каждого состояния вещества, поэтому для повышения температуры льда потребуется всего 2 секунды.03 джоулей тепла, чтобы поднять 1 грамм вещества на 1 градус Цельсия.
Точно так же и с паром, для этого требуется всего 2,01, поэтому для повышения температуры льда или пара требуется вдвое меньше энергии по сравнению с водой. Алюминий также относительно высок по сравнению с другими металлами. Металлы обычно имеют очень низкую удельную теплоемкость. Но алюминий на самом деле довольно высокий – 0,897 джоулей на грамм градуса Цельсия, поэтому, чем ниже значение, тем легче ему нагреться. Хорошо, когда мы используем это в настоящих формулах и на самом деле говорим о количестве необходимого тепла или о том, насколько изменилась температура или какая масса нам нужна для определенных веществ.Итак, мы собираемся использовать эту формулу, q равно mc delta t или q равно m cad. q означает, когда мы говорим о тепле, является символом тепла и обычно измеряется в джоулях, может быть измерено в килоджоулях или калориях, которые не имеют значения, но это q представляет количество необходимого тепла или требуемого тепла или энергия.
м – это наш символ массы, который обычно измеряется в граммах, c – наша удельная теплоемкость этого конкретного вещества, а дельта t – это изменение, которое может быть снова, оно может быть в градусах Кельвина или градусах Цельсия, это не имеет значения. потому что это изменение тепла.Теперь поговорим о том, как это влияет на диаграмму фазового перехода. Хорошо, это диаграмма фазового перехода для воды, позвольте мне ее записать. Хорошо, обратите внимание, если вы посмотрите на наклон изменения энергии при повышении температуры твердого тела по сравнению с жидкостью. Обратите внимание, твердое тело имеет более крутой наклон, чем жидкость, это потому, что жидкость требует больше энергии для повышения температуры на грамм, чем твердое тело или газ. На самом деле они более крутые, чем для жидкости, поэтому это также влияет на диаграмму фазового перехода, и это из-за удельной теплоемкости.
Давайте вместе решим проблему и выясним, как это на самом деле влияет на другие вещи. Итак, у нас есть архитектор, и он действительно заинтересован в устойчивой энергетике. Таким образом, архитектор проектирует дом, который частично нагревается солнечной энергией, тепло от солнца будет накапливаться в солнечном пруду, как и в другом бассейне. Итак, у нас есть пруд, с которым мы имеем дело. Он состоит из 14 500 килограммов гранитной породы, а внутри он содержит 22 500 килограммов воды.Хорошо вместе, гранит и вода поглощают тепло днем и выделяют его ночью, а затем ночью отдают тепло в дом, нагревая его ночью. Архитектор обнаружил, что температура солнечного пруда повышается на 22 градуса по Цельсию днем и опускается до 22 градусов по Цельсию ночью. Итак, сколько энергии он выделяет и поглощает в течение дня? Итак, давайте подчеркнем то, что у нас есть, информацию, которая у нас есть.
Давайте начнем с воды, так как у нас есть 2 вещества – гранит и вода, количество энергии, которое на самом деле требуется, общее количество энергии будет равно q гранита плюс q h3O плюс, причем q, как мы знаем, равно mc delta t.Хорошо, давайте сначала займемся водой, хорошо, колодец, колодец, вода, у нас есть масса 22 500 килограммов, и мы хотим, чтобы она была в граммах. Итак, мы сделаем это 2,25 раза по 10 до седьмого грамма, хорошо. C воды или удельная теплоемкость воды составляет 4,184 джоулей на грамм градусов Цельсия. Причина, по которой я хотел это даже в граммах и не мог использовать килограммы, заключается в том, что в моей единице удельной теплоемкости были граммы. Итак, я хочу убедиться, что эти единицы одинаковые, хорошо. Итак, мы собираемся, мы знаем, что это меняет температуру, она увеличивает и понижает температуру на 22 градуса по Цельсию.Итак, у нас изменение температуры составляет 22 градуса по Цельсию.
Хорошо, когда я умножаю все это вместе, я получаю количество энергии, которое требуется или которое поглощается водой солнечного пруда [IB], находящейся в солнечном пруду. Итак, мы умножаем их вместе и получаем 2,1 умножить на 10 до девятых джоулей, и причина в том, что снова удельная теплоемкость измеряется в джоулях или q измеряется в джоулях. Хорошо, давайте поговорим о q для гранита, потому что бассейн состоит из воды и гранита. Масса воды 14, извините, масса гранита 14 500 кг, что составляет 1.45 раз по 10 до седьмого грамма. Q для гранита, если вы посмотрите на нашу таблицу, составляет 0,803 и снова изменяется на 22 градуса по Цельсию. И я просто не ставлю единицы, потому что хочу сэкономить место. Хорошо, когда я умножаю все это вместе, я получаю 2,4, извините, это неправда, мне очень жаль, что я получаю 2,6 умножить на 10 до восьмых джоулей. Итак, общее количество энергии, которое получает этот реальный солнечный бассейн, и это за день, равно 2. Мы собираемся сложить это в 2,4 раза умножить на 10 до девятых джоулей энергии.Так что это на самом деле экономит нам много энергии, когда мы имеем дело, когда мы на самом деле собираемся обогреть или охладить наш дом. Таким образом, мы экономим много денег на устойчивой энергии, используя солнечный бассейн. Таким образом, удельная теплоемкость на самом деле говорит нам о многом, и она уникальна для каждого конкретного вещества, и это количество энергии, необходимое для подъема 1 грамма вещества на 1 градус Цельсия.
Онлайн-калькулятор: Количество тепла
Начнем с пары определений:
- Тепло – это количество энергии, перетекающее от одного тела материи к другому самопроизвольно из-за разницы температур или любым другим способом, кроме работы или передачи материи.Исторически для измерения тепла использовалось много единиц энергии. Единицей измерения в Международной системе единиц (СИ) является джоуль (Дж).
- Теплоемкость или теплоемкость – это измеримая физическая величина, равная отношению тепла, добавленного (или удаленного) к объекту, к результирующему изменению температуры. Удельная теплоемкость, часто называемая просто , удельная теплоемкость – это теплоемкость на единицу массы материала.
Из этого определения имеем следующую формулу для удельной теплоемкости:
,
где c – удельная теплоемкость,
Q – тепло, добавленное или отведенное к телу,
m – масса тела,
ΔT – изменение температуры.
На теплоемкость могут влиять многие переменные состояния, которые описывают исследуемую термодинамическую систему. К ним относятся начальная и конечная температура, а также давление и объем системы до и после добавления тепла. Таким образом, приведенная ниже формула будет несколько более правильной:
Однако в школьных задачах мы обычно используем постоянную удельную теплоемкость при стандартном давлении. Таким образом, взаимосвязь между теплом и изменением температуры обычно выражается в форме, показанной ниже:
Обратите внимание, что это соотношение не применяется, если происходит фазовое изменение, потому что тепло, добавленное или удаленное во время фазового перехода, не изменяет температуру.
Калькулятор ниже может найти пропущенное значение в приведенной выше формуле, если указаны все остальные значения. Он может найти добавленное или отведенное тепло, удельную теплоемкость, массу, начальную или конечную температуру:
Количество тепла
Значение для поиска ТеплоУдельная теплоемкость Масса Начальная температура Конечная температура Точность вычисленияЦифры после десятичной точки: 1
Ссылка Сохранить Виджет
Как рассчитать время нагрева или охлаждения | Блог
Во многих случаях может быть полезно узнать, сколько времени потребуется, чтобы нагреть или охладить вашу систему до определенной температуры.Или вы можете рассчитать, сколько энергии требуется для нагрева или охлаждения данного объема жидкости за определенный промежуток времени.
К счастью, есть довольно простое уравнение, которое можно использовать, если вы знаете массу жидкости в ванне, ее удельную теплоемкость, разницу температур, а также мощность или время.
Тем не менее, использование этого уравнения не совсем надежно, поскольку существуют различные факторы, которые могут нарушить расчет. В этом посте мы рассмотрим уравнение для расчета времени нагрева или охлаждения и причины, по которым вам следует искать систему с чуть большей мощностью, чем вы думаете, что вам нужно.
Расчет времени нагрева или охлаждения
Вы можете использовать то же основное уравнение для расчета времени нагрева или охлаждения, хотя для расчета времени охлаждения требуется немного больше работы. При нагреве подаваемая мощность постоянна, но при охлаждении мощность (или охлаждающая способность) изменяется в зависимости от температуры.
Расчет времени нагрева
Чтобы узнать, сколько времени потребуется для нагрева ванны до определенной температуры, можно использовать следующее уравнение:
t = mcΔT / P
Где:
- т – время нагрева или охлаждения в секундах
- м – масса жидкости в килограммах
- c – удельная теплоемкость жидкости в джоулях на килограмм и на Кельвин
- ΔT – разница температур в градусах Цельсия или Фаренгейта
- P – мощность, при которой подается энергия, в ваттах или джоулях в секунду
Аналогичным образом, чтобы рассчитать мощность, необходимую для нагрева или охлаждения ванны до определенной температуры за заданный промежуток времени, вы можете использовать это уравнение:
P = mcΔT / т
Хотя этим уравнениям довольно просто следовать, может возникнуть некоторая путаница, когда дело доходит до того, какие единицы использовать.Вместо этого вы можете использовать онлайн-калькулятор.
Этот красивый и простой калькулятор позволяет рассчитать время, мощность или потребляемую энергию, но он годится только для расчетов, связанных с водой. Если вам нужно рассчитать время нагрева для других жидкостей, этот калькулятор больше подходит, поскольку он позволяет вам ввести удельную теплоемкость вещества, которое вы используете. У него есть две опции, позволяющие рассчитать либо требуемую мощность, либо необходимое время.
Калькулятор услуг по технологическому отоплению.
Расчет времени охлаждения
Для расчета времени охлаждения вы можете использовать то же уравнение, что и выше. Вопрос в том, какое значение вы должны использовать для мощности. Холодопроизводительность (или мощность охлаждения) зависит от температуры. Холодопроизводительность снижается при более низких заданных температурах, поскольку разница температур между охлаждающей жидкостью и хладагентом меньше. Теплопередача снижается, поэтому снижается охлаждающая способность.
Например, вот характеристики охлаждающей способности для охлаждающих и нагреваемых циркуляционных ванн PolyScience 45 л.
У вас есть несколько вариантов, в зависимости от того, насколько точно вы хотите, чтобы ваш расчет был:
- Используйте консервативную оценку , предполагая более низкую мощность до следующей указанной температуры. Например, принимая указанные выше характеристики, вы можете предположить, что охлаждающая способность составляет 250 Вт для всех температур от -20 ° C до 0 ° C и 800 Вт для всех температур от 0 ° C до 20 ° C.
- Возможно заниженная оценка, но с большей точностью. путем измерения средней мощности между различными температурами.
- Используйте быстрый и грязный (и, вероятно, менее точный) метод , учитывая только охлаждающую способность при средней температуре.
- Выбирайте альтернативный быстрый метод , который использует средние значения холодопроизводительности в различных точках диапазона температур (точки должны включать верхний и нижний пределы диапазона температур, чтобы это было жизнеспособным).
Что делать, если ваша минимальная температура ниже минимальной указанной температуры холодопроизводительности? Как правило, это не должно вызывать беспокойства, поскольку значения холодопроизводительности обычно указываются для температуры, равной или ниже минимальной температуры агрегата.
Если вы пытаетесь охладить до более низкой температуры, она может быть слишком низкой, а это значит, что устройство не сможет обеспечить необходимую вам охлаждающую способность. Однако, если в технических характеристиках не указана охлаждающая способность при температуре, близкой к минимальной температуре устройства, вы можете попросить производителя или нас предоставить необходимую информацию.
Факторы, которые следует учитывать при расчете времени нагрева или охлаждения
Как уже упоминалось, есть несколько причин, по которым ваши расчеты могут не дать реалистичного результата.Таким образом, если вы используете это уравнение для определения времени нагрева или охлаждения, вы должны предположить, что процесс займет немного больше времени, чем ожидалось. Точно так же, если вы используете расчет, чтобы определить, сколько энергии вам нужно для достижения заданного времени нагрева или охлаждения, вы должны предположить, что потребуется некоторая дополнительная мощность.
Вот факторы, которые необходимо учитывать:
1. Повышение или потеря тепла окружающей среды
Прирост или потеря тепла из-за окружающей среды неизбежны даже в закрытой системе.Охлаждаемая система может поглощать тепло из окружающего воздуха или компонентов системы, снижая ее охлаждающую способность. В системе отопления вы можете терять тепло в окружающий воздух или компоненты системы, например, когда оно проходит по трубам или трубам.
Изоляция вашей системы и контроль температуры окружающей среды могут помочь, но все же может быть неизвестное количество тепла.
2. Потери жидкости из-за испарения
Если вы работаете с открытой системой, вы можете потерять часть жидкости из-за испарения во время процесса нагрева или охлаждения.Количество происходящего испарения будет зависеть от нескольких факторов, в том числе:
- Какая жидкость вы используете: Жидкости с более низкой точкой кипения, такие как этанол, метанол и вода, могут легко испаряться.
- Площадь поверхности ванны: Чем больше площадь поверхности, тем выше скорость испарения.
- Используемый диапазон температур: Чем выше температура, тем выше скорость испарения.
Потеря тепла происходит из-за испарения, и когда вы тратите тепловую энергию впустую, время, необходимое для нагрева ванны, увеличивается.Кроме того, в результате потери жидкости значение массы (m) в уравнении не будет точным, что может привести к ухудшению результатов. Если вы используете смесь из двух или более жидкостей, и один компонент смеси испаряется быстрее, чем другие, соотношение будет изменено, что приведет к неточности в определении удельной теплоемкости (c).
Испарение трудно предсказать и точно учесть (и если вы достаточно хорошо разбираетесь в термодинамике, чтобы делать это комфортно, вы, вероятно, не читали бы эту статью).Таким образом, лучше всего либо оценить скорость испарения с помощью эмпирического теста, а затем учесть это математически, используя теплоту испарения, либо просто добавить коэффициент безопасности.
3. Проблемы с обслуживанием
В системах отопления на элементах водяной бани часто образуется накипь из-за отложений минералов. При отсутствии контроля это накопление может повлиять на эффективность передачи тепла от элемента к жидкости. Поскольку элемент изолирует накипь, требуется больше энергии для нагрева системы до желаемой температуры.
При нагревании увеличивается время, необходимое для достижения желаемой температуры в системе заданной мощности. Если вы смотрите на мощность, она увеличит количество энергии, необходимое для достижения желаемой температуры за определенное время.
Для систем охлаждения на холодопроизводительность также могут влиять проблемы с обслуживанием. В конденсаторах с водяным охлаждением коррозия, образование накипи или биологический рост могут препятствовать передаче тепла, снижая охлаждающую способность. В конденсаторах с воздушным охлаждением скопление пыли и мусора на лопастях и ребрах вентилятора может уменьшить воздушный поток, что приведет к аналогичному эффекту снижения охлаждающей способности.
Регулярное техническое обслуживание вашего устройства, включая очистку различных компонентов, промывку жидкости и использование ингибитора коррозии, может помочь.
Калькулятор удельной теплоемкости – определение теплоемкости веществ
Онлайн-калькулятор удельной теплоемкости помогает определить удельную теплоемкость, тепловую энергию, массу вещества, начальную и конечную температуры любого вещества. Когда дело доходит до анализа удельной теплоемкости воды или любого другого вещества, он сообщает нам формулу теплоемкости вместе со всем раствором для соответствующего вещества.
Вы попробуете этот калькулятор удельной теплоемкости, чтобы определить теплоемкость нагретого или охлажденного образца.
Хорошо, прочтите данный контекст, чтобы понять, как вычислить удельную теплоемкость (шаг за шагом) и с помощью калькулятора уравнения q = mc∠† t. Но давайте начнем с основ!
Что такое удельная теплоемкость?Это количество тепла, необходимое для изменения температуры единицы массы любого вещества всего на один градус.Чтобы найти удельную теплоемкость, мы можем сказать, что это мера общей энергии, необходимой для нагрева 1 килограмма любого материала до 1 ° Цельсия или 1 Кельвина. Эти явления должны происходить в диапазоне температур, в котором вещество не меняет своего состояния, например в случае воды она не должна закипать.
Для удобства используйте этот бесплатный, но лучший калькулятор закона Ома для расчета напряжения (В) и сопротивления (R). Ток (I) и мощность (P).
Формула удельной теплоемкости:Формула теплоемкости:
$$ C = \ frac {Q} {m \ times \ Delta T} $$
А:
- \ (C \) представляет собой удельную теплоемкость
- \ (Q \) представляет индуцированную тепловую энергию
- \ (м \) представляет собой массу
- \ (\ Delta T \) – разница температур
- \ (J \) – это джоулей
- \ (° C \) – градусы Цельсия или Цельсия
- \ (K \) – кельвинов
Пример:
Если у вас есть кусок любого металла весом \ (15 г \), который поглощает \ (134 Дж \) тепла, увеличиваясь с \ (24.От 0 ° C \) до \ (62,7 ° C \). Как вы рассчитаете его удельную теплоемкость?
- С учетом тепла \ (q = 134 Дж \)
- Заданная масса \ (m = 15,0 г \)
- Изменение температуры: \ (\ Delta T = 62,7 – 24,0 = 38,7 \)
Чтобы найти удельную теплоемкость, введите значения в приведенное выше уравнение теплоемкости: \ (\ frac {q} {m \ times \ Delta T} = \ frac {134} {15 \ times 38,7} = 0,231 \). Однако калькулятор удельной теплоемкости может помочь вам найти значения без каких-либо ручных расчетов.
Однако плотность имеет решающее значение для определения чистоты веществ, поэтому попробуйте онлайн-калькулятор плотности, чтобы найти взаимосвязь между плотностью, массой и весом объекта.
Единица удельной теплоемкости:Определение удельной теплоемкости показало, что это количество тепла, необходимое для повышения температуры 1 килограмма любого вещества на 1 кельвин. Следовательно, его производная единица \ (SI \) равна \ (J kg − 1 K − 1 \). Калькулятор удельной теплоемкости служит для получения результатов вместе со стандартизованными единицами измерения.
Удельная теплоемкость воды? Удельная теплоемкость водыимеет одно из максимальных значений удельной теплоемкости среди обычных веществ.Это примерно \ (4182 Дж / (К · кг) при 20 ° C \). В случае льда это всего \ (2093 Дж / (К · кг) \).
Как рассчитать удельную теплоемкость (пошагово)?С поддержкой формулы удельной теплоемкости расчет удельной теплоемкости является простым процессом. Посмотрите ниже и выполните несколько простых шагов:
Шаг 1:
Прежде всего, вы должны определить, хотите ли вы нагреть вещество или охладить его. Теперь представьте количество подаваемой энергии как положительное значение.Охлаждая образец, вы должны дать вычтенную энергию как отрицательное значение. Например, предположим, что мы хотим уменьшить тепловую энергию дегустатора на \ (63000 Дж \). Тогда \ (Q \) будет \ (- 63 000 Дж \).
Шаг 2:
Теперь определите разницу между начальным и конечным состоянием образца. Предположим, что разница равна \ (ΔT = -3 K \), а m равно 5 кг.
Шаг 3:
Просто введите значения в уравнение теплоемкости как \ (c = Q / (m x ΔT) \).В этом примере это будет равно c = \ (- 63 000 Дж / (5 кг * -3 K) = 4 200 Дж / (кг • K) \).
Это типичная теплоемкость воды, которую также можно рассчитать с помощью калькулятора удельной теплоемкости за один раз.
Удельная теплоемкость некоторых распространенных веществ:Нет необходимости использовать калориметрический калькулятор, чтобы определить удельную теплоемкость обычных веществ, как мы их перечислили ниже:
Стол:
Как пользоваться калькулятором удельной теплоемкости?Онлайн-калькулятор удельной теплоемкости помогает определить теплоемкость различных веществ.Просто выполните следующие действия, чтобы получить точные результаты для веществ:
Ввод:
- Прежде всего, выберите вариант, хотите ли вы найти тепловую энергию, удельную теплоемкость, массу, начальную температуру, конечную температуру любого вещества
- Затем выберите вариант, в котором необходимо выполнить расчеты по изменению температуры \ (ΔT) \) или начальной и конечной температуры.
- Теперь вы можете добавлять значения в назначенные поля для выбранных опций
- Затем выберите вещество, такое как (вода, почва, алюминий, асфальт и т. Д.), Для которого вам нужно найти удельную теплоемкость (это поле необязательно).
- Нажмите кнопку «рассчитать»
Выход:
Калькулятор удельной теплоемкости вычисляет:
- Тепловая энергия, удельная теплоемкость, масса, начальная или конечная температура вещества
- Удельная теплоемкость данного вещества
- Формула для выбранного варианта
- Пошаговое решение по формуле согласно выбранному варианту
Примечание: Калькулятор удельной теплоемкости поддерживает различные единицы измерения, чтобы предоставить вам точные результаты для веществ.
Сколько энергии требуется для повышения температуры одного грамма воды на 1 градус?Калории определяются как количество тепла, которое требуется при давлении 1 для повышения температуры 1 грамма воды при \ (1 ° \) Цельсия. Кроме того, калории были определены в джоулях, и одна калория равна примерно \ (4,2 джоуля \). Следовательно, мы можем сказать, что для повышения температуры 1 грамма воды требуется \ (4,2 джоуля \) энергии. Однако калькулятор теплоемкости – лучший способ получить безошибочный ответ.
Часто задаваемые вопросы: Почему у воды такая высокая теплоемкость?Высокая теплоемкость воды обусловлена водородными связями между ее молекулами. Когда тепло поглощается водой, связи водородных тормозов и молекул воды начинают свободно перемещаться. При понижении температуры воды водородные связи выделяют значительное количество энергии.
Сколько тепла нужно, чтобы растопить 200 г льда?Обычно \ (250 × 332 джоулей \) энергии, необходимой для плавления \ (200 нг \) льда.
Сколько энергии нужно, чтобы растопить лед?Если вы хотите растопить, требуется 1 г льда с \ (0 ° C \) общим \ (334 Джоуля \) энергии. Его еще называют скрытой теплотой плавления. Калькулятор удельной теплоемкости может рассчитать джоули энергии для нескольких граммов любого вещества за несколько секунд.
Еда на вынос:У всех нас есть некоторое представление о том, что такое удельная теплоемкость, как мы изучали физику в наших академических кругах. Это количество тепла, которое необходимо для повышения температуры определенного материала на определенное количество, и это количество тепла будет изменяться для разнородных веществ.Конкретный калькулятор – лучший способ найти количество тепла, необходимое для повышения температуры \ (1 (г) \) вещества \ (1 (° C) \).
Артикул:Из информационного источника Википедии: Удельная теплоемкость
Из источника викторины: тепловая энергия (практические задачи)
От источника искры (ИОП): полное обсуждение теплоемкости
Требования к тепловой энергии
Целью любого нагревательного устройства является повышение или поддержание температуры твердого, жидкого или газообразного вещества до или на уровне, подходящем для конкретного процесса или применения.Большинство систем отопления можно разделить на две основные ситуации; приложения, требующие поддержания постоянной температуры, и приложения или процессы, требующие нагрева рабочего продукта до различных температур. Принципы и процедуры расчета аналогичны для любой ситуации.
Приложения с постоянной температурой
Большинство применений с постоянной температурой – это особые случаи, когда температура твердого тела, жидкости или газа поддерживается на постоянном уровне независимо от температуры окружающей среды.Расчетные коэффициенты и расчеты основаны на установившемся режиме при фиксированной разнице температур. Потери тепла и потребности в энергии оцениваются с использованием условий «наихудшего случая».
По этой причине определить потребность в тепловой энергии для применения с постоянной температурой относительно просто. Комфортный обогрев (постоянная температура воздуха) и защита трубопроводов от замерзания являются типичными примерами приложений с постоянной температурой. Уравнения и процедуры для расчета потребности в тепле для нескольких приложений обсуждаются далее в этом разделе.
Приложения с переменной температурой
Приложения с переменной температурой (технологические процессы) обычно включают последовательность запуска и имеют множество рабочих переменных. Общая потребность в тепловой энергии для технологических процессов определяется как сумма этих расчетных переменных. В результате расчет тепловой энергии обычно более сложен, чем для приложений с постоянной температурой. Переменные:
Общая поглощенная тепловая энергия – Сумма всей тепловой энергии, поглощенной во время запуска или работы, включая рабочий продукт, скрытую теплоту плавления (или испарения), материалы, контейнеры и оборудование.
Общие потери тепловой энергии – Сумма потерь тепловой энергии в результате теплопроводности, конвекции, излучения, вентиляции и испарения во время запуска или работы.
Расчетный коэффициент безопасности – Коэффициент для компенсации неизвестных факторов в процессе или применении.
Технологические приложения
Выбор и определение размеров установленного оборудования в технологическом процессе основывается на большем из двух рассчитанных требований к тепловой энергии.В большинстве технологических процессов параметры запуска и эксплуатации представляют собой два совершенно разных состояния одного и того же процесса. Тепловая энергия, необходимая для запуска, обычно значительно отличается от энергии, необходимой для рабочих условий. Чтобы точно оценить требования к теплу для приложения, необходимо оценить каждое условие. Сравнительные значения определены следующим образом:
- Расчетная тепловая энергия, необходимая для запуска процесса в течение определенного периода времени.
- Расчетная тепловая энергия, необходимая для поддержания температуры процесса и рабочих условий в течение определенного времени цикла.
Определение поглощенной тепловой энергии
Первым шагом в определении общей потребности в тепловой энергии является определение поглощенной тепловой энергии. Если изменение состояния происходит как прямая или косвенная часть процесса, тепловая энергия, необходимая для изменения состояния, должна быть включена в расчеты.Это правило применяется независимо от того, происходит ли изменение во время запуска или позже, когда материал находится при рабочей температуре. Факторы, которые необходимо учитывать при расчетах поглощения тепла, показаны ниже:
Требования к запуску (начальный нагрев)- Тепло, поглощаемое при запуске:
- Рабочие продукты и материалы
- Оборудование (цистерны, стеллажи и др.)
- Скрытое поглощение тепла при запуске или во время запуска:
- Теплота плавления
- Теплота испарения
- Фактор времени
- Тепло, поглощаемое во время работы:
- Рабочий продукт в процессе
- Погрузка оборудования (ремни, стеллажи и др.))
- Макияжные материалы
- Скрытое поглощение тепла при работе:
- Теплота плавления
- Теплота испарения
- Коэффициент времени (или цикла), если применимо
Требования к запуску (начальный нагрев)
| Рабочие требования (процесс)
|
Определение потерь тепловой энергии
Объекты или материалы, температура которых превышает температуру окружающей среды, теряют тепловую энергию за счет теплопроводности, конвекции и излучения.Жидкие поверхности, контактирующие с атмосферой, теряют тепловую энергию за счет испарения. При расчете общей потребности в тепловой энергии необходимо учитывать эти потери и обеспечивать достаточное количество энергии для их компенсации. Тепловые потери оцениваются как для условий запуска, так и для условий эксплуатации и добавляются в соответствующий расчет. Тепловые потери при запуске – Первоначально тепловые потери при запуске равны нулю, поскольку все материалы и оборудование находятся при температуре окружающей среды. Тепловые потери возрастают до максимума при рабочей температуре.Следовательно, потери тепла при запуске обычно основываются на среднем значении потерь при запуске и потерь при рабочей температуре. Потери тепла при рабочей температуре – тепловые потери максимальны при рабочей температуре. Тепловые потери при рабочей температуре принимаются за полную стоимость и добавляются к общей потребности в энергии.
Оценка коэффициентов тепловых потерь
Обсуждаемые теплопотери можно оценить, используя коэффициенты из диаграмм и графиков, представленных в этом разделе.Общие потери включают излучение, конвекцию и теплопроводность от различных поверхностей и выражаются в ваттах в час на единицу площади поверхности на градус температуры (Вт / час / фут 2 / ° F).
Примечание – Поскольку значения в таблицах уже выражены в ваттах в час, на них не влияет фактор времени «t» в уравнениях тепловой энергии.
Расчетный коэффициент безопасности
Во многих системах отопления фактические условия эксплуатации, тепловые потери и другие факторы, влияющие на процесс, можно только оценить.В большинстве расчетов рекомендуется использовать коэффициент запаса прочности, чтобы компенсировать такие неизвестные факторы, как вентиляционный воздух, теплоизоляция, материалы для подпитки и колебания напряжения. Например, колебание (или падение) напряжения на 5% приводит к изменению выходной мощности нагревателя на 10%.
Коэффициенты безопасности варьируются от 10 до 25% в зависимости от уровня уверенности проектировщика в оценке неизвестных. Коэффициент запаса прочности применяется к сумме рассчитанных значений поглощенной и потерянной тепловой энергии.
Общая потребность в тепловой энергии
Общая тепловая энергия (Q T ), необходимая для конкретного применения, является суммой ряда переменных. Основное уравнение полной энергии:
Q T = Q M + Q L + коэффициент безопасности
Где:
- Q T = Общая требуемая энергия в киловаттах
- Q M = Общая энергия в киловаттах, поглощенная рабочим продуктом, включая скрытую теплоту, вспомогательные материалы, емкости и оборудование
- Q L = Общая энергия в киловаттах, теряемая поверхностями из-за теплопроводности, конвекции, излучения, вентиляции и испарения
- Коэффициент безопасности = от 10% до 25%
Хотя Q T традиционно выражается в британских тепловых единицах (BTU), при использовании электрических нагревателей удобнее использовать ватты или киловатты.В этом случае выбор оборудования может основываться непосредственно на номинальной мощности нагревателя. Уравнения и примеры в этом разделе преобразованы в ватты.
Основные уравнения тепловой энергии
Следующие уравнения описывают вычисления, необходимые для определения переменных в приведенном выше уравнении полной энергии. Уравнения 1 и 2 используются для определения тепловой энергии, поглощаемой рабочим продуктом и оборудованием. Удельная теплоемкость и скрытая теплота различных материалов указаны в этом разделе в таблицах свойств неметаллических твердых тел, металлов, жидкостей, воздуха и газов.Уравнения 3 и 4 используются для определения потерь тепловой энергии. Потери тепловой энергии с поверхностей можно оценить, используя значения из кривых в таблицах G-114S, G-125S, G-126S или G-128S. Потери проводимости рассчитываются с использованием коэффициента теплопроводности или коэффициента «k», указанного в таблицах свойств материалов.
Уравнение 1 – Тепловая энергия, необходимая для повышения температуры материалов (без изменения состояния)Поглощенная тепловая энергия определяется по весу материалов, удельной теплоемкости и изменению температуры.Некоторые материалы, такие как свинец, имеют разную удельную температуру в разных состояниях. Когда происходит изменение состояния, для этих материалов требуются два расчета: один для твердого материала и один для жидкости после того, как твердое тело расплавится.
| Q A = | фунт x C P x Δ T 3412 БТЕ / кВт |
Где:
- Q A = кВтч, необходимый для повышения температуры
- Lbs = Вес материала в фунтах
- C p = Удельная теплоемкость материала (БТЕ / фунт / ° F)
- Δ T = изменение температуры в ° F [ T 2 (окончание) – T 1 (начало) ]
Поглощенная тепловая энергия определяется на основе веса материалов и скрытой теплоты плавления или испарения.
| Q F или Q v = | фунтов x H fus или H vap 3412 BTU / кВт |
Где:
- Q F = кВтч, необходимый для преобразования материала из твердого в жидкое
- Q v = кВтч, необходимый для преобразования материала из жидкости в пар или газ
- Lbs = Вес материала в фунтах
- H fus = теплота плавления (БТЕ / фунт / ° F)
- H vap = Теплота испарения (БТЕ / фунт / ° F)
Тепловая энергия, теряемая поверхностями из-за излучения, конвекции и испарения, определяется по площади поверхности и скорости потерь в ваттах на квадратный фут в час.
Где:
- Q LS = кВтч, потерянное с поверхностей из-за излучения, конвекции и испарения
- A = Площадь поверхностей в квадратных футах
- L S = Коэффициент потерь в ваттах на квадратный фут при конечной температуре (Вт / фут 2 / час по графикам)
Тепловая энергия, теряемая за счет теплопроводности, определяется площадью поверхности, теплопроводностью материала, толщиной и разницей температур в материале.
| Q LC = | A x k x Δ T d x 3412 БТЕ / кВт |
Где:
- Q LC = кВтч, потерянное из-за теплопроводности
- A = Площадь поверхностей в квадратных футах
- k = Теплопроводность материала в британских тепловых единицах на дюйм на квадратный фут в час (британские тепловые единицы на дюйм на фут 2 на час)
- Δ T = Разница температур в ° F по материалу [T2 – T1]
- d = Толщина материала в дюймах
Обобщение требований к энергии
Уравнения 5a и 5b используются для суммирования результатов всех других уравнений, описанных на этой странице.Эти два уравнения определяют общую потребность в энергии для двух условий процесса, запуска и эксплуатации.
Уравнение 5a – Тепловая энергия, необходимая для запуска| Q T = | ( | Q A + Q F [или Q V ] т | + | Q LS + Q LC 2 | ) | (1 + SF) |
Где:
- Q T = Общая требуемая энергия в киловаттах
- Q A = кВтч, необходимый для повышения температуры
- Q F = кВтч, необходимый для преобразования материала из твердого в жидкое
- Q V = кВтч, необходимый для преобразования материала из жидкости в пар или газ
- Q LS = кВтч, потерянное с поверхностей из-за излучения, конвекции и испарения
- Q LC = кВтч, потерянное из-за теплопроводности
- SF = коэффициент безопасности (в процентах)
- t = Время запуска в часах 2
| Q T = | ( Q A + Q F [или Q V ] + Q LS + Q LC ) (1 + SF) |
Где:
- Q T = Общая требуемая энергия в киловаттах
- Q A = кВтч, необходимый для повышения температуры добавляемого материала
- Q F = кВтч, необходимый для изменения добавляемого материала с твердого на жидкое
- Q V = кВтч, необходимый для замены добавляемого материала с жидкости на пар или газ
- Q LS = кВтч, потерянное с поверхностей из-за излучения, конвекции и испарения
- Q LC = кВтч, потерянное из-за теплопроводности
- SF = коэффициент безопасности (в процентах)
Определение размеров и выбор оборудования
Размер и номинальные характеристики установленного нагревательного оборудования основаны на большем из результатов расчетов по уравнениям 5a или 5b.
Банкноты –
Коэффициенты потерь из таблиц в этом разделе включают потери от излучения, конвекции и испарения, если не указано иное.
Время ( t ) учитывается в уравнении запуска, поскольку запуск процесса может варьироваться от минут или часов до дней.
Требования к эксплуатации обычно основаны на стандартном периоде времени в один час ( t = 1). Если продолжительность цикла и потребность в тепловой энергии не совпадают с часовыми интервалами, их следует пересчитать на почасовую основу.
Как рассчитать тепловую нагрузку
Важным аспектом правильного планирования системы центрального кондиционирования является включение расчета BTU, чтобы гарантировать, что ваша система HVAC может адекватно обогревать и охлаждать ваш дом или офис. Прежде чем объяснять , как рассчитать тепловую нагрузку , мы должны ответить на важный вопрос:
Что такое тепловая нагрузка?
Очевидно, что климат снаружи влияет на температуру в помещении.В экстремальных климатических условиях системы HVAC должны усердно работать, чтобы поддерживать комфортную среду. «Тепловая нагрузка» описывает количество охлаждения или нагрева , необходимое для достижения желаемой температуры в доме.
Оценка вашего расчета тепловой нагрузки
Для точного измерения мы рекомендуем обратиться к специалисту по HVAC , потому что существует множество факторов, которые могут иметь значение. Эти факторы включают изоляцию, строительные материалы, количество окон, размер и расположение окон, бытовую технику, электронику (компьютеры, принтеры и т. Д.).все откладывают тепло), сколько людей обычно занимают дома и многое другое. Тепловая нагрузка измеряется в БТЕ (британские тепловые единицы). Одна БТЕ составляет примерно 1055 джоулей и определяется количеством энергии, необходимой для нагрева или охлаждения одного фунта воды на один градус. Вот простая в использовании формула . Он не предназначен для того, чтобы быть эталоном истины, но он определенно даст вам представление о том, в каком направлении следует двигаться при планировании вашей системы HVAC:
Формула для расчета тепловой нагрузки
- Возьмите квадратный метр вашего дома
- Умножьте это на среднюю высоту потолка в вашем доме
- Умножается на разницу желаемой температуры и температуры за пределами
- Умножьте множитель, который означает, что целевое здание представляет собой герметичное сооружение (.135)
Чтобы проиллюстрировать это дальше, вот пример расчета : если вы сталкиваетесь с 30-градусной температурой в вашем регионе и хотите, чтобы она составляла 70 градусов в доме площадью 3000 квадратных футов с 8-футовыми потолками, ваш расчет будет выглядеть так: 3000 x 8 x 40 x 0,135 = 129 600 БТЕ. Имейте в виду, что это очень консервативная оценка , а это означает, что вам, вероятно, не понадобится система отопления, вентиляции и кондиционирования, выдающая 129 000 БТЕ. Когда вы рассчитываете тепловую нагрузку, вместо того, чтобы обращаться к профессионалу, вы получите менее точную цифру.Для справки: профессиональные расчеты, как правило, находятся в диапазоне 65-80% от того, что рассчитывается по приведенной выше формуле. Пример: профессионал, скорее всего, сочтет, что для этого дома требуется от 80 000 до 100 000 БТЕ. Как говорится, лучше проявить осторожность. Как уже упоминалось, для правильного планирования мы настоятельно рекомендуем вам профессионально измерить тепловую нагрузку.
Купить запчасти и аксессуары для систем отопления, вентиляции и кондиционирования воздуха в Интернете
Помните, что если вам нужно заменить какой-либо компонент вашей системы, PlumbersStock предлагает отличные цены на огромный выбор запчастей HVAC .Если у вас возникли проблемы с поиском того, что вам нужно, свяжитесь с нами. Не забудьте обновить HVAC tools . Если вы все еще не совсем понимаете, как рассчитать тепловую нагрузку, свяжитесь с нами. Если вы отапливаете свой дом с помощью котла , печи или просто обогревателя , у нас есть все необходимое.
Ресурсы по теме:
Какого размера требуется система HVAC?
Какой размер котла купить?
|
| ||||||||||||
