Калькулятор ЭДС гальванического элемента
Калькулятор ЭДС гальванического элемента – это простой инструмент, который предоставляет вам значение электродвижущей силы (EMF) для любой гальванической ячейки с заданным потенциалом электродов. Если вы немного запутались со всеми этими терминами, не волнуйтесь!
В статье ниже вы найдете краткое описание того, что такое ЭДС, как рассчитать ЭДС и примеры источников электродвижущей силы. Более того, мы подготовили объяснение окислительно-восстановительной реакции и гальванического элемента. Краткое пошаговое руководство демонстрирует использование калькулятора.
Что такое ЭДС?
ЭДС – это сокращение от электродвижущей силы. По определению, ЭДС – это сила или электрическое давление, которое генерирует ток в цепи. Единицы измерения ЭДС в вольтах [В].
Чтобы лучше понять это определение, рассмотрим типичную гальваническую ячейку, состоящую из двух электродов. Электродвижущая сила – это разность потенциалов между ними.
Кроме того, электродвижущая сила гальванического элемента определяет способность электрохимического элемента вызывать поток электронов через электрическую цепь.
Уравнение ЭДС
Электродвижущая сила электрохимической ячейки может быть рассчитана с использованием уравнения:
EMFcell [V] = Ecathode [V] – Eanode [V]
где Ecathode – это потенциал катода (в вольтах), а Eanode – это потенциал анода (в вольтах). Помните, что в ячейке потенциал катода выше, чем потенциал анода.
Электропотенциал анода и катода
Если вы хотите найти потенциал металлического электрода, один из способов – проверить гальванический ряд и найти конкретный металл в таблице. Второй способ – рассчитать его, используя уравнение Нерста, также известное как уравнение потенциала ячейки. Эта формула позволяет рассчитать восстановительный потенциал полуклеточной или полной клеточной реакции.
В таблице ниже вы можете найти электропотенциал металлов:
Стандартные электродные потенциалы металлов при 25 °С
Электрод | Электродная реакция | Потенциалы Е°, В |
|---|---|---|
Li / Li+ | Li+ + e–= Li | -3,045 |
Rb / Rb+ | Rb+ + e–= Rb | -2,925 |
K / K+ | K+ + e–= K | -2,924 |
Cs / Cs+ | Cs+ + e–= Cs | -2,923 |
Ba / Ba2+ | Ba2+ + 2e–= Ba | -2,905 |
Sr / Sr2+ | Sr2+ + 2e–= Sr | -2,888 |
Ca / Ca2+ | Ca2+ + 2e | -2,866 |
Na / Na+ | Na+ + e–= Na | -2,714 |
Mg / Mg2+ | Mg2+ + 2e–= Mg | -2,363 |
Sc / Sc3+ | Sc3+ +3e–= Sc | -2,077 |
Be / Be2+ | Be2+ + 2e–= Be | -1,847 |
Al / Al3+ | Al3+ + 3e–= Al | -1,660 |
Mn / Mn2+ | Mn2+ + 2e–= Mn | -1,179 |
Cr / Cr2+ | Cr2+ + 2e–= Cr | -0,913 |
Zn / Zn2+ | Zn2+ + 2e–= Zn | -0,760 |
Fe / Fe2+ | Fe2+ + 2e–= Fe | -0,440 |
Cd / Cd2+ | Cd2+ + 2e–= Cd | -0,400 |
Co / Co2+ | Co2 | -0,277 |
Ni / Ni2+ | Ni2+ + 2e–= Ni | -0,250 |
Sn / Sn2+ | Sn2+ + 2e–= Sn | -0,136 |
Pb / Pb2+ | Pb2+ + 2e–= Pb | -0,126 |
h3 / H+ | 2H+ + 2e–= H2 | 0,000 |
Sb / Sb3+ | Sb3+ + 3e–= Sb | +0,2 |
Bi / Bi3+ | Bi3+ + 3e–= Bi | +0,23 |
Cu / Cu2+ | Cu2+ + 2e–= Cu | +0,337 |
Hg / Hg+ | Hg+ + 1e–= Hg | +0,788 |
Ag / Ag+ | Ag+ + e–= Ag | +0,799 |
Pd / Pd2+ | Pd2+ 2e–= Pd | +0,987 |
Pt / Pt2+ | Pt2+ + 2e–= Pt | +1,188 |
Au / Au+ | Au+ + e–= Au | +1,692 |
Как рассчитать ЭДС?
Взгляните на пример расчета ЭДС ниже.
Давайте рассмотрим ячейку Даниэля – простую электрохимическую ячейку, изобретенную в 1836 году Джоном Фредериком Даниэлем (британский химик и метеоролог). В этой ячейке медь погружается в раствор сульфата меди (II), а цинк – в раствор сульфата цинка.
Схема ячейки: (-) Zn | Zn2 + || Cu2 + | Cu (+)
Проверьте потенциал металла: электродный потенциал цинка составляет -0,76 В, а меди – +0,34 В ⇒ из-за более низкого потенциала цинк является анодом, а медь – катодом. Введите эти значения в наш калькулятор.
Рассчитайте значение ЭДС электрохимической ячейки, используя уравнение:
EMFcell = +0,34 В – (-0,76 В) = 1,10 В
Электродвижущая сила ячейки Даниэля равна 1,10 вольт.
Источники электродвижущей силы
Ниже вы можете найти несколько примеров источников ЭМП:
- батареи
- генераторы переменного тока
- гальванические элементы
- солнечные батареи
- топливные элементы
- термопары
- некоторые живые организмы (например, электрический угорь)
Каждый из перечисленных выше источников ЭДС содержит источник энергии, который вызывает поток электрических зарядов. Этими источниками могут быть химические процессы (в батареях, топливе и гальванических элементах), механические силы (в генераторах), электромагнитное излучение, излучаемое Солнцем (в солнечных элементах) и разность температур (в термопарах).
Этими источниками могут быть химические процессы (в батареях, топливе и гальванических элементах), механические силы (в генераторах), электромагнитное излучение, излучаемое Солнцем (в солнечных элементах) и разность температур (в термопарах).
Типы электрохимических ячеек
Электрохимическая ячейка является одним из видов источников энергии. Его можно создать, поместив металлические электроды в электролит, где химическая реакция генерирует или использует электрический ток.
Электрохимические элементы, которые генерируют электрический ток, называются гальваническими элементами (названными в честь их изобретателя, итальянского физика Алессандро Вольта) или гальваническими элементами (названными в честь итальянского физика и врача Луиджи Гальвани).
Обычные батареи состоят из одного или нескольких таких элементов. В других электрохимических элементах электрический ток, подаваемый извне, используется для запуска химической реакции (которая не должна происходить самопроизвольно).
Окислительно-восстановительная реакция
Процессы восстановления и окисления происходят только вместе (невозможно, чтобы эти реакции происходили отдельно). Вот почему окислительно-восстановительные реакции могут быть описаны как две полуреакции, одна представляет процесс окисления, а другая – процесс восстановления. Давайте посмотрим на это на примере ячейки Даниэля.
В ячейке Даниэля медь погружается в раствор сульфата меди (II), а цинк – в раствор сульфата цинка. В этой ячейке цинк действует как анод (из-за более низкого электрического потенциала), а медь действует как катод (из-за более высокого электропотенциала):
E⁰ цинкового электрода = -0,76 В
E⁰ медного электрода = +0,34 В
Общая химическая реакция клетки Даниэля: Zn (s) + Cu2⁺ (aq) → Zn²⁺ (aq) + Cu (s)
Окисление (на аноде): Zn (s) → Zn²⁺ (aq) + 2e⁻
Восстановление (на катоде): Cu2⁺ (aq) + 2e⁻ → Cu (s)
Количество электронов, потерянных восстановителем, равно числу электронов, полученных окислителем (для любой окислительно-восстановительной реакции).
Электродвижущая сила ЭДС – Справочник химика 21
На поверхности контакта двух проводящих фаз электрохимической системы (различной химической природы, агрегатного состояния и типа проводимости) наблюдаются скачки потенциала. Сумма скачков потенциала на всех границах раздела фаз равновесной электрохимической системы называется электродвижущей силой (ЭДС) элемента или цепи. Она может быть непосредственно измерена как разность потенциалов фаз, находящихся на концах цепи. Для электрохимических систем характерны три основные типа скачков потенциала скачки потенциала металл — раствор, раствор — раствор и металл — металл. [c.280]Основная характеристика гальванического элемента — электродвижущая сила (эдс) равна разности его электродных потенциалов [c.135]
Стандартные потенциалы металлов, расположенные в порядке возрастания их алгебраической величины, образуют так называемый ряд напряжений металлов, или ряд стандартных электродных потенциалов. Для определения электродвижущей силы (ЭДС) гальванического элемента следует из стандартного потенциала с большей алгебраической величиной вычесть стандартный потенциал с меньшей алгебраической величиной. Так, ЭДС медно-цинкового гальванического элемента составляет (см. приложение V) [c.126]
Для определения электродвижущей силы (ЭДС) гальванического элемента следует из стандартного потенциала с большей алгебраической величиной вычесть стандартный потенциал с меньшей алгебраической величиной. Так, ЭДС медно-цинкового гальванического элемента составляет (см. приложение V) [c.126]
Электродвижущая сила (ЭДС) химического источника тока равна разности электродных потенциалов катода, и анода. Существует большое количество гальванических элементов, важнейшие из которых приведены в табл. 96. [c.155]
ЭНЕРГЕТИКА ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ И СОЗДАНИЕ ЭЛЕКТРОДВИЖУЩЕЙ СИЛЫ (ЭДС) [c.227]
Таким образом, разность потенциалов на концах равновесной электрохимической цепи однозначно связана с изменением свободной энергии Гиббса в ходе соответствующей химической реакции. Величина Е, т. е. разность потенциалов на концах равновесной электрохимической цепи, называется ее электродвижущей, силой (ЭДС). Если же на отдельных фазовых границах (хотя бы на одной) равновесие не устанавливается, то разность потенциалов на концах цепи не равна ЭДС и уравнение (VI. 19) оказывается неприменимым. Величина пРЕ характеризует максимальную электрическую работу, которую можно получить при помощи электрохимической цепи. Уравнение (VI.19) служит основой для расчета АО различных химических реакций. Часто электрохимический метод определения изобарного потенциала имеет существенные преимущества перед термохимическим методом. [c.118]
19) оказывается неприменимым. Величина пРЕ характеризует максимальную электрическую работу, которую можно получить при помощи электрохимической цепи. Уравнение (VI.19) служит основой для расчета АО различных химических реакций. Часто электрохимический метод определения изобарного потенциала имеет существенные преимущества перед термохимическим методом. [c.118]
Основной характеристикой электрохимической системы является электродвижущая сила (ЭДС) — разность потенциалов между двумя металлическими электродами, измеряемая при протекании обратимых процессов в системе. [c.314]
Разность потенциалов электродов гальванического элемента называется его электродвижущей силой ЭДС( ). При расчете значения Е принято из значения потенциала фз электрода, записанного в обозначении состава гальванического элемента справа, вычесть значение потенциала ф1 электрода, записанного в обозначении состава слева, в начале записи Е = = Ф2—Ф1- [c.188]
Разность электродных потенциалов — это электродвижущая сила (ЭДС) гальванического элемента.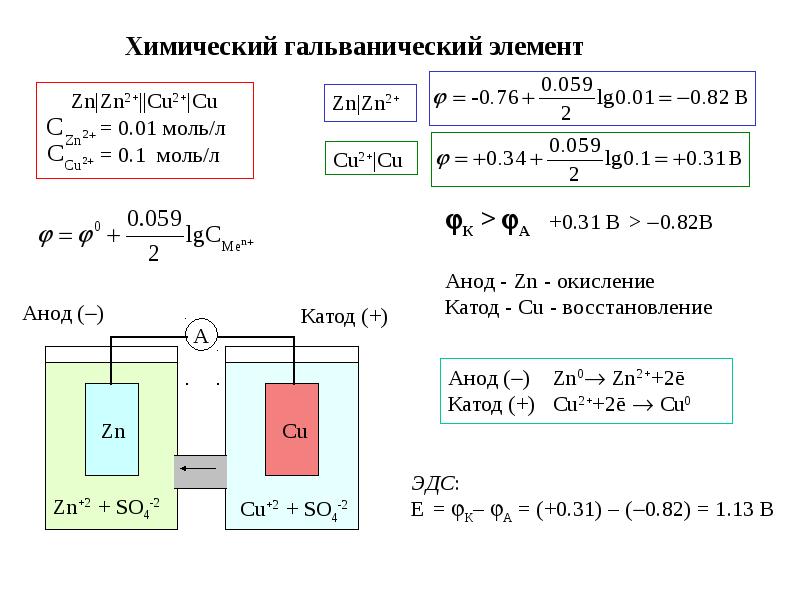 Так как водородный электрод служит электродом сравнения, для которого о=ОВ, то измеряемая ЭДС рассматриваемого элемента — это потенциал медного электрода по отношению к водородному. Ниже значения электродных потенциалов будем обозначать символом Е (иногда пользуются символом ф), как и ЭДС электродных реакций. Таким образом, потенциалы металлов можно сравнивать по ЭДС гальванической цепи с водородным электродом. [c.326]
Так как водородный электрод служит электродом сравнения, для которого о=ОВ, то измеряемая ЭДС рассматриваемого элемента — это потенциал медного электрода по отношению к водородному. Ниже значения электродных потенциалов будем обозначать символом Е (иногда пользуются символом ф), как и ЭДС электродных реакций. Таким образом, потенциалы металлов можно сравнивать по ЭДС гальванической цепи с водородным электродом. [c.326]
Потенциометрические методы основаны на измерении потенциалов различных электродов или, точнее, электродвижущих сил (ЭДС) различных цепей, поскольку экспериментально измеряется именно ЭДС, являющаяся разностью потенциалов. [c.240]
Электрохимическая цепь находится в равновесии, если на всех межфазных границах достигнуто равновесие и исключен диффузионный потенциал. В этом случае разность потенциалов между концами проводников первого рода, присоединенных к электродам, называется электродвижущей силой (ЭДС) гальванического элемента. [c.218]
[c.218]
Если в цепи 1 > Уз, то ток всегда течет от к Уд для того чтобы цепь была замкнутой, ток внутри электрической батареи — источника тока — должен течь в обратную сторону, т. е. от отрицательного электрода к положительному. Это осуществляется за счет так называемой электродвижущей силы (ЭДС), уравновешивающей разность потенциалов во внешней цепи и падение потенциала на внутреннем сопротивлении Ло батареи [c.185]
Разность электродных потенциалов Е — это электродвижущая сила (эдс) гальванического элемента. Так как водородный электрод служит электродом сравнения, для которого °н /н2 = = 0, то измеряемая эдс рассматриваемого элемента — это потенциал медного электрода по отношению к водородному. [c.261]
Определение энергии Гиббса процесса. Подобно энтальпии ЛЯ и энтропии 5 величину ЬС физико-химических процессов можно определить экспериментально. Один из широко применяемых методов определения ДС окислительно-восстановительных реакций заключается в проведении их в гальваническом элементе и измерении его электродвижущей силы (эдс). Рассмотрим этот метод определения ДС7 на примере реакции вытеснения цинком меди из раствора сульфата меди [c.203]
Рассмотрим этот метод определения ДС7 на примере реакции вытеснения цинком меди из раствора сульфата меди [c.203]
Электродвижущая сила (ЭДС) этой цепи при протекании какой-либо химической реакции в стандартных условиях (температура 25°С, давление 1 атм, концентрации всех веществ в ячейках- [c.163]
По табл. 93 находим, что для С1 – -С1 о= 1,359 В, а для SOi S05 o = = 0,17 В. Разность стандартных потенциалов ионов, участвующих в реакции, называется электродвижущей силой (ЭДС) реакции. Чем больше ЭДС, тем энергичнее протекает реакция. Для реакции окисления сульфит-иона ЭДС равна [c.150]
Вертикальные черточки здесь обозначают поверхности раздела фаз. В случае положительной электродвижущей силы (ЭДС) слева располагают отрицательный электрод, справа — положительный. Для того чтобы учесть соединение меди и цинка (непосредственное или с помощью промежуточных металлов), про- [c.232]
Соединение электродов металлическим проводником приводит к возникновению электрического тока. Следовательно, в этой системе возникает электродвижущая сила — ЭДС элемента. 3)та ЭДС способна совершать работу по переносу электрона по металлическому проводнику (а следовательно, и любые виды работы, в которые можно преобразовать энергию электрического тока) за счет химической реакции окисления — восстановления. Таким образом, гальванический элемент представляет собой устройство, в котором уменьшение термодинамического потенциала в результате окислительно-восстановительной реакции преобразуется в энергию электрического тока. [c.294]
Следовательно, в этой системе возникает электродвижущая сила — ЭДС элемента. 3)та ЭДС способна совершать работу по переносу электрона по металлическому проводнику (а следовательно, и любые виды работы, в которые можно преобразовать энергию электрического тока) за счет химической реакции окисления — восстановления. Таким образом, гальванический элемент представляет собой устройство, в котором уменьшение термодинамического потенциала в результате окислительно-восстановительной реакции преобразуется в энергию электрического тока. [c.294]
Электродвижущая сила элемента. Электрическая работа равна произведению разности потенциалов на количество электричества. Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента, называется электродвижущей силой (ЭДС) элемента. Она равна разности равновесных потенциалов катода и анода элемента. Если на электродах превращается один моль эквивалентов вещества, то по закону Фарадея через систему протекает один фарадей электричества, при превращении одного моля вещества — п фарадеев электричества, равное числу молей эквивалентов в одном моле вещества. Таким образом, максимальная электрическая работа гальванического элемента при превращении одного моля вещества равна [c.194]
Таким образом, максимальная электрическая работа гальванического элемента при превращении одного моля вещества равна [c.194]
Устройство, схематически изображенное на рис. 6.1, называют гальваническим элементом, а каждый из сосудов, содержащий раствор и платиновую пластину, — электродом или полуэлемеитом, хотя собственно электродом часто называют платиновую или другую пластину, служащую проводником электронов. При проведении реакции в гальваническом элементе химическая энергия превращается в электрическую. Электродвижущая сила ЭДС гальванического элемента может быть измерена с помощью потенциометра. Она непосредственно характеризует способность электронов данного восстановителя переходить к данному окислителю. [c.105]
Что называется электродвижущей силой (ЭДС) гальванического элемента [c.74]
Если теперь пластинку любого металла, погруженную в раствор его соли, содержащий 1 моль ионов металла в 1000 г воды, соединить с водородным электродом, как показано на рис. 5.7, то получится гальванический элемент, электродвижущую силу (ЭДС) которого легко измерить. Эта ЭДС, измеренная при 25 С, и называется стандартным электродным потенциалом данного металла (обычно обозначается ). [c.158]
5.7, то получится гальванический элемент, электродвижущую силу (ЭДС) которого легко измерить. Эта ЭДС, измеренная при 25 С, и называется стандартным электродным потенциалом данного металла (обычно обозначается ). [c.158]
Теплоемкость Коэффициент диффузии Плотность вещества Электродвижущая сила (ЭДС) Напряжение разложения Тепловое напряжение разложения Электрон [c.4]
Напряжением разложения разл в ваннах и электродвижущей силой (ЭДС) в ХИТ называют разность равновесных потенциалов системы [c.11]
Величина электродвижущей силы (ЭДС) различных термопар при температуре холодного спая С° [c.473]
Электродвижущая сила (ЭДС) этой реакции имеет положительное значение [c.148]
Электродвижущая сила (эдс) химического источника тока представляет собой разность потенциалов положительного и отрицательного электродов [c.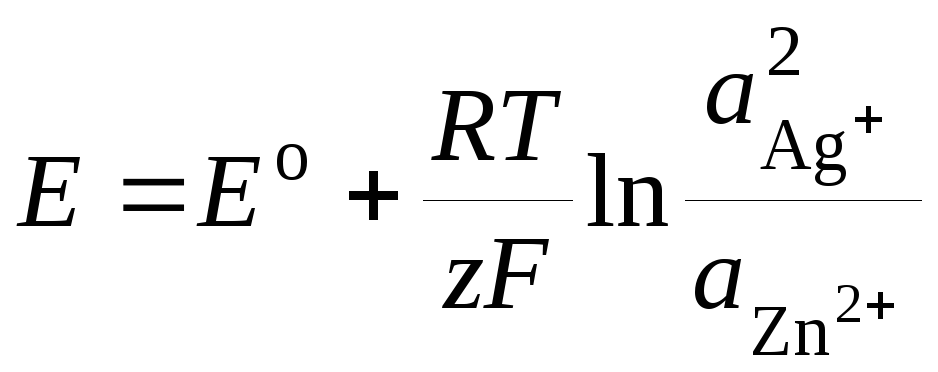 18]
18]
По определению условный (относительный) окислительно-восстановительный потенциал редокс-пары (эмектродпый потенциал редокс-пары) — это электродвижущая сила (ЭДС) гальванической цепи, составленной из данного окислительно-восстановительного электрода и стандартного водородного электрода При этом в схеме записи гальва- [c.149]
Элeктpoxимичe кaя цепь является равновесной при условии, что электрохимическое равновесие имеет место на каждой из ее фазовых границ. Разность потенциалов на концах такой цепи называется электродвижущей силой (ЭДС) цепи. Рассмотрим цепь а (рис. 2.1) и предположим, что электрод М1 — цинковый, электрод М2 — хлорсеребряный, а раствором электролита служит 2пС12- В этом случае, как следует из рисунка, [c.80]
Назовем потенциалом реакции Е, или электродвижущей силой (ЭДС) реакции величину, равную ра шости окислительно-восстановительных потенциалов редокс-пар (т. е. их электродных потенциалов). В рассматриваемом случае [c. 154]
154]
При стандартных условиях, т. е. при 298,15 К,/)Н2 = 1,013 -10 Па и Смп04- = Смпг+—Сн+ =1 моль/л, электродвижущая сила (эдс) этого элемента равна 1,51 В, Значит, стандартный электродный потенциал Мп04 /Мп составляет 1,51 В. Аналогично определяют стандартный электродный потенциал системы Ы0з / Ы02 он равен -(-0,94 В. [c.330]
Если замкнуть внешнюю цепь на сопротивление, то будет происходить лишь выделение бесполезной теплоты, затрачиваемой на нагревание сопротивления, при этом полезная работа Л не производится (см. (2.19)]. Соединив же гальванический элемент с электромотором, робратная электродвижущая сила (эдс) практически уравновесит эдс элемента, получим иной результат тепловая потеря станет минимальной, а раСюта, нао рот, достигнет предельного значения К тому же [c.204]
НлО+ -1-е-=Н-1-Н20 Если пластинку металла, погруженную в раствор его соли с активностью ионов, равной единице, соединить со стандартным водородным электродом, как показано на рис. 62, то получится гальванический элемент (электрохимическая цепь), электродвижущую силу (ЭДС) которого легко измерить. ЭДС, измеренная при 25 °С, и будет величиной стандартного электродного потенциала металла. Стандартный электродньсй потенциал обычно обозначают Е°. [c.230]
62, то получится гальванический элемент (электрохимическая цепь), электродвижущую силу (ЭДС) которого легко измерить. ЭДС, измеренная при 25 °С, и будет величиной стандартного электродного потенциала металла. Стандартный электродньсй потенциал обычно обозначают Е°. [c.230]
Если на одном и том же электроде могут осуществляться две реакции и более, то предпочтительней оказывается та, для протекания которой требуется наименьщая электродвижущая сила (ЭДС). [c.166]
Важнейшей количественной характеристикой электрохимического элемента является электродвижущая сила (ЭДС, обозначаемая в дальнейшем буквой ), которая равна равновесной разности потенциалов между двумя полуэлемен-тами. [c.238]
Внутренние потенциалы отдельных фаз ср е и ф , к сожалению, экспериментально измерить нельзя. Любая попытка подключить раствор с помощью провода к измерительному прибору вызывает появление новой поверхности соприкосновения фаз поверхность соприкосновения провода с раствором, на которой возникает свойственное ей редоксиравновесие.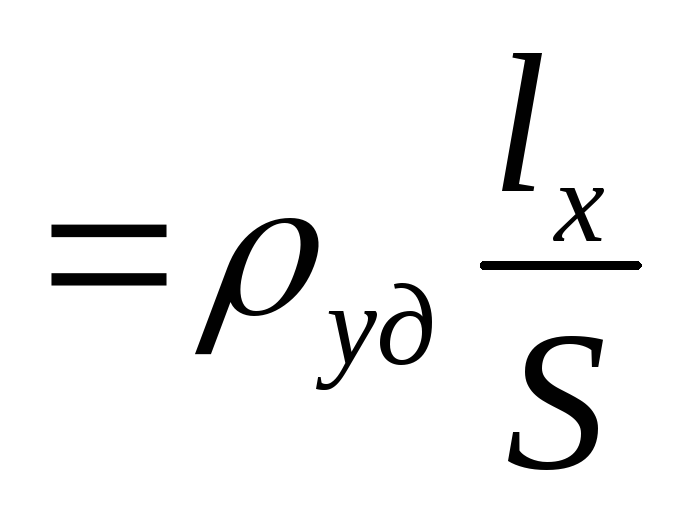 Например, если провод сделан из меди, возникает равновесие Си ” + 2е Си. Следовательно, при попытке подключить раствор к измерительному прибору возникает новый электрод со своей разностью потенциалов фаз. Из обоих электродов образуется гальванический элемент, электродвижущая сила (ЭДС) которого алгебраически складывается из разностей потенциалов отдельных электродов. ЭДС такого гальванического элемента можно измерить. [c.89]
Например, если провод сделан из меди, возникает равновесие Си ” + 2е Си. Следовательно, при попытке подключить раствор к измерительному прибору возникает новый электрод со своей разностью потенциалов фаз. Из обоих электродов образуется гальванический элемент, электродвижущая сила (ЭДС) которого алгебраически складывается из разностей потенциалов отдельных электродов. ЭДС такого гальванического элемента можно измерить. [c.89]
Как осуществляется взаимодер]ствие двух окисли-Тельно-Босстаиовительных систем при работе гальванического элемента н что называют его электродвижущей силой (ЭДС) [c.258]
ЭДС гальванического элемента | Задания 251-255
Решение задач на составление схемы гальванического элемента
Задание 251.
При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, в котором один никелевый электрод находится в 0,001 М растворе, а другой такой же электрод – в 0,01 М растворе сульфата никеля. Ответ: 0,0295 В.
Ответ: 0,0295 В.
Решение:
Гальванический элемент, электроды которого сделаны из одного и того же металла будет работать при условии, что электроды будут опущены в растворы солей с разной концентрацией. Схема гальванического элемента, в котором один никелевый электрод находится в 0,001М растворе, а другой – в 0,01М растворе сульфата никеля имеет вид:
Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Е0 – стандартный электродный потенциал металла; n – число электронов, принимающих участие в процессе; с – концентрация ионов металла в растворе его соли (при точных вычислениях – активность).
Определим электродные потенциалы никелевых электродов при разных концентрациях ионов серебра Ni2+, получим:
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода, получим:
Ответ: 0,0295 В.
Задание 252.
Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин, опущенных в растворы своих солей с концентрацией [Рb2+] = [Мg2+] = 0,01 моль/л. Изменится ли ЭДС этого элемента, если концентрацию каждого из ионов увеличить в одинаковое число раз? Ответ: 2,244 В.
Решение:
Схема гальванического элемента
Вертикальная линейка обозначает поверхность раздела между металлом и раствором, а две линейки – границу раздела двух жидких фаз – пористую перегородку (или соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (—2,37 В) и является анодом, на котором протекает окислительный процесс:
Мg0 – 2 = Mg2+ (1)
Свинец, потенциал которой -0,127 В – катод, т.е. электрод, на котором протекает восстановительный процесс:
Pb2+ + 2 = Pb0 (2)
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного (1) и катодного (2) процессов:
Mg0 + Pb2+ = Mg2+ + Pb0
Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Эта зависимость выражается уравнением Нернста:
Е0 – стандартный электродный потенциал металла; n – число электронов, принимающих участие в процессе; с – концентрация ионов металла в растворе его соли (при точных вычислениях – активность). Определим электродные потенциалы кадмия и меди при заданных концентрациях:
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода, получим:
Если концентрацию каждого из ионов Mg2+ и Pb2+ увеличить в одинаковое число раз, то ЭДС гальванического элемента не изменится, так как при этом соответственно будут уменьшаться численные значения потенциалов металлов, а разница между значениями их не изменится. Например, при увеличении концентрации ионов в 100 раз концентрация их примет значения 1 моль/л, а потенциалы электродов станут равными стандартным потенциалам металлов, то ЭДС = -0,127 – (-2,37) = 2,243 В.
Ответ: 2,243 В.
Задание 253.
Составьте схемы двух гальванических элементов, в одном из которых никель является катодом, а в другом – анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и на аноде.
Решение:
а) Схема гальванического элемента, в котором никель является катодом:
Вертикальная линейка обозначает поверхность раздела между металлом и раствором, а две линейки – границу раздела двух жидких фаз – пористую перегородку (или соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (-2,37 В) и является анодом, на котором протекает окислительный процесс:
Mg0 – 2 = Mg2+ (1)
Никель, потенциал которой -0,25 В – катод, т.е. электрод, на котором протекает восстановительный процесс:
Ni2+ + 2 = Ni0 (2)
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного (1) и катодного (2) процессов:
Mg0 + Ni2+ = Mg2+ + Ni0
б) Схема гальванического элемента, в котором никель является анодом:
Никель имеет меньший потенциал (-0,25 В) и является анодом, на котором протекает окислительный процесс:
Ni0 – 2 = Ni2+ (1)
Медь, потенциал которой (+0,34 В) – катод, т. е. электрод, на котором протекает восстановительный процесс:
е. электрод, на котором протекает восстановительный процесс:
Сu2+ + 2 = Сu0 (2)
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного (1) и катодного (2) процессов:
Ni0 + Cu2+ = Ni2+ + Cu0
Задание 254.
Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов, происходящих на аноде и на катоде.
Решение:
Стандартные электродные потенциалы железа и серебра соответственно равны -0,44 В и +0,80 В. Исходя из того, что железо имеет более электроотрицательный потенциал, чем водород 0,00 В, то между железом и раствором серной кислоты проходит реакция (железо вытесняет водород из кислоты), и железная пластинка при этом будет уменьшаться по массе:
Fe + H2SO4 = FeSO4 + H2
Исходя из того, что серебро имеет более электроположительный потенциал, чем водород, то между серебром и раствором серной кислоты реакция не проходит. Но так как железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты, то между ними будет проходить окислительно-восстановительный процесс, в котором железная пластина будет анодом, а серебряная – катодом.
Но так как железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты, то между ними будет проходить окислительно-восстановительный процесс, в котором железная пластина будет анодом, а серебряная – катодом.
На аноде протекает процесс:
Fe0 → Fe2+ + 2
На катоде серебряной пластинке будут разряжаться ионы водорода:
2Н+ + 2 → Н20
Схема гальванического элемента имеет вид:
(-) Fe | Fe2+ || 2H+ | H2, Ag (+)
Задание 255.
Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из пластин кадмия и магния, опущенных в растворы своих солей с концентрацией [Мg2+] = [Cd2+] = 1 моль/л. Изменится ли значение ЭДС, если концентрацию каждого из ионов понизить до 0,01 моль/л? Ответ: 1,967 В.
Решение:
Магний имеет меньший потенциал (-2,37 В) и является анодом, на котором протекает окислительный процесс:
Mg0 – 2 = Mg2+ (1)
Кадмий, потенциал которой (-0,403 В) – катод, т.е. электрод, на котором протекает восстановительный процесс:
Cd2+ + 2 = Cd0 (2)
Схема гальванического элемента имеет вид:
Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Е0 – стандартный электродный потенциал металла; n – число электронов, принимающих участие в процессе; с – концентрация ионов металла в растворе его соли (при точных вычислениях – активность). Определим электродные потенциалы кадмия и меди при заданных концентрациях:
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода, получим:
Рассчитаем электродные потенциалы магния и кадмия при концентрации их ионов в растворе равной 0,01 моль/л:
Рассчитаем ЭДС:
Таким образом, ЭДС гальванического элемента при равном уменьшении концентрации ионов металлов в их растворах не изменяется.
Ответ: 1,967 В.
Занятие 1
%PDF-1.5 % 1 0 obj > /Metadata 2 0 R /PageLayout /OneColumn /Pages 3 0 R /StructTreeRoot 4 0 R /Type /Catalog >> endobj 5 0 obj /CreationDate (D:20141031085413+03’00’) /Creator /Keywords () /ModDate (D:20141031085421+03’00’) /Producer (Adobe PDF Library 10.0) /SourceModified (D:20141031055348) /Subject () /Title >> endobj 2 0 obj > stream 2014-10-31T08:54:21+03:002014-10-31T08:54:13+03:002014-10-31T08:54:21+03:00Acrobat PDFMaker 10.1 для Worduuid:6231a161-2615-443a-986e-e1dd01ca90e4uuid:25028417-6bdf-4189-a47c-62a4b0015fc9
Уравнение Нернста. Применение в решении задач.
При рассмотрении вопроса об окислительно-восстановительных реакциях часто возникает необходимость расчета электродвижущей силы (ЭДС) и потенциалов отдельных полуреакций. В справочниках обычно приведены таблицы т.н. стандартных потенциалов тех или иных процессов, рассчитанных при р=1 атм, Т=298К и активностях участников равных 1. Однако в реальных задачах условия могут значительно отличаться от указанных выше. Как быть в таком случае? Ответ дает уравнение Нернста. В оригинальном виде оно выглядит так:
Как можно заметить, в уравнении фигурируют несколько постоянных величин. Также температура в подавляющем большинстве случаев равна 298К. Кроме того, можно заменить натуральный логарифм на десятичный. Это можно сделать путем умножения на коэффициент перевода. Если собрать все постоянные в единый множитель, то приходим к несколько иному, но более знакомому по учебным пособиям виду уравнения Нернста:
Такой вариант уравнения сильно облегчает жизнь в ряде случаев, например рассмотрении рН-зависимых процессов. Используя данное уравнение можно провести вычисления в любых условиях, приведенных в задаче. Рассмотрим характерные примеры задания по данной теме.
Пример 1:
Рассчитать ЭДС гальванического элемента, составленного из медной и цинковой пластин, погруженных в растворы 0.1М CuSO4 и 0.01М ZnSO4 соответственно. Коэффициенты активности ионов Cu2+ и Zn2+ принять равными единице.
Решение:
Для начала запишем уравнения протекающих процессов:
Далее находим по таблице стандартные потенциалы процессов:
Если в условиях задачи ничего не сказано про коэффициенты активности ионов, то можно считать их равными единице, как и в нашем случае. Тогда активности участников процессов можно принять равными их аналитическим концентрациям.
Найдем реальные потенциалы с учетом нестандартных активностей ионов:
Далее необходимо сравнить полученные величины между собой, чтобы определить, кто из участников процесса – окислитель. Потенциал меди больше, чем у цинка, поэтому она будет окислителем. Тогда найдем ЭДС системы:
Ответ: 1.13 В
Пример 2:
Одним из лабораторных способов получения хлора является действие KMnO4 на концентрированную соляную кислоту. Можно ли провести процесс при рН=4?
Решение:
Для начала запишем уравнения протекающих процессов.
Далее находим по таблице стандартные потенциалы процессов:
Несложно заметить, что от рН в данном случае зависит только потенциал перманганата. Тогда воспользуемся уравнением Нернста и рассчитаем его реальный потенциал в условиях задачи:
Получается, что потенциал KMnO4 стал меньше, чем у хлора, а значит, реакция не пойдет.
Ответ: процесс не идет.
В конце приведем общий алгоритм решения задач с использованием уравнения Нернста:
- 1) Написать уравнения полуреакций, соответствующие процессу.
- 2) Определить, в каком из уравнений концентрации отличаются от стандартных.
- 3) Определить число электронов, участвующих в процессе.
- 4) Рассчитать реальные потенциалы, применяя уравнение Нернста.
- 5) Ответить на вопрос задачи.
Московский государственный университет путей сообщения (МИИТ) Кафедра «Химия и инженерная экология»
КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
Общая химия Студент: Группа: Дата выполнения работы: Лабораторная работа Цель работы: КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ Основные понятия: коррозия: химическая, электрохимическая; коррозионный гальванический элемент;
ПодробнееЛекция 1, 2. Основы электрохимии
Лекция 1, 2. Основы электрохимии Лектор: асс. каф. ОХХТ к.х.н. Абрамова Полина Владимировна еmail: [email protected] ПЛАН ЛЕКЦИИ I. Основные понятия II. Ряд напряжений металлов III. Гальванические элементы
ПодробнееЭЛЕКТРОХИМИЯ. Лекция 2
ЭЛЕКТРОХИМИЯ Лекция 2 Электрохимия – раздел химии, в котором изучаются химические процессы, идущие с поглощением или выделением электрической энергии. Они протекают на электродах (на границе раздела двух
ПодробнееЭЛЕКТРО- ХИМИЧЕСКИЕ ПРОЦЕССЫ
ЭЛЕКТРО- ХИМИЧЕСКИЕ ПРОЦЕССЫ 1. Электроды и электродные потенциалы Эл/хим. процессы окисл/восстан. реакции, протекание которых сопровождается выделением или поглощением электроэнергии: – ХИТ; – электролизёры;
ПодробнееЭлектрохимические процессы
Электрохимические процессы План лекции 1.Основные понятия электрохимии. 2. Гальванический элемент, его ЭДС. 3. Коррозия. 4. Электролиз, законы электролиза. 2 1.Основные понятия электрохимии Электрохимические
ПодробнееЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ ЭЛЕКТРОЛИТОВ
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Новгородский государственный университет им. Ярослава Мудрого Факультет естественных
ПодробнееЛекция 7, 8. Основы электрохимии
Химия 1.2 Лекция 7, 8. Основы электрохимии Лектор: асс. каф. ОХХТ к.х.н. Абрамова Полина Владимировна еmail: [email protected] ПЛАН ЛЕКЦИИ I. Основные понятия II. Ряд напряжений металлов III. Гальванические
ПодробнееТема: Электролиз расплавов и растворов
Тема: Электролиз расплавов и растворов Учебный материал, задания с решением и для самостоятельной работы Составитель: профессор Литвинова Т.Н. Теоретическая часть. Электролиз совокупность окислительно-восстановительных
ПодробнееРАЗДЕЛ 6 ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
РАЗДЕЛ 6 ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ Электрохимия область химии, изучающая процессы с возникновением электрического тока или протекающие под его воздействием. В электрохимических процессах происходит превращение
ПодробнееЭлектрохимия. Тема 11
Электрохимия Тема 11 Процессы на поверхности электрода При погружении металла в раствор его соли на границе раздела фаз могут происходить ионообменные процессы: Металл Раствор 2+ 2+ 2+ гидратация 2+ 2+
ПодробнееЭлектрохимические процессы
Электрохимические процессы Электрохимические процессы это все химические процессы, связанные с переносом заряда Red1 + Ox2 = Ox1 +Red2 Zn + Cu +2 = Zn +2 + Cu Sn 2+ + Fe 3+ = Sn 4+ + Fe 2+ окисление –
ПодробнееЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ Электрохимические процессы – процессы взаимного превращения химической и электрической энергии, основанные на окислительно-восстановительных реакциях (ОВР). Процесс преобразования
Подробнее«Электрохимические процессы»
«Электрохимические процессы» Лекция 1-2 Дисциплина «Химия 2.6» для студентов заочного отделения Лектор: к.т.н., Мачехина Ксения Игоревна * План лекции 1. Основные понятия 2. Гальванические элементы 3.
ПодробнееЭЛЕКТРОХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ЖЕЛЕЗНОДОРОЖНОГО ТРАНСПОРТА Уральский государственный университет путей сообщения Кафедра «Инженерная защита окружающей среды» А.Г.Мохов ЭЛЕКТРОХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ Екатеринбург
ПодробнееХимия. 9 класс Тема «Металлы» Электролиз
Химия. 9 класс Тема «Металлы» Электролиз Сазонов В.В., учитель химии МОУ средней общеобразовательной школы д.васькино Нижнесергинского района Свердловской области План изучения 1. Определение электролиза
Подробнее«Электрохимические процессы»
«Электрохимические процессы» Лекция 5-6 Дисциплина «Химия 2» для студентов очного отделения Лектор: к.т.н., доцент Мачехина Ксения Игоревна * План лекции 1. Основные понятия 2. Гальванические элементы
ПодробнееХИМИЯ МЕТАЛЛОВ
ХИМИЯ МЕТАЛЛОВ 1. Какая из электронных формул отражает строение атома натрия: 1. 1s 2 2s 2 2p 6 3s 1 ; 2. 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 ; 3. 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 ; 4. 1s 2 2s 1. 2. Какие
ПодробнееГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ЖЕЛЕЗНОДОРОЖНОГО ТРАНСПОРТА Уральский государственный университет путей сообщения Кафедра «Инженерная защита окружающей среды» А.Г. Мохов ГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ Екатеринбург 2007
ПодробнееЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ И ЭДС
ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ И ЭДС озникновение разности потенциалов на границе металл-раствор. При контакте металлической пластины с водой катионы, расположенные на поверхности металла, взаимодействуют с диполями
ПодробнееГальванические элементы
Московский Государственный Технический Университет им. Н.Э.Баумана Калужский филиал Кафедра химии З.Н.Пивченко Гальванические элементы Методические указания к проведению упражнений по курсу “Общая химия”
ПодробнееЛекция 7. Окислительновосстановительные
Лекция 7 Окислительновосстановительные реакции 1 План лекции 1. Понятия окисления и восстановления. 2. Типичные восстановители и окислители. 3. Метод электронно-ионного баланса. 4. Окислительно-восстановительные
Подробнее9 класс Учитель Черных Н.А. Серная кислота
9 класс Учитель Черных Н.А. Серная кислота Цель урока: учащиеся должны провести анализ общих свойств минеральных кислот, и на его основе изучить свойства разбавленной и концентрированной серной кислоты,
ПодробнееЛекция 9. Электрохимические равновесия
Лекция 9 Электрохимические равновесия 1 План лекции 1. Электрохимический потенциал. 2. Реакции на электродах и межфазный потенциал. 3. Зависимость электродных потенциалов от концентрации. 4. Уравнение
ПодробнееNaOH Na + + HSO 4. (1 ступень) HSO 4 H + + SO 4
ЗАНЯТИЕ 5 ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ СРЕДЫ. ГИДРОЛИЗ СОЛЕЙ ТЕОРЕТИЧЕСКАЯ ЧАСТЬ Электролиты вещества, проводящие электрический ток. Процесс распада вещества на ионы под действием растворителя называется электролитической
ПодробнееГальванический элемент в химии с примером
Гальванический элемент (гэ). Напряжение гальванического элементаГальванический элемент — это, прибор, который преобразует химическую энергию окислительно-восстановительной реакции в электрическую энергию.
Схема простейшего ГЭ Даниэля-Якоби представлена на рис. 5.
Гальванический элемент состоит из двух электродов, каждый из которых опущен в сосуд с соответствующим раствором соли: цинковый электрод погружен в раствор соли . Медный электрод погружен в раствор .
Сосуды соединены электролитическим мостиком, заполненным концентрированным раствором электролита (например, или ), который служит ионным проводником между двумя сосудами.
На поверхности цинковой пластины возникает двойной электрический слой и устанавливается равновесие
В результате протекания этого процесса возникает электродный потенциал цинка. На поверхности медной пластины также возникает двойной электрический слой и устанавливается равновесие
поэтому возникает электродный потенциал меди. Потенциал цинкового электрода имеет более отрицательное значение, чем потенциал медного электрода, поэтому при замыкании внешней цепи, т.е. при соединении цинка с медью металлическим проводником, электроны будут переходит от цинка к меди. В результате перехода электронов от цинка к меди равновесие на цинковом электроде сместиться вправо, поэтому в раствор перейдет дополнительное количество ионов цинка. В то же время равновесие на медном электроде сместиться влево и произойдет разряд ионов меди.
Итак, при работе элемента Даниэля-Якоби протекают следующие процессы:
1) реакция окисления цинка
Процессы окисления в электрохимии получили название анодных процессов, а электроды, на которых идут процессы окисления, называют анодами;
2) реакция восстановления ионов меди
Процессы восстановления в электрохимии получили название электродных процессов, а электроды, на которых идут процессы восстановления, назвают катодами;
3) движение электронов во внешней цепи;
4) движение ионов в растворе: через электролитический мостик анионов к аноду, катионов к катоду. Движение ионов в растворе замыкает электрическую цепь гальванического элемента. Суммируя электродные реакции, получаем
Вследствие этой химической реакции в гальваническом элементе возникает движение электронов во внешней цепи и ионов внутри элемента, т.е. электрический ток, поэтому суммарная химическая реакция, протекающая в гальваническом элементе, называется токообразующей.
При схематической записи, заменяющей рисунок гальванического элемента, границу раздела между проводником 1-го рода и проводником 2-го рода обозначают одной вертикальной чертой, а границу раздела между проводниками 2-го рода — двумя чертами. Схема элемента Даниэля-Якоби, например, записывается в виде:
для упрощения в таких схемах обычно опускается внешняя цепь. Как видно, в гальваническом элементе идет химическая реакция, а во внешней цепи элемента протекает электрический ток, т.е. в гальваническом элементе происходит превращение химической энергии в электрическую.
Электродвижущая сила. Напряжение элемента. Электрическая работа равна произведению разности потенциалов электродов на количество электричества. Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента, называется электродвижущей силон (ЭДС) элемента. Она равна разности равновесных потенциалов катода и анода элемента.
= Если на электродах испытывает превращение один моль вещества, то по закону Фарадея через систему протекает количество электричества, равное nF, где n — число молей эквивалентов в одном моле вещества. Таким образом, максимальная электрическая работа гальванического элемента при превращении одного моля вещества равна
где — напряжение гальванического элемента.
В то же время максимальная полезная работа , которую может совершить система при протекании реакции при постоянном давлении, равна энергии Гиббса реакции
Так как , то, приравнивая первые части уравнений получаем
Значения термодинамических характеристик процесса получаются равными . Отсюда =-216800 + 16,1 Т и при температуре 25°С. = -212,3- Вт, г/моль.
Согласно уравнения Нернста один и тот же электрод при различных концентрациях ионов имеет различное значение потенциала, поэтому возможны так называемые концентрационные ГЭ. Рассмотрим, например, ГЭ, составленный из двух медных электродов, опущенных в электролиты с разными концентрациями ионов .
Схема такого ГЭ:
Положим, что , тогда
Работа в концентрационном ГЭ совершается не за счет реакции окисления восстановления, а за счет выравнивания концентрации растворов. Если концентрация электролитов отличаются в 10 раз, то напряжение (э.д.с.) ГЭ равна 0,0295 в, а если в 100 раз, то — 0,059 в.
Применяются для определения одной из концентраций .
Концентрационная и химическая поляризация электронов.
На медном катоде в замкнутом элементе происходит восстановление ионов меди. При этом концентрация их при электродном слое снижается и тем сильнее, чем больше сила тока. Это затрудняет протекание реакции восстановления, и скорость катодной реакции определяется скоростью диффузии ионов к электроду. Уменьшение концентрации катионов меди по формуле Нернста приводит к уменьшению величины потенциала меди. Цинковый анод растворяется и тем с большей скоростью, чем больше сила тока. Это приводит к накоплению ионов цинка в приэлектродном слое, в результате чего его потенциал смещается по указанной причине в положительную сторону. Электроды в этом случае поляризуются благодаря изменению концентрации ионов у их поверхности. Такая поляризация носит название концентрационный или диффузионный.
В ряде случаев кроме поляризации, при протекании тока имеет место и так называемая химическая поляризация. Для иллюстрации этого явления составим следующую цепь:
В данном случае на платине восстанавливаются не ее ионы, поскольку их нет в растворе, а ионы водорода до атомного водорода, который адсорбируется на платине и частично растворяется в ней, а также превращается в молекулярный водород. Платиновый электрод, таким образом, превратится в водородный, т.е. изменится химическая природа электрода. При этом его потенциал сместится в отрицательную сторону. Иными словами, произойдет химическая поляризация катода, которая, как и концентрационная, приводит к уменьшению напряжения гальванического элемента.
Классификация гальванических элементовГальванический элемент состоит из двух электродов: катода (+) и анода (-) и из одного или дух электролитов, разделенных между собой пористой перегородкой, ограничивающей их смешивание. Известны типы гальванических элементов: химические, концентрационные,
окислительно-восстановительные. В гальваническую пару можно сочетать также электроды, принадлежащие к различным видам. При таком сочетании электродов не представляется возможным классифицировать элементы, исходя из природы электродов. Классификация окажется очень громоздкой. Поэтому элементы подразделяют по другим признакам: по особенностям работы, назначению и конструкциям.
Гальванические элементы делят на первичные химические источники тока и вторичные. К первичным относятся вес ранее рассмотренные элементы. Их можно использовать только один раз. После разряда они становятся непригодными к дальнейшей работе.
К вторичным относят аккумуляторы (накопители электричества). Аккумулятор после разряда можно снова зарядить, г.е. превратить продукты реакции путем электролиза в исходные вещества. При этом электрическая энергия превращается в химическую.
Первичные источники тока в свою очередь делят на элементы с жидким электролитом (наливные) и «сухие» (непроливающиеся) элементы с загущенным электролитом. Сухие элементы можно подразделить по признаку катодных деполяризаторов на элементы с твердыми окислителями, воздушной системы и смешанной марганцово-воздушной системы.
Аккумуляторы. Аккумуляторы — обратимые гальванические элементы.
Вещества, из которых изготовляют электроды, и электролиты подобраны в аккумуляторах с таким расчетом, чтобы обратимость химических процессов при электролизе (зарядке) достигалась с минимальной потерей энергии на побочные реакции и в виде теплоты.
Понятно, что медно-цинковый элемент с двумя разделенными пористой перегородкой растворами не пригоден в качестве аккумулятора. Так как происходящие в нем диффузионные процессы необратимы. При этом восстановление ионов цинка до металлического при зарядке будет сопровождаться побочной реакцией восстановления водорода.
Из огромного количества исследованных гальванических элементов удовлетворяют указанным требованиям свинцовый аккумулятор Плантэ, железо-никелевый (кадмиево-никелевый) аккумулятор Эдиссона и серебряно-цинковый аккумулятор Андре.
Свинцовый аккумулятор (рис. 6) был изобретен в результате работ Якоби, Плате и братьев Тюдор. В незаряженном виде он состоит из свинцовых пластин, отлитых в виде решеток. Отверстия отрицательных решеток заполнены пастой из свинцового глета РЬО и воды, а положительных — суриком . Пластины сушат и путем электролиза РЬО превращают губчатый свинец, а — в двуокись свинца . После «формовки током» отрицательные пластины имеют светло-серый цвет, а положительные темно-коричневый. Такие аккумуляторы называют сухозаряженными.
Перед использованием в аккумулятор наливают 30%-ый раствор серной кислоты.
При этом образуется гальваническая цепь:
с напряжением около 2 в (при 18°С в 20%-ый
При разрядке аккумулятора на электродах протекают следующие реакции: на катоде
на аноде
Вещества катода и анода превращаются в сернокислый свинец, а химическая энергия — в электрическую.
При зарядке аккумулятора на электродах протекают следующие реакции:
на катоде
на аноде
Суммируя процессы зарядки и разрядки, получим:
В гальваническом элементе катод заряжен положительно, а анод -отрицательно. При электролизе, наоборот, катод заряжен отрицательно, а анод -положительно. Однако в любом случае на катоде протекает реакция восстановления, а на аноде — окисления. При зарядке и разрядке аккумулятора полярность электродов остается неизменной.
Исходя из равновесных потенциалов и , казалось бы, можно ожидать, что при зарядке свинцового аккумулятора на катоде будет преимущественно восстанавливаться водород, так как равновесный потенциал водородного электрода в сравнении с потенциалом свинца более положителен. В действительности же потенциал восстановления водорода на свинце благодаря его высокому перенапряжению оказывается значительно отрицательнее не только равновесного потенциала водородного электрода, но и потенциала восстановления двухвалентного свинца до металлического. Поэтому на катоде восстанавливается при зарядке только свинец.
После того как на катоде закончится восстановление катионов свинца до металлического свинца, а на аноде — окисление , при дальнейшем электролизе на электродах наблюдается бурное выделение водорода (на катоде) и кислорода (на аноде). При этом напряжение на зажимах повышается до 2,6 в, что указывает на окончание зарядки аккумулятора и начало электролиза воды. Зарядка ведется так, чтобы температура электролита не повышалась более 40°С.
Емкость свинцового аккумулятора около 35вт/ч (20000 кулонов) на 1 кг веса. Последняя возрастает с повышением концентрации кислоты до некоторого предела; максимум емкости соответствует концентрации кислоты около 30% (плотность 1,224).
Свинцовый аккумулятор отдает около 80% подведенной к нему электроэнергии и дает примерно 4 а/ч на 1 дм2 поверхности пластин. Аккумулятор считают практически разряженным, если его напряжение на зажимах упало на 10% (от 2 в).
В щелочном аккумуляторе Эдиссона электродами служат порошкообразное железо и (гидрат окиси никеля, который частично дегидратируется до ), в качестве электролита берут 21%-ный раствор КОН:
К электролиту часто добавляют гидрат окиси лития , который заметно повышает емкость аккумулятора.
Электроды щелочных аккумуляторов изготавливают в виде пакетов из стальной стали с большим числом отверстий для прохода электролита к действующей массе, закладываемой в пакеты. При сборке пластины изолируют одну от другой эбонитовыми стержнями.
При разрядке на электродах протекают следующие процессы:
на катоде
на аноде
Напряжение щелочного аккумулятора равна 1,33 — 1,40 в.
При зарядке на катоде железо из гидрата закиси восстанавливается до металлического; на аноде окисляется до . Водород на железном катоде при зарядке аккумулятора не восстанавливается благодаря чрезвычайно низкой концентрации ионов водорода в растворе щелочи и значительному перенапряжению водорода на железе.
Суммарно процесс зарядки и разрядки можно изобразить следующим уравнением:
Максимальное напряжение при зарядке щелочного аккумулятора равно 1,8 в, конечное напряжение при разрядке 1 — 1,1 в. К.п.д. у щелочных аккумуляторов меньше, чем у свинцовых. Преимуществом щелочных аккумуляторов является их малый вес, простота ухода за ними, а также то обстоятельство, что случайные короткие замыкания не приносят такого вреда, как свинцовым аккумуляторам. При большой скорости образования сернокислого свинца он полу рыхлым, в результате чего электроды аккумулятора разрушаются.
Срок службы щелочных аккумуляторов в зависимости от электролита составляет 250-750 циклов.
Эта теория взята со страницы помощи по химии:
Онлайн помощь по химии
Возможно эти страницы вам помогут:
Пример проблемы ЭДС электрохимической ячейки
Электродвижущая сила ячейки или ЭДС ячейки – это суммарное напряжение между полуреакциями окисления и восстановления, имеющими место между двумя полуреакциями окислительно-восстановительного потенциала. ЭДС ячейки используется, чтобы определить, является ли ячейка гальванической. В этом примере задачи показано, как рассчитать ЭДС ячейки с использованием стандартных восстановительных потенциалов.
Для этого примера необходима таблица стандартных восстановительных потенциалов. В домашней задаче вам должны быть предоставлены эти значения или доступ к таблице.
Пример расчета ЭДС
Рассмотрим окислительно-восстановительную реакцию:
- Mg (тв) + 2 H + (водн.) → Mg 2+ (водн.) + H 2 (г)
- а) Рассчитайте ЭДС ячейки для реакции.
- б) Определите, является ли реакция гальванической.
- Решение:
- Шаг 1: Разбейте окислительно-восстановительную реакцию на полуреакции восстановления и окисления.
Ионы водорода, H + , приобретают электроны при образовании газообразного водорода, H 2 .Атомы водорода восстанавливаются за счет полуреакции:
2 H + + 2 e – → H 2
Магний теряет два электрона и окисляется за счет полуреакции:
Mg → Mg 2+ + 2 e – - Шаг 2: Найдите стандартные восстановительные потенциалы для полуреакций.
Восстановление: E 0 = 0,0000 В
В таблице показаны полуреакции восстановления и стандартные потенциалы восстановления. Чтобы найти E 0 для реакции окисления, переверните реакцию. - Обратная реакция:
Mg 2+ + 2 e – → Mg
Эта реакция имеет E 0 = -2,372 В.
E 0 Окисление = – E 0 Восстановление
E 0 Окисление = – (-2,372 В) = + 2,372 В - Шаг 3: Сложите два E 0 вместе, чтобы найти полную ЭДС ячейки, E 0 ячейка
E 0 ячейка = E 0 уменьшение + E 0 окисление
E 0 ячейка = 0.0000 В + 2,372 В = +2,372 В - Шаг 4: Определите, является ли реакция гальванической. Окислительно-восстановительные реакции с положительным значением E 0 ячейки являются гальваническими.
E 0 Ячейка этой реакции положительная и, следовательно, гальваническая.
- Шаг 1: Разбейте окислительно-восстановительную реакцию на полуреакции восстановления и окисления.
- Ответ:
ЭДС ячейки реакции составляет +2,372 Вольт и является гальванической.
Cell EMF – Chemistry LibreTexts
Электродвижущая сила (ЭДС) – это максимальная разность потенциалов между двумя электродами гальванической или гальванической ячейки.2+ \: (1 \: M) \, | \, Cu _ {\ large {(s)}}} \)
Было измерено, чтосоставляет 1,100 В. Концентрация 1 M в идеальном растворе определяется как стандартное состояние, и 1,100 В, таким образом, составляет стандартную электродвижущую силу , D E o , или потенциал стандартной ячейки для гальванической ячейки \ (\ ce {Zn-Cu} \).
Стандартный потенциал ячейки, D E o , гальванического элемента можно оценить по стандартным потенциалам восстановления двух полуэлементов E o .+ \: (1.0 \: M)} \).
Его восстановительный или окислительный потенциал точно равен нулю.
Восстановительные потенциалы всех других полуэлементов, измеренные в вольтах относительно SHE, представляют собой разность электрической потенциальной энергии на кулон заряда.
Обратите внимание, что единица измерения энергии J = кулоновский вольт, а свободная энергия Гиббса G является произведением заряда q и разности потенциалов E :
для расчета электрической энергии.2 +} \) составляет 1,0 M, а давление \ (\ ce {h3} \) составляет 1,0 атм, разность напряжений между двумя электродами будет -0,763 В (\ (\ ce {Zn} \ ) электрод является отрицательным электродом). Вышеуказанные условия называются стандартными условиями , а полученная таким образом ЭДС равна стандартному восстановительному потенциалу .
Обратите внимание, что указанная выше ячейка находится в обратном порядке по сравнению с ячейкой, приведенной во многих учебниках, но эта компоновка дает стандартные потенциалы восстановления напрямую, потому что полуячейка \ (\ ce {Zn} \) является полуячейкой восстановления. + \ 🙁 1.\ circ = \ textrm {-3,844 В} \)
ОБСУЖДЕНИЕ
Отрицательный потенциал указывает на то, что обратная реакция должна быть спонтанной.
В некоторых калькуляторах используется литиевая батарея. Атомный вес \ (\ ce {Li} \) равен 6.94, что намного легче, чем \ (\ ce {Zn} \) (65.4).
Калькулятор ЭДС– Электродвижущая сила ячейки
Калькулятор ЭДС ячейки – это простой инструмент, который предоставляет вам значение электродвижущей силы (ЭДС) для любой гальванической (гальванической) ячейки с заданным потенциалом электродов.Если вы немного запутались во всех этих терминах, не волнуйтесь! В статье ниже вы найдете краткое описание того, что такое ЭДС, как рассчитать ЭДС, а также примеры источников электродвижущей силы. Кроме того, мы подготовили объяснение окислительно-восстановительной реакции и гальванического элемента. Краткое пошаговое руководство демонстрирует использование нашего калькулятора. Прокрутите вниз, чтобы продолжить чтение!
Что такое ЭДС?
ЭДС – это сокращение от электродвижущей силы. По определению, ЭДС – это сила или электрическое давление, которое генерирует ток в цепи.Единицы измерения ЭДС – вольт [В].
Чтобы лучше понять это определение, рассмотрим типичный гальванический или гальванический элемент, состоящий из двух электродов. Электродвижущая сила – это разность потенциалов между ними.
Кроме того, электродвижущая сила гальванического элемента определяет способность электрохимического элемента вызывать поток электронов через электрическую цепь.
Уравнение ЭДС
Электродвижущую силу электрохимической ячейки можно рассчитать по уравнению:
ЭДС ячейка [В] = E катод [В] – E анод [В]
, где E катод – потенциал катода (в вольтах), а E anode – потенциал анода (в вольтах).Помните, что в ячейке потенциал катода выше, чем потенциал анода.
Электропотенциалы анода и катода
Если вы хотите определить потенциал металлического электрода, один из способов – проверить гальваническую серию и найти конкретный металл в таблице. Второй способ – рассчитать его с помощью уравнения Нерста, также известного как уравнение потенциала клетки. Эта формула позволяет рассчитать восстановительный потенциал реакции полуячейки или целой клетки. Щелкните здесь и узнайте, как это сделать.
В приведенной ниже таблице можно найти электропотенциал металлов :
| Электрод | E⁰ [V] |
|---|---|
| Li / Li⁺ | -3,04 |
| Ca / Ca²⁺ | -2,86 |
| Мг / Мг²⁺ | -2,36 |
| Al / Al³⁺ | -1,69 |
| Mn / Mn²⁺ | -1,18 |
| Zn / Zn²⁺ | -0.76 |
| Cr / Cr³⁺ | -0,74 |
| Fe / Fe²⁺ | -0,44 |
| Кд / Кд²⁺ | -0,40 |
| Co / Co²⁺ | -0,28 |
| Ni / Ni²⁺ | -0,26 |
| Sn / Sn²⁺ | -0,14 |
| Pb / Pb²⁺ | -0,14 |
| Fe / Fe³⁺ | -0.04 |
| H₂ / 2H⁺ | 0,00 |
| Bi / Bi³⁺ | +0,32 |
| Cu / Cu²⁺ | +0,34 |
| Ag / Ag⁺ | +0,80 |
| Hg / Hg²⁺ | +0,85 |
| Au / Au³⁺ | +1,52 |
Как рассчитать ЭДС?
Взгляните на приведенный ниже пример расчета ЭДС.
Рассмотрим элемент Даниэля – простой электрохимический элемент, изобретенный в 1836 году британским химиком и метеорологом Джоном Фредериком Дэниеллом. В этой ячейке медь погружена в раствор сульфата меди (II), а цинк – в раствор сульфата цинка.
Схема ячейки: (-) Zn | Zn2 + || Cu2 + | Cu (+)
- Проверить потенциал металла: электродный потенциал цинка -0,76 В, меди +0,34 В ⇒ из-за более низкого потенциала цинк является анодом, а медь – катодом.Введите эти значения в наш калькулятор.
- Рассчитайте значение ЭДС электрохимической ячейки по формуле:
ЭДС ячейка = +0,34 В – (-0,76 В) = 1,10 В
Вот оно! Электродвижущая сила ячейки Даниэля равна 1,10 вольт.
Источники электродвижущей силы
Ниже вы можете найти несколько примеров источников ЭМП:
- батареи
- генераторы
- гальванические элементы
- солнечные элементы
- топливные элементы
- термопары
- некоторые живые организмы (например,г., электрический угорь)
Каждый из перечисленных выше источников ЭДС содержит источник энергии, который индуцирует поток электрических зарядов. Этими источниками могут быть химические процессы (в батареях, топливе и гальванических элементах), механические силы (в генераторах переменного тока), электромагнитное излучение, испускаемое Солнцем (в солнечных элементах) и разница температур (в термопарах).
Типы электрохимических ячеек
Электрохимический элемент – один из видов источников энергии. Его можно создать, поместив металлические электроды в электролит, где в результате химической реакции либо генерируется, либо используется электрический ток.Электрохимические ячейки, генерирующие электрический ток, называются гальваническими ячейками (названными в честь их изобретателя, итальянского физика Алессандро Вольта) или гальваническими ячейками (названными в честь итальянского физика и врача Луиджи Гальвани). Обычные батареи состоят из одного или нескольких таких элементов. В других электрохимических ячейках внешний электрический ток используется для запуска химической реакции (которая не может происходить спонтанно).
Гальванический элемент
В любом электрохимическом процессе электроны (полученные в результате окислительно-восстановительной реакции) переходят от одного химического вещества к другому.Два металлических электрода (анод и катод), погруженные в солевой раствор, создают гальванический элемент, который вызывает прохождение электрического тока. У этих металлов должна быть другая тенденция к потере электронов. Катод (+) – это электрод с более высоким электрическим потенциалом, а анод (-) – с более низким электрическим потенциалом.
Полуреакция окисления происходит на аноде, а полуреакция восстановления происходит на катоде. И анод, и катод являются электродами, но анод заряжен отрицательно, а катод – положительно.Обычный ток идет от катода к аноду, а электроны текут от анода к катоду.
Окислительно-восстановительная реакция
Процессы восстановления и окисления происходят только вместе (невозможно, чтобы эти реакции происходили отдельно). Вот почему окислительно-восстановительные реакции можно описать как две полуреакции, одна представляет собой процесс окисления, а другая – процесс восстановления. Посмотрим на это на примере ячейки Даниэля. В ячейке Даниэля медь погружается в раствор сульфата меди (II), а цинк – в раствор сульфата цинка.В этой ячейке цинк действует как анод (из-за более низкого электрического потенциала), а медь действует как катод (из-за более высокого электропотенциала):
- E⁰ из цинкового электрода = -0,76 В
- E⁰ из меди электрода = +0,34 В
Общая химическая реакция ячейки Даниелла: Zn (тв.) + Cu²⁺ (водн.) → Zn²⁺ (водн.) + Cu (s)
Окисление (на аноде): Zn (s) → Zn²⁺ (водн.) + 2e⁻
Восстановление (на катоде): Cu²⁺ (водн.) + 2e⁻ → Cu (s)
Число электронов, потерянных восстановителем, равно числу электронов, полученных окислителем (для любой окислительно-восстановительной реакции).
КАК РАССЧИТАТЬ ЭДС ЯЧЕЙКИ?
Что такое электродвижущая сила (ЭДС)?Электродвижущая сила (ЭДС) – это самая высокая разность потенциалов между двумя электродами гальванического или гальванического элемента. Это количество отождествляется со склонностью атома принимать (приобретать) или высвобождать (терять) электроны. Например, самый экстремальный потенциал среди Zn и Cu известной ячейки был определен как 1,100 В.
Zn (ов) | Zn2 + (1M) || Cu2 + (1M) | Cu (т)
В идеальном растворе концентрация 1 M характеризуется как типичное состояние, а 1.100 В – это стандартная электродвижущая сила, Eo или стандартный потенциал ячейки для гальванической ячейки Zn-Cu.
Стандартный потенциал гальванического элемента можно оценить по стандартным потенциалам восстановления двух полуэлементов. Потенциалы восстановления оцениваются по стандартному водородному аноду (SHE):
Pt (s) | H 2 (г, 1,0 атм) | H + (1.0M)
Его восстановительный или окислительный потенциал фактически равен нулю.
Восстановительные потенциалы всех других полуэлементов, рассчитанные в вольтах относительно SHE, представляют собой разность потенциальной энергии (электрической) для каждого кулоновского заряда.
Единица измерения энергии, Дж = кулон-вольт,
Свободная энергия Гиббса (G) – это результирующая разность потенциалов (E) и заряда (q)
G (в Дж) = q E (в КВ) для расчетов электроэнергии.
Стандартный потенциал гальванических элементовГальванический элемент состоит из двух полуэлементов.Согласно правилам записи гальванических элементов катод (восстановительный) помещается с правой стороны, а анод (окислительный) – с левой.
Pt | h3 | H + || Zn 2+ | Zn
Например, ячейка включает реакции восстановления и окисления:
h3 → 2e− + 2H + анодная (окислительная) реакция
Zn 2+ + 2e− → Zn катодная (восстановительная) реакция
Если концентрация ионов H + и Zn 2+ равна 1.0 M и давление H 2 составляет 1,0 атм, разность напряжений между двумя электродами будет -0,763 В (катод из цинка является отрицательной клеммой). Вышеуказанные условия известны как стандартные условия, а полученная таким образом ЭДС является стандартным восстановительным потенциалом ячейки.
Вышеупомянутое представление ячеек в порядке, обратном тому, что дано во многих учебниках; однако эта ориентация напрямую указывает на стандартные восстановительные потенциалы, поскольку Zn-полуячейка является восстановительной полуячейкой.Отрицательное напряжение предполагает, что обратная химическая реакция является спонтанной. Это соответствует тому, как металлический Zn реагирует с кислотой с образованием газа h3.
В качестве другой модели ячейка представлена как Pt | h3 | H + || Cu + | Cu состоит из реакции восстановления и реакции окисления.
H 2 → 2e− + 2H + анодная реакция
Cu 2+ + 2e− → Cu катодная реакция
Стандартный потенциал ячейки равен 0,337 В.Положительный потенциал означает спонтанную реакцию,
Cu 2+ + H 2 → Cu + 2H +
В любом случае потенциал настолько мал, что реакция идет слишком медленно, чтобы ее можно было как-либо наблюдать.
Видео по теме:
Уравнения для расчета ЭДСЕсть два основных уравнения для вычисления ЭДС. Наиболее важным определением является количество джоулей энергии (E), которое выделяет каждый кулон заряда (Q) при прохождении через ячейку.
ε = E ÷ Q
Здесь
ε à символ электродвижущей силы,
E в цепи энергии
Q à заряд цепи.
Если дана результирующая энергия и мера заряда, проходящего через элемент, то это простейший метод вычисления ЭДС; однако вы не будете часто получать эту информацию.
Найдите ЭДС по формуле:ε = V + Ir
Здесь
В à напряжение ячейки
I – ток в цепи
r à внутреннее сопротивление ячейки.
Его также можно записать и использовать в форме закона Ома (V = IR).
При сравнении закона Ома с уравнением ЭДС его можно записать как:
ε = I (R + r)
Здесь
I à ток
R à сопротивление цепи
R à внутреннее сопротивление ячейки.
Сходство двух уравнений (a) и (b), указанных ниже
ε = IR + Ir…. (а)
= V + Ir…. (б)
показывает, что вы можете вычислить ЭДС в том случае, если заданы напряжение на клеммах, протекающий ток и внутреннее сопротивление ячейки.
Шаги для расчета ЭДСПример задачи 1: Если есть цепь с разностью потенциалов 3,2 В, ток 0,6 А течет с внутренним сопротивлением батареи 0,5 Ом. Найдите ЭДС клетки.
Sol 1: Дано: V = 3,2 V
I = 0,6 А
r = 0,5 Ом
Мы знаем, что ε = V + Ir
Подставляя указанные значения в приведенную выше формулу, получаем:
= 3,2 В + 0.6 А × 0,5 Ом
= 3,2 В + 0,3 В = 3,5 В
Значит, ЭДС цепи 3,5 В.
В приведенном выше примере показано, как вычислить ЭДС ячейки с использованием стандартных восстановительных потенциалов.
Пример задачи 2 : Рассчитать ЭДС ячейки (при стандартных условиях), в которой металлический цинк соединяется с кислотой с образованием ионов цинка и газообразного водорода?
Sol 2: Первый шаг – записать реакции полуэлементов в виде одноэлектронных восстановлений R:
Если ячейка не изображена, случайным образом назначьте реакции правой и левой руки
R : H + + e- → ½ H 2 (g) E o = 0 В (согласно определению)
L : ½ Zn 2+ + e = Zn (s) E o = – 0.76В
Так как ЭМП – интенсивное свойство; следовательно, это не зависит от количества реагирующего материала. Если мы разделим уравнение уменьшения на некоторое число, как это сделано во втором уравнении выше, ЭДС не изменится.
ЭДС ячейки: E o справа – E o слева
Таким образом, (R – L) à H + (вод.) + ½ Zn (s) = ½ H 2 (г) + ½ Zn 2+ (вод.)
ЭДС ячейки = + 0,76В.
Пример задачи 3 :: Рассчитать ЭДС ячейки для реакции между Zn и Fe3 + / Fe2 +
Sol 3: Как и в предыдущей задаче,
Сначала мы записываем правую и левую реакции случайным образом
R : Fe 3+ (водный) + e- (водный) = Fe2 + (водный)… ..E o = + 0,77V
L : ½ Zn2 + (водн.) + E – (водн.) = ½ Zn (s)…. .E o = – 0,76 В
Так как ЭМП – интенсивное свойство; следовательно, это не зависит от количества реагирующего материала.Если мы разделим уравнение уменьшения на некоторое число, как это сделано во втором уравнении выше, ЭДС не изменится.
ЭДС ячейки: E o справа – E o слева
- (R – L): Fe 3+ (водн.) + ½ Zn (s) = Fe 2+ (водн.) + ½ Zn 2+ (водн.) ….
ЭДС ячейки = +0,77 – (- 0,76) = + 1,53В
Важные разделы:
Потенциал ячеек | Безграничная химия
Уравнение Нернста
В электрохимии уравнение Нернста можно использовать для определения восстановительного потенциала электрохимической ячейки.
Цели обучения
Вспомните уравнение Нернста
Основные выводы
Ключевые моменты
- В электрохимии уравнение Нернста можно использовать для определения восстановительного потенциала полуячейки в электрохимической ячейке.
- Уравнение Нернста также можно использовать для определения полного напряжения (электродвижущей силы) для полной электрохимической ячейки.
- Уравнение Нернста дает формулу, которая связывает численные значения градиента концентрации с электрическим градиентом, который его уравновешивает.
Ключевые термины
- электрохимия : Наука о химии, связанная с потоком электричества, особенно на поверхности электрода.
- электрохимическая ячейка : емкость, содержащая электролит и два электрода; используется для производства электроэнергии постоянного тока. Один или несколько из них составляют батарею.
- напряжение : величина электростатического потенциала между двумя точками в пространстве.
- электродвижущая сила : Напряжение, генерируемое батареей или переменным магнитным полем.
В электрохимии уравнение Нернста может использоваться вместе с другой информацией для определения восстановительного потенциала полуэлемента в электрохимическом элементе. Его также можно использовать для определения полного напряжения или электродвижущей силы для полной электрохимической ячейки. \ text {o} – \ frac {0.\ text {b}} [/ latex], где прописные буквы означают концентрации, а строчные буквы – стехиометрические коэффициенты реакции: [latex] \ text {aA} + \ text {bB} \ rightarrow \ text {cC} + \ text {dD} [/ latex]
Пример
Найдите потенциал гальванического элемента на основе следующих полуреакций восстановления, где [Ni 2+ ] = 0,030 M и [Pb 2+ ] = 0,300 M.
Ni 2+ + 2 e- → Ni, E 0 = -0,25 В
Pb 2+ + 2 e- → Pb, E 0 = -0.\ text {o} – \ frac {0.0257} {\ text {n}} \ text {ln} \ Q [/ latex]
[латекс] \ text {E} = 0.12 \ text {V} – \ frac {0.0257} {2} \ text {ln} \ frac {0.030} {0.300} [/ latex]
[латекс] \ text {E} = 0,15 \ \ text {V} [/ латекс]
Концентрация клеток
Вальтер Нернст предложил математическую модель для определения влияния концентрации реагента на потенциал электрохимической ячейки.
Цели обучения
Обсудите последствия уравнения Нернста для электрохимического потенциала ячейки
Основные выводы
Ключевые моменты
- В 20 веке немецкий химик Вальтер Нернст предложил математическую модель для определения влияния концентрации реагента на потенциал электрохимической ячейки.\ text {o} – \ frac {\ text {RT}} {\ text {nF}} \ times \ text {ln} \ \ text {Q} [/ latex].
Ключевые термины
- электрохимическая ячейка : емкость, содержащая электролит и два электрода; используется для производства электроэнергии постоянного тока. Один или несколько из них составляют батарею.
- свободная энергия : разница между внутренней энергией системы и произведением ее энтропии и абсолютной температуры.
Свободная энергия Гиббса и потенциал ячейки
Стандартный потенциал электрохимической ячейки требует стандартных условий для всех реагентов.\ text {o} + \ text {RT} \ times \ text {ln} \ \ text {Q} [/ latex]
Здесь ΔG – изменение свободной энергии Гиббса, T – абсолютная температура, R – газовая постоянная и Q – коэффициент реакции. В химии коэффициент реакции является функцией активности или концентрации химических веществ, участвующих в химической реакции. Ключевой вклад Гиббса заключался в формализации понимания влияния концентрации реагентов на спонтанность.\ text {o} – \ text {RT} \ times \ text {ln} \ \ text {Q} [/ latex]
Здесь n – число молей электронов, F – постоянная Фарадея ([latex] \ frac {\ text {Coulombs}} {\ text {мол}} [/ latex]) и ΔE – потенциал клетки.
Вальтер Нернст : Портрет Вальтера Нернста
Уравнение Нернста
Наконец, Нернст разделил на количество переданного заряда, чтобы получить новое уравнение, которое теперь носит его имя.\ text {o} – \ frac {\ text {RT}} {\ text {nF}} \ times \ text {ln} \ \ text {Q} [/ latex]
Уравнение Нернста можно использовать для расчета изменений выходного напряжения в паре полуэлементов в нестандартных условиях.
Типичный гальванический электрохимический элемент : В стандартных условиях выходной сигнал этой пары полуэлементов хорошо известен. Когда происходит изменение концентрации или активности реагентов, либо изменяется температура или давление, выходное напряжение изменяется.Он рассчитывается с помощью уравнения Нернста.
Свободная энергия и потенциал клеток
В гальванической ячейке, где спонтанная окислительно-восстановительная реакция заставляет ячейку производить электрический потенциал, изменение свободной энергии Гиббса должно быть отрицательным.
Цели обучения
Рассчитайте изменение свободной энергии Гиббса электрохимической ячейки и обсудите его значение для того, будет ли окислительно-восстановительная реакция спонтанной
Основные выводы
Ключевые моменты
- В гальваническом элементе свободная энергия Гиббса связана с потенциалом следующим образом: Δ G ° ячейка = – nFE ° ячейка .
- Если E ° cell> 0, то процесс самопроизвольный (гальванический элемент).
- Если E ° ячейки <0, то процесс не самопроизвольный (электролитическая ячейка).
Ключевые термины
- гальванический элемент : Электрохимический элемент, который получает электрическую энергию в результате спонтанной окислительно-восстановительной реакции, происходящей внутри элемента.
- потенциал электрода : разность потенциалов полуреакции, которая происходит в обратимой ячейке, состоящей из любого электрода и стандартного водородного электрода.
- Свободная энергия Гиббса : разница между энтальпией системы и произведением ее энтропии и абсолютной температуры; мера полезной работы, получаемой от термодинамической системы при постоянных температуре и давлении.
- окислитель : Любое вещество, которое окисляет другое или принимает электроны от другого; при этом он уменьшается.
Основой для электрохимического элемента, такого как гальванический элемент, всегда является окислительно-восстановительная реакция, которая может быть разбита на две полураакции: окисление происходит на аноде, где происходит потеря электронов, и восстановление происходит на катоде. , где происходит усиление электронов.Электричество генерируется из-за разницы электрических потенциалов между двумя электродами. Это связано с тем, насколько легко окисленные частицы отдают электроны и насколько сильно восстановленные частицы хотят их получить.
Электрохимическая ячейка : Демонстрационная установка электрохимической ячейки, напоминающая ячейку Даниэля. Две полуячейки связаны солевым мостиком, переносящим ионы между собой. Электроны текут во внешней цепи.
В электрохимии стандартный потенциал электрода, обозначаемый сокращенно E °, является мерой индивидуального потенциала обратимого электрода в стандартном состоянии, который представляет собой растворенные вещества с эффективной концентрацией 1 М и газы под давлением 1 атм.Чаще всего значения табулируются при 25 ° C (298 K).
Он окислен или восстановлен?
Поскольку стандартные электродные потенциалы указаны в их способности снижаться, чем больше стандартные потенциалы восстановления, тем легче их уменьшить; Другими словами, они просто лучшие окислители. Например, F 2 имеет потенциал 2,87 В, а Li + имеет потенциал -3,05 В. F 2 легко восстанавливается и поэтому является хорошим окислителем.Напротив, Li (s) скорее подвергнется окислению, поэтому он является хорошим восстановителем.
В примере Zn 2+ , стандартный потенциал восстановления которого составляет -0,76 В, он может быть окислен любым другим электродом, стандартный потенциал восстановления которого больше -0,76 В, и может быть уменьшен любым электродом со стандартным потенциалом восстановления меньше чем -0,76 В.
Знак изменения свободной энергии Гиббса
В гальванической ячейке, где спонтанная окислительно-восстановительная реакция заставляет ячейку производить электрический потенциал, изменение свободной энергии Гиббса должно быть отрицательным.\ text {o} [/ latex]
Здесь n – число молей электронов, а F – постоянная Фарадея (96 485 [латекс] \ frac {\ text {Coulombs}} {\ text {мол}} [/ латекс]). Таким образом, применяются следующие правила:
- Если E ° ячейка > 0, то процесс самопроизвольный (гальванический элемент)
- Если E ° ячейка <0, то процесс не самопроизвольный (необходимо подавать напряжение, как в электролитической ячейке)
Пример
Рассчитайте изменение свободной энергии Гиббса электрохимической ячейки, в которой происходит следующая окислительно-восстановительная реакция:
[латекс] \ text {Pb} ^ {2+} + \ text {Ni} \ rightarrow \ text {Ni} ^ {2+} + \ text {Pb} \ \ \ \ \ \ \ \ \ text {E } ^ \ text {o} = 0.\ text {o} = -23,156 \ \ text {J} \ = -2,3 \ \ text {kJ} [/ latex]
Поскольку изменение свободной энергии Гиббса отрицательно, окислительно-восстановительный процесс является спонтанным.
Константа равновесия и потенциал ячейки
Константу равновесия K можно рассчитать с помощью уравнения Нернста.
Цели обучения
Рассчитайте константу равновесия K для гальванического элемента, используя уравнение Нернста
Основные выводы
Ключевые моменты
- В электрохимической ячейке каждый химический компонент будет перемещаться из областей с более высоким электрохимическим потенциалом в области с более низким электрохимическим потенциалом.
- Уравнение Нернста можно использовать для определения равновесного восстановительного потенциала полуячейки в электрохимической ячейке.
- Уравнение Нернста также можно использовать для определения полного напряжения или электродвижущей силы для полной электрохимической ячейки.
Ключевые термины
- Уравнение Нернста : Используется для определения равновесного восстановительного потенциала полуячейки в электрохимической ячейке, а также общего напряжения для полной электрохимической ячейки.
Электрохимический потенциал
Каждый химический вид имеет электрохимический потенциал (количество в единицах энергии) в любом заданном месте, что показывает, насколько легко или сложно добавить больше этого вида в это место. Если возможно, вид переместится из областей с более высоким электрохимическим потенциалом в области с более низким электрохимическим потенциалом. В равновесии электрохимический потенциал будет постоянным везде для каждого вида. Для каждого вида может быть разное значение.
Например, если в стакане воды есть ионы натрия (Na + ), растворенные в нем однородно, и электрическое поле приложено к воде, то ионы натрия будут стремиться притягиваться электрическим полем в одну сторону. Мы говорим, что ионы обладают электрической потенциальной энергией и движутся, чтобы снизить свою потенциальную энергию.
Точно так же, если стакан воды имеет много растворенного сахара с одной стороны и ни одного – с другой стороны, каждая молекула сахара будет беспорядочно распространяться вокруг воды до тех пор, пока повсюду не будет равная концентрация сахара.Мы говорим, что молекулы сахара обладают «химическим потенциалом», который выше в областях с высокой концентрацией, и молекулы движутся, чтобы снизить свой химический потенциал.
Эти два примера показывают, что электрический потенциал и химический потенциал могут дать один и тот же результат: перераспределение химических частиц. Следовательно, имеет смысл объединить их в единый «потенциал», электрохимический потенциал, который может напрямую дать общее перераспределение, если учесть и то, и другое.
Уравнение Нернста и электрохимический потенциал
В электрохимии уравнение Нернста может использоваться вместе с другой информацией для определения равновесного восстановительного потенциала полуячейки. Его также можно использовать для определения полного напряжения или электродвижущей силы для полной электрохимической ячейки. Уравнение Нернста дает формулу, которая связывает численные значения градиента концентрации с электрическим градиентом, который его уравновешивает.
Например, допустим, градиент концентрации был установлен путем растворения KCl в половине разделенного сосуда, который изначально был заполнен H 2 O.Между двумя половинами была введена мембрана, проницаемая для ионов K + . Эмпирически может возникнуть ситуация равновесия, когда градиент химической концентрации может быть уравновешен электрическим градиентом, который противодействует движению заряда. Другими словами, можно было приложить напряжение, чтобы остановить движение ионов K + .
Можно также рассмотреть пример, в котором решениями являются CuSO 4 и ZnSO 4 . В каждом растворе есть соответствующая металлическая полоска и солевой мостик или пористый диск, соединяющий два раствора.Это позволяет ионам SO 4 2- свободно перемещаться между растворами меди и цинка. Чтобы рассчитать стандартный потенциал, мы должны найти полуракции меди и цинка.
Стандартный потенциал ячейки для реакции равен +0,34 В – (-0,76 В) = +1,10 В. Полярность ячейки определяется, зная, что металлический цинк является более сильным восстановителем, чем металлическая медь. Следовательно, стандартный восстановительный потенциал цинка более отрицательный, чем у меди.\ text {o} – \ frac {\ text {RT}} {\ text {nF}} \ text {ln} \ text {Q} [/ latex]
В этом уравнении E – потенциал ячейки, E o – стандартный потенциал ячейки (т. Е. Измеренный в стандартных условиях), F – постоянная Фарадея, R – универсальная газовая постоянная, T – температура в градусах Кельвина, Q – коэффициент реакции (который имеет то же алгебраическое значение, что и выражение константы равновесия, за исключением того, что оно применяется к любому времени в ходе реакции), а n – количество молей электронов. которые передаются в сбалансированном химическом уравнении окислительно-восстановительного процесса.\ text {o}} {\ text {RT}} [/ latex]
В этой задаче переносятся 2 моля электронов, F – 96485 [латекс] \ frac {\ text {Coulombs}} {\ text {мол}} [/ latex], R – 8,31 [латекс] \ frac {\ text {Джоуль}} {\ text {K} \ times \ text {моль}} [/ latex], T – 298 K, а E o – 1,10 [латекс] \ frac {\ text {Джоуль}} {\ текст {Кулон}} [/ латекс].
Подставляя значения в уравнение, получаем:
[латекс] \ text {ln} \ \ text {K} = \ frac {2 \ times 96485 \ times 1.10} {8.31 \ times 298} [/ латекс]
[латекс] \ text {ln} \ \ text {K} = 85.7 [/ латекс]
Решая относительно K, получаем:
К = е 85,7
К = 1,68 x 10 37
Это особенно высокое значение константы равновесия, указывающее на то, что равновесие сильно способствует образованию продуктов (реакция фактически необратима по отношению к образованию продуктов).
Электродвижущая сила – обзор
2.6 Серия электродвижущей силы
Ряды ЭДС стандартного потенциала электрода полуячейки по водородной шкале приведены в таблице 2.2. Реакции в этой таблице записаны как реакции восстановления слева направо при T = 25 ° C. Они имеют ту же полярность, что и восстановительный потенциал, который измеряется экспериментально.
Таблица 2.2. Стандартные электродные потенциалы при 25 ° C и их изотермические температурные коэффициенты [12]
| Реакция электродов | e ° ( V по сравнению с SHE) | dE ° dT × 103V ° C | |||
|---|---|---|---|---|---|
| Li + | Li | Li + + e – = Li | – 3.045 | – 0,534 | ||
| руб. + | руб. | руб. + + e – = | руб. + + e – = Cs– 2,923 | – 1,197 | ||
| K + | K | K + + e – = K | – 2,925 | – 1,080 | ||
| Ra 2 + | Ra | Ra 2 + + 2e – = Ra | – 2.916 | – 0,59 | ||
| Ba 2 + | Ba | Ba 2 + + 2e – = Ba | – 2,906 | – 0,395 | ||
| Ca 2 + | Ca | Ca 2 + | Ca | Ca 2 + + 2e – = Ca | – 2,866 | – 0,175 | |
| Na + | Na | Na + + e – = Na | – 2,714 | – 0,772 | ||
| La 3 + | La | La 3 + + 3e – = La | – 2.522 | + 0,085 | ||
| Mg 2 + | Mg | Mg 2 + + 2e – = Mg | – 2,363 | + 0,103 | ||
| Be 2 + + 2e – = Be | – 1,847 | + 0,565 | |||
| Al 3 + | Al | Al 3 + + 3e – = Al | – 1,662 | + 0,504 | ||
| Ti 2 + | Ti | Ti 2 + + 2e – = Ti | – 1.628 | – | ||
| Zr 4 + | Zr | Zr 4 + + 4e – = Zr | – 1,529 | – | ||
| V 2 + 3 | V | | V | 2 + + 2e – = V | – 1.186 | – | |
| Mn 2 + | Mn | Mn 2 + + 2e – = Mn | – 1.180 | – 0,08 | ||
| Zn 2 + | Zn | Zn 2 + + 2e – = Zn | – 0.762 | + 0,09 | ||
| Cr 3 + | Cr | Cr 3 + + 3e – = Cr | – 0,744 | + 0,468 | ||
| SbO 2 – Sb | SbO 2 – + 2H 2 O + 3e – = Sb + 4OH – | – 0,670 | – | ||
| Ga 3 + | Ga | Ga 3 + + 3e – = Ga | – 0.529 | + 0,67 | ||
| S 2– | S | S + 2e – = S 2– | –0,510 | – | ||
| Fe 2 + 3 | Fe | Fe 2 + + 2e – = Fe– 0,440 | + 0,052 | |||
| Cr 3 + , Cr 2 + | Pt | Cr 3 + + e – = Cr 2 + | – 0,408 | – | ||
| Cd 2 + | Cd | Cd 2 + + 2e – = Cd | – 0.402 | – 0,093 | ||
| Ti 3 + , Ti 2 + | Pt | Ti 3 + + e – = Ti 2 + | – 0,369 | – | ||
| Tl + | Tl | Tl + + e – = Tl | – 0,336 | – 1,327 | ||
| Co 2 + | Co | Co 2 + + 2e – = Co | – 0,277 | + 0,06 | ||
| Ni 2 + | Ni | Ni 2 + + 2e – = Ni | – 0.250 | + 0,06 | ||
| Mo 3 + | Mo | Mo 3 + + 3e – = Mo | – 0,20 | – | ||
| Sn 2 + | Sn | Sn 2 + + 2e – = Sn– 0,138 | – 0,282 | |||
| Pb 2 + | Pb | Pb 2 + + 2e – = Pb | – 0,126 | – 0,451 | ||
| Ti 4 + , Ti 3 + | Pt | Ti 4 + + e – = Ti 3 + | – 0.040 | – | ||
| H + , H 2 | Pt | H + + e – = ½ H 2 | ± 0,000 | ± 0,000 (+ 0,871) ⁎ | ||
| Sn 4 + , Sn 2 + | Pt | Sn 4 + + 2e – = Sn 2 + | + 0,015 | – | ||
| Cu 2 + , Cu + | Pt | Cu 2 + + e – = Cu + | + 0.153 | + 0,073 | ||
| Cu 2 + | Cu | Cu 2 + + 2e – = Cu | + 0,337 | + 0,008 | ||
| Fe (CN) 6 3 – , Fe (CN) 6 4 – | Pt | Fe (CN) 6 3 – + e – = Fe (CN) 6 4 – | + 0,360 | – | ||
| OH – , O 2 | Pt | ½ O 2 + H 2 O + 2e – = 2OH – | + 0.401 | – 0,440 | ||
| Cu + | Cu | Cu + + e – = Cu | + 0,521 | – 0,058 | ||
| I – | I 2 , Pt | I 2 + 2e – = 2I – | + 0,535 | – 0,148 | ||
| MnO 4 – , MnO 4 2- 3 | Pt | 4 – + e – = MnO 4 2 –+ 0.564 | – | |||
| Fe 3 + , Fe 2 + | Pt | Fe 3 + + e – = Fe 2 + | + 0,771 | + 1,188 | ||
| Hg 2 2 + | Hg | Hg 2 2 + + 2e – = 2Hg | + 0,788 | – | ||
| Ag + | Ag | Ag + + e – = Ag | + 0.799 | – 1.000 | ||
| Hg 2 + | Hg | Hg 2 + + 2e – = Hg | + 0.854 | – | ||
| Hg g + + Hg g + + | Pt | Hg 2 + + e – = Hg + | + 0,910 | – | ||
| Pd 2 + | Pd | Pd 2 + + 2e – = Pd | + 0,987 | – | ||
| Br – | Br 2 , Pt | Br 2 + 2e – = 2Br – | + 1.065 | – 0,629 | ||
| Pt 2 + | Pt | Pt 2 + + 2e – = Pt | + 1.200 | – | ||
| Mn + , H | MnO 2 , Pt | MnO 2 + 4H + + 2e – = Mn 2 + + 2H 2 O | + 1,230 | – 0,661 | ||
| Cr 3 + , Cr 2 O 7 2 – , H + | Pt | Cr 2 O 7 2 – + 14H + + 6e – = 2Cr 3 + + 7H 2 O | + 1.330 | – 1,263 | ||
| Класс – | Класс 2 , Pt | Класс 2 + 2e – = 2Cl – | + 1,359 | – 1,260 | ||
| PbO 2 + 4H + + 2e – = Pb 2 + + 2H 2 O | + 1.455 | – 0,238 | |||
| Au 3 + | Au | Au 3 + + 3e – = Au | + 1.498 | – | ||
| MnO 4 – , H + | MnO 2 , Pt | MnO 4 – + 4H + + 3e – = MnO 2 + 2H 2 O | + 1,695 | – 0,666 | ||
| Ce 4 + , Ce 3 + | Pt | Ce 4 + + e – = Ce 3 + | + 1.610 | – | ||
| SO 4 2 – , H + | PbSO 4 , PbO 2 , Pb | PbO 2 + SO 4 2 – + 4H + + 2e – = PbSO 4 + 2H 2 O | + 1.682 | + 0,326 | ||
| Au + | Au | Au + + e – = Au | + 1,691 | – |
Из уравнения. (2.38) невозможно различить, какие из участников реакции являются реагентами (окисленные частицы), а какие – продуктами (восстановленные частицы). Следующие правила были приняты Международным союзом теоретической и прикладной химии (IUPAC) в Стокгольме в 1953 году, чтобы решить вопрос о признаках электродного потенциала и определить, какие вещества следует рассматривать как реагенты, а какие как продукты.Любая электрохимическая ячейка в соответствии с этим соглашением записывается слева направо следующим образом: (i) материал одного из двух электродов, (ii) раствор, контактирующий с одним электродом, (iii) раствор, контактирующий с второй электрод и (iv) материал второго электрода. В записанном выражении электроды отделены от растворов одной полосой, а растворы – двойной полосой, что указывает на отсутствие диффузионного потенциала между растворами в ячейке.
Из двух электродных потенциалов полуэлемента только потенциал E может быть измерен экспериментально. Следовательно, невозможно измерить абсолютные значения потенциала какого-либо одного электрода полуячейки. Чтобы решить эту проблему, Нернст предположил, что потенциал водородного электрода при давлении водорода 1 атм и при единичной концентрации иона водорода должен служить произвольным нулевым потенциалом. В таблице 2.2 все перечисленные потенциалы относятся к водородной шкале, в которой потенциал полуячейки водородного электрода eH + | h3o находится в стандартном состоянии и был произвольно взят за нулевую точку отсчета в ряду электродвижущей силы.Свободная энергия Гиббса для реакции выделения водорода не равна нулю.
(2.9b) 2H ++ 2e- → h3
Нулевое значение водородного электрода сравнения было принято IUPAC, как было предложено Нернстом для удобства, чтобы стандартный водородный электрод (SHE) служил в качестве образца сравнения. потенциал. Используя эту шкалу, можно определить потенциал электрода при всех температурах. Однако произвольный ноль будет другим при разных температурах [12–14].
Потенциал полуэлемента любой окислительно-восстановительной коррозии измеряется, когда полуэлемент соединен с SHE.Пример измерения потенциала полуячейки приведен для электрода Sn | Sn 2 + на рис. 2.2. Металлическое олово погружают в 1M стандартный раствор Sn 2 + в соляной кислоте и отделяют через мембрану от электрода сравнения H 2 | H + . Это соединение образует гальванический элемент, который, согласно соглашению IUPAC, записывается как:
Рис. 2.2. Схема электрохимической ячейки, показывающая измерение потенциала ячейки.
(2.46) Pt, h3 | HCl || Sn2 + | Sn
(2.47) Sn + 2H + → Sn2 ++ h3
И Sn, и Sn 2 + в реакции коррозии находятся в стандартном состоянии. Потенциал, измеренный для электрода Sn | Sn 2 + , составляет 0,138 В с отрицательным значением Sn | Sn 2 + относительно водородного электрода сравнения. Поскольку потенциал SHE равен нулю, стандартный потенциал окислительно-восстановительной системы Sn 2 + | Sn равен e o = -0,138 В, как показано в таблице 2.2. Электроды показаны в таблице 2.2 с большим отрицательным e o по сравнению со стандартным водородным электродом сильно восстанавливаются. Они подвергаются окислению и переносят электроны в реакцию другой полуячейки, где процесс восстановления происходит на границе раздела. Такие электроды, как Au | Au 3 + или Pt | Pt 2 + , положительны по отношению к SHE. Они сильно окисляют и захватывают электроны из другой полуячейки.
В спонтанной реакции между двумя полуячейками полуячейка с более положительным потенциалом в таблице 2.2 подвергается восстановлению, а более отрицательный – окислению. Перенос заряда изменяет стандартный электродный потенциал из-за изменения состава электроактивных частиц в электролите. Когда окончательное соотношение активностей реактивных частиц, как определено в формуле. (2.38), равна константе равновесия реакции, система будет находиться в равновесии.
17.4 Уравнение Нернста – Химия
Цели обучения
К концу этого раздела вы сможете:
- Связать потенциалы клеток с изменениями свободной энергии
- Используйте уравнение Нернста для определения потенциалов ячеек в нестандартных условиях
- Выполнение расчетов, включающих преобразование потенциалов ячеек, изменений свободной энергии и констант равновесия
Теперь мы расширим электрохимию, определив взаимосвязь между [латексом] E _ {\ text {cell}} ^ {\ circ} [/ latex] и термодинамическими величинами, такими как Δ G ° (свободная энергия Гиббса) и К. (константа равновесия).{-}) \; \ times \; F = nF [/ латекс]
В этом уравнении n – количество молей электронов для сбалансированной реакции окисления-восстановления . Измеренный потенциал ячейки – это максимальный потенциал, который может создать ячейка, и он связан с электрической работой ( w ele ) на
.[латекс] E_ \ text {cell} = \ frac {-w _ {\ text {ele}}} {nF} \; \; \; \; \; \; \; \ text {или} \; \; \; \; \; \; \; w _ {\ text {ele}} = -nFE _ {\ text {cell}} [/ latex]
Отрицательный знак для работы указывает, что электрические работы выполняются системой (гальваническим элементом) в окружающей среде.В предыдущей главе свободная энергия определялась как энергия, доступная для выполнения работы. В частности, изменение свободной энергии было определено в терминах максимальной работы ( w max ), которая для электрохимических систем составляет w ele . {\ circ} = \ frac {0.{\ circ} [/ latex] известен или может быть вычислен, два других количества могут быть легко определены. Отношения показаны графически на Рисунке 1.
Рис. 1. Соотношения между Δ G ° , K и E ° ячейка . Учитывая любую из трех величин, две другие можно вычислить, поэтому любую из величин можно использовать для определения, был ли процесс самопроизвольным.Если задано одно из значений, можно вычислить два других.{\ circ} = -2 \; \ times \; 96 485 \; \ frac {\ text {J}} {\ text {V} {\ cdot} \ text {mol}} \; \ times \; 1.247 \; \ text {V} = -240,6 \; \ frac {\ text {kJ}} {\ text {mol}} [/ latex]
Проверьте свой ответ: Положительный стандартный потенциал клетки означает спонтанную реакцию, поэтому стандартное изменение свободной энергии должно быть отрицательным, а константа равновесия должна быть> 1.
Проверьте свои знания
Что такое стандартное изменение свободной энергии и константа равновесия для следующей реакции при комнатной температуре? Реакция спонтанная?
[латекс] \ text {Sn} (s) \; + \; 2 \ text {Cu} ^ {2 +} (aq) \; {\ leftrightharpoons} \; \ text {Sn} ^ {2 +} ( aq) \; + \; 2 \ text {Cu} ^ {+} (aq) [/ latex]
Ответ:
Спонтанный; n = 2; [латекс] E _ {\ text {cell}} ^ {\ circ} = +0. {2 +} (aq \ text {, \;} 1.{2 +} (aq \ text {, \;} 0,15 \; M) \; + \; \ text {Fe} (s) [/ latex]
Процесс самопроизвольный?
Решение
Есть два способа решить проблему. Если бы термодинамическая информация в Приложении G была доступна, вы могли бы рассчитать изменение свободной энергии. Если изменение свободной энергии отрицательное, процесс происходит самопроизвольно. Другой подход, который мы будем использовать, требует информации, подобной той, что дана в Приложении L. Используя эти данные, можно определить потенциал клетки. Если потенциал клетки положительный, процесс происходит самопроизвольно.{\ circ} \; – \; \ frac {0.0592 \; \ text {V}} {n} \; \ text {log} \; Q [/ latex]
[латекс] E _ {\ text {cell}} = -0,17 \; \ text {V} \; – \; \ frac {0.0592 \; \ text {V}} {2} \; \ text {log} \ ; 0,077 [/ латекс]
[латекс] E _ {\ text {cell}} = -0,17 \; \ text {V} \; + \; 0,033 \; \ text {V} = -0,014 \; \ text {V} [/ latex]
Процесс (все еще) не спонтанный. {3 +} (aq \ text {, \;} 0.{2 +} (aq \ text {, \;} 0,025 \; M) {\ mid} \ text {Cu} (s) [/ latex]
Каковы значения n и Q для общей реакции? Является ли реакция в этих условиях спонтанной?
Ответ:
n = 6; Q = 1440; E ячейка = +1,97 В, самопроизвольно.
Наконец, мы кратко рассмотрим особый тип ячейки, называемый ячейкой концентрации . В концентрационной ячейке электроды сделаны из одного и того же материала, а полуячейки различаются только концентрацией.{\ circ} = 0.000 \; \ text {V} \ end {array} [/ latex]
Стандартный потенциал ячейки равен нулю, потому что анод и катод участвуют в одной и той же реакции; изменяется только концентрация Zn 2+ . Подставляя в уравнение Нернста,
[латекс] E _ {\ text {cell}} = 0,000 \; \ text {V} \; – \; \ frac {0.0592 \; \ text {V}} {2} \; \ text {log} \; \ frac {0.10} {0.50} = +0.021 \; \ text {V} [/ latex]
и в этих условиях процесс происходит самопроизвольно.
Проверьте свой ответ: В ячейке для концентрации стандартный потенциал ячейки всегда будет равен нулю.Чтобы получить положительный потенциал клетки (самопроизвольный процесс), коэффициент реакции Q должен быть <1. Q <1 в данном случае, значит, процесс спонтанный.
Проверьте свои знания
Какое значение Q для предыдущей ячейки концентрации даст напряжение 0,10 В? Если концентрация иона цинка на катоде составляла 0,50 M , какова была концентрация на аноде?
Ответ:
Q = 0.00042; [Zn 2+ ] cat = 2,1 × 10 -4 M .
Электротехническая работа ( w ele ) – это отрицательная величина произведения полного заряда ( Q ) на потенциал ячейки ( E cell ). Общий заряд может быть рассчитан как количество молей электронов ( n ), умноженное на постоянную Фарадея ( F = 96 485 Кл / моль e –). Электрическая работа – это максимальная работа, которую может произвести система, и поэтому она равна изменению свободной энергии.{\ circ} [/ латекс]
Химия: упражнения в конце главы
- Для приведенных здесь стандартных потенциалов ячейки определите Δ G ° для ячейки в кДж.
(а) 0,000 В, n = 2
(б) +0,434 В, n = 2
(в) −2,439 В, n = 1
- Для приведенных здесь значений Δ G ° определите стандартный потенциал ячейки для ячейки.
(а) 12 кДж / моль, n = 3
(б) -45 кДж / моль, n = 1
- Определите стандартный потенциал ячейки и потенциал ячейки в указанных условиях для электрохимических реакций, описанных здесь.{+} (aq \ text {, \;} 0,25 \; M) \; {\ longrightarrow} \; 2 \ text {Ag} (s) \; + \; \ text {HgS} (s) [/ latex ]
(b) Гальванический элемент, состоящий из полуэлемента, состоящего из алюминиевого электрода в 0,015 M растворе нитрата алюминия и полуэлемента, состоящего из никелевого электрода в 0,25 M растворе нитрата никеля (II). {\ circ} \; \ text {C} [/ latex]
Глоссарий
- ячейка концентрации
- гальванический элемент, в котором два полуэлемента одинаковы, за исключением концентрации растворенных веществ; самопроизвольно, когда общей реакцией является разбавление растворенного вещества
- электромонтажные работы ( w ele )
- отрицательных значений общего заряда, умноженного на потенциал ячейки; равно w max для системы, и, таким образом, равно изменению свободной энергии (Δ G )
- Постоянная Фарадея (F)
- заряд на 1 моль электронов; F = 96,485 Кл / моль –
- Уравнение Нернста
- уравнение, связывающее логарифм коэффициента реакции ( Q ) с нестандартными потенциалами ячейки; может использоваться, чтобы связать константы равновесия со стандартными потенциалами ячейки
Решения
Ответы на упражнения в конце главы по химии
1.(а) 0 кДж / моль; (b) -83,7 кДж / моль; (в) +235,3 кДж / моль
3. (а) стандартный потенциал ячейки: 1,50 В, спонтанный; потенциал клетки при указанных условиях: 1,43 В, спонтанный; (б) стандартный потенциал клетки: 1,405 В, спонтанный; потенциал клетки в указанных условиях: 1,423 В, спонтанный; (c) стандартный потенциал ячейки: -2,749 В, неспонтанный; потенциал ячейки при указанных условиях: -2,757 В, несамопроизвольный
5. (а) 1,7 × 10 −10 ; (б) 2,6 × 10 −21 ; (в) 8.9 × 10 19 ; (г) 1.0 × 10 −14
.