Молекулярная физика и термодинамика – Формулы, теоремы, определения
Нет нужного материала?
Укажите материал, который Вы не нашли, и он будет добавлен в самое ближайшее время!
Название*:
Раздел науки:
———Математика > АрифметикаМатематика > Арифметика > Арифметические действияМатематика > Арифметика > Рациональные числаФизика > Атомная и ядерная физикаМатематика > Квадратные уравненияФизика > Колебания и волныФизика > Колебания и волны > Механические волныФизика > Колебания и волны > Механические колебанияФизика > Колебания и волны > Электромагнитные волныМатематика > ЛогарифмыФизика > МеханикаФизика > Механика > ДинамикаФизика > Механика > Импульс, энергияФизика > Механика > КинематикаФизика > Механика > Механика жидкостиФизика > Молекулярная физика и термодинамикаФизика > ОптикаГеометрия > ПланиметрияМатематика > ПределыМатематика > ПрогрессииМатематика > Прогрессии > Арифметическая прогрессияМатематика > Прогрессии > Геометрическая прогрессияМатематика > Производная функцииФизика > Специальная теория относительностиГеометрия > СтереометрияМатематика > Теория группМатематика > Теория чиселМатематика > ТригонометрияМатематика > Формулы сокращенного умноженияФизика > ЭлектричествоФизика > Электричество > МагнетизмФизика > Электричество > Переменный электрический токФизика > Электричество > Постоянный электрический токФизика > Электричество > Электрическое полеФизика > Электричество > Электронные и ионные явленияМатематика > Элементарная математика
Данное поле ОБЯЗАТЕЛЬНО к заполнению, чтобы убедиться, что Вы человек
06-з.
 Первый закон термодинамики
Первый закон термодинамики§ 06-з. Первый закон термодинамики
Мы знаем, что внутреннюю энергию тел можно менять теплообменом – передавая или забирая некоторое количество теплоты (см. § 6-в). Но опыты Румфорда и Джоуля продемонстрировали, что внутреннюю энергию тел можно менять совершением работы (см. § 6-ж). То есть существуют два различных равноправных способа изменения внутренней энергии тел: теплопередача и работа (см. формулу).
Математическая запись первого закона термодинамики. Формулаа читается так: «дэльта у равно ку плюс а».
| ΔU = Q + A | ΔU – изменение внутренней энергии тела, Дж |
Эта формула гласит, что изменение внутренней энергии тела есть величина, равная сумме количества теплоты, полученной этим телом, и совершённой над ним работы. Это утверждение, отражающее закон сохранения и превращения энергии, называется первым законом термодинамики
Это утверждение, отражающее закон сохранения и превращения энергии, называется первым законом термодинамики
Опыт «воздушное огниво». Возьмём толстостенный стеклянный цилиндр с поршнем. На дно цилиндра насыпем немного «серы» от спичек. Резко ударив по рукоятке, мы совершим механическую работу над воздухом: сожмём его. В результате воздух нагреется настолько сильно, что серный порошок в нём воспламенится без поджигания!
Объясним опыт. Удар длился недолго, поэтому передачей теплоты из цилиндра наружу можно пренебречь. Извне теплота также не поступала. Следовательно, теплообмен отсутствовал, то есть Q = 0. Тогда формула первого закона термодинамики применительно к этому опыту запишется так:
Последнюю формулу лучше писать наоборот: A = ΔU, что читается так: совершённая над телом работа идёт на изменение его внутренней энергии (если теплообмен отсутствует). То есть работа, совершённая над воздухом, привела к росту его внутренней энергии, и он нагрелся.
То есть работа, совершённая над воздухом, привела к росту его внутренней энергии, и он нагрелся.
Опыт «туман в бутыли». Для него нам потребуются бутыль, пробка, шланг и насос (см. рисунок). Прежде чем вставить пробку, в бутыль наливают немного воды и несколько раз встряхивают, чтобы воздух внутри стал влажным. Удерживая пробку рукой, накачивают воздух. Когда нам становится трудно удерживать пробку, накачивание прекращают и ожидают 5–10 минут, чтобы воздух в бутыли охладился до комнатной температуры (так как при совершении над ним работы он нагрелся). При отпускании пробки она вылетает, и в бутыли образуется туман!
Разделим объяснение результатов этого опыта на три этапа.
1-й этап. Накачивая воздух, мы совершаем над ним работу. По аналогии с опытом «воздушное огниво», запишем первый закон термодинамики так: ΔU = 0 + A. Поскольку А – положительная величина, значит, и ΔU положительна. То есть внутренняя энергия воздуха изменяется в большую сторону – возрастает.
2-й этап. Давая воздуху охладиться, работу не совершали:
3-й этап. Пробку отпускают, и она выталкивается струёй воздуха. Всё происходит быстро, поэтому теплообмен не успевает произойти: Q = 0. Кроме того, работа совершается не над воздухом, а им самим, следовательно, первый закон термодинамики запишется: ΔU = –A. Поскольку величина –A является отрицательной, то и величина
Чтобы произвести расчеты, необходимо разрешить элементы ActiveX!
Источник
Больше интересного в телеграм @calcsboxосновные понятия, формулы, законы.
 Основные законы физики, которые должен знать человек. Основные формулы молекулярной физики и термодинамики
Основные законы физики, которые должен знать человек. Основные формулы молекулярной физики и термодинамикиРазмер: px
Начинать показ со страницы:
Транскрипт1 ОСНОВНЫЕ ФОРМУЛЫ ПО ФИЗИКЕ ДЛЯ СТУДЕНТОВ ТЕХНИЧЕСКИХ ВУЗОВ.. Физические основы механики. Скорость мгновенная dr r- радиус-вектор материальной точки, t- время, Модуль мгновенной скорости s- расстояние вдоль траектории движения, Длина пути Ускорение: мгновенное тангенциальное нормальное полное τ- единичный вектор, касательный к траектории; R- радиус кривизны траектории, n- единичный вектор главной нормали. СКОРОСТЬ УГЛОВАЯ ds = S t t t d a d a a n n R a a a, n a a a n d φ- угловое перемещение. Ускорение угловое d.. Связь между линейными и.. угловыми величинами s= φr, υ= ωr, а τ = εr, a n = ω R.3. Импульс.4. материальной точки p масса материальной точки. Основное уравнение динамики материальной точки (второй закон Ньютона)
2
a dp Fi, Fi Закон сохранения импульса для изолированной механической системы Радиус-вектор центра масс Сила сухого трения μ- коэффициент трения, N- сила нормального давления.
3 .4.4. Напряженность гравитационного.4.5. поля Земли g= G (R h) 3 масса Земли, R 3 – радиус Земли, h- расстояние от поверхности Земли. Потенциал гравитационного поля Земли 3 Кинетическая энергия материальной точки φ= G Т= (R 3 3 h) p Закон сохранения механической энергии для механической системы Е=Т+П=onst Момент инерции материальной точки J=r r- расстояние до оси вращения. Моменты инерции тел массой относительно оси, проходящей через центр масс: тонкостенного цилиндра (кольца) радиуса R, если ось вращения совпадает с осью цилиндра J о =R сплошного цилиндра (диска) радиуса R, если ось вращения совпадает с осью цилиндра J о = R шара радиуса R J о = 5 R тонкого стержня длиной l, если ось вращения перпендикулярна стержню J о = l Момент инерции тела массой относительно произвольной оси (теорема Штейнера) J=J +d
4
J – момент инерции относительно параллельной оси, проходящей через центр масс, d-расстояние между осями.
5
.4.3. Полная энергия релятивисткой.4.4. частицы.4.5. Е=.4.6. Релятивистский импульс Р=.4.7. Кинетическая энергия.4.8. релятивистской частицы.4.9. Т=Е- Е о = Релятивистское соотношение между полной энергией и импульсом Е =р с +Е о Закон сложения скоростей в релятивистской механике и и и – скорости в двух инерциальных системах отсчета, движущихся относительно друг друга со скоростью υ, совпадающей по направлению с и(знак -) или противоположно ей направленной (знак +) u u u Физика механических колебаний и волн. Смещение колеблющейся материальной s Aos(t) точки А- амплитуда колебания, – собственная циклическая частота, φ о – начальная фаза. Циклическая частота T
Смещение колеблющейся материальной s Aos(t) точки А- амплитуда колебания, – собственная циклическая частота, φ о – начальная фаза. Циклическая частота T
6 T период колебаний – частота Скорость колеблющейся материальной точки Ускорение колеблющейся материальной точки Кинетическая энергия материальной точки, совершающей гармонические v ds d s a колебания v T Потенциальная энергия материальной точки, совершающей гармонические колебания Ï kx коэффициент жесткости (коэффициент упругости) Полная энергия материальной точки, совершающей гармонические колебания A sin(t) dv E T Ï A os(t) A A A sin (t) os (t) d s Дифференциальное уравнение s свободных гармонических незатухающих колебаний величины s d s ds Дифференциальное уравнение s свободных затухающих колебаний величины s, – коэффициент затухания A(t) T Логарифмический декремент ln T A(T t) затухания, время релаксации d s ds Дифференциальное уравнение s F ost Период колебания маятников: пружинного T, k
7
физического T J, gl – масса маятника, k- жесткость пружины, J- момент инерции маятника, g- ускорение свободного падения, l- расстояние от точки подвеса до центра масс. Уравнение плоской волны, распространяющейся в направлении оси Ох, v скорость распространения волны Длина волны Т- период волны, v- скорость распространения волны, частота колебаний Волновое число Скорость распространения звука в газах γ – отношение теплоемкостей газа, при постоянном давлении и объеме, R- молярная газовая постоянная, Т- термодинамическая температура, М- молярная масса газа x (x, t) Aos[ (t) ] v v T v vt v RT Молекулярная физика и термодинамика..4.. Количество вещества N N A, N- число молекул, N А – постоянная Авогадро – масса вещества М молярная масса. Уравнение Клапейрона-Менделеева р = ν RT,
Уравнение плоской волны, распространяющейся в направлении оси Ох, v скорость распространения волны Длина волны Т- период волны, v- скорость распространения волны, частота колебаний Волновое число Скорость распространения звука в газах γ – отношение теплоемкостей газа, при постоянном давлении и объеме, R- молярная газовая постоянная, Т- термодинамическая температура, М- молярная масса газа x (x, t) Aos[ (t) ] v v T v vt v RT Молекулярная физика и термодинамика..4.. Количество вещества N N A, N- число молекул, N А – постоянная Авогадро – масса вещества М молярная масса. Уравнение Клапейрона-Менделеева р = ν RT,
8
р- давление газа, – его объем, R- молярная газовая постоянная, Т- термодинамическая температура. Уравнение молекулярно-кинетической теории газов Р= 3 n = 3 nо n- концентрация молекул, – средняя кинетическая энергия поступательного движения молекулы. о – масса молекулы – средняя квадратичная скорость. Средняя энергия молекулы = i kt i – число степеней свободы k- постоянная Больцмана. Внутренняя энергия идеального газа U= i νrt Cкорости молекул: средняя квадратичная = 3kT = 3RT ; средняя арифметическая = 8 8RT = kt ; наиболее вероятная = Средняя длина свободного kt = RT ; пробега молекулы d-эффективный диаметр молекулы Среднее число столкновений (d n) молекулы в единицу времени z d n v
Внутренняя энергия идеального газа U= i νrt Cкорости молекул: средняя квадратичная = 3kT = 3RT ; средняя арифметическая = 8 8RT = kt ; наиболее вероятная = Средняя длина свободного kt = RT ; пробега молекулы d-эффективный диаметр молекулы Среднее число столкновений (d n) молекулы в единицу времени z d n v
9 Распределение молекул в потенциальном поле сил П-потенциальная энергия молекулы. Барометрическая формула p – давление газа на высоте h, p – давление газа на уровне, принятому за нулевой, – масса молекулы, Закон диффузии Фика j -плотность потока массы, n n exp kt gh p p exp kt j d ds d =-D dx d -градиент плотности, dx D- коэффициент диффузии, ρ-плотность, d -масса газа, ds- элементарная площадка, перпендикулярная оси Оx. Закон теплопроводности Фурье j – плотность теплового потока, Q j Q dq ds dt =-æ dx dt -градиент температуры, dx æ- коэффициент теплопроводности, Сила внутреннего трения η- коэффициент динамической вязкости, dv df ds dz d – градиент скорости, dz Коэффициент диффузии D= 3 Коэффициент динамической вязкости (внутреннего трения) v 3 D Коэффициент теплопроводности æ = 3 сv ρ=ηс v
10
с v удельная изохорная теплоемкость, Молярная теплоемкость идеального газа изохорная изобарная Первое начало термодинамики i C v R i C p R dq=du+da, da=pd, du=ν C v dt Работа расширения газа при процессе изобарном А=р(-)= ν R(T -T) изотермическом p А= ν RТ ln = ν RТ ln p адиабатном A C T T) γ=с р /С v (RT A () p A= () Уравнения Пуассона Коэффициент полезного действия цикла Карно. 4.. Q н и T н – количество теплоты полученное от нагревателя и его температура; Q х и T х – количество теплоты переданное холодильнику и его температура. Изменение энтропии при переходе системы из состояния в состояние Р γ =onst Т γ- =onst Т γ р – γ =onst Qí Q Q S S í õ Tí T T dq T í õ
4.. Q н и T н – количество теплоты полученное от нагревателя и его температура; Q х и T х – количество теплоты переданное холодильнику и его температура. Изменение энтропии при переходе системы из состояния в состояние Р γ =onst Т γ- =onst Т γ р – γ =onst Qí Q Q S S í õ Tí T T dq T í õ
Примеры решения задач Пример 6 Один конец тонкого однородного стержня длиной жестко закреплен на поверхности однородного шара так, что центры масс стержня и шара, а также точка крепления находятся на одной
Сокращения: Опр определение Ф-ка формулировка Ф-ла – формула Пр – пример 1. Кинематика точки 1) Физические модели: материальная точка, система материальных точек, абсолютно твердое тело (Опр) 2) Способы
1 О с н о в н ы е ф о р м у л ы Кинематика 1 Кинематическое уравнение движения материальной точки в векторной форме r r (t), вдоль оси х: x = f(t), где f(t) некоторая функция времени Перемещение материальной
КОЛЛОКВИУМ 1 (механика и СТО) Основные вопросы 1. Система отсчета. Радиус вектор. Траектория. Путь. 2. Вектор смещения. Вектор линейной скорости. 3. Вектор ускорения. Тангенциальное и нормальное ускорение.
Система отсчета. Радиус вектор. Траектория. Путь. 2. Вектор смещения. Вектор линейной скорости. 3. Вектор ускорения. Тангенциальное и нормальное ускорение.
Задача 5 Идеальная тепловая машина работает по циклу Карно При этом N% количества теплоты, получаемой от нагревателя, передаётся холодильнику Машина получает от нагревателя при температуре t количество
Физические основы механики Пояснение к рабочей программе Физика наряду с другими естественными науками изучает объективные свойства окружающего нас материального мира Физика исследует наиболее общие формы
Министерство образования Республики Беларусь Учреждение образования «Гомельский государственный технический университет имени П. О. Сухого» Кафедра «Физика» П. А. Хило, Е. С. Петрова ФИЗИКА ПРАКТИКУМ по
2 1. Цели освоения дисциплины Целью освоения дисциплины «Физика» является формирование у студентов навыка проведения измерений, изучение различных процессов и оценка результатов экспериментов. 2. Место
2. Место
Закон сохранения импульса Закон сохранения импульса Замкнутая (или изолированная) система – механическая система тел, на которую не действуют внешние силы. d v ” ” d d v d… ” v ” v v “… ” v… v v
Министерство образования и науки, молодежи и спорта Украины Государственное высшее учебное заведение «Национальный горный университет» Методические указания к лабораторной работе 1.0 СПРАВОЧНЫЙ МАТЕРИАЛ
Вопросы к лабораторным работам по разделу физики Механика и молекулярная физика Изучение погрешности измерения (лабораторная работа 1) 1. Физические измерения. Прямые и косвенные измерения. 2. Абсолютные
Экзаменационные вопросы по физике для групп 1АМ, 1ТВ, 1 СМ, 1ДМ 1-2 1. Определение процесса измерения. Прямые и косвенные измерения. Определение погрешностей измерения. Запись окончательного результата
Восточно-Сибирский государственный университет технологий и управления Лекция 3 Динамика вращательного движения ВСГУТУ, кафедра «Физика» План Момент импульса частицы Момент силы Уравнение моментов Момент
Сафронов В. П. 1 ОСНОВЫ МОЛЕКУЛЯРНО КИНЕТИЧЕСКОЙ ТЕОРИИ – 1 – ЧАСТЬ МОЛЕКУЛЯРНАЯ ФИЗИКА И ОСНОВЫ ТЕРМОДИНАМИКИ Глава 8 ОСНОВЫ МОЛЕКУЛЯРНО КИНЕТИЧЕСКОЙ ТЕОРИИ 8.1. Основные понятия и определения Опытное
П. 1 ОСНОВЫ МОЛЕКУЛЯРНО КИНЕТИЧЕСКОЙ ТЕОРИИ – 1 – ЧАСТЬ МОЛЕКУЛЯРНАЯ ФИЗИКА И ОСНОВЫ ТЕРМОДИНАМИКИ Глава 8 ОСНОВЫ МОЛЕКУЛЯРНО КИНЕТИЧЕСКОЙ ТЕОРИИ 8.1. Основные понятия и определения Опытное
ЯВЛЕНИЯ ПЕРЕНОСА В ГАЗАХ Средняя длина свободного пробега молекулы n, где d эффективное сечение молекулы, d эффективный диаметр молекулы, n концентрация молекул Среднее число соударений, испытываемое молекулой
1 Складываются два гармонических колебания одного направления с одинаковыми частотами x (t) A cos(t) x (t) A cos(t) 1 1 1 Построить векторную диаграмму сложения колебаний найти амплитуду и начальную
8 6 баллов удовлетворительно 7 балл хорошо Задание (балла) На горизонтальной доске лежит брусок массы. Доску медленно наклоняют. Определить зависимость силы трения, действующей на брусок, от угла наклона
5. Динамика вращательного движения твердого тела Твердое тело это система материальных точек, расстояния между которыми не меняются в процессе движения.
Тема: «Динамика материальной точки» 1. Тело можно считать материальной точкой если: а) его размерами в данной задаче можно пренебречь б) оно движется равномерно ось вращения является неподвижной угловое
СПбГЭТУ ЛЭТИ Конспект по физике за 1 семестр Лектор: Ходьков Дмитрий Афанасьевич Работу выполнили: студент группы 7372 Чеканов Александр студент группы 7372 Когогин Виталий 2018 г КИНЕМАТИКА (МАТЕРИАЛЬНОЙ
Динамика вращательного движения План Момент импульса частицы Момент силы Уравнение моментов Собственный момент импульса Момент инерции Кинетическая энергия вращающегося тела Связь динамики поступательного
ОГЛАВЛЕНИЕ Предисловие 9 Введение 10 ЧАСТЬ 1. ФИЗИЧЕСКИЕ ОСНОВЫ МЕХАНИКИ 15 Глава 1. Основы математического анализа 16 1.1. Система координат. Операции над векторными величинами… 16 1.2. Производная
Программа вступительных испытаний по учебному предмету «Физика» для лиц, имеющих общее среднее образование, для получения высшего образования І ступени, 2018 год 1 УТВЕРЖДЕНО Приказ Министра образования
1 Кинематика 1 Материальная точка движется вдоль оси x так, что времени координата точки x(0) B Найдите x (t) V x At В начальный момент Материальная точка движется вдоль оси x так, что ax A x В начальный
Тихомиров Ю.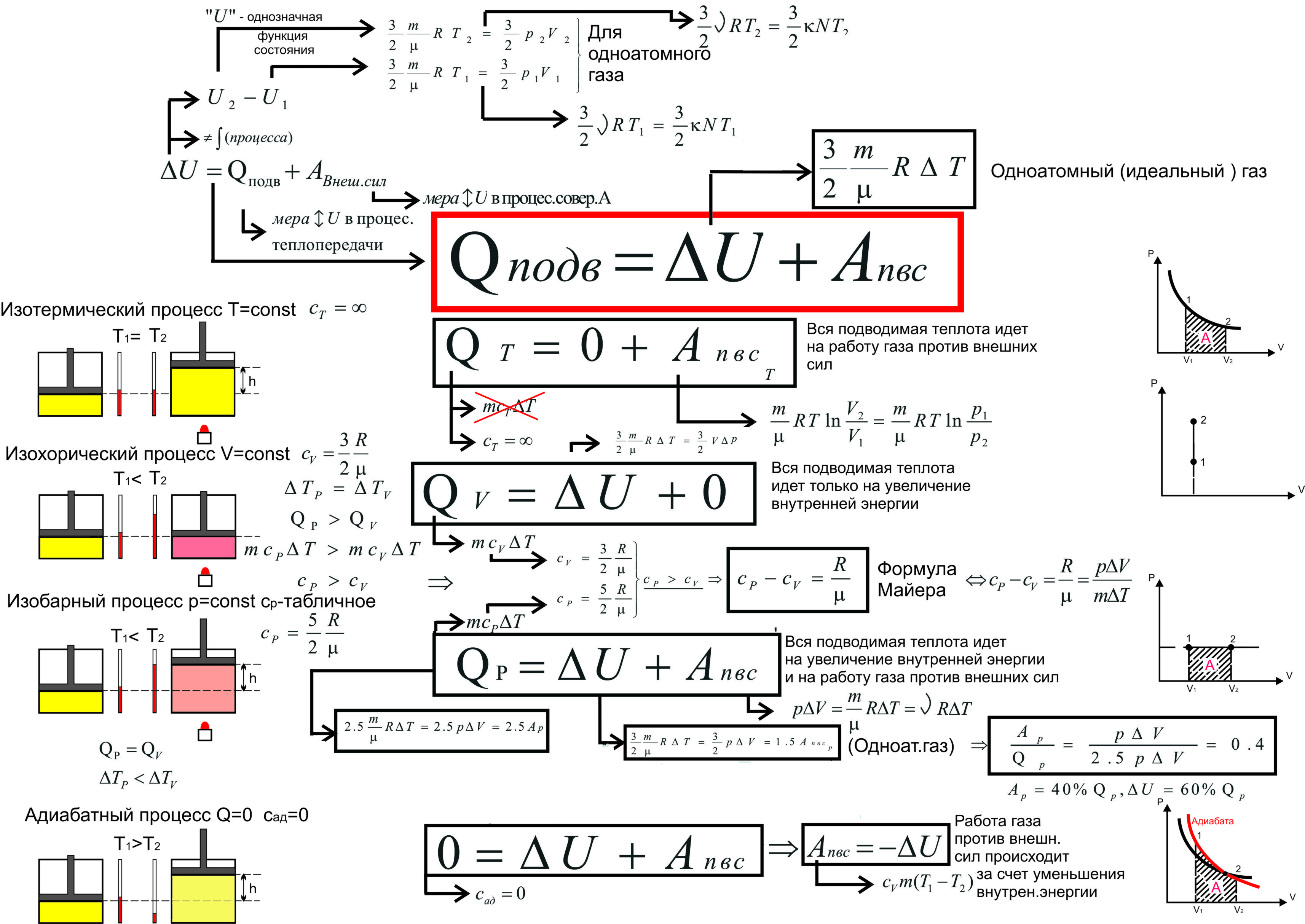 В. СБОРНИК контрольных вопросов и заданий с ответами для виртуального физпрактикума Часть 1. Механика 1_1. ДВИЖЕНИЕ С ПОСТОЯННЫМ УСКОРЕНИЕМ… 2 1_2. ДВИЖЕНИЕ ПОД ДЕЙСТВИЕМ ПОСТОЯННОЙ СИЛЫ…7
В. СБОРНИК контрольных вопросов и заданий с ответами для виртуального физпрактикума Часть 1. Механика 1_1. ДВИЖЕНИЕ С ПОСТОЯННЫМ УСКОРЕНИЕМ… 2 1_2. ДВИЖЕНИЕ ПОД ДЕЙСТВИЕМ ПОСТОЯННОЙ СИЛЫ…7
2 6. Количество заданий в одном варианте теста 30. Часть А 18 заданий. Часть В 12 заданий. 7. Структура теста Раздел 1. Механика 11 заданий (36,7 %). Раздел 2. Основы молекулярно-кинетической теории и
Список формул по механике, необходимых для получения оценки удолетворительно Все формулы и текст должны быть выучены наизусть! Всюду ниже точка над буквой обозначает производную по времени! 1. Импульс
ПРОГРАММА ВСТУПИТЕЛЬНЫХ ИСПЫТАНИЙ (БАКАЛАВРИАТ/СПЕЦИАЛИТЕТ) ПО ОБЩЕОБРАЗОВАТЕЛЬНОЙ ДИСЦИПЛИНЕ «ФИЗИКА» Программа составлена на основе Федерального государственного образовательного стандарта среднего общего
Экзаменационные билеты по разделу «Механика» общего курса физики (2018 г.). 1-й курс: 1-й, 2-й, 3-й потоки. Билет 1 Лекторы: доц.а.а.якута, проф. А.И.Слепков, проф. О.Г.Косарева 1. Предмет механики. Пространство
А.И.Слепков, проф. О.Г.Косарева 1. Предмет механики. Пространство
Задание 8 Физика для заочников Контрольная работа 1 Диск радиусом R = 0, м вращается согласно уравнению φ = А + Вt + Сt 3, где А = 3 рад; В = 1 рад/с; C = 0,1 рад/с 3 Определите тангенциальное а τ, нормальное
Лекция 9 Средняя длина свободного пробега. Явления переноса. Теплопроводность, диффузия, вязкость. Средняя длина свободного пробега Средняя длина свободного пробега это среднее расстояние, которое молекула
Лекция 5 ДИНАМИКА ВРАЩАТЕЛЬНОГО ДВИЖЕНИЯ Термины и понятия Метод интегрального исчисления Момент импульса Момент инерции тела Момент силы Плечо силы Реакция опоры Теорема Штейнера 5.1. МОМЕНТ ИНЕРЦИИ ТВЕРДОГО
СТОЛКНОВЕНИЕ ЧАСТИЦ Ударом МТ (частиц, тел) будем называть такое механическое взаимодействие, при котором при непосредственном контакте за бесконечно малое время частицы обмениваются энергией и импульсом
Билет 1. 1. Предмет механики. Пространство и время в механике Ньютона. Тело отсчета и система координат. Часы. Синхронизация часов. Система отсчета. Способы описания движения. Кинематика точки. Преобразования
Студентыфизики Лектор Алешкевич В. А. Январь 2013 Неизвестный Студент физфака Билет 1 1. Предмет механики. Пространство и время в механике Ньютона. Система координат и тело отсчета. Часы. Система отсчета.
УТВЕРЖДЕНО Приказ Министра образования Республики Беларусь от 30.10.2015 817 Программы вступительных испытаний в учреждения образования для лиц, имеющих общее среднее образование, для получения высшего
СТАТИСТИЧЕСКАЯ ФИЗИКА ТЕРМОДИНАМИКА Распределение Максвелла Начала термодинамики Цикл Карно Распределение Максвелла В газе, находящемся в состоянии равновесия, устанавливается некоторое стационарное, не
6 Молекулярная физика и термодинамика Основные формулы и определения Скорость каждой молекулы идеального газа представляет собой случайную величину. Функция плотности распределения вероятности случайной
Варианты домашнего задания ГАРМОНИЧЕСКИЕ КОЛЕБАНИЯ И ВОЛНЫ Вариант 1. 1. На рисунке а приведен график колебательного движения. Уравнение колебаний x = Asin(ωt + α o). Определить начальную фазу. x О t
1. На рисунке а приведен график колебательного движения. Уравнение колебаний x = Asin(ωt + α o). Определить начальную фазу. x О t
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Национальный минерально-сырьевой университет
Волгоградский государственный университет Кафедра Судебной экспертизы и физического материаловедения УТВЕРЖДЕНО УЧЕНЫМ СОВЕТОМ Протокол 1 от «08» февраля 2013 г. Директор физико-технического института
Лекция 3 Кинематика и динамика вращательного движения Вращательное движение движение, при котором все точки тела движутся по окружностям, центры которых лежат на одной и той же прямой. Кинематика вращательного
Вопросы к экзамену по физике МЕХАНИКА Поступательное движение 1. Кинематика поступательного движения. Материальная точка, система материальных точек. Системы отсчета. Векторный и координатный способы описания
ЛЕКЦИЯ 6 7 октября 011 года Тема 3: Динамика вращения твердого тела. Кинетическая энергия вращательного движения твердого тела Колесников Ю.Л., 011 1 Вектор момента силы относительно неподвижной точки.
Кинетическая энергия вращательного движения твердого тела Колесников Ю.Л., 011 1 Вектор момента силы относительно неподвижной точки.
Номера задач КОНТРОЛЬНАЯ РАБОТА по молекулярной физике Варианты 3 4 5 6 7 8 9 0 Таблица 8. 8. 8.3 8.4 8.5 8.6 8.7 8.8 8.9 8.0 8. 8. 8.3 8.4 8.5 8.6 8.7 8.8 8.9 8.0 8. 8. 8.3 8.4 8.5 8.6 8.7 8.8 8.9 8.30
I. МЕХАНИКА 1. Общие понятия 1 Механическое движение изменение положения тела в пространстве и во времени относительно других тел (движется тело или находится в состоянии покоя невозможно определить до
Кафедра физики, Пестряев Е.М.: ГТЗ МТЗ СТЗ 06 1 Контрольная работа 1 Механика 1. Велосипедист проехал первую половину времени своего движения со скоростью V 1 = 16 км/ч, вторую половину времени со скоростью
КОНТРОЛЬНАЯ РАБОТА 2 Таблица вариантов задач Вариант Номера задач 1 2 3 4 5 6 7 8 9 10 209 214 224 232 244 260 264 275 204 220 227 238 243 254 261 278 207 217 221 236 249 251 268 278 202 218 225 235 246
Задача Шарик с высоты hм вертикально падает на наклонную плоскость и упруго отражается. На каком расстоянии от места падения он снова ударится о ту же плоскость? Угол наклона плоскости к горизонту α3.
На каком расстоянии от места падения он снова ударится о ту же плоскость? Угол наклона плоскости к горизонту α3.
СПЕЦИФИКАЦИЯ теста по учебному предмету «Физика» для проведения централизованного тестирования в 2017 году 1. Назначение теста объективное оценивание уровня подготовки лиц, имеющих общее среднее образование
Законы идеального газа Молекулярно-кинетическая теория Статическая физика и термодинамика Статическая физика и термодинамика Макроскопические тела – это тела, состоящие из большого количества молекул Методы
Примерные задачи на компьютерном интернет-тестировании (ФЕПО) Кинематика 1) Радиус-вектор частицы изменяется во времени по закону В момент времени t = 1 с частица оказалась в некоторой точке А. Выберите
ДИНАМИКА АБСОЛЮТНО ТВЕРДОГО ТЕЛА Динамика вращательного движения АТТ Момент силы и момент импульса относительно неподвижной точки Момент силы и момент импульса относительно неподвижной точки B C B O Свойства:
1. Целью изучения дисциплины является: формирование естественнонаучного мировоззрения, развитие логического мышления, интеллектуальных и творческих способностей, развитие умения применять знание законов
Целью изучения дисциплины является: формирование естественнонаучного мировоззрения, развитие логического мышления, интеллектуальных и творческих способностей, развитие умения применять знание законов
Федеральное агентство по образованию ГОУ ВПО Тульский государственный университет Кафедра физики Семин В.А. Тестовые задания по механике и молекулярной физике для проведения практических занятий и контрольных
Билет 1 Поскольку направление скорости постоянно изменяется, то криволинейное движение – всегда движение с ускорением, в том числе, когда модуль скорости остается неизменным В общем случае ускорение направлено
Рабочая программа по физике 10 класс (2 часа) 2013-2014 учебный год Пояснительная записка Рабочая общеобразовательная программа «Физика.10 класс. Базовый уровень» составлена на основе Примерной программы
А Р, Дж 00 0 0 03 04 05 06 07 08 09 Т, К 480 485 490 495 500 505 50 55 50 55 Т, К 60 65 70 75 80 85 90 95 300 305 5. Газ совершает цикл Карно. Абсолютная температура нагревателя в n раз выше, чем температура
Абсолютная температура нагревателя в n раз выше, чем температура
СПЕЦИФИКАЦИЯ теста по учебному предмету «Физика» для проведения централизованного тестирования в 2018 году 1. Назначение теста объективное оценивание уровня подготовки лиц, имеющих общее среднее образование
МИНОБРНАУКИ РОССИИ Федеральное государственное автономное образовательное учреждение высшего образования «Национальный исследовательский университет «Московский институт электронной техники» РАБОЧАЯ ПРОГРАММА
СОДЕРЖАНИЕ ПРВДИСЛОВИЕ 3 ПРИНЯтаЕ ОБОЗНАЧЕНИЯ 5 Обозначения и названия основных единиц физических величин 6 ВВДЦЕНИЕ 7 РАЗДЕЛ 1. ФИЗИЧЕСКИЕ ОСНОВЫ МЕХАНИКИ 9 Тема 1. Физика как фувдаментальная наука 9
ТИПОВЫЕ ВОПРОСЫ К ТЕСТУ (ч.) Уравнения Максвелла 1. Полная система уравнений Максвелла для электромагнитного поля имеет вид: Укажите следствием каких уравнений являются следующие утверждения: в природе
Билет 1 Билет 2 Билет 3 Билет 4 Билет 5 Билет 6 Билет 7 Билет 8 Билет 9 Билет 10 Билет 11 Билет 12 Билет 13 Билет 14 Билет 15 Билет 16 Билет 17 Билет 18 Билет 19 Билет 20 Билет 21 Билет 22 Билет 23 Билет
Лекция 11 Момент импульса Закон сохранения момента импульса твердого тела, примеры его проявления Вычисление моментов инерции тел Теорема Штейнера Кинетическая энергия вращающегося твердого тела Л-1: 65-69;
Примеры решения задач 1. Движение тела массой 1 кг задано уравнением найти зависимость скорости и ускорения от времени. Вычислить силу, действующую на тело в конце второй секунды. Решение. Мгновенную скорость
Движение тела массой 1 кг задано уравнением найти зависимость скорости и ускорения от времени. Вычислить силу, действующую на тело в конце второй секунды. Решение. Мгновенную скорость
Министерство образования Республики Беларусь Учреждение образования «Гомельский государственный университет имени Франциска Скорины» А.Л. САМОФАЛОВ ОБЩАЯ ФИЗИКА: МЕХАНИКА ТЕСТОВЫЕ ЗАДАНИЯ для студентов
Календарно-тематическое планирование по физике (среднее общее образование, профильный уровень) 10 класс, 2016-2017 учебный год Пример Физика в познании вещества, поля, пространства и времени 1н IX 1 Что
Абсолютно необходимы для того, чтобы человек, решивший изучать эту науку, вооружившись ими, мог чувствовать себя в мире физики как рыба в воде. Без знания формул немыслимо решение задач по физике. Но все формулы запомнить практически невозможно и важно знать, особенно для юного ума, где найти ту или иную формулу и когда ее применить.
Расположение физических формул в специализированных учебниках распределяется обычно по соответствующим разделам среди текстовой информации, поэтому их поиск там может отнять довольно-таки много времени, а тем более, если они вдруг понадобятся Вам срочно!
Представленные ниже шпаргалки по физике содержат все основные формулы из курса физики , которые будут полезны учащимся школ и вузов.
Все формулы школьного курса по физике с сайта http://4ege.ru
I. Кинематика скачать
1. Основные понятия
2. Законы сложения скоростей и ускорений
3. Нормальное и тангенциальное ускорения
4. Типы движений
4.1. Равномерное движение
4.1.1. Равномерное прямолинейное движение
4.1.2. Равномерное движение по окружности
4.2. Движение с постоянным ускорением
4.2.1. Равноускоренное движение
4.2.2. Равнозамедленное движение
4.3. Гармоническое движение
II. Динамика скачать
1. Второй закон Ньютона
2. Теорема о движении центра масс
3. Третий закон Ньютона
4. Силы
5. Гравитационная сила
6. Силы, действующие через контакт
III. Законы сохранения. Работа и мощность скачать
1. Импульс материальной точки
2. Импульс системы материальных точек
3. Теорема об изменении импульса материальной точки
4. Теорема об изменении импульса системы материальных точек
5. Закон сохранения импульса
6. Работа силы
Работа силы
7. Мощность
8. Механическая энергия
9. Теорема о механической энергии
10. Закон сохранения механической энергии
11. Диссипативные силы
12. Методы вычисления работы
13. Средняя по времени сила
IV. Статика и гидростатика скачать
1. Условия равновесия
2. Вращающий момент
3. Неустойчивое равновесие, устойчивое равновесие, безразличное равновесие
4. Центр масс, центр тяжести
5. Сила гидростатического давления
6. Давлением жидкости
7. Давление в какой-либо точке жидкости
8, 9. Давление в однородной покоящейся жидкости
10. Архимедова сила
V. Тепловые явления скачать
1. Уравнение Менделеева-Клапейрона
2. Закон Дальтона
3. Основное уравнение МКТ
4. Газовые законы
5. Первый закон термодинамики
6. Адиабатический процесс
7. КПД циклического процесса (теплового двигателя)
8. Насыщенный пар
VI. Электростатика скачать
1. Закон Кулона
2. Принцип суперпозиции
3. Электрическое поле
3. 1. Напряженность и потенциал электрического поля, созданного одним точечным зарядом Q
1. Напряженность и потенциал электрического поля, созданного одним точечным зарядом Q
3.2. Напряженность и потенциал электрического поля, созданного системой точечных зарядов Q1, Q2, …
3.3. Напряженность и потенциал электрического поля, созданного равномерно заряженным по поверхности шаром
3.4. Напряженность и потенциал однородного электрического поля, (созданного равномерно заряженной плоскотью или плоским конденсатором)
4. Потенциальная энергия системы электрических зарядов
5. Электроемкость
6. Свойства проводника в электрическом поле
VII. Постоянный ток скачать
1. Упорядоченная скорость
2. Сила тока
3. Плотность тока
4. Закон Ома для участка цепи, не содержащего ЭДС
5. Закон Ома для участка цепи, содержащего ЭДС
6. Закон Ома для полной (замкнутой) цепи
7. Последовательное соединение проводников
8. Параллельное соединение проводников
9. Работа и мощность электрического тока
10. КПД электрической цепи
11. Условие выделения максимальной мощности на нагрузке
12. Закон Фарадея для электролиза
Закон Фарадея для электролиза
VIII. Магнитные явления скачать
1. Магнитное поле
2. Движение зарядов в магнитном поле
3. Рамка с током в магнитном поле
4. Магнитные поля, создаваемые различными токами
5. Взаимодействие токов
6. Явление электромагнитной индукции
7. Явление самоиндукции
IX. Колебания и волны скачать
1. Колебания, определения
2. Гармонические колебания
3. Простейшие колебательные системы
4. Волна
X. Оптика скачать
1. Закон отражения
2. Закон преломления
3. Линза
4. Изображение
5. Возможные случаи расположения предмета
6. Интерференция
7. Дифракция
Большая шпаргалка по физике . Все формулы изложены в компактном виде с небольшими комментариями. Шпаргалка также содержит полезные константы и прочую информацию. Файл содержит следующие разделы физики:
Механика (кинематика, динамика и статика)
Молекулярная физика. Свойства газов и жидкостей
Термодинамика
Электрические и электромагнитные явления
Электродинамика. Постоянный ток
Постоянный ток
Электромагнетизм
Колебания и волны. Оптика. Акустика
Квантовая физика и теория относительности
Маленькая шпора по физике . Все самое необходимое для экзамена. Нарезка основных формул по физике на одной странице. Не очень эстетично, зато практично. 🙂
Доброго дня уважаемые радиолюбители!
Приветствую вас на сайте “ “
Формулы составляют скелет науки об электронике. Вместо того, чтобы сваливать на стол целую кучу радиоэлементов, а потом переподключать их между собой, пытаясь выяснить, что же появится на свет в результате, опытные специалисты сразу строят новые схемы на основе известных математических и физических законов. Именно формулы помогают определять конкретные значения номиналов электронных компонентов и рабочих параметров схем.
Точно так же эффективно использовать формулы для модернизации уже готовых схем. К примеру, для того, чтобы выбрать правильный резистор в схеме с лампочкой, можно применить базовый закон Ома для постоянного тока (о нем можно будет прочесть в разделе “Соотношения закона Ома” сразу после нашего лирического вступления). Лампочку можно заставить, таким образом, светить более ярко или, наоборот – притушить.
Лампочку можно заставить, таким образом, светить более ярко или, наоборот – притушить.
В этой главе будут приведены многие основные формулы физики, с которыми рано или поздно приходится сталкиваться в процессе работы в электронике. Некоторые из них известны уже столетия, но мы до сих пор продолжаем ими успешно пользоваться, как будут пользоваться и наши внуки.
Соотношения закона ОмаЗакон Ома представляет собой взаимное соотношение между напряжением, током, сопротивлением и мощностью. Все выводимые формулы для расчета каждой из указанных величин представлены в таблице:
В этой таблице используются следующие общепринятые обозначения физических величин:
U – напряжение (В),
I – ток (А),
Р – мощность (Вт),
R – сопротивление (Ом),
Потренируемся на следующем примере: пусть нужно найти мощность схемы. Известно, что напряжение на ее выводах составляет 100 В, а ток- 10 А. Тогда мощность согласно закону Ома будет равна 100 х 10 = 1000 Вт. Полученное значение можно использовать для расчета, скажем, номинала предохранителя, который нужно ввести в устройство, или, к примеру, для оценки счета за электричество, который вам лично принесет электрик из ЖЭК в конце месяца.
Полученное значение можно использовать для расчета, скажем, номинала предохранителя, который нужно ввести в устройство, или, к примеру, для оценки счета за электричество, который вам лично принесет электрик из ЖЭК в конце месяца.
А вот другой пример: пусть нужно узнать номинал резистора в цепи с лампочкой, если известно, какой ток мы хотим пропускать через эту цепь. По закону Ома ток равен:
I = U / R
Схема, состоящая из лампочки, резистора и источника питания (батареи) показана на рисунке. Используя приведенную формулу, вычислить искомое сопротивление сможет даже школьник.
Что же в этой формуле есть что? Рассмотрим переменные подробнее.
> U пит (иногда также обозначается как V или Е): напряжение питания. Вследствие того, что при прохождении тока через лампочку на ней падает какое-то напряжение, величину этого падения (обычно рабочее напряжение лампочки, в нашем случае 3,5 В) нужно вычесть из напряжения источника питания. К примеру, если Uпит = 12 В, то U = 8,5 В при условии, что на лампочке падает 3,5 В.
> I : ток (измеряется в амперах), который планируется пропустить через лампочку. В нашем случае – 50 мА. Так как в формуле ток указывается в амперах, то 50 миллиампер составляет лишь малую его часть: 0,050 А.
> R : искомое сопротивление токоограничивающего резистора, в омах.
В продолжение, можно проставить в формулу расчета сопротивления реальные цифры вместо U, I и R:
R = U/I = 8,5 В / 0,050 А= 170 Ом
Расчёты сопротивленияРассчитать сопротивление одного резистора в простой цепи достаточно просто. Однако с добавлением в нее других резисторов, параллельно или последовательно, общее сопротивление цепи также изменяется. Суммарное сопротивление нескольких соединенных последовательно резисторов равно сумме отдельных сопротивлений каждого из них. Для параллельного же соединения все немного сложнее.
Почему нужно обращать внимание на способ соединения компонентов между собой? На то есть сразу несколько причин.
> Сопротивления резисторов составляют только некоторый фиксированный ряд номиналов. В некоторых схемах значение сопротивления должно быть рассчитано точно, но, поскольку резистор именно такого номинала может и не существовать вообще, то приходится соединять несколько элементов последовательно или параллельно.
> Резисторы – не единственные компоненты, которые имеют сопротивление. К примеру, витки обмотки электромотора также обладают некоторым сопротивлением току. Во многих практических задачах приходится рассчитывать суммарное сопротивление всей цепи.
Расчет сопротивления последовательных резисторовФормула для вычисления суммарного сопротивления резисторов, соединенных между собой последовательно, проста до неприличия. Нужно просто сложить все сопротивления:
Rобщ = Rl + R2 + R3 + … (столько раз, сколько есть элементов)
В данном случае величины Rl, R2, R3 и так далее – сопротивления отдельных резисторов или других компонентов цепи, а Rобщ – результирующая величина.
Так, к примеру, если имеется цепь из двух соединенных последовательно резисторов с номиналами 1,2 и 2,2 кОм, то суммарное сопротивление этого участка схемы будет равно 3,4 кОм.
Расчет сопротивления параллельных резисторовВсе немного усложняется, если требуется вычислить сопротивление цепи, состоящей из параллельных резисторов. Формула приобретает вид:
R общ = R1 * R2 / (R1 + R2)
где R1 и R2 – сопротивления отдельных резисторов или других элементов цепи, а Rобщ -результирующая величина. Так, если взять те же самые резисторы с номиналами 1,2 и 2,2 кОм, но соединенные параллельно, получим
776,47 = 2640000 / 3400
Для расчета результирующего сопротивления электрической цепи из трех и более резисторов используется следующая формула:
Расчёты ёмкостиФормулы, приведенные выше, справедливы и для расчета емкостей, только с точностью до наоборот. Так же, как и для резисторов, их можно расширить для любого количества компонентов в цепи.
Если нужно вычислить емкость цепи, состоящей из параллельных конденсаторов, необходимо просто сложить их номиналы:
Собщ = CI + С2 + СЗ + …
В этой формуле CI, С2 и СЗ – емкости отдельных конденсаторов, а Собщ суммирующая величина.
Расчет емкости последовательных конденсаторовДля вычисления общей емкости пары связанных последовательно конденсаторов применяется следующая формула:
Собщ = С1 * С2 /(С1+С2)
где С1 и С2 – значения емкости каждого из конденсаторов, а Собщ – общая емкость цепи
Расчет емкости трех и более последовательно соединенных конденсаторовВ схеме имеются конденсаторы? Много? Ничего страшного: даже если все они связаны последовательно, всегда можно найти результирующую емкость этой цепи:
Так зачем же вязать последовательно сразу несколько конденсаторов, когда могло хватить одного? Одним из логических объяснений этому факту служит необходимость получения конкретного номинала емкости цепи, аналога которому в стандартном ряду номиналов не существует. Иногда приходится идти и по более тернистому пути, особенно в чувствительных схемах, как, например, радиоприемники.
Иногда приходится идти и по более тернистому пути, особенно в чувствительных схемах, как, например, радиоприемники.
Наиболее широко на практике применяют такую единицу измерения энергии, как киловатт-часы или, если это касается электроники, ватт-часы. Рассчитать затраченную схемой энергию можно, зная длительность времени, на протяжении которого устройство включено. Формула для расчета такова:
ватт-часы = Р х Т
В этой формуле литера Р обозначает мощность потребления, выраженную в ваттах, а Т – время работы в часах. В физике принято выражать количество затраченной энергии в ватт-секундах, или Джоулях. Для расчета энергии в этих единицах ватт-часы делят на 3600.
Расчёт постоянной ёмкости RC-цепочкиВ электронных схемах часто используются RC-цепочки для обеспечения временных задержек или удлинения импульсных сигналов. Самые простые цепочки состоят всего лишь из резистора и конденсатора (отсюда и происхождение термина RC-цепочка).
Принцип работы RC-цепочки состоит в том, что заряженный конденсатор разряжается через резистор не мгновенно, а на протяжении некоторого интервала времени. Чем больше сопротивление резистора и/или конденсатора, тем дольше будет разряжаться емкость. Разработчики схем очень часто применяют RC-цепочки для создания простых таймеров и осцилляторов или изменения формы сигналов.
Каким же образом можно рассчитать постоянную времени RC-цепочки? Поскольку эта схема состоит из резистора и конденсатора, в уравнении используются значения сопротивления и емкости. Типичные конденсаторы имеют емкость порядка микрофарад и даже меньше, а системными единицами являются фарады, поэтому формула оперирует дробными числами.
T = RC
В этом уравнении литера Т служит для обозначения времени в секундах, R – сопротивления в омах, и С – емкости в фарадах.
Пусть, к примеру, имеется резистор 2000 Ом, подключенный к конденсатору 0,1 мкФ. Постоянная времени этой цепочки будет равна 0,002 с, или 2 мс.
Для того чтобы на первых порах облегчить вам перевод сверхмалых единиц емкостей в фарады, мы составили таблицу:
Расчёты частоты и длины волныЧастота сигнала является величиной, обратно пропорциональной его длине волны, как будет видно из формул чуть ниже. Эти формулы особенно полезны при работе с радиоэлектроникой, к примеру, для оценки длины куска провода, который планируется использовать в качестве антенны. Во всех следующих формулах длина волны выражается в метрах, а частота – в килогерцах.
Расчет частоты сигналаПредположим, вы хотите изучать электронику для того, чтобы, собрав свой собственный приемопередатчик, поболтать с такими же энтузиастами из другой части света по аматорской радиосети. Частоты радиоволн и их длина стоят в формулах бок о бок. В радиолюбительских сетях часто можно услышать высказывания о том, что оператор работает на такой-то и такой длине волны. Вот как рассчитать частоту радиосигнала, зная длину волны:
Частота = 300000 / длина волны
Длина волны в данной формуле выражается в миллиметрах, а не в футах, аршинах или попугаях. Частота же дана в мегагерцах.
Частота же дана в мегагерцах.
Ту же самую формулу можно использовать и для вычисления длины волны радиосигнала, если известна его частота:
Длина волны = 300000 / Частота
Результат будет выражен в миллиметрах, а частота сигнала указывается в мегагерцах.
Приведем пример расчета. Пусть радиолюбитель общается со своим другом на частоте 50 МГц (50 миллионов периодов в секунду). Подставив эти цифры в приведенную выше формулу, получим:
6000 миллиметров = 300000 / 50 МГц
Однако чаще пользуются системными единицами длины – метрами, поэтому для завершения расчета нам остается перевести длину волны в более понятную величину. Так как в 1 метре 1000 миллиметров, то в результате получим 6 м. Оказывается, радиолюбитель настроил свою радиостанцию на длину волны 6 метров. Прикольно!
Определение 1
Физика является естественной наукой, которая изучает общие и фундаментальные закономерности строения и эволюции материального мира.
Важность физики в современном мире огромна. Ее новые идеи и достижения приводят к развитию других наук и новых научных открытий, которые, в свою очередь, используются в технологиях и промышленности. Например, открытия в области термодинамики делают возможным строительство автомобиля, а также развитие радиоэлектроники привело к появлению компьютеров.
Несмотря на невероятное количество накопленных знаний о мире, человеческое понимание процессов и явлений, постоянно меняется и развивается, новые исследования приводят к возникновению новых и нерешенных вопросов, которые требуют новых объяснений и теорий. В этом смысле, физика находится в непрерывном процессе развития и до сих пор далека от возможности объяснить все природные явления и процессы.
Все формулы за $7$ класс
Скорость равномерного движения
Все формулы за 8 класс
Количество теплоты при нагревании (охлаждении)
$Q$ – количество теплоты [Дж], $m$ – масса [кг], $t_1$- начальная температура, $t_2$ – конечная температура, $c$ – удельная теплоемкость
Количество теплоты при сгорании топлива
$Q$ – количество теплоты [Дж], $m$ – масса [кг], $q$ – удельная теплота сгорания топлива [Дж /кг]
Количество теплоты плавления (кристаллизации)
$Q=\lambda \cdot m$
$Q$ – количество теплоты [Дж], $m$ – масса [кг], $\lambda$ – удельная теплота плавления [Дж/кг]
КПД теплового двигателя
$КПД=\frac{A_n\cdot 100%}{Q_1}$
КПД – коэффициент полезного действия [%], $А_n$ – полезная работа [Дж], $Q_1$ – количество теплоты от нагревателя [Дж]
Сила тока
$I$ – сила тока [А], $q$ – электрический заряд [Кл], $t$ – время [с]
Электрическое напряжение
$U$ – напряжение [В], $A$ – работа [Дж], $q$ – электрический заряд [Кл]
Закон Ома для участка цепи
$I$ – сила тока [А], $U$ – напряжение [В], $R$ – сопротивление [Ом]
Последовательное соединение проводников
Параллельное соединение проводников
$\frac{1}{R}=\frac{1}{R_1} +\frac{1}{R_2}$
Мощность электрического тока
$P$ – мощность [Вт], $U$ – напряжение [В], $I$ – сила тока [А]
Шпаргалка с формулами по физике для ЕГЭ
и не только (может понадобиться 7, 8, 9, 10 и 11 классам).
Для начала картинка, которую можно распечатать в компактном виде.
Механика
- Давление Р=F/S
- Плотность ρ=m/V
- Давление на глубине жидкости P=ρ∙g∙h
- Сила тяжести Fт=mg
- 5. Архимедова сила Fa=ρ ж ∙g∙Vт
- Уравнение движения при равноускоренном движении
X=X 0 +υ 0 ∙t+(a∙t 2)/2 S=(υ 2 –υ 0 2) /2а S=(υ +υ 0) ∙t /2
- Уравнение скорости при равноускоренном движении υ =υ 0 +a∙t
- Ускорение a=(υ –υ 0)/t
- Скорость при движении по окружности υ =2πR/Т
- Центростремительное ускорение a=υ 2 /R
- Связь периода с частотой ν=1/T=ω/2π
- II закон Ньютона F=ma
- Закон Гука Fy=-kx
- Закон Всемирного тяготения F=G∙M∙m/R 2
- Вес тела, движущегося с ускорением а Р=m(g+a)
- Вес тела, движущегося с ускорением а↓ Р=m(g-a)
- Сила трения Fтр=µN
- Импульс тела p=mυ
- Импульс силы Ft=∆p
- Момент силы M=F∙ℓ
- Потенциальная энергия тела, поднятого над землей Eп=mgh
- Потенциальная энергия упруго деформированного тела Eп=kx 2 /2
- Кинетическая энергия тела Ek=mυ 2 /2
- Работа A=F∙S∙cosα
- Мощность N=A/t=F∙υ
- Коэффициент полезного действия η=Aп/Аз
- Период колебаний математического маятника T=2π√ℓ/g
- Период колебаний пружинного маятника T=2 π √m/k
- Уравнение гармонических колебаний Х=Хmax∙cos ωt
- Связь длины волны, ее скорости и периода λ= υ Т
Молекулярная физика и термодинамика
- Количество вещества ν=N/ Na
- Молярная масса М=m/ν
- Cр.
 кин. энергия молекул одноатомного газа Ek=3/2∙kT
кин. энергия молекул одноатомного газа Ek=3/2∙kT - Основное уравнение МКТ P=nkT=1/3nm 0 υ 2
- Закон Гей – Люссака (изобарный процесс) V/T =const
- Закон Шарля (изохорный процесс) P/T =const
- Относительная влажность φ=P/P 0 ∙100%
- Внутр. энергия идеал. одноатомного газа U=3/2∙M/µ∙RT
- Работа газа A=P∙ΔV
- Закон Бойля – Мариотта (изотермический процесс) PV=const
- Количество теплоты при нагревании Q=Cm(T 2 -T 1)
- Количество теплоты при плавлении Q=λm
- Количество теплоты при парообразовании Q=Lm
- Количество теплоты при сгорании топлива Q=qm
- Уравнение состояния идеального газа PV=m/M∙RT
- Первый закон термодинамики ΔU=A+Q
- КПД тепловых двигателей η= (Q 1 – Q 2)/ Q 1
- КПД идеал. двигателей (цикл Карно) η= (Т 1 – Т 2)/ Т 1
Электростатика и электродинамика – формулы по физике
- Закон Кулона F=k∙q 1 ∙q 2 /R 2
- Напряженность электрического поля E=F/q
- Напряженность эл.
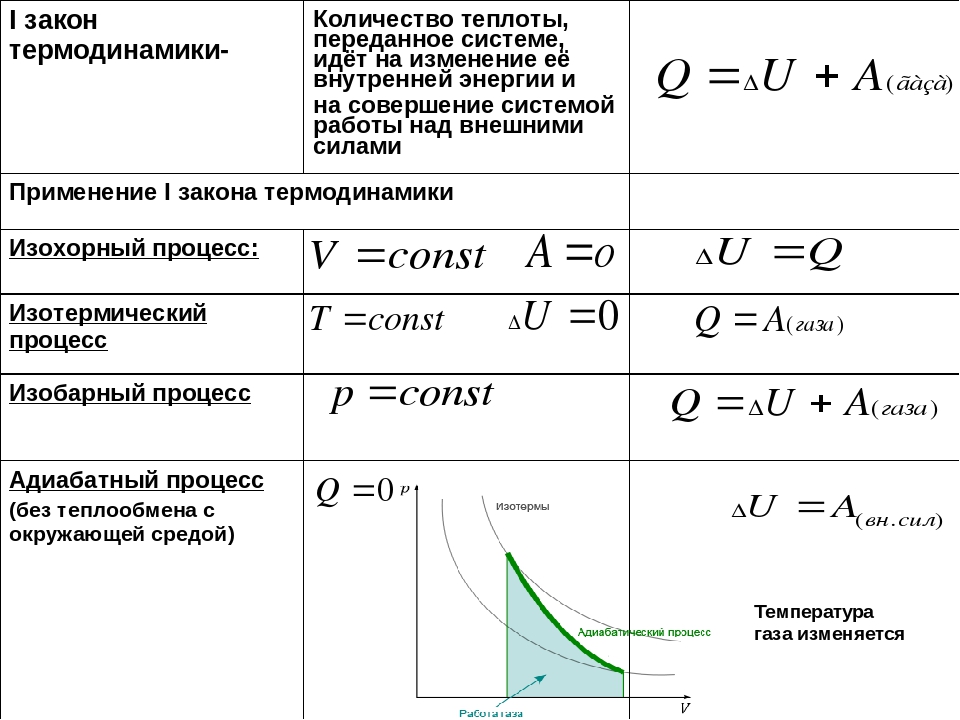 поля точечного заряда E=k∙q/R 2
поля точечного заряда E=k∙q/R 2 - Поверхностная плотность зарядов σ = q/S
- Напряженность эл. поля бесконечной плоскости E=2πkσ
- Диэлектрическая проницаемость ε=E 0 /E
- Потенциальная энергия взаимод. зарядов W= k∙q 1 q 2 /R
- Потенциал φ=W/q
- Потенциал точечного заряда φ=k∙q/R
- Напряжение U=A/q
- Для однородного электрического поля U=E∙d
- Электроемкость C=q/U
- Электроемкость плоского конденсатора C=S∙ε ∙ε 0 /d
- Энергия заряженного конденсатора W=qU/2=q²/2С=CU²/2
- Сила тока I=q/t
- Сопротивление проводника R=ρ∙ℓ/S
- Закон Ома для участка цепи I=U/R
- Законы послед. соединения I 1 =I 2 =I, U 1 +U 2 =U, R 1 +R 2 =R
- Законы паралл. соед. U 1 =U 2 =U, I 1 +I 2 =I, 1/R 1 +1/R 2 =1/R
- Мощность электрического тока P=I∙U
- Закон Джоуля-Ленца Q=I 2 Rt
- Закон Ома для полной цепи I=ε/(R+r)
- Ток короткого замыкания (R=0) I=ε/r
- Вектор магнитной индукции B=Fmax/ℓ∙I
- Сила Ампера Fa=IBℓsin α
- Сила Лоренца Fл=Bqυsin α
- Магнитный поток Ф=BSсos α Ф=LI
- Закон электромагнитной индукции Ei=ΔФ/Δt
- ЭДС индукции в движ проводнике Ei=Вℓυ sinα
- ЭДС самоиндукции Esi=-L∙ΔI/Δt
- Энергия магнитного поля катушки Wм=LI 2 /2
- Период колебаний кол.
 контура T=2π ∙√LC
контура T=2π ∙√LC - Индуктивное сопротивление X L =ωL=2πLν
- Емкостное сопротивление Xc=1/ωC
- Действующее значение силы тока Iд=Imax/√2,
- Действующее значение напряжения Uд=Umax/√2
- Полное сопротивление Z=√(Xc-X L) 2 +R 2
Оптика
- Закон преломления света n 21 =n 2 /n 1 = υ 1 / υ 2
- Показатель преломления n 21 =sin α/sin γ
- Формула тонкой линзы 1/F=1/d + 1/f
- Оптическая сила линзы D=1/F
- max интерференции: Δd=kλ,
- min интерференции: Δd=(2k+1)λ/2
- Диф.решетка d∙sin φ=k λ
Квантовая физика
- Ф-ла Эйнштейна для фотоэффекта hν=Aвых+Ek, Ek=U з е
- Красная граница фотоэффекта ν к = Aвых/h
- Импульс фотона P=mc=h/ λ=Е/с
Физика атомного ядра
Термическое уравнение состояния и термодинамические свойства молибдена при высоких давлениях: Journal of Applied Physics: Vol 113, No 9
Полный набор данных PVT для bcc-Mo был получен при давлениях до 31 ГПа и температурах от 300 до 1673 K с использованием калибрантов MgO и Aupressure. Термодинамический анализ этих данных был выполнен с использованием высокотемпературных уравнений состояния Берча-Мурнагана (HTBM), соотношения Ми-Грюнайзена-Дебая (MGD) в сочетании с EOS Винета при комнатной температуре и недавно предложенного Кунца-Эйнштейна ( KE) подход.Анализ данных сжатия при комнатной температуре с помощью Vinet EOS дает В 0 = 31,14 ± 0,02 Å 3 , K T = 260 ± 1 ГПа и K T ′ = 4,21 ± 0,05. Полученные термоупругие параметры для HTBM включают (∂ K T / ∂ T ) P = −0,019 ± 0,001 ГПа / K и тепловое расширение α = a 0 + a 1 T с a 0 = 1.55 (± 0,05) × 10 −5 K −1 и a 1 = 0,68 (± 0,07) × 10 −8 K −2 . Подгонка к соотношению MGD дает γ 0 = 2,03 ± 0,02 и q = 0,24 ± 0,02 с температурой Дебая ( θ 0 ), установленной на уровне 455–470 K.
Термодинамический анализ этих данных был выполнен с использованием высокотемпературных уравнений состояния Берча-Мурнагана (HTBM), соотношения Ми-Грюнайзена-Дебая (MGD) в сочетании с EOS Винета при комнатной температуре и недавно предложенного Кунца-Эйнштейна ( KE) подход.Анализ данных сжатия при комнатной температуре с помощью Vinet EOS дает В 0 = 31,14 ± 0,02 Å 3 , K T = 260 ± 1 ГПа и K T ′ = 4,21 ± 0,05. Полученные термоупругие параметры для HTBM включают (∂ K T / ∂ T ) P = −0,019 ± 0,001 ГПа / K и тепловое расширение α = a 0 + a 1 T с a 0 = 1.55 (± 0,05) × 10 −5 K −1 и a 1 = 0,68 (± 0,07) × 10 −8 K −2 . Подгонка к соотношению MGD дает γ 0 = 2,03 ± 0,02 и q = 0,24 ± 0,02 с температурой Дебая ( θ 0 ), установленной на уровне 455–470 K. Для KE EOS предлагаются две модели. Модель 1 (Mo-1) лучше всего соответствует нашим данным P-V-T , тогда как вторая модель (Mo-2) получена путем включения ударного сжатия и других экспериментальных измерений.Тем не менее обе модели обеспечивают близкие термоупругие параметры. Параметры, используемые для Mo-1, включают две температуры Эйнштейна E10 = 366 K и Θ E20 = 208 K; Параметр Грюнайзена при окружающих условиях γ 0 = 1,64 и бесконечном сжатии γ ∞ = 0,358 с β = 0,323; и дополнительные параметры подгонки м = 0,195, e 0 = 0,9 × 10 −6 K −1 и g = 5.6. Фиксированные параметры включают k = 2 в Kunc EOS, м E1 = м E2 = 1,5 в выражении для температуры Эйнштейна и a 0 = 0 (параметр внутренней ангармоничности) . Эти параметры являются наилучшим представлением экспериментальных данных для Mo и могут использоваться для различных термодинамических расчетов для Mo и Mo-содержащих систем, включая фазовые диаграммы, химические реакции и электронную структуру.
Для KE EOS предлагаются две модели. Модель 1 (Mo-1) лучше всего соответствует нашим данным P-V-T , тогда как вторая модель (Mo-2) получена путем включения ударного сжатия и других экспериментальных измерений.Тем не менее обе модели обеспечивают близкие термоупругие параметры. Параметры, используемые для Mo-1, включают две температуры Эйнштейна E10 = 366 K и Θ E20 = 208 K; Параметр Грюнайзена при окружающих условиях γ 0 = 1,64 и бесконечном сжатии γ ∞ = 0,358 с β = 0,323; и дополнительные параметры подгонки м = 0,195, e 0 = 0,9 × 10 −6 K −1 и g = 5.6. Фиксированные параметры включают k = 2 в Kunc EOS, м E1 = м E2 = 1,5 в выражении для температуры Эйнштейна и a 0 = 0 (параметр внутренней ангармоничности) . Эти параметры являются наилучшим представлением экспериментальных данных для Mo и могут использоваться для различных термодинамических расчетов для Mo и Mo-содержащих систем, включая фазовые диаграммы, химические реакции и электронную структуру.
БЛАГОДАРНОСТИ
Мы благодарим рецензентов за критические комментарии и предложения.Работа проводилась в рамках программы Глобального центра передового опыта «Глобальный образовательный и исследовательский центр динамики Земли и планет» в Университете Тохоку при поддержке Минобрнауки России, проект 14.B37.21.0457. Интеграционный проект СО РАН № 97 на 2012-2014 годы и Российского фонда фундаментальных исследований (№ 12-05-00758-а). Эксперименты проводились в соответствии с общими исследовательскими предложениями SPring-8 №№ 2009A1278, 2009B1327 и 2012B1289.
Amazon.com: Футболка «Формула энтропии физики термодинамики черной дыры»: Одежда, обувь и украшения
- Сплошные цвета: 100% хлопок; Серый вереск: 90% хлопок, 10% полиэстер; Все прочие верески: 50% хлопок, 50% полиэстер
- Imported
- Машинная стирка в холодной воде с похожими цветами, сушка при слабом нагреве
- Термодинамика черных дыр стремится согласовать законы термодинамики с существованием черных дыр и их энтропией.
 Квантовая механика также полезна при изучении черных дыр.
Квантовая механика также полезна при изучении черных дыр. - Отличная футболка для студентов и преподавателей ученых, физиков и математиков.
- Легкий, классический крой, рукава с двойной иглой и нижний край
Все формулы термодинамики, химия, класс 11, JEE, NEET
Загрузите лучшее приложение для подготовки к экзаменам в Индии
класс 9-10, JEE и NEET
Скачать приложение eSaral
Вот список всех формул 11 класса термодинамической химии, JEE, NEET.Пожалуйста, просмотрите все приведенные ниже формулы.
Прочие важные ссылки
Все формулы термодинамики Класс химии 11
- Термодинамические процессы:
- Изотемический процесс:
$ \ quad T = $ constant $ $ \ begin {array} {l} dT = 0 \\ \ Delta T = 0 \ end {array} - Изохорный процесс:
$ V = $ constant $ $ \ begin {array} {l} d V = 0 \\ \ Delta V = 0 \ end {array} - Изобарический процесс:
$ P = $ constant $ $ \ begin {array} {l} dP = 0 \\ \ Delta P = 0 \ end {array} - Адиабатический процесс:
q = 0
или теплообмен с окружающей средой $ = 0 $ (ноль)
- Изотемический процесс:
- Знаковое соглашение IUPAC о тепле и работе:
Работа, выполненная в системе = положительная работа, выполненная системой = отрицательная - $ 1 ^ {\ text {st}} $ Закон термодинамики
$$ \ Delta U = \ left (U_ {2} -U_ {1} \ right) = q + w $$ - Закон уравновешивания энергии:
$$ U = \ frac {f} {2} nRT \ quad \ text {(только для идеального газа)} $$
$$ \ Delta E = \ frac {f} {2} nR (\ Delta T) $$
, где $ f = $ степеней свободы для этого газа. {\ gamma-1} долл. США
{\ gamma-1} долл. США - Обратимая работа:
$$ W = \ frac {P_ {2} V_ {2} -P_ {1} V_ {1}} {\ gamma-1} = \ frac {\ operatorname {nR} \ left (T_ { 2} -T_ {1} \ right)} {\ gamma-1} $$ - Необратимая работа:
$$ W = \ frac {P_ {2} V_ {2} -P_ {1} V_ {1}} {\ gamma-1} = \ frac {n R \ left (T_ {2} – T_ {1} \ right)} {\ gamma-1} n C_ {v} \ left (T_ {2} -T_ {1} \ right) = – P_ {ext} \ left (V_ {2} -V_ { 1} \ right) $$ и используйте $$ \ frac {P_ {1} V_ {1}} {T_ {1}} = \ frac {P_ {2} V_ {2}} {T_ {2}} $$
, поэтому $ \ quad d W = -P _ {\ text {ext}} \ cdot d V = 0 $
Если нет .подается тепло $ q = 0 $, тогда $ \ Delta E = 0 $ $ \ begin {array} {ll} \ text {S0} & \ Delta T = 0 \ end {array} $
$$ \ begin {align}
\ Delta U = \ Delta Q + \ Delta W & \ Rightarrow \ quad \ Delta W = – P \ Delta V \\
\, следовательно, U = \ Delta Q – P \ Delta V
\ end {align} $$
Тепло, отдаваемое при постоянном объеме = изменение внутренней энергии $ \ поэтому du = (dq) _ {v} $
$ du = nC _ {v} d T $
$ C _ {v} = \ frac {1} {n} \ cdot \ frac {du} {dT} = \ frac {f} {2}
$ H \ Equiv $ Энтальпия (функция состояния и расширенное свойство)
$$ H = U + PV $$
$ \ Rightarrow C_ {0} -C_ {y} = R $ (только для идеального газа )
$ \ Delta S _ {\ text {unverse}} = \ Delta S _ {\ text {system}} + \ Delta S _ {\ text {окружение}}> 0 $ для спонтанного процесса.
 {B} \ frac {d q_ {r e v}} {T} $$
{B} \ frac {d q_ {r e v}} {T} $$Состояние $ A \ quad \ frac {\ text {irr}} {\ Delta s _ {\ text {irr}}} $
Состояние $ B $
$ P _ {1 }, V _ {1}, T _ {1} \ quad P _ {2}, V _ {2}, T _ {2} $
$ \ Delta S _ {\ text {system}} = n c_ {v } \ ln \ frac {T_ {2}} {T_ {1}} + n R \ ln \ frac {V_ {2}} {V_ {1}} \ quad $ (только для идеального газа)
Энтропия идеальных кристаллов всех чистых элементов \ & соединений равна нулю при абсолютном нуле температуры.
$$ G _ {\ text {system}} = H _ {\ text {system}} – TS _ {\ text {system}} $$
(i) Если $ \ Delta G _ {\ text {system}} $ равно $ (- ve) <0 \ Rightarrow $, процесс является спонтанным
(ii) Если $ \ Delta G _ {\ text {system }} $ is $> 0 $
$ \ Rightarrow $
процесс не является спонтанным
(iii) Если $ \ Delta G _ {\ text {system}} = 0 $
$ \ Rightarrow $
система находится в состоянии равновесия.
 {\ circ} + \ Delta C _ {p} \ left (T _ {2} – T _ {1} \ right) $
{\ circ} + \ Delta C _ {p} \ left (T _ {2} – T _ {1} \ right) $ , где $ \ Delta C _ {p} = C _ {p} ($ products $) – C _ {p } $ (реактивы).{\ circ} {} _ {c, \ text {экспериментальный}}
\ end {align}
Это был список всех формул термодинамического класса химии 11. Вы можете получить полный банк формул здесь.
Химические формулы класса 11
Загрузите лучшее приложение для подготовки к экзаменам в Индии
класс 9-10, JEE и NEET
Скачать приложение eSaral
Тепловое равновесие: определение, формула и пример – видео и стенограмма урока
Механизм
Температура – это средняя кинетическая энергия или энергия движения молекул в веществе.Когда вы помещаете два объекта с разной температурой в контакт друг с другом, более быстро движущиеся молекулы одного материала будут сталкиваться с более медленными молекулами другого. Тепловая энергия будет постепенно распространяться, пока два объекта не будут иметь одинаковую температуру – пока они не достигнут теплового равновесия. Это в основном то же самое, что и второй закон термодинамики , который гласит, что тепло только самопроизвольно перемещается из более горячих мест в более холодные, а не наоборот.
Тепловая энергия будет постепенно распространяться, пока два объекта не будут иметь одинаковую температуру – пока они не достигнут теплового равновесия. Это в основном то же самое, что и второй закон термодинамики , который гласит, что тепло только самопроизвольно перемещается из более горячих мест в более холодные, а не наоборот.
Формула
Если объект (или система) находится в термодинамическом равновесии, то можно сказать, что система минимизировала свой термодинамический потенциал. В физике упоминается много типов термодинамического потенциала, но, пожалуй, наиболее распространенным из них является свободная энергия Гельмгольца , которая измеряет общее количество полезной работы, которую можно извлечь из системы. Уравнение для свободной энергии Гельмгольца выглядит следующим образом:
Как упоминалось ранее, если система достигла термодинамического равновесия, это число будет минимально возможным.
Пример
Итак, предположим, вы смешиваете чай и молоко до тех пор, пока они не достигнут термодинамического равновесия, и вы хотите знать, какое максимальное количество полезной энергии вы можете извлечь из этой чашки чая, если ваше тело полностью работоспособно.
Температура чая и молока (в Кельвинах) составляет 373 К, полная внутренняя энергия системы составляет 3000 Дж, а энтропия системы составляет 6 Дж на Кельвин. Подставьте эти числа в уравнение:
И вы получите 762 Джоуля полезной работы.
Резюме урока
Тепловое равновесие определяется как состояние, в котором два объекта, соединенные проницаемым барьером, не имеют теплообмена между ними. Или, другими словами, два объекта, в которых тепло не передается между объектами, даже если они соединены. Это происходит, когда у них одинаковая температура . В общем, когда два объекта не имеют одинаковой температуры, тепло передается, потому что более быстро движущиеся молекулы в более горячем объекте сталкиваются с более медленными молекулами в более холодном объекте.
Объект в термодинамическом равновесии имеет минимально возможное значение своего термодинамического потенциала. Один из таких потенциалов называется свободной энергией Гельмгольца , которая измеряет общее количество полезной работы, которая может быть извлечена из системы. Это можно вычислить с помощью уравнения, обсуждаемого в этом уроке, и оно связано с температурой системы, энтропией системы и полной внутренней энергией системы.
Ключевые термины
Тепловое равновесие: состояние, в котором два объекта, соединенные проницаемым барьером, не имеют теплообмена между собой
Температура: средняя кинетическая энергия или энергия движения молекул в веществе
Второй закон термодинамики: тепло только самопроизвольно перемещается из более горячих мест в более холодные, а не наоборот
Свободная энергия Гельмгольца: измеряет общий объем полезной работы, которую можно извлечь из системы. Результаты
Результаты
После просмотра и изучения видеоурока вы сможете:
- Объяснить значение теплового равновесия
- Укажите второй закон термодинамики
- Приведите пример термодинамического равновесия
- Продемонстрируйте, как использовать уравнение для свободной энергии Гельмгольца
NEET Учебные заметки по термодинамике, простые определения с важными формулами и вопросы за предыдущий год
Термодинамика – это раздел физики, который занимается процессами, включающими тепло, работу и внутреннюю энергию. Система определяется как область пространства или количества исследуемой материи. Все, что находится вне этой системы, называется средой или окружением.
- Тема термодинамики имеет вес около 8-10% в NEET, что означает, что в этом разделе можно задать 2–3 вопроса или около 8–12 баллов.
- Некоторые из важных подтем термодинамики включают: тепловое равновесие, первый закон термодинамики, второй закон термодинамики и т.
 Д. Проверить Учебный план по физике NEET
Д. Проверить Учебный план по физике NEET
Термодинамика также занимается макроскопическим поведением, а не микроскопическим поведением этой системы, и понимание таких тем очень важно для решения вопросов из этого раздела. Ниже в статье приведены краткие заметки и важные вопросы по этим темам с советами и приемами, которые помогут вам подготовиться к NEET 2021.
Обязательно к прочтению:
Термодинамические процессы
Процесс, при котором один или несколько параметров термодинамической системы претерпевают изменения, называется термодинамическими процессами.В него входят:
- Изотермический процесс: При этом изменение давления и объема происходит с постоянной скоростью, и общее количество тепла в системе не остается постоянным.
- Изобарический процесс: В этом процессе изменение объема и температуры газа происходит на постоянном уровне.

- Изохорный процесс: В этом процессе изменение давления и температуры происходит таким образом, что объем системы остается постоянным.
- Адиабатический процесс: В этом процессе изменение объема, давления и температуры происходит без поступления тепла в систему и выхода из нее.
Вопрос: «CT», приведенная ниже – молярная теплоемкость. Найти его значение при постоянной температуре?
(А) 0
(B) 0 < C T < C v
(C) C v < C T (D) C T = Решение: (A) Первый закон термодинамики Первый закон термодинамики гласит, что если количество тепла подводится к системе, способной выполнять работу, то количество тепла, поглощаемого системой, равно сумме увеличения внутренней энергии системы, т. dQ = dU + dW Применение первого закона динамики – Вопрос: Прочтите приведенные ниже процессы и определите, какие из них нарушают Первый закон термодинамики? (A) W> 0, Q <0 и? Eint> 0 (B) W> 0, Q <0 и? Eint <0 (C) W <0, Q> 0 и? Eint <0 (D) W> 0, Q> 0 и? Eint <0 Решение: (D) Второй закон термодинамики Он утверждает, что состояние энтропии всей Вселенной всегда увеличивается со временем, и изменения во Вселенной никогда не могут быть отрицательными. Вопрос: Сколько тепла передается в резервуар с более высокой температурой, если тепловой насос использует 300 Дж или работает для отвода 400 Дж тепла из резервуара с низкой температурой? Решение: (C) Check Лучшие мобильные приложения для Android для подготовки к NEET Что такое двигатель Карно? Двигатель Карно – это теоретическая концепция, которая дает оценку максимально возможной эффективности, которой может обладать тепловой двигатель при преобразовании тепла в работу. КПД двигателя Карно: КПД двигателя η определяется как отношение полезного тепла (тепла, преобразованного в работу) к общему количеству тепла, подводимого к двигателю. η = W / Q 1 = [Q1 – Q2] / Q1 = 1- [Q2 / Q1] = 1- T2 / T1 Цикл Карно: Ниже приведены этапы цикла Карно: Вопрос: Если двигатель Карно с КПД 40% принимает тепло от источника, поддерживаемого при температуре 500 К, то какой будет температура на впуске от того же источника, если теперь КПД двигателя составляет 60%? Решение: (A) Вопрос: Сколько тепловой энергии извлекается из высокотемпературного резервуара за цикл, если КПД составляет 33%, а рабочая мощность составляет 24 Дж за цикл? Решение: (B) Обязательно к прочтению: Важные формулы Термодинамика – важная и обширная тема, когда дело касается NEET. Решенные вопросы за предыдущий год Вопрос: На приведенном ниже рисунке, на каком пути между начальным состоянием «I» и конечным состоянием «f» работа, выполняемая с газом, является наибольшей? (А) – А (В) – В (К) – С (Д) – Д Решение: (D) Вопрос: Морозильник Carnot забирает тепло от воды при температуре 0 ° C и отводит его при температуре 27 ° C. (А) 1,67 × × 105 Дж (В) 1,68 × × 106 Дж (К) 1,51 × × 105 Дж (D) 1,71 × × 107 Дж Решение: (A) Вопрос: Какова эффективность энергии Карно, которая отводит 3 Дж тепла в низкотемпературный резервуар на каждые 2 Дж выходной мощности. (D) 2/3 Решение: (A) Вопрос: Найдите, для какого из заданных процессов изменение энтропии было бы нулевым? (B) Изотермический (C) Адиабатический (D) Постоянный объем (E) Ни один из этих Решение: (C) Вопрос: 200 г воды нагревается с 40oC до 60oC. (A) 8,4 кДж (B) 4,2 кДж (C) 16,7 кДж (D) 167,4 кДж Решение: (C) Загрузить Практические материалы NEET Некоторые советы и приемы для решения проблемы NEET приведены ниже: Понимание концепций решения термодинамики и бумаги NEET является предварительным условием, поскольку прямых вопросов не будет, и каждый вопрос потребует отдельного приложения и подхода.Итак, будьте ясны и подробно изложите свои концепции. Сдача практических, пробных или секционных тестов является основным процессом для получения хороших оценок на любом экзамене. Очень важно соблюдать правильное расписание.Это поможет вам уделять должное время учебе и другим занятиям. Также помните, что не менее важно делать перерывы между ними. Найдите время и пересмотрите все важные темы, чтобы они были в ваших советах в день экзамена. для экзаменационного дня, В день экзамена сначала попытайтесь задать простые вопросы, а затем переходите к умеренным вопросам, а если позволяет время, то задавайте только сложные вопросы.Также не тратьте больше времени на один вопрос. Сохраняйте спокойствие и сосредоточенность и не паникуйте, если вы не можете решить один вопрос. Вдохните, расслабьтесь и решите следующую задачу, а потом вернитесь к ней, если у вас будет время. Внимательно прочтите вопросы дважды, а затем просмотрите варианты, прежде чем решать вопрос.Поскольку документ будет MCQ, во многих случаях вопрос может быть решен путем исключения и не требует полного решения и процедуры подачи заявки. План исследования NEET Physics Так как до NEET осталось почти 30 дней, большинство студентов закончили бы свою программу и будут делать только ее пересмотр. Но уловка здесь в том, что ваша доработка также должна быть спланирована. Ниже приведены некоторые вещи, которые вы можете сделать в следующие 30 дней, чтобы хорошо подготовиться к NEET: Энтропия – это макроскопическая термодинамическая величина, которая показывает, насколько случайным образом энергия в системе распределяется между ее степенями свободы. Чем более хаотично он распределен, тем выше энтропия. Поскольку случайные тепловые движения, как правило, делают вещи более случайными, чем менее, энтропия – это функция, которая может сказать нам, как макроскопические системы будут спонтанно развиваться (см. Закон термодинамики 2 и : вероятностный закон).Энтропия связывает микроскопическое и макроскопическое, и ее можно вычислить с обеих точек зрения. Как работает эта связь, описано на нашей странице Пример: Упорядочение энергии и энтропии. У нас есть два способа вычисления энтропии: макроскопический и микроскопический. Важной частью энтропии является тепловое равновесие: как энергия самопроизвольно перемещается от одной части системы к другой, когда температуры двух частей различны. $$ ΔS = Q / T $$ , где $ Q $ – тепло, поглощаемое системой, а $ T $ – температура системы. Как это использовать, показано на нашей странице «Пример: энтропия и тепловой поток». Хотя это нормально, если единственная проблема заключается в перемещении тепловой энергии, энтропия имеет гораздо более общий характер. Для этого нам нужно более микроскопическое изображение.{-4} \ mathrm {eV / K} $), а $ W_A $ – количество микросостояний, соответствующих макросостоянию A. Эта версия устанавливает связь между микроскопическим изображением – где указаны микроскопические детали распределения энергии в системе – и макроскопическим описанием. (Это неявно подчеркивает, что энтропия является свойством макросостояния. Нет смысла спрашивать, какова энтропия микросостояния.) Как это использовать, показано на нашей странице Пример: Расчет энтропии путем подсчета микросостояний. Подсчет микросостояний может быть немного сложным из-за проблемы, которая исходит из квантовой физики: неразличимость. На нашей странице «Степени свободы» мы узнали, что вращение отдельного атома не дает различимого состояния, поэтому мы не считаем вращение отдельного атома степенью свободы. Точно так же мы не можем различить вращение двухатомной молекулы вокруг своей оси симметрии. С классической точки зрения мы могли бы представить атомы как маленькие блоки чего-то, что можно пометить.Но в квантовой физике ясно, что все атомы (или молекулы) одного и того же вида неотличимы. Поэтому их обмен не ведет к новому соглашению. Эффект от этого на счет называется Парадокс Гиббса и описан на нашей странице Пример: Энтропия смешения и Парадокс Гиббса. Джо Редиш 15.02.18 Термодинамика – это раздел физики, который занимается концепциями теплового потока и изменения температуры в системе, а также взаимного преобразования тепла и других форм энергии. Термодинамика – это раздел физики, который занимается концепциями теплового потока и изменения температуры в системе, а также взаимного преобразования тепла и других форм энергии. Узнайте здесь о двойной природе материи и излучения. Прочтите о звуковых волнах здесь. Термодинамика определяется как раздел науки, который занимается изучением различных форм энергии и их преобразованием. Это действительно важная отрасль науки, поскольку она дает объяснение макроскопических свойств материи с точки зрения микроскопической концепции материи. В отличие от кинетики, которая занимается скоростью реакции, термодинамика занимается только начальным и конечным состояниями системы, претерпевающей изменения.Следует отметить, что законы термодинамики применимы только для тех систем, которые находятся в равновесии. Как известно, существует три основных закона термодинамики. Но прежде чем обсуждать их подробно, при обсуждении термодинамики мы будем использовать некоторые важные термины. Определенная часть вселенной, которая находится под наблюдением, называется системой. Типы систем Оставшаяся часть Вселенной, которая не является частью системы, называется окружением. Это свойства любой системы, которые возникают в результате объемного поведения материи.Эти свойства можно разделить на два типа: Измеряемые свойства, необходимые для описания состояния системы: переменные состояния. Например, температура, давление, объем, состав и т. Д. Это свойство системы, значение которого зависит только от состояния системы и не зависит от пути или способа, которым состояние достигнуто.Изменение значения этих свойств зависит только от начального и конечного состояний системы, а не от пути, по которому осуществляется переход от начального состояния к конечному. Определяется как процесс, при котором изменение давления или объема не влияет на температуру. Следовательно, температура в этом процессе остается постоянной. Процесс, при котором система не обменивается теплом с окружающей средой. Это означает, что тепло не выходит и не входит в систему. Определяется как процесс, при котором давление в системе остается постоянным. Когда объем системы остается постоянным независимо от изменения давления или температуры, этот процесс известен как изохорный процесс. Процесс, в котором направление может быть изменено на противоположное на любой стадии путем простого небольшого изменения переменной, такой как температура, давление и т. Процесс необратимый процесс называется необратимым. Естественные процессы необратимы. Процесс, в котором система претерпевает серию изменений и в конечном итоге возвращается в исходное состояние. Теперь, чтобы понять тепловой поток и механику термодинамики, были предложены четыре закона, которые называются законами термодинамики, которые можно представить как Этот закон был впервые предложен в 1931 году Р. Х. Фаулером. В нем говорится, что если две термодинамические системы каждая находится в тепловом равновесии с третьей, то они находятся в тепловом равновесии друг с другом. Либо мы можем сказать, что когда тело A находится в тепловом равновесии с телом B, а также отдельно с телом C, тогда B и C будут находиться в тепловом равновесии друг с другом. Это основа измерения температуры. Первый закон термодинамики – это повторение закона сохранения энергии.В нем говорится, что энергия не может быть создана или уничтожена в изолированной системе; энергия может только передаваться или изменяться из одной формы в другую. Когда в газ подается тепловая энергия, могут произойти две вещи: Внутренняя энергия газа может измениться Газ может выполнять некоторую внешнюю работу, расширяясь Согласно первому закону термодинамики: δQ = δW + ΔU Когда процесс выполняется системой, изменение накопленной энергии системы численно равно общему тепловому взаимодействию за вычетом сетевого взаимодействия во время процесса: Для циклического процесса: ΔU = 0 \ (W = P \ Delta V \ text {или} W = \ int_ {V_1} ^ {V_2} PdV \) Итак, отсюда можно сказать, что работа, выполняемая системой, будет полностью зависеть от изменения объема ΔV и давления в системе. Следовательно, мы можем сказать, что работа, выполняемая системой, полностью зависит от пути, пройденного системой. Проверьте здесь основные и важные физические единицы и измерения. Степень случайности системы называется энтропией системы. , т.е. энтропия системы может быть выражена как \ (\ Delta S = {\ Delta Q \ over {\ Delta T}} \ text {или} \ int {dQ \ over T} \) Где, ΔS = изменение энтропии; ΔQ / dQ = теплопередача; T = температура Итак, для адиабатических процессов ΔQ = 0, следовательно, энтропия данной системы также будет равна нулю. Подробности см. Здесь. \ (\ Delta S = \ int { dQ \ over T} \) Необратимые или спонтанные процессы могут происходить только в том направлении, в котором энтропия Вселенной или изолированной системы увеличивается. Для изолированной системы Узнайте подробнее о магнитном эффекте электрического тока. Третий закон термодинамики гласит, что: При абсолютной нулевой температуре энтропия идеального и идеально кристаллического твердого тела равна нулю. Итак, это все о термодинамике. Надеюсь, это помогло вам изучить концепции. Если вы с нетерпением ждете такой же практики, то были бы рады узнать, что мы предлагаем бесплатные пробные тесты в нашем приложении Testbook.Скачайте бесплатно прямо сейчас! Q.1 Что такое нулевой закон термодинамики? Ans. Q.2 Каков первый закон термодинамики? Ans.2 Первый закон термодинамики – это повторение закона сохранения энергии.В нем говорится, что энергия не может быть создана или уничтожена в изолированной системе; энергия может только передаваться или изменяться из одной формы в другую. Q.3 Что такое второй закон термодинамики? Ans.3 Согласно второму закону термодинамики, для естественных систем тепло всегда течет в одном направлении (от более высокой температуры к более низкой температуре тела), если этому не способствует внешний фактор. Q.4 Каков третий закон термодинамики? Отв.4 Третий закон термодинамики гласит: При абсолютной нулевой температуре энтропия идеального и идеально кристаллического твердого тела равна нулю. Первый закон термодинамики
 е.е,
е.е,
Пример вопроса Второй закон термодинамики
Пример вопроса 
Двигатель Карно

Пример вопроса Некоторые важные определения, которые следует запомнить
Система Часть вселенной исследуется. 
Открытая система Система, которая может обмениваться энергией и веществом с окружающей средой. Закрытая система Система, которая допускает прохождение энергии, но не массы, через ее границу. Изолированная система Система, которая не может обмениваться энергией или веществом с окружающей средой. Окрестности Часть вселенной, кроме системы, которая может с ней взаимодействовать. Граница Все, что отделяет систему от окружающего. Переменные состояния Переменные, которые необходимо определить для определения состояния любой системы, т. Е. Давление, объем, масса, температура, площадь поверхности и т. Д. Функции состояния Свойство системы, зависящее только от состояния системы, а не от пути. Пример: давление, объем, температура, внутренняя энергия, энтальпия, энтропия и т.  Д.
Д. Интенсивные свойства Свойства системы, не зависящие от массы системы, т.е. температура, давление, плотность, концентрация, Обширная собственность Свойства системы, которые зависят от массы системы, т. Е. Объема, энергии, энтальпии, энтропии и т. Д. Процесс Путь, по которому изменяется состояние системы. Важные формулы
Важные темы термодинамики
 Этой теме важно уделить должное внимание. Мало того, в термодинамике есть множество подтем, которые также требуют много времени и внимания. Они приведены ниже:
Этой теме важно уделить должное внимание. Мало того, в термодинамике есть множество подтем, которые также требуют много времени и внимания. Они приведены ниже: Примеры вопросов, решенных за предыдущий год
 Дано: скрытая теплота льда 336 × 103 Дж кг − 1. Найдите энергию, потребляемую морозильной камерой, если 5 кг воды при 0 ° C превращаются в морозильной камере в лед при 0 ° C.
Дано: скрытая теплота льда 336 × 103 Дж кг − 1. Найдите энергию, потребляемую морозильной камерой, если 5 кг воды при 0 ° C превращаются в морозильной камере в лед при 0 ° C.  Найдите изменение его внутренней энергии, где теплота воды = 4184 Дж / кг / К. (Небольшое изменение расширения воды можно не учитывать.)
Найдите изменение его внутренней энергии, где теплота воды = 4184 Дж / кг / К. (Небольшое изменение расширения воды можно не учитывать.) Несколько советов и приемов для решения вопросов
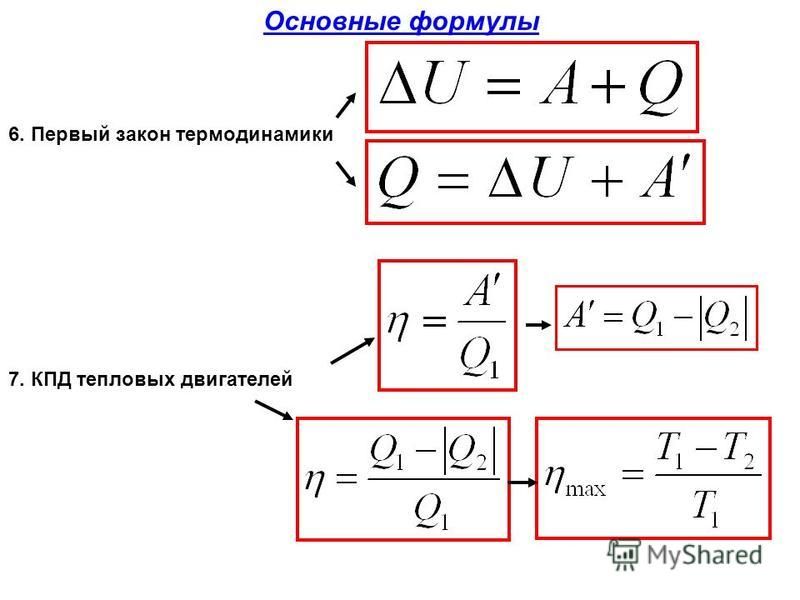 То же самое и с экзаменом NEET. Решение этих тестов и вопросов подготовит вас к уровню задаваемых вопросов, а также поможет вам повысить эффективность и рациональное использование времени в день экзамена.
То же самое и с экзаменом NEET. Решение этих тестов и вопросов подготовит вас к уровню задаваемых вопросов, а также поможет вам повысить эффективность и рациональное использование времени в день экзамена. Если вы не можете его решить, оставьте этот вопрос и переходите к следующему.
Если вы не можете его решить, оставьте этот вопрос и переходите к следующему. План исследования NEET Physics


Расчет энтропии – Nexus Wiki
Макроскопическое уравнение для энтропии
 Для этого мы можем сделать макроскопическое представление системы и вычислить изменение энтропии той части системы, которая получает или теряет тепловую энергию, по уравнению
Для этого мы можем сделать макроскопическое представление системы и вычислить изменение энтропии той части системы, которая получает или теряет тепловую энергию, по уравнению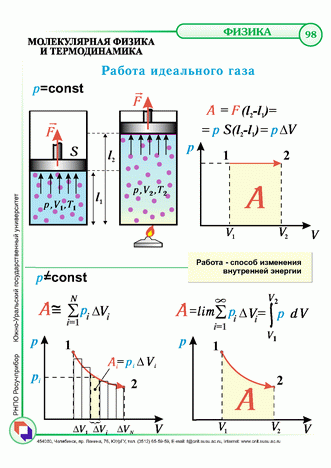
Проверить определение, уравнения, законы и формулы
 Чтобы понять термодинамику, вы должны знать тепловые свойства Материи. Термодинамика подчиняется четырем законам. В этой статье мы подробно изучим эти законы и поймем, как мы можем представить систему, используя термодинамические свойства, на примерах. Мы также изучим, как мы можем предсказать результат конкретного процесса с помощью термодинамики. Во-первых, давайте разберемся с термодинамической системой.
Чтобы понять термодинамику, вы должны знать тепловые свойства Материи. Термодинамика подчиняется четырем законам. В этой статье мы подробно изучим эти законы и поймем, как мы можем представить систему, используя термодинамические свойства, на примерах. Мы также изучим, как мы можем предсказать результат конкретного процесса с помощью термодинамики. Во-первых, давайте разберемся с термодинамической системой.

2. Окружение
4. Переменная состояния 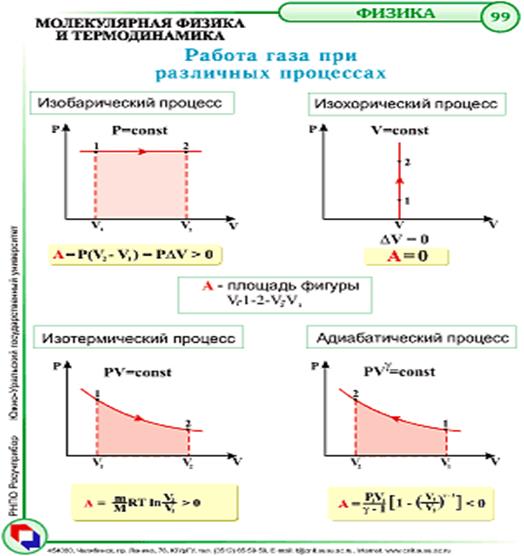 Например, масса, объем, молярные свойства (молярный объем, молярная теплоемкость и т. Д.), Площадь поверхности, внутренняя энергия, энтальпия, энтропия, свободная энергия, теплоемкость, сила и т. Д.
Например, масса, объем, молярные свойства (молярный объем, молярная теплоемкость и т. Д.), Площадь поверхности, внутренняя энергия, энтальпия, энтропия, свободная энергия, теплоемкость, сила и т. Д. Например – давление, объем, температура, внутренняя энергия, энтальпия, энтропия.
Например – давление, объем, температура, внутренняя энергия, энтальпия, энтропия. Д.
Д.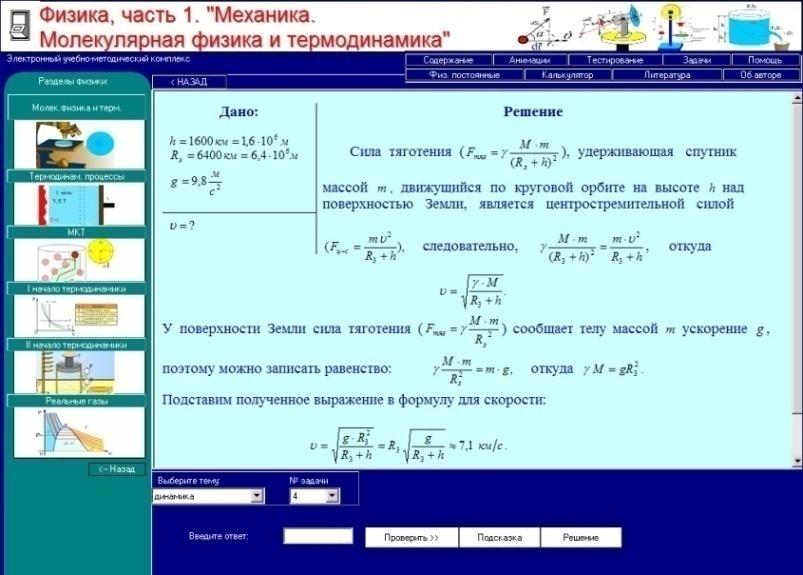 (b) Адиабатическая стенка между A и B заменена проводящей стенкой, а C изолирована от A и B адиабатической стенкой.
(b) Адиабатическая стенка между A и B заменена проводящей стенкой, а C изолирована от A и B адиабатической стенкой.
 Например, если лед тает, тепло всегда будет перетекать ото льда в горячую окружающую среду, если только он не будет удерживаться в морозильной камере.
Например, если лед тает, тепло всегда будет перетекать ото льда в горячую окружающую среду, если только он не будет удерживаться в морозильной камере. Эти процессы не могут происходить в направлении уменьшения энтропии.
Эти процессы не могут происходить в направлении уменьшения энтропии. 1 Он утверждает, что если две термодинамические системы каждая находится в тепловом равновесии с третьей, то они находятся в тепловом равновесии друг с другом.
1 Он утверждает, что если две термодинамические системы каждая находится в тепловом равновесии с третьей, то они находятся в тепловом равновесии друг с другом.
