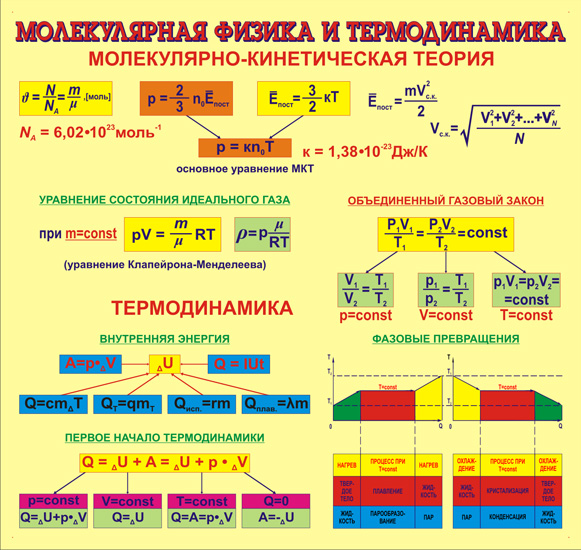
основные формулы с пояснениями, обозначения давления и объёма
Содержание:
- Что такое молекулярная физика
- Основные величины молекулярной физики и соотношения между ними
-
Формулы с пояснениями и обозначениями, к каким процессам применимы
- Основное уравнение молекулярно-кинетической теории идеального газа
- Уравнение Менделеева-Клапейрона
- Законы физиков Бойля, Гей-Люссака и Шарля
- Закон Дальтона
Содержание
- Что такое молекулярная физика
- Основные величины молекулярной физики и соотношения между ними
-
Формулы с пояснениями и обозначениями, к каким процессам применимы
- Основное уравнение молекулярно-кинетической теории идеального газа
- Уравнение Менделеева-Клапейрона
- Законы физиков Бойля, Гей-Люссака и Шарля
- Закон Дальтона
Что такое молекулярная физика
Молекулярная физика — раздел физики, который изучает физические свойства тел на основе рассмотрения их молекулярного строения.
Свойства любого вещества диктуются особенностями его молекулярного строения. От индивидуальных характеристик строения молекулярной решетки, изменения межмолекулярных связей под воздействием факторов окружающей среды и времени их контакта зависят закономерности тех или иных процессов.
На физические свойства тел могут влиять давление, температура, электромагнитные поля. В результате этого первоначальные свойства предмета частично либо полностью видоизменяются. На практике, выбирая тот или иной состав вещества, обязательно учитывают его поведение при различных условиях эксплуатации: смену фазового состояния, появление поверхностных явлений и т.п.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Дать объяснение кардинальному либо частичному качественному изменению свойств можно только с позиции описания их макроскопических характеристик, вытекающих из микроскопического строения. Проявление законов межмолекулярных связей дают пояснение поведению тел при любых условиях.
Проявление законов межмолекулярных связей дают пояснение поведению тел при любых условиях.
Основные величины молекулярной физики и соотношения между ними
В основе физики, основывающейся на молекулярных особенностях, лежат величины, от них зависящие. Схематически их можно охарактеризовать следующим образом:
- Масса вещества (m).
- Объем (V).
- Плотность (ρ).
- Концентрация (n).
- Число частиц вещества (N).
Основные величины молекулярной физики взаимосвязаны друг с другом посредством следующих математических выражений:
\(\rho=m\div V\)
а значит \(\rho m=\rho\times V\\\)
Если N — число частиц вещества, а mo — масса каждой из них, то общая масса равна:
\(m=N\times mo\\\)
Концентрацию вещества можно высчитать по формуле:
\(n=N\div V\left\{\right\}\\\)
При умножении mo на N получится плотность ρ.
Формулы с пояснениями и обозначениями, к каким процессам применимы
В зависимости от условий окружающей среды вещества могут переходить из одного агрегатного состояния в другое:
- твердое;
- жидкое;
- газообразное.

Исходя из этого, оно проявляет различные свойства, изучение которых — задача молекулярной физики. Ее главной основой является молекулярно-кинетическая теория, рассматривающая тепловое движение молекул и атомов.
Основное уравнение молекулярно-кинетической теории идеального газа
Основополагающими моментами молекулярно-кинетической теории являются следующие:
- любое вещество имеет молекулярно-атомное строение;
- внутренние микрочастицы находятся в постоянном, хаотическом движении;
- они способны взаимодействовать друг с другом.
Примечание
Атомы, как и молекулы, электрически нейтральны, однако способны становиться положительными или отрицательными ионами, получая элетрозаряд. Тогда они называются катионами и анионами.
Если в обычном состоянии молекулы движутся хаотично (беспорядочно), то с возрастанием температуры увеличивается их кинетическая энергия, они разлетаются, а само вещество постепенно переходит в газообразную стадию.
Характер движения молекул в различных фазах различается. Если в твердой фазе они колеблются вокруг зафиксированных центров, то в жидкостях более свободны и могут осуществлять движение по всему объему. Именно этой особенностью вызывается такое свойство, как текучесть.
Для газообразного состояния характерно значительное превышение размеров расстояния между молекулами, чем их собственные габариты. Поэтому силы взаимодействия между ними невелики. Каждая микрочастица движется беспорядочно, пока не столкнется с себе подобной или стенкой сосуда. Это свойство вызывает способность газа расширяться и распространяться по всему объему сосуда.
Идеальный газ — теоретическая модель, широко применяемая для описания свойств и поведения реальных газов при умеренных давлениях и температурах.
Математическое выражение основного уравнения молекулярно-кинетической теории выглядит так:
\(p=1⁄3n\times mo\times V2 кв\)
Где p — давление газа, n — концентрация молекул в единице объема, mo — масса одной молекулы, Vкв — среднеквадратичная скорость молекулы.
Теоретическая суть уравнения заключается в определении зависимости между макротелом (газ, заключенный в сосуд) и его микропараметрами (характер движения молекул и атомов).
Молекула, сталкиваясь со стенкой сосуда, меняет свой импульс, поскольку не только она передает энергию стенке, но и получает противоположно направленный импульс. Это явление объясняют второй и третий законы Ньютона. Сумма всех ударов молекул о стенку создает давление газа.
Уравнение Менделеева-Клапейрона
Из постулатов молекулярно-кинетической теории вытекает уравнение состояния идеального газа:
\(p\times V=v\times R\times T\)
Где p — давление, V — объем, v — скорость движения частиц, R — универсальная газовая постоянная, равная 8,31 Дж/(моль∙К), T — температура
Это уравнение состояния идеального газа. Его открытие принадлежит Клайперону.
Примечание
Первоначально оно было сформулировано для одного моля газообразного вещества, позднее Менделеев установил его справедливость для большего количества молей.
Данное уравнение подразумевает определение параметров идеального газа, находящегося при нормальных условиях (температуре 273 К и давлении 1 атм).
Исходя из анализируемого равенства, известные параметры состояния идеального газа всегда помогут найти искомую величину. В то же время изменение любого из них вызовет коррекцию всех остальных.
Законы физиков Бойля, Гей-Люссака и Шарля
Физические законы, которые объясняют поведение идеального газа и дают возможность определить заданные показатели, носят имена своих открывателей. В зависимости от того, о чем идет речь в задаче, важно правильно выбрать закон, отражающий нужный критерий. Перед тем, как перейти к их характеристике, нужно обозначить следующие термины:
- парциальное давление — P, оказываемое газом, если бы в смеси не присутствовали другие компоненты;
- изотермический процесс — условия с постоянной температурой;
- изохорный — с постоянным объемом.

Примечание
Если в задаче идет речь о количестве молекул применяется закон Авагадро, о смеси газов — закон Дальтона, при постоянном объеме газа — закон Шарля, изобарном процессе — Гей-Люссака, изотермическом — Бойля-Мариотта. При постоянной массе газа действует универсальный закон Клайперона.
Следствием уравнения Клайперона-Менделеева является газовый закон, открытый в 1662 году Р.Бойлем и параллельно — Э.Мариоттом (1676 г). Он гласит, что при постоянных массе и температуре величина, равная произведению давления газа на его объем остается неизменной.
Существует и другая, параллельная первой, формулировка: если температура газа постоянна, то давление его определенной массы обратно пропорционально объему.
Математическая запись выглядит следующим образом:
\(p1\div p2=V2\div V1\)
Закон Гей-Люссака гласит, что объем газа прямо пропорционален его абсолютной температуре. Обязательное условие для данного выражения — постоянное давление (процесс изобарный). Закон был открыт в 1802 году.
Закон был открыт в 1802 году.
В качестве следствия из этого закона в курсе физики приводится заключение, что при постоянных массе и давлении газа соотношение объема и температуры газа остается постоянной величиной.
Для закона Гей-Люссака необходимо соблюдение изобарности процесса и постоянстве массы.
Закон Шарля называют вторым законом Гей-Люссака. В нем идет речь о соотношении температуры и давления идеального газа при постоянном объеме. Закон был открыт в 1787 году Шарлем. Уточнен в 1802 году Гей-Люссаком.
Формулировка закона Шарля: при фиксированных массе и объеме идеального газа давление прямо пропорционально абсолютной температуре идеального газа.
Закон имеет теоретическое подтверждение, поскольку мера средней кинетической энергии вещества — это температура. При ее увеличении частицы сильнее ударяются о стенку сосуда и количество ударов создает более высокое давление.
В качестве следствия из этого закона часто применяется следующее понятие: при постоянных массе и объеме идеального газа отношение его давления к температуре является постоянным. Обязательное условие — изохорность процесса.
Обязательное условие — изохорность процесса.
Для решения задач с помощью газовых законов температура переводится из градусов Цельсия в Кельвины.
Закон Дальтона
Если сосуд заполняется не чистым газом, а смесью нескольких компонентов, то для определения давления на стенки применяется закон Дальтона.
Согласно закону Дальтона, общее давление будет равно сумме давлений каждого из компонентов смеси.
В этом законе вводится термин «парциальное» давление, т.е. то, которое производил бы один из компонентов, если бы был единственным.
Математическое выражение выглядит следующим образом:
p=p1+p2+p3+…pn
Обязательным условием действия этого закона является отсутствие химического взаимодействия между входящими в состав газовой смеси элементами.
Насколько полезной была для вас статья?
Рейтинг: 5.00 (Голосов: 1)
Поиск по содержимому
Молекулярная физика в 📙 формулах
1. Базовые формулы молекулярной физики
Базовые формулы молекулярной физики
2. Формулы, описывающие процессы в молекулярной физике
Задачей молекулярной физики является исследование физических свойств тел, основанное на длительном наблюдении состояний их кристаллических решеток. Данный раздел физики ориентируется на методологию статической механики, кинетики и термодинамики.
Областью изучения молекулярной физики являются поведение и взаимодействие мельчайших частиц физического тела – атомов, молекул, ионов.
То есть данный раздел физики исследует свойства тел, исходя из характеристик отдельных молекул. Считается, что все взаимные действия и движения происходят на микроуровне, и при этом все изменения, которые можно наблюдать невооруженным взглядом, являются последствием данных микропроцессов.
Основными формулами молекулярной физики устанавливаются взаимосвязи разных характеристик системы, при этом пользуются уравнением Клапейрона, законами Бойля-Мариотта, Шарля и Гей-Люссака.
Уравнение Клапейрона имеет следующий вид:
\(pV=nRT\),
где \(p\) – давление;
\(V\) – объем, который занимает газ;
\(n\) – количество вещества, моль;
\(R\) – универсальная газовая постоянная;
\(T\) – температура.
Путем простых преобразований из данной формулы выводятся следующие законы:
- Бойля-Мариотта для изотермического процесса:
\(pV=const.\)
- Гей-Люссака для изобарического процесса:
\({V\over T}=const.\)
- Шарля для изохорического процесса:
\({p\over T}=const.\)
Все физические величины и явления имеют свои особенные обозначения и их описывают свои формулы, отображающие взаимосвязь различных параметров. Различные явления пересекаются в своем проявлении, поэтому в разных формулах встречаются одни и те же величины, выраженные различными способами.
Например, количество вещества зависит от его массы и числа молекул в этой массе. Причиной этого является различие в количестве молекул в одной и той же массе для разных веществ. В процессах, что происходят на микроуровне, принимают участие атомы, они являются непосредственными участниками различных взаимных действий.
Количество вещества определяется по следующей формуле:
\(m={N\over N_A}\) ,
где \(m\) – масса;
\( N\) – число молекул;
\(N_A\) – число Авогадро.
Молекулы являются сложными системами и обладают многоступенчатой структурой. Для упрощенного понимания представим газ, находящийся в закрытом сосуде, частичками которого есть упругие однородные шарики, которые не взаимодействуют между собой. Такой газ принято считать идеальным, формула для его расчета имеет следующий вид:
\(P=nkT\),
где \(n\) – концентрация молекул;
\(T\) – абсолютная температура.
Количество частичек (молекул) \(N\) в этой массе можно рассчитать таким образом:
\(N=mN_A\).
Один моль всегда содержит одинаковое число минимальных частиц, которое равно числу Авогадро. То есть, если мы знаем массу моля, то поделив ее на число Авогадро, мы получим массу системной единицы:
\(m={M\over N_A}\) ,
где \(M\) – молярная масса.
Необходимо помнить, что данная формула используется лишь для молекул неорганической химии. Если рассматривать молекулы органических веществ, то они намного больше в размерах и весе.
Молярная масса показывает массу одного моля вещества. Так как один моль вещества вмещает одинаковое число частичек вещества, формула для расчета молярной массы будет иметь вид:
Так как один моль вещества вмещает одинаковое число частичек вещества, формула для расчета молярной массы будет иметь вид:
\(M=kM_r\),
где \(k\) – коэффициент пропорциональности;
\(M_r\) – атомная масса вещества.
Молярную массу вещества можно выразить из закона Менделеева-Клапейрона, который имеет следующий вид:
\(pV={mRT\over M}\),
отсюда молярная масса запишется как:
\(M={mRT\over pV}\).
Формулы статической физики и термодинамики
Для статической физики, как раздела молекулярной физики, справедливы такие формулы:
\(Q=mc(t_2-t_1) \\ Q=A+(U_2-U_1)\\ H=TdS+Vdp.\\\)
\(H\) – это энтальпия.
\(V={dG\over dpS}\),
где \(G\) – энергия Гиббса или термодинамический потенциал;
\(S\) – энтропия, которую ввел ученый Клаузиус.
С помощью формул термодинамики и молекулярной физики становится возможным рассчитывать все процессы, происходящие в твердых веществах и газах. Данные расчеты являются немаловажными при исследованиях и на практике, так как позволяют решать различные задачи.
Молекулярная кинетика | Формулы физики
Количество вещества (моль)
Находить
Известно, что:
νNN_A =
Рассчитать ‘ν’Молярная масса
Находить
Известно, что:
Ммν =
Рассчитать ‘M’Масса молекулы
Находить
Известно, что:
м0мН =
Рассчитать m0Молярная масса
Находить
Известно, что:
Мм0Н_А =
Рассчитать «М»Количество молекул
Находить
Известно, что:
NmN_AM =
Рассчитать ‘N’Формула кинетической теории
Находить
Известно, что:
pnm0v =
Рассчитать pВнутренняя энергия молекул
Находить
Известно, что:
Эмв =
Рассчитать ЕДавление идеального газа
Находить
Известно, что:
pnE =
Рассчитать «p»Концентрация молекул
Находить
Известно, что:
нНВ =
Рассчитать ‘n’Давление газа, объем и средняя кинетическая энергия
Находить
Известно, что:
pVNE =
Рассчитать «p»Газ: давление, объем, температура
Находить
Известно, что:
pVNkT =
Рассчитать pСредняя кинетическая энергия
Находить
Известно, что:
ЭкТ =
Рассчитать «E»Газ: давление, концентрация, температура
Находить
Известно, что:
рнкТ =
Рассчитать «p»Газ: количество вещества, объем
Находить
Известно, что:
νВВ_М =
Рассчитать ‘ν’Среднеквадратичная скорость молекулы газа
Находить
Известно, что:
vkTm0 =
Рассчитать ‘v’Закон идеального газа (уравнение Менделеева – Клапейрона)
Находить
Известно, что:
pVmRTM =
Рассчитать ‘p’Закон идеального газа (уравнение Менделеева-Клапейрона)
Находить
Известно, что:
pVTνR =
Рассчитать pЗакон Бойля и Мариотта (изотермический процесс)
Находить
Известно, что:
p1V1p2V2 =
Рассчитать p1Закон Гей-Люссака (изобарический процесс)
Находить
Известно, что:
В1Т1В2Т2 =
Рассчитать «V1»Тепловое расширение газа
Находить
Известно, что:
VV0αT =
Вычислить ‘V’Закон Шарля (изохорический процесс)
Находить
Известно, что:
p1T1p2T2 =
Рассчитать ‘p1’Температурная зависимость давления газа
Находить
Известно, что:
pp0γT =
Вычислить ‘p’6.
 8: Силы между молекулами — Физика LibreTexts
8: Силы между молекулами — Физика LibreTexts- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 8589
- Джереми Татум
- Университет Виктории
В разделе 6.3 мы описали в качественной форме силы между молекулами — дальнодействующие силы Ван-дер-Ваальса притяжения, вызванные взаимодействием индуцированный диполь/индуцированный диполь, и короткодействующие кулоновские силы отталкивания, возникающие при близком сближении молекул, и как эти межмолекулярные силы вызывают отклонения от ожиданий «закона Бойля» для уравнения состояния идеального газа. Предположительно, если бы мы знали точное уравнение закона силы как функции межмолекулярного расстояния, мы могли бы в принципе вычислить уравнение состояния; и наоборот, если бы мы знали посредством измерения форму уравнения состояния, мы могли бы вывести форму межмолекулярных сил. На самом деле я сам этого не делал; ранней ссылкой, которую стоит посмотреть, будет Lennard-Jones, Proc. Рой, соц. 9{2}\]
На самом деле я сам этого не делал; ранней ссылкой, которую стоит посмотреть, будет Lennard-Jones, Proc. Рой, соц. 9{2}\]
Каждый из них переходит в V → D при r → ∞ и V = 0, когда r = re. Потенциал Леннарда-Джонса (но не потенциал Морзе) стремится к ∞ при r → 0,
. Эти выражения не могут быть «выведены» в обычном смысле; это просто выражения, которые полезны для обсуждения, поскольку они качественно описывают форму потенциальной функции, которую вы ожидаете. Выражение Леннарда-Джонса часто используется при обсуждении силы Ван-дер-Ваальса: если сила притяжения Ван-дер-Ваальса обусловлена главным образом взаимодействием индуцированный диполь/индуцированный диполь, то r −6 термин примерно правильный. Потенциал Морзе чаще используется при обсуждении силы между атомами в связанной молекуле. Если потенциал Морзе подставить в уравнение Шредингера для ангармонически колеблющейся двухатомной молекулы, это приведет к простому решению для собственных функций и собственных значений с уровнями энергии, заданными как квадратичные (и не выше) в \( v + \frac{ 1}{2}\).