Формулы для решения задач по химии
Так как химия наука точная, она неразрывно связана с различного рода вычислениями. Чтобы решать задачи, нужно знать формулы и хорошо в них ориентироваться. Без этих базовых знаний и навыков изучение химии становится невозможным.
Мы собрали для вас основные химические формулы, изучаемые в школьном курсе. Они пригодятся каждому ученику, особенно тем, кто будет сдавать ОГЭ или ЕГЭ по этому непростому, но очень интересному предмету.
Нахождение количества вещества
Первое и основное понятие, которое необходимо усвоить – это количество вещества, измеряемое в молях и обозначающееся латинской буквой «n». Для его нахождения нужно основываться на условии задачи, так как вычислить количество вещества можно по трём формулам:
1) По массе. n=m/M — Массу вещества (в граммах) разделить на его молярную массу (в г/моль).
2) По объёму. n=V/Vm — Отношением объёма вещества к его молярному объёму (используется для газов).
3) По числу молекул. n=N/NA – Число молекул вещества делённое на число Авогадро. Число Авогадро (NA) – физическая величина, указывающая на число молекул, содержащихся в 1 моле вещества, и численно равная 6,0221 * 1023 моль-1.
Формулы для нахождения массы
Массу вещества можно найти несколькими способами:
1. Умножив количество вещества на молярную массу: m (г) = n (моль)×M (г/моль).
2. Произведением объёма раствора и его плотности: m = V (л) ×ρ (г/л).
3. Перемножив массовую долю с массой раствора: m = m(р-ра) × ω.
Молярная масса (М) – это масса одного моля вещества. Вычисляется она следующим образом: посредством сложения атомных масс элементов, из которых состоит вещество, получаем относительную молекулярную массу. Молярная масса численно равна относительной молекулярной массе, но имеет размерность «г/моль». Также молярную массу можно найти с помощью отношения массы вещества к его количеству:
Также молярную массу можно найти с помощью отношения массы вещества к его количеству:
M = m/n
Формулы для нахождения объёма
Для вычисления объёма того или иного вещества можно воспользоваться одной из формул:
1. Объём раствора находится как отношение массы раствора к его плотности:
V(р-ра) = m(р-ра) / ρ
2. Объём газа равен отношению его количества вещества к молярному объёму:
V(газа) = n/VM
Молярный объём (VM) – объём, который занимает 1 моль вещества при определённых показателях давления и температуры. Находится при делении молярной массы вещества на его плотность:
VM = M/ρ
При нормальных условиях молярный объём газа равен 22,4 л/моль.
Формулы для нахождения плотности и относительной плотности
Плотность (ρ) – физическая величина, указывающая на массу определённого вещества, содержащуюся в единице объёма.
Следовательно, формула для её вычисления имеет вид:
ρ=m/V
Помимо основной, существует формула для нахождения плотности газа при нормальных условиях, где молярная масса делится на молярный объём газа при н.у.:
ρ=M/VM
Относительная плотность (D) газов – величина, указывающая насколько одно вещество тяжелее или легче другого. Вычисляется она отношением молярных масс газов:
D = M(1) / M(2)
Например, условием было найти плотность газа по водороду. Решение будет иметь вид: D = M(газа)/M(H2) = M(газа)/2. Относительная плотность является безразмерной величиной.
Формулы для нахождения концентрации
Молярная концентрация (С) – отношение количества растворённого вещества к объёму раствора. Единица измерения – моль/л. Молярная концентрация вычисляется по формуле:
С = n/V
Массовая концентрация чаще всего называется титром (Т). Это отношение массы растворённого вещества к объёму раствора. Единица измерения — г/л.
Это отношение массы растворённого вещества к объёму раствора. Единица измерения — г/л.
T = m/V
Массовая доля (ω) – это один из вариантов выражения концентрации. С её помощью можно вычислить процентное содержание растворённого вещества в общей массе раствора:
ω = (mр.в./mр-ра) × 100%
По такому же принципу вычисляется массовая доля определённого компонента в смеси:
ω = (mкомпонента / mсистемы) × 100%
Если возникает необходимость найти массовую долю химического элемента в соединении, то нужно относительную атомную массу этого элемента умножить на число атомов в соединении и разделить на молекулярную массу вещества:
ω = (Ar × N) / M
Формулы для нахождения выхода продукта реакции
Под выходом продукта реакции (ᶯ) подразумевается отношение массы (объёма, количества) вещества, полученного на практике, к теоретически возможному (рассчитанному по уравнению реакции). Единица измерения – доля, а проценты — если результат умножить на 100 !
Единица измерения – доля, а проценты — если результат умножить на 100 !
Для его вычисления, в зависимости от условия задачи, используются следующие формулы:
ᶯ=(mпракт./mтеорет.) × 100%
ᶯ=(Vпракт./Vтеорет.) × 100%
ᶯ=(nпракт./nтеорет.) × 100%
Попрактиковать решение задач и знание формул возможно в приложении «ХиШник». Оно содержит в себе каталог заданий, которые, в свою очередь, разделены по темам и уровням сложности. Если вы дали неверный ответ, то приложение не просто уведомит об этом, а предложит правильный алгоритм решения. Также в нём есть раздел для подготовки к ОГЭ и ЕГЭ, в котором собраны типовые задания.
Знание расчётных формул – это ключевой момент при решении задач. Главное, понимать их, а не бездумно заучивать. Так как они будут использоваться не только в школьных задачах, на ЕГЭ и ОГЭ, но и в дальнейшей жизни, даже если ваша профессиональная сфера будет далека от химии.
Формулы для решения задач по химии
Химия формулы для задач
Так как химия наука точная, она неразрывно связана с различного рода вычислениями. Чтобы решать задачи, нужно знать формулы и хорошо в них ориентироваться. Без этих базовых знаний и навыков изучение химии становится невозможным.
Чтобы решать задачи, нужно знать формулы и хорошо в них ориентироваться. Без этих базовых знаний и навыков изучение химии становится невозможным.
Мы собрали для вас основные химические формулы, изучаемые в школьном курсе. Они пригодятся каждому ученику, особенно тем, кто будет сдавать ОГЭ или ЕГЭ по этому непростому, но очень интересному предмету.
Нахождение количества вещества
Первое и основное понятие, которое необходимо усвоить – это Количество вещества, измеряемое в молях и обозначающееся латинской буквой «n». Для его нахождения нужно основываться на условии задачи, так как вычислить количество вещества можно по трём формулам:
1) По массе. N=m/M — Массу вещества (в граммах) разделить на его молярную массу (в г/моль).
2) По объёму. N=V/Vm — Отношением объёма вещества к его молярному объёму (используется для газов).
3) По числу молекул. N=N/NA – Число молекул вещества делённое на число Авогадро. Число Авогадро (NA) – физическая величина, указывающая на число молекул, содержащихся в 1 моле вещества, и численно равная 6,0221 * 10 23 моль -1 .
Формулы для нахождения массы
Массу вещества можно найти несколькими способами:
1. Умножив количество вещества на молярную массу: M (г) = n (моль)×M (г/моль).
2. Произведением объёма раствора и его плотности:
3. Перемножив массовую долю с массой раствора: M = m(р-ра) × ω.
Молярная масса (М) – это масса одного моля вещества. Вычисляется она следующим образом: посредством сложения атомных масс элементов, из которых состоит вещество, получаем относительную молекулярную массу. Молярная масса численно равна относительной молекулярной массе, но имеет размерность «г/моль». Также молярную массу можно найти с помощью отношения массы вещества к его количеству:
Формулы для нахождения объёма
Для вычисления объёма того или иного вещества можно воспользоваться одной из формул:
1. Объём раствора находится как отношение массы раствора к его плотности:
2. Объём газа равен отношению его количества вещества к молярному объёму:
Объём газа равен отношению его количества вещества к молярному объёму:
Молярный объём (VM) – объём, который занимает 1 моль вещества при определённых показателях давления и температуры. Находится при делении молярной массы вещества на его плотность:
При нормальных условиях молярный объём газа равен 22,4 л/моль.
Формулы для нахождения плотности и относительной плотности
Плотность (ρ) – физическая величина, указывающая на массу определённого вещества, содержащуюся в единице объёма.
Помимо основной, существует формула для нахождения плотности газа при нормальных условиях, где молярная масса делится на молярный объём газа при н. у.:
Относительная плотность (D) газов – величина, указывающая насколько одно вещество тяжелее или легче другого. Вычисляется она отношением молярных масс газов:
Например, условием было найти плотность газа по водороду. Решение будет иметь вид: D = M(газа)/M(h3) = M(газа)/2. Относительная плотность является безразмерной величиной.
Относительная плотность является безразмерной величиной.
Формулы для нахождения концентрации
Молярная концентрация (С) – отношение количества растворённого вещества к объёму раствора. Единица измерения – моль/л. Молярная концентрация вычисляется по формуле:
Массовая концентрация чаще всего называется титром (Т). Это отношение массы растворённого вещества к объёму раствора. Единица измерения — г/л.
Массовая доля (ω) – это один из вариантов выражения концентрации. С её помощью можно вычислить процентное содержание растворённого вещества в общей массе раствора:
По такому же принципу вычисляется массовая доля определённого компонента в смеси:
Ω = (mкомпонента / mсистемы) × 100%
Если возникает необходимость найти массовую долю химического элемента в соединении, то нужно относительную атомную массу этого элемента умножить на число атомов в соединении и разделить на молекулярную массу вещества:
Формулы для нахождения выхода продукта реакции
Под Выходом продукта реакции (ᶯ) подразумевается отношение массы (объёма, количества) вещества, полученного на практике, к теоретически возможному (рассчитанному по уравнению реакции). Единица измерения – доля, а проценты — если результат умножить на 100 !
Единица измерения – доля, а проценты — если результат умножить на 100 !
Для его вычисления, в зависимости от условия задачи, используются следующие формулы:
Попрактиковать решение задач и знание формул возможно в приложении «ХиШник». Оно содержит в себе каталог заданий, которые, в свою очередь, разделены по темам и уровням сложности. Если вы дали неверный ответ, то приложение не просто уведомит об этом, а предложит правильный алгоритм решения. Также в нём есть раздел для подготовки к ОГЭ и ЕГЭ, в котором собраны типовые задания.
Знание расчётных формул – это ключевой момент при решении задач. Главное, понимать их, а не бездумно заучивать. Так как они будут использоваться не только в школьных задачах, на ЕГЭ и ОГЭ, но и в дальнейшей жизни, даже если ваша профессиональная сфера будет далека от химии.
Плотность ρ физическая величина, указывающая на массу определённого вещества, содержащуюся в единице объёма.
Okulyk. com
06.09.2017 9:18:41
2017-09-06 09:18:41
Источники:
Https://okulyk. com/materials/formuly-dlja-reshenija-zadach-po-himii/
com/materials/formuly-dlja-reshenija-zadach-po-himii/
Формулы и калькуляторы для решения задач по химии » /> » /> .keyword { color: red; }
Химия формулы для задач
Ежедневно, сами того не замечая, мы на каждом шагу имеем дело с химией. Умывшись и одевшись с утра мы уже имеем дело с рядом химических продуктов и процессов. Вода, мыло, одежда — разные виды продуктов химии. Действие воды, мыла на кожу, реакция тела на теплую одежду — химические процессы. Сегодня, как и тысячи лет назад, мы едим, дышим, плачем, смеемся и независимо от нас в организме совершаются самые разные химические процессы. Химия имеет дело не с вещами, а с веществами, из них состоят вещи, животные и растительные организмы, минералы. Вещество имеет массу, вес, занимает объем, обладает как физическими, так и химическими свойствами. Химия изучает строение, свойства вещества и происходящие с ним в результате химических реакций изменения, законы, которым эти превращения подчиняются.
- аналитическая химия, ее задача — качественный и количественный анализ веществ; физическая химия, исследующая физические явления, химические реакции и их закономерности; биохимия, изучающая на молекулярном уровне химические реакции, происходящие в живых организмах; неорганическая химия, где изучают все элементы (кроме углерода) периодической таблицы Менделеева; органическая химия — исследует все соединения углерода.

Не секрет, что химия многим из нас кажется наукой сложной и далеко не всем понятной. Хотя именно с химией мы ежедневно сталкиваемся на каждом шагу. Окружающий нас мир можно легко представить в виде химических элементов, химических процессов и реакций, ежесекундно происходящих в мире. Многим специалистам приходиться ежедневно решать задачки по химии. Так, врач-диетолог обсчитывает калорийность пищи, врач-косметолог уделяет огромное внимание взаимодействию разных веществ, чтобы предложенное им средство являлось максимально эффективным и безопасным для организма человека. Студентам и учащимся приходиться выполнять довольно сложные лабораторные и контрольные работы, решать многочисленные задачи по химии. Помочь в решении всевозможных задач, связанных с такой достаточно нелегкой, но весьма интересной наукой как химия, сможет предлагаемый нами онлайн калькулятор.
Сегодня без химии и ее знаний невозможно обойтись. Без знания химии тренер не сможет рассчитать количество калория спортсмену, диетолог — расписать рацион питания больному, фармаколог — приготовить раствор, соблюдая нужные пропорции и учитывая принципы взаимодействия веществ и т. д. С помощью онлайн калькулятора вы сможете быстро и правильно определить плотность вещества, находить химические реакции, решать разнообразные химические задачи и уравнения, выполнять различные работы и контрольные по химии, На основе уравнения можно вычислить объем, массу или количество искомых веществ.
д. С помощью онлайн калькулятора вы сможете быстро и правильно определить плотность вещества, находить химические реакции, решать разнообразные химические задачи и уравнения, выполнять различные работы и контрольные по химии, На основе уравнения можно вычислить объем, массу или количество искомых веществ.
Вода, мыло, одежда разные виды продуктов химии.
Infofaq. ru
14.11.2019 5:47:22
2019-11-14 05:47:22
Источники:
Https://infofaq. ru/ximiya
Химия 8 класс Все формулы и определения. Кратко, таблицы, схемы. » /> » /> .keyword { color: red; }
Химия формулы для задач
Химия 8 класс
Все формулы и определения
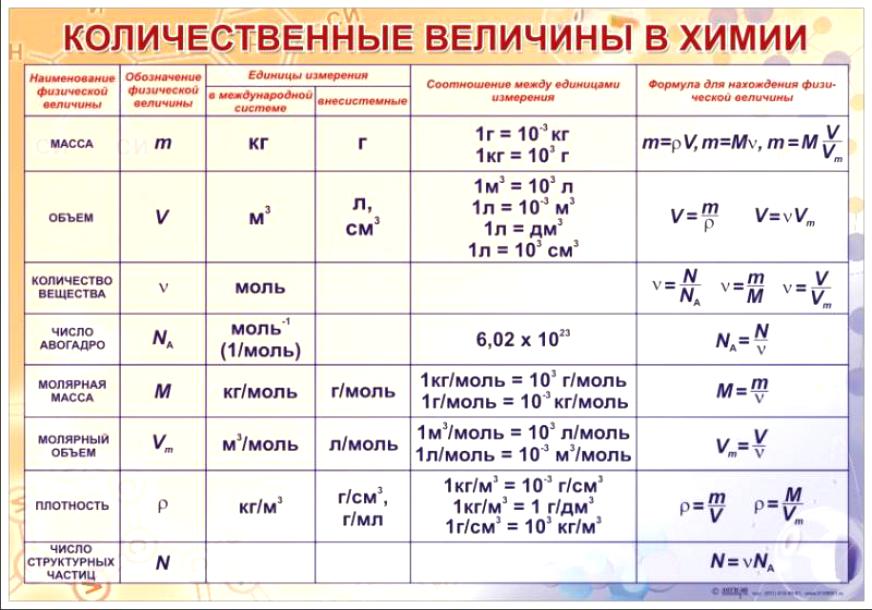
Ключевые слова: Химия 8 класс Все формулы и определения, условные обозначения физических величин, единицы измерения, приставки для обозначения единиц измерения, соотношения между единицами, химические формулы, основные определения, кратко, таблицы, схемы.
1. Условные обозначения, названия и единицы измеренияНекоторых физических величин, используемых в химии
| Физическая величина | Обозначение | Единица измерения |
| Время | T | С |
| Давление | P | Па, кПа |
| Количество вещества | Ν | Моль |
| Масса вещества | m | Кг, г |
| Массовая доля | Ω | Безразмерная |
| Молярная масса | М | Кг/моль, г/моль |
| Молярный объем | V n | М 3 /моль, л/моль |
| Объем вещества | V | М 3 , л |
| Объемная доля | Безразмерная | |
| Относительная атомная масса | A r | Безразмерная |
| Относительная молекулярная масса | M r | Безразмерная |
| Относительная плотность газа А по газу Б | D Б (А) | Безразмерная |
| Плотность вещества | Р | Кг/м 3 , г/см 3 , г/мл |
| Постоянная Авогадро | N A | 1/моль |
| Температура абсолютная | Т | К (Кельвин) |
| Температура по шкале Цельсия | t | °С (градус Цельсия) |
| Тепловой эффект химической реакции | Q | КДж/моль |
 Соотношения между единицами физических величин3. Химические формулы в 8 классе
Соотношения между единицами физических величин3. Химические формулы в 8 классеСхема. Химические формулы в 8 классе
4. Основные определения в 8 классе- Атом — мельчайшая химически неделимая частица вещества. Химический элемент — определённый вид атомов. Молекула — мельчайшая частица вещества, сохраняющая его состав и химические свойства и состоящая из атомов. Простые вещества — вещества, молекулы которых состоят из атомов одного вида. Сложные вещества — вещества, молекулы которых состоят из атомов разного вида. Качественный состав вещества показывает, из атомов каких элементов оно состоит. Количественный состав вещества показывает число атомов каждого элемента в его составе. Химическая формула — условная запись качественного и количественного состава вещества посредством химических символов и индексов.
 Атомная единица массы (а. е.м.) — единица измерения массы атома, равная массы 1/12 атома углерода 12 С. Моль — количество вещества, в котором содержится число частиц, равное числу атомов в 0,012 кг углерода 12 С. Постоянная Авогадро (Na = 6*10 23 моль -1 ) — число частиц, содержащихся в одном моле. Молярная масса вещества (М) — масса вещества, взятого в количестве 1 моль. Относительная атомная масса элемента АR — отношение массы атома данного элемента m0 к 1/12 массы атома углерода 12 С. Относительная молекулярная масса вещества МR — отношение массы молекулы данного вещества к 1/12 массы атома углерода 12 С. Относительная молекулярная масса равна сумме относительных атомных масс химических элементов, образующих соединение, с учётом числа атомов данного элемента. Массовая доля химического элемента Ω(Х) показывает, какая часть относительной молекулярной массы вещества X приходится на данный элемент.
Атомная единица массы (а. е.м.) — единица измерения массы атома, равная массы 1/12 атома углерода 12 С. Моль — количество вещества, в котором содержится число частиц, равное числу атомов в 0,012 кг углерода 12 С. Постоянная Авогадро (Na = 6*10 23 моль -1 ) — число частиц, содержащихся в одном моле. Молярная масса вещества (М) — масса вещества, взятого в количестве 1 моль. Относительная атомная масса элемента АR — отношение массы атома данного элемента m0 к 1/12 массы атома углерода 12 С. Относительная молекулярная масса вещества МR — отношение массы молекулы данного вещества к 1/12 массы атома углерода 12 С. Относительная молекулярная масса равна сумме относительных атомных масс химических элементов, образующих соединение, с учётом числа атомов данного элемента. Массовая доля химического элемента Ω(Х) показывает, какая часть относительной молекулярной массы вещества X приходится на данный элемент.
АТОМНО-МОЛЕКУЛЯРНОЕ УЧЕНИЕ
1. Существуют вещества с молекулярным и немолекулярным строением.
2. Между молекулами имеются промежутки, размеры которых зависят от агрегатного состояния вещества и температуры.
3. Молекулы находятся в непрерывном движении.
4. Молекулы состоят из атомов.
6. Атомы характеризуются определённой массой и размерами.
При физических явлениях молекулы сохраняются, при химических, как правило, разрушаются. Атомы при химических явлениях перегруппировываются, образуя молекулы новых веществ.
ЗАКОН ПОСТОЯНСТВА СОСТАВА ВЕЩЕСТВА
Каждое химически чистое вещество молекулярного строения независимо от способа получения имеет постоянный качественный и количественный состав.
ВАЛЕНТНОСТЬ
Валентность — свойство атома химического элемента присоединять или замещать определённое число атомов другого элемента.
ХИМИЧЕСКАЯ РЕАКЦИЯ
Химическая реакция — явление, в результате которого из одних веществ образуются другие. Реагенты — вещества, вступающие в химическую реакцию. Продукты реакции — вещества, образующиеся в результате реакции.
Реагенты — вещества, вступающие в химическую реакцию. Продукты реакции — вещества, образующиеся в результате реакции.
Признаки химических реакций:
1. Выделение теплоты (света).
2. Изменение окраски.
3. Появление запаха.
4. Образование осадка.
5. Выделение газа.
- Химическое уравнение — запись химической реакции с помощью химических формул. Показывает, какие вещества и в каком количестве вступают в реакцию и получаются в результате реакции.
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ
Масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции. В результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка.
Конспект урока «Химия 8 класс Все формулы и определения». Выберите дальнейшее действие:
Ключевые слова: Химия 8 класс Все формулы и определения, условные обозначения физических величин, единицы измерения, приставки для обозначения единиц измерения, соотношения между единицами, химические формулы, основные определения, кратко, таблицы, схемы.
Условные обозначения, названия и единицы измерения некоторых физических величин, используемых в химии
Атомы при химических явлениях перегруппировываются, образуя молекулы новых веществ.
Uchitel. pro
17.04.2020 22:44:42
2020-04-17 22:44:42
Источники:
Https://uchitel. pro/%D1%85%D0%B8%D0%BC%D0%B8%D1%8F-8-%D0%BA%D0%BB%D0%B0%D1%81%D1%81-%D0%B2%D1%81%D0%B5-%D1%84%D0%BE%D1%80%D0%BC%D1%83%D0%BB%D1%8B/
“Решение задач на вывод формул органических веществ»
Интегрированный урок
(математика + химия),
11-й класс
Тема:
“Решение задач на вывод формул органических веществ»
Тип урока: комбинированный.
Вид урока: интегрированный.
Задачи:
- Способствовать развитию умений выводить формулы веществ через массовую долю химических элементов, с использованием относительной плотности газов, применяя основное свойство пропорции.

- Способствовать развитию умений работать по алгоритму, развитию навыков самообразования, логического мышления, устной и письменной речи учащихся.
- Формировать целостную систему знаний, воспитывать ответственность при работе в коллективе, исполнительность.
Формы учебной деятельности: коллективная и групповая.
Технические средства и оборудование: мультимедийная презентация, компьютер, мультимедийный экран, периодическая система Д. И. Менделеева, раздаточные листы на печатной основе (задачи, алгоритмы)
План урока:
- Организационный момент;
- Подготовка к усвоению нового учебного материала;
- Усвоение новых знаний;
- Закрепление новых знаний;
- Подведение итогов урока;
- Информация о домашнем задании, инструкция его выполнении.
- Презентация урока
ХОД УРОКА
I. Организационный момент
II. Подготовка к усвоению нового учебного материала
Подготовка к усвоению нового учебного материала
Сообщение о связи химии с математикою:
Учитель математики: Природа – единое целое, характеризующееся общими процессами и управляемая общими законами. Математические методы (решение систем линейных однородных уравнений, исследование функций и построение графиков) находят широкое применение в таких понятиях химии как протекание химических реакций; при решении химических задач.
Учитель химии сообщает учащимся план урока, цель и задачи:
Учитель химии: Химические процессы – это сложнейшие реакции, которые требуют огромных вычислений. И сегодня на уроке мы предлагаем вам решение химических задач с помощью математики, оформление результатов решения в виде программного продукта: презентации,.
Учитель математики: Для решения задач вспомним, что такое отношение двух чисел? (Частное двух чисел)
– Что показывает отношение? (Во сколько раз одно число больше или меньше другого или какую часть одно число составляет от другого)
– Что такое пропорция (Это равенство двух отношений)
Учащийся записывает пропорцию в общем виде на доске:– Как называются члены пропорции? (а и d – крайние, b и c – средние)
– Сформулируйте основное свойство пропорции (Произведение крайних членов равно произведению средних членов a • d = b • c)
– Как найти неизвестный член пропорции?
a : x = b : c
xb = ac
Учитель химии: Для решения задач необходимо вспомнить:
– Что такое массовая доля элемента? (Это отношение относительной атомной массы элемента, умноженной на число его атомов в молекуле, к относительной молекулярной массе вещества. )
)
– Как определить массовую долю элемента?
(– Как определить количество вещества? или)
– Что такое относительная молекулярная масса? (Относительная молекулярная масса Mr – число, показывающее во сколько раз реальная масса молекулы, выраженная в граммах, больше массы 1/12 части атома элемента углерода, выраженной тоже в граммах.)
– Как определить относительную молекулярную массу углеводорода, зная относительную плотность по водороду или воздуху? (Mr (вещества) = D(H2) • Mr (H2) или Mr (вещества) = D(возд) • Mr (возд)).
Учитель математики: Решим устные упражнения:
- Найти отношение: 0,25 к 0,55; 9,1 к 0,07; 12,3 к 3; 1 кг к 250 г; 0,1 кг к 0,1 г.
- Найти неизвестный член пропорции: 5 : х = 4: 12;
- Определите Мr углеводорода, если D(возд) = 2, D(H2) = 15.
- Определите Mr: СН3, С2Н6, С2Н2.

- Определите количество вещества, если известна массовая доля углерода 80%, водорода 20% .
III. Усвоение новых знаний
Учитель химии: Решим задачу на определение молекулярной формулы вещества на основании результатов количественного анализа (массовой доли элементов) и относительной плотности.
Задача 1.
Найдите молекулярную формулу углеводорода, содержание углерода в котором 80%, а водорода – 20%, относительная плотность по водороду равна 15.
1-й способ решения (соотношение атомов).
На каждой парте алгоритм решения задачи.
Алгоритм решения задачи
Задача 1.
Найдите молекулярную формулу углеводорода, содержание углерода в котором 80%, а водорода – 20%, относительная плотность по водороду равна 15.
1 – й способ решения (соотношение атомов).
Алгоритм решения задачи
- 1.
 Внимательно прочитайте условие задачи и кратко запишите его простейшую формулу
Внимательно прочитайте условие задачи и кратко запишите его простейшую формулу
2. Определите соотношение атомов в молекуле, разделив массовые доли каждого из элементов на их относительные атомные массы.
3. Установите соотношение атомов
4. Определите относительную молекулярную массу углеводорода
5. Установите, во сколько раз истинная относительная молекулярная масса углеводорода больше относительной молекулярной массы простейшей его молекулы
6. Напишите истинную формулу углеводорода, увеличив число атомов каждого элемента
7. Запишите ответ
Решение:
1. Внимательно прочитайте условие задачи и кратко запишите его
Дано:
D (H2) = 15
_____________
Mr (СхНy) – ?
2. Определите соотношение атомов в молекуле, разделив массовые доли каждого из элементов на их относительные атомные массы (учитель математики)
3. Установите соотношение атомов
Установите соотношение атомов
4. Напишите простейшую формулу (учитель химии)
Учитывая соотношение можно записать – СН3
5. Определите относительную молекулярную массу углеводорода
Mr (CH3) = 15
Mr (СхНy) = D H2 • Mr H2 = 15 • 2 = 30
6. Установите, во сколько раз истинная относительная молекулярная масса углеводорода больше относительной молекулярной массы простейшей его молекулы
7. Напишите истинную формулу углеводорода, увеличив число атомов каждого элемента в 2 раза СН3 – С2Н6
8. Запишите ответ
Ответ: молекулярная формула углеводорода – С2Н6 (этан).
Учитель математики:
Мы можем решить эту задачу вторым способом способом пропорции.
На каждой парте алгоритм решения задачи).
Алгоритм решения задачи
Задача 1.
Найдите молекулярную формулу углеводорода, содержание углерода в котором 80%, а водорода – 20%, относительная плотность по водороду равна 15.
2 – й способ решения (способ пропорции).
1. Внимательно прочитайте условие задачи и кратко запишите его
D (H2) = 15
______________
Mr (СхНy) – ?
2. Определите массу водорода, содержащегося в веществе (составьте на основании логического рассуждения пропорцию и решите ее)
Процентное содержание элементов в веществе есть не что иное, как отношение массы атомов данного элемента к массе атомов второго элемента и т.д., т.е.
На 80 мас.ч. углерода приходится 20 мас.ч. водорода.
А на 1 моль атомов углерода, масса которого m(C) = 12 г (М(С) = 12 г/моль), приходится х г водорода.
Составьте пропорцию:
80 : 12 = 20 : х,
Это составляет 3 моль атомов водорода (М (Н) = 1 г/моль).
3. Установите соотношение атомов элементов в молекуле данного вещества, приведя их значения к целым числам n (C) : n (H) = 1 : 3
4. Напишите простейшую формулу вещества и рассчитайте по ней относительную молекулярную массу СН3
Mr (Ch4) = 15
5. Определите истинную относительную молекулярную массу Mr (СхНy) = D H2 • Mr H2 = 15 • 2 = 30
Определите истинную относительную молекулярную массу Mr (СхНy) = D H2 • Mr H2 = 15 • 2 = 30
6. Установите, во сколько раз истинная относительная молекулярная масса углеводорода больше относительной молекулярной массы простейшей его молекулы
7. Напишите истинную формулу углеводорода, увеличив число атомов каждого элемента в 2 раза СН3 – С2Н6
8. Напишите ответ
Ответ: молекулярная формула вещества С2Н6 – этан.
Учитель химии: Существует и третий способ решения подобных задач.
3-й способ решения (по формуле расчета массовой доли элемента в веществе)
На каждой парте алгоритм решения задачи
Задача 1.
Найдите молекулярную формулу углеводорода, содержание углерода в котором 80%, а водорода – 20%, относительная плотность по водороду равна 15.
1. Внимательно прочитайте условие задачи и кратко запишите его
Внимательно прочитайте условие задачи и кратко запишите его
Дано:
D (H2) = 15
____________
Mr (СхНy) – ?
2. Запишите формулы расчета массовой доли элемента вещества.;
Mr = 2 . D h3;
3. Все данные внесите в формулу
4. Установите соотношение атомов
n(C) : n(H) = 2 : 6
5. Напишите формулу вещества С2Н6
6. Запишите ответ
Ответ: молекулярная формула вещества С2Н6 – этан.
Учитель химии: Эту задачу можно решить используя ещё один способ – нахождению доли части от целого.
1. Mr = 2 • D h3
Mr = 2 • 15 = 30
2. По относительной молекулярной массе (целое) и массовой доле элемента в веществе (доля части от целого) найдите массу элемента в веществе (часть от целого):
b = C • массовая доля части.
На долю углерода приходится: 30 • 0,8 = 24
На долю водорода приходится: 30 • 0,2 = 6
3. Число атомов элементов в молекуле газообразного вещества определяют как частное от деления полученных чисел на относительные атомные массы соответствующих элементов:
Число атомов элементов в молекуле газообразного вещества определяют как частное от деления полученных чисел на относительные атомные массы соответствующих элементов:
n (C) = 24 : 12 = 2
n (Н) = 6 : 1 = 1
4. Установите соотношение атомов n(C) : n(H) = 2 : 6
5. Запишите формулу вещества С2Н6
6. Запишите ответ
Ответ: молекулярная формула вещества С2Н6 – этан.
Учитель математики: Я хочу предложить вам ещё один математический способ решения подобных задач
1. По относительной плотности вычисляем относительную молекулярную массу вещества:
Mr (CH3) = 15
Mr (СхНy) = D H2 • Mr H2 = 15 • 2 = 30
2. Предположим, что углеводород имеет формулу СхНу, тогда, подставим относительные атомные массы элементов, получим:
12х + у = 30.
3. Общая формула углеводорода – СхH2х+2.
Для углеводородов значение у будет равно или меньше (в случае непредельных углеводородов) значения 2х + 2:
4. Из уравнения находим значение у = 30 – 12х, подставляем его в неравенство и получаем:
Если х = 2, то у = 2 ? 2 + 2 = 6.
Если х >2.
Например, если х = 3, то 12х + у = 36 + у > 30, что не соответствует уравнению 12х + у = 30.
у = 30 – 12х
12х + 2х + 2 = 30
14х = 30 – 2
14х = 28
х = 28 : 14
х = 2, тогда
если х = 2, то 2х + 2 = 2 . 2 + 2 = 6.
5. Формула углеводорода: С2Н6
IV. Закрепление новых знаний
(работа по группам)
На каждой парте листы с задачами.
Задачи для самостоятельного решения дома.
- В углеводороде массовая доля углерода равна 84%. Относительная плотность паров углеводорода по воздуху равна 3,45. Определите эмпирическую формулу углеводорода.

- Массовая доля углерода в углеводороде равна 85,71%, водорода – 14,29%. Относительная плотность углеводорода по азоту равна 1. Выведите молекулярную формулу углеводорода, напишите его структурную формулу.
- Массовая доля водорода в углеводороде 7,7%. Молярная масса углеводорода 78 г/моль. Выведите формулу вещества.
- В углеводороде массовые доли углерода и водорода соответственно равны 82,76 и 17,24%. Относительная плотность углеводорода по воздуху равна 2,0. выведите его молекулярную формулу.
- Относительная плотность алкана по воздуху равна 1,52. Выведите его молекулярную формулу.
1 группа – решение задачи 1 способом (соотношение атомов).
2 группа – решение задачи 2 способом (способ пропорции).
3 группа – решение задачи 3 способом (по формуле расчета массовой доли элемента в веществе).
4 группа – решение задачи 4 способом (по нахождению доли части от целого).
5 группа – решение задачи 5 способом (математический).
V. Подведение итогов
Подведение итогов
Учитель химии:
Химия тесно связана с математикой. Сегодня на уроке мы познакомились, как знания некоторых разделов математики необходимы для умения решать задачи по химии.
VI. Домашнее задние Каждой группе оформить решение задач в виде презентаций, статьи.
Все формулы по химии для решения задач: Основные Химические формулы для решения задач. — ЭкоДом: Дом своими руками
Содержание
Основные Химические формулы для решения задач.
| № | Количественные характеристики вещества | Обозначение | Единицы измерения | Формула для расчета |
|---|---|---|---|---|
| 1 | Плотность вещества | ρ | кг/м³ | ρ = m / V(Массу делим на объем вещества) |
| 2 | Относительная атомная масса элемента | Аr | — | Ar = ma / u см. в периодической система химических элементов |
| 3 | Атомная единица массы | u а.  е.м. е.м. | кг | u = 1/12 * ma (12C) const = 1.66*10-27 |
| 4 | Масса атома (абсолютная) | ma | кг | ma = Ar * u |
| 5 | Относительная молекулярная (формульная) масса вещества | Mr | — | Mr (AxBy)=m(AB) / u Mr(AxBy)=x*Ar(A) + y*Ar(B) |
| 6 | Масса молекулы (формульной единицы) | m M | кг | mM = Mr*u |
| 7 | Количество вещества | n | моль | n=m/M n=N/NA n=V/VM |
| 8 | Молярная масса (масса 1 моль вещества) | M | г/моль | M=m/n M=Mr M=Ar (для простых веществ) |
| 9 | Масса вещества | m | г (кг) | m=M*n m=ρ*V |
| 10 | Число структурных единиц | N | атомов, молекул, ионов, частиц, формульных единиц (Ф. Е.) | N=NA*n |
| 11 | Молярный объем — число 1 моль ГАЗООБРАЗНОГО вещества в нормальных условиях (н. у.) у.) | VM | л/моль | const=22,4 |
| 12 | Объем газа при н.у. | V | л | V=VM*n V=m/ρ |
| 13 | Постоянная Авогадро | NA | частиц/моль | const=6,02*1023 |
| 14 | Массовая доля вещества (омега) | ωЭ/В | % | ωЭ/В = (Ar(э) * k) / Mr(В) |
| Формула | Название кислоты | Формула кислотного остатка | Название кислотного остатка |
|---|---|---|---|
| HF | Фтороводород, плавиковая | F— | Фторид |
| HCl | Хлороводород, соляная | Cl— | Хлорид |
| HBr | Бромоводород | Br— | Бромид |
| HI | Йодоводород | I— | Йодид |
| h4S | Сероводород | S2- | Сульфид |
| HCN | Циановодородная | CN— | Цианид |
| HNO2 | Азотистая | NO2— | Нитрит |
| HNO3 | Азотная | NO3— | Нитрат |
| h5PO4 | Ортофосфорная | PO43- | Фосфат |
| h5AsO4 | Мышьяковая | AsO43- | Арсенат |
| h4SO3 | Сернистая | SO32- | Сульфит |
| h4SO4 | Серная | SO42- | Сульфат |
| h4CO3 | Угольная | CO32- | Карбонат |
| h4SiO3 | Кремниевая | SiO32- | Силикат |
| h4CrO4 | Хромовая | CrO42- | Хромат |
| h4Cr2O7 | Дихромовая | Cr2O72- | Дихромат |
| HMnO4 | Марганцовая | MnO4— | Перманганат |
| HClO | Хлорноватистая | ClO— | Гипохлорит |
| HClO2 | Хлористая | ClO2— | Хлорит |
| HClO3 | Хлорноватая | ClO3— | Хлорат |
| HClO4 | Хлорная | ClO4— | Перхлорат |
| HCOOH | Метановая, муравьиная | HCOO— | Формиат |
| Ch5COOH | Этановая, уксусная | Ch5COO— | Ацетат |
| h5C2O4 | Этандиовая, щавелевая | C2O42- | Оксалат |
Нажмите на картинку для увеличения
Формулы для решения задач по химии
от 01. 01.2017 года
01.2017 года
Настоящее пользовательское (лицензионное) соглашение (далее – «Соглашение»)
заключается между Обществом с ограниченной ответственностью «АЛЕКТА» (далее –
«Лицензиар»), и Пользователем (физическим лицом, выступающем в роли конечного
потребителя Продукта) совместно именуемые «Стороны».
Пожалуйста, внимательно ознакомьтесь с текстом настоящего Соглашения. Оно
представляет собой публичную оферту и, после его принятия Вами, образует соглашение
между Вами (Пользователем) и Лицензиаром о предмете и на условиях, изложенных в
тексте Соглашения.
Принимая настоящее Соглашение, Вы соглашаетесь с положениями, принципами, а
также соответствующими условиями лицензионного соглашения, изложенными ниже.
1. ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
1.1. Программный продукт — экземпляры программы для ЭВМ «ХиШник», состоящей
из Серверной части (свидетельство о государственной регистрации базы данных
№2014621526) и Клиентского приложения (свидетельство о государственной
регистрации программы для ЭВМ № 2014661592), права на использование которой
предоставляются в соответствии с настоящим Соглашением.
1.2. Серверная часть — часть Программного продукта, размещенная в сети Интернет и
используемая для хранения данных в базе данных Лицензиара под наименованием
«ХиШник» (далее также – «база данных»), а также для хранения, обработки,
передачи данных Пользователя между базой данных и клиентским приложением.
1.3. Клиентское приложение — часть Программного продукта, устанавливаемая на
компьютер Пользователя или на мобильное устройство Пользователя и
позволяющая получить доступ к базе данных Лицензиара, а также данным
Пользователя, хранящимся в памяти сервера Лицензиара.
1.4. Пользовательское (лицензионное) соглашение – текст настоящего Соглашения со
всеми дополнениями, изменениями, приложениями к нему, размещенный на сайте
Лицензиара и доступный в сети интернет по адресу: http://www.hishnik-school.ru
1. 5. Заключение Пользовательского (лицензионного) соглашения (акцепт
публичной оферты) — полное и безоговорочное принятие условий настоящего
Соглашения Пользователем путем совершения Пользователем одного (или
нескольких) из следующих действий:
прохождение регистрации и (или) авторизации на Сайте Лицензиара в
установленном им порядке;
внесение платежа за предоставление права на использование Программного
продукта;
начало использования Пользователем Программного продукта в любой иной
форме.
1.6. Лицензиар — сторона в настоящем Соглашении, обладающая исключительным
правом на Программный продукт и предоставляющая по настоящему Соглашению
Пользователю право использования Программного продукта, в пределах и
способами, указанными в настоящем Соглашении.
1. 7. Пользователь — физическое лицо, которое устанавливает на компьютер или
мобильное устройство Клиентское приложение и использует его.
1.8. Неисключительная лицензия — лицензионный договор, предусматривающий
предоставление права использования Программного продукта с сохранением за
Лицензиаром права заключения лицензионного договора с другими лицами.
1.9. Роль – набор функций, которые доступны в Программном продукте Пользователю.
Настоящим Соглашением предусмотрены следующие роли:
1.9.1. Администратор — сотрудник образовательного учреждения,
осуществляющий регистрацию и предоставление доступа к Программному
продукту Пользователям – участникам образовательного процесса в
образовательном учреждении.
1.9.2. Преподаватель – сотрудник образовательного учреждения, организующий
и осуществляющий образовательный процесс посредством использования
функций Программного продукта.
1.9.3. Репетитор – преподаватель, дающий частные уроки, может проводить как
индивидуальные, так и групповые занятия посредством использования
функций Системы вне рамок Образовательного учреждения.
1.9.4. Учащийся – обучающийся в Образовательном учреждении и (или) вне его,
получающий и проверяющий свои знания посредством Системы.
1.10. Профиль — запись в базе данных, содержащая идентифицирующие сведения о
Пользователе и его роли.
1.11. Демонстрационный режим – режим использования Программного продукта для
целей ознакомления с его функциональными возможностями.
1.12. Продуктивный режим – режим использования Программного продукта для целей
применения в образовательном процессе.
1.13. Регистрационный ключ — набор цифр и букв, посредством которого Пользователь
получает право использования Программного продукта в Продуктивном режиме с
полным доступом к Серверной части.
1.14. Логин – уникальный идентификатор Пользователя в базе данных.
1.15. Пароль – набор цифр и букв, посредством которого и совместно с Логином
Пользователь получает доступ в Клиентское приложение Программного продукта.
1.16. Интернет сайт Лицензиара — http://www.hishnik-school.ru.
1.17. Контент — все объекты, размещенные на Сайте и в Программном продукте, в том
числе элементы дизайна, текст, графические изображения, иллюстрации, видео,
скрипты, программы, музыка, звуки и другие объекты и их подборки.
2. ПРЕДМЕТ СОГЛАШЕНИЯ
2.1. Лицензиар предоставляет Пользователю право использования Программного
продукта «ХиШник» на условиях простой (неисключительной) лицензии в пределах
и способами, указанными в настоящем Соглашении, а Пользователь обязуется
уплатить Лицензиару вознаграждение за предоставление права использования
Программного продукта в соответствии с условиями настоящего Соглашения.
2.2. Лицензиар гарантирует, что он является правообладателем исключительных прав на
Программный продукт и имеет права на заключение Соглашения. Лицензиару в
Лицензиару в
настоящий момент в соответствии с тем знанием, которым он обладает, не известны
права третьих лиц, нарушаемые данным Соглашением.
2.3. Пользователь не вправе полностью или частично предоставлять (передавать) права
третьим лицам, полученные им по Соглашению, в том числе продавать,
тиражировать, копировать Программный продукт, предоставлять доступ третьим
лицам, отчуждать иным образом, в т.ч. безвозмездно, без получения на все
вышеперечисленные действия предварительного письменного согласия Лицензиара.
2.4. Соглашение предоставляет Пользователю право использования Программного
продукта с сохранением за Лицензиаром права выдачи лицензий другим лицам.
Пользователь может использовать экземпляр Программного продукта только в
пределах тех прав и теми способами, которые предусмотрены Соглашением.
Предоставляемое Пользователю Лицензиаром право на использование
Программного продукта действует в течение срока действия Соглашения.
2.5. Программный продукт «ХиШник», состоящий из Серверной части и Клиентского
приложения, представляет собой программу для ЭВМ, предназначенную для
осуществления образовательного процесса.
2.6. Право использования Программного продукта (неисключительная лицензия),
предоставляемое Пользователю в соответствии с настоящим Соглашением,
включает право на использование Программного продукта в двух режимах:
2.6.1. Демонстрационный режим, ограниченный правом установки на компьютер
или мобильное устройство, запуска, настройки Клиентского приложения и
ограниченного доступа к Серверной части, для целей ознакомления с
функциональными возможностями Программного продукта.
2.6.2. Продуктивный режим, ограниченный правом установки на компьютер или
мобильное устройство, запуска, настройки Клиентского приложения и
полного доступа к Серверной части, для целей применения Программного
продукта в образовательном процессе.
2.7. Право использования Программного продукта предоставляется:
2. 7.1. В демонстрационном режиме — с момента установки Клиентского приложения
7.1. В демонстрационном режиме — с момента установки Клиентского приложения
на компьютер или мобильное устройство.
2.7.2. В продуктивном режиме — с момента поступления денежных средств на счет
Лицензиара.
2.8. Права на использование Программного продукта считаются предоставленными
Пользователю:
2.8.1. В демонстрационном режиме — в момент установки Клиентского приложения
на компьютер или мобильное устройство.
2.8.2. В продуктивном режиме — в момент направления Пользователю на
электронную почту письма с регистрационным ключом.
2.9. Право использования Программного продукта предоставляется как на территории
Российской Федерации, так и на территории всех иных стран мира, если не
противоречит национальному законодательству этих стран.
2.10. Требования к компьютерам (оборудованию), необходимому для функционирования
Клиентского приложения размещены в сети Интернет на сайте Лицензиара.
3. СТОИМОСТЬ И ПОРЯДОК ОПЛАТЫ
3. 1. Размер вознаграждения Лицензиара за предоставление Пользователю прав на
1. Размер вознаграждения Лицензиара за предоставление Пользователю прав на
продуктивное использование Программного продукта размещен на Сайте
Лицензиара.
3.2. Вознаграждение Лицензиара за предоставление прав продуктивного использования
Программного продукта не облагаются НДС на основании подпункта 26 пункта 2
статьи 149 Налогового кодекса РФ.
3.3. Оплата предоставленных прав за продуктивное использование Программного
продукта по настоящему Соглашению производится Пользователем в форме
ежегодных платежей.
3.4. Способ оплаты по Соглашению: безналичное перечисление Пользователем
денежных средств в валюте Российской Федерации (рубль) на расчетный счет
Лицензиара способами, обозначенными на Сайте Лицензиара. При этом обязанность
Пользователя в части оплаты вознаграждения по Соглашению считается
исполненной со дня зачисления денежных средств банком на счет Лицензиара.
3.5. Лицензиар имеет право на одностороннее изменение условий и размера
вознаграждения по настоящему Соглашению. Актуальный размер вознаграждения
Актуальный размер вознаграждения
публикуется на Сайте Лицензиара.
4. СРОК ДЕЙСТВИЯ СОГЛАШЕНИЯ
4.1. Настоящее Соглашение вступает в силу с момента его заключения в соответствии с
п.2.7.
4.2. Срок предоставления права продуктивного использования Программного продукта в
соответствии с Соглашением составляет 1 (Один) год с момента авторизации
Пользователя посредством Регистрационного ключа. Соглашение считается
заключенным на тех же условиях на новый срок, равный 1 (Одному) году, при
условии осуществления Пользователем полной оплаты за продление права
продуктивного использования Программного продукта. Количество пролонгаций не
ограничивается.
4.3. Предоставление права демонстрационного использования Программного продукта
не ограничен по сроку.
4.4. Расторжение настоящего Соглашения возможно в соответствии с условиями,
указанным в действующем законодательстве РФ.
5. ПРАВА И ОБЯЗАННОСТИ СТОРОН
5.1. Пользователь обязуется:
5. 1.1. Соблюдать права Лицензиара на Программный продукт и не использовать
1.1. Соблюдать права Лицензиара на Программный продукт и не использовать
Программный продукт иными способами кроме тех, что предусмотрены
настоящим Соглашением.
5.1.2. Не предпринимать попыток получения исходного кода Программного
продукта для дальнейшего его использования, а также не извлекать материалы
базы данных.
5.1.3. Своевременно уплачивать Лицензиару вознаграждение за предоставление
Пользователю права продуктивного использования Программного продукта в
порядке и сроки, установленные настоящим Соглашением.
5.1.4. Указывать достоверную информацию, в том числе свой адрес электронной
почты и иные данные, запрашиваемые Лицензиаром. При этом в случае
указания Пользователем недостоверной информации, все возможные риски,
которые могут возникнуть в связи с выполнением настоящего Соглашения,
Пользователь принимает на себя.
5.1.5. Строго придерживаться и не нарушать условий Соглашения, а также
обеспечить конфиденциальность коммерческой и технической информации
Лицензиара.
5.1.6. Не устанавливать Программный продукт на компьютерах (оборудованиях), не
соответствующих техническим требованиям для функционирования
Программного продукта.
5.1.7. Заботиться о том, чтобы права Лицензиара на Программный продукт не были
нарушены третьими лицами на территории действия настоящего Соглашения,
и обязан сообщить Лицензиару обо всех ставших ему известными
нарушениях.
5.2. Пользователь вправе:
5.2.1. Использовать Программный продукт только посредством установки (записи)
Клиентского приложения Программного продукта на компьютер или
мобильное устройство и его настройки для осуществления ознакомительного
или образовательного процесса с помощью базы данных.
5.2.2. Использовать Программный продукт для любых целей Пользователя, за
исключением ограничений, определенных Соглашением.
5.3. Лицензиар обязуется:
5.3.1. Обеспечить технические условия функционирования Серверной части и
Клиентского приложения для использования Программного продукта
Пользователем, в том числе обеспечить возможность получения и/или
предоставить дистрибутив (установочные файлы) Клиентского приложения, с
помощью которого осуществляется использование Программного продукта.
5.3.2. Защищать данные Пользователя, которые стали известны Лицензиару в связи
с исполнением Сторонами своих обязательств в соответствии с настоящим
Соглашением.
5.3.3. Уведомлять Пользователя о невозможности использования Программного
продукта в связи с выполнением сервисных работ не менее чем за 48 (Сорок
восемь) часов путем отправки сообщения на электронную почту, указанную
при регистрации.
5.3.4. Воздерживаться от каких-либо действий, способных затруднить
осуществление Пользователя предоставленного ему права использования
Программного продукта в установленных Соглашением пределах.
5.3.5. Предоставлять новые версии (обновления) Программного продукта путем их
размещения в сети Интернет на сайте Лицензиара либо в системе Google Play
с возможностью скачивания.
5. 3.6. Информировать Пользователя о новых версиях (обновлениях) Программного
продукта, посредством направления уведомления на адрес электронной почты
Пользователя, указанный при регистрации и (или) авторизации на Сайте
Лицензиара.
5.3.7. Обеспечивать круглосуточный прием обращений в Службу поддержки по
адресу электронной почты: [email protected]
5.3.8. Осуществлять обработку поступивших обращений и консультации через
Службу поддержки, в период с 5:00 до 14:00 по московскому времени с
понедельника по пятницу, за исключением выходных и праздничных дней.
5.4. Лицензиар вправе:
5.4.1. Производить сервисные работы, которые могут повлечь перерывы в работе
Клиентского приложения.
5.4.2. В случае нарушения Пользователем условий (способов) использования прав
на Программный продукт в соответствии с настоящим Соглашением, лишить
Пользователя лицензии на использование прав на Программный продукт
путем закрытия доступа к Программному продукту.
5.4.3. Изменять в одностороннем порядке условия настоящего Соглашения в
установленном порядке.
5.4.4. Отказаться в одностороннем порядке от исполнения Соглашения в порядке,
предусмотренном применимым правом и/или настоящим Соглашением;
5. 4.5. Осуществлять иные права, предусмотренные применимым правом, а также
4.5. Осуществлять иные права, предусмотренные применимым правом, а также
настоящим Соглашением.
6. ПОРЯДОК ИСПОЛЬЗОВАНИЯ ПРОГРАММНОГО ПРОДУКТА
6.1. Пользователю для использования Программного продукта предлагается установить
(записать в память ЭВМ) и запустить Клиентское приложение Лицензиара,
экземпляр которого скачивается Пользователем самостоятельно одним из
следующих способов:
в сети Интернет на сайте Лицензиара;
в системе Google Play;
с флэш-накопителя, предоставленного Лицензиаром (опция).
6.2. После установки (записи в память ЭВМ) и запуска Клиентского приложения
Лицензиара Пользователю предоставляется право использования Программного
продукта в Демонстрационном режиме.
6.3. Для использования Программного продукта в Продуктивном режиме Пользователю
необходимо в Клиентском приложении ввести Регистрационный ключ, который
Лицензиар направляет Пользователю на адрес электронной почты, указанный на
Сайте Лицензиара в запросе на предоставление доступа. Пользователь
Пользователь
самостоятельно осуществляет использование Программного продукта путем запуска
и настройки Клиентского приложения.
6.4. Программный продукт предоставляется Пользователю по принципу «as is» («как
есть»), что подразумевает: Пользователю известны важнейшие функциональные
свойства продукта, в отношении которого предоставляются права на использование,
Пользователь несет риск соответствия Программного продукта его желаниям и
потребностям, а также риск соответствия условий и объема предоставляемых прав
своим желаниям и потребностям. Лицензиар не несет ответственность за какие-либо
убытки или ущерб, независимо от причин их возникновения (включая особый,
случайный или косвенный ущерб; убытки, связанные с недополученной прибылью,
прерыванием коммерческой или производственной деятельности, утратой деловой
информации, небрежностью, или какие-либо иные убытки), возникшие вследствие
использования или невозможности использования Программного продукта.
6.5. Программный продукт предназначен для личных, образовательных и иных не
связанных с осуществлением предпринимательской деятельности нужд физических
лиц. Использование Программного продукта в коммерческих целях не допускается.
7. ОТВЕТСТВЕННОСТЬ СТОРОН
7.1. За невыполнение или ненадлежащее выполнение обязательств по настоящему
Соглашению Стороны несут ответственность в соответствии с действующим
законодательством, если иное не установлено Соглашением.
7.2. Стороны освобождаются от ответственности за неисполнение (ненадлежащее
исполнение) Соглашения, если такое неисполнение (ненадлежащее исполнение)
явилось следствием действий обстоятельств непреодолимой силы, наступление
которых Стороны не могли предвидеть и предотвратить. Сторона, для которой
надлежащее исполнение обязательства стало невозможным ввиду действия
обстоятельств непреодолимой силы, обязана незамедлительно уведомить об этом
другую Сторону. Стороны вправе ссылаться на действия обстоятельств
непреодолимой силы лишь при условии, что они сделали все возможное в целях
предотвращения и/или минимизации негативных последствий действия указанных
обстоятельств.
7.3. Лицензиар не гарантирует абсолютную бесперебойность использования
Программного продукта и не дает гарантию того, что произведенные третьими
лицами программы для ЭВМ или любые другие средства, используемые при работе
Программного продукта, абсолютно защищены от компьютерных вирусов и других
вредоносных компонентов. Лицензиар обязуется осуществить все разумные меры
для защиты информации Пользователя и обеспечения бесперебойного
использования Программного продукта.
7.4. Пользователь самостоятельно отвечает за содержание информации, передаваемой им
или иным лицом по сети Интернет и хранимой в памяти сервера Лицензиара, в том
числе за ее достоверность и правомерность ее хранения и распространения.
7.5. В случае привлечения Лицензиара к ответственности или наложения на него
взыскания в связи с допущенными Пользователем нарушениями прав третьих лиц, а
равно установленных законодательством запретов или ограничений, Пользователь
обязан в полном объеме возместить убытки Лицензиара.
7.6. В случае нарушения Пользователем условий и ограничений настоящего
Соглашения, он является нарушителем исключительного права на Программный
продукт. За нарушение авторских прав на Программный продукт Пользователь несет
ответственность в соответствии с законодательством Российской Федерации.
7.7. Совокупная кумулятивная ответственность Лицензиара перед Пользователем в
отношении требований любого рода, возникающих из настоящего Соглашения, не
будет превышать сумму вознаграждения по данному Соглашению, фактически
выплаченного Пользователем за Программный продукт, в отношении которого
возникло требование, в течение 12 (двенадцати) месяцев, предшествующих
возникновению требования. Вышеуказанные ограничения ответственности
применяются даже в том случае, если с помощью вышеуказанного способа защиты
права не удается добиться его основной цели.
8. ПЕРСОНАЛЬНЫЕ ДАННЫЕ
8.1. Информация, предоставленная Пользователем является конфиденциальной.
8. 2. Предоставляя свои персональные данные Лицензиару, Пользователь соглашается на
их обработку, как с использованием средств автоматизации, так и без использования
средств автоматизации, в частности сбор, хранение, передачу третьим лицам и
использование информации Лицензиаром в целях исполнения обязательств перед
Пользователем в соответствии с настоящим Соглашением; получения
Пользователем персонализированной рекламы; проверки, исследования и анализа
данных, позволяющих поддерживать и улучшать Программный продукт.
8.3. Лицензиар обязуется не разглашать полученную от Пользователя информацию. Не
считается нарушением предоставление Лицензиаром информации, в том числе
персональные данные Пользователя третьим лицам, действующим на основании
договора с Лицензиаром, в целях исполнения настоящего Соглашения.
8.4. Не считается нарушением обязательств по неразглашению информации
предоставленной Пользователем, в том числе персональные данные Пользователя, в
целях обеспечения соблюдения требований действующего законодательства
Российской Федерации (в том числе в целях предупреждения и/или пресечения
незаконных и/или противоправных действий Пользователей).
8.5. Пользователь не имеет права передавать свои Логин и Пароль третьим лицам.
8.6. Пользователь обязуется обеспечивать конфиденциальность своего Логина и Пароля
и несет ответственность за использование Логина и Пароля третьими лицами. Ни
при каких обстоятельствах Лицензиар не несет ответственность за использование
третьими лицами Логина и пароля Пользователя.
8.7. В случае несанкционированного доступа к логину и паролю и/или персональной
странице Пользователя, или распространения логина и пароля Пользователь обязан
незамедлительно сообщить об этом Лицензиару посредством заполнения формы
обратной связи, представленной на Сайте.
8.8. Лицензиар не несет ответственности за использование кем бы то ни было
общедоступных персональных данных Пользователей.
9. ИСКЛЮЧИТЕЛЬНЫЕ ПРАВА НА КОНТЕНТ
9.1. Все объекты, размещенные на Сайте и в Программном продукте, в том числе
элементы дизайна, текст, графические изображения, иллюстрации, видео, скрипты,
программы, музыка, звуки и другие объекты и их подборки (далее — Контент),
являются объектами исключительных прав Лицензиара, все права на эти объекты
защищены.
9.2. Кроме случаев, установленных настоящим Соглашением, а также действующим
законодательством Российской Федерации, Контент не может быть скопирован
(воспроизведен), переработан, распространен, отображен во фрейме, опубликован,
скачан, передан, продан или иным способом использован целиком или по частям без
предварительного разрешения правообладателя, кроме случаев, когда
правообладатель явным образом выразил свое согласие на свободное использование
Контента любым лицом.
9.3. Использование Пользователем Контента, доступ к которому получен исключительно
для личного некоммерческого использования, допускается при условии сохранения
всех знаков авторства или других уведомлений об авторстве, сохранения имени
автора в неизменном виде, сохранении произведения в неизменном виде.
9.4. Любое использование Контента, кроме разрешенного в настоящем Соглашении или
в случае явно выраженного согласия правообладателя на такое использование, без
предварительного письменного разрешения правообладателя, категорически
запрещено.
10. ПРОЧИЕ УСЛОВИЯ
10.1. Все споры и разногласия, возникающие в связи с исполнением и (или) толкованием
настоящего Соглашения, разрешаются Сторонами путем переговоров. При
невозможности урегулирования Сторонами возникших разногласий путем
переговоров, спор подлежит разрешению в арбитражном суде по месту нахождения
ответчика с обязательным соблюдением претензионного порядка урегулирования
споров и разногласий. Срок ответа на претензию 30 (тридцать) календарных дней с
момента ее поступления в письменной форме или в электронном виде.
10.2. Ни одно из положений настоящего Соглашения не является и не может
рассматриваться как передача (отчуждение) исключительных прав на
интеллектуальную собственность Лицензиара.
10.3. В случае поступления от Пользователя замечаний к Программному продукту,
предоставляемому в рамках настоящего Соглашения, такие замечания подлежат
рассмотрению Лицензиаром по его желанию и необязательны для учета.
10. 4. Условия настоящего Соглашения распространяются на последующие версии
4. Условия настоящего Соглашения распространяются на последующие версии
Программного продукта, которые являются его обновлениями. Заключения иных
соглашений в отношении обновлений Программного продукта не требуется.
10.5. Во всем ином, что не предусмотрено настоящим Соглашением, Стороны
руководствуются действующим законодательством РФ.
11. АДРЕС, РЕКВИЗИТЫ ЛИЦЕНЗИАРА
ООО «АЛЕКТА»
Юридический адрес: 630090, г. Новосибирск, Проспект академика Лаврентьева 2/2.
Почтовый адрес: 630090, г. Новосибирск, Проспект академика Лаврентьева 2/2.
ОГРН 1025403657135
ИНН 5408128408
КПП 540801001
ОКВЭД 72.19, 62.01, 62.02, 68.20.2;
ОКПО 26335100;
ОКАТО 50401384000;
ОКФС 16;
ОКОПФ 65.
E-mail: [email protected]
Формулы для решения задач по химии ЕГЭ 2021 / Блог / Справочник :: Бингоскул
Формулы для расчета:
- v — количества моль, моль
- m — масса, г
- M — молярная масса, г/моль
- C — концентрация, моль/л
- N — количество атомов, молекул
- NA — число Авогадро
- V — объем, л
- Vm — молярный объем = 22,4 л/моль
- p — плотность
- D — относительная плотность
Число Авогадро NA
1 моль = 6,02 · 1023 частиц
Закон Авогадро: 1 моль идеального газа при нормальных условиях имеет один и тот же объём Vm = 22,413 996(39) л
Количество вещества n (моль) |
|
| Масса вещества m (г) | |
| Объем вещества V(л) |
|
| Масса |
|
| Количество вещества |
|
| Объем |
|
| Число частиц |
|
| Молярный объем |
|
| Молярная масса | |
| Относительная молекулярная масса |
|
Решай с ответами:
Основные формулы для решения задач по химии
05-Авг-2012 | комментариев 440 | Лолита Окольнова
Все, все основные задачи по химии решаются с помощью
нескольких основных понятий и формул.
У всех веществ разная масса, плотность и объем. Кусочек металла одного элемента может весить во много раз больше, чем точно такого же размера кусочек другого металла.
Моль (количество моль)
обозначение: моль, международное: mol — единица измерения количества вещества. Соответствует количеству вещества, в котором содержится NA частиц (молекул, атомов, ионов). Поэтому была введена универсальная величина — количество моль. Часто встречающаяся фраза в задачах — «было получено… моль вещества»
NA = 6,02 · 1023
NA — число Авогадро. Тоже «число по договоренности». Сколько атомов содержится в стержне кончика карандаша? Несколько миллионов. Оперировать такими величинами не удобно. Поэтому химики и физики всего мира договорились — обозначим 6,02 · 1023 частиц (атомов, молекул, ионов) как 1 моль вещества.
1 моль = 6,02 · 1023 частиц
Это была первая из основных формул для решения задач.
Молярная масса вещества
Молярная масса вещества — это масса одного моль вещества. Обозначается как M
Есть еще молекулярная масса — Mr
Находится по таблице Менделеева — это просто сумма атомных масс вещества.
Например, нам дана серная кислота — H2SO4. Давайте посчитаем молярную массу вещества: атомная масса H =1, S-32, O-16.
Mr(H2SO4)=1•2+32+16•4=98 г\моль.
Вторая необходимая формула для решения задач —
формула массы вещества:
Т.е., чтобы найти массу вещества, необходимо знать количество моль (n), а молярную массу мы находим из Периодической системы.
Закон сохранения массы — масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ.
Если мы знаем массу (массы) веществ, вступивших в реакцию, мы можем найти массу (массы) продуктов этой реакции. И наоборот.
Третья формула для решения задач по химии —
объем вещества:
Откуда взялось число 22.4? Из закона Авогадро:
в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул.
Согласно закону Авогадро, 1 моль идеального газа при нормальных условиях (н.у.) имеет один и тот же объём Vm = 22,413 996(39) л
Т.е., если в задаче нам даны нормальные условия, то, зная количество моль (n), мы можем найти объем вещества.
Итак, основные формулы для решения задач по химии
Число Авогадро NA
6,02 · 1023 частиц
Количество вещества n (моль)
n=m\M
n=V\22. 4 (л\моль)
4 (л\моль)
Масса вещества m (г)
m=n•Mr
Объем вещества V(л)
V=n•22.4 (л\моль)
или вот еще удобная табличка:
Это формулы. Часто для решения задач нужно сначала написать уравнение реакции и (обязательно!) расставить коэффициенты — их соотношение определяет соотношение молей в процессе.
В ОГЭ и ЕГЭ по химии задач , в которых нужно было бы найти только объем \ массу \ кол-во моль нет — это обычно ЧАСТЬ решения задачи. Однако, чтобы легко решать более сложные задачи, нужно тренироваться на таких вот небольших упражнениях.
Находим количество вещества по массе
1 Какое количество вещества алюминия содержится в образце металла массой 10.8 г?2 Какое количество вещества содержится в оксиде серы (VI) массой 12 г?
3 Определите количество моль брома, содержащееся в массе 12. 8 г.
Находим массу по количеству вещества:
4.Определите массу карбоната натрия количеством вещества 0.25 моль.
Объем по количеству вещества:
5. Какой объем будет иметь азот при н.у., если его количество вещества 1.34 моль?6. Какой объем занимают при н.у. 2 моль любого газа?
Ответы:/p>
- 0.4 моль
- 0.15 моль
- 0.08 моль
- 26.5 г
- 30 л
- 44.8 л
Категории:
|
Обсуждение: «Основные формулы для решения задач по химии»
(Правила комментирования)
Решение сложных задач на нахождение формулы вещества
Фреоны
Задача. В мастерской по ремонту холодильников и климатического оборудования отклеились этикетки от 5 баллонов с хранившимися в них фреонами (техническое название группы насыщенных алифатических галогенсодержащих углеводородов, применяемых в качестве хладагентов). Этикетки содержали следующие надписи: R-12, R-23, R-32, R-41, R-161. Для установления формул фреонов были проведены исследования. При сжигании фреона 1 образовалось 2,24 л СО2 и 4 г HF. Фреон 2 не горит (ω(C) = 9,92%; D(H2) = 60,5). У фреона 3 (ω(F) = 39,58%, ω(Н) = 10,42%). При взаимодействии фреона 4 с натрием образовался этан и фторид натрия. При щелочном гидролизе фреона 5 образовались две соли: формиат натрия (ω(C) = 17,65%; ω(О) = 47,06%) и фторид натрия. Установите структурные формулы указанных фреонов и дайте им химические названия, установите соответствие между кодом фреона и его формулой.
Для установления формул фреонов были проведены исследования. При сжигании фреона 1 образовалось 2,24 л СО2 и 4 г HF. Фреон 2 не горит (ω(C) = 9,92%; D(H2) = 60,5). У фреона 3 (ω(F) = 39,58%, ω(Н) = 10,42%). При взаимодействии фреона 4 с натрием образовался этан и фторид натрия. При щелочном гидролизе фреона 5 образовались две соли: формиат натрия (ω(C) = 17,65%; ω(О) = 47,06%) и фторид натрия. Установите структурные формулы указанных фреонов и дайте им химические названия, установите соответствие между кодом фреона и его формулой.
Данная задача предназначена для десятиклассников, которые еще не освоили курс кислородсодержащих органических соединений, поэтому даны массовые доли.
1. Начнем с фреона № 1. При его сжигании образовалось 2,24 л углекислого газа. Найдем количество углекислого газа. Делим его объем на молярный объем и получаем 0,1 моль. Соответственно, атомов углерода тоже 0,1 моль, поскольку в каждой молекуле углекислого газа содержится один атом углерода.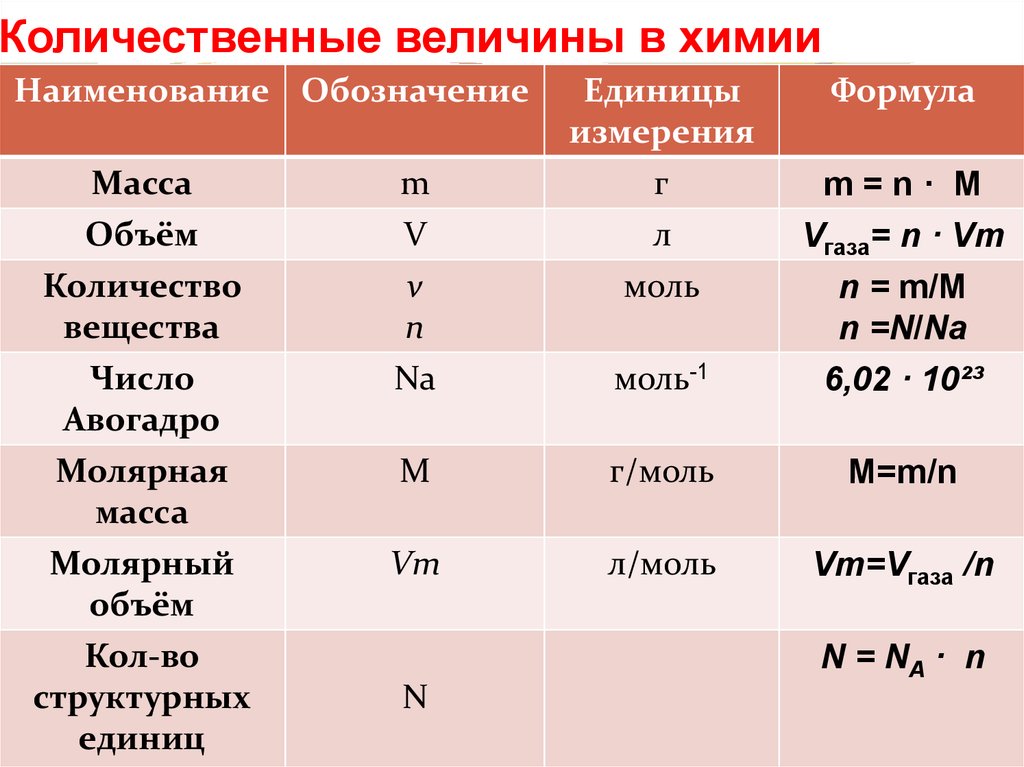
Информацию по водороду возьмем из фтороводорода. Найдем количество фтороводорода. Поскольку дана его масса, мы должны поделить массу (4 г) на молярную массу. Молекула фтороводорода состоит из атома фтора и атома водорода. Масса атома фтора 19, у водорода масса 1, значит, молярная масса 20. И мы получаем 0,2 моль.
Следовательно, H = 0,2 и F = 0,2. Формула вещества, фреона № 1: CH2F2 (на один атом углерода приходится два атома водорода и два атома фтора).
2. Узнаем, что скрывается под фреоном № 2. Известно, что он не горит, и дана его плотность по водороду. Это относительная плотность, которая показывает, во сколько раз молярная масса вещества больше молярной массы (в данном случае) водорода. Молярная масса фреона № 2 равна 121 г/моль.
Сколько атомов углерода во фреоне № 2? Для подсчета используем массовую долю углерода. Масса углерода равна: молярную массу умножить на массовую долю. Получаем 12. Значит, в данной молекуле фреона № 2 содержится только один атом углерода.
Получаем 12. Значит, в данной молекуле фреона № 2 содержится только один атом углерода.
Нарисуем этот атом углерода. У него имеется четыре связи, поскольку в органической химии углерод четырехвалентный. Попробуем определить атомы, исходя из того, что в сумме один атом углерода и все остальные атомы должны равняться молярной массе (равной молекулярной) 121. Попробуем рассчитать. Если это четыре атома фтора, то получается мало. А если это четыре атома хлора, то много. Возьмем нечто среднее: половина — атомы фтора и половина — атомы хлора. Единица в показателе 121 говорит о том, что имеются нечетные значения. Молярная масса хлора 35,5. Для того чтобы получить целое численное значение, вероятно, нужны два атома хлора.
121 – 71 – 12 = 38 (ровно на два атома фтора)
3. Перейдем к фреону № 3. Нам дана массовая доля фтора: 39,58. Дана массовая дола водорода: 10,42. Поскольку это органическое вещество, должен быть и углерод — попробуем его найти.
100 – 39,58 – 10,42 = 50
Проверим вариант, что там только хлор и нет других атомов. Предположим, что там всего один атом углерода (его масса будет равна 12). Посчитаем, какая масса при этом будет приходиться, например, на атом фтора.
12 ∙ 39,58 : 50 = 9,5
Как указано в периодической системе Менделеева, атомная масса фтора — 19. Ровно половина одного атома фтора — 9,5, так что в составе этой молекулы не может быть один атом углерода, их должно быть как минимум два. Следовательно, на углерод приходиться масса 24, на фтор — 19. Какая масса в данном случае приходится на водород? По сути, должно оставаться пять атомов водорода.
24 ∙ 10,42 : 50 = 5
Поскольку у нас один атом фтора, пять атомов водорода и два атома углерода, мы имеем дело с фторэтаном.
4. Что касается фреона № 4, то в реакции с натрием образовались этан и фторид натрия. Это реакция Вюрца — Фиттига. Мы имеем исходное вещество фторметан, которое реагирует с натрием, и образуются этан и фторид натрия.
Мы имеем исходное вещество фторметан, которое реагирует с натрием, и образуются этан и фторид натрия.
5. Переходим к фреону № 5. Формиат натрия образуется при гидролизе трифторметана. Получается формиат натрия, фторид натрия и две молекулы воды.
Посмотрев в справочную информацию, вы можете соотнести с кодами каждый из найденных фреонов.
Изучение фреонов очень интересно. Каждый тип холодильного оборудования требует особую марку фреона. Сегодня холодильное оборудование часто заполняют и углеводородами, поскольку, как известно, фреоны способствуют разрушению озонового слоя Земли. Но на сегодняшний день полного отказа от фреонов еще не произошло.
Химия. 10 класс. Углубленный уровень. Учебник.
Учебник написан преподавателями химического факультета МГУ им. М. В. Ломоносова и продолжает курс химии, изложенный в учебниках «Химия. 8 класс» и «Химия. 9 класс» данного авторскогo коллектива. Предназначен для изучения химии на углубленном уровне. Учебник соответствует федеральному государственному образовательному стандарту среднего общeгo образования.
Предназначен для изучения химии на углубленном уровне. Учебник соответствует федеральному государственному образовательному стандарту среднего общeгo образования.
Купить
Вильгельм Рудольф Фиттиг
Задача. Вещество, открытое в 1862 году немецким ученым Вильгельмом Рудольфом Фиттигом, представляет собой бесцветные кристаллы (tпл = +690С). Они широко применяются в качестве пищевой добавки для сохранения товарного вида фруктов (например, цитрусовых) путем нанесения на кожуру плода. Для установления состава вещество массой 15,4 г сожгли, образовалось 26,88 л (н.у.) углекислого газа и 9 г воды. Установите структурную формулу, если известно, что оно может подвергаться каталитическому галогенированию. Составьте уравнение этого вещества с избытком водорода на платиновом катализаторе при повышенном давлении.
Похожую задачу часто можно встретить на ЕГЭ.
Начнем с определения молекулярной формулы вещества, то есть узнаем состав этой молекулы. Найдем количество углекислого газа, а оно равно количеству углерода. Разделим объем на молярный объем. Поскольку условия нормальные, молярный объем для газообразного вещества составляет около 22,4 л/моль.
Найдем количество углекислого газа, а оно равно количеству углерода. Разделим объем на молярный объем. Поскольку условия нормальные, молярный объем для газообразного вещества составляет около 22,4 л/моль.
26,88 л : 22,4 л/моль = 1,2 моль
Поскольку воды 9 г, а молярная масса воды 18 г, следовательно, воды 0,5 моль, а водорода 1 моль. Как такое может быть? В одной молекуле воды содержится целых два атома водорода. Но нам не сказано: соединение ли углеводородом? содержит ли кислород? Мы должны проверить наличие кислорода и найти массу углерода и водорода.
1,2 моль ∙ 12 = 14,4 г
Сумма углерода и водорода: 14,4 + 1 = 15,4. Следовательно, в составе неизвестного вещества нет кислорода.
Молярное соотношение показывает, что формула вещества С12H10. Почему не С6H5? Потому что в углеводородах никогда не бывает нечетного числа атомов водорода. Радикал С6H5 в химии называется фенилом. Иными словами, мы имеем соединение, которое называется в химии дифенил. На это также указывают химические свойства дифенила, и он является разрешенной пищевой добавкой. В магазинах можно встретить, например, апельсины, покрытые белым веществом — это и есть дифенил. Иногда его применяют в изрядном количестве, поэтому нужно тщательно мыть фрукты.
Иными словами, мы имеем соединение, которое называется в химии дифенил. На это также указывают химические свойства дифенила, и он является разрешенной пищевой добавкой. В магазинах можно встретить, например, апельсины, покрытые белым веществом — это и есть дифенил. Иногда его применяют в изрядном количестве, поэтому нужно тщательно мыть фрукты.
Составим уравнение реакции с избытком водорода. Очень просто посчитать, сколько атомов водорода потребуется на реакцию с дифенилом. Мы видим шесть двойных связей. Следовательно, на одну двойную связь нужна одна молекула водорода, а на шесть двойных связей — шесть молекул водорода при исчерпывающем гидрировании. Конечно, на platinum-катализаторе, потому что соединение ароматическое и требует преодоления достаточно высокого энергетического барьера. Мы получаем соединение, которое нельзя назвать никак иначе, кроме как дициклогексил.
Соединение дифенил и было открыто Рудольфом Фиттигом в 1862 году с температурой плавления 69°С.
Желеобразующая жидкость
Задача. Некоторая нерастворимая в воде жидкость при хранении на воздухе способна уплотняться, превращаясь в желе. Химик отобрал, отмерив, некоторый объем этой жидкости и установил, что при действии избытка раствора брома в четыреххлористом углероде образовалось 26,4 г дибромида. А при действии раствора хлора на такой же объем этой жидкости образовалось 17,5 г дихлорида. Определите структурную формулу этой жидкости, если известно, что в ее состав входят только атомы водорода и углерода. Составьте уравнение реакции полимеризации этой жидкости.
Обозначим неизвестную жидкость-углеводород через формулу CXHY. О какой реакции идет речь: замещения или присоединения? Поскольку реакция протекает при обычных условиях, значит, речь идет о реакции присоединения.
Для решения данной задачи нужно применить прием, известный в учебной химии как прием вычитания массы. Представим, что жидкости у нас ровно 1 моль. В этом случае разница между массой дибромида и дихлорида будет разницей между массой брома и хлора.
В этом случае разница между массой дибромида и дихлорида будет разницей между массой брома и хлора.
Молекула брома имеет массу 160, а молекула хлора — 71. Получаем 89. То есть если бы вещества у нас было 1 моль, то разница составила бы 89 г. Вычислим разницу массы дибромида и дихлорида:
26,4 – 17,5 = 8,9
Искомого вещества 0,1 моль.
Теперь установим формулу. Обратимся к молекулярной записи. На углеводородную часть приходится 104. Сколько там может быть углеродов и водородов? Если углеродов 8 (что подходит), тогда на углероды приходится 96 и на водороды — 8.
Формула углеводорода C8H8.
Разберемся, о каком углеводороде идет речь. Обратим внимание, что соединение непредельное, но оно способно присоединить только одну молекулу брома или одну молекулу хрома. Значит, исходя из малого числа атомов водорода по отношению к атомам углерода, скорее всего, это соединение есть не что иное, как производное бензола, то есть ароматическое соединение. В бензоле шесть атомов углерода и пять атомов водорода в остатке. У нас получается кетастирол.
В бензоле шесть атомов углерода и пять атомов водорода в остатке. У нас получается кетастирол.
Чтобы не было полимеризации, обычно в тот стирол, который можно купить в магазине, добавляют стабилизатор.
Уравнение полимеризации. Из n молекул стирола получается полимер, состоящий из n фрагментов.
Полистирол — это, например, одноразовая посуда. Она наносит существенный вред окружающей среде, и сейчас идет речь о том, чтобы ее запретить.
Что ещё почитать?
Отдушка для мыла
Задача. Некоторое легкоплавкое вещество, обладающее приятным запахом, используют в качестве ингибитора полимеризации, в качестве отдушки для мыла. При сжигании этого вещества массой 8,4 г получили 11,2 л (н.у.) углекислого газа, 7,2 г воды. Установите структурную формулу неизвестного соединения, если известно, что оно не реагирует с бромной водой, но реагирует с водородом в присутствии катализатора. Известно, что это соединение может быть получено в результате прокаливания кальциевой соли органической кислоты. Составьте уравнение соответствующей химической реакции.
Известно, что это соединение может быть получено в результате прокаливания кальциевой соли органической кислоты. Составьте уравнение соответствующей химической реакции.
По данным задачи, углекислый газ составляет 0,1 моль, соответственно, столько же и углерода. Поскольку воды 7,2 г, что в молях 0,4, то водорода 0,8. Проверим на наличие кислорода. Масса углерода 6, масса водорода – 0,8. Поскольку общая масса сожженного вещества составляет 8,4, то на кислород приходится масса 1,6 (в молях 0,1). Получается молекулярная формула C5H8O.
Перейдем к структурой формуле вещества. Вещество не реагирует с бромной водой — из этого можно делать вывод, что нет кратных соединений (то есть двойных, тройных углерод-углеродных связей). Но вещество реагирует с водородом в присутствии катализатора. Исходя из условий, скорее всего, речь идет о двухосновной кислоте. В результате прокаливания, нагревания (в пределах 200–250°С) отщепляется карбонат кальция и образуется кетон циклопентанон.
Циклопентанон как раз используют в качестве отдушки для мыла.
Ошибка А. М. Бутлерова
Задача. Установите структурную формулу альдегида, в определении которой немного ошибся великий А. М. Бутлеров, если известно, что в результате взаимодействия 100 г 0,9%-го раствора этого вещества с избытком раствора перманганата калия образуется осадок массой 3,48 г. Составьте уравнение реакции этого альдегида с раствором перманганата калия.
Все великие химики ошибались, в том числе и А. М. Бутлеров.
Для начала вспомним, как альдегиды взаимодействуют с перманганатом калия. Мы не знаем, о каком альдегиде идет речь. Допустим, у него была одна альдегидная группа (хотя, если в соединении две альдегидные группы, он все равно будет альдегидом). Возьмем также перманганат калия и мысленно нагреем. Мы получаем калиевую соль некой карбоновой кислоты, оксид марганца (IV) и гидроксид калия. Степень окисления углерода в альдегидной группе была +1, а стала +3. Получается, что углерод альдегид потерял два электрона. Марганец был +7, стал +4? значит, он принял три электрона. Так мы определили ключевые коэффициенты. Проблема состоит в том, что калия всего два атома. Можно сказать, что две молекулы были в форме соли, а одна молекула в форме кислоты. Поскольку гидроксида калия 3, мы видим, что его не хватает — вместо него будет вода.
Получается, что углерод альдегид потерял два электрона. Марганец был +7, стал +4? значит, он принял три электрона. Так мы определили ключевые коэффициенты. Проблема состоит в том, что калия всего два атома. Можно сказать, что две молекулы были в форме соли, а одна молекула в форме кислоты. Поскольку гидроксида калия 3, мы видим, что его не хватает — вместо него будет вода.
После составления уравнения найдем массу альдегида и массу осадка. Но осадок — это, разумеется, оксид марганца (IV).
Поскольку у нас 100 г 0,2%-го раствора и на 1% приходится 1 г, масса альдегида 0,9 г. Чтобы найти количество оксида марганца, 3,48 разделим на молярную масса оксида марганца — 87. Получаем 0,04 моль. В соответствии с этим уравнением альдегида у нас должно быть больше в полтора раза: 0,06 моль.
Найдем молярную массу альдегида.
Где вы видели альдегид с молярной массой 15? Только на атом кислорода приходится 16. Значит, что либо альдегид содержал две альдегидные группы, либо это был формальдегид. Если бы он содержал две альдегидные группы, он бы отдал не два, а четыре электрона. Столько же отдал бы и формальдегид. Перманганат калия принимал бы три электрона. У оксида марганца (IV) было бы 4 моль. В этом случае оксида марганца 0,4 моль, а альдегида 0,3 моль.
Если бы он содержал две альдегидные группы, он бы отдал не два, а четыре электрона. Столько же отдал бы и формальдегид. Перманганат калия принимал бы три электрона. У оксида марганца (IV) было бы 4 моль. В этом случае оксида марганца 0,4 моль, а альдегида 0,3 моль.
Тогда
Следовательно, искомый альдегид — формальдегид. CH2O.
А. М. Бутлеров изначально определил формулу как C2H4O2.
Химия. 11 класс. Углубленный уровень. Учебник.
Учебник написан преподавателями химического факультета МГУ им. М. В. Ломоносова и продолжает курс химии для старшей школы, изложенный в учебнике «Химия. Углубленный уровень. 10 класс» данного авторского коллектива. Учебник предназначен для изучения химии на углублённом уровне. Учебник соответствует Федеральному государственному образовательному стандарту среднего общего образования.
Купить
…ловая кислота
Задача. На полке в химической лаборатории стояла склянка с полустертой надписью. Единственное, что можно было разобрать: «…ловая кислота». Для установления состава кислоты провели ряд экспериментов. Для полной нейтрализации раствора, содержащего 0,36 г этой кислоты, понадобилось 50 мл 0,1-молярного раствора гидроксида натрия. Такая же навеска кислоты смогла обесцветить V = 80 мл (ω = 1%, ρ ≈ 1 г/мл) бромной воды. Восстановите надпись на склянке.
На полке в химической лаборатории стояла склянка с полустертой надписью. Единственное, что можно было разобрать: «…ловая кислота». Для установления состава кислоты провели ряд экспериментов. Для полной нейтрализации раствора, содержащего 0,36 г этой кислоты, понадобилось 50 мл 0,1-молярного раствора гидроксида натрия. Такая же навеска кислоты смогла обесцветить V = 80 мл (ω = 1%, ρ ≈ 1 г/мл) бромной воды. Восстановите надпись на склянке.
Обозначим формулу кислоты (будем считать, что она монокарбоновая). Если она одноосновная, то реакция идет один к одному. Найдем количество гидроксида натрия: 50 миллилитров 0,1-молярного раствора. У нас раствор, в одном литре которого содержится 0,1 моль вещества. Поскольку 50 мл — это в 20 раз меньше, то 0,1 разделим на 20. Получаем 0,005 гидроксида натрия. Столько же и карбоновой кислоты.
Отсюда легко находим молекулярную массу карбоновой кислоты.
На карбоксильную группу приходится 45. Значит, на углеводородную часть приходится 27. В них поместятся два атома углерода и три атома водорода. Искомая кислота — акриловая.
В них поместятся два атома углерода и три атома водорода. Искомая кислота — акриловая.
Электроны
Задача. 0,800000 кг вещества содержит 0,2743 г электронов. Установите формулу вещества, если известно, что масса электрона равна 0,0005486 а.е.м.
Начнем с количества электронов. Масса электронов у нас известна и молярная масса тоже.
Число протонов равно количеству электронов:
Отсюда находим массу, которая приходится на нейтроны (поскольку с точки зрения школьной химии любое число состоит из протонов, нейтронов и электронов). Обычно мы пренебрегаем массой электронов, но в данной задаче ей пренебрегать не нужно.
Получается интересное вещество. Обычно в атомах число нейтронов либо равно числу протонов, либо больше. В данном веществе протоны преобладают. Скорее всего, мы имеем дело с водородным соединением. Найдем соотношение между числом протонов и числом нейтронов.
Если мы переберем водородные соединения элементов второго периода, то для метана получим, что в составе метана протонов буде 10, а нейтронов — 6.
Поделив 10 на 6, получаем 1,67. Следовательно, искомым соединением был родоначальник предельных углеводородов, первый член гомологического ряда — метан.
#ADVERTISING_INSERT#
Формулы для решения задач — ХИМИЯ!FOREVER!
Все, все основные задачи по химии решаются с помощью нескольких основных понятий и формул.
Моль (количество моль)
обозначение: моль, международное: mol — единица измерения количества вещества. Соответствует количеству вещества, в котором содержится NA частиц (молекул, атомов, ионов)Поэтому была введена универсальная величина —количество моль. Часто встречающаяся фраза в задачах — «было получено… моль вещества»
Часто встречающаяся фраза в задачах — «было получено… моль вещества»
NA = 6,02 · 1023
NA — число Авогадро. Тоже «число по договоренности». Сколько атомов содержится в стержне кончика карандаша? Порядка тысячи. Оперировать такими величинами не удобно. Поэтому химики и физики всего мира договорились — обозначим 6,02 · 1023 частиц (атомов, молекул, ионов) как 1 моль вещества.
1 моль = 6,02 · 1023 частиц
Это была первая из основных формул для решения задач.
Молярная масса вещества
Молярная масса вещества — это масса одного моль вещества.
Обозначается как Mr. Находится по таблице Менделеева — это просто сумма атомных масс вещества.
Например, нам дана серная кислота — H2SO4. Давайте посчитаем молярную массу вещества: атомная масса H =1, S-32, O-16. Mr(H2SO4)=1•2+32+16•4=98 г\моль.
Давайте посчитаем молярную массу вещества: атомная масса H =1, S-32, O-16. Mr(H2SO4)=1•2+32+16•4=98 г\моль.
Вторая необходимая формула для решения задач —
формула массы вещества:
Т.е., чтобы найти массу вещества, необходимо знать количество моль (n), а молярную массу мы находим из Периодической системы.
Закон сохранения массы — масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ.
Если мы знаем массу (массы) веществ, вступивших в реакцию, мы можем найти массу (массы) продуктов этой реакции. И наоборот.
Третья формула для решения задач по химии —
объем вещества:
Откуда взялось число 22.4? Из закона Авогадро:
в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул.
Согласно закону Авогадро, 1 моль идеального газа при нормальных условиях (н.у.) имеет один и тот же объём Vm = 22,413 996(39) л
Т.е., если в задаче нам даны нормальные условия, то, зная количество моль (n), мы можем найти объем вещества.
Итак, основные формулы для решения задач по химии
Число Авогадро NA
6,02 · 1023 частиц
Количество вещества n (моль)
n=m\Mr
n=V\22.4 (л\моль)
Масса веществаm (г)
m=n•Mr
Объем вещества V(л)
V=n•22.4 (л\моль)
Решение задач
ХИМИЯ
Предлагаем цикл занятий “Развивай навыки решения задач по химии” (программа 12.5 ч , 5 дней) для учеников 8-9 классов. К курсу также могут присоединиться ученики 10-12-х классов, которые хотят улучшить свои знания основ химии.
Достаточно часто решение задач по химии доставляет определенные сложности. Почему? У каждого будет свой ответ. Мы в свою очередь на дополнительных занятиях по химии освоим алгоритмы решения задач, которые помогут справиться не только с задачами уровня основной школы, но и сформируют базовые навыки для решения задач уровня средней школы. Во время занятий поможем систематизировать алгоритмы решения задач таким образом, чтобы в процессе решения можно было легко выбрать наиболее подходящие формулы и путь решения.
Наша цель, чтобы в результате данных занятий участники приобрели следующие навыки и умения:
- научились правильно определять заданные величины в заданиях и таблицах данных;
- научились использовать и преобразовывать формулы в соответствии с условиями задач;
- определять свой путь решения задачи;
- выбрать соответствующие формулы в комплексных задачах;
- правильно составлять химические формулы по названиям;
- правильно составлять уравнения реакций;
- проверять правильность составленного уравнения реакций;
- находить взаимосвязь уравнений реакций с расчетами.

Темы занятий:
- Количество вещества. Молярная масса. Молярный объем. Число Авогадро. Число атомов и молекул.
- Уравнения реакций. Степени окисления. Индексы. Коэффициенты. Цепи реакций.
- Задачи с уравнениями реакций. Молярное соотношение. Преобладание реагентов.
- Задачи, в вычисление которых используют растворы. Молярная масса. Молярная концентрация. Кристаллогидраты. Смешивание растворов.
- Комбинированные задачи с уравнениями реакций и растворами.
ЗАПИСАТЬСЯ
ФИЗИКА
Предлагаем цикл занятий “Развивай навыки решения задач по физике” (программа 12.5 ч , 5 дней) для учеников 8-9 классов. К курсу также могут присоединиться ученики 10-12-х классов, которые хотят улучшить свои знания основ физики.
Достаточно часто решение задач по физике доставляет определенные сложности. Почему? У каждого будет свой ответ. Мы в свою очередь на дополнительных занятиях по физике освоим алгоритмы решения задач, которые помогут справиться не только с задачами уровня основной школы, но и сформируют базовые навыки для решения задач уровня средней школы. Во время занятий поможем систематизировать алгоритмы решения задач таким образом, чтобы в процессе решения можно было легко выбрать наиболее подходящий путь решения и формулы.
Во время занятий поможем систематизировать алгоритмы решения задач таким образом, чтобы в процессе решения можно было легко выбрать наиболее подходящий путь решения и формулы.
Цель команды нашей школы, чтобы в результате этих занятий участники приобрели следующие навыки и умения:
- правильно определить заданные величины и задании и в таблицах данных;
- использовать и преобразовывать формулы в соответствии с условиями задач;
- объединить несколько формул решений в одно;
- определить свой путь решения задачи;
- преобразовывать и анализировать единицы измерения;
- вычислить и преобразовать числа в нормальную форму;
- оценить достоверность полученного ответа;
- отобразить в задании происходящие процессы и развить воображение.
Темы занятий:
- Механика (скорость, ускорение, сила, гравитация)
- Энергия (потенциальная и кинетическая энергия, теплота, сохранение энергии)
- Волны (свет, звук)
- Электричество (Закон Ома, электрические цепи, мощность)
- Комбинированные задачи (в которых объединены несколько тем по физике)
ЗАПИСАТЬСЯ
ОПЛАТА И ДРУГАЯ ВАЖНАЯ ИНФОРМАЦИЯ
Занятия будут проходить 1 раз в неделю, 5 раз.
Длительность одного занятия — 2,5 часа (включен перерыв — 15 минут).
В каждом занятии 20% времени предусмотрено на разъяснение теории и 80% времени на практическое решение задач.
Количество участников: до 16 учеников
Взять с собой: тетрадь для записей, ручка, калькулятор.
Занятия будут проходить удаленно через платформу Google Classroom
Включенные в программу задачи дифференцированы по нескольким уровням сложности, начиная с базового и вплоть до уровня олимпиадных задач. Таким образом каждый участник приобретет новые знания и навыки независимо от уровня знаний на начало занятий. Занятие проводит учитель с ассистентом, чтобы была возможность при решении задач уделить каждому участнику индивидуальное внимание и обеспечить максимально эффективные процесс обучения. Уровень освоения материала будет оцениваться с помощью теста в конце каждого занятия. По окончанию всего цикла занятий будет проведен завершающий тест для закрепления и проверки приобретенных знаний и навыков.
Цена: 75 Eur за всю программу (5 раз), 20 Eur за отдельное занятие (отдельно можно посещать только темы 1, 2, 3, 4 занятия).
Оплатить занятия следует до начала первого занятия по Счету, который будет вам выставлен и выслан после заполнения заявки — анкеты.
ЗАПИСАТЬСЯ
ДАТЫ БЛИЖАЙШИХ КУРСОВ
ДРУГИЕ КУРСЫ:
УРАВНЕНИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
Коллекция из 62 химических калькуляторов и утилит
В вашем браузере отключен JavaScript.
Вам необходимо включить его, чтобы использовать наши калькуляторы на основе JavasSript.
Содержание
Обзор
Химия — это наука о материи: о ее составе, свойствах, изменениях, которые приводят к ее образованию, и способах ее взаимодействия с другими веществами в окружающей среде. Мы начинаем со строительных блоков материи — электронов, нейтронов и протонов — и строим атомы и ионы, которые затем образуют молекулы и ионные соединения, которые могут реагировать, создавая известный нам материальный мир. Тщательное исследование свойств и тенденций этих материальных образований способствует лучшему пониманию возможностей материального мира.
Тщательное исследование свойств и тенденций этих материальных образований способствует лучшему пониманию возможностей материального мира.
Этот сборник химических калькуляторов, разбитых на различные фундаментальные концепции, является хорошим обзором вводной химии, но также содержит некоторые инструменты для более высокого уровня усилий по таким темам, как квантовые числа и продвинутая стехиометрия.
Кислотно-основные реакции
- Калькулятор pH WebQC — нужно знать pKa раствора? Или, может быть, даже просто pH? Посетите эту страницу, чтобы узнать обо всех ваших потребностях в кислотно-щелочной реакции.
- EasyCalculation Neutralization Reaction — Есть два способа проверить вашу работу: сдать ее и надеяться на лучшее или использовать этот сайт. Это так же просто, как нажмите, подключите и проверьте!
- Meracalculator Neutralization Reactions — Отлично подходит при работе с реакциями нейтрализации кислот и оснований, возвращайтесь к «нормальному состоянию» с помощью этого простого в использовании инструмента для решения проблем.

Буферы
- Рецепты буфера PFG — этот простой инструмент дает быстрые и точные ответы, а также дает возможность распечатать результаты и сохранить рецепт для дальнейшего использования.
- Wiley Buffers — Очень простой сайт без рекламы для расчета буфера.
- Science Gateway Общие реагенты и буферы — нужно знать массу или объем буферов? Как насчет объема буфера, необходимого для разбавления раствора? Щелкните здесь также, чтобы увидеть список общих реагентов.
Катализ
- Энергия активации — Вам нужно знать энергию активации реакции в Дж / моль, а не в британских тепловых единицах / фунт-моль? Просто подключите и выпейте здесь свои ответы об энергии активации, чтобы быстро и удобно проводить вычисления.
Химическое равновесие
- Onlinesciencetools Химическое равновесие — склоните чашу весов в правильном направлении с помощью этих простых в использовании равновесных весов. Просто вставьте свои фигуры в отведенные места, и ваши формулы всегда будут одинаковыми.

- Tutorvista Equilibrium Constant — Найдите константу равновесия для любого уравнения с помощью этого простого в использовании онлайн-уравнения. Просто введите значения равновесия и нажмите «рассчитать константу равновесия».”
- Colorado State Equilibria — более продвинутый и точный онлайн-источник для подсчета равновесий.
Эмпирические и молекулярные формулы
Электрохимия
- Калькулятор электрической движущей силы — Определите движущую силу любой электрохимической реакции с помощью этого простого в использовании инструмента.
- Calctool.org Nernst Solver — Вам нужно знать фактический или стандартный обратимый потенциал уравнения Нернста? Введите свои данные в текстовые поля и начните получать ответы.
- TutorVista Nernst Equation — Найдите редукционный потенциал уравнения, используя это простое уравнение Нернста. Заполните отведенные текстовые поля своими фигурами и позвольте ему сделать все остальное.
Электролиз
Электронные квантовые числа
Газовые законы (идеальный закон, закон Далтона и Грэма)
- AJ Design Формулы и уравнения закона идеального газа — Решаете ли вы для плотности, давления, температуры или объема с помощью закона идеального газа,
- WebQC Ideal Gas Law — идеальное место для любого химика, студента или любого другого специалиста, чтобы получить быстрый доступ к множеству уравнений и простому в использовании расчету.

- EasyCalculation Закон идеального газа — Просто введите цифры, которые вы знаете из уравнений закона идеального газа, а все остальное сделает easycalculation.com.
- Mera Закон Дальтона — Если вам нужно знать парциальные давления уравнения, то meracalculator.com — это то, что вам нужно. Этот сайт использует закон Далтона для вычисления этих значений парциального давления за вас.
- 1728 Закон диффузии Грэма. Это отличное место для изучения закона диффузии уравнений Грэма.Удобные, точные результаты.
Калькулятор
Ионные / ковалентные связи
Ионы и молекулы
- Цифровое ионное уравнение — Вы знаете название молекулы, но не знаете, из чего она состоит? Просто введите имя, и этот инструмент предоставит вам молярную массу и эмпирическую формулу молекулы.
- Shodor Polyatomic Ion — Если вы знаете эмпирическую формулу иона или молекулы, то можете узнать ее название. Отлично подходит, если вы новичок в ионах и молекулах или просто хотите перепроверить свою работу.

- Mera Calculator Polyatomic Ion — Простой, но эффективный, этот калькулятор позволяет ввести положительные и отрицательные ионы из эмпирической формулы, а затем выдает название молекулы.
Кинетика
Масс-спектрометрия
Ядерный распад
Реакции окисления-восстановления
Процентный состав
Значимые цифры
Концентрация раствора
Стехиометрия раствора (моли, титрование и расчеты молярности)
- Endmemo Chemical Mole Grams — Введите здесь химические формулы, чтобы вычислить количество молей или граммов в химической формуле.
- AJ Design Формулы и уравнения закона идеального газа — Используйте этот онлайн-вычислитель для решения уравнений и формул закона идеального газа с использованием давления, объема и температуры.
- Lenntech Molecular Weights — Рассчитайте среднюю молекулярную массу (MW) по молекулярной формуле или по одному из двух списков распространенных органических соединений или элементов периодической таблицы.

- Stoichiometry Tool — Введите ваши сбалансированные химические уравнения (при необходимости используйте Chemical Equation Balancer!), Чтобы получить стехиометрию каждого уравнения.
- OST Стехиометрия. Благодаря широкому диапазону входных параметров и опций для типа газа, а также выхода, этот инструмент незаменим для ваших расчетов стехиометрии.
- Стехиометрия реакции — задайте реакцию и выберите, хотите ли вы рассчитать реагент или продукт.
- Концентрация раствора с помощью титрования — онлайн-инструмент для титрования образцов с учетом концентрации стандарта, объема титранта, необходимого для титрования стандарта и образца.
- GraphPad Molarity — Масса, объем и концентрация: имея два, легко вычислить другое или разбавить исходный раствор.
- Molaritycalculator.com — Позволяя вам рассчитать массу, объем или концентрацию в зависимости от того, какие два из них известны, на этой странице также есть подробные объяснения различных способов выполнения этих расчетов вручную.

- Sigma-Aldrich Mass Molarity — Рассчитайте массу, необходимую для молярного раствора определенной концентрации и объема.
Дополнительные инструменты
Список общих уравнений
Периодическая таблица
- Интерактивная таблица Менделеева — Нужна справочная информация, пока вы делаете домашнее задание по химии, или, может быть, вы просто хотите узнать больше об элементах? В таком случае эта интерактивная таблица Менделеева идеально подходит для обычного браузера или подготовки к тестам.
Основные единицы измерения (метрическая система / СИ)
- UCDavis Единицы СИ — Вам нужно знать, какую единицу измерения использовать для этого уравнения плотности? Может быть, вам нужно освежить свои префиксы измерений? В любом случае, этот список единиц СИ является удобной справочной информацией.
В вашем браузере отключен JavaScript.
Вам необходимо включить его, чтобы использовать наши калькуляторы на основе JavasSript.
1.8: Решение химических проблем — Chemistry LibreTexts
Цели обучения
- Объясните подход размерного анализа (факторная метка) к математическим вычислениям, связанным с величинами.
- Опишите, как использовать анализ размеров для выполнения преобразования единиц для данного свойства и вычислений, включающих два или более свойств.
- Преобразование между тремя основными единицами измерения температуры: Фаренгейтом, Цельсием и Кельвином.
Часто бывает так, что интересующее количество может быть нелегко (или даже возможно) измерить напрямую, но вместо этого оно должно быть вычислено на основе других непосредственно измеряемых свойств и соответствующих математических соотношений. Например, рассмотрите возможность измерения средней скорости спортсмена, бегущего на спринт. Обычно это достигается путем измерения времени , необходимого спортсмену для пробега от стартовой линии до финишной линии, и расстояния между этими двумя линиями, а затем вычисления скорости из уравнения, которое связывает эти три свойства:
\ [\ mathrm {speed = \ dfrac {distance} {time}} \]
Спринтер олимпийского качества может пробежать 100 м примерно за 10 с, что соответствует средней скорости
\ [\ mathrm {\ dfrac {100 \: m} {10 \: s} = 10 \: m / s} \]
Обратите внимание, что эта простая арифметика включает деление чисел каждой измеренной величины, чтобы получить число вычисленной величины (100/10 = 10) и аналогичным образом деление единиц каждой измеренной величины, чтобы получить единицу вычисленной величины (m / с = м / с). Теперь рассмотрите возможность использования этого же соотношения для прогнозирования времени, необходимого человеку, бегущему с этой скоростью, для преодоления расстояния 25 м. Используется такое же соотношение между тремя свойствами, но в этом случае предоставляются две величины: скорость (10 м / с) и расстояние (25 м). Чтобы получить искомое свойство, время, уравнение необходимо переставить соответствующим образом:
Теперь рассмотрите возможность использования этого же соотношения для прогнозирования времени, необходимого человеку, бегущему с этой скоростью, для преодоления расстояния 25 м. Используется такое же соотношение между тремя свойствами, но в этом случае предоставляются две величины: скорость (10 м / с) и расстояние (25 м). Чтобы получить искомое свойство, время, уравнение необходимо переставить соответствующим образом:
\ [\ mathrm {time = \ dfrac {distance} {speed}} \]
Время может быть вычислено как:
\ [\ mathrm {\ dfrac {25 \: m} {10 \: m / s} = 2.5 \: s} \]
И снова арифметика с числами (25/10 = 2,5) сопровождалась той же арифметикой по единицам измерения (м / м / с = с), давая число и единицу результата, 2,5 с. Обратите внимание, что, как и в случае с числами, когда единица делится на идентичную единицу (в данном случае м / м), результатом становится «1» — или, как обычно выражается, единицы «отменяются».
Эти расчеты являются примерами универсального математического подхода, известного как размерный анализ (или метод метки факторов). Анализ размеров основан на этой предпосылке: единицы величин должны подвергаться тем же математическим операциям, что и соответствующие числа .Этот метод может применяться к вычислениям, начиная от простого преобразования единиц измерения и заканчивая более сложными, многоэтапными вычислениями, включающими несколько различных величин.
Анализ размеров основан на этой предпосылке: единицы величин должны подвергаться тем же математическим операциям, что и соответствующие числа .Этот метод может применяться к вычислениям, начиная от простого преобразования единиц измерения и заканчивая более сложными, многоэтапными вычислениями, включающими несколько различных величин.
Коэффициенты преобразования и размерный анализ
Отношение двух эквивалентных величин, выраженных в разных единицах измерения, может использоваться в качестве коэффициента преобразования единиц. Например, длины 2,54 см и 1 дюйм эквивалентны (по определению), и поэтому коэффициент преобразования единиц может быть получен из соотношения,
\ [\ mathrm {\ dfrac {2.54 \: cm} {1 \: дюйм} \ 🙁 2.54 \: cm = 1 \: дюйм) \: или \: 2.54 \: \ dfrac {cm} {дюйм}} \]
Несколько других часто используемых коэффициентов пересчета приведены в таблице \ (\ PageIndex {1} \).
 2046 фунтов
2046 фунтовКогда мы умножаем величину (например, расстояние в дюймах) на соответствующий коэффициент преобразования единиц, мы преобразуем количество в эквивалентное значение с различными единицами измерения (например, расстояние в сантиметрах).Например, вертикальный прыжок баскетболиста на 34 дюйма можно преобразовать в сантиметры следующим образом:
\ [\ mathrm {34 \: \ cancel {in.} \ Times \ dfrac {2.54 \: cm} {1 \: \ cancel {in. }} = 86 \: cm} \]
}} = 86 \: cm} \]
Поскольку эта простая арифметика включает в себя величин , предпосылка размерного анализа требует, чтобы мы умножали как чисел, так и единицы . Числа этих двух величин умножаются, чтобы получить номер количества продукта, 86, тогда как единицы умножаются, чтобы получить
.
\ [\ mathrm {\ dfrac {дюйм.\ times cm} {дюймы}}. \]
Как и в случае с числами, соотношение одинаковых единиц численно равно единице,
\ [\ mathrm {\ dfrac {дюйм} {дюйм} = 1} \]
, и таким образом единичный продукт упрощается до см . (Когда идентичные единицы делятся, чтобы получить коэффициент 1, они называются «отменяющими».) Используя анализ размеров, мы можем определить, что коэффициент преобразования единиц был установлен правильно, проверив, чтобы подтвердить, что исходная единица будет отменена, и результат будет содержать искомую (преобразованную) единицу.
Пример \ (\ PageIndex {1} \): использование коэффициента преобразования единиц
Масса соревновательного фрисби 125 г. Преобразуйте его массу в унции, используя коэффициент преобразования единиц, полученный из соотношения 1 унция = 28,349 г (Таблица \ (\ PageIndex {1} \)).
Преобразуйте его массу в унции, используя коэффициент преобразования единиц, полученный из соотношения 1 унция = 28,349 г (Таблица \ (\ PageIndex {1} \)).
Решение
Если у нас есть коэффициент преобразования, мы можем определить массу в килограммах, используя уравнение, подобное тому, которое используется для преобразования длины из дюймов в сантиметры.
\ [x \: \ mathrm {oz = 125 \: g \ times unit \: conversion \: factor} \ nonumber \]
Мы записываем коэффициент преобразования единиц в двух формах:
\ [\ mathrm {\ dfrac {1 \: oz} {28.349 \: g} \: и \: \ dfrac {28.349 \: g} {1 \: oz}} \ nonumber \]
Правильный коэффициент преобразования единиц — это соотношение, которое отменяет единицы граммов и оставляет унции.
\ [\ begin {align *}
x \: \ ce {oz} & = \ mathrm {125 \: \ cancel {g} \ times \ dfrac {1 \: oz} {28.349 \: \ cancel {g} }} \\
& = \ mathrm {\ left (\ dfrac {125} {28.349} \ right) \: oz} \\
& = \ mathrm {4. 41 \: oz \: (три \: значащие \: цифры )}
41 \: oz \: (три \: значащие \: цифры )}
\ end {align *} \]
Упражнение \ (\ PageIndex {1} \)
Преобразует объем 9.345 кварты в литры.
- Ответ
8,844 л
Помимо простых преобразований единиц, метод меток факторов может использоваться для решения более сложных задач, связанных с вычислениями. Независимо от деталей, основной подход один и тот же — все факторы , участвующие в расчетах, должны быть соответствующим образом ориентированы, чтобы гарантировать, что их метки (единицы) будут соответствующим образом отменены и / или объединены, чтобы дать желаемую единицу в результате. .Вот почему он называется методом факторной метки. По мере продолжения вашего изучения химии вы столкнетесь с множеством возможностей применить этот подход.
Пример \ (\ PageIndex {2} \): вычисление величин по результатам измерений
Какова плотность обычного антифриза в г / мл? Образец антифриза объемом 4,00 кварты весит
фунта.
Решение
Поскольку \ (\ mathrm {density = \ dfrac {mass} {volume}} \), нам нужно разделить массу в граммах на объем в миллилитрах.3 \: mL} = 1.11 \: г / мл} \ nonumber \]
В качестве альтернативы расчет может быть настроен таким образом, чтобы последовательно использовать три коэффициента преобразования единиц измерения, как показано ниже:
\ [\ mathrm {\ dfrac {9.26 \: \ cancel {lb}} {4.00 \: \ cancel {qt}} \ times \ dfrac {453.59 \: g} {1 \: \ cancel {lb}} \ times \ dfrac {1.0567 \: \ cancel {qt}} {1 \: \ cancel {L}} \ times \ dfrac {1 \: \ cancel {L}} {1000 \: mL} = 1.11 \: г / мл} \ nonumber \]
Упражнение \ (\ PageIndex {2} \)
Каков объем в литрах 1000 унций, если 1 л = 1.{-2} \: L} \)
Пример \ (\ PageIndex {3} \): вычисление величин по результатам измерений
На пути из Филадельфии в Атланту, расстояние около 1250 км, Lamborghini Aventador Roadster 2014 года использует 213 л бензина.
- Какая (средняя) экономия топлива в милях на галлон была у Roadster во время этой поездки?
- Если бензин стоит 3,80 доллара за галлон, какова стоимость топлива для этой поездки?
Решение
(a) Сначала мы конвертируем расстояние из километров в мили:
\ [\ mathrm {1250 \: км \ раз \ dfrac {0. 62137 \: mi} {1 \: km} = 777 \: mi} \ nonumber \]
62137 \: mi} {1 \: km} = 777 \: mi} \ nonumber \]
, а затем переведите объем из литров в галлоны:
\ [\ mathrm {213 \: \ cancel {L} \ times \ dfrac {1.0567 \: \ cancel {qt}} {1 \: \ cancel {L}} \ times \ dfrac {1 \: gal} {4 \: \ cancel {qt}} = 56.3 \: gal} \ nonumber \]
Затем,
\ [\ mathrm {(средний) \: пробег = \ dfrac {777 \: mi} {56,3 \: гал} = 13,8 \: миль / галлон = 13,8 \: миль на галлон} \ nonumber \]
В качестве альтернативы расчет можно настроить таким образом, чтобы все коэффициенты пересчета использовались последовательно, как показано ниже:
\ [\ mathrm {\ dfrac {1250 \: \ cancel {km}} {213 \: \ cancel {L}} \ times \ dfrac {0.62137 \: mi} {1 \: \ cancel {km}} \ times \ dfrac {1 \: \ cancel {L}} {1.0567 \: \ cancel {qt}} \ times \ dfrac {4 \: \ cancel { qt}} {1 \: gal} = 13,8 \: миль на галлон} \ nonumber \]
(b) Используя ранее рассчитанный объем в галлонах, находим:
\ [\ mathrm {56.3 \: gal \ times \ dfrac {$ 3.80} {1 \: gal} = $ 214} \ nonumber \]
Упражнение \ (\ PageIndex {3} \)
Toyota Prius Hybrid использует 59,7 л бензина для поездки из Сан-Франциско в Сиэтл на расстояние 1300 км (две значащие цифры).
- Какую (среднюю) экономию топлива в милях на галлон получил Prius во время этой поездки?
- Если бензин стоит 3 доллара.90 за галлон, какова была стоимость топлива в этой поездке?
- Ответьте на
51 миль на галлон
- Ответ б
$ 62
Преобразование единиц температуры
Мы используем слово «температура» для обозначения жара или холода вещества. Один из способов измерить изменение температуры — это использовать тот факт, что большинство веществ расширяются при повышении температуры и сжимаются при понижении температуры.Ртуть или спирт в обычном стеклянном термометре изменяют свой объем при изменении температуры. Поскольку объем жидкости изменяется больше, чем объем стекла, мы можем видеть, как жидкость расширяется, когда становится теплее, и сжимается, когда становится холоднее.
Чтобы разметить шкалу на термометре, нам понадобится набор эталонных значений: два из наиболее часто используемых — это температура замерзания и кипения воды при заданном атмосферном давлении. По шкале Цельсия 0 ° C определяется как температура замерзания воды и 100 ° C как температура кипения воды.Пространство между двумя температурами разделено на 100 равных интервалов, которые мы называем градусами. По шкале Фаренгейта точка замерзания воды определяется как 32 ° F, а температура кипения — как 212 ° F. Пространство между этими двумя точками на градуснике Фаренгейта разделено на 180 равных частей (градусов).
По шкале Цельсия 0 ° C определяется как температура замерзания воды и 100 ° C как температура кипения воды.Пространство между двумя температурами разделено на 100 равных интервалов, которые мы называем градусами. По шкале Фаренгейта точка замерзания воды определяется как 32 ° F, а температура кипения — как 212 ° F. Пространство между этими двумя точками на градуснике Фаренгейта разделено на 180 равных частей (градусов).
Определение температурных шкал Цельсия и Фаренгейта, как описано в предыдущем абзаце, приводит к немного более сложной взаимосвязи между значениями температуры на этих двух шкалах, чем для разных единиц измерения для других свойств.Большинство единиц измерения для данного свойства прямо пропорциональны друг другу (y = mx). На примере знакомых единиц длины:
\ [\ mathrm {length \: in \: ft = \ left (\ dfrac {1 \: ft} {12 \: in.} \ Right) \ times length \: in \: inch} \]
где
- y = длина в футах,
- x = длина в дюймах и
- коэффициент пропорциональности m является коэффициентом преобразования.

Температурные шкалы Цельсия и Фаренгейта, однако, не имеют общей нулевой точки, поэтому связь между этими двумя шкалами является линейной, а не пропорциональной (\ (y = mx + b \)).Следовательно, преобразование температуры из одной из этих шкал в другую требует большего, чем простое умножение на коэффициент преобразования, m, оно также должно учитывать различия в нулевых точках шкалы (\ (b \)). \ circ F} +32)} \]
Как упоминалось ранее в этой главе, единицей измерения температуры в системе СИ является кельвин (K).В отличие от шкал Цельсия и Фаренгейта шкала Кельвина представляет собой шкалу абсолютных температур, в которой 0 (ноль) К соответствует самой низкой температуре, которая теоретически может быть достигнута. Открытие в начале 19 века взаимосвязи между объемом газа и температурой предполагало, что объем газа будет равен нулю при -273,15 ° C. В 1848 году британский физик Уильям Томпсон, который позже принял титул лорда Кельвина, предложил шкалу абсолютных температур, основанную на этой концепции (дальнейшее рассмотрение этой темы дается в главе этого текста, посвященной газам). \ circ C} = T _ {\ ce K} -273,15 \]
\ circ C} = T _ {\ ce K} -273,15 \]
Значение 273,15 в этих уравнениях было определено экспериментально, поэтому оно неточно. На рисунке \ (\ PageIndex {1} \) показано соотношение между тремя температурными шкалами. Напомним, что мы не используем знак градуса с температурами по шкале Кельвина. \ circ C} +273.2 \, K \ hspace {20px} (две \: значащие \: цифры)} \ nonumber \]
Упражнение \ (\ PageIndex {5} \)
Преобразование 50 ° F в ° C и К.
- Ответ
10 ° С, 280 К
Сводка
Измерения производятся с использованием различных единиц. Часто бывает полезно или необходимо преобразовать измеренную величину из одной единицы в другую. Эти преобразования выполняются с использованием коэффициентов преобразования единиц, которые выводятся с помощью простых приложений математического подхода, называемого методом метки факторов или анализом размеров.\ circ C} = \ ce K-273.15 \)
Глоссарий
- анализ размеров
- (также метод метки факторов) универсальный математический подход, который может применяться к вычислениям, начиная от простого преобразования единиц измерения и заканчивая более сложными многоэтапными вычислениями, включающими несколько различных величин
- по Фаренгейту
- единица температуры; вода замерзает при 32 ° F и закипает при 212 ° F по этой шкале
- коэффициент преобразования
- соотношение эквивалентных величин, выраженных в разных единицах; используется для преобразования одной единицы в другую
Авторы и авторство
Решение проблем в химии Учебник
Ключевые понятия
Есть 5 шагов к решению задач по химии (1) , которые можно представить как набор светофоров:
| 1: | СТОП! | S проблема времени. | ↓ | СТОП | ← | 5: | СТОП! | S tate solution or S tart again |
|---|---|---|---|---|---|---|---|---|
| 2: | ПАУЗА! | P план ремонта ремонт. | ↓ | ПАУЗА | ↑ | 4: | ПАУЗА! | P на достоверность. |
| 3: | GO! | G o с планом игры. | → | GO | ↑ |
AUS-e-TUTE называет это подходом к решению проблем Sto P Go P S :
| Шаг 1: | Sto p, чтобы сформулировать проблему и извлечь все данные из вопроса. |
|---|---|
| Шаг 2: | P поможет подготовить ваш план игры, ваш подход к решению проблемы. |
| Шаг 3: | Go сделай это! Следуйте инструкциям вашего плана игры. |
| Шаг 4: | P позволяет задуматься о том, разумно ли ваше решение проблемы. Проверьте правильность примененных вами научных принципов. Проверить правильность формул, расчетов, единиц измерения и т. Д. |
| Шаг 5: | S верх. Довольны вашим решением? Назовите решение! Не устраивает ваше решение? Снова начните процесс решения проблемы с шага 1. |
Здесь вы найдете одностраничный шаблон (pdf), который можно использовать для решения проблем.
Все учебные пособия AUS-e-TUTE используют эту эвристическую «временную» процедуру для решения проблем.
Это руководство намного длиннее, чем нам хотелось бы, но это потому, что мы собираемся сосредоточиться на некоторых проблемных областях, поднятых экзаменаторами (экзаменаторами) в их отчетах о внешних экзаменах.
Итак, прежде чем вы начнете, вы можете пойти в ванную, взять что-нибудь попить и / или поесть и получить дополнительную подушку для своего стула….
Пожалуйста, не блокируйте рекламу на этом сайте.
Без рекламы = для нас нет денег = для вас нет бесплатных вещей!
СТОП! Сформулируйте проблему
Цель этого первого шага — разобрать вопрос так, чтобы вы могли ясно видеть:
- что вас просит сделать вопрос
- какие научные принципы необходимо применять
- какая информация была предоставлена вам в вопросе
Шаг 1. Внимательно прочтите вопрос.
Шаг 2. Подчеркните слова или фразы в вопросе, которые говорят вам, что вас просят сделать.
| Ключевое слово | Значение |
|---|---|
| счет | укажите причины этого или сообщите об этом |
| анализировать | определить компоненты в этом и отношения между этими компонентами |
| применить | использовать информацию, данную в данной конкретной ситуации |
| оценка | оцените стоимость этого |
| оценить | оценить стоимость этого |
| оценить | выносит суждение об этом на основании его ценности, качества, результата, результата или размера |
| рассчитать | определить значение для этого на основе данных |
| уточнить | сделайте это ясным или простым |
| классифицировать | упорядочить данные по группам, категориям или классам |
| сравнить | показать, как эти вещи одинаковы или разные |
| конструкция | создать или построить вещь или набор аргументов |
| контраст | показывают, чем все отличается, или как одно противоположно другому |
| критически | проанализировать и оценить это на предмет степени точности и глубины понимания, то есть определить компоненты и взаимосвязь между ними, а затем сделать суждение. |
| вывести | сделать выводы по этому поводу |
| определить | указать значение этого и определить его основные компоненты |
| продемонстрировать | покажите это на примере |
| описать | дать характеристики и особенности этого |
| обсудить | выявить проблемы и дать ключевые аргументы за и против этого |
| различить | обратите внимание на различия между этими вещами |
| оценить | сделать суждение об этом на основе определенных критериев или определить стоимость этого |
| изучить | запросить |
| объяснить | связывает причину и следствие, проясняет взаимосвязь между вещами, объясняет причины, почему и как это так |
| исследовать | внимательно изучите предоставленную информацию, чтобы что-то обнаружить |
| экстракт | из предоставленной информации выберите соответствующие и / или соответствующие данные |
| экстраполировать | сделать вывод об этом из того, что известно |
| идентифицировать | узнайте и назовите это |
| интерпретировать | извлечь смысл из этого |
| расследовать | планировать, исследовать и делать выводы об этом |
| по ширине | поддержать аргумент или вывод, указав причины |
| организовать | использовать разные фрагменты информации для создания единого целого |
| контур | приведите основные характеристики этого, набросайте в общих чертах |
| прогноз | предположить, что может произойти на основании предоставленной информации |
| предложить | выдвинул на рассмотрение пример, точку зрения, идею, аргумент, предложение и т. Д. Д. |
| отзыв | представить запомненные идеи, факты, опыт |
| признать | определить по знаниям, опыту или характеру |
| рекомендовать | аргументы в пользу этого |
| пересчет | пересказать серию событий |
| выбрать | тщательно выбирайте что-то, отдавая предпочтение другому |
| подвести итог | кратко укажите соответствующие подробности |
| синтезировать | объединить различные фрагменты данных в единое целое |
Шаг 3. Запишите, что вас просят сделать в вопросе, то есть сформулируйте проблему.
Используйте ключевое слово в начале утверждения.
Пример: Вычислить молей газа.
Пример: Объясните , почему скорость реакции увеличивается.
Шаг 4. Выделите ключевых слов, которые указывают на научные принципы, которые вам нужно будет применить.
| Слово / фраза | Научный принцип (тип проблемы) |
|---|---|
| кислота | Определение (Аррениус? Бронстед-Лоури? Льюис? Монопротический? Дипротический? Трипротический? Полипротический?)? Нейтрализация? Титрование? Расчет pH / pOH / концентрации? Равновесие? Буфер? Скорость реакции? Кислотный дождь? |
| активность | Activity Series? Тенденция периодической таблицы? |
| аммиак | Структура / внутримолекулярные силы (связывание)? Межмолекулярные силы? Газ (стехиометрия? Газовые законы?)? Процесс Габера (равновесие? Скорость реакции? Катализаторы? Уравнение? Стехиометрия?)? |
| основание | Определение (Аррениус? Бронстед-Лоури?), Нейтрализация? Титрование? Расчет pH / pOH / концентрации? Равновесие? Буфер? Скорость реакции? |
| связка | Внутримолекулярные силы (ковалентные? Ионные? Металлические?)? Межмолекулярные силы (дисперсионные силы? Диполь-дипольные взаимодействия? Водородная связь?)? |
| буфер | Равновесие? Кислотно-щелочная? Теория Бронстеда-Лоури? Сила кислот / оснований? |
| катализатор | Скорость реакции? Изменение энтальпии? Энергетический профиль? Использование? Фермент? |
| хроматография | Тип (бумага? Тонкий слой? Газ? Высокоэффективная жидкость?)? Расчет (коэффициент замедления? Время удерживания? Концентрация?)? |
| горение | Органическая химия (написать уравнение? Полное / неполное?)? Энтальпия (Расчет теплоты сгорания? Энергетический профиль? Закон Гесса?)? Калориметрия? Топливо (эффективность сгорания? Факторы, влияющие на?) |
| концентрация | Тип раствора (водный раствор? Газовая смесь? И т. Д.)? Стехиометрия (расчет)? Преобразование единиц измерения? Разбавление? Д.)? Стехиометрия (расчет)? Преобразование единиц измерения? Разбавление? |
| конъюгат | Теория Бренстеда-Лоури? Сила кислот / оснований? |
| цикл | Тип (углерод? Азот?)? Стехиометрия (расчет)? Химическое уравнение? Равновесие? Скорость реакции? |
| моющее средство | Структура (анионная, катионная, нейтральная)? Очистка (мицеллы? Межмолекулярные силы? Поверхностное натяжение?)? |
| рабочий объем | Уравнение реакции вытеснения? Серия мероприятий? Расчет электродного потенциала (ЭДС)? |
| электролизный / электролитический | Электролитическая ячейка? Уравнение окислительно-восстановительной реакции? Расчет электродного потенциала (ЭДС)? Применение (зарядка аккумуляторов? Гальваника? Извлечение / рафинирование металлов?)? |
| электрофорез | Техника? Разделение аминокислот? ДНК? |
| энтальпия | Расчет стохиометрии? Закон Гесса? Энергетический профиль? Жар реакции? Жар нейтрализации? Теплота раствора? Теплота сгорания? Теплота образования? Связанная энергия? Скрытая теплота? Калориметрия? Равновесие? Скорость реакции? |
| равновесие | Принцип Ле Шателье? Расчет / с использованием константы равновесия (K)? Расчет / использование коэффициента реакции (Q)? Кислота (K a )? База (K b )? Вода (K aw )? Осадок (K sp )? Применение (кровь? Процесс Хабера? Контактный процесс? Процесс Solvay?)? |
| формула | Органический (молекулярная формула? 2-мерная структурная формула? 3-мерная структурная формула? Сжатая (полу) структурная формула? Скелетная формула?)? Соль? Переходный Металлический Комплекс? |
| газ | Закон Гей-Люссака? Принцип Авогадро? Закон Бойля? Закон Чарльза? Комбинированное газовое уравнение? Закон об идеальном газе? Кинетическая теория газов? Закон частичных давлений Дальтона? Законы Грэма излияния и диффузии? |
| теплица | Эффект? Газы (тип «стехиометрических» уравнений?) |
| период полураспада | Ядерный распад? Скорость реакции? |
| изотоп | Атомная теория? Ядерный распад? Относительная атомная масса? Масс-спектроскопия? Период полураспада? Свойства / использование? Стабильность? |
| масса | Стехиометрия (расчет?)? Преобразование единиц измерения? Относительная атомная масса? Молярная масса? Молекулярная масса? Формула массы? Изотопная масса? Масс-спектроскопия? |
| металл | Периодическая таблица Тенденции? Реакции? Стехиометрия? Металлическое соединение? Серия мероприятий? Извлечение металлов из руд? Свойства / использование? |
| молярность | Стехиометрия (расчет)? Тип реакции (кислотно-щелочной? Окислительно-восстановительный? Металл + кислота? Вытеснение? Горение? Синтез и т. Д?)? Написать химическое уравнение? Разбавление? Д?)? Написать химическое уравнение? Разбавление? |
| моль | Стехиометрия (расчет)? Газ? Твердый? Жидкость? Решение? Тип реакции (кислотно-щелочное? Вытеснение? Окислительно-восстановительный? Синтез? Горение? И т. Д.)? Ограничение количества реагента / реагента в избытке? |
| наименование | Органическая номенклатура (IUPAC? Common?), Бинарное неорганическое соединение или соль? Переходный Металлический Комплекс? |
| нейтрализация | Теория Аррениуса? Теория Бронстеда-Лоури? Перенос протонов? Титрование? Соль (pH? Концентрация? Идентичность?)? |
| ядерный распад | Написать уравнение? Расчет (период полураспада? Масса? Процент?) Изотопов? Излучение (альфа?, Бета?, Гамма?)? |
| окисление | Органическая химия (напишите уравнение? Окислители?)? Электрохимия (степень окисления? Написать полууравнение? Окислитель?) |
| озон | Структура? Озоновый слой? Истощение озонового слоя? Стехиометрия (расчет)? Химическое уравнение? |
| полимер | Имя / Структура? Типа (добавление / конденсация?)? Примеры? |
| осадок | Уравнение (молекулярное? Ионное? Чистое ионное?)? Стехиометрия (расчет?)? Правила растворимости? Продукт растворимости (K sp )? Гравиметрический анализ? Межмолекулярные силы? |
| оценка | Теория столкновений? Распределение кинетической энергии? Закон о ставке? Равновесие? Энтальпия / энергия? |
| редокс | Состояние окисления? Реакция окисления? Редукционная реакция? Полуравнение? Уравнение окислительно-восстановительного потенциала? Электродные потенциалы (ЭДС)? Гальванический элемент? Электролитическая ячейка? Законы электролиза Фарадея? Гальваника (электроосаждение)? Добыча металла из руды? Титрование? |
| редуктор | Органическая химия (напишите уравнение? Восстанавливающий агент?)? Электрохимия (степень окисления? Полууравнение? Восстановитель?) |
| соль | Реакция нейтрализации? Бинарная неорганическая номенклатура? Металл + кислота? Карбонат + кислота? Теория Аррениуса? Теория Бронстеда-Лоури? Титрование? |
| мыло | Синтез / структура (омыление)? Очистка (мицеллы? Межмолекулярные силы? Поверхностное натяжение?)? |
| спектроскопия | Тип (масса? Атомная абсорбция? Излучение? Инфракрасное? УФ-видимое? 1 H? 13 C?)? Качественный? Количественный? |
| серная кислота | Стехиометрия? Кислотная сила? Нейтрализация? Реакция обезвоживания? Окисляющая кислота? Контактный процесс (равновесие? Скорость реакции? Катализаторы? Стехиометрия?) |
| поверхность | Адгезия? Сплоченность? Поверхностное натяжение? Смачивание? Капиллярное действие? Межмолекулярные силы? Моющее средство? Мыло? Катализ (скорость реакции? Изменение энтальфии?)? |
| раствор | Расчет стехиометрии (концентрация, разведение)? Коллигативные свойства растворов (понижение точки замерзания, повышение температуры кипения, понижение давления пара, осмотическое давление)? |
| растворимость | Правила растворимости? Осадки? Межмолекулярные силы? Энергия решетки? Стехиометрия (расчет)? Продукт растворимости (K sp )? Равновесие? Скорость реакции? Решение? |
| титрование | Тип (прямое кислотно-основное? Обратное титрование? Окислительно-восстановительный? Комплексометрический? Кондуктометрический?)? Техника? Стехиометрия (расчет)? Нейтрализация? Показатель? Кривая титрования? |
| объем | Твердый? Жидкость? Газ? Решение? Преобразование единиц измерения? Плотность? |
| вода | Равновесие (K w )? Водные растворы (стехиометрия? Уравнения? Реакции?)? Анализ? Очищение? Поверхностное натяжение? Смачивание? Структура / внутримолекулярные силы (связь)? Межмолекулярные силы? |
| выход | Расчет стехиометрии? Равновесие против скорости реакции? |
Под вашей формулировкой проблемы напишите краткую заметку, в которой сообщается, какой научный принцип (выделен) вы будете применять.
Начните заметку со слов вроде «Использовать …» или «Применить ….»
Шаг 5. Извлеките всю информацию, данные, приведенные в вопросе, и запишите их в виде списка под своим примечанием о применимых научных принципах.
При необходимости укажите единицы измерения.
Шаг 6. При необходимости напишите символ для фрагмента данных рядом с ним в списке.
| Некоторые примеры | |||
|---|---|---|---|
| количество | символ | кол-во | условное обозначение |
| число Авогадро | N A | моль | n |
| изменение: макроскопическое | Δ | давление | -П, |
| изменение: бесконечно малое | δ | коэффициент реакции | Q |
| концентрация (молярность) | с | коэффициент замедления | R f |
| энтальпия | H | время удерживания | R т |
| константа равновесия | К | удельная теплоемкость | C г |
| постоянная Фарадея | F | стандартный потенциал электрода | E o |
| период полураспада | т 1/2 | температура | т |
| постоянная идеального газа | R | раз | т |
| масса | м | том | В |
| молярная масса | M | ||
ПАУЗА! Подготовьте план игры
После выполнения шага СТОП, описанного выше, у вас должна появиться страница, которая выглядит как на диаграмме ниже:
| Проблема:………… Применить ……………. Данные |
Цель этого шага — подготовить план игры, которому вы можете следовать, чтобы решить проблему.
План может быть набором пронумерованных шагов или блок-схемой, но это должно быть что-то, чему вы можете следовать последовательно.
Шаг 1: Под списком данных, которые вы уже записали, запишите список шагов , скажем, 10 шагов, оставляя достаточно места между каждым из них:
| Проблема:………… Применить …………….. Данные |
Шаг 1 Шаг 2 Шаг 3 и т. Д. |
Вы всегда можете добавить дополнительные шаги позже, если вам нужно, или проигнорировать те, которые вы не используете.
Шаг 2: Подумайте о том, как ваше неизвестное (то, что вам нужно найти) связано с информацией, полученной вами в соответствии с научными принципами, которые вы выбрали.
От того, как неизвестное связано с известными, указанными в вопросе, будет зависеть, что вы напишете рядом с каждым числом в вашем списке шагов.
- Что вам нужно сделать в первую очередь?
Вам нужно написать химическое уравнение? Сделайте этот шаг 1.
Пример: Шаг 1: напишите сбалансированное химическое уравнение реакции между X и Y с образованием Z - Что вам нужно делать дальше?
Вам нужно найти стехиометрическое (мольное) соотношение? Сделайте этот шаг 2.
Пример: Шаг 2: найдите n (x): n (z), используя сбалансированное химическое уравнение.
- Что вам нужно делать дальше?
Вам нужно рассчитать количество молей реагента? Сделайте этот шаг 3.
Пример: Шаг 3: вычислить n (X)
- Что вам нужно делать дальше?
Нужно ли использовать мольное соотношение для расчета количества молей образовавшегося продукта? Сделайте этот шаг 4.
Пример: Шаг 4: используйте мольное отношение для расчета n (Z) - Что вам нужно делать дальше?
Вам нужно рассчитать массу продукта? Сделайте этот шаг 5.
Пример: Шаг 5: вычислить m (Z) в граммах
- Позволяет ли этот последний шаг решить проблему? Если да, то у вас есть основа для вашего плана!
Шаг 3: Прочтите свои шаги и решите, нужно ли вам использовать формулу (уравнение) , и запишите это как часть этого шага:
| Шаг 1: | запишите вычисленное химическое уравнение реакции между X и Y с образованием Z |
| Шаг 2: | найдите n (x): n (z), используя вычисленное химическое уравнение |
| Шаг 3: | вычислить n (X) n (X) = c (X) x V (X) |
| Шаг 4: | использовать мольное соотношение для расчета n (Z) |
| Шаг 5: | вычислить m (Z) в граммах м (Z) = n (Z) x M (Z) |
Шаг 4: Прочитайте ваши шаги еще раз и поместите информацию , которую вам дали , под заголовком для соответствующего шага.
| Шаг 1: | запишите вычисленное химическое уравнение реакции между X и Y с образованием Z |
| Шаг 2: | найдите n (x): n (z), используя вычисленное химическое уравнение |
| Шаг 3: | вычислить n (X) п (Х) = с (Х) х V (Х) c (X) = 0,010 моль л -1 В (Х) = 25. |
| Шаг 4: | использовать мольное соотношение для расчета n (Z) |
| Шаг 5: | вычислить m (Z) в граммах м (Z) = n (Z) x M (Z) |
Шаг 5: Прочтите шаги еще раз. Вам нужно сделать какие-либо предположения , чтобы решить проблему? Если да, запишите их на этом этапе:
| Шаг 1: | запишите вычисленное химическое уравнение реакции между X и Y с образованием Z |
| Шаг 2: | найдите n (x): n (z), используя вычисленное химическое уравнение |
| Шаг 3: | вычислить n (X) п (Х) = с (Х) х V (Х) с (Х) = 0.010 моль л -1 V (X) = 25,0 мл |
| Шаг 4: | использовать мольное соотношение для расчета n (Z) предполагаем, что реакция завершается |
| Шаг 5: | вычислить m (Z) в граммах м (Z) = n (Z) x M (Z) |
Шаг 6: Нужна ли вам дополнительная информация ? , например, нужно ли вам использовать Периодическую таблицу для определения относительных атомных масс? Или вам нужно использовать таблицу данных, чтобы найти физическую / химическую константу? Если да, запишите это в соответствующем шаге:
| Шаг 1: | запишите вычисленное химическое уравнение реакции между X и Y с образованием Z |
| Шаг 2: | найдите n (x): n (z), используя вычисленное химическое уравнение |
| Шаг 3: | вычислить n (X) п (Х) = с (Х) х V (Х) с (Х) = 0.010 моль л -1 V (X) = 25,0 мл |
| Шаг 4: | использовать мольное соотношение для расчета n (Z) предположим, что реакция завершится |
| Шаг 5: | вычислить m (Z) в граммах используйте таблицу Менделеева для определения относительных атомных масс элементов, составляющих соединение Z рассчитать M (Z), используя относительные атомные массы м (Z) = n (Z) x M (Z) |
Шаг 7: Вам нужно преобразовать единиц в , чтобы все используемые вами единицы были согласованы? Например, вам нужно преобразовать объем в мл в объем в л? Если да, добавьте это к соответствующему шагу:
| Шаг 1: | запишите вычисленное химическое уравнение реакции между X и Y с образованием Z |
| Шаг 2: | найдите n (x): n (z), используя вычисленное химическое уравнение |
| Шаг 3: | вычислить n (X) п (Х) = с (Х) х V (Х) с (Х) = 0.010 моль л -1 V (X) = 25,0 мл преобразовать V (X) в мл в V (X) в л (поскольку концентрация выражена в молях на л) |
| Шаг 4: | использовать мольное соотношение для расчета n (Z) предположим, что реакция завершится |
| Шаг 5: | вычислить m (Z) в граммах используйте Периодическую таблицу, чтобы найти относительные атомные массы элементов, составляющих соединение Z рассчитать M (Z), используя относительные атомные массы м (Z) = n (Z) x M (Z) |
Шаг 8: Прочтите шаги еще раз.Переходит ли шаг 1 логически к шагу 2, затем к шагу 3 и т. Д.?
Если кажется, что все это имеет смысл, то пора реализовать план игры!
GO! с планом игры
Если вы подготовили хороший план игры, описанный выше, все, что вам нужно сделать, это следовать каждому шагу, который вы написали.
Если вы обнаружите, что в вашем плане игры есть пробелы, то есть вещи, которые вам нужны, но еще не включены, пора сделать паузу! и внимательно прочитайте каждый шаг в своем плане игры, внося необходимые дополнения, ПРЕЖДЕ, чем вы продолжите реализацию плана игры.
Подставляйте значения в уравнения по мере продвижения, шаг за шагом, и вычисляйте каждое значение по мере его появления.
Когда вы выполните последний шаг в своем плане игры, вы должны искать решение проблемы.
На этом этапе важно сделать ПАУЗУ! и вдумайтесь!
ПАУЗА! Обдумайте правдоподобность своего решения
Прежде чем вы назовете эту проблему «завершенной» и перейдете к следующей проблеме, подумайте о своем решении в связи с заданным вопросом.
Шаг 1: Вы действительно ответили на заданный вопрос?
Прежде, чем вы рассмеетесь, я должен вам сказать, что одна из многих жалоб на экзаменационные работы студентов заключается в том, что студенты НЕ ответили на заданный вопрос … так что давайте продолжим …
Прочтите вопрос еще раз.
Прочтите свое решение.
Дает ли ваше решение ответ на заданный вопрос?
Проверьте это, задав себе следующий вопрос: «Если бы я дал свое решение проблемы кому-то, кто не читал проблему, могли бы они угадать, какой вопрос был задан?»
Если ваше решение действительно ответит на вопрос… отличная работа!
Но если этого не произойдет … ОСТАНОВИТЕСЬ прямо здесь! Вернитесь к началу процесса решения проблемы!
Шаг 2: Разумно ли ваше решение?
Одна из наиболее распространенных ошибок, которые студенты допускают при сдаче экзаменационных работ, заключается в том, что они неправильно или пренебрегают преобразованием единиц измерения, в результате чего получается неправильный ответ на несколько порядков (множитель 10).
Вы можете проверить, кажется ли ваше решение разумным во многих отношениях, вот несколько:
- Получите цифру о парке мячей и посмотрите, как она соотносится с вашим ответом.
То есть округлите все числа, которые вы используете, в большую или меньшую сторону до ближайших 5 или 10, например, 0,89, потому что 1, 22,76 станет 20 и т. Д., А затем используйте эти округленные числа для быстрых вычислений в уме, просто чтобы проверить что вы не на порядки.
Д., А затем используйте эти округленные числа для быстрых вычислений в уме, просто чтобы проверить что вы не на порядки.Если вы в конечном итоге получите число мячей 50, а решение, которое вы тщательно рассчитали, было 64,71, вы выглядите хорошо, но если ваше тщательно рассчитанное решение было 0,6471, это указывает на то, что где-то что-то ужасно не так, поэтому пора ОСТАНОВИТЬ и вернитесь к началу процесса решения проблемы.
- Должно ли число быть больше или меньше заданного?
Если вопрос касается, например, разбавления раствора, то концентрация раствора после разбавления будет меньше, чем концентрация раствора до его разбавления.
Если ваш ответ дает концентрацию разбавленного раствора выше, чем исходный раствор, ОСТАНОВИТЕСЬ и вернитесь к началу процесса решения проблемы.
Если реакция выделяет энергию (экзотермическая), температура реакционной смеси должна повыситься, если ваш ответ показывает падение температуры, вам нужно ОСТАНОВИТЬ и вернуться к началу процесса решения проблемы.

Точно так же, если температура реакционной смеси увеличилась, поскольку реакция выделяла тепло, но ваш ответ дает положительное (а не отрицательное) значение для изменения энтальпии, вам нужно ОСТАНОВИТЬ и вернуться к началу решения проблемы. процесс.
- Вернитесь назад, используя свой ответ, чтобы вычислить одну из известных величин, указанных в вопросе (или используйте все известные величины и ваше значение для неизвестного, чтобы вычислить значение константы в уравнении) и т. Д.
Шаг 3: Убедитесь, что все данные, которые вы использовали, верны.
Да, это еще одна распространенная ошибка экзаменационных работ.
Проверьте, например, формулу ионов; сульфат — SO 4 2-, сульфит — SO 3 2- , сульфид — S 2-
Убедитесь, что химические уравнения правильно сбалансированы.
Убедитесь, что вы использовали правильное стехиометрическое (мольное) соотношение.
Убедитесь, что вы использовали правильную формулу (уравнение) при каждом расчете.
Если вы изменили формулу, убедитесь, что вы сделали это правильно, например, если c = n / V, то V = n / c
Убедитесь, что вы использовали правильные единицы измерения и что все используемые единицы согласованы.
Убедитесь, что у вас есть соответствующее количество значащих цифр, например, если вам дали pH = 1,32, концентрация ионов водорода НЕ будет 0,047863!
Шаг 4: Проверьте правописание!
Есть некоторые орфографические ошибки, которые, вероятно, не будут волновать экзаменаторов, например, там / их / они, где / носят и т. Д.
Но некоторые орфографические ошибки, например, алкан / алкен / алкин (огромная разница в реакционной способности, во-первых!), Гарантированно лишат вас отметки.
Шаг 5: Убедитесь, что научные принципы, которые вы применили, действительны для этой проблемы.
Это также означает проверку любых предположений, которые вы могли сделать.
Если вы проверили все вышеперечисленное, то пора ….
СТОП!
Если после выполнения шага ПАУЗА для размышления, описанного выше, все выглядело хорошо, значит, проблема решена.
Запишите свое решение проблемы.
Прекратите работу над этой проблемой.
Если, однако, есть некоторые сомнения в ценности или качестве вашего ответа после прохождения вышеуказанных проверок, вам следует ОСТАНОВИТЬ здесь и начать процесс решения проблемы снова, с самого начала, с шага 1.
Сноски:
(1) Этот подход основан на подходе Пойи к решению задач по математике, который я всегда называю «оружием деконструкции математики», но это хороший общий подход к решению задач.
Polya, G. Как решить ; 2 д изд .; Издательство Принстонского университета: Принстон, Нью-Джерси, 1985.
Онлайн-программа для решения проблем химии | Домашнее задание по химии
Если эти странные уравнения, записанные учителем химии на классной доске, сводят вас с ума, не нужно мучить себя. Благодаря цифровому и технологическому прогрессу вы можете найти решение химических проблем для любого случая. Вот некоторые из них, которые вы можете использовать.
- Chem Wiz
- Калькулятор pH
- Балансировка химических уравнений
- Калькулятор кротов
- Калькулятор периодов полураспада (реакция второго порядка)
- Номенклатура
- Калькулятор химических реакций
- Калькулятор молярности Philip Harris
- Калькулятор химических реакций
- Балансир реакции
- Калькулятор частотного коэффициента
- Поиск элементов
- Generador de Estructuras de Lewis ITPA
- Калькулятор периодов полураспада (реакция нулевого порядка)
- Калькулятор pH
- Виджет VSEPR
- Калькулятор электронной конфигурации
- Оксид
- Фазовая диаграмма
- Химическая формула
- Элементы периодической таблицы
- Калькулятор валентности оболочки
- Химическая структура
- Калькулятор температуры воспламенения
- Найти и преобразовать массу по формуле грамма
- Этикетки NFPA для химических веществ
- Структура Льюиса
- Калькулятор периодов полураспада (реакция первого порядка)
- Идентификатор соединения
- Генератор трехмерной химической структуры
- Закон об идеальном газе
- Создатель молекулярной структуры
- Ящик для химикатов
- Калькулятор решений
- JOULES в eV
- Онлайн-решение проблем
- градусов
- Калькулятор молярной массы
- Таблица реактивов Свойства II
- Калькулятор плотности воды
- Конвертер молей
- Калькулятор массового дефекта
- Определение постоянной скорости
- Поиск структуры Льюиса
- Калькулятор таблицы реагентов — настольный гаджет
- Поиск элемента
- Калькулятор pH для слабых кислот
10 лучших справочных приложений по химии
Химия — молярная масса Это приложение предназначено как для iPhone, так и для iPad |
Химическая формула Практика бесплатно Это приложение предназначено как для iPhone, так и для iPad |
Химия и периодическая таблица Это приложение предназначено как для iPhone, так и для iPad |
Основы органической химии Это приложение предназначено как для iPhone, так и для iPad |
Банк тестов по органической химии Lite Это приложение предназначено как для iPhone, так и для iPad |
Решение задач по химии для всех студентов-химиков
Когда вам нужно рассчитать молярную массу или уравновесить химическое уравнение, вы можете рассчитывать на решение химических задач, которое поможет вам. Этот инструмент достаточно всеобъемлющий. Это полезно для любого студента, независимо от типа и уровня курса химии, который он или она изучает. Если вам сложно что-то понять, решатель проблем поможет вам в процессе обучения. Если у вас есть опыт и навыки, это позволит вам сэкономить массу времени при выполнении домашней работы. Инструмент интуитивно понятен и очень прост в использовании.
Этот инструмент достаточно всеобъемлющий. Это полезно для любого студента, независимо от типа и уровня курса химии, который он или она изучает. Если вам сложно что-то понять, решатель проблем поможет вам в процессе обучения. Если у вас есть опыт и навыки, это позволит вам сэкономить массу времени при выполнении домашней работы. Инструмент интуитивно понятен и очень прост в использовании.
Домашнее задание по химии поможет получить хорошие оценки
Химия — это раздел науки, который учит студентов, как вещества ведут себя и взаимодействуют друг с другом.Это очень интересный предмет, который расширяет знания учащихся об элементах и принципах, регулирующих эти элементы. Но одна и та же химия оказывается сложной задачей для многих студентов, которые не могут запомнить формулы и уравнения, необходимые для понимания предмета. Это факт, что студенты должны запоминать множество формул и свойств веществ и газов, помимо запоминания того, как они реагируют с другими веществами и газами. Именно эти знания пригодятся при поиске ответов на домашние задания по химии, которые ставят учителя в школе.Для таких студентов, которые боятся химии, особенно формул этого предмета, становится важным организовать домашнее задание по химии, чтобы иметь возможность выполнять свои задания.
Именно эти знания пригодятся при поиске ответов на домашние задания по химии, которые ставят учителя в школе.Для таких студентов, которые боятся химии, особенно формул этого предмета, становится важным организовать домашнее задание по химии, чтобы иметь возможность выполнять свои задания.
Вам действительно нужна помощь, если вы не запомнили символы и значения
Если вы оказались одним из тысяч студентов, которые боятся химии из-за имен, символов и формул, которые вам нужно запомнить, чтобы решать задачи, вы повезло. Теперь вы можете получать домашние задания по химии, сидя дома, и то же самое с помощью всего лишь нескольких щелчков мышью на компьютере.Да, существует множество порталов, на которых можно найти ответы на домашние задания по химии учащимся, которые не могут выполнять задания, данные им учителями в школе. Конечно, вы платите небольшую сумму за такую услугу, но представьте себе комфорт и удобство, связанные с такой услугой.
Держитесь подальше от бесплатных онлайн-ресурсов
Если вас интересует программа для решения проблем химии , но вам трудно запомнить символы, валентности, свойства и характеристики различных веществ, лучший способ действий для вас — зарегистрироваться на веб-сайте или у онлайн-преподавателя, который может решить ваши проблемы в кратчайшие сроки. Хотя есть также репетиторы и веб-сайты, которые бесплатно предоставляют домашние задания по химии, вам лучше работать с веб-сайтами, которые взимают небольшую плату за свои услуги. Это связано с тем, что вы можете застрять в критический момент и не получить ответ на опубликованную вами проблему в случае бесплатного обслуживания. Это может нарушить ваши расчеты и снизить ваши оценки на выпускном экзамене. Чтобы избежать всего этого и получить быструю и эффективную помощь с домашним заданием по химии, разумно выбирайте онлайн-справку.
Хотя есть также репетиторы и веб-сайты, которые бесплатно предоставляют домашние задания по химии, вам лучше работать с веб-сайтами, которые взимают небольшую плату за свои услуги. Это связано с тем, что вы можете застрять в критический момент и не получить ответ на опубликованную вами проблему в случае бесплатного обслуживания. Это может нарушить ваши расчеты и снизить ваши оценки на выпускном экзамене. Чтобы избежать всего этого и получить быструю и эффективную помощь с домашним заданием по химии, разумно выбирайте онлайн-справку.
Есть несколько веб-сайтов, на которых работают лучшие из имеющихся специалистов в области химии.Эти эксперты остаются в распоряжении веб-сайта и в короткие сроки отвечают на вопросы зарегистрированных студентов. Из обзоров этих сайтов нужно убедиться в эффективности решателя домашних заданий по химии. Многие веб-сайты утверждают, что взломали вопросы из сотен учебников по химии. Вам нужно выбрать компанию с лучшими отзывами студентов. Если вы проведете небольшое исследование, прежде чем закончить онлайн-справку, вам никогда не придется беспокоиться о том, «как делать домашнее задание по химии» дома, не получив помощи от родителей, братьев и сестер.
Chemistry Step-by-Step Solutions: Химические реакции — Блог Wolfram
Если вы изучаете химию или изучаете дисциплину, требующую обязательных курсов по химии, то вы знаете, насколько дорогими могут быть необходимые учебники. Чтобы бороться с этим, сообщество химического образования разработало открытые образовательные ресурсы, чтобы предоставить бесплатные учебники химии. Однако, хотя бесплатные учебники хранят деньги в вашем кошельке, они не содержат руководств по решению всех домашних задач.
К счастью, функция «Пошаговые решения» в Wolfram | Alpha вас поддержала! Независимо от того, учитесь ли вы удаленно или сотрудничаете с помощью видеоконференцсвязи, Wolfram | Alpha поможет вам изучить и применить фреймворки для решения проблем с химическими текстами. Пошаговые решения содержат пошаговые руководства по решениям, которые можно просматривать по очереди или все сразу. Руководства не только оттачивают эффективное решение проблем, но и способствуют более глубокому изучению концепций, которые все еще могут быть неясными.
В течение следующих нескольких недель мы будем изучать некоторые популярные темы, с которыми учащиеся средних школ, старшеклассников и колледжей сталкиваются на курсах химии и выпускных экзаменах: химические реакции, структура и связывание, химические растворы и, наконец, квантовая химия. Прочтите, например, о проблемах химических реакций и их пошаговых решениях!
Балансировка химических уравнений
Фундаментальный аспект химии — уравновешивание химических уравнений. Если химические уравнения — это язык, на котором выражаются химические процессы, то сбалансированные химические уравнения — это соответствующая грамматика.Пошаговое решение проведет вас через надежный алгебраический подход к определению стехиометрических коэффициентов.
Пример проблемы
Напишите сбалансированное уравнение реакции меди с азотной кислотой с образованием нитрата меди, оксида азота и воды.
Пошаговое решение
Для этого класса задач просто введите «баланс медь + азотная кислота -> нитрат меди + диоксид азота + вода».
Масса
После уравновешивания соответствующих химических уравнений следующим шагом в планировании лабораторного эксперимента является вычисление количества каждого реагента, которое необходимо отмерить.Для этого нужна молярная масса каждого реагента. Доступны пошаговые решения для молекулярной массы и относительной молекулярной массы в дополнение к молярной массе. Во всех случаях общая структура для решения этих типов проблем предоставляется на этапе «Планирование». Предоставляется подробная информация о том, какую формулу использовать и как собрать необходимую информацию.
Пример проблемы
Рассчитайте молярную массу сульфата серебра Ag 2 SO 4 .
Пошаговое решение
В этом случае просто введите «молярная масса сульфата серебра».
Массовый состав
Одним из способов анализа отдельных химических веществ является вычисление и сравнение массовых и атомных процентов. Пошаговое решение обеспечивает общую основу для решения этого класса проблем на этапе «Планирование». Предоставляется подробная информация о соответствующих уравнениях, а также о том, как вычислить необходимые промежуточные значения. Способы, которыми вы можете проверить свою работу во время расчетов, также доступны с помощью кнопок «Показать промежуточные шаги».
Предоставляется подробная информация о соответствующих уравнениях, а также о том, как вычислить необходимые промежуточные значения. Способы, которыми вы можете проверить свою работу во время расчетов, также доступны с помощью кнопок «Показать промежуточные шаги».
Пример проблемы
Антигемофильный фактор — коагулянт с формулой C 11794 H 18314 N 3220 O 355 S 83 .Каков его процентный состав?
Пошаговое решение
Для ответа просто введите «элементный состав антигемофильного фактора».
Химическая конверсия
Химические превращения возникают почти в каждом домашнем задании по химии или в каждой исследовательской задаче. Таким образом, доступны пошаговые решения для преобразования между молями, массой, объемом, молекулами и атомами. Предоставляется преобразование единиц измерения и подробный анализ размеров.
Пример проблемы
Сколько атомов в пяти миллилитрах единицы.5 мМ раствор гидроксида магния?
Пошаговое решение
Чтобы решить эту проблему, просто введите «преобразовать 5 мл 1,5 мМ гидроксида магния в атомы».
Стехиометрия
После проведения химической реакции часто хочется узнать, как протекает реакция, вычисляя выходы реакции. Доступны пошаговые решения для расчета количества необходимых реагентов и теоретического выхода в дополнение к процентному выходу. Подробно объясняется использование стехиометрических факторов для получения желаемых значений.
Пример проблемы
При взаимодействии 1,274 грамма сульфата меди с избытком металлического цинка было получено 0,392 грамма металлической меди в соответствии со следующим уравнением: CuSO 4 (водн.) + Zn (s) & xrarr; Cu (s) + ZnSO 4 (водн.). Какой процент доходности?
Пошаговое решение
Чтобы найти процентный выход, просто добавьте значения массы к соответствующим химическим соединениям и запросите стехиометрию: «1,274 г CuSO4 + Zn -> 0,392 г Cu + ZnSO4, стехиометрия».
Задачи вызова
Проверьте свои навыки решения проблем с химическими реакциями, используя описанные инструменты Wolfram | Alpha для решения этих текстовых задач. Ответы будут предоставлены в следующем сообщении в блоге этой серии.
Ответы будут предоставлены в следующем сообщении в блоге этой серии.
- Вычислите молекулярную массу ацетаминофена. Является ли элемент с наибольшим количеством атомов элементом с наибольшим массовым процентом?
- Каков предельный реагент и теоретический выход при 24,8 граммах белого фосфора и 0.200 молей кислорода реагируют с образованием 10,0 граммов пятиокиси фосфора?
и больше химии в будущем
Готовитесь ли вы к предстоящим выпускным экзаменам, решаете ли вы домашнее задание или просто хотите освежиться, химические реакции — одна из многих тем по химии, охватываемых базой знаний Wolfram | Alpha. На следующей неделе мы рассмотрим пошаговые инструкции для химических растворов, затем структуру и связывание, а затем квантовую химию. Если у вас есть предложения по другому пошаговому содержанию (по химии или другим предметам), сообщите нам об этом! Вы можете связаться с нами, оставив комментарий ниже или отправив отзыв внизу любой страницы запроса Wolfram | Alpha.
Молекулярная формула и пример простейшей формулы Задача
Молекулярная формула соединения перечисляет все элементы и количество атомов каждого элемента, которые фактически составляют соединение. Самая простая формула аналогична, когда все элементы перечислены, но числа соответствуют соотношениям между элементами. Этот рабочий пример задачи демонстрирует, как использовать простейшую формулу соединения и его молекулярную массу, чтобы найти молекулярную формулу.
Молекулярная формула из задачи простейшей формулы
Простейшая формула витамина C: C 3 H 4 O 3 . Экспериментальные данные показывают, что молекулярная масса витамина С составляет около 180. Какова молекулярная формула витамина С?
Решение
Сначала вычислите сумму атомных масс для C 3 H 4 O 3 . Найдите атомные массы для элементов из Периодической таблицы. Атомные массы оказались равными:
H = 1.01
C составляет 12,01
O составляет 16,00
Подставляя эти числа, сумма атомных масс для C 3 H 4 O 3 составляет:
3 (12,0) + 4 (1,0) + 3 (16,0 ) = 88,0
Это означает, что формула массы витамина С равна 88,0. Сравните формулу массы (88,0) с приблизительной молекулярной массой (180). Молекулярная масса в два раза превышает формульную массу (180/88 = 2,0), поэтому простейшую формулу нужно умножить на 2, чтобы получить молекулярную формулу:
Сравните формулу массы (88,0) с приблизительной молекулярной массой (180). Молекулярная масса в два раза превышает формульную массу (180/88 = 2,0), поэтому простейшую формулу нужно умножить на 2, чтобы получить молекулярную формулу:
молекулярная формула витамин C = 2 x C 3 H 4 O 3 = C 6 H 8 O 6
Ответ
C 6 H 8 O 6
Советы по устранению рабочих проблем
Приблизительной молекулярной массы обычно достаточно для определения формулы массы, но расчеты, как правило, не работают «даже», как в этом примере.Вы ищете ближайшее целое число, которое нужно умножить на формулу массы, чтобы получить молекулярную массу.
Если вы видите, что соотношение между формульной массой и молекулярной массой составляет 2,5, возможно, вы смотрите на соотношение 2 или 3, но более вероятно, что вам нужно умножить формулу массы на 5. Часто в процессе проб и ошибок получение правильного ответа. Хорошая идея — проверить свой ответ, выполнив математические вычисления (иногда более чем одним способом), чтобы увидеть, какое значение ближе всего.
Хорошая идея — проверить свой ответ, выполнив математические вычисления (иногда более чем одним способом), чтобы увидеть, какое значение ближе всего.
Если вы используете экспериментальные данные, в расчете молекулярной массы будет некоторая ошибка.Обычно соединения, назначаемые в лабораторных условиях, будут иметь отношения 2 или 3, а не большие числа, такие как 5, 6, 8 или 10 (хотя эти значения также возможны, особенно в лаборатории колледжа или в реальных условиях).
Стоит отметить, что в то время как химические задачи решаются с использованием молекулярных и простейших формул, реальные соединения не всегда подчиняются правилам. Атомы могут иметь общие электроны, например, в соотношении 1,5. Однако при выполнении домашних заданий по химии используйте целые числа!
Определение молекулярной формулы по простейшей формуле
Формульная задача
Самая простая формула бутана — это C2H5, а его молекулярная масса составляет около 60.Какова молекулярная формула бутана?
Решение
Сначала вычислите сумму атомных масс для C2H5. Найдите атомные массы для элементов из Периодической таблицы. Атомные массы оказываются равными:
Найдите атомные массы для элементов из Периодической таблицы. Атомные массы оказываются равными:
H составляет 1,01
C составляет 12,01
Подставляя эти числа, сумма атомных масс для C2H5 составляет:
2 (12,0) + 5 (1,0) = 29,0
Это означает, что формула массы бутана 29,0. Сравните формулу массы (29,0) с приблизительной молекулярной массой (60). Молекулярная масса практически вдвое превышает формульную массу (60/29 = 2.1), поэтому простейшую формулу нужно умножить на 2, чтобы получить молекулярную формулу:
молекулярная формула бутана = 2 x C2H5 = C4h30
Ответ
Молекулярная формула бутана — C4h30.
Арифметика химических формул
1 Как читать и писать формулы
Формула соединения определяет количество атомов каждого типа, присутствующих в одной молекулярной единице соединения. Поскольку каждое уникальное химическое вещество имеет определенный состав, каждое такое вещество должно быть описано с помощью
химическая формула.
Пример задачи 1: запись молекулярной формулы
Хорошо известный спирт этанол состоит из молекул, содержащих два атома углерода, пять атомов водорода и один атом кислорода. Какова его молекулярная формула?
Решение: Просто напишите символ каждого элемента, за которым следует нижний индекс, указывающий количество атомов, если их больше одного.Таким образом: C 2 H 5 O
Обратите внимание:
- Число атомов каждого элемента записывается в нижнем индексе;
- Когда присутствует только один атом элемента, нижний индекс опускается.
- В случае органических (углеродсодержащих) соединений в формуле принято помещать символы элементов C, H, (и, если есть,) O, N в указанном порядке.
Формулы элементов
Символ элемента — это одно- или двухбуквенная комбинация, которая представляет атом определенного элемента, например Au (золото) или O (кислород). Символ может использоваться как аббревиатура для имени элемента (это
Символ может использоваться как аббревиатура для имени элемента (это
проще написать «Mb» вместо «молибден»!) В более формальном химическом использовании символ элемента может также обозначать один атом или, в зависимости от контекста, один моль (число Авогадро) атомов элемента .
Различные молекулярные формы одного и того же элемента (например, O 2 и O 3 ) называются аллотропами .
Некоторые из неметаллических элементов существуют в форме молекул, содержащих два или более атомов элемента. Эти молекулы описываются формулами , такими как N 2 , S 6 и P 4 . Некоторые из этих элементов
может образовывать более одного вида молекул; наиболее известным примером этого является кислород, который может существовать как O 2 (обычная форма, составляющая 21% молекул в воздухе), а также как O 3 , нестабильный и очень реактивный
Молекула, известная как озон . Углеродные молекулы в форме футбольного мяча, которые иногда называют бакиболлы , имеют формулу C 60 .
Углеродные молекулы в форме футбольного мяча, которые иногда называют бакиболлы , имеют формулу C 60 .
Формулы ионов
Ионы — это атомы или молекулы, несущие электрический заряд. Эти заряды представлены в ионных формулах в виде верхних индексов. Таким образом:
| Класс — | хлорид-ион, с одним отрицательным зарядом на атом |
| S 2– | сульфид-ион несет два отрицательных заряда |
| HCO 3 2– | ион гидрокарбоната («бикарбонат») — молекулярный ион |
| NH 4 + | ион аммония |
Обратите внимание, что количество зарядов (в единицах заряда электрона) всегда должно предшествовать положительному или отрицательному знаку, но это число опускается, если заряд равен ± 1.
Формулы расширенных твердых тел и минералов
В твердом CdCl 2 атомы Cl и Cd организованы в бесконечно протяженные слои. Каждый атом окружен шестью атомами противоположного типа, поэтому можно произвольно выбрать любую единицу CdCl 2 в качестве «молекулярной единицы». Одна такая единица обозначена двумя связями красного цвета на диаграмме, но она не составляет дискретную «молекулу» CdCl 2 .
Многие на первый взгляд «простые» твердые тела существуют только в виде ионных твердых частиц (например, NaCl) или протяженных твердых частиц (например, CuCl 2 ), в которых нет дискретных молекул.
можно идентифицировать. Формулы, которые мы пишем для этих соединений, просто выражают относительные числа различных типов атомов в соединении в наименьших возможных целых числах. Они идентичны эмпирическим или «простейшим»
формулы, которые мы обсудим далее.
Многие минералы и большинство горных пород содержат различные соотношения определенных элементов и могут быть точно охарактеризованы только на структурном уровне. Поскольку это обычно не чистые вещества, «формулы», обычно используемые для их описания
Поскольку это обычно не чистые вещества, «формулы», обычно используемые для их описания
имеют ограниченное значение.
Например, оливин обыкновенной породы, который можно рассматривать как твердый раствор Mg 2 SiO 4 и Fe 2 SiO 4 , может быть представлен как (Mg, Fe) 2 SiO 4 .Это означает, что отношение
содержание металлов в SiO 4 постоянно, и магний обычно присутствует в большем количестве, чем железо.
Эмпирические «простейшие» формулы
Эмпирические формулы дают относительных номеров различных элементов в образце соединения, выраженных в наименьших возможных целых числах.Термин эмпирический относится к тому факту, что формулы такого рода
определяются экспериментально; такие формулы также обычно называют простейшими формулами .
Пример задачи 2: Простейшая формула из молекулярной формулы
Глюкоза («топливо», на котором работает ваше тело) состоит из молекулярных единиц, имеющих формулу C 6 H 12 O 6 . Какая эмпирическая формула глюкозы?
Какая эмпирическая формула глюкозы?
Раствор: Молекула глюкозы содержит в два раза больше атомов водорода, чем углерод или кислород, поэтому мы разделим на 6, чтобы получить CH 2 O .
Примечание: эта простейшая формула, которая применяется ко всем 6-углеродным сахарам, указывает, что эти соединения «состоят» из углерода и воды, что объясняет, почему сахара известны как углеводов .
Некоторые твердые соединения не существуют в виде дискретных молекулярных единиц, а построены в виде протяженных двух- или трехмерных решеток атомов или ионов. Составы таких соединений обычно описываются их простейшими формулами. в
очень распространенный случай ионных твердых частиц , такая формула также выражает минимальное количество положительных и отрицательных ионов, необходимых для создания электрически нейтрального элемента, как в NaCl или CuCl 2 .
Пример проблемы 3: Молекулярная формула для ионных зарядов
a) Напишите формулу бромида трехвалентного железа, учитывая, что ион трехвалентного железа (III) — это Fe 3+ , а ион бромида несет единственный отрицательный заряд.
b) Напишите формулу сульфида висмута, образующегося при соединении ионов Bi 3+ и S 2– .
Решение:
a) Три иона Br — необходимы для уравновешивания трех положительных зарядов Fe 3+ , отсюда формула FeBr 3 .
b) Единственный способ получить равное количество противоположных зарядов — иметь шесть зарядов каждого, поэтому формула будет Bi 2 S 3 .
Какие формулы
не говорят нам
Формулы, которые мы обычно пишем, не передают никакой информации о структуре соединения — то есть о порядке, в котором атомы связаны химическими связями или расположены в трехмерном пространстве.Это ограничение
особенно важно для органических соединений, в которых сотни, если не тысячи различных молекул могут иметь одну и ту же эмпирическую формулу.
Соединения этанола и диметилового эфира имеют простейшую формулу C 2 H 6 O. Структурные формулы показывают совершенно разную природу этих двух молекул:
Структурные формулы показывают совершенно разную природу этих двух молекул:
Формулы могут быть составлены для передачи структурной информации
Часто бывает полезно писать формулы таким образом, чтобы передать хотя бы некоторую информацию о структуре соединения.Например, формула твердого вещества (NH 4 ) 2 CO 3 сразу идентифицируется.
как карбонат аммония и по существу соединение ионов аммония и карбоната в соотношении 2: 1, тогда как простейший или эмпирическая формула N 2 H 8 CO 3 скрывает эту информацию.
Точно так же различие между этанолом и диметиловым эфиром можно провести, записав формулы как C 2 H 5 OH и CH 3 –O – CH 3 соответственно.Хотя ни одна из этих формул не указывает
структуры, любой, кто изучал органическую химию, может их вычислить и сразу же распознает группу –OH (гидроксил), которая является определяющей характеристикой большого класса известных органических соединений
как спиртов . Атом –O–, связывающий два атома углерода, также является определяющей чертой простых эфиров .
Атом –O–, связывающий два атома углерода, также является определяющей чертой простых эфиров .
2 Формулы подразумевают молярные массы
Несколько связанных терминов используются для выражения массы одного моля вещества.
- Молекулярный вес Это аналог атомного веса: это относительный вес одной формульной единицы соединения по шкале углерода-12. Молекулярная масса определяется сложением атомных масс всех атомов.
присутствует в формульной единице. Молекулярные веса, как и атомные веса, безразмерны; т.е. у них нет единиц. - Формула веса То же, что и молекулярная масса.Этот термин иногда используется в связи с ионными твердыми телами и другими веществами, в которых отсутствуют дискретные молекулы.
- Молярная масса Масса (в граммах, килограммах или любой другой единице массы) одного моля частиц или формульных единиц. Выраженная в граммах молярная масса численно совпадает с молекулярной массой, но должна сопровождаться
единицей массы.
Пример задачи 4: Формула веса и молярной массы
a) Рассчитайте формулу веса хлорида меди (II), CuCl 2 .
b) Как бы вы выразили это же количество как молярной массы ?
Решение:
a) Атомные массы Cu и Cl составляют соответственно 63,55 и 35,45; сумма каждого атомного веса, умноженная на количество атомов каждого типа в формульной единице, дает 63,55 + 2 (25,35) = 134,45 .
б) Масса одного моля атомов Cu и Cl соответственно равна 63.55 г и 35,45 г; масса одного моля CuCl 2 единиц равна (63,55 г) + 2 (25,35 г) = 134,45 г .
Мольные отношения и мольные доли из формул
Информация, содержащаяся в формулах, может использоваться для сравнения составов родственных соединений, как в следующем примере:
Пример задачи 5: расчет мольного отношения
Отношение водорода к углероду часто представляет интерес при сравнении различных видов топлива. Рассчитайте эти отношения для метанола (CH 3 OH) и этанола (C 2 H 5 OH).
Рассчитайте эти отношения для метанола (CH 3 OH) и этанола (C 2 H 5 OH).
Раствор: отношения H: C для двух спиртов составляют 4: 1 = 4,0 для метанола и 6: 2 (3,0) для этанола.
Или же иногда используют мольные доли, чтобы выразить то же самое. Мольная доля элемента M в соединении — это просто количество атомов M, деленное на общее количество атомов в формульной единице.
Пример задачи 6: мольная доля и молярный процент
Рассчитайте мольную долю и молярный процент углерода в этаноле (C 2 H 5 OH).
Раствор: Формульная единица содержит девять атомов, два из которых являются углеродом. Мольная доля углерода в соединении составляет 2/9 = 0,22. Таким образом, 22 процента атомов в этаноле составляют углерод.
Процентный состав и элементные массы из формул
Поскольку формула соединения выражает соотношение количества составляющих его атомов, формула также передает информацию об относительных массах элементов, которые оно содержит. Но для того, чтобы установить эту связь, нам нужно знать
Но для того, чтобы установить эту связь, нам нужно знать
относительные массы различных элементов.
Пример задачи 7: масса каждого элемента в данной массе соединения
Найдите массы углерода, водорода и кислорода в одном моль этанола (C 2 H 5 OH).
Решение: Используя атомные массы (молярные массы) этих трех элементов, мы имеем
углерод: (2 моль) (12.0 г моль –1 ) = 24 г водорода C
: (6 моль) (1,01 г моль –1 ) = 6 г кислорода H
: (1 моль) (16,0 г моль –1 ) = 16 г O
массовая доля элемента в соединении — это просто отношение массы этого элемента к массе всей формульной единицы. Массовые доли всегда находятся в диапазоне от 0 до 1, но часто выражаются в процентах.
Пример задачи 8: массовая доля и массовый процент элемента в соединении
Найдите массовую долю и массовый процент кислорода в этаноле (C 2 H 5 OH)
Решение: Используя информацию, полученную в предыдущем примере, молярная масса этанола составляет (24 + 6 + 16) г моль –1 = 46 г моль –1 . Из них 16 г приходится на кислород, поэтому его массовая доля
Из них 16 г приходится на кислород, поэтому его массовая доля
в соединении составляет (16 г) / (46 г) = 0,35, что соответствует 35%.
Определение процентного содержания соединения по его формуле — это фундаментальный расчет, который вы должны освоить; техника в точности такая, как показано выше. Определение массовой доли часто является первым шагом в решении связанных
видов проблем:
Пример задачи 9: масса элемента в данной массе соединения
Сколько тонн калия содержится в 10 тоннах KCl?
Раствор: Массовая доля K в KCl составляет 39.1 / 74,6 = 0,524; 10 тонн KCl содержат (39,1 / 74,6) × 10 тонн K, или 5,24 тонны K. (Атомный вес: K = 39,1, Cl = 35,5.)
Обратите внимание, что нет необходимости явно иметь дело с молями, что потребовало бы преобразования тонн в кг.
Pro blem Пример 10: масса соединения, содержащего заданную массу элемента
Сколько граммов KCl будет содержать 10 г калия?
Раствор: Массовое отношение KCl / K составляет 74. 6 ÷ 39,1; 10 г калия будет присутствовать в (74,6 / 39,1) × 10 граммах KCl, или 19 граммов .
6 ÷ 39,1; 10 г калия будет присутствовать в (74,6 / 39,1) × 10 граммах KCl, или 19 граммов .
Массовые отношения двух элементов в соединении могут быть найдены непосредственно из мольных соотношений, выраженных в формулах.
Пример задачи 11: Массовое соотношение элементов из формулы
Расплавленный хлорид магния (MgCl 2 ) может быть разложен на элементы, пропуская через него электрический ток.Сколько кг хлора будет выделено при образовании 2,5 кг магния? (Mg = 24,3, Cl = 35,5)
Раствор: Раствор : массовое отношение Cl / Mg составляет (35,5 × 2) / 24,3 или 2,9; таким образом, 2,9 кг хлора будет производиться на каждый кг Mg, или (2,9 × 2,5) = 7,2 кг хлора для 2,5 кг Mg
(обратите внимание, что нет необходимости знать формулу элементарного хлора (Cl 2 ), чтобы решить эту проблему.)
3 Простейшие формулы из экспериментальных данных
Как было объяснено выше, простейшая формула ( эмпирическая формула ) — это формула, в которой относительные числа различных элементов выражены в наименьших возможных целых числах. Хлорид алюминия, например, существует
Хлорид алюминия, например, существует
в виде структурных единиц, имеющих состав Al 2 Cl 6 ; Простейшая формула этого вещества — AlCl 3 .
Простейшие формулы из атомных соотношений
Некоторые методы анализа предоставляют информацию об относительном количестве различных типов атомов в соединении.
Процесс определения формулы соединения на основе анализа его состава зависит от вашей способности распознавать десятичные эквиваленты обычных целочисленных соотношений, таких как 2: 3, 3: 2, 4: 5 и т. Д.
Пример задачи 12: Простейшая формула из мольного отношения
Анализ соединения алюминия показал, что 1,7 моль Al объединяется с 5,1 моль хлора. Напишите простейшую формулу этого соединения.
Раствор: Формула Al 1,7 Cl 5,1 выражает относительные количества молей двух элементов в соединении. Его можно преобразовать в простейшую формулу, разделив оба нижних индекса на меньшие.
один, давая AlCl 3 .
Простейшие формулы из массового состава
Чаще обнаруживается, что произвольная масса соединения содержит определенные массы его элементов.Их необходимо преобразовать в моли, чтобы найти формулу.
Пример задачи 13: Простейшая формула для масс сгорания
Когда 10,0 г определенного органического соединения, содержащего только C, H и O, подвергаются сгоранию в присутствии избытка O 2 , образуется 9,56 г CO 2 и 3,92 г H 2 O. Найдите простейшую формулу
это вещество.
Решение: Начните с вычисления молей двух продуктов сгорания:
CO
2 : (9.56 г) / (44 г моль –1 ) = 0,217 моль
H
2 O: (3,92 г) / (18 г моль –1 ) = 0,218 моль (с содержанием 2 × 0,218 моль = 0,436 моль водорода)
Теперь мы можем записать предварительную формулу соединения как C . 217 H .436 O x , оставив значение x для определения. Самый простой способ сделать это — вычислить разницу
217 H .436 O x , оставив значение x для определения. Самый простой способ сделать это — вычислить разницу
между 10.0 г массы неизвестного соединения и общая масса углерода плюс водород в продуктах сгорания. Последние количества рассчитываются следующим образом: C: (0,217 моль × 12 г моль –1 ) = 2,60 г;
H: (0,436 моль × 1,01 г моль –1 ) = 0,440 г. Масса кислорода в соединении составляет
(10,0 г) — (0,440 + 2,60) г = 6,96 г, что соответствует (6,96 г / 16 г моль –1 ) =
,435 моль. Подставляя это количество в предварительную формулу, получаем C ,217 H ,436 O .435 . С учетом экспериментальной ошибки и ошибки округления это сокращается до CH 2 O 2 .
Комментарий: Эта задача может сначала показаться очень сложной, но на самом деле это просто комбинация ряда почти тривиально простых вычислений, выполняемых в логической последовательности. Ваша способность построить эту последовательность
Ваша способность построить эту последовательность
является неотъемлемой частью решения практических задач такого рода.стоит потратить время на самостоятельную работу над этим упражнением, возможно, начиная с 5,0 г соединения, что даст пропорционально меньшее количество
количество продуктов.
Пример задачи 14: Простейшая формула на основе масс элементов
Образец соединения алюминия массой 4,67 г содержит 0,945 г Al и 3,72 г Cl. Найдите простейшую формулу этого соединения.Атомный вес: Al = 27,0, Cl = 35,45.
Раствор: Образец содержит (0,945 г) / (27,0 г моль –1 ) = 0,035 моль алюминия и (3,72 г) (35,45) = 0,105 моль хлора. Формула Al .035 Cl .105 выражает относительные числа
молей двух элементов в соединении. Его можно преобразовать в простейшую формулу, разделив оба нижних индекса на меньший, что даст AlCl 3 .
Простейшие формулы из соотношений масс
Состав бинарного (двухэлементного) соединения иногда выражают через массовое отношение. Самый простой подход здесь — рассматривать числа, выражающие отношение, как массы, таким образом превращая проблему в тот вид, который описывается немедленно.
Самый простой подход здесь — рассматривать числа, выражающие отношение, как массы, таким образом превращая проблему в тот вид, который описывается немедленно.
выше.
Пример задачи 15: Простейшая формула из отношения масс элементов
Соединение, состоящее только из углерода и кислорода, содержит эти два элемента в массовом соотношении C: H, равном 0.375. Найдите простейшую формулу.
Раствор: Выразите это соотношение как 0,375 г C на 1,00 г O.
моль углерода: (0,375 г) / (12 г / моль) = 0,03125 моль C;
моль кислорода: (1,00 г) / (16 г / моль) = 0,0625 моль O
мольное соотношение C / O = 0,03125 / 0,0625 = 0,5;
это соответствует формуле C 0,5 O, которую мы выражаем целыми числами
как CO 2 .
Простейшие формулы процентного состава
Массовый состав соединения чаще всего выражается в массовых процентах (граммы на 100 граммов соединения). Первый шаг — снова преобразовать их в относительное количество молей каждого элемента в фиксированной массе соединения.
Хотя эта фиксированная масса совершенно произвольна (в 100 граммах нет ничего особенного!), Соотношение и мольных количеств различных элементов не является произвольным: эти отношения должны быть выражены в виде целых чисел, поскольку они
представляют собой отношения целых чисел атомов.
Пример задачи 16: Простейшая формула из массового процента
Найдите простейшую формулу соединения, имеющего следующий массовый процентный состав. В скобках указаны атомные веса.
36,4% Mn (54,9), 21,2% S (32,06), 42,4% O (16,0)
Раствор: В 100 г этого соединения содержится:
Mn: (36.4 г) / (54,9 г моль –1 ) = 0,663 моль
S: (21,2 г) / (32,06 г моль –1 ) = 0,660 моль
O: (42,4 г) / (16,0 г моль — 1 ) = 2,65 моль
Формула Mn .663 S .660 O 2,65 выражает относительное количество молей трех элементов в соединении. Его можно преобразовать в простейшую формулу, разделив все индексы на наименьшие.
один, давая Mn 1.00 S 1,00 O 4,01 который мы записываем как MnSO 4 .
Примечание: поскольку экспериментально определенные массы подвержены небольшим ошибкам, обычно необходимо пренебречь небольшими отклонениями от целых значений.
Пример задачи 17: Простейшая формула из массового процента
Найдите простейшую формулу соединения, имеющего следующий массовый процентный состав.В скобках указаны атомные веса.
27,6% Mn (54,9), 24,2% S (32,06), 48,2% O (16,0)
Раствор: Предварительная формула на основе 100 г этого соединения может быть записана как
Mn (27,6 / 54,9) S (24,2 / 32,06) O (42,4 / 16,0) или Mn .503 S .754 O 3,01
Если разделить на наименьший индекс, получим Mn 1 S 1.5 О 6 . Изучение этой формулы предполагает, что умножение каждого нижнего индекса на 2 дает целочисленную формулу Mn 2 S 3 O 12 .
4 Подробнее об элементном анализе
Элементный анализ в лаборатории
Одна из самых фундаментальных операций в химии состоит из разложения соединения на его элементы (процесс, известного как анализ ) и последующего определения простейшей формулы из относительных количеств каждого типа атомов.
присутствует в соединении.Лишь в очень немногих случаях целесообразно проводить такой процесс напрямую: таким образом, нагревание сульфида ртути (II) приводит к его прямому разложению: 2 HgS → 2Hg + O 2 . Аналогично электролизу
воды образует газы H 2 и O 2 в объемном соотношении 2: 1.
Однако большинство элементных анализов необходимо проводить косвенно. Наиболее широко используемым из этих методов традиционно был анализ горения органических соединений.Неизвестный углеводород C a H b O c можно охарактеризовать, нагревая его в потоке кислорода так, чтобы он полностью разложился на газообразный CO 2 и H 2 O. Эти газы проходят через трубки содержащие вещества, избирательно поглощающие каждый газ.
Эти газы проходят через трубки содержащие вещества, избирательно поглощающие каждый газ.
Путем тщательного взвешивания каждой трубки до и после процесса сгорания можно рассчитать значения a и b для углерода и водорода, соответственно.Индекс c для кислорода находится путем вычитания рассчитанного
массы углерода и водорода из исходного образца.
Справа: иллюстрация из книги Марка Бишопа Введение в химию: онлайн-учебник .
Эта страница также содержит подробные примеры эмпирических
формулы расчетов.
← С 1970-х годов стало возможным проводить анализ горения с помощью автоматизированного оборудования.Также можно определить азот и серу.
Для анализа соединений, содержащих элементы, отличные от C, H и O, в настоящее время широко используются спектроскопические методы, основанные на атомной абсорбции и атомной абсорбции с индуктивно-связанной плазмой.
Весы аналитические
Измерения массы или веса долгое время были основным инструментом для количественного понимания химических изменений. Весы и весы используются в коммерческих и фармацевтических целях с начала регистрации
Весы и весы используются в коммерческих и фармацевтических целях с начала регистрации
истории, но этим устройствам не хватало точности 0,001 г, необходимой для количественного химического и элементного анализа, проводимого в лабораторном масштабе.
Классические равноручные аналитические весы и набор калиброванных гирь
Только в середине 18 века шотландский химик Джозеф Блэк изобрел аналитические весы с равным плечом .Ключевой особенностью этого изобретения было
легкая, жесткая балка, опирающаяся на острие опоры; дополнительные лезвия поддерживали чаши весов. Лезвия лезвий значительно уменьшили трение, которое ограничивало чувствительность предыдущих моделей; это не случайно, что
Примерно в это же время начались точные измерения сочетания весов и атомных весов.
Аналитические весы
помещены в стеклянный корпус, чтобы избежать помех от воздушных потоков, а калиброванные гири обрабатываются пинцетом, чтобы предотвратить адсорбцию влаги или масел с обнаженных пальцев.
Любой, кто изучал общую химию в колледже вплоть до 1960-х годов, вспомнит обучение (и скуку), связанное с этими устройствами. Они могут считываться с точностью до 1 миллиграмма и позволяют делать оценки до ± 0,1 мг. Позже технический
Доработки добавили магнитное демпфирование качания балки, тормоза панорамирования и встроенные наборы грузов, управляемые ручками. Самые лучшие весы исследовательского класса достигли точности 0,001 мг.
Начиная с 1970-х годов, электронных весов получили широкое распространение, особенно популярны были весы с одной чашей весов.Весы с одной чашкой избавляют от необходимости сравнивать вес образца с весом калиброванных гирь.
Добавление образца в чашу вызывает смещение тензодатчика , который генерирует компенсирующее электромагнитное поле достаточной величины, чтобы поднять чашу в исходное положение. Ток, необходимый для выполнения
это воспринимается и преобразуется в измерение веса. Лучшие электронные весы исследовательского класса могут показывать до 1 микрограмма, но 0.
Все формулы по химии для решения задач егэ по
все формулы по химии для решения задач егэ по
Так как химия наука точная, она неразрывно связана с различного рода вычислениями. Чтобы решать задачи, нужно знать формулы и хорошо в них ориентироваться. Без этих базовых знаний и навыков изучение химии становится невозможным.
Мы собрали для вас основные химические формулы, изучаемые в школьном курсе. Они пригодятся каждому ученику, особенно тем, кто будет сдавать ОГЭ или ЕГЭ по этому непростому, но очень интересному предмету.
Нахождение количества вещества
Первое и основное понятие, которое необходимо усвоить – это Количество вещества, измеряемое в молях и обозначающееся латинской буквой «n». Для его нахождения нужно основываться на условии задачи, так как вычислить количество вещества можно по трём формулам:
1) По массе. N=m/M — Массу вещества (в граммах) разделить на его молярную массу (в г/моль).
2) По объёму. N=V/Vm — Отношением объёма вещества к его молярному объёму (используется для газов).
N=V/Vm — Отношением объёма вещества к его молярному объёму (используется для газов).
3) По числу молекул. N=N/NA – Число молекул вещества делённое на число Авогадро. Число Авогадро (NA) – физическая величина, указывающая на число молекул, содержащихся в 1 моле вещества, и численно равная 6,0221 * 10 23 моль -1 .
Формулы для нахождения массы
Массу вещества можно найти несколькими способами:
1. Умножив количество вещества на молярную массу: M (г) = n (моль)×M (г/моль).
2. Произведением объёма раствора и его плотности: M = V (л) ×ρ (г/л).
3. Перемножив массовую долю с массой раствора: M = m(р-ра) × ω.
Молярная масса (М) – это масса одного моля вещества. Вычисляется она следующим образом: посредством сложения атомных масс элементов, из которых состоит вещество, получаем относительную молекулярную массу. Молярная масса численно равна относительной молекулярной массе, но имеет размерность «г/моль». Также молярную массу можно найти с помощью отношения массы вещества к его количеству:
Также молярную массу можно найти с помощью отношения массы вещества к его количеству:
Формулы для нахождения объёма
Для вычисления объёма того или иного вещества можно воспользоваться одной из формул:
1. Объём раствора находится как отношение массы раствора к его плотности:
2. Объём газа равен отношению его количества вещества к молярному объёму:
Молярный объём (VM) – объём, который занимает 1 моль вещества при определённых показателях давления и температуры. Находится при делении молярной массы вещества на его плотность:
При нормальных условиях молярный объём газа равен 22,4 л/моль.
Формулы для нахождения плотности и относительной плотности
Плотность (ρ) – физическая величина, указывающая на массу определённого вещества, содержащуюся в единице объёма.
Следовательно, формула для её вычисления имеет вид:
Помимо основной, существует формула для нахождения плотности газа при нормальных условиях, где молярная масса делится на молярный объём газа при н. у.:
у.:
Относительная плотность (D) газов – величина, указывающая насколько одно вещество тяжелее или легче другого. Вычисляется она отношением молярных масс газов:
Например, условием было найти плотность газа по водороду. Решение будет иметь вид: D = M(газа)/M(h3) = M(газа)/2. Относительная плотность является безразмерной величиной.
Формулы для нахождения концентрации
Молярная концентрация (С) – отношение количества растворённого вещества к объёму раствора. Единица измерения – моль/л. Молярная концентрация вычисляется по формуле:
Массовая концентрация чаще всего называется титром (Т). Это отношение массы растворённого вещества к объёму раствора. Единица измерения — г/л.
Массовая доля (ω) – это один из вариантов выражения концентрации. С её помощью можно вычислить процентное содержание растворённого вещества в общей массе раствора:
По такому же принципу вычисляется массовая доля определённого компонента в смеси:
Ω = (mкомпонента / mсистемы) × 100%
Если возникает необходимость найти массовую долю химического элемента в соединении, то нужно относительную атомную массу этого элемента умножить на число атомов в соединении и разделить на молекулярную массу вещества:
Формулы для нахождения выхода продукта реакции
Под Выходом продукта реакции (ᶯ) подразумевается отношение массы (объёма, количества) вещества, полученного на практике, к теоретически возможному (рассчитанному по уравнению реакции). Единица измерения – доля, а проценты — если результат умножить на 100 !
Единица измерения – доля, а проценты — если результат умножить на 100 !
Для его вычисления, в зависимости от условия задачи, используются следующие формулы:
Попрактиковать решение задач и знание формул возможно в приложении «ХиШник». Оно содержит в себе каталог заданий, которые, в свою очередь, разделены по темам и уровням сложности. Если вы дали неверный ответ, то приложение не просто уведомит об этом, а предложит правильный алгоритм решения. Также в нём есть раздел для подготовки к ОГЭ и ЕГЭ, в котором собраны типовые задания.
Знание расчётных формул – это ключевой момент при решении задач. Главное, понимать их, а не бездумно заучивать. Так как они будут использоваться не только в школьных задачах, на ЕГЭ и ОГЭ, но и в дальнейшей жизни, даже если ваша профессиональная сфера будет далека от химии.
Еще по этой теме:
Серная кислота
Основные сведения о серной кислоте: свойства, получение, применение.
Теперь «ХиШник» стал полностью бесплатным
Как развивалось приложение все эти годы, и почему мы им так гордимся.
Азотная кислота
Статья содержит основную информацию об азотной кислоте: её свойства, получение и применение.
Диены
Основные сведения о диеновых углеводородах: номенклатура и изомерия, классификация, химические свойства, получение.
Правило Марковникова
Правило Марковникова: формулировка, механизм протекания реакций, исключения из правила.
Таблицы для ЕГЭ по химии
В статье представлены таблицы, необходимые при изучении химии и сдаче ЕГЭ.
Внеклассное мероприятие по химии
Идеи интересных внеклассных мероприятий по химии.
Химические профессии
Обзор необычных профессий, связанных с химией.
ЕГЭ по химии 2019
Основная информация о ЕГЭ по химии 2019: структура экзамена, баллы, даты проведения.
Критерии оценивания ОГЭ по химии, баллы 2019
Подробно расскажем о баллах ОГЭ по химии 2019, методах и критериях оценивания заданий и переводе первичных баллов в школьную оценку.
Изменения ОГЭ по химии в 2019 году
Расскажем об изменениях, которые ждут школьников при сдаче ОГЭ по химии в 2019 году.
Подготовка к ОГЭ по химии
Несколько советов и рекомендаций, следуя которым подготовка к ОГЭ по химии будет проходить результативно.
Онлайн тесты по химии
Немного информации о проверке знаний с помощью тестов по химии в режиме онлайн.
Все об ОГЭ по химии в 2019
Основные сведения об ОГЭ по химии 2019: даты, время, баллы, материалы для подготовки.
Тест по химии 11 класс
Рассказываем о тестах по химии, используемых для проверки знаний в 11 классе.
Тест по химии 10 класс
Общие сведения о тестах по химии в 10 классе.
Тест по химии 9 класс
Рассказываем о тестах по химии, используемых для проверки знаний в 9 классе.
Тест по химии 8 класс
Рассказываем в общих чертах о тестах по химии в 8 классе
Ионная связь
Статья, содержащая в себе базовые понятие об ионном виде химической связи.
Водородная связь
Статья о водородном типе химической связи и его особенностях.
Подготовка к ЕГЭ по химии с нуля
В статье дано несколько действенных советов по подготовке к ЕГЭ по химии «с нуля».
Металлическая связь
Продолжаем серию статей про виды химической связи.
Ковалентная связь
Начинаем серию статей про виды химической связи.
Шкала перевода баллов ЕГЭ по химии 2018
Отвечаем на вопросы о системе оценивания и переводе первичных баллов в тестовые.
Учимся на летних каникулах
Размышляем о том, как полезно провести время во время летнего отдыха на каникулах. (в статье есть подарок внимательным читателям)
«ХиШник» приехал на Сахалин!
Этим летом открывается очередная летняя сессия областной профильной школы для одаренных детей «Эврика».
Мой сын увлёкся химией, что делать?
Собрали ТОП-5 полезных материалов для старшеклассника.
Двенадцать сервисов для изучения химии, с которыми ты точно сдашь
Великолепная подборка полезных сайтов для самостоятельного изучения химии.
О правах и обязанностях в школе: почему необходимо сотрудничество учеников и учителей
Что такое право само по себе и откуда оно берется. Как не заработать славу скандалистов, «вечно качающих права», и при этом не переносить безропотно нарушение своих личных границ…
Современный задачник по химии
Материал о том, какие виды задачников по химии существуют и как среди них ориентироваться.
Выбираем репетитора по химии: инструкция
Или не выбираем
Научиться решать задачи по химии легко: следуем инструкции
Учимся решать задачи по химии к ОГЭ, ЕГЭ, инструкция от ХиШника
Изменения в ЕГЭ по химии 2018 года, новая демоверсия, спецификация, кодификаторы ЕГЭ
ФИПИ снова решил усложнить нам жизнь новыми требованиями к ЕГЭ. О том, почему изменения не всегда плохи, и как встретить их с достоинством.
Обновление в демонстрационной версии «ХиШника»
Мы расширили приветственное окно, чтобы при входе в приложение всем новым пользователям были понятны основные принципы работы «ХиШника».
Активация лицензионного ключа и первые шаги в «ХиШнике».
Что такое лицензионный ключ и как происходит его активация в приложении
Современный урок химии по ФГОС
Для чего нужны стандарты, по которым происходит обучение химии в российских школах, и как приложение “ХиШник” поможет соответствовать этим стандартам?
ХиШник в школе: ИКТ на уроках химии
Как наше приложение поможет внедрить ИКТ в уроки
Ура! Новые планы ХиШника и подарочки
Подводим итоги 2017, планируем 2018 и, конечно же, дарим подарки!
Родина приложения «ХиШник» – Новосибирский Академгородок
Почему же родиной «ХиШника» стал Новосибирский Академгородок?
Совпадение не случайное.
Можно ли просматривать историю решения задач учениками в онлайн-режиме?
Итак, «ХиШник» это приложение, в котором могут работать и ученики, и преподаватели. После того, как преподаватель создает в приложении учебную группу
После того, как преподаватель создает в приложении учебную группу
Можно ли заниматься в «ХиШнике» со смартфона/планшета?
Сегодня у нас вопрос, которого мы давно ждали: можно ли заниматься в «ХиШнике» со смартфона/планшета?
Семинар от «ХиШника» на КПК для учителей химии
На прошлой неделе мы провели семинар в рамках масштабных ежегодных курсов повышения квалификации на базе СУНЦ НГУ (Новосибирск, Академгородок).
Команда «ХиШника» провела мастер-класс для преподавателей химии и методистов
Вчера команда «ХиШника» провела мастер-класс для преподавателей химии и методистов программ повышения квалификации из разных регионов России.
Как купить полный доступ к приложению?
Сегодня новый вопрос: что делать, если решать задачи в демо-версии приложения понравилось, как получить полный доступ? Отвечаем!
«ХиШник» представляет два кейса на ярмарке кейсов «Школа реальных дел»
Ярмарка кейсов «Школы реальных дел» – уже в эту пятницу! В этом году «ХиШник» представляет два кейса.
Служба поддержки:
Support@hishnik-school. ru
Для СМИ:
Onp@alekta. ru
Спасибо!
От 01.01.2017 года
Настоящее пользовательское (лицензионное) соглашение (далее – «Соглашение») заключается между Обществом с ограниченной ответственностью «АЛЕКТА» (далее – «Лицензиар»), и Пользователем (физическим лицом, выступающем в роли конечного потребителя Продукта) совместно именуемые «Стороны».
Пожалуйста, внимательно ознакомьтесь с текстом настоящего Соглашения. Оно представляет собой публичную оферту и, после его принятия Вами, образует соглашение между Вами (Пользователем) и Лицензиаром о предмете и на условиях, изложенных в тексте Соглашения.
Принимая настоящее Соглашение, Вы соглашаетесь с положениями, принципами, а также соответствующими условиями лицензионного соглашения, изложенными ниже.
Общие сведения о тестах по химии в 10 классе.
Так как химия наука точная, она неразрывно связана с различного рода вычислениями. Чтобы решать задачи, нужно знать формулы и хорошо в них ориентироваться. Без этих базовых знаний и навыков изучение химии становится невозможным.
Без этих базовых знаний и навыков изучение химии становится невозможным.
Мы собрали для вас основные химические формулы, изучаемые в школьном курсе. Они пригодятся каждому ученику, особенно тем, кто будет сдавать ОГЭ или ЕГЭ по этому непростому, но очень интересному предмету.
Нахождение количества вещества
Первое и основное понятие, которое необходимо усвоить – это Количество вещества, измеряемое в молях и обозначающееся латинской буквой «n». Для его нахождения нужно основываться на условии задачи, так как вычислить количество вещества можно по трём формулам:
1) По массе. N=m/M — Массу вещества (в граммах) разделить на его молярную массу (в г/моль).
2) По объёму. N=V/Vm — Отношением объёма вещества к его молярному объёму (используется для газов).
3) По числу молекул. N=N/NA – Число молекул вещества делённое на число Авогадро. Число Авогадро (NA) – физическая величина, указывающая на число молекул, содержащихся в 1 моле вещества, и численно равная 6,0221 * 10 23 моль -1 .
Формулы для нахождения массы
Массу вещества можно найти несколькими способами:
1. Умножив количество вещества на молярную массу: M (г) = n (моль)×M (г/моль).
2. Произведением объёма раствора и его плотности: M = V (л) ×ρ (г/л).
3. Перемножив массовую долю с массой раствора: M = m(р-ра) × ω.
Молярная масса (М) – это масса одного моля вещества. Вычисляется она следующим образом: посредством сложения атомных масс элементов, из которых состоит вещество, получаем относительную молекулярную массу. Молярная масса численно равна относительной молекулярной массе, но имеет размерность «г/моль». Также молярную массу можно найти с помощью отношения массы вещества к его количеству:
Формулы для нахождения объёма
Для вычисления объёма того или иного вещества можно воспользоваться одной из формул:
1. Объём раствора находится как отношение массы раствора к его плотности:
2. Объём газа равен отношению его количества вещества к молярному объёму:
Объём газа равен отношению его количества вещества к молярному объёму:
Молярный объём (VM) – объём, который занимает 1 моль вещества при определённых показателях давления и температуры. Находится при делении молярной массы вещества на его плотность:
При нормальных условиях молярный объём газа равен 22,4 л/моль.
Формулы для нахождения плотности и относительной плотности
Плотность (ρ) – физическая величина, указывающая на массу определённого вещества, содержащуюся в единице объёма.
Следовательно, формула для её вычисления имеет вид:
Помимо основной, существует формула для нахождения плотности газа при нормальных условиях, где молярная масса делится на молярный объём газа при н. у.:
Относительная плотность (D) газов – величина, указывающая насколько одно вещество тяжелее или легче другого. Вычисляется она отношением молярных масс газов:
Например, условием было найти плотность газа по водороду. Решение будет иметь вид: D = M(газа)/M(h3) = M(газа)/2. Относительная плотность является безразмерной величиной.
Относительная плотность является безразмерной величиной.
Формулы для нахождения концентрации
Молярная концентрация (С) – отношение количества растворённого вещества к объёму раствора. Единица измерения – моль/л. Молярная концентрация вычисляется по формуле:
Массовая концентрация чаще всего называется титром (Т). Это отношение массы растворённого вещества к объёму раствора. Единица измерения — г/л.
Массовая доля (ω) – это один из вариантов выражения концентрации. С её помощью можно вычислить процентное содержание растворённого вещества в общей массе раствора:
По такому же принципу вычисляется массовая доля определённого компонента в смеси:
Ω = (mкомпонента / mсистемы) × 100%
Если возникает необходимость найти массовую долю химического элемента в соединении, то нужно относительную атомную массу этого элемента умножить на число атомов в соединении и разделить на молекулярную массу вещества:
Формулы для нахождения выхода продукта реакции
Под Выходом продукта реакции (ᶯ) подразумевается отношение массы (объёма, количества) вещества, полученного на практике, к теоретически возможному (рассчитанному по уравнению реакции). Единица измерения – доля, а проценты — если результат умножить на 100 !
Единица измерения – доля, а проценты — если результат умножить на 100 !
Для его вычисления, в зависимости от условия задачи, используются следующие формулы:
Попрактиковать решение задач и знание формул возможно в приложении «ХиШник». Оно содержит в себе каталог заданий, которые, в свою очередь, разделены по темам и уровням сложности. Если вы дали неверный ответ, то приложение не просто уведомит об этом, а предложит правильный алгоритм решения. Также в нём есть раздел для подготовки к ОГЭ и ЕГЭ, в котором собраны типовые задания.
Знание расчётных формул – это ключевой момент при решении задач. Главное, понимать их, а не бездумно заучивать. Так как они будут использоваться не только в школьных задачах, на ЕГЭ и ОГЭ, но и в дальнейшей жизни, даже если ваша профессиональная сфера будет далека от химии.
Немного информации о проверке знаний с помощью тестов по химии в режиме онлайн.
Мой сын увлёкся химией, что делать?
Рассказываем о тестах по химии, используемых для проверки знаний в 9 классе.
Hishnik-school. ru
16.09.2018 3:21:05
2018-09-16 03:21:05
Источники:
Https://hishnik-school. ru/bez-rubriki/formuly-dlya-resheniya-zadach-po-himii/
“Решение задач на нахождение формулы органического вещества” (10 класс)
Цель: применение алгоритма при решении задач на вывод формул.
Задачи:
- расширить знания учащихся о способах решения задач;
- закрепить навыки работы с алгоритмами;
- показать взаимосвязь химии и математики.
ХОД УРОКА
1. Оргмомент
Учитель знакомит класс с темой урока, целью и задачами урока.
2. Повторение общих формул органических веществ.
Учитель предлагает учащимся назвать общие формулы алканов, алкенов, алкинов, циклоалканов, алкадиенов, типы гибридицациии атомов углерода, характерные изомерии для каждого класса.
3. Составление алгоритма для решения задач на нахождение формулы вещества по продуктам сгорания вещества, если дана относительная плотность.
АЛГОРИТМ №1.
1. Вычисляем молярную массу вещества.
М(в) = D(x)*М(х) (1)
2. Вычисляем количество атомов С:
а) если СО2 дано по массе:
n(C) = (2)
б) если СО2 дано в объеме:
n(C) = (3)
3. Вычисляем количество атомов Н:
Так как в молекуле Н2О 2 моля Н, тогда формулу умножаем на 2 (это применимо и к N)
n(Н) = 2 (4)
4. Вычисляем молярную массу полученного вещества.
5. Если молярная масса полученного вещества равна молярной массе вещества (1), тогда задача решена правильно; если молярная масса полученного вещества отличается от молярной массы вещества (1), вычисляем разность и определяем количество атомов кислорода, если вещество кислородосодержащие, или азота, если вещество азотосодержащее.
Пример:
При сгорании органического вещества массой 2, 37 г образовалось 3,36 г оксида углерода(IV) (н.у.), 1,35 г воды и азот. Относительная плотность этого вещества по воздуху равна 2,724. Выведите молекулярную формулу вещества.
Выведите молекулярную формулу вещества.
Дано:
m ( в-ва) = 2,37г
V (CO2) = 3,36 л
m (h3O) = 1,35 г
D (возд.) = 2,724.
_________________
Найти:
CxHyNz
М(возд) = 29 г/моль
М(Н2О) = 18 г/моль
Vm = 22,4л/моль
Решение:
1. Применяем формулу (1)
M(в-ва) = 29 г/моль * 2,724 =79 г/моль.
Находим количество атомов С по формуле (3)
n(C) = = 5
2. Находим количество атомов Н по формуле (4)
n(Н) = 2 = 5
3. Вычисляем молярную массу С5Н5.
М(С5Н5) = 12 * 5 + 1 * 5 = 65г/моль
4. Вычисляем количество атомов азота (5)
79 – 65 = 14. т.к. атомная масса азота – 14, значит в данной формулу один атом N.
Ответ: С5Н5N
4. Составление алгоритма нахождение молекулярной формулы вещества по его относительной плотности и массовой доле элементов в соединении.
АЛГОРИТМ № 2
1. Вычисляем молярную массу вещества.
Вычисляем молярную массу вещества.
М(в) = D(x)*М(х) (1)
2. Вычисляем количество атомов элемента:
а) если w дана в процентах:
n(Э) = (2)
б) если w дана в долях:
n(Э) = (3)
3. Вычисляем молярную массу полученного вещества.
4. Если молярная масса полученного вещества равна молярной массе вещества (1), тогда задача решена правильно; если молярная масса полученного вещества отличается от молярной массы вещества (1), вычисляем разность и определяем количество атомов кислорода, если вещество кислородосодержащие, или азота, если вещество азотосодержащее.
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
=> ПОЛУЧИТЬ СУПЕРСПОСОБНОСТИ УЧИТЕЛЯ
Просмотр содержимого документа
«”Решение задач на нахождение формулы органического вещества” (10 класс)»
Тема: “Решение задач на нахождение формулы органического вещества” (10 класс)
Цель: применение алгоритма при решении задач на вывод формул.
Задачи:
расширить знания учащихся о способах решения задач;
закрепить навыки работы с алгоритмами;
показать взаимосвязь химии и математики.
ХОД УРОКА
1. Оргмомент
Учитель знакомит класс с темой урока, целью и задачами урока.
2. Повторение общих формул органических веществ.
Учитель предлагает учащимся назвать общие формулы алканов, алкенов, алкинов, циклоалканов, алкадиенов, типы гибридицациии атомов углерода, характерные изомерии для каждого класса.
3. Составление алгоритма для решения задач на нахождение формулы вещества по продуктам сгорания вещества, если дана относительная плотность.
АЛГОРИТМ №1.
1. Вычисляем молярную массу вещества.
М(в) = D(x)*М(х) (1)
2. Вычисляем количество атомов С:
а) если СО2 дано по массе:
n(C) = (2)
б) если СО2 дано в объеме:
n(C) = (3)
3. Вычисляем количество атомов Н:
Так как в молекуле Н2О 2 моля Н, тогда формулу умножаем на 2 (это применимо и к N)
n(Н) = 2 (4)
4. Вычисляем молярную массу полученного вещества.
Вычисляем молярную массу полученного вещества.
5. Если молярная масса полученного вещества равна молярной массе вещества (1), тогда задача решена правильно; если молярная масса полученного вещества отличается от молярной массы вещества (1), вычисляем разность и определяем количество атомов кислорода, если вещество кислородосодержащие, или азота, если вещество азотосодержащее.
Пример:
При сгорании органического вещества массой 2, 37 г образовалось 3,36 г оксида углерода(IV) (н.у.), 1,35 г воды и азот. Относительная плотность этого вещества по воздуху равна 2,724. Выведите молекулярную формулу вещества.
Дано:
m ( в-ва) = 2,37г
V (CO2) = 3,36 л
m (H2O) = 1,35 г
D (возд.) = 2,724.
_________________
Найти:
CxHyNz
М(возд) = 29 г/моль
М(Н2О) = 18 г/моль
Vm = 22,4л/моль
Решение:
1. Применяем формулу (1)
Применяем формулу (1)
M(в-ва) = 29 г/моль * 2,724 =79 г/моль.
Находим количество атомов С по формуле (3)
n(C) = = 5
2. Находим количество атомов Н по формуле (4)
n(Н) = 2 = 5
3. Вычисляем молярную массу С5Н5.
М(С5Н5) = 12 * 5 + 1 * 5 = 65г/моль
4. Вычисляем количество атомов азота (5)
79 – 65 = 14. т.к. атомная масса азота – 14, значит в данной формулу один атом N.
Ответ: С5Н5N
4. Составление алгоритма нахождение молекулярной формулы вещества по его относительной плотности и массовой доле элементов в соединении.
АЛГОРИТМ № 2
1. Вычисляем молярную массу вещества.
М(в) = D(x)*М(х) (1)
2. Вычисляем количество атомов элемента:
Вычисляем количество атомов элемента:
а) если w дана в процентах:
n(Э) = (2)
б) если w дана в долях:
n(Э) = (3)
3. Вычисляем молярную массу полученного вещества.
4. Если молярная масса полученного вещества равна молярной массе вещества (1), тогда задача решена правильно; если молярная масса полученного вещества отличается от молярной массы вещества (1), вычисляем разность и определяем количество атомов кислорода, если вещество кислородосодержащие, или азота, если вещество азотосодержащее.
Пример:
Выведите формулу вещества, содержащего 82,75% углерода и 17,25 % водорода. Относительная плотность паров этого вещества по воздуху равна 2.
Дано:
w(C) = 82,75%
w(H) = 17,25%
D(возд) = 2
______________
Найти:
СхНу
M(воздуха) = 29г/моль
М(С4Н10) =12 * 4 + 1 * 10 = 58г/моль
Решение:
1. Применяем формулу (1)
Применяем формулу (1)
M(в-ва) = 29 г/моль * 2 =58 г/моль.
2. Находим количество атомов С по формуле (2)
n(С) = = 4
3. Находим количество атомов Н по формуле (2)
n(Н) = = 1
4. Вычисляем молярную массу С4Н10
М(С4Н10) = 12 * 4 + 1 * 10 = 58г/моль
5. Вычисленная молярная масса совпадает с (1), задача решена.
Ответ: С4Н10
5. Закрепление материала
Учащиеся решают задачи самостоятельно, по необходимости консультируются с учителем.
Задача 1. При сгорании 11,2 г. Углеводорода получили оксид углерода массой 35,2 г и воду массой 14,4 г. Относительная плотность этого углеводорода по воздуху равна 1,93. Выведите молекулярную формулу.
Задача 2. При сжигании 2.2 г. вещества получили 4,4 г оксида углерода и 1,8 г. воды. Относительная плотность вещества по водороду равна 44. Определите молекулярную формулу вещества.
При сжигании 2.2 г. вещества получили 4,4 г оксида углерода и 1,8 г. воды. Относительная плотность вещества по водороду равна 44. Определите молекулярную формулу вещества.
Задача 3. Выведите формулу вещества, содержащего 81,8% углерода и 18,2 % водорода, если относительная плотность по водороду равна 22.
Задача 4. Определите молекулярную формулу углеводорода, если массовая доля углерода равна 85,75, а водорода –14,3%. Относительная плотность этого вещества по азоту примерно равна 2.
6. Домашнее задание
Задачи по химии с ответами — Научные заметки и проекты
Изучение и решение задач по химии — отличный способ освоить понятия.
Используйте задачи по химии в качестве инструмента для усвоения понятий химии. Некоторые из этих примеров показывают использование формул, а другие включают списки примеров.
Кислоты, основания и pH Задачи по химии
Узнайте о кислотах и основаниях. Посмотрите, как рассчитать pH, pOH, K a , K b , pK a и pK б .
Посмотрите, как рассчитать pH, pOH, K a , K b , pK a и pK б .
- Практика расчета pH.
- Получить пример расчетов pH, pK a , pK b , K a и K b .
- Получить примеры амфотеризма.
Проблемы строения атома
Узнайте об атомной массе, модели Бора и части атома.
- Потренируйтесь определять атомный номер, массовое число и атомную массу.
- Получите примеры, показывающие способы определения атомной массы.
- Используйте число Авогадро и найдите массу отдельного атома.
- Рассмотрите модель атома Бора.
- Найдите число валентных электронов атома элемента.
Химические связи
Узнайте, как использовать электроотрицательность, чтобы определить, образуют ли атомы ионные или ковалентные связи. См. задачи по химии, рисующие структуры Льюиса.
- Определите ионные и ковалентные связи.

- Узнайте об ионных соединениях и получите примеры.
- Практика определения ионных соединений.
- Получить примеры бинарных соединений.
- Узнайте о ковалентных соединениях и их свойствах.
- См., как присваивать степени окисления.
- Практика рисования структур Льюиса.
- Практикуйтесь в расчете энергии связи.
Химические уравнения
Практикуйтесь в написании и составлении химических уравнений.
- Изучите шаги уравнений балансировки.
- Практика балансировки химических уравнений (практический тест).
- Получить примеры определения теоретического выхода.
- Попрактикуйтесь в расчете процентной доходности.
- Научитесь распознавать реакции разложения.
- Практика распознавания реакций синтеза.
- Практика распознавания одиночных реакций замещения.
- Распознавание реакций двойного замещения.
- Найдите молярное соотношение между химическими веществами в уравнении.

Концентрация и растворы
Узнайте, как рассчитать концентрацию и исследовать химические проблемы, влияющие на концентрацию химических веществ, включая понижение температуры замерзания, повышение температуры кипения и повышение давления пара.
- Получить пример расчета концентрации в нескольких единицах.
- Потренируйтесь вычислять нормальность (N).
- Практика расчета моляльности (m).
- Ознакомьтесь с примерами расчета молярности (M).
- Получить примеры коллигативных свойств растворов.
- См. определение и примеры насыщенных растворов.
- См. определение и примеры ненасыщенных растворов.
- Получите примеры смешивающихся и несмешивающихся жидкостей.
Расчеты ошибок
Узнайте о типах ошибок и просмотрите примеры задач по химии.
- Посмотрите, как рассчитать проценты.
- Потренируйтесь в расчетах абсолютных и относительных погрешностей.
- Посмотрите, как рассчитать процент ошибки.

- Узнайте, как найти стандартное отклонение.
- Вычислить среднее значение, медиану и моду.
- Ознакомьтесь с разницей между точностью и прецизионностью.
Задачи по химии равновесия
Узнайте о принципе Ле Шателье, скорости реакции и равновесии.
- Решение задач по химии энергии активации.
- Просмотрите факторы, влияющие на скорость реакции.
- Попрактикуйтесь в расчете фактора Вант-Гоффа.
Газовые законы
Решайте задачи по химии, используя газовые законы, включая закон Рауля, закон Грэма, закон Бойля, закон Чарльза и закон Дальтона о парциальных давлениях.
- Рассчитать давление пара.
- Решите задачи закона Авогадро.
- Занятия по закону Бойля.
- См. примеры задач по закону Чарльза.
- Решение задач по комбинированному газовому праву.
- Решите проблемы закона Гей-Люссака.
Материя
Некоторые задачи по химии требуют указать примеры состояний материи и типов смесей. Хотя есть какие-то химические формулы, которые нужно знать, все равно приятно иметь списки примеров.
Хотя есть какие-то химические формулы, которые нужно знать, все равно приятно иметь списки примеров.
- Практика расчета плотности.
- Определите интенсивные и экстенсивные свойства материи.
- См. примеры внутренних и внешних свойств материи.
- Получить определение и примеры твердых тел.
- Получить определение и примеры газов.
- См. определение и примеры жидкостей.
- Узнайте, что такое температура плавления, и получите список значений для различных веществ.
- Получите определение азеотропа и посмотрите примеры.
- Посмотрите, как рассчитать удельный объем газа.
- Получить примеры физических свойств материи.
- Получить примеры химических свойств вещества.
- Обзор состояния вещества.
Молекулярная структура Задачи по химии
См. задачи по химии, написание химических формул. См. примеры одноатомных и двухатомных элементов.
- Практика эмпирических и молекулярных формул.

- Практикуйте простейшие формулы.
- Узнайте, как рассчитать молекулярную массу.
- Получить примеры одноатомных элементов.
- См. примеры бинарных соединений.
- Подсчитайте количество атомов и молекул в капле воды.
Номенклатура
Задания по химии на названия ионных соединений, углеводородов и ковалентных соединений.
- Практикуйтесь в назывании ковалентных соединений.
- Изучите префиксы углеводородов в органической химии.
Ядерная химия
Эти задачи по химии включают изотопы, ядерные символы, период полураспада, радиоактивный распад, деление, синтез.
- Обзор типов радиоактивного распада.
Периодическая таблица
Узнайте, как использовать периодическую таблицу и изучить тенденции периодической таблицы.
- Знать тенденции в периодической таблице.
- Узнайте, как пользоваться периодической таблицей.
- Изучите разницу между атомным и ионным радиусами и посмотрите их тенденции в периодической таблице.

Физическая химия
Изучение термохимии и физической химии, включая энтальпию, энтропию, теплоту плавления и теплоту парообразования.
- Практика задач по химии теплоты парообразования.
- Практика задач по химии теплового синтеза.
- Рассчитайте количество тепла, необходимое для превращения льда в пар.
- Практика расчета удельной теплоемкости.
- Получить примеры потенциальной энергии.
- Получить примеры кинетической энергии.
- См. пример расчета энергии активации.
Спектроскопия и проблемы квантовой химии
См. задачи по химии, связанные с взаимодействием света и вещества.
- Расчет длины волны по частоте или частоты по длине волны.
Стехиометрия Задачи по химии
Практические задачи по химии с балансировкой формул для массы и заряда. Узнайте о реагентах и продуктах.
- Получить примеры задач на молярное соотношение.
- Рассчитать выход в процентах.

- Узнайте, как присваивать степени окисления.
- Получить определение и примеры реагентов в химии.
- Получить определение и примеры продуктов химических реакций.
Преобразование единиц измерения
Существует множество примеров преобразования единиц измерения, которым посвящена отдельная страница!
Несколько слов о решении задач по химии
Несколько слов о решении задач по химииА Несколько слов о решении задач по химии
Доктор Э.Т. Белл-Лонселла
Вы вероятно, сидит там, задаваясь вопросом: “Раздаточный материал по решению проблем? Это уроке химии, что она думает?” Вы помните текстовые задачи из школьных уроков математики? Вот такая проблема! Есть несколько причин для этого раздаточного материала:
- Большинство проблем, которые
вы встретите в этом классе то, что вы могли бы назвать словесными задачами .

- Очень полезно учиться как решать проблемы. Решение проблем является частью реального мира .
- За годы преподавания я наблюдали, как учащиеся используют стратегии для решения проблем, которые кажутся неэффективно и неэффективно.
- Есть еще много причин
Вы также, вероятно, задаетесь вопросом, что я имею в виду под стратегиями которые неэффективны и неэффективны. Я вижу три классических поведения:
- Студент читает задачу, и почти сразу начинает нажимать кнопки на калькуляторе.
- Студент читает задачу, нацарапает несколько уравнений на странице, а затем проверит, верен ли ответ. в конце книги.
- Студент читает задачу,
нацарапает несколько уравнений на странице, нажмет несколько кнопок на
калькулятор. Потом в раздражении наклоняется к соседке и говорит:
ты понял?”
Если задача не имеет числового ответа,
раздражение нарастает. Если в конце книги нет ответа (потому что
проблема пришла не из книги), студент становится еще более
раздраженный. Тогда студент расстраивается из-за профессора, а класс и
иногда просто выпадает. Это не должно быть так.
Если в конце книги нет ответа (потому что
проблема пришла не из книги), студент становится еще более
раздраженный. Тогда студент расстраивается из-за профессора, а класс и
иногда просто выпадает. Это не должно быть так.
Решение проблем – это навык и метод решения проблем.
Вы увидите, как я моделирую этот метод в классе. Вы заметите (как студенты всегда
делать), что я редко полностью решу проблему; Я только что установил его. Этот
кажется, расстраивает студентов. Однако я знаю, что вы являетесь экспертами по вводу
цифры в ваших калькуляторах и нажатие Кнопка “Вперед” . Есть
несколько подходов; все они основаны на одной и той же идее.
- Самая общая стратегия имеет только три основных шага:
- Сначала прочитайте задачу
и ищите информацию, которую вы получили дали .
Определите каждую часть числовых данных в задаче и запишите ее.
Иногда полезно нарисовать эскиз.

- Перечитайте задачу ищешь какую проблему хочешь с тобой решишь . Обычно вы найдите это в предложении, которое заканчивается знаком вопроса, или последним приговор. Другими ключами являются такие слова, как “ определить” и . “вычислить” .
- В настоящее время
вы должны выяснить, что вам нужно для того, чтобы решить проблему.
Если вы еще этого не сделали, самое время нарисовать эскиз.
(ничего особенного, просто набросок) ситуации. Схема (или карта)
ваша стратегия решения помогает. Часто вы не знаете, как будет выглядеть карта
нравится, когда вы начинаете, но это станет яснее, когда вы будете работать по-своему
хотя это. Вы также захотите составить список необходимых преобразований, или
соответствующие уравнения (которые становятся очевидно необходимыми по мере того, как вы разрабатываете
стратегия решения). Когда вы, наконец, имеете довольно четкое представление о том, что вы
стратегия будет, тогда (и только тогда) приступайте к составлению уравнений,
вставляя числа и (наконец) вводя их в свои калькуляторы.

Этот подход очень общий и может применяться к любому проблема в любой дисциплине. Это может показаться слишком схематичным. следующая стратегия имеет немного больше структуры . это представлен в тексте Prep-Chem, Базовая химия: подход к решению проблем (1) . Он использует те же принципы, но добавляет несколько дополнительных шагов. Генделл начинает свой обсуждение решения проблем с оговоркой:
Совет: начните решение проблемы с повторения точного значения
все используемые термины, учитывая конкретную физическую ситуацию, к которой
относится к проблеме и точно определяет, о чем идет речь в проблеме. Делать
не начинать решение задачи с подстановки значений в то или иное уравнение в
в надежде получить правильный ответ. Вероятно, это займет хорошее
много работы с вашей стороны, чтобы привыкнуть решать проблемы таким образом. если ты
хотите добиться успеха в химии, однако, это то, что вам придется делать.
Когда вы читаете задачу
в первый раз попытайтесь создать в уме картину физической ситуации
к которому относится проблема. Переведите свою ментальную картину в набросок, который
вы можете комментировать физические данные (длина, ширина, температура, давление и т. д.)
Переведите свою ментальную картину в набросок, который
вы можете комментировать физические данные (длина, ширина, температура, давление и т. д.)
- Рассмотрите свою фотографию и подумайте о ней. физические принципы или математические уравнения, связывающие фрагменты данных при условии.
- Сделать “карту”. То есть спланировать необходимые шаги расчета, которые позволят вам преобразовать предоставленные данные в желаемый результат. Генделл предлагает задать себе следующий ряд вопросов по мере того, как вы разрабатываете свою «карту».
- Что количества известны, а какие неизвестны?
- Ар достаточно ли соотношений, связывающих известные и неизвестные величины?
- Банка разбить проблему на ряд более простых шагов?
- Если Я хочу определить значение определенной величины, какие другие величины мне нужно определить, чтобы выполнить это? Как мне определить эти количества?
- Используйте свой калькулятор для выполнения числового
расчеты.

- Двойная проверка: разумен ли ответ? Вот где умение оценивать очень ценно!
- Чему вы научились (о решении задач)? Как можете ли вы применить это к следующей (связанной) проблеме, которую вам нужно решить?
Еще одна стратегия
изложили Патрисия Хеллер и Марк Холлабо, профессора физики. (2) Они используют пять основных шагов. Посмотрите, сможете ли вы найти сходство между этим
стратегия и стратегия Генделла, описанная выше.
- Фокус проблема – качественное описание в картинках и (своими) словами.
- Описывать физика (химия) – более полная схема с физическим (химических) объектов и физических (химических) величин, а также математические уравнения, связывающие эти величины.
- План
решение – наметьте стратегию решения проблемы, используя
уравнения и другие соотношения из предыдущего шага (b).

- Выполнить проблема в том, что теперь (наконец) время нажимать кнопки.
- Оценить ответ – обоснованно и полно?
Каждый
описанных до сих пор стратегий носит несколько общий характер — это основные шаги.
Если вы не чувствуете, что хорошо работаете с чем-то настолько общим, вы
возможно, вам понадобятся более конкретные рекомендации. я настоятельно призываю к прочтению
глава 10 «Решение химических задач: общие задачи» в книге
Кин и Мидлкэмп. (3) Хотя может показаться, что идеи, которые они предлагают, трудоемки и требуют времени
(особенно когда у вас есть и другие предметы для изучения), я считаю, что если
вы применяете эти стратегии (ко всем вашим классам, а не только к вашей химии)
вы обнаружите, что в целом станете лучше решать проблемы. (Ты будешь
начать есть лотов хороших идей, как у маленького парня слева
там.)
Наконец, есть те
задачи, которые не имеют номеров и не обязательно имеют правильный ответ. Они могут быть самыми сложными и сложными. Я утверждаю, что это
стремясь решить такого рода задачи, вы действительно научитесь
химия . Во введении к своей книге « путешествий в концептуальном
Химия , автор Дэн Барух говорит:
Они могут быть самыми сложными и сложными. Я утверждаю, что это
стремясь решить такого рода задачи, вы действительно научитесь
химия . Во введении к своей книге « путешествий в концептуальном
Химия , автор Дэн Барух говорит:
В качестве
студенты, пожалуйста, не просто заучивайте и повторяйте, слепо заучивая формулы и
выполнение многочисленных расчетов. Вы должны исследовать и думать, чтобы расцвести
интеллектуально. Исследуя, вы откроете, а благодаря открытиям вы
учиться. Соответственно, это не просто задачник. Это не сборник
упражнений по чтению, а не длинный список чисел, которые нужно вставить в длинный список
формулы, а не источник утомительных домашних заданий. Ни в одной из этих проблем не будет
Вы делаете численные расчеты. так что уберите свои калькуляторы!! Используйте эти
проблемы как трамплин для концептуального мышления и качественного понимания.
Эти задачи требуют от вас решения головоломок, интерпретации наблюдений, проектирования
экспериментировать и ценить тонкости в материале. Они также бросают вам вызов
использовать универсальность общей химии в применении своих знаний к
решать задачи по смежным предметам, которые вы могли бы изучать в будущем (4)
Они также бросают вам вызов
использовать универсальность общей химии в применении своих знаний к
решать задачи по смежным предметам, которые вы могли бы изучать в будущем (4)
В течение
семестр мы будем работать над самыми разнообразными задачами: Упражнения, задачи, которые приносят
вместе идеи образуют различные части главы (см. «Собираем все вместе» ).
в задачах в конце главы в вашем учебнике), задач, в которых используется много
математические формулы (и уравнения) и требуют обширной “кнопки
нажимая” на свой калькулятор, и концептуальные задачи, взятые у Дэна
Книга Баруха. Обязательно сохраните этот раздаточный материал в надежном месте, чтобы вы могли обратиться к
это по мере необходимости.
Несколько слов о калькуляторах: Они могут быть скорее проклятием, чем удобством! Ваш калькулятор даст вам
миллионы сигов инжира; но если вы не ввели правильный номер, то сиг фиг
бессмысленны. Таким образом, вы должны научиться оценивать свои ответы, чтобы вы могли
проверьте еще раз, что ваш калькулятор дал вам правильное число! Вы не будете
всегда разрешается использовать ваши калькуляторы во время викторин. Акцент будет
от того, насколько хорошо вы поставили задачу и смогли ли вы оценить
ответьте на правильное количество сиг инжир. Вы бы б
Акцент будет
от того, насколько хорошо вы поставили задачу и смогли ли вы оценить
ответьте на правильное количество сиг инжир. Вы бы б
е рекомендуется практиковать это при решении домашних заданий.
1. Гендель, Жюльен. Основы химии: подход к решению проблем ; Запад: Миннеаполис, Миннесота, 1993.
.2. Хеллер, Патрисия; Холлабо, Марк «Обучение решению проблем через Кооперативная группировка. Часть 2: Разработка задач и структурирование групп. Аме. Дж. Физ. 1992 , 60 , 637-645.
3. Кин, Элизабет; Мидлкэмп, Кэтрин Как выжить и даже преуспеть в Общая химия ; Макгроу-Хилл: Нью-Йорк, 1994.
. 4. Barouch, DH Путешествия по концептуальной химии ; Джонс и Бартлетт:
Садбери, Массачусетс, 1997.
.
советов по запоминанию формул по химии, математике и физике | Кулдип | SpeedLabs
Прежде чем приступить к работе, убедитесь, что все формулы важны и их легко освоить!
Когда у вас такой большой учебный план, запоминание формул может быть затруднено. Много раз вам придется искать старые формулы в старых книгах, которые вы, возможно, забыли. Итак, вот как вы можете запоминать формулы по физике, химии и математике.
Много раз вам придется искать старые формулы в старых книгах, которые вы, возможно, забыли. Итак, вот как вы можете запоминать формулы по физике, химии и математике.
Может быть множество причин, в том числе недостаток концентрации (сосредоточенности), нехватка времени и слишком много для понимания или трудности с определением того, какая формула используется для решения той или иной задачи. Работа над такими проблемами должна быть вашим главным приоритетом; в противном случае вы рискуете забыть некоторые важные формулы. Вы должны понимать, что все формулы важны и просты в освоении.
Как запоминать формулы на:
ФИЗИКА- Визуализируйте и проверьте себя .
Выберите несколько задач для работы и запишите формулу, которую вы будете использовать для каждой из них. Если вы столкнулись с проблемой, когда не можете вспомнить формулу, обведите ее красным цветом в своем списке, чтобы не забыть ее снова.
- Применять и практиковать методы решения проблем.

Практика поможет вам научиться правильно и в правильном порядке применять формулы. Когда вы будете решать задачи с формулами, вы узнаете, как использовать каждую формулу и когда ее использовать. Кроме того, по мере решения задач формулы будут возвращаться к вам автоматически.
- Приобретите способность выводить формулы
Всего не запомнишь. В результате вы должны уменьшить нагрузку на запоминание сотен формул одновременно. Вывод формулы – лучший способ сделать это. Некоторые формулы могут быть выведены из других формул, что значительно облегчает запоминание.
МАТЕМАТИКАВ математике больше, чем в любом другом предмете, имеется большое количество формул, которые необходимо хорошо усвоить. Вы не хотите тратить свои оценки на несколько формул.
- Ознакомьтесь со списком математических символов .
Составьте список всех формул по главам, чтобы вы могли обращаться к ним всякий раз, когда они вам понадобятся. После того, как вы составили список формул, просмотрите все новые символы, с которыми вы столкнулись. Составьте список неизвестных математических символов и попытайтесь их понять.
После того, как вы составили список формул, просмотрите все новые символы, с которыми вы столкнулись. Составьте список неизвестных математических символов и попытайтесь их понять.
- Структура формул и способы их получения
Научитесь выводить формулы, понимая, как они работают и как они устроены.
- Практика
Для каждой главы напишите формулу не менее трех раз, прежде чем начать решать. Математика — это решение задач, поэтому решение сумм является обязательным. Чем больше вы решите, тем больше вам понравится и вы станете перфекционистом в своем решении. Во время учебы вы также можете пригласить друга и посоревноваться за кусок пирога. Это будет мотивировать вас и поможет дольше запоминать формулы.
- Повторяйте, повторяйте и проверяйте себя с помощью карточек .
Для формул по математике вы можете использовать карточки (краткие заметки для просмотра), чтобы помочь вам запомнить их атомный номер. Итак, вот как сделать химию более интересной и увлекательной.
Итак, вот как сделать химию более интересной и увлекательной.
- Составьте список самых важных .
Создайте диаграмму периодической таблицы, к которой вы сможете получить доступ из любого места в любое время. Затем выучите химический символ для каждого элемента, который легче всего найти в периодической таблице, который включает как полное название символа, так и полное название элемента, например, C для углерода и He для гелия, H для водорода и Cl для хлор. Некоторые из них легко запомнить, а другие сложнее. Помните, что таблица Менделеева в первую очередь предназначена для справки, так что подумайте об этом.
- Соединения и решения
Повесьте список формул на стену, чтобы вы могли его видеть. Однако не консультируйтесь с ним во время работы над проблемой. Решите не менее трех задач в каждой главе по каждой формуле, то есть одну главу в неделю. Если у вас возникли проблемы с решением задачи или запоминанием формул, обведите это красным и прикрепите к стене.
- Выбирайте проблемы наугад и сведите количество ссылок к минимуму.
И последнее, но не менее важное: выбирайте и решайте случайные задачи. Если вы не можете этого сделать, напишите формулу не менее 5 раз в течение недели. По мере знакомства с формулами старайтесь использовать их, не сверяясь со списком формул. Если вы решаете задачи наугад и забываете формулу, вам следует записать ее.
Ключевые выводыВ конце концов, помните, что нет ничего сложного.
Первоначально опубликовано по адресу Блог SpeedLabs .
4.3 – Решение задач на равновесие – Общая химия для ну и дела
Мы знаем, что в равновесии значение коэффициента любой реакции равно ее константе равновесия. Таким образом, мы можем использовать математическое выражение для Q , чтобы определить ряд величин, связанных с реакцией, находящейся в равновесии или приближающейся к равновесию. Хотя мы научились определять, в каком направлении сместится реакция, чтобы достичь равновесия, мы хотим распространить это понимание на количественные расчеты. Мы делаем это, оценивая способы изменения концентраций продуктов и реагентов по мере того, как реакция приближается к равновесию, имея в виду стехиометрические отношения реакции. Этот алгебраический подход к расчетам равновесия будет рассмотрен в этом разделе.
Хотя мы научились определять, в каком направлении сместится реакция, чтобы достичь равновесия, мы хотим распространить это понимание на количественные расчеты. Мы делаем это, оценивая способы изменения концентраций продуктов и реагентов по мере того, как реакция приближается к равновесию, имея в виду стехиометрические отношения реакции. Этот алгебраический подход к расчетам равновесия будет рассмотрен в этом разделе.
Относительные изменения концентрации
Изменения концентрации или давления реагентов и продуктов происходят по мере приближения реакционной системы к равновесию. В этом разделе мы увидим, что мы можем связать эти изменения друг с другом, используя коэффициенты в сбалансированном химическом уравнении, описывающем систему. В качестве примера возьмем разложение аммиака.
При нагревании аммиак обратимо разлагается на азот и водород по следующему уравнению:
2 NH 3 ( G) ⇌ N 2 (G) + 3 H 2 (G)
Если выборка Ammonia Dehaspose In in Antaination и концентрация и концентрация и концентрация и концентрация и концентрация и концентрация и концентрация. N 2 увеличивается на 0,11 моль/л, изменение концентрации N 2 , Δ[N 2 ] = [N 2 ] f – [N 907 2 ] i , составляет 0,11 М. Изменение положительное , поскольку концентрация N 2 увеличивает .
N 2 увеличивается на 0,11 моль/л, изменение концентрации N 2 , Δ[N 2 ] = [N 2 ] f – [N 907 2 ] i , составляет 0,11 М. Изменение положительное , поскольку концентрация N 2 увеличивает .
Изменение концентрации H 2 , Δ[H 2 ], также положительное – концентрация H 2 увеличивается по мере разложения аммиака. Химическое уравнение говорит нам, что изменение концентрации H 2 в три раза превышает изменение концентрации N 2 , потому что на каждый произведенный моль N 2 приходится 3 моля H 2 .
[Н 2 ] = 3 × [N 2 ]
= 3 × 0,11 моль/л = 0,33 моль/л
Изменение концентрации NH 3 , Δ[NH 3 ], вдвое больше, чем Δ[N
9 2 90]; уравнение показывает, что 2 моля NH
3 должны разложиться на каждый образовавшийся моль N 2 . Однако изменение концентрации NH 3 является отрицательным , потому что концентрация аммиака уменьшается по мере его разложения.
Однако изменение концентрации NH 3 является отрицательным , потому что концентрация аммиака уменьшается по мере его разложения.∆[NH 3 ] = – 2 × ∆[N 2 ] = – 2 × 0,11 моль/л = – 0,22 моль/л
Мы можем напрямую связать эти отношения с коэффициентами в уравнении
Обратите внимание, что все изменения с одной стороны стрелок одного знака и что все изменения по другую сторону стрелок имеют противоположный знак.
Если бы мы не знали величину изменения концентрации N 2 , мы могли бы представить ее символом + x .
∆[N 2 ] = + х
Изменения других концентраций будут тогда представлены как: [N 2 ] = – 2x
Коэффициенты в членах Δ идентичны коэффициентам в сбалансированном уравнении реакции.
| 2 NH 3 (g) ⇌ | N 2 (g) + | 3 Ч 2 (г) |
| -2x | +x | + 3x |
Самый простой способ найти коэффициенты для изменения концентрации в любой реакции — использовать коэффициенты в сбалансированном химическом уравнении. Знак коэффициента положительный при увеличении концентрации; он отрицательный, когда концентрация уменьшается.
Знак коэффициента положительный при увеличении концентрации; он отрицательный, когда концентрация уменьшается.
Пример 4.3.1 – Определение относительных изменений концентрации
Завершите изменения концентраций для каждой из следующих реакций.
Решение
Проверьте свое обучение 4.3.1 – Определение относительных изменений в концентрации
Заполните изменения в концентрациях для каждой из следующих реакций:
Ответ(A) +
(A) +
(A) +
(A) +
. 2 х , + х , – 2 х; (б) + х , – 2 х; (в) + 4 x , + 7 x , – 4 x , – 6 x или – 4 x , – 7 x , + 4 x , + 6 x , + 4 x , + 6 x , + 4 x , + 6 7777777777 гг. Равновесные концентрации или давления
Равновесные концентрации или давления
Поскольку значение отношения реакции любой реакции в равновесии равно ее константе равновесия, мы можем использовать математическое выражение для Q , чтобы определить количество величин, связанных с реакцией в равновесии. Это может помочь, если мы будем помнить, что Q = K (в равновесии) во всех этих ситуациях и что существует только два основных типа задач равновесия:
- Расчет константы равновесия. Если известны концентрации/парциальные давления реагентов и продуктов при равновесии, можно рассчитать значение константы равновесия реакции.
- C расчет равновесных концентраций/парциальных давлений. Если значение константы равновесия и все равновесные концентрации/давления, кроме одного, известны, можно рассчитать остальные неизвестные. Кроме того, если известно значение константы равновесия и набор концентраций или давлений реагентов и продуктов, которые не находятся в равновесии, можно рассчитать количество в равновесии.

В следующем обсуждении мы рассмотрим примеры расчетов равновесия с участием растворенных веществ и значений K в единицах концентрации ( K C ). Однако обратите внимание, что процедуры решения задач в равной степени справедливы для реакций с участием газов и значений K в единицах давления ( K P ).
Расчет константы равновесия
Для расчета константы равновесия необходимо иметь достаточно информации для определения равновесных концентраций всех реагентов и продуктов. Вооружившись концентрациями, мы можем решить уравнение для K , так как это будет единственный неизвестный.
В предыдущем разделе мы узнали, как определить константу равновесия реакции, если известны концентрации реагентов и продуктов при равновесии. В следующем примере показано, как использовать стехиометрию реакции и комбинацию начальных концентраций и равновесных концентраций для определения константы равновесия. Этот метод, обычно называемый диаграммой ICE (начальное состояние, изменение и равновесие), будет полезен при решении многих проблем с равновесием. Диаграмма создается, начиная с рассматриваемой равновесной реакции. Начальные концентрации реагентов и продуктов приведены в первой строке таблицы ICE (эти концентрации, по сути, нулевые по времени, которые предполагают, что реакция не произошла). Следующая строка таблицы содержит изменения концентраций, происходящие при приближении реакции к равновесию (не забывайте учитывать стехиометрию реакции). Последняя строка содержит концентрации после достижения равновесия.
Этот метод, обычно называемый диаграммой ICE (начальное состояние, изменение и равновесие), будет полезен при решении многих проблем с равновесием. Диаграмма создается, начиная с рассматриваемой равновесной реакции. Начальные концентрации реагентов и продуктов приведены в первой строке таблицы ICE (эти концентрации, по сути, нулевые по времени, которые предполагают, что реакция не произошла). Следующая строка таблицы содержит изменения концентраций, происходящие при приближении реакции к равновесию (не забывайте учитывать стехиометрию реакции). Последняя строка содержит концентрации после достижения равновесия.
Пример 4.3.2 – Расчет константы равновесия – 1
Молекулы йода обратимо реагируют с ионами йода с образованием ионов трийодида.
I 2 ( aq ) + I – ( aq ) ⇌ I 3 – ( aq )
If a раствор с концентрациями I 2 и I − , равными 1,000 × 10 -3 моль/л до реакции дает равновесную концентрацию I 2 , равную 6,61 × 10 -4 моль/л, какова константа равновесия реакции?
Решение
Мы начнем эту задачу с расчета изменений концентрации по мере того, как система приходит в равновесие. Затем определяем равновесные концентрации и, наконец, константу равновесия. Во-первых, мы составили таблицу с начальными концентрациями, изменениями концентраций и равновесными концентрациями, используя – x как изменение концентрации I 2 .
Затем определяем равновесные концентрации и, наконец, константу равновесия. Во-первых, мы составили таблицу с начальными концентрациями, изменениями концентраций и равновесными концентрациями, используя – x как изменение концентрации I 2 .
I 2 +I − ⇌ I 3 −
| I 2 | I – | I 3 – |
Начальная концентрация ( моль/л ) | 1.000 х 10 −3 | 1.000 x 10 −3 | 0 |
Изменение ( моль/л ) | – 𝑥 | – 𝑥 | +𝑥 |
Равновесная концентрация ( моль/л ) | 1. 000 x 10 −3 – 𝑥 000 x 10 −3 – 𝑥 | 1.000 x 10 −3 – 𝑥 | +𝑥 |
Поскольку равновесная концентрация I 2 задана, мы можем найти x . В равновесии концентрация I 2 составляет 6,61 × 10 −4 М, поэтому: – 6,61 × 10 -4
x = 3,39 × 10 -4 моль/л
Теперь мы можем заполнить таблицу равновесными концентрациями.
I 2 +I − ⇌ I 3 −
| 8 | |||
| I 2 | I − | I 3 − | |
| Начальная концентрация ( моль/л ) | 1.000 x 10 −3 | 1.000 x 10 −3 | 0 |
| Изменение ( моль/л ) | – 𝑥 = -3,39 x 10 −4 | – 𝑥 | +𝑥 |
| Равновесная концентрация ( моль/л ) | 6,61 x 10 −4 | 6,61 x 10 −4 | 3,39 x 10 −4 |
Теперь вычислим значение константы равновесия.
Это значение для K имеет смысл — он близок к 1, что указывает на то, что при равновесии система будет содержать сопоставимые количества реагентов и продуктов. Это верно, когда мы смотрим на равновесную концентрацию в таблице ICE или даже визуализируем близость кривых концентрации (на графике) видов при достижении равновесия (рис. 4.3.1).
Рисунок 4.3.1. При значении K относительно близком к 1 концентрации реагентов и продуктов приближаются друг к другу, когда система движется к равновесию.
Проверьте свои знания 4.3.2 – Расчет константы равновесия – 1
Этанол и уксусная кислота реагируют с образованием воды и этилацетата, растворителя, ответственного за запах некоторых жидкостей для снятия лака:
C 2 H 5 OH + CH 3 CO 2 H ⇌ CH 3 CO 2 C 2 H 5 + H 2 O
Когда 1,00 моль C 2 ч. 5 OH и CH 3 CO 2 H дают прореагировать в 1 л растворителя диоксана, равновесие устанавливается, когда остается 0,13 моль каждого из реагентов. Рассчитайте константу равновесия реакции. (Примечание: вода не является растворителем в этой реакции.)
5 OH и CH 3 CO 2 H дают прореагировать в 1 л растворителя диоксана, равновесие устанавливается, когда остается 0,13 моль каждого из реагентов. Рассчитайте константу равновесия реакции. (Примечание: вода не является растворителем в этой реакции.)
Ответ
K C = 45
Пример 4.3.3 – Расчет константы равновесия – 2
3.003. моль образца NOCl помещали в реактор объемом 2,00 л и нагревали до 227°С до достижения системой равновесия. Затем содержимое реактора было проанализировано и было обнаружено, что оно содержит 0,056 моль Cl 9 .0008 2 . Рассчитайте K C при этой температуре. Уравнение разложения NOCl на NO и Cl 2 выглядит следующим образом:
2 NOCl ( г) ⇌ 2 NO (г) + Cl 2 8 Решение
Первым шагом в любой такой задаче является балансирование химического уравнения реакции (если оно еще не сбалансировано) и использование его для получения выражения для константы равновесия. В этом случае уравнение уже уравновешено, и выражение для константы равновесия имеет следующий вид:
В этом случае уравнение уже уравновешено, и выражение для константы равновесия имеет следующий вид:
Изначально система содержит 1,00 моль NOCl в 2,00-литровом контейнере. Таким образом, [NOCl] i = 1,00 моль/2,00 л = 0,500 моль/л. Начальные концентрации NO и Cl 2 равны 0 моль/л, поскольку изначально продукты отсутствуют. Более того, нам говорят, что в равновесии система содержит 0,056 моль Cl 2 в сосуде объемом 2,00 л, поэтому [Cl 2 ] f = 0,056 моль/2,00 л = 0,028 моль/л. Вставляем эти значения в следующую таблицу:
2 NOCl ( g) ⇌ 2 NO (g) + Cl 2 | |||
[ NOCl ] | [НО] | [Кл 2 ] | |
Исходная концентрация (моль/л) | 0,500 | 0 | 0 |
Изменение (моль/л) | |||
Равновесная концентрация (моль/л) | 0,028 | ||
Используя стехиометрические соотношения, приведенные в сбалансированном химическом уравнении, найдем изменение концентрации Cl 2 , вещества, для которого известны начальная и конечная концентрации:
Δ[Cl 2 ] = [0,028 моль /л (конечная) − 0,00 моль/л (исходная)] = + 0,028 моль/л
Согласно коэффициентам в сбалансированном химическом уравнении, на каждый 1 моль Cl 2 образуется 2 моль NO, поэтому изменение концентрации NO выглядит следующим образом:
Аналогично, на каждый 1 моль произведенного Cl 2 расходуется 2 моля NOCl, поэтому изменение концентрации NOCl выглядит следующим образом:
Вставляем эти значения в нашу таблицу:
2 NOCl ( g) ⇌ 2 NO (g) + Cl 2 | |||
[ NOCl ] | [НО] | [Кл 2 ] | |
| Исходная концентрация (M) | 0,500 | 0 | 0 |
| Смена (М) | -0,056 | +0,056 | 907:35|
| Равновесная концентрация (M) | 0,028 | ||
Суммируем числа в столбцах [NOCl] и [NO] для получения конечных концентраций NO и NOCl:
[NO] f = 0,000 М + 0,056 М = 0,056 М
[NOCl] f = 0,500 М + (-0,056 М) = 0,444 М
Теперь мы можем заполнить таблицу:
2 NOCl ( g) ⇌ 2 NO (g) + Cl 2 | |||
[ NOCl ] | [НО] | [Кл 2 ] | |
| Исходная концентрация (M) | 0,500 | 0 | 0 |
| Смена (М) | -0,056 | +0,056 | +0,028 |
| Равновесная концентрация (M) | 0,444 | 0,056 | 0,028 |
Теперь мы можем рассчитать константу равновесия реакции:
Проверьте свои знания 4. 3.3 – Расчет константы равновесия – 2
3.3 – Расчет константы равновесия – 2
Немецкий химик Фриц Габер (1868–1934; Нобелевская премия по химии, 1918 г.) ) смог синтезировать аммиак (NH 3 ) путем взаимодействия 0,1248 M H 2 и 0,0416 M N 2 при температуре около 500 °C (рис. 4.3.2). При равновесии смесь содержала 0,00272 М NH 3 . Что такое K C для реакции N 2 + 3H 2 ⇌ 2NH 3 при этой температуре? Каково значение K P ?
Рисунок 4.3.2. Оригинальный лабораторный аппарат, разработанный Фрицем Хабером и Робертом Ле Россиньолем в 1908 году для синтеза аммиака из его элементов. Слой металлического катализатора, на котором производился аммиак, находится в большом цилиндре слева. Процесс Габера-Боша, используемый для промышленного производства аммиака, использует по существу тот же процесс и компоненты, но в гораздо большем масштабе. К сожалению, процесс Габера позволил Германии продлить Первую мировую войну, когда немецкие запасы соединений азота, которые использовались для взрывчатых веществ, были исчерпаны в 1919 г.14.
К сожалению, процесс Габера позволил Германии продлить Первую мировую войну, когда немецкие запасы соединений азота, которые использовались для взрывчатых веществ, были исчерпаны в 1919 г.14.
Ответ
К С = 0,105; K P = 2,61 × 10 −5
Расчет равновесной концентрации (концентраций) равновесия всех реагентов и продуктов, кроме одного, можно вычислить недостающую концентрацию.
Пример 4.3.4 – Расчет недостающей равновесной концентрации
Оксиды азота представляют собой загрязнители воздуха, образующиеся в результате реакции азота и кислорода при высоких температурах. При 2000°С значение константы равновесия К С для реакции, Н 2 (г) + О 2 ( 7 7 7 NO г г) г) ) , равно 4,1 × 10 −4 . Рассчитайте равновесную концентрацию NO (г) в воздухе при давлении 1,00 атм и температуре 2000°С. Равновесные концентрации N 2 и О 2 при этих давлении и температуре равны 0,036 М и 0,0089 М соответственно.
Равновесные концентрации N 2 и О 2 при этих давлении и температуре равны 0,036 М и 0,0089 М соответственно.
Раствор
Нам даны все равновесные концентрации, кроме NO. Таким образом, мы можем найти недостающую равновесную концентрацию, изменив уравнение для константы равновесия.
Таким образом, [NO] составляет 3,6 × 10 -4 моль/л в равновесии в этих условиях.
Мы можем проверить наш ответ, подставив все равновесные концентрации в выражение для коэффициента реакции, Q C , чтобы увидеть, равна ли она константе равновесия, и тем самым подтвердить, что система действительно находится в равновесии.
Проверка ответа; наше вычисленное значение дает константу равновесия в пределах погрешности, связанной со значащими цифрами в задаче.
Проверьте свои знания 4.3.4 – Расчет недостающей равновесной концентрации
Константа равновесия реакции азота и водорода с образованием аммиака при определенной температуре составляет 6,00 × 10 −2 . Рассчитайте равновесную концентрацию аммиака, если равновесные концентрации азота и водорода равны 4,26 М и 2,09 М соответственно.
Рассчитайте равновесную концентрацию аммиака, если равновесные концентрации азота и водорода равны 4,26 М и 2,09 М соответственно.
Ответ
1,53 моль/л
В другом сценарии, если мы знаем константу равновесия реакции и набор концентраций реагентов и продуктов, которые не находятся в равновесии , мы можем рассчитать изменения концентраций по мере того, как система приходит в равновесие, а также новые концентрации при равновесии. Типичная процедура может быть сведена к четырем этапам.
1. Определите направление, в котором протекает реакция, чтобы прийти к равновесию.
а. Напишите сбалансированное химическое уравнение реакции.
б. Если направление, в котором должна идти реакция для достижения равновесия, не совсем очевидно, вычислите Q по начальным значениям и сравните его с K с
и определите направление изменения.
2. Определите относительные изменения, необходимые для достижения равновесия, затем запишите
равновесные концентрации с точки зрения этих изменений.
а. Определите изменения начальных концентраций, необходимые для достижения равновесия реакции
. Как правило, мы обозначаем наименьшее изменение
символом x , а остальные изменения выражаем через наименьшее изменение
.
б. Определить отсутствующие равновесные концентрации с точки зрения исходных
концентраций и изменений концентрации, определенных в (а).
3. Найдите изменение и равновесные концентрации.
а. Подставьте равновесные концентрации в выражение для константы равновесия
, найдите x и проверьте все допущения, использованные для нахождения x .
б. Рассчитайте равновесные концентрации.
4. Проверьте арифметику.
5. Проверьте рассчитанные равновесные концентрации, подставив их в
выражения равновесия и определить, дают ли они константу равновесия
.
Иногда конкретный шаг может отличаться от проблемы к проблеме — он может быть более сложным в одних задачах и менее сложным в других. Однако каждый расчет равновесных концентраций по набору начальных концентраций будет включать эти этапы.
Однако каждый расчет равновесных концентраций по набору начальных концентраций будет включать эти этапы.
При решении задач равновесия, связанных с изменением концентрации, снова очень удобно составить таблицу ICE.
Пример 4.3.5 – Расчет изменения концентрации при переходе реакции к равновесию (г) и Cl 2 (г) составляет 0,0211. Каковы равновесные концентрации PCl 5 , PCl 3 и Cl 2 , если исходная концентрация PCl 5 была 1,00 М?
Решение
Используйте пошаговый процесс, описанный ранее.
1. Определите направление реакции.
The balanced equation for the decomposition of PCl 5 is
PCl 5 ( g) ⇌ PCl 3 (g) + Cl 2 (g)
Поскольку изначально у нас нет продуктов, Q = 0 и реакция должна идти вправо (в сторону продуктов).
2. Определите относительные изменения, необходимые для достижения равновесия, затем запишите равновесные концентрации в терминах этих изменений.
Обозначим увеличение концентрации PCl 3 символом x . Другие изменения могут быть записаны в терминах x с учетом коэффициентов в химическом уравнении.
PCl 5 ( г) ⇌ PCl 3 (g) + Cl 2 (g)
– x + x + x
Изменения концентрации и выражения для концентрации равновесия:
PCL 5 ⇌ PCL 3 + Cl 2
| PCl 5 | PCl 3 | Класс 2 |
| Начальная концентрация (M) | 1,00 | 0 | 0 |
| Смена (М) | – 𝑥 | +𝑥 | +𝑥 |
| Равновесная концентрация (M) | 1,00 – 𝑥 | 0 + 𝑥 = 𝑥 | 0 + 𝑥 = 𝑥 |
3. Найдите изменение и равновесные концентрации.
Найдите изменение и равновесные концентрации.
Подстановка равновесных концентраций в уравнение константы равновесия дает
Это уравнение содержит только одну переменную, x , изменение концентрации. Мы можем написать уравнение как квадратное уравнение и решить для x , используя квадратную формулу.
В приложении C показано уравнение вида x 2 + bx + c = 0, которое можно преобразовать для решения для x :
90,477. В этом случае б = 0,0211 и с = -0,0211. Подставляя соответствующие значения для a , b и c выходы:
| ПРИМЕЧАНИЕ: |
Квадратные уравнения часто имеют два разных решения: одно физически возможно , а другое физически невозможно (посторонний корень). Посторонний корень может быть, например, отрицательным значением или физически незначительным (например, если «Изменение» в таблице ICE равно 0,100 — x и одно возможное значение для x равно 0,300, то это значение не может быть физически возможным, потому что это дало бы отрицательное значение для равновесной концентрации). |
В этом случае второе решение (-0,156) физически невозможно, поскольку мы знаем, что изменение должно быть положительным числом (иначе мы получили бы отрицательные значения концентраций продуктов). Таким образом, x = 0,135 M.
Равновесные концентрации равны
[PCL 5 ] = 1,00 – 0,135 = 0,87 м
[PCL 3 ] = x = 0,135 м
[CL 2 ] = x = 0,135 м
4. Проверьте аритметику.
Подстановка в выражение для K c (для проверки расчета) дает
Константа равновесия, рассчитанная по равновесным концентрациям, равна значению K 90 задача (при округлении до нужного числа значащих цифр). Таким образом, расчетные равновесные концентрации подтверждаются.
Проверьте свои знания 4.3.5 – Расчет изменения концентрации при переходе реакции к равновесию для образования воды и этилацетата, CH 3 CO 2 C 2 H 5 .
CH 3 CO 2 H + C 2 H 5 OH ⇌ CH 3 CO 2 C 2 H0008 2 O
Константа равновесия этой реакции при определенной температуре с использованием диоксана в качестве растворителя равна 4,0. Каковы равновесные концентрации, когда 0,15 моль Ch 3 CO 2 H, 0,15 моль C 2 H 5 OH, 0,40 моль CH 3 CO 2 C 2 H 5 и и и 0,40 моль H 2 O смешивают с диоксановым растворителем в количестве, достаточном для получения 1,0 л раствора?
Ответить
[CH 3 СО 2 Н] = 0,36 М, [С 2 Н 5 ОН] = 0,36 М, [СН 3 СО 2 С 2 Н 1 9000. 2 O] = 0,17 М
Проверьте свои знания 4.3.6 – Расчет изменения концентрации по мере того, как реакция достигает равновесия I 2 . Значение константы равновесия К С для реакции водорода и йода, реагирующих с образованием йодистого водорода, составляет 50,5 при данных условиях. Каковы равновесные концентрации H 2 , I 2 и HI в молях/л?
Значение константы равновесия К С для реакции водорода и йода, реагирующих с образованием йодистого водорода, составляет 50,5 при данных условиях. Каковы равновесные концентрации H 2 , I 2 и HI в молях/л?
H 2 (G) + I 2 ( G) ⇌ 2 HI (G)
Ответ
[H 2 = = INS [H 2 . 2 ] = 1,06 M, [HI] = 1,88 M Теперь давайте рассмотрим другой пример, в котором мы можем использовать метод быстрого извлечения квадратного корня для облегчения решения задач. Если мы обнаружим, что дробный член, состоящий из реагентов (знаменатель) и продуктов (числитель), имеет совершенные квадраты, мы можем извлечь квадратный корень из обеих частей при решении для х . Пример 4.3.6. Изменение концентрации по мере того, как реакция достигает равновесия. . This reaction can be written as follows: H 2 (g) + CO 2 ( g) ⇌ H 2 O (g) + CO (g) K C = 0,106 при 700 K. Раствор Начальные концентрации реагентов: [H 2 ] i = [CO 2 ] i = 0,0150 М. концентрации различных веществ между начальным и конечным состояниями. Если определить изменение концентрации H 2 O равно x , тогда Δ[H 2 O] = + x . Мы можем использовать стехиометрию реакции, чтобы выразить изменения концентраций других веществ в терминах x . Например, на каждый 1 моль H 2 O образуется 1 моль CO, поэтому изменение концентрации CO можно выразить как Δ[CO] = + x . Аналогично, на каждый 1 моль полученного H 2 O расходуется по 1 молю H 2 и CO 2 , поэтому изменение концентрации реагентов равно Δ[H 2 ] = Δ[CO 2 ] = – x . H 2 (g) + CO 2 ( g) ⇌ H 2 O (г) + CO (г) [Н 2 ] [CO 2 ] [Н 2 О] [СО] 0,0150 0,0150 0 0 – х – х + х + х + х + х Теперь мы можем использовать уравнение равновесия и заданное K для решения для x : Мы могли бы решить это уравнение с помощью квадратичной формулы, но гораздо проще решить для x , если признать, что левая часть уравнения — полный квадрат; то есть Извлечение квадратного корня из обеих частей этого уравнения дает Конечные концентрации всех соединений в реакционной смеси следующие: Мы можем проверить нашу работу, подставив вычисленные значения обратно в выражение для константы равновесия: Проверьте свои знания 4.3.7 – Изменения концентрации по мере того, как реакция достигает равновесия – Квадратный корень Ярлык Газообразный водород реагирует с парами йода с образованием йодистого водорода в соответствии со следующим химическим уравнением: К С = 54,0 при 425°С. Если 0,172 М H 2 и I 2 вводят в реактор и поддерживают при 425°C до тех пор, пока система не уравновесится, какова будет конечная концентрация каждого вещества в реакционной смеси? Ответ [HI] f = 0,270 М; [H 2 ] f = [I 2 ] f = 0,037 M Иногда можно использовать химическую интуицию, чтобы найти решения проблем равновесия без фактического решения квадратного (или более сложного) уравнения. Однако сначала полезно проверить, что равновесие может быть достигнуто, исходя из двух крайностей: всех (или большей части) реагентов и всех (или большей части) продуктов. Рассмотрим ионизацию 0,150 М ГК, слабой кислоты. HA ( aq ) + H 2 O ( l ) ⇌ H 3 O + ( aq ) + A – ( aq ) K C =6,80×10 -4 Наиболее очевидный способ определения равновесных концентраций – начать с системы, содержащей только реагенты. Это можно назвать отправной точкой «все реагенты». Использование x для количества кислоты, ионизированной в равновесии, это таблица и решение ICE. HA ( aq ) + H 2 O ( l ) ⇌ H 3 O + ( aq ) + A – ( водный ) ─ ─ ─ Составление и решение квадратного уравнения дает Используя положительный (физический) корень, равновесные концентрации равны 0,00977 M Менее очевидный способ решения проблемы состоит в том, чтобы предположить, что все ГА сначала ионизируется, затем система приходит в равновесие. [ГК] = 0,150 – 0,150 = 0 М [H 3 O + ] = 0 + 0,150 = 0,150 M [A – ] = 0 + 0,150 = 0,150 M Если смесь газов, первоначально содержащая 0,0150 M H 2 и 0,0150 M CO 2 , уравновесить конечные концентрации всех концентраций при 700 K, каковы присутствующие вещества?
Если смесь газов, первоначально содержащая 0,0150 M H 2 и 0,0150 M CO 2 , уравновесить конечные концентрации всех концентраций при 700 K, каковы присутствующие вещества? Мы вводим значения в следующую таблицу и рассчитываем конечные концентрации.
Мы вводим значения в следующую таблицу и рассчитываем конечные концентрации. Исходная концентрация (M) Смена (М) Равновесная концентрация (M) (0,0150- x ) (0,0150– x ) 

Исходная концентрация (M) 0,150 0 0 Смена (М) – х + х + х Равновесная концентрация (M) 0,150 – x + х + х  Это можно назвать отправной точкой для «всех продуктов». Предполагая, что все ГК ионизируются, получаем
Это можно назвать отправной точкой для «всех продуктов». Предполагая, что все ГК ионизируются, получаем
HA ( AQ ) + H 2 O ( L ) ⇌ h 3 O +
) ⇌ H 3 O +
: .0478 + А – ( водный номер )
Начальная концентрация (M) | 0 | ─ | 0,150 | 0,150 |
Смена (М) | +у | ─ | – у | – у |
Равновесная концентрация (M) | +у | ─ | 0,150 – г | 0,150 – г |
Составление и решение квадратного уравнения дает
Оставьте несколько лишних значащих цифр, чтобы свести к минимуму проблемы с округлением.
Округление каждого решения до трех значащих цифр дает
y = 0,160 М или y = 0,140 М
Использование физически значимого корня (0,140 М) дает равновесные концентрации как
[HA] = y = 9,140 М0004
[H 3 O + ] = 0,150 – y = 0,010 M
[A – ] = 0,150 – y = 0,010 M
Таким образом, два десятичных подхода дают одинаковые результаты расставляет 90 478 ), и покажите, что 90 477 обеих 90 478 исходных точек приводят к одним и тем же условиям равновесия (рис. 4.3.3). Начальная точка «все реагенты» привела к относительно небольшому изменению ( x ), поскольку система была близка к равновесию, в то время как исходная точка «все продукты» имела относительно большое изменение ( y ), что почти равнялось размеру начальных концентраций. Обратите внимание, что на графике в части (а) рис. 4.3.3 наблюдается незначительное изменение концентрации; следовательно, можно сказать, что системе, которая начинается «близко» к равновесию, потребуется лишь «небольшое» изменение условий ( x ), чтобы достичь равновесия.
Рисунок 4.3.3. Независимо от того, где вы начинаете, будь то 100 % реагентов в (а) или 100 % продуктов в (б), мы все равно окажемся в одной и той же точке равновесия. (а) Изменение концентраций реагентов и продуктов изображается как HA ( aq ) ⇌ H + ( aq ) + A – ( aq ) reaction approaches equilibrium, when going from an “all reactant ” отправная точка. (б) Изменение концентраций реагентов и продуктов изображается как реакция HA ( aq ) ⇌ H + ( aq ) 7
– + A0478 aq ) приближается к равновесию при переходе от исходной точки «все продукты». Напомним, что небольшое значение K означает, что очень небольшое количество реагентов образует продукты, а большое K означает, что большинство реагентов образуют продукты. Если систему можно устроить так, чтобы она начиналась «близко» к равновесию, то если изменение ( x ) мало по сравнению с любыми исходными концентрациями, им можно пренебречь. Следующие два примера демонстрируют это.
Если систему можно устроить так, чтобы она начиналась «близко» к равновесию, то если изменение ( x ) мало по сравнению с любыми исходными концентрациями, им можно пренебречь. Следующие два примера демонстрируют это.
ПРИМЕЧАНИЕ: |
Для задач равновесия в CHM1311, «x мало» официально определено как приводящее к ошибке менее 5% . |
Пример 4.3.7 – Приблизительное начало раствора близко к равновесию
Каковы равновесные концентрации 0,15 М раствора HCN?
HCN ( aq ) + H 2 O (l) ⇌ H 3 O + ( aq ) + CN – ( aq ) K = 4,9 x 10 -10
Раствор
Использование « x » для представления концентрации каждого продукта в равновесии дает эту таблицу ICE.
HCN ( водный ) + H 2 O (l) ⇌ H 3 O + ( aq ) + CN – ( aq )
| ХКН ( водный номер ) | Н 2 О (л) | H 3 O + ( водный ) | CN – ( aq ) | |
| Начальная концентрация (M) | 0,15 | ─ | 0 | 0 |
| Смена (М) | -х | ─ | +х | +х |
| Равновесная концентрация (M) | 0,15 -х | ─ | +х | +х |
Точное решение можно получить с помощью квадратичной формулы с
решение
Таким образом, [H 3 O + ] = [CN – ] = x = 8,6 × 10 –6 M и [HCN] = 0,47 x M и [HCN] = 0,47 x 9,15 – 9,15 x M.
В этом случае химическая интуиция может дать более простое решение. Из константы равновесия и начальных условий х должно быть мало по сравнению с 0,15 М. Более формально, если х ≪ 0,15, то 0,15 – х ≈ 0,15 (рис. 4.3.4 наглядно демонстрирует это).
Рисунок 4.3.4. Концентрации реагентов и продуктов показаны исходно и в равновесии для следующей реакции: HCN ( водный ) +H 2 O (l ) 3 7 O 4 3 7 O 4 ( aq ) + CN – ( aq ) . Реакция начинается только с HCN ( aq ) , но даже при равновесии можно сказать, что относительные количества H + и CN – настолько мало, что ими можно пренебречь – остается практически пока единственный реагент, который демонстрирует крайне малую K величину реакции и подтверждает справедливость предположения о том, что 0,15 – x ≈ 0,15.
Если это предположение верно, то оно упрощает получение x
В этом примере решение точного (квадратного) уравнения и использование приближений дали один и тот же результат для двух значащих цифр. Хотя в большинстве случаев приближение немного отличается от точного решения, если ошибка составляет менее 5%, приближенное решение считается действительным. В этой задаче 5% относятся к (0,15 – x ) ≈ 0,15 М, поэтому, если
меньше 5%, как в данном случае, предположение верно. Таким образом, приближенное решение является допустимым решением.
Проверьте свои знания 4.3.8 – Приблизительное решение, начиная с близкого к равновесию
Каковы равновесные концентрации в 0,25 М растворе NH 3 ?
NH 3 ( aq ) + H 2 O (l ) ⇌ NH 4 90
 8 x 10 -5
8 x 10 -5 Assume that x is much less than 0.25 M and посчитайте ошибку в вашем предположении.
Ответ
[OH − ] = [NH 4 + ] = 0,0021 М; [NH 3 ] = 0,25 М, ошибка = 0,84%
Всякий раз, когда вы делаете предположение, что [ начальный ] ≈ [ равновесный ] поскольку ошибка составляет менее 5%, вы ДОЛЖНЫ фактически выполнить расчеты и проверить, действительно ли ошибка меньше 5% и, следовательно, предположение верно. |
Второй пример требует, чтобы исходная информация была немного обработана, но его все еще можно решить, используя небольшое приближение x .
Пример 4.3.8 – Приблизительное решение после изменения начальной концентрации
Ионы меди(II) образуют комплексный ион в присутствии аммиака
Если 0,010 моль Cu 2+ добавить к 1,00 л раствора, содержащего 1,00 М NH 3 приходит в равновесие?
Решение:
Начальная концентрация меди(II) равна 0,010 М. Константа равновесия очень велика, поэтому было бы лучше начать с как можно большего количества продукта, потому что «все продукты» гораздо ближе к равновесию, чем «все реагенты» (рис. 4.3.5). Поэтому для упрощения расчетов будем считать, что реакция идет на 100% до конца. Обратите внимание, что Cu 2+ – лимитирующий реагент; Если все 0,010 М от него реагирует на формирование продукта, концентрации
Константа равновесия очень велика, поэтому было бы лучше начать с как можно большего количества продукта, потому что «все продукты» гораздо ближе к равновесию, чем «все реагенты» (рис. 4.3.5). Поэтому для упрощения расчетов будем считать, что реакция идет на 100% до конца. Обратите внимание, что Cu 2+ – лимитирующий реагент; Если все 0,010 М от него реагирует на формирование продукта, концентрации
будут
[CU 2 + ] = 0,010 – 0,010 = 0 м
[CU (NH 3 ) 4 2 2+ ] = 0,010 M
[NH 3 ] = 1,00 – 4 x 0,010 = 0,96 M
Рисунок 4.3.5. Значение K очень велико для равновесной реакции Cu 2+ ( aq ) + 4NH 3 ( AQ ) ⇌ CU (NH 3 ) 2+ ( 2+ ( . Изменение концентрации как продуктов, так и реагентов почти минимально, поскольку в нынешнем виде относительная концентрация всех частиц первоначально почти уже соответствует относительным количествам в равновесии, когда продукт близок к максимально возможной концентрации.
Использование этих «смещенных» значений в качестве начальных концентраций с x в качестве концентрации свободных ионов меди (II) в равновесии дает эту таблицу ICE.
Cu 2+ ( aq ) +4NH 3 ( aq ) ⇌Cu(NH 3 ) 4 2+ ( водный )
| Cu 2+ ( водный номер ) | 4NH 3 ( водный ) | Cu(NH 3 ) 4 2+ ( водный ) |
| Начальная концентрация (M) | 0 | 0,96 | 0,010 |
| Смена (М) | +х | +4x | -х |
| Равновесная концентрация (M) | +х | 0,96 + 4x | 0,010 – х |
Поскольку мы начинаем близко к равновесию, x должно быть небольшим, чтобы
Выберите наименьшую концентрацию для правила 5% – проверить правило 5%.
Это намного меньше 5%, так что предположения верны. Равновесные концентрации равны
[CU 2+ ] = x = 2,4 x 10 -16 M
[NH 3 ] = 0,96 -4x = 0,96 М
[CU (NH 3 ) 4 2 2 2 2 [NH 3 ) 4 0009 2 2 [NH 3 ) + ] = 0,010 – x = 0,010 M
Если мы, например, вычтем x из 0,010 M, мы получим 0,00999999… M, что при подсчете значащих цифр все равно округляется до 0,010 M.
В целом, мы начали с гораздо более высокой концентрации реагента по сравнению с продуктом – обратите внимание, что мы израсходовали Cu 2+ поэтому изначально имеем максимально возможную концентрацию продуктов. Но поскольку K очень велико, изменение концентрации сохраняется минимальным, поскольку эта реакционная смесь почти практически соответствует тому, что ожидается при равновесии.
Начиная с максимального количества продукта, эта система была близка к равновесию, и изменение ( x ) было очень небольшим – это очень небольшое изменение было вызвано, в частности, полным отсутствием Cu 2+ изначально (мы обсудим это в контексте принципа Ле Шателье в следующем разделе). С небольшим изменением, необходимым для достижения равновесия, уравнение для x было значительно упрощено и дало достоверный результат в пределах максимума ошибки 5%.
С небольшим изменением, необходимым для достижения равновесия, уравнение для x было значительно упрощено и дало достоверный результат в пределах максимума ошибки 5%.
Проверьте свои знания 4.3.9 – Приблизительное решение после изменения начальной концентрации
Каковы равновесные концентрации при добавлении 0,25 моль Ni 2+ к 1,00 л 2,00 М NH 3 решение?
NI 2+ ( AQ ) + 6 NH 3 ( AQ ) ⇌ NI (NH ). aq ) K C = 5,5 x 10 8
При такой большой константе равновесия сначала сформируйте как можно больше продукта, а затем предположите, что осталось лишь небольшое количество ( x ) продукта. . Вычислите ошибку в вашем предположении.
. Вычислите ошибку в вашем предположении.
Ответ
[NI (NH 3 ) 6 2+ ] = 0,25 м, [NH 3 ] = 0,50 м, [Ni 2+ ] = 2,] = 0,50 м, [NI 2+ ] = 2,] = 0,50 м, [NI 2+ ] = 2,] = 0,50 м, [NI 2+ ] = 2,] = 0,50 м, 8 м, ошибка = 1,2 × 10 –5 %
Вопросы
★ Вопросы
1. В равновесном реакции A + B ⇌ C, то, что происходит до K 9078. реагентов увеличилось вдвое? утроился? Можно ли то же самое сказать о равновесной реакции А ⇌ В + С?
2. В следующей таблице приведены зарегистрированные значения равновесия P{O 2 } при трех температурах для реакции Ag 2 O ( с) ⇌ 2 Ag (с) + 2 O 2 (ж) для которых Δ H ° = 31 кДж/моль. Соответствуют ли эти данные тому, что вы ожидаете? Почему или почему нет?
Т (°С) | П (О 2 ) мм рт. |
150 | 182 |
184 | 143 |
191 | 126 |
3. Учитывая систему равновесия N 2 O 4 ( g) ⇌ 2 NO 2 (g),
8 что происходит с (g),80477 K P , если начальное давление N 2 O 4 удваивается? Если K P равно 1,7 × 10 −1 при 2300 °С, а система исходно содержит 100 % N 2 O 4 при давлении 2,7 × 3 3 29093 бар, чему равно равновесное давление каждого компонента? 4. При 430°C 4,20 моль HI в реакционном сосуде объемом 9,60 л достигает равновесия в соответствии со следующим уравнением: H 2 (г) + I 2 ( г) ⇌ 2 HI (г). В равновесии [H 2 ] = 0,047 M и [HI] = 0,345 M. Что такое K и K P для этой реакции?
В равновесии [H 2 ] = 0,047 M и [HI] = 0,345 M. Что такое K и K P для этой реакции?
5. Метанол, жидкость, используемая в качестве добавки к автомобильному топливу, производится в промышленных масштабах из монооксида углерода и водорода при температуре 300 °C в соответствии со следующей реакцией: CO (g) + 2 H 2 (г) ⇌ CH 3 OH (г) и K P = 1,3 × 10 −4 . Если 56,0 г CO смешать с избытком водорода в колбе на 250 мл при этой температуре и постоянно поддерживать давление водорода на уровне 100 бар, каков будет максимальный выход метанола в процентах? Какое давление водорода потребуется для получения минимального выхода метанола 95% в этих условиях?
★★ Вопросы
6. Начиная с чистого А, если полное равновесное давление равно 0,969 атм для реакции А ( с) ⇌ 2 7 В (г) 9044 что такое K P (подсказка: при работе с K P необходимо использовать единицу измерения «бар»)?
7. Разложение карбамата аммония до NH 3 и CO 2 при 40°C записывается как NH 4 CO 2 NH 2 (s) ⇌ 2 NH 3 (g) + CO 2 (в атм) CO 2 ? Каково общее давление газа в системе (в атм)? Что такое K P (подсказка: при работе с K p необходимо использовать единицу «бар» )?
Разложение карбамата аммония до NH 3 и CO 2 при 40°C записывается как NH 4 CO 2 NH 2 (s) ⇌ 2 NH 3 (g) + CO 2 (в атм) CO 2 ? Каково общее давление газа в системе (в атм)? Что такое K P (подсказка: при работе с K p необходимо использовать единицу «бар» )?
8. При 375 К, К П для реакции SO 2 CL 2 ( G) ⇌ SO 2 (G) + CL 2 (G) IS 2,4, с пресс -экспрессией в атмосфора. При 303 K K P равно 2,9 × 10 −2 .
а. Что такое K для реакции при каждой температуре?
б. Если образец при 375 К содержит 0,100 М Cl 2 и 0,200 М SO 2 в равновесии, какова концентрация SO 2 Класс 2 ?
в. Если образец, указанный в части б, охладить до 303 К, каково будет давление внутри колбы (в атм)?
9. Экспериментальные данные по системе Br 2 (l ) ⇌ Br 2 ( aq ) приведены в следующей таблице . График [Br 2 ] относительно молей Br 2 (л) в наличии; затем напишите уравнение равновесия постоянное выражение и определите К .
Экспериментальные данные по системе Br 2 (l ) ⇌ Br 2 ( aq ) приведены в следующей таблице . График [Br 2 ] относительно молей Br 2 (л) в наличии; затем напишите уравнение равновесия постоянное выражение и определите К .
В граммах Br 2 в 100 мл воды | [Бр 2 ] (М) |
1,0 | 0,0626 |
2,5 | 0,156 |
3,0 | 0,188 |
4,0 | 0,219 |
4,5 | 0,219 |
10. Накопленные данные для реакции н-бутана ( г) ⇌ изобутана (г) при равновесии приведены в следующей таблице. Какова константа равновесия для этого превращения? Если 1 моль н -бутана уравновешивается при тех же условиях реакции, каково окончательное число молей n -бутан и изобутан?
Накопленные данные для реакции н-бутана ( г) ⇌ изобутана (г) при равновесии приведены в следующей таблице. Какова константа равновесия для этого превращения? Если 1 моль н -бутана уравновешивается при тех же условиях реакции, каково окончательное число молей n -бутан и изобутан?
11. Solid ammonium carbamate (NH 4 CO 2 NH 2 ) dissociates completely to ammonia and carbon dioxide when it vaporizes:
NH 4 CO 2 NH 2 ( у) ⇌ 2 NH 3 (ж) + CO 2 (ж)
При 25°С общее давление газов, находящихся в равновесии с твердым телом, равно 0,116 атм. Каково равновесное парциальное давление каждого газа (в атм)? Что такое K p (подсказка: при работе с K P необходимо использовать единицу измерения «брусок»)? Если концентрацию CO 2 удвоить, а затем уравновесить до своего начального равновесного парциального давления + x атм, какое изменение концентрации NH 3 необходимо для того, чтобы система восстановила равновесие?
12. Константа равновесия реакции COCl 2 ( г) ⇌ CO (г) + Cl 2 (г) равно К P = 2,2 × 10 -10 при 100°C. Если начальная концентрация COCl 2 составляет 3,05 × 10 −3 M, каково парциальное давление каждого газа в состоянии равновесия при 100°C (в барах)? Какое предположение можно сделать для упрощения расчетов?
Константа равновесия реакции COCl 2 ( г) ⇌ CO (г) + Cl 2 (г) равно К P = 2,2 × 10 -10 при 100°C. Если начальная концентрация COCl 2 составляет 3,05 × 10 −3 M, каково парциальное давление каждого газа в состоянии равновесия при 100°C (в барах)? Какое предположение можно сделать для упрощения расчетов?
13. Водное разбавление IO4 − приводит к следующей реакции:0477 ) + 2 H 2 O (l ) ⇌ H 4 IO 6 – ( aq )
and K = 3.5 × 10 − 2 . Если начать с 50 мл 0,896 М раствора IO 4 − , разбавленного водой до 250 мл, сколько молей H 4 IO 6 − образуется при равновесии?
★★★ Вопросы
14. Йод и бром реагируют с образованием IBr, который затем возгоняется. При 184,4 ° C общая реакция продолжается в соответствии со следующим уравнением:
Йод и бром реагируют с образованием IBr, который затем возгоняется. При 184,4 ° C общая реакция продолжается в соответствии со следующим уравнением:
I 2 (G) + BR 2 ( G) ⇌ 2 IBR (G)
K 8 8 8 8 8 8 8 8 8 9 P = 1,2 × 10 2 (Подсказка: предполагается, что при расчете K P в качестве единицы измерения использовалось «бар»). Если начать реакцию с 7,4 г паров I 2 и 6,3 г Br 2 пара в контейнере объемом 1,00 л, какова концентрация IBr (г) при равновесии (гмоль-1)? Каково парциальное давление каждого газа в равновесии (в барах)? Каково общее давление в системе (в барах)?
15. Для реакции
Для реакции
C (S) + 12 N 2 (G) + 5/2 H 2 ( G) ⇌ CH 3 NH 2 G) ⇌ CH 3 2 G) . (г)
К = 1,8 × 10 −6 . Если начать реакцию с 1,0 моль N 2 , 2,0 моль H 2 и достаточное количество C(s) в контейнере объемом 2,00 л, каковы концентрации N 2 и CH 3 NH 2 при равновесии (гмоль-1)? Что произойдет с K , если концентрацию H 2 увеличить вдвое?
Ответы
1. Значение K теперь увеличено до рассматриваемого коэффициента. Когда его удваивают, K становится K 2 , а когда его утраивают, K равно K 3
2. Эти результаты не ожидаются, так как с повышением температуры должно происходить повышение давления. ∆H० в данном случае является положительным значением (31 кДж/моль), указывающим на то, что это эндотермическая реакция. При этом с повышением температуры реакция сдвинется вперед, а это означает, что будет произведено больше продукта. Чем больше продукта произведено, тем больше присутствует газообразного кислорода, поэтому его давление увеличивается.
При этом с повышением температуры реакция сдвинется вперед, а это означает, что будет произведено больше продукта. Чем больше продукта произведено, тем больше присутствует газообразного кислорода, поэтому его давление увеличивается.
3. Kp останется прежним, P N2O2 = 2,3 x 10 2 бар, P NO2 = 6,6 бар
4. K = 53,88; Kp = 53,88
5,215 бар MeOH; 383 бар H 2
6. Kp = 0,140
7. Парциальное давление CO 2 = 0,121 атм; полное давление газа в системе = 0,363 атм; Kp = 7,37 x 10 -3
8. (a) K = 7,8 x 10 -2 при 375K, K = 1,2 x 10 -3 при 303K; (б) 0,256 М; (в) 14,13 атм
9.
K = 0,046 (на основе наклона линии наилучшего соответствия)
10. K = 2,5; конечные моли будут составлять 0,3 моль н-бутана и 0,7 моль изобутана.
11. P Nh4 = 0,0773 атм, P CO2 = 0,0387 атм; К р = 2,411 х 10 -4 ; концентрация NH 3 упадет, чтобы равновесие восстановилось.
12. P COCl2 = 0,042 бар, P CO = 4,59 x 10 -6 бар, P Cl2 = 4,59 x 10 -6 бар; Предполагается, что общий объем составляет 1 л.
13. H 4 IO 6 – = 9,09 x 10 -3 MOL
14. P I2 = 2,7 бар, P BR2 = 47 бар, P IBR = 2.11, P BR2 = 47 BAR, P IBR = 2.11. x10 2 бар = 0,054 м, стр. T = 2,6 x 10 2 Бар
15. [N 2 ] ≈ 0,99 м, [H 2 ] ≈ 2 М, [CH 3 99 м, [H 2 ] ≈ 2 м, [CH 3 99.0009 NH 2 ] = 1,02 x 10 -5 М; если [H 2 ] удваивается, K остается неизменным (только температура может изменить значение K)
Химия Решения Практические задачи | Центр знаний Каролины
Перейти к содержимому
Решения по химии Практические задачи
Молярные растворы
1. Опишите, как вы приготовили бы 1 л 1 М раствора хлорида натрия. Масса грамм-формулы хлорида натрия составляет 58,44 г/моль.
Опишите, как вы приготовили бы 1 л 1 М раствора хлорида натрия. Масса грамм-формулы хлорида натрия составляет 58,44 г/моль.
Чтобы приготовить 1 М раствор хлорида натрия, растворите 58,44 г хлорида натрия в 500 мл воды в мерной колбе вместимостью 1000 мл. Когда все твердое вещество растворится и раствор станет комнатной температуры, разбавьте до метки и несколько раз переверните колбу для перемешивания.
2. Опишите, как вы приготовите 1 л 2 М раствора уксусной кислоты. Масса грамм-формулы уксусной кислоты составляет 60,05 г/моль, а ее плотность – 1,049 г/мл.
Для приготовления 2 М раствора уксусной кислоты растворяют 120,1 г уксусной кислоты в 500 мл дистиллированной или деионизированной воды в мерной колбе вместимостью 1000 мл. Поскольку уксусная кислота является жидкостью, ее также можно измерять по объему. Разделите массу кислоты на ее плотность (1,049г/мл) для определения объема (114 мл). Для приготовления раствора используйте 120,1 г или 114 мл уксусной кислоты. Аккуратно встряхните колбу, чтобы перемешать раствор. Как только раствор станет комнатной температуры, разбавьте его до метки и несколько раз переверните колбу для перемешивания.
Аккуратно встряхните колбу, чтобы перемешать раствор. Как только раствор станет комнатной температуры, разбавьте его до метки и несколько раз переверните колбу для перемешивания.
Процентные растворы
1. Опишите, как можно приготовить 100 г раствора, содержащего 0,5% фенолфталеина по массе.
Поскольку растворенное вещество (фенолфталеин) представляет собой твердое вещество, раствор выражается в процентах по массе. Массовый процент означает количество граммов растворенного вещества на 100 г раствора.
массовые проценты = (масса растворенного вещества/масса раствора) x 100%
масса растворенного вещества = массовые проценты x масса раствора/100%
= 0,5% x 100 г/100% Поскольку общая масса раствора равна 100 г, остальные 99,5 г раствора составляют вода. Для приготовления раствора растворяют 0,5 г фенолфталеина в 99,5 г дистиллированной или деионизированной воды.
2. Опишите, как вы приготовите 100 мл раствора, содержащего 22% уксусной кислоты по объему.
Объемный процент означает количество миллилитров растворенного вещества на 100 мл раствора. Разбавьте 22 мл уксусной кислоты дистиллированной или деионизированной водой, чтобы получить 100 мл раствора.
Разведения
1. Опишите, как можно приготовить 1,0 л 0,10 М раствора серной кислоты из 3,0 М раствора серной кислоты.
Рассчитайте объем 3,0 М серной кислоты, необходимый для приготовления раствора.
M реагент × V реагент = M dilution × V dilution
3.0 M × V reagent = 0.10 M × 1.0 L
V reagent = 0.033 L = 33 mL
Slowly add 33 мл 3,0 М серной кислоты в мерную колбу вместимостью 1000 мл, наполовину заполненную дистиллированной или деионизированной водой, и встряхивают колбу для перемешивания. Когда раствор станет комнатной температуры, разбавьте его водой до метки и несколько раз переверните колбу для перемешивания.
2. Опишите, как можно приготовить 500 мл 0,25 М раствора гидроксида натрия из 5,0 М раствора гидроксида натрия.
Рассчитайте объем 5,0 М гидроксида натрия, необходимый для приготовления раствора.
M reagent × V reagent = M dilution × V dilution
5.0 M × V reagent = 0.25 M × 0.500 L
V реагент = 0,025 л = 25 мл
Медленно добавьте 25 мл 5,0 М гидроксида натрия в мерную колбу на 500 мл, наполовину заполненную дистиллированной или деионизированной водой, и встряхните колбу, чтобы перемешать. Когда раствор станет комнатной температуры, разбавьте его водой до метки и несколько раз переверните колбу для перемешивания.
Особые случаи
1. Опишите, как вы приготовите 500 мл 1,0 М раствора хлорида калия с чистотой 93,0%. Масса грамм-формулы хлорида калия составляет 74,56 г/моль.
Рассчитайте необходимую массу неочищенного хлорида калия.
Масса нечистого хлорида калия = M Pure × V PURE × Грамб Формулы / Процент Чистота
= 1,0 м × 0,500 л × 74,56 г / молю Медленно добавьте 40 г 93% хлорида калия в мерную колбу вместимостью 500 мл, наполовину заполненную дистиллированной или деионизированной водой, и встряхните колбу, чтобы перемешать. Когда все твердое вещество растворится и раствор станет комнатной температуры, разбавьте до метки и несколько раз переверните колбу для перемешивания.
2. Опишите, как можно приготовить 500 мл 1,0 М раствора фосфорной кислоты из чистой 85,0% фосфорной кислоты. Масса грамм-формулы фосфорной кислоты составляет 98,00 г/моль, а плотность 85,0%-ной фосфорной кислоты составляет 1,685 г/мл.
Рассчитайте необходимый объем 85,0% фосфорной кислоты.
объем нечистой фосфорной кислоты = M чистая × V чистая × грамм формула веса / (процент чистоты x плотность) = (1,0 M × 0,500 л x 98,00 г/моль) ÷ 1,685 г/мл
0,850
= 34 мл
Медленно добавьте 34 мл 85,0% фосфорной кислоты в мерную колбу на 500 мл, наполовину заполненную дистиллированной или деионизированной водой, и встряхните колбу, чтобы перемешать. Когда раствор станет комнатной температуры, разбавьте его водой до метки и несколько раз переверните колбу для перемешивания.
Когда раствор станет комнатной температуры, разбавьте его водой до метки и несколько раз переверните колбу для перемешивания.
Нормальные растворы
1. Опишите, как вы приготовите 1000 мл 1,0 н. раствора гидроксида магния. Масса грамм-формулы гидроксида магния составляет 58,33 г/моль.
Гидроксид магния содержит две гидроксильные группы. Таким образом, половина моля гидроксида магния принимает один моль протонов. Чтобы приготовить 1,0 н. раствор гидроксида магния, медленно добавляют 29 г гидроксида магния в мерную колбу вместимостью 500 мл, наполовину заполненную дистиллированной или деионизированной водой, и встряхивают колбу для перемешивания. Когда все твердое вещество растворится и раствор станет комнатной температуры, разбавьте до метки и несколько раз переверните колбу для перемешивания.
Магазин Химия
2.4 Решение задач и преобразование единиц измерения
Цели обучения
К концу этого раздела вы сможете:
- Объяснять подход размерного анализа (метка фактора) к математическим расчетам с использованием величин
- Использовать размерный анализ для преобразования единиц измерения для заданного свойства и вычислений, включающих два или более свойства
Часто бывает так, что интересующую величину нелегко (или даже невозможно) измерить напрямую, а вместо этого ее необходимо рассчитать на основе других непосредственно измеренных свойств и соответствующих математических взаимосвязей. Например, рассмотрим измерение средней скорости спортсмена, бегущего на короткие дистанции. Обычно это достигается путем измерения время , необходимое спортсмену, чтобы пробежать от линии старта до линии финиша, и расстояние между этими двумя линиями, а затем вычисление скорости из уравнения, которое связывает эти три свойства:
Например, рассмотрим измерение средней скорости спортсмена, бегущего на короткие дистанции. Обычно это достигается путем измерения время , необходимое спортсмену, чтобы пробежать от линии старта до линии финиша, и расстояние между этими двумя линиями, а затем вычисление скорости из уравнения, которое связывает эти три свойства:
[латекс]\большой \text{speed}=\frac{\text{distance}}{\text{time}}[/latex]
Спринтер олимпийского уровня может пробежать 100 м примерно за 10 с, что соответствует средней скорости [латекс ]\large\frac{\text{100 м}}{\text{10 с}}=\text{10 м/с}[/latex].
Обратите внимание, что эта простая арифметика включает в себя деление чисел каждой измеренной величины, чтобы получить число вычисляемой величины (100/10 = 10) , а также деление единиц каждой измеряемой величины, чтобы получить единицу вычисляемой величины ( м/с = м/с). Теперь рассмотрите возможность использования этого же соотношения для предсказания времени, необходимого человеку, бегущему с этой скоростью, чтобы пройти расстояние 25 м. Используется то же соотношение между тремя свойствами, но в данном случае предоставлены две величины: скорость (10 м/с) и расстояние (25 м). Чтобы получить искомое свойство, время, уравнение должно быть изменено соответствующим образом:
Используется то же соотношение между тремя свойствами, но в данном случае предоставлены две величины: скорость (10 м/с) и расстояние (25 м). Чтобы получить искомое свойство, время, уравнение должно быть изменено соответствующим образом:
[латекс]\большой\текст{время}=\фракция{\текст{расстояние}}{\текст{скорость}}[/латекс]
Затем время можно вычислить как [латекс]\большой\фрак{ \text{25 м}}{\text{10 м/с}}=\text{2,5 с}[/latex].
Опять же, арифметика с числами (25/10 = 2,5) сопровождалась той же арифметикой с единицами (м/м/с = с), чтобы получить число и единицу результата, 2,5 с. Обратите внимание, что, как и в случае с числами, когда единица делится на идентичную единицу (в данном случае m/m), результат равен «1» или, как обычно говорят, единицы «отменяются».
Эти расчеты являются примерами универсального математического подхода, известного как размерный анализ (или метод меток факторов ). Анализ размерностей основан на следующем предположении: единицы величин должны подвергаться тем же математическим операциям, что и связанные с ними числа . Этот метод может применяться к вычислениям, начиная от простого преобразования единиц измерения и заканчивая более сложными многоэтапными вычислениями, включающими несколько различных величин.
Этот метод может применяться к вычислениям, начиная от простого преобразования единиц измерения и заканчивая более сложными многоэтапными вычислениями, включающими несколько различных величин.
Отношение двух эквивалентных величин, выраженное в разных единицах измерения, может быть использовано в качестве коэффициента преобразования единиц . Например, длины 2,54 см и 1 дюйм эквивалентны (по определению), поэтому коэффициент преобразования единиц может быть получен из соотношения
[латекс]\большой\текст{(2,54 см = 1 дюйм)} \text{ или }\frac{\text{2,54 см}}{\text{1 дюйм}}\text{ или }\text{ 2,54}\frac{\text{см}}{\text{дюйм}} [ /латекс]
Несколько других широко используемых коэффициентов пересчета приведены в таблице 1.
Когда мы умножаем количество (например, расстояние, указанное в дюймах) на соответствующий коэффициент преобразования единиц измерения, мы преобразуем количество в эквивалентное значение с другими единицами измерения (например, расстояние в сантиметрах). Например, вертикальный прыжок баскетболиста на 34 дюйма можно перевести в сантиметры следующим образом:
Например, вертикальный прыжок баскетболиста на 34 дюйма можно перевести в сантиметры следующим образом:
[латекс]\большой\текст{34}\отмена{\текст{в}}\раз \фракция{\текст{2,54 см}}{1\отмена{\текст{в}}}=\текст{86 cm}[/latex]
Поскольку эта простая арифметика включает величин , предпосылка размерного анализа требует, чтобы мы умножали как чисел, так и единиц . Числа этих двух величин умножаются, чтобы получить число количества продукта, 86, тогда как единицы умножаются, чтобы получить [латекс]\large\frac{\text{in}\times \text{cm}}{\text {in}}[/латекс] . Так же, как и для чисел, отношение одинаковых единиц также численно равно единице, [латекс]\большой\фрак {\текст{в}}{\текст{в}}=\текст{1,}[/латекс] и таким образом, единичный продукт упрощается до см . (Когда идентичные единицы делятся, чтобы получить коэффициент, равный 1, говорят, что они «отменяются».) Используя анализ размерностей, мы можем определить, что коэффициент преобразования единиц был установлен правильно, проверив, чтобы подтвердить, что исходная единица будет аннулирована, и результат будет содержать искомую (преобразованную) единицу.
Способность создавать и применять правильные коэффициенты преобразования — очень мощный математический прием в химии. Вам необходимо освоить эту технику, если вы собираетесь добиться успеха в этом и будущих курсах.
Пример 1:
Использование коэффициента преобразования единицМасса фрисби для соревнований составляет 125 г. Переведите его массу в унции, используя коэффициент преобразования единиц измерения, полученный из соотношения 1 унция = 28,349 г (таблица 1).
Показать ответ
Проверьте свои знанияПреобразование объема 9,345 кварты в литры.
Показать ответ
Помимо простого преобразования единиц измерения, метод меток факторов можно использовать для решения более сложных задач, связанных с вычислениями. Независимо от деталей, основной подход один и тот же — все коэффициенты , участвующие в вычислении, должны быть соответствующим образом ориентированы, чтобы гарантировать, что их метки (единицы) будут соответствующим образом сокращаться и/или объединяться для получения желаемой единицы в результате. Вот почему он называется методом факторной метки. По мере продолжения изучения химии у вас будет много возможностей применить этот подход.
Вот почему он называется методом факторной метки. По мере продолжения изучения химии у вас будет много возможностей применить этот подход.
Пример 2:
Расчет величин по результатам измерений и известным математическим соотношениямКакова плотность обычного антифриза в единицах г/мл? Образец антифриза объемом 4,00 л весит 90,26 фунта
Показать ответ
Check Your LearningКаков объем 1000 унций в литрах, если 1 л = 1,0567 кварты и 1 кварта = 32 унции (точно)?
Показать ответ
Пример 3:
Расчет величин по результатам измерений и известным математическим соотношениямВо время поездки из Филадельфии в Атланту на расстояние около 1250 км Lamborghini Aventador Roadster 2014 года потребляет 213 л бензина.
- Какой (средний) расход топлива, в милях на галлон, получил родстер во время этой поездки?
- Если бензин стоит 3,80 доллара за галлон, сколько стоило топливо для этой поездки?
Показать ответ
Проверьте свои знания Toyota Prius Hybrid использует 59,7 л бензина для поездки из Сан-Франциско в Сиэтл на расстояние 1300 км (две значащие цифры).
- Какой (средний) расход топлива, в милях на галлон, получил Prius во время этой поездки?
- Если бензин стоит 3,90 доллара за галлон, сколько стоило топливо для этой поездки?
Показать ответ
Пример 4:
Преобразование производной единицыПреобразование 88,4 м/мин в метры/секунду.
Показать ответ
Проверьте свои знанияПреобразование 0,203 м/мин в метры/секунду.
Показать ответ
Химия повсюду: планер Гимли
23 июля 1983 года самолету Air Canada Boeing 767 пришлось совершить аварийную посадку в аэропорту промышленного парка Гимли в Гимли, Манитоба, поскольку во время полета у него неожиданно закончилось топливо. Людей в ходе аварийной посадки не было, только легкие травмы, частично связанные с эвакуацией корабля после приземления. До конца срока службы (самолет был списан в 2008 году) самолет получил прозвище «планер Гимли».
Боинг-767 вылетел из Монреаля в Оттаву и в конечном итоге направился в Эдмонтон, Канада. Примерно в середине полета все двигатели самолета начали глохнуть из-за нехватки топлива. Когда последний двигатель отключился, все электричество (которое вырабатывалось двигателями) было потеряно; самолет стал, по сути, бессильным планером. Капитан Роберт Пирсон был опытным пилотом-планеристом, хотя он никогда не летал на планере размером с Боинг-767. Первый офицер Морис Куинтал быстро определил, что самолет не сможет долететь до Виннипега, следующего крупного аэропорта. Он предложил свою старую базу Королевских ВВС на станции Гимли, одна из взлетно-посадочных полос которой все еще использовалась как общественный аэропорт. Благодаря усилиям пилотов и летного экипажа им удалось благополучно посадить самолет на землю (хотя и с пристегнутым шасси) и благополучно покинуть всех пассажиров.
Что случилось? В то время Канада переходила от старой английской системы к метрической системе. Боинг 767 был первым самолетом, датчики которого были откалиброваны в метрической системе единиц (литры и килограммы), а не в английской системе единиц (галлоны и фунты). Таким образом, когда указатель уровня топлива показывал 22 300, он означал килограммы, но наземная команда по ошибке заправила самолет 22 300 90 477 фунтов 90 478 топлива. В итоге это составило чуть меньше половины топлива, необходимого для поездки, в результате чего двигатели остановились примерно на полпути к Оттаве. Сообразительность и экстраординарное мастерство спасли жизни 61 пассажиру и 8 членам экипажа — инцидента, которого бы не произошло, если бы люди следили за своими подразделениями.
Таким образом, когда указатель уровня топлива показывал 22 300, он означал килограммы, но наземная команда по ошибке заправила самолет 22 300 90 477 фунтов 90 478 топлива. В итоге это составило чуть меньше половины топлива, необходимого для поездки, в результате чего двигатели остановились примерно на полпути к Оттаве. Сообразительность и экстраординарное мастерство спасли жизни 61 пассажиру и 8 членам экипажа — инцидента, которого бы не произошло, если бы люди следили за своими подразделениями.
Источник видео: Преобразование единиц измерения с помощью ключа j (https://viuvideos.viu.ca/media/Unit+Conversion/0_o671v9j6)
Упражнения
Объем
- На этикетке бутылки безалкогольного напитка указан объем в двух единицах : 2,0 л и 67,6 жидких унций. Используйте эту информацию для получения коэффициента пересчета между английскими и метрическими единицами измерения. Сколько значащих цифр вы можете оправдать в коэффициенте пересчета?
- На этикетке коробки хлопьев указана масса хлопьев в двух единицах: 978 грамм и 34,5 унции.
 Используйте эту информацию, чтобы найти коэффициент преобразования между английскими и метрическими единицами измерения. Сколько значащих цифр вы можете оправдать в коэффициенте пересчета?
Используйте эту информацию, чтобы найти коэффициент преобразования между английскими и метрическими единицами измерения. Сколько значащих цифр вы можете оправдать в коэффициенте пересчета? - Сколько миллилитров безалкогольного напитка содержится в банке на 12,0 унций?
- В барреле нефти ровно 42 галлона. Сколько литров нефти в бочке?
- Многие медицинские лабораторные тесты проводятся с использованием 5,0 мкл сыворотки крови. Чему равен этот объем в миллилитрах?
- Молоко продается литрами во многих странах. Каков объем ровно 1/2 галлона молока в литрах?
- Бензин продается литрами во многих странах. Сколько литров нужно, чтобы заполнить 12,0-галлонный бензобак?
- Рассчитайте эти объемы.
- Каков объем 11,3 г графита, плотность = 2,25 г/см 3 ?
- Каков объем 39,657 г брома, плотность = 2,928 г/см 3 ?
- Рассчитайте эти объемы.
- Каков объем 25 г йода, плотность = 4,93 г/см 3 ?
- Каков объем 3,28 г газообразного водорода, плотность = 0,089 г/л?
Показать выбранные ответы
Масса
- Является ли тяжелоатлет весом 197 фунтов достаточно легким, чтобы соревноваться в классе, ограниченном для тех, кто весит 90 кг или меньше?
- Очень хороший тяжелоатлет весом 197 фунтов поднял 192 кг в движении, называемом толчком.
 Какова была масса поднятого груза в фунтах?
Какова была масса поднятого груза в фунтах? - Если таблетка аспирина содержит 325 мг аспирина, сколько граммов аспирина она содержит?
- Длинная тонна определяется точно как 2240 фунтов. Какова эта масса в килограммах?
- Согласно инструкции по эксплуатации, бензобак одного роскошного автомобиля вмещает 22,3 галлона. Если плотность бензина 0,8206 г/мл, определите массу в килограммах и фунтах топлива в полном баке.
- Рассчитайте эти массы.
- Какова масса 6,00 см 3 ртути, плотность = 13,5939 г/см 3 ?
- Какова масса 25,0 мл октана, плотность = 0,702 г/см 3 ?
- Рассчитайте эти массы.
- Какова масса 4,00 см 3 натрия, плотность = 0,97 г/см?
- Какова масса 125 мл газообразного хлора, плотность = 3,16 г/л?
Показать выбранные ответы
Длина
- Диаметр эритроцита составляет примерно 3 × 10 −4 дюймов.


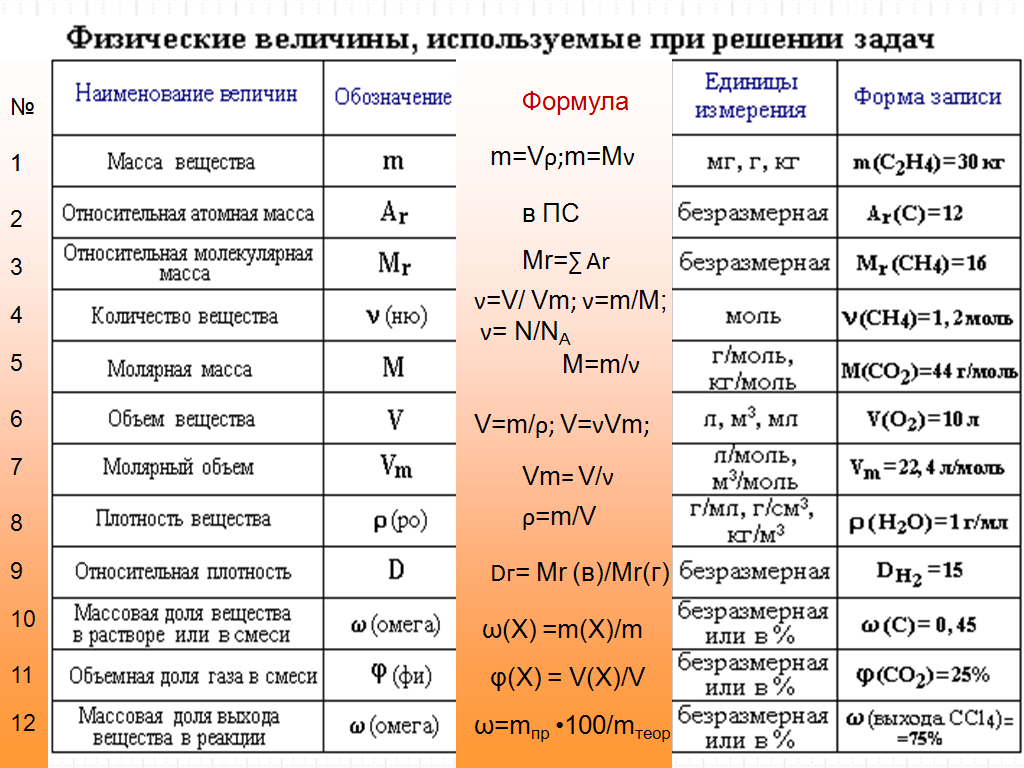 4 (л/моль)
4 (л/моль)