строение атомов F и Cl
Характеристика фтора:
1. Элемент №9 фтор, знак F, его атомная масса Ar=19, его заряд ядра Z=+9, в ядре 9 p⁺(протонов), 10 n⁰ (нейтронов).
Вокруг ядра находятся 9 e⁻(электронов), которые размещаются на двух энергетических уровнях, так как фтор находится во втором периоде.
Напишем модели строения атома фтора:
а). Модель атома фтора при помощи дуг:
₊₉F)₂)₇
б). Модель атома, через электронную формулу (электронная конфигурация):
₊₉F 1s²2s²2p⁵
в). Электронно-графическая модель атома:
⇅ ⇅ ↑
2уровень ⇅
1уровень ⇅
₊₉F
2. Молекула простого вещества фтора двухатомная F₂ . Фтор
неметалл, в химических реакциях только окислитель.
5. Оксидов и гидроксидов у
фтора нет, так как он самый электроотрицательный элемент.:
6. Летучее соединение с водородом HF фтороводород, бесцветный
газ, с резким запахом, ниже
19,9°C — бесцветная подвижная летучая жидкость.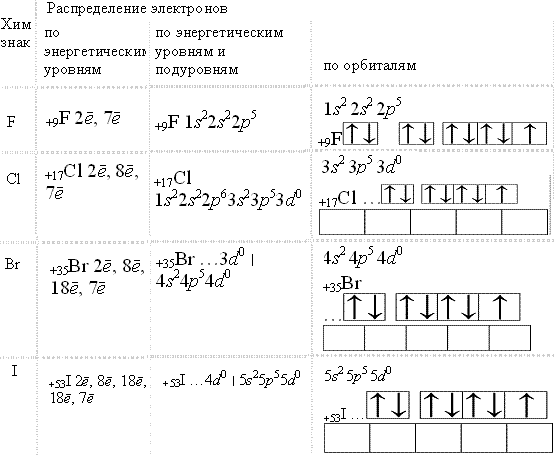
Характеристика хлора:
1. Элемент №17 хлор, знак CI. его атомная масса Ar=35,5 (два изотопа Ar =35. Ar = 37 ), его заряд ядра Z=+17, в ядре 17 p⁺(протонов) в изотопе Ar =35 18 n⁰, а в изотопе
Ar = 37 n⁰ 20 (нейтронов).
Вокруг ядра находятся 17 e⁻(электронов), которые размещаются на трех энергетических уровнях, так как хлор находится в третьем периоде.
Напишем
модели строения атома хлора:
а). Модель атома хлора при помощи дуг:
₊₁₇CI)₂)₈)₇
б). Модель атома, через электронную формулу (электронная конфигурация):
₊₁₇CI 1s²2s²2p⁶3s²3p⁵
в). Электронно-графическая модель атома:
⇵
⇵
↑
3уровень ⇵
⇅
⇅
⇅
2уровень ⇅
1уровень ⇅
₊₁₇CI
2. Молекула простого вещества хлора двухатомная CI₂ . Хлор неметалл, в химических
реакциях может быть восстановителем, может быть окислителем.
5. Высший оксид хлора–CI₂O₇, кислотный оксид:
6. Гидроксид –HCIO₄ ,
хлорная , сильная кислота,
7. Летучее соединение с водородом HCI хлороводород, бесцветный газ, с неприятным запахом, хорошо растворим в воде, раствор соляная кислота HCI.
Иод, Фтор, Хлор электронное строение
Галогены — фтор, хлор, бром, нод — расположены в главной подгруппе седьмой группы периодической системы элементов. В атомах галогенов на внешнем энергетическом уровне находится по семь электронов и они могут присоединять один электрон, превращаясь в отрицательные ионы 1 . Отрицательную степень окисления галогены имеют в соединениях с водородом и металлами. Однако атомы галогенов, кроме фтора, могут проявлять и положительные степени окисления +1, +3, +5, +7. Это объясняется электронным строением атомов. Атом фтора имеет следующее электронное строениеЭлементы фтор F, хлор С1, бром Вг, иод I и астат At составляют V1IA группу Периодической системы Д.
 И. Менделеева. Групповое название этих элементов — галогены. Строение валентного электронного уровня атомов галогенов одинаково ns np атом фтора не имеет /г -подуровня, поэтому он образует только одну ковалентную связь. Фтор — самый электроотрицательный элемент и встреч ается только в состояниях Р- и F . [c.219]
И. Менделеева. Групповое название этих элементов — галогены. Строение валентного электронного уровня атомов галогенов одинаково ns np атом фтора не имеет /г -подуровня, поэтому он образует только одну ковалентную связь. Фтор — самый электроотрицательный элемент и встреч ается только в состояниях Р- и F . [c.219] Электронное строение атома хлора отличается от рассмотренного атома фтора
Различие в строении второго снаружи энергетического уровня, на котором у атомов фтора находятся только два электрона у атомов хлора — восемь а у атомов брома, иода и астата — [c.386]
В соответствии с особенностями строения электронных оболочек атомов элементы VII группы подразделяются на три подгруппы типические элементы (водород, фтор, хлор), элементы подгруппы брома (бром, иод, астат) и элементы подгруппы марганца (марганец, технеций, рений). [c.287]
Будучи наиболее электроотрицательным элементом, фтор может только принимать один электрон на 2 р-подуровень.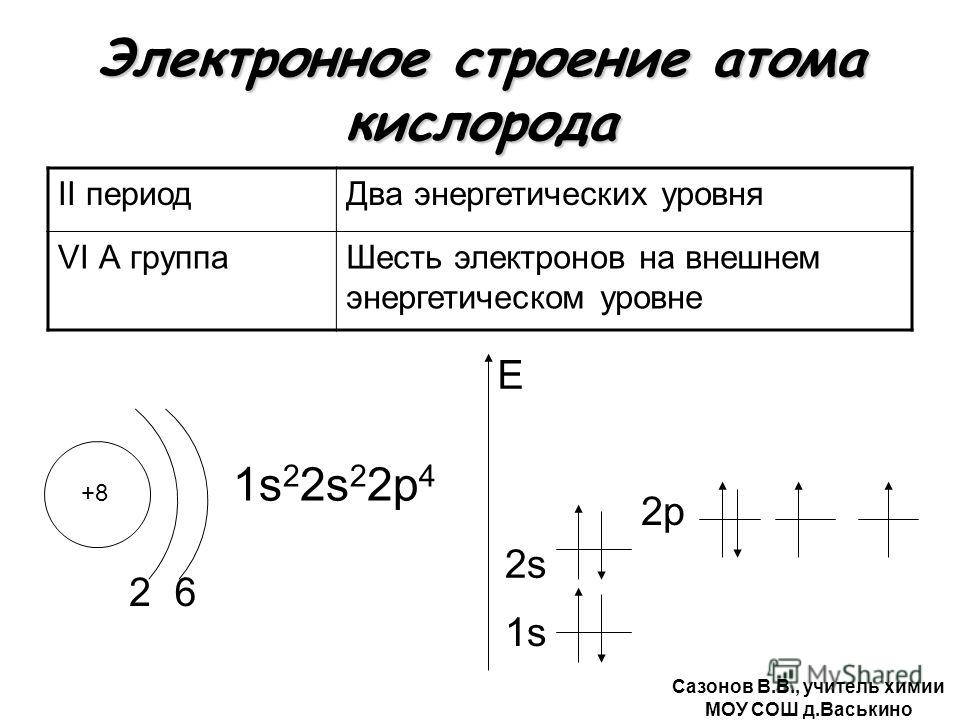
Галогены —это элементы, расположенные в правой части периодической таблицы, в группе, которая находится непосредственно перед группой инертных газов. Элементы этой группы — фтор, хлор, бром, иод и астат — имеют заметное сходство и некоторые общие тенденции в изменении химических свойств. Такое сходство естественно, так как электронное строение внешних уровней у всех этих элементов одинаково. Каждый элемент имеет на один электрон меньше, чем последующий инертный газ. Различия в химическом поведении галогенов нетрудно понять в свете увеличения заряда ядра, числа электронов и размера атома при перемещении сверху вниз по этой группе периодической таблицы.
Д. И. Менделеев, открывший объективный закон природы, не имел возможности вскрыть причины периодического изменения свойств элементов.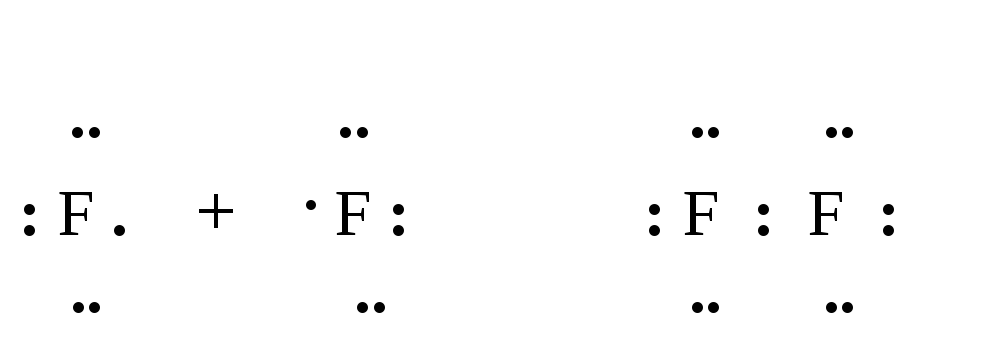 Причины периодичности в изменении свойств элементов были раскрыты только с помощью теории строения атома. Эта теория показала, что в ходе развития электронных оболочек атомов (стр. 45) периодически повторяются одинаковые конфигурации внешних электронов, от которых более всего зависят химические свойства. Таким образом, периодическое изменение свойств элементов является следствием периодического возвращения электронных оболочек атомов к одним и тем же конфигурациям электронов внешнего слоя. Например, свойства самых активных щелочных металлов периодически повторяются у лития, натрия, калия, рубидия, цезия и франция потому именно, что в наружном слое их атомов периодически повторяется одноэлектронная конфигурация. Подобно этому свойства наиболее активных неметаллов — галогенов — периодически повторяются у фтора, хлора, брома, йода и астата, так как атомы их имеют по семь электронов во внешнем слое.
Причины периодичности в изменении свойств элементов были раскрыты только с помощью теории строения атома. Эта теория показала, что в ходе развития электронных оболочек атомов (стр. 45) периодически повторяются одинаковые конфигурации внешних электронов, от которых более всего зависят химические свойства. Таким образом, периодическое изменение свойств элементов является следствием периодического возвращения электронных оболочек атомов к одним и тем же конфигурациям электронов внешнего слоя. Например, свойства самых активных щелочных металлов периодически повторяются у лития, натрия, калия, рубидия, цезия и франция потому именно, что в наружном слое их атомов периодически повторяется одноэлектронная конфигурация. Подобно этому свойства наиболее активных неметаллов — галогенов — периодически повторяются у фтора, хлора, брома, йода и астата, так как атомы их имеют по семь электронов во внешнем слое.
НИИ электроны с Зр- и Зх-подуровней переходят на Зй-подуровень (на схеме показано стрелками).
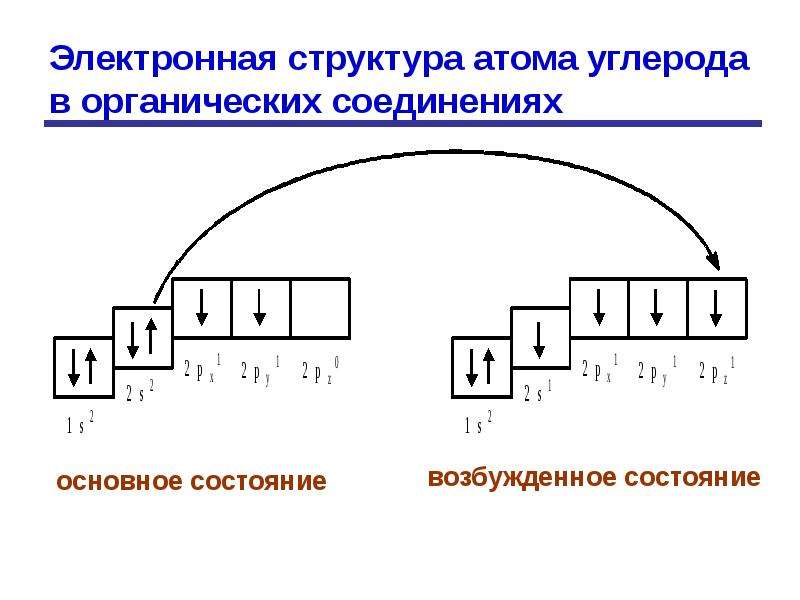
Общая характеристика галогенов. Галогенами называют элементы фтор, хлор, бром, нод и астат. Атомы всех галогенов имеют в наружном слое 7 электронов. Одинаковое строение наружного электронного слоя обусловливает большое сходство их друг с другом. Это проявляется в общности химических свойств, в формах и свойствах образуемых ими соединений. Атомы всех галогенов весьма легко присоединяют один электрон, образуя отрицательно заряженные ионы. Изображая галоген буквой R, можно процесс этот выразить электронно-1юнным уравнением [c. 94]
94]
Искаженная Т-образная структура молекулы трифторида хлора может рассматриваться как производная от модели тригональ-ной бипирамиды [90]. Атом хлора находится в центре бипирамиды, а атомы фтора расположены таким образом, что два из них находятся в противоположных углах двух пирамид, а третий — в одном из углов треугольника, образуемого основаниями пирамид. Два остальных угла треугольника заняты электронной парой атома хлора. Такое строение молекулы удовлетворительно объясняет способность трифторида хлора к димеризации.
У всех элементов, находящихся в одной и той же подгруппе периодической системы, строение внешних электронных оболочек одинаково, поэтому в свойствах таких элементов наблюдается наибольшее сходство, хотя металлические свойства в группе сверху вниз нарастают. Характер изменения свойств в группах элементов в данном случае определяется главным образом изменением радиусов атомов. Однако необходимо обратить внимание на следующее.
В молекуле фтора этих дополнительных связей нет (фтор не имеет ( -орбиталей) и поэтому его молекула менее прочна. Сродство к электрону у фтора несколько меньше, чем у хлора, но больше, чем у брома, и составляет 350 кДж/моль атомов. Стандартный окислительно-восстановительный потенциал фтора очень высок ( + 2,85 В) фтор — сильнейший окислитель, способный оттягивать электроны даже от атома кислорода.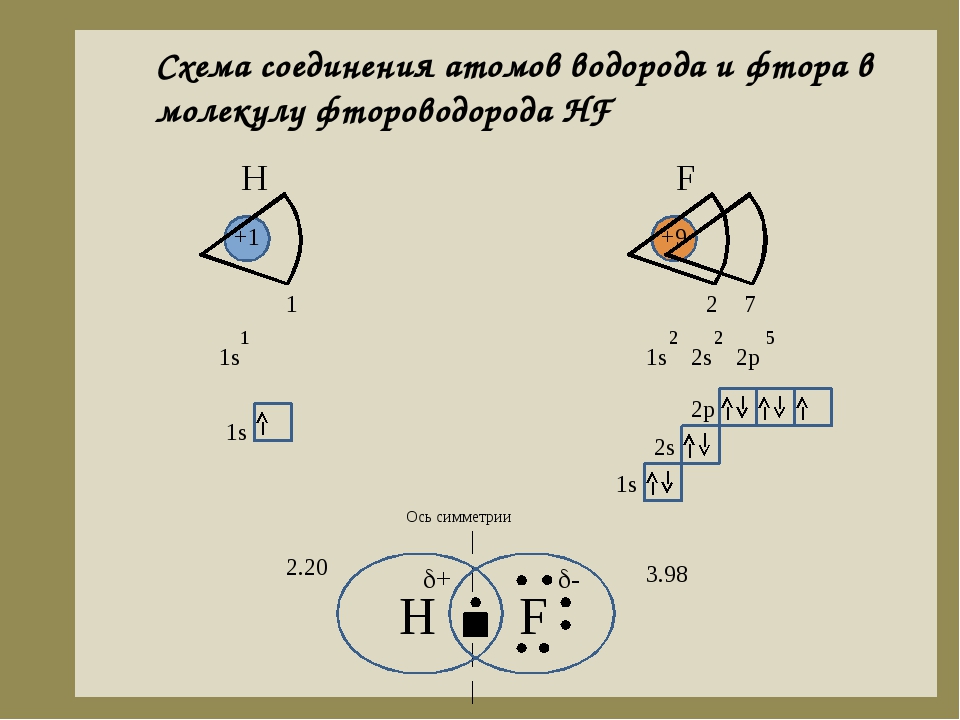 Ион фтора по размерам почти точно равен иону кислорода О -, поэтому оба иона образуют соединения, похожие друг на друга. Между фторидами ионного тина, например фторидом натрия, и оксидами, например оксидом кальция, наблюдается сходство в строении кристаллической решетки. По ряду свойств фториды металлов резко отличаются от хлоридов и бромидов. Так, фторид серебра растворим в воде, в то время как его хлориды и бромиды почти нерастворимы. [c.194]
Ион фтора по размерам почти точно равен иону кислорода О -, поэтому оба иона образуют соединения, похожие друг на друга. Между фторидами ионного тина, например фторидом натрия, и оксидами, например оксидом кальция, наблюдается сходство в строении кристаллической решетки. По ряду свойств фториды металлов резко отличаются от хлоридов и бромидов. Так, фторид серебра растворим в воде, в то время как его хлориды и бромиды почти нерастворимы. [c.194]
Самым распространенным из галогенов является хлор, который содержится в биосфере в макроколичествах, тогда как фтор, бром, иод являются микроэлементами. Все галогены имеют сходное строение внешнего электронного слоя. [c.74]
Строение внешнего электронного слоя атомов хлора, брома, иода rts p . Для всех рассматриваемых элементов возможен переход атомов в возбужденные состояния, отвечающие w > 0 этим они отличаются от фтора. Если для F единственной ненулевой степенью окисления является —1, то для остальных галогенов она лишь наиболее устойчивая. 7 [c.474]
7 [c.474]
Высшие интергалогенные соединения имеют формулы ХХ3, ХХ5 или XX,, где Х -хлор, бром или иод, а Х -фтор (единственным исключением является 1С1з, в котором Х -хлор). Из проведенного в разд. 7.7, ч. 1, обсуждения химической связи и структуры следует, что соединения такого типа образуются с участием надвалентных орбиталей центрального атома. Пользуясь теорией отталкивания валентных электронных пар (ОВЭП), изложенной в разд. 8.1, ч. 1, можно предсказать геометрическое строение таких соединений. Характер химической связи между центральным и периферическими атомами в интергалогенных соединениях можно описать и в рамках представлений [c.295]
Строение внешнего. электронного слог атомов хлора, брВнешние электронные оболочки атомов хлора, брома и иода имеют свободные (/-орбитали, поэтому для всех рассматриваемых элементов возможен переход атомов в возбужденные состояния, отвечающие степеням окисления >0 этим они отличаются от фтора.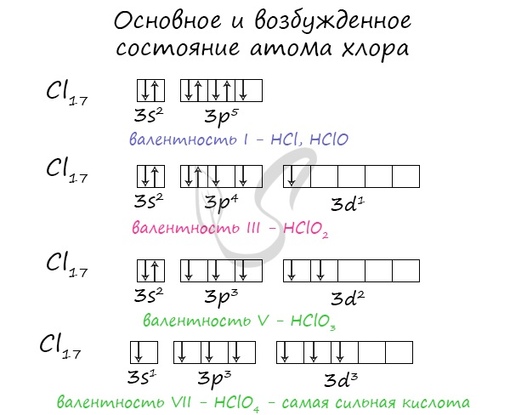 Если для фтора единственной ненулевой степенью окисления является -1, то для остальных галогенов она лишь наиболее устойчива. [c.461]
Если для фтора единственной ненулевой степенью окисления является -1, то для остальных галогенов она лишь наиболее устойчива. [c.461]
Из сделанного обзора строения атомов первых 20 элементов периодической системы можно сделать чрезвычайно важные выводы. У атомов водорода и гелия, входящих в п е р в ы й период периодической системы Д. И. Менделеева, имеется одна электронная оболочка, причем образование этой оболочки начинается у водорода, первого элемента этого периода, и кончается у гелия, последнего элемента этого периода. У атомов лития, бериллия, бора, углерода, азота, кислорода, фтора и неона, входящих во второй период периодической системы, имеются две электронные оболочки, причем образование второй оболочки начинается у лития, первого элемента этого периода, и кончается у неона, последнего элемента этого периода. У атомов натрия, магния, алюминия, кремния, фосфора, серы, хлора и аргона, входящих в третий период периодической системы, имеются три электронные оболочки, причем образование третьей электронной оболочки начинается у натрия, первого элемента этого периода, и кончается у аргона, последнего элемента этого периода.
 У атома калия, начинающего четвертый период периодической системы, начинается образование четвертой электрон- [c.212]
У атома калия, начинающего четвертый период периодической системы, начинается образование четвертой электрон- [c.212]Следует отметить, что среди полифосфонитрилгалогенидов изучались производные хлора, брома и фтора методом получения, строению, свойствам и применению которых посвящен ряд обзоров Методом МО ЛКАО исследована электронная [c.610]
При изучении химических свойств элементов выявилось одно очень важное явление — они образуют естественные группы. Действительно, сравнивая свойства фтора, хлора, брома и иода, мы видели, что эти элементы обладают близкими свойствами все они образуют соединения с водородом типа HR, где R — один из представителей этой группы они непосредственно реагируют с металлами, образуя при этом типичные соли, например, NaF, Na l, NaBr и KJ. Они образуют соли кислородсодержащих кислот, которые обладают сильными окислительными свойствами КСЮ, КВгО и KJO. Можно было бы указать еще ряд их общих свойств. При изучении строения их атомов было установлено, что у всех этих элементов, и только у них, внешний электронный слой состоит из 7 электронов. Все это дало право объединить их в одну группу и дать общее название — галогены. [c.271]
Все это дало право объединить их в одну группу и дать общее название — галогены. [c.271]
Строение атома фосфора. Соответственно порядковому номеру фосфора 15 его атом имеет три электронные оболочки из 2, 8 и 5 эл ктро- ов. Лишь при взаимодействии с наиболее электроположительными металлами атом фосфора может восполнять внешнюю оболочку до. октета, превращаясь в троекратно отрицательный ион Р. Обычно же атом фосфора образует ковалентные связи, выступая либо как трехвалент-яый, либо же — в соединениях с наиболее электроотрицательными, правее и выше стоящими элементами (фтором, кислородо М, хлором и серой) — как положительно поляризованный пятивалентный элемент. [c.347]
Вопросы и задачи. 1. Рассказать о строении атомов элементов. 2. Привести схемы строения атомов элементов, учитывая заряд ядра атома, указанный в скобках водорода (1), хлора (17), алюминия (13), серы (16 , кислорода (8), гелия (2), лития (3), фтора (9), калия (19), неона (10), кальция (20), фосфора (15). 3. Что такое- ноны Привести примеры положительно и отрицательно заряженных ионов. 4. Привести символы следующих ионов а) положительно заряженного нона меди, несущего 2 заряда б) отрицательно заряженного иона фтора, несущего один заряд в) положительно заряженного иона железа, несущего три заряда г) отрицательно заряженного нона серы, несущего два заряда. 5. Привести схемы строения следующих атомов и ионов, учитывая заряд ядра атома, указанный в скобках а) атома кальция и положительно заряженного иона кальция (20), б) атома фтора и отрицательно заряженного иона фтора (9), в) атома магния и положительно заряженного иона магния (12), г) атома лития и положительно ааряженного иона лития (3), д) атома серы и отрицательно заряженного иона серы (16). 6. Изобразить в виде электронно-ионного уравнения процесс превращения атома в ион а) хлора (в отрицательно заряженный ион), б) серы (в отрицательно заряженный ион), [c.34]
3. Что такое- ноны Привести примеры положительно и отрицательно заряженных ионов. 4. Привести символы следующих ионов а) положительно заряженного нона меди, несущего 2 заряда б) отрицательно заряженного иона фтора, несущего один заряд в) положительно заряженного иона железа, несущего три заряда г) отрицательно заряженного нона серы, несущего два заряда. 5. Привести схемы строения следующих атомов и ионов, учитывая заряд ядра атома, указанный в скобках а) атома кальция и положительно заряженного иона кальция (20), б) атома фтора и отрицательно заряженного иона фтора (9), в) атома магния и положительно заряженного иона магния (12), г) атома лития и положительно ааряженного иона лития (3), д) атома серы и отрицательно заряженного иона серы (16). 6. Изобразить в виде электронно-ионного уравнения процесс превращения атома в ион а) хлора (в отрицательно заряженный ион), б) серы (в отрицательно заряженный ион), [c.34]
Химические свойства элементов, как известно из неорганической химии, определяются структурой электронного окружения ядер, и в первую очередь структурой внешних электронных слоев — так называемыми валентными электронами.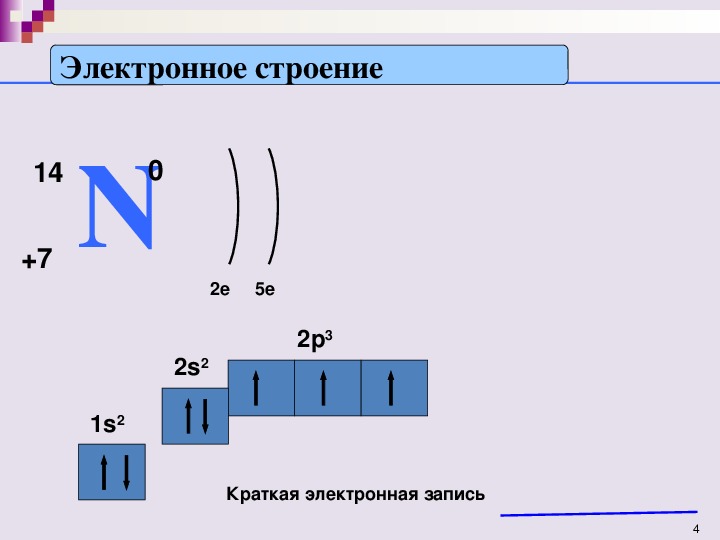 Сходство строения внешних электронных слоев элементов проявляется в сходстве свойств этих элементов — такие элементы входят в состав одной группы Периодической системы Д. И. Менделеева. Вступая в химическую реакцию, элементы в большей или меньшей степени деформируют свои внешние электронные слои электроны внешних слоев реагирующих элементов взаимпдрйствуют между собой (перекрываются) и образуют более сложное, в значительной степени общее, электронное облако. При схарактер взаимодействия будет зависеть от свойств партнеров по реакции. Так, например, сера, взаимодействуя с металлами, оттягивает электроны к себе, электронное облако металла в большей или меньшей степени (в зависимости от свойств металла) смещается в сторону ядра серы, и в отдельном случае может образоваться почти чисто ионная связь. При взаимодействии же серы с кислородом, хлором или фтором электронное облако оказывается смещенным в сторону ядер кислорода, хлора или фтора. В элементарной сере все атомы связаны между собой типичными атомными связями.
Сходство строения внешних электронных слоев элементов проявляется в сходстве свойств этих элементов — такие элементы входят в состав одной группы Периодической системы Д. И. Менделеева. Вступая в химическую реакцию, элементы в большей или меньшей степени деформируют свои внешние электронные слои электроны внешних слоев реагирующих элементов взаимпдрйствуют между собой (перекрываются) и образуют более сложное, в значительной степени общее, электронное облако. При схарактер взаимодействия будет зависеть от свойств партнеров по реакции. Так, например, сера, взаимодействуя с металлами, оттягивает электроны к себе, электронное облако металла в большей или меньшей степени (в зависимости от свойств металла) смещается в сторону ядра серы, и в отдельном случае может образоваться почти чисто ионная связь. При взаимодействии же серы с кислородом, хлором или фтором электронное облако оказывается смещенным в сторону ядер кислорода, хлора или фтора. В элементарной сере все атомы связаны между собой типичными атомными связями. [c.6]
[c.6]
Если опираться на формальное лрименедие периодического закона, то следовало бы ожидать энергию связи в молекуле фтора большей, чем тако-, вая- в молекуле хлора. Для ia, Вгг и Ь отчетливо видна закономерность чем меньше порядковый номер галогена, тем больше энергия связи, и эта закономерность i.e выполняется для фтора. Есть два объяснения такому факту. Первое предполагает более сильное взаимное отталкивание электронных оболочек двух атомов фтора в молекуле вследствие их меньшего, у других галогенов, размера. Второе опирается на то, что у свободногв атома фтора в отличие от атомов других галогенов отсутствуют вакант-иые d-ячейки. В самом деле, сопоставив строение электронной оболочки атома фтора (см. рис. 30) и строение электронной оболочки атома хлора (рис. 31), мы находим, что в отличие от атома фтора во внешнем валент- [c.65]
Отталкивающее влияние уединенных пар уменьшает углы РС1Р от 90 до 87°29. Строение молекул пентафторида приведено на рис. 302. В этом случае имеется гибридная конфигурация врЫ , т. е. шесть пар октаэдриче-ски расположенных электронов одна пара уединенная и отталкивает четыре атома фтора, выводя их из плоскости, в которой лежит ядро атома хлора. Энергетика образования фторидов хлора представлена в табл. 122. [c.324]
302. В этом случае имеется гибридная конфигурация врЫ , т. е. шесть пар октаэдриче-ски расположенных электронов одна пара уединенная и отталкивает четыре атома фтора, выводя их из плоскости, в которой лежит ядро атома хлора. Энергетика образования фторидов хлора представлена в табл. 122. [c.324]
Энергия ионизации. Степень ионности связи | Задачи 228
Задача 228.
Энергия ионизации атомов фтора и хлора составляет соответственно 17,4 и 13,0 эВ, а энергия сродства к электрону 3,45 и 3,61 эВ. для какого из этих элементов более характерно образование ионных соединений? Указать знак заряда ионов галогенов в этих соединениях.
Решение:
Энергия ионизации – это энергия, которую необходимо затратить для удаления электрона из изолированного, свободного атома, находящегося в основном состоянии, на бесконечно большое расстояние.
Сродство к электрону – это энергия, которая выделяется в результате присоединения электрона электроотрицательным атомом и превращения его в анион.
Таким образом, фтор, обладая большей энергией ионизации, чем хлор, способен сильнее удерживать неспаренный электрон, т.е. проявляет в большей степени неметаллические свойства. Фтор обладает самой высокой электроотрицательностью из всех химических элементов, поэтому обладает более выраженной способностью к образованию ионных соединений, чем хлор.
Обладая меньшей энергией сродства к электрону фтор в большей степени, чем хлор, способен образовывать ионы.
Электронная конфигурация валентного энергетического уровня атомов фтора и хлора может быть представлена формулой ns2np5, т.е на внешнем валентном слое их атомы содержат по семь электронов и, присоединяя недостающий восьмой электрон, превращаются в однозарядные анионы F– и Cl–, которые имеют устойчивую электронную конфигурацию благородного газа аргона.
Таким образом, для фтора более характерно образование ионных соединений, чем для хлора. Фтор и хлор образуют ионы знак заряда, которых -1.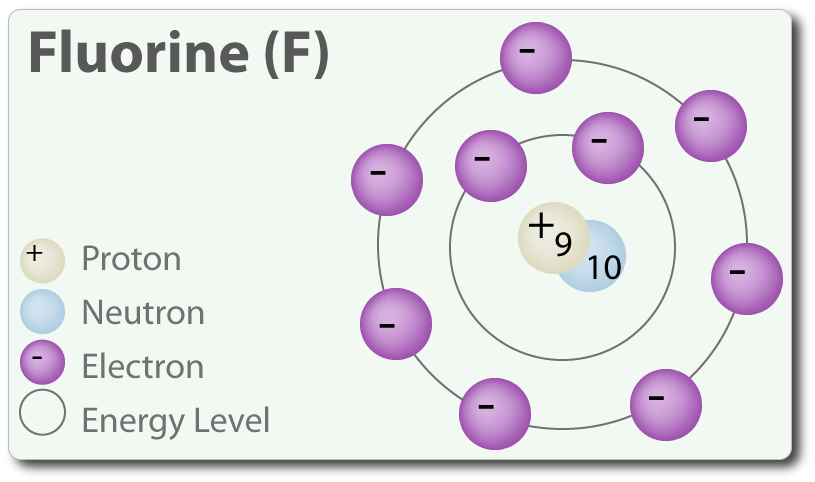
Задача 229.
Указать тип химической связи в молекулах Н2, С12, НСI. Привести схему перекрывания электронных облаков.
Решение:
В молекулах Н2 и Cl2 наблюдается ковалентная неполярная связь, а в HCl – ковалентная полярная.
Ковалентная химическая связь образуется двумя электронами от двух разных атомов, причём электроны с противоположно направленными спинами. Эта электронная пара принадлежит одновременно двум атомам. Комбинации таких двухэлектронных двухцентровых связей, отражающие электронную структуру молекулы, получили название валентных схем. Например:
Схемы перекрывания электронных облаков имеют вид:
а) Для Н2.
Общая электронная пара расположена на одинаковом расстоянии от центров обоих атомов водорода – связь ковалентная неполярная.
б) Для Cl2
Общая электронная пара расположена на одинаковом расстоянии от центров обоих атомов хлора – связь ковалентная неполярная.
в) Для HCl
Общая электронная пара атомов водорода и хлора смещена в сторону более электроотрицательного атома хлора – связь ковалентная полярная.
Во всех случаях перекрывание атомных орбиталей происходит на межъядерной оси, т.е. образуются -связи (сигма-связь).
В молекулах Н2 и Cl2 электронная пара расположена на одинаковом расстоянии от атомных ядер, потому что электроотрицательность атомов в молекулах простых веществ Н2 и Cl2 одинаковая, связь ковалентная неполярная. В молекуле HCl электронная пара смещена в сторону более электроотрицательного атома Cl (электроотрицательность Cl равна 2,9, а Н – 2,16), связь ковалентная полярная, образующаяся между разными атомами.
Задача: 230.
Пользуясь таблицей относительных электроотрицательностей, вычислить их разность для связей К — С1, Са — С1, Fе — С1, Gе — С1. Какая из связей характеризуется наибольшей степенью ионности?
Решение:
По данным таблицы «Относительная электроотрицательность элементов» вычисляем разность электроотрицательностей для связей:
Наибольшей разностью электроотрицательности характеризуется связь K—Cl. Таким образом, связь K—Cl характеризуется наибольшей ионностью, так как она более полярная. Диссоциация по связи K—Cl в водных растворах будет проходить легче, чем во всех других случаях, при этом образуются ионы:
Таким образом, связь K—Cl характеризуется наибольшей ионностью, так как она более полярная. Диссоциация по связи K—Cl в водных растворах будет проходить легче, чем во всех других случаях, при этом образуются ионы:
KCl ⇔ K+ + Cl–
Задача 231.
Какой характер имеют связи в молекулах NCl3, СS2, JCl5, NF3, OF2, ClF, СО2? Указать для каждой из них направление смещения общей электронной пары.
Решение:
а) При соединении атома азота с тремя атомами хлора образуется молекула NCl3, в которой каждый из трёх атомов хлора связан с атомом азота парой общих электронов (один электрон от атома хлора, другой – от атома азота). Схема молекулы NCl3 имеет вид:
Разность электроотрицательностей связи N—C равна 0,26 ( = 3,16 – 2,9 = 0,26), т. е. имеет незначительное численное значение, значит, связь ковалентная слабополярная (<1). Так как азот более электроотрицательнее (3,16), чем хлор (2,9), то направление смещения общей электронной пары будет в сторону атома азота. Связь слабополярная, характеризуется небольшой степенью ионности.
Так как азот более электроотрицательнее (3,16), чем хлор (2,9), то направление смещения общей электронной пары будет в сторону атома азота. Связь слабополярная, характеризуется небольшой степенью ионности.
б) При соединении атома углерода с двумя атомами серы образуется молекула СS2, в которой каждый из двух атомов серы связан с атомом углерода двумя парами электронов (два электрона от атома серы и два других от атома углерода). Схема строения молекулы СS2 имеет вид:
Атом углерода имеет на внешнем электронном слое четыре sp3-гибридных электронных облака, которые перекрываются с электронными облаками четырёх p-электронов атомов серы (по два неспаренных электрона от каждого атома серы). Так как атом углерода более электроотрицательней (2,57), чем атом серы (2,5), то направление смещения общей электронной пары будет в сторону атома углерода. Разность электроотрицательностей связи С—S равна 0,07 ( = 2,57 – 2,5 = 0,07). Связь малополярная, характеризуется ничтожно малой степенью ионности ( <1).
в) При соединении атома йода с пятью атомами хлора образуется молекула JCl5, в которой каждый из пяти атомов хлора связан с атомом йода парой общих электронов (один электрон от атома хлора, другой – от йода). Схема строения молекулы JCl5:
Разность электроотрицательностей связи J—Cl равна 0,62 (= 2,9 – 2, 28 = 0,62), значит, связь ковалентная полярная, в которой наблюдается смещение электронной пары в сторону более электроотрицательного атома хлора. Связь слабополярная, характеризуется небольшой степенью ионности
(<1).
г) При соединении атома азота с тремя атомами фтора образуется молекула NF3, в которой каждый из трёх атомов фтора связан с атомом азота парой общих электронов (один электрон от атома фтора, другой – от азота). Электронная схема строения молекулы NF3:
Разность электроотрицательностей связи N—F равна 1,04 (= 4,2 – 3,16 = 1,04). Связь N—F сильно полярна, т.е. характеризуется большой степенью ионности ( >1).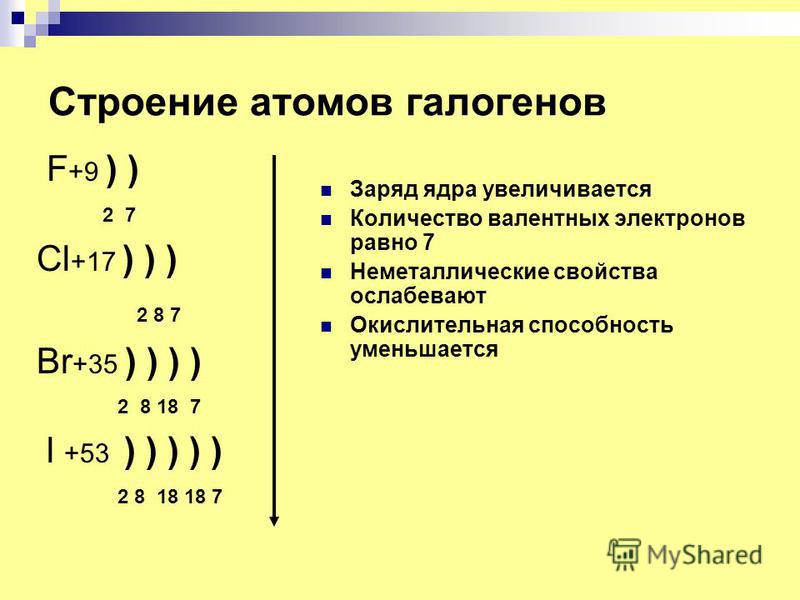 Смещение электронной пары связи N—F будет в сторону более электроотрицательного атома – фтору.
Смещение электронной пары связи N—F будет в сторону более электроотрицательного атома – фтору.
д) При соединении атома кислорода с двумя атомами фтора образуется молекула OF2, в которой каждый из атомов фтора соединён с атомом кислорода парой общих электронов (один от атома фтора, другой – от кислорода). Электронная схема строения молекулы OF2:
Разность электроотрицательностей связи F—O равна 0,6 (= 4,2 – 3,6 = 0,6), т. е. является ковалентной слабополярной, так как меньше единицы. Смещение электронной пары связи F—O будет в сторону более электроотрицательного атома – фтору.
е) При соединении атома фтора с атомом хлора образуется молекула ClF, в которой атом фтора соединён с атомом хлора электронной парой за счёт одного электрона от атома фтора, другого – от атома хлора. Электронная схема строения молекулы ClF:
Разность электроотрицательностей связи F—Cl равна 1,3 (= 4,2 – 2,9 = 1,3), т. е. имеет большое численное значение, что указывает на большую степень ионности. Связь сильнополярная. Смещение электронной пары связи F—Cl будет в сторону более электроотрицательного атома – фтору.
Связь сильнополярная. Смещение электронной пары связи F—Cl будет в сторону более электроотрицательного атома – фтору.
ж) При соединении атома углерода с двумя атомами кислорода образуется молекула СО2, в которой каждый из двух атомов кислорода связан с атомом углерода двумя парами электронов (два электрона от атома кислорода, другие два – от углерода). Электронная схема строения молекулы СО2:
Разность электроотрицательностей связи С—О равна 0,5 = 3,6 – 2,9 = 0,5), т. е. имеет небольшое численное значение, что указывает на слабую степень ионности. Связь слабополярная. Смещение электронной пары связи С—О будет в сторону более электроотрицательного атома – кислороду.
Схема образования ионной связи калия и хлора. Схемы образования веществ с различным типом связи
Часть I
1. Атомы металлов, отдавая внешние электроны, превращаются в положительные ионы:
где n – число электронов внешнего слоя атома, соответствующее номеру группы химического элемента.
2. Атомы неметаллов, принимая электроны, недостающие до завершения внешнего электронного слоя , превращаются в отрицательные ионы:
3. Между разноимённо заряженными ионами возникает связь, которая называется ионной.
4. Дополните таблицу «Ионная связь».
Часть II
1. Дополните схемы образования положительно заряженных ионов. Из букв, соответствующих правильным ответам, вы составите название одного из древнейших природных красителей: индиго.
2. Поиграйте в «крестики-нолики». Покажите выигрышный путь, который составляют формулы веществ с ионной химической связью.
3. Верны ли следующие утверждения?
3) верно только Б
4. Подчеркните пары химических элементов, между которыми образуется ионная химическая связь.
1) калий и кислород
3) алюминий и фтор
Составьте схемы образования химической связи между выбранными элементами.
5. Придумайте рисунок в стиле комиксов, отражающий процесс образования ионной химической связи.
Придумайте рисунок в стиле комиксов, отражающий процесс образования ионной химической связи.
6. Составьте схему образования двух химических соединений с ионной связью по условной записи:
Выберите химические элементы «А» и «Б» из следующего списка:
кальций, хлор, калий, кислород, азот, алюминий, магний, углерод, бром.
Подходят для данной схемы кальций и хлор, магний и хлор, кальций и бром, магний и бром.
7. Напишите небольшое литературное произведение (эссе, новеллу или стихотворение) об одном из веществ с ионной связью, которое человек применяет в быту или на производстве. Для выполнения задания используйте возможности Интернета.
Хлорид натрия – вещество с ионной связью, без него нет жизни, хотя, когда его много – это тоже нехорошо. Даже есть такая народная сказка, где рассказывается о том, что принцесса любила своего отца короля так сильно, как соль, за что была изгнана из королевства. Но, когда король однажды попробовал еду без соли и понял, что есть невозможно, он тогда понял, что дочь его очень сильно любила. Значит, соль – есть жизнь, но её потребление должно быть в
Значит, соль – есть жизнь, но её потребление должно быть в
меру. Потому что чрезмерное потребление соли сильно вредит здоровью. Избыток соли в организме приводит к заболеванию почек, меняет цвет кожи, задерживает излишнюю жидкость в организме, что приводит к отёкам и нагрузке на сердце. Поэтому, надо контролировать потребление соли. 0,9% раствор хлорида натрия – это физиологический раствор, используется для вливания лекарств в организм. Поэтому, очень трудно ответить на вопрос: полезна или вредна соль? Она нам нужна в меру.
Помощь уже в пути, держи.
а) Рассмотрим схему образования ионной связи между натрием и
кислородом.
1. Натрий – элемент главной подгруппы I группы, металл. Его атому легче отдать I внешний электрон, чем принять недостающие 7:
1. Кислород- элемент главной подгруппы VI группы, неметалл.
Его атому легче принять 2 электрона, которых не хватает до завершения внешнего уровня, чем отдать 6 электронов с внешнего уровня.
1. Сначала найдем наименьшее общее кратное между зарядами образовавшихся ионов, оно равно 2(2∙1). Чтобы атомы Naотдали 2 электрона, их надо взять 2(2:1), чтобы атомы кислорода смогли принять 2 электрона, их нужно взять 1.
Чтобы атомы Naотдали 2 электрона, их надо взять 2(2:1), чтобы атомы кислорода смогли принять 2 электрона, их нужно взять 1.
2. Схематично образование ионной связи между атомами натрия и кислорода можно записать так:
б) Рассмотрим схему образования ионной связи между атомами лития и фосфора.
I. Литий – элемент I группы главной подгруппы, металл. Его атому легче отдать 1 внешний электрон, чем принять недостающие 7:
2. Хлор- элемент главной подгруппы VII группы, неметалл. Его
атому легче принять 1 электрон, чем отдать 7 электронов:
2. Наименьшее общее кратное 1, т.е. чтобы 1 атом лития отдал, а атом хлора принял 1 электрон, надо взять их по одному.
3. Схематично образование ионной связи между атомами лития и хлора можно записать так:
в) Рассмотрим схему образования ионной связи между атомами
магния и фтора.
1. Магний- элемент II группы главной подгруппы, металл. Его
атому легче отдать 2 внешних электрона, чем принять недостающие 6:
2. Фтор – элемент главной подгруппы VII группы, неметалл. Его
Фтор – элемент главной подгруппы VII группы, неметалл. Его
атому легче принять 1 электрон, которого не хватает до завершения вешнего уровня, чем отдать 7 электронов:
2. Найдем наименьшее общее кратное между зарядами образовавшихся ионов, оно равно 2(2∙1). Чтобы атомы магния отдали 2 электрона, нужен только один атом, чтобы атомы фтора смогли принять 2 электрона, их нужно взять 2(2:1).
3. Схематично образование ионной связи между атомами лития и фосфора можно записать так:
Назад
Вперёд
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Цели урока :
- Сформировать понятие об химических связях на примере ионной связи. Добиться понимания образования ионной связи как крайнего случая полярной.

- Обеспечить в ходе урока усвоение следующих основных понятий: ионы (катион, анион), ионная связь.
- Развивать умственную деятельность учащихся через создание проблемной ситуации при изучении нового материала.
Задачи:
- научить распознавать виды химической связи;
- повторить строение атома;
- исследовать механизм образования ионной химической связи;
- научить составлять схемы образования и электронные формулы ионных соединений, уравнения реакций с обозначением перехода электронов.
Оборудование : компьютер, проектор, мультимедийный ресурс, периодическая система химических элементов Д.И. Менделеева, таблица «Ионная связь».
Тип урока: Формирование новых знаний.
Вид урока: Мультимедиа урок.
Х од урока I. Организационный момент . II. Проверка домашнего задания .Учитель: Как атомы могут принимать устойчивые электронные конфигурации? Каковы cпособы образования ковалентной связи?
Ученик: Полярная и неполярная ковалентные связи образованы по обменному механизму. К обменному механизму относят случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону. Например, водород: (слайд 2)
К обменному механизму относят случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону. Например, водород: (слайд 2)
Связь возникает благодаря образованию общей электронной пары за счет объединения неспаренных электронов. У каждого атома есть по одному s-электрону. Атомы Н равноценны и пары одинаково принадлежат обоим атомам. Поэтому же принципу происходит образование общих электронных пар (перекрывание р-электронных облаков) при образовании молекулы F 2 . (слайд 3)
Запись H· означает, что у атома водорода на внешнем электронном слое находится 1 электрон. Запись показывает, что на внешнем электронном слое атома фтора находится 7 электронов.
При образовании молекулы N 2 . Образуются 3 общие электронные пары. Перекрываются р-орбитали. (слайд 4)
Связь называется неполярная.
Учитель: Мы сейчас рассмотрели случаи, когда образуются молекулы простого вещества. Но вокруг нас множество веществ, сложного строения. Возьмем молекулу фтороводорода. Как в этом случае происходит образование связи?
Возьмем молекулу фтороводорода. Как в этом случае происходит образование связи?
Ученик: При образовании молекулы фтороводорода перекрывается орбиталь s-электрона водорода и орбиталь р-электрона фтора Н-F. (слайд 5)
Связывающая электронная пара смещена к атому фтора, в результате чего образуется диполь . Связь называется полярная .
III. Актуализация знаний .Учитель: Химическая связь возникает вследствие изменений, которые происходят с наружными электронными оболочками соединяющихся атомов. Это возможно потому, что наружные электронные слои не завершены у элементов, кроме инертных газов. Химическая связь объясняется стремлением атомов приобрести устойчивую электронную конфигурацию, подобную конфигурации «ближайшего» к ним инертного газа.
Учитель: Записать схему электронного строения атома натрия (у доски). (слайд 6)
Ученик: Атому натрия для достижения устойчивости электронной оболочки необходимо либо отдать один электрон, либо принять семь. Натрий легко отдаст свой далекий от ядра и слабо связанный с ним электрон.
Натрий легко отдаст свой далекий от ядра и слабо связанный с ним электрон.
Учитель: Составить схему отдачи электрона.
Nа° – 1ē → Nа+ = Ne
Учитель: Записать схему электронного строения атома фтора (у доски).
Учитель: Как добиться завершения заполнения электронного слоя?
Ученик: Атому фтора для достижения устойчивости электронной оболочки необходимо либо отдать семь электронов, либо принять один. Энергетически выгоднее фтору принять электрон.
Учитель: Составить схему приема электрона.
F° + 1ē → F- = Ne
IV. Изучение нового материал.Учитель обращается с вопросом к классу, в котором ставится задача урока:
Возможны ли другие варианты, при которых атомы могут принимать устойчивые электронные конфигурации? Каковы пути образования таких связей?
Сегодня мы рассмотрим один из видов связей – ионную связь. Сопоставим строение электронных оболочек уже названных атомов и инертных газов.
Беседа с классом.
Учитель: Какой заряд имели атомы натрия и фтора до реакции?
Ученик: Атомы натрия и фтора электронейтральны, т.к. заряды их ядер уравновешиваются электронами, вращающимися вокруг ядра.
Учитель: Что происходит между атомами при отдаче и принятии электронов?
Ученик: Атомы приобретают заряды.
Учитель дает пояснения: В формуле иона дополнительно записывают его заряд. Для этого используют верхний индекс. В нем цифрой указывают величину заряда (единицу не пишут), а потом – знак (плюс или минус). Например, ион Натрия с зарядом +1 имеет формулу Na + (читается «натрий-плюс»), ион Фтора с зарядом -1 – F – («фтор-минус»), гидроксид-ион с зарядом -1 – ОН – («о-аш-минус»), карбонат-ион с зарядом -2 – CO 3 2- («цэ-о-три-два-минус»).
В формулах ионных соединений сначала записывают, не указывая зарядов, положительно заряженные ионы, а потом – отрицательно заряженные. Если формула правильная, то сумма зарядов всех ионов в ней равна нулю.
Положительно заряженный ионназывается катионом ,аотрицательно заряженный ион- анионом.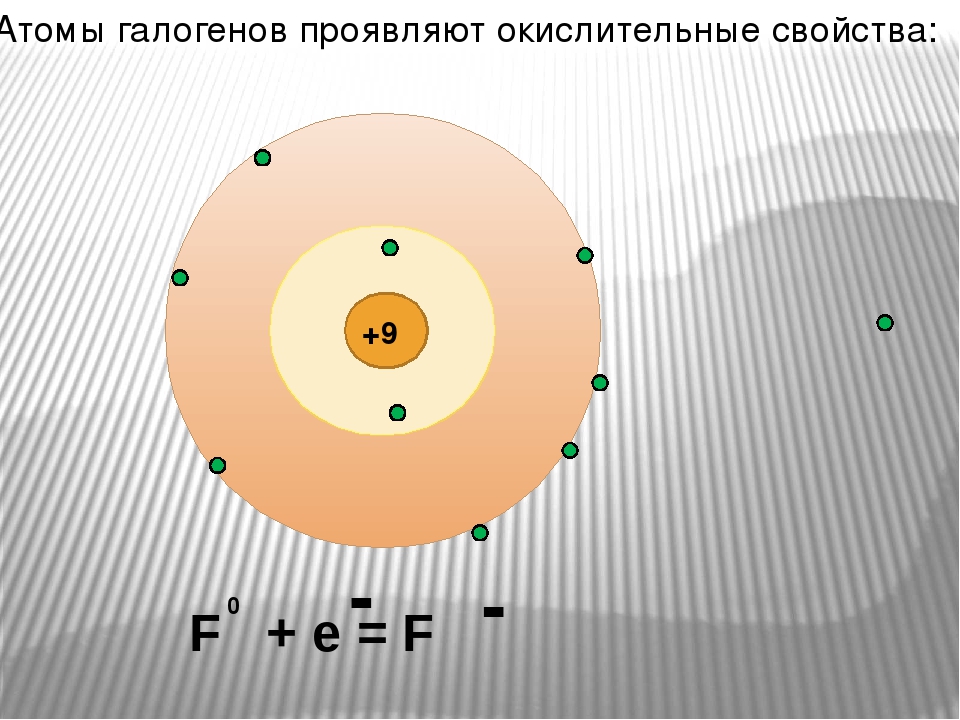
Учитель: Записываем определение в рабочие тетради:
Ион – это заряженная частица, в которую превращается атом в результате принятия или отдачи электронов.
Учитель: Как определить величину заряда иона кальция Ca 2+ ?
Ученик: Ио́н – электрически заряженная частица, образующаяся в результате потери или присоединения одного или нескольких электронов атомом. У кальция на последнем электронном уровне находятся два электрона, ионизация атома кальция происходит при отдаче двух электронов. Ca 2+ – двухзарядный катион.
Учитель: Что происходит с радиусами этих ионов?
При переходе электронейтрального атома в ионное состояние размер частицы сильно изменяется. Атом, отдавая свои валентные электроны, превращается при этом в более компактную частицу – катион. Например, при переходе атома натрия в катион Na+, имеющий, как указано выше, структуру неона, радиус частицы сильно уменьшается. Радиус аниона всегда больше радиуса соответствующего электронейтрального атома.
Учитель: Что происходит с разноименно заряженными частицами?
Ученик: Разноименно заряженные ионы натрия и фтора, возникающие в результате перехода электрона от атома натрия к атому фтора, взаимно притягиваются и образуют фторид натрия. (слайд 7)
Nа + + F – = NаF
Рассмотренная нами схема образования ионов показывает, как между атомом натрия и атомом фтора образуется химическая связь, которую называют ионной.
Ионная связь – химическая связь, образованная электростатическим притяжением друг к другу разноименно заряженных ионов.
Соединения, которые при этом образуются, называют ионными соединениями.
V. Закрепление нового материала .Задания для закрепления знаний и умений
1. Сравните строение электронных оболочек атома кальция и катиона кальция, атома хлора и хлорид – аниона:
Прокомментируйте схему образования ионной связи в хлориде кальция:
2. Для выполнения данного задания необходимо разделиться на группы по 3–4 человека. Каждый участник группы рассматривает один пример и результаты представляет всей группе.
Каждый участник группы рассматривает один пример и результаты представляет всей группе.
Ответ учащихся:
1. Кальций – это элемент главной подгруппы II группы, металл. Его атому легче отдать два внешних электрона, чем принять недостающие шесть:
2. Хлор – это элемент главной подгруппы VII группы, неметалл. Его атому легче принять один электрон, которого ему не хватает до завершения внешнего уровня, чем отдать семь электронов с внешнего уровня:
3. Сначала найдем наименьшее общее кратное между зарядами образовавшихся ионов, оно равно 2 (2×1). Затем определим, сколько атомов кальция нужно взять, чтобы они отдали два электрона, то есть надо взять один атом Са и два атома CI.
4. Схематично образование ионной связи между атомами кальция и хлора можно записать: (слайд 8)
Са 2+ + 2СI – → СаСI 2
Задания для самоконтроля
1. На основе схемы образования химического соединения составьте уравнение химической реакции: (слайд 9)
2. На основе схемы образования химического соединения составьте уравнение химической реакции: (слайд 10)
На основе схемы образования химического соединения составьте уравнение химической реакции: (слайд 10)
3. Дана схема образования химического соединения: (слайд 11)
Выберите пару химических элементов, атомы которых могут взаимодействовать в соответствии с этой схемой:
а) Na и O ;
б) Li и F ;
в) K и O ;
г) Na и F
Данный урок посвящен обобщению и систематизации знаний о видах химической связи. В процессе урока будут рассмотрены схемы образования химической связи в различных веществах. Урок поможет закрепить умение определять вид химической связи в веществе по его химической формуле.
Тема: Химическая связь. Электролитическая диссоциация
Урок: Схемы образования веществ с различным типом связи
Рис. 1. Схема образования связи в молекуле фтора
Молекула фтора состоит из двух атомов одного химического элемента-неметалла с одинаковой электроотрицательностью, следовательно, в этом веществе реализуется ковалентная неполярная связь. Изобразим схему образования связи в молекуле фтора. Рис. 1.
Изобразим схему образования связи в молекуле фтора. Рис. 1.
Вокруг каждого атома фтора с помощью точек нарисуем семь валентных, то есть внешних, электронов. До устойчивого состояния каждому атому необходим еще один электрон. Таким образом, образуется одна общая электронная пара. Заменив ее черточкой, изобразим графическую формулу молекула фтора F-F.
Вывод: ковалентная неполярная связь образуется между молекулами одного химического элемента-неметалла. При таком типе химической связи образуются общие электронные пары, которые в равной степени принадлежат обоим атомам, то есть не происходит смещения электронной плотности ни к одному из атомов химического элемента
Рис. 2. Схема образования связи в молекуле воды
Молекула воды состоит из атомов водорода и кислорода – двух элементов-неметаллов с разными значениями относительной электроотрицательности, следовательно, в этом веществе – ковалентная полярная связь.
Так как кислород – более электроотрицательный элемент, чем водород, общие электронные пары смещаются в сторону кислорода. На атомах водорода возникает частичный заряд, а на атоме кислорода – частичный отрицательный. Заменив обе общие электронные пары черточками, а точнее стрелками, показывающими смещение электронной плотности, запишем графическую формулу воды Рис. 2.
На атомах водорода возникает частичный заряд, а на атоме кислорода – частичный отрицательный. Заменив обе общие электронные пары черточками, а точнее стрелками, показывающими смещение электронной плотности, запишем графическую формулу воды Рис. 2.
Вывод: ковалентная полярная связь возникает между атомами разных элементов-неметаллов, то есть с разными значениями относительной электроотрицательности. При этом типе связи образуются общие электронные пары, которые смещаются в сторону более электроотрицательного элемента .
1. №№ 5,6,7 (с.145) Рудзитис Г.Е. Неорганическая и органическая химия. 8 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман. М.: Просвещение. 2011 г.176с.:ил.
2. Укажите частицу с наибольшим и наименьшим радиусом: атом Ar, ионы: K + , Ca 2+ , Cl – .Ответ обоснуйте.
3. Назовите три катиона два аниона, которые имеют такую же электронную оболочку, что и ион F – .
Тема 22. Галогены.
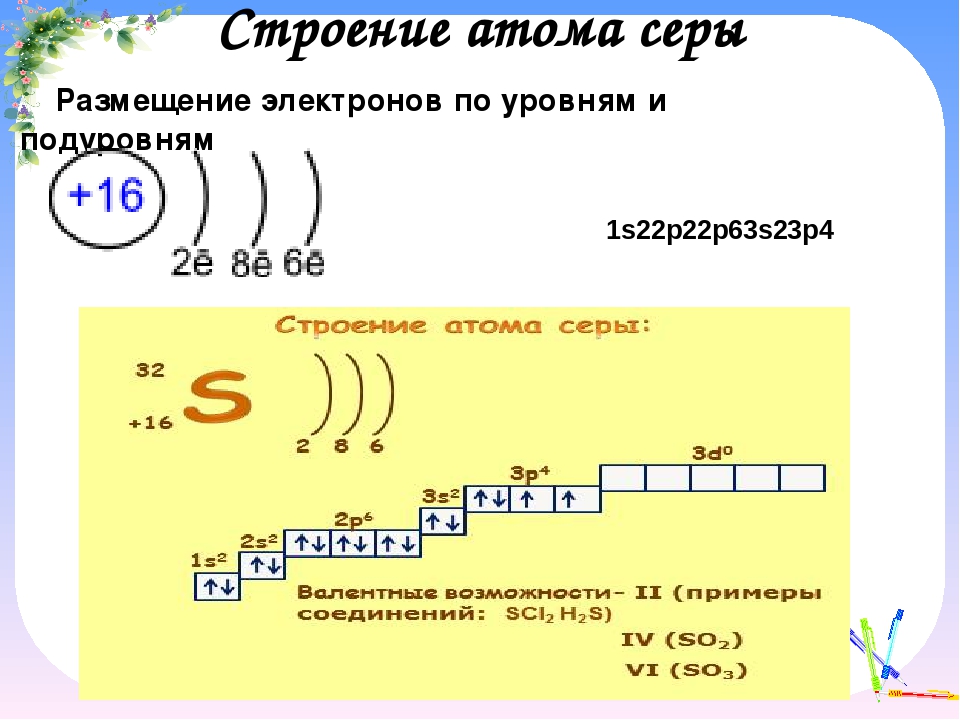 | 9 класс
| 9 классЧасть I
1. Строение атомов.
Схема строения внешнего электронного слоя:
R атома ↑ от F к I.
Восстановительные свойства ↑ от F к I.
Степень окисления F в соединениях -1, у остальных -1, а также +3, +5, +7, +1.
2. Строение молекулы.
Молекула Г2 образована за счёт ковалентной неполярной химической связи.
Молекулярная формула – Г2.
Электронная формула –
Структурная формула – Г-Г
3. Все галогены – простые вещества имеют молекулярную кристаллическую решётку. от F2 к Cl2 (поставьте знак ↑ или ↓):
– интенсивность цвета ↑;
– плотность ↑;
– металлические свойства ↑;
– неметаллические свойства ↓.
Агрегатное состояние:
F2 – газ;
Cl2 – газ;
Br2 – жидкость;
I2 – твёрдое вещество.
4. Химические свойства.
Наиболее характерны окислительные свойства, которые галогены проявляют по отношению:
1) к металлам (рассмотреть в свете ОВР):
а) Г2+2Na→2NaГ
Г2 – окислитель, Nа – восстановитель.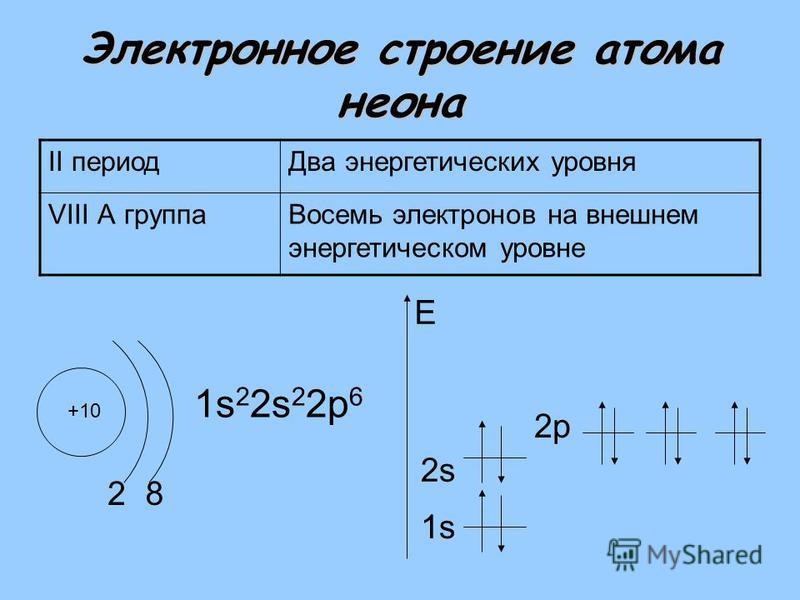
б) Г2+Са→СаГ2
Г2 – окислитель, Са – восстановитель
в) 3Г2+2Fe→2FeГ3
Г2 – окислитель, Fe – восстановитель.
2) к водороду
Vp↓ уменьшается, т.к. в ряду F2, Cl2, Br2, I2 – окислительные способности уменьшаются.
Потому что: в ряду HF, HCl, HBr, HI – прочность связи уменьшается.
3) к растворам солей, содержащим менее активные галогены (рассмотреть в свете ОВР):
5. Соединения в природе.
В свободном виде в виде двухатомных молекул, или в виде солей из-за высокой активности.
Это галогениды металлов IA и IIA групп (приведите примеры) запишите формулы основных соединений минералов, дайте их названия и синонимы):
Галит – NaCl
Сильвин – КCl
сильвинит – nNaCl + mKCl+ примеси
флюорит – CaF2
6. Получение галогенов электролизом: Cl2.
7. Заполните таблицу «Применение хлора».
Часть II
1. Максимально возможную степень окисления хлор проявляет в соединении с формулой:
Максимально возможную степень окисления хлор проявляет в соединении с формулой:
3) Cl2O7
2. Характерными степенями окисления хлора являются:
1) -1, +1, +3, +5, +7
3. Степень окисления хлора увеличивается в ряду веществ:
3) Ca(ClO)2, KClO3, HСlO4
4. Самый сильный окислитель-галоген – это фтор, который в результате восстановления получает с.о. -1. Самый сильный восстановитель – это йод, который в результате окисления получает максимальную с.о. +7.
5. Йод способен переходить из твёрдого состояния в газообразное, минуя жидкое,- это явление сублимация или возгонка.
6. Из бромида натрия можно получить бром:
1) электролизом NaBr, схема которого
ток
2NaBr→2Na+Br2
2) реакцией замещения Br2+NaI, уравнение которой
Br2+2NaI→2NaBr+I2
7. Дополните схему реакции. Расставьте коэффициенты в реакции методом электронного баланса.
8. С помощью дополнительных источников информации, в том числе Интернета, подготовьте небольшое сообщение об истории открытия и значении одного из галогенов. Составьте план сообщения или запишите тезисы в особой тетради.
Йод был открыт в 1811 г. Куртуа в золе морских водорослей, а с 1815 г. Гей-Люссак стал рассматривать его как химический элемент.
Йод находится в виде иодидов в морской воде. Присутствует в живых организмах, больше всего в водорослях (ламинарии). Известен в природе также в свободной форме, в качестве минерала.
Применение
• 5% спиртовой раствор йода используется для дезинфекции кожи вокруг повреждения, но не для приема внутрь при дефиците йода в организме.
• В рентгенологических исследованиях широко применяются йодсодержащие контрастные препараты.
• В криминалистике пары йода применяются для обнаружения отпечатков пальцев на бумажных поверхностях, например на купюрах.
• Лазерный синтез.
• Производство аккумуляторов.
• Источники света.
Значение
У животных и человека йод входит в состав гормонов, вырабатываемых щитовидной железой, оказывающих важное воздействие на рост, развитие и обмен веществ организма. Суточная потребность человека в йоде определяется возрастом, физиологическим состоянием и массой тела. Для человека среднего возраста нормальной комплекции суточная доза йода составляет 0,15 мг.
Отсутствие или недостаток йода в рационе приводит к заболеваниям (эндемический зоб, кретинизм, гипотиреоз). Также при небольшом недостатке йода отмечается усталость, головная боль, подавленное настроение, природная лень, нервозность и раздражительность; слабеет память и интеллект. Со временем появляется аритмия, повышается артериальное давление, падает уровень гемоглобина в крови.
В связи с этим к поваренной соли, поступающей в продажу в местностях с дефицитом йода, с профилактической целью добавляют иодид калия, иодид натрия или йодат калия (йодированная соль).
Расшифровка: Химия в ее элементе: фтор(Promo) Вы слушаете Химию в ее элементе, представленную вам журналом Chemistry World , журналом Королевского химического общества. (Конец промо) Крис Смит На этой неделе это не сильная кислота, но она определенно смертельна. Кира Дж. Вайсман 37-летний техник пролил себе на колени всего несколько сотен миллилитров во время обычного палеонтологического эксперимента. Он принял обычные меры предосторожности в таких ситуациях, быстро облившись водой из лабораторного шланга, и даже нырнул в ближайший бассейн, пока парамедики были в пути. Но через неделю врачи удалили ногу, а через неделю он умер. В отличие от своих близких родственников, соляной и бромистоводородной кислот, HF является слабой кислотой. Это, в сочетании с его небольшим размером молекулы, позволяет ему проникать через кожу и быстро мигрировать в более глубокие слои ткани. Пройдя через эпидермис, HF начинает диссоциировать, высвобождая высокореактивный фторид-ион. Свободный фторид прочно связывается как с кальцием, так и с магнием, образуя нерастворимые соли, которые осаждаются в окружающих тканях. Лишенные сопутствующих факторов, важные метаболические ферменты больше не могут функционировать, клетки начинают умирать, ткани – разжижаться, а кости – разъедать.И если потеря кальция происходит достаточно быстро, такие мышцы, как сердце, перестают работать. Ожоги с концентрированной HF с поражением всего 2,5% поверхности тела – например, размера подошвы стопы – закончились смертельным исходом. HF имеет долгую историю деструктивного поведения, унесшего жизни нескольких химиков в 1800-х годах, в том числе бельгийца Полена Луайе и француза Жерома Никлеса. По иронии судьбы, хотя элементарный фтор явно вреден для вашего здоровья, атомы фтора встречаются примерно в 20% всех фармацевтических препаратов. У большинства из нас тоже есть фтор, за который мы сияем улыбками. Средствами для борьбы с кариесами в зубной пасте являются неорганические фториды, такие как фторид натрия и монофторфосфат натрия. Фторид не только снижает количество растворяющей эмаль кислоты, производимой бактериями зубного налета, но и помогает в процессе восстановления зубов, проникая в эмаль, образуя еще более твердую поверхность, которая противостоит будущим атакам.И на этом список медицинских приложений не заканчивается. Усыпление вызывает немного меньше беспокойства благодаря фторированным анестетикам, таким как изофлуран и десфлуран, которые заменили легковоспламеняющиеся и взрывоопасные альтернативы, такие как диэтиловый эфир и хлороформ. Фторуглероды также являются одними из ведущих кандидатов в разработке в качестве искусственной крови, поскольку кислород более растворим в этих материалах, чем в большинстве других растворителей. А радиоактивный фтор ( 18 F, а не встречающийся в природе 19 F) является ключевым ингредиентом позитронно-эмиссионной томографии (или ПЭТ), метода визуализации всего тела, который позволяет обнаруживать раковые опухоли до их распространения. Фторохимические продукты также являются основой промышленности. Одним из самых известных является полимерный политетрафторэтилен, более известный как тефлон, который считается самым скользким твердым телом в мире. Обладая высокой термостабильностью и водонепроницаемостью, он используется в качестве покрытия для кастрюль и сковородок, в аэрозолях для выпечки, а также для отталкивания пятен на мебели и коврах. Нагревание и растяжение превращают тефлон в Gore-Tex, пористую мембрану, известную как спортивная одежда. Поры Gore-tex достаточно малы, чтобы не пропускать капли воды, а водяной пар (то есть пот) выходит наружу.Так вы сможете бегать в дождливый день и при этом оставаться сухим. Фтор играет еще одну важную роль в поддержании прохлады, поскольку кондиционеры и бытовые холодильные установки работают на энергоэффективных фторуглеродных жидкостях. И использование фтора не ограничивается землей. Когда астронавты отправляются в космос, они доверяют фторэластомерам, разновидности фторированного каучука. Эти материалы, изготовленные из уплотнительных колец и других уплотнительных устройств, гарантируют отсутствие утечек в самолетах даже в экстремальных условиях жары и холода.А когда все же случаются несчастные случаи, космические путешественники могут положиться на огнетушители на основе фторуглерода, чтобы потушить пламя. Фтор давно известен как «химический тигр». И хотя элемент, безусловно, сохраняет свою дикую сторону, мы можем с полным основанием утверждать, что приручили его. Поскольку когда-либо было обнаружено лишь небольшое количество фторорганических соединений природного происхождения, некоторые могут возразить, что теперь мы используем фтор лучше, чем сама природа. Крис Смит Итак, тефлон признан самой скользкой вещью в мире, и я готов поспорить, что есть один или два политика, которые бьют за это фтор.Спасибо также Кире Вайсманн из Заарландского университета в Германии. На следующей неделе. Touch Стив Милон Я не могу представить, что это все, что кто-то сказал бы, если бы они были достаточно неудачливы, чтобы заболеть одноименной болезнью. Болезнь ай-ай. Заболевание возникает в результате чрезмерного отравления кадмием и впервые было зарегистрировано в небольшом городке примерно в 200 милях к северо-западу от Токио. Рис, выращенный на почвах, загрязненных кадмием, содержал более чем в 10 раз больше кадмия, чем обычный рис.Причина этого заболевания – слабые и хрупкие кости, подверженные разрушению из-за высокой пористости. Крис Смит И вы можете узнать о факторе ай-ай вместе со Стивом Милоном, когда он раскроет историю кадмия на следующей неделе в «Химии в его элементе». Я Крис Смит, спасибо за внимание и до свидания. (Промо) (Окончание промо) |
Химия фтора (Z = 9) – Chemistry LibreTexts
Фтор (F) – первый элемент в группе галогенов (группа 17) в периодической таблице.Его атомный номер 9 и атомный вес 19, и это газ при комнатной температуре. Это наиболее электроотрицательный элемент, учитывая, что он является верхним элементом в галогенной группе, и, следовательно, очень реактивен. Это неметалл и один из немногих элементов, которые могут образовывать двухатомные молекулы (F2). Он имеет 5 валентных электронов на уровне 2p. Его электронная конфигурация: 1s 2 2s 2 2p 5 . Обычно он образует анион F –, поскольку он чрезвычайно электроотрицателен и является сильным окислителем.Фтор – это кислота Льюиса в слабой кислоте, что означает, что он принимает электроны при реакции. У фтора много изотопов, но единственный стабильный изотоп, встречающийся в природе, – это F-19.
Краткая история
В конце 1600-х годов минералы, которые, как мы теперь знаем, содержат фтор, использовались для травления стекла. Открытие элемента было вызвано поиском химического вещества, способного разрушать стекло (это HF, слабая кислота). Ранняя история изоляции и работы с фтором и фтористым водородом полна несчастных случаев, поскольку оба они чрезвычайно опасны.В конце концов, электролиз смеси KF и HF (тщательно следя за тем, чтобы образующиеся водород и фтор не вступили в контакт) в платиновом аппарате дал элемент.
Рисунок 1: Изображение любезно предоставлено ВикипедиейФтор был открыт в 1530 году Георгием Агриколой. Первоначально он обнаружил его в составе плавикового шпата, который использовался для плавления металлов. Он находился под этим приложением до 1670 года, когда Шванхард обнаружил его полезность для травления стекла. Чистый фтор (от латинского fluere, что означает «поток») не был выделен до 1886 года Анри Муассаном, сжигая и даже убивая многих ученых.Сегодня он имеет множество применений, в частности, в Манхэттенском проекте для создания первой ядерной бомбы.
Электроотрицательность фтора
Фтор – это самый электроотрицательный элемент в периодической таблице, что означает, что он является очень сильным окислителем и принимает электроны других элементов. Электронная конфигурация атома фтора 1s 2 2s 2 2p 5 . (см. рисунок 2)
Рисунок 2: Электронная конфигурация фтораФтор является наиболее электроотрицательным элементом, потому что он имеет 5 электронов в его 2P-оболочке.Оптимальная электронная конфигурация 2P-орбитали содержит 6 электронов, поэтому, поскольку фтор настолько близок к идеальной электронной конфигурации, электроны очень плотно прилегают к ядру. Высокая электроотрицательность фтора объясняет его малый радиус, потому что положительные протоны имеют очень сильное притяжение к отрицательным электронам, удерживая их ближе к ядру, чем более крупные и менее электроотрицательные элементы.
Реакции фтора
Из-за своей реакционной способности элементарный фтор никогда не встречается в природе, и никакой другой химический элемент не может вытеснить фтор из своих соединений.Фтор связывается практически с любым элементом, как с металлами, так и с неметаллами, потому что это очень сильный окислитель. Он очень нестабилен и реактивен, поскольку настолько близок к своей идеальной электронной конфигурации. Он образует ковалентные связи с неметаллами, и, поскольку он является наиболее электроотрицательным элементом, всегда будет восстановленным элементом. Он также может образовывать двухатомный элемент с самим собой (\ (F_2 \)) или ковалентные связи, где он окисляет другие галогены (\ (ClF \), \ (ClF_3 \), \ (ClF_5 \)). Он будет взрывоопасно реагировать со многими элементами и соединениями, такими как водород и вода.- \ tag {2} \]
Есть также некоторые органические соединения из фтора, от нетоксичных до высокотоксичных. Фтор образует ковалентные связи с углеродом, которые иногда образуют стабильные ароматические кольца. Когда углерод взаимодействует с фтором, реакция является сложной и образует смесь \ (CF_4 \), \ (C_2F_6 \), и \ (C_5F_ {12} \).
\ [C _ {(s)} + F_ {2 (g)} \ rightarrow CF_ {4 (g)} + C_2F_6 + C_5F_ {12} \ tag {3} \]
Фтор реагирует с кислородом с образованием \ (OF_2 \), потому что фтор более электроотрицателен, чем кислород.Реакция идет:
\ [2F_2 + O_2 \ rightarrow 2OF_2 \ tag {4} \]
Фтор настолько электроотрицателен, что иногда он даже образует молекулы с благородными газами, такими как ксенон, например, молекула дифторида ксенона, \ (XeF_2 \).
\ [Xe + F_2 \ rightarrow XeF_2 \ tag {5} \]
Фтор также образует сильные ионные соединения с металлами. Некоторые общие ионные реакции фтора:
\ [F_2 + 2NaOH \ rightarrow O_2 + 2NaF + H_2 \ tag {6} \]
\ [4F_2 + HCl + H_2O \ rightarrow 3HF + OF_2 + ClF_3 \ tag {7} \]
\ [F_2 + 2HNO_3 \ rightarrow 2NO_3F + H_2 \ tag {8} \]
Применение фтора
Соединения фтора присутствуют во фторированной зубной пасте и во многих городских системах водоснабжения, где они помогают предотвратить разрушение зубов.И, конечно же, фторуглероды, такие как тефлон, оказали большое влияние на жизнь в 20 веке. Есть много применений фтора:
- Ракетное топливо
- Производство полимеров и пластиков
- производство тефлона и тефзеля
- В сочетании с кислородом используется в качестве холодильника
- Плавиковая кислота для травления стекла
- Очистить коммунальное водоснабжение
- Добыча урана
- Кондиционер
Источники
Фтор может быть найден в природе или произведен в лаборатории.Чтобы сделать это в лаборатории, такие соединения, как фторид калия, подвергают электролизу с плавиковой кислотой для создания чистого фтора и других соединений. Это может быть выполнено с различными соединениями, обычно ионными с участием фтора и металла. Фтор также можно найти в природе в различных минералах и соединениях. Два основных соединения, в которых он содержится, – это плавиковый шпат (\ (CaF_2 \)) и криолит (\ (Na_3AlF_6 \)).
Список литературы
- Ньют, Г. С. Неорганическая химия .Лонгманс, Грин и Ко: Нью-Йорк, 1903.
- Латимер, Венделл М., Хильдебранд, Джоэл Х. Справочник по неорганической химии . Компания Macmillan: Нью-Йорк, 1938.
Проблемы
(выделите для просмотра ответов)
1. В. Какова электронная конфигурация фтора? из F – ?
А. 1с 2 2с 2 2п 5
1 с 2 2 с 2 2 с 6
2.В. Обычно фтор окисляется или восстанавливается? объяснять.
A. Фтор обычно восстанавливается, потому что он принимает электрон от других элементов, поскольку он настолько электроотрицателен.
3. В. Каковы некоторые распространенные применения фтора?
A. Зубная паста, пластмассы, ракетное топливо, травление стекла и т. Д.
4. В. Образует ли фтор соединения с неметаллами? если да, то приведите два примера, один из которых относится к оксиду.
A. OF 2 , ClF
5.В. В какой группе находится фтор? (укажите название группы и номер)
А. 17, галогены
Авторы и авторство
- Рэйчел Фельдман (Калифорнийский университет в Дэвисе)
Стивен Р. Марсден
Фтор – Key Stage Wiki
Ключевой этап 2
Значение
Фтор – газ желтого цвета.
Ключевой этап 3
Значение
Фтор – это элемент 7 группы Периодической таблицы с атомным номером 9.
О фторе
Молекулярная структура
- Фтор имеет химическую формулу F 2 .
Атомная структура
- Фтор в виде 9 протонов и 10 нейтронов в ядре, что дает ему атомный номер 9 и атомную массу 19.
- У атома фтора отсутствует один электрон в полной внешней оболочке.
Недвижимость
- Фтор – неметаллический элемент.
- Фтор – самый реактивный галоген.
- Фтор сильно реагирует с водородом с образованием фтористого водорода, который растворяется в воде с образованием плавиковой кислоты.
- Фтор – сильное отбеливающее средство.
- Фтор убивает бактерии.
- Фтор представляет собой газ желтого цвета при комнатной температуре.
Ключевой этап 4
Значение
Фтор – это элемент 7-й группы Периодической таблицы с 9 протонами в ядре.
О фторе
Молекулярная структура
- Фтор имеет химическую формулу F 2 .
- Атомы фтора соединяются ковалентной связью.
Атомная структура
- Самый стабильный изотоп фтора имеет в своем ядре 10 нейтронов, что дает ему атомную массу 19.
- У атома фтора отсутствует один электрон в полной внешней оболочке.
- Ионы фторида получают 1 электрон, чтобы получить полную внешнюю оболочку, и становятся отрицательно заряженными.
| Диаграмма, показывающая образование иона фторида . |
Недвижимость
- Фтор – неметаллический элемент.
- Фтор – самый реактивный галоген.
- Фтор сильно реагирует с водородом с образованием фтористого водорода, который растворяется в воде с образованием плавиковой кислоты.
- Фтор – сильное отбеливающее средство.
- Фтор убивает бактерии.
- Фтор – газ желтого цвета при стандартной температуре и давлении.
Тест на фтор
- Соберите газ в пробирку.
- Поместите кусочек лакмусовой бумаги на горлышко пробирки.
- Если лакмусовая бумага обесцвечивается, это означает, что это фтор или хлор.
Список литературы
AQA
- Фтор, стр. 61, GCSE Chemistry, CGP, AQA
- Фтор, стр. 61, Объединенная научная трилогия GCSE; Химия, CGP, AQA
- Фтор, страницы 26, 44-5, 61, GCSE Chemistry; Student Book, Collins, AQA
Ковалентные связи
Каждая из трех линий представляет собой общую пару электронов в ковалентной связи.Когда линии используются для представления связывающих пар электронов, структуру часто называют структурной формулой . Некоторые учебники для простоты опускают несвязывающие электроны.
Поскольку атом водорода имеет свою единственную 1 s орбиталь, завершенную только двумя электронами, молекула хлористого водорода нарисована, как показано на рисунке 7.
Рисунок 7. Молекула хлористого водорода.
Каждый из атомов водорода и хлора отдает по одному электрону ковалентной связи.В молекуле водород завершил свою валентную оболочку двумя электронами, а хлор имеет полную оболочку с восемью валентными электронами.
В некоторых молекулах связанные атомы имеют более двух общих электронов, как в этилене (C 2 H 4 ), где два атома углерода имеют четыре общих электрона. (См. Рисунок 8.)
Рис. 8. Двойная связь между двумя атомами углерода.
Обратите внимание, что каждый углерод получает восемь электронов в результате этого обмена. Поскольку каждая общая пара представляет собой одинарную ковалентную связь, две общие пары называются двойной связью .Структура на правой стороне рисунка 8 показывает эту двойную связь четырех общих электронов двумя линиями, а левая часть рисунка
показывает двойную связь в виде двух пар точек.Есть даже тройные связи шести общих электронов, как в молекуле азота. В N 2 каждый атом азота вносит пять валентных электронов. Из 10 электронов, показанных на рисунке 9, четыре не связывают, а шесть составляют тройную связь, удерживающую атомы азота вместе.
Рисунок 9.Тройная связь между двумя атомами азота.
- Посмотрите на таблицу Менделеева и определите количество валентных электронов алюминия и кислорода по положению столбцов этих двух элементов.
- Нарисуйте диаграмму Льюиса, представляющую электронную конфигурацию молекулы сероводорода, H 2 S.
фтор | Использование, свойства и факты
фтор (F) , наиболее реактивный химический элемент и самый легкий член галогеновых элементов, или Группа 17 (Группа VIIa) периодической таблицы.Его химическая активность может быть объяснена его исключительной способностью притягивать электроны (это наиболее электроотрицательный элемент) и небольшим размером его атомов.
| атомный номер | 9 |
|---|---|
| атомный вес | 18.998403163 |
| точка плавления | −219.62 ° C (−363.326325 ° F) 188 ° C (-306 ° F) |
| плотность (1 атм, 0 ° C или 32 ° F) | 1.696 г / литр (0,226 унции / галлон) |
| степени окисления | −1 |
| электронная конфигурация. | 1 s 2 2 s 2 2 p 5 |
История
Фторсодержащий минерал плавиковый шпат (или флюорит) был описан в 1529 году немецким врачом и минералог Георгий Агрикола. Похоже, что сырая плавиковая кислота была впервые получена неизвестным английским стекольником в 1720 году.В 1771 году шведский химик Карл Вильгельм Шееле получил фтористоводородную кислоту в нечистом состоянии путем нагревания плавикового шпата с концентрированной серной кислотой в стеклянной реторте, которая сильно подверглась коррозии продуктом; В результате в последующих экспериментах с веществом были использованы сосуды из металла. Почти безводная кислота была получена в 1809 году, а два года спустя французский физик Андре-Мари Ампер предположил, что это соединение водорода с неизвестным элементом, аналогичным хлору, для чего он предложил название фтор.Плавиковый шпат затем был признан фторидом кальция.
Британская викторина
118 Названия и символы из таблицы Менделеева
Периодическая таблица Менделеева состоит из 118 элементов. Насколько хорошо вы знаете их символы? В этой викторине вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них.
Выделение фтора долгое время было одной из главных нерешенных проблем неорганической химии, и только в 1886 году французский химик Анри Муассан получил этот элемент путем электролиза раствора фтороводорода калия во фтористом водороде. Он получил Нобелевскую премию по химии 1906 года за выделение фтора. Сложность обращения с элементом и его токсические свойства способствовали медленному прогрессу в химии фтора.Действительно, до Второй мировой войны этот элемент казался лабораторным диковинным предметом. Однако затем использование гексафторида урана для разделения изотопов урана, наряду с разработкой органических фторсодержащих соединений, имеющих промышленное значение, сделало фтор значительным промышленным химическим веществом.
Возникновение и распространение
Фторсодержащий минерал плавиковый шпат (флюорит, CaF 2 ) веками использовался в качестве флюса (очищающего агента) в различных металлургических процессах.Название плавиковый шпат происходит от латинского fluere , «течь». Впоследствии выяснилось, что минерал является источником элемента, который получил название фтор. Бесцветные прозрачные кристаллы плавикового шпата при освещении приобретают голубоватый оттенок, и это свойство, соответственно, известно как флуоресценция.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчасФтор встречается в природе только в форме своих химических соединений, за исключением следовых количеств свободного элемента в плавиковом шпате, который подвергся облучению радием.Не редкий элемент, он составляет около 0,065 процента земной коры. Основными фторсодержащими минералами являются (1) плавиковый шпат, месторождения которого находятся в Иллинойсе, Кентукки, Дербишире, на юге Германии, на юге Франции и в России и являются основным источником фтора, (2) криолит (Na 3 AlF 6 ), главным образом из Гренландии, (3) фторапатит (Ca 5 [PO 4 ] 3 [F, Cl]), широко распространенный и содержащий различные количества фтора и хлора, (4) топаз ( Al 2 SiO 4 [F, OH] 2 ), драгоценный камень и (5) лепидолит, слюда, а также компонент костей и зубов животных.
Физические и химические свойства
При комнатной температуре фтор представляет собой газ светло-желтого цвета с раздражающим запахом. Вдыхание газа опасно. При охлаждении фтор превращается в жидкость желтого цвета. Есть только один стабильный изотоп элемента – фтор-19.
Поскольку фтор является наиболее электроотрицательным из элементов, атомные группы, богатые фтором, часто имеют отрицательный заряд. Метилиодид (CH 3 I) и трифториодметан (CF 3 I) имеют разные распределения заряда, как показано в следующих формулах, в которых греческий символ δ указывает на частичный заряд:
Первая энергия ионизации фтора очень высока (402 килокалорий на моль), что дает стандартное тепловыделение для катиона F + 420 килокалорий на моль.
Небольшой размер атома фтора позволяет упаковать относительно большое количество атомов или ионов фтора вокруг данного координационного центра (центрального атома), где он образует множество стабильных комплексов, например, гексафторсиликат (SiF 6 ) 2− и гексафторалюминат (AlF 6 ) 3−. Фтор – наиболее сильно окисляющий элемент. Следовательно, никакое другое вещество не способно окислять фторид-анион до свободного элемента, и по этой причине элемент не находится в свободном состоянии в природе.За более чем 150 лет все химические методы не смогли произвести элемент, успех был достигнут только с помощью электролитических методов. Однако в 1986 году американский химик Карл О. Кристе сообщил о первом химическом получении фтора, где «химическое получение» означает метод, в котором не используются такие методы, как электролиз, фотолиз и разрядка, или сам фтор используется в синтезе любого из химических веществ. исходные материалы. Он использовал K 2 MnF 6 и пентафторид сурьмы (SbF 5 ), оба из которых могут быть легко получены из растворов HF.
Высокая окислительная способность фтора позволяет элементу производить наивысшие степени окисления, возможные в других элементах, и известно множество фторидов элементов с высокой степенью окисления, для которых нет других соответствующих галогенидов, например дифторид серебра (AgF 2 ), трифторид кобальта (CoF 3 ), гептафторид рения (ReF 7 ), пентафторид брома (BrF 5 ) и гептафторид йода (IF 7 ).
Фтор (F 2 ), состоящий из двух атомов фтора, соединяется со всеми другими элементами, кроме гелия и неона, с образованием ионных или ковалентных фторидов.Некоторые металлы, такие как никель, быстро покрываются фторидным слоем, который предотвращает дальнейшее разрушение металла элементом. Некоторые сухие металлы, такие как низкоуглеродистая сталь, медь, алюминий или монель (66 процентов никеля, 31,5 процента медного сплава), не подвергаются воздействию фтора при обычных температурах. Для работы с фтором при температуре до 600 ° C (1100 ° F) подходит монель; спеченный оксид алюминия устойчив до 700 ° C (1300 ° F). Когда требуются смазочные материалы, наиболее подходят фторуглеродные масла.Фтор бурно реагирует с органическими веществами (такими как резина, дерево и ткань), и контролируемое фторирование органических соединений под действием элементарного фтора возможно только при соблюдении особых мер предосторожности.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
4.6 Электронная конфигурация | Атом
4.6 Электронная конфигурация (ESABE)
Энергия электронов (ЭСАБФ)
Все электроны атома имеют одинаковый заряд и одинаковую массу, но каждый электрон имеет разное количество. энергия .Электроны с наименьшей энергией находятся ближе всего к ядру (где сила притяжения положительно заряженного ядра наибольшая) и электроны, у которых выше энергии (и способны преодолеть силу притяжения ядра) находятся дальше.
Электронная система (ESABG)
Мы начнем с очень простого представления о расположении или конфигурации электронов вокруг атома. Этот Представление просто утверждает, что электроны расположены на энергетических уровнях (или оболочках) вокруг ядра атома.Эти уровни энергии пронумерованы 1, 2, 3 и т. д. Электроны, которые находятся на первом уровне энергии (уровень энергии 1), являются ближе всего к ядру и будет иметь самую низкую энергию. Электроны, находящиеся дальше от ядра, будут иметь высшая энергия.
В следующих примерах уровни энергии показаны в виде концентрических кругов вокруг центрального ядра. В Для этих диаграмм важно знать, что первый энергетический уровень может содержать 2 электрона, второй энергетический уровень может содержать 8 электронов, а третий энергетический уровень может содержать 8 электронов.
Литий
Литий (\ (\ text {Li} \)) имеет атомный номер 3, что означает, что в нейтральном атоме количество электронов также будет 3. Первые два электрона находятся на первом уровне энергии, а третий электрон находится на находится на втором энергетическом уровне (рис. 4.7).
Рисунок 4.7: Электронное устройство атома лития.
Фтор
Фтор (\ (\ text {F} \)) имеет атомный номер 9, что означает, что нейтральный атом также имеет 9 электронов.В первые 2 электрона находятся на первом уровне энергии, а остальные 7 – на втором уровне энергии. уровень (рисунок 4.8).
Рисунок 4.8: Электронное расположение атома фтора.
Неон
Неон (\ (\ text {Ne} \)) имеет атомный номер 10, что означает, что нейтральный атом также имеет 10 электронов. В первые 2 электрона находятся на первом энергетическом уровне, а последние 8 – на втором энергетическом уровне.(Рисунок 4.9).
Рис. 4.9: Электронное устройство атома неона.
Но ситуация несколько сложнее. В пределах каждого энергетического уровня электроны движутся в орбиталей . Орбиталь определяет пространства или области, в которых движутся электроны.
- Атомная орбиталь
Атомная орбиталь – это область, в которой электрон может находиться вокруг отдельного атома.
Первый энергетический уровень содержит только одну s-орбиталь, второй энергетический уровень содержит одну s-орбиталь и три p-орбитали. орбитали, а третий энергетический уровень содержит одну s-орбиталь и три p-орбитали (а также пять d-орбиталей). В пределах каждого энергетического уровня s-орбиталь имеет более низкую энергию, чем p-орбитали. Это расположение показано на Рисунок 4.10.
Рисунок 4.10: Положение первых десяти орбиталей атома на энергетической диаграмме.
Каждый блок на рисунке 4.10 может удерживать два электрона. Это означает, что s-орбиталь может содержать два электрона, а p-орбиталь может содержать в общей сложности шесть электронов, по два в каждом из трех блоков.
Эта диаграмма также помогает нам, когда мы разрабатываем электронную конфигурацию элемента. Электрон Конфигурация элемента – это расположение электронов в оболочках и подоболочках. Есть несколько рекомендации по разработке электронной конфигурации.Это:
Каждая орбиталь может содержать только двух электронов . Электроны, которые встречаются вместе на орбитали, являются назвал электронную пару .
Электрон всегда будет пытаться войти на орбиталь с наименьшей возможной энергией.
Электрон будет занимать орбиталь самостоятельно, а не делить орбиталь с другим электроном.An электрон также предпочел бы занять более низкую энергетическую орбиталь с другим электроном, прежде чем занять орбиталь с более высокой энергией. Другими словами, в пределах одного энергетического уровня электроны заполнят s-орбиталь до того, как начинает заполнять p-орбитали.
Подоболочка может содержать 2 электрона
Подоболочка p может содержать 6 электронов
Способ, которым электроны расположены в атоме, называется его электронной конфигурацией .
Когда на орбитали два электрона, они называются электронной парой . Если орбиталь имеет только один электрон, этот электрон называется неспаренным электроном . Электрон пары показаны стрелками, указывающими в противоположных направлениях.
- Электронная конфигурация
Электронная конфигурация – это расположение электронов в атоме, молекуле или другой физической структуре.
Диаграммы Aufbau (ESABH)
Электронная конфигурация элемента может быть представлена с помощью диаграмм Ауфбау или уровня энергии диаграммы. На диаграмме Ауфбау для обозначения электронов используются стрелки. Вы можете использовать следующие шаги, чтобы помочь вам нарисуйте диаграмму Ауфбау:
Определите количество электронов в атоме.
Заполните s-орбиталь на первом уровне энергии (1s-орбиталь) первыми двумя электронами.
Заполните s-орбиталь второго энергетического уровня (2s-орбиталь) двумя вторыми электронами.
Поместите по одному электрону в каждую из трех p-орбиталей второго энергетического уровня (2p-орбитали), а затем, если есть еще электроны, вернитесь и поместите второй электрон на каждую из 2p-орбиталей, чтобы заполните электронные пары.
Продолжайте таким образом через каждый из последовательных уровней энергии, пока не будут втянуты все электроны.
Вы можете думать о диаграммах Ауфбау как о людях, садящихся в автобус или поезд. Сначала люди сядут на пустых местах с пустыми местами между ними и другими людьми (если они не знают людей, а затем они сяду рядом с ними). Это самая низкая энергия. Когда все места так заполнены, больше людей, которые получить будет вынужден сесть рядом с кем-то. Это выше по энергии. По мере того, как автобус или поезд заполняется еще больше, люди должны стоять, чтобы соответствовать.Это высшая энергия.
Aufbau в переводе с немецкого означает «строить». Ученые использовали этот термин, поскольку именно он мы делаем, когда мы разрабатываем электронную конфигурацию, мы строим структуру атомов.
Правило Хунда и принцип Паули
Иногда люди ссылаются на правило Хунда для электронной конфигурации. Это правило просто говорит, что электроны будут скорее быть в подоболочке самостоятельно, чем совместно использовать подоболочку.Вот почему при заполнении подоболочек вы поместите один электрон в каждую подоболочку, а затем вернитесь и заполните подоболочку, прежде чем перейти к следующей энергии уровень. {2} \).{6} \). Диаграмма Ауфбау:
Когда мы рисуем орбитали, мы рисуем фигуру с границей (т.е. замкнутую фигуру). Это представляет собой расстояние от ядра, в котором мы \ (\ text {95} \% \) уверены, что найдем электроны. В реальности электроны атома можно было найти на любом расстоянии от ядра.
Орбитальные формы (ESABJ)
Каждая из орбиталей имеет различную форму.Орбитали s сферические, а орбитали p – гантели. сформированный.
Рисунок 4.13: Орбитальные формы. Слева направо: s-орбиталь, p-орбиталь, три p-орбитали
.Остовные и валентные электроны (ЭСАБК)
электронов на внешнем энергетическом уровне атома называются валентными электронами . Электроны которые находятся в энергетических оболочках ближе к ядру, называются остовными электронами . Основные электроны все электроны в атоме, за исключением валентных электронов.Элемент, имеющий валентный уровень энергии. полный – более стабильный и реже реагируют , чем другие элементы с валентным уровнем энергии это не полно.
- Валентные электроны
Электроны на внешнем энергетическом уровне атома.
- Электроны ядра
Все электроны в атоме, кроме валентных электронов.
Остовные и валентные электроны
Учебное упражнение 4.4Заполните следующую таблицу:
Элемент или ион | Электронная конфигурация | Электроны ядра | Валентные электроны |
Калий (\ (\ text {K} \)) | |||
Гелий (\ (\ text {He} \)) | |||
Ион кислорода (\ (\ text {O} ^ {2 -} \)) | |||
Ион магния (\ (\ text {Mg} ^ {2 +} \)) |
Решение пока недоступно
Важность понимания электронной конфигурации (ESABL)
На этом этапе у вас может возникнуть вопрос, почему для вас важно понимать, как устроены электроны. вокруг ядра атома.Помните, что во время химических реакций, когда атомы вступают в контакт с одним во-вторых, это электронов и этих атомов, которые будут взаимодействовать первыми. В частности, это валентных электронов атомов, которые будут определять, как они реагируют друг с другом.
Чтобы продвинуться дальше, атом наиболее стабилен (и, следовательно, нереактивен ), когда все его орбитали заполнены. С другой стороны, атом наименее стабилен (и, следовательно, больше всего реактивен ), когда его орбитали валентных электронов не полны.Это станет более понятным, если мы продолжим рассмотрение химической связи в более поздняя глава. Проще говоря, валентные электроны в значительной степени ответственны за химический состав элемента. поведение и элементы, которые имеют одинаковое количество валентных электронов, часто имеют схожие химические свойства.
Самые стабильные конфигурации – это те, которые имеют полный уровень энергии. Эти конфигурации встречаются в благородные газы. Благородные газы – очень стабильные элементы, которые не реагируют легко (если вообще не реагируют) с какими-либо другими. элементы.Это связано с полным уровнем энергии. Все элементы стремятся достичь наиболее стабильного электрона. конфигурации, т.е. все элементы хотят быть благородными газами. Этот принцип устойчивости иногда называют как правило октета. Октет – это набор из 8, а количество электронов на полном уровне энергии равно 8.
Испытания на пламя
Цель
Чтобы определить, какого цвета катион металла вызывает пламя.
Аппарат
Стекло для часов
Горелка Бунзена
метанол
зубочистки (или палочки для шампуров)
солей металлов (например,грамм. \ (\ text {NaCl} \), \ (\ text {CuCl} _ {2} \), \ (\ text {CaCl} _ {2} \), \ (\ text {KCl} \) и т. д. )
металлические порошки (например, медь, магний, цинк, железо и т. Д.)
Будьте осторожны при работе с горелками Бунзена, так как вы можете легко обжечься. Убедитесь, что все шарфы / свободные одежда надежно заправлена, а длинные волосы собраны назад. Убедитесь, что вы работаете в хорошо вентилируемом помещении. и что рядом с открытым пламенем нет ничего легковоспламеняющегося.
Метод
Для каждой соли или порошка выполните следующие действия:
Окуните чистый зубочиститель в метанол
Окуните зубочистку в соль или порошок
Проведите зубочисткой сквозь пламя горелки Бунзена. Не держи зубочистку в пламени, а лучше махайте им взад и вперед через пламя.
Посмотрите, что происходит
Результаты
Запишите результаты в таблицу, указав соль металла и цвет пламени.
Заключение
Вы должны были заметить разные цвета для каждой из солей металлов и порошков, которые вы тестировали.
Вышеупомянутый эксперимент по испытанию пламени относится к линейчатым спектрам излучения металлов.Эти линии излучения спектры являются прямым результатом расположения электронов в металлах. Каждая металлическая соль имеет уникальный цвет. пламя.
Энергетические диаграммы и электроны
Учебное упражнение 4.5Нарисуйте диаграммы Ауфбау, чтобы показать электронную конфигурацию каждого из следующих элементов:
- магний
- калий
- сера
- неон
- азот
Используя правила рисования диаграмм Ауфбау, получаем следующее.
Магний имеет 12 электронов. Итак, мы начинаем с энергетического уровня 1 и помещаем в него 2 электрона. Затем мы переезжаем к энергетическому уровню два, который имеет 2s и 2p орбитали. Этот уровень может содержать 8 электронов. Сложения общее количество используемых электронов дает 10 электронов. Итак, мы должны разместить еще два электрона, и они уйдут. на третий уровень.
Калий имеет 19 электронов.Получаем:
Сера имеет 14 электронов, поэтому мы получаем:
Неон имеет 10 электронов, поэтому получаем:
Азот имеет 7 электронов, поэтому мы получаем:
Используйте нарисованные вами диаграммы Aufbau, чтобы заполнить следующую таблицу:
| Элемент | №уровней энергии с электронами | Кол-во электронов | Кол-во валентных электронов | Электронная конфигурация (стандартное обозначение) |
| \ (\ text {Mg} \) | ||||
| \ (\ text {K} \) | ||||
| \ (\ text {S} \) | ||||
| \ (\ text {Ne} \) | ||||
| \ (\ text {N} \) |
Уровни энергии указаны цифрами над полями, поэтому 1, 2, 3 и т.

 Виновник: плавиковая кислота (в просторечии известная как HF), и несчастный человек был не первой ее жертвой.
Виновник: плавиковая кислота (в просторечии известная как HF), и несчастный человек был не первой ее жертвой. Эти отважные ученые боролись за то, чтобы первыми выделить элементарный фтор (F 2 ) из его различных соединений с помощью электролиза.Однако в 1886 году это удалось соотечественнику Никлеса, Анри Муассану. Чтобы добиться этого, Муассану пришлось бороться не только с HF – предпочтительным электролитом в таких экспериментах, но и с самим фтором, очень реактивным газом. Его ключевым нововведением было создание устройства из платины, одного из немногих металлов, способных противостоять атакам, при охлаждении электролитического раствора до -50 ° C для ограничения коррозии. Подвиг Муассана принес ему Нобелевскую премию по химии 1906 года, но празднование длилось недолго.Еще одна жертва токсического действия фтора, он умер всего два месяца спустя. Тем не менее, метод Муассана выжил и используется сегодня для производства многотонных количеств фтора из руды плавикового шпата.
Эти отважные ученые боролись за то, чтобы первыми выделить элементарный фтор (F 2 ) из его различных соединений с помощью электролиза.Однако в 1886 году это удалось соотечественнику Никлеса, Анри Муассану. Чтобы добиться этого, Муассану пришлось бороться не только с HF – предпочтительным электролитом в таких экспериментах, но и с самим фтором, очень реактивным газом. Его ключевым нововведением было создание устройства из платины, одного из немногих металлов, способных противостоять атакам, при охлаждении электролитического раствора до -50 ° C для ограничения коррозии. Подвиг Муассана принес ему Нобелевскую премию по химии 1906 года, но празднование длилось недолго.Еще одна жертва токсического действия фтора, он умер всего два месяца спустя. Тем не менее, метод Муассана выжил и используется сегодня для производства многотонных количеств фтора из руды плавикового шпата.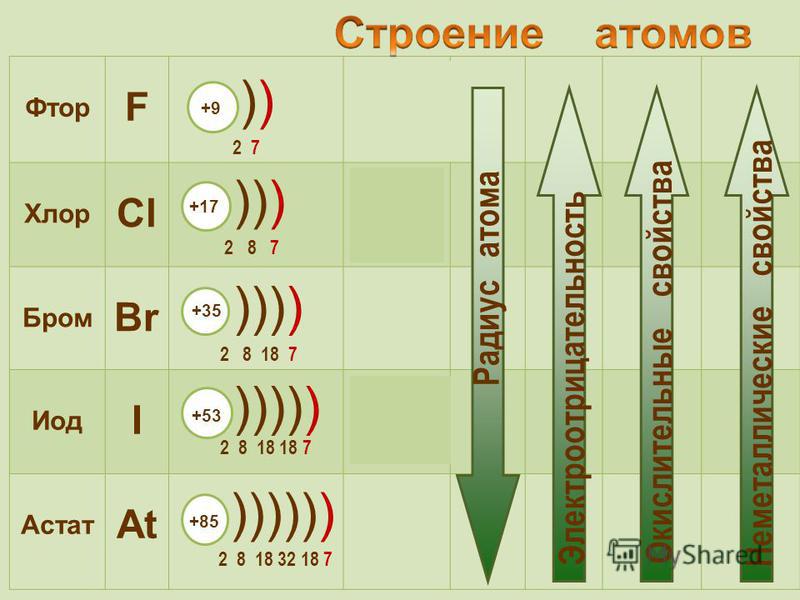 Самый продаваемый антидепрессант Прозак, препарат для снижения уровня холестерина Lipitor и антибактериальный препарат Ципро – все они имеют фтор, которым следует благодарить за свой успех. Как это возможно? Потому что обратной стороной чрезвычайной реакционной способности фтора является прочность связей, которые он образует с другими атомами, особенно с углеродом.Это свойство делает фторорганические соединения одними из самых стабильных и инертных веществ, известных человеку. Особый статус фтора также проистекает из «фторного фактора», способности этого маленького атома точно настраивать химические свойства всей молекулы. Например, замена водорода фтором может защитить лекарства от разложения метаболическими ферментами, увеличивая время их активного существования в организме. Или же введенный фтор может изменить форму молекулы, чтобы она лучше связывалась с целевым белком.Такие точные химические манипуляции теперь можно проводить в фармацевтических лабораториях с использованием множества безопасных, имеющихся в продаже фторирующих агентов, или же сложные преобразования можно просто поручить кому-то другому.
Самый продаваемый антидепрессант Прозак, препарат для снижения уровня холестерина Lipitor и антибактериальный препарат Ципро – все они имеют фтор, которым следует благодарить за свой успех. Как это возможно? Потому что обратной стороной чрезвычайной реакционной способности фтора является прочность связей, которые он образует с другими атомами, особенно с углеродом.Это свойство делает фторорганические соединения одними из самых стабильных и инертных веществ, известных человеку. Особый статус фтора также проистекает из «фторного фактора», способности этого маленького атома точно настраивать химические свойства всей молекулы. Например, замена водорода фтором может защитить лекарства от разложения метаболическими ферментами, увеличивая время их активного существования в организме. Или же введенный фтор может изменить форму молекулы, чтобы она лучше связывалась с целевым белком.Такие точные химические манипуляции теперь можно проводить в фармацевтических лабораториях с использованием множества безопасных, имеющихся в продаже фторирующих агентов, или же сложные преобразования можно просто поручить кому-то другому.