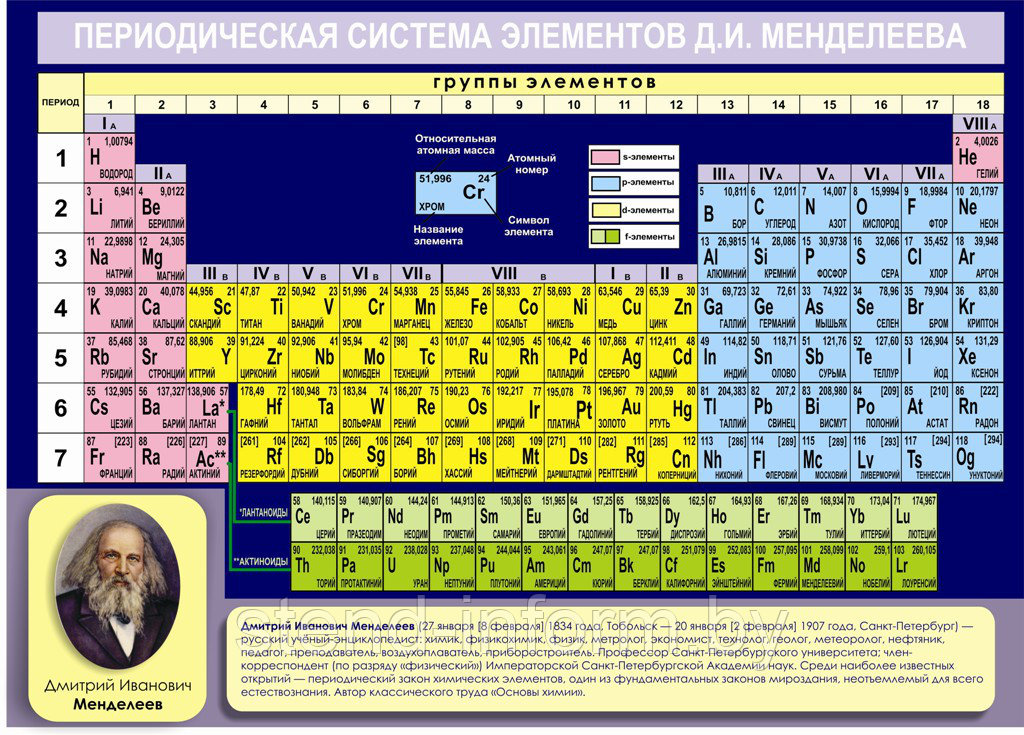
Структура Периодической системы химических элементов. Объяснительная и предсказательная функции Периодического закона 9
Характеристика разных форм таблицы
В начале XX века было открыто строение атома и стало ясно, что свойства химических элементов находятся в периодической зависимости не от атомных масс, а от заряда ядра атома, т. е. числа протонов в ядре.
Рис. 1. “Длинная” форма таблицы
Дальнейшее развитие Периодической системы заключалось в том, что ученые заполняли пустые клетки в таблице Менделеева: открыли семейство благородных газов. Открывались естественно и искусственно полученные радиоактивные элементы. В 2010 году был открыт последний 117 химический элемент, 7 периода Периодической системы.
Таким образом, перед учеными встал вопрос о нижней границе Периодической системы, который остается открытым до сих пор.
Чаще всего можно увидеть три формы выражения Периодической системы: короткая или короткопериодная, длинная или длиннопериодная или сверхдлинная.
В короткой форме таблица изображена на рис. 2.
1-3 периоды занимают по 1 строке, 4-ый и последующие периоды занимают по 2 строчки. Символы элементов главных и побочных подгрупп выравниваются относительно разных краев клеток. Лантаноиды и актиноиды вынесены из общей таблицы.
В длинном варианте лантаноиды и актиноиды вынесены из общей таблицы, соответственно, так же как и в короткой, делая её более компактной. Нет главных и побочных подгрупп. Каждый период занимает ровно одну строчку (рис. 1).
Короткая форма Периодической системы
| Рис. 2. “Короткая форма” | Рис. 3. Клеточка таблицы |
Каждая клеточка Периодической системы содержит символ одного химического элемента, у которого указан порядковый номер и значения относительной атомной массы элемента (рис.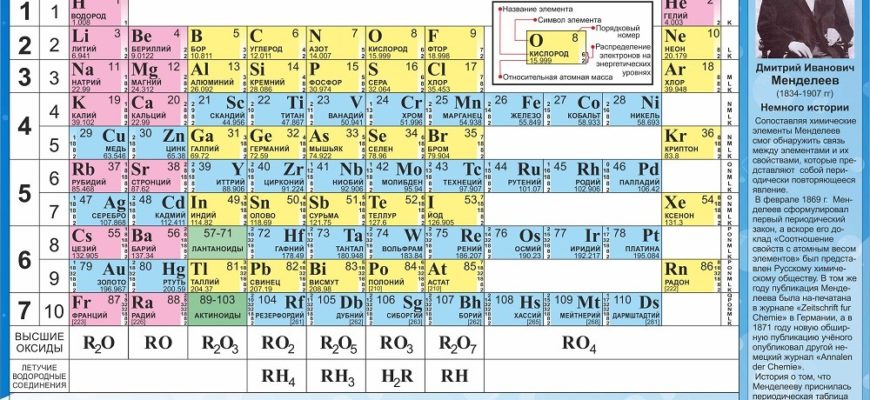 3).
3).
Период начинается щелочным металлом и заканчивается инертным газом.
Всего периодов семь. Исключением является 1-ый период. В его состав входит только 2 химических элемента: водород, который не считается щелочным металлом, и гелий.
1-ый, 2-ой, 3-ий периоды называются малыми. Они содержат 2 и 8 химических элементов и состоят из одного ряда.
Совокупность переходных металлов в каждом периоде называется вставной декадой, потому что этих металлов в каждом периоде 10.
Рис. 4. Вторая группа
Группой называется вертикальный ряд химических элементов.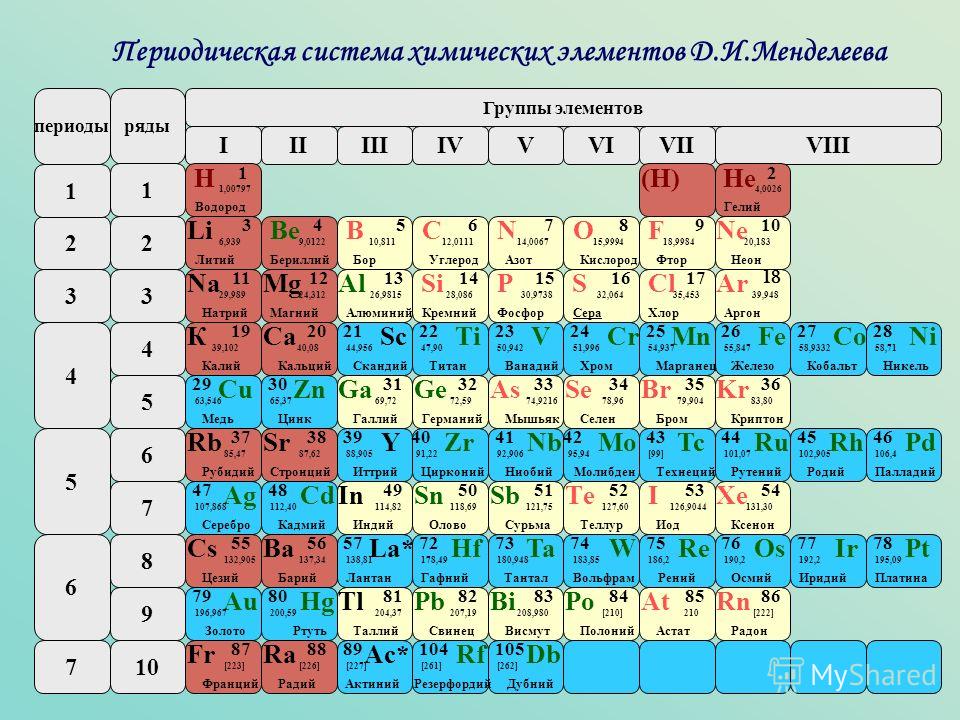
Группы в короткой форме таблицы делятся на главную «А» и побочную «Б» подгруппы.
В каждой главной подгруппе с ростом порядкового номера элемента химические свойства меняются от неметаллических на металлические.
В побочную подгруппу включаются только металлы, называемые переходными элементами.
Если подгруппа начинается элементами малого периода – это главная подгруппа. Подгруппа, которая начинается элементами большого периода, – это побочная подгруппа. Например, рассмотрим II группу периодической системы (рис. 4).
Бериллий Be – элемент 2-го периода.
Цинк Zn начинает побочную подгруппу, так как он входит в состав 4-го периода. В побочную подгруппу входит Zn, Cd, Hg.
Характеристика химического элемента по положению в таблице
Рис.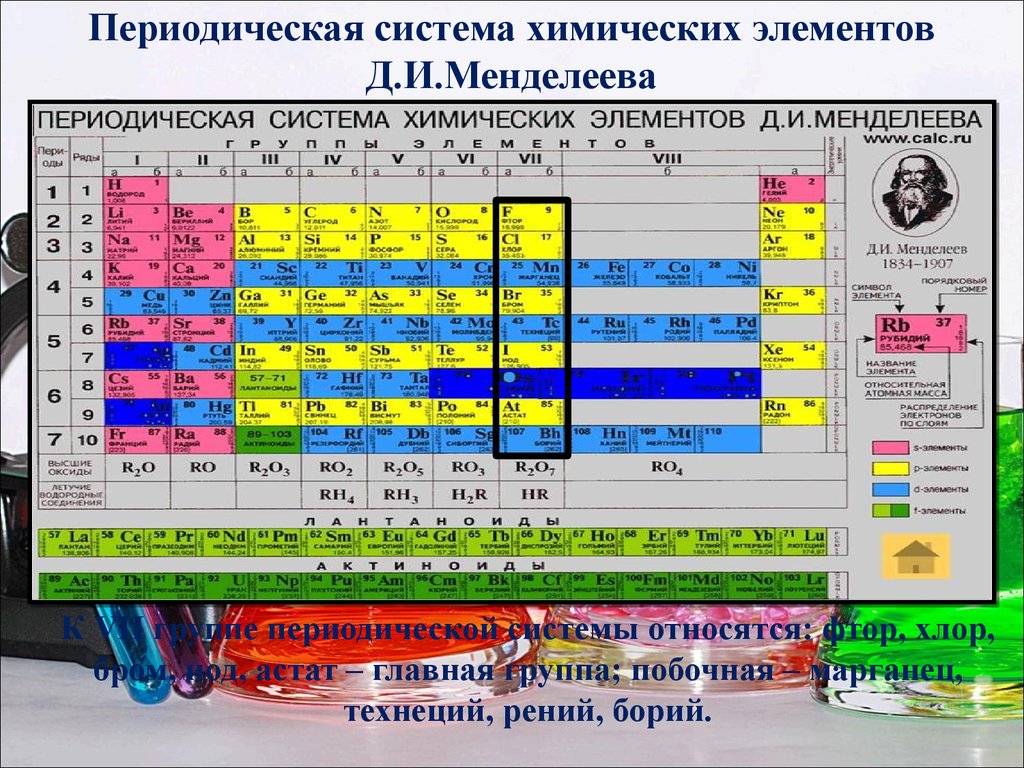 5. Химический элемент бром
5. Химический элемент бром
Рассмотрим элемент Br (рис. 5). Его порядковый номер – 35, относительная атомная масса – 80. Находится в 4-ом периоде, в 7-ой главной подгруппе.
Рис. 6. Химический элемент платина
Рассмотрим элемент платину (рис. 6).
Символ – Pt, порядковый номер – 78, относительная атомная масса – 195. Находится в 6-м периоде, в 8-й побочной подгруппе.
В состав каждой группы входит элементы с одинаковым числом валентных электронов. Следовательно, они будут обладать схожими химическими свойствами.
Названия некоторых групп элементов
Это отражается в названии некоторых групп элементов.
- Например, элементы главной подгруппы 1-ой группы – Li, Na, K, Rb, Cs, Fr – называются щелочные металлы.
- Элементы главной подгруппы 2-ой группы – Ca, Sr, Ba, Ra – называются щелочноземельные металлы.
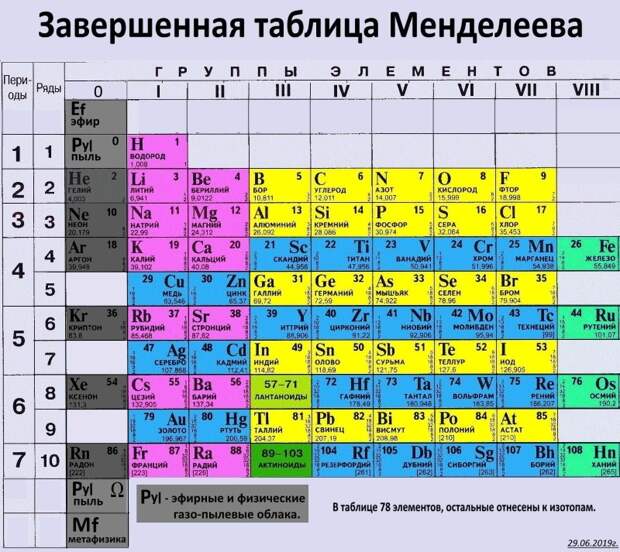
- Галогены: F, Cl, Br, J, At – элементы 7-й группы главной подгруппы.
- 8-ю главную подгруппу называют подгруппой инертных или благородных газов. Это He, Ne, Ar, Kr, Xe, Ra.
Химические свойства в периодах меняются с металлических через амфотерные на неметаллические. Таким образом, зная химические свойства элемента, можно предположить, где конкретно он находится в Периодической системе. И наоборот, если знать положение элемента в Периодической системе, можно предположить его химические свойства.
Значение Периодического закона Д. И. Менделеева
С момента открытия Периодического закона и Периодической системы химических элементов Д. И. Менделеева, химия перестала быть описательной наукой. Теперь при помощи его таблицы можно предсказывать свойства любого химического элемента. Дальнейшее развитие физики и химии полностью подтвердило правоту Д. И. Менделеева, так были открыты семейства инертных газов. Для радиоактивных элементов были сначала описаны свойства, а затем они были получены. Периодический закон и Периодическая система химических элементов Д. И. Менделеева носят фундаментальный характер, являются основным законом природы.
Менделеева, так были открыты семейства инертных газов. Для радиоактивных элементов были сначала описаны свойства, а затем они были получены. Периодический закон и Периодическая система химических элементов Д. И. Менделеева носят фундаментальный характер, являются основным законом природы.
Подведение итога урока
На уроке вы изучили тему «Структура Периодической системы химических элементов. Объяснительная и предсказательная функции Периодического закона». Вы узнали о значении Периодической таблицы Менделеева, ее функциях и возможностях.
Список литературы
- Рудзитис Г. Е. Неорганическая и органическая химия. 8 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – М.: Просвещение. 2011. – 176 с.: ил.
- Попель П. П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П. П. Попель, Л. С. Кривля. – К.: ИЦ «Академия», 2008.

- Габриелян О. С. Химия. 9 класс. Учебник. – Дрофа, 2001. – 224 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Интернет-портал «chemport.ru» (Источник)
- Интернет-портал «Химик» (Источник)
- Интернет-портал «hemi.nsu.ru» (Источник)
Домашнее задание
- №№ 193, 194 (с. 143) Попель П. П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П. П. Попель, Л. С. Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
- Сформулируйте Периодический закон. Чем отличается современная формулировка закона от данной Д. И. Менделеевым?
Структура таблицы «Периодическая система химических элементов Д.И.Менделеева»
Тема: Структура таблицы «Периодическая система химических элементов Д. И. Менделеева» (короткая форма): А- и группы, периоды
Менделеева» (короткая форма): А- и группы, периоды
Задачи урока:
Образовательные – сформировать знания о периодическом законе и периодической системе Д.И.Менделеева. Научить учащихся работать с периодической системой (уметь определять положение элемента в периодической системе, свойства элемента в зависимости от положения его в периодической системе).
Воспитательные – патриотическое воспитание, формирование естественно – научной картины мира, экологическое воспитание, способствование осознанию роли химических знаний в развитии личности, преодоление трудностей.
Развивающие – развивать наблюдательность, память (при изучении физического смысла периодического закона и графического его отображения). Развивать умение сравнивать. Научить учащихся обобщать и делать выводы, анализировать, составлять, систематизировать.
Содержание материала.
Новая тема. Сегодня мы с Вами продолжаем говорить об атомах хим. элементов, а точнее о расположении определённых видов атомов в ПС и её структуре. Д.И. Менделеев разработал научную классификацию химических элементов – Периодическую систему в форме таблицы. Эту таблицу можно представить в виде дома, где «живут» все химические элементы. Каждому химическому элементу отведена своя «квартира», т.е. клетка с определенным номером.
Сегодня мы с Вами продолжаем говорить об атомах хим. элементов, а точнее о расположении определённых видов атомов в ПС и её структуре. Д.И. Менделеев разработал научную классификацию химических элементов – Периодическую систему в форме таблицы. Эту таблицу можно представить в виде дома, где «живут» все химические элементы. Каждому химическому элементу отведена своя «квартира», т.е. клетка с определенным номером.
Лантаноиды актиноиды расположены под основной таблицей элементов, в них по 14 элементов, похожих по своим свойствам. Одни похожи на лантан и называются, поэтому лантаноиды (лантаниды), другие похожи на актиний и называются актиноиды (актиниды). Обе группы включают в себя металлы. Все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
По вертикали химические элементы тоже «живут» друг под другом. Эти вертикальные ряды называются группами. Группами называют вертикальные ряды в периодической системе.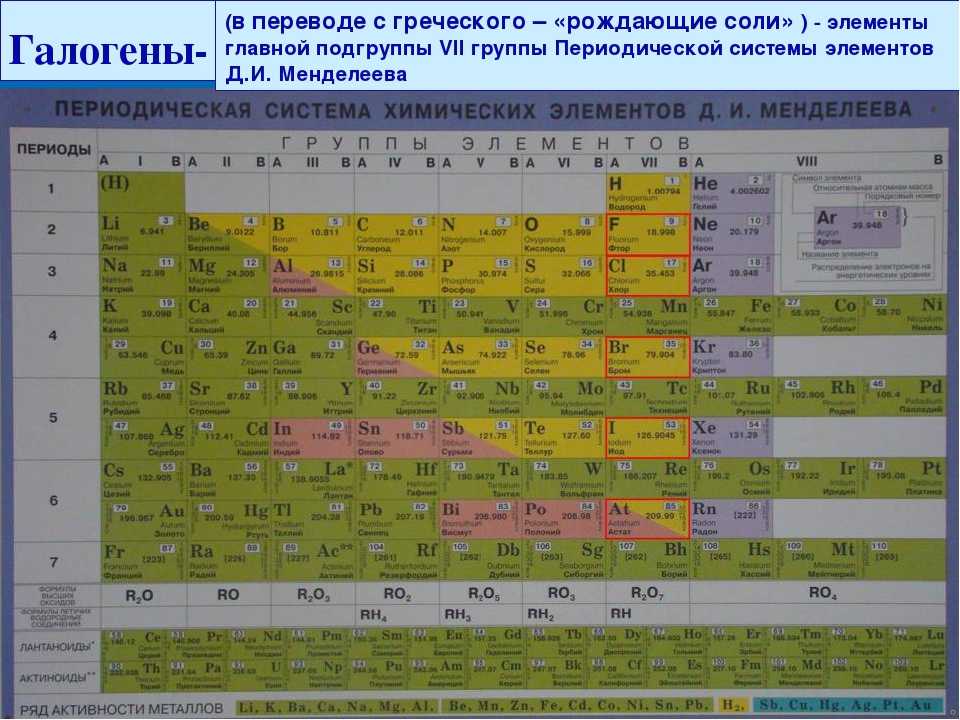 В этих вертикальных группах химические элементы имеют сходные свойства. Этих групп всего 8. Каждая группа состоит из двух подгрупп: главной и побочной. Главную подгруппу еще называют группой А, в нее входят элементы малых и больших периодов. Побочную подгруппу называют еще группой В, в нее входят элементы только больших периодов.
В этих вертикальных группах химические элементы имеют сходные свойства. Этих групп всего 8. Каждая группа состоит из двух подгрупп: главной и побочной. Главную подгруппу еще называют группой А, в нее входят элементы малых и больших периодов. Побочную подгруппу называют еще группой В, в нее входят элементы только больших периодов.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической систем семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Эти периоды называют большими, т.к. здесь много химических элементов, расположенных в два ряда. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.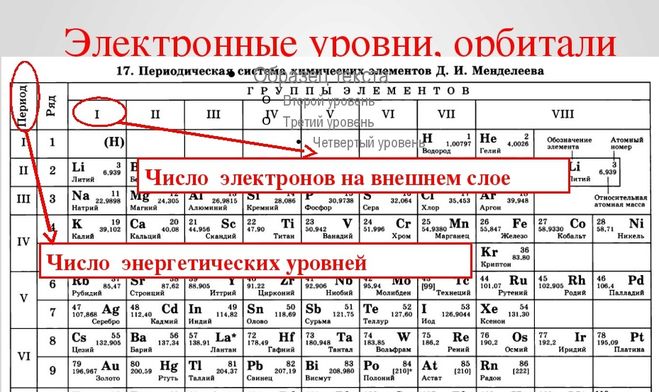
Рассмотрим главную подгруппу I группы, в нее входят Li, Na, K, Rb, Cs, Fr. Это подгруппа лития, ведь литий в ней первый. Побочная подгруппа этой группы образована Cu, Ag, Au, поэтому ее называют подгруппой меди.
Кроме короткопериодной таблицы Д.И. Менделеева, которая у вас в учебнике, есть еще и длиннопериодный вариант (см. рис.)
Всего в таблице 118 химических элементов и подобно тому, как 33 буквы алфавита образует множество слов, так и 118 химических элемента образует множество веществ.
КОРОТКОПЕРИОДНАЯ ТАБЛИЦА
Длиннопериодный вариант таблицы
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру.
2.Закрепление новой темы (выполнить письменно):
Назовите элементы IVA и VI B групп.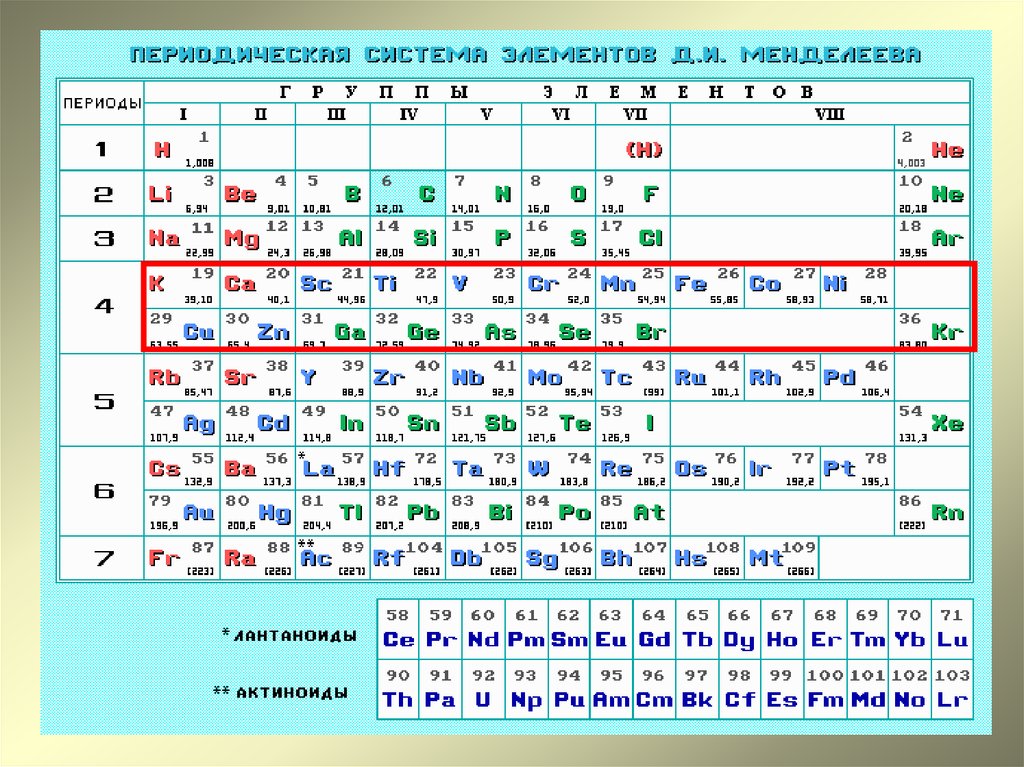
Прямыми линиями выделите ряды, где находятся: элементы одного и того же периода одной линией; элементы одной и той же группы – двумя линиями.
Be, С, N, O, Ne
Be, Mg, Ca, Bа
3.Найдите в каждом ряду один из элементов, который отличается от остальных по положению в периодической системе химических элементов.
а) H, He, Ne, Ar
б) H, Li, Be, B
в) Fe, Co, Ni, Ar
г) F, Cl, Mn, Br
Ответы: а) H; б) H; в) Ar; г) Mn.
4.Выберите группы сходных элементов:
а) Na, Ca, O
б) Ne, Ar, He
в) F, Cl, Br
г) P, В, Li
Ответы: б; в.
3.Задание для самостоятельного изучения (домашнее задание).
Британика
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Этот день в истории
- Викторины
- Подкасты
- Словарь
- Биографии
- Резюме
- Популярные вопросы
- Обзор недели
- Инфографика
- Демистификация
- Списки
- #WTFact
- Товарищи
- Галереи изображений
- Прожектор
- Форум
- Один хороший факт
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Britannica Classics
Посмотрите эти ретро-видео из архивов Encyclopedia Britannica.
- Demystified Videos
В Demystified у Britannica есть все ответы на ваши животрепещущие вопросы. - #WTFact Видео
В #WTFact Britannica делится некоторыми из самых странных фактов, которые мы можем найти. - На этот раз в истории
В этих видеороликах узнайте, что произошло в этом месяце (или любом другом месяце!) в истории. - Britannica объясняет
В этих видеороликах Britannica объясняет различные темы и отвечает на часто задаваемые вопросы.
- Студенческий портал
Britannica — лучший ресурс для учащихся по ключевым школьным предметам, таким как история, государственное управление, литература и т. д. - Портал COVID-19
Хотя этот глобальный кризис в области здравоохранения продолжает развиваться, может быть полезно обратиться к прошлым пандемиям, чтобы лучше понять, как реагировать сегодня. - 100 женщин
Britannica празднует столетие Девятнадцатой поправки, выделяя суфражисток и политиков, творящих историю.
- Britannica Beyond
Мы создали новое место, где вопросы находятся в центре обучения. Вперед, продолжать. Спросить. Мы не будем возражать. - Спасение Земли
Британника представляет список дел Земли на 21 век. Узнайте об основных экологических проблемах, стоящих перед нашей планетой, и о том, что с ними можно сделать! - SpaceNext50
Britannica представляет SpaceNext50. От полёта на Луну до управления космосом — мы исследуем широкий спектр тем, которые подпитывают наше любопытство к космосу!
Страница не найдена
Приносим свои извинения! Этот контент недоступен. Посетите домашнюю страницу Britannica или воспользуйтесь полем поиска ниже.
Энциклопедия спорта
На морском языке: мореходные термины в первом издании Britannica
Что такое нейронная сеть? Ученый-компьютерщик объясняет
Что такое «период» периодической таблицы?
спросил
Изменено 2 года, 11 месяцев назад
Просмотрено 4к раз
$\begingroup$
Я знаком с таблицей Менделеева/периодической системой, но мне интересно, почему она называется “периодической”, так как там не так много периодичности (кажется, мало или совсем нет предсказуемости того, какие элементы стабильны) и из физики я знаю Z-значение элементов, которое также не является периодическим. Так что же такое «период» в этом контексте?
Так что же такое «период» в этом контексте?
- периодическая таблица
$\endgroup$
$\begingroup$
Я согласен с тем, что «периоды» в периодической таблице математически нерегулярны. Самое простое определение состоит в том, что период начинается, когда начинает заполняться новая s -подоболочка. Напомним, что в подоболочках s, p, d, f имеется 2, 8, 10 и 14 электронов соответственно, поэтому периоды должны увеличиваться со временем и, следовательно, не могут быть регулярными. Что касается отсутствия предсказуемости стабильности, это может быть правдой, но периодическая таблица довольно хорошо предсказывает химия элементов путем объединения сходных элементов в группы (столбцы). Это сходство в основном выражается в подоболочках s и p , в которых проявляется большая реактивность.
$\endgroup$
2
$\begingroup$
Так что же такое “период” в данном контексте? Чтобы ответить на это напрямую, период – это строка таблицы.