Таблица менделеева – Электронный учебник K-tree
Электронный учебник
Периодический закон, открытый Д. И. Менделеевым был выражен в таблице. Периодическая таблица химических элементов, или таблица менделеева.
1
H
1.008
2
He
4.003
3
Li
6.938
4
Be
9.012
5
B
10.806
6
C
12.01
7
N
14.006
8
O
15.999
9
F
18.998
10
Ne
20.18
11
Na
22.99
12
Mg
24.304
13
Al
26.982
14
Si
28.084
15
P
30.974
16
S
32.059
17
Cl
35.446
18
Ar
39.948
19
K
39.098
20
Ca
40.078
21
Sc
44.956
22
Ti
47.867
23
V
50.942
24
Cr
51. 996
996
Mn
54.938
26
Fe
55.845
27
Co
58.933
28
Ni
58.693
29
Cu
63.546
30
Zn
65.38
31
Ga
69.723
32
Ge
72.63
33
As
74.922
34
Se
78.971
35
Br
79.901
36
Kr
83.798
37
Rb
85.468
38
Sr
87.62
39
Y
88.906
40
Zr
91.224
41
Nb
92.906
42
Mo
95.95
44
Ru
101.07
45
Rh
102.906
46
Pd
106.42
47
Ag
107.868
48
Cd
112.414
49
In
114.818
50
Sn
118.71
51
Sb
121.76
52
Te
127.6
53
I
126.904
54
Xe
131.293
55
Cs
132.905
56
Ba
137.327
57
La
138.905
72
Hf
178. 49
49
73
Ta
180.948
74
W
183.84
75
Re
186.207
76
Os
190.23
77
Ir
192.217
78
Pt
195.084
79
Au
196.967
80
Hg
200.592
81
Tl
204.382
82
Pb
207.2
83
Bi
208.98
58
Ce
140.116
59
Pr
140.908
60
Nd
144.242
62
Sm
150.36
63
Eu
151.964
64
Gd
157.25
65
Tb
158.925
66
Dy
162.5
67
Ho
164.93
68
Er
167.259
69
Tm
168.934
70
Yb
173.045
71
Lu
174.967
90
Th
232.038
91
Pa
231.036
92
U
238.029
В таблице менделеева колонки называются группами, строки называются периодами. Элементы в группах как правило имеют
одинаковые электронные конфигурации внешних оболочек, например, благородные газы – последняя группа, имеют законченную
электронную конфигурацию.
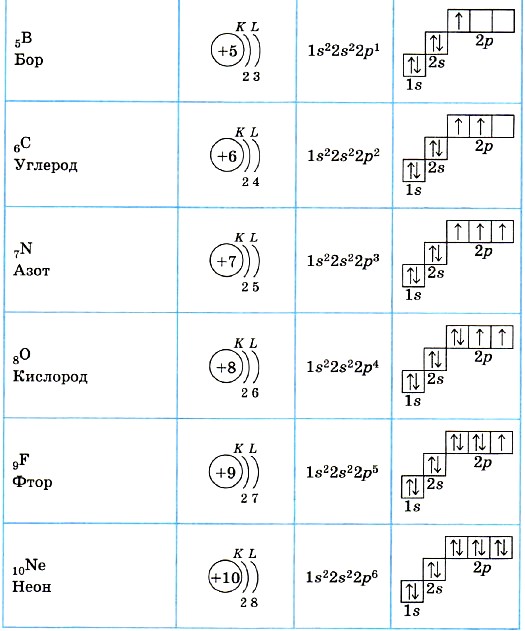
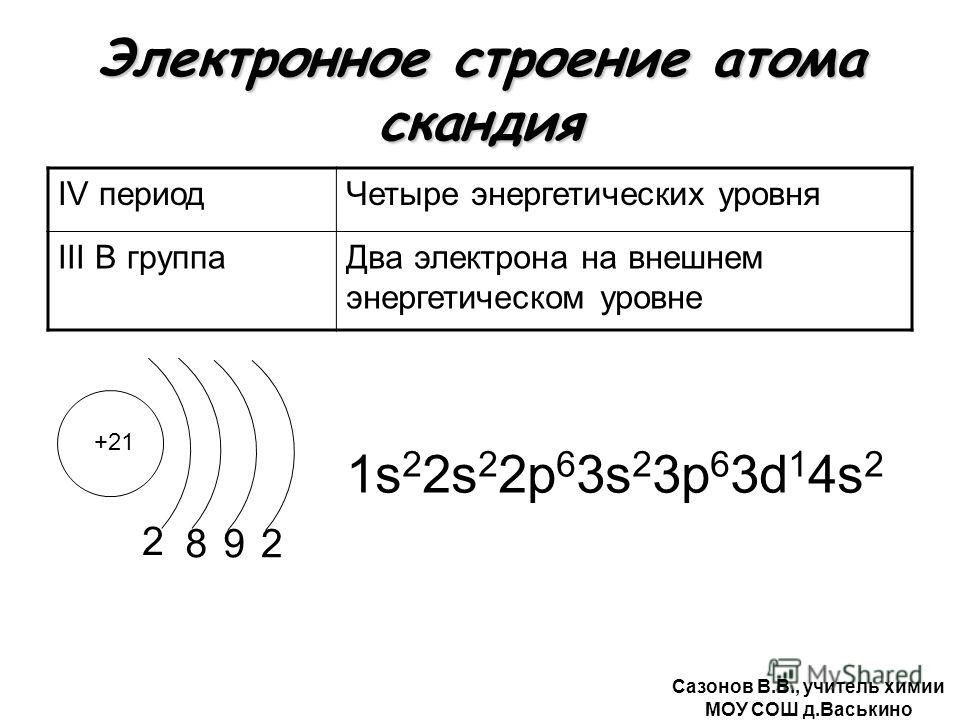
Как заполняется электронная конфигурация элементов подробно описано в статье
Скачать таблицу менделеева в хорошем качестве
© 2015-2022 – K-Tree.ru • Электронный учебник
По любым вопросам Вы можете связаться по почте [email protected]
Копия материалов, размещённых на данном сайте, допускается только по письменному разрешению владельцев сайта.
Германий, свойства атома, химические и физические свойства
Германий, свойства атома, химические и физические свойства.
Поделиться в:
Ge 32 Германий
72,630(8) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p2
Германий — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 32. Расположен в 14-й группе (по старой классификации — главной подгруппе четвертой группы), четвертом периоде периодической системы.
И. Менделеева с атомным номером 32. Расположен в 14-й группе (по старой классификации — главной подгруппе четвертой группы), четвертом периоде периодической системы.
Атом и молекула германия. Формула германия. Строение германия
Изотопы и модификации германия
Свойства германия (таблица): температура, плотность, давление и пр.
Физические свойства германия
Химические свойства германия. Взаимодействие германия. Реакции с германием
Получение германия
Применение германия
Таблица химических элементов Д.И. Менделеева
Атом и молекула германия. Формула германия. Строение германия:
Германий (лат. Germanium) – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением Ge и атомным номером 32. Расположен в 14-й группе (по старой классификации – главной подгруппе четвертой группы), четвертом периоде периодической системы.
Германий – металл. Относится к группе редких, рассеянных, цветных металлов. Является полуметаллом.
Германий обозначается символом Ge.
Как простое вещество германий при нормальных условиях представляет собой полуметалл серо-белого цвета с металлическим блеском.
Молекула германия одноатомна.
Химическая формула германия Ge.
Электронная конфигурация атома германия 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p2. Потенциал ионизации (первый электрон) атома германия равен 762,18 кДж/моль (7,899435(12) эВ).
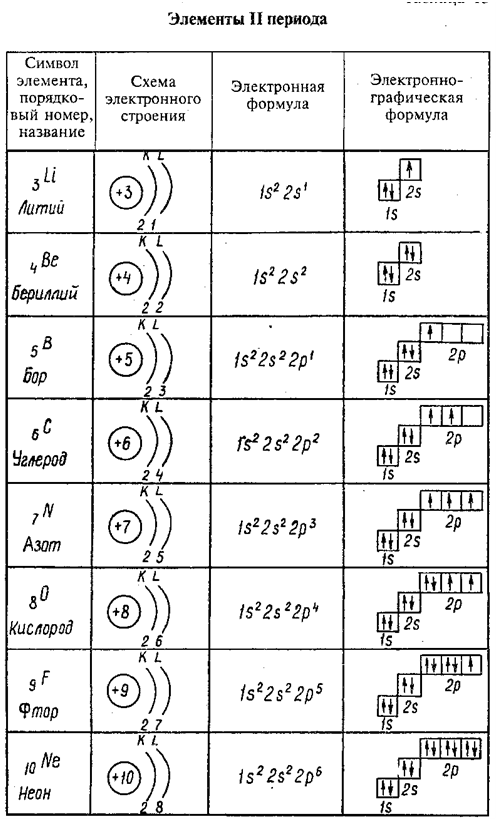
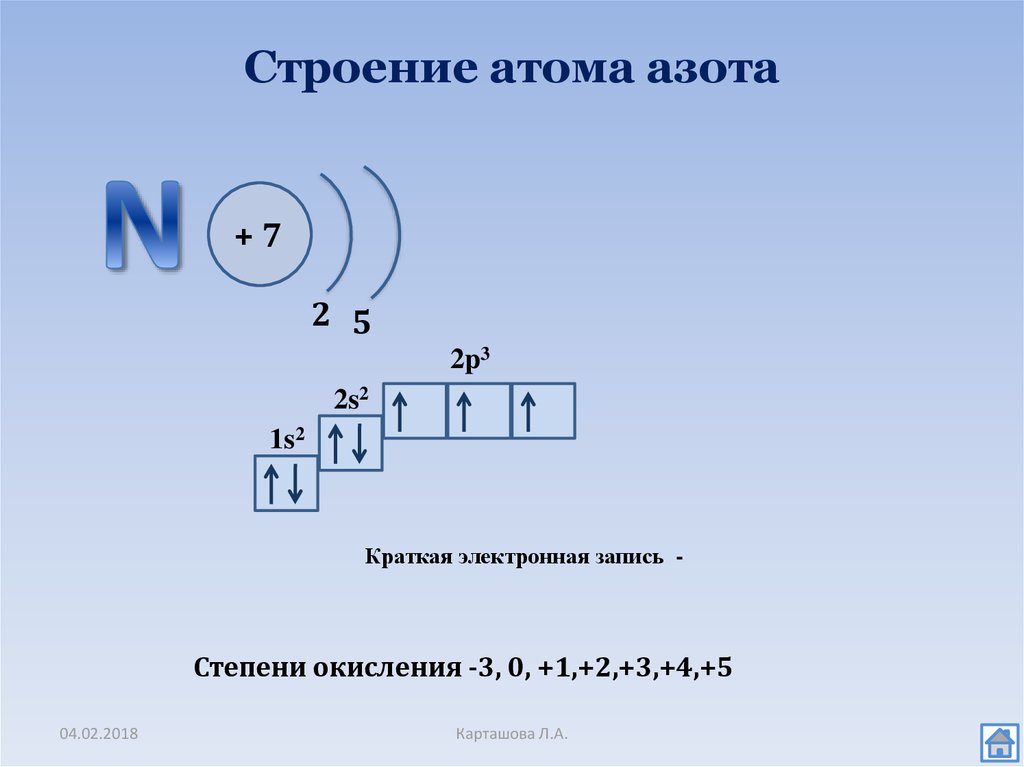
Строение атома германия. Атом германия состоит из положительно заряженного ядра (+32), вокруг которого по четырем атомным оболочкам движутся 32 электрона.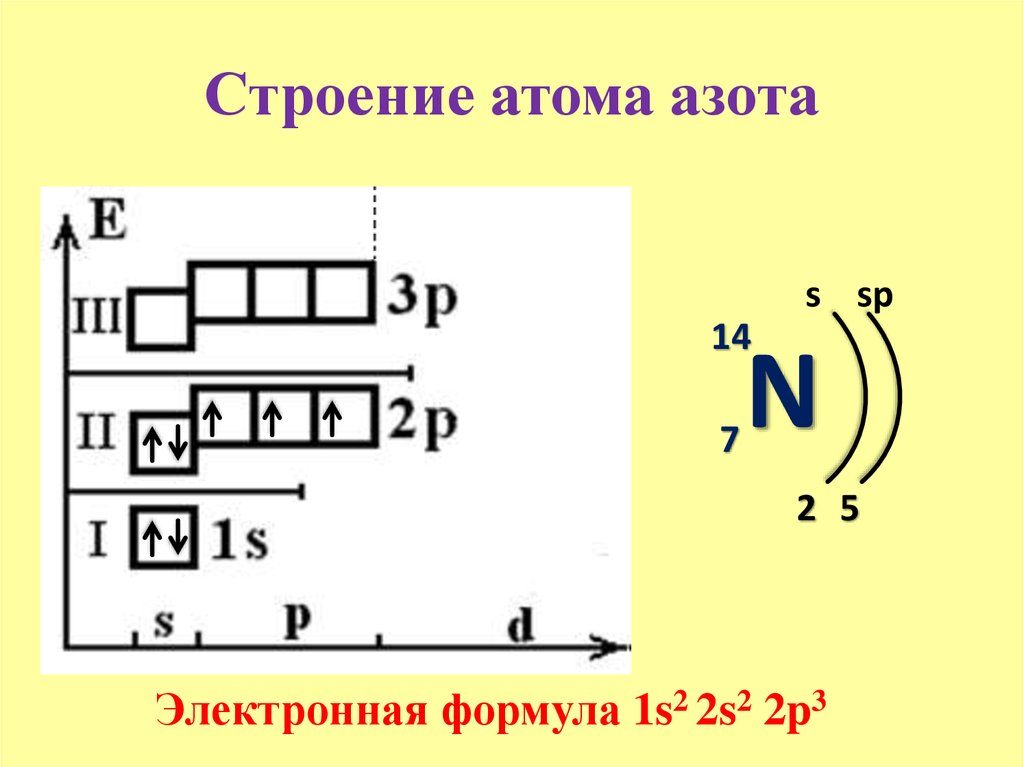 При этом 28 электронов находятся на внутреннем уровне, а 4 электрона – на внешнем. Поскольку германий расположен в четвертом периоде, оболочек всего четыре. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлена s- и р-орбиталями. Третья – внутренняя оболочка представлена s-, р- и d-орбиталями. Четвертая – внешняя оболочка представлена s- и р- орбиталями. На внешнем энергетическом уровне атома германия на s-орбитали находятся два спаренных электрона и на p-орбитали – два неспаренных электрона. В свою очередь ядро атома германия состоит из 32 протонов и 41 нейтрона.
При этом 28 электронов находятся на внутреннем уровне, а 4 электрона – на внешнем. Поскольку германий расположен в четвертом периоде, оболочек всего четыре. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлена s- и р-орбиталями. Третья – внутренняя оболочка представлена s-, р- и d-орбиталями. Четвертая – внешняя оболочка представлена s- и р- орбиталями. На внешнем энергетическом уровне атома германия на s-орбитали находятся два спаренных электрона и на p-орбитали – два неспаренных электрона. В свою очередь ядро атома германия состоит из 32 протонов и 41 нейтрона.
Радиус атома германия (вычисленный) составляет 125 пм.
Атомная масса атома германия составляет 72,630(8) а. е. м.
Германий, подобно кремнию, является полупроводником.
Германий, свойства атома, химические и физические свойства
Изотопы и модификации германия:
Свойства германия (таблица): температура, плотность, давление и пр.
 :
:Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Германий |
| 102 | Прежнее название | |
| 103 | Латинское название | Germanium |
| 104 | Английское название | Germanium |
| 105 | Символ | Ge |
| 106 | Атомный номер (номер в таблице) | 32 |
| 107 | Тип | Металл |
| 108 | Группа | Редкий, рассеянный, цветной металл. Полуметалл. |
| 109 | Открыт | Дмитрий Иванович Менделеев, Россия, 1869 г. (предсказан), Клеменс Александр Винклер, Германия, 1886 г. |
| 110 | Год открытия | 1886 г. |
| 111 | Внешний вид и пр. | Полуметалл серо-белого цвета с металлическим блеском |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | 2 аллотропные модификации: – α-германий с кубической алмазной кристаллической решёткой, – β-германий с тетрагональной кристаллической решёткой |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | Германен |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,00014 % |
| 120 | Содержание в морях и океанах (по массе) | 6,0·10-9 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,00002 % |
| 122 | Содержание в Солнце (по массе) | 0,00002 % |
| 123 | Содержание в метеоритах (по массе) | 0,0021 % |
| 124 | Содержание в организме человека (по массе) | |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 72,630(8) а. |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p2 |
| 203 | Электронная оболочка | K2 L8 M18 N4 O0 P0 Q0 R0
|
| 204 | Радиус атома (вычисленный) | 125 пм |
| 205 | Эмпирический радиус атома* | 125 пм |
| 206 | Ковалентный радиус | 122 пм |
| 207 | Радиус иона (кристаллический) | Ge2+ 87 (6) пм, Ge4+ 53 (4) пм, 67 (6) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 211 пм |
| 209 | Электроны, Протоны, Нейтроны | 32 электрона, 32 протона, 41 нейтрон |
| 210 | Семейство (блок) | элемент p-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 14-ая группа (по старой классификации – главная подгруппа 4-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | -4 -3, -2, -1, 0, +1, +2 , +3, +4 |
| 302 | Валентность | II, IV |
| 303 | Электроотрицательность | 2,01 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 762,18 кДж/моль (7,899435(12) эВ) |
| 305 | Электродный потенциал | Ge2+ + 2e– → Ge, Eo = 0,000 В |
| 306 | Энергия сродства атома к электрону | 118,9352(2) кДж/моль (1,2326764(13) эВ) |
| 400 | ||
| 401 | Плотность | 5,323 г/см3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело), 5,60 г/см3 (при температуре плавления 938,25 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления* | 938,25 °C (1211,40 K, 1720,85 °F) |
| 403 | Температура кипения* | 2833 °C (3106 K, 5131 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 36,94 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 334 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | 0,31 Дж/г·K (при 0-100 °C) |
| 410 | Молярная теплоёмкость* | 23,222 Дж/(K·моль) |
| 411 | Молярный объём | 13,6464 см³/моль |
| 412 | Теплопроводность | 60,2 Вт/(м·К) (при стандартных условиях), 60,2 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | α-германий
|
| 512 | Структура решётки | Кубическая алмазная |
| 513 | Параметры решётки | 5,660 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 360 K |
| 516 | Название пространственной группы симметрии | Fm_ 3m |
| 517 | Номер пространственной группы симметрии | 225 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-56-4 |
Примечание:
205* Эмпирический радиус атома германия согласно [1] и [3] составляет 122 пм и 122,5 пм соответственно.
402* Температура плавления германия согласно [3] и [4] составляет 937,45 °С (1210,6 K, 1719,41 °F) и 937 °C (1210,15 K, 1718,6 °F) соответственно.
403* Температура кипения германия согласно [3] и [4] составляет 2829,85 °С (3103 K, 5125,73 °F) и 2850 °C (3123,15 K, 5162 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) германия согласно [3] и [4] составляет 36,8 кДж/моль и 37 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) германия согласно [3] составляет 328 кДж/моль.
410* Молярная теплоёмкость германия согласно [3] составляет 23,32 Дж/(K·моль).
Физические свойства германия:
Химические свойства германия. Взаимодействие германия. Реакции с германием:
1. Реакция взаимодействия германия и атомарного водорода:
Ge + 2H2 → GeH4.
В результате реакции образуется гидрид германия.
2. Реакция взаимодействия германия и кислорода:
Ge + O2 → GeO2 (t > 700 °C).
В результате реакции образуется оксид германия.
3. Реакция взаимодействия германия и фтора:
Ge + 2F2 → GeF4 (t = 100 °C).
В результате реакции образуется фторид германия.
4. Реакция взаимодействия германия и хлора:
Ge + 2Cl2 → GeCl4 (t = 150-200 °C).
В результате реакции образуется хлорид германия.
5. Реакция взаимодействия германия и брома:
Ge + 2Br2 → GeBr4 (t = 350 °C).
В результате реакции образуется бромид германия.
6. Реакция взаимодействия германия и йода:
Ge + 2I2 → GeI4 (t = 560 °C).
В результате реакции образуется йодид германия.
7. Реакция взаимодействия германия и серы:
Ge + 2S → GeS2 (t = 600-860 °C),
Ge + S → GeS (t = 1000 °C).
В результате реакции образуется в первом случае сульфид германия (IV), во втором – сульфид германия (II).
8. Реакция взаимодействия германия и селена:
Ge + Se → GeSe (t = 600-700 °C).
В результате реакции образуется селенид германия.
9. Реакция взаимодействия германия и оксида углерода:
Ge + CO2 → GeO + CO (t = 700-900 °C).
В результате реакции образуются оксид германия (II) и оксид углерода (II).
10. Реакция взаимодействия германия и оксида германия (IV):
GeO2 + Ge → 2GeO (t = 1350-1400 °C).
В результате реакции образуется оксид германия (II).
11. Реакция взаимодействия германия и оксида серы:
3Ge + 2SO2 → 2GeO2 + GeS2 (t > 500 °C).
В результате реакции образуются оксид германия (IV) и сульфид германия.
12. Реакция взаимодействия германия и фтороводорода:
Ge + 2HF → GeF2 + H2 (t = 200 °C, р).
В результате реакции образуются фторид германия (II) и водород. В ходе реакции используется жидкий фтороводород. Реакция протекает при избыточном давлении.
В ходе реакции используется жидкий фтороводород. Реакция протекает при избыточном давлении.
13. Реакция взаимодействия германия и сероводорода:
Ge + H2S → GeS + H2 (t = 600-800 °C).
В результате реакции образуются сульфид германия (II) и водород.
14. Реакция взаимодействия германия и азотной кислоты:
Ge + 4HNO3 → H2GeO3 + 4NO2 + H2O,
Ge + 4HNO3 → GeO2 + 4NO2 + 2H2O
В результате реакции в первом случае образуются германиевая кислота, оксид азота и вода, во втором – оксид германия, оксид азота и вода. В ходе реакции в обоих случаях используется концентрированная азотная кислота. Вторая реакция протекает медленно.
Аналогичные реакции протекают и с другими минеральными кислотами.
15. Реакция взаимодействия германия и хлорида германия (IV):
Ge + GeCl4 → GeCl2 (t = 300-350 °C).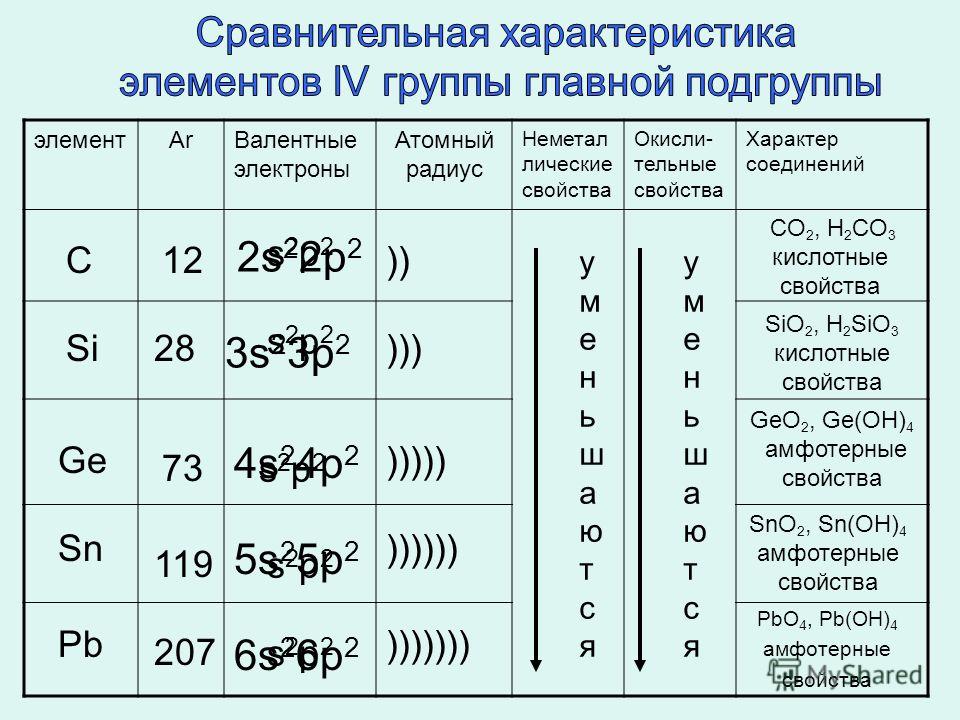
В результате реакции образуется хлорид германия (II).
16. Реакция взаимодействия германия, гидроксида натрия и пероксида водорода:
Ge + 2NaOH + 2H2O2 → Na2GeO3 + 3H2O,
Ge + 2NaOH + 2H2O2 → Na2[Ge(OH)6].
В результате реакции в первом случае образуются германат натрия и вода, во втором гексагидроксогерманат натрия. В ходе реакции в первом случае используется разбавленный раствор гидроксида натрия, во втором – концентрированный раствор гидроксида натрия.
17. Реакция взаимодействия германия, гидроксида калия и пероксида водорода:
Ge + 2KOH + 2H2O2 → K2[Ge(OH)6].
В результате реакции образуется гексагидроксогерманат калия.
Получение германия:
Применение германия:
Таблица химических элементов Д.И. Менделеева
- 1.
 Водород
Водород - 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35.
 Бром
Бром - 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68.
 Эрбий
Эрбий - 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101.
 Менделеевий
Менделеевий - 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
Таблица химических элементов Д.И. Менделеева
Источники:
- https://en.wikipedia.org/wiki/Germanium
- https://de.wikipedia.org/wiki/Germanium
- https://ru.wikipedia.org/wiki/Германий
- http://chemister.ru/Database/properties.php?dbid=1&id=242
- https://chemicalstudy.ru/germaniy-svoystva-atoma-himicheskie-i-fizicheskie-svoystva/
Примечание: © Фото https://www. pexels.com, https://pixabay.com
pexels.com, https://pixabay.com
германий атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решетка
атом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома
электронные формулы сколько атомов в молекуле германия
сколько электронов в атоме свойства металлические неметаллические термодинамические
Коэффициент востребованности 2 678
Германий, атомная структура – Стоковая фотография – C018/3713
Похоже, вы используете старый веб-браузер, который не поддерживается.
Некоторые части этого веб-сайта могут работать некорректно. Пожалуйста, используйте более новый веб-браузер.
Пожалуйста, используйте более новый веб-браузер.
Это изображение недоступно для покупки в вашей стране.
C018/3713
Управление правами
74,5 МБ (74,0 МБ со сжатием)
5197 x 5008 пикселей
43,9 x 42,4 см ⏐ 17,3 х 16,7 дюйма (300 точек на дюйм)
Это изображение недоступно для покупки в вашей стране.
Пожалуйста, свяжитесь с вашим менеджером по работе с клиентами, если у вас есть какие-либо вопросы.
Запрос
Цена Добавить в корзину Удалять ДОБАВИТЬ НА ДОСКУ ДелитьсяКупить Распечатать
Кредит
КАРЛОС КЛАРИВАН / НАУЧНАЯ ФОТОБИБЛИОТЕКА КАРЛОС КЛАРИВАН / НАУЧНАЯ ФОТОБИБЛИОТЕКА
Подпись
Германий (Ge). Схема ядерного состава, электронной конфигурации, химических данных и валентных орбиталей атома германия-73 (атомный номер: 32), изотопа этого элемента. Ядро состоит из 32 протонов (красные) и 41 нейтрона (оранжевые). 32 электрона (белые) последовательно занимают доступные электронные оболочки (кольца). Стабильность внешних (валентных) электронов элемента определяет его химические и физические свойства. Германий представляет собой металлоид в группе 14, периоде 4 и р-блоке периодической таблицы. Используемый в первых полупроводниках, он в основном был заменен кремнием. Имеет температуру плавления 938 градусов Цельсия.
32 электрона (белые) последовательно занимают доступные электронные оболочки (кольца). Стабильность внешних (валентных) электронов элемента определяет его химические и физические свойства. Германий представляет собой металлоид в группе 14, периоде 4 и р-блоке периодической таблицы. Используемый в первых полупроводниках, он в основном был заменен кремнием. Имеет температуру плавления 938 градусов Цельсия.
Сведения о выпуске
Разрешение модели не требуется. Разрешение собственности не требуется.
Ключевые слова
- 4p
- 4п2
- 4с
- 4с2
- а.е.м.
- атом
- атомный
- атомный номер
- атомных орбиталей
- атомный радиус
- атомный вес
- черный фон
- химические данные
- химические свойства
- химическое свойство
- химия
- схема
- электронная конфигурация
- номер электрона
- электронная оболочка
- электронный
- электронов
- элемент
- элементаль
- элементов
- уровней энергии
- гэ
- германий
- германий-73
- группа 14
- иллюстрация
- изотоп
- уровень
- уровней
- металлоид
- металлоиды
- нейтрон
- нейтрон номер
- нейтронов
- ядерный
- ядерные данные
- нуклон
- нуклонов
- ядро
- орбитальный
- орбитальные типы
- орбиталей
- р блок
- р-блок
- период 4
- физическая химия
- физические свойства
- физическое имущество
- вечера
- протон номер
- квантовая химия
- оболочка
- каркасная конструкция
- снаряды
- простая электронная конфигурация
- твердый
- твердые вещества
- структурный
- структура
- субатомный
- субатомный
- подоболочка
- подоболочек
- символ
- валентная орбиталь
- волновая функция
Собственный полупроводник — атомная структура Si и Ge
Собственный полупроводник — атомная структура Si и Ge| |
Физика | Электроника Устройства и схемы | Электромагнетизм | СИДЕЛ Связь | Компьютер Основы | Карта сайта | В сети тест | Блог
внутренний
полупроводник Введение | Электроника
приборы и схемы >> Полупроводники >>
внутренний
полупроводник
>> Атомный
структура кремния и германия атомная структура собственного полупроводника
такие материалы, как кремний и германий,
следует. Атомный структура кремнияКремний — это вещество, состоящее из атомов, каждый из которых имеет одинаковое количество протонов. Атомный номер кремния 14 т.е. 14 протонов. число протонов в ядре атома называется атомным число. Атом кремния имеет 14 электронов (два электрона в первая орбита, восемь электронов на второй орбите и 4 электрона на крайней орбите). Атомный структура германия Германий представляет собой вещество, состоящее из атомов, каждый из которых имеет
одинаковое количество протонов. Атомный номер германия 32.
то есть 32 протона. Число протонов в ядре атома равно
называется атомным номером. |