Главные подгруппы металлов I-III групп в таблице Д.И. Менделеева
Похожие презентации:
Главная подгруппа II группы
Общая характеристика металлов IА группы ПСХЭ Д.И. Менделеева
Электронное строение элементов главной подгруппы III группы
Свойства химических элементов I и II А подгрупп периодической системы Д.И. Менделеева
Общая характеристика элементов I группы главной подгруппы Периодической системы химических элементов Д.И. Менделеева
Главная подгруппа V группы..Азот
Главная подгруппа IV группы
Общая характеристика элементов I группы главной подгруппы Периодической системы Д.И. Менделеева
Первая группа периодической системы Менделеева. Щелочные металлы
Алюминий и его соединения. Строение атома
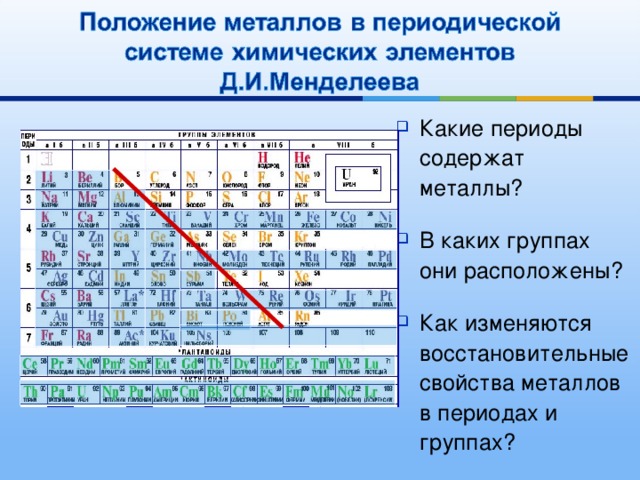
1. Общая характеристика металлов главных подгрупп I-III групп ПСХЭ Д.И.Менделеева
2. Характеристика металлов главной подгруппы I группы
Щелочны́е мета́ллы: литий Li, натрий Na,калий K, рубидий Rb, цезий Cs и франций
Fr.
 Эти металлы получили название
Эти металлы получили названиещелочных, потому что большинство их
соединений растворимо в воде. По-славянски
«выщелачивать» означает «растворять»,
это и определило название данной группы
металлов. При растворении щелочных
металлов в воде образуются растворимые
гидроксиды, называемые щёлочами.
3. Строение атомов щелочных металлов
Все щелочные металлы имеют один s-электрон на внешнемэлектронном слое, который при химических реакциях легко теряют,
проявляя степень окисления +1. Поэтому щелочные металлы
являются сильными восстановителями.
4. Физические свойства
цезийлитий
Все металлы этой подгруппы имеют серебристо-белый цвет
(кроме серебристо-жёлтого цезия), они очень мягкие, их
можно резать скальпелем. Литий, натрий и калий легче
воды и плавают на её поверхности, реагируя с ней. Поэтому
хранят эти металлы под слоем керосина или парафина.
калий
натрий
рубидий
6. Получение щелочных металлов
1. Для получения щелочных металлов используют в основном
Для получения щелочных металлов используют в основномэлектролиз расплавов их галогенидов, чаще всего — хлоридов,
образующих природные минералы:
катод: Li+ + e → Li
анод: 2Cl- — 2e → Cl2
2. Иногда для получения щелочных металлов проводят электролиз
расплавов их гидроксидов:
катод: Na+ + e → Na
анод: 4OH- — 4e → 2h3O + O2
Поскольку щелочные металлы в электрохимическом ряду напряжений
находятся левее водорода, то электролитическое получение их из растворов
солей невозможно; в этом случае образуются соответствующие щёлочи и
водород.
7. Химические свойства
Реакции с неметаллами(образуются бинарные соединения):
4Li + O2 2Li2O(оксид лития)
2Na + O2 Na2O2(пероксид натрия)
K + O2 KO2(надпероксид калия)
2Li + Cl2 = 2LiCl(галогениды)
2Na + S = Na2S(сульфиды)
2Na + h3 = 2NaH(гидриды)
6Li + N2 = 2Li3N(нитриды)
2Li + 2C = 2Li2C2(карбиды)
Активно взаимодействуют с водой:
2Na + 2h3O 2NaOH + h3
2Li + 2h3O 2LiOH + h3
Реакция с кислотами:
2Na + 2HCl 2NaCl + h3
Качественная реакция на катионы щелочных металлов окрашивание пламени в следующие цвета:
Li+ – карминово-красный
Na+ – желтый
K+, Rb+ и Cs+ – фиолетовый
Так выглядит проба
на окрашивание
пламени солями
натрий
Карминовокрасное
окрашивание
пламени солями
лития
Окрашивание
пламени
горелки
ионами калия
10.
 Обобщим химические свойства щелочных металлов
Обобщим химические свойства щелочных металлов11. Характеристика металлов главной подгруппы II группы
Атомы этихэлементов имеют на
внешнем
электронном уровне
два s-электрона: ns2.
В реакциях атомы
элементов подгруппы
легко отдают оба
электрона внешнего
энергетического
уровня и образуют
соединения, в
которых степень
окисления элемента
равна +2.
12. Физические свойства
Бериллий, магний,кальций, барий и
радий – металлы
серебристо-белого
цвета. Стронций имеет
золотистый цвет. Эти
металлы легкие,
особенно низкие
плотности имеют
кальций, магний,
бериллий. Радий
является
радиоактивным
химическим
элементом.
13. Получение щелочноземельных металлов
Электролизом расплавов их хлоридов илитермическим восстановлением их
соединений:
BeF2 + Mg = Be + MgF2
MgO + C = Mg + CO
3CaO + 2Al = 2Ca + Al2O3
3BaO + 2Al = 3Ba + Al2O3
14.
 Химические свойстваЩелочноземельные элементы – химически активные
Химические свойстваЩелочноземельные элементы – химически активныеметаллы. Они являются сильными
восстановителями. Из металлов этой подгруппы
несколько менее активен бериллий, что обусловлено
образованием на поверхности этого металла защитной
оксидной пленки.
кальций
магний
бериллий
15. Взаимодействие с простыми веществами
Все легко взаимодействуют с кислородом и серой, образуяоксиды и сульфаты:
2Be + O2 = 2BeO
Ca + S = CaS
Бериллий и магний реагируют с кислородом и серой при
нагревании, остальные металлы – при обычных условиях.
Все металлы этой группы легко реагируют с галогенами:
Mg + Cl2 = MgCl2
При нагревании все реагируют с водородом, азотом, углеродом,
кремнием и другими неметаллами:
Ca + h3 = Cah3 (гидрид кальция)
3Mg + N2 = Mg3N2 (нитрид магния)
Ca + 2C = CaC2 (карбид кальция)
16. Взаимодействие с кислотами
Все взаимодействуют с хлороводородной и разбавленнойсерной кислотами с выделением водорода:
Be + 2HCl = BeCl2 + h3
Разбавленную азотную кислоту металлы восстанавливают
главным образом до аммиака или нитрата аммония:
2Ca + 10HNO3(разб.
 ) = 4Ca(NO3)2 + Nh5NO3 +
) = 4Ca(NO3)2 + Nh5NO3 +3h3O
В концентрированных азотной и серной кислотах (без
нагревания) бериллий пассивирует, остальные металлы
реагируют с этими кислотами.
17. Взаимодействие со щелочами
Бериллий взаимодействует с воднымирастворами щелочей с образованием
комплексной соли и выделением водорода:
Be + 2NaOH + 2h3O = Na2[Be(OH)4] + h3
Остальные металлы II группы с щелочами не
реагируют.
18. Алюминий
13Al[Ne]
2
1
3s 3p
Алюминий находится в главной п/группе III
группы периодической системы.
На внешнем энергетическом уровне
имеются свободные р-орбитали, что
позволяет ему переходить в возбужденное
состояние. В возбужденном состоянии атом
алюминия образует три ковалентные связи
или полностью отдает три валентных
электрона, проявляя степень окисления +3.
19. Физические свойства
Металл серебристо-белого цвета, легкий, плотность 2,7 г/см³,температура плавления у технического 658 °C, у алюминия
высокой чистоты 660 °C, температура кипения 2500 °C, временное
сопротивление литого 10-12 кг/мм², деформируемого 18-25
кг/мм2,сплавов 38-42 кг/мм².

Твердость по Бринеллю 24-32 кгс/мм², высокая пластичность: у
технического 35 %, у чистого 50 %, прокатывается в тонкий лист и
даже фольгу.
20. Химические свойства
С простыми веществами:1)
С кислородом:
4Al0 + 3O2 → 2Al+32O3
2)
С галогенами:
2Al0 + 3Br20 → 2Al+3Br3
3) С другими неметаллами (азотом, серой, углеродом) реагирует
при нагревании:
2Al0 + 3S t°→ Al2+3S3(сульфид алюминия)
2Al0 + N2 t° → 2Al+3N(нитрид алюминия)
4Al0 + 3С → Al4+3С3(карбид алюминия)
Сульфид и карбид алюминия полностью гидролизуются:
Al2S3 + 6h3O → 2Al(OH)3¯ + 3h3S
Al4C3 + 12h3O → 4Al(OH)3¯+ 3Ch5
Со сложными веществами:
4)
С водой (после удаления защитной оксидной пленки):
2Al0 + 6h3O ® 2Al+3(OH)3 + 3h3
5)
Со щелочами:
2Al0 + 2NaOH + 6h3O ® 2Na[Al+3(OH)4]
(тетрагидроксоалюминат натрия) + 3h3
6) Легко растворяется в соляной и разбавленной серной
киcлотах:
2Al + 6HCl ® 2AlCl3 + 3h3
2Al + 3h3SO4(разб) ® Al2(SO4)3 + 3h3
При нагревании растворяется в кислотах – окислителях:
2Al + 6h3SO4(конц) ® Al2(SO4)3 + 3SO2 + 6h3O
Al + 6HNO3(конц) ® Al(NO3)3 + 3NO2 + 3h3O
7)
Восстанавливает металлы из их оксидов (алюминотермия):
8Al0 + 3Fe3O4 ® 4Al2O3 + 9Fe
2Al + Cr2O3 ® Al2O3 + 2Cr
22.
 Получение алюминия
Получение алюминия23. Применение алюминия
— в электротехнике— для производства легких сплавов
(дюралюмин, силумин) в самолето- и
автомобилестроении
— для алитирования чугунных и
стальных изделий с целью повышения
их коррозионной стойкости
— для термической сварки
свободном виде
— в строительной промышленности
— для изготовления контейнеров,
фольги и т.п.
English Русский Правила
ОБ ОДНОЙ «ОШИБКЕ» Д.И. МЕНДЕЛЕЕВА. ПРОБЛЕМА «НУЛЕВЫХ» – статья
- Автор: Рязанцев Г.Б.
- Журнал: Российское Атомное Сообщество, сверхновая энергетика http://www.atomic-energy.ru/papers/44698
- Год издания: 2013
 в «Петербургском листке» № 5 по случаю 70-летия Д.И. Менделеева опубликован его портрет и интервью. На вопрос, какими научными исследованиями он занят в настоящее время, ученый ответил: «Они направлены исключительно к подтверждению выставленной мною в прошедшем году теории, или, вернее, попытки, химического понимания мирового эфира».
Что это за теория, о которой мы так мало знаем и к которой были прикованы исключительно все последние исследования ученого [1,2,3]?
Статью “Попытка химического понимания мирового эфира” Д.И. Менделеев окончил в октябре 1902 г., а опубликовал в январе 1903 г. в №1-4 “ Вестника и библиотеки самообразования” и часто о ней говорил, так в мае 1904 г. написал письма известному ученому С. Ньюкомбу; в котором ссылается на свою работу о мировом эфире, где касается вопроса о природе эфира, сообщает, что в ближайшее время собирается написать статью
«по поводу современных представлений о сложности химических элементов и об электронах…».
О сложности химических элементов и об электронах – это понятно современному читателю, но …мировой эфир…?! Сейчас даже школьники знают, что эта идея отброшена современной наукой.
в «Петербургском листке» № 5 по случаю 70-летия Д.И. Менделеева опубликован его портрет и интервью. На вопрос, какими научными исследованиями он занят в настоящее время, ученый ответил: «Они направлены исключительно к подтверждению выставленной мною в прошедшем году теории, или, вернее, попытки, химического понимания мирового эфира».
Что это за теория, о которой мы так мало знаем и к которой были прикованы исключительно все последние исследования ученого [1,2,3]?
Статью “Попытка химического понимания мирового эфира” Д.И. Менделеев окончил в октябре 1902 г., а опубликовал в январе 1903 г. в №1-4 “ Вестника и библиотеки самообразования” и часто о ней говорил, так в мае 1904 г. написал письма известному ученому С. Ньюкомбу; в котором ссылается на свою работу о мировом эфире, где касается вопроса о природе эфира, сообщает, что в ближайшее время собирается написать статью
«по поводу современных представлений о сложности химических элементов и об электронах…».
О сложности химических элементов и об электронах – это понятно современному читателю, но …мировой эфир…?! Сейчас даже школьники знают, что эта идея отброшена современной наукой.






 В открытом им законе ученый пытается с физической стороны выяснить природу массы как основной характеристики вещества. Выясняя физические основы тяготения (об этом мы тоже мало знаем – как много сил и времени он уделял этой проблеме), тесно связанные с понятием мирового эфира как «передающей» среды, он ищет легчайший Элемент (намного легче Водорода). Однако результаты опытов 70-х годов, сводившиеся к тому, чтобы доказать, что «эфир есть сумма разреженнейших газов», не удовлетворили Менделеева. На какое-то время он прекратил исследования в этом направлении, нигде не писал, но как видно, никогда и не забывал о них. В конце жизни в поисках ответа на вопросы, касающиеся глубинных свойств материи, он вновь обращается к «мировому эфиру», с помощью которого пытается проникнуть в природу основного понятия естествознания XIX в. (да и ХХ, и даже ХХI вв.) – массы, а также дать объяснения новым открытиям и прежде всего радиоактивности. Основная мысль ученого заключается в следующем: «Реального понимания эфира нельзя достичь, игнорируя его химизм* и не считая его элементарным веществом; элементарные же вещества ныне немыслимы без подчинения их периодической законности».
В открытом им законе ученый пытается с физической стороны выяснить природу массы как основной характеристики вещества. Выясняя физические основы тяготения (об этом мы тоже мало знаем – как много сил и времени он уделял этой проблеме), тесно связанные с понятием мирового эфира как «передающей» среды, он ищет легчайший Элемент (намного легче Водорода). Однако результаты опытов 70-х годов, сводившиеся к тому, чтобы доказать, что «эфир есть сумма разреженнейших газов», не удовлетворили Менделеева. На какое-то время он прекратил исследования в этом направлении, нигде не писал, но как видно, никогда и не забывал о них. В конце жизни в поисках ответа на вопросы, касающиеся глубинных свойств материи, он вновь обращается к «мировому эфиру», с помощью которого пытается проникнуть в природу основного понятия естествознания XIX в. (да и ХХ, и даже ХХI вв.) – массы, а также дать объяснения новым открытиям и прежде всего радиоактивности. Основная мысль ученого заключается в следующем: «Реального понимания эфира нельзя достичь, игнорируя его химизм* и не считая его элементарным веществом; элементарные же вещества ныне немыслимы без подчинения их периодической законности». Характеризуя мировой эфир, Менделеев считает его « во-первых, наилегчайшим из всех элементов как по плотности, так и по атомному весу, во-вторых, наибыстрее движущимся газом, в-третьих, наименее способным к образованию с какими-либо другими атомами или частицами определенных сколь-либо прочных соединений и, в-четвертых, элементом, всюду распространенным и всепроникающим».
Вес атома этого гипотетического элемента X , по расчетам ученого, может колебаться в пределах 9.6 *10(в -7 степени) до 5.3*10(в -11 степени) (если атомный вес Н равен 1). Для оценки массы гипотетического элемента привлекает знания механики и астрономии (он даже прикидывает массу звезды, которую из-за величины силы тяготения не может покинуть свет, предвидение черных дыр более ста лет назад! Но это все так, между прочим, просто для оценки границ массы нового элемента). Элемент X (Менделеев называет его «Ньютонием» – «Мне бы хотелось предварительно назвать его «ньютонием» – в честь бессмертного Ньютона») получал свое место в периодической системе – в нулевом периоде нулевой группы, как легчайший аналог инертных газов.
Характеризуя мировой эфир, Менделеев считает его « во-первых, наилегчайшим из всех элементов как по плотности, так и по атомному весу, во-вторых, наибыстрее движущимся газом, в-третьих, наименее способным к образованию с какими-либо другими атомами или частицами определенных сколь-либо прочных соединений и, в-четвертых, элементом, всюду распространенным и всепроникающим».
Вес атома этого гипотетического элемента X , по расчетам ученого, может колебаться в пределах 9.6 *10(в -7 степени) до 5.3*10(в -11 степени) (если атомный вес Н равен 1). Для оценки массы гипотетического элемента привлекает знания механики и астрономии (он даже прикидывает массу звезды, которую из-за величины силы тяготения не может покинуть свет, предвидение черных дыр более ста лет назад! Но это все так, между прочим, просто для оценки границ массы нового элемента). Элемент X (Менделеев называет его «Ньютонием» – «Мне бы хотелось предварительно назвать его «ньютонием» – в честь бессмертного Ньютона») получал свое место в периодической системе – в нулевом периоде нулевой группы, как легчайший аналог инертных газов. Кроме того, Менделеев допускал существование еще одного элемента легче водорода – элемента Y, «Корония» (предположительно линии «Корония» были зафиксированы при солнечном затмении в 1869 г. в спектре короны; открытие гелия на земле давало основание считать реальным и существование «Корония»). Вместе с тем Менделеев не раз подчеркивал гипотетичность элементов X и Y и не включал их в таблицы элементов 7-го и 8-го изданий «Основ химии». Научная требовательность и ответственность в работах Менделеева не нуждается в комментариях! Но, как мы видим, если это требует логика поиска, он смело выдвигал самые необычные гипотезы, основанные на глубокой интуиции. Следует напомнить, что в своих предсказаниях новых элементов до этого Менделеев не ошибался! Все предсказания, сделанные им на основе периодического закона (существование 12 неизвестных в то время элементов), а также исправления атомных масс элементов блестяще подтвердились!
«Когда я прилагал периодический закон к аналогам бора, алюминия и кремния, я был на 33 года моложе, во мне жила полная уверенность, что рано или поздно предвидимое должно непременно оправдаться, потому что мне все там было ясно видно.
Кроме того, Менделеев допускал существование еще одного элемента легче водорода – элемента Y, «Корония» (предположительно линии «Корония» были зафиксированы при солнечном затмении в 1869 г. в спектре короны; открытие гелия на земле давало основание считать реальным и существование «Корония»). Вместе с тем Менделеев не раз подчеркивал гипотетичность элементов X и Y и не включал их в таблицы элементов 7-го и 8-го изданий «Основ химии». Научная требовательность и ответственность в работах Менделеева не нуждается в комментариях! Но, как мы видим, если это требует логика поиска, он смело выдвигал самые необычные гипотезы, основанные на глубокой интуиции. Следует напомнить, что в своих предсказаниях новых элементов до этого Менделеев не ошибался! Все предсказания, сделанные им на основе периодического закона (существование 12 неизвестных в то время элементов), а также исправления атомных масс элементов блестяще подтвердились!
«Когда я прилагал периодический закон к аналогам бора, алюминия и кремния, я был на 33 года моложе, во мне жила полная уверенность, что рано или поздно предвидимое должно непременно оправдаться, потому что мне все там было ясно видно. Оправдание пришло скорее, чем я мог надеяться. Тогда я не рисковал, теперь рискую. На это надобна решимость. Она пришла, когда я видел радиоактивные явления … и когда я сознал, что откладывать мне уже невозможно и что, быть может, мои несовершенные мысли наведут кого-нибудь на путь более верный, чем тот возможный, какой представляется моему слабеющему зрению».
Так что же, это первая крупная ошибка, может даже глубокое заблуждение великого ученого, как сейчас считают очень многие, или всего лишь прискорбное недопонимание гения его малоспособными учениками? Давайте попробуем разобраться!
В начале XX века не только Менделеев, но и многие физики и химики верили в существование «эфира». Однако после создания Альбертом Эйнштейном специальной и общей теории относительности эта вера стала угасать. Принято считать, что к 1930-м годам проблема «эфира» уже не существовала в науке, а вопрос об элементах легче водорода сам собой отпал. Но, опять же, следует напомнить, что проблема классического эфира отпала, эфира однородного, а вот эфир структурный (эфир Менделеева) вполне жив, только называется он сейчас структурным вакуумом или вакуумом Дирака! Так что, вопрос только в терминологии.
Оправдание пришло скорее, чем я мог надеяться. Тогда я не рисковал, теперь рискую. На это надобна решимость. Она пришла, когда я видел радиоактивные явления … и когда я сознал, что откладывать мне уже невозможно и что, быть может, мои несовершенные мысли наведут кого-нибудь на путь более верный, чем тот возможный, какой представляется моему слабеющему зрению».
Так что же, это первая крупная ошибка, может даже глубокое заблуждение великого ученого, как сейчас считают очень многие, или всего лишь прискорбное недопонимание гения его малоспособными учениками? Давайте попробуем разобраться!
В начале XX века не только Менделеев, но и многие физики и химики верили в существование «эфира». Однако после создания Альбертом Эйнштейном специальной и общей теории относительности эта вера стала угасать. Принято считать, что к 1930-м годам проблема «эфира» уже не существовала в науке, а вопрос об элементах легче водорода сам собой отпал. Но, опять же, следует напомнить, что проблема классического эфира отпала, эфира однородного, а вот эфир структурный (эфир Менделеева) вполне жив, только называется он сейчас структурным вакуумом или вакуумом Дирака! Так что, вопрос только в терминологии. Вернемся к элементам легче водорода. Говорят, что их не нашли. А может, просто не искали? Или лучше сказать, когда нашли, просто не узнали!
Любому химику известны гомологические ряды, и хорошо известно, как ведут себя первые члены, особенно первый. Как известно первый всегда особенный. Он всегда сильно выделяется из общего ряда. Водород размещают и в I и в VII группах (он в чем-то подобен и щелочным металлам и галогенам одновременно). Так вот водород вовсе и не первый! Так как же должны отличаться настоящие первые элементы, элементы нулевого периода, от всех остальных, обычных элементов? Будут ли они вообще похожи на, привычные, и хорошо известные, так сказать «родные» химические элементы? Тут пробирает сильное сомнение! Похоже, мы попадем совсем в другой «мир» и, похоже, что это «мир элементарных частиц». Понимание Химии как науки о качественных изменениях, которые ей сплошь и рядом сопутствуют, по мнению многих исследователей, составляющих всю «прелесть» и даже «волшебство» этой науки, стирающих грань между ней и «магией» (для очень многих даже сейчас, так или иначе, но не понятно различие Химии и Алхимии) – такое понимание в Периодической системе проявляется наиболее отчетливо, а в самом начале Системы просто ослепительно ярко! «Распространеннейшие в природе простые тела имеют малый атомный вес, а все элементы с малым атомным весом характеризуются резкостью свойств.
Вернемся к элементам легче водорода. Говорят, что их не нашли. А может, просто не искали? Или лучше сказать, когда нашли, просто не узнали!
Любому химику известны гомологические ряды, и хорошо известно, как ведут себя первые члены, особенно первый. Как известно первый всегда особенный. Он всегда сильно выделяется из общего ряда. Водород размещают и в I и в VII группах (он в чем-то подобен и щелочным металлам и галогенам одновременно). Так вот водород вовсе и не первый! Так как же должны отличаться настоящие первые элементы, элементы нулевого периода, от всех остальных, обычных элементов? Будут ли они вообще похожи на, привычные, и хорошо известные, так сказать «родные» химические элементы? Тут пробирает сильное сомнение! Похоже, мы попадем совсем в другой «мир» и, похоже, что это «мир элементарных частиц». Понимание Химии как науки о качественных изменениях, которые ей сплошь и рядом сопутствуют, по мнению многих исследователей, составляющих всю «прелесть» и даже «волшебство» этой науки, стирающих грань между ней и «магией» (для очень многих даже сейчас, так или иначе, но не понятно различие Химии и Алхимии) – такое понимание в Периодической системе проявляется наиболее отчетливо, а в самом начале Системы просто ослепительно ярко! «Распространеннейшие в природе простые тела имеют малый атомный вес, а все элементы с малым атомным весом характеризуются резкостью свойств. Они поэтому суть типические элементы», а по мере приближения к «нулевой точке» должны происходить просто фантастически «резкие» качественные скачки, что следует из ее сингулярного характера, так как «…здесь не только край системы, но и типические элементы, а потому можно ждать своеобразия и особенностей»!
Мы часто говорим о фундаментальности Периодического закона, но кажется, что по-настоящему этого все-таки не понимаем. Повторим Менделеева:
«… элементарные же вещества ныне немыслимы без подчинения их периодической законности» или «сущность понятий, вызывающих периодический закон, кроется в общем физико-химическом начале соответствия, превращаемости и эквивалентности сил природы», еще « по-видимому, периодическому закону – будущее не грозит разрушением, а только надстройки и развитие обещает».
Дмитрий Иванович верил, что сущность Периодического закона только начинает проявляться и очень надеялся на ее проявление в будущем:
«…тут я надеюсь на будущее. Поймут же, что найденное мной и
общо и важно для понимания всей природы и бесконечно малого…» -
писал Менделеев в последние годы жизни.
Они поэтому суть типические элементы», а по мере приближения к «нулевой точке» должны происходить просто фантастически «резкие» качественные скачки, что следует из ее сингулярного характера, так как «…здесь не только край системы, но и типические элементы, а потому можно ждать своеобразия и особенностей»!
Мы часто говорим о фундаментальности Периодического закона, но кажется, что по-настоящему этого все-таки не понимаем. Повторим Менделеева:
«… элементарные же вещества ныне немыслимы без подчинения их периодической законности» или «сущность понятий, вызывающих периодический закон, кроется в общем физико-химическом начале соответствия, превращаемости и эквивалентности сил природы», еще « по-видимому, периодическому закону – будущее не грозит разрушением, а только надстройки и развитие обещает».
Дмитрий Иванович верил, что сущность Периодического закона только начинает проявляться и очень надеялся на ее проявление в будущем:
«…тут я надеюсь на будущее. Поймут же, что найденное мной и
общо и важно для понимания всей природы и бесконечно малого…» -
писал Менделеев в последние годы жизни. Последуем же логике Дмитрия Ивановича, но учтем современные сведения, которые в его время просто еще не существовали. За основу возьмем порядковый номер элемента, который соответствует заряду ядра.Тогда, если водород имеет порядковый номер 1, то элемент перед ним, естественно, 0! Этот элемент окажется в нулевом периоде в группе инертных газов (в современной стандартной Периодической таблице) или в нулевой группе первого периода (по Менделееву), положение {1,0}, где {период, группа}. Формальный аналог благородных газов, инертный с формальным зарядом ядра 0.
Рассмотрим возможных кандидатов на это место в Периодической системе.
Выбор-то и не очень большой, но главное он есть! Из известных ныне физических объектов микромира это: либо нейтрон (попытка поставить нейтрон перед Водородом предпринималась другими авторами неоднократно и ранее, и для многих физиков и радиохимиков кажется совершенно очевидной), либо нейтрино (фотон как не имеющий массы покоя и короткоживущие частицы, а также гипотетический гравитон выведем пока за скобки).
Последуем же логике Дмитрия Ивановича, но учтем современные сведения, которые в его время просто еще не существовали. За основу возьмем порядковый номер элемента, который соответствует заряду ядра.Тогда, если водород имеет порядковый номер 1, то элемент перед ним, естественно, 0! Этот элемент окажется в нулевом периоде в группе инертных газов (в современной стандартной Периодической таблице) или в нулевой группе первого периода (по Менделееву), положение {1,0}, где {период, группа}. Формальный аналог благородных газов, инертный с формальным зарядом ядра 0.
Рассмотрим возможных кандидатов на это место в Периодической системе.
Выбор-то и не очень большой, но главное он есть! Из известных ныне физических объектов микромира это: либо нейтрон (попытка поставить нейтрон перед Водородом предпринималась другими авторами неоднократно и ранее, и для многих физиков и радиохимиков кажется совершенно очевидной), либо нейтрино (фотон как не имеющий массы покоя и короткоживущие частицы, а также гипотетический гравитон выведем пока за скобки). Кому отдавать предпочтение тоже воздержимся. Формально нас удовлетворяет и нейтрон и нейтрино. Перейдем пока к следующему элементу перед водородом, тоже элементу нулевого периода, но уже попадающему в первую группу нулевого периода и аналогу водороду. Но формальный порядковый номер его -1. И такой же заряд «ядра». Суммарный же заряд, как и у всех элементов должен быть нулевым. И на это место в Периодической системе есть законный кандидат. Это хорошо известный физикам и радиохимикам Позитроний (положение {0,1}). Кстати, он вообще–то очень похож на предсказанный Менделеевым «Короний», и, вполне, может наблюдаться на Звездах типа Солнца и других, особенно более горячих. Возможность возникновения связанных состояний системы электрон- позитрон была постулирована Мохоровичичем в 1934 г.[8,9], а название «позитроний» для атома электрон-позитрон предложено в 1945 г. Руарком [10] , химический символ – Ps – появился в работе Мак Гервея и де Бенедетти [11]. Эксперементальное доказательство существования позитрония получено впервые Дейчем [12,13].
Кому отдавать предпочтение тоже воздержимся. Формально нас удовлетворяет и нейтрон и нейтрино. Перейдем пока к следующему элементу перед водородом, тоже элементу нулевого периода, но уже попадающему в первую группу нулевого периода и аналогу водороду. Но формальный порядковый номер его -1. И такой же заряд «ядра». Суммарный же заряд, как и у всех элементов должен быть нулевым. И на это место в Периодической системе есть законный кандидат. Это хорошо известный физикам и радиохимикам Позитроний (положение {0,1}). Кстати, он вообще–то очень похож на предсказанный Менделеевым «Короний», и, вполне, может наблюдаться на Звездах типа Солнца и других, особенно более горячих. Возможность возникновения связанных состояний системы электрон- позитрон была постулирована Мохоровичичем в 1934 г.[8,9], а название «позитроний» для атома электрон-позитрон предложено в 1945 г. Руарком [10] , химический символ – Ps – появился в работе Мак Гервея и де Бенедетти [11]. Эксперементальное доказательство существования позитрония получено впервые Дейчем [12,13]. Итак, Позитроний (Ps) – система, состоящая из электрона и позитрона, удовлетворяет формальным требованиям элемента нулевого периода. То, что здесь трудно выделить, где ядро, а где оболочка, нас не смутит, так как мы ожидали ведь, что элементы нулевого периода будут необычными! Кроме того, как раз из-за симметричности Позитрония и других доводородных элементов в дальнейшем раскроются совершенно новые перспективы Периодической системы. Но не будем забегать вперед.
Вернемся, к элементу с нулевым порядковым номером в традиционной системе, но с положением {1,0} в системе Менделеева. Кто же это Нейтроний или Нейтриний? Кто же больше соответствует Ньютонию Менделеева? Прежде чем сделать выбор, давайте остановимся на одном факте, который нельзя игнорировать. Для простоты рассмотрения мы предложили в качестве кандидатов на нулевое положение нейтрон и нейтрино (как уже отмечалось выше, попытки включения в Периодическую систему неатомных частиц: нейтрона, электрона, позитрона и нейтрино – предпринимались ранее и подвергались обоснованной критике ), это просто элементарные частицы, а все другие химические элементы («атомы») это сложные системы, где присутствуют противоположные заряды, как кулоновские, так и другие (частицы и античастицы – электрон и позитрон, лептонный заряд).
Итак, Позитроний (Ps) – система, состоящая из электрона и позитрона, удовлетворяет формальным требованиям элемента нулевого периода. То, что здесь трудно выделить, где ядро, а где оболочка, нас не смутит, так как мы ожидали ведь, что элементы нулевого периода будут необычными! Кроме того, как раз из-за симметричности Позитрония и других доводородных элементов в дальнейшем раскроются совершенно новые перспективы Периодической системы. Но не будем забегать вперед.
Вернемся, к элементу с нулевым порядковым номером в традиционной системе, но с положением {1,0} в системе Менделеева. Кто же это Нейтроний или Нейтриний? Кто же больше соответствует Ньютонию Менделеева? Прежде чем сделать выбор, давайте остановимся на одном факте, который нельзя игнорировать. Для простоты рассмотрения мы предложили в качестве кандидатов на нулевое положение нейтрон и нейтрино (как уже отмечалось выше, попытки включения в Периодическую систему неатомных частиц: нейтрона, электрона, позитрона и нейтрино – предпринимались ранее и подвергались обоснованной критике ), это просто элементарные частицы, а все другие химические элементы («атомы») это сложные системы, где присутствуют противоположные заряды, как кулоновские, так и другие (частицы и античастицы – электрон и позитрон, лептонный заряд). Поэтому, подчиняясь закону сохранения зарядов, под Нейтринием будем понимать пару нейтрино и антинейтрино (сохранение нулевого лептонного заряда), а под Нейтронием- пару нейтрон и антинейтрон (сохранение нулевого барионного заряда). Отсюда видно, что ничего не надо выбирать, правда концепция «атома» несколько видоизменяется. Они (нейтрон и нейтрино в паре с их античастицами) оба нам подходят, и более того у них изотопическое соотношение, они отличаются только по массе. Просто они формально «изотопы». Также как, например, протий, дейтерий и тритий. Но, о каком же из этих «изотопов» все-таки говорил Менделеев? Тут все ясно, конечно же, Ньютоний Менделеева это Нейтриний! Надо вспомнить свойства Ньютония: чрезвычайно малая масса и практически полная инертность во взаимодействии с другими веществами.
«Чрезвычайно малая плотность газа, т.е. чрезвычайная быстрота
собственного движения его частиц – при ничтожном весе их, должны
влиять на то, что газ этот везде проникнет, будет наполнять
вселенную, но ни к чему прочно не примкнет – для согласованного
движения в химическом соединении, т.
Поэтому, подчиняясь закону сохранения зарядов, под Нейтринием будем понимать пару нейтрино и антинейтрино (сохранение нулевого лептонного заряда), а под Нейтронием- пару нейтрон и антинейтрон (сохранение нулевого барионного заряда). Отсюда видно, что ничего не надо выбирать, правда концепция «атома» несколько видоизменяется. Они (нейтрон и нейтрино в паре с их античастицами) оба нам подходят, и более того у них изотопическое соотношение, они отличаются только по массе. Просто они формально «изотопы». Также как, например, протий, дейтерий и тритий. Но, о каком же из этих «изотопов» все-таки говорил Менделеев? Тут все ясно, конечно же, Ньютоний Менделеева это Нейтриний! Надо вспомнить свойства Ньютония: чрезвычайно малая масса и практически полная инертность во взаимодействии с другими веществами.
«Чрезвычайно малая плотность газа, т.е. чрезвычайная быстрота
собственного движения его частиц – при ничтожном весе их, должны
влиять на то, что газ этот везде проникнет, будет наполнять
вселенную, но ни к чему прочно не примкнет – для согласованного
движения в химическом соединении, т. е. он ни с чем не соединится»
Все это отвечает паре нейтрино и антинейтрино, Нейтринию (Nn – масса близка 0 ), который можно рассматривать как «легкий Ньютоний»! И чрезвычайная быстрота собственного движения – близкая скорости света, и ничтожный вес – около 10(в -9 степени) , что соответствует предсказанию Менделеева, везде проникает, практически ни с чем не взаимодействует (Земля и даже Солнце для него почти прозрачны), и наполняет всю Вселенную (масса нейтрино во Вселенной, по некоторым моделям, в 30 раз больше плотности обычного вещества, хотя вопрос о его точной массе еще не получил окончательного ответа). Наиболее реальная оценка дает значение для массы <17 эВ .
Вообще, не понятно как может наше миропонимание «простых веществ», элементов Вселенной обходиться без Нейтриния-Ньютония, если претендовать, хоть на какую-то полноту взглядов на Мир. Нейтроний (Nn), «тяжелый Ньютоний», также один из самых распространенных во Вселенной (это вещество нейтронных звезд и возможно «черных дыр»).
е. он ни с чем не соединится»
Все это отвечает паре нейтрино и антинейтрино, Нейтринию (Nn – масса близка 0 ), который можно рассматривать как «легкий Ньютоний»! И чрезвычайная быстрота собственного движения – близкая скорости света, и ничтожный вес – около 10(в -9 степени) , что соответствует предсказанию Менделеева, везде проникает, практически ни с чем не взаимодействует (Земля и даже Солнце для него почти прозрачны), и наполняет всю Вселенную (масса нейтрино во Вселенной, по некоторым моделям, в 30 раз больше плотности обычного вещества, хотя вопрос о его точной массе еще не получил окончательного ответа). Наиболее реальная оценка дает значение для массы <17 эВ .
Вообще, не понятно как может наше миропонимание «простых веществ», элементов Вселенной обходиться без Нейтриния-Ньютония, если претендовать, хоть на какую-то полноту взглядов на Мир. Нейтроний (Nn), «тяжелый Ньютоний», также один из самых распространенных во Вселенной (это вещество нейтронных звезд и возможно «черных дыр»). На долю же классических химических элементов приходится лишь малая часть массы Вселенной. Все классическое химическое вещество по отношению к Нейтринию и Нейтронию это, образно говоря, все равно, что пена на берегу морей к самим морям. Или если прибегать к другому образному сравнению, то наш обычный атомно-молекулярный мир – это лишь отдельные маленькие островки в бесконечном океане Ньютония!
Нейтриний, Нейтроний и Позитроний, а вслед за ними и другие доводородные элементы (в том числе динейтрон, тетранейтрон и вообще нейтронное вещество, существование которого мы уже не имеем права игнорировать[16]) необходимо должны найти свое место в Периодической системе. Только с элементами нулевого периода Периодическая система получает свое «логическое завершение», если конечно не считать ее зеркального отражения по отношению опять же к нулевому периоду, где проглядываются все прочие Антиэлементы, т.е. химические элементы Антимира. Эта идея (зеркальности Периодической системы) высказывалась значительно ранее, и тоже кажется совершенно очевидной.
На долю же классических химических элементов приходится лишь малая часть массы Вселенной. Все классическое химическое вещество по отношению к Нейтринию и Нейтронию это, образно говоря, все равно, что пена на берегу морей к самим морям. Или если прибегать к другому образному сравнению, то наш обычный атомно-молекулярный мир – это лишь отдельные маленькие островки в бесконечном океане Ньютония!
Нейтриний, Нейтроний и Позитроний, а вслед за ними и другие доводородные элементы (в том числе динейтрон, тетранейтрон и вообще нейтронное вещество, существование которого мы уже не имеем права игнорировать[16]) необходимо должны найти свое место в Периодической системе. Только с элементами нулевого периода Периодическая система получает свое «логическое завершение», если конечно не считать ее зеркального отражения по отношению опять же к нулевому периоду, где проглядываются все прочие Антиэлементы, т.е. химические элементы Антимира. Эта идея (зеркальности Периодической системы) высказывалась значительно ранее, и тоже кажется совершенно очевидной. «Нулевая точка» отделяет Элементы от Антиэлементов, является границей Мира и Антимира, отражает грандиозный качественный скачок, что еще раз показывает ее сингулярность. То, что в нулевой период попадают симметричные относительно системы частица-античастица объекты (Нейтриний, Нейтроний, Позитроний), как нельзя лучше соответствует идее зеркальности Периодической системы, т.к. нулевой период в равной степени принадлежит как Системе атомов, так и Системе антиатомов. Следует заметить, что и «Цветок Менделеева-Шанкуртуа-Рязанцева» существует в двух асимметричных формах, «левой» и «правой» [17].
Так же, из диадной парадигмы Периодической системы следует необходимость удвоения первого периода и как следствие появление подобного ему нулевого периода [15,18].
Модификация концепции «атома»
Как уже отмечалось выше при таком решении проблемы «нулевых» несколько меняется концепция «атома». Конечно правы те, кто скажет, что Нейтриний и Нейтроний нельзя называть атомами в «привычном понимании», тем не менее Позитроний давно уже изучают как атомную систему, хотя он тоже мало напоминает традиционный атом.
«Нулевая точка» отделяет Элементы от Антиэлементов, является границей Мира и Антимира, отражает грандиозный качественный скачок, что еще раз показывает ее сингулярность. То, что в нулевой период попадают симметричные относительно системы частица-античастица объекты (Нейтриний, Нейтроний, Позитроний), как нельзя лучше соответствует идее зеркальности Периодической системы, т.к. нулевой период в равной степени принадлежит как Системе атомов, так и Системе антиатомов. Следует заметить, что и «Цветок Менделеева-Шанкуртуа-Рязанцева» существует в двух асимметричных формах, «левой» и «правой» [17].
Так же, из диадной парадигмы Периодической системы следует необходимость удвоения первого периода и как следствие появление подобного ему нулевого периода [15,18].
Модификация концепции «атома»
Как уже отмечалось выше при таком решении проблемы «нулевых» несколько меняется концепция «атома». Конечно правы те, кто скажет, что Нейтриний и Нейтроний нельзя называть атомами в «привычном понимании», тем не менее Позитроний давно уже изучают как атомную систему, хотя он тоже мало напоминает традиционный атом. Изучают не только сам Позитроний, но и его « химические соединения». Так что, необходимость наличия «ядра» в атоме совершенно не обязательна, также как, и большого время жизни. Может быть, также не обязательно наличие кулоновских зарядов, ведь могут быть и другие заряды (лептонные, барионные и др.). Главное в атоме: это сложная система, состоящая из элементарных частиц, в которой выполняется закон сохранения заряда вообще. Наличием же определенного физического размера совсем просто пожертвовать (Нейтроний и Нейтриний – это сложные нейтральные (зарядно) системы, не имеющие определенного размера). Есть два способа выйти из несколько затруднительного положения (но скорее непривычного):
1) просто назвать эти системы квази(псевдо?)-атомными (но это тривиально) или
2) несколько откорректировать понятие «атома» (более креативно).
Корректировка понятия «атома»
После принятия Резерфордовской модели атома, эта модель многократно корректировалась (Бор, Зоммерфельд, Шредингер, Борн и др.
Изучают не только сам Позитроний, но и его « химические соединения». Так что, необходимость наличия «ядра» в атоме совершенно не обязательна, также как, и большого время жизни. Может быть, также не обязательно наличие кулоновских зарядов, ведь могут быть и другие заряды (лептонные, барионные и др.). Главное в атоме: это сложная система, состоящая из элементарных частиц, в которой выполняется закон сохранения заряда вообще. Наличием же определенного физического размера совсем просто пожертвовать (Нейтроний и Нейтриний – это сложные нейтральные (зарядно) системы, не имеющие определенного размера). Есть два способа выйти из несколько затруднительного положения (но скорее непривычного):
1) просто назвать эти системы квази(псевдо?)-атомными (но это тривиально) или
2) несколько откорректировать понятие «атома» (более креативно).
Корректировка понятия «атома»
После принятия Резерфордовской модели атома, эта модель многократно корректировалась (Бор, Зоммерфельд, Шредингер, Борн и др. ). «Атом» постепенно обогащался частицами: электроном, протоном, нейтроном (рассматриваем пока только относительно стабильные частицы и постоянно присутствующие в нем, фотон как «квартирант» то появляется, то изчезает, но зато делает это очень часто) и «законами» их движения.
Но все-таки, можно рассматривать каждый «атом» состоящим из собственно атома (что сейчас мы понимаем под атомом) и его фотонного окружения, своеобразного «светового ореола» (нимба) вокруг него, не имеющего определенного размера:
A* = A + фотоны , где A* -множество возбужденных состояний атома (электронных и ядерных),
A –нормальное состояние атома,
фотоны – множество фотонов, соответствующих переходу из нормального состояния во множество возбужденных.
То есть было бы более последовательным, если бы рассматривали Периодическую систему не только основных состояний атома, а и всех возможных возбужденных состояний (электронных и ядерных), тогда в каждой клетке Таблицы были бы указаны энергии фотонов, соответствующие спектру (электронному и ядерному) каждого атома.
). «Атом» постепенно обогащался частицами: электроном, протоном, нейтроном (рассматриваем пока только относительно стабильные частицы и постоянно присутствующие в нем, фотон как «квартирант» то появляется, то изчезает, но зато делает это очень часто) и «законами» их движения.
Но все-таки, можно рассматривать каждый «атом» состоящим из собственно атома (что сейчас мы понимаем под атомом) и его фотонного окружения, своеобразного «светового ореола» (нимба) вокруг него, не имеющего определенного размера:
A* = A + фотоны , где A* -множество возбужденных состояний атома (электронных и ядерных),
A –нормальное состояние атома,
фотоны – множество фотонов, соответствующих переходу из нормального состояния во множество возбужденных.
То есть было бы более последовательным, если бы рассматривали Периодическую систему не только основных состояний атома, а и всех возможных возбужденных состояний (электронных и ядерных), тогда в каждой клетке Таблицы были бы указаны энергии фотонов, соответствующие спектру (электронному и ядерному) каждого атома. Это можно назвать «фотонным ореолом» (нимбом) атома, и реальный атом постоянно находится во взаимодействии со своим «фотонным нимбом», переходя из одного состояния в другое, естественно нимбы разных атомов не имеют определенного размера и всегда перекрываются. Это довольно просто, и не приводит к качественным изменениям (обмен фотонами не меняет природы атома). Не стоило бы об этом говорить, если бы кроме фотонного нимба вокруг каждого атома не было еще и других нимбов: нейтринного и антинейтринного. Но вот их поглощение или испускание не проходит бесследно для атома, ведет к его качественному изменению, он превращается в другой атом.
То, что один атом может превращаться в другой сейчас ни для кого не секрет. Но обычно этот механизм довольно хорошо представляют для радиоактивных атомов, а вот со стабильными немного сложнее, хотя и они могут превращаться в другие, взаимодействуя с элементарными частицами, например: поглощая нейтрино или антинейтрино (весь вопрос только в сечении реакции, но сейчас это не принципиально).
Это можно назвать «фотонным ореолом» (нимбом) атома, и реальный атом постоянно находится во взаимодействии со своим «фотонным нимбом», переходя из одного состояния в другое, естественно нимбы разных атомов не имеют определенного размера и всегда перекрываются. Это довольно просто, и не приводит к качественным изменениям (обмен фотонами не меняет природы атома). Не стоило бы об этом говорить, если бы кроме фотонного нимба вокруг каждого атома не было еще и других нимбов: нейтринного и антинейтринного. Но вот их поглощение или испускание не проходит бесследно для атома, ведет к его качественному изменению, он превращается в другой атом.
То, что один атом может превращаться в другой сейчас ни для кого не секрет. Но обычно этот механизм довольно хорошо представляют для радиоактивных атомов, а вот со стабильными немного сложнее, хотя и они могут превращаться в другие, взаимодействуя с элементарными частицами, например: поглощая нейтрино или антинейтрино (весь вопрос только в сечении реакции, но сейчас это не принципиально). Реакции под действием нейтрино протекают очень медленно и такие взаимодействия называются слабыми. Сечение слабого взаимодействия очень мало, и нужны огромные потоки нейтрино, чтобы зарегистрировать процесс взаимодействия нейтрино с веществом, поэтому только в 1956 году было доказано, что нейтрино существует. Ф. Райнесом впервые наблюдалась реакция взаимодействия нейтрино с протоном вблизи ядерного реактора. Хотя гипотеза о существовании нейтрино была высказана Паули еще в 1930 году, чтобы избежать нарушения закона сохранения, импульса и момента количества движения при бета– распаде. В настоящее время реакции нейтрино с нейтронами ядер являются основой всей «нейтринной астрономии». Главное сам факт, что все атомы могут превращаться друг в друга и это является собственным свойством самой Системы «атомов» и вся совокупность «атомов» представляет собой единую целостную Систему.
Реакции, лежащие в основе превращения радиоактивных атомов, связаны с превращениями протона в нейтрон в ядре и обратно:
p = n + e+ + нейтрино , n = p + e- + антинейтрино
где: p – протон, n – нейтрон, e+ – позитрон, e- – электрон, нейтрино, антинейтрино.
Реакции под действием нейтрино протекают очень медленно и такие взаимодействия называются слабыми. Сечение слабого взаимодействия очень мало, и нужны огромные потоки нейтрино, чтобы зарегистрировать процесс взаимодействия нейтрино с веществом, поэтому только в 1956 году было доказано, что нейтрино существует. Ф. Райнесом впервые наблюдалась реакция взаимодействия нейтрино с протоном вблизи ядерного реактора. Хотя гипотеза о существовании нейтрино была высказана Паули еще в 1930 году, чтобы избежать нарушения закона сохранения, импульса и момента количества движения при бета– распаде. В настоящее время реакции нейтрино с нейтронами ядер являются основой всей «нейтринной астрономии». Главное сам факт, что все атомы могут превращаться друг в друга и это является собственным свойством самой Системы «атомов» и вся совокупность «атомов» представляет собой единую целостную Систему.
Реакции, лежащие в основе превращения радиоактивных атомов, связаны с превращениями протона в нейтрон в ядре и обратно:
p = n + e+ + нейтрино , n = p + e- + антинейтрино
где: p – протон, n – нейтрон, e+ – позитрон, e- – электрон, нейтрино, антинейтрино. Это реакции соответствующие двум типам бета – распада, сопровождающиеся испусканием нейтрино или антинейтрино. Возможны реакции для стабильных атомов связанные с захватом нейтрино или антинейтрино (так называемый обратный бета – распад или точнее обратный бета – процесс):
p + антинейтрино = n + e+ , n + нейтрино = p + e –
За счет взаимных превращений протона и нейтрона, а также их античастиц все атомы и антиатомы окружены нейтринными и антинейтринными ореолами. Этот процесс наиболее интенсивно шел на первых этапах зарождения Вселенной (гипотеза Большого взрыва), а сейчас активно идет только на Звездах, но очень медленно он идет везде и всегда.
Пары нейтрино-антинейтрино, составляют Нейтриний («легкий» Ньютоний – эфир Менделеева), таким образом, все множество «атомов» погружено в эфир Менделеева – квазиинертной всюду проникающей среде, но все-таки способной взаимодействовать с ними, обеспечивая им взаимопревращаемость и целостное единство.
Таким образом, в общем случае «атом» можно рассматривать как:
систему элементарных частиц, в которой выполняются законы сохранения разных зарядов (алгебраическая сумма всех зарядов равна нулю) и которая структурно может состоять из следующих компонент: «тяжелой» барионной (нейтроны, протоны или их античастицы) основы (ядра) и «нетяжелой» лептонной (электрон, мюон, нейтрино или/и их античастицы) оболочки, причем лептонная оболочка подразделяется на «легкую» (электрон, мюон или/и позитрон, антимюон), имеющую кулоновские заряды и конечный средний радиус** и «сверхлегкую» (нейтрино и антинейтрино) оболочку, не имеющую кулоновских зарядов и конечного радиуса (фотонную оболочку как тривиальный случай не рассматриваем).
Это реакции соответствующие двум типам бета – распада, сопровождающиеся испусканием нейтрино или антинейтрино. Возможны реакции для стабильных атомов связанные с захватом нейтрино или антинейтрино (так называемый обратный бета – распад или точнее обратный бета – процесс):
p + антинейтрино = n + e+ , n + нейтрино = p + e –
За счет взаимных превращений протона и нейтрона, а также их античастиц все атомы и антиатомы окружены нейтринными и антинейтринными ореолами. Этот процесс наиболее интенсивно шел на первых этапах зарождения Вселенной (гипотеза Большого взрыва), а сейчас активно идет только на Звездах, но очень медленно он идет везде и всегда.
Пары нейтрино-антинейтрино, составляют Нейтриний («легкий» Ньютоний – эфир Менделеева), таким образом, все множество «атомов» погружено в эфир Менделеева – квазиинертной всюду проникающей среде, но все-таки способной взаимодействовать с ними, обеспечивая им взаимопревращаемость и целостное единство.
Таким образом, в общем случае «атом» можно рассматривать как:
систему элементарных частиц, в которой выполняются законы сохранения разных зарядов (алгебраическая сумма всех зарядов равна нулю) и которая структурно может состоять из следующих компонент: «тяжелой» барионной (нейтроны, протоны или их античастицы) основы (ядра) и «нетяжелой» лептонной (электрон, мюон, нейтрино или/и их античастицы) оболочки, причем лептонная оболочка подразделяется на «легкую» (электрон, мюон или/и позитрон, антимюон), имеющую кулоновские заряды и конечный средний радиус** и «сверхлегкую» (нейтрино и антинейтрино) оболочку, не имеющую кулоновских зарядов и конечного радиуса (фотонную оболочку как тривиальный случай не рассматриваем). Отсюда следует и некоторый фундаментальный мировоззренческий принцип, который всегда интуитивно присутствовал в нашем сознании (естествоиспытателей), но очень трудно формулировался: «атом» только в своей основе микроскопичен, а по существу он мегаскопичен, и его (каждого атома) реальные границы – это граница всего Мира! В этом и заключается единство Микро- и Мега Космоса, которое очень часто декларируют, но которое еще чаще ускользает от ясного осознания этого факта:
«…нет столь малого, от которого не зависело бы все крупнейшее».
В такой постановке вопроса, и Нейтриний, и Нейтроний, и тем более Позитроний, могут рассматриваться как частные случаи «атома» лишенного тех или иных компонент.
Нейтриний и Позитроний это «легкие» (лептонные***) «атомы», лишенные барионной компоненты.
Нейтроний это первый «тяжелый» (барионный****) «атом», лишенный лептонной компоненты.
Так как они находятся в самом основании Системы «атомов», некоторые исключения из общего случая для них вполне понятны.
Отсюда следует и некоторый фундаментальный мировоззренческий принцип, который всегда интуитивно присутствовал в нашем сознании (естествоиспытателей), но очень трудно формулировался: «атом» только в своей основе микроскопичен, а по существу он мегаскопичен, и его (каждого атома) реальные границы – это граница всего Мира! В этом и заключается единство Микро- и Мега Космоса, которое очень часто декларируют, но которое еще чаще ускользает от ясного осознания этого факта:
«…нет столь малого, от которого не зависело бы все крупнейшее».
В такой постановке вопроса, и Нейтриний, и Нейтроний, и тем более Позитроний, могут рассматриваться как частные случаи «атома» лишенного тех или иных компонент.
Нейтриний и Позитроний это «легкие» (лептонные***) «атомы», лишенные барионной компоненты.
Нейтроний это первый «тяжелый» (барионный****) «атом», лишенный лептонной компоненты.
Так как они находятся в самом основании Системы «атомов», некоторые исключения из общего случая для них вполне понятны. Еще раз вспомним, что первые всегда особенные и первые члены гомологического ряда всегда выбиваются из общей закономерности. В основании Системы качественные скачки просто грандиозны (сингулярная точка)! В «нулевой точке» многие параметры принимают нулевые, а их обратные величины бесконечные значения. Масса, зарядовые величины, потенциал ионизации стремятся к нулю, а вот размеры системы могут принимать бесконечные значения. Позитроний и Нейтриний похожи тем, что у них нет «ядра», но отсутствие ядра и не является сильным препятствием для признания их «атомами». Сложность для Нейтриния – это отсутствие кулоновских зарядов, которые характерны для всех традиционных атомов, а главное отсутствие определенных размеров и отсутствие практически массы, что и является главным психологическим барьеров на пути признания его «атомом». Но в этом-то и заключается грандиозность качественного скачка в «нулевой точке» – заряды и масса принимают нулевые значения, размеры становятся бесконечными и скорости световыми.
Еще раз вспомним, что первые всегда особенные и первые члены гомологического ряда всегда выбиваются из общей закономерности. В основании Системы качественные скачки просто грандиозны (сингулярная точка)! В «нулевой точке» многие параметры принимают нулевые, а их обратные величины бесконечные значения. Масса, зарядовые величины, потенциал ионизации стремятся к нулю, а вот размеры системы могут принимать бесконечные значения. Позитроний и Нейтриний похожи тем, что у них нет «ядра», но отсутствие ядра и не является сильным препятствием для признания их «атомами». Сложность для Нейтриния – это отсутствие кулоновских зарядов, которые характерны для всех традиционных атомов, а главное отсутствие определенных размеров и отсутствие практически массы, что и является главным психологическим барьеров на пути признания его «атомом». Но в этом-то и заключается грандиозность качественного скачка в «нулевой точке» – заряды и масса принимают нулевые значения, размеры становятся бесконечными и скорости световыми. Проведем «мысленный эксперимент»: Возьмем Позитроний и, не уменьшая его энергии, будем уменьшать величину кулоновских зарядов его составляющих от 1 до 0, что произойдет? Размеры системы будут расти от исходных, до бесконечных, потенциал ионизации от исходного до нуля, система из связанной станет свободной, т.е. получим Нейтриний, если еще массу составляющих уменьшим до нуля. Так что, самые
грандиозные резкие качественные изменения можно свести к постепенным
количественным, конечно «мысленно». Все другие последующие за ними (традиционные) атомы содержат и барионную и лептонную компоненты, к чему мы давно привыкли и лишь их обычно считаем «истинно химическими элементами» (барионно-лептонные атомы). По мере удаления от начала Системы и качественные скачки не так значительны и постепенно убывая, сходят на нет. Правда, из такого определения «атома» вытекает еще одно следствие, если строго придерживаться законов сохранения всех зарядов (алгебраическая сумма всех зарядов, кулоновских и других, равна нулю): строго говоря «обобщенный атом» – это всегда пара атом-антиатом*****.
Проведем «мысленный эксперимент»: Возьмем Позитроний и, не уменьшая его энергии, будем уменьшать величину кулоновских зарядов его составляющих от 1 до 0, что произойдет? Размеры системы будут расти от исходных, до бесконечных, потенциал ионизации от исходного до нуля, система из связанной станет свободной, т.е. получим Нейтриний, если еще массу составляющих уменьшим до нуля. Так что, самые
грандиозные резкие качественные изменения можно свести к постепенным
количественным, конечно «мысленно». Все другие последующие за ними (традиционные) атомы содержат и барионную и лептонную компоненты, к чему мы давно привыкли и лишь их обычно считаем «истинно химическими элементами» (барионно-лептонные атомы). По мере удаления от начала Системы и качественные скачки не так значительны и постепенно убывая, сходят на нет. Правда, из такого определения «атома» вытекает еще одно следствие, если строго придерживаться законов сохранения всех зарядов (алгебраическая сумма всех зарядов, кулоновских и других, равна нулю): строго говоря «обобщенный атом» – это всегда пара атом-антиатом*****. Но это и не вызывает удивления, если учитывать «зеркальность» Периодической системы, и симметричность Мира-Антимира. Может быть, точнее, сказать: химический элемент – это пара атом-антиатом, т.к. по своим химическим свойствам они неразличимы. Казалось бы, всего лишь небольшое «расширение» понятия атома, а какие далеко идущие последствия, об этом говорил еще Нильс Бор: «расширение системы понятий дает надлежащие средства… для расширения объективного описания». В механизме рождения и взаимопревращений, единства всех «атомов» существенна роль не только Нейтриния – «легкого» Ньютония – Эфира Менделеева, но и Нейтрония – «тяжелого» Ньютония. Нейтрон участвует и обеспечивает множество процессов, ведущих к рождению и взаимопревращению «атомов», начиная с процесса собственного распада и рождения Водорода (первого атома), проходя через реакции синтеза и деления, испускания и захвата, и заканчивая образованием нейтронных звезд (последних «атомов» в эволюции химических элементов), а может и далее, чего мы пока не знаем и не догадываемся.
Но это и не вызывает удивления, если учитывать «зеркальность» Периодической системы, и симметричность Мира-Антимира. Может быть, точнее, сказать: химический элемент – это пара атом-антиатом, т.к. по своим химическим свойствам они неразличимы. Казалось бы, всего лишь небольшое «расширение» понятия атома, а какие далеко идущие последствия, об этом говорил еще Нильс Бор: «расширение системы понятий дает надлежащие средства… для расширения объективного описания». В механизме рождения и взаимопревращений, единства всех «атомов» существенна роль не только Нейтриния – «легкого» Ньютония – Эфира Менделеева, но и Нейтрония – «тяжелого» Ньютония. Нейтрон участвует и обеспечивает множество процессов, ведущих к рождению и взаимопревращению «атомов», начиная с процесса собственного распада и рождения Водорода (первого атома), проходя через реакции синтеза и деления, испускания и захвата, и заканчивая образованием нейтронных звезд (последних «атомов» в эволюции химических элементов), а может и далее, чего мы пока не знаем и не догадываемся. По современным теориям астросинтеза химических элементов, особенно тяжелых (>Fe), роль нейтрон просто исключительна. Можно утверждать, что вся Система «тяжелых» (барионных) «атомов» начинается и заканчивается Нейтронием – «тяжелым» Ньютонием, да и все традиционные химические Элементы можно рассматривать всего лишь как определенные состояния изотопов Нейтрония. Именно Нейтроний рождает первый элемент стандартной Периодической системы – Водород и симметрично ему первый элемент Антимира – Антиводород. И именно, «супертяжелым» Нейтронием заканчивается симметричная Периодическая система химических элементов! А в астрономии «супертяжелым» Нейтронием заканчивается эволюция некоторых Звезд!
Нейтроний и Нейтриний оказываются как раз теми основными «элементами» (хотя их трудно и не привычно назвать «химическими»*), которые порождают или участвуют в рождении всех остальных элементов Периодической системы и которые являются тем «цементом», который связывает в единое Целое всю Систему атомов и всю нашу Вселенную.
По современным теориям астросинтеза химических элементов, особенно тяжелых (>Fe), роль нейтрон просто исключительна. Можно утверждать, что вся Система «тяжелых» (барионных) «атомов» начинается и заканчивается Нейтронием – «тяжелым» Ньютонием, да и все традиционные химические Элементы можно рассматривать всего лишь как определенные состояния изотопов Нейтрония. Именно Нейтроний рождает первый элемент стандартной Периодической системы – Водород и симметрично ему первый элемент Антимира – Антиводород. И именно, «супертяжелым» Нейтронием заканчивается симметричная Периодическая система химических элементов! А в астрономии «супертяжелым» Нейтронием заканчивается эволюция некоторых Звезд!
Нейтроний и Нейтриний оказываются как раз теми основными «элементами» (хотя их трудно и не привычно назвать «химическими»*), которые порождают или участвуют в рождении всех остальных элементов Периодической системы и которые являются тем «цементом», который связывает в единое Целое всю Систему атомов и всю нашу Вселенную. Настало время признать реальность, предсказанного Д.И. Менделеевым тринадцатого неизвестного элемента, Ньютония (Нейтриния и Нейтрония), а вместе с ним и существование нулевого периода, и очередную правоту великого ученого, даже как казалось, в «очевидной ошибке».
Ньютоний и без нашего признания является основным и, абсолютно преобладающим, Элементом Вселенной, несмотря на нашу абсолютную слепоту!
Посмотрим, что об этом думают современные физики:
« Основными проблемами астрофизики элементарных частиц являются существование темной материи, ее состав и детектирование, дефицит солнечных нейтрино, нейтрино от сверхновых, проблема физического вакуума.
В настоящее время трудно установить доли разных компонент материи во Вселенной. Один из возможных вариантов, встречающийся в разных моделях, оценивает эти доли следующим образом (с точностью примерно 10%): вакуум (60%), темная материя (38%), обычная материя (2%), излучение (10-4%).
Основной вклад в полную плотность материи во Вселенной вносит темная материя (Dark Matter – DM).
Настало время признать реальность, предсказанного Д.И. Менделеевым тринадцатого неизвестного элемента, Ньютония (Нейтриния и Нейтрония), а вместе с ним и существование нулевого периода, и очередную правоту великого ученого, даже как казалось, в «очевидной ошибке».
Ньютоний и без нашего признания является основным и, абсолютно преобладающим, Элементом Вселенной, несмотря на нашу абсолютную слепоту!
Посмотрим, что об этом думают современные физики:
« Основными проблемами астрофизики элементарных частиц являются существование темной материи, ее состав и детектирование, дефицит солнечных нейтрино, нейтрино от сверхновых, проблема физического вакуума.
В настоящее время трудно установить доли разных компонент материи во Вселенной. Один из возможных вариантов, встречающийся в разных моделях, оценивает эти доли следующим образом (с точностью примерно 10%): вакуум (60%), темная материя (38%), обычная материя (2%), излучение (10-4%).
Основной вклад в полную плотность материи во Вселенной вносит темная материя (Dark Matter – DM). Доля обычного вещества составляет малую часть полной плотности материи во Вселенной. Предполагают, что темную материю составляют частицы, не обнаруживающие себя путем испускания фотонов. Среди них первое место занимает массивное нейтрино.
Рассматривают два вида темной материи: горячая темная материя, которая состоит из релятивистских частиц, и холодная темная материя, которая состоит из очень тяжелых нерелятивистских частиц. Изучение структуры темной материи играет важную роль в понимании эволюции Вселенной.
Проблема темной материи тесно связана с проблемой физического вакуума. Вакуум – это среда с очень сложной структурой, которая изменяется в ходе эволюции Вселенной и которую можно перестраивать путем изменения состояния материи, взаимодействующей с вакуумом. В физическом вакууме происходит концентрация энергии в малых областях пространства. Вакуум является характеристикой пространства-времени. Вопрос о составе физического вакуума непрерывно изучается. В его состав могут входить различные физические поля.
Доля обычного вещества составляет малую часть полной плотности материи во Вселенной. Предполагают, что темную материю составляют частицы, не обнаруживающие себя путем испускания фотонов. Среди них первое место занимает массивное нейтрино.
Рассматривают два вида темной материи: горячая темная материя, которая состоит из релятивистских частиц, и холодная темная материя, которая состоит из очень тяжелых нерелятивистских частиц. Изучение структуры темной материи играет важную роль в понимании эволюции Вселенной.
Проблема темной материи тесно связана с проблемой физического вакуума. Вакуум – это среда с очень сложной структурой, которая изменяется в ходе эволюции Вселенной и которую можно перестраивать путем изменения состояния материи, взаимодействующей с вакуумом. В физическом вакууме происходит концентрация энергии в малых областях пространства. Вакуум является характеристикой пространства-времени. Вопрос о составе физического вакуума непрерывно изучается. В его состав могут входить различные физические поля. Известно, что средняя энергия физического вакуума не равна нулю. Вакуум может являться частью темной материи.»
Л.И. Сарычева [7]
Видно, что Ньютоний Менделеева своим «легким» изотопом, Нейтринием обеспечивает заполняемость Вселенной горячей темной материей, а своим «тяжелым» изотопом, Нейтронием – холодной темной материей.
Как мог заметить внимательный Читатель, у нас осталась пустой абсолютная нулевая точка (0 –период, 0 – группа, положение {0,0}) – что же там?
Многие серьезные исследователи, совершенно справедливо, призывают с недоверием относится ко всяким сингулярным состояниям. Конечно, когда-нибудь надо сделать последний шаг, но давайте не будем спешить. Сделаем только несколько осторожных предположений: Позитроний занимает 0 –период, 1 – группу (положение{0,1}), Нейтриний мы предварительно разместили в 0 –группе 1 – периода (положение {1,0}) вместе с Нейтронием, исходя из того, что обладает пусть и не большой, но массой и его логично рассматривать как изотоп Нейтрония.
Известно, что средняя энергия физического вакуума не равна нулю. Вакуум может являться частью темной материи.»
Л.И. Сарычева [7]
Видно, что Ньютоний Менделеева своим «легким» изотопом, Нейтринием обеспечивает заполняемость Вселенной горячей темной материей, а своим «тяжелым» изотопом, Нейтронием – холодной темной материей.
Как мог заметить внимательный Читатель, у нас осталась пустой абсолютная нулевая точка (0 –период, 0 – группа, положение {0,0}) – что же там?
Многие серьезные исследователи, совершенно справедливо, призывают с недоверием относится ко всяким сингулярным состояниям. Конечно, когда-нибудь надо сделать последний шаг, но давайте не будем спешить. Сделаем только несколько осторожных предположений: Позитроний занимает 0 –период, 1 – группу (положение{0,1}), Нейтриний мы предварительно разместили в 0 –группе 1 – периода (положение {1,0}) вместе с Нейтронием, исходя из того, что обладает пусть и не большой, но массой и его логично рассматривать как изотоп Нейтрония. Но вопрос о массе нейтрино окончательно не решен, и если у него окажется нулевая масса, то тогда и место его не {1.0}, а {0,0}. Возможно, на положение {0,0} могут претендовать также Фотон и даже Гравитон или, сделаем смелое предположение: в ортогональных измерениях в этой точке находятся вообще все элементарные частицы и в этой точке смыкаются Система химических элементов и Система элементарных частиц, появляется Единая Периодическая Система.
В заключение хочется еще раз привести слова Дмитрия Ивановича:
«Я и смотрю на свою далекую от полноты попытку понять природу мирового эфира с реально химической стороны не более, как на выражение суммы накопившихся у меня впечатлений, вырывающихся исключительно лишь по той причине, что мне не хочется, чтобы мысли, навеваемые действительностью, пропадали. Вероятно, что подобные же мысли приходили многим, но, пока они не изложены, они легко и часто исчезают и не развиваются, не влекут за собой постепенного накопления достоверного, которое одно сохраняется.
Но вопрос о массе нейтрино окончательно не решен, и если у него окажется нулевая масса, то тогда и место его не {1.0}, а {0,0}. Возможно, на положение {0,0} могут претендовать также Фотон и даже Гравитон или, сделаем смелое предположение: в ортогональных измерениях в этой точке находятся вообще все элементарные частицы и в этой точке смыкаются Система химических элементов и Система элементарных частиц, появляется Единая Периодическая Система.
В заключение хочется еще раз привести слова Дмитрия Ивановича:
«Я и смотрю на свою далекую от полноты попытку понять природу мирового эфира с реально химической стороны не более, как на выражение суммы накопившихся у меня впечатлений, вырывающихся исключительно лишь по той причине, что мне не хочется, чтобы мысли, навеваемые действительностью, пропадали. Вероятно, что подобные же мысли приходили многим, но, пока они не изложены, они легко и часто исчезают и не развиваются, не влекут за собой постепенного накопления достоверного, которое одно сохраняется. Если в них есть хоть часть природной правды, которую мы все ищем, попытка моя не напрасна, ее разработают, дополнят и поправят, а если моя мысль неверна в основаниях, ее изложение, после того или иного вида опровержения, предохранит других от повторения. Другого пути для медленного, но прочного движения вперед я не знаю»
*) – как видно Химия для Д.И. Менделеева имела значительно более удаленные границы, чем те, которые ей отводят сейчас.
**) – кулоновский ион может быть примером «атома» с «легкой» лептонной оболочкой, не имеющей конечного радиуса.
***) – к «лептонным» атомам может быть отнесен и Мюоний (Mu-система ;+;- ), он «изотопичен» Позитронию (Ps), и может превращаться в него при распаде мюона на электрон и нейтрина.
****) – к «барионным» атомам лишенным лептонной оболочки может быть отнесен Протоний (система р+р-) и другие подобные системы, таким образом чисто лептонные и чисто барионные атомы достаточно многочисленны.
*****) – в системе сохранения полного заряда (кулоновского, барионного, лептонного и др.
Если в них есть хоть часть природной правды, которую мы все ищем, попытка моя не напрасна, ее разработают, дополнят и поправят, а если моя мысль неверна в основаниях, ее изложение, после того или иного вида опровержения, предохранит других от повторения. Другого пути для медленного, но прочного движения вперед я не знаю»
*) – как видно Химия для Д.И. Менделеева имела значительно более удаленные границы, чем те, которые ей отводят сейчас.
**) – кулоновский ион может быть примером «атома» с «легкой» лептонной оболочкой, не имеющей конечного радиуса.
***) – к «лептонным» атомам может быть отнесен и Мюоний (Mu-система ;+;- ), он «изотопичен» Позитронию (Ps), и может превращаться в него при распаде мюона на электрон и нейтрина.
****) – к «барионным» атомам лишенным лептонной оболочки может быть отнесен Протоний (система р+р-) и другие подобные системы, таким образом чисто лептонные и чисто барионные атомы достаточно многочисленны.
*****) – в системе сохранения полного заряда (кулоновского, барионного, лептонного и др. ) обычный атом – это барионно-лептонный ион (катион), а антиатом – барионно-лептонный анион. Только пара атом-антиатом составляет собственно нейтральный «обобщенный атом». Потенциал ионизации «обобщенного атома» (атома и антиатома) равен нулю, а его размеры бесконечности.
) обычный атом – это барионно-лептонный ион (катион), а антиатом – барионно-лептонный анион. Только пара атом-антиатом составляет собственно нейтральный «обобщенный атом». Потенциал ионизации «обобщенного атома» (атома и антиатома) равен нулю, а его размеры бесконечности.- Добавил в систему: Рязанцев Георгий Борисович
ТЕМАТИЧЕСКИЙ ТЕСТ “ПЕРИОДИЧЕСКАЯ ТАБЛИЦА Д.И.МЕНДЕЛЕЕВА”
1 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Ряд химических элементов периодической системы Д.И. Менделеева,
начинающийся щелочным металлом и заканчивающийся инертным газом, называется:
1) группой 2) подгруппой 3) периодом 4) периодическим законом
2. В IV периоде главной подгруппы
(А) V группы находится элемент с
порядковым номером:
В IV периоде главной подгруппы
(А) V группы находится элемент с
порядковым номером:
1) 33 2) 23 3) 50 4) 75
3. Общим для элементов подгруппы II группы является:
1) число электронных слоев 2) высшая валентность
3) число электронов в атоме 4) величина зарядов ядер
4. Номер периода периодической таблицы определяет:
1) высшую валентность атома 2) число электронов в атоме
3) число протонов в ядре 4) число электронных слоев в атоме
5. Изотопы хлора 35CI и 37CI различаются
1) числом электронов 2) числом нейтронов 3) числом протонов 4) зарядом ядра атома
6. Указать распределение электронов в атоме магния:
1) +12 Mg )2 )8 )2 2) +12Mg )2 )2 3) +12Mg )2 )8 )4 4) +12Mg )2 )8
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) водорода 2) магния 3) кальция 4) калия
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) хлора 2) серы 3) кремния 4) кальция
9. Заряд ядра атома натрия: 1) +1 2) +3 3) +23 4) +11
10. Число нейтронов в атоме изотопа фосфора 31Р: 1) 5 2) 15 3) 16 4) 31
11. Установить соответствие между химическим элементом и его положением в Периодической системе. ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) Fe а) IV период, VII группа, главная (А) подгруппа
2) F б) IV период, VII группа, побочная (Б) подгруппа
3) Mn в) II период, VII группа, главная (А) подгруппа
4) Br г) IV период, VIII группа, побочная (Б) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ, ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 3 а) S2-
2) 2, 8, 8 б) Ne
3) 2, 8 в) AI
4) 2, 5 г) N
13. Записать название изотопа элемента с массовым числом 37, в ядре атома
которого находится 20 протонов. Ответ: _____
2 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Элементы с одинаковой высшей валентностью и сходными свойствами образуют:
1) группу 2) подгруппу 3) ряд 4) период
2. В IV периоде побочной подгруппы
(Б) VI группы находится элемент с
В IV периоде побочной подгруппы
(Б) VI группы находится элемент с
порядковым номером: 1) 34 2) 32 3) 24 4) 22
3. Общим в строении атомов элементов III периода является:
1) число валентных электронов 2) число электронных слоев
3) число электронов в атоме 4) величина зарядов ядер атомов
4. Номер группы в периодической таблице равен:
1) высшей валентности атома 2) числу электронов в атоме
3) числу протонов в ядре 4) числу электронных слоев
5. Атомы изотопов углерода 12С и 13С различаются числом:
1) нейтронов 2) электронов 3) протонов 4) электронов на внешнем слое
6. Указать распределение электронов в атоме серы:
1) +16 S )2 )8 )8 2) +16 S )2 )8 )6 3) +16 S )2 )8 )4 4) +16 S )2 )8 )3
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) бор 2) магния 3) бериллий 4) алюминий
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) хлора 2) фтор 3) бром 4) марганец
9. Заряд ядра атома фосфора: 1) +3 2) +5 3) +15 4) +31
10. Число нейтронов в атоме изотопа кислорода 18О: 1) 6 2) 8 3) 10 4) 16
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) Cu а) II период, V группа, главная (А) подгруппа
2) Mg б) IV период, II группа, главная (А) подгруппа
3) N в) III период, II группа, главная (А) подгруппа
4) Ca г) IV период, I группа, побочная (Б) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ, ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 4 а) AI3+
2) 2, 8, 8 б) Si
3) 2, 8 в) Ar
4) 2, 8, 8, 1 г) К
13. Записать название изотопа элемента с массовым числом 37, в ядре атома
которого находится 17 протонов. Ответ: __________
3 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Ряд химических элементов периодической системы Д.И. Менделеева, начинающийся щелочным металлом и заканчивающийся инертным газом, состоит из двух рядов, называется:
1) группой 2) подгруппой 3) малым периодом 4) большим периодом
2. В IV периоде побочной подгруппы
(В) V группы находится элемент с
В IV периоде побочной подгруппы
(В) V группы находится элемент с
порядковым номером: 1) 33 2) 23 3) 50 4) 75
3. Общим для элементов главной подгруппы IV группы является:
1) число электронных слоев 2) высшая валентность
3) число электронов в атоме 4) величина зарядов ядер
4. Номер группы периодической таблицы определяет:
1) число электронов на последнем электронном слое 2) число электронов в атоме
3) число протонов в ядре 4) число электронных слоев в атоме
5. Изотопы цинка 64Zn и 66Zn различаются:
1) числом электронов 2) числом нейтронов 3) числом протонов 4) зарядом ядра атома
6. Указать распределение электронов в атоме алюминия:
1) +13 AI )2 )8 )3 2) +13AI )2 )2 3) +13AI )2 )3 )8 4) +13AI )2 )8
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) бора 2) магния 3) алюминия 4) калия
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) кислорода 2) серы 3) фтора 4) кальция
9. Заряд ядра атома лития: 1) +1 2) +3 3) +23 4) +11
10. Число нейтронов в атоме изотопа цинка 65Zn: 1) 25 2) 35 3) 16 4) 31
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) S а) III период, IV группа, главная (А) подгруппа
2) Cr б) IV период, VI группа, главная (А) подгруппа
3) Se в) IVпериод, VI группа, побочная (Б) подгруппа
4) Si г) III период, VI группа, главная (А) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ, ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 5 а) S4-
2) 2, 8, 2 б) Ar
3) 2, 8,8 в) P
4) 2, 6 г) O
13. Записать название изотопа элемента с массовым числом 80, в ядре атома
которого находится 34 протонов. Ответ: _______________
4 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Химические элементы, проявляют типичные металлические свойства, располагаются:
1) в 1-3 группе 2) в одной подгруппе 3) в четных рядах 4) в одном периоде
2. В IV периоде главной подгруппы (А)
VII группы находится элемент с
порядковым номером:
В IV периоде главной подгруппы (А)
VII группы находится элемент с
порядковым номером:
1) 17 2) 32 3) 35 4) 26
3. Общим в строении атомов элементов III периода является:
1) число валентных электронов 2) число электронных слоев
3) число электронов в атоме 4) величина зарядов ядер атомов
4. Номер II группы в периодической таблице равен:
1) высшей валентности атома 2) числу электронов в атоме
3) числу протонов в ядре 4) числу электронных слоев
5. Атомы изотопов селена 78Se и 80Se различаются числом:
1) нейтронов 2) электронов 3) протонов 4) электронов на внешнем слое
6. Указать распределение электронов в атоме фосфора:
1) +15 Р )2 )8 )8 2) +15 Р )2 )8 )5 3) +31 Р )2 )8 )5 4) +15 S )2 )8 )8
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) кислород 2) сера 3) натрий 4) калий
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) алюминий 2) кремний 3) фосфор 4) кальций
9. Заря ядра атома бора: 1) +3 2) +5 3) +11 4) +12
10. Число нейтронов в атоме изотопа кислорода 17О: 1) 6 2) 9 3) 8 4) 18
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) Mn а) III период, V группа, главная (А) подгруппа
2) Mg б) IV период, II группа, главная (А) подгруппа
3) P в) III период, II группа, главная (А) подгруппа
4) Ca г) IV период, VII группа, побочная (Б) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 4 а) Mg2+
2) 2, 8, 8 б) Si
3) 2, 8 в) Ar
4) 2, 8, 8, 1 г) К
13. Записать название изотопа элемента с массовым числом 23, в ядре атома
которого находится 11 протонов. Ответ: ________________
5 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Ряд химических элементов периодической системы Д.И. Менделеева,
начинающийся щелочным металлом и заканчивающийся щелочным металлом, называется:
1) группой 2) подгруппой 3) периодом 4) периодическим законом
2. В V периоде главной подгруппы
(А) I группы находится элемент с
порядковым номером:
В V периоде главной подгруппы
(А) I группы находится элемент с
порядковым номером:
1) 33 2) 23 3) 47 4) 37
3. Общим для элементов подгруппы III группы является:
1) число электронных слоев 2) высшая валентность
3) число электронов в атоме 4) величина зарядов ядер
4. Номер периода периодической таблицы определяет:
1) высшую валентность атома 2) число электронов в атоме
3) число протонов в ядре 4) число электронных слоев в атоме
5. Изотопы меди 63Cu и 65Cu различаются
1) числом электронов 2) числом нейтронов 3) числом протонов 4) зарядом ядра атома
6. Указать распределение электронов в атоме натрия:
1) +11 Na )2 )8 )2 2) +11 Na )8 )3 3) +11 Na )2 )8 )1 4) +16 Na )8 )8
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) хлора 2) магния 3) лития 4) калия
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) хлора 2) серы 3) кремния 4) кальция
9. Заряд ядра атома натрия: 1) +1 2) +3 3) +23 4) +11
10. Число нейтронов в атоме изотопа фосфора 31Р: 1) 5 2) 15 3) 16 4) 31
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) Co а) V период, VII группа, главная (А) подгруппа
2) F б) IV период, VII группа, побочная (Б) подгруппа
3) Mn в) II период, VII группа, главная (А) подгруппа
4) I г) IV период, VIII группа, побочная (Б) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 3 а) S6+
2) 2, 8, 18, 8 б) Kr
3) 2, 8 в) AI
4) 2, 5 г) N
13. Записать название изотопа элемента с массовым числом 120, в ядре атома которого находится
50 протонов. Ответ: ______________________
6 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Элементы с одинаковой высшей валентностью и сходными свойствами образуют:
1) группу 2) подгруппу 3) ряд 4) период
2. В IV периоде побочной главной (А)
I группы находится элемент с
порядковым номером:
В IV периоде побочной главной (А)
I группы находится элемент с
порядковым номером:
1) 19 2) 29 3) 39 4) 64
3. Общим в строении атомов элементов I периода является:
1) число валентных электронов 2) число электронных слоев
3) число электронов в атоме 4) величина зарядов ядер атомов
4. Номер группы в периодической таблице равен:
1) высшей валентности атома 2) числу электронов в атоме
3) числу протонов в ядре 4) числу электронных слоев
5. Атомы изотопов олова 120 Sn и 122 Sn различаются числом:
1) нейтронов 2) электронов 3) протонов 4) электронов на внешнем слое
6. Указать распределение электронов в атоме кремния:
1) +14 Si )2 )8 )4 2) +14 Si )2 )7 )5 3) +14 Si )2 )8 )1 4) +14 Si )2 )8 )3
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) азот 2) фосфор 3) бериллий 4) алюминий
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) хлора 2) азот 3) бром 4) железо
9. Заряд ядра атома олова: 1) +35 2) +50 3) +55 4) +31
10. Число нейтронов в атоме изотопа кислорода 18О: 1) 6 2) 8 3) 10 4) 16
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) Мо а) II период, VI группа, главная (А) подгруппа
2) Sr б) IV период, II группа, главная (А) подгруппа
3) О в) Vпериод, I группа, главная (А) подгруппа
4) К г) V период, VI группа, побочная (Б) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ, ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 4 а) AI3+
2) 2, 8, 8 б) Si
3) 2, 8 в) Ar
4) 2, 8, 8, 1 г) К
13. Записать название изотопа элемента с массовым числом 37, в ядре атома
которого находится 17 протонов. Ответ: ____________________________
7 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Ряд химических элементов периодической системы Д.И. Менделеева, начинающийся щелочным металлом и заканчивающийся инертным газом, состоит из двух рядов, называется:
1) группой 2) подгруппой 3) малым периодом 4) большим периодом
2. В IV периоде побочной подгруппы
(В) V группы находится элемент с
В IV периоде побочной подгруппы
(В) V группы находится элемент с
порядковым номером: 1) 33 2) 23 3) 50 4) 75
3. Общим для элементов главной подгруппы IV группы является:
1) число электронных слоев 2) высшая валентность
3) число электронов в атоме 4) величина зарядов ядер
4. Номер группы периодической таблицы определяет:
1) число электронов на последнем электронном слое 2) число электронов в атоме
3) число протонов в ядре 4) число электронных слоев в атоме
5. Изотопы цинка 64Zn и 66Zn различаются:
1) числом электронов 2) числом нейтронов 3) числом протонов 4) зарядом ядра атома
6. Указать распределение электронов в атоме алюминия:
1) +13 AI )2 )8 )3 2) +13AI )2 )2 3) +13AI )2 )3 )8 4) +13AI )2 )8
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) бора 2) магния 3) алюминия 4) калия
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) кислорода 2) серы 3) фтора 4) кальция
9. Заряд ядра атома лития: 1) +1 2) +3 3) +23 4) +11
10. Число нейтронов в атоме изотопа цинка 65Zn: 1) 25 2) 35 3) 16 4)31
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) S а) III период, IV группа, главная (А) подгруппа
2) Cr б) IV период, VI группа, главная (А) подгруппа
3) Se в) IVпериод, VI группа, побочная (Б) подгруппа
4) Si г) III период, VI группа, главная (А) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ, ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 5 а) S4-
2) 2, 8, 2 б) Ar
3) 2, 8,8 в) P
4) 2, 6 г) O
13. Записать название изотопа элемента с массовым числом 80, в ядре атома которого находится 34 протонов. Ответ: ____________________________
8 вариант Периодический закон Д.И. Менделеева Тематический тест
1. Химические элементы, проявляют типичные металлические свойства, располагаются:
1) в 1-3 группе 2) в одной подгруппе 3) в четных рядах 4) в одном периоде
2. В IV периоде главной подгруппы (А)
VII группы находится элемент с
порядковым номером:
В IV периоде главной подгруппы (А)
VII группы находится элемент с
порядковым номером:
1) 17 2) 32 3) 35 4) 25
3. Общим в строении атомов элементов II периода является:
1) число валентных электронов 2) число электронных слоев
3) число электронов в атоме 4) величина зарядов ядер атомов
4. Номер II группы в периодической таблице равен:
1) высшей валентности атома 2) числу электронов в атоме
3) числу протонов в ядре 4) числу электронных слоев
5. Атомы изотопов селена 78Se и 80Se различаются числом:
1) нейтронов 2) электронов 3) протонов 4) электронов на внешнем слое
6. Указать распределение электронов в атоме фосфора:
1) +15 Р )2 )8 )8 2) +15 Р )2 )8 )5 3) +31 Р )2 )8 )5 4) +15 S )2 )8 )8
7. Наиболее ярко выражены металлические свойства у элемента:
Наиболее ярко выражены металлические свойства у элемента:
1) кислород 2) сера 3) натрий 4) калий
8. Наиболее ярко выражены неметаллические свойства у элемента:
1) алюминий 2) кремний 3) фосфор 4) кальций
9. Заряд ядра атома бора: 1) +3 2) +5 3) +11 4) +12
10. Число нейтронов в атоме изотопа кислорода 17О: 1) 6 2) 9 3) 8 4) 18
11. Установить соответствие между химическим элементом и его положением
в Периодической системе.
ЭЛЕМЕНТ ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
1) Cr а) II период, V группа, главная (А) подгруппа
2) Mg б) IV период, II группа, главная (А) подгруппа
3) N в) III период, II группа, главная (А) подгруппа
4) Ca г) IV период, VI группа, побочная (Б) подгруппа
12. Установить соответствие
между распределением электронов по энергетическим уровням
Установить соответствие
между распределением электронов по энергетическим уровням
и формулами химических частиц:
РАСПРЕДЕЛЕНИЕ ФОРМУЛЫ, ЧАСТИЦ
ЭЛЕКТРОНОВ ПО УРОВНЯМ
1) 2, 8, 4 а) Mg2+
2) 2, 8, 8 б) Si
3) 2, 8 в) Ar
4) 2, 8, 8, 1 г) К
13. Записать название изотопа элемента с массовым числом 23, в ядре атома
которого находится 11 протонов. Ответ: _______________
Периодическая таблица химических элементов (Д. И. Менделеева) в химии
Содержание:
- Периодическая таблица химических элементов
- Классификация химических элементов
- Структура периодической системы
- Горизонтальные ряды элементов называют периодами
- Вертикальные столбцы элементов называют группами
- Естественные семейства химических элементов
- Структура периодической системы химических элементов
- Периодическое изменение некоторых характеристик и свойств атомов химических элементов
- Характеристика элемента по положению в периодической системе
- Значение периодического закона Д.
 И. Менделеева
И. Менделеева
Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Периодическая таблица химических элементовПериодическая система химических элементов (таблица Менделеева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда их атомного ядра. … Первоначальный вариант был разработан Д. И. Менделеевым в 1869, и приведен к традиционному графическому виду в 1871 году.
… Первоначальный вариант был разработан Д. И. Менделеевым в 1869, и приведен к традиционному графическому виду в 1871 году.
В качестве основного варианта IUPAC утвердил длинный вариант Периодической таблицы. Короткая форма таблицы, содержащая восемь групп элементов, официально отменена ИЮПАК еще в 1989 г.
Нильсом Бором разработана лестничная (пирамидальная) форма периодической системы.
Классификация химических элементовВ первой половине XIX века химики открыли 25 новых химических элементов. К середине XIX века число известных элементов приблизилось к 60. В настоящее время известно 118 элементов (116 — открыты, 114 — названы и еще по двум проводятся исследования). По каким же признакам их классифицируют?
Многие химики пытались найти связь между химическими свойствами и атомным весом давно известных и вновь открытых элементов. Однако создать естественную систему химических элементов удалось лишь Д. И. Менделееву.
И. Менделееву.
Первоначально шведский ученый И. Берцелиус предложил разделить элементы на металлы и неметаллы по свойствам простых веществ, образованных ими.
Металлы в свободном виде обладают характерным металлическим блеском, хорошо проводят электрический ток и теплоту. Неметаллы плохо проводят электрический ток и, как правило, не имеют металлического блеска. Металлы и неметаллы различаются и по химическим свойствам (рис. 18). Металлы образуют соединения, проявляющие основные свойства, а неметаллы образуют кислотные соединения.
Рис. 18. Металлы и неметаллы
И. В. Дёберейнер
В 1829 г. немецкий химик И. В. Дёберейнер заметил, что некоторые сходные по своим свойствам элементы можно объединить группы. Он назвал их триадами.
Сущность данной классификации заключается в следующем: в каждой триаде есть средний элемент, масса атома которого будет равна средней арифметической массе двух крайних элементов.
Например. рассмотрим одну из триад: Li, Na, К.
рассмотрим одну из триад: Li, Na, К.
Их атомные массы соответственно равны 7, 23, 39.
Система классификации И. В. Дёберейнера оказалась несовершенной . Ошибка немецкого химика заключалась в том, что он ограничил себя поиском тройственных союзов, т. е. триад.
Но И. В. Дёберейнер был первым из естествоиспытателей, который связал свойства химических элементов с их атомными массами.
Дж. А. Ньюклендс
В 1865 г. английский ученый Дж. А. Ньюклендс расположил химические цементы в порядке возрастания их атомных масс. В результате он заметил, что каждый восьмой элемент напоминает по свойствам первый элемент. Найденную закономерность он назвал законом октав по аналогии с семью интервалами музыкальной гаммы (рис. 19).
Рис. 19. Октавы Ньюклендса
Закон октав он сформулировал следующим образом:
“Номера аналогичных элементов, как правило, отличаются или на целое число семь или на кратное семи; другими словами, члены одной и той же группы соотносятся друг с другом в том же отношении, как и крайние точки одной или больше октав в музыке”.
Он расположил элементы по семь в группы. Таким образом, он заметил, что вертикальные ряды, полученные после такого расположения включают в себя элементы, схожие по своим химическим свойствам. Дж. А. Ньюклендс был первым, кто соотнес атомные массы химических элементов и их химические свойства и присвоил каждому элементу порядковый номер. Но все же в его таблице не было свободных мест. Он ограничил себя семью клетками в каждом периоде и в некоторые клетки ему пришлось поместить по несколько элементов. Поэтому научный мир отнесся скептически к его открытию.
Д. И. Менделеев
В начале 1869 г., обдумывая структуру учебника “Основы химии”, он постепенно пришел к выводу, что между свойствами и атомными массами элементов существует какая-то закономерность. Первым шагом к появлению периодического закона стала таблица “Опыт системы элементов, основанный на их атомном весе и химическом сходстве”. Позднее Д. И. Менделеев сам сформулировал закон: “Свойства элементов, а также состав образуемых ими простых и сложных веществ находятся в периодической зависимости от их атомного веса”.
Положив в основу своего закона сходство элементов и их соединений, Менделеев не стал слепо следовать принципу возрастания атомных масс. Он учитывал, что для некоторых элементов атомные массы могли быть определены недостаточно точно. Но даже в современной Периодической системе известны некоторые исключения в порядке возрастания масс атомов, что связано с особенностями изотопного состава элементов:
| Cl – 35,5 | Ar – 39,9 | K – 39,1 |
| Fe – 55,8 | Co – 58,9 | Ni – 58,7 |
| Sb – 121,8 | Te – 127,6 | I – 126,9 |
Кроме того, Менделеев оставил пустые места для еще не открытых элементов, которые были заполнены в последующие десятилетия, что лишний раз подтвердило правильность периодического закона и Периодической системы элементов (рис. 20).
Рис. 20. Первоначальный вариант периодической таблицы Д. И. Менделеева
И. Менделеева
Каждому элементу в Периодической системе Д. И. Менделеевым был присвоен порядковый номер, исходя из увеличения атомной массы. С развитием теории строения атома был выявлен физический смысл порядкового номера. Так, было доказано, что порядковый номер элемента совпадает с зарядом его ядра.
Менделеев открыл периодический закон, ничего не зная о строении атома. После того как было доказано ядерное строение атома и равенство порядкового номера элемента заряду ядра его атома, периодический закон получил новую формулировку: “Свойства элементов, а также образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядра”.
Периодический закон не имеет количественного математического выражения в виде уравнения или формулы. Формой отображения периодического закона является таблица — Периодическая система химических элементов.
Самое важное
Такие ученые, как Й. Берцелиус, И. В. Дёберейнер. Дж. А. Ньюлендс и другие, предложили разные способы систематизации химических элементов. Д. И. Менделеев искал связь между всеми химическими элементами, как сходными по свойствам, так и несходными между собой. Чтобы найти закономерность, которая объединила бы все химические элементы в единую систему, он сопоставлял свойства и относительные атомные массы. Дмитрий Иванович расположил элементы в порядке возрастания атомных масс в ряд. В результате ученый обнаружил, что сходные по химическим свойствам элементы встречаются через определенные интервалы.
Берцелиус, И. В. Дёберейнер. Дж. А. Ньюлендс и другие, предложили разные способы систематизации химических элементов. Д. И. Менделеев искал связь между всеми химическими элементами, как сходными по свойствам, так и несходными между собой. Чтобы найти закономерность, которая объединила бы все химические элементы в единую систему, он сопоставлял свойства и относительные атомные массы. Дмитрий Иванович расположил элементы в порядке возрастания атомных масс в ряд. В результате ученый обнаружил, что сходные по химическим свойствам элементы встречаются через определенные интервалы.
Периодическая система элементов является важнейшим инструментом, которым пользуются не только химики, но и специалисты других предметов. В первоначальном варианте, предложенном Д. И. Менделеевым, элементы располагались по возрастанию атомных масс. Но ряд элементов (например, аргон и калий) затем поменяли местами, хотя это нарушало данную последовательность. Поэтому в современном варианте Периодической системы элементы расположены в порядке возрастания заряда атомных ядер. Существует множество вариантов такой таблицы (рис. 21 а, б, в).
Поэтому в современном варианте Периодической системы элементы расположены в порядке возрастания заряда атомных ядер. Существует множество вариантов такой таблицы (рис. 21 а, б, в).
В настоящее время их всего 7. С 1-го по 3-й период обычно называют малым, а с 4-го по 7-й — большим.
Рис. 21. а — короткий вариант таблицы; б — полудлинный вариант таблицы; в — длинный вариант таблицы
Вертикальные столбцы элементов называют группамиГрупп в коротком варианте восемь, и они подразделены на главные подгруппы (обозначаются буквой “А”) и на побочные подгруппы (обозначают буквой “В”). В одном подгруппе располагаются сходные по химическим свойствам элементы (семейства). В полудлинном и длинном вариантах Периодической системы элементов обычно восемнадцать групп, и они включают все подгруппы.
Ряд подгрупп носит специальные названия. Например, I А группа — щелочные металлы, VII А группа — галогены.
Большинство среди элементов Периодической системы — металлы (больше 90), неметаллов меньше.
Знаешь ли ты?
Широко распространена легенда, что мысль о периодической таблице химических элементов пришла к Менделееву во сне. Однажды его спросили, так ли это, на что ученый ответил: “Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг…готово”.
Знаешь ли ты?
Множество химических элементов получили свое название в честь стран или других географических объектов. Сразу 4 элемента — иттрий; иттербий, тербий и эрбий — были названы в честь шведской деревни Иттербю, около которой обнаружили крупное месторождение редкоземельных металлов.
Знаешь ли ты?
Шведский ученый Карл Шееле является рекордсменом по количеству открытых химических элементов. На его счету хлор, фтор, барий, вольфрам, кислород, марганец, молибден.
| Элементы в природе | |
| Элемент | % (в атомах) |
| 1. Водород | 73,9 |
| 2. Гелий | 24,0 |
| 3. Кислород | 1,1 |
| 4. Углерод | 0,46 |
| 5. Неон | 0,13 |
| 6. Железо | 0,11 |
| 7. Азот | 0,097 |
| 8. Кремний | 0,065 |
| 9. Магний | 0,058 |
| 10. Сера | 0,044 |
Самое важное
Горизонтальные ряды элементов называют периодами. В настоящее время их всего 7. С 1-го по 3-й периоды называют малыми, а с 4-го по 7-й — большими периодами. Вертикальные столбцы элементов называют группами. Групп всего 8, они подразделены на главные и побочные подгруппы (в коротком варианте таблицы).
Естественные семейства химических элементовГруппа элементов, объединенных по сходству химических и физических свойств, называется семейством сходных цементов или естественным семейством химических элементов.
IA группа — щелочные металлы. В это семейство входят элементы: литий, натрий, калий, рубидий, цезий и франций. Эти элементы являются самыми активными металлами (рис. 22). А наиболее активный среди них — франций, король среди металлов! Щелочные металлы очень мягкие, пластичные, но из-за высокой активности их приходится хранить под слоем керосина или машинного масла. Они очень бурно реагируют с водой (со взрывом), образуя щелочи, отсюда и происходит их название.
Рис. 22. Щелочные металлы
Несложно заметить, что с увеличением порядкового номера щелочного металла уменьшаются температуры кипения и плавления, а также твердость (табл. 10). Это связано с увеличением размеров атомов. Натрии и калии столь мягкие, что легко режутся ножом.
Знаешь ли ты?
Йод был открыт с помощью кота! У французского ученого Куртуа был любимый кот, который во время обеда испугался и, спрыгнув на пол, разбил склянки. С пола стали подниматься клубы сине-фиолетового пара, которые оседали на окружающих предметах в виде мельчайших черно-фиолетовых кристалликов с металлическим блеском и едким запахом. Это и был новый химический элемент — йод.
С пола стали подниматься клубы сине-фиолетового пара, которые оседали на окружающих предметах в виде мельчайших черно-фиолетовых кристалликов с металлическим блеском и едким запахом. Это и был новый химический элемент — йод.
Таблица 10
| Металл | Температура плавления, °С | Температура кипения, °С | Твердость |
| литий | 180 | 1340 | мягкий |
| натрий | 98 | 880 | очень мягкий |
| калий | 64 | 760 | совсем мягкий |
VIIА группа (17) — галогены. В это семейство входят элементы: фтор, хлор, бром, йод и астат. Они являются самыми активными неметаллами. Самый активный среди галогенов — фтор, король среди неметаллов. Они очень опасные, имеют различные цвета: фтор — бледно-желтый и хлор — желто-зеленый газы, бром— красно-коричневая жидкость, а йод — твердое вещество темно-фиолетового цвета (рис. 23, табл. 11), Из-за высокой активности их приходится хранить в закрытом виде. Они очень бурно реагируют с металлами, образуя соли, отсюда и происходит их название (галогены — “солерождающие”), и с водородом, образуя кислоты (например. соляную кислоту).
23, табл. 11), Из-за высокой активности их приходится хранить в закрытом виде. Они очень бурно реагируют с металлами, образуя соли, отсюда и происходит их название (галогены — “солерождающие”), и с водородом, образуя кислоты (например. соляную кислоту).
Рис. 23. (слева направо): хлор, бром и йод
Знаешь ли ты?
Современные автомобили используют в подушках безопасности соединение натрия и азота — азид натрия (NaN3), — выделяющее при нагревании газ азот, который и заполняет подушку. Это изобретение впервые применили в 1980 г.
Знаешь ли ты?
Хлор — токсичный удушливый газ, который при попадании в легкие вызывает ожог легочной ткани, удушье.
Во многих городах водоочистные системы применяют хлор для уничтожения бактерий. При этом на один миллион частей воды используют четыре-пять частей хлора. Это количество безвредно для человека, однако иногда вода имеет привкус хлора.
Таблица 11
Физические свойства галогенов
| Галоген | Внешний вид, агрегатное состояние | Температура плавления, °С | Температура кипения, °С |
| фтор | бледно-желтый газ | -220 | -188 |
| хлор | желто-зеленый газ | -101 | -35 |
| бром | красно-коричневая жидкость | -7 | 59 |
| йод | темно-фиолетовое твердое вещество | 114 | 184 |
Подумай:
• Почему хлор используют для обеззараживания воды?
• Почему гелий используют для заполнения аэростатов?
VIIIA группа (18) — инертные газы. В это семейство входят гелий, неон, аргон, криптон, ксенон и радон. Эти элементы являются самыми неактивными неметаллами. Они представляют собой газы. Многие из них широко используются, так, например, гелий применяют в аэростатах вместо взрывоопасного водорода. Аргон используют при сварке металлов, а также, как и неон, — для рекламного освещения (рис. 24).
Аргон используют при сварке металлов, а также, как и неон, — для рекламного освещения (рис. 24).
Рис. 24. Инертные газы
Переходные металлы (металлы побочных подгрупп). Эти семейства металлов включают очень важные металлы, такие как золото, серебро, платина и др. (рис. 25). Они являются хорошими проводниками тепла и электричества, имеют высокие температуры плавления и кипения (за исключением ртути — единственного жидкого металла). Часто используются как катализаторы в химических процессах.
Рис. 25. Переходные металлы: а — платина; б — серебро; в — золото
Знаешь ли ты?
После крушения дирижабля “Гинденбург” в 1937 году гелий благодаря легкости и невоспламеняемости заменил водород в качестве поднимающего газа в дирижаблях и воздушных шарах.
Самое важное
В результате классификации природные элементы делятся на металлы и неметаллы. Дальнейшая классификация химических элементов привела к открытию естественных семейств элементов. Химические элементы, сходные по химическим свойствам, относятся к одному семейству. К типичным металлам относятся щелочные металлы, а к типичным неметаллам — галогены.
Химические элементы, сходные по химическим свойствам, относятся к одному семейству. К типичным металлам относятся щелочные металлы, а к типичным неметаллам — галогены.
Структура периодической системы химических элементов
Ядро, электроны, электронная формула
Периодическая система Д. И. Менделеева состоит из семи периодов. Обозначаются они арабскими цифрами.
Периодами называются горизонтальные ряды элементов, расположенные по возрастанию их атомных масс. Начинаются периоды со щелочных металлов и заканчиваются инертными газами.
В соответствии с современными научными представлениями о структуре атома Периодический закон формулируется так:
Свойства химических элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от величины заряда их атомных ядер.
Почти все элементы за исключением некоторых в Периодической системе пронумерованы в порядке возрастания их относительных атомных масс, т. е. каждый элемент имеет свой порядковый номер. Его физический смысл – заряд ядра атомов элементов. Периоды подразделяются на малые (1–3), которые состоят из одного ряда, и большие (4–7), состоящие из двух рядов. Седьмой период не завершен.
е. каждый элемент имеет свой порядковый номер. Его физический смысл – заряд ядра атомов элементов. Периоды подразделяются на малые (1–3), которые состоят из одного ряда, и большие (4–7), состоящие из двух рядов. Седьмой период не завершен.
Вертикальные ряды элементов называются группами. Обозначаются они римскими цифрами. В Периодической системе восемь групп, каждая из них состоит из двух подгрупп: главной и побочной. В главную подгруппу входят элементы как малых, так и больших периодов, а в побочную подгруппу – только элементы больших периодов.
Например, в главную подгруппу IV группы входят углерод (С), кремний (Si), германий (Ge), олово (Sn), свинец (Pb), а в побочную – титан (Ti), цирконий (Zr), гафний (Hf).
Группами называются вертикальные ряды элементов, сходных по свойствам и расположенных по возрастанию атомных масс.
Подытоживая эти особенности, Д. И. Менделеев выдвинул следующие предположения:
И. Менделеев выдвинул следующие предположения:
1. Периоды могут быть разной длины.
2. Некоторые химические элементы еще не открыты (для них он оставил пустые места).
Периодическое изменение некоторых характеристик и свойств атомов химических элементов
Периоды, группы.
Периодическая система является графическим изображением Периодического закона Д. И. Менделеева. Она состоит из восьми групп и семи периодов. Периоды подразделяются на большие и малые. Первые три периода – малые, они состоят из одного ряда. Большие периоды состоят из двух рядов.
Далее рассмотрим изменение свойств атомов элементов (радиусы, металлические и неметаллические свойства, валентности) и их соединений (кислотно-основные свойства оксидов и гидроксидов).
Хотя число энергетических уровней у элементов одного периода одинаково, по периоду слева направо радиусы атомов уменьшаются, так как заряды ядер атомов постепенно возрастают в этом направлении.
По периодам слева направо увеличивается число электронов на внешнем энергетическом уровне, что приводит к ослаблению металлических свойств и усилению неметаллических свойств.
У атомов металлов мало электронов на внешних энергетических уровнях (1–3), поэтому они легко их отдают.
У атомов неметаллов для завершения внешнего энергетического уровня не хватает 1–4 электронов, поэтому неметаллы легко их принимают. Их валентность в водородных соединениях определяется числом присоединенных электронов.
На примере атома фосфора рассмотрим валентность элемента. Валентность атомов элементов с точки зрения электронного строения атомов определяется участием неспаренных электронов в образовании химических связей между атомами. Электронная формула последнего энергетического уровня атома фосфора:
Третий энергетический уровень состоит из трех подуровней 3s, 3p, 3d. На 3d-орбитали 5 ячеек.
Валентных электронов пять, три из них неспаренные. На 3р-орбитали находятся три неспаренных электрона, поэтому фосфор проявляет валентность, равную III При подаче определенного количества энергии один электрон с 3s-орбитали переходит на 3d-орбиталь, такое состояние атома называется возбужденным. В результате атом фосфора становится пятивалентным В водородных соединениях фосфор трехвалентен так как до завершения внешнего энергетического уровня не хватает 3 электронов (8–5 = 3).
Оксиды первых двух элементов каждого периода Периодической системы являются основными оксидами, которым соответствуют основные гидроксиды. Далее идут элементы, оксиды и гидроксиды которых проявляют амфотерность. В конце периодов расположены элементы, оксиды и гидроксиды которых проявляют кислотные свойства.
Каждая группа Периодической системы подразделяется на две подгруппы: главную (А) и побочную (В).
Число валентных электронов элементов одной группы одинаково. Валентные электроны элементов главных подгрупп (А) расположены на внешних энергетических уровнях.
Валентные электроны элементов главных подгрупп (А) расположены на внешних энергетических уровнях.
Высшая валентность в соединениях элементов одной группы одинаковая.
Элементы побочных подгрупп – металлы, у многих из них на внешнем энергетическом уровне имеется по два электрона, поэтому их низшая валентность равна II, а высшая соответствует номеру группы, они проявляют переменную валентность. Исключение: цинк имеет постоянную валентность (II) а, например, медь и серебро – низшую валентность (I).
В главной подгруппе сверху вниз увеличиваются значения атомных радиусов, так как увеличивается число энергетических уровней. Поэтому уменьшается количество энергии, необходимой для отрыва электрона от внешнего электронного слоя, что приводит к усилению металлических свойств.
Основываясь на этих рассуждениях, можно сделать следующий вывод:
Свойства химических элементов и образуемых ими простых и сложных веществ периодически повторяются, так как периодически изменяется электронное строение атомов.
Валентные электроны, переменная валентность.
Играем, думаем, учимся!
При правильном заполнении вы прочитаете названия 12 химических элементов.
Характеристика элемента по положению в периодической системе
Протоны, нейтроны, заряд ядра, относительная атомная масса.
После того как мы выяснили зависимость свойств химических элементов от электронного строения атома, можно предположить свойства любого элемента Периодической системы (табл. 12). Для этого предлагаем следующий алгоритм:
I. Место химического элемента в Периодической системе.
II. Строение атома химического элемента в зависимости от положения в Периодической системе.
III. Свойства химического элемента и его соединений.
ДЕЛЛЕМ ВЫВОДЫ
- 1. Период – горизонтальный ряд элементов в Периодической системе, который начинается со щелочного металла и заканчивается инертным газом. В периодах число энергетических уровней одинаково, элементы расположены по возрастанию зарядов ядер атомов.

- 2. Группа – вертикальный ряд сходных по свойствам элементов, у которых число валентных электронов одинаково. Валентные электроны элементов главных подгрупп расположены на внешнем энергетическом уровне, у элементов побочных подгрупп – на внешних и предвнешних уровнях.
- 3. По периодам слева направо металлические свойства постепенно ослабевают, а неметаллические – усиливаются, так как в этом направлении уменьшаются радиусы атомов и увеличивается число электронов на последнем уровне.
- 4. По группам сверху вниз из-за увеличения атомных радиусов усиливаются металлические свойства, а неметаллические – ослабевают.
Периодический закон и Периодическая система элементов Д. И. Менделеева оказали огромное влияние на развитие не только химии, но и теоретической физики, астрономии, медицины, геологии и многих других наук. Руководствуясь Периодическим законом, ученые-физики определили электронное строение атомов.
Д. И. Менделеев открыл фундаментальный закон периодичности изменений свойств элементов и на основе этого закона создал свою знаменитую таблицу химических элементов.
На основе открытого им закона Д. И. Менделеев удивительно точно предсказал физико-химические свойства еще не открытых в то время элементов, заложив тем самым методологическую основу неорганической химии (экаалюминий – галлий, экабор – скандий, экасилиций – германий).
Периодический закон утвердился в науке и стал путеводной звездой в поисках еще не открытых в земной природе элементов, а также еще не полученных соединений уже известных элементов.
Периодическая система привела в строгий порядок огромное число фактов и разрозненных знаний о химических элементах и их соединениях. Опираясь на Периодический закон, ученые-физики синтезировали ряд трансурановых элементов, которые дополнили Периодическую систему и оказались дополнительным свидетельством ее правильности.
В Периодическом законе нашли свое отражение важнейшие законы диалектики.
Заслуги Д. И. Менделеева были отмечены американским ученым Г. Сиборгом, который назвал открытый им элемент №101 менделеевием.
Дмитрий Иванович Менделеев родился 27 января (8 февраля) 1834 г. в г. Тобольске в Сибири. Его отец был директором городской гимназии. После окончания гимназии будущий ученый поступил в Петербургский педагогический институт, который окончил в 1857 г. с золотой медалью. Свои первые научные работы он опубликовал еще в студенческие годы.
После защиты магистерской диссертации в 1859 г. Д. И. Менделеев был командирован в заграничную научную поездку в Германию. Вернувшись на родину, он с головой уходит в науку и педагогическую деятельность. После двух лет профессорской деятельности в Петербургском технологическом институте переходит в университет, где успешно работает в течение 23 лет.
В 1876 г. Д. И. Менделеев был избран членом-корреспондентом Петербургской академии наук.
Д. И. Менделеев был человеком широких, прогрессивных взглядов, крупным общественным деятелем, много сил отдавал развитию народного образования. Во время студенческих волнений 1890-х годов ученый выступил на стороне студентов и был вынужден уйти из университета.
Во время студенческих волнений 1890-х годов ученый выступил на стороне студентов и был вынужден уйти из университета.
Последние годы жизни Д. И. Менделеев возглавлял Палату мер и весов.
Круг его научных интересов не ограничивался химией. Он является автором фундаментальных исследований по физике, метрологии, химической технологии, экономике, воздухоплаванию, сельскому хозяйству и др. Его работы не утратили своего значения и в наши дни.
Любознательный ум ученого не ведал страха. Исследуя земную атмосферу, он в одиночку совершил полет на воздушном шаре. «Заболев» освоением Арктики, он разработал проект ледокола. Также Д. И. Менделеев разработал состав бездымного пороха.
Д. И. Менделеев тщательно изучал нефтяные месторождения, самое серьезное внимание уделял вопросам технологии нефти, считая нефть важнейшим сырьем для получения многих ценных химических продуктов.
Вершиной его творческой деятельности, бесспорно, является открытый им Периодический закон и созданная на его основе Периодическая система химических элементов. Д. И. Менделеевым написан первый российский учебник по неорганической химии «Основы химии», в котором свойства неорганических соединений впервые описаны на основе Периодического закона.
Д. И. Менделеевым написан первый российский учебник по неорганической химии «Основы химии», в котором свойства неорганических соединений впервые описаны на основе Периодического закона.
За выдающиеся заслуги в науке Д. И. Менделеев был избран почетным членом академий и научных обществ многих стран мира; удостоен золотой медали им. М. Фарадея.
В возрасте 73 лет он скончался. Проститься с одним из величайших ученых мира пришло множество людей. Впереди процессии несли Периодическую таблицу.
ДЕЛЛЕМ ВЫВОДЫ
1. Периодическая система состоит из 7 периодов, 8 групп.
2. Периоды подразделяются на малые (1-3) и большие (4-7).
3. Каждая группа состоит из двух подгрупп: главной (А) и побочной (В).
4. Порядковый номер элемента указывает на заряд его ядра.
Услуги по химии:
- Заказать химию
- Заказать контрольную работу по химии
- Помощь по химии
Лекции по химии:
- Основные понятия и законы химии
- Атомно-молекулярное учение
- Периодический закон Д.
 И. Менделеева
И. Менделеева - Химическая связь
- Скорость химических реакций
- Растворы
- Окислительно-восстановительные реакции
- Дисперсные системы
- Атомно-молекулярная теория
- Строение атома в химии
- Простые вещества
- Химические соединения
- Электролитическая диссоциация
- Химия и электрический ток
- Чистые вещества и смеси
- Изменения состояния вещества
- Атомы. Молекулы. Вещества
- Воздух
- Химические реакции
- Закономерности химических реакций
- Относительная атомная масса химических элементов
- Химические формулы
- Движение электронов в атомах
- Формулы веществ и уравнения химических реакций
- Химическая активность металлов
- Количество вещества
- Стехиометрические расчёты
- Энергия в химических реакциях
- Вода
- Необратимые реакции
- Кинетика
- Химическое равновесие
- Разработка новых веществ и материалов
- Зеленая химия
- Термохимия
- Правило фаз Гиббса
- Диаграммы растворимости
- Законы Рауля
- Растворы электролитов
- Гидролиз солей и нейтрализация
- Растворимость электролитов
- Электрохимические процессы
- Электрохимия
- Кинетика химических реакций
- Катализ
- Строение вещества в химии
- Строение твердого тела и жидкости
- Протекание химических реакций
- Комплексные соединения
Лекции по неорганической химии:
- Важнейшие классы неорганических соединений
- Водород и галогены
- Подгруппа кислорода
- Подгруппа азота
- Подгруппа углерода
- Общие свойства металлов
- Металлы главных подгрупп
- Металлы побочных подгрупп
- Свойства элементов первых трёх периодов периодической системы
- Классификация неорганических веществ
- Углерод
- Качественный анализ неорганических соединений
- Металлы и сплавы
- Металлы и неметаллы
- Производство металлов
- Переходные металлы
- Элементы 1 (1А), 2 IIA и 13 IIIA групп и соединения
- Элементы 17(VIIA), 16(VIA) 15(VA), 14(IVA) групп и их соединения
- Важнейшие S -элементы и их соединения
- Важнейшие d элементы и их соединения
- Важнейшие р-элементы и их соединения
- Производство неорганических соединений и сплавов
- Главная подгруппа шестой группы
- Главная подгруппа пятой группы
- Главная подгруппа четвертой группы
- Первая группа периодической системы
- Вторая группа периодической системы
- Третья группа периодической системы
- Побочные подгруппы четвертой, пятой, шестой и седьмой групп
- Восьмая группа периодической системы
- Водород
- Кислород
- Озон
- Водород
- Галогены
- Естественные семейства химических элементов и их свойства
- Химические элементы и соединения в организме человека
- Геологические химические соединения
Лекции по органической химии:
- Органическая химия
- Углеводороды
- Кислородсодержащие органические соединения
- Азотсодержащие органические соединения
- Теория А.
 М. Бутлерова
М. Бутлерова - Соединения ароматического ряда
- Циклические соединения
- Карбонильные соединения
- Амины и аминокислоты
- Химия живого вещества
- Синтетические полимеры
- Органический синтез
- Элементы 14(IVA) группы
- Азот и сера
- Растворы кислот и оснований
Четвертый период, 4 период, периодическая система химических элементов
Четвертый период, 4 период, периодическая система химических элементов- Главная
- Статьи
- Периодическая система элементов — Периодическая система химических элементов, периодическая система элементов Менделеева
- Четвертый период, 4 период, периодическая система химических элементов
+++++
Четвёртый период периодической системы элементов
Четвёртый период (K — Kr) содержит 18 элементов (первый большой период, по Менделееву). После щелочного металла K и щёлочноземельного Ca (s-элементы) следует ряд из десяти так называемых переходных элементов (Sc — Zn), или d-элементов (символы даны синим цветом), которые входят в подгруппы б соответствующих групп П. с. э.
После щелочного металла K и щёлочноземельного Ca (s-элементы) следует ряд из десяти так называемых переходных элементов (Sc — Zn), или d-элементов (символы даны синим цветом), которые входят в подгруппы б соответствующих групп П. с. э.
Большинство переходных элементов (все они металлы) проявляет высшие степени окисления, равные номеру группы. Исключение — триада Fe — Co — Ni, где два последних элемента максимально положительно трёхвалентны, а железо в определённых условиях известно в степени окисления VI. Элементы, начиная с Ga и кончая Kr (р-элементы), принадлежат к подгруппам а, и характер изменения их свойств такой же, как и в соответствующих интервалах Z у элементов второго и третьего периодов. Установлено, что Kr способен образовывать химические соединения (главным образом с F), но степень окисления VIII для него неизвестна.
Четвертый период периодической системы химических элементов
|
IA |
IIA |
IIIB |
IVB |
VB |
VIB |
VIIB |
—- |
VIIIB |
—- |
IB |
IIB |
IIIA |
IVA |
VA |
VIA |
VIIA |
VIIIA |
|
| Период | ||||||||||||||||||
| 4 |
19
K |
20
Ca |
21
Sc |
22
Ti |
23
V |
24
Cr |
25
Mn |
26
Fe |
27
Co |
28
Ni |
29
Cu |
30
Zn |
31
Ga |
32
Ge |
33
As |
34
Se |
35
Br |
36
Kr |
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
| IA | IIA | IIIB | IVB | VB | VIB | VIIB | —- | VIIIB | —- | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |
| Период | ||||||||||||||||||
| 1 |
1 H Водород |
2 He Гелий |
||||||||||||||||
| 2 |
3 Li Литий |
4 Be Бериллий |
5 B Бор |
6 C Углерод |
7 N Азот |
8 O Кислород |
9 F Фтор |
10 Ne Неон |
||||||||||
| 3 |
11 Na Натрий |
12 Mg Магний |
13 Al Алюминий |
14 Si Кремний |
15 P Фосфор |
16 S Сера |
17 Cl Хлор |
18 Ar Аргон |
||||||||||
| 4 |
19 K Калий |
20 Ca Кальций |
21 Sc Скандий |
22 Ti Титан |
23 V Ванадий |
24 Cr Хром |
25 Mn Марганец |
26 Fe Железо |
27 Co Кобальт |
28 Ni Никель |
29 Cu Медь |
30 Zn Цинк |
31 Ga Галлий |
32 Ge Германий |
33 As Мышьяк |
34 Se Селен |
35 Br Бром |
36 Kr Криптон |
| 5 |
37 Rb Рубидий |
38 Sr Стронций |
39 Y Иттрий |
40 Zr Цирконий |
41 Nb Ниобий |
42 Mo Молибден |
(43) Tc Технеций |
44 Ru Рутений |
45 Rh Родий |
46 Pd Палладий |
47 Ag Серебро |
48 Cd Кадмий |
49 In Индий |
50 Sn Олово |
51 Sb Сурьма |
52 Te Теллур |
53 I Иод |
54 Xe Ксенон |
| 6 |
55 Cs Цезий |
56 Ba Барий |
* |
72 Hf Гафний |
73 Ta Тантал |
74 W Вольфрам |
75 Re Рений |
76 Os Осмий |
77 Ir Иридий |
78 Pt Платина |
79 Au Золото |
80 Hg Ртуть |
81 Tl Таллий |
82 Pb Свинец |
83 Bi Висмут |
(84) Po Полоний |
(85) At Астат |
86 Rn Радон |
| 7 |
87 Fr Франций |
88 Ra Радий |
** |
(104) Rf Резерфордий |
(105) Db Дубний |
(106) Sg Сиборгий |
(107) Bh Борий |
(108) Hs Хассий |
(109) Mt Мейтнерий |
(110) Ds Дармштадтий |
(111) Rg Рентгений |
(112) Cp Коперниций |
(113) Uut Унунтрий |
(114) Uuq Унунквадий |
(115) Uup Унунпентий |
(116) Uuh Унунгексий |
(117) Uus Унунсептий |
(118) Uuo Унуноктий |
| 8 |
(119) Uue Унуненний |
(120) Ubn Унбинилий |
||||||||||||||||
| Лантаноиды * |
57 La Лантан |
58 Ce Церий |
59 Pr Празеодим |
60 Nd Неодим |
(61) Pm Прометий |
62 Sm Самарий |
63 Eu Европий |
64 Gd Гадолиний |
65 Tb Тербий |
66 Dy Диспрозий |
67 Ho Гольмй |
68 Er Эрбий |
69 Tm Тулий |
70 Yb Иттербий |
71 Lu Лютеций |
|||
| Актиноиды ** |
89 Ac Актиний |
90 Th Торий |
91 Pa Протактиний |
92 U Уран |
(93) Np Нептуний |
(94) Pu Плутоний |
(95) Am Америций |
(96) Cm Кюрий |
(97) Bk Берклий |
(98) Cf Калифорний |
(99) Es Эйнштейний |
(100) Fm Фермий |
(101) Md Менделевий |
(102) No Нобелей |
(103) Lr Лоуренсий |
|||
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
получение, физические и химические свойства, применение в медицине.

Подгруппа бора — главная подгруппа III группы. По новой классификации ИЮПАК: 13 группа элементов Периодической системы химических элементов Д. И. Менделеева, в которую входят бор B, алюминий Al, галлий Ga, индий In и таллий Tl. Все элементы данной подгруппы, за исключением бора, металлы.
|
|
|
К III группе относятся бор, алюминий, галлий, индии, таллий (главная подгруппа), а также скандий, иттрий, лантан и лантаноиды, актиний и актиноиды (побочная подгруппа).
На внешнем электронном уровне элементов главной подгруппы имеется по три электрона (s2р1). Они легко отдают эти электроны или образуют три неспаренных электрона за счет перехода одного электрона на р-уровень. Для бора и алюминия характерны соединения только со степенью окисления +3. У элементов подгруппы галлия (галлий, индий, таллий) на внешнем электронном уровне также находится по три электрона, образуя конфигурацию s2р1, но они расположены после 18-электронного слоя. Поэтому в отличие от алюминия галлий обладает явно неметаллическими свойствами. Эти свойства в ряду Gа, In, Тl ослабевают, а металлические свойства усиливаются.
Они легко отдают эти электроны или образуют три неспаренных электрона за счет перехода одного электрона на р-уровень. Для бора и алюминия характерны соединения только со степенью окисления +3. У элементов подгруппы галлия (галлий, индий, таллий) на внешнем электронном уровне также находится по три электрона, образуя конфигурацию s2р1, но они расположены после 18-электронного слоя. Поэтому в отличие от алюминия галлий обладает явно неметаллическими свойствами. Эти свойства в ряду Gа, In, Тl ослабевают, а металлические свойства усиливаются.
Электронное строение валентного слоя актиноидов во многом напоминает электронное строение валентного слоя лантаноидов. Все лантаноиды и актиноиды — типичные металлы.
Все элементы III группы обладают очень сильным сродством к кислороду, и образование их оксидов сопровождается выделением большого количества теплоты.
Элементы III группы находят самое разнообразное применение.
Бор был открыт Ж. Гей-Люссаком и Л. Тенаром в 1808 г. Содержание его в земной коре составляет 1,2·10-3 %.
Гей-Люссаком и Л. Тенаром в 1808 г. Содержание его в земной коре составляет 1,2·10-3 %.
Соединения бора с металлами (б о р и д ы ) обладают высокой твердостью и термостойкостью. Поэтому их используют для получения сверхтвердых и жаропрочных специальных сплавов. Большой термостойкостью обладают карбид и нитрид бора. Последний применяют в качестве высокотемпературной смазки. Кристаллогидрат тетрабората натрия Nа2В4O7·10Н2О (бура) имеет постоянный состав, его растворы применяют в аналитической химии для установления концентрации растворов кислот.
Содержание галлия в земной коре составляет 1,9·10-3 %. Он был предсказан Д. И. Менделеевым (экаалюминий) и открыт французским химиком Р. Э. Лекок де Буабодраном в 1875 г. Свойства галлия почти полностью совпали со свойствами экаалюминия, предсказанными Д, И. Менделеевым на основе периодического закона.
Соединения галлия с элементами VI группы (серой, селеном, теллуром) являются полупроводниками. Жидким галлием наполняют высокотемпературные термометры.
Жидким галлием наполняют высокотемпературные термометры.
Индий был открыт Т. Рихтером и Ф. Райхом в 1863 г. Содержание его в земной коре составляет 2,5·10-5 %. Добавка индия к сплавам меди увеличивает устойчивость последних к действию морской воды. Присадка этого металла к серебру увеличивает блеск серебра и препятствует его тускнению на воздухе. Индиевые покрытия предохраняют металлы от коррозии. Он входит в состав некоторых сплавов, применяющихся в стоматологии, а также некоторых легкоплавких сплавов (сплав индия, висмута, свинца, олова и кадмия плавится при 47 °С). Соединения индия с различными неметаллами обладают полупроводниковыми свойствами.
Таллий был открыт У. Круксом в 1861 г. Содержание его в земной коре составляет 10-4 %. Сплав таллия (10 %) с оловом (20 %) и свинцом (70 %) обладает очень высокой кислотоупорностью, он выдерживает действие смеси серной, соляной и азотной кислот. Таллий повышает чувствительность фотоэлементов к инфракрасному излучению, исходящему от нагретых предметов. Соединения таллия весьма ядовиты и вызывают выпадение волос.
Соединения таллия весьма ядовиты и вызывают выпадение волос.
Галлий, индий и таллий относятся к рассеянным элементам. Содержание их в рудах, как правило, не превышает тысячных долей процент [3].
ХИМИЧЕСКИЕ СВОЙСТВА БОРА. ПРИМЕНЕНИЕ
Твердый, хрупкий, блестяще-чёрный полуметалл.
Химически бор при обычных условиях довольно инертен взаимодействует активно лишь с фтором, причем кристаллический Бор менее активен, чем аморфный.
С повышением температуры активность бора возрастает и он соединяется с кислородом, серой, галогенами. При нагревании на воздухе до 700°С Бор горит красноватым пламенем, образуя борный ангидрид B2O3 – бесцветную стекловидную массу.
При нагревании выше 900 °С бор с азотом образует нитрид бора BN, при нагревании с углем -карбид бора B4C3, с металлами – бориды.
С водородом бор заметно не реагирует; его гидриды (бороводороды) получают косвенным путем. При температуре красного каления бор взаимодействует с водяным паром:
При температуре красного каления бор взаимодействует с водяным паром:
2B + 3Н2О = B2O3 + 3H2.
Бор реагирует только с горячей азотной, серной кислотой и в царской водкой, с образованием борной кислоты H3BO3.
Медленно растворяется в концентрированных растворах щелочей с образованием боратов.
При сильном нагревании бор проявляет восстановительные свойства. Он способен, например, восстановить кремний или фосфор из их оксидов:
Данное свойство бора можно объяснить очень высокой прочностью химических связей в оксиде бора B2O3.
Применение.
Элементарный бор
Бор (в виде волокон) служит упрочняющим веществом многих композиционных материалов.
Также бор часто используют в электронике для изменения типа проводимости кремния.
Бор применяется в металлургии в качестве микролегирующего элемента, значительно повышающего прокаливаемость сталей.
Соединения бора.
Карбид бора применяется в компактном виде для изготовления газодинамических подшипников.
Пербораты / пероксобораты (содержат ион [B2(O2)2(OH)4]2-) Технический продукт содержит до 10,4% «активного кислорода», на их основе производят отбеливатели, «не содержащие хлор» («персиль», «персоль» и др.).
Отдельно также стоит указать на то что сплавы бор-углерод-кремний обладают сверхвысокой твёрдостью и способны заменить любой шлифовальный материал (кроме нитрида углерода, алмаза, нитрида бора по микротвёрдости), а по стоимости и эффективности шлифования (экономической) превосходят все известные человечеству абразивные материалы.
Сплав бора с магнием (диборид магния MgB2) обладает, на данный момент, рекордно высокой критической температурой перехода в сверхпроводящее состояние среди сверхпроводников первого рода. Появление вышеуказанной статьи стимулировало большой рост работ по этой тематике.
Борная кислота (H3BO3) широко применяется в атомной энергетике в качестве поглотителя нейтронов в ядерных реакторах типа ВВЭР (PWR) на «тепловых» («медленных») нейтронах. Благодаря своим нейтронно-физическим характеристикам и возможности растворяться в воде, применение борной кислоты делает возможным плавное (не ступенчатое) регулирование мощности ядерного реактора путем изменения ее концентрации в теплоносителе – так называемое «борное регулирование».
Бороводороды и борорганические соединения
Ряд органических производных бора (бороводороды) являются чрезвычайно эффективными ракетными топливами (диборан(B2h5), пентаборан, тетраборан и др.), а некоторые полимерные соединения с водородом и углеродом являются чрезвычайно стойкими к химическим воздействиям и высоким температурам, например широко известный пластик Карборан-22.
Биологическая роль
Бор — важный микроэлемент, необходимый для нормальной жизнедеятельности растений. Недостаток бора останавливает их развитие, вызывает у культурных растений различные болезни. В основе этого лежат нарушения окислительных и энергетических процессов в тканях, снижение биосинтеза необходимых веществ. При дефиците бора в почве в сельском хозяйстве применяют борные микроудобрения (борная кислота, бура и другие), повышающие урожай, улучшающие качество продукции и предотвращающие ряд заболеваний растений.
Недостаток бора останавливает их развитие, вызывает у культурных растений различные болезни. В основе этого лежат нарушения окислительных и энергетических процессов в тканях, снижение биосинтеза необходимых веществ. При дефиците бора в почве в сельском хозяйстве применяют борные микроудобрения (борная кислота, бура и другие), повышающие урожай, улучшающие качество продукции и предотвращающие ряд заболеваний растений.
Роль бора в животном организме не выяснена. В мышечной ткани человека содержится (0,33—1)•10 – 4% бора, в костной ткани (1,1—3,3)•10 – 4%, в крови— 0,13мг/л. Ежедневно с пищей человек получает 1—3 мг бора. Токсичная доза— 4г.
Один из редких типов дистрофии роговицы связан с геном, кодирующим белок-транспортер, предположительно регулирующий внутриклеточную концентрацию бора.
Дата добавления: 2016-06-22; просмотров: 26308; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Элементы основной группы | ChemTalk
Учебные пособия
- Сообщение от Доннелл Грин
18 Aug
Основные понятия
В этом уроке вы познакомитесь с основными групповыми элементами в химии и физике и узнаете, почему они считаются основными групповыми элементами.
Темы, освещенные в других статьях
- Электронные орбитали и формы орбит
- Что такое Ка, константа кислотной диссоциации
- Привлекательный и катастрофический элемент Хлор
- Что такое валентные электроны
- Балансирующие химические уравнения
репрезентативные элементы, состоят из элементов, принадлежащих к s-блоку и p-блоку периодической таблицы, и наиболее распространены на Земле и в космосе. Многие элементы основной группы необходимы для жизни на Земле, особенно кислород, углерод, азот и водород.
Орбитальные блоки периодической таблицы
Элементы, находящиеся в одинаковых группах или столбцах, могут быть объединены в блоки периодической таблицы на основе их валентных электронов (самых удаленных электронов). В периодической таблице есть четыре блока s, p, d и f. Если элементы находятся в одном блоке, их последний валентный электрон занимает одну и ту же орбиталь. Периодическая таблица упорядочивает элементы в соответствии с их электронной конфигурацией.
В периодической таблице есть четыре блока s, p, d и f. Если элементы находятся в одном блоке, их последний валентный электрон занимает одну и ту же орбиталь. Периодическая таблица упорядочивает элементы в соответствии с их электронной конфигурацией.
S-блок
Все элементы в этом блоке будут занимать один и тот же блок. Это означает, что атомы этих элементов имеют свои валентные электроны на s-орбитали. Элементы в этом блоке расположены в первой и второй группах, включая гелий.
www.flexiprep.com .За исключением водорода и гелия, все элементы в этом блоке являются металлами и имеют схожие свойства.
Свойства элемента S-блока
- Элементы S-блока имеют одну степень окисления
- Их общая конфигурация валентных электронов нс 1-2
- Щелочные металлы (группа 1) имеют степень окисления +1 Элементы 2 группы (щелочноземельные металлы) имеют степень окисления +2.
- Все элементы s-блока обладают высокой реакционной способностью, кроме гелия.

- Они имеют тенденцию быть мягкими с низкой температурой кипения
- Металлы S-блока очень электроположительны.
P-Block
Этот блок находится в правой части периодической таблицы и содержит элементы, расположенные в шести разных столбцах. Валентные электроны этих элементов находятся на р-орбитали. Гелий исключен из p-блока, который начинается со столбца 3A и заканчивается столбцом 8A.
Свойства этих элементов будут различаться, поскольку они охватывают большую часть периодической таблицы элементов.
Свойства элемента P-блока
- Элементы p-блока имеют несколько степеней окисления. Например, сера имеет -2, 0, +2, +4 и +6.
- Степень окисления зависит от группы. Элементы группы 17 (галогены) имеют степень окисления -1, но группа 18 (благородные газы) имеет степень окисления 0.
- Общая степень окисления n s 2 n p 1–6 . Их валентный электрон находится на p-орбитали
- .
 Они содержат металлы, неметаллы и металлоиды, поэтому их свойства зависят от их группы.
Они содержат металлы, неметаллы и металлоиды, поэтому их свойства зависят от их группы.
Важность элементов главной группы
Элементы главной группы важны по нескольким причинам:
Земля и Вселенная
Элементы основной группы наиболее распространены в составе Земли и Вселенной. Эти элементы составляют 80% земной коры. Кислород и кремний составляют большую часть земной коры. Например, кислород и кремний, водород и гелий составляют большую часть Вселенной. Водород, который, как говорят, был создан во время горячего Большого взрыва, составляет почти 70% Вселенной. Углерод является важным элементом для всех форм жизни на Земле.
Промышленные
Эти элементы основной группы и их соединения относятся к наиболее экономически важным элементам. Элемент литий является ключевым фактором в лечении таких заболеваний, как шизофрения и биполярное расстройство. Чаще всего элемент натрия (Na) используется для приправы к пище в виде поваренной соли или хлорида натрия (NaCl). В атомных часах используется цезий, потому что он может точно измерять резонансные частоты.
В атомных часах используется цезий, потому что он может точно измерять резонансные частоты.
Биологическое использование
Магний является одним из наиболее распространенных щелочноземельных металлов. Это очень полезно в медицинских учреждениях. Магний используется в антацидах, слабительных и солях Эпсона. Кальция на Земле даже больше, чем магния. Это ключевой компонент в структурах живых существ, таких как кости, зубы, раковины и экзоскелеты. В отличие от бериллия, очень прозрачного элемента, рентгеновские лучи не могут проникать через барий, поэтому его используют для осмотра желудочно-кишечного тракта.
А как насчет элементов D-блока?
По большей части элементы в d-блоке не считаются входящими в основную группу элементов периодической таблицы. Переходные металлы в середине периодической таблицы, лантаноиды и актиноиды ниже основной части периодической таблицы не классифицируются как элементы основной группы. Некоторые ученые не считают водород элементом главной группы.
Части периодической таблицы
Части периодической таблицыЭлементы основной группы
| 1А | 2А | 3А | 4А | 5А | 6А | 7А | 8А | ||||||||||||
| (1) | (2) | (13) | (14) | (15) | (16) | (17) | (18) | ||||||||||||
| 3Б | 4Б | 5Б | 6Б | 7Б | — | 8Б | — | 1Б | 2Б | ||||||||||
| (3) | (4) | (5) | (6) | (7) | (8) | (9) | (10) | (11) | (12) | ||||||||||
| 1 | Х | Он | |||||||||||||||||
| 2 | Ли | Бе | Б | С | Н | О | Ф | Не | |||||||||||
| 3 | Нет | мг | Ал | Си | Р | С | Кл | Ар | |||||||||||
| 4 | К | Са | Sc | Ти | В | Кр | Мн | Фе | Со | Ni | Медь | Цинк | Га | Гэ | Как | Se | Бр | Кр | |
| 5 | руб | Ср | Д | Зр | № | Пн | ТК | Ру | Rh | ПД | Аг | CD | В | Сн | Сб | Те | я | Хе | |
| 6 | цезий | Ба | Ла | Хф | Та | Вт | Ре | ОС | Ир | Пт | Золото | рт. ст. ст. | Тл | Пб | Би | По | В | Р-н | |
| 7 | Пт | Ра | Ас | Рф | Дб | Сг | Бх | Гс | Мт | Дс | № | Ууб | — | Уук | — | — | — | — | |
| 6 | Се | Пр | Нд | вечера | См | ЕС | Гд | Тб | Дай | Хо | Er | Тм | Ыб | Лу | |||||
| 7 | Т | Па | У | Нп | Пу | Ам | см | Бк | См. | Эс | ФМ | МД | № | Лр |
Элементы основной группы (или репрезентативные элементы ) включают в себя многие из наиболее знакомых элементов периодической таблицы. Они находятся в двух высоких столбцах с левой стороны периодического журнала. стол и шесть высоких колонн с правой стороны.
Элементы основной группы включают ряд химических свойств, от металлов до неметаллов, и ряд физических состояний, от твердых до газов. Для многих периодических свойств, существуют довольно предсказуемые тенденции и закономерности во всем элементы основной группы.
В разделах под этим заголовком свойства каждой группы кратко описаны, наряду с некоторыми из наиболее важных химических свойства элементов этой группы.
Переходные металлы
Переходные металлы Металлы
| Позиция переходных металлов в периодической таблице | Переход Металлы и элементы основной группы | Электронная конфигурация ионов переходных металлов |
| Окисление Состояния переходных металлов | ||
Позиция Переходные металлы в периодической таблице
Элементы в периодической таблице часто делятся на четыре
категории: (1) элементы главной группы, (2) переходные металлы, (3)
лантаноиды и (4) актиниды. Элементы основной группы включите активные металлы в два крайних левых столбца
периодической таблицы и металлов, полуметаллов и неметаллов
в шести колонках справа. Переходные металлы металлические элементы, служащие мостом или переходом,
между двумя сторонами стола. Лантаниды и актинидов внизу таблицы иногда
известные как внутренних переходных металлов потому что у них есть
атомные номера, находящиеся между первым и вторым элементами в
последние два ряда переходных металлов.
Элементы основной группы включите активные металлы в два крайних левых столбца
периодической таблицы и металлов, полуметаллов и неметаллов
в шести колонках справа. Переходные металлы металлические элементы, служащие мостом или переходом,
между двумя сторонами стола. Лантаниды и актинидов внизу таблицы иногда
известные как внутренних переходных металлов потому что у них есть
атомные номера, находящиеся между первым и вторым элементами в
последние два ряда переходных металлов.
Переходные металлы в сравнении с Элементы основной группы
Существуют некоторые разногласия по поводу классификации элементы на границе между основной группой и элементы из переходного металла в правой части таблицы. рассматриваемые элементы – цинк (Zn), кадмий (Cd) и ртуть. (рт.ст.).
Разногласия по поводу того, должны ли эти элементы
классифицируются как элементы основной группы или переходные металлы. что различия между этими категориями не ясны.
Переходные металлы во многом похожи на металлы основной группы: они
похожи на металлы, они податливы и пластичны, проводят
тепла и электричества, и они образуют положительные ионы. Тот факт,
два лучших проводника электричества – переходный металл
(медь) и металл основной группы (алюминий) показывает степень
которые определяют физические свойства металлов основной группы и переходных
металлы перекрываются.
что различия между этими категориями не ясны.
Переходные металлы во многом похожи на металлы основной группы: они
похожи на металлы, они податливы и пластичны, проводят
тепла и электричества, и они образуют положительные ионы. Тот факт,
два лучших проводника электричества – переходный металл
(медь) и металл основной группы (алюминий) показывает степень
которые определяют физические свойства металлов основной группы и переходных
металлы перекрываются.
Между этими металлами также есть различия. переходные металлы более электроотрицательны, чем основная группа металлов, например, и, следовательно, с большей вероятностью образуют ковалентные соединения.
Другое различие между металлами основной группы и
переходные металлы можно увидеть в формулах соединений
они формируют. Металлы основной группы склонны к образованию солей (например,
NaCl, Mg 3 N 2 и CaS), в которых присутствуют
достаточно отрицательных ионов, чтобы сбалансировать заряд положительных
ионы. Переходные металлы образуют аналогичные соединения [например, FeCl 3 ,
HgI 2 или Cd(OH) 2 ], но они более вероятны
чем металлы основной группы с образованием комплексов, таких как FeCl 4 – ,
HgI 4 2- и Cd(OH) 4 2- ионы, которые имеют избыточное количество отрицательных ионов.
Переходные металлы образуют аналогичные соединения [например, FeCl 3 ,
HgI 2 или Cd(OH) 2 ], но они более вероятны
чем металлы основной группы с образованием комплексов, таких как FeCl 4 – ,
HgI 4 2- и Cd(OH) 4 2- ионы, которые имеют избыточное количество отрицательных ионов.
Третье различие между основной группой и переходным металлом ионов является легкость, с которой они образуют стабильные соединения с нейтральные молекулы, такие как вода или аммиак. Соли основной группы ионы металлов растворяются в воде с образованием водных растворов.
| Н 2 О | ||||
| NaCl( с ) | Na + ( водный раствор ) | + | Кл – ( водный ) |
Когда мы позволяем воде испариться, мы возвращаемся к исходному
исходный материал, NaCl ( с ). Соли переходного металла
ионы могут вести себя по-разному. Хром(III)
хлорид, например, представляет собой соединение фиолетового цвета, которое растворяется в
жидкий аммиак с образованием соединения желтого цвета с формулой CrCl 3 6 NH 3 , которые можно выделить, когда аммиак
дали испариться.
Соли переходного металла
ионы могут вести себя по-разному. Хром(III)
хлорид, например, представляет собой соединение фиолетового цвета, которое растворяется в
жидкий аммиак с образованием соединения желтого цвета с формулой CrCl 3 6 NH 3 , которые можно выделить, когда аммиак
дали испариться.
CrCl 3 ( с ) + 6 NH 3 ( л ) CrCl 3 6 НХ 3 ( с )
Электрон Конфигурация ионов переходных металлов
Соотношение между электронными конфигурациями элементы переходных металлов и их ионы являются сложными.
Пример: Рассмотрим химию кобальта, который образует комплексы, содержащие Co 2+ или Co 3+ ионы.
Электронная конфигурация нейтрального атома кобальта записывается
следующим образом.
Co: [Ar] 4 s 2 3 d 7
Обсуждение относительных энергий атомных орбиталей предполагает, что орбиталь 4 s имеет более низкую энергию, чем 3 d . орбитали. Таким образом, можно ожидать, что кобальт потеряет электроны из более высокой энергии 3 d орбиталей, но это не то, что наблюдаемый. Ко 2+ и Co 3+ имеют следующих электронных конфигураций.
Co 2+ : [Ar] 3 d 7
Co 3+ : [Ar] 3 d 6 валентная оболочка s орбиталей до того, как они будут удалены из валентность d орбиталей при ионизации переходных металлов.
Поскольку валентные электроны в ионах переходных металлов
сконцентрировано в d орбитали, эти ионы часто описывают
как имеющие конфигурации d n . Компания 3+ и Fe 2+ , например, говорят, что они имеют d 6 конфигурация.
Co 3+ : [Ar] 3 d 6
Fe 2+ : [Ar] 3 d 6
Oxidation States of в Переходные металлы
Большинство переходных металлов имеют более одной степени окисления.
Однако некоторые степени окисления встречаются чаще, чем другие. Наиболее распространенные степени окисления первой серии переходные металлы приведены в таблице ниже. Усилия по объяснить очевидную закономерность в этой таблице в конечном итоге не удается для сочетание причин. Некоторые из этих степеней окисления являются общими потому что они относительно стабильны. Другие описывают соединения которые не обязательно стабильны, но реагируют медленно. Все еще другие распространены только с исторической точки зрения.
Общие степени окисления первой серии переходных металлов
| Sc | Ти | В | Кр | Мн | Fe | Ко | Ni | Медь | Цинк | |||||||||||
| +1 | г 10 | |||||||||||||||||||
| +2 | д 3 | г 5 | г 6 | г 7 | д 8 | г 9 | г 10 | |||||||||||||
| +3 | г 0 | д 3 | г 5 | г 6 | ||||||||||||||||
| +4 | г 0 | д 3 | ||||||||||||||||||
| +5 | г 0 | |||||||||||||||||||
| +6 | д 0 | |||||||||||||||||||
| +7 | г 0 |
Одно замечание о степенях окисления переходных металлов
Особого внимания заслуживают: ионы переходных металлов с зарядами
больше +3 не может существовать в водном растворе.
Рассмотрим следующую реакцию окисления марганца от степени окисления +2 до +7.
| Mn 2+ ( водный ) + 4 H 2 O( л ) MnO 4 – ( водный раствор ) + 8 H + ( водный раствор ) + 5 е – |
Когда атом марганца окисляется, он становится более электроотрицательный. В степени окисления +7 этот атом достаточно электроотрицательны, чтобы реагировать с водой с образованием ковалентных оксид, MnO 4 – .
Полезно иметь способ различать заряд иона переходного металла и степень окисления переходный металл. По соглашению такие символы, как Mn 2+ относятся к ионам, которые несут заряд +2. Такие символы, как Mn(VII), используется для описания соединений, в которых марганец находится в +7 степень окисления.
Mn(VII) — не единственный пример сильной степени окисления. достаточно для разложения воды. Как только Mn 2+ окислится
до Mn(IV), он реагирует с водой с образованием MnO 2 . А
подобное явление можно увидеть в химии как ванадия
и хром. Ванадий существует в водных растворах в виде V 2+ ион. Но как только он окисляется до степени окисления +4 или +5, он
реагирует с водой с образованием VO 2+ или VO 2 + ион. Ион Cr 3+ можно найти в водном растворе.
Но как только этот ион окисляется до Cr(VI), он реагирует с водой до
образуют CrO 4 2- и Cr 2 O 7 2- ионы.
достаточно для разложения воды. Как только Mn 2+ окислится
до Mn(IV), он реагирует с водой с образованием MnO 2 . А
подобное явление можно увидеть в химии как ванадия
и хром. Ванадий существует в водных растворах в виде V 2+ ион. Но как только он окисляется до степени окисления +4 или +5, он
реагирует с водой с образованием VO 2+ или VO 2 + ион. Ион Cr 3+ можно найти в водном растворе.
Но как только этот ион окисляется до Cr(VI), он реагирует с водой до
образуют CrO 4 2- и Cr 2 O 7 2- ионы.
Объяснение названий групп периодической таблицы для родителей
Периодическая таблица представляет собой набор химических элементов в табличной форме.
Все элементы периодической таблицы расположены в соответствии с несколькими символами. К ним относятся: общие химические свойства, электронная конфигурация (распределение электронов по орбитам) и атомные номера (количество протонов в атоме).
Периодическая таблица разделена на семь строк, называемых периодами, и 18 столбцов, называемых группами. Вот сжатый список всех групп периодической таблицы, которым вы можете легко научить своих детей.
Чтобы узнать больше о разных именах, взгляните на эти королевские фамилии или эти тайские фамилии и их значения.
Группы периодической таблицы
Группа 1: Щелочные металлы
Щелочные металлы мягкие, пластичные и хорошо проводят электричество и тепло. В эту группу входят элементы литий, натрий, калий, рубидий, цезий и франций. Щелочные металлы очень реакционноспособны. По сравнению с другими элементами они имеют более низкую температуру плавления и кипения.
Группа 2: Щелочноземельные металлы
Вторая группа элементов в периодической таблице – щелочноземельные металлы. Эти элементы находятся в земной коре и представляют собой мягкие и серебристые металлы. Они могут проводить тепло и электричество и могут быть превращены в листы. Некоторыми элементами этой группы являются бериллий, кальций и магний.
Некоторыми элементами этой группы являются бериллий, кальций и магний.
Группы с 3 по 12: переходные металлы
Элементы с 3 по 12 группы называются переходными металлами. К ним относятся семейства элементов скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Переходные металлы твердые и плотные, являются хорошими проводниками тепла и электричества и легко гнутся. Золото, железо и медь являются важными такими элементами.
Группа 13: Группа бора
Группа бора названа в честь ведущего элемента бора. Они хорошие проводники, но редко встречаются в природе. Алюминий является исключением в этой группе, так как он встречается в изобилии.
Группа 14: Группа углерода
Группа углерода состоит из углерода, кремния, германия, олова, свинца и флеровия. Все элементы встречаются в природе достаточно широко, кроме флеровия. Элементы этой группы и их соединения обычно токсичны.
Группа 15: Пниктогены
Пниктогены состоят из азота (N), за которым следуют фосфор (представленный как P), мышьяк (As), сурьма (Sb), висмут (Bi) и, наконец, московий (Mc ). В то время как азот и фосфор встречаются в природе, другие не встречаются, поскольку московий является синтетическим элементом, производимым только в лабораториях.
Группа 16: Халькогены
В состав халькогенов входят кислород, сера, селен, теллур и радиоактивный элемент полоний. Ливерморий – синтетический элемент, входящий в эту группу. В то время как кислорода и фосфора в природе много, селена и теллура нет. Полоний обнаруживается только в следовых количествах из-за радиоактивного распада, а ливермориум производится только в лабораториях.
Группа 17: Галогены
Галогены состоят из фтора, хлора, брома, йода, астата и синтетического элемента теннессина. Это неметаллы, которые являются плохими проводниками с низкими температурами плавления и кипения. Группа галогенов также является единственной группой, в элементах которой при комнатной температуре можно увидеть все три состояния вещества.
Группа галогенов также является единственной группой, в элементах которой при комнатной температуре можно увидеть все три состояния вещества.
Группа 18: Благородные газы
Благородные газы состоят из гелия, неона, аргона, криптона, ксенона, радона и синтетического газа Оганесон. Они составляют около 0,96% атмосферы. Эти газы имеют различные применения, такие как освещение, сварка и исследование космоса, хотя по своей природе они крайне нереакционноспособны и бесцветны.
В Kidadl есть много замечательных именных статей, которые могут вас вдохновить. Если вам понравился наш список имен периодической таблицы, то почему бы не узнать об этих венгерских фамилиях или об этих индийских фамилиях с историей и значениями.
Заявление об отказе от ответственности
В Kidadl мы гордимся тем, что предлагаем семьям оригинальные идеи, чтобы максимально использовать время, проведенное вместе дома или на улице, где бы вы ни находились. Мы стремимся рекомендовать самые лучшие вещи, предложенные нашим сообществом, и то, что мы сделали бы сами – наша цель – быть надежным другом для родителей.
Мы стараемся изо всех сил, но не можем гарантировать совершенство. Мы всегда будем стремиться предоставить вам точную информацию на дату публикации, однако информация может меняться, поэтому важно, чтобы вы провели собственное исследование, перепроверили и приняли решение, подходящее для вашей семьи.
Kidadl вдохновляет детей развлекать и обучать их. Мы понимаем, что не все виды деятельности и идеи подходят и подходят для всех детей и семей или во всех обстоятельствах. Наши рекомендуемые занятия основаны на возрасте, но это ориентир. Мы рекомендуем использовать эти идеи в качестве вдохновения, чтобы идеи воплощались в жизнь под надлежащим наблюдением взрослых, и чтобы каждый взрослый использовал свое собственное усмотрение и знания своих детей для рассмотрения безопасности и пригодности.
Kidadl не может нести ответственность за реализацию этих идей, поэтому рекомендуется постоянно находиться под присмотром родителей, так как безопасность превыше всего. Любой, кто использует информацию, предоставленную Kidadl, делает это на свой страх и риск, и мы не несем ответственности, если что-то пойдет не так.
Политика в отношении спонсорства и рекламы
Kidadl является независимой организацией, и чтобы сделать наши услуги бесплатными для вас, читатель, мы поддерживаем рекламу.
Надеемся, вам понравились наши рекомендации по продуктам и услугам! То, что мы предлагаем, выбирается независимо командой Kidadl. Если вы совершаете покупку с помощью кнопки «Купить сейчас», мы можем получить небольшую комиссию. Это не влияет на наш выбор. Обратите внимание: цены указаны правильно, а товары есть в наличии на момент публикации статьи.
У Kidadl есть ряд партнеров, с которыми мы работаем, включая Amazon. Обратите внимание, что Kidadl является участником партнерской программы Amazon Services LLC, партнерской рекламной программы, предназначенной для предоставления сайтам средств для получения платы за рекламу за счет рекламы и ссылок на Amazon.
Мы также ссылаемся на другие веб-сайты, но не несем ответственности за их содержание.
Ознакомьтесь с нашей Политикой в отношении спонсорства и рекламы
Основная группа Renaissance | Особенность
После долгих лет, проведенных за более модными направлениями исследований, основные групповые элементы снова в моде. Джеймс Митчелл Кроу выясняет, почему
Джеймс Митчелл Кроу выясняет, почему
Precision Graphics
Справедливости ради стоит сказать, что основные элементы группы не являются самыми гламурными элементами периодической таблицы. Металлы s-блока, такие как кальций, и элементы p-блока, такие как бор и германий, буквально затмевают своих более ярких соседей из переходных металлов — золото, палладий и родий. Даже с точки зрения чистой химии реакционная способность элементов главной группы всегда казалась несколько стабильной по сравнению с виртуозными каталитическими трюками, которые обычно выполняют многие переходные металлы. Уже в 19В 70-е годы казалось, что основные элементы группы уже раскрыли все свои секреты, оставив будущим поколениям исследователей мало что нового.
«Что касается неорганической химии, основная группа была самой скучной частью моего бакалавриата, — вспоминает Кэмерон Джонс, научный сотрудник Университета Монаш в Мельбурне, Австралия, получивший степень в Университете Западной Австралии в 1984 году. «В то время считалось, что все, что нам нужно было знать о химии элементов главной группы, было известно: свойства, степени окисления и реакционная способность были довольно хорошо изучены, и не было никаких новых направлений», — говорит он. Для сравнения, химия переходных металлов переживала период взрывного роста, который еще не прекратился.
«В то время считалось, что все, что нам нужно было знать о химии элементов главной группы, было известно: свойства, степени окисления и реакционная способность были довольно хорошо изучены, и не было никаких новых направлений», — говорит он. Для сравнения, химия переходных металлов переживала период взрывного роста, который еще не прекратился.
Но в то самое время, когда Джонс изучал сухие условности классической химии главных групп, в литературе уже начали появляться первые признаки возрождения в этой области. В начале 1980-х годов было обнаружено, что элементы p-блока, такие как кремний и фосфор, могут быть переведены в экзотические состояния существования — низкие состояния окисления и низкой координации — в соединениях, которые были совершенно стабильны при комнатной температуре. Хотя потенциальные применения были бы далеки от мысли химиков, впервые открывших этот дикий новый рубеж соединений главных групп, более поздние работы показывают, что их химия обладает богатством и полезностью, чтобы соперничать с химией переходных металлов, которые долгое время затмевали их. И Джонс входит в число тех исследователей, которые в настоящее время находятся в авангарде возрождения.
И Джонс входит в число тех исследователей, которые в настоящее время находятся в авангарде возрождения.
Эти три соединения, каждое из которых имеет необычную кратную связь, вызвали новый интерес к химии основных групп
1981 год считается поворотным моментом, говорит Джонс. В том же году были опубликованы три прорывных открытия, которые начали разрушать ортодоксию основной групповой химии — начиная с так называемого правила двойной связи, которое гласило, что только самые легкие члены периодической таблицы могут образовывать стабильные двойные связи. Роберт Уэст из Университета Висконсин-Мэдисон в США и его коллеги были первыми нарушителями правил, создав самый ранний пример стабильного соединения, включающего двойную связь кремний-кремний, эквивалент алкена в органической химии. 1
Вскоре после этого Масааки Йошифудзи из Токийского университета в Японии и его команда получили первую двойную связь фосфор-фосфор. 2 В том же году Герд Беккер и его коллеги из Штутгартского университета (Германия) синтезировали соединение, содержащее тройную связь фосфор-углерод. 3 В последнем соединении фосфор находился не только в низкой степени окисления, но и был однокоординированным, что указывает на будущее, в котором элементы главной группы с вакантными координационными центрами могут действовать как каталитические центры, способные захватывать субстраты для катализа. .
3 В последнем соединении фосфор находился не только в низкой степени окисления, но и был однокоординированным, что указывает на будущее, в котором элементы главной группы с вакантными координационными центрами могут действовать как каталитические центры, способные захватывать субстраты для катализа. .
Увеличение объема
Ключом к этому прорыву стал дизайн лиганда. Эти три соединения объединяет использование объемных заместителей для стабилизации рассматриваемого элемента основной группы в состоянии, которое в противном случае было бы слишком нестабильным. «Стерический объем позволяет кинетическую стабилизацию систем с низкими координатами и низкими степенями окисления», — объясняет Джонс. «Это мешает им реагировать с кислородом или водой или подвергаться процессам диспропорционирования [которые возвращают элемент к его более обычным состояниям окисления]». Дисилен Уэста, например, содержал в общей сложности четыре объемных лиганда на основе бензола, называемых мезитильными группами, тогда как Йошифуджи использовал две еще более объемные три-трет-бутилфенильные группы для создания своего дифосфена.
По мере того, как объемная конструкция лиганда позволяла получать все больше и больше стабильных примеров элементов основной группы с низкой степенью окисления или координационным числом, все большее число исследователей начало присоединяться к этой области. «Возможно, только на рубеже тысячелетий он действительно взлетел — теперь кажется, что почти в каждом выпуске Nature Chemistry или Science что-то есть», — говорит Джонс.
Этот силилен стабилен, несмотря на то, что он только двухкоординатный
Примеры стабильных соединений, содержащих элементы главной группы в состояниях, которые когда-то считались невозможными, продолжают появляться. Не так давно появились стабильные ациклические силилены – кремниевый эквивалент карбена, высокореакционное соединение, которое является только двухкоординатным и имеет свойства неподеленная электронная пара на кремнии – неслыханно. В 2012 году Джонс и его сотрудники из Оксфордского университета и Университетского колледжа Лондона в Великобритании опубликовали первый пример, стабилизированный объемным лигандом на основе бора. 4 «На самом деле это хорошо связано с первым дисилиленом Уэста», — говорит он. «Способ, которым он это сделал, заключался в том, чтобы начать с [обычного] соединения кремния (iv) и провести его фотолиз. Он предположил, что получил силиленовый промежуточный продукт темно-синего цвета, стабильный только при температуре ниже 77К, а затем димеризировался с образованием двойной кремний-кремниевой связи». Уэста и Йошифудзи. «Их прорыв, демонстрирующий, что можно выделить эти соединения, поместить их в бутылку и изучить их реакционную способность — на этом этапе я был очарован», — вспоминает он. В настоящее время Дрисс работает исследователем в этой области в Берлинском техническом университете в Германии — в этой области претерпевает переход от простого создания этих новых соединений к попыткам их применения. «После того, как люди охотились на новые виды, они задавались вопросом: «Что мы можем с ними сделать?», — говорит он. «После некоторого времени, когда вы поиграете с новыми системами, как только вы поймете, на что они способны, вы захотите использовать их на благо человечества.
4 «На самом деле это хорошо связано с первым дисилиленом Уэста», — говорит он. «Способ, которым он это сделал, заключался в том, чтобы начать с [обычного] соединения кремния (iv) и провести его фотолиз. Он предположил, что получил силиленовый промежуточный продукт темно-синего цвета, стабильный только при температуре ниже 77К, а затем димеризировался с образованием двойной кремний-кремниевой связи». Уэста и Йошифудзи. «Их прорыв, демонстрирующий, что можно выделить эти соединения, поместить их в бутылку и изучить их реакционную способность — на этом этапе я был очарован», — вспоминает он. В настоящее время Дрисс работает исследователем в этой области в Берлинском техническом университете в Германии — в этой области претерпевает переход от простого создания этих новых соединений к попыткам их применения. «После того, как люди охотились на новые виды, они задавались вопросом: «Что мы можем с ними сделать?», — говорит он. «После некоторого времени, когда вы поиграете с новыми системами, как только вы поймете, на что они способны, вы захотите использовать их на благо человечества. Что касается химии основных групп, это только началось».
Что касается химии основных групп, это только началось».
Разработкой, указывающей на возможность использования соединений основной группы с низкой степенью окисления, стало осознание в середине прошлого десятилетия того, что они способны активировать небольшие молекулы, такие как углеводороды, диводород и двуокись углерода. «Мечта состоит в том, чтобы использовать неметаллы в качестве катализаторов важных преобразований малых молекул, на которые мы все полагаемся», — говорит Дрисс.
Подвинься, металл
Зачем утруждать себя разработкой катализаторов на основе основных групп? Переходные металлы являются хорошо зарекомендовавшими себя мастерами химии катализа, и новые грани их реакционной способности продолжают открываться. Но у них есть и недостаток, отмечает Даг Стефан, исследователь катализа основных групп из Университета Торонто в Канаде, который, возможно, приблизил катализ основных групп к синтетической полезности (см. вставку). Наиболее активными катализаторами на основе переходных металлов обычно являются дорогие драгоценные металлы, такие как родий, палладий и платина. Эти металлы также считаются токсичными, что создает проблемы, например, при их использовании для синтеза фармацевтических препаратов. «Одна из самых больших затрат, связанных с производством лекарств в наши дни, — это удаление переходных металлов», — говорит Стефан. По его словам, переход на катализаторы основной группы облегчил бы эту проблему, а, скажем, бор или кремний также значительно дешевле любого драгоценного металла. Он признает, что другие переходные металлы, такие как железо или никель, также имеют эту привлекательность — системы основной группы просто предлагают другую альтернативу.
Эти металлы также считаются токсичными, что создает проблемы, например, при их использовании для синтеза фармацевтических препаратов. «Одна из самых больших затрат, связанных с производством лекарств в наши дни, — это удаление переходных металлов», — говорит Стефан. По его словам, переход на катализаторы основной группы облегчил бы эту проблему, а, скажем, бор или кремний также значительно дешевле любого драгоценного металла. Он признает, что другие переходные металлы, такие как железо или никель, также имеют эту привлекательность — системы основной группы просто предлагают другую альтернативу.
Мечту Дрисса о безметалловом катализе разделяют многие другие специалисты в этой области, включая Джонса. «Люди все больше и больше обращают внимание на реакционную способность, а это очень реактивные системы — я думаю, это следующий этап возрождения химии основных групп», — говорит он. Недавняя публикация Джонса, раскрывающая, например, первый ациклический силилен, также показала, что соединение активирует диводород даже при температуре ниже комнатной — первое соединение кремния, которое, как было показано, делает это.
Использование соединения основной группы для активации диводорода — разрыв связи водород-водород в процессе окислительного присоединения, так что два атома водорода в конечном итоге ковалентно связаны с атомом кремния — было впервые достигнуто Филом Пауэром и его командой в университете. Калифорнии, Дэвис в США. Пауэр использовал дигермин, германиевый эквивалент алкина. 5 Процесс может показаться тривиальным, но на самом деле это немалое достижение. «Диводород — это самая маленькая молекула, которую только можно себе представить, но с самой прочной ковалентной связью между двумя гомоэлементами», — говорит Дрисс.
Независимо от того, является ли элемент основной группой или переходным металлом, элемент должен иметь несколько ключевых свойств, чтобы таким образом разделить диводород. «Центру нужен свободный координационный центр — пустая орбиталь, на которую можно всосать электроны диводорода», — говорит Дрисс. Чтобы сделать это эффективно, энергия этой орбитали (самая низкая незанятая молекулярная орбиталь, или НСМО) должна довольно близко совпадать с энергией орбитали донора диводорода (ее самая высокая занятая молекулярная орбиталь, или ВЗМО). «Это то, что прекрасно выполняют переходные металлы — вакантное координационное место и НСМО, который соответствует энергии ВЗМО молекулы диводорода», — говорит Дрисс. «Но в этом также прелесть некоторых низкокоординатных соединений основной группы», — добавляет он. «Сегодня у нас есть много примеров соединений кремния с вакантным координационным центром — теперь нам нужно научиться настраивать электронный уровень, акцепторный уровень НСМО. Мы как раз на том этапе, когда можем показать, что это действительно возможно».
«Это то, что прекрасно выполняют переходные металлы — вакантное координационное место и НСМО, который соответствует энергии ВЗМО молекулы диводорода», — говорит Дрисс. «Но в этом также прелесть некоторых низкокоординатных соединений основной группы», — добавляет он. «Сегодня у нас есть много примеров соединений кремния с вакантным координационным центром — теперь нам нужно научиться настраивать электронный уровень, акцепторный уровень НСМО. Мы как раз на том этапе, когда можем показать, что это действительно возможно».
Science/AAAS
N-гетероциклические карбеновые лиганды превращают бор из кислоты Льюиса в основание Льюиса Необходимым условием является стерический объем, но он слишком громоздкий, и входящая молекула диводорода не сможет получить доступ к центральному атому кремния. Точно так же химический состав лиганда влияет на уровни орбитальной энергии. «На данный момент одними из лучших лигандов, которые у нас есть, являются лиганды, хелатирующие азот, называемые бета-дикетаминатильными лигандами», — говорит Дрис. «А еще у нас есть карбены. Я думаю, что на данный момент это звездные лиганды; N -гетероциклический карбеновый лиганд действительно является одним из прорывов в химии основных групп». в котором центральный атом бора окружен с каждой стороны N-гетероциклическим карбеном (NHC). 6 Бор, как правило, представляет собой квинтэссенцию кислоты Льюиса: атом, наделенный только тремя электронами в нейтральном состоянии, ему далеко до восьми, необходимых для максимальной стабильности, и поэтому он известен как превосходный акцептор электронов. Однако NHC являются настолько мощными донорами электронов, что сам атом бора меняет поведение, чтобы стать донором электронов. «Это переворачивает мир с ног на голову», — говорит Стефан, чей взгляд также был захвачен работой. «Он берет кислоту Льюиса и превращает ее в основание Льюиса. На данном этапе это фундаментальное исследование, но ужасно интересное», — добавляет он.
«А еще у нас есть карбены. Я думаю, что на данный момент это звездные лиганды; N -гетероциклический карбеновый лиганд действительно является одним из прорывов в химии основных групп». в котором центральный атом бора окружен с каждой стороны N-гетероциклическим карбеном (NHC). 6 Бор, как правило, представляет собой квинтэссенцию кислоты Льюиса: атом, наделенный только тремя электронами в нейтральном состоянии, ему далеко до восьми, необходимых для максимальной стабильности, и поэтому он известен как превосходный акцептор электронов. Однако NHC являются настолько мощными донорами электронов, что сам атом бора меняет поведение, чтобы стать донором электронов. «Это переворачивает мир с ног на голову», — говорит Стефан, чей взгляд также был захвачен работой. «Он берет кислоту Льюиса и превращает ее в основание Льюиса. На данном этапе это фундаментальное исследование, но ужасно интересное», — добавляет он.
Обучение циклированию
Хотя разработка низковалентных соединений основной группы, которые могут успешно координировать небольшие молекулы, такие как диводород, в настоящее время достигнута, этот шаг является лишь первым в последовательности реакций, которые необходимо разработать, чтобы мечта Дрисса превратить основную группу сгруппировать соединения в полезные катализаторы. Например, активация диводорода может быть первой стадией процесса гидрирования для каталитического превращения алкена в алкан путем добавления диводорода через двойную углерод-углеродную связь. В реакции гидрирования, катализируемой переходными металлами, этапом после окислительного присоединения диводорода будет координация алкенового субстрата, на который переносятся атомы водорода, прежде чем он отщепится для регенерации исходного металлического центра, и процесс начнется снова.
Например, активация диводорода может быть первой стадией процесса гидрирования для каталитического превращения алкена в алкан путем добавления диводорода через двойную углерод-углеродную связь. В реакции гидрирования, катализируемой переходными металлами, этапом после окислительного присоединения диводорода будет координация алкенового субстрата, на который переносятся атомы водорода, прежде чем он отщепится для регенерации исходного металлического центра, и процесс начнется снова.
Но чтобы такой цикл заработал, нужно избежать нескольких ловушек. «Для соединений основной группы с низким координационным числом, если вы активируете диводород, но связь образовавшегося элемента с водородом слишком сильна, или если для второго субстрата больше нет вакантного координационного центра, то это тупик», — говорит Дрисс. . Навигация по этой сложной территории, чтобы реализовать все шаги для полного каталитического цикла, еще не завершена.
«До сих пор показывают, что соединения p-блока с низкой степенью окисления могут участвовать в реакциях, обычно связанных только с переходными металлами», — добавляет Джонс. «Настоящего катализа еще предстоит достичь, но я думаю, что это вполне осуществимо, и в течение следующих нескольких лет мы увидим появление настоящего катализа, особенно из элементов 14-й группы — кремния и германия».0003
«Настоящего катализа еще предстоит достичь, но я думаю, что это вполне осуществимо, и в течение следующих нескольких лет мы увидим появление настоящего катализа, особенно из элементов 14-й группы — кремния и германия».0003
Дрис еще более оптимистичен в отношении перспектив области: «Я ожидаю, что еще через 10 лет низковалентные соединения главной группы будут так же хороши, как традиционные соединения переходных металлов для активации малых молекул». – ломая исследования катализа переходных металлов, он, безусловно, имеет право судить.
Джеймс Митчелл Кроу — научный писатель из Мельбурна, Австралия. (ФЛП), — говорит Джонс.
John Hryniuk
Doug Stephan
FLP были открытием, сделанным Дугом Стефаном и его командой в Университете Торонто в Канаде в 2006 году. , стабилизируя некоторые очень активные катализаторы полимеризации с помощью доноров фосфина», — вспоминает Стефан. «Проведя серию реакций, мы обнаружили, что очень объемные фосфины ведут себя совсем по-другому — они реагируют не с титаном, а только с борным центром». 0003
0003
Стефан обнаружил, что он получил особенно маловероятно звучащее соединение: такое, которое будет реагировать с молекулой водорода, чтобы включить как протон (H + ), так и ион гидрида (H – ), первый расположен на атоме фосфора и последний в боре. Такое соединение звучит точно так, как будто оно должно спонтанно терять диводород, а не поглощать его. Ключом к такому поведению является использование объемных лигандов в исходных соединениях бора и фосфора, что предотвращает рекомбинацию протона и гидрид-иона с образованием диводорода при комнатной температуре. «После того, как вы активировали водород, очевидным следующим шагом будет его использование в катализе гидрирования, чем мы и занимались последние несколько лет», — говорит Стефан. Команда успешно гидрировала имины и алкены таким образом и теперь перешла к каталитическим реакциям, включающим активацию диоксида углерода, исходного сырья, которого в избытке.
‘Нашей первой попыткой было просто уловить углекислый газ с помощью ФЛП. Затем мы обнаружили, что если мы перейдем на стехиометрический алюминий-фосфор, мы сможем добиться стехиометрического восстановления, восстанавливая углекислый газ до монооксида углерода, а также двуокись углерода до метанола. Затем следующей эволюцией стала попытка получить каталитическую систему», — говорит Стефан. Процесс работал, но в процессе образовывался неприятный побочный продукт, оксид фосфина. «Нам нужен еще один акцептор кислорода, более ценный, чем оксид фосфина», — резюмирует Стефан. «Эта работа продолжается, но хорошая новость заключается в том, что мы можем заниматься катализом без использования драгоценных металлов».
Затем мы обнаружили, что если мы перейдем на стехиометрический алюминий-фосфор, мы сможем добиться стехиометрического восстановления, восстанавливая углекислый газ до монооксида углерода, а также двуокись углерода до метанола. Затем следующей эволюцией стала попытка получить каталитическую систему», — говорит Стефан. Процесс работал, но в процессе образовывался неприятный побочный продукт, оксид фосфина. «Нам нужен еще один акцептор кислорода, более ценный, чем оксид фосфина», — резюмирует Стефан. «Эта работа продолжается, но хорошая новость заключается в том, что мы можем заниматься катализом без использования драгоценных металлов».
Ссылки
1 R West, M J Fink and J Michl, Science , 1981, 214 , 1343 (DOI: 10.1126/science.214.4527.1343)
9004ji . хим. Soc ., 1981, 103 , 4587 (DOI: 10.1021/ja00405a054)3 G Becker, G Gresser and W Z Uhl, Z. Naturforsch. В , 1981, 36 , 16
4 Протченко А. В. и др., J. Am. хим. Soc ., 2012, 134 , 6500 (DOI: 10.1021/ja301042u)
В. и др., J. Am. хим. Soc ., 2012, 134 , 6500 (DOI: 10.1021/ja301042u)
5 GH Spikes, JC Fettinger and PP Power, J. Am. хим. SOC ., 2005, 127 , 12232 (doi: 10.1021/ja053247a)
6 R Kinjo и др., Science , 2011, 333 , 610 (doi: 10.1126/Science.1207333333) , 610 (DOI: 10.1126/Science.120733333)
70003 70003 7000373333) . Стефан, Орг. биомол. Chem ., 2012, 10 , 5740 (DOI: 10.1039/c2ob25339a)Периодическая таблица – tec-science
В периодической таблице все химические элементы классифицируются в соответствии с их атомным номером и химическими свойствами.
В периодической таблице все химические элементы классифицируются в соответствии с их атомным номером и их химическими свойствами в элементах основной группы (столбцы IA–VIIIA) и элементах переходной группы (IB–VIIIB). Число протонов непрерывно увеличивается слева направо. В дополнение к этой горизонтальной классификации периодическая таблица разделена по вертикали на периода . Эти периоды выбраны не случайно, а соответствуют в оболочечной модели электронной оболочке, введенной Бором (K, L, M, N, O, P и Q).
Число протонов непрерывно увеличивается слева направо. В дополнение к этой горизонтальной классификации периодическая таблица разделена по вертикали на периода . Эти периоды выбраны не случайно, а соответствуют в оболочечной модели электронной оболочке, введенной Бором (K, L, M, N, O, P и Q).
Все элементы в определенной группе демонстрируют одинаковое химическое поведение из-за одинакового количества электронов в их самой внешней оболочке (это относится только к элементам в основной группе).
В периодической таблице элементы разбиты на группы с одинаковыми химическими свойствами и периодами с одинаковым количеством оболочек!
Рисунок: Периодическая таблица элементов По мере увеличения числа периодов добавляется новая электронная оболочка. Следовательно, атомы внутри определенной группы увеличиваются в размерах сверху вниз периодической таблицы. С другой стороны, атомный радиус уменьшается слева направо в периодической таблице. Это связано с увеличением числа протонов, которое появляется вместе с атомным номером. Количество электронов в оболочке также будет увеличиваться. Чем больше протонов содержит атомное ядро, тем выше его заряд и тем выше заряд электронной оболочки. Однако более высокий заряд приводит к более сильной силе притяжения между ядром и оболочкой. Так как число оболочек не будет увеличиваться в течение периода, то чем больше сила притяжения, тем сильнее будет связь оболочки с ядром.
Количество электронов в оболочке также будет увеличиваться. Чем больше протонов содержит атомное ядро, тем выше его заряд и тем выше заряд электронной оболочки. Однако более высокий заряд приводит к более сильной силе притяжения между ядром и оболочкой. Так как число оболочек не будет увеличиваться в течение периода, то чем больше сила притяжения, тем сильнее будет связь оболочки с ядром.
Размер атома будет увеличиваться внутри группы сверху вниз, но будет уменьшаться в течение периода слева направо!
В течение каждого периода элемент в самой правой части периодической таблицы будет иметь наибольшую силу притяжения между его ядром и его оболочкой. Такая конфигурация делает элемент чрезвычайно устойчивым. Поскольку элементы с правой стороны являются газообразными, они обозначаются как благородные газы (или инертные газы ).
Классификация периодической таблицы на основные группы и переходные группы обусловлена их разным распределением электронов на атомных орбиталях (электронная конфигурация). По той же причине дальнейшее деление может быть произведено на лантаноиды и актиниды (термин акционид происходит от того факта, что все эти элементы радиоактивны).
По той же причине дальнейшее деление может быть произведено на лантаноиды и актиниды (термин акционид происходит от того факта, что все эти элементы радиоактивны).
В основной группе s- и p-орбитали соответствующих атомов заняты электронами («s-блок» или «p-блок»), а в переходной группе электрон добавляется на d-орбиталь соответствующего атом («d-блок»). В случае лантаноидов и актиноидов происходит заселение f-орбитали («f-блок»).
Рисунок: Занятие орбиты в периодической таблицеЭлементы основной группы можно дополнительно подразделить в соответствии с их физическими и химическими свойствами. Обычно это делается следующим образом:
- неметаллы
- щелочные металлы
- щелочноземельные металлы
- металлы
- металлоиды (иногда вводящие в заблуждение названия полуметаллы ) 05 9
Обратите внимание, что щелочные металлы и щелочноземельные металлы являются «металлами» в прямом смысле. Между группой щелочноземельные металлы и металлы переходной группы , которая не показана на этом рисунке. Причина использования слова «переход» теперь становится ясной, и поскольку все элементы переходной группы являются металлами, их также называют переходными металлами . Таким образом, около 80 % существующих элементов составляют металлы!
Между группой щелочноземельные металлы и металлы переходной группы , которая не показана на этом рисунке. Причина использования слова «переход» теперь становится ясной, и поскольку все элементы переходной группы являются металлами, их также называют переходными металлами . Таким образом, около 80 % существующих элементов составляют металлы!
Некоторые элементы имеют свойства как металлов, так и неметаллов. Их называют металлоиды . Однако четкого определения металлоида не существует! Металлоиды включают в себя:
- Boron (B)
- Силиконовый (SI)
- Германия (GE)
- ARSENIC (AS)
- Возбуждение (SB)
- Bismuth (BI)
- Selenium (Se)
- 5 теллур (Te)
- полоний (Po)
Количество внешних электронов атома (также называемых валентными электронами ) в значительной степени определяет химические свойства соответствующего элемента.
