|
Область применения графита, описание и свойства. Виды природного и искусственного графита – химическая структура, механические и физические характеристики. Графит (от др.-греч. γράφω — пишу) – это природный материал, относящийся к классу самородных элементов, аллотропная модификация углерода. Он имеет слоистую структуру. Каждый слой кристаллической решетки графита может по-разному располагаться по отношению друг к другу, образуя политипы. Графит находит свое применение в производственной и промышленной деятельности. Графитовые изделия отличаются повышенными эксплуатационными характеристиками. Графит устойчив к химическим и природным воздействиям, он достаточно прочный, хорошо проводит электрический ток, отличается низкой твердостью, относительной мягкостью, после воздействия высоких температур затвердевает. Плотность составляет 2.23 г/см3. Структура и состав графитаСтруктура имеет свои определенные особенности. Атомы углерода ковалентно связаны между собой. Модификаций природного минерала существует две:
Химический состав графита не отличается чистотой. В большом количестве (до 10-20%) присутствует зола, состоящая из разных составляющих (FeO, SiO2, Аl2O3, MgO, Р2О5, CuO, СаО и др. Цвет преобладает железно-черный, доходя до стально-серого. Имеет сильный металловидный блеск; скрытокристаллические агрегаты не блестят, матовые. Показатель преломления графита Nm==l,93-2,07. На ощупь жирный, оставляет след на бумаге и пальцах. Удельный вес графита 2,09-2,23 (меняется исходя от степени дисперсности и присутствия тончайших пор), у шунгита 1,84-1,98. Обладает высокой электропроводностью, что связано с очень плотным расположением атомов в листах. Графит не плавится, если накаливать в струе кислорода, то сгорает тяжелее в сравнении с алмазом. Улетучивается лишь в пламени вольтовой дуги, не плавясь. В кислотах не растворяется. В смеси с KNO3 порошок при нагревании дает вспышку. Графит в природеВ природе содержится в гранитах, пирите. Он образуется в магматических и вулканических горных породах, скарнах и пегматитах при высоких температурах, встречается в кварцевых жилах с различными материалами, широко распространен в мраморе, кристаллических сланцах, гнейсах. Показатели:
Виды природного графита:
Искусственный графит – область примененияИскусственно производится конструкционный, мелкозернистый, антифрикционный и литейный графит. Область применения материала достаточно широкая. Графит используется для изготовления огнеупорных материалов, электрических машин и установок, в химической, горнодобывающей промышленности, а также на производстве. Из него также изготавливают стержневые карандаши, краски, покрытия и аккумуляторные батареи. Графит незаменим в ядерной промышленности и в других узконаправленных областях. Заказать |
Новости и акции [ 25.01.2021 ] [ 24.12.2019 ] Поздравляем покупателей из РФ, СНГ с Новым годом!… >> [ 16.10.2017 ] Готовы поставить графит С-0 партией любого объема. Отгрузка в день оплаты…. >> Архив новостей |
Формула графита.
 Аллотропия углерода :: SYL.ru
Аллотропия углерода :: SYL.ruПростым карандашом с графитовым стержнем пользовался каждый из нас. Его след на бумаге – не что иное, как углерод. В нашей статье вы узнаете, какова формула графита, его физические и химические свойства.
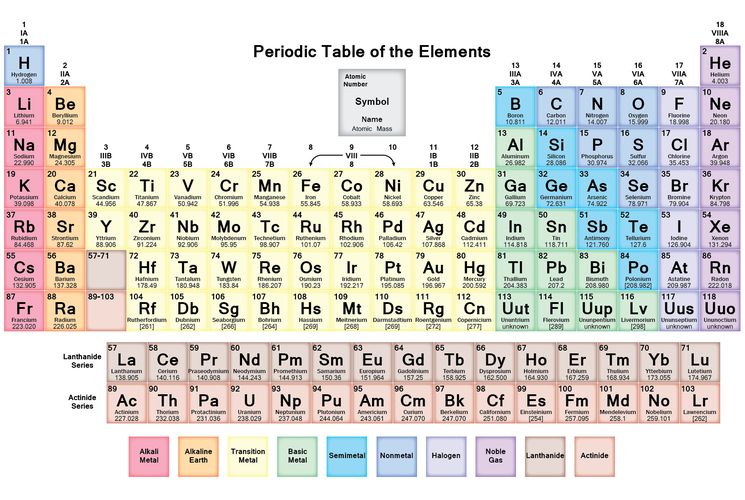
Положение углерода в периодической таблице
Углерод – элемент четвертой группы, второго периода периодической системы химических элементов Д. И. Менделеева. Он является органогенным. К данной группе также относятся кислород, азот и водород. Это значит, что они входят в состав всех живых организмов на планете, составляя их основу.
Такое положение определяет строение атома углерода. На его внешнем энергетическом уровне находится четыре электрона. Это значит, что данный химический элемент может проявлять как положительную, так и отрицательную степень окисления (+4 или – 4).
Понятие об аллотропии
Формула графита показывает, что в состав этого вещества входит только углерод в свободном виде. Хотя в природе он часто встречается и в виде соединений. Такими примерами являются углекислый и угарный газ, известняк, мел, мрамор.
Такими примерами являются углекислый и угарный газ, известняк, мел, мрамор.
Дело в том, что формула графита в химии такая же, как и у алмаза. Возможно ли это? Получается, что вещества с одинаковым составом имеют абсолютно разные свойства. Такое явление называется аллотропией. Она может быть обусловлена количеством атомов в молекуле вещества или их пространственным расположением. Примером первого случая является кислород. Если в молекуле два атома этого химического элемента, образуется кислород, а если три – озон.
Формула графита в химии
Аллотропия углерода является пространственной. Обратите внимание на рисунок ниже. Первый из них – это формула графита. Атомы углерода формируют слои, расположенные друг от друга на значительном расстоянии. Поэтому связи между ними не прочные. Каждый раз, проводя графитовым стержнем по бумаге, мы оставляем на нем слой углерода.
В кристаллической решетке алмаза (ее демонстрирует рисунок справа) расстояние между атомами в узлах одинаково во всех направлениях. Такое строение обеспечивает и прочность связей. Алмаз является самым твердым веществом. Считается, что его нельзя разбить.
Такое строение обеспечивает и прочность связей. Алмаз является самым твердым веществом. Считается, что его нельзя разбить.
Графит: формула, химическая и физическая характеристика
Как мы уже сказали, графит – это углерод. Соответственно, в химии записывается он как С. Несмотря на то что формула алмаза и графита сходна по качественному составу, эти вещества имеют значительные отличия в свойствах. Это объясняется разным пространственным расположением атомов углерода в их молекулах.
Графит – это мягкое вещество серого цвета с металлическим блеском. Оно без усилий расслаивается на мелкие пластинки и проводит электрический ток. Ученые доказали, что если графит нагреть до 1 600 градусов по шкале Цельсия под давлением 104 МПа при наличии катализаторов, то он превратится в алмаз. Таким способом в промышленности получают искусственные драгоценности.
Графит не является химически активным веществом. Он реагирует только с некоторыми солями и щелочными металлами. Продуктами таких реакций являются подобия включений. Сгорание графита в кислороде происходит только при очень высокой температуре с образованием углекислого газа. Однако он вступает в реакцию фторирования. При этом образуется порошок белого цвета, структура которого изменяется на зигзагообразную, приобретая лучшие смазочные свойства по сравнению с обычным графитом.
Сгорание графита в кислороде происходит только при очень высокой температуре с образованием углекислого газа. Однако он вступает в реакцию фторирования. При этом образуется порошок белого цвета, структура которого изменяется на зигзагообразную, приобретая лучшие смазочные свойства по сравнению с обычным графитом.
Отличия модификаций углерода
А вот алмаз является твердым прозрачным и бесцветным веществом, которое не проводит электрический ток. Хотя иногда в природе встречаются розовые, желтоватые, синие или зеленые минералы. Формула алмаза и графита в химии одинаково представлена углеродом – С. Однако благодаря своей кубической кристаллической системе это вещество является одновременно твердым и хрупким. Обработанные алмазы называют бриллиантами. Удивительным является еще и тот факт, что в природе невозможно найти двух одинаковых камней. Наверное, поэтому в переводе с греческого языка название этого вещества означает “непревзойденный”.
Аллотропия углерода
Структурная формула графита может искусственно видоизменяться. Благодаря этому был получен целый ряд аллотропных модификаций углерода. Это карбин, графен и фуллерены.
Благодаря этому был получен целый ряд аллотропных модификаций углерода. Это карбин, графен и фуллерены.
Первое вещество имеет линейную структуру из атомов углерода. Они могут быть соединены либо двойными, либо чередующимися тройными и одинарными связями. Карбин представляет собой черный порошок с мелкокристаллической структурой. Его уникальным свойством является абсолютная совместимость с тканями организма человека. Благодаря этому карбин используют для изготовления искусственных кровеносных сосудов.
Графен – это однослойное вещество, также состоящее из углерода. Такое строение делает его самым прочным и тонким. Графен применяется в различных областях нанотехнологии: точное приборостроение, искусственные мембраны, сенсорные устройства.
Из атомов углерода состоит еще одна аллотропная модификация углерода – фуллерены. Их молекулы имеют сферическую или эллипсовидную форму с полостью внутри. Фуллерены получают из паров графита при их дальнейшей лазерной обработке. Его используют в качестве полупроводника, фоторезиста, элемента аккумуляторов и электрических батарей, катализатора роста алмазной пленки.
Итак, в нашей статье мы рассмотрели особенности строения графита. Это вещество состоит из атомов углерода. Они образуют отдельные слои, связи между которыми не очень сильные. Поэтому графит является мягким, легко отслаивается в горизонтальном направлении, имеет серый цвет с металлическим блеском и хорошо проводит электрический ток.
Что такое графит? Химическая формула графита и периодическая таблица графита
Графит — неметаллический материал, аллотроп углерода, химическая формула С; С высокой термостойкостью, высокопрочный проводящий материал; Подходит для изготовления огнеупорных материалов, графитовых электродов, огнеупорных кирпичей и изделий из графита.
Что такое графит?
Графит серо-черный, непрозрачный твердый, стабильные химические свойства, коррозионная стойкость, кислота, щелочь и другие вещества не легко реагируют. Горение в кислороде для получения двуокиси углерода, может быть концентрированной азотной кислотой, перманганатом калия и другими сильными окислителями.
Атомы углерода графита имеют гексагональную слоистую структуру, которая не образует «пространственной сети». Графит имеет слоистую структуру. Если вы посмотрите на нее в одном слое, связь С-С образует правильную шестиугольную вытянутую форму, а если вы посмотрите на нее в целом, это будет послойная структура. Таким образом, монослой чрезвычайно твердый, а промежуточный слой чрезвычайно мягкий. Каждый слой состоит из бесчисленных маленьких шестиугольных ячеек. Но прочных связей между соседними слоями нет, поэтому в качестве смазки можно использовать графит.
Графическая схема молекулярной структуры
Химическая формула графита
Химическая формула графита C. Молекулярная масса: 12,01. Нанотрубки, алмаз и графит являются аллотропами углерода, и химическая формула может быть выражена буквой «С».
Свойства графита:
1) высокая термостойкость: температура плавления графита составляет 3850 ± 50 ℃, температура кипения составляет 4250 ℃, горение дуги при сверхвысокой температуре, небольшая потеря веса, небольшой коэффициент теплового расширения.
2) Электро- и теплопроводность: электропроводность графита в сто раз выше, чем у обычных неметаллических руд. Теплопроводность превосходит сталь, железо, свинец и другие металлические материалы. Теплопроводность уменьшается с повышением температуры, и даже при экстремально высоких температурах графит становится изолирующим телом.
4) химическая стабильность: графит обладает хорошей химической стабильностью при комнатной температуре, кислотостойкостью, щелочестойкостью и коррозионной стойкостью к органическим растворителям.
5) Пластичность: графит обладает хорошей ударной вязкостью и может превращаться в очень тонкие листы.
6) Стойкость к тепловому удару: графит выдерживает резкие перепады температуры без повреждений при использовании при комнатной температуре.
Периодическая таблица графита
Графит – Minerals Education Coalition
Чистый графит представляет собой минеральную форму элемента углерода (элемент № 6, символ C). Образуется в виде прожилков и вкраплений в метаморфических породах в результате метаморфизма органического материала, включенного в известняковые отложения. Это чрезвычайно мягкий минерал, который распадается на мельчайшие гибкие чешуйки, которые легко скользят друг по другу. Эта особенность объясняет характерное жирное ощущение графита. Эта жирная характеристика делает графит хорошей смазкой. Поскольку это твердый материал, он известен как сухая смазка. Это полезно в тех случаях, когда нельзя использовать «влажные» смазочные материалы, такие как масло. Графит — единственный неметаллический элемент, хорошо проводящий электричество. Природный графит в основном используется в так называемых огнеупорных изделиях. Применение огнеупоров связано с чрезвычайно высокой температурой и, следовательно, требует материалов, которые не будут плавиться или разрушаться в таких экстремальных условиях. Одним из примеров такого использования являются тигли, используемые в сталелитейной промышленности. Такие огнеупорные применения составляют большую часть использования графита.
Применение огнеупоров связано с чрезвычайно высокой температурой и, следовательно, требует материалов, которые не будут плавиться или разрушаться в таких экстремальных условиях. Одним из примеров такого использования являются тигли, используемые в сталелитейной промышленности. Такие огнеупорные применения составляют большую часть использования графита.
Он также используется для изготовления тормозных колодок, смазочных материалов и форм в литейных цехах. Множество других промышленных применений составляют оставшийся графит, потребляемый каждый год.
Тип
Минерал
Классификация минералов
Native
Химическая формула
C
Стрик
Черный
Мохс. темно-синий в проходящем свете
Блеск
Металлик
Излом
Шелушение
Описание
Чистый графит представляет собой минеральную форму элемента углерода (элемент № 6, символ C).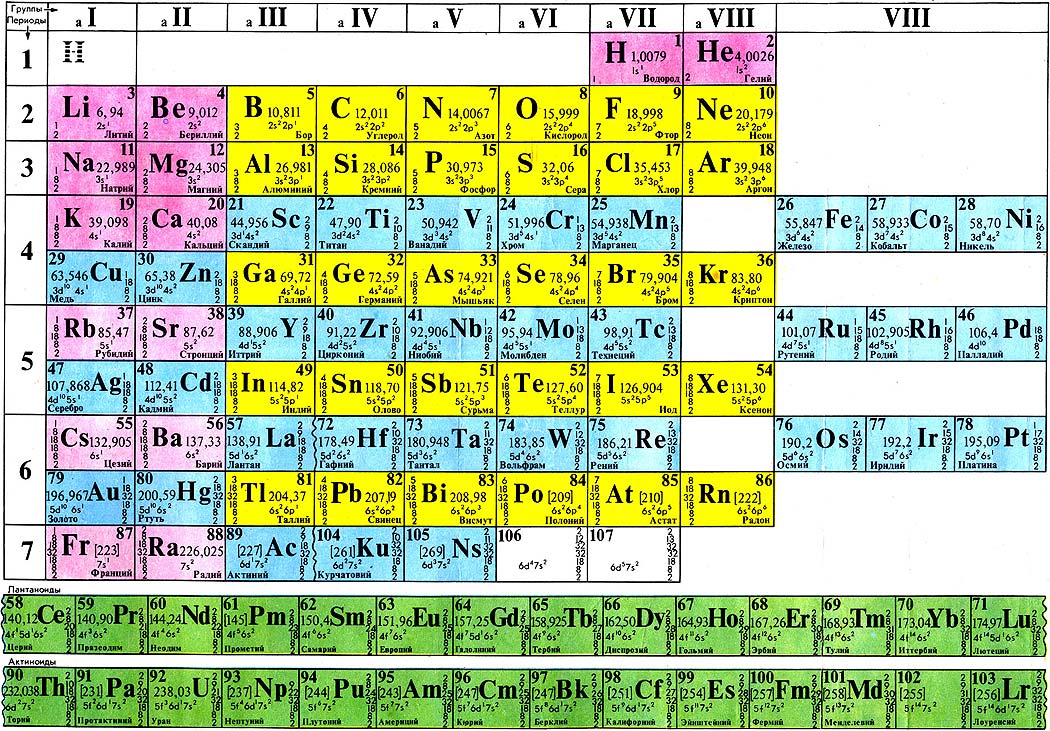 Образуется в виде прожилков и вкраплений в метаморфических породах в результате метаморфизма органического материала, включенного в известняковые отложения. Это чрезвычайно мягкий минерал, который распадается на мельчайшие гибкие чешуйки, которые легко скользят друг по другу. Эта особенность объясняет характерное жирное ощущение графита. Эта жирная характеристика делает графит хорошей смазкой. Поскольку это твердый материал, он известен как сухая смазка. Это полезно в тех случаях, когда нельзя использовать «влажные» смазочные материалы, такие как масло. Графит — единственный неметаллический элемент, хорошо проводящий электричество. Природный графит в основном используется в так называемых огнеупорных изделиях. Применение огнеупоров связано с чрезвычайно высокой температурой и, следовательно, требует материалов, которые не будут плавиться или разрушаться в таких экстремальных условиях. Одним из примеров такого использования являются тигли, используемые в сталелитейной промышленности.
Образуется в виде прожилков и вкраплений в метаморфических породах в результате метаморфизма органического материала, включенного в известняковые отложения. Это чрезвычайно мягкий минерал, который распадается на мельчайшие гибкие чешуйки, которые легко скользят друг по другу. Эта особенность объясняет характерное жирное ощущение графита. Эта жирная характеристика делает графит хорошей смазкой. Поскольку это твердый материал, он известен как сухая смазка. Это полезно в тех случаях, когда нельзя использовать «влажные» смазочные материалы, такие как масло. Графит — единственный неметаллический элемент, хорошо проводящий электричество. Природный графит в основном используется в так называемых огнеупорных изделиях. Применение огнеупоров связано с чрезвычайно высокой температурой и, следовательно, требует материалов, которые не будут плавиться или разрушаться в таких экстремальных условиях. Одним из примеров такого использования являются тигли, используемые в сталелитейной промышленности. Такие огнеупорные применения составляют большую часть использования графита.
Такие огнеупорные применения составляют большую часть использования графита.
Он также используется для изготовления тормозных колодок, смазочных материалов и форм в литейных цехах. Множество других промышленных применений составляют оставшийся графит, потребляемый каждый год.
Отношение к горнодобывающей промышленности
IMAR 7 th Edition
С 1890 по 1920 год подземная добыча графита практиковалась в Нью-Йорке и Пенсильвании. С 1942 г. и до конца Второй мировой войны применялись только открытые методы добычи, поскольку добыча выветрелых пород была относительно легкой. Графит добывали под землей в Диллоне, штат Монтана, во время Второй мировой войны, но вскоре после этого добыча прекратилась, потому что он был слишком дорогим, чтобы конкурировать с графитом Шри-Ланки.
Разработка на Мадагаскаре полностью ведется открытым способом, но в Баварии, Корее, Мексике и Шри-Ланке из-за глубины и физических характеристик месторождений практикуется подземная добыча. Мексиканские подземные горные работы ведутся на глубине 100–400 м от поверхности, измеренной по углу жилы. Некоторые из старых рудников в Шри-Ланке достигали глубины более 450 м по вертикали. В течение многих лет добыча полезных ископаемых на Шри-Ланке была примитивной, а добыча руды была медленной и трудоемкой. Шахты были механизированы после Второй мировой войны.
Мексиканские подземные горные работы ведутся на глубине 100–400 м от поверхности, измеренной по углу жилы. Некоторые из старых рудников в Шри-Ланке достигали глубины более 450 м по вертикали. В течение многих лет добыча полезных ископаемых на Шри-Ланке была примитивной, а добыча руды была медленной и трудоемкой. Шахты были механизированы после Второй мировой войны.
Мадагаскарские операции также были примитивными, поскольку низкая стоимость рабочей силы не позволяла механизировать. После 1938 года на рудниках стали использовать механическое оборудование для удаления вскрышных пород, а бульдозеры и тракторы легко удаляли графитосодержащие сланцы.
Мировой спрос на графит неуклонно рос в течение 2012 и 2013 годов. Это увеличение стало результатом улучшения мировых экономических условий и их влияния на отрасли, использующие графит.
Основными источниками импорта природного графита были, в порядке убывания тоннажа, Китай, Мексика, Канада, Бразилия и Мадагаскар, на долю которых в совокупности приходилось 97% тоннажа и 90% стоимости всего импорта. Мексика и Вьетнам предоставили весь аморфный графит, а Шри-Ланка предоставила весь ассортимент кусковой и крошащейся пыли. Китай, Канада и Мадагаскар были, в порядке убывания тоннажа, основными поставщиками кристаллического чешуйчатого графита и пылевидного графита.
Мексика и Вьетнам предоставили весь аморфный графит, а Шри-Ланка предоставила весь ассортимент кусковой и крошащейся пыли. Китай, Канада и Мадагаскар были, в порядке убывания тоннажа, основными поставщиками кристаллического чешуйчатого графита и пылевидного графита.
В 2013 году Китай произвел большую часть мирового графита. Производство графита увеличилось в Китае, на Мадагаскаре и Шри-Ланке по сравнению с 2012 годом, в то время как производство сократилось в Бразилии по сравнению с уровнем производства 2012 года.
Применение
Поскольку чешуйки графита скользят друг по другу, придавая им жирный вид, графит уже давно используется в качестве смазки в тех случаях, когда нельзя использовать «влажные» смазки, такие как масло. Технологические изменения снижают потребность в этом приложении.
Природный графит используется в основном в так называемых огнеупорных применениях. Применение огнеупоров связано с чрезвычайно высокой температурой и, следовательно, требует материалов, которые не будут плавиться или разрушаться в таких экстремальных условиях.

 Графит имеет металлический блеск и темно-серый цвет. Теплопроводность этого минерала достаточно большая, поэтому его используют для изготовления комплектующих деталей электрооборудования.
Графит имеет металлический блеск и темно-серый цвет. Теплопроводность этого минерала достаточно большая, поэтому его используют для изготовления комплектующих деталей электрооборудования. ), газы (до 2%) и битумы, иногда вода.
), газы (до 2%) и битумы, иногда вода.