Часть 1. Химическая термодинамика
Министерство образования и науки Российской Федерации
Ростовский государственный университет
Сергей Иванович ЛЕВЧЕНКОВ
ФИЗИЧЕСКАЯ И КОЛЛОИДНАЯ ХИМИЯ
Конспект лекций для студентов 3-го курса вечернего отделения
биолого-почвенного факультета РГУ
Часть 1. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
г. Ростов-на-Дону
2004 г.
|
|
| 2 |
|
| ОГЛАВЛЕНИЕ |
|
ВВЕДЕНИЕ | 3 | ||
1 ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА | 4 | ||
1.1 ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ | 4 | ||
1.2 ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ | 6 | ||
1.3 | ПРИЛОЖЕНИЯ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ | 9 | |
1. | 8 | ||
1.3.2 | Зависимость теплового эффекта химической реакции от температуры | 12 | |
1.4 | ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ЭНТРОПИЯ | 13 | |
1.4.1 | Статистическая интерпретация энтропии | 19 | |
1.5 | ТРЕТЬЕ НАЧАЛО ТЕРМОДИНАМИКИ | 19 | |
1.5.1 | Расчет абсолютной энтропии | 20 | |
1.6 | ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ | 21 | |
1.7 | ХИМИЧЕСКОЕ РАВНОВЕСИЕ | 24 | |
1.7.1 | Влияние внешних условий на химическое равновесие | 30 | |
1. | Влияние давления и концентрации | 30 | |
1.7.3 | Влияние температуры на положение равновесия | 31 | |
1.8 | ФАЗОВЫЕ РАВНОВЕСИЯ | 33 | |
Опубликовано по решению кафедры физической и коллоидной химии
Ростовского государственного университета.
Copyright © С. И. Левченков, 1996-2004
3
В В Е Д Е Н И Е
Предметом физической химии является объяснение химических явлений на основе более общих законов физики. Физическая химия рассматривает две
основные группы вопросов:
1.Изучение строения и свойств вещества и составляющих его частиц;
2.Изучение процессов взаимодействия веществ.
В курсе физической химии обычно выделяют несколько разделов.
Строение вещества. В этот раздел входят учение о строении атомов и молекул и учение об агрегатных состояниях вещества. Изучение строение вещества
необходимо для выяснения важнейших вопросов об образовании молекул из атомов, о природе химической связи, о строении и взаимодействии молекул. Именно
Именно
в этой своей части физическая химия очень тесно переплетается со всеми направлениями современной химии, поскольку изучение химических свойств
вещества вне связи со строением атомов и молекул на современном уровне невозможно.
Химическая термодинамика изучает энергетические эффекты химических процессов; позволяет определить возможность, направление и глубину протекания химического процесса в конкретных условиях.
Химическая кинетика. В этом разделе физической химии изучается скорость и механизм протекания химических процессов в различных средах при различных
условиях.
Учение о растворах рассматривает процессы образования растворов, их внутреннюю структуру и важнейшие свойства, зависимость структуры и свойств от
природы компонентов раствора.
Электрохимия изучает особенности свойств растворов электролитов,
явления электропроводности, электролиза, коррозии, работу гальванических элементов.
Коллоидная химия изучает поверхностные явления и свойства
мелкодисперсных гетерогенных систем.
Все разделы физической химии объединяет единая основа – общие законы
природы, которые применимы к любым процессам и любым системам, независимо
от их строения.
4
1 ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
Термодинамика – наука о взаимопревращениях различных форм энергии и законах этих превращений. Термодинамика базируется только на экспериментально
обнаруженных объективных закономерностях, выраженных в двух основных началах термодинамики.
Термодинамика изучает:
1.Переходы энергии из одной формы в другую, от одной части системы к другой;
2.Энергетические эффекты, сопровождающие различные физические и химические процессы и зависимость их от условий протекания данных процессов;
3.Возможность, направление и пределы самопроизвольного протекания процессов в рассматриваемых условиях.
Необходимо отметить, что классическая термодинамика имеет следующие
ограничения:
1.Термодинамика не рассматривает внутреннее строение тел и механизм протекающих в них процессов;
2. Классическая термодинамика изучает только макроскопические системы;
Классическая термодинамика изучает только макроскопические системы;
3.В термодинамике отсутствует понятие “время”.
1.1 ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ
Термодинамическая система – тело или группа тел, находящихся во взаимодействии, мысленно или реально обособленные от окружающей среды.
Гомогенная система – система, внутри которой нет поверхностей, разделяющих отличающиеся по свойствам части системы (фазы).
Гетерогенная система – система, внутри которой присутствуют поверхности, разделяющие отличающиеся по свойствам части системы.
Фаза – совокупность гомогенных частей гетерогенной системы, одинаковых по физическим и химическим свойствам, отделённая от других частей системы видимыми поверхностями раздела.
Изолированная система – система, которая не обменивается с окружающей средой ни веществом, ни энергией.
Закрытая система – система, которая обменивается с окружающей средой энергией, но не обменивается веществом.
Открытая система – система, которая обменивается с окружающей средой и веществом, и энергией.
5
Совокупность всех физических и химических свойств системы характеризует её термодинамическое состояние. Все величины, характеризующие какое-либо макроскопическое свойство рассматриваемой системы – параметры состояния.
Опытным путем установлено, что для однозначной характеристики данной системы необходимо использовать некоторое число параметров, называемых независимыми;
все остальные параметры рассматриваются как функции независимых параметров. В качестве независимых параметров состояния обычно выбирают параметры, поддающиеся непосредственному измерению, например температуру, давление,
концентрацию и т.д. Всякое изменение термодинамического состояния системы (изменения хотя бы одного параметра состояния) есть термодинамический процесс.
Обратимый процесс – процесс, допускающий возможность возвращения системы в исходное состояние без того, чтобы в окружающей среде остались какие-
либо изменения.
Равновесный процесс – процесс, при котором система проходит через
непрерывный ряд равновесных состояний.
Энергия – мера способности системы совершать работу; общая качественная
мера движения и взаимодействия материи. Энергия является неотъемлемым
свойством материи. Различают потенциальную энергию, обусловленную положением тела в поле некоторых сил, и кинетическую энергию, обусловленную изменением положения тела в пространстве.
Внутренняя энергия системы – сумма кинетической и потенциальной энергии
всех частиц, составляющих систему. Можно также определить внутреннюю энергию
системы как её полную энергию за вычетом кинетической и потенциальной энергии системы как целого.
Формы перехода энергии от одной системы к другой могут быть разбиты на
две группы. В первую группу входит только одна форма перехода движения путем
хаотических столкновений молекул двух соприкасающихся тел, т.е. путём
теплопроводности (и одновременно путём излучения). Мерой передаваемого таким способом движения является теплота. Теплота есть форма передачи энергии
путём неупорядоченного движения молекул. Во вторую группу включаются различные формы перехода движения, общей чертой которых является перемещение масс, охватывающих очень большие числа молекул (т.е. макроскопических масс), под действием каких-либо сил. Таковы поднятие тел в поле
Во вторую группу включаются различные формы перехода движения, общей чертой которых является перемещение масс, охватывающих очень большие числа молекул (т.е. макроскопических масс), под действием каких-либо сил. Таковы поднятие тел в поле
тяготения, переход некоторого количества электричества от большего
6
электростатического потенциала к меньшему, расширение газа, находящегося под давлением и др. Общей мерой передаваемого такими способами движения является
работа – форма передачи энергии путём упорядоченного движения частиц.
Теплота и работа характеризуют качественно и количественно две различные формы передачи движения от данной части материального мира к другой. Теплота и
работа не могут содержаться в теле. Теплота и работа возникают только тогда, когда возникает процесс, и характеризуют только процесс. В статических условиях теплота и работа не существуют. Различие между теплотой и работой, принимаемое
термодинамикой как исходное положение, и противопоставление теплоты работе имеет смысл только для тел, состоящих из множества молекул, т. к. для одной
к. для одной
молекулы или для совокупности немногих молекул понятия теплоты и работы теряют смысл. Поэтому термодинамика рассматривает лишь тела, состоящие из большого числа молекул, т.е. так называемые макроскопические системы.
1.2 ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Первое начало термодинамики представляет собой закон сохранения энергии, один из всеобщих законов природы (наряду с законами сохранения импульса,
заряда и симметрии):
Энергия неуничтожаема и несотворяема; она может только переходить из одной формы в другую в эквивалентных соотношениях.
Первое начало термодинамики представляет собой постулат – оно не может
быть доказано логическим путем или выведено из каких-либо более общих положений. Истинность этого постулата подтверждается тем, что ни одно из его следствий не находится в противоречии с опытом. Приведем еще некоторые формулировки первого начала термодинамики:
Полная энергия изолированной системы постоянна;
Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Первое начало термодинамики устанавливает соотношение между теплотой
Q, работой А и изменением внутренней энергии системы ∆U:
Изменение внутренней энергии системы равно количеству сообщенной
системе теплоты минус количество работы, совершенной системой против внешних сил.
7
∆U = Q – А | (I.1) |
dU = δQ – δА | (I.2) |
Уравнение (I.1) является математической записью 1-го начала термодинамики
для конечного, уравнение (I.2) – для бесконечно малого изменения состояния
системы.
Внутренняя энергия является функцией состояния; это означает, что
изменение внутренней энергии ∆U не зависит от пути перехода системы из состояния 1 в состояние 2 и равно разности величин внутренней энергии U2 и U1 в этих состояниях:
∆U = U2 – U1 | (I.3) |
Следует отметить, что определить абсолютное значение внутренней энергии
системы невозможно; термодинамику интересует лишь изменение внутренней
энергии в ходе какого-либо процесса.
Рассмотрим приложение первого начала термодинамики для определения
работы, совершаемой системой при различных термодинамических процессах (мы будем рассматривать простейший случай – работу расширения идеального газа).
Изохорный процесс (V = const; ∆V = 0).
Поскольку работа расширения равна произведению давления и изменения
объема, для изохорного процесса получаем: |
|
∆U = Q – А | (I.1) |
А = Р∆V = 0 | (I.4) |
∆U = QV | (I.5) |
Изотермический процесс (Т = const ).
Из уравнения состояния одного моля идеального газа получаем:
Р = | RT | (I.6) | ||
| V |
| ||
Отсюда: |
|
|
| |
δА = PdV = RT | dV | (I. | ||
V | ||||
|
|
| ||
Проинтегрировав выражение (I.6) от V1 до V2, получим
8
V2 |
| =RT ln V2 | =RT ln P1 |
|
A = ∫RT dV | (I.8) | |||
V1 | V | V1 | P2 |
|
Изобарный процесс (Р = const). |
|
| ||
V2 |
|
|
|
|
A = ∫PdV = | Р∆V = R(T2 – T1) | (I.9) | ||
V1 |
|
|
|
|
Подставляя полученные выражения для работы различных процессов в уравнение (I. 1), для тепловых эффектов этих процессов получим:
1), для тепловых эффектов этих процессов получим:
QV = ∆U |
| (I.10) | |
| V1 | P2 |
|
QT = A =RT ln |
| =RT ln P1 | (I.11) |
V2 | |||
QP = ∆U + P∆V |
| (I.12) | |
В уравнении (I.12) сгруппируем переменные с одинаковыми индексами. Получаем:
QP = U2 – U1 + P(V2 – V1) = (U2 + PV2) – (U1 + PV1) | (I.13) |
Введем новую функцию состояния системы – энтальпию H, тождественно равную сумме внутренней энергии и произведения давления на объем: H ≡ U + PV. Тогда выражение (I.13) преобразуется к следующему виду:
QP = Н2 – Н1 = ∆Н | (I. |
Т.о., тепловой эффект изобарного процесса равен изменению энтальпии системы.
Адиабатический процесс (Q = 0).
При адиабатическом процессе работа расширения совершается за счёт
уменьшения внутренней энергии газа:
2 | T1 |
|
A = – ∫dU = ∫CVdT | (I.15) | |
1T2
Вслучае если CV не зависит от температуры (что справедливо для многих
реальных газов), работа, произведённая газом при его адиабатическом расширении, прямо пропорциональна разности температур:
A = – CV ∆T | (I.16) |
9
1.3ПРИЛОЖЕНИЯ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ
КХИМИЧЕСКИМ ПРОЦЕССАМ
1.3.1Закон Гесса
Как известно, большинство химических реакций сопровождаются выделением
(экзотермические реакции) либо поглощением (эндотермические реакции)
теплоты. Первое начало термодинамики дает возможность рассчитать тепловой
Первое начало термодинамики дает возможность рассчитать тепловой
эффект химической реакции при различных условиях её проведения.
Тепловой эффект (теплота) химической реакции – количество теплоты,
выделившейся либо поглотившейся в ходе реакции. Тепловой эффект относят, как
правило, к числу молей прореагировавшего исходного вещества, стехиометрический коэффициент перед которым максимален.
Например, реакцию окисления водорода в химической термодинамике
записывают в виде:
Н2 + 1/2 О2 = Н2О
и тепловой эффект рассчитывают на 1 моль водорода.
Тепловые эффекты, сопровождающие протекание химических реакций, являются предметом одного из разделов химической термодинамики – термохимии. Определим некоторые понятия термохимии.
Теплота образования вещества – тепловой эффект реакции образования 1
моля сложного вещества из простых. Теплоты образования простых веществ
принимаются равными нулю.
Теплота сгорания вещества – тепловой эффект реакции окисления 1 моля
вещества в избытке кислорода до высших устойчивых оксидов.
Теплота растворения – тепловой эффект процесса растворения 1 моля вещества в бесконечно большом количестве растворителя. Теплота растворения складывается из двух составляющих: теплоты разрушения кристаллической решетки
(для твердого вещества) и теплоты сольватации:
∆Нраств = ∆Нкр.реш.+ ∆Нсольв
Поскольку ∆Нкр.реш всегда положительно (на разрушение кристаллической
решетки необходимо затратить энергию), а ∆Нсольв всегда отрицательно, знак ∆Нраств
определяется соотношением абсолютных величин ∆Нкр.реш. и ∆Нсольв:
∆Нраств = ∆Нкр.реш. – ∆Нсольв
10
Основным законом термохимии является закон Гесса, являющийся частным
случаем первого начала термодинамики:
Тепловой эффект химической реакции, проводимой в изобарноизотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не
зависит от пути её протекания.
Выше было показано, что изменение энтальпии ∆Н (тепловой эффект изобарного процесса Qp) и изменение внутренней энергии ∆U (тепловой эффект
изохорного процесса Qv) не зависят от пути, по которому система переходит из
начального состояния в конечное.
Рассмотрим некоторый обобщенный химический процесс превращения
исходных веществ А1, А2, А3… в продукты реакции В1, В2, В3…, который может быть
осуществлен различными путями в одну или несколько стадий:
|
| ∆H5 |
|
|
|
|
∆h5 |
| ∆H6 |
|
| ||
A1,A2,A3… |
| ∆h2 |
| B | ,B ,B … | |
|
|
| ||||
|
|
| 1 | 2 | 3 | |
∆h3 ∆h4
Согласно закону Гесса, тепловые эффекты всех этих реакций связаны
следующим соотношением:
∆Н1 = ∆Н2 + ∆Н3 = ∆Н4 + ∆Н5 + ∆Н6 | (I. |
Практическое значение закона Гесса состоит в том, что он позволяет
рассчитывать тепловые эффекты химических процессов. В термохимических
расчетах обычно используют ряд следствий из закона Гесса:
1.Тепловой эффект прямой реакции равен по величине и противоположен по знаку тепловому эффекту обратной реакции (закон Лавуазье-Лапласа).
2.Для двух реакций, имеющих одинаковые исходные, но разные конечные состояния, разность тепловых эффектов представляет собой тепловой эффект
перехода из одного конечного состояния в другое.
Основы химической термодинамики – презентация онлайн
1. ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ
Лекция 1Основы химической термодинамики
• Основные понятия химической термодинамики.
• Функции состояния системы.
• Первый закон термодинамики.
Лектор: Степанова Ирина Петровна
доктор биологических наук,
профессор, зав. кафедрой химии
ЦЕЛИ ЛЕКЦИИ
ОБУЧАЮЩАЯ: сформировать знания об основах
химической термодинамики, первом законе
термодинамики и законе Гесса.

РАЗВИВАЮЩАЯ: расширить кругозор
обучающихся на основе интеграции знаний, развить
логическое мышление.
ВОСПИТАТЕЛЬНАЯ: содействовать формированию
у обучающихся устойчивого интереса к изучению
дисциплины.
3. Основные понятия химической термодинамики
Термодинамика – это наука,изучающая взаимные
превращения различных видов
энергии, связанные с
переходом энергии в форме
теплоты и работы.
Медико-биологическое значение темы
Медико-биологическое значение темы
Термодинамика теоретическая основа при
осуществлении химического и
биологического синтеза при
изготовлении лекарственных
препаратов.
6. Медико-биологическое значение темы
Термодинамический метод исследования являетсяодним из наиболее надежных способов изучения
обмена веществ и энергии в живых организмах.
Превращения энергии,
происходящие в живых
организмах, являются
предметом
биоэнергетики.
Основные понятия и термины
Термодинамическая система (ТД
система) – это любой объект природы,
состоящий из достаточно большого числа
структурных единиц, в частности
молекул, отделенных от других объектов
природы реальной или воображаемой
границей раздела.

8. Основные понятия химической термодинамики
Часть объектов природы, не входящих всистему, называется средой.
Важными характеристиками системы являются
масса вещества (m) и энергия (Е или U).
Классификация систем по характеру
взаимодействия с окружающей средой
↔
энергия
масса
Открытая
система
(живой организм)
↔ энергия
Закрытая
система
(запаянная
ампула с
лекарством)
Изолированная
система
(термос)
10. Основные понятия химической термодинамики
Фаза – это часть системы содинаковыми физическими
и химическими свойствами,
отделенная от других частей
границей
раздела,
при
переходе через которую
свойства резко меняются.
11. Основные понятия химической термодинамики
В зависимости от фазового состоянияразличают:
1. Гомогенные системы. Это системы, в которых
все компоненты находятся в одной фазе, и в них
отсутствуют границы раздела.
 Пример: растворы
Пример: растворыглюкозы, солей, кислот.
2. Гетерогенные системы. Они состоят из
нескольких фаз, отделенных границей раздела.
Пример: эритроциты – плазма крови, живой
организм.
12. Основные понятия химической термодинамики
Термодинамическое состояние системы совокупность всех физических и химических свойствсистемы. Качественно характеризуется числом фаз и
химическим составом, количественно термодинамическими параметрами.
Для термодинамики особое значение имеет
равновесное состояние системы – постоянство всех
свойств в любой точке системы и отсутствие потоков
массы и энергии в системе.
13. Основные понятия химической термодинамики
Термодинамические параметры – это совокупность
физических величин, определяющих состояние
системы: температура (t), давление (р), объем (V).
концентрация (с).
• Функциональная зависимость термодинамических
параметров выражается уравнением состояния.
• Для газообразных систем эти параметры связаны
между собой уравнением Менделеева – Клапейрона:
p·V= n(х)·R·Т,
n(x) =m(x)/M(x) [моль]
R= 8,3 14 Дж · моль-1·К-1
m(х)
p·V=
·R·T
M(х)
14.
 Основные понятия химической термодинамикиТермодинамические параметры
Основные понятия химической термодинамикиТермодинамические параметрыназываются стандартными, если они
определяются при стандартных условиях.
К стандартным условиям относят:
t=250С или
Т= (t0С +273) = 298 К
р= 101,3 кПа = 1 атм
С(х) = 1 моль · дм-3
15. Основные понятия химической термодинамики
Термодинамический процесс – переход системы изодного равновесного состояния в другое,
сопровождающийся изменением хотя бы одного
термодинамического параметра.
16. Основные понятия химической термодинамики
В зависимости от того, какой из параметровсостояния при протекании термодинамического
процесса остается постоянным, различают
следующие термодинамические процессы:
изотермический (Т = const),
изобарный (р = const),
изохорный (V = const),
адиабатический (Q= const).
17. Функции состояния системы
В термодинамике дляопределения изменения энергии
системы пользуются различными
энергетическими
характеристиками, которые
называются термодинамическими
функциями состояния системы.

18. Функции состояния системы
К термодинамическим функциям системы относятся:1. Внутренняя энергия (U).
2. Энтальпия (Н).
3. Энтропия (S).
4. Энергия Гельмгольца (F).
5. Энергия Гиббса (свободная энергия) (G).
6. Химический потенциал (μ).
19. Функции состояния системы
1. Внутренняя энергия (U)Внутренняя энергия системы складывается
из кинетической энергии движения молекул
или атомов, образующих систему,
потенциальной энергии их взаимодействия
и внутримолекулярной энергии.
Внутренняя энергия (U):
Абсолютное значение внутренней энергии измерить
невозможно, поэтому измеряют ее приращение:
Uсистемы = Uкон – Uнач
Бесконечно малое изменение U является полным
дифференциалом dU.
20
Знак U:
(+) значения: система получила энергию;
(-) значения: система потеряла энергию.
h3 (г), O2 (г)
Внутренняя энергия U
2h3(г) + O2(г) 2h3O(г)
2h3O(г)
U< 0
2h3(г) + O2(г)
ΔU>0
h3O (г)
21
Знак U:
(+) значения: система получила энергию;
(-) значения: система потеряла энергию.

h3 (г), O2 (г)
Внутренняя энергия U
2h3(г) + O2(г) 2h3O(г)
+ энергия
(выделяется)
U< 0
2h3O(г)
ΔU>0
2h3(г) + O2(г)
– энергия (поглощается)
h3O (г)
22
23. Функции состояния системы
Внутренняя энергия есть функция состояниясистемы, приращение которой (ΔU) равно
теплоте, поступающей в систему при
изохорном процессе (ΔV=const).
ΔU=Q V , где Q V – теплота изохорного
процесса.
ΔU – кДж/моль или кДж· моль-1
Единицы измерения энергии:
Джоуль = Дж
Так как Дж очень маленькая величина,
обычно используют кДж.
калория = кал 1 кал = 4.184 Дж
1 кал
4.184 Дж
Коэффициент пересчета!
24
Функции состояния системы
Калория – это количество
теплоты, необходимое для
нагревания 1 г воды на 1oC
(от 14.5 to 15.5oC)
Первый закон термодинамики
Первый закон термодинамики
является постулатом: он не
может быть доказан логическим
путем, а вытекает из суммы
человеческого опыта.
Большая роль в обобщении
эмпирического опыта при
открытии закона принадлежит
Г.К. Гессу, Р. Майеру, Джоулю,
Гельмгольцу.
26
Первый закон термодинамики
Химические процессы сопровождаются изменением энергии.
27
Первый закон термодинамики
Является количественным выражением всеобщего
закона природы о вечности материи и движения:
энергия в системе не создается из ничего и
не исчезает бесследно.
28
Первый закон термодинамики
Вечный двигатель
первого рода
невозможен (работа
требует энергии).
Первый закон термодинамики
Система получает
теплоту за счет работы
внешних сил.
Система теряет теплоту за
счет совершение ею
работы против внешних
сил.
Q>0
Q<0
w<0
w>0
Как изменяется внутренняя энергия системы?
U
Q>0
Q<0
w<0
w>0
На что расходуется теплота, подведенная к системе?
Первый закон термодинамики
Пример:
Первая
ситуация:
идеальный газ
находится в
изолированном
цилиндре с
поршнем.

34. Первый закон термодинамики
Что произойдетс газом, если
поршень будет
перемещаться?
35. Первый закон термодинамики
Если цилиндризолирован,
температура будет
расти, атомы
будут двигаться
быстрее, а
давление
повышаться.
36. Первый закон термодинамики
При этомвнешние силы
совершат работу
в продвижении
поршня:
W = P V
x
37. Первый закон термодинамики
Работа,проделанная над
газом, равна
изменению
внутренней
энергии газа:
W = U
x
38. Первый закон термодинамики
Вторая ситуация:цилиндр
помещен на
горячую плиту.
Что произойдет с
газом?
39. Первый закон термодинамики
Атомы будутдвигаться быстрее,
в системе будет
увеличиваться
внутренняя
энергия:
Q = U
40. Первый закон термодинамики
Что произойдет,если к системе
одновременно
подвести теплоту
и продвинуть
поршень?
F
41.
 Первый закон термодинамикиПодведенная
Первый закон термодинамикиПодведеннаятеплота будет
расходоваться на
увеличение
внутренней
энергии и на
совершение
системой работы
против внешних
сил:
Q = U +W
F
Первый закон термодинамики
Теплота, подведенная к системе,
расходуется
только
на
увеличение
внутренней энергии системы и на
совершение системой работы против
внешних сил.
±δQ =dU ± δW
(дифференциальная форма)
± Q = ΔU ± W (интегральная
форма)
Теплота и работа: приращение внутренней работы
± Q = U ± W
Работа, совершаемая системой (+)
или (-) над системой.
Внутренняя энергия система
Теплота получаемая (+)
или отданная (-) системой.
43
Первый закон термодинамики
В биологических системах теплота обычно
отдается системой во внешнюю среду, а работа
совершается за счет убыли внутренней
энергии. Поэтому для биологических систем
математическую запись первого начала
термодинамики представляют:
– Q = ΔU – W.

45. Первый закон термодинамики
Теплота (Q) – форма передачи энергии,посредством хаотического столкновения частиц
соприкасающихся систем, системы и среды.
Q = С·ΔT [Дж], где
С – молярная теплоемкость [Дж моль/К].
46. Первый закон термодинамики
Работа (W) – форма передачи энергии отсистемы в окружающую среду или другой
системе, посредством упорядоченного
взаимодействия частиц, вызванная
преодолением сопротивления.
Простейшей работой является работа
расширения идеального газа в цилиндре с
поршнем (открытая система): W = р ΔV.
Первый закон термодинамики
Падающий груз поворачивает лопасти
вертушки в изолированном стакане воды.
Температура
воды
возрастает
из-за
механической работы внутри системы.
Первый закон термодинамики
Пар, идущий из чайника, заставляет
вертушку крутиться в обычной паровой
турбине. Работа, совершаемая паром,
поднимает небольшой груз.
Энтальпия (от греч.
 entalpio нагреваю) – это часть
entalpio нагреваю) – это частьвнутренней энергии системы,
которая может совершить
полезную работу.
Теплота расширения в
изобарном процессе:
W= p·ΔV, где
ΔV – изменение объема
системы, ΔV=V2-V1
Энтальпия
H 2 (г)
HCl раствор
HCl раствор
51. Функции состояния системы
• Из первого закона ТД:Q = ΔU + W
Qр = ΔU + р·Δ V =(U2+р·V2) – (U1+ p·V1), где:
Qр – теплота изобарного процесса при
р=const;
U + р·V = Н, т. е. энтальпия,
=> Qр=Н2-Н1=ΔН,
т.е.
ΔН=Qр
52. Функции состояния системы
Энтальпия – это функция состояниясистемы, приращение которой равно
теплоте, поступившей в систему в изобарном
процессе.
Т.к. ΔН=Qр, => ΔН = ΔU + р·ΔV [кДж·моль-1]
Энтальпию часто называют «тепловой функцией»
или «теплосодержанием» системы.
Функции состояния системы
Экзотермический
процесс, ΔН<0 .
Эндотермический
процесс, ΔН>0
Энтальпия (H):
Абсолютное значение энтальпии измерить
невозможно, поэтому измеряют ее приращение:
Hсистемы = Hкон – Hнач
ΔН = Ср ΔТ
54
Энтропия (S) характеризует связанную энергию.

В реальных необратимых системах только часть
энергии превращается в работу, другая часть
энергии является как бы связанной. Мера
неупорядоченности системы.
56. Функции состояния системы
Энтропия (по Клаузиусу) – функциясостояния система, приращение которой (ΔS)
равно
минимальной
теплоте
(Qmin),
поступившей в систему в обратимом
изотермическом процессе, деленной на
абсолютную температуру (Т), при которой
совершается этот процесс.
ΔS=Qmin/T, [Дж · моль-1 · К-1].
57. Функции состояния системы
Энтропия связана с вероятностью состояниясистемы уравнением Больцмана:
S=КБ · InW, где
KБ-постоянная Больцмана,
KБ = R/Nа= 1,38· 10-23 Дж· К-1;
W-вероятность состояния системы, т.е. число
микросостояний, которым может быть реализовано
данное макросостояние.
Опытным путем определяют приращение
энтропии: ΔS = S2 – S1.
Чем выше энтропия, тем больше неупорядоченность системы.
Энтропия
Твердое тело
Sкристалла
Жидкость
Газ
Sжидкости Sгаз
60.
 ЭнтропияЖидкость
ЭнтропияЖидкостьЭнтропия, S
Твердое
тело
Газ
Кипение
Плавление
Температура, К
61. Функции состояния системы
Ростом энтропии ΔS 0 сопровождаются такиесамопроизвольные процессы, как испарение жидкости,
таяние льда, растворение веществ в растворителях, т.е.
процессы, которые приводят к увеличению беспорядка в
системе.
Снижением энтропии ΔS 0 сопровождаются
процессы кристаллизации веществ, реакции
полимеризации, поликонденсации, т.е. процессы,
которые приводят к увеличению упорядоченности в
системе.
Как бы Вы описали объект, у которого S=0?
0K
Абсолютно твердый кристалл
без движения
Чисто теоретически
Невозможно достигнуть абсолютного
нуля!
Энтропия Вселенной всегда возрастает!
“Мама, это не моя вина…
Это Вселенная хочет, чтобы моя
комната выглядела так!”
Для изолированных систем
является
критерием
протекания процессов:
энтропия
самопроизвольного
a) Самопроизвольный процесс S>0
b) Обратный процесс
S<0
c) Состояние равновесия
S=0
Приращение энтропии:
1.
 ) Ag+(р-р)+ Cl-(р-р) AgCl(к)
) Ag+(р-р)+ Cl-(р-р) AgCl(к)1) S < 0
2.) Nh5Cl(к) Nh4(г)+ HCl(г)
2) S > 0
3.) h3(г) + Br2(г) 2HBr(г)
3) S?
4. Свободная энергия Гельмгольца
Свободная энергия Гельмгольца термодинамический потенциал, убыль которого
в изотермическом процессе равна работе,
совершённой системой над внешними силами.
ΔF = ΔU – TΔS
67. Функции состояния системы
5. Свободная энергия Гиббса (G)Энергия Гиббса (G) – это часть потенциальной
энергии реагирующих веществ, которая может
быть использована для осуществления полезной
работы.
При протекании изобарно-изотермических
процессов:
ΔG = ΔH – TΔS
68. Функции состояния системы
Анализ уравнения:1 Энтальпийный фактор ΔH. Определяет
стремление системы снизить свою энергию за счет
образования сложных частиц из более простых, при
этом совершается полезная работа.
2 Энтропийный фактор TΔS. Определяет
стремление системы к хаотичному
неупорядоченному состоянию за счет распада
сложных частиц на более простые и распределению
их по всему объему системы.

69. Функции состояния системы
Величина ΔG служит критерием возможностисамопроизвольного протекания процессов.
Процесс протекает самопроизвольно, если ΔG<0.
При ΔG>0, процесс самопроизвольно не протекает.
Если ΔG=0, то в системе установилось состояние
равновесия.
70. Влияние температуры на величину ΔG:
1. При ΔН>0 , ΔS>0 , процесс протекаетсамопроизвольно только при высоких температурах.
2. При ΔН>0, ΔS<0 , процесс самопроизвольно не
протекает ни при каких температурах.
3. При ΔН<0, ΔS>0, процесс самопроизвольно
протекает при любых температурах.
4. При ΔН<0, ΔS<0, процесс самопроизвольно
протекает только при низких температурах.
71. Функции состояния системы
6. Химический потенциал(μ)Химический потенциал какого-либо вещества в
системе равен отношению энергии Гиббса (G) к
количеству вещества (n).
μ=G(x)/n(x),
отсюда
G(х)=n(х)·μ(х).
Если система состоит из нескольких веществ x1, x2, x3…,
то: G=n(x1) ·μ(x1)+n(x2) ·μ(x2)+n(x3) ·μ(x3) + …
72.
 Функции состояния системыДля вещества, находящегося в растворе, μ зависит
Функции состояния системыДля вещества, находящегося в растворе, μ зависитот концентрации раствора, и природы растворителя.
Уравнением изотермы:
μ(x) = μ0(x) + R·T ·In C(x),
где
μ(x)- химический потенциал [Дж · моль-1];
μ0(x)- стандартный химический потенциал;
С(x) – молярная концентрация вещества x [моль · дм-3].
С увеличением концентрации вещества в системе μ
увеличивается, т.е. ∆ μ(х) 0, а с уменьшением снижается, т.е. ∆ μ(х) 0.
73. Вопросы для самоконтроля
1. Что Вы понимаете под термодинамическойсистемой?
2. Охарактеризуйте термодинамические
функции состояния (внутренняя энергия,
энтальпия, энтропия, свободная энергия
Гельмгольца, свободная энергия Гиббса,
химический потенциал).
3. Сформулируйте первый закон термодинамики.
СПАСИБО ЗА ВАШЕ
ВНИМАНИЕ!
75. ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ
Лекция 2Термохимия. Второй закон термодинамики.
Химическое равновесие
Основные понятия.

Закон Гесса и его следствия.
Второй закон термодинамики.
Химическое равновесие.
Лектор: Степанова Ирина Петровна
доктор биологических наук,
профессор, зав. кафедрой химии
ЦЕЛИ ЛЕКЦИИ
ОБУЧАЮЩАЯ: сформировать знания об основах
химической термодинамики, втором законе
термодинамики и химическом равновесии.
РАЗВИВАЮЩАЯ: расширить кругозор
обучающихся на основе интеграции знаний, развить
логическое мышление.
ВОСПИТАТЕЛЬНАЯ: содействовать формированию
у обучающихся устойчивого интереса к изучению
дисциплины.
Термохимия
Раздел ТД, изучающий изменение
энергии при протекании химических
процессов, называется химической
термодинамикой или термохимией.
78. Основные понятия термохимии
Химическая реакция как термодинамическийпроцесс, заключается в превращении одних
веществ в другие за счет изменения состава и
(или) строения.
Для физико-химических процессов действует
закон сохранения массы, установленный
М.
 В. Ломоносовым (m1 = m2).
В. Ломоносовым (m1 = m2).79. Основные понятия термохимии
Термохимическое уравнение условное изображение физикохимического процесса.80. Особенности термохимических уравнений:
1. Уравнения записываются с учетом ТД функцийсостояния системы (ΔH, Δ S).
2. Учитывается 1 моль вещества, поэтому возможны
дробные коэффициенты.
3. Указываются агрегатные состояния веществ.
4. С ТХ уравнениями могут производиться обычные
алгебраические действия.
Пример: ½ N2(г)+ ½ O2(г)= NO(г),ΔH>0.
81. 1. Основные понятия термохимии
Тепловой эффект (Q, кДж·моль-1 ) – энергия, котораявыделяется или поглощается в форме теплоты, при
необратимом протекании физико-химического
процесса при условии: Т, р = const или р, V = const,
система совершает только работу расширения (А’ = 0 ).
Если процесс проводится в автоклаве (V=const)
тепловой эффект равен приращению внутренней
энергии: Qv = ΔU.
Eсли процесс проводится в открытой системе
(р = const) тепловой эффект равен приращению
энтальпии: Qp = ΔН.

82. Основные понятия термохимии
Стандартный тепловой эффект – теплота физикохимического процесса, протекающего в стандартныхусловиях: Т=298К, р=101,3 кПа.
При этом твердые и жидкие вещества находятся в
устойчивой модификации, газы близки к состоянию
идеального газа.
Стандартные тепловые эффекты экспериментально
определены и приводятся в специальных
справочниках.
Закон Гесса
Частным выражением 1-го начала термодинамики
применительно к химическим процессам является закон
Гесса (1840 г):
Приращение энтальпии (тепловой эффект)
химического процесса в изобарноизотермических условиях зависит только от
природы и состояния реагентов и продуктов
реакции и не зависит от пути протекания
реакции.
Приращение энтальпии ( H)
H = h3 – h2
Энтальпия является функцией состояния.
A
B
С
Приращение
энтальпии
не зависит
от пути
процесса.
84
85. Закон Гесса
Например: ЕслиС (т) + О2 (г) = СО2 (г), ΔН1;
или провести процесс по этапам:
С (т) + 1/2О2 (г) = СО (г), ΔН2;
СО (г) + 1/2О2 (г) = СО2 (г), ΔН3,
то
ΔН1 = ΔН2 + ΔН3.

Приращение энтальпии ( H)
В реакции:
H = Hпродукты – Hреагенты
H > 0 – теплота поглощается,
H < 0 – теплота выделяется.
Окружающая среда
Система
Окружающая среда
Система
Теплота
Теплота
Энтальпия, кДж
Энергия выделяется Экзотермическая реакция
Реагенты
H < 0 теплота выделяется.
Экзотермический
процесс
Продукты
Энтальпия, кДж
Энергия поглощается Эндотермическая реакция
Продукты
H >
0 теплота поглощается
Реагенты
Эндотермический
процесс
Закон Гесса:
Из первого закона термодинамики:
Uсистема = – Uсреда
Каждому экзотермическому процессу
соответствует эндотермический процесс.
89
Задача:
Реакция происходит в присутствии катализатора
MnO2:
2KClO3(к) 2KCl(к) + 3O2(г)
H = -89.7 кДж
Какой знак имеет H обратной реакции?
+89.7 кД
90
Определите знак теплового эффекта процесса:
Плавление льда?
Кристаллизация воды ?
Горение свечи?
Взрыв динамита?
91
92.
 Закон ГессаРасчеты тепловых эффектов реакций (ΔН0х.р.) по
Закон ГессаРасчеты тепловых эффектов реакций (ΔН0х.р.) потермохимическим уравнениям производят либо по
теплотам образования веществ, либо по теплота их
сгорания, которые определены экспериментально и
являются табличными величинами.
Калори́метр (от лат. calor тепло и metor – измерять)
прибор для измерения
количества теплоты,
выделяющейся или
поглощающейся в какомлибо физическом,
химическом или
биологическом процессе.
вода
реагенты
Стальная
«бомба»
Калориметр
94. Закон Гесса
Энтальпия образования вещества(теплота образования) – это
тепловой эффект реакции
образования 1 моля вещества из
простых веществ, обозначается:
ΔНобр(Х) [кДж · моль-1].
Калориметр
95. Закон Гесса
Энтальпия образования, измеренная пристандартных условиях, называется
стандартной энтальпией образования и
является справочной величиной,
обозначается:
ΔН0обр(Х) [кДж · моль-1].
Для простых веществ стандартная
энтальпия образования = 0.

ΔН0обр(простых веществ) = 0
96. Первое следствие закона Гесса
Тепловой эффект процесса равеналгебраической сумме энтальпий образования
продуктов за вычетом алгебраической суммы
энтальпий образования реагентов с учетом их
стехиометрических коэффициентов.
ΔН0проц. = ∑nΔН0обр(прод) – ∑nΔН0обр(реагент),
ΔН0проц.[кДж ·моль-1].
CS2(к) + 3O2(г) CO2(г) + 2SO2(г)
ΔН0обр:
87.9кДж/моль
0 кДж/моль -393.5 кДж/моль -296.8 кДж/моль
Каждое значение ΔН0 должно быть
умножено на количество моль
вещества в уравнении.
97
CS2(к) + 3O2(г) CO2(г) + 2SO2(г)
ΔН0обр:
87.9кДж/моль
0 кДж/моль
-393.5 кДж/моль -296.8 кДж/моль
ΔН0проц.= ∑nΔН0обр(прод.) – ∑nΔН0обр(реаг.)
ΔН0х.р. = [-393.5 + 2(-296.8)] – [87.9 + 3(0)]
ΔН0х.р. = -1073.4 кДж
98
99. Закон Гесса
Для многих органических соединенийневозможно одновременно синтезировать
сложное вещество из простых и при этом
определить тепловой эффект химической
реакции, поэтому для них основой расчетов
является энтальпия сгорания.

100. Закон Гесса
Энтальпия сгорания (теплотасгорания) – тепловой эффект
реакции сгорания 1 моля
вещества до высших оксидов,
обозначается:
ΔHсгор.(Х) [кДж · моль-1].
Калориметр
101. Закон Гесса
Энтальпия сгорания, измеренная пристандартных условиях, называется
стандартной,
обозначается ΔН0сгор.(Х) [кДж · моль-1].
Энтальпии сгорания высших
оксидов равны 0.
Второе следствие закона Гесса:
Тепловой эффект химического процесса равен
алгебраической сумме энтальпий сгорания
реагентов за вычетом алгебраической суммы
энтальпий сгорания продуктов с учетом их
стехиометрических коэффициентов.
ΔН0проц. = ∑nΔН0сгор(реаг.) -∑nΔН0сгор(прод.), [кДж · моль-1]
103. Закон Гесса
Задача 2. Рассчитать тепловой эффектреакции спиртового брожения глюкозы,
исходя из стандартных энтальпий сгорания:
С6Н12О6 (к) = 2С2Н5ОН(ж) + 2СО2 (г).
ΔН0сгор(С6Н12О6 (к)) = – 2815,78 кДж · моль-1
ΔН0сгор(С2Н5ОН(ж)) = – 1366,9 кДж · моль-1
Решение: по второму следствию закона Гесса:
ΔН0х.
 р. = ΔН0сгор(С6Н12О6 (к)) – 2ΔН0сгор(С2Н5ОН(ж)) =
р. = ΔН0сгор(С6Н12О6 (к)) – 2ΔН0сгор(С2Н5ОН(ж)) =– 82 кДж · моль-1.
Реакция экзотермическая.
104. Закон Гесса
Закон Гесса и его следствия применяют внаучной диетологии. С его помощью оценивают
калорийность пищевых продуктов.
Коэффициентом калорийности называется
тепловой эффект реакции сгорания одного
грамма вещества, взятый с противоположным
знаком.
К= – ΔН0сгор(Х)
Пищевая калорийность
1000 кал = 1 ккал
Так… Пончик с калорийностью в 500 ккал на самом деле
содержит 500.000 кал.
(Съешь два, чтобы был миллион!)
105
Пищевая
калорийность
107. Закон Гесса
Коэффициенты калорийности основныхкомпонентов пищи равны:
К (белков и углеводов) = 16,5 – 17,2 кДж · г-1,
К (жиров) = 37,7 – 39,8 кДж · г-1.
Первое значение (16,5 и 37,7) – нижняя
граница. Второе значение (17,2 – 39,8) –
верхняя граница.
108. Закон Гесса
Для расчета калорийности пищевых продуктовиспользуют формулы:
По нижней границе:
К = 16,5 m(б) + 16,5 m(у) + 37,7 m(ж) [кДж]
По верхней границе:
К = 17,2 m(б) + 17,2 m(у) + 39,8 m(ж) [кДж]
109.
 Закон ГессаЗадача 3. Рассчитайте калорийность 300
Закон ГессаЗадача 3. Рассчитайте калорийность 300граммов порции рыбы, если известно, что в 100 г
этого продукта содержится 12 г белка, 8 г жиров и
0,3 г углеводов. Коэффициенты калорийности
возьмите по нижней границе.
Решение:
К = 3·[16,5 m(б) + 16,5 m(у) + 37,7 m(ж)] [кДж]
К = 1514 кДж (336 кКал)
110. Закон Гесса
• На основании данных по калорийности пищевыхпродуктов, составляется научно- обоснованные
нормы их потребления для различных граждан
населения, в зависимости от пола, возраста,
характера труда.
• Пользуясь этими данными как средними
величинами, врач составляет нормы потребления
пищевых веществ для каждого пациента в
отдельности.
• Норма суточного потребления для взрослого
организма:
Белков-80-100 г.
Жиров-60-70 г.
Углеводов-370-450 г.
111. Закон Гесса
Суточная потребность человека в энергиисоставляет:
1. При легкой работе в сидячем положении8400-11700 кДж (2000-2800 ккал).

2. При умеренной и напряженной мышечной
работе- 12500-15100 кДж (3000-3600 ккал).
3. При тяжелых физических нагрузках-1670020900 кДж (4000-5000 ккал).
Второе начало термодинамики
Второй закон термодинамики
устанавливает направление
протекания самопроизвольных
процессов.
113. Второе начало термодинамики
Существуют различныеравнозначные по смыслу
формулировки 2-го начала
термодинамики.
М.В. Ломоносов (1850),
Р. Клаузиус, (1850): теплота
не может переходить сама
собой от более холодного
тела к более теплому.
Второе начало термодинамики
Второе начало термодинамики
200°
100°
Второе начало термодинамики
200°
100°
Второе начало термодинамики
200°
100°
Второе начало термодинамики
150°
Второе начало термодинамики
150°
Второе начало термодинамики
У. Кельвин (1854):
Никакая тепловая
машина не может
полностью
превратить тепло в
работу: часть его
обязательно должна
быть отдана
холодильнику.

T1
Q
1
Q
2
T2
T1
A
Q
1
Q
2
T2
A
Второе начало термодинамики
В. Освальд (1888):
Невозможен вечный
двигатель второго
рода, т.е. невозможно
полное превращение
теплоты в работу.
122. Второе начало термодинамики
Паровой двигатель123. Второе начало термодинамики
СПОНТАННОНЕ-
СПОНТАННО
Второе начало термодинамики
Больцман:
самопроизвольно могут
протекать только
такие процессы, при
которых система из
менее вероятного
состояния переходит в
более вероятное
состояние.
124. Второе начало термодинамики
Для изолированной системы (при Е=const, V=const) критерием самопроизвольности процесса
является энтропия (S).
Процесс протекает самопроизвольно, если ΔS > 0.
Протекает обратный процесс, если ΔS < 0
В момент равновесия ΔS = 0.
125. Самопроизвольные процессы
• Пример– Свободное перемещение газа
Вакуум Вентиль
закрыт
Газ
126.
 Самопроизвольные процессы– Пример
Самопроизвольные процессы– Пример– Свободное перемещение газа
Увеличение энтропии
Равновесие
Газ
Вентиль
открыт
Газ
127. Второе начало термодинамики
Современнаяформулировка:
энергия
любого вида может переходить от одного
тела к другому только в том случае, если
термодинамический потенциал её у первого
тела выше, чем у второго.
128. Второе начало термодинамики
Для процессов, протекающих при р=соnst иТ=соnst, роль термодинамического потенциала
выполняет энергия Гиббса (изобарно-изотермический
потенциал),
а в случае процессов, протекающих при V=соnst и
Т=соnst – энергия Гельмгольца ΔF (изохорноизотермический потенциал).
129. Второе начало термодинамики
В условиях постоянной температуры идавления
самопроизвольно
могут
протекать только такие процессы, при
которых система способна совершать
работу против внешних сил, то есть для
которых изменение энергии Гиббса –
величина отрицательная.

130. Второе начало термодинамики
Математическое выражение 2-го началатермодинамики:
ΔG0пр. = ∑nΔG0обр(прод) – ∑nΔG0обр(реагент),
ΔG0пр.= ΔН0 – ТΔS0.
131. Биоэнергетика
131132. Особенности организации живых систем:
Биологические системы являютсяоткрытыми.
Процессы в живых системах в
конечном итоге необратимы.
Живые системы не находятся в
состоянии равновесия.
Все биологические системы
гетерогенны.
133. Биоэнергетика
Основным источником энергии для организма человекаявляется химическая энергия, заключенная в пищевых
продуктах, часть которой (за вычетом энергии, выводимой из
организма с продуктами жизнедеятельности) расходуется на:
1) совершение работы внутри организма, связанной с
дыханием, кровообращением и т.д.; 2) нагревание
вдыхаемого воздуха, потребляемой воды и пищи; 3) покрытие
потерь теплоты в окружающую среду с выдыхаемым
воздухом и с продуктами жизнедеятельности и т.
 д.
д.Биоэнергетика
Химическая энергия также расходуется на совершение
внешней работы, связанной с перемещениями человека, его
трудовой деятельностью и т.д.
уменьшается
135. Белки, жиры и углеводы служат субстратами окислительного фосфорилирования – одного из важнейших компонентов клеточного дыхания, приводящ
БиоэнергетикаБелки, жиры и углеводы
служат субстратами
окислительного
фосфорилирования – одного из
важнейших компонентов
клеточного дыхания,
приводящего к получению
энергии в виде АТФ.
135
136. Энергетический обмен
Используетсядля многих
реакций
Энергия
Энергия
• Энергетический обмен в клетке в основном связан с
расщеплением макроэргических связей АТФ.
Энергетический обмен
Продукты
Реагенты
Энергия АТФ используется, например, для
биосинтеза белка.
138. Биоэнергетика
Состояние открытой системы,для которой характерно
постоянство ее параметров,
неизменность во времени
скоростей притока и удаления
веществ и энергии,
называется стационарным.

139. Биоэнергетика
В термодинамике открытых систем важной величинойявляется производная энтропии по времени, которая
показывает прирост энтропии в единицу времени. В
стационарном состоянии организма эта производная
всегда больше нуля.
Cнижении энтропии (негэнтропия) за счет потребления
организмом из окружающей среды питательных веществ
с низким значением энтропии происходит одновременно
с увеличением энтропии за счет выделения в среду
продуктов распада, обладающих высокой энтропией.
140. Теорема Пригожина
Производство энтропии системой, находящейсяв стационарном состоянии, стремится к
минимуму.
dS/dt = dS орг/dt орг + dS среда/dt среда
dS/dt – скорость изменения энтропии;
dS орг/dt орг – скорость изменения энтропии
внутри организма;
dS среда/dt среда – скорость изменения энтропии
вследствие обмена организма с окружающей
средой и массой и энергией.
141. Биоэнергетика
Производство энтропии возрастает в периодэмбриогенеза, при процессах регенерации и при
росте злокачественных новообразований.

142. Вопросы для самоконтроля
1. В чем состоят особенности термохимическихуравнений?
2. Сформулируйте закон Гесса и его следствия.
3. Сформулируйте закон Кирхгоффа.
4. В чем сущность современной формулировки
второго закона термодинамики?
СПАСИБО ЗА ВАШЕ
ВНИМАНИЕ!
Химическое равновесие
145. Равновесное состояние –
Равновесное состояние такое состояние системы, когда припостоянных внешних условиях параметры
системы не изменяются во времени.
Динамическое равновесие:
с одинаковой скоростью
146. Химическое равновесие
• ИстинноеCO + h3O
• Метастабильное
CO2 + h3
2h3 + O2 = 2h3O
147. Термодинамика химического равновесия
Состояние химического равновесия характеризуют закономдействующих масс.
Для обратимой химической реакции вида:
aA + bB ↔ dD + eE
при постоянных внешних условиях отношение
произведения концентрации продуктов к
произведению концентрации реагентов с
учетом
стехиометрии
есть
величина
постоянная
и
называется
константой
химического равновесия (kc).

148. Закон действующих масс (гомогенные системы)
aA + bB
c(A) = [A] = const
c(B) = [B] = const
c(D) = [D] = const
c(E) = [E] = const
dD + eE
d
e
[ D] [ E ]
Kc
a
b
[ A] [ B]
Вещества в твердой фазе в уравнение не входят.
149. Термодинамика химического равновесия
Константа химического равновесия зависитот природы реагирующих веществ и
температуры и не зависит от их концентрации.
Константа равновесия (КС ) может
изменяться от 0 до ∞.
Если k = 0, реакция не протекает;
K = ∞, реакция идет до конца;
K> 1, химическое равновесие смещено в
сторону образования продуктов;
K< 1, химическое равновесие смещено в
сторону образования реагентов.
150. Сдвиг химического равновесия
• Анри Луи Ле Шателье (1884):• Любое воздействие на систему,
находящуюся в состоянии химического
равновесия, вызывает в ней изменения,
стремящиеся ослабить это воздействие.

151. Влияние температуры
• Реакцияэндотермическая
• – Q, ΔH > 0
• при повышении
температуры
• при понижении
температуры
• Реакция экзотермическая
• + Q, ΔH < 0
• при повышении
температуры
• при понижении
температуры
152. Принцип Ле Шателье
• CaCO3CaO + CO2 – Q (ΔH > 0)
• при повышении температуры
• 2NO
N2 + O2 + Q (ΔH < 0)
• при повышении температуры
Kc = f(T)
153. Влияние концентрации
[ D] d [ E ] eKc
[ A]a [ B]b
При V = const:
• Введение реагента
• Введение продукта
• Удаление реагента
• Удаление продукта
Kc = const
154. Принцип Ле Шателье
• 2SO2 + O22SO3
• при увеличении концентрации О2
155. Влияние давления
aA + bBdD + eE
d
e
[ D] [ E ]
Kc
a
b
[ A] [ B]
если d + e = a + b
Δn(газ.) = 0
давление не влияет
156. Принцип Ле Шателье
• Δn(газ.) > 0• при повышении давления
• Δn(газ.
 ) < 0
) < 0• при повышении давления
• при понижении давления
• при понижении давления
Kc = const
157. Влияние давления
• N2 + 3h32Nh4
• Δn(газ.) = 2 – 4 < 0
• при повышении давления
158. Принцип Ле Шателье
Катализатор• не влияет на Kc
• не является реагентом или продуктом
=> не смещает химическое равновесие
ускоряет его достижение
159. Термодинамика химического равновесия
Направление данной химической реакцииобщего вида:
aA + bB
cC + dD
при заданных концентрациях веществ (A, B, C, D)
при постоянной температуре можно представить с
помощью уравнения изотермы:
ΔGр-я = ΔG0р-я + RT ℓn Пс,
где ΔGр-я –изменение энергии Гиббса реакции,
ΔG 0р-я – изменение стандартной энергии Гиббса
ΔG0р-я = -RТℓnКс.
160. Термодинамика химического равновесия
Пс – величина стехиометрического соотношенияконцентраций веществ, участвующих в реакции
при заданных условиях:
СCс * СDd
Пс a
C A * CBb
Преобразованное уравнение изотермы:
ΔGр-я = -RT ℓn К С + RT ℓn ПС =RT (ℓn ПС – ℓn К С )
ΔGр-я = RT ℓn ПС
КС
161.
 Термодинамика химического равновесияАнализ уравнения изотермы
Термодинамика химического равновесияАнализ уравнения изотермыПс
П
1, ln с 0, G 0
Кс
Кс
Если ПС > КС, то
– протекает обратный процесс.
Пс
Пс
1, ln
0, G 0
Кс
Кс
Если ПС < КС, то
– протекает прямой процесс.
Пс
П
1, ln с 0, G 0
Кс
Кс
Если ПС = КС, то
– состояние равновесия.
Спасибо
за Ваше внимание!
три закона термодинамики. Как построить вечный двигатель первого, второго начала?
В продолжение нашего курса «Физика для чайников» начнем рассматривать основы такого важнейшего раздела как термодинамика.
Активное развитие термодинамики началось в девятнадцатом веке. Именно тогда люди начали строить первые паровые машины, а потом активно внедрять их в производство. Началась промышленная революция, и, естественно, всем хотелось увеличить коэффициент полезного действия машин, чтобы произвести больше продукции, доехать подальше и в конце-концов получить больше денег. Все это очень хорошо стимулировало развитие науки и наоборот. Но давайте ближе к сути вопроса.
Все это очень хорошо стимулировало развитие науки и наоборот. Но давайте ближе к сути вопроса.
Парогенераторная прожекторная установка
Термодинамика – раздел физики, изучающий макроскопические системы, их наиболее общие свойства, способы передачи и превращения энергии в таких системах.
Что такое макроскопические системы? Это системы, состоящие из очень большого числа частиц. Например, баллон с газом или воздушный шар. Описание таких систем методами классической механики просто невозможно – ведь мы не можем измерить скорость, энергию и другие параметры каждой молекулы газа в отдельности. Тем не менее, поведение всей совокупности частиц подчиняется статистическим закономерностям. По сути любой видимый нами (невооруженным глазом) предмет может быть определен как термодинамическая система.
Термодинамическая системаТермодинамическая система – реально или мысленно выделяемая макроскопическая физическая система, состоящая из большого числа частиц, не требующая для своего описания привлечения микроскопических характеристик отдельных частиц. Соответственно, для описания термодинамической системы используются макроскопические параметры, не относящиеся к каждой частице, но описывающие систему целиком. Это температура, давление, объем, масса системы и проч.
Соответственно, для описания термодинамической системы используются макроскопические параметры, не относящиеся к каждой частице, но описывающие систему целиком. Это температура, давление, объем, масса системы и проч.
Важно отметить, что термодинамические системы могут быть замкнутыми и незамкнутыми. Замкнутая система – это такая система, которую при помощи реальной или воображаемой оболочки оградили от окружающей среды, при этом количество частиц в системе остается постоянным.
Замкнутая системаСистема может находится в разных состояниях. Например, мы взяли баллон с газом и начали его нагревать. Тем самым мы изменили энергию молекул газа, они стали двигаться быстрее, и система перешла в какое-то новое состояние с более высокой температурой. Но что будет, если систему оставить в покое? Тогда система через какое-то время придет в состояние термодинамического равновесия.
Что это значит?
Термодинамическое равновесие – это состояние системы, в котором ее макроскопические параметры (температура, объем и др.
) остаются неизменными с течением времени.
Термодинамика стоит на трех своих столпах. Существуют три основных постулата или три закона термодинамики. Они называются соответственно первым, вторым и третьим началами термодинамики. Рассмотрим первое начало или первый закон термодинамики.
Первое начало термодинамики
Первое начало термодинамики гласит:
В любой изолированной системе запас энергии остается постоянным.
К слову, у данного постулата есть еще несколько эквивалентных формулировок. Приведем их ниже:
Количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил.
Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Запишем также математическое выражение первого начала термодинамики:
Здесь Q – количество теплоты, дельта U – изменение внутренней энергии, A – работа против внешних сил. Для различных термодинамических процессов в силу их особенностей запись первого начала будет выглядеть по-разному.
Для различных термодинамических процессов в силу их особенностей запись первого начала будет выглядеть по-разному.
Почему невозможен вечный двигатель первого рода?
Людей издревле привлекала ее величество Халява. Философский камень, превращающий любой металл в золото, скатерть самобранка, с которой не нужно готовить, джин, исполняющий любые желания. Еще одной такой идеей была идея вечного двигателя.
Если никто не пытался найти скатерть-самобранку, то вечный двигатель пытались изобрести очень много раз. На протяжении веков разные люди спрашивали себя: как построить вечный двигатель? Согласно историческим записям первым такую попытку предпринял в двенадцатом веке некий индийский ученый. Затем было еще множество попыток, в том числе плотно занимался вопросом и Леонардо да Винчи. Наконец, в девятнадцатом веке светлые головы Германа Гельмгольца и Джеймса Джоуля сформулировали первое начало динамики и подтвердили его опытами, чем развеяли все сомнения. В помощь также статья, о том, как делать презентацию в ворде и powerpoint.
Вечный двигатель невозможен, потому что так устроен мир. Об этом говорят нам законы термодинамики. Согласно первому началу термодинамики, количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил. Например, газ, помещенный в цилиндр с поршнем, получая определенное количество теплоты, увеличивает свою внутреннюю энергию, молекулы движутся быстрее, газ занимает больший объем и толкает поршень (работа против внешних сил). Иными словами, если работа совершается без внешнего притока энергии, она может совершаться лишь за счет внутренней энергии системы, которая рано иди поздно иссякнет, преобразовавшись в совершенную работу, на чем все закончится и система придет к состоянию термодинамического равновесия. Ведь энергия в мире никуда не уходит и не приходит, ее количество остается постоянным, а меняется лишь форма. Конечно, Вы обратили внимание на то, что речь идет о так называемом вечном двигателе первого рода (который может совершать работу без энергии). Спешим заверить, существование вечного двигателя второго рода также невозможно и объясняется вторым началом термодинамики, о котором мы поговорим в ближайшем будущем.
Спешим заверить, существование вечного двигателя второго рода также невозможно и объясняется вторым началом термодинамики, о котором мы поговорим в ближайшем будущем.
Надеемся, знакомство с термодинамикой прошло для Вас приятно и Вы полюбите ее всем сердцем. Если же этого не произойдет, Вы всегда можете поручить выполнение задач по термодинамике нашим авторам, пока сами занимаетесь более приятными делами.
Тема3.Основы химической термодинамики — Студопедия.Нет
Термодинамический метод полезен для прикладной химии тем, что позволяет рассчитать для химических реакций и других физико-химических процессов (фазовые переходы, растворение, адсорбция, электродные процессы и т. д.): а) тепловой эффект (расчет ∆Н), б) принципиальную возможность протекания процесса в нужном направлении (расчет ∆G), в) глубину протекания процесса – выход продуктов – и ее изменение в зависимости от условий (расчет Кравн.).
Для этого в термодинамику вводятся, так называемые, термодинамические функции состояния – величины часто абстрактные, связанные между собой и с измеряемыми свойствами системы (параметрами состояния) математическими зависимостями на основе законов термодинамики.
Советуем начать с ознакомления с содержанием программы и с указанных параграфов учебника, типовыми задачами и, что очень важно, с таблицами стандартных термодинамических функций. К этим таблицам следует возвращаться и в дальнейшем при более углубленном изучении материала с тем, чтобы проанализировать порядок величии термодинамических функций, характер их изменения в зависимости от различных факторов.
В конспекте должны быть определения, принятые обозначения и размерности параметров и функций состояния и математические выражения их связывающие.
Вас не должно пугать обилие новых терминов и формул. Нужно понять их смысл и уметь использовать при решении задач.
Вопросы для самопроверки:
1. Что такое параметр состояния?Какие параметры состояния термодинамической системы являются интенсивными?экстенсивными? Перечислите термодинамические параметры, применяющиеся для описания систем (в том числе и биологических), в которых протекает химическая реакция.
2.Какформулируетсяпервоеначалотермодинамики? Приведите его математическое выражение.
3.Что такое энергия?Перечислите известные вамвиды энергии.
4.Что понимается под внутренней энергиейтермодинамической системы? Что такое энтальпия? Какова связь между внутренней энергией и энтальпией?
5.КакформулируетсязаконГесса?Какрассчитывают тепловые эффекты реакций, которые не могут быть найдены экспериментально? Какие для этого необходимы данные?
6.Что такое теплотасгорания, как ее определяют экспериментально?
7.Как формулируется второе начало термодинамики?
8.Какие процессы в термодинамике называются обратимыми и необратимыми? Приведите примеры.
9.Что такое энтропия?Какой физический смыслимеет различие величин ∆S и ∆Qв случае необратимых процессов? Как может изменяться энтропия изолированной, закрытой и открытой систем?
10.Каково статистическое толкование понятия энтропия?
11.Сформулируйте третий закон термодинамики. Как на его основе производят вычисление абсолютных энтропии? Длячего нужны эти величины?
12. Как связаноизменение изобарного потенциаласнаправлением химических процессов?
Как связаноизменение изобарного потенциаласнаправлением химических процессов?
13.Каким уравнением связаны величины ∆G, ∆H и ∆S?
14.Как связана величина свободной энергии химического процесса с константой его равновесия? Каково значение этого выражения?
Решениетиповыхзадач
1. Определить тепловой эффект реакции образования сульфата алюминия из оксида алюминия и оксида серы при стандартных условиях. Тепловой эффект реакции (q) по принятой в термохимии системе знаков равен изменению энтальпии (∆Нреакц) в ходе реакции, взятому с обратным знаком.
Решение. Для стандартной температуры и стандартных условий *q = –∆Нореакц. По закону Гесса:
,
где ∑ – знак суммирования;
ni – стехиометрические коэффициенты;
∆Но298 – стандартные энтальпии образования (или теплоты образования) химических веществ;
∆Но298 – табличные значения. Приведены в таблице 2 приложения.
Приведены в таблице 2 приложения.
Решение задачи рекомендуется проводить по следующей схеме:
1) Составляем уравнение реакции (в скобках указываем агрегатное состояние вещества).
2) Находим по таблице 2 приложения значения ∆Но298образования Al2O3, Al2(SO4)3 и под каждым химическим символом уравнения реакции подписываем значение ∆Но298, взятое из таблицы, с множителем, равным стехиометрическому коэффициенту:
| ∆Но298: | Al2O3 | + | 3SO3 | = | Al2(SO4)3 |
| кДж/моль | –1670 | 3(–395) | –3444,9 |
3) Суммируем все значения энтальпий продуктов реакции и вычитаем из них сумму энтальпий исходных веществ:
∆Но298 = –3444,9 –(–1670) – 3(–395) = –589,9 кДж
Итак, q = –∆Нореакц = 589,9 кДж/моль. Реакция экзотермическая. термохимическое уравнение образования сульфата алюминия из оксидов:
Реакция экзотермическая. термохимическое уравнение образования сульфата алюминия из оксидов:
Al2O3 + 3SO3 = Al2(SO4)3 + 589,9 кДж.
2. Определить тепловой эффект реакции образования бензола из углерода и водорода по теплотам сгорания С6Н6 (ж), Н2 (г), С(тв).
Решение. Решение проводим по схеме, предложенной в предыдущем примере:
1) Составляем уравнение реакции.
2) Находим в таблице 2 приложения значения ∆Но сгорания; записываем из под соответствующимихимическими символами в уравнение реакции:
| ∆Носгорания: | 6С (тв) | + | 3Н2 (г) | = | С6Н2 (ж) |
| кДж/моль | 6(–393,8) | 3(–286,0) | –3269,9 |
3) По закону Гесса:
,
тогда ∆Нореакц. = 6(–393,8) + 3(–286,0) – (–3269,9) = 49,2 кДж
= 6(–393,8) + 3(–286,0) – (–3269,9) = 49,2 кДж
Тепловой эффект реакции образования бензола С6Н2 (ж):
q = –∆Нореакц = –49,2 кДж/моль
Рекомендуемым способом * можно решать задачи на определение изменений стандартных энтропий (∆S) и изобарного потенциала (∆G) в ходе химических реакций по данным Sо298Gо298 образования участвующих в реакции веществ, пользуясь уравнениями:
,
,
Химическая термодинамика и биоэнергетика. Второй закон термодинамики презентация, доклад
Химическая термодинамика и биоэнергетика
Второй закон термодинамики
План лекции
Обратимые и необратимые процессы
Понятие энтропии
Второй закон термодинамики
Уравнение Больцмана
Энергия Гиббса
Применение второго закона термодинамики к живым системам
Первый закон термодинамики позволяет количественно оценить энергетические характеристики природных, технологических и биологических процессов, но не может определить возможен ли тот или иной процесс и в каком направлении он пойдет
Химические реакции
Обратимые
Na2CO3 + h3O ⇄ NaHCO3 + NaOH
SO2 + O2 ⇄ 2SO3
N2 + 3h3 ⇄ 2Nh4
Необратимые
Zn + h3SO4 = ZnSO4 + h3↑
CuSO4 + 2KOH = K2SO4 + Cu(OH)2↓
NaOH + HCl = NaCl + h3O
Условия состояния равновесия при обратимом процессе
В системе не происходит видимых изменений при отсутствии внешнего воздействия
Легкость его смещения в ту или иную сторону при незначительном внешнем воздействии
Независимость состояния системы при равновесии от направления движения к этому состоянию в результате прямой или обратной реакции
Обратимость процесса
Термодинамическим условием обратимости является возможность обратимого превращения масс (веществ) и обратимого изменения внутренней энергии без ее потери во внешнюю среду в форме теплоты или механической работы
Пример
Необратимость процесса
Термодинамическим условием необратимости является невозможность после реакции получить исходные вещества в первоначальном состоянии без дополнительных затрат энергии
2h3 + O2 2h3O
электролиз
Все процессы жизнедеятельности организмов относятся к необратимым (происходит обмен с окружающей средой массой и энергией)
Принцип Ле Шателье
Если на систему, находящуюся в равновесии, направить внешнее воздействие (изменять концентрацию, давление или температуру), нарушающее это равновесие, то в ней происходят изменения, уменьшающие это воздействие
↓pO2
Hb + O2 HbO2
↑pO2
Энтропия
(термодинамическое определение)
Функция состояния системы, приращение которой равно теплоте, подведенной к системе в обратимом изотермическом процессе, деленной на абсолютную температуру, при которой осуществляется этот процесс
ΔS = S2 – S1
конеч. состояния нач. состояния
состояния нач. состояния
Q
ΔS = —– Дж/моль⋅К
T
В отличие от энтальпии и внутренней энергии, можно рассчитать абсолютное значение энтропии всех веществ, в том числе и простых
С(графит) : ΔH°298 = 0 кДж/моль
ΔS°298 = 5,69 Дж/моль⋅К
Абсолютное значение энтропии можно вычислить, исходя из постулата Планка:
Энтропия кристаллического вещества при абсолютном нуле равна 0 («третий закон термодинамики»)
Закрытая система
6000 Дж
ΔS = ——– = 22 ——-
273 моль⋅К
6000 Дж – теплота таяния 1 моль льда
Изолированная система
ТА > ТВ
-Q Q
ΔSА = —– ; ΔSВ = —–
ТА ТВ
ΔS = ΔSА+ ΔSВ
-Q Q Q(ТА – ТВ)
—– + —– = ————–
ТА ТВ ТА ⋅ ТВ
ΔS > 0
Пример
Упорядоченное состояние системы
Неупорядоченное состояние системы
Молекулярно-кинетическое определение
Энтропия есть мера вероятности пребывания системы в данном состоянии (мера неупорядоченности системы)
Энтропия возрастает при протекании в изолированной системе необратимого процесса, переводящего систему из менее вероятного состояния в более вероятное
Уравнение Больцмана
S = KlnW, где
S – абсолютное значение энтропии
W – число микросостояний
R
K = —– = 1,38⋅10-23 Дж/К
NA
Уравнение показывает, что чем больше микросостояний включено в макросистему, тем больше и энтропия
При обратимой химической реакции в состоянии равновесия в изолированной системе вероятность состояния исходных веществ = вероятности состояния продуктов реакции
Изменение энтропии в состоянии равновесия равно нулю (ΔS = 0)
S(г) > S(ж) > S(аморф) > S(кр)
Энтропия более сложной молекулы > энтропии простой
S°298(СН4) = 186,44 Дж/моль⋅К
S°298(С2Н6) = 229,65 Дж/моль⋅К
Сумма энтропии мономеров > энтропии полимеров
Стандартные энтропии некоторых веществ
Второй закон термодинамики
Любая изолированная система, представленная самой себе, изменяется в направлении состояния, обладающего максимальной вероятностью
Энтропия изолированной системы возрастает в необратимом процессе и остается неизменной в обратимом; она никогда не убывает
Самопроизвольные процессы идут в направлении от менее вероятного к более вероятному состоянию системы
Теплота не может самопроизвольно передаваться от холодного тела к горячему (Клаузиус)
Обстоятельства жизни имеют тенденцию развиваться от плохого к худшему (физики шутят)
Теория Клаузиуса
Тепловая смерть Вселенной неизбежна, так как энтропия стремится к максимуму, а во всем мире будет одна и та же температура
Но:
Вселенная – не изолированная система; она бесконечна
Критерий осуществимости химических реакций
В изолированной системе
ΔS > 0: необратимая реакция
ΔS ΔS = 0: обратимая химическая реакция, находящаяся в равновесии
Энергия Гиббса (G)
Критерий возможности протекания реакции в закрытых и открытых системах (изобарно-изотермический потенциал Z)
G = H – TS
ΔG = ΔH – TΔS
В таких системах самопроизвольно протекают только такие процессы, в результате которых ΔG уменьшается
(II закон)
Закон Гесса для энергии Гиббса
Энергия Гиббса для химической реакции равна разности энергий Гиббса образования продуктов реакции и образования исходных веществ при стандартных условиях
ΔG°298 = ∑ΔG°298 – ∑ΔG°298
реакции обр. продуктов обр.исходных вв.
продуктов обр.исходных вв.
ΔG°298 образования некоторых веществ и ионов
Химические реакции
Экзэргонические – при протекании которых происходит уменьшение энергии Гиббса системы (ΔG Эндэргонические – в результате которых энергия Гиббса возрастает (ΔG > 0) и над системой совершается работа
Движущие силы процессов
ΔG = ΔH – TΔS
Стремление системы к минимальному содержанию внутренней энергии, т.е. к снижению энтальпии (энтальпийный фактор реакции)
Стремление системы к увеличению энтропии (энтропийный фактор реакции)
Реакция идет самопроизвольно, если ΔG
Влияние факторов на направление процессов
Константа химического равновесия
а А + b В ⇄ d D + c C
V1 = K1[A]a⋅[B]b ; V2 = K2[D]d⋅[C]c
K1, K2 = const
V1 и V2 изменяются во времени
При V1 = V2; K1[A]a⋅[B]b = K2[D]d⋅[C]c
K1 [D]d⋅[C]c
Кравн. = —– = ———–
= —– = ———–
K2 [A]a⋅[B]b
Характеризует степень полноты данной реакции; зависит от температуры и не зависит от начальных концентраций реагирующих веществ
Уравнение изотермы химической реакции
ΔG = –RTlnK , где
R = 8,3146 Дж/моль⋅К
Зная значение энергии Гиббса, можно рассчитать константу равновесия
Измерив концентрации продуктов реакции и исходных веществ можно определить ΔG процесса
Уравнение изобары химической реакции
d ln Kравн ΔH°
———– = ——–
d T RT2
Повышение температуры смещает равновесие в сторону реакции, идущей с поглощением тепла (эндотермически) и наоборот, охлаждение сдвигает равновесие в сторону реакции, идущей с выделением тепла
Особенности термодинамики живых систем
Организм обменивается с внешней средой как массой, так и энергией
Все системы живого организма гетерогенны и многофазны
Процессы в живых системах в конечном итоге необратимы
Живые системы находятся не в равновесном состоянии, а в стационарном
Стационарное состояние
Состояние системы, при котором ее параметры со временем не изменяются, но происходит обмен веществом и энергией с окружающей средой
Скорость протекания обратимых реакций в одном направлении больше, чем в другом; разница скоростей в обоих направлениях во времени постоянна
Стационарное состояние организма предполагает сохранение гомеостаза
Случаи нестационарного состояния – стрессовые
Принцип Пригожина
В стационарном состоянии, обусловленным протеканием необратимых процессов, скорость возрастания энтропии имеет положительное и минимальное из возможных значений
Принцип в большей степени применим для зрелого возраста
ΔS живого организма
В процессе усвоения пищи из относительно больших молекул углеводов, жиров, белков образуются мономеры с более простой структурой, CO2, h3O, Nh4, CO(Nh3)2 и др. (ΔS > 0)
(ΔS > 0)
Изменение энтропии, связанное с выведением продуктов окисления в окружающую среду (ΔS Синтез высокомолекулярных веществ в организме, составляющих основу тканей, а также макроэргических соединений (ΔS Производство энтропии возрастает, по сравнению со зрелым организмом, в период эмбриогенеза и старения, во время инфекционных и злокачественных заболеваний
Второе начало термодинамики • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Природным процессам свойственна направленность и необратимость, однако в большинстве законов, описанных в этой книге, это не находит отражения — по крайней мере, явного. Разбить яйца и сделать яичницу не сложно, воссоздать же сырые яйца из готовой яичницы — невозможно. Запах из открытого флакона духов наполняет комнату — однако обратно во флакон его не соберешь. И причина такой необратимости процессов, происходящих во Вселенной, кроется во втором начале термодинамики, который, при всей его кажущейся простоте, является одним из самых трудных и часто неверно понимаемых законов классической физики.
Прежде всего, у этого закона имеется как минимум три равноправные формулировки, предложенные в разные годы физиками разных поколений. Может показаться, что между ними нет ничего общего, однако все они логически эквивалентны между собой. Из любой формулировки второго начала математически выводятся две другие.
Начнем с первой формулировки, принадлежащей немецкому физику Рудольфу Клаузиусу (см. Уравнение Клапейрона—Клаузиуса). Вот простая и наглядная иллюстрация этой формулировки: берем из холодильника кубик льда и кладем его в раковину. По прошествии некоторого времени кубик льда растает, потому что теплота от более теплого тела (воздуха) передастся более холодному (кубику льда). С точки зрения закона сохранения энергии, нет причин для того, чтобы тепловая энергия передавалась именно в таком направлении: даже если бы лед становился всё холоднее, а воздух всё теплее, закон сохранения энергии всё равно бы выполнялся. Тот факт, что этого не происходит, как раз и свидетельствует об уже упоминавшейся направленности физических процессов.
Почему именно так взаимодействуют лед и воздух, мы можем легко объяснить, рассматривая это взаимодействие на молекулярном уровне. Из молекулярно-кинетической теории мы знаем, что температура отражает скорость движения молекул тела — чем быстрее они движутся,тем выше температура тела. Значит, молекулы воздуха движутся быстрее молекул воды в кубике льда. При соударении молекулы воздуха с молекулой воды на поверхности льда, как подсказывает нам опыт, быстрые молекулы, в среднем, замедляются, а медленные ускоряются. Таким образом, молекулы воды начинают двигаться всё быстрее, или, что то же самое, температура льда повышается. Именно это мы имеем в виду, когда говорим, что тепло передается от воздуха ко льду. И в рамках этой модели первая формулировка второго начала термодинамики логически вытекает из поведения молекул.
При перемещении какого-либо тела на какое-либо расстояние под действием определенной силы совершается работа, и различные формы энергии как раз и выражают способность системы произвести определенную работу. Поскольку теплота, отражающая кинетическую энергию молекул, представляет собой одну из форм энергии, она тоже может быть преобразована в работу. Но опять мы имеем дело с направленным процессом. Перевести работу в теплоту можно со стопроцентной эффективностью — вы делаете это каждый раз, когда нажимаете на педаль тормоза в своем автомобиле: вся кинетическая энергия движения вашего автомобиля плюс затраченная вами энергия силы нажатия на педаль через работу вашей ноги и гидравлической системы тормозов полностью превращается в теплоту, выделяющуюся в процессе трения колодок о тормозные диски. Вторая формулировка второго начала термодинамики утверждает, что обратный процесс невозможен. Сколько ни пытайтесь всю тепловую энергию превратить в работу — тепловые потери в окружающую среду неизбежны.
Поскольку теплота, отражающая кинетическую энергию молекул, представляет собой одну из форм энергии, она тоже может быть преобразована в работу. Но опять мы имеем дело с направленным процессом. Перевести работу в теплоту можно со стопроцентной эффективностью — вы делаете это каждый раз, когда нажимаете на педаль тормоза в своем автомобиле: вся кинетическая энергия движения вашего автомобиля плюс затраченная вами энергия силы нажатия на педаль через работу вашей ноги и гидравлической системы тормозов полностью превращается в теплоту, выделяющуюся в процессе трения колодок о тормозные диски. Вторая формулировка второго начала термодинамики утверждает, что обратный процесс невозможен. Сколько ни пытайтесь всю тепловую энергию превратить в работу — тепловые потери в окружающую среду неизбежны.
Проиллюстрировать вторую формулировку в действии несложно. Представьте себе цилиндр двигателя внутреннего сгорания вашего автомобиля. В него впрыскивается высокооктановая топливная смесь, которая сжимается поршнем до высокого давления, после чего она воспламеняется в малом зазоре между головкой блока цилиндров и плотно пригнанным к стенкам цилиндра свободно ходящим поршнем. При взрывном сгорании смеси выделяется значительное количество теплоты в виде раскаленных и расширяющихся продуктов сгорания, давление которых толкает поршень вниз. В идеальном мире мы могли бы достичь КПД использования выделившейся тепловой энергии на уровне 100%, полностью переведя ее в механическую работу поршня.
При взрывном сгорании смеси выделяется значительное количество теплоты в виде раскаленных и расширяющихся продуктов сгорания, давление которых толкает поршень вниз. В идеальном мире мы могли бы достичь КПД использования выделившейся тепловой энергии на уровне 100%, полностью переведя ее в механическую работу поршня.
В реальном мире никто и никогда не соберет такого идеального двигателя по двум причинам. Во-первых, стенки цилиндра неизбежно нагреваются в результате горения рабочей смеси, часть теплоты теряется вхолостую и отводится через систему охлаждения в окружающую среду. Во-вторых, часть работы неизбежно уходит на преодоление силы трения, в результате чего, опять же, нагреваются стенки цилиндров — еще одна тепловая потеря (даже при самом хорошем моторном масле). В-третьих, цилиндру нужно вернуться к исходной точке сжатия, а это также работа по преодолению трения с выделением теплоты, затраченная вхолостую. В итоге мы имеем то, что имеем, а именно: самые совершенные тепловые двигатели работают с КПД не более 50%.
Такая трактовка второго начала термодинамики заложена в принципе Карно, который назван так в честь французского военного инженера Сади Карно. Она сформулирована раньше других и оказала огромное влияние на развитие инженерной техники на многие поколения вперед, хотя и носит прикладной характер. Огромное значение она приобретает с точки зрения современной энергетики — важнейшей отрасли любой национальной экономики. Сегодня, сталкиваясь с дефицитом топливных ресурсов, человечество, тем не менее, вынуждено мириться с тем, что КПД, например, ТЭЦ, работающих на угле или мазуте, не превышает 30-35% — то есть, две трети топлива сжигается впустую, точнее расходуется на подогрев атмосферы — и это перед лицом угрозы глобального потепления. Вот почему современные ТЭЦ легко узнать по колоссальным башням-градирням — именно в них остужается вода, охлаждающая турбины электрогенераторов, и избытки тепловой энергии выбрасываются в окружающую среду. И столь низкая эффективность использования ресурсов — не вина, а беда современных инженеров-конструкторов: они и без того выжимают близко к максимуму того, что позволяет цикл Карно. Те же, кто заявляет, что нашел решение, позволяющее резко сократить тепловые потери энергии (например, сконструировал вечный двигатель), утверждают тем самым, что они перехитрили второе начало термодинамики. С тем же успехом они могли бы утверждать, что знают, как сделать так, чтобы кубик льда в раковине не таял при комнатной температуре, а, наоборот, еще больше охлаждался, нагревая при этом воздух.
Те же, кто заявляет, что нашел решение, позволяющее резко сократить тепловые потери энергии (например, сконструировал вечный двигатель), утверждают тем самым, что они перехитрили второе начало термодинамики. С тем же успехом они могли бы утверждать, что знают, как сделать так, чтобы кубик льда в раковине не таял при комнатной температуре, а, наоборот, еще больше охлаждался, нагревая при этом воздух.
Третья формулировка второго начала термодинамики, приписываемая обычно австрийскому физику Людвигу Больцману (см. Постоянная Больцмана), пожалуй, наиболее известна. Энтропия — это показатель неупорядоченности системы. Чем выше энтропия — тем хаотичнее движение материальных частиц, составляющих систему. Больцману удалось разработать формулу для прямого математического описания степени упорядоченности системы. Давайте посмотрим, как она работает, на примере воды. В жидком состоянии вода представляет собой довольно неупорядоченную структуру, поскольку молекулы свободно перемещаются друг относительно друга, и пространственная ориентация у них может быть произвольной. Другое дело лед — в нем молекулы воды упорядочены, будучи включенными в кристаллическую решетку. Формулировка второго начала термодинамики Больцмана, условно говоря, гласит, что лед, растаяв и превратившись в воду (процесс, сопровождающийся снижением степени упорядоченности и повышением энтропии) сам по себе никогда из воды не возродится. И снова мы видим пример необратимого природного физического явления.
Другое дело лед — в нем молекулы воды упорядочены, будучи включенными в кристаллическую решетку. Формулировка второго начала термодинамики Больцмана, условно говоря, гласит, что лед, растаяв и превратившись в воду (процесс, сопровождающийся снижением степени упорядоченности и повышением энтропии) сам по себе никогда из воды не возродится. И снова мы видим пример необратимого природного физического явления.
Тут важно понимать, что речь не идет о том, что в этой формулировке второе начало термодинамики провозглашает, что энтропия не может снижаться нигде и никогда. В конце концов, растопленный лед можно поместить обратно в морозильную камеру и снова заморозить. Смысл в том, что энтропия не может уменьшаться в замкнутых системах — то есть, в системах, не получающих внешней энергетической подпитки. Работающий холодильник не является изолированной замкнутой системой, поскольку он подключен к сети электропитания и получает энергию извне — в конечном счете, от электростанций, ее производящих. В данном случае замкнутой системой будет холодильник, плюс проводка, плюс местная трансформаторная подстанция, плюс единая сеть энергоснабжения, плюс электростанции. И поскольку рост энтропии в результате беспорядочного испарения из градирен электростанции многократно превышает снижение энтропии за счет кристаллизации льда в вашем холодильнике, второе начало термодинамики ни в коей мере не нарушается.
В данном случае замкнутой системой будет холодильник, плюс проводка, плюс местная трансформаторная подстанция, плюс единая сеть энергоснабжения, плюс электростанции. И поскольку рост энтропии в результате беспорядочного испарения из градирен электростанции многократно превышает снижение энтропии за счет кристаллизации льда в вашем холодильнике, второе начало термодинамики ни в коей мере не нарушается.
А это, я полагаю, приводит еще к одной формулировке второго начала: Холодильник не работает, если он не включен в розетку.
Термодинамика Для чайников – чайники
Обзор
Разберитесь со сложностью термодинамики
Вы потеете при одной мысли о термодинамике? Это не обязательно! Это практическое руководство поможет вам набрать максимальное количество баллов по курсу термодинамики, предлагая простые и понятные объяснения того, как энергия используется в таких вещах, как автомобили, самолеты, кондиционеры и электростанции.
Термодинамика 101 — взгляните на некоторые примеры как естественных, так и искусственных термодинамических систем и узнайте, как можно использовать энергию для выполнения работы
Увеличьте температуру — узнайте, как использовать первый и второй законы термодинамики для определения (и повышения) эффективности машин другой в разных ситуациях, от законов идеального газа до реальных газов
Гори желанием — узнай все, что тебе нужно знать о сохранении массы и энергии в процессах горения
Открыть книгу и найти:
Законы термодинамики
Важные свойства и их отношения
Циклы, приводящие в действие термодинамические процессы
Химические смеси и реакции
Десять пионеров термодинамики
Реальные применения термодинамических законов и концепций
Ученитесь:
Магистр.
 Концепции и принципы термодинамики
Концепции и принципы термодинамики.
Пройдите свой курс термодинамики
Разберитесь со сложностью термодинамики
Вы потеете при одной мысли о термодинамике? Это не обязательно! Это практическое руководство поможет вам набрать максимальное количество баллов по курсу термодинамики, предлагая простые и понятные объяснения того, как энергия используется в таких вещах, как автомобили, самолеты, кондиционеры и электростанции.
Термодинамика 101 — взгляните на некоторые примеры естественных и искусственных термодинамических систем и узнайте, как можно использовать энергию для выполнения работы
Увеличьте тепло — узнайте, как использовать первую и вторые законы термодинамики для определения (и улучшения) эффективности машин
О, веди себя — узнай 411 о том, как газы ведут себя и взаимодействуют друг с другом в различных ситуациях, от законов идеальных газов до реальных газов
Горите с желанием — узнайте все, что вам нужно знать о сохранении массы и энергии в процессах горения их отношения
Подробная информация о твердых телах, жидкостях и газах
Как работа и тепло идут рука об руку
Циклы, приводящие в действие термодинамические процессы
Химические смеси и реакции
Десяти пионеров в термодинамике
Применение термодинамических законов и концепций
. Развитие навыков решения проблем, используемых профессиональными инженерами Завершите курс термодинамики
Памятка по термодинамике для чайников
Термодинамика звучит пугающе, и это может быть так. Однако, если вы сосредоточитесь на наиболее важных термодинамических формулах и уравнениях, научитесь конвертировать одни физические единицы измерения в другие и познакомитесь с физическими константами, связанными с термодинамикой, вы будете первыми в классе.
Статьи из книги
3 результатов
Статьи по физике
Коэффициенты пересчета физических величин
Рано или поздно вам придется перевести одну единицу измерения физических величин в другую. Этот список дает вам некоторые из наиболее распространенных коэффициентов преобразования, которые вам нужны в термодинамике.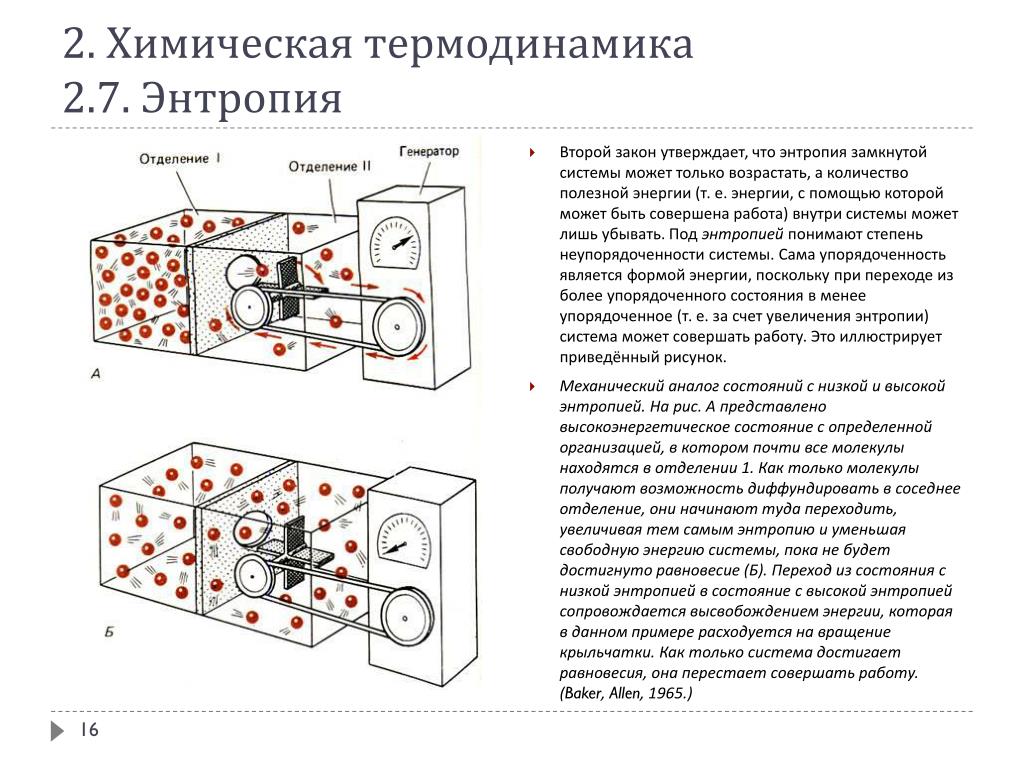
Ускорение: 1 м/с 2 = 100 см/с 2
Площадь: 1 м 2 = 10 4 см 2 = 10 6 мм 2
Плотность: 1 г/см 3 = 1 кг/л = 1000 кг/м 3
Энергия, теплота, работа, внутренняя энергия, энтальпия: 1 кДж = 1000 Дж = 1000 Н·м = 1 кПа·м 3
1 кДж/кг = 1000 м 2 /с 2
Сила: 1 Н = 1 кг·м/с 2
Длина: 1 м = 100 см = 1000 мм
Масса: 1 кг = 1000 г
Мощность, скорость теплопередачи: 1 Вт = 1 Дж/с, 1 кВт = 1000 Вт
Давление: 1 Па = 1 Н/м 2 , 1 кПа = 1000 кПа, 1 МПа = 1000 кПа
1 атмосфера (атм) = 101,325 кПа
Удельная теплоемкость, энтропия: 1 кДж/кг · °C = 1 кДж/кг · K = 1 Дж/г·°C
Удельный объем: 1 м 3 /кг = 1000 л/кг = 1000 см 3 /кг
Температура: T(K) = T(°C) + 273,15, T(°C) = (5/9) T(°F) – 32, T(°F) = (9/5) T (°С) + 32
Скорость: 1 м/с = 3,6 км/ч
Объем: 1 м 3 = 1000 л = 10 6 см 3
Статьи по физике
Физические константы в термодинамике
При решении термодинамических задач вы сталкиваетесь с несколькими физическими константами. Ниже приведен список констант, которые вам понадобятся при работе с потенциальной энергией, давлением или законом идеального газа.
Ниже приведен список констант, которые вам понадобятся при работе с потенциальной энергией, давлением или законом идеального газа.
Ускорение свободного падения: g = 9,81 м/с 2
Стандартное атмосферное давление: 1 атм = 101,3 кПа
Универсальная газовая постоянная:
Статьи по физике
Важные термодинамические уравнения и формулы
Термодинамика наполнена уравнениями и формулами. Вот список наиболее важных из них, которые вам понадобятся для выполнения расчетов, необходимых для решения задач термодинамики.
Уравнения горения:
Расчеты на сжимаемость:
Коэффициент сжимаемости Z: Pv = Z RT
Пониженная температура:
Пониженное давление:
Псевдоуменьшенный удельный объем:
Уравнения эффективности:
Уравнения энергии:
Уравнения энтропии:
Изменение энтропии для идеального газа, постоянная удельная теплоемкость:
Изменение энтропии идеального газа, переменная удельная теплоемкость:
Необратимость процесса:
Формулы идеального газа:
Закон идеального газа: Pv = RT
Газовая постоянная:
Отношение удельных теплоемкостей:
Изэнтропический процесс для идеального газа:
Свойства влажного воздуха:
Относительная влажность:
Удельная влажность:
Свойства смесей:
Рабочие расчеты:
Термодинамика для майки чит-шпаргалка
BY: Mike Pauken и
Обновлено: 02-15-2022
Из книги: Thermodynamics для Dummies
Термодинамика звучит пугающе, и это может быть так. Однако, если вы сосредоточитесь на наиболее важных термодинамических формулах и уравнениях, научитесь конвертировать одни физические единицы измерения в другие и познакомитесь с физическими константами, связанными с термодинамикой, вы будете первыми в классе.
Однако, если вы сосредоточитесь на наиболее важных термодинамических формулах и уравнениях, научитесь конвертировать одни физические единицы измерения в другие и познакомитесь с физическими константами, связанными с термодинамикой, вы будете первыми в классе.Важные термодинамические уравнения и формулы
Термодинамика наполнена уравнениями и формулами. Вот список наиболее важных из них, которые вам понадобятся для выполнения расчетов, необходимых для решения задач термодинамики.
Уравнения горения:
Расчеты сжимаемости:
Коэффициент сжимаемости Z: Pv = Z RT
Пониженная температура:
Пониженное давление:
Псевдоуменьшенный удельный объем:
Уравнения эффективности:
Уравнения энергии:
Уравнения энтропии:
Изменение энтропии идеального газа, постоянная удельная теплоемкость:
Изменение энтропии идеального газа, переменная удельная теплоемкость:
Необратимость процесса:
Формулы идеального газа:
Закон идеального газа: Pv = RT
Газовая постоянная:
Отношение удельных теплоемкостей:
Изэнтропический процесс для идеального газа:
Свойства влажного воздуха:
Относительная влажность:
Удельная влажность:
Свойства смесей:
Рабочие расчеты:
Переводные коэффициенты для физических величин
Рано или поздно вам придется перевести одну единицу измерения в другую. Этот список дает вам некоторые из наиболее распространенных коэффициентов преобразования, которые вам нужны в термодинамике.
Этот список дает вам некоторые из наиболее распространенных коэффициентов преобразования, которые вам нужны в термодинамике.
Ускорение: 1 м/с 2 = 100 см/с 2
Площадь: 1 м 2 = 10 4 см 2 = 10 6 мм 2
Плотность: 1 г/см 3 = 1 кг/л = 1000 кг/м 3
Энергия, теплота, работа, внутренняя энергия, энтальпия: 1 кДж = 1000 Дж = 1000 Н·м = 1 кПа·м 3
1 кДж/кг = 1000 м 2 /с 2
Сила: 1 Н = 1 кг·м/с 2
Длина: 1 м = 100 см = 1000 мм
Масса: 1 кг = 1000 г
Мощность, скорость теплопередачи: 1 Вт = 1 Дж/с, 1 кВт = 1000 Вт
Давление: 1 Па = 1 Н/м 2 , 1 кПа = 1000 кПа, 1 МПа = 1000 кПа
1 атмосфера (атм) = 101,325 кПа
Удельная теплоемкость, энтропия: 1 кДж/кг · °C = 1 кДж/кг · K = 1 Дж/г·°C
Удельный объем: 1 м 3 /кг = 1000 л/кг = 1000 см 3 /кг
Температура: T(K) = T(°C) + 273,15, T(°C) = (5/9) T(°F) – 32, T(°F) = (9/5) T( °С) + 32
Скорость: 1 м/с = 3,6 км/ч
Объем: 1 м 3 = 1000 л = 10 6 см 3
Физические константы в термодинамике
При решении термодинамических задач вы сталкиваетесь с несколькими физическими константами. Ниже приведен список констант, которые вам понадобятся при работе с потенциальной энергией, давлением или законом идеального газа.
Ниже приведен список констант, которые вам понадобятся при работе с потенциальной энергией, давлением или законом идеального газа.
Ускорение свободного падения: g = 9,81 м/с 2
Стандартное атмосферное давление: 1 атм = 101,3 кПа
Универсальная газовая постоянная:
Об этой статье
Эта статья взята из книги:
- Термодинамика для чайников,
Об авторе книги:
Майкл Паукен, доктор философии, старший инженер-механик Лаборатории реактивного движения НАСА, операционного подразделения Калифорнийского технологического института, где он также читает курсы по термодинамике и теплопередаче.Этот артикул находится в категории:
- Физика,
Термодинамика для чайников | Wiley
Выбранный тип: Мягкая обложка
Количество:
36,95 австралийских долларов
* Цена и налоги информация
Цифровая пробная копия
Запросить цифровую оценочную копиюМайк Паукен
ISBN: 978-1-118-00291-9
июль 2011 г. 384 страницы
384 страницы
Электронная книга
От 24,99 австралийских долларов
Печать
От 36,95 австралийских долларов
Электронная книга com are delivered on the VitalSource platform. To download and read them, users must install the VitalSource Bookshelf Software.</li><li>E-books have DRM protection on them, which means only the person who purchases and downloads the e-book can access it.</li><li>E-books are non-returnable and non-refundable.</li><li>To learn more about our e-books, please refer to our <a href="https://www.wiley.com/wiley-ebooks" target="_blank">FAQ</a>.</li></ul>” data-original-title=”” title=””/>
24,99 австралийских долларов
Мягкая обложка
36,95 австралийских долларов
Загрузить рекламный проспект
Загрузить рекламный проспект
Загрузить флаер продукта для загрузки PDF в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF в новой вкладке. Это фиктивное описание.
Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF в новой вкладке. Это фиктивное описание.
Загрузить флаер продукта — загрузить PDF в новой вкладке. Это фиктивное описание.
Описание
Термодинамика для чайников соответствует типичному курсу термодинамики, предлагаемому на уровне бакалавриата, и помогает читателям понять фундаментальные концепции предмета и помогает развить навыки решения проблем посредством практики решения проблем, связанных с энергетикой. Конкретный охват включает:
- Общий принцип баланса (открытые системы, закрытые системы, балансы ставок, балансы приращений)
- Балансы масс (удельный объем, масса системы, массовый расход)
- Нулевой закон (термодинамическое равновесие и температура)
- Балансы первого закона (внутренняя энергия, энтальпия)
- Балансы второго закона (наличие, энтропия)
- Циклы (Ренкина, Брайтона, парокомпрессионный)
- Нереагирующие смеси идеальных газов
- Реагирующие смеси (массовые балансы, энергетические балансы, теплота сгорания, нормированная энтальпия)
Об авторе
Майкл Паукен , доктор философии, старший инженер-механик Лаборатории реактивного движения НАСА, операционного подразделения Калифорнийского технологического института, где он также читает курсы по термодинамике и теплопередаче.
Разрешения
Запросить разрешение на повторное использование контента с этого сайта
Содержание
Введение. Вещества 39
Глава 4. Работа и тепло идут вместе, как макароны с сыром 57
Часть II. Применение законов термодинамики 75
Глава 5. Использование первого закона в закрытых системах 77
Глава 6. Использование первого закона в открытых системах 91
Глава 7. Управление тепловыми двигателями и холодильниками с помощью второго закона 111
Глава 8. Энтропия — это конец Вселенной 123 Второй закон термодинамики 145
Часть III. Самолеты, поезда и автомобили: заставим тепло работать на вас 165
Глава 10. Работа с циклами Карно и Брайтона 167
Глава 11. Работа с циклами Отто и Дизеля 197
Работа с циклами Отто и Дизеля 197
Глава 12. Работа с циклами Ренкина 221
Глава 13. Охлаждение с помощью циклов охлаждения 243
Часть IV. Работа с термодинамическими отношениями, реакциями и смесями 265
Глава 14. Понимание реального поведенияГлава 15. Смешивание газов, которые не реагируют друг с другом 277
Глава 16. Горение при горении 303
Часть V. Часть десятков 325
Глава 17. Десять знаменитых имен в термодинамике 3270007
Глава 18: Еще десять циклов примечаний 331
Приложение: Таблицы термодинамических свойств 341
Алфавитный указатель 351
19: Химическая термодинамика – Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 21674
Наша цель в этой главе состоит в том, чтобы расширить понятия термохимии до исследования термодинамики (от греческого thermo и dynamic , что означает «тепло» и «мощность» соответственно), изучение взаимосвязей между теплом, работу и запас энергии в системе, находящейся в равновесии. Термодинамика сообщает химикам, возможна ли та или иная реакция энергетически в том направлении, в котором она написана, и дает состав реакционной системы в состоянии равновесия. Однако оно ничего не говорит о том, будет ли энергетически возможная реакция на самом деле происходят так, как написано, и это ничего не говорит нам о скорости реакции или пути, по которому она будет происходить (описываемом химической кинетикой). Химическая термодинамика обеспечивает связь между макроскопическими свойствами вещества и индивидуальными свойствами составляющих его молекул и атомов. Как вы увидите, термодинамика объясняет, почему графит можно превратить в алмаз; как химическая энергия, запасенная в молекулах, может быть использована для выполнения работы; и почему некоторые процессы, такие как ржавление железа и старение и умирание организмов, протекают спонтанно только в одном направлении, не требуя для этого никакого чистого подвода энергии.
Термодинамика сообщает химикам, возможна ли та или иная реакция энергетически в том направлении, в котором она написана, и дает состав реакционной системы в состоянии равновесия. Однако оно ничего не говорит о том, будет ли энергетически возможная реакция на самом деле происходят так, как написано, и это ничего не говорит нам о скорости реакции или пути, по которому она будет происходить (описываемом химической кинетикой). Химическая термодинамика обеспечивает связь между макроскопическими свойствами вещества и индивидуальными свойствами составляющих его молекул и атомов. Как вы увидите, термодинамика объясняет, почему графит можно превратить в алмаз; как химическая энергия, запасенная в молекулах, может быть использована для выполнения работы; и почему некоторые процессы, такие как ржавление железа и старение и умирание организмов, протекают спонтанно только в одном направлении, не требуя для этого никакого чистого подвода энергии.
- 19.
 1: Самопроизвольные процессы
1: Самопроизвольные процессы - Химические и физические процессы имеют естественную тенденцию протекать в одном направлении при определенных условиях. Самопроизвольный процесс протекает без необходимости постоянного подвода энергии из какого-либо внешнего источника, в то время как несамопроизвольный процесс требует этого. Системы, подвергающиеся спонтанному процессу, могут испытывать или не испытывать прирост или потерю энергии, но они будут испытывать изменения в способе распределения материи и/или энергии внутри системы.
- 19.
- 19.2: Энтропия и второй закон термодинамики
- Энтропия (S) — это функция состояния, значение которой увеличивается с увеличением количества доступных микросостояний. Для данной системы, чем больше количество микросостояний, тем выше энтропия. Во время самопроизвольного процесса энтропия Вселенной возрастает.
- 19.3: Молекулярная интерпретация энтропии
- Эти формы движения представляют собой способы накопления энергии молекулой.
 Чем больше молекулярное движение системы, тем больше число возможных микросостояний и тем выше энтропия. Совершенно упорядоченная система с единственным доступным микросостоянием будет иметь нулевую энтропию. Единственная система, отвечающая этому критерию, — это совершенный кристалл при температуре абсолютного нуля (0 К), в котором каждый атом, молекула или ион компонента закреплены на своем месте в идеальной кристаллической решетке.
Чем больше молекулярное движение системы, тем больше число возможных микросостояний и тем выше энтропия. Совершенно упорядоченная система с единственным доступным микросостоянием будет иметь нулевую энтропию. Единственная система, отвечающая этому критерию, — это совершенный кристалл при температуре абсолютного нуля (0 К), в котором каждый атом, молекула или ион компонента закреплены на своем месте в идеальной кристаллической решетке.
- 19.4: Изменения энтропии в химических реакциях
- Изменения внутренней энергии, не сопровождающиеся изменением температуры, могут отражать изменения энтропии системы.
- 19.5: Свободная энергия Гиббса
- Мы можем предсказать, будет ли реакция происходить самопроизвольно, объединив энтропию, энтальпию и температуру системы в новую функцию состояния, называемую свободной энергией Гиббса (G). Изменение свободной энергии (ΔG) представляет собой разницу между теплотой, выделяемой в ходе процесса, и теплотой, выделяемой в ходе того же процесса, протекающего обратимым образом.
 Если система находится в равновесии, ΔG = 0. Если процесс самопроизвольный, ΔG < 0. Если процесс не является самопроизвольным, как написано.
Если система находится в равновесии, ΔG = 0. Если процесс самопроизвольный, ΔG < 0. Если процесс не является самопроизвольным, как написано.
- 19.6: Свободная энергия и температура
- Мы можем предсказать, будет ли реакция происходить самопроизвольно, объединив энтропию, энтальпию и температуру системы в новую функцию состояния, называемую свободной энергией Гиббса (G). Изменение свободной энергии (ΔG) представляет собой разницу между теплотой, выделяемой в ходе процесса, и теплотой, выделяемой в ходе того же процесса, протекающего обратимым образом. Если система находится в равновесии, ΔG = 0. Если процесс самопроизвольный, ΔG < 0. Если процесс самопроизвольный в обратном направлении, ΔG > 0,9.1007
- 19.7: Свободная энергия и константа равновесия
- Для обратимого процесса (без внешней работы) изменение свободной энергии можно выразить через объем, давление, энтропию и температуру.
 Если продукты и реагенты находятся в своих стандартных состояниях и ΔG° < 0, то K > 1, и продукты имеют преимущество перед реагентами в равновесии. Если ΔG° > 0, то K < 1, и реагенты имеют преимущество перед продуктами, находящимися в равновесии. Если ΔG° = 0, то K = 1, и ни реагенты, ни продукты не благоприятствуют равновесию. Мы можем использовать измеренную константу равновесия
Если продукты и реагенты находятся в своих стандартных состояниях и ΔG° < 0, то K > 1, и продукты имеют преимущество перед реагентами в равновесии. Если ΔG° > 0, то K < 1, и реагенты имеют преимущество перед продуктами, находящимися в равновесии. Если ΔG° = 0, то K = 1, и ни реагенты, ни продукты не благоприятствуют равновесию. Мы можем использовать измеренную константу равновесия
- 19.E: Химическая термодинамика (упражнения)
- Это домашнее задание, сопровождающее текстовую карту, созданную для «Химия: центральная наука» Брауном и др.
19: Chemical Thermodynamics распространяется под лицензией CC BY-NC-SA 3.0, автором, ремиксом и/или куратором является LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Глава
- Лицензия
- СС BY-NC-SA
- Версия лицензии
- 3,0
- Показать страницу TOC
- № на стр.

- Теги
Химическая термодинамика: определение | StudySmarter
Химическая термодинамика: определение | StudySmarterВыберите язык
Предлагаемые языки:
Европа
английский (DE) английский (Великобритания)
StudySmarter — универсальное учебное приложение.
4.8 • Рейтинг +11k
Более 3 миллионов загрузок
Бесплатно
Сохранять
Распечатать
Редактировать
Химическая термодинамика
СОДЕРЖАНИЕ :
ОГЛАВЛЕНИЕ
Когда вы думаете о химии, вы можете представить себе ученого в лаборатории, создающего взрывную реакцию. Некоторые химические реакции выделяют энергию в виде тепла. Физические процессы также связаны с энергией. Например, когда лед тает, ему требуется энергия, чтобы перейти из твердого состояния в жидкое. Термодинамика посвящена изменениям энергии, связанным с физическими и химическими процессами . В химической термодинамике мы уделяем особое внимание термодинамике химических систем .
Некоторые химические реакции выделяют энергию в виде тепла. Физические процессы также связаны с энергией. Например, когда лед тает, ему требуется энергия, чтобы перейти из твердого состояния в жидкое. Термодинамика посвящена изменениям энергии, связанным с физическими и химическими процессами . В химической термодинамике мы уделяем особое внимание термодинамике химических систем .
- Эта статья о химической термодинамике .
- Мы дадим определение химической термодинамике , прежде чем исследовать два ее ключевых закона .
- Затем мы рассмотрим приложения химической термодинамики .
- После этого мы рассмотрим как важность, так и ограничения химической термодинамики .
Химическая термодинамика определение
Химическая термодинамика — это изучение тепловой энергии (теплоты) в химических и физических процессах, таких как химические реакции и изменения состояния . Он касается того, как тепловая энергия преобразуется в другие виды энергии и как это влияет на свойства системы.
Он касается того, как тепловая энергия преобразуется в другие виды энергии и как это влияет на свойства системы.
Давайте немного разберем это определение.
Энергия
Чтобы понять термодинамику, нам нужно поговорить о энергии . Что такое энергия? Ученые пытаются определить его. Вот простое определение:
Энергия — это способность выполнять работу или передавать тепло .
В химии W ork (w или W) — это когда на что-то действует сила, заставляющая это двигаться. Итак, если нет движения, работа не совершается. Тепло (q или Q) означает передачу энергии посредством тепловых взаимодействий, таких как R излучение или проводимость .
Все во Вселенной состоит из энергии. Это означает, что все может совершать работу или передавать тепло. Энергия хранится в виде двух основных типов, которые могут быть преобразованы из одного в другой:
- Кинетическая энергия — это энергия, которую объект имеет благодаря своему движению .

- Потенциальная энергия — это энергия объекта благодаря его относительному положению либо по отношению к различным частям самого себя, либо по отношению к другим объектам.
Все формы энергии относятся к этим двум основным типам. Например, тепловая энергия является формой кинетической энергии. Однако, как и всякая энергия, она может быть преобразована в другие формы, такие как химическая энергия или электрическая энергия .
Системы
Нам также необходимо рассмотреть системы . В термодинамике мы разделяем Вселенную на две части, чтобы упростить наши расчеты:
- А система — вещество или совокупность веществ и энергии. Системы могут быть открытыми , закрытыми , или изолированными , и это определяет, могут ли они обмениваться друг с другом энергией или веществом.

- окружение просто все остальное, чего нет в системе.
Например, если в банке происходит реакция, то банка является системой. Все, что находится за пределами банки, — это окружение.
Система и ее окружение. StudySmarter Originals
Таким образом, термодинамика представляет собой исследование того, как тепловая энергия преобразуется в другие виды энергии в определенных средах, называемых системами . В химической термодинамике мы уделяем особое внимание тому, как тепловая энергия превращается в химическую энергию , и как это влияет на химические реакции или изменения в состоянии .
Законы химической термодинамики
Химическая термодинамика основана на четыре закона термодинамики . Эти четыре основных принципа, открытые такими учеными, как Исаак Ньютон и Джеймс Джоуль, помогают нам понять, как движется энергия, и лежат в основе изучения термодинамики. В этой статье мы рассмотрим первый и второй законы.
В этой статье мы рассмотрим первый и второй законы.
Первый закон термодинамики
Ранее вы узнали о законе сохранения энергии. Этот закон гласит:
“Энергия не может быть создана или уничтожена, она только преобразуется из одной формы в другую.”
Первый закон термодинамики основан на сохранении энергии. Однако мы добавляем дополнительное предложение:
«Общее количество энергии во Вселенной постоянно».
Мы называем общее количество энергии в конкретной системе ее энтальпией.
Энтальпия (H) является мерой тепловой энергии в химической системе. Обычно измеряется в кДж моль -1 .
Энергия внутри системы может переходить из одной формы в другую. Он также может быть передан из системы в ее окружение. Однако общее количество энергии во всей вселенной всегда остается одним и тем же.
Ознакомьтесь с изменениями энтальпии для примеров энтальпии в химических реакциях.
Второй закон термодинамики
Первый закон термодинамики говорит нам, что энергия не может быть создана или уничтожена, и объясняет многие повседневные процессы, например, как электрический ток питает лампочку или глюкоза дает нам энергию для движения. Но хотя энергию можно использовать снова и снова, она не всегда используется эффективно. На самом деле многое тратится впустую. Это помогает объяснить некоторые более случайные явления, которые мы наблюдаем в окружающей нас Вселенной, и составляет основу второго закона термодинамики:
“Не вся тепловая энергия преобразуется в полезную энергию.”
Но куда девается эта энергия? Это способствует тому, что называется энтропией .
Энтропия (S) является мерой беспорядка в системе. Чем больше беспорядок, тем выше энтропия. Обычно он измеряется в Дж К -1 моль -1 .
Это приводит нас к следующей части второго закона термодинамики:
«При самопроизвольных изменениях Вселенная стремится к состоянию большей энтропии».
-Второй закон термодинамики
Второй закон говорит нам, что энергия в природных системах имеет тенденцию двигаться в направлении увеличения энтропии или, другими словами, большего беспорядка. Это объясняет, почему энергия движется в одном направлении, а не в другом. Примеры увеличения энтропии включают растворение твердых веществ или смешивание газов.
Применение химической термодинамики
Мы узнали о двух законах термодинамики. Давайте теперь рассмотрим, как они применимы к реальным химическим процессам.
Самопроизвольные реакции
Мы можем комбинировать принципы, изученные в первых двух законах термодинамики, энтальпии и энтропии, чтобы предсказать, являются ли реакции самопроизвольными или нет.
Спонтанные реакции — это реакции, протекающие без постороннего вмешательства, например, при подаче энергии. Их также называют возможными реакциями .
Примеры спонтанных реакций включают растворение солей, ржавление железа или таяние льда.
Ржавление железа – пример самопроизвольной реакции. Изображение предоставлено: pixabay.com
Мы используем количество под названием Свободная энергия Гиббса (ΔG) , чтобы определить, является ли реакция самопроизвольной или нет. Он связывает энтальпию и энтропию следующим уравнением:
ΔG = ΔH – TΔS
Обратите внимание на следующее:
- ΔG представляет собой изменение свободной энергии Гиббса, измеренное в кДж моль -1 .
- ΔH – изменение энтальпии, измеренное в кДж моль -1 .
- T – температура, измеренная в K.
- ΔS – изменение энтропии, измеренная в кДж K -1 моль -1 .
Энтропия обычно измеряется в Дж К -1 моль -1 . Убедитесь, что вы переводите его в кДж K -1 моль -1 путем деления на 1000.
Если ΔG отрицательно, то реакция идет самопроизвольно. Из этого уравнения мы можем сделать вывод, что сильно экзотермические реакции или реакции с большим увеличением энтропии имеют тенденцию к самопроизвольному протеканию.
Циклы Борна-Габера
Возможно, вы уже узнали о Законе Гесса ранее в своем путешествии по химии.
Закон Гесса гласит, что изменение энтальпии реакции всегда одинаково , независимо от выбранного пути.
Пока вы начинаете с одних и тех же реагентов и заканчиваете одними и теми же продуктами, изменение энтальпии одинаково. Неважно, делаете ли вы это за один шаг, за два шага или за пятнадцать шагов.
Цикл Гесса. StudySmarter Original
Мы выражаем закон Hess по следующему уравнению:
ΔH R = ΔH 1 + ΔH 2
В этом уравнении:
- Δ 11. реакция прямого маршрута.
- ΔH 1 и ΔH 2 представляют собой изменения энтальпии, связанные с косвенным путем.
Изменение энтальпии обычно измеряется в кДж·моль -1 , но при условии, что все единицы измерения согласованы, можно использовать Дж·моль -1 в ваших расчетах.
Отличным применением закона Гесса является вычисление энтальпии решетки .
Энтальпия решетки ( Δ LE H° ), также известная как энтальпия образования решетки , представляет собой изменение энтальпии, когда один моль ионной решетки образуется из ее газообразных ионов в стандартных условиях.
Цикл Борна-Габера
Цикл Борна-Габера (часто пишется без дефиса) — это теоретическая модель, основанная на законе Гесса, которую мы используем для расчета энтальпии решетки.
Принцип здесь такой же, как тот, который мы используем в циклах закона Гесса: Если мы создадим непрямой путь к газообразным ионам, мы можем использовать уравнение для закона Гесса, чтобы найти энтальпию решетки . Например, мы можем не знать прямого маршрута для энтальпии решетки. Однако мы можем решить это, используя косвенный маршрут , который включает известные нам изменения энтальпии. Вот краткий обзор того, как работают циклы:
Вот краткий обзор того, как работают циклы:
Мы берем реакцию, для которой мы хотим найти изменение энтальпии, и создаем косвенный маршрут, который начинается с тех же реагентов и заканчивается теми же продуктами. В этом случае мы хотим найти энтальпию образования решетки.
Мы представляем каждую точку прямого и непрямого маршрута в виде линии, показывающей ее энтальпию.
Разница высот между линиями представляет изменение энтальпии между этими точками.
Мы записываем известные изменения энтальпии непрямого пути и используем их для расчета неизвестного изменения энтальпии прямого пути.
Вот пример. Не волнуйтесь, если это покажется немного запутанным — мы рассмотрим каждый термин более подробно в «Циклах Борна Хабера». Вы также сможете попрактиковаться в использовании циклов Борна-Габера в Расчетах циклов Борна-Габера.
Цикл Борна-Габера для энтальпии кристаллической решетки фторида лития, LiF. StudySmarter Originals
Важность химической термодинамики
Теперь мы рассмотрим важность химической термодинамики . Вот некоторые из его преимуществ:
- Это важная область науки, потому что она объясняет, как и почему происходят многие повседневные реакции.
- Это позволяет нам рассчитать неизвестные изменения энтальпии и предсказать, произойдет реакция или нет .
- Термодинамика также позволяет нам оптимизировать химические процессы и повысить эффективность передачи энергии . Например, это может помочь нам сэкономить на счетах за электроэнергию и сократить затраты на промышленные реакции.
- Термодинамика объясняет, почему реакции достигают химического равновесия.
Ограничения химической термодинамики
Наконец, мы рассмотрим некоторые из ограничений химической термодинамики :
- Это ничего не говорит нам о скорости реакции или о том, сколько времени требуется для завершения реакции.

- Он имеет дело с системами в целом и не дает нам никакой информации о отдельных частицах в них.
Это конец этой статьи. Теперь вы должны понимать, что мы подразумеваем под термином химическая термодинамика и как энтальпия и энтропия соотносятся с ее первыми двумя законами. Вы также должны знать некоторые приложения термодинамики, такие как расчет изменений энтальпии и прогнозирование возможности реакций, и почему термодинамика является полезной областью науки. Наконец, вы должны быть в состоянии понять, почему термодинамика имеет свои ограничения.
Химическая термодинамика. Ключевые выводы
- Химическая термодинамика — это изучение тепловой энергии (тепла) в химических и физических процессах, таких как химические реакции и изменения состояния . Он касается того, как тепловая энергия преобразуется в другие виды энергии и как это влияет на свойства системы.

- Энтальпия (H) является мерой тепловой энергии в химической системе.
- Энтропия (S) является мерой беспорядка в системе.
- Законы термодинамики основаны на энтальпии и энтропии и диктуют реакции в окружающем нас мире:
- первый закон термодинамики гласит, что энергия не может быть создана или уничтожена , и поэтому полная энергия во Вселенной остается постоянным.
- Второй закон термодинамики утверждает, что при спонтанных изменениях Вселенная стремится к состоянию большая энтропия .
- Химическая термодинамика имеет множество применений:
- Циклы Борна-Габера являются теоретической моделью, которую мы используем для расчета энтальпии решетки . Принцип тот же, что и у циклов закона Гесса. Если мы создадим непрямой путь к газообразным ионам, мы сможем использовать уравнение для закона Гесса, чтобы найти энтальпию решетки.

- Свободная энергия Гиббса (ΔG) связывает энтальпию и энтропию и используется для предсказания того, идет ли реакция спонтанных или нет.
- Циклы Борна-Габера являются теоретической моделью, которую мы используем для расчета энтальпии решетки . Принцип тот же, что и у циклов закона Гесса. Если мы создадим непрямой путь к газообразным ионам, мы сможем использовать уравнение для закона Гесса, чтобы найти энтальпию решетки.
- Как и все области науки, химическая термодинамика имеет важность , а также ограничения .
Часто задаваемые вопросы о химической термодинамике
Система – это вещество или совокупность веществ и энергии. В зависимости от типа системы они могут обмениваться с окружающей средой энергией или веществом, или тем и другим, или ни тем, ни другим. Примером закрытой химической системы является реакция внутри герметичного стакана.
Химическая энергия — это энергия, выделяющаяся при взаимодействии химических веществ. Она часто преобразуется в тепловую энергию.
Термодинамика позволяет нам предсказать, произойдет ли реакция, и рассчитать неизвестные изменения энтальпии.
Химическая термодинамика основана на тех же законах, что и обычная термодинамика. Например, первый закон термодинамики говорит нам, что энергия не может быть создана или уничтожена, в то время как второй закон термодинамики утверждает, что спонтанные реакции стремятся к состоянию большей энтропии.
Например, первый закон термодинамики говорит нам, что энергия не может быть создана или уничтожена, в то время как второй закон термодинамики утверждает, что спонтанные реакции стремятся к состоянию большей энтропии.
Физическая и химическая термодинамика основаны на одних и тех же фундаментальных законах. Однако химическая термодинамика уделяет особое внимание термодинамике химических систем и тому, как тепловая энергия превращается в химическую энергию и наоборот.
Заключительный тест по химической термодинамике
Вопрос
Что такое энтальпия решетки?
Показать ответ
Ответ
Энтальпия решетки представляет собой изменение энтальпии, связанное с образованием 1 моля ионной решетки e из газообразных ионов при стандартных условиях.
Показать вопрос
Вопрос
Что из следующего представляет собой энтальпию решетки?
Показать ответ
Ответ
Δ в точке H °
Показать вопрос
Вопрос
Что такое энтальпия?
Показать ответ
Ответ
Энтальпия (H) – это тепловая энергия, хранящаяся в системе.
Показать вопрос
Вопрос
Что такое энтропия?
Показать ответ
Ответ
Энтропия (S) является мерой беспорядка в системе.
Показать вопрос
Вопрос
Что такое второй закон термодинамики?
Показать ответ
Ответ
При спонтанных изменениях Вселенная стремится к состоянию большего беспорядка.
Показать вопрос
Вопрос
Что такое спонтанная реакция?
Показать ответ
Ответ
Спонтанная реакция — это реакция, которая происходит сама по себе, без поступления энергии извне. В самопроизвольной реакции изменение энтальпии (ΔH) уменьшается, а энтропия увеличивается (ΔS).
Показать вопрос
Вопрос
Каково уравнение для свободной энергии Гиббса?
Показать ответ
Ответ
ΔG = ΔH – T ΔS
Показать вопрос
Вопрос
Для чего мы используем циклы Борна-Габера?
Показать ответ
Ответ
Расчет энтальпии решетки
Показать вопрос
Вопрос
Что такое закон Гесса?
Показать ответ
Ответ
Изменение энтальпии в химической реакции не зависит от пути, по которому происходит химическое изменение.
Показать вопрос
Вопрос
В чем разница между энтальпией кристаллической решетки диссоциации и энтальпией кристаллической решетки образования?
Показать ответ
Ответ
Энтальпия образования решетки представляет собой изменение энтальпии образования одного моля ионной решетки из газообразных ионов в стандартных условиях.
Энтальпия диссоциации решетки представляет собой изменение энтальпии, связанное с разрушением одного моля ионной решетки с образованием рассеянных газообразных ионов в стандартных условиях.
Показать вопрос
Вопрос
Порядок шагов для построения цикла Борна-Габера
- Энергия первой ионизации металла
- Энтальпии последующей ионизации, если применимо
- Энтальпия атомизации каждого элемента
- Последующее сродство электрона к электрону, если применимо
- 4
- неметалл
Показать ответ
Ответ
- Энтальпия атомизации каждого элемента
- Первая энергия ионизации металла
- Последующие энтальпии ионизации, если применимо
- Первое сродство к электрону неметалла
- Последующее сродство к электрону, если применимо
- Показать вопрос
Вопрос
Что такое сродство к электрону?
Показать ответ
Ответ
Энергия, высвобождаемая, когда один моль атомов газа присоединяет электрон, образуя один моль ионов газа.

Показать вопрос
Вопрос
Какие два фактора влияют на энтальпию решетки?
Показать ответ
Ответ
Заряд иона
Показать вопрос
Вопрос
Как заряд иона влияет на энтальпию решетки?
Показать ответ
Ответ
Ионы с большим ионным зарядом имеют более сильное электростатическое притяжение между ионами. Это приводит к большей энтальпии решетки.
Показать вопрос
Вопрос
Как радиус иона влияет на энтальпию решетки? Приведите пример.
Показать ответ
Ответ
Ионы с большими радиусами обычно имеют меньшую энтальпию решетки , потому что ионы расположены дальше друг от друга в структуре решетки .
 Электростатическое притяжение между более мелкими ионами сильнее, так как сила ионного притяжения зависит от близости центров притягиваемых ионов .
Электростатическое притяжение между более мелкими ионами сильнее, так как сила ионного притяжения зависит от близости центров притягиваемых ионов .Например, ионы в MgO меньше, чем ионы в NaCl, поэтому NaCl имеет меньшую энтальпию решетки.
Показать вопрос
Вопрос
Почему расчеты энтальпии решетки в физическом стиле являются теоретическими?
Показать ответ
Ответ
Они основаны на предположении, что вещество является высокоионным с сильным электростатическим притяжением между ионами.
Показать вопрос
Вопрос
О чем говорят большие различия между теоретическими и экспериментальными значениями энтальпии решетки?
Показать ответ
Ответ
Большие различия между теоретическими и экспериментальными значениями энтальпии решетки позволяют предположить наличие ковалентного характера в ионной связи.
 Это происходит в результате поляризации из-за радиуса ионов и заряда ионов .
Это происходит в результате поляризации из-за радиуса ионов и заряда ионов .Показать вопрос
Вопрос
Почему энтальпии решетки, рассчитанные с использованием циклов Борна-Габера, называются экспериментальными?
Показать ответ
Ответ
Энтальпии решетки, рассчитанные с использованием циклов Борна-Габера, являются экспериментальными, поскольку они используют изменения энтальпии, которые можно измерить.
Показать вопрос
Вопрос
Почему изменение энтальпии гидратации ионов хлора является экзотермическим?
Показать ответ
Ответ
Тепловая энергия выделяется, когда ионы образуют связи с молекулами воды, поэтому энтальпия гидратации всегда экзотермическая.

Показать вопрос
Вопрос
Что такое энтропия? Дайте два определения.
Показать ответ
Ответ
Энтропия:
- Мера беспорядка в системе.
- Количество возможных способов распределения частиц и их энергии в системе.
Показать вопрос
Вопрос
Что такое спонтанная или возможная реакция?
Показать ответ
Ответ
Спонтанная или возможная реакция — это реакция, которая происходит сама по себе.
Показать вопрос
Вопрос
Что такое второй закон термодинамики?
Показать ответ
Ответ
Изолированные системы всегда имеют тенденцию к большей энтропии.

Показать вопрос
Вопрос
Возможные реакции имеют ____ изменение полной энтропии.
Показать ответ
Ответ
Положительный
Показать вопрос
Вопрос
Каковы единицы измерения энтропии?
Показать ответ
Ответ
J K -1 моль -1
Показать вопрос
Вопрос
Расположить в порядке возрастания энтропии:
- Газ
- Твердое тело
- Жидкость
Показать ответ
Ответ
Твердое, жидкое, газообразное.
Показать вопрос
Вопрос
Какой символ обозначает энтропию?
Показать ответ
Ответ
Показать вопрос
Вопрос
Что такое стандартные значения энтропии?
Показать ответ
Ответ
Значения энтропии, измеренные при стандартных условиях.

Показать вопрос
Вопрос
Что такое свободная энергия Гиббса?
Показать ответ
Ответ
Свободная энергия Гиббса — это энергия, доступная для выполнения работы. Он показывает взаимосвязь между энтальпией и энтропией, чтобы определить, возможна ли реакция, ∆G = ∆H – T∆S.
Показать вопрос
Вопрос
Каково уравнение для свободной энергии?
Показать ответ
Ответ
∆G = ∆H – T∆S
Показать вопрос
Вопрос
Почему ∆G уменьшается с увеличением T?
Показать ответ
Ответ
Потому что изменение энтропии (∆S) увеличивается с температурой.
 Выражение -T∆S станет достаточно большим, чтобы преодолеть ∆H.
Выражение -T∆S станет достаточно большим, чтобы преодолеть ∆H.Показать вопрос
Вопрос
Предложите, как значения ∆H, ∆S и T можно использовать для прогнозирования возможности реакции.
Показать ответ
Ответ:
Используйте уравнение для свободной энергии ∆G = ∆H – T∆S, чтобы определить осуществимость. Если ∆G меньше или равно 0, то реакция возможна.
Показать вопрос
Вопрос
Какая связь между свободной энергией и изменениями энтропии и энтальпии реакции?
Показать ответ
Ответ
Большее увеличение энтропии (система становится более неупорядоченной) и большее уменьшение энтальпии (система выделяет больше тепла) способствуют более низкому (более отрицательному) значению свободной энергии.
 Меньшая (более отрицательная) свободная энергия означает, что реакция более возможно .
Меньшая (более отрицательная) свободная энергия означает, что реакция более возможно .Показать вопрос
Вопрос
Каковы единицы измерения энтальпии?
Показать ответ
Ответ
кДж моль -1
Показать вопрос
Вопрос
Каковы единицы измерения энтропии?
Показать ответ
Ответ
J K -1 моль -1
Показать вопрос
Вопрос
Что такое первый закон термодинамики?
Показать ответ
Ответ
Энергия не может быть создана и уничтожена; общее количество энергии во Вселенной постоянно.

Показать вопрос
Вопрос
Правда или ложь? Химическая термодинамика подчиняется законам, отличным от законов физической термодинамики.
Показать ответ
Ответ
Показать вопрос
Вопрос
Каковы единицы свободной энергии Гиббса?
Показать ответ
Ответ
кДж моль -1
Показать вопрос
Вопрос
Нагрев системы _____ ее энтропия.
Показать ответ
Ответ
Уменьшение
Показать вопрос
Вопрос
Правда или ложь? Реакции никогда не влияют на энтропию их окружения.

Показать ответ
Ответ
Ложь. Только реакции в изолированных системах не влияют на энтропию их окружения. Однако идеально изолированных природных систем не существует.
Показать вопрос
Вопрос
Что обычно имеет более высокую энтропию?
Показать ответ
Ответ
Простая молекула
Показать вопрос
Вопрос
Что свободная энергия Гиббса говорит нам о реакции?
Показать ответ
Ответ
Возможна реакция или нет.
Показать вопрос
Вопрос
Какие единицы используются для количественного определения сродства к электрону?
Показать ответ
Ответ
кДж на моль
Показать вопрос
Вопрос
Сродство к электрону измеряется по реакции целого моля или только одного атома?
Показать ответ
Ответ
Показать вопрос
Вопрос
Определение сродства к электрону
Показать ответ
Ответ
Энергия, высвобождаемая, когда газообразный моль атомов присоединяет электрон.

Показать вопрос
Вопрос
Что подразумевается под сродством к первому электрону?
Показать ответ
Ответ
Электронное сродство нейтрального атома, приобретающего один электрон и превращающегося в анион.
Показать вопрос
Вопрос
Что подразумевается под последовательным сродством к электрону?
Показать ответ
Ответ
Второе, третье и так далее… сродство к электрону.
Показать вопрос
Вопрос
Какой из них описывает сродство ко второму электрону?
Показать ответ
Ответ
Присоединение 2 электронов к атому.

Показать вопрос
Вопрос
Какие три фактора влияют на сродство к электрону?
Показать ответ
Ответ
Заряд ядра, электронная конфигурация и размер атома.
Показать вопрос
Вопрос
Какова тенденция сродства к электрону при переходе через период слева направо?
Показать ответ
Ответ
Сродство к электрону увеличивается.
Показать вопрос
Вопрос
Какова тенденция сродства к электрону при переходе вниз по группе?
Показать ответ
Ответ
Сродство к электрону уменьшается.
Показать вопрос
Подробнее о химической термодинамике
Откройте для себя подходящий контент для ваших тем
Не нужно обманывать, если у вас есть все необходимое для успеха! Упаковано в одно приложение!
Учебный план
Будьте идеально подготовлены вовремя с индивидуальным планом.

Тесты
Проверьте свои знания с помощью игровых тестов.
Карточки
Создавайте и находите карточки в рекордно короткие сроки.
Заметки
Создавайте красивые заметки быстрее, чем когда-либо прежде.
Учебные наборы
Все учебные материалы в одном месте.
Документы
Загружайте неограниченное количество документов и сохраняйте их в Интернете.
Study Analytics
Определите сильные и слабые стороны вашего исследования.
Еженедельные цели
Ставьте индивидуальные учебные цели и зарабатывайте баллы за их достижение.
Умные напоминания
Хватит откладывать на потом наши напоминания об учебе.
Награды
Зарабатывайте очки, открывайте значки и повышайте уровень во время учебы.
Волшебный маркер
Создавайте карточки в заметках полностью автоматически.
Умное форматирование
Создавайте самые красивые учебные материалы, используя наши шаблоны.

Chemical Thermodynamics: Advanced Applications – 1st Edition
Select country/regionUnited States of AmericaUnited KingdomAfghanistanÅland IslandsAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntigua and BarbudaArgentinaArmeniaArubaAustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelgiumBelizeBeninBermudaBhutanBoliviaBonaire, Sint Eustatius and SabaBosnia and HerzegovinaBotswanaBrazilBritish Indian Ocean TerritoryBritish Virgin IslandsBruneiBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCanary IslandsCape VerdeCayman IslandsCentral African RepublicChadChileChinaChristmas IslandCocos (Keeling) IslandsColombiaComorosCongoCook IslandsCosta RicaCroatiaCubaCuraçaoCyprusCzech RepublicDemocratic Republic КонгоДанияДжибутиДоминикаДоминиканская РеспубликаЭквадорЕгипетСальвадорЭкваториальная ГвинеяЭритреяЭстонияЭфиопияФолклендские (Мальвинские) островаФарерские островаФедеративные Штаты МикронезииФиджиФинляндияФранцияФранцузская ГвианаФранцузская ПолинезияГабонГамбияГрузияГерманияГанаG ibraltarGreeceGreenlandGrenadaGuadeloupeGuamGuatemalaGuernseyGuineaGuinea-BissauGuyanaHaitiHondurasHong KongHungaryIcelandIndiaIndonesiaIranIraqIrelandIsle of ManIsraelItalyJamaicaJapanJerseyJordanKazakhstanKenyaKiribatiKuwaitKyrgyzstanLaoLatviaLesothoLiberiaLibyaLiechtensteinLuxembourgMacaoMacedoniaMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMoldovaMonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNepalNetherlandsNew CaledoniaNew ZealandNicaraguaNigerNiueNorfolk IslandNorth KoreaNorthern Mariana IslandsNorwayOmanPakistanPalauPanamaPapua New GuineaParaguayPeruPhilippinesPitcairnPolandPortugalPuerto RicoQatarRéunionRomaniaRwandaSaint BarthélemySaint HelenaSaint Kitts and NevisSaint LuciaSaint Martin (French part)Saint Pierre and MiquelonSaint Vincent and the GrenadinesSamoaSan MarinoSao Tome and PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Maarten (Dutch part)SlovakiaSloveniaSolomon IslandsSoma liaSouth AfricaSouth Georgia and the South Sandwich IslandsSouth KoreaSouth SudanSpainSri LankaSudanSurinameSvalbard and Jan MayenSwazilandSwedenSwitzerlandSyriaTaiwanTajikistanTanzaniaThailandTimor LesteTogoTokelauTongaTrinidad and TobagoTunisiaTurkeyTurkmenistanTurks and Caicos IslandsTuvaluUgandaUkraineUnited Arab EmiratesUruguayUS Virgin IslandsUzbekistanVanuatuVatican CityVenezuelaVietnamWallis and FutunaWestern SaharaYemenZambiaZimbabwe
Варианты покупкиЭлектронная книга $138,00
Налог с продаж рассчитывается при оформлении заказа
Бесплатная доставка по всему миру
Нет минимального заказа
Описание
Эта книга является прекрасным дополнением к книге «Химическая термодинамика: принципы и приложения».
 Вместе они составляют полный справочный набор для практикующего ученого. Этот том расширяет круг тем и приложений до тех, которые обычно не рассматриваются в начальном тексте по термодинамике. В некотором смысле книга охватывает «золотую середину» между основными принципами, разработанными в учебнике по термодинамике для начинающих, и очень специализированными приложениями, которые являются частью продолжающегося исследовательского проекта. Таким образом, он может оказаться бесценным для практикующего ученого, которому необходимо применять термодинамические соотношения, чтобы помочь в понимании рассматриваемого химического процесса. Стиль письма в этом томе остается неформальным, но более техническим, чем в «Принципах и приложениях». Он начинается с главы 11, в которой резюмируются термодинамические соотношения, разработанные в предыдущем томе. Для тех, кто хочет или нуждается в более подробной информации, даны ссылки на разделы в «Принципах и приложениях», куда можно обратиться, чтобы узнать больше о разработке, ограничениях и условиях, в которых применяются эти уравнения.
Вместе они составляют полный справочный набор для практикующего ученого. Этот том расширяет круг тем и приложений до тех, которые обычно не рассматриваются в начальном тексте по термодинамике. В некотором смысле книга охватывает «золотую середину» между основными принципами, разработанными в учебнике по термодинамике для начинающих, и очень специализированными приложениями, которые являются частью продолжающегося исследовательского проекта. Таким образом, он может оказаться бесценным для практикующего ученого, которому необходимо применять термодинамические соотношения, чтобы помочь в понимании рассматриваемого химического процесса. Стиль письма в этом томе остается неформальным, но более техническим, чем в «Принципах и приложениях». Он начинается с главы 11, в которой резюмируются термодинамические соотношения, разработанные в предыдущем томе. Для тех, кто хочет или нуждается в более подробной информации, даны ссылки на разделы в «Принципах и приложениях», куда можно обратиться, чтобы узнать больше о разработке, ограничениях и условиях, в которых применяются эти уравнения. Это единственное место, где Advanced Applications связаны с предыдущим томом. Глава 11 может служить обзором фундаментальных термодинамических уравнений, которые необходимы для более сложных приложений, описанных в оставшейся части этой книги. Это может быть все, что необходимо практикующему ученому, который некоторое время не работал в этой области и нуждается в некотором обзоре. Оставшаяся часть этой книги применяет термодинамику для описания различных проблем. Затрагиваются темы, которые, вероятно, представляют наиболее фундаментальный и широкий интерес. На протяжении всей книги по возможности используются примеры «реальных» систем. Это контрастирует со многими книгами, где почти исключительно используются «общие» примеры. Включен полный набор ссылок на все источники данных и дополнительные источники для чтения. В конце каждой главы даны задачи. Это делает книгу идеально подходящей для использования в качестве учебника в углубленном курсе по химической термодинамике.
Это единственное место, где Advanced Applications связаны с предыдущим томом. Глава 11 может служить обзором фундаментальных термодинамических уравнений, которые необходимы для более сложных приложений, описанных в оставшейся части этой книги. Это может быть все, что необходимо практикующему ученому, который некоторое время не работал в этой области и нуждается в некотором обзоре. Оставшаяся часть этой книги применяет термодинамику для описания различных проблем. Затрагиваются темы, которые, вероятно, представляют наиболее фундаментальный и широкий интерес. На протяжении всей книги по возможности используются примеры «реальных» систем. Это контрастирует со многими книгами, где почти исключительно используются «общие» примеры. Включен полный набор ссылок на все источники данных и дополнительные источники для чтения. В конце каждой главы даны задачи. Это делает книгу идеально подходящей для использования в качестве учебника в углубленном курсе по химической термодинамике.Ключевые характеристики
- Отличный обзор термодинамических принципов и математических взаимосвязей со ссылками на соответствующие разделы в Принципы и приложения , где эти уравнения разработаны
- Применение термодинамики в самых разных химических процессах, включая фазовые равновесия , химическое равновесие, свойства смесей и химия поверхности
- Тематический подход для демонстрации применения термодинамики к биохимическим, геохимическим и промышленным процессам
- Приложения на «переднем крае» термодинамики
- Примеры и задачи для помощи в обучении
- Включает полный набор ссылок на все литературные источники специалисты в дисциплинах, где термодинамика имеет ключевое значение, таких как химия, физика, материаловедение, геология и биохимия.

Содержание
- Предисловие к двухтомной серии. Предисловие ко второму тому. Резюме термодинамических отношений. Термодинамика других переменных. Приложения термодинамики к изучению фазовых равновесий чистых веществ. Приложения термодинамики к изучению фазовых равновесий смесей. Приложения термодинамики к химическим процессам. Приложения термодинамики к биологическим процессам. Приложения термодинамики к растворам неэлектролитов. Приложения термодинамики к растворам, содержащим растворенные электролиты. ПРИЛОЖЕНИЕ 5: Термодинамические свойства некоторых химических веществ. ПРИЛОЖЕНИЕ 6: Расчеты по статистической термодинамике. ПРИЛОЖЕНИЕ 7: Коэффициенты для уравнений Питцера.
Подробная информация о продукте
- Компания. Страницы: 260
- Язык: английский
- Copyright: © Academic Press 2000
- Опубликовано: 16 июня 2000
- Imprint: Academic Press
- EBIB ISBN: 9780080808080111119999999999999999 1111119999999999999999999999
11119999991111199999999999111111991 год.
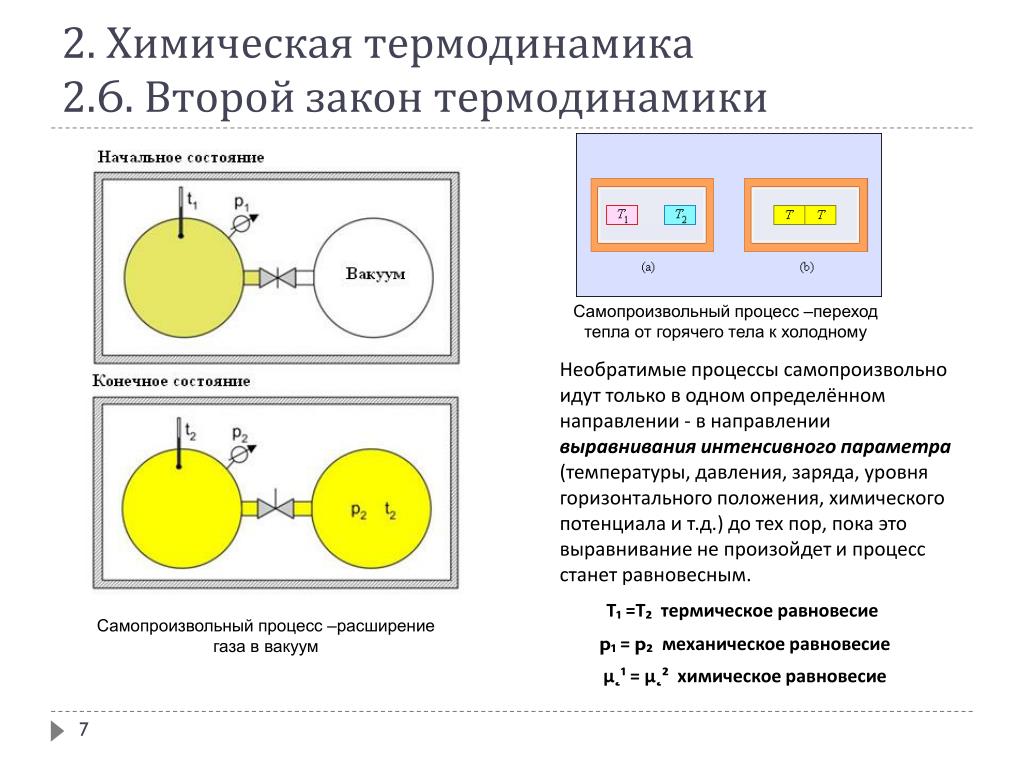 Об авторах
Об авторахДж. Отт
Дж. Беван Отт — почетный профессор химии имени Джозефа К. Николса, Университет Бригама Янга, США. Он провел 40 лет, преподавая термодинамику студентам и аспирантам, написал 120 статей в научной литературе, а также является автором и соавтором ряда книг. Профессор Отт получил крупные награды от Университета Бригама Янга, которые признают его достижения в преподавании и исследованиях, в том числе награду за выдающиеся преподавательские лекции, самую престижную награду, присуждаемую университетом.
Принадлежности и опыт
Университет Бригама Янга, Прово, Юта, США
Джулиана Боерио-Гоутс
Джулиана Боерио-Гоутс — профессор химии в Университете Бригама Янга, США. Она преподавала химическую термодинамику студентам и аспирантам в течение 18 лет и написала почти 50 публикаций в научной литературе. Профессор Боэрио-Гоатес входит в состав Консультативного совета журнала Journal of Chemical Thermodynamics и получила крупные награды за преподавание и исследования от Университета Бригама Янга, которые признают ее достижения и способности в обеих областях.


 3.1 Закон Гесса
3.1 Закон Гесса 7.2
7.2 7)
7) 14)
14) 17)
17)