Неорганическая химия для чайников. Эффективное самостоятельное изучение химии
Е.Н.ФРЕНКЕЛЬ
Пособие для тех, кто не знает, но хочет узнать и понять химию
Я, Френкель Евгения Николаевна, заслуженный работник высшей школы РФ, выпускница химического факультета МГУ 1972 г., педагогический стаж 34 года. Кроме того, я мать троих детей и бабушка четырех внуков, старший из которых школьник.
Меня волнует проблема школьных учебников. Главная беда многих из них – тяжелый язык, который требует дополнительного «перевода» на понятный школьнику язык изложения учебного материала. Ко мне часто обращаются ученики средней школы с такой просьбой: «Переведите текст учебника, чтобы понятно было». Поэтому я написала «Самоучитель по химии», в котором многие сложные вопросы изложены вполне доступно и в то же время научно. На основе этого «Самоучителя», который был написан в 1991 г.
, я разработала программу и содержание подготовительных курсов. На них обучались сотни школьников. Многие из них начинали с нуля и за 40 занятий понимали предмет настолько, что сдавали экзамены на «4» и «5». Поэтому в нашем городе мои пособия-самоучители расходятся как горячие пирожки. Может, и другим пригодятся мои наработки?
Статья подготовлена при поддержке учебного центра «МакарОФФ». Учебный центр предлагает Вам пройти курсы маникюра в Москве недорого . Профессиональная школа маникюра проводит обучение по маникюру, педикюру, наращиванию и дизайну ногтей, а также курсы мастеров-универсалов ногтевого сервиса, наращивание ресниц, микроблейдинг, шугаринг и эпиляция воском. Центр выдаёт дипломы после обучения и гарантированное трудоустройство. Подробная информация обо всех программах обучения, цены, расписание, акции и скидки, контакты на сайте: www.akademiyauspeha.ru .
Уважаемые читатели! Предлагаемый вашему
вниманию «Самоучитель по химии» – не обычный
учебник. В нем не просто излагаются какие-то
факты или описываются свойства веществ.
«Самоучитель» объясняет и учит даже в том случае,
если вы, к сожалению, не знаете и не понимаете
химии, а к учителю обратиться за разъяснениями не
можете или стесняетесь. В виде рукописи эта книга
используется школьниками с 1991 г., и не было ни
одного ученика, который бы провалился на
экзамене по химии и в школе, и в вузах. Причем
многие из них совсем не знали химии.
В нем не просто излагаются какие-то
факты или описываются свойства веществ.
«Самоучитель» объясняет и учит даже в том случае,
если вы, к сожалению, не знаете и не понимаете
химии, а к учителю обратиться за разъяснениями не
можете или стесняетесь. В виде рукописи эта книга
используется школьниками с 1991 г., и не было ни
одного ученика, который бы провалился на
экзамене по химии и в школе, и в вузах. Причем
многие из них совсем не знали химии.
«Самоучитель» рассчитан на самостоятельную работу ученика. Главное – отвечать по ходу чтения на те вопросы, которые встречаются в тексте. Если вы не смогли ответить на вопрос, то читайте внимательнее текст еще раз – все ответы имеются рядом. Желательно также выполнять все упражнения, которые встречаются по ходу объяснения нового материала. В этом помогут многочисленные обучающие алгоритмы, которые практически не встречаются в других учебниках. С их помощью вы научитесь:
Составлять химические формулы по валентности;
Составлять уравнения химических реакций, расставлять в них коэффициенты, в том числе в уравнениях окислительно-восстановительных процессов;
Составлять электронные формулы (в том числе краткие электронные формулы) атомов и определять свойства соответствующих химических элементов;
Предсказывать свойства
некоторых соединений и определять, возможен
данный процесс или нет.
В пособии два уровня сложности. Самоучитель первого уровня сложности состоит из трех частей.
I часть. Элементы общей химии (публикуемая ).
II часть. Элементы неорганической химии. III часть. Элементы органической химии.
Книг второго уровня сложности тоже три.
Теоретические основы общей химии.
Теоретические основы неорганической химии.
Теоретические основы органической химии.
Глава 1. Основные понятия химии.
Глава 2. Важнейшие классы неорганических соединений.
 И.Менделеева. И.Менделеева.
Глава 4. Понятие о химической связи. Глава 5. Растворы. Глава 6. Электролитическая диссоциация.
Глава 7. Понятие об окислительно-восстановительных реакциях. Глава 8. Расчеты по химическим формулам и уравнениям.
Приложение. |
Что такое химия? Где мы встречаемся с химическими явлениями?
Химия – везде. Сама жизнь – это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов.
Что изучает химия?
Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество?
Вещество – это то, из чего состоит окружающий нас мир и мы сами.
Что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество*. Изменились молекулы – изменилось вещество (оно стало другим), изменились его свойства. Например, свежее молоко стало кислым, зеленые листья стали желтыми, сырое мясо при обжаривании изменило запах.
Все эти изменения – следствие сложных и
многообразных химических процессов. Однако
признаки простых химических реакций, в
результате которых изменяется состав и строение
молекул, такие же: изменение цвета, вкуса или
запаха, выделение газа, света или тепла,
появление осадка.
Однако
признаки простых химических реакций, в
результате которых изменяется состав и строение
молекул, такие же: изменение цвета, вкуса или
запаха, выделение газа, света или тепла,
появление осадка.
Что же такое молекулы, изменение которых влечет за собой столь разнообразные проявления?
Молекулы – это мельчайшие частицы вещества, отражающие его качественный и количественный состав и его химические свойства.
Изучая состав и строение одной молекулы, можно предсказать многие свойства данного вещества в целом. Такие исследования – одна из главных задач химии.
Как устроены молекулы? Из чего они состоят?
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака). Например, Н – атом водорода, О – атом кислорода.
Число атомов в молекуле обозначают при помощи индекса – цифры внизу справа после символа.
Например:
Примеры молекул:
О 2 – это молекула вещества кислорода, состоящая из двух атомов кислорода;
Н 2 О – это молекула вещества воды,
состоящая из двух атомов водорода и одного атома
кислорода.
Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента – цифры перед символом:
Аналогично изображают число молекул:
2Н 2 – две молекулы водорода;
3Н 2 О – три молекулы воды.
Почему атомы водорода и кислорода имеют разные названия и разные символы? Потому что это атомы разных химических элементов.
Химический элемент – это вид атомов с одинаковым зарядом ядер.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях, из чего состоит атом?
Нейтральный атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:
В ходе химических реакций число электронов
любого атома может изменяться, а вот заряд ядра
атома не меняется . Поэтому заряд ядра
атома – своеобразный «паспорт» химического
элемента. Все атомы с зарядом ядра +1 принадлежат
химическому элементу под названием водород.
Атомы с зарядом ядра +8 относятся к химическому
элементу кислороду.
Все атомы с зарядом ядра +1 принадлежат
химическому элементу под названием водород.
Атомы с зарядом ядра +8 относятся к химическому
элементу кислороду.
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Д.И.Менделеева (порядковый номер равен заряду ядра атома), определенное название, а для некоторых химических элементов – особое прочтение символа в химической формуле (табл. 1).
Таблица 1
Символы (знаки) химических элементов
| № п/п | № в таблице Д.И.Менделеева | Символ | Прочтение в формуле | Название |
| 1 | 1 | H | аш | Водород |
| 2 | 6 | C | це | Углерод |
| 3 | 7 | N | эн | Азот |
| 4 | 8 | O | о | Кислород |
| 5 | 9 | F | фтор | Фтор |
| 6 | 11 | Na | натрий | Натрий |
| 7 | 12 | Mg | магний | Магний |
| 8 | 13 | Al | алюминий | Алюминий |
| 9 | 14 | Si | силициум | Кремний |
| 10 | 15 | P | пэ | Фосфор |
| 11 | 16 | S | эс | Сера |
| 12 | 17 | Cl | хлор | Хлор |
| 13 | 19 | K | калий | Калий |
| 14 | 20 | Ca | кальций | Кальций |
| 15 | 23 | V | ванадий | Ванадий |
| 16 | 24 | Cr | хром | Хром |
| 17 | 25 | Mn | марганец | Марганец |
| 18 | 26 | Fe | феррум | Железо |
| 19 | 29 | Cu | купрум | Медь |
| 20 | 30 | Zn | цинк | Цинк |
| 21 | 35 | Br | бром | Бром |
| 22 | 47 | Ag | аргентум | Серебро |
| 23 | 50 | Sn | станнум | Олово |
| 24 | 53 | I | йод | Йод |
| 25 | 56 | Ba | барий | Барий |
| 26 | 79 | Au | аурум | Золото |
| 27 | 80 | Hg | гидраргирум | Ртуть |
| 28 | 82 | Pb | плюмбум | Cвинец |
Вещества бывают простые и сложные . Если молекула состоит из атомов одного
химического элемента, это простое вещество. Простые
вещества – Са, Сl 2 , О 3 , S 8 и т. д.
Если молекула состоит из атомов одного
химического элемента, это простое вещество. Простые
вещества – Са, Сl 2 , О 3 , S 8 и т. д.
Молекулы сложных веществ состоят из атомов разных химических элементов. Сложные вещества – H 2 O, NO, H 3 PO 4, C 12 H 22 O 11 и т. д.
Задание 1.1. Укажите число атомов в молекулах сложных веществ H 2 O, NO, H 3 PO 4 , C 12 H 22 O 11 , назовите эти атомы.
Возникает вопрос: почему для воды всегда записывается формула Н 2 О, а не НО или НО 2 ? Опыт доказывает, что состав воды, полученной любым способом или взятой из любого источника, всегда соответствует формуле Н 2 О (речь идет о чистой воде).
Дело в том, что атомы в молекуле воды и в
молекуле любого другого вещества соединены при
помощи химических связей. Химическая связь
соединяет как минимум два атома. Поэтому, если
молекула состоит из двух атомов и один из них
образует три химические связи, то другой также
образует три химические связи.
Число химических связей , образуемых атомом, называют его валентностью .
Если обозначить каждую химическую связь черточкой, то для молекулы из двух атомов АБ получим АБ, где тремя черточками показаны три связи, образуемые элементами А и Б между собой.
В данной молекуле атомы А и Б трехвалентны.
Известно, что атом кислорода двухвалентен, атом водорода одновалентен.
В о п р о с. Сколько атомов водорода может присоединиться к одному атому кислорода?
О т в е т. Два атома. Состав воды описывают формулой Н–О–Н, или Н 2 О.
П о м н и т е! В устойчивой молекуле не может быть «свободных», «лишних» валентностей. Поэтому для двухэлементной молекулы число химических связей (валентностей) атомов одного элемента равно общему числу химических связей атомов другого элемента.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Таблица 2
Значение постоянных валентностей некоторых элементов
Для других атомов валентность** можно определить (вычислить)
из химической формулы вещества. При этом нужно
учитывать изложенное выше правило о химической
связи. Например, определим валентность x марганца Mn по формуле вещества MnO 2:
При этом нужно
учитывать изложенное выше правило о химической
связи. Например, определим валентность x марганца Mn по формуле вещества MnO 2:
Общее число химических связей, образуемых
одним и другим элементом (Mn и О), одинаково:
x · 1 = 4; II · 2 = 4. Отсюда х = 4, т.е. в этой
химической формуле марганец четырехвалентен.
П р а к т и ч е с к и е в ы в о д ы
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
4. В остальных случаях ставьте валентности «крест-накрест», т.е. валентность одного элемента равна индексу другого элемента:
Задание 1.2. Определите валентности элементов в соединениях:
CO 2 , CO, Mn 2 O 7 , Cl 2 O, P 2 O 3 ,
AlP, Na 2 S, NH 3 , Mg 3 N 2 .
П о д с к а з к а. Сначала укажите валентность атомов, у которых она постоянная. Аналогично определяется валентность атомных групп ОН, РО 4 , SО 4 и др.
Задание 1.3. Определите валентности атомных групп (в формулах подчеркнуты):
H 3 PO 4 , Ca(OH ) 2 , Ca 3 (PO 4) 2 , H 2 SO 4 , CuSO 4 .
(Обратите внимание! Одинаковые группы атомов имеют одинаковые валентности во всех соединениях.)
Зная валентности атома или группы атомов, можно составить формулу соединения. Для этого пользуются следующими правилами.
Если валентности атомов одинаковы, то и число атомов одинаково, т.е. индексы не ставим:
Если валентности кратны (обе делятся на одно и то же число), то число атомов элемента с меньшей валентностью определяем делением:
В остальных случаях индексы определяют «крест-накрест»:
Задание 1.4. Составьте химические формулы соединений:
Вещества, состав которых отражают химические
формулы, могут участвовать в химических
процессах (реакциях). Графическая запись,
соответствующая данной химической реакции,
называется уравнением реакции . Например, при
сгорании (взаимодействии с кислородом) угля
происходит химическая реакция:
Графическая запись,
соответствующая данной химической реакции,
называется уравнением реакции . Например, при
сгорании (взаимодействии с кислородом) угля
происходит химическая реакция:
С + O 2 = CO 2 .
Запись показывает, что один атом углерода С, соединяясь с одной молекулой кислорода O 2 , образует одну молекулу углекислого газа СО 2 . Число атомов каждого химического элемента до и после реакции должно быть одинаково . Это правило – следствие закона сохранения массы вещества. Закон сохранения массы: масса исходных веществ равна массе продуктов реакции.
Закон был открыт в XVIII в. М.В.Ломоносовым и, независимо от него, А.Л.Лавуазье.
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли KClO 3 получается соль KСl и кислород О 2:
KClO 3 KСl + О 2 .
Число атомов калия и хлора одинаково, а кислорода – разное. Уравняем их:
Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
Наконец, между правой и левой частями уравнения можно поставить знак равенства:
2KClO 3 = 2KСl + 3О 2 .
Полученная запись показывает, что при разложении сложного вещества KClO 3 получаются два новых вещества – сложное KСl и простое – кислород O 2 . Числа перед формулами веществ в уравнениях химических реакций называют коэффициентами .
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым. Составим уравнение реакции веществ CaCl 2 и Na 3 PO 4:
CaCl 2 + Na 3 PO 4 ……………… .
П о с л е д о в а т е л ь н о с т ь д е й с т в и й
1) Определим валентность исходных атомов и группы PO 4:
2) Напишем правую часть уравнения (пока без индексов, формулы веществ в скобках надо уточнить):
3) Составим химические формулы полученных веществ по валентностям составных частей:
4) Обратим внимание на состав самого сложного соединения Ca 3 (PO 4) 2 и уравняем число атомов кальция (их три) и число групп РО 4 (их две):
5) Число атомов натрия и хлора до реакции теперь
стало равным шести. Поставим соответствующий
коэффициент в правую часть схемы перед формулой
NaCl:
Поставим соответствующий
коэффициент в правую часть схемы перед формулой
NaCl:
3CaCl 2 + 2Na 3 PO 4 = Ca 3 (PO 4) 2 + 6NaCl.
Пользуясь такой последовательностью, можно уравнять схемы многих химических реакций (за исключением более сложных окислительно-восстановительных реакций, см. главу 7).
Типы химических реакций. Химические реакции бывают разных типов. Основными являются четыре типа – соединение, разложение, замещение и обмен.
1. Реакции соединения – из двух и более веществ образуется одно вещество:
Например:
Са + Сl 2 = CaCl 2 .
2. Реакции разложения – из одного вещества получаются два вещества или более:
Например:
Ca(HCO 3) 2 CaCO 3 + CO 2 + H 2 O.
3. Реакции замещения – реагируют простое и сложное вещества, образуются также простое и сложное вещества, причем простое вещество замещает часть атомов сложного вещества:
А + ВХ АХ + В.
Например:
Fe + CuSO 4 = Cu + FeSO 4 .
4. Реакции обмена – здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
Упражнения к главе 1
1. Выучите табл. 1. Проверьте себя, напишите химические символы: серы, цинка, олова, магния, марганца, калия, кальция, свинца, железа и фтора.
2. Напишите символы химических элементов, которые в формулах произносятся как: «аш», «о», «купрум», «эс», «пэ», «гидраргирум», «станнум», «плюмбум», «эн», «феррум», «це», «аргентум». Назовите эти элементы.
3. Укажите число атомов каждого химического элемента в формулах соединений:
Al 2 S 3 , СаS, МnО 2 , NH 3 , Mg 3 P 2 , SO 3 .
4. Определите, какие из веществ – простые, а какие – сложные:
Na 2 O, Na, O 2 , CaCl 2 , Cl 2 .
Прочитайте формулы этих веществ.
5. Выучите табл. 2. Составьте химические формулы веществ по известной валентности элементов и атомных групп:
6. Определите валентность химических
элементов в соединениях:
Определите валентность химических
элементов в соединениях:
N 2 O, Fe 2 O 3 , PbO 2 , N 2 O 5, HBr, SiH 4 , H 2 S, MnO, Al 2 S 3 .
7. Расставьте коэффициенты и укажите типы химических реакций:
а) Mg + O 2 MgO;
б) Al + CuCl 2 AlCl 3 + Cu;
в) NaNO 3 NaNO 2 + O 2 ;
г) AgNO 3 + BaCl 2 AgCl + Ba(NO 3) 2 ;
д) Al + HCl AlCl 3 + H 2 ;
е) KOH + H 3 PO 4 K 3 PO 4 + H 2 O;
ж) CH 4 C 2 H 2 + H 2 .
* Существуют вещества, построенные не из молекул. Но об этих веществах речь пойдет позже (см. главу 4).
** Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. главу 7). Однако во многих соединениях числовые значения этих понятий совпадают, поэтому по формуле вещества можно определять и валентность.
Печатается с продолжением
Все книги можно скачать бесплатно и без регистрации.
NEW.
В.Н. Верховский, Я.Л. Гольдфарб, Л. М. Сморгонский. Органическая химия. Учебник для 10 класса. 1946 год. 156 стр. djvu. 19.2 Мб.
М. Сморгонский. Органическая химия. Учебник для 10 класса. 1946 год. 156 стр. djvu. 19.2 Мб.
Этот учебник написан практиками и рассчитан на то, что дети будут понимать химию, а не вызубривать различные правила-скороговорки.
Объем изложенного материала значительно превышает таковой для учебника Цветкова. Очень рекомендую книгу, особенно учителям.
Сопоставление данной книги с современными учебниками четко показывает тенденции современных учебников:
учебники пишутся все более абстрактными и скупыми на материал и все более оторванными от практики.
Скачать.
NEW.
Никольский А.Б., Суворов А.В. Химия. 2001 год. 512 стр. djvu. 4.1 Мб.
В учебнике нового типа, рассчитанном прежде всего на формирование химического мышления студентов, системно и точно и в то же время ясно и доступно изложен огромный объем современных общехимических знаний.
На современном уровне рассмотрено учение о химическом процессе с акцентом на механизм реакции. Прослежена взаимосвязь между электронным строением и химическим поведением веществ. Логичность и популярность изложения материала, оригинальность контрольных вопросов, доступность иллюстраций способствуют усвоению химических знаний и развитию научного мышления.
Логичность и популярность изложения материала, оригинальность контрольных вопросов, доступность иллюстраций способствуют усвоению химических знаний и развитию научного мышления.
Предназначен студентам вузов, учащимся средних специальных учебных заведений, будет полезен преподавателям вузов и учителям школ. Полезно посмотреть и школьникам, неЕГЭотикам, хотя бы первые главы.
Скачать.
Алексинский В.Н. Занимательные опыты по химии. 2-е испр. изд. 1995 год. 95 стр. djvu. 1.9 Мб.
Книга для учитилей.
В книге рассмотрены опыты, которые можно использовать не только на внеклассных мероприятиях, но и при подготовке к урокам. Опыты, обладая элементом развлекательности, способствуют развитию у учащихся умения наблюдать и объяснять химические явления. Пособие окажет помощь учителям в воспитании у учащихся интереса к изучению химии, в выработке более глубокого и сознательного усвоения ими теоретического материала.
Скачать.
Т.М. Варламова, А.И. Кракова. ОБЩАЯ И НЕОРГАНИЧЕСКАЯ ХИМИЯ: БАЗОВЫЙ КУРС. 263 стр. djvu. 2.2 Мб.
263 стр. djvu. 2.2 Мб.
В данном пособии изложены основные вопросы общей и неорганической химии, многие из которых вызывают трудности у учащихся и абитуриентов. Подробно рассмотрены типовые задачи по всем разделам школьного курса химии и предложены задания для самостоятельного решения.
Пособие предназначено слушателям подготовительных отделений при высших учебных заведениях, а также лицам, готовящимся для поступления в вузы самостоятельно, учащимся старших классов средних школ, лицеев, гимназий и колледжей.
Скачать.
Габриелян О.С., Маскаев Ф.Н., Теренин В.И. Химия 10 класс. Учебник.2002 год. 304 стр. djvu. 3.9 Мб.
Книга для учитилей.
Учебник продолжает и развивает курс химии, изложенный в учебниках “Химия-8” и “Химия-9” автора О.С.Габриеляна. Учебный материал по органической химии излагается с учетом того, что первоначальные сведения об органических веществах учащиеся получили в 9 классе. Учебник соответствует обязательному минимуму содержания образования. Материал учебника распределен по двум уровням – базисному и углубленному и дается в связи с экологией, медициной, биологией. В курсе приводятся сведения о жизненно важных веществах: витаминах, ферментах, гормонах, лекарствах. Широко представлен химический эксперимент, в том числе новые практические работы, в ходе которых рассматриваются свойства витаминов, ферментов, лекарственных препаратов.
В курсе приводятся сведения о жизненно важных веществах: витаминах, ферментах, гормонах, лекарствах. Широко представлен химический эксперимент, в том числе новые практические работы, в ходе которых рассматриваются свойства витаминов, ферментов, лекарственных препаратов.
Скачать.
П.А. Гуревич, М.А. Кубешов. Органическая химия. Полезные сведения для школьников и учителей – история, теория, задачи и решения. 2004 год. 350 стр. djvu. 4.6 Мб.
Скачать.
Егоров А.С. ред. Репетитор по химии. 2003 год. 770 стр. PDF. 16.3 Мб.
Пособие содержит подробное изложение основ общей, неорганической и органической химии, а также типовые задачи с решениями и большое число заданий разной степени сложности для самостоятельной работы (в том числе элективные тесты).
Рекомендуется учащимся школ, гимназий и лицеев, абитуриентам химических и медико-биологических вузов.
Скачать.
Кузьменко Н.Е., Еремин В.В., Попков В.А. Начала химии. Современный курс для поступающих в вузы. В 2-х томах. 7-е изд. перераб. доп. 2002 год. 384+384 стр. djvu. в одном архиве 16.9 Мб.
В 2-х томах. 7-е изд. перераб. доп. 2002 год. 384+384 стр. djvu. в одном архиве 16.9 Мб.
Книга представляет собой попытку современного, всеобъемлющего и систематического изложения основ химии, которые необходимо знать в первую очередь поступающим в вузы. Ее содержание основано на тщательном анализе программ вступительных экзаменов по химии большинства вузов (химических, медицинских, биологических и т.д.), а также конкретных экзаменационных заданий.
Пособие предназначено для школьников, абитуриентов и учителей. В пособии изложены основы современной химии, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом – химиком, медиком или биологом XXI века. В новом издании отражены последние достижения химии и приведены новые задачи вступительных экзаменов.
Скачать.
Н.Е. Кузьменко и др. Начала химии. Современный курс для поступающих в вузы. 2001 год. 360 стр. djvu. 16.3 Мб.
Скачать.
Кузьменко и др. Химия. Для школьнико старших классов и поступающих в вузы. Пособие представляет собой учебник и справочник по химии. 525 стр. Размер 4.7 Мб. djvu.
Химия. Для школьнико старших классов и поступающих в вузы. Пособие представляет собой учебник и справочник по химии. 525 стр. Размер 4.7 Мб. djvu.
Скачать.
Кузьменко, Еремин, Попков. Краткий курс химии. Для поступающих в ВУЗы. 2002 год. 410 стр. PDF. Размер 12.4 Мб.
Пособие предназначено для школьников, абитуриентов и учителей. В пособии в краткой, но информативной и ясной форме изложены современные основы химии. Это – основы, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом-химиком, медиком или биологом XXI века.
В тех частях: 1. Теоретическая химия, 2. Неорганическая химя. 3. Органическая химия.
Скачать
Т.Н. Литвинова, Е.Д. Мельникова, М.В. Соловьёва, Л.Т. Ажипа, Н.К. Выскубова. Химия в задачах для поступающих в вузы. 2009 год. 832 стр. PDF. 4.7 Мб.
Сборник содержит более 2500 задач, охватывающих основные темы школьного курса химии. Среди них представлены качественные и расчетные типовые задачи с решениями и задачи разного уровня сложности для самостоятельного решения. Ко всем задачам даны ответы, а к наиболее трудным – подробные решения.
Ко всем задачам даны ответы, а к наиболее трудным – подробные решения.
По каждой теме приведен теоретический материал, преимущественно в виде таблиц, – основные понятия, законы химии, формулы, классификации, свойства, способы получения неорганических и органических веществ.
Пособие поможет при подготовке к выпускным экзаменам в средней школе, сдаче ЕГЭ и вступительным экзаменам в вуз. Книга адресована школьникам старших классов, абитуриентам и преподавателям.
Скачать.
Некрашевич И. Химия. 8 – 11 классы. 2008 год. 304 стр. PDF. 1.7 Мб.
Химия кажется вам сложным и непонятным предметом? Вы не знаете, как решать химические задачи, составлять уравнения реакций, строить формулы?
Репетитор по химии, который вы держите в руках, поможет решить эти проблемы.
Скачать.
Г.К. Прохорова. Качественный химический анализ. Практикум для школьников. 2002 год. 33 стр. PDF. в общем архиве 424 Кб.
Практикум предназначен для учащихся 9 классов школ с углубленным
изучением химии и школы юных химиков для ознакомления их с основами аналитической химии.
Подготовлен на Химфаке МГУ.
Скачать.
Рудзитис Г.Е., Фельдман Ф.Г. Химия. 7-11 класс. В 2-х книгах. 1985 год. djvu. две книги в одном архиве. 12.3 Мб.
Книга 1. 204 стр. Учебное пособие для 7-11 классов вечерней (сменной) средней общеобразовательной школы. Учебник соответствует действующим школьным программам и обязательному минимуму химического образования. Он имеет классическую структуру школьного учебника по химии и включает весь необходимый теоретический и практический материал для изучения курса неорганической химии.
Книга 1. 306 стр. Учебное пособие для 7-11 классов вечерней (сменной) средней общеобразовательной школы. Учебник соответствует действующим школьным программам и обязательному минимуму химического образования. Он имеет классическую структуру школьного учебника по химии и включает весь необходимый теоретический и практический материал для изучения курса неорганической органической химии. Во второй книге органическая химия занимает половину его объема. Материал дифференцирован по уровням сложности.
Материал дифференцирован по уровням сложности.
Многочисленные таблицы, схемы и рисунки способствуют усвоению и повторению теоретического и практического материала. Доступность и наглядность изложения основных понятий, определений и законов химии позволяют рекомендовать этот учебник не только для школьного обучения, но и для самообразования.
При изучении химии с нуля лучше пользоваться этим учебником, а не современными, так как он лучше и понятней. Это не мое мнение, а химика-профессионала.
Скачать.
Семенов. Химия: пособие для поступающих в вузы. 1989 год. 225 стр. djvu. 3.7 Мб.
В отличие от существующих в данном пособии сделан упор на углубленное повторение основных понятий и законов химии, «узловых» вопросов, от понимания которых зависит осмысление изучаемого в школе фактического материала. На небольшом числе примеров показаны главные закономерности поведения химических систем, общие приемы подхода к их рассмотрению, то, как свойства вещества определяют его применение. Приводимые вопросы и упражнения выбраны из тех, которые предлагались на вступительных экзаменах в химические вузы или использовались автором на Подготовительном отделении ЛГУ. Как правило, для ответа не нужны громоздкие расчет и – надо лишь хорошо усвоить основные законы химии.
Приводимые вопросы и упражнения выбраны из тех, которые предлагались на вступительных экзаменах в химические вузы или использовались автором на Подготовительном отделении ЛГУ. Как правило, для ответа не нужны громоздкие расчет и – надо лишь хорошо усвоить основные законы химии.
Предназначено прежде всего для абитуриентов, самостоятельно готовящихся к экзамену в вуз, но будет полезно также слушателям подготовительных отделений и курсов.
Скачать.
Стахеев. Вся химия в 50 таблицах. Приведены все основные понятия ШКОЛЬНОЙ хими. Представляет собой этакую шпаргалку – напоминалку. 60 стр. Размер 1.2 Мб. djvu.
Скачать.
Хомченко Г.П. Пособие по химии для поступающих в вузы. 2002 год. 480 стр. PDF. Размер 11.6 Мб.
В пособии освещены все вопросы приемных экзаменов по химии. Для лучшего усвоения курса химии приведены некоторые дополнительные сведения. В конце каждой главы даются типовые задачи с решениями и задачи для самостоятельной работы.
Книга предназначена поступающим в вузы. Она также может быть рекомендована преподавателям химии при подготовке учащихся к сдаче выпускных экзаменов за курс средней школы. Мне пособие понравилось.
Она также может быть рекомендована преподавателям химии при подготовке учащихся к сдаче выпускных экзаменов за курс средней школы. Мне пособие понравилось.
Скачать
Черникова Л.П. Шпаргалки по химии. 2003 год. 144 стр. PDF. 2.4 Мб.
Материал разбит на три темы: Основные понятия хими, Общая химия, Органическая химия. Нормальное пособие. Не понял зачем такое название.
Всем известно, что школьный курс является той основой, которая дает самые необходимые знания о мире, в котором мы живем. Это действительно так и такой предмет как химия прекрасное тому подтверждение, так как, по сути, абсолютно все, что нас окружает и есть химия — химические элементы, их соединения, процессы взаимодействия и т.д. Поэтому неудивительно, что в школьный курс входит много тем по химии .
Важность изучения химииИзучая предмет химии, школьник не только познает мир и определенные законы его существования, но и развивает память, логическое и абстрактное мышление, аналитические способности и интеллектуальные возможности в целом. ЕГЭ по химии, который является предметом по выбору, есть ни что иное как закономерное подведение итогов учебно-образовательной деятельности.
ЕГЭ по химии, который является предметом по выбору, есть ни что иное как закономерное подведение итогов учебно-образовательной деятельности.
Кроме того, успешная сдача ЕГЭ по химии после окончания школы облегчит получение высшего образования, ведь его результаты высшими учебными заведениями засчитываются как вступительные экзамены. Поэтому нужно относиться к этому экзамену как к важному этапу в вашем будущем. Благодаря полученным знаниям будет проще потом осваивать другие сложные предметы в университете.
Что представляет собой подготовка к ЕГЭ по химииКонечно, залогом успешного изучения и усвоения материала является постоянная работа — это касается абсолютно всех предметов. Однако такой специфический предмет как химия, зачастую требует особого подхода и применения дополнительных методов обучения. Например, таковыми являются самостоятельная работа или систематические занятия с репетитором. Но что делать, когда возможности для дополнительных занятий с преподавателем нет, а некоторые разобрать по учебнику практически не реально, впрочем, как и систематизировать все полученные знания, когда это необходимо для подготовки к ЕГЭ по химии?
Сегодня существует прекрасная возможность для дополнительного образования, расширения, углубления знаний и закрепления пройденных материалов — химия онлайн бесплатно. Такие уроки основаны на многолетнем педагогическо-психологическом опыте. Всемирная сеть в этом случае становится надежным другом и помощником современной молодежи, предлагая изучение различных тем по химии, включая различные методы подачи материала — видеоуроки с пояснениями, примерами опытов, решением практических задач и многое другое, систематизированные оптимальным образом электронные конспекты и таблицы.
Такие уроки основаны на многолетнем педагогическо-психологическом опыте. Всемирная сеть в этом случае становится надежным другом и помощником современной молодежи, предлагая изучение различных тем по химии, включая различные методы подачи материала — видеоуроки с пояснениями, примерами опытов, решением практических задач и многое другое, систематизированные оптимальным образом электронные конспекты и таблицы.
Эта наука столь сложна, сколь и интересна. Однако уроки химии онлайн позволяют наиболее эффективно усвоить даже самую сложную тему, а при необходимости — проконсультироваться с квалифицированным преподавателем, в том числе и по вопросам, касающимся ЕГЭ по химии. Все это делает обучение легким и понятным, каждый может избежать сложных вопросов, разобраться в темах, которые пропустил ранее.
ИтогоЗанимаясь химией онлайн и бесплатно , вы в доступной для усвоения форме перенимаете многолетний опыт и получаете багаж систематизированных знаний. Каждый может выбрать для себя различные режимы и варианты обучения. Выпускники могут повторять пройденный в школе материал и восполнять имеющиеся пробелы в знаниях, выполняя задания различной сложности и изучая темы по химии по той системе, на которой и основан ЕГЭ. Конечно, готовых ответов никто не предоставит, тем более что каждый год список вопросов и заданий меняется. Однако структура в основном остается прежней, позволяя разработчикам совершенствовать эффективность оценки, а учащимся — наиболее полно раскрывать свой потенциал. Возможно, это поможет и школам показывать лучшую успеваемость своих учеников.
Выпускники могут повторять пройденный в школе материал и восполнять имеющиеся пробелы в знаниях, выполняя задания различной сложности и изучая темы по химии по той системе, на которой и основан ЕГЭ. Конечно, готовых ответов никто не предоставит, тем более что каждый год список вопросов и заданий меняется. Однако структура в основном остается прежней, позволяя разработчикам совершенствовать эффективность оценки, а учащимся — наиболее полно раскрывать свой потенциал. Возможно, это поможет и школам показывать лучшую успеваемость своих учеников.
Кроме того, уроки химии онлайн — это удобно, а также может пригодиться как практикующим преподавателям для перенятия опыта, так и родителям, для того чтобы быть в курсе того, как сегодня строится процесс обучения их детей. Занятия химией онлайн помогут освежить знания будущим абитуриентам, желающим получить еще одно образование. Поэтому трудно поспорить с тем, что благодаря возможностям Интернета учиться становится проще абсолютно всем.
Химия считается одним из самых сложных и трудных предметов. Причем сложности возникают в освоении этого предмета и у школьников, и у студентов. Почему? Школьники ожидают от урока фокусов, интересных опытов и демонстраций. Но уже после первых занятий разочаровываются: лабораторных работ с реактивами совсем не много, в основном приходится изучать новую терминологию, делать объемные домашние задания. Химический язык совершенно не похож на повседневный, поэтому нужно ускоренными темпами изучать термины и названия. Кроме того, нужно уметь логически мыслить и применять математические знания.
Причем сложности возникают в освоении этого предмета и у школьников, и у студентов. Почему? Школьники ожидают от урока фокусов, интересных опытов и демонстраций. Но уже после первых занятий разочаровываются: лабораторных работ с реактивами совсем не много, в основном приходится изучать новую терминологию, делать объемные домашние задания. Химический язык совершенно не похож на повседневный, поэтому нужно ускоренными темпами изучать термины и названия. Кроме того, нужно уметь логически мыслить и применять математические знания.
Можно ли выучить химию самостоятельно?
Ничего невозможного нет. Несмотря на сложность науки, химию можно выучить с нуля. В ряде случаев, когда тема особенно сложная или требует дополнительных знаний, можно воспользоваться услугами онлайн репетитора. Самый удобный способ обучения – с помощью репетиторов по химии по скайпу . Дистанционное обучение позволяет подробно изучить отдельную тему или уточнить сложные моменты. По скайпу можно в любое время связаться с квалифицированным преподавателем.
Для того чтобы процесс изучения был эффективным, нужно несколько факторов:
- Мотивация . В любом деле необходима цель, к которой стремятся. Не важно, для чего изучается химия – для поступления в мединститут или биологический факультет, просто для саморазвития. Главное, поставить цель и определить способ ее достижения. Мотивация будет основным движущим фактором, который заставит продолжать самообучение.
- Важность деталей . За короткое время выучить большой объем информации просто невозможно. Чтобы выучить химию эффективно и уметь правильно использовать знания, нужно уделять внимание деталям: формулам, решать большое количество примеров, задач. Для качественного усвоения материала требуется систематизация информации: самостоятельно изучают новую тему, в дополнение решают задачи и примеры, учат формулы и т.д.
- Проверка знаний
. Для закрепления пройденного материала рекомендуется периодически делать проверочные работы. Умение понимать и логически анализировать позволяет усваивать знания лучше, чем «зубрежка».
 Преподаватели рекомендуют периодически делать себе зачеты и контрольные работы. Не лишним будут повторения пройденного материала. Самостоятельно выучить химию помогают решебники и самоучители.
Преподаватели рекомендуют периодически делать себе зачеты и контрольные работы. Не лишним будут повторения пройденного материала. Самостоятельно выучить химию помогают решебники и самоучители. - Практика и еще раз практика… Не достаточно хорошо владеть теоретическими знаниями, нужно их уметь применять на практике, во время решения задач. Практические занятия помогают выявить слабые места в знаниях и закрепить пройденный материал. Кроме того, развиваются аналитические способности и логическое построение цепочки решения. Во время решения примеров и задач вы делаете выводы и происходит систематизация полученных знаний. Когда задачи становятся абсолютно понятными, можно приступать к изучению следующей темы.
- Учите сами . Не уверены в полноценном освоении химии? Попробуйте обучить этому предмету кого-нибудь. Во время объяснения материала выявляются слабые места в знаниях, выстраивается системность. Важно не торопиться, уделяя внимание деталям и практическим моментам.
Выучить химию самостоятельно с нулевого уровня можно, если есть сильная мотивация и время. Если же материал сложный, разобраться в премудростях темы помогут профессиональные репетиторы. Будет ли это очное консультирование или с помощью скайпа – зависит только от вас. Не обязательно брать полный курс у репетитора, в ряде случаев можно взять урок по отдельной теме.
Если же материал сложный, разобраться в премудростях темы помогут профессиональные репетиторы. Будет ли это очное консультирование или с помощью скайпа – зависит только от вас. Не обязательно брать полный курс у репетитора, в ряде случаев можно взять урок по отдельной теме.
Глава 1.
Общие химические и экологические закономерности.
С чего начинается химия?
Cложный ли это вопрос? На него каждый ответит по-своему.
В середней школе учащиеся изучают химию в течение ряда лет. Многие довольно хорошо сдают выпускной экзамен по химии. Однако…
Беседы с абитуриентами и затем и студентами первых курсов говорят о том, что остаточные знания по химии после средней школы незначительные. Одни путаются в различных определениях и химических формулах, а другие вообще не могут воспроизвести даже основные понятия и законы химии, не говоря уже о понятиях и законах экологии.
У них химия так и не начиналась.
Химия, по-видимому, начинается с глубокого освоения ее основ, и прежде всего, основных понятий и законов.
1.1. Основные химические понятия.
В таблице Д.И.Менделеева рядом с символом элемента стоят цифры. Одна цифра обозначает порядковый номер элемента, а вторая атомную массу. Порядковый номер имеет свой физический смысл. О нем мы будем вести разговор позже, здесь остановимся на атомной массе и выделим в каких единицах она измеряется.
Следует сразу оговориться, что атомная масса элемента, приведенная в таблице, величина относительная. За единицу относительной величины атомной массы принята 1/12 часть массы атома углерода, изотопа с массовым числом 12, и назвали ее атомной единицей массы /а.е.м./. Следовательно, 1 а.е.м. равна 1/12 части массы изотопа углерода 12 С. И она равна 1,667*10 –27 кг. /Абсолютная масса атома углерода равна 1,99*10 –26 кг./
Атомная масса , приведенная в таблице, является массой атома, выраженной в атомных единицах массы. Величина безразмерная. Конкретно для каждого элемента атомная масса показывает, во сколько раз масса данного атома больше или меньше 1/12 части массы атома углерода.
Аналогичное можно сказать и о молекулярной массе.
Молекулярная масса – это масса молекулы, выраженная в атомных единицах массы. Величина тоже относительная. Молекулярная масса конкретного вещества равна сумме масс атомов всех элементов, входящих в состав молекулы.
Важным понятием химии является понятие «моль». Моль – такое количество вещества, которое содержит 6,02*10 23 структурных единиц /атомов, молекул, ионов, электронов и т.д./. Моль атомов, моль молекул, моль ионов и т.д.
Масса одного моля данного вещества называется его молярной /или мольной/ массой. Она измеряется в г/моль или кг/моль и обозначается буквой «М». Например, молярная масса серной кислоты М Н 2 SO4 =98г/моль.
Следующее понятие «Эквивалент». Эквивалентом /Э/ называют такое весовое количество вещества, которое взаимодействует с одним молем атомов водорода или замещают такое его количество в химических реакциях. Следовательно, эквивалент водорода Э Н
равен единице. /Э Н
=1/. Эквивалент кислорода Э О
равен восьми /Э О
=8/.
Различают химический эквивалент элемента и химический эквивалент сложного вещества.
Эквивалент элемента – величина переменная. Она зависит от атомной массы /А/ и валентности /В/, которую элемент имеет в конкретном соединении. Э=А/В. Например, определим эквивалент серы в оксидах SO 2 и SO 3 . В SO 2 Э S =32/4=8, а в SO 3 Э S =32/6=5,33.
Молярную массу эквивалента, выраженную в граммах, называют эквивалентной массой. Следовательно, эквивалентная масса водорода МЭ Н =1г/моль, эквивалентная масса кислорода МЭ О =8г/моль.
Химический эквивалент сложного вещества /кислоты, гидроксида, соли, оксида/– такое количество соответствующего вещества, которое взаимодействует с одним молем атомов водорода, т.е. с одним эквивалентом водорода или замещает такое количество водорода или любого другого вещества в химических реакциях.
Эквивалент кислоты /Э К
/ равен частному от деления молекулярной массы кислоты на число атомов водорода, участвующих в реакции. Для кислоты H 2
SO 4
, когда оба атома водорода вступают в реакцию H 2
SO 4
+2NaOH=Na 2
SO+2H 2
O эквивалент будет равен Э Н
2
SO4
= М Н
2
SO
4
/n Н
=98/2=49
Для кислоты H 2
SO 4
, когда оба атома водорода вступают в реакцию H 2
SO 4
+2NaOH=Na 2
SO+2H 2
O эквивалент будет равен Э Н
2
SO4
= М Н
2
SO
4
/n Н
=98/2=49
Эквивалент гидроксида /Э гидр. / определяется как частное от деления молекулярной массы гидроксида на число гидроксогрупп, вступающих в реакцию. Например, эквивалент NaOH будет равен: Э NaOH =М NaOH /n ОН =40/1=40.
Эквивалент соли /Э соли / можно рассчитать, поделив ее молекулярную массу на произведение числа атомов металла, вступающих в реакцию, и их валентность. Так, эквивалент соли Al 2 (SO 4) 3 будет равен Э Al 2 (SO 4) 3 =М Al 2 (SO 4) 3 /6=342/2,3=342/6=57.
Эквивалент оксида /Э ок / можно определить, как сумму эквивалентов соответствующих элемента и кислорода. Например, эквивалент СО 2 будет равен сумме эквивалентов углерода и кислорода: Э СО 2 =Э С +Э О =3+8=7.
Для газообразных веществ удобно пользоваться эквивалентными объемами /Э V
/. Так как при нормальных условиях моль газа занимает объем 22,4л, то исходя из этой величины, легко определить эквивалентный объем любого газа. Рассмотрим водород. Мольная масса водорода 2г занимает объем 22,4л, тогда его эквивалентная масса 1г занимает объем 11,2л /или 11200мл /. Следовательно Э V
Н
=11,2л. Эквивалентный объем хлора равен 11,2л /Э VCl
=11,2л/. Эквивалентный объем СО равен 3,56 /Э VC
О
=3,56л/.
Рассмотрим водород. Мольная масса водорода 2г занимает объем 22,4л, тогда его эквивалентная масса 1г занимает объем 11,2л /или 11200мл /. Следовательно Э V
Н
=11,2л. Эквивалентный объем хлора равен 11,2л /Э VCl
=11,2л/. Эквивалентный объем СО равен 3,56 /Э VC
О
=3,56л/.
Химический эквивалент элемента или сложного вещества используется в стехиометрических расчетах обменных реакций, а в соответствующих расчетах окислительно–восстановительных реакций применяют уже окислительный и восстановительный эквиваленты.
Окислительный эквивалент определяют как частное от деления молекулярной массы окислителя на число электронов, которое он принимает в данной окислително–восстановительной реакции.
Восстановительный эквивалент равен молекулярной массе восстановителя поделенной на число электронов, которое он отдает в данной реакции.
Напишем окислително–восстановительную реакцию и определим эквивалент окислителя и восстановителя:
5N 2 aS+2KMnO 4 +8H 2 SO 4 =S+2MnSO 4 +K 2 SO 4 +5Na 2 SO 4 +8H 2 O
Окислителем в этой реакции является перманганат калия. Эквивалент окислителя будет равен массе KMnO 4
деленной на число электронов, принятых окислителем в реакции (nе=5). Э KMnO
4
=М KMnO
4
/nе=158/5=31,5. Молярная масса эквивалента окислителя KMnO 4
в кислой среде равна 31,5г/моль.
Эквивалент окислителя будет равен массе KMnO 4
деленной на число электронов, принятых окислителем в реакции (nе=5). Э KMnO
4
=М KMnO
4
/nе=158/5=31,5. Молярная масса эквивалента окислителя KMnO 4
в кислой среде равна 31,5г/моль.
Эквивалент восстановителя Na 2 S будет: Э Na 4 S =М Na 4 S /nе=78/2=39. Молярная масса эквивалента Na 2 S равна 39г/моль.
В электрохимических процессах, в частности при электролизе веществ, пользуются электрохимическим эквивалентом. Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Валентность . При взаимодействии атомов между ними образуется химическая связь. Каждый атом может образовывать только определенное количество связей. Количество связей предопределяет такое уникальное свойство каждого элемента, которое называют валентностью. В наиболее общем виде валентностью называют способность атома образовывать химическую связь. За единицу валентности принимают одну химическую связь, которую способен образовать атом водорода. В связи с этим, водород является одновалентным элементом, а кислород – двухвалентным, т.к. с атомом кислорода могут образовывать связь не более двух водородов.
За единицу валентности принимают одну химическую связь, которую способен образовать атом водорода. В связи с этим, водород является одновалентным элементом, а кислород – двухвалентным, т.к. с атомом кислорода могут образовывать связь не более двух водородов.
Умение определять валентность каждого элемента, в том числе и в химическом соединении, является необходимым условием успешного усвоения курса химии.
С валентностью соприкасается и такое понятие химии как степень окисления . Подстепенью окисления понимают тот заряд, который имеет элемент в ионном соединении или имел бы в ковалентном соединении, если бы общая электронная пара бала бы полностью смещена к более электроотрицательному элементу. Степень окисления имеет не только цифровое выражение, но и соответствующий знак заряда (+) или (–). Валентность не имеет этих знаков. Например, в H 2 SO 4 степень окисления: водорода +1, кислорода –2, серы +6, а валентность, соответственно, будет 1, 2, 6.
Валентность и степень окисления в числовых значениях не всегда совпадают по величине. Например, в молекуле этилового спирта СН 3
–СН 2
–ОН валентность углерода 6, водорода 1, кислорода 2, а степень окисления, например, углерода первого –3, второго –1: –3
СН 3
– –1
СН 2
–ОН.
Например, в молекуле этилового спирта СН 3
–СН 2
–ОН валентность углерода 6, водорода 1, кислорода 2, а степень окисления, например, углерода первого –3, второго –1: –3
СН 3
– –1
СН 2
–ОН.
1.2. Основные экологические понятия.
За последнее время понятие “экология” глубоко входит в наше сознание. Это понятие, введенное еще в 1869г Э.Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
В учебниках биологии экологию определяют как науку о взаимоотношениях живых организмов и среды их обитания. Практически созвучное определение экологии дает Б.Небел в своей книге «Наука об окружающей среде» – Экология – наука о различных аспектах взаимодействия организмов между собой и с окружающей средой. В других источниках можно встретить и более широкое толкование. Например, Экология – 1/. Наука, изучающая отношение организмов и их системных совокупностей и окружающей среды; 2/. Совокупность научных дисциплин, исследующих взаимоотношение системных биологических структур /от макромолекул до биосферы/ между собой и с окружающей средой; 3/. Дисциплина, изучающая общие законы функционирования экосистем различного иерархического уровня; 4/. Комплексная наука, исследующая среду обитания живых организмов; 5/. Исследование положения человека как вида в биосфере планеты, его связей с экологическими системами и воздействие на них; 6/. Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
Неорганическая химия – Химия для чайников
Неоргани́ческая хи́мия — раздел химии, связанный с изучением
строения, реакционной способности и свойств всех химических элементов и их
неорганических соединений. Это область охватывает все химические соединения, за
исключением органических веществ (класса соединений, в которые входит углерод,
за исключением нескольких простейших соединений, обычно относящихся к
неорганическим). Теоретическим фундаментом неорганической химии является периодический закон и основанная на нём периодическая система Д. И. Менделеева. Важнейшая задача неорганической химии состоит в разработке и научном обосновании способов создания новых материалов с нужными для современной техники свойствами. История определения Исторически название неорганическая химия происходит от
представления о части химии, которая занимается исследованием элементов,
соединений, а также реакций веществ, которые не образованы живыми существами.
Однако со времен синтеза мочевины из неорганического соединения цианата аммония
(Nh5OCN), который совершил в 1828 году выдающийся немецкий химик Фридрих Вёлер,
стираются границы между веществами неживой и живой природы. Сложные вещества Большую часть сложных неорганических веществ (то есть состоящих из двух и более химических элементов) можно разделить на следующие группы: – Оксиды, – Соли, – Основания, – Кислоты. |
Показывать 4 элементов
Показывать 4 элементов
Химия для чайников. Вещество и одеялка
Меня пугает то, во что превратилась школа. В советском образовании были дыры и завалы ненужных знаний. Можно долго спорить, но уверен в одном, тогда было интересно учиться, несмотря на политические и академические перекосы.
Считайте это брюзжанием, но сегодня урок превратился в натаскивание на вопросы к тестам, которые сделали совсем ненужным познавательную составляющую. Конечно, нормальный человек доберет недостающее самообразованием, доступ к знаниям сегодня безграничен. Но для этого его нужно научить его учиться, простите за тавтологию. И к счастью, науки не стоят на месте. Меняется окружающий мир и представления о нем.
Что такое химия?
Химия – это наука о веществах, которые нас окружают, она неразрывно связана с другими науками, с физикой, например. Признаюсь, что физику терпеть не могу. Постараемся касаться знаний из смежных областей минимальным образом, достаточном для понимания процессов.
Что такое вещество и из чего оно состоит?
Считается, что вещество – это и есть разновидность материи, из которой состоит окружающий мир. Различные вещества обладают разными качествами и свойствами. Вода мокрая, мыло жжет глаза, а одеялка – кусачая! Кстати, мыло и одеялка – это смеси веществ, а слова «одеялка» не существует в русском языке.
Почему так?
Почему нет слова «одеялка» я не знаю, население на Волге часто использует этот термин. А если брать ее состав, то давайте посмотрим, что же там внутри. Обычно – это ткань из плетеных ниток. Нитки – это крученые волоски шерсти или растительные волокна. Если посмотреть в микроскоп, то можно выделить в их составе связанные молекулы отдельных веществ. Они большей частью растительного происхождения. Их собрали и «вырастили» растения из других мелких молекул.
А вода — это отдельное вещество?
Если брать абсолютно чистую воду, то да. Но такой в природе, да и в лабораториях не существует. Помимо молекул самой воды (ее формула Н2О) в ней найдется огромное количество примесей. Идеально чистых веществ не бывает. Есть даже шкала по степени чистоты. Например, уровень «химически чистый» требует содержания заявленного вещества свыше 99%.
Значит материя состоит из вещества, вещество из молекул?
Похоже на смерть Кощея. Почти верно. Но вещество в бытовом понимании может состоять из смеси молекул. Все слышали про соляную кислоту? Если быть дотошным, то это – смесь. Концентрация «солянки» редко превышает 40%, это определено растворимостью хлороводорода в воде. Значит концентрированная соляная кислота – это смесь молекул соляной кислоты и воды. Кстати, если на бутылке написано «концентрированная уксусная кислота», это вранье. Название уксусной кислоты «ледянка». Получено оно неспроста. Если убрать из нее воду, то это твердая кислота, похожая на лед.
Почти верно. Но вещество в бытовом понимании может состоять из смеси молекул. Все слышали про соляную кислоту? Если быть дотошным, то это – смесь. Концентрация «солянки» редко превышает 40%, это определено растворимостью хлороводорода в воде. Значит концентрированная соляная кислота – это смесь молекул соляной кислоты и воды. Кстати, если на бутылке написано «концентрированная уксусная кислота», это вранье. Название уксусной кислоты «ледянка». Получено оно неспроста. Если убрать из нее воду, то это твердая кислота, похожая на лед.
Почему вещества такие разные?
Действительно разные, и по запаху, и по цвету, форме и, иногда, на вкус. Кстати, вещества имеют так называемые агрегатные состояния. Возьмем ту же воду. Все знают, что она жидкая. Но лед, снег и пар – все это вода. Агрегатных состояний обычно три, реже четыре. Твердое, жидкое, газообразное, ну и плазму часто считают четвертым. Вот ртуть – это металл. При обычной температуре он жидкий, но нагревая или охлаждая его, изменяя давление, можно изменить агрегатное состояние этого вещества. Или водород. Это – газ, но при охлаждении под большим давлением он становится жидким, из астрономии мы знаем о существовании твердого водорода при низких температурах.
Или водород. Это – газ, но при охлаждении под большим давлением он становится жидким, из астрономии мы знаем о существовании твердого водорода при низких температурах.
Молекулы – это основа, из которой все строится?
В точку! Как раз молекулы и определяют все химические свойства вещества. Они имеют химические формулы, такие условные написания, например С2Н5ОН.
Сейчас мозг лопнет. Если веществ много, то и молекулы все разные?
Конечно. Их бесчисленное множество. Они могут быть совсем маленькими как у водорода и громадными многомерными цепочками, как у органических веществ или образовывать кристаллические решетки. Все зависит от того, какие атомы их образовали, от расположения и свойств этих атомов в молекуле.
Значит молекулы состоят из атомов?
Да, но это совсем другая история, через неделю посвятим этому новую статью.
Химия, 8–9 класс: уроки, тесты, задания
Химия, 8–9 класс: уроки, тесты, задания-
-
Предмет химии
-
Физические тела и вещества
-
Чистые вещества и их смеси
-
Разделение смесей.
 Методы очистки веществ
Методы очистки веществ
-
Атомы и молекулы
-
Химические элементы. Знаки химических элементов
-
Закон постоянства состава
-
Химические формулы
-
Отличия простых и сложных веществ
-
Валентность.
 Степень окисления. Составление формул по валентностям и степеням окисления
Степень окисления. Составление формул по валентностям и степеням окисления
-
Физические и химические явления
-
Признаки и условия протекания химических реакций
-
Закон сохранения массы веществ в химических реакциях
-
Уравнения химических реакций
-
-
-
Классификация веществ
-
Металлы
-
Неметаллы
-
Оксиды: классификация, свойства, получение
-
Основания: классификация, свойства, получение
-
Кислоты: состав, свойства, получение
-
Амфотерные гидроксиды
-
Соли: состав и свойства
-
Взаимосвязь между классами неорганических веществ
-
-
-
Периодический закон
-
Периодическая система
-
Строение ядра атома
-
Строение электронной оболочки атома
-
Периодическая таблица и закономерности изменения свойств химических элементов
-
-
-
Электроотрицательность
-
Типы химической связи
-
Ионная связь
-
Ковалентная связь
-
Металлическая связь
-
Аморфные и кристаллические вещества
-
Кристаллические решётки
-
-
-
Степени окисления элементов
-
Окислители и восстановители, окисление и восстановление
-
-
-
Состав растворов
-
Растворение.
 Растворимость
Растворимость
-
Электролиты и неэлектролиты
-
Электролитическая диссоциация кислот, оснований и солей
-
Свойства ионов
-
Среда растворов.
 Индикаторы
Индикаторы
-
Реакции ионного обмена. Реакция нейтрализации
-
-
-
Классификация химических реакций по числу и составу вступивших в реакцию и образовавшихся веществ
-
Классификация химических реакций по тепловому эффекту
-
Классификация химических реакций, ОВР
-
Скорость протекания химической реакции.
 Катализаторы
Катализаторы
-
-
-
Свойства водорода
-
Свойства кислорода
-
Вода
-
Галогены.
 Хлор и его соединения
Хлор и его соединения
-
Сера и её соединения
-
Азот и его соединения
-
Фосфор. Соединения фосфора
-
Углерод.
 Соединения углерода
Соединения углерода
-
Кремний. Соединения кремния
-
-
-
Щелочные металлы и их соединения
-
Щелочноземельные металлы и их соединения
-
Алюминий и его соединения
-
Железо и его соединения
-
-
-
Состав и строение органических веществ
-
Углеводороды.
 Полимеры
Полимеры
-
Одноатомные и многоатомные спирты
-
Карбоновые кислоты
-
Жиры
-
Углеводы: классификация и свойства
-
Белки
-
-
-
Природные источники углеводородов
-
Химия и пища.
 Химия и здоровье
Химия и здоровье
-
-
-
Методы научного познания. Химический эксперимент
-
Методы получения, собирания и распознавания газов
-
Обнаружение ионов
-
-
-
Физические величины
-
Относительная атомная и молекулярная массы.
 Вычисление относительной молекулярной массы вещества
Вычисление относительной молекулярной массы вещества
-
Количество вещества
-
Вычисление молярной массы вещества
-
Вычисление количества вещества
-
Вычисление массовой доли элемента в химическом соединении
-
Установление простейшей формулы вещества по массовым долям элементов
-
Простейшие вычисления по уравнениям химических реакций
-
Вычисления по уравнениям реакций, если исходное вещество содержит определённую долю примесей
-
Вычисление массовой доли вещества в растворе
-
Вычисления, связанные с приготовлением растворов с заданной массовой долей растворённого вещества
-
Комбинированные задачи
-
эффективные способы.
 Химия. Самоучитель. Книга для тех, кто хочет сдать экзамены, а также понять и полюбить химию. Элементы общей, неорганической и органической химии
Химия. Самоучитель. Книга для тех, кто хочет сдать экзамены, а также понять и полюбить химию. Элементы общей, неорганической и органической химииКак выучить химию самостоятельно с нуля: эффективные способы. Химия. Самоучитель. Книга для тех, кто хочет сдать экзамены, а также понять и полюбить химию. Элементы общей, неорганической и органической химии
Это сообщение вы получилиНеорганическая химия является базовым разделом химии.
Кроме того, это и самый простой раздел химии, органическая химия гораздо
сложнее. Именно поэтому мы начнем наше изучение химии с неорганической
химии. Как вы уже знаете из
, неорганическая химия – это наука о химических
элементах и их неорганических соединениях. Что же такое химический
элемент? Химический элемент – это абстрактное понятие, которое
обозначает простое вещество, которые состоит из атомов одного вида.
Каждый химический элемент имеет порядковый номер в таблице Менделеева,
который совпадает с количеством протонов в атомном ядре. Необходимо
отличать сам химический элемент от вещества, который он обозначает.
Химический элемент – это просто название атомов вещества. А вот само
вещество, даже состоящее из одного атома, может быть в различных формах.
Яркий тому пример – углерод. Он может быть в форме черных угольков,
остающихся после костра, в форме брикетов каменного угля или торфа,
которым топят печь, в форме графитного стержня, который имеется внутри
карандаша и даже в форме алмазов. Все это разновидности одного и того же
химического элемента – углерода. Все разница лишь в том, как
располагаются атомы по отношению к друг другу. Например, в алмазе атомы
углерода образуют объемную пространственную решеткув форме тетраэдра (пирамиды):
Необходимо
отличать сам химический элемент от вещества, который он обозначает.
Химический элемент – это просто название атомов вещества. А вот само
вещество, даже состоящее из одного атома, может быть в различных формах.
Яркий тому пример – углерод. Он может быть в форме черных угольков,
остающихся после костра, в форме брикетов каменного угля или торфа,
которым топят печь, в форме графитного стержня, который имеется внутри
карандаша и даже в форме алмазов. Все это разновидности одного и того же
химического элемента – углерода. Все разница лишь в том, как
располагаются атомы по отношению к друг другу. Например, в алмазе атомы
углерода образуют объемную пространственную решеткув форме тетраэдра (пирамиды):
Именно благодаря такой решетке алмаз очень твердый. У графита другая форма кристаллической решетки, поэтому он мягкий и его частицы легко отслаиваются друг от друга:
Для понимания химических процессов а так же почему
вещество может иметь разную структуру, необходимо знать строение атомов. Сейчас мы его рассмотрим.
Сейчас мы его рассмотрим.
И так, что представляет собой атом? А он представляет собой ядро, расположенное в центре атома, вокруг которого вращаются электроны. При этом не следует представлять, что они прямо такие летают вокруг ядра, аки спутники вокруг Земли или планеты вокруг Солнца. На самом деле, что электроны, что протоны, что другие элементраные частицы – это такая неведомая непонятная штуковина, с очень экзотическими свойствами, которая может одновременно находиться в разных местах. Поэтому электроны как бы “размазаны” по своим орбитам. И, такие электронные орбиты в атомах получили название орбитали .
Ядро состоит из нейтронов и протонов. Нейтроны, являются
нейтрально заряженными частицами, протоны – положительно заряженными частицами, а электроны отрицательно заряженными. Поэтому между
последними существуют силы электромагнитного притяжения, вследствие чего
электроны обычно никуда не улетают из атомов. Да, именно обычно не улетают,
потому что иногда случается, что электроны все таки отрываются от своих ядер. По
какой причине? Например, если к куску вещества приложить электрическое поле,
которое будет вырывать электроны из атомов (пойдет электрический ток). Или
какая-нибудь элементарная частица типа фотона (кусочка света) может его выбить.
Но обсуждение физики выходит за рамки данных уроков, тут у нас химия. Поэтому
идем дальше.
По
какой причине? Например, если к куску вещества приложить электрическое поле,
которое будет вырывать электроны из атомов (пойдет электрический ток). Или
какая-нибудь элементарная частица типа фотона (кусочка света) может его выбить.
Но обсуждение физики выходит за рамки данных уроков, тут у нас химия. Поэтому
идем дальше.
Вот как вы думаете, может ли ядро притянуть электрон из
соседнего атома? Почему нет? Между ними действуют такие силы
электромагнитного взаимодействия. Правда, у другого атома тоже есть ядро,
которое не даст электрону улететь. Но сила притяжения то никуда не девается. Как
вы думает, что произойдет с атомами, которые будут находиться достаточно близко
друг к друг. Правильно, они буду как то взаимодействовать. С одной
стороны, ядра пытаются отобрать у соседа электроны, создавая силу притяжения, с
другой стороны, электроны соседних атомов будут отталкиваться друг от друга.
Таким образом, атомы будут смещать на такое расстояние, что бы эти силы
уравновесить. Если все атомы одинаковые, то получиться кристаллическая решетка
(если это твердое вещество), либо, допустим, для газов, образуются двухатомные
молекулы. Есть, конечно, еще варианты, но мы их рассмотрим позже в
соответствующих разделах.
Есть, конечно, еще варианты, но мы их рассмотрим позже в
соответствующих разделах.
А если атомы разные? Тогда они могут образовывать между собой разные связки, которые принято называть химическими связями . Различают следующие типа химических связей:
1 . Ковалентная неполярная связь. Она обусловлена перекрытием так называемых электронных облаков двух атомов. Я уже говорил, что электрон в атоме не находиться в одном месте, а как бы размазан по своей орбите (орбитали). Этот “размазанный” по пространству электрон и есть электронное облако. Вот таки облака частично перекрывают друг друга при ковалентной неполярной связи. Такая связь свойственна простым молекула, например, H 2 – водород, O 2 – кислород.
2. Ковалентная полярная связь. Это, по сути, тоже самое, что и ковалентная неполярная связь, но один из атомов немного перетягивает на себя электрон другого атома.
3. Ионная связь. В случае такой связи один из атомов
теряет электрон а другой “хапает” его себе. В результате оба из них становятся
ионами с разноименным зарядами, которые, как известно, притягиваются.
В результате оба из них становятся
ионами с разноименным зарядами, которые, как известно, притягиваются.
4. Металлическая связь. Такой связью связаны все атомы в куске металла. Ее суть состоит в том, что атомы металла не могут удержать один из электронов и легко теряют его. Поэтому свободные электроны легко циркулируют между атомами.
5. Водородная связь. Это связь, образующаяся между атомом водорода одной молекулы и сильно электроотрицательным атомом другой молекулы. Электроотрицательность – это способность атомов оттягивать на себя электроны с других атомов. Наибольшая электроотрицательно у галогенов – фтора, хлора, а так же у сильных окислителей, например, у кислорода. Суть такой связи в том, что одна молекула, содержащая сильный электроотрицательный атом, притягивает к себе атом водорода из другой молекулы.
Может возникнуть вопрос: А почему такие связи образует именно водород?
Это объясняется тем, что атомный радиус водорода очень мал. Кроме того, при смещении или полной отдаче своего единственного электрона
водород приобретает сравнительно высокий положительный заряд, за счет которого
водород одной молекулы взаимодействует с атомами электроотрицательных элементов,
имеющих частичный отрицательный заряд, выходящий в состав других молекул (HF, H 2 O,
NH 3).
Кроме того, при смещении или полной отдаче своего единственного электрона
водород приобретает сравнительно высокий положительный заряд, за счет которого
водород одной молекулы взаимодействует с атомами электроотрицательных элементов,
имеющих частичный отрицательный заряд, выходящий в состав других молекул (HF, H 2 O,
NH 3).
Водородную связь обычно обозначают точками или пунктирной линией, потому что она представляет собой что то средне между химической связью (ковалентной, ионной) и обычной молекулярной связью: гораздо слабее первой но сильнее последней.
Еще в неорганической химии принято классифицировать неорганические вещества. Сначала они группируются на простые и сложные.
Простые вещества это такие вещества, которые состоят только из одного элемента. Они, в свою очередь делятся на группы:
Металлы. Это такие вещества, которые имеют ярко
выраженные металлические свойства, а именно: высокая тепло- и электропроводность
и характерный металлический блеск, твердость. . К металлам относятся такие
вещества как железо (Fe),
медь (Cu),
натрий (Na),
калий (K),
литий (Li),
серебро (Ag),
золото (Au)
и
другие.К химическим свойствам металлов относится то,
что они легко отдают свой электрон с последних орбиталей.
. К металлам относятся такие
вещества как железо (Fe),
медь (Cu),
натрий (Na),
калий (K),
литий (Li),
серебро (Ag),
золото (Au)
и
другие.К химическим свойствам металлов относится то,
что они легко отдают свой электрон с последних орбиталей.
Неметаллы. Это вещества, имеющие типичные неметаллические свойства: плохая электропроводность, среди неметаллов присутствуют много веществ, которые при комнатной температуре находятся в газообразном состоянии, например, кислород (O 2 ), азот (N 2) . Но среди неметаллов есть и твердые вещества, например, сера (S 2), кремний (Si). К химическим свойствам неметаллов относиться то, что они легче забирают себе электроны, чем отдают.
Инертные газы. Есть целая группа химических элементов,
атомы которых ни с чем не взаимодействую и не образуют ни каких соединений. При
комнатной температуре такие вещества находятся в газообразном состоянии. Это
гелий (He),
неон (Ne), аргон (Ar)
и другие. Такие газы получили название инертных газов .
Сложные вещества так же группируются:
Оксиды. В этих веществам один из компонентов кислород.
Гидроксилы. Один из компонентов таких соединений – гидроксильная группа (OH – кислород + водород). Чисто такие соединения имеют щелочные свойства.
Кислоты. Соединение водорода с кислотной группой, такие вещества очень часто бывают химически активные, вступая в реакцию со многими веществами, в том числе, даже разъедают многие металлы.
Соли. Если в кислоте атом водорода заменить на атом металла – то получиться соль. Например, формула соляной кислоты HCl . А форума полученной на основе нее поваренной соли NaCl.
Бинарные соединения. Это соединения двух элементов, например, сероводород H 2 S (ядовитый и очень вонючий газ).
Карбонаты. Соли и эфиры угольной кислоты (H 2 CO 3)
Карбиды. Соединения металлов и неметаллов с углеродом.
Цианиды. Соли синильной кислоты (HCN).
Оксиды углерода. Их выделили в отельную группу, потому что непонятно, то ли это оксид углерода, то ли карбид кислорода. но принято все таки считать, что соединение углерода с кислородом – это именно оксид углерода.
Прочие экзотические соединения.
На этом краткий экскурс в неорганическую химию закончен, на следующем уроке начнется сама химия.
Химия считается одним из самых сложных и трудных предметов. Причем сложности возникают в освоении этого предмета и у школьников, и у студентов. Почему? Школьники ожидают от урока фокусов, интересных опытов и демонстраций. Но уже после первых занятий разочаровываются: лабораторных работ с реактивами совсем не много, в основном приходится изучать новую терминологию, делать объемные домашние задания. Химический язык совершенно не похож на повседневный, поэтому нужно ускоренными темпами изучать термины и названия. Кроме того, нужно уметь логически мыслить и применять математические знания.
Можно ли выучить химию самостоятельно?
Ничего невозможного нет. Несмотря на сложность науки, химию можно выучить с нуля. В ряде случаев, когда тема особенно сложная или требует дополнительных знаний, можно воспользоваться услугами онлайн репетитора. Самый удобный способ обучения – с помощью репетиторов по химии по скайпу . Дистанционное обучение позволяет подробно изучить отдельную тему или уточнить сложные моменты. По скайпу можно в любое время связаться с квалифицированным преподавателем.
Несмотря на сложность науки, химию можно выучить с нуля. В ряде случаев, когда тема особенно сложная или требует дополнительных знаний, можно воспользоваться услугами онлайн репетитора. Самый удобный способ обучения – с помощью репетиторов по химии по скайпу . Дистанционное обучение позволяет подробно изучить отдельную тему или уточнить сложные моменты. По скайпу можно в любое время связаться с квалифицированным преподавателем.
Для того чтобы процесс изучения был эффективным, нужно несколько факторов:
- Мотивация . В любом деле необходима цель, к которой стремятся. Не важно, для чего изучается химия – для поступления в мединститут или биологический факультет, просто для саморазвития. Главное, поставить цель и определить способ ее достижения. Мотивация будет основным движущим фактором, который заставит продолжать самообучение.
- Важность деталей
. За короткое время выучить большой объем информации просто невозможно. Чтобы выучить химию эффективно и уметь правильно использовать знания, нужно уделять внимание деталям: формулам, решать большое количество примеров, задач.
 Для качественного усвоения материала требуется систематизация информации: самостоятельно изучают новую тему, в дополнение решают задачи и примеры, учат формулы и т.д.
Для качественного усвоения материала требуется систематизация информации: самостоятельно изучают новую тему, в дополнение решают задачи и примеры, учат формулы и т.д. - Проверка знаний . Для закрепления пройденного материала рекомендуется периодически делать проверочные работы. Умение понимать и логически анализировать позволяет усваивать знания лучше, чем «зубрежка». Преподаватели рекомендуют периодически делать себе зачеты и контрольные работы. Не лишним будут повторения пройденного материала. Самостоятельно выучить химию помогают решебники и самоучители.
- Практика и еще раз практика…
Не достаточно хорошо владеть теоретическими знаниями, нужно их уметь применять на практике, во время решения задач. Практические занятия помогают выявить слабые места в знаниях и закрепить пройденный материал. Кроме того, развиваются аналитические способности и логическое построение цепочки решения. Во время решения примеров и задач вы делаете выводы и происходит систематизация полученных знаний.
 Когда задачи становятся абсолютно понятными, можно приступать к изучению следующей темы.
Когда задачи становятся абсолютно понятными, можно приступать к изучению следующей темы. - Учите сами . Не уверены в полноценном освоении химии? Попробуйте обучить этому предмету кого-нибудь. Во время объяснения материала выявляются слабые места в знаниях, выстраивается системность. Важно не торопиться, уделяя внимание деталям и практическим моментам.
Выучить химию самостоятельно с нулевого уровня можно, если есть сильная мотивация и время. Если же материал сложный, разобраться в премудростях темы помогут профессиональные репетиторы. Будет ли это очное консультирование или с помощью скайпа – зависит только от вас. Не обязательно брать полный курс у репетитора, в ряде случаев можно взять урок по отдельной теме.
Глава 1.
Общие химические и экологические закономерности.
С чего начинается химия?
Cложный ли это вопрос? На него каждый ответит по-своему.
В середней школе учащиеся изучают химию в течение ряда лет. Многие довольно хорошо сдают выпускной экзамен по химии. Однако…
Однако…
Беседы с абитуриентами и затем и студентами первых курсов говорят о том, что остаточные знания по химии после средней школы незначительные. Одни путаются в различных определениях и химических формулах, а другие вообще не могут воспроизвести даже основные понятия и законы химии, не говоря уже о понятиях и законах экологии.
У них химия так и не начиналась.
Химия, по-видимому, начинается с глубокого освоения ее основ, и прежде всего, основных понятий и законов.
1.1. Основные химические понятия.
В таблице Д.И.Менделеева рядом с символом элемента стоят цифры. Одна цифра обозначает порядковый номер элемента, а вторая атомную массу. Порядковый номер имеет свой физический смысл. О нем мы будем вести разговор позже, здесь остановимся на атомной массе и выделим в каких единицах она измеряется.
Следует сразу оговориться, что атомная масса элемента, приведенная в таблице, величина относительная. За единицу относительной величины атомной массы принята 1/12 часть массы атома углерода, изотопа с массовым числом 12, и назвали ее атомной единицей массы /а. е.м./. Следовательно, 1 а.е.м. равна 1/12 части массы изотопа углерода 12
С. И она равна 1,667*10 –27
кг. /Абсолютная масса атома углерода равна 1,99*10 –26
кг./
е.м./. Следовательно, 1 а.е.м. равна 1/12 части массы изотопа углерода 12
С. И она равна 1,667*10 –27
кг. /Абсолютная масса атома углерода равна 1,99*10 –26
кг./
Атомная масса , приведенная в таблице, является массой атома, выраженной в атомных единицах массы. Величина безразмерная. Конкретно для каждого элемента атомная масса показывает, во сколько раз масса данного атома больше или меньше 1/12 части массы атома углерода.
Аналогичное можно сказать и о молекулярной массе.
Молекулярная масса – это масса молекулы, выраженная в атомных единицах массы. Величина тоже относительная. Молекулярная масса конкретного вещества равна сумме масс атомов всех элементов, входящих в состав молекулы.
Важным понятием химии является понятие «моль». Моль – такое количество вещества, которое содержит 6,02*10 23 структурных единиц /атомов, молекул, ионов, электронов и т.д./. Моль атомов, моль молекул, моль ионов и т.д.
Масса одного моля данного вещества называется его молярной /или мольной/ массой. Она измеряется в г/моль или кг/моль и обозначается буквой «М». Например, молярная масса серной кислоты М Н
2
SO4
=98г/моль.
Она измеряется в г/моль или кг/моль и обозначается буквой «М». Например, молярная масса серной кислоты М Н
2
SO4
=98г/моль.
Следующее понятие «Эквивалент». Эквивалентом /Э/ называют такое весовое количество вещества, которое взаимодействует с одним молем атомов водорода или замещают такое его количество в химических реакциях. Следовательно, эквивалент водорода Э Н равен единице. /Э Н =1/. Эквивалент кислорода Э О равен восьми /Э О =8/.
Различают химический эквивалент элемента и химический эквивалент сложного вещества.
Эквивалент элемента – величина переменная. Она зависит от атомной массы /А/ и валентности /В/, которую элемент имеет в конкретном соединении. Э=А/В. Например, определим эквивалент серы в оксидах SO 2 и SO 3 . В SO 2 Э S =32/4=8, а в SO 3 Э S =32/6=5,33.
Молярную массу эквивалента, выраженную в граммах, называют эквивалентной массой. Следовательно, эквивалентная масса водорода МЭ Н
=1г/моль, эквивалентная масса кислорода МЭ О
=8г/моль.
Химический эквивалент сложного вещества /кислоты, гидроксида, соли, оксида/– такое количество соответствующего вещества, которое взаимодействует с одним молем атомов водорода, т.е. с одним эквивалентом водорода или замещает такое количество водорода или любого другого вещества в химических реакциях.
Эквивалент кислоты /Э К / равен частному от деления молекулярной массы кислоты на число атомов водорода, участвующих в реакции. Для кислоты H 2 SO 4 , когда оба атома водорода вступают в реакцию H 2 SO 4 +2NaOH=Na 2 SO+2H 2 O эквивалент будет равен Э Н 2 SO4 = М Н 2 SO 4 /n Н =98/2=49
Эквивалент гидроксида /Э гидр. / определяется как частное от деления молекулярной массы гидроксида на число гидроксогрупп, вступающих в реакцию. Например, эквивалент NaOH будет равен: Э NaOH =М NaOH /n ОН =40/1=40.
Эквивалент соли /Э соли
/ можно рассчитать, поделив ее молекулярную массу на произведение числа атомов металла, вступающих в реакцию, и их валентность. Так, эквивалент соли Al 2
(SO 4) 3
будет равен Э Al
2
(SO
4)
3
=М Al
2
(SO
4)
3
/6=342/2,3=342/6=57.
Так, эквивалент соли Al 2
(SO 4) 3
будет равен Э Al
2
(SO
4)
3
=М Al
2
(SO
4)
3
/6=342/2,3=342/6=57.
Эквивалент оксида /Э ок / можно определить, как сумму эквивалентов соответствующих элемента и кислорода. Например, эквивалент СО 2 будет равен сумме эквивалентов углерода и кислорода: Э СО 2 =Э С +Э О =3+8=7.
Для газообразных веществ удобно пользоваться эквивалентными объемами /Э V /. Так как при нормальных условиях моль газа занимает объем 22,4л, то исходя из этой величины, легко определить эквивалентный объем любого газа. Рассмотрим водород. Мольная масса водорода 2г занимает объем 22,4л, тогда его эквивалентная масса 1г занимает объем 11,2л /или 11200мл /. Следовательно Э V Н =11,2л. Эквивалентный объем хлора равен 11,2л /Э VCl =11,2л/. Эквивалентный объем СО равен 3,56 /Э VC О =3,56л/.
Химический эквивалент элемента или сложного вещества используется в стехиометрических расчетах обменных реакций, а в соответствующих расчетах окислительно–восстановительных реакций применяют уже окислительный и восстановительный эквиваленты.
Окислительный эквивалент определяют как частное от деления молекулярной массы окислителя на число электронов, которое он принимает в данной окислително–восстановительной реакции.
Восстановительный эквивалент равен молекулярной массе восстановителя поделенной на число электронов, которое он отдает в данной реакции.
Напишем окислително–восстановительную реакцию и определим эквивалент окислителя и восстановителя:
5N 2 aS+2KMnO 4 +8H 2 SO 4 =S+2MnSO 4 +K 2 SO 4 +5Na 2 SO 4 +8H 2 O
Окислителем в этой реакции является перманганат калия. Эквивалент окислителя будет равен массе KMnO 4 деленной на число электронов, принятых окислителем в реакции (nе=5). Э KMnO 4 =М KMnO 4 /nе=158/5=31,5. Молярная масса эквивалента окислителя KMnO 4 в кислой среде равна 31,5г/моль.
Эквивалент восстановителя Na 2 S будет: Э Na 4 S =М Na 4 S /nе=78/2=39. Молярная масса эквивалента Na 2 S равна 39г/моль.
В электрохимических процессах, в частности при электролизе веществ, пользуются электрохимическим эквивалентом. Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Валентность . При взаимодействии атомов между ними образуется химическая связь. Каждый атом может образовывать только определенное количество связей. Количество связей предопределяет такое уникальное свойство каждого элемента, которое называют валентностью. В наиболее общем виде валентностью называют способность атома образовывать химическую связь. За единицу валентности принимают одну химическую связь, которую способен образовать атом водорода. В связи с этим, водород является одновалентным элементом, а кислород – двухвалентным, т.к. с атомом кислорода могут образовывать связь не более двух водородов.
Умение определять валентность каждого элемента, в том числе и в химическом соединении, является необходимым условием успешного усвоения курса химии.
С валентностью соприкасается и такое понятие химии как степень окисления . Подстепенью окисления понимают тот заряд, который имеет элемент в ионном соединении или имел бы в ковалентном соединении, если бы общая электронная пара бала бы полностью смещена к более электроотрицательному элементу. Степень окисления имеет не только цифровое выражение, но и соответствующий знак заряда (+) или (–). Валентность не имеет этих знаков. Например, в H 2 SO 4 степень окисления: водорода +1, кислорода –2, серы +6, а валентность, соответственно, будет 1, 2, 6.
Валентность и степень окисления в числовых значениях не всегда совпадают по величине. Например, в молекуле этилового спирта СН 3 –СН 2 –ОН валентность углерода 6, водорода 1, кислорода 2, а степень окисления, например, углерода первого –3, второго –1: –3 СН 3 – –1 СН 2 –ОН.
1.2. Основные экологические понятия.
За последнее время понятие “экология” глубоко входит в наше сознание. Это понятие, введенное еще в 1869г Э. Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
В учебниках биологии экологию определяют как науку о взаимоотношениях живых организмов и среды их обитания. Практически созвучное определение экологии дает Б.Небел в своей книге «Наука об окружающей среде» – Экология – наука о различных аспектах взаимодействия организмов между собой и с окружающей средой. В других источниках можно встретить и более широкое толкование. Например, Экология – 1/. Наука, изучающая отношение организмов и их системных совокупностей и окружающей среды; 2/. Совокупность научных дисциплин, исследующих взаимоотношение системных биологических структур /от макромолекул до биосферы/ между собой и с окружающей средой; 3/. Дисциплина, изучающая общие законы функционирования экосистем различного иерархического уровня; 4/. Комплексная наука, исследующая среду обитания живых организмов; 5/. Исследование положения человека как вида в биосфере планеты, его связей с экологическими системами и воздействие на них; 6/. Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
Если вы поступили в университет, но к этому времени так и не разобрались в этой нелегкой науке, мы готовы раскрыть вам несколько секретов и помочь изучить органическую химию с нуля (для “чайников”). Вам же остается только читать и внимать.
Основы органической химии
Органическая химия выделена в отдельный подвид благодаря тому, что объектом ее изучения является все, в составе чего есть углерод.
Органическая химия – раздел химии, который занимается изучением соединения углерода, структуру таких соединений, их свойства и методы соединения.
Как оказалось, углерод чаще всего образует соединения со следующими элементами – H, N, O, S, P. Кстати, эти элементы называются органогенами .
Органические соединения, количество которых сегодня достигает 20 млн, очень важны для полноценного существования всех живых организмов. Впрочем, никто и не сомневался, иначе человек просто закинул бы изучение этого непознанного в долгий ящик.
Цели, методы и теоретические представления органической химии представлены следующим:
- Разделение ископаемого, животного или растительного сырья на отдельные вещества;
- Очистка и синтез разных соединений;
- Выявление структуры веществ;
- Определение механики протекания химических реакций;
- Нахождение зависимости между структурой и свойствами органических веществ.
Немного из истории органической химии
Вы можете не верить, но еще в далекой древности жители Рима и Египта понимали кое-что в химии.
Как мы знаем, они пользовались натуральными красителями. А нередко им приходилось использовать не готовый естественный краситель, а добывать его, вычленяя из цельного растения (например, содержащиеся в растениях ализарин и индиго).
Можем вспомнить и культуру употребления алкоголя. Секреты производства спиртных напитков известны в каждом народе. Причем многие древние народы знали рецепты приготовления «горячей воды» из крахмал- и сахарсодержащих продуктов.
Так продолжалось долгие, долгие годы, и только в 16-17 веках начались какие-то изменения, небольшие открытия.
В 18 веке некто Шееле научился выделять яблочную, винную, щавелевую, молочную, галловую и лимонную кислоту.
Тогда всем стало ясно, что продукты, которые удалось выделить из растительного или животного сырья, имели много общих черт. В то же время они сильно отличались от неорганических соединений. Поэтому служителям науки нужно было срочно выделить их в отдельный класс, так и появился термин «органическая химия».
Несмотря на то, что сама органическая химия как наука появилась лишь в 1828 году (именно тогда господину Вёлеру удалось выделить мочевину путем упаривания цианата аммония), в 1807 году Берцелиус ввел первый термин в номенклатуру в органической химии для чайников:
Раздел химии, который изучает вещества, полученные из организмов.
Следующий важный шаг в развитии органический химии – теория валентности, предложенная в 1857 году Кекуле и Купером, и теория химического строения господина Бутлерова от 1861 года. Уже тогда ученые стали обнаруживать, что углерод – четырехвалентен и способен образовывать цепи.
В общем, с эти самых пор наука регулярно испытывала потрясения и волнения благодаря новым теориям, открытиям цепочкам и соединениям, что позволяло так же активно развиваться органической химии.
Сама наука появилась благодаря тому, что научно-технический прогресс не в состоянии был стоять на месте. Он продолжал и продолжал шагать, требуя новых решений. И когда каменноугольной смолы в сфере промышленности перестало хватать, людям просто пришлось создать новый органический синтез, который со временем перерос в открытие невероятно важного вещества, которое и по сей день дороже золота – нефть. Кстати, именно благодаря органической химии на свет появилась ее «дочка» – поднаука, которая получила название «нефтехимия».
Но это уже совсем другая история, которую вы можете изучить сами. Далее мы предлагаем вам посмотреть научно-популярное видео про органическую химию для чайников:
Ну а если вам некогда и срочно нужна помощь профессионалов , вы всегда знаете, где их найти.
Все книги можно скачать бесплатно и без регистрации.
NEW.
В.Н. Верховский, Я.Л. Гольдфарб, Л.М. Сморгонский. Органическая химия. Учебник для 10 класса. 1946 год. 156 стр. djvu. 19.2 Мб.
Этот учебник написан практиками и рассчитан на то, что дети будут понимать химию, а не вызубривать различные правила-скороговорки.
Объем изложенного материала значительно превышает таковой для учебника Цветкова. Очень рекомендую книгу, особенно учителям.
Сопоставление данной книги с современными учебниками четко показывает тенденции современных учебников:
учебники пишутся все более абстрактными и скупыми на материал и все более оторванными от практики.
Скачать.
NEW.
Никольский А. Б., Суворов А.В. Химия. 2001 год. 512 стр. djvu. 4.1 Мб.
Б., Суворов А.В. Химия. 2001 год. 512 стр. djvu. 4.1 Мб.
В учебнике нового типа, рассчитанном прежде всего на формирование химического мышления студентов, системно и точно и в то же время ясно и доступно изложен огромный объем современных общехимических знаний.
На современном уровне рассмотрено учение о химическом процессе с акцентом на механизм реакции. Прослежена взаимосвязь между электронным строением и химическим поведением веществ. Логичность и популярность изложения материала, оригинальность контрольных вопросов, доступность иллюстраций способствуют усвоению химических знаний и развитию научного мышления.
Предназначен студентам вузов, учащимся средних специальных учебных заведений, будет полезен преподавателям вузов и учителям школ. Полезно посмотреть и школьникам, неЕГЭотикам, хотя бы первые главы.
Скачать.
Алексинский В.Н. Занимательные опыты по химии. 2-е испр. изд. 1995 год. 95 стр. djvu. 1.9 Мб.
Книга для учитилей.
В книге рассмотрены опыты, которые можно использовать не только на внеклассных мероприятиях, но и при подготовке к урокам. Опыты, обладая элементом развлекательности, способствуют развитию у учащихся умения наблюдать и объяснять химические явления. Пособие окажет помощь учителям в воспитании у учащихся интереса к изучению химии, в выработке более глубокого и сознательного усвоения ими теоретического материала.
Опыты, обладая элементом развлекательности, способствуют развитию у учащихся умения наблюдать и объяснять химические явления. Пособие окажет помощь учителям в воспитании у учащихся интереса к изучению химии, в выработке более глубокого и сознательного усвоения ими теоретического материала.
Скачать.
Т.М. Варламова, А.И. Кракова. ОБЩАЯ И НЕОРГАНИЧЕСКАЯ ХИМИЯ: БАЗОВЫЙ КУРС. 263 стр. djvu. 2.2 Мб.
В данном пособии изложены основные вопросы общей и неорганической химии, многие из которых вызывают трудности у учащихся и абитуриентов. Подробно рассмотрены типовые задачи по всем разделам школьного курса химии и предложены задания для самостоятельного решения.
Пособие предназначено слушателям подготовительных отделений при высших учебных заведениях, а также лицам, готовящимся для поступления в вузы самостоятельно, учащимся старших классов средних школ, лицеев, гимназий и колледжей.
Скачать.
Габриелян О.С., Маскаев Ф.Н., Теренин В.И. Химия 10 класс. Учебник.2002 год. 304 стр. djvu. 3.9 Мб.
Книга для учитилей.
Учебник продолжает и развивает курс химии, изложенный в учебниках “Химия-8” и “Химия-9” автора О.С.Габриеляна. Учебный материал по органической химии излагается с учетом того, что первоначальные сведения об органических веществах учащиеся получили в 9 классе. Учебник соответствует обязательному минимуму содержания образования. Материал учебника распределен по двум уровням – базисному и углубленному и дается в связи с экологией, медициной, биологией. В курсе приводятся сведения о жизненно важных веществах: витаминах, ферментах, гормонах, лекарствах. Широко представлен химический эксперимент, в том числе новые практические работы, в ходе которых рассматриваются свойства витаминов, ферментов, лекарственных препаратов.
Скачать.
П.А. Гуревич, М.А. Кубешов. Органическая химия. Полезные сведения для школьников и учителей – история, теория, задачи и решения. 2004 год. 350 стр. djvu. 4.6 Мб.
Скачать.
Егоров А.С. ред. Репетитор по химии. 2003 год. 770 стр. PDF. 16.3 Мб.
2003 год. 770 стр. PDF. 16.3 Мб.
Пособие содержит подробное изложение основ общей, неорганической и органической химии, а также типовые задачи с решениями и большое число заданий разной степени сложности для самостоятельной работы (в том числе элективные тесты).
Рекомендуется учащимся школ, гимназий и лицеев, абитуриентам химических и медико-биологических вузов.
Скачать.
Кузьменко Н.Е., Еремин В.В., Попков В.А. Начала химии. Современный курс для поступающих в вузы. В 2-х томах. 7-е изд. перераб. доп. 2002 год. 384+384 стр. djvu. в одном архиве 16.9 Мб.
Книга представляет собой попытку современного, всеобъемлющего и систематического изложения основ химии, которые необходимо знать в первую очередь поступающим в вузы. Ее содержание основано на тщательном анализе программ вступительных экзаменов по химии большинства вузов (химических, медицинских, биологических и т.д.), а также конкретных экзаменационных заданий.
Пособие предназначено для школьников, абитуриентов и учителей. В пособии изложены основы современной химии, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом – химиком, медиком или биологом XXI века. В новом издании отражены последние достижения химии и приведены новые задачи вступительных экзаменов.
В пособии изложены основы современной химии, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом – химиком, медиком или биологом XXI века. В новом издании отражены последние достижения химии и приведены новые задачи вступительных экзаменов.
Скачать.
Н.Е. Кузьменко и др. Начала химии. Современный курс для поступающих в вузы. 2001 год. 360 стр. djvu. 16.3 Мб.
Скачать.
Кузьменко и др. Химия. Для школьнико старших классов и поступающих в вузы. Пособие представляет собой учебник и справочник по химии. 525 стр. Размер 4.7 Мб. djvu.
Скачать.
Кузьменко, Еремин, Попков. Краткий курс химии. Для поступающих в ВУЗы. 2002 год. 410 стр. PDF. Размер 12.4 Мб.
Пособие предназначено для школьников, абитуриентов и учителей. В пособии в краткой, но информативной и ясной форме изложены современные основы химии. Это – основы, которые надо понимать каждому выпускнику средней школы и совершенно обязательно знать каждому, кто видит себя студентом-химиком, медиком или биологом XXI века. В тех частях: 1. Теоретическая химия, 2. Неорганическая химя. 3. Органическая химия.
В тех частях: 1. Теоретическая химия, 2. Неорганическая химя. 3. Органическая химия.
Скачать
Т.Н. Литвинова, Е.Д. Мельникова, М.В. Соловьёва, Л.Т. Ажипа, Н.К. Выскубова. Химия в задачах для поступающих в вузы. 2009 год. 832 стр. PDF. 4.7 Мб.
Сборник содержит более 2500 задач, охватывающих основные темы школьного курса химии. Среди них представлены качественные и расчетные типовые задачи с решениями и задачи разного уровня сложности для самостоятельного решения. Ко всем задачам даны ответы, а к наиболее трудным – подробные решения.
По каждой теме приведен теоретический материал, преимущественно в виде таблиц, – основные понятия, законы химии, формулы, классификации, свойства, способы получения неорганических и органических веществ.
Пособие поможет при подготовке к выпускным экзаменам в средней школе, сдаче ЕГЭ и вступительным экзаменам в вуз. Книга адресована школьникам старших классов, абитуриентам и преподавателям.
Скачать.
Некрашевич И. Химия. 8 – 11 классы. 2008 год. 304 стр. PDF. 1.7 Мб.
8 – 11 классы. 2008 год. 304 стр. PDF. 1.7 Мб.
Химия кажется вам сложным и непонятным предметом? Вы не знаете, как решать химические задачи, составлять уравнения реакций, строить формулы?
Репетитор по химии, который вы держите в руках, поможет решить эти проблемы.
Скачать.
Г.К. Прохорова. Качественный химический анализ. Практикум для школьников. 2002 год. 33 стр. PDF. в общем архиве 424 Кб.
Практикум предназначен для учащихся 9 классов школ с углубленным
изучением химии и школы юных химиков для ознакомления их с основами аналитической химии.
Подготовлен на Химфаке МГУ.
Скачать.
Рудзитис Г.Е., Фельдман Ф.Г. Химия. 7-11 класс. В 2-х книгах. 1985 год. djvu. две книги в одном архиве. 12.3 Мб.
Книга 1. 204 стр. Учебное пособие для 7-11 классов вечерней (сменной) средней общеобразовательной школы. Учебник соответствует действующим школьным программам и обязательному минимуму химического образования. Он имеет классическую структуру школьного учебника по химии и включает весь необходимый теоретический и практический материал для изучения курса неорганической химии.
Книга 1. 306 стр. Учебное пособие для 7-11 классов вечерней (сменной) средней общеобразовательной школы. Учебник соответствует действующим школьным программам и обязательному минимуму химического образования. Он имеет классическую структуру школьного учебника по химии и включает весь необходимый теоретический и практический материал для изучения курса неорганической органической химии. Во второй книге органическая химия занимает половину его объема.
Материал дифференцирован по уровням сложности.
Многочисленные таблицы, схемы и рисунки способствуют усвоению и повторению теоретического и практического материала. Доступность и наглядность изложения основных понятий, определений и законов химии позволяют рекомендовать этот учебник не только для школьного обучения, но и для самообразования.
При изучении химии с нуля лучше пользоваться этим учебником, а не современными, так как он лучше и понятней. Это не мое мнение, а химика-профессионала.
Скачать.
Семенов. Химия: пособие для поступающих в вузы. 1989 год. 225 стр. djvu. 3.7 Мб.
1989 год. 225 стр. djvu. 3.7 Мб.
В отличие от существующих в данном пособии сделан упор на углубленное повторение основных понятий и законов химии, «узловых» вопросов, от понимания которых зависит осмысление изучаемого в школе фактического материала. На небольшом числе примеров показаны главные закономерности поведения химических систем, общие приемы подхода к их рассмотрению, то, как свойства вещества определяют его применение. Приводимые вопросы и упражнения выбраны из тех, которые предлагались на вступительных экзаменах в химические вузы или использовались автором на Подготовительном отделении ЛГУ. Как правило, для ответа не нужны громоздкие расчет и – надо лишь хорошо усвоить основные законы химии.
Предназначено прежде всего для абитуриентов, самостоятельно готовящихся к экзамену в вуз, но будет полезно также слушателям подготовительных отделений и курсов.
Скачать.
Стахеев. Вся химия в 50 таблицах. Приведены все основные понятия ШКОЛЬНОЙ хими. Представляет собой этакую шпаргалку – напоминалку. 60 стр. Размер 1.2 Мб. djvu.
60 стр. Размер 1.2 Мб. djvu.
Скачать.
Хомченко Г.П. Пособие по химии для поступающих в вузы. 2002 год. 480 стр. PDF. Размер 11.6 Мб.
В пособии освещены все вопросы приемных экзаменов по химии. Для лучшего усвоения курса химии приведены некоторые дополнительные сведения. В конце каждой главы даются типовые задачи с решениями и задачи для самостоятельной работы.
Книга предназначена поступающим в вузы. Она также может быть рекомендована преподавателям химии при подготовке учащихся к сдаче выпускных экзаменов за курс средней школы. Мне пособие понравилось.
Скачать
Черникова Л.П. Шпаргалки по химии. 2003 год. 144 стр. PDF. 2.4 Мб.
Материал разбит на три темы: Основные понятия хими, Общая химия, Органическая химия. Нормальное пособие. Не понял зачем такое название.
8 лучших учебников по химии
Обновлено: 22.04.2021 15:24:18*Обзор лучших по мнению редакции expertology.ru. О критериях отбора. Данный материал носит субъективный характер, не является рекламой и не служит руководством к покупке. Перед покупкой необходима консультация со специалистом.
Перед покупкой необходима консультация со специалистом.
С 8 класса в школах начинают изучать химию. К учебникам по этому предмету предъявляют довольно много требований. Наши эксперты выяснили, какое пособие по дисциплине педагоги и ученики считают лучшим. При составлении рейтинга учитывались следующие факторы:
- последовательность изложенного материала;
- качественная расшифровка определений;
- наличие тестовых упражнений и задач разной запутанности;
- присутствие в комплекте рабочей книги для учителя, тетради для школьников.
Каждый из представленных учебников имеет свои особенности подачи информации. Стоит познакомиться с ними получше.
Рейтинг лучших учебников по химии
Лучшие учебники по химии российских авторов
Авторы отразили в своих работах неоспоримую роль химии и ее влияние на жизнь человека. Активное развитие науки в 20 веке стало толчком для создания многих популярных учебных пособий.
Читайте также: 15 лучших кистей для макияжа
Химия. 9 класс. Учебник.Гузей Л.С. и др.
Рейтинг: 4.9
На вершине рейтинга располагается двухуровневое пособие для девятого класса. Издание включает материалы, направленные на углубленное изучение предмета. В книге изложены новые достижения науки, предложены актуальные методики преподавания. Вместе с учебником предусмотрены рабочая тетрадь, пособия для учителей. Примечательно то, что начинается учебник с раздела «Вспомним прошлый год». Далее речь пойдет о жидких, атомных и молекулярных кристаллах.
Педагоги в восторге от ясного изложения материала, в котором необходимость заучивания информации сведена к минимуму. Школьник начинает осознавать суть практического применения знаний. Это облегчает задачу преподавателя. Именно поэтому книга является лучшим вариантом для начинающих.
Н. Е. Кузнецова Химия 8 класс
Рейтинг: 4.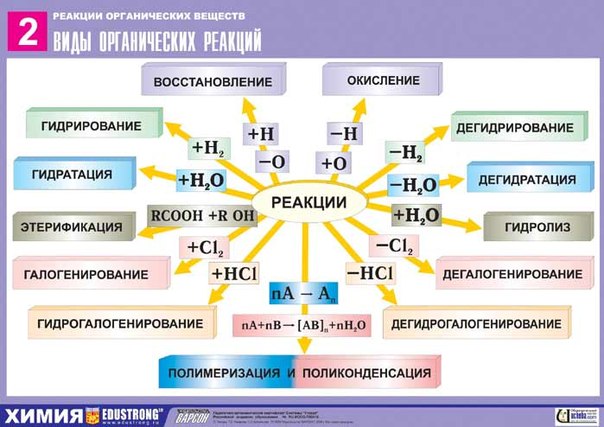 8
8
Следующий участник рейтинга по достоинству оценен многими преподавателями. В этом учебнике вразумительно и грамотно изложена органическая химия. Радует доступная для школьных умов информация, отдельный раздел с методами современной науки. В тексте представлены различные работы по практике и лабораторные опыты. В конце параграфов предлагаются задания, в том числе и творческие.
Автором пособия является доктор педагогических наук. Кузнецова грамотно и корректно отобразила материал, который носит исследовательский характер. Содержание книги мотивирует учебную деятельность и объединяет знания по физике, химии и биологии. Руководство побуждает к поиску информации и изучению дисциплины в будущем. Язык учебника ясный и научный. Таким образом «Химия 8 класс» в полной мере отвечает личностным и предметным требованиям.
О. С. Габриелян Учебник по химии для 8 класса
Рейтинг: 4.7
В рамках курса восьмого класса предлагается методическое пособие Габриеляна. Автор книги – профессор и заслуженный учитель РФ. Учебник соответствует Госстандарту образования. Учащимся нравятся красочные рисунки, интересные задания и разные вопросы. Все они способствуют активному усвоению материала.
Автор книги – профессор и заслуженный учитель РФ. Учебник соответствует Госстандарту образования. Учащимся нравятся красочные рисунки, интересные задания и разные вопросы. Все они способствуют активному усвоению материала.
Сейчас этим пособием пользуются многие классы. В нем присутствуют ясность и смысл сведений. Здесь подробно рассказано о химикатах, а на форзаце отображена таблица Менделеева. Среди недостатков выделяют несоответствие задач возрасту школьников. Некоторые формулировки приходится заучивать наизусть.
Читайте также: 12 лучших помад для губ
Е. Е. Минченков Общая методика преподавания химии
Рейтинг: 4.6
Автор этого учебника предлагает поверхностное и глубокое изучение тем. Подобный подход удобен тем, что школьники лучше воспринимают информацию, усваивают сложные химические термины. Особую роль играет практический эксперимент. В учебнике грамотно отобран теоретический материал, есть много примеров, которые поясняют изложенные сведения. Текст свободно воспринимается подростками. Вопросы и задачи помогают закрепить материал, сконцентрироваться на главном.
Текст свободно воспринимается подростками. Вопросы и задачи помогают закрепить материал, сконцентрироваться на главном.
В этом пособии охвачено больше тем, чем в других учебниках. Все, что написано, подкреплено аргументами. Читается издание с большим интересом. Отзывы о нем преимущественно положительные. Книгу сложно найти в печатном варианте, зато она широко доступна в электронном виде.
Химия. 9 класс. Шелинский и Юрова
Рейтинг: 4.5
Завершает рейтинг руководство, которое познакомит учащихся с видами металлов, возможностью применения их в различных областях жизни. В этой книге школьники познакомятся с природой химических связей, строениями предметов, теорией растворов проводников второго рода и т. д. В конце курса учеников ждет сокращенное изложение основ химии органических элементов.
Автором пособия стал преподаватель кафедры химии ЛИТМО, участник ВОВ, главный инженер химического завода, кандидат педагогических наук. В 2010 году профессора Шелинского не стало, но по его книгам до сих пор занимаются многие ученики, чтобы расширить свой кругозор. Педагоги обращаются к его учебникам по химии, если хотят глубже познакомиться с материалом, который сжато передан в других книгах.
В 2010 году профессора Шелинского не стало, но по его книгам до сих пор занимаются многие ученики, чтобы расширить свой кругозор. Педагоги обращаются к его учебникам по химии, если хотят глубже познакомиться с материалом, который сжато передан в других книгах.
Лучшие учебники по химии иностранных авторов
Во всех развитых государствах изучению химии отводится особое место. В России эта наука только начинает набирать популярность. Поэтому всем тем, кто хочет пополнить свои знания в области данной сферы, нужно обязательно познакомиться с работами европейских ученых, которые считают химию областью будущего.
Читайте также: 10 лучших хайлайтеров
Фримантл М. Химия в действии. Часть 1
Рейтинг: 4.9
Пособие Фримантла в двух томах прекрасно подходит для подготовки к Единому государственному экзамену. Оно позволяет восполнить интервалы в школьной программе. Это отличный выбор для студентов-химиков. Весь материал отображен на простом и вразумительном языке. Здесь есть вся необходимая информация о современной науке. В учебнике нет неподтвержденной теории. Он включает исторические данные, выдержки из популярных публикаций, множество примеров и фотоснимков. Присутствуют в книге схематические таблицы и графики. Темы изложены в стандартной последовательности.
Весь материал отображен на простом и вразумительном языке. Здесь есть вся необходимая информация о современной науке. В учебнике нет неподтвержденной теории. Он включает исторические данные, выдержки из популярных публикаций, множество примеров и фотоснимков. Присутствуют в книге схематические таблицы и графики. Темы изложены в стандартной последовательности.
Стоит учесть, что с 1998 года учебник не издается. Его можно найти в библиотеках, в электронной интернет-версии. Встречается он в магазинах, которые специализируются на вторичной торговле печатными изданиями.
Неорганическая химия, Том первый, Шрайвер, Эткинс
Рейтинг: 4.8
Далее в рейтинге располагается ценное издание по неорганической химии, которое было составлено специалистами из Америки и Великобритании. Авторы занимаются педагогической деятельностью. В своей книге они подробно рассматривают концепции теории, в том числе модели химических связей, теории кислот. Особе внимание уделяется актуальным проблемам науки.
Особе внимание уделяется актуальным проблемам науки.
Учебник прекрасно иллюстрирован и содержит богатый справочный материал, много задач разной сложности. На русском языке книга выпускается в двух частях. Это хороший выбор для студентов и педагогов химических факультетов, который позволит расширить свои знания.
Аналитическая химия. Проблемы и подходы. Том 1. Под ред. Р. Кельнера, Ж.-М. Мерме, М. Отто.
Рейтинг: 4.7
Последнее учебное пособие создано авторитетными учеными из организации научной деятельности в Европе. Оно рекомендовано в качестве главного руководства по основам химического анализа для студентов и учителей в высших учебных заведениях. Рассматриваемые темы – компьютерные технологии, хемометрика, физические методы анализа, контроль процессов технологий и т. д.
На русском языке пособие выходит в двух томах под руководством ак. Золотова. Оно доступно в интернете для скачивания. Отзывы о нем в основном одобрительные. Это отличный вариант для тех, кто увлечен химией и хочет связать свою жизнь с этой наукой.
Отзывы о нем в основном одобрительные. Это отличный вариант для тех, кто увлечен химией и хочет связать свою жизнь с этой наукой.
| Оцените статью | |
Всего голосов: 1, рейтинг: 5 |
Химия для чайников (бумажный учебник)
Мы все прирожденные химики. Каждый раз, когда мы готовим, убираемся, принимаем душ, водим машину, используем растворитель, например жидкость для снятия лака с ногтей, или выполняем любую из бесчисленных повседневных действий, связанных со сложными химическими реакциями, мы занимаемся химией. Можно даже сказать, что мы все участвуем в грандиозном химическом эксперименте, который начался с первого человека, который смешал пигменты, чтобы нарисовать наскальную живопись. Почему многие из нас отчаянно сопротивляются изучению химии в молодости? Возможно, это как-то связано с тем, как этому учат в школе.
Почему многие из нас отчаянно сопротивляются изучению химии в молодости? Возможно, это как-то связано с тем, как этому учат в школе.Теперь есть веселый и простой способ выучить основы химии. Изучаете ли вы химию в школе и ищете небольшой помощи в понимании того, чему учат в классе, или вы просто изучаете новые вещи ради них самих, Chemistry For Dummies поможет вам справиться со всеми основы материи и энергии, атомы и молекулы, кислоты и основания и многое другое. За короткое время вы:
- Поймете строение и функции атома
- Пользуетесь Периодической таблицей элементов
- Знаете, что происходит, когда вещество переходит из одного состояния в другое
- Изучите ионную и ковалентную связь
- Получите представление о химических реакции
- Выполнять простые химические расчеты
- Понимать кислоты, основания, рН, антациды и газы
- Разбираться в законах Бойля, Аврогадро и других ключевых химических законах
Содержит примеры химии в действии в повседневной жизни, Chemistry For Dummies — это увлекательное исследование широкого круга вопросов химии, в том числе:
- Состояние вещества, от макроскопического до микроскопического
- Понимание того, как элементы расположены в периодической таблице
- Ядерная химия, радиоактивность и радиоактивный распад
- Положительные и отрицательные ионы и ионные соединения 900 08
- Ковалентная связь в ковалентных соединениях
- Химические реакции, химическое равновесие и электрохимия
- Моль и ее использование для расчета химических реакций
- Великие открытия в области химии по счастливой случайности
- Химия окружающей среды
Написано на простом английском языке базовая математика, Химия для чайников поможет вам быстро освоить основы химии.
Джон Т. Мур Эд.Д. работает учителем более тридцати лет. Многочисленные гранты позволили ему сосредоточиться на профессиональном развитии учителей начальной и средней школы в области естественных наук.
Химия для чайников 2-е издание Джона Т. Мура EdD
Химия для чайников 2-е издание Джона Т. Мура EdD – Мягкая обложка
Химия для чайников, 2-е издание (9781119293460) ранее публиковалось как Химия для чайников, 2-е издание (9781118007303).
Хотя эта версия имеет новую обложку и дизайн для чайников, содержание такое же, как и в предыдущем выпуске, и его не следует рассматривать как новый или обновленный продукт. Посмотрите, как химия работает во всем, от мыла до лекарств и нефти. Мы все прирожденные химики.
Каждый раз, когда мы готовим, убираемся, принимаем душ, водим машину, используем растворитель (например, жидкость для снятия лака) или выполняем любое из бесчисленных повседневных действий, связанных со сложными химическими реакциями, мы занимаемся химией! Так почему же многие из нас отчаянно сопротивляются изучению химии в молодости? Теперь есть веселый и простой способ выучить основы химии. Изучаете ли вы химию в школе и ищете небольшой помощи, чтобы понять, чему учат в классе, или вы просто изучаете новые вещи, «Химия для чайников» знакомит вас со всеми основами материи и энергии. , атомы и молекулы, кислоты и основания и многое другое!
Изучаете ли вы химию в школе и ищете небольшой помощи, чтобы понять, чему учат в классе, или вы просто изучаете новые вещи, «Химия для чайников» знакомит вас со всеми основами материи и энергии. , атомы и молекулы, кислоты и основания и многое другое!
Отслеживает типичный курс химии, давая вам пошаговые уроки, которые вы можете легко понять Содержит основные принципы химии и советы профессоров химии по экономии времени Примеры из реальной жизни обеспечивают повседневный контекст для сложных тем Полный современных, актуальных и обновленных примеров «Химия для чайников», отражающая текущие методы преподавания и протоколы занятий, поможет вам быстро освоить основы химии.
Введение. Часть I: Основные понятия химии.
Глава 1: Что такое химия и зачем мне ее знать?
Глава 2: Рассмотрение химических расчетов.
Глава 3: Материя и энергия.
Глава 4: Что-то меньше атома? Атомная структура.
Глава 5: Периодическая таблица (но без стульев).
Глава 6: Воздушные шары, шины и акваланги: удивительный мир газов.
Часть II: Рог изобилия химических понятий.
Глава 7: Химическая кулинария: Химические реакции.
Глава 8: Крот: сможешь ли ты его выкопать?
Глава 9: Смешивание материи: Решения.
Глава 10: Термохимия: горячий материал.
Глава 11: Кислое и горькое: Кислоты и щелочи.
Часть III: Да будут благословенны узы, которые связывают.
Глава 12: Куда я положил этот электрон? Квантовая теория.
Глава 13: Противоположности притягиваются: ионная связь.
Глава 14: Приятно делиться: ковалентная связь.
Глава 15. Как на самом деле выглядят молекулы? Молекулярная геометрия и гибридизация.
Глава 16: Работа с периодическими трендами.
Глава 17: Изучение связи между межмолекулярными силами и конденсированными состояниями.
Часть IV: Химия окружающей среды: преимущества и проблемы.
Глава 18: Кашель! Кашель! Взломать! Взломать! Загрязнение воздуха.
Глава 19: Изучение плюсов и минусов загрязнения воды.
Глава 20: Ядерная химия: это поразит вас.
Часть V: Часть десятков.
Глава 21: Десять удачных открытий в химии.
Глава 22: Десять (или около того) великих химиков.
Глава 23: Десять потрясающих советов по сдаче химии I.
Глава 24: Десять лучших промышленных химикатов.
Глоссарий.
Индекс.
Полное название: Chemistry For Dummies
Издание: 2-е издание
ISBN-13: 978-1119293460
Формат: Мягкая/мягкая обложка
Издатель: For Dummies (31.05.2016)
Copyright: 2011
Размеры: 7.4 x 9 x 0,8 дюйма
Вес: 1,1 фунта
Рабочая тетрадь по химии для чайников | Отзыв
Эта полезная книга будет полезна учащимся старше 16 лет, которые хотят попрактиковаться в различных типах химических расчетов, встречающихся на уровне AS и выше. Содержание разделено на пять частей (22 главы), и они четко объяснены на вводных страницах, например, часть первая – Знакомство с числами , атомы и элементы – подчеркивает, как химики должны обращаться с числами осторожно и согласно к определенным правилам.
Значки на полях помогают учащимся разобраться с наиболее важными аспектами этой главы, например, значок «запомнить» указывает на то, что они должны знать, а значок «предупреждение» говорит им обратить внимание, иначе им будет трудно понять. Существует множество проработанных примеров, и предоставленные подробные решения будут полезны увлеченным независимым учащимся, которые хотят улучшить свое понимание темы. В конце каждой главы есть множество дополнительных упражнений, и, что более важно, авторы дают не просто числовые ответы, а краткое описание того, как получаются решения.
Главы охватывают многие области, которые являются частью текущих спецификаций химии AS/A2. Ключевые примеры включают моль и стехиометрию, термохимию, кислотно-щелочное равновесие и электрохимию. Шестая глава, посвященная названиям соединений, хорошо структурирована и необходима для прочтения заинтересованными студентами выпускных экзаменов в школе, которые хотят достичь высокого уровня в области неорганической химии. Глава седьмая, Управление могучим кротом , дает хорошее представление о том, насколько велика постоянная Авогадро, утверждая, что она больше, чем количество звезд на небе или количество рыб в море.
Глава седьмая, Управление могучим кротом , дает хорошее представление о том, насколько велика постоянная Авогадро, утверждая, что она больше, чем количество звезд на небе или количество рыб в море.
Это не тот тип книг, которые вы будете читать от корки до корки, но если ваши ученики захотят прочитать весь текст, они найдут много маленьких жемчужин, которые помогут им запомнить некоторые ключевые факты, например, фраза «рыжий кот» — полезный способ запомнить, что восстановление происходит на катоде. Раздел о балансировке окислительно-восстановительных уравнений превосходен и не хуже всего, что я видел.
Поскольку книга ориентирована на рынок США, в ней ничего не говорится об атомной экономике, единицей объема является литр, а не дм 3 , и используются такие названия, как формальдегид и уксусная кислота, а не метаналь и этановая кислота.
Напечатано на некачественной, впитывающей бумаге, интенсивное использование маркера не рекомендуется, так как это затрудняет чтение страницы.
Химия “Химия для чайников” Модульный исследовательский проект SciYeung
Химия для чайников ЗаданиеТорговая марка «Манекены» — чрезвычайно популярная серия обучающих книг «Как помочь».Темы варьируются от садоводства до квантовой механики, где рассматриваются самые разные темы. Книги написаны на языке, понятном обычному непрофессионалу, и содержат множество иллюстраций, иллюстрирующих концепции.
Вот как я представляю задание:
Видео на Youtube
Ваша задача для этого задания (Выберите только 1 из следующих действий)
Написать буклет с инструкциями по разделам этого раздела.
Создайте обучающее видео о разделах устройства.
Создать настольную игру о частях отряда.
Короткое музыкальное видео с правильным текстом о разделах блока
Комикс о разделах блока
Выберите 5 из 6 тем из списка ниже и превратите их в СОБСТВЕННУЮ химию для чайников. «НЕ ОПЦИОНАЛЬНЫЕ» должны быть заполнены. Его нельзя копировать и вставлять, его необходимо написать своими словами
«НЕ ОПЦИОНАЛЬНЫЕ» должны быть заполнены. Его нельзя копировать и вставлять, его необходимо написать своими словами
Вот темы:
Знакомство с атомом – *НЕ ДОПОЛНИТЕЛЬНО*
Что это?
Из каких компонентов состоит атом? Где они расположены?
Что говорит вам каждый из компонентов?
Тема 1: Что такое периодическая таблица?
Что это? Кто это придумал?
Какую информацию можно получить из периодической таблицы?
Как это устроено?
Тема 2: Различные семейства периодической таблицы
Какие они?
Чем они отличаются от других семей?
Как устроены семьи?
Тема 3: Ковалентная и ионная связь и названия соединений
Опишите каждый тип связи
Приведите примеры каждого типа (наглядные примеры)
Опишите, как их назвать (с многоатомными ионами, переходными металлами и ковалентными связями)
Тема 4: Закон Сохранение массы
Что это такое?
Приведите реальный пример того, что это такое.
Уравнения баланса – как вы их делаете?
Тема 5: Типы реакций
Какие существуют 5 типов реакций?
Каковы некоторые примеры каждого из них? Проведите эксперимент из реальной жизни, показывающий 1 из 5 различных типов
Придумайте аналогию/пример 5 различных типов реакций?
Тема 6: Кислоты и основания
Что такое кислоты и основания?
Приведите примеры кислот и оснований?
Какой тип реакции участвует в реакции кислоты и основания?
Пожалуйста, посетите мой магазин, чтобы увидеть больше моих забавных вещей!
Почему бы не скачать это и все мои ресурсы всего за 9 долларов.![]() 95 долларов в месяц или 34,95 доллара в год на моем сайте Teacheridoo.com? Неограниченное количество загрузок по цене ежемесячной подписки.
95 долларов в месяц или 34,95 доллара в год на моем сайте Teacheridoo.com? Неограниченное количество загрузок по цене ежемесячной подписки.
Эта работа находится под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
Источники кислотных дождей Деятельность человека является основной причиной кислотных дождей. За последние несколько десятилетий люди выпустили в воздух так много различных химических веществ, что они изменили состав газов в атмосфере. Электростанции выделяют большую часть диоксида серы и большую часть оксидов азота, когда они сжигают ископаемое топливо, такое как уголь, для производства электроэнергии. Кроме того, выхлопные газы автомобилей, грузовиков и автобусов выделяют в воздух оксиды азота и диоксид серы.Эти загрязняющие вещества вызывают кислотные дожди. Кислотные дожди вызываются реакциями в окружающей среде |



 Различие между органическими и неорганическими соединениями,
содержащими углерод, являются по некоторым представлениям произвольными.Неорганическая
химия изучает химические элементы и образуемые ими простые и сложные вещества
(кроме органических соединений). Обеспечивает создание материалов новейшей
техники. Число неорганических веществ приближается к 400 тысячам.
Различие между органическими и неорганическими соединениями,
содержащими углерод, являются по некоторым представлениям произвольными.Неорганическая
химия изучает химические элементы и образуемые ими простые и сложные вещества
(кроме органических соединений). Обеспечивает создание материалов новейшей
техники. Число неорганических веществ приближается к 400 тысячам. Так, живые существа
производят много неорганических веществ. С другой стороны, почти все
органические соединения можно синтезировать в лаборатории. Однако деление на
различные области химии является актуальным и необходимым, как и раньше,
поскольку механизмы реакций, структура веществ в неорганической и органической
химии различаются. Это позволяет проще систематизировать методы и способы
исследования в каждой из отраслей.
Так, живые существа
производят много неорганических веществ. С другой стороны, почти все
органические соединения можно синтезировать в лаборатории. Однако деление на
различные области химии является актуальным и необходимым, как и раньше,
поскольку механизмы реакций, структура веществ в неорганической и органической
химии различаются. Это позволяет проще систематизировать методы и способы
исследования в каждой из отраслей.

