Химия – с нуля! 1-й шаг. Учимся составлять, называть и понимать формулы веществ | Репетитор Богунова В.Г.
Вы хотите познавать химию и профессионально, и с удовольствием? Тогда вам сюда! Автор методики системно-аналитического изучения химии Богунова В.Г. раскрывает тайны решения задач, делится секретами мастерства при подготовке к ОГЭ, ЕГЭ, ДВИ и олимпиадам
Хочешь сдать ЕГЭ по химии и биологии на 90+? WhatsApp репетитора Богуновой В.Г. +7(903)186-74-55
Сайт репетитора Богуновой В.Г.
Репетитор Богунова В.Г. ВК
Ютуб-канал репетитора Богуновой В.Г.
Полный каталог статей – на авторском сайте в разделе “Статьи репетитора Богуновой В.Г.”
Внимание! Продолжается набор учеников на летний онлайн-курс “Стартап+ (химия с нуля по-взрослому)” с 12 июня по 28 августа.
Подробная информация по WhatsApp +7(903)186-74-55
Обязательно прочитайте мою статью “Летний курс Стартап+ (химия с нуля по-взрослому).Присоединяйся!” Там вы найдете много интересных, важных и нужных учебных материалов как для самостоятельной работы, так и для занятий с репетитором.
Знаете, в чем ошибка большинства преподавателей химии и репетиторов? Желая продемонстрировать степень собственного образования и никчемность знаний абитуриента, они, практически с первых занятий, начинают решать трудные задачи “уровня Белавина” и задания олимпиад. Кстати, профильные лицеи при ведущих медицинских ВУЗах – не исключение (у каждого ученика есть репетиторы). Как результат, у ребенка формируется страх перед сложным и объемным учебным материалом, который необходимо освоить. Нервная система включает защитный механизм – блокирование негативно воспринимаемой информации. И все … у абитуриента развивается стойкое отвращение к предмету! Теперь, чтобы инициировать ребенка на изучение химии, необходим опытный Преподаватель и много-много времени для работы. И нет никакой гарантии, что ученик раскроется и позволит Учителю выстроить у себя в голове стройную систему предмета. Поэтому, в преподавании, как и во врачевании, важны принципы: “Не навреди!”, “Пироги должен печь пирожник, а не сапожник”! Это я к тому, что репетиторов в последнее время развелось, как тараканов, очень много, а преподавателей среди них – днем с огнем не найдешь!
Поэтому, в преподавании, как и во врачевании, важны принципы: “Не навреди!”, “Пироги должен печь пирожник, а не сапожник”! Это я к тому, что репетиторов в последнее время развелось, как тараканов, очень много, а преподавателей среди них – днем с огнем не найдешь!
Не будем спотыкаться о чужие ошибки (своих не допустить бы, тьфу-тьфу), начнем изучение химии с нуля и сделаем первый шаг – составление, название и понимание формул веществ.
Конспект репетитора
Химическая формула – это запись состава вещества с помощью символов элементов и подстрочных индексов.
Индекс (подстрочный) обозначает число атомов данного элемента в молекуле вещества.
Коэффициент – число, стоящее перед химической формулой, обозначает число молекул вещества.
Например, запись 7h3SO4 означает: семь молекул серной кислоты, каждая из которых состоит из двух атомов водорода, одного атома серы и четырех атомов кислорода.
Познакомимся с алгоритмом составления формул веществ на примере бинарных соединений.
Бинарные соединения – вещества, образованные двумя химическими элементами (h3O, Al2S3, PCl5, Nh4 и др.). Поучимся составлять формулы бинарных соединений по конкретному заданию.
Задание
Написать одну из формул и назвать соединение, молекула которого содержит атомы серы и фосфора
Алгоритм составления формул:
1. Выписать символы химических элементов в порядке увеличения их электроотрицательности.
Электроотрицательность (ЭО на схеме) – способность атома притягивать к себе электроны (и свои, и чужие).
2. Определить валентность элементов
Валентность – способность атомов химических элементов образовывать определенное число химических связей.
Высшая валентность (в) равна номеру группы. У первого элемента, стоящего левее, валентность либо определена, либо высшая. В нашем случае валентность фосфора не озвучена, поэтому берем высшую.
Низшая валентность (н) равна “восемь минус номер группы” (определяется только для элементов IVA-VIIA групп). У второго элемента, стоящего правее, валентность всегда низшая. В нашем случае сера – элемент VIA-группы, ее низшая валентность равна 8-6=2.
Запомнить: у кислорода валентность всегда 2, у фтора – всегда 1!
3. Определить число атомов каждого элемента (нижние индексы).
Для этого находим наименьшее общее кратное значений валентностей и делим его на каждое из них.
Для справки
Наименьшее общее кратное двух целых чисел m и n есть наименьшее натуральное число, которое делится на m и n без остатка.
4. Назвать вещество
Название бинарного соединения состоит из двух слов.
Первое слово – название второго элемента, стоящего правее (с низшей валентностью) с добавлением суффикса -ИД. В нашем случае – сульфид. Таким образом, суффикс -ИД указывает на то, что этот элемент имеет низшую валентность “восемь минус номер группы”.
Второе слово – название первого элемента, стоящего левее (с более низкой электроотрицательностью) – в родительном падеже. В нашем случае – фосфора (кого? чего?).
Если первый элемент может иметь несколько значений валентности, то в конце названия указывается конкретное значение валентности в скобках римскими цифрами. В нашем случае фосфор может иметь валентности 3 и 5, поэтому название вещества – сульфид фосфора (V).
Репетитор Богунова В.Г. с ученикамиРепетитор Богунова В. Г. с учениками
Г. с учениками
Вы хотите поступить в медицинский? Обязательно посетите мой сайт Репетитор по химии и биологии. Здесь вы найдете огромное количество задач, заданий, теоретического материала и познакомитесь с моими учениками, многие из которых уже давно закончили ВУЗы и, работая врачами, спасают наши с вами жизни.
На странице ВК я анонсирую свои публикации, вебинары, уроки, рассказываю и показываю решение задач и заданий, выкладываю новинки теоретического материала, конспекты и лекции. Добавляйтесь ко мне в друзья, и вы всегда будете в курсе всех событий, связанных с подготовкой к ЕГЭ, ДВИ, олимпиадам!
Полный каталог статей репетитора Богуновой В.Г. вы найдете на странице сайта Статьи репетитора
Подписывайтесь на YouTube-канал Репетитор по химии и биологии.Здесь ежедневно появляются новые вебинары, видео-уроки, видео-консультации, видео-решения.
Пишите мне в WhatsApp +7(903)186-74-55, я отвечу вам обязательно.
Приходите ко мне на занятия, я помогу вам фундаментально изучить химию и биологию, научу решать любые задачи, даже самые сложные.
Репетитор по химии и биологии кбн В.Богунова
Химия онлайн с нуля. Эффективное самостоятельное изучение химии
Если вы поступили в университет, но к этому времени так и не разобрались в этой нелегкой науке, мы готовы раскрыть вам несколько секретов и помочь изучить органическую химию с нуля (для “чайников”). Вам же остается только читать и внимать.
Основы органической химии
Органическая химия выделена в отдельный подвид благодаря тому, что объектом ее изучения является все, в составе чего есть углерод.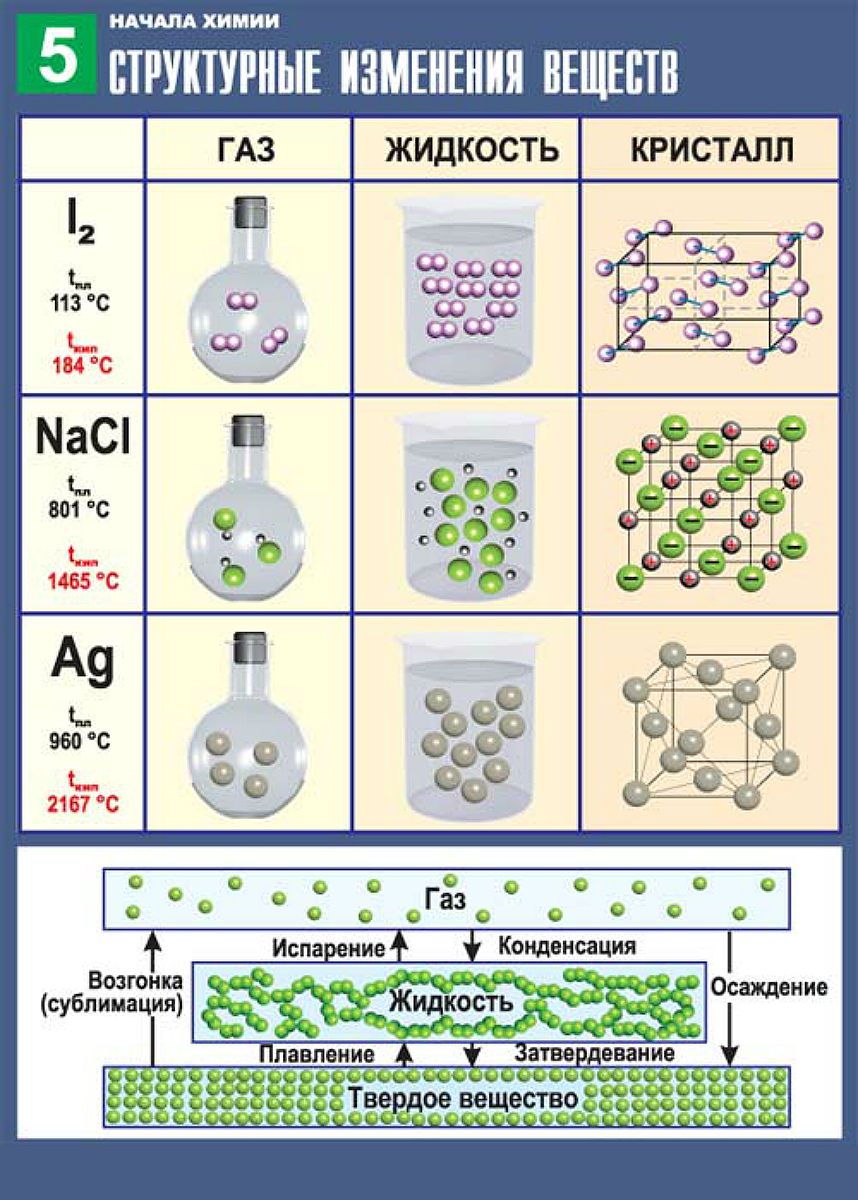
Органическая химия – раздел химии, который занимается изучением соединения углерода, структуру таких соединений, их свойства и методы соединения.
Как оказалось, углерод чаще всего образует соединения со следующими элементами – H, N, O, S, P. Кстати, эти элементы называются органогенами .
Органические соединения, количество которых сегодня достигает 20 млн, очень важны для полноценного существования всех живых организмов. Впрочем, никто и не сомневался, иначе человек просто закинул бы изучение этого непознанного в долгий ящик.
Цели, методы и теоретические представления органической химии представлены следующим:
- Разделение ископаемого, животного или растительного сырья на отдельные вещества;
- Очистка и синтез разных соединений;
- Выявление структуры веществ;
- Определение механики протекания химических реакций;
- Нахождение зависимости между структурой и свойствами органических веществ.

Немного из истории органической химии
Вы можете не верить, но еще в далекой древности жители Рима и Египта понимали кое-что в химии.
Как мы знаем, они пользовались натуральными красителями. А нередко им приходилось использовать не готовый естественный краситель, а добывать его, вычленяя из цельного растения (например, содержащиеся в растениях ализарин и индиго).
Можем вспомнить и культуру употребления алкоголя. Секреты производства спиртных напитков известны в каждом народе. Причем многие древние народы знали рецепты приготовления «горячей воды» из крахмал- и сахарсодержащих продуктов.
Так продолжалось долгие, долгие годы, и только в 16-17 веках начались какие-то изменения, небольшие открытия.
В 18 веке некто Шееле научился выделять яблочную, винную, щавелевую, молочную, галловую и лимонную кислоту.
Тогда всем стало ясно, что продукты, которые удалось выделить из растительного или животного сырья, имели много общих черт.
Несмотря на то, что сама органическая химия как наука появилась лишь в 1828 году (именно тогда господину Вёлеру удалось выделить мочевину путем упаривания цианата аммония), в 1807 году Берцелиус ввел первый термин в номенклатуру в органической химии для чайников:
Раздел химии, который изучает вещества, полученные из организмов.
Следующий важный шаг в развитии органический химии – теория валентности, предложенная в 1857 году Кекуле и Купером, и теория химического строения господина Бутлерова от 1861 года. Уже тогда ученые стали обнаруживать, что углерод – четырехвалентен и способен образовывать цепи.
В общем, с эти самых пор наука регулярно испытывала потрясения и волнения благодаря новым теориям, открытиям цепочкам и соединениям, что позволяло так же активно развиваться органической химии.
Сама наука появилась благодаря тому, что научно-технический прогресс не в состоянии был стоять на месте. Он продолжал и продолжал шагать, требуя новых решений. И когда каменноугольной смолы в сфере промышленности перестало хватать, людям просто пришлось создать новый органический синтез, который со временем перерос в открытие невероятно важного вещества, которое и по сей день дороже золота – нефть. Кстати, именно благодаря органической химии на свет появилась ее «дочка» – поднаука, которая получила название «нефтехимия».
Но это уже совсем другая история, которую вы можете изучить сами. Далее мы предлагаем вам посмотреть научно-популярное видео про органическую химию для чайников:
Ну а если вам некогда и срочно нужна помощь профессионалов , вы всегда знаете, где их найти.
Глава 1.
Общие химические и экологические закономерности.
С чего начинается химия?
Cложный ли это вопрос? На него каждый ответит по-своему.
В середней школе учащиеся изучают химию в течение ряда лет. Многие довольно хорошо сдают выпускной экзамен по химии. Однако…
Многие довольно хорошо сдают выпускной экзамен по химии. Однако…
Беседы с абитуриентами и затем и студентами первых курсов говорят о том, что остаточные знания по химии после средней школы незначительные. Одни путаются в различных определениях и химических формулах, а другие вообще не могут воспроизвести даже основные понятия и законы химии, не говоря уже о понятиях и законах экологии.
У них химия так и не начиналась.
Химия, по-видимому, начинается с глубокого освоения ее основ, и прежде всего, основных понятий и законов.
1.1. Основные химические понятия.
В таблице Д.И.Менделеева рядом с символом элемента стоят цифры. Одна цифра обозначает порядковый номер элемента, а вторая атомную массу. Порядковый номер имеет свой физический смысл. О нем мы будем вести разговор позже, здесь остановимся на атомной массе и выделим в каких единицах она измеряется.
Следует сразу оговориться, что атомная масса элемента, приведенная в таблице, величина относительная.
Атомная масса , приведенная в таблице, является массой атома, выраженной в атомных единицах массы. Величина безразмерная. Конкретно для каждого элемента атомная масса показывает, во сколько раз масса данного атома больше или меньше 1/12 части массы атома углерода.
Аналогичное можно сказать и о молекулярной массе.
Молекулярная масса – это масса молекулы, выраженная в атомных единицах массы. Величина тоже относительная. Молекулярная масса конкретного вещества равна сумме масс атомов всех элементов, входящих в состав молекулы.
Важным понятием химии является понятие «моль». Моль – такое количество вещества, которое содержит 6,02*10 23
структурных единиц /атомов, молекул, ионов, электронов и т. д./. Моль атомов, моль молекул, моль ионов и т.д.
д./. Моль атомов, моль молекул, моль ионов и т.д.
Масса одного моля данного вещества называется его молярной /или мольной/ массой. Она измеряется в г/моль или кг/моль и обозначается буквой «М». Например, молярная масса серной кислоты М Н 2 SO4 =98г/моль.
Следующее понятие «Эквивалент». Эквивалентом /Э/ называют такое весовое количество вещества, которое взаимодействует с одним молем атомов водорода или замещают такое его количество в химических реакциях. Следовательно, эквивалент водорода Э Н равен единице. /Э Н =1/. Эквивалент кислорода Э О равен восьми /Э О =8/.
Различают химический эквивалент элемента и химический эквивалент сложного вещества.
Эквивалент элемента – величина переменная. Она зависит от атомной массы /А/ и валентности /В/, которую элемент имеет в конкретном соединении. Э=А/В. Например, определим эквивалент серы в оксидах SO 2 и SO 3 . В SO 2 Э S =32/4=8, а в SO 3 Э S =32/6=5,33.
Молярную массу эквивалента, выраженную в граммах, называют эквивалентной массой. Следовательно, эквивалентная масса водорода МЭ Н
=1г/моль, эквивалентная масса кислорода МЭ О
=8г/моль.
Следовательно, эквивалентная масса водорода МЭ Н
=1г/моль, эквивалентная масса кислорода МЭ О
=8г/моль.
Химический эквивалент сложного вещества /кислоты, гидроксида, соли, оксида/– такое количество соответствующего вещества, которое взаимодействует с одним молем атомов водорода, т.е. с одним эквивалентом водорода или замещает такое количество водорода или любого другого вещества в химических реакциях.
Эквивалент кислоты /Э К / равен частному от деления молекулярной массы кислоты на число атомов водорода, участвующих в реакции. Для кислоты H 2 SO 4 , когда оба атома водорода вступают в реакцию H 2 SO 4 +2NaOH=Na 2 SO+2H 2 O эквивалент будет равен Э Н 2 SO4 = М Н 2 SO 4 /n Н =98/2=49
Эквивалент гидроксида /Э гидр. / определяется как частное от деления молекулярной массы гидроксида на число гидроксогрупп, вступающих в реакцию. Например, эквивалент NaOH будет равен: Э NaOH =М NaOH /n ОН =40/1=40.
Эквивалент соли /Э соли
/ можно рассчитать, поделив ее молекулярную массу на произведение числа атомов металла, вступающих в реакцию, и их валентность.
Эквивалент оксида /Э ок / можно определить, как сумму эквивалентов соответствующих элемента и кислорода. Например, эквивалент СО 2 будет равен сумме эквивалентов углерода и кислорода: Э СО 2 =Э С +Э О =3+8=7.
Для газообразных веществ удобно пользоваться эквивалентными объемами /Э V /. Так как при нормальных условиях моль газа занимает объем 22,4л, то исходя из этой величины, легко определить эквивалентный объем любого газа. Рассмотрим водород. Мольная масса водорода 2г занимает объем 22,4л, тогда его эквивалентная масса 1г занимает объем 11,2л /или 11200мл /. Следовательно Э V Н =11,2л. Эквивалентный объем хлора равен 11,2л /Э VCl =11,2л/. Эквивалентный объем СО равен 3,56 /Э VC О =3,56л/.
Химический эквивалент элемента или сложного вещества используется в стехиометрических расчетах обменных реакций, а в соответствующих расчетах окислительно–восстановительных реакций применяют уже окислительный и восстановительный эквиваленты.
Окислительный эквивалент определяют как частное от деления молекулярной массы окислителя на число электронов, которое он принимает в данной окислително–восстановительной реакции.
Восстановительный эквивалент равен молекулярной массе восстановителя поделенной на число электронов, которое он отдает в данной реакции.
Напишем окислително–восстановительную реакцию и определим эквивалент окислителя и восстановителя:
5N 2 aS+2KMnO 4 +8H 2 SO 4 =S+2MnSO 4 +K 2 SO 4 +5Na 2 SO 4 +8H 2 O
Окислителем в этой реакции является перманганат калия. Эквивалент окислителя будет равен массе KMnO 4 деленной на число электронов, принятых окислителем в реакции (nе=5). Э KMnO 4 =М KMnO 4 /nе=158/5=31,5. Молярная масса эквивалента окислителя KMnO 4 в кислой среде равна 31,5г/моль.
Эквивалент восстановителя Na 2 S будет: Э Na 4 S =М Na 4 S /nе=78/2=39. Молярная масса эквивалента Na 2 S равна 39г/моль.
В электрохимических процессах, в частности при электролизе веществ, пользуются электрохимическим эквивалентом. Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Валентность . При взаимодействии атомов между ними образуется химическая связь. Каждый атом может образовывать только определенное количество связей. Количество связей предопределяет такое уникальное свойство каждого элемента, которое называют валентностью. В наиболее общем виде валентностью называют способность атома образовывать химическую связь. За единицу валентности принимают одну химическую связь, которую способен образовать атом водорода. В связи с этим, водород является одновалентным элементом, а кислород – двухвалентным, т.к. с атомом кислорода могут образовывать связь не более двух водородов.
Умение определять валентность каждого элемента, в том числе и в химическом соединении, является необходимым условием успешного усвоения курса химии.
С валентностью соприкасается и такое понятие химии как степень окисления . Подстепенью окисления понимают тот заряд, который имеет элемент в ионном соединении или имел бы в ковалентном соединении, если бы общая электронная пара бала бы полностью смещена к более электроотрицательному элементу. Степень окисления имеет не только цифровое выражение, но и соответствующий знак заряда (+) или (–). Валентность не имеет этих знаков. Например, в H 2 SO 4 степень окисления: водорода +1, кислорода –2, серы +6, а валентность, соответственно, будет 1, 2, 6.
Валентность и степень окисления в числовых значениях не всегда совпадают по величине. Например, в молекуле этилового спирта СН 3 –СН 2 –ОН валентность углерода 6, водорода 1, кислорода 2, а степень окисления, например, углерода первого –3, второго –1: –3 СН 3 – –1 СН 2 –ОН.
1.2. Основные экологические понятия.
За последнее время понятие “экология” глубоко входит в наше сознание. Это понятие, введенное еще в 1869г Э. Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
В учебниках биологии экологию определяют как науку о взаимоотношениях живых организмов и среды их обитания. Практически созвучное определение экологии дает Б.Небел в своей книге «Наука об окружающей среде» – Экология – наука о различных аспектах взаимодействия организмов между собой и с окружающей средой. В других источниках можно встретить и более широкое толкование. Например, Экология – 1/. Наука, изучающая отношение организмов и их системных совокупностей и окружающей среды; 2/. Совокупность научных дисциплин, исследующих взаимоотношение системных биологических структур /от макромолекул до биосферы/ между собой и с окружающей средой; 3/. Дисциплина, изучающая общие законы функционирования экосистем различного иерархического уровня; 4/. Комплексная наука, исследующая среду обитания живых организмов; 5/. Исследование положения человека как вида в биосфере планеты, его связей с экологическими системами и воздействие на них; 6/. Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
Всем известно, что школьный курс является той основой, которая дает самые необходимые знания о мире, в котором мы живем. Это действительно так и такой предмет как химия прекрасное тому подтверждение, так как, по сути, абсолютно все, что нас окружает и есть химия — химические элементы, их соединения, процессы взаимодействия и т.д. Поэтому неудивительно, что в школьный курс входит много тем по химии .
Важность изучения химииИзучая предмет химии, школьник не только познает мир и определенные законы его существования, но и развивает память, логическое и абстрактное мышление, аналитические способности и интеллектуальные возможности в целом. ЕГЭ по химии, который является предметом по выбору, есть ни что иное как закономерное подведение итогов учебно-образовательной деятельности.
Кроме того, успешная сдача ЕГЭ по химии после окончания школы облегчит получение высшего образования, ведь его результаты высшими учебными заведениями засчитываются как вступительные экзамены. Поэтому нужно относиться к этому экзамену как к важному этапу в вашем будущем. Благодаря полученным знаниям будет проще потом осваивать другие сложные предметы в университете.
Что представляет собой подготовка к ЕГЭ по химииКонечно, залогом успешного изучения и усвоения материала является постоянная работа — это касается абсолютно всех предметов. Однако такой специфический предмет как химия, зачастую требует особого подхода и применения дополнительных методов обучения. Например, таковыми являются самостоятельная работа или систематические занятия с репетитором. Но что делать, когда возможности для дополнительных занятий с преподавателем нет, а некоторые разобрать по учебнику практически не реально, впрочем, как и систематизировать все полученные знания, когда это необходимо для подготовки к ЕГЭ по химии?
Сегодня существует прекрасная возможность для дополнительного образования, расширения, углубления знаний и закрепления пройденных материалов — химия онлайн бесплатно. Такие уроки основаны на многолетнем педагогическо-психологическом опыте. Всемирная сеть в этом случае становится надежным другом и помощником современной молодежи, предлагая изучение различных тем по химии, включая различные методы подачи материала — видеоуроки с пояснениями, примерами опытов, решением практических задач и многое другое, систематизированные оптимальным образом электронные конспекты и таблицы.
Такие уроки основаны на многолетнем педагогическо-психологическом опыте. Всемирная сеть в этом случае становится надежным другом и помощником современной молодежи, предлагая изучение различных тем по химии, включая различные методы подачи материала — видеоуроки с пояснениями, примерами опытов, решением практических задач и многое другое, систематизированные оптимальным образом электронные конспекты и таблицы.
Эта наука столь сложна, сколь и интересна. Однако уроки химии онлайн позволяют наиболее эффективно усвоить даже самую сложную тему, а при необходимости — проконсультироваться с квалифицированным преподавателем, в том числе и по вопросам, касающимся ЕГЭ по химии. Все это делает обучение легким и понятным, каждый может избежать сложных вопросов, разобраться в темах, которые пропустил ранее.
ИтогоЗанимаясь химией онлайн и бесплатно , вы в доступной для усвоения форме перенимаете многолетний опыт и получаете багаж систематизированных знаний. Каждый может выбрать для себя различные режимы и варианты обучения. Выпускники могут повторять пройденный в школе материал и восполнять имеющиеся пробелы в знаниях, выполняя задания различной сложности и изучая темы по химии по той системе, на которой и основан ЕГЭ. Конечно, готовых ответов никто не предоставит, тем более что каждый год список вопросов и заданий меняется. Однако структура в основном остается прежней, позволяя разработчикам совершенствовать эффективность оценки, а учащимся — наиболее полно раскрывать свой потенциал. Возможно, это поможет и школам показывать лучшую успеваемость своих учеников.
Выпускники могут повторять пройденный в школе материал и восполнять имеющиеся пробелы в знаниях, выполняя задания различной сложности и изучая темы по химии по той системе, на которой и основан ЕГЭ. Конечно, готовых ответов никто не предоставит, тем более что каждый год список вопросов и заданий меняется. Однако структура в основном остается прежней, позволяя разработчикам совершенствовать эффективность оценки, а учащимся — наиболее полно раскрывать свой потенциал. Возможно, это поможет и школам показывать лучшую успеваемость своих учеников.
Кроме того, уроки химии онлайн — это удобно, а также может пригодиться как практикующим преподавателям для перенятия опыта, так и родителям, для того чтобы быть в курсе того, как сегодня строится процесс обучения их детей. Занятия химией онлайн помогут освежить знания будущим абитуриентам, желающим получить еще одно образование. Поэтому трудно поспорить с тем, что благодаря возможностям Интернета учиться становится проще абсолютно всем.
Еще в средней школе многие ученики сталкиваются с вопросом, как выучить химию самостоятельно с нуля, потому что эта наука редко усваивается с первого раза. Школьные учителя часто не задумываются, что дети не получают весь необходимый багаж знаний, позволяющий изучать науку на более сложном уровне. Поэтому ребята не понимают все новые и новые задачи, делая вывод о своей плохой предрасположенности к предмету. На самом деле пробелы в знаниях могут возникать не из-за проблем с мышлением, а из-за неправильной методики школьного обучения.
Школьные учителя часто не задумываются, что дети не получают весь необходимый багаж знаний, позволяющий изучать науку на более сложном уровне. Поэтому ребята не понимают все новые и новые задачи, делая вывод о своей плохой предрасположенности к предмету. На самом деле пробелы в знаниях могут возникать не из-за проблем с мышлением, а из-за неправильной методики школьного обучения.
Поговорим о том, как выучить химию самостоятельно с нуля в домашних условиях. Этот вопрос актуален и для выпускников школ, которые собираются сдавать ЕГЭ и поступать в университеты.
Многие студенты, которые учатся в медицинских университетах, сталкиваются с химией каждый день. И при этом далеко не каждый из них хорошо знал эту науку в школе. Вот какие советы они дают подрастающему поколению:
- Для сдачи экзамена нужны знания всего школьного курса химии. А вот для обучения в университете понадобятся только азы неорганики, всему остальному вас научат опытные профессора. Поэтому развивайте краткосрочную память.
 Всю лишнюю информацию после сдачи ЕГЭ вам придется выбросить из головы.
Всю лишнюю информацию после сдачи ЕГЭ вам придется выбросить из головы. - Занятия с репетитором принесут гораздо больше пользы, чем самостоятельные. Однако если у вас нет возможности посещать индивидуальные уроки, не отчаивайтесь, поскольку химию можно выучить и самому, но для этого придется упорно поработать.
- Помните о том, что человечество не придумало еще более эффективной методики изучения дисциплин, чем упорная работа над своими знаниями и умениями. Постоянная практика – это ваш ключ к успеху.
Именно непрерывность в обучении является ключевым фактором достижения цели. Для эффективных занятий вам нужно создать соответствующий психологический настрой.
Многих учеников волнует не столько качество полученных знаний, сколько сроки, которые придется потратить на обучение. Поверьте, чем тщательнее вы изучите азы науки, чем понятнее для вас будет смысл каждого уравнения, тем быстрее вы освоите более сложные темы. В данном случае Трудно вам будет только в самом начале. Вникните в суть базовых понятий, а дальше осознание каждого химического закона само придет вам в голову.
Вникните в суть базовых понятий, а дальше осознание каждого химического закона само придет вам в голову.
Только не обращая внимания на сроки, вы сможете выучить химию быстро. За месяц это сделать реально, если речь идет о школьном курсе. Обычно такую цель перед собой ставят ученики, которые готовятся к сдаче экзамена. Воспользуйтесь методикой, предложенной ниже, для создания соответствующего психологического настроя.
Мотивация – ключ к успеху
Чтобы создать для себя соответствующую мотивацию и удержать ее на протяжении всего времени обучения, воспользуйтесь такими рекомендациями:
- Поставьте перед собой цель, сформулируйте ее, четко осознавая, какого результата вы хотите добиться.
- Помните, что не следует пытаться выучить большой объем информации за короткое время. Она не задержится в ваших мыслях надолго, а все формулы сольются воедино.
- Теоретический материал не будет понятым вами до конца, если вы его не закрепите, решая практические задания.
 К тому же ваша самооценка значительно повысится, если вы будете уметь решать задачи.
К тому же ваша самооценка значительно повысится, если вы будете уметь решать задачи. - Устраивайте для себя зачеты, на которых вы будете проверять степень освоенности материала.
Химия – это всего лишь наука. Человеческий мозг устроен таким образом, что мы можем запомнить и понять абсолютно любую информацию. Поэтому перестаньте внушать себе, что химия – это не ваше, тогда у вас все получится.
Побудьте педагогом
Как бы странно это ни звучало, лучше всего вы усвоите материал, если объясните его кому-то. Выучили новую тему, но не уверены, что поняли ее до конца? Найдите человека, который совсем не разбирается в ней, и объясните ему суть материала. Поверьте, после этого урока, на котором вы будете выступать в роли педагога, знаний прибавится не только у вашего «ученика», но и у вас.
Почему химия является проблемным предметом
Обычно химия изначально не вызывает восторга у школьников. Уже после первого урока большинство детей ставят крест на изучении этой науки, считая, что способностей у них нет. Это происходит из-за того, что с детства нам внушают, что химия – это наука, которая подарила человечеству массу интересных экспериментов, удивительных зрелищ и потрясающих нововведений. Когда ученики средней школы приходят на первый урок, они готовятся получить незабываемые впечатления и поучаствовать в проведении интересных опытов. Вместо этого школьники видят только сухую теорию и множество непонятных задач. Они разочаровываются в предмете, а когда наступает время сдачи экзамена, понимают, что знаний у них нет.
Это происходит из-за того, что с детства нам внушают, что химия – это наука, которая подарила человечеству массу интересных экспериментов, удивительных зрелищ и потрясающих нововведений. Когда ученики средней школы приходят на первый урок, они готовятся получить незабываемые впечатления и поучаствовать в проведении интересных опытов. Вместо этого школьники видят только сухую теорию и множество непонятных задач. Они разочаровываются в предмете, а когда наступает время сдачи экзамена, понимают, что знаний у них нет.
В этом присутствует вина взрослых людей. Ребенок должен понимать, что зрелища в химии формируются через упорную работу, только приложив определенные усилия, можно проводить интересные эксперименты.
Сдача ЕГЭ
Выпускники часто задумываются о том, как выучить химию самостоятельно с нуля, чтобы сдать ЕГЭ. Ответ на этот вопрос очень простой. Нужно всего лишь учить химию, не задумываясь об экзаменах. Ваши знания будут гораздо качественнее и глубже, если вы будете осваивать предмет для себя, а не для поступления в университет. Вникнув в суть науки, следуя вышеперечисленным советам, вы без труда сможете написать тесты на
Вникнув в суть науки, следуя вышеперечисленным советам, вы без труда сможете написать тесты на
М.: 201 7. – 3 51 с.
Самоучитель основан на методике, которую автор с
успехом использует более 20 лет. С её помощью множество школьников смогли
поступить на химические факультеты и в медицинские вузы. Эта книга – именно
Самоучитель, а не Учебник. Вы не столкнётесь здесь с простым описанием научных
фактов и свойств веществ. Материал структурирован таким образом, что,
встретившись со сложными вопросами, которые вызывают затруднения, вы сразу же
найдёте пояснение автора. В конце каждой главы приводятся проверочные задания и
упражнения для закрепления материала. Любознательному читателю, который просто
хочет расширить свой кругозор, Самоучитель даст возможность освоить этот предмет
«с нуля». Прочитав его, вы не сможете не влюбиться в эту интереснейшую науку –
химию!
Формат: pdf
Размер: 2,7 Мб
Смотреть, скачать: drive. google
google
Оглавление
От автора 7
ЧАСТЬ 1. ЭЛЕМЕНТЫ ОБЩЕЙ ХИМИИ 9
Глава 1. Основные понятия и законы предмета «Химия» 9
1.1. Простейшие понятия: вещество, молекула, атом, химический элемент 9
1.2. Простые и сложные вещества. Валентность 13
1.3. Уравнения химических реакций 17
Глава 2. Основные классы неорганических соединений 23
2.1. Оксиды 23
2.2. Кислоты 32
2.3. Основания 38
2.4. Соли 44
Глава 3. Элементарные сведения о строении атома 55
3.1. Структура Периодической системы Менделеева 55
3.2. Ядро атома. Изотопы 57
3.3. Распределение электронов в поле ядра атома 60
3.4. Строение атома и свойства элементов 65
Глава 4. Понятие о химической связи 73
4.1. Ионная связь 73
4.2. Ковалентная связь 75
4.3. Химическая связь и агрегатные состояния вещества. Кристаллические решётки
80
Глава 5. Скорость химической реакции 87
5.1. Зависимость скорости химической реакции от различных факторов 87
5. 2. Обратимость химических процессов. Принцип Ле-Шателье 95
2. Обратимость химических процессов. Принцип Ле-Шателье 95
Глава 6. Растворы 101
6.1. Понятие о растворах 101
6.2. Электролитическая диссоциация 105
6.3. Ионно-молекулярные уравнения реакций 111
6.4. Понятие о рН (водородном показателе) 113
6.5. Гидролиз солей 116
Глава 7. Понятие об окислительно-восстановительных реакциях123
ЧАСТЬ 2. ЭЛЕМЕНТЫ НЕОРГАНИЧЕСКОЙ ХИМИИ 130
Глава 8. Общие свойства металлов 130
8.1. Внутреннее строение и физические свойства металлов 131
8.2. Сплавы 133
8.3. Химические свойства металлов 135
8.4. Коррозия металлов 139
Глава 9. Щелочные и щёлочноземельные металлы 142
9.1. Щелочные металлы 142
9.2. Щелочноземельные металлы 145
Глава 10. Алюминий 153
Глава 11. Железо 158
11.1. Свойства железа и его соединений 158
11.2. Получение железа (чугуна и стали) 160
Глава 12. Водород и кислород 163
12.1. Водород 163
12.2. Кислород 165
12.3. Вода 166
Глава 13. Углерод и кремний 170
Углерод и кремний 170
13.1. Строение атома и свойства углерода 170
13.2. Свойства соединений углерода 173
13.3. Строение атома и свойства кремния 176
13.4. Кремниевая кислота и силикаты 178
Глава 14. Азот и фосфор 182
14.1. Строение атома и свойства азота 182
14.2. Аммиак и соли аммония 184
14.3. Азотная кислота и её соли 187
14.4. Строение атома и свойства фосфора 189
14.5. Свойства и значение соединений фосфора 191
Глава 15. Сера 195
15.1. Строение атома и свойства серы 195
15.2. Сероводород 196
15.3. Сернистый газ и сернистая кислота 197
15.4. Серный ангидрид и серная кислота 198
Глава 16. Галогены 202
16.1. Строение атома и свойства галогенов 202
16.2. Соляная кислота 205
РАЗДЕЛ 3. ЭЛЕМЕНТЫ ОРГАНИЧЕСКОЙ ХИМИИ 209
Глава 17. Основные понятия органической химии 210
17.1. Предмет органической химии. Теория строения органических веществ 210
17.2. Особенности строения органических соединений 212
17. 3. Классификация органических соединений 213
3. Классификация органических соединений 213
17.4. Формулы органических соединений 214
17.5. Изомерия 215
17.6. Гомологи 217
17.7. Названия углеводородов. Правила международной номенклатуры 218
Глава 18. Алканы 225
18.1. Понятие об алканах 225
18.2. Гомологический ряд, номенклатура, изомерия 225
18.3. Строение молекул 226
18.4. Свойства алканов 226
18.5. Получение и применение алканов 229
Глава 19. Алкены 232
19.1. Гомологический ряд, номенклатура, изомерия 232
19.2. Строение молекул 234
19.3. Свойства алкенов 234
19.4. Получение и применение алкенов 238
19.5. Понятие об алкадиенах (диены) 239
Глава 20. Алкины 244
20.1. Определение. Гомологический ряд, номенклатура, изомерия 244
20.2. Строение молекул 245
20.3. Свойства алкинов 246
20.4. Получение и применение ацетилена 248
Глава 21. Циклические углеводороды. Арены 251
21.1. Понятие о циклических углеводородах. Циклоалканы 251
21. 2. Понятие об ароматических углеводородах 252
2. Понятие об ароматических углеводородах 252
21.3. История открытия бензола. Строение молекулы 253
21.3. Гомологический ряд, номенклатура, изомерия 255
21.4. Свойства бензола 256
21.5. Свойства гомологов бензола 259
21.6. Получение бензола и его гомологов 261
Глава 22. Спирты 263
22.1. Определение 263
22.2. Гомологический ряд, номенклатура, изомерия 264
22.3. Строение молекул 265
22.4. Свойства одноатомных спиртов 266
22.5. Получение и применение спиртов (на примере этилового спирта) 268
22.6. Многоатомные спирты 269
22.7. Понятие о фенолах 271
Глава 23. Альдегиды 276
23.1. Определение. Гомологический ряд, номенклатура, изомерия 276
23.2. Строение молекул 277
23.3. Свойства альдегидов 278
23.4. Получение и применение альдегидов на примере уксусного альдегида 280
Глава 24. Карбоновые кислоты 282
24.1. Определение 282
24.2. Гомологический ряд, номенклатура, изомерия 283
24.3. Строение молекул 284
24. 4. Свойства кислот 285
4. Свойства кислот 285
24.5. Получение и применение кислот 287
Глава 25. Сложные эфиры. Жиры 291
Глава 26. Углеводы 297
Глава 27. Азотсодержащие соединения 304
27.1. Амины 304
27.2. Аминокислоты 306
27.3. Белки 308
Глава 28. Понятие о полимерах 313
ЧАСТЬ 4. РЕШЕНИЕ ЗАДАЧ 316
Глава 29. Основные расчётные понятия 317
Глава 30. Задачи, решаемые по стандартным формулам 320
30.1. Задачи по теме «Газы» 320
30.2. Задачи по теме «Способы выражения концентрации растворов» 324
Глава 31. Задачи, решаемые по уравнениям реакций 330
31.1. Оформление расчётов по уравнениям реакций 330
31.2. Задачи по теме «Количественный состав смесей» 333
31.3. Задачи на «избыток-недостаток» 337
31.4. Задачи на установление формулы вещества 342
31.5. Задачи, в которых учитывается «выход» полученного вещества 349
Уроки химии для начинающих: бесплатные видео для самостоятельного обучения
Уроки химии для начинающих: бесплатные видео для самостоятельного обучения
Химия – точная наука об окружающих веществах и явлениях. Изучение предмета помогает глубже вникнуть в мироздание и жизнь собственного организма. Любое бытовое действие, от зажжения спички до приготовления обеда, завязано на химических процессах. А современная фармацевтика, медицина и косметология тем более.
Изучение предмета помогает глубже вникнуть в мироздание и жизнь собственного организма. Любое бытовое действие, от зажжения спички до приготовления обеда, завязано на химических процессах. А современная фармацевтика, медицина и косметология тем более.
Мы собрали лучшие бесплатные видео с уроками по химии, понятные и интересные. Подойдут для желающих подготовиться к ЕГЭ, улучшить успеваемость по предмету, освежить или углубить старые знания.
Основные понятия и определения
Бич любого постигающего новую область знаний – терминология. Придется изучить основные законы, дефиниции, термины. Главное – запоминать осознанно, без изнуряющей зубрежки. Тогда наука будет вызывать интерес, а не отторжение. Если до конца понять, осознать суть каждого понятия, последующие уроки станут намного проще и эффективнее. Помочь собственному мозгу быстрее зафиксировать новые понятия можно с помощью записей и шпаргалок. Чем чаще что-то мелькает перед глазами, тем быстрее откладывается. Вести конспект любого урока (аудио, видео, текстового) – самая полезная привычка. Во-первых, дисциплинирует, во-вторых, включает механическую и зрительную память.
Вести конспект любого урока (аудио, видео, текстового) – самая полезная привычка. Во-первых, дисциплинирует, во-вторых, включает механическую и зрительную память.
Агрегатные состояния
Каждое вещество имеет определенный вид, называемый агрегатным состоянием. Легко определяется на вид и ощупь. Даже ребенок с закрытыми глазами определит жидкую воду и твердый пластик. О существовании газообразных тел узнают гораздо позже. Но самое интересное – возможность перехода из одного состояния в другое, похожее на волшебство. Самый простой пример – когда жидкость под воздействием разных температур превращается то в воздушный пар, то в ледяной булыжник. Причиной разного состояния явлений окружающего мира – структура кристаллической решетки.
Структура атома
Строение мельчайшего компонента всех веществ – одна из самых простых тем в химии и физике в силу наглядности. Каждый учившийся в школе человек отлично представляет Солнечную систему с огромной звездой по имени Солнце в центре и крутящимися вокруг шариками-планетами. Конструкция устойчива в силу притяжения и центробежных сил. Атом – будто макет Солнечной системы в миниатюре.
Конструкция устойчива в силу притяжения и центробежных сил. Атом – будто макет Солнечной системы в миниатюре.
Периодическая система элементов
Каждый в течение жизни много раз упоминает названия химических элементов в бытовых разговорах и ситуациях. «Вашим костям не хватает кальция», – слышим от врача. «Возьмите крем-сыворотку с цинком», – советует консультант косметической компании. «Хочу покрытие с эффектом хрома», – думаем при выборе мебели или сантехники. В мире химии есть целая система, упорядочивающая и описывающая известные всем элементы. Таблица разделена на периоды, группы и блоки в зависимости от физических свойств веществ.
Химические связи
Свободные, несвязанные атомы в природе встречаются очень редко. Частички элементов, обычно называемые благородными газами, являются исключением. Атомы большинства веществ в подавляющем большинстве случаев связаны. Однако качество связей бывает разное: сильные и слабые, водородные и металлические, ионные и ковалентные. Начинающих химиков ждет знакомство с силами Ван-дер-Ваальса. Звучит увлекательно и таинственно, будто очередная часть саги о Властелине колец.
Начинающих химиков ждет знакомство с силами Ван-дер-Ваальса. Звучит увлекательно и таинственно, будто очередная часть саги о Властелине колец.
Основы термохимии
Закон Гесса и энтальпия – теоретический минимум, обязательный к изучению. Дальше – язык формул и схем. Лайфхак для непонимающих с первого раза – попробовать изучить тему с разных сторон и посмотреть несколько уроков, по-разному толкующих суть. Всегда найдется преподаватель или лектор, который «разжует» доходчивее остальных. Многократное пересматривание одного и того же материала напоминает вышибание стены лбом.
Электролиты
Диссоциация на ионы является причиной прохождения электротока сквозь вещества и предметы. Пропускающие электричество жидкие тела называют электролитами. Выделяют сильные и слабые, кислоты, соли и щелочи. Важная задача – понять суть электролитической диссоциации, научиться составлять уравнения реакции и проследить протекание процесса на конкретных примерах.
Закон действия масс
Химические равновесия – существенная часть теории. Закон действующих масс был открыт опытным путем давно, во второй половине 19 века. Полученная формула носит имя ученых-первооткрывателей, Гульдберга и Вааге. С первого раза формулировка разочаровывает непонятностью. Поэтому обязательно нужно смотреть разъясняющее видео, которое позволяет быстрее «ухватить за хвост» суть.
Основы кинетики
Кинетика (с древнегреческого «движение») изучает механизмы, скорость и порядок протекания химических реакций в зависимости от внешних условий. Раздел тесно связан с физической наукой. Термин встречается и в механике. Химические процессы протекают под действием многих факторов, изменение которых позволяет влиять на механизм и скорость. Значение скорости меняется в разных временных интервалах. Поэтому существует понятие истинной (мгновенной) скорости реакции.
Окислительно-восстановительные реакции
Любая точная наука (физика, математика) немыслима без решения уравнений. Химия в том числе. В уравнениях отражаются процессы окисления и восстановления. Переходя к решению подобных задач, придется освоить ряд напряжения металлов, стандартные потенциалы, электрохимические ячейки, степени окисления, восстановители и окислители. В некоторых источниках процесс именуется сокращенно ОВР или редокс – от англ. reduction-oxidation (восстановление-окисление).
Химия в том числе. В уравнениях отражаются процессы окисления и восстановления. Переходя к решению подобных задач, придется освоить ряд напряжения металлов, стандартные потенциалы, электрохимические ячейки, степени окисления, восстановители и окислители. В некоторых источниках процесс именуется сокращенно ОВР или редокс – от англ. reduction-oxidation (восстановление-окисление).
Бесплатный курс химии
Занимательные лекции для «чайников» в плейлисте Первого образовательного телеканала, где представлены обучающие видеоролики по популярным естественным наукам.
Основы химии стоит знать хотя бы для общего умственного развития. А более фундаментальное изучение поможет в профессиональной деятельности или может стать интересным хобби.
Смотрите также:
Подготовка к ЕГЭ по химии 2020
Программа курса
Показать все Показать все Скрыть
Тесты для данного курса появятся в ближайшее время. Регистрируйтесь и подписывайтесь на курс, чтобы не пропустить эту новость.
Регистрируйтесь и подписывайтесь на курс, чтобы не пропустить эту новость.
Лента новостей
Будь в курсе всего! Новости по курсу, уведомления о новых уроках и заданиях, и многое другое.
Обсуждение
Пойми предмет полностью! Задавай вопросы преподавателям и соученикам, высказывай предположения, участвуй в дискуссиях.
Учащиеся
Знакомься с соучениками, общайся, вместе готовьтесь к экзаменам, становитесь
настоящими друзьями.
Документы
Скачивай нужную информацию в удобном формате. Распечатывай или используй на компьютере, планшете, смартфоне.
Письменные работы
Загружай сочинения, решения задач, языковые упражнения для проверки преподавателем.
Личные сообщения и уведомления
Мгновенно узнавай о новостях сервиса, поступивших сообщениях от сокурсников и
преподавателей, общайся в личке с педагогами и соучениками.
Химическая термодинамика. Основы химической термодинамики 10 класс онлайн-подготовка на Ростелеком Лицей
Термодинамика – это наука, изучающая законы обмена энергией между системой и окружающей средой. Химическая термодинамика изучает превращения энергии в ходе химических реакций и физико-химических процессов.
Любой объект, который является предметом рассмотрения с точки зрения превращения энергии, называют термодинамической системой.
Классификация термодинамических систем
|
Вид системы |
Характеристика |
Примеры |
|
Открытая |
Возможен обмен с внешней средой веществом и энергией |
Человеческое тело. Открытая колба, из которой может испаряться растворитель, и которая может охлаждаться и нагреваться |
|
Замкнутая |
Невозможен обмен с внешней средой веществом, возможен обмен энергией |
Плотно закрытая колба с реагентами |
|
Изолированная |
Невозможен обмен с внешней средой ни веществом, ни энергией |
Термос, сосуд Дьюара |
Два основных способа передачи внутренней энергии: теплота Q и работа W. Если система отдает в окружающую среду теплоту или совершает работу против внешних сил, внутренняя энергия уменьшается, изменение внутренней энергии отрицательно, меньше ноля ∆U < 0 Следовательно, соответствующие функции также отрицательны Q < 0, W < 0 Обратным действием можно пополнить запас внутренней энергии системы ∆U > 0 В этом случае функции (теплота и работа) положительны Q > 0, W >0.
Первый закон термодинамики: Изменение внутренней энергии системы при протекании какого-либо процесса равно алгебраической сумме всех видов энергии, которыми система обменивается с окружающей средой. ∆U = Q+W. Следствие из первого закона термодинамики закон Гесса: Тепловой эффект реакции изменение энтальпии, внутренней энергии не зависит от промежуточных стадий (от пути процесса, а зависит только от исходного и конечного состояний реагирующих веществ.
Второй закон термодинамики: В любой изолированной система самопроизвольно протекают только те процессы, которые приводят к увеличению энтропии.
Третий закон термодинамики: Энтропия любой системы, находящейся в равновесном состоянии при стремлении температуры к абсолютному нулю начинает стремиться к определенному пределу и перестает зависеть от любых параметров состояния.
Конспект для подготовки к ЗНО по химии
Краткий конспект подготовки к ЗНО по химии №1 “Основные химические понятия”
Краткий конспект подготовки к ЗНО по химии №2 “Вещество”
Краткий конспект подготовки к ЗНО по химии №3 “Законы в химии. Химические реакции”
Химические реакции”
Краткий конспект подготовки к ЗНО по химии №4 “Периодический закон”
Краткий конспект подготовки к ЗНО по химии №5 “Строение атома”
Краткий конспект подготовки к ЗНО по химии №6 “Химическая связь”
Краткий конспект подготовки к ЗНО по химии №7 “Раствор”
Краткий конспект подготовки к ЗНО по химии №8 “Оксиды”
Краткий конспект подготовки к ЗНО по химии №9 “Основания”
Краткий конспект подготовки к ЗНО по химии №10 “Кислоты”
Краткий конспект подготовки к ЗНО по химии №11 “Соли”
Краткий конспект подготовки к ЗНО по химии №12 “Амфотерные соединения”
Краткий конспект подготовки к ЗНО по химии №13 “Общие сведения о металлах”
Краткий конспект подготовки к ЗНО по химии №14 “Щелочные металлы”
Краткий конспект подготовки к ЗНО по химии №15 “Щелочноземельные металлы”
Краткий конспект подготовки к ЗНО по химии №16 “Аллюминий и соединения аллюминия”
Краткий конспект подготовки к ЗНО по химии №17 “Железо и соединения железа”
Краткий конспект подготовки к ЗНО по химии №18 “Неметаллические элементы”
Краткий конспект подготовки к ЗНО по химии №19 “Водород и его соединения”
Краткий конспект подготовки к ЗНО по химии №20 “Водород и его соединения”
Краткий конспект подготовки к ЗНО по химии №21 “Подгруппа оксигена”
Краткий конспект подготовки к ЗНО по химии №22 “Подгруппа нитрогена”
Краткий конспект подготовки к ЗНО по химии №23 “Подгруппа карбона”
Краткий конспект подготовки к ЗНО по химии №24 “Теоретические основы органической химии”
Краткий конспект подготовки к ЗНО по химии №25 “Алканы. Строение молекул, номенклатура, физические и химические свойства”
Строение молекул, номенклатура, физические и химические свойства”
Краткий конспект подготовки к ЗНО по химии №26 “Алкены”
Краткий конспект подготовки к ЗНО по химии №27 “Алкины”
Краткий конспект подготовки к ЗНО по химии №28 “Арены. Номенклатура, изомерия,
Краткий конспект подготовки к ЗНО по химии №29 “Природные источники углеводородов”
Краткий конспект подготовки к ЗНО по химии №30 “Спирты”
Краткий конспект подготовки к ЗНО по химии №31 “Фенолы”
Краткий конспект подготовки к ЗНО по химии №32 “Альдегиды”
Краткий конспект подготовки к ЗНО по химии №33 “Карбоновые кислоты”
Краткий конспект подготовки к ЗНО по химии №34 “Сложные эфиры. Жиры”
Краткий конспект подготовки к ЗНО по химии №35 “Углеводы”
Краткий конспект подготовки к ЗНО по химии №36 “Повторение кислородсодержащих органических соединений”
Краткий конспект подготовки к ЗНО по химии №37 “Амины”
Краткий конспект подготовки к ЗНО по химии №38 “Аминокислоты”
Краткий конспект подготовки к ЗНО по химии №39 “Белки”
Краткий конспект подготовки к ЗНО по химии №40 “Синтетические высокомолекулярные соединения и полимерные материалы на их основе”
Краткий конспект подготовки к ЗНО по химии №41 “Обобщение сведений об органических соединениях”
Краткий конспект подготовки к ЗНО по химии №42 “Решение задач по химическим формулам”
Краткий конспект подготовки к ЗНО по химии №43 “Решение задач: выражение количественного состава раствора”
Краткий конспект подготовки к ЗНО по химии №44 “Решение задач по уравнению реакции”
Если вы когда-нибудь хотели изучать химию на университетском уровне дома, посмотрите этот сборник лекций, которые я собрал! (Общий, Органический, Био, Аналитический, Физический, Вычислительный, Квантовый .
 ..): химия
..): химияЯ часто получаю много вопросов о том, как изучать химию в Интернете или как подготовиться к курсам химии университетского уровня или дополнить их. Итак, я потратил несколько часов и составил список самых полных, полезных и интересных серий лекций по химии. Почти все они записываются в реальных классах колледжа и преподаются профессорами.Я попытался организовать его по подразделам, но заголовки каждой серии должны давать довольно очевидное представление о том, какой тип материала охватывает курс! Я большой поклонник публикации лекций в колледже и надеюсь, что по крайней мере некоторые из вас сочтут это полезным! Имейте в виду, что это ПОЛНЫЕ КУРСЫ, и что каждая из этих ссылок ведет к первой лекции всего триместра / семестра курсов, поэтому обычно есть около 30-40 видео, которые идут после того, которое я связал Вам!
РЕДАКТИРОВАТЬ 1 : Добавлены лекции по химической инженерии, биотехнологии, металлургии, продвинутому органическому синтезу: стехиометрическая металлоорганическая химия, химическая и биомолекулярная инженерия – 179, Введение в химическую инженерию, астробиологию и космические исследования, а также ряд вопросов квантовой химии / механики классы (10-30-14). РАЗМЫШЛЕНИЕ О ДОБАВЛЕНИИ КАТЕГОРИЙ ФИЗИКИ, БИОЛОГИИ, МАТЕМАТИКИ И МЕДИЦИНЫ. Дайте мне знать, если это будет уместно / если кому-то будет интересно!
РАЗМЫШЛЕНИЕ О ДОБАВЛЕНИИ КАТЕГОРИЙ ФИЗИКИ, БИОЛОГИИ, МАТЕМАТИКИ И МЕДИЦИНЫ. Дайте мне знать, если это будет уместно / если кому-то будет интересно!
РЕДАКТИРОВАТЬ 2 : Вау, спасибо за мое самое первое золото Reddit! (10-30-14)
РЕДАКТИРОВАТЬ 3 : ДРУГОЕ ЗОЛОТО?!?! Серьезно, спасибо вам, ребята! Я сделаю все возможное, чтобы постоянно обновлять этот список и добавлять новые темы! Также имейте в виду, что этот пост вошел в 100 лучших постов всех времен на r / chemistry, так что это действительно здорово! Очень рад, что могу отдать такой полезный и интересный сабреддит! (10-30-14)
РЕДАКТИРОВАТЬ 4 : Я написал модератору (u / chemjobber) сообщение о том, что это прикреплено / добавлено на боковую панель из-за того, сколько из вас это просили.Скорее всего, это произойдет, если все, кто хотел бы, наклеили сообщение об этом модератору! (10-30-14)
РЕДАКТИРОВАТЬ 5 : Моды добавили этот пост на боковую панель r / chemistry! Он находится под заголовком Chemistry Links и называется «Онлайн-лекции по химии». Кроме того, я ценю отзывы и предложения и добавлю категории по другим темам, как только у меня будет время! (11-2-14)
Кроме того, я ценю отзывы и предложения и добавлю категории по другим темам, как только у меня будет время! (11-2-14)
Общая химия
Подготовка к общей химии – 1P (UCIrvine)
Общая химия – 1A (UCIrvine)
Общая химия – 1B (UCIrvine)
– 10002C Общая химия (UCIrvine) – 10002C Общая химия )Органическая химия
Органическая химия – 51A (UCIrvine)
Органическая химия – 51B (UCIrvine)
Органическая химия – 51C (UCIrvine)
Органическая химия – Механизм реакции
II – 202 (UCIrvine)
Органическая спектроскопия – 203 (UCIrvine)
Введение в металлоорганическую химию (IIS)
Продвинутый органический синтез: стехиометрическая металлоорганическая химия (руб.)
Гетероциклическая химия и химия 9000 (
Heterocyclic Chemistry 5) (IIS)
Биохимия
Введение в химическую биологию – 128 (UCIrvine)
Биохимия – BB 350 (Штат Орегон)
Биохимия – BB 450/550 (штат Орегон)
Биохимия I (IIS)
Иммунология с гематологией – M121 (UCIrvine)
Биохимия – основы иммунологии (IIS)
Биохимия, биохимия, биохимия, биохимия, экспрессия. (IIS)
(IIS)
Астробиология и исследования космоса (Стэнфорд)
Аналитическая химия
Аналитическая химия и хроматография для аспирантов (Университет Миннесоты)
Инструментальный анализ – Ch504 (Limestone College)
Современные инструментальные методы анализа IISC)
Симметрия, структура и тензорные свойства материала / Рентгеновская кристаллография – 3.60 (MIT)
Расширенная аналитическая химия (IIS)
Physical Chemistry
Physical Chemistry – 131A (UCIrvine)
Physical Chemistry – 131B (UCIrvine)
Physical Chemistry Solid – 131vC (UCI) State Chemistry – 3.091SC (MIT)
Термодинамика и кинетика – 5.60 (MIT)
Спектроскопия и динамика малых молекул – 5.80 (MIT)
Скоростные процессы (IIS)
Математика для химии (IIS)
Электрохимия Gupta Tutorials)
Квантовая химия
Введение в квантовую химию (IIS)
Квантовая химия и спиновая динамика (Оксфорд)
Современная физика: квантовая механика (Стэнфорд)
Физика элементарных частиц (Стэнфордская физика частиц)
Физика: стандартная модель (Стэнфорд)
Теоретический минимум: квантовая механика (Стэнфорд)
Продвинутая квантовая механика (Stanf ord)
Квантовые запутывания: Часть 1 (Стэнфорд)
Квантовые запутывания: Часть 3 (Стэнфорд)
Неорганическая химия
Неорганическая химия – 107 (UCIrvine)
Координационная химия / химия элементов ( IIS)
Био-неорганическая химия (IIS)
Вычислительная химия
Навыки в области научных вычислений – 5 (UCIrvine)
Вычислительные методы (IIS)
Медицинская / фармацевтическая химия (UCLA) Polymer Chemistry Polymer Chemistry (IIS) Нестабильность и формирование рисунка тонких полимерных пленок (IIS) Lab Technique Chemistry Lab Techniques – 5. Химическая инженерия Введение в химическую инженерию (Стэнфорд) Разработка химических реакций I (IIS) Разработка химических реакций II (IIS) Интеграция процессов, методы и область интеграции (IIS) Решения по проектированию процессов и экономика проекта (IIS) Основы транспортных процессов I (IIS) Основы транспортных процессов II (IIS) Химическая технология I (IIS) Контроль химических процессов на предприятии (IIS) Продвинутые математические методы в химической инженерии (IIS) Операции массопереноса I (IIS) Операции массопереноса II (IIS) Гетерогенный катализ и каталитические процессы (IIS) Микромасштабные процессы переноса (IIS) Многофазный поток (IIS) Fluid Mechanics (IIS) Скорость процессов (IIS) Нестабильность и формирование паттернов Тонкие полимерные пленки (IIS) Управление процессом и приборы (IIS) Определение характеристик частиц (IIS) Вычислительная гидродинамика (IIS) Теплопередача (IIS) Современные инструментальные методы анализа (IIS) Новый Процессы разделения (IIS) Engineering Chemistry 1 (IIS) Biotechnology Аналитические технологии в биотехнологии (IIS) Downstream Processing (IIS) Proteomics: Principles and Techniques (IIS) Thermodynamics Биоматематика (IIS) Химическая / биохимическая инженерия (IIS) Биохимическая инженерия / ферментная наука и инженерия (IIS) [Химическая и биомолекулярная инженерия – 179 (UCBerkeley)] (https: // www. Металлургия Электронные материалы, устройства и материалы для производства (IIS) 301 (MIT)
301 (MIT) youtube.com/watch?v=TylPELl–Qs&t=0s&list=PL-XXv-cvA_iCrUepjUAo_pwNpJQJ6B3FH)
youtube.com/watch?v=TylPELl–Qs&t=0s&list=PL-XXv-cvA_iCrUepjUAo_pwNpJQJ6B3FH)
Деградация материалов в окружающей среде (IIS)
Наука и технология полимеров (IIS)
Обработка полупроводниковых материалов (IIS)
Advanced Ceramics for Strategic Applications (IIS)
Principles of Physical Metallurgy ( IIS)
Электрокерамика (IIS)
Усовершенствованная металлургическая термодинамика (IIS)
Добыча цветных металлов (IIS)
Производство стали (IIS)
Введение в биоматериалы (IIS)
Материальный и энергетический баланс
Топливо, огнеупоры и печи (IIS)
Physics of Materials (IIS)
Кодирование с нуля – Пенсильвания 4-H
Возраст Соответствующий легкость
От начальной до средней школы (* все 4 года)
Рекомендуемое количество времени для урока
1-2 часа
Требуются припасы
- Компьютер или планшет с доступом в Интернет *
- Дополнительно: карточки для печати скретч-кодирования
* Действие может быть выполнено онлайн или офлайн
Материалы онлайн-версии
- Компьютер или планшет с доступом в Интернет
Материалы офлайн-версии
- Offline Activity Guide for Pitch Your Passion
- Компьютер (ы) с установленной программой Scratch
4-H Project соответствует
Учебная программа по информатике, 4 часа
Урок
.
Цели
- Выявить элемент для царапин, компьютерное кодирование
- Дайте возможность для самоопределения
- Делитесь своей страстью с другими
Деятельность
- Войдите в Goggle Classroom по адресу g.co / csfirst как студент
- Код класса c9z8zc
- Запишите ваше имя пользователя и пароль, они вам понадобятся позже. Это позволит вам вернуться к этому занятию или попробовать другие занятия на Scratch.
- Выберите уровень вашей страсти и следуйте интерактивным инструкциям. В нижней части экрана есть обучающие видеоролики. Чтобы начать работу, выберите «стартовый проект»
- Это запустит Scratch. В правом верхнем углу будет еще один вариант входа.Используйте логин и пароль, которые были назначены вам при входе в систему ранее, чтобы вы могли вернуться в систему и просмотреть свои проекты
- В меню «Файл» выберите «Сохранить», когда вы работаете над своим проектом. После завершения выберите вариант публикации и совместного использования вашего проекта.

Вспоминая
- Что такое царапины?
- Как можно использовать Scratch для создания PSA?
Понимание
- Как вы относитесь к использованию CS для обмена сообщениями?
Применение
- Как бы вы использовали CS для передачи вашего сообщения?
- Какие элементы они решили изменить?
- Что было бы, если бы у вас не было Интернета? Вы скачали офлайн-версию Scratch?
Анализируем
- Какие части или особенности Scratch?
- Какова функция спрайта?
- Вы пробовали весь Код, чтобы увидеть, что он делает?
Оценка
- Довольны ли вы своим PSA?
- Это передало ваше предполагаемое сообщение?
Создание
- Как бы вы улучшили свою социальную рекламу, чтобы лучше делиться своим сообщением?
- Каким образом вы могли увидеть использование Scratch в своей жизни?
Ссылки, использованные в этом уроке
- NYSD Game Changers: National 4-H Council
- MIT Scratch
- Классная комната с очками
Кредиты
Lyndsey Androstic- lma216 @ psu. edu
edu
Мелони Андростик – [email protected]
Toni Stuetz – [email protected]
Лучшие книги для изучения химии в средней школе (Руководство на 2021 год)
Для многих людей средняя школа – их первое официальное знакомство с миром химии. К сожалению, это не всегда самый положительный опыт, и многие студенты в конечном итоге чувствуют себя совершенно потерянными. Поначалу непросто усвоить основы химии. Если ваш учитель не выбрал лучший учебник химии для средней школы, но вы полны решимости учиться, посмотрите одну или несколько книг из этого списка.Это одни из лучших книг для самостоятельного изучения химии , и они могут помочь вам удержаться на плаву в вашем классе химии в средней школе.
Кроме того, если вы учитель химии и ищете способ спланировать свои курсы или какой-либо дополнительный материал для своих учеников, обязательно ознакомьтесь с ними!
Лучшие книги для изучения химии, когда вы потерялись в классе Учителя
растянуты довольно тонко, и часто они не могут дать каждому
ученику индивидуальное внимание, которое они хотели бы. Иногда их учение
стиль не согласуется с вашим стилем обучения, и иногда вы просто плохо
учитель.
Иногда их учение
стиль не согласуется с вашим стилем обучения, и иногда вы просто плохо
учитель.
Если у вас есть мотивация и у вас есть лучших школьных учебников химии , возможно, вы сможете разобраться в этом самостоятельно. Но если вы все еще пытаетесь соединить точки, любая из этих лучших книг для изучения химии потенциально может помочь вам.
Кроме того, если вы ищете хорошие материалы для самостоятельного изучения химии или просто обучаете детей на дому, это руководство также для вас.
Помните, что учеба в старшей школе обычно формирует то, как вы в целом любите науку, поэтому старайтесь подходить к ним с умом и особенно для того, чтобы получать от них удовольствие!
Во-первых, мы начнем с краткого знакомства с двумя нашими лучшими выборами. Обе книги отлично подходят для изучения общей химии в средней школе или в колледже. Вы можете использовать любой из них для изучения с нуля без предварительного знания химии , или вы можете использовать их в качестве дополнения к вашему классу в школе.
По этому случаю наш лучший выбор для старшеклассников, которым нужна книга, чтобы помочь им учиться самостоятельно, или для тех, кто хочет изучать химию с нуля, is Houk & Post’s Химия: концепции и проблемы: самообучающее руководство .Эта книга идеально подходит практически для любого студента, потому что, как видно из названия, предназначена для самостоятельного обучения вводному курсу химии. Это очень дешевый вариант, доступный каждому.
В первый раз, когда мы выпустили этот обзор, мы выбрали в качестве второго лучшего выбора Chemistry for Dummies.
Однако недавно мы получили копию Focus On High School Chemistry Ребекки В. Келлер, и мы сразу же побежали обновить обзор!
Этот учебник просто потрясающий для средней школы химии.Если вам нужна чрезвычайно полная книга, выберите этот вариант. Если вам нужно дополнить традиционное школьное образование, это прекрасно. Если он вам нужен для домашнего обучения, в нем есть все, что вам нужно. Это более дорогой вариант, но уверяю вас, это отличное вложение.
Если он вам нужен для домашнего обучения, в нем есть все, что вам нужно. Это более дорогой вариант, но уверяю вас, это отличное вложение.
Вот краткая справочная таблица со всеми книгами, рассматриваемыми в этом обзоре. Чтобы увидеть полные обзоры, просто прокрутите вниз.
Лучшие книги для изучения химии в средней школеЗдесь мы собрали подробные обзоры шести лучших книг, которые помогут вам выучить химию, когда школьный учебник просто не сокращает ее.
1. Химия: концепции и проблемы: руководство для самообученияНаш лучший выбор в этом списке и наша рекомендация лучший учебник химии для самостоятельного изучения . Это руководство для самообучения – всего лишь то, что означает, что в нем есть все необходимое для изучения этой увлекательной науки.
Химия: концепции и проблемы: руководство для самообучения
Это отличный инструмент для тех, кто хочет изучать химию, но не записан в класс, но он также может быть спасением для средней школы или студенты колледжа , которые не чувствуют, что они учатся эффективно у своего учителя и учебника.
Важно отметить, что за подходом книги к доставке и усилению содержания стоит много исследований. В нем используется метод запрограммированного обучения, при котором задает вопросы сразу после объяснения новой концепции , а затем использует упражнения с интервалом повторения, чтобы заложить прочную основу.
2. Сосредоточьтесь на химии в старших классах
Недавно мы обновили эту статью, чтобы показать вам, что теперь наш второй первый выбор для школьного учебника химии : Сосредоточьтесь на химии в старших классах .
В центре внимания химия в старших классах
Эта книга предназначена для изучения химии в старших классах с 9 по 12 класс. И делает это красиво. Эта книга является частью учебной программы Science-4-Kids, которая пытается охватить науку, используя нейтральный взгляд на мир (то есть только научные факты, а не попытки навязывать религиозные или философские интерпретации).
Книга начинается с самого начала, что такое химия? И, безусловно, следует учить химию с отличным педагогическим подходом.Оно имеет . очень увлекательный язык, и он удобен как для государственных / частных школ, так и для программ домашнего обучения.
На почти 300 страницах вы найдете не только теорию и объяснения, но и пошаговые объяснения химических экспериментов, которые можно проводить как в химической лаборатории, так и дома.
Он охватывает введение в химию и материю, прежде чем перейти к химическим связям и основным реакциям. Он отлично справляется с описанием равновесий, таких как кислотно-щелочные реакции или концепции смесей.Он заканчивается введением в органическую химию (химию углерода) и даже немного переходит к полимерам и биохимическим системам.
В целом, занимательный и полный охват школьной химии. Это не так дешево, как другие дополнительные варианты, но однозначно рекомендуется.
3. Химия для чайников Если у вас никогда в жизни не было уроков химии, Chemistry for Dummies – одна из лучших книг для изучения химии с нуля . Если вы умеете читать и выполнять основы математики, у вас есть все необходимое для успешного использования этой книги.
Если вы умеете читать и выполнять основы математики, у вас есть все необходимое для успешного использования этой книги.
Химия для чайников
В этом, конечно же, прелесть всех «чайников». Они написаны для того, чтобы их понял каждый, кто хочет учиться. Кроме того, они на привлекательнее, чем средний учебник химии из-за чувства юмора авторов и веселого тона.
Этот конкретный элемент отслеживает типичный двухсеместровый курс химии, который будет составлять одного года химии в средней школе или общей химии I и II на уровне колледжа.Кроме того, он предоставляет множество примеров реальных приложений, которые помогут вам понять эту науку в контексте повседневной жизни.
4. Основы химии для чайников Можно сказать, что это лучший справочник по химии в нашем списке. Chemistry Essentials for Dummies написан тем же автором, что и Chemistry for Dummies . Разница в том, что эта книга более полезна в качестве краткого справочника или освежения ключевых понятий .
Chemistry Essentials для чайников
Это часть относительно новой серии от издателя под названием The Essentials для чайников . Таким образом, он в первую очередь предназначен для студентов, которые активно учатся перед началом нового класса, повторяют экзамены или просто обновляют свои знания по предмету химии.
Но это еще не все! Кроме того, очень полезен для родителей , которые, возможно, изучали химию много лет назад и хотят получить быстрый обзор, чтобы они могли помочь своим детям с домашним заданием.
5. AP Chemistry for DummiesЭта книга, как следует из названия, рассчитана на более узкую аудиторию. Хотя это не лучший школьный учебник химии для общего пользования , это отличный компаньон для продвинутого уровня или AP по химии.
AP Chemistry для чайников
AP классы
принимаются в старшей школе для получения кредита в колледже, и поэтому ожидается, что они покроют
тот же материал, что и два семестра университетской общей химии. Но затем
не означает, что старая книга обзоров обязательно поможет
этот класс.
Но затем
не означает, что старая книга обзоров обязательно поможет
этот класс.
AP Chemistry for Dummies имеет то преимущество, что он нацелен на студентов AP и решает уникальные задачи , которые возникают в этом продвинутом классе . Не в последнюю очередь, конечно, ужасный экзамен по химии в конце года.
Эта книга предлагает не только углубленный обзор концепции и двух полных практических экзаменов , но также расписание занятий для предотвращения зубрежки и ценные стратегии сдачи тестов.
Но если вам действительно нужен какой-то материал для подготовки к экзаменам AP по химии, просто ознакомьтесь с этой другой статьей с большим количеством более конкретных обзоров.
6. Органическая химия I для чайниковКак и предыдущий пункт, эта книга имеет гораздо более конкретную направленность. В данном случае это по органической химии, а не по общей химии .
Органическая химия I для чайников
Органическая химия I для чайников охватывает отрасль химии, которая может или не может появиться в вашей школьной программе. Тем не менее, определенно будет полезен, если вы изучаете органическую химию в колледже , или даже если вы просто хотите узнать как можно больше о химии самостоятельно.
Тем не менее, определенно будет полезен, если вы изучаете органическую химию в колледже , или даже если вы просто хотите узнать как можно больше о химии самостоятельно.
Доказано, что самый эффективный способ подготовиться к экзамену – это пройти практические тесты, а лучший способ чему-либо научиться – это делать. Имея это в виду, мы могли бы сказать, что Chemistry Workbook for Dummies – лучший инструмент, который вы можете найти для изучения химии в средней школе с более практическим подходом .
Учебное пособие по химии для чайников
В этой книге даются ключевые концептуальные обзоры по каждому разделу, но на самом деле он особенно выделяется сотнями практических задач с полными объяснениями . В последних выпусках также есть доступ к онлайн-банку тестов, который поможет вам разобраться со всем.
Заключительные мысли о лучшем учебнике химии для старших классов s Естественно, выбор подходящей книги для вас будет зависеть от того, какой именно уроки химии вы посещаете, даже если вы вообще посещаете формальный класс.
Однако мы бы сказали, что первые два пункта в этом списке, Chemistry: Concepts and Problems: A Self-Teaching Guide and Focus on High School Chemistry , будут лучшими вариантами для большинства школьников, изучающих химию. или колледж общей химии .
Это связано с тем, что общая направленность этих двух книг делает их более подходящими для людей, пытающихся изучать химию. Оба предназначены для студентов, которые не имеют предварительных знаний по химии , и содержат четкие, подробные объяснения всего, что вам нужно знать в этом классе.
Подводя итог всему обзору: Если вам нужен лучший и более дешевый вариант, воспользуйтесь Руководством по самообучению. Если вам нужен более полный вариант, выберите Focus On High School Chemistry!
Если вы хотите расширить свои знания по химии, ознакомьтесь с лучшими учебниками по общей химии. Кроме того, если вы особенно заинтересованы в самообучении, у нас есть для вас еще один обзорный пост!
Что бы вы ни выбрали, мы рекомендуем покупать новую книгу по химии раньше, чем позже . Чем раньше вы начнете использовать дополнительный материал, тем меньше вам придется компенсировать после того, как вы потерялись в классе на несколько недель или месяцев.
Чем раньше вы начнете использовать дополнительный материал, тем меньше вам придется компенсировать после того, как вы потерялись в классе на несколько недель или месяцев.
Учитесь понемногу, каждый день или большую часть дня, последовательно выполняйте задачи и не ждите, чтобы втиснуть все в последнюю минуту – – это путь к успеху на вашем уроке химии .
3.5E: Начало кристаллизации – Chemistry LibreTexts
- Последнее обновление
- Сохранить как PDF
- Contributor
Иногда кристаллы не образуются, даже если раствор перенасыщен, поскольку существует кинетический барьер для образования кристаллов.Иногда может потребоваться инициировать кристаллизацию, например, если раствор становится слегка мутным при охлаждении или если раствор не дает кристаллов, даже если он заметно холоднее, чем первоначально. Методы, описанные в этом разделе, предпочтительно следует использовать для еще теплых растворов, поскольку начало кристаллизации уже холодных (или холодных) растворов вызовет слишком быструю кристаллизацию.
Методы, описанные в этом разделе, предпочтительно следует использовать для еще теплых растворов, поскольку начало кристаллизации уже холодных (или холодных) растворов вызовет слишком быструю кристаллизацию.
Самый простой способ инициировать кристаллизацию – поцарапать дно или сторону колбы стеклянной палочкой для перемешивания (рис. 3.45a) с достаточной силой, чтобы царапины были слышны (но, конечно, не настолько, чтобы вы разбили стекло!) . Кристаллизация часто начинается сразу после царапания, и могут быть видны линии, показывающие рост кристаллов в тех областях стекла, которые были поцарапаны (рис. 3.46).
Рис. 3.46: Линии кристаллов на начальных стадиях роста кристаллов, берущие начало в месте поцарапания стекла: а + b) \ (\ ce {N} \) – бромсукцинимид, кристаллизующийся из воды, в) Ацетанилид, кристаллизующийся из воды. Хотя нет сомнений в том, что этот метод работает, существуют разногласия относительно механизма действия. Одна из теорий заключается в том, что царапание инициирует кристаллизацию, выделяя энергию от высокочастотных колебаний. Другая теория состоит в том, что крошечные фрагменты стекла смещаются во время царапания, что обеспечивает места зарождения кристаллов. Другая гипотеза состоит в том, что растворитель может испариться со стеклянной палочки для перемешивания после того, как она будет удалена, а частичка твердого вещества может упасть в раствор и действовать как «затравочный кристалл» (см. Следующий абзац).Не совсем понятно, как царапина инициирует кристаллизацию, но это есть в арсенале “хитростей” каждого химика.
Одна из теорий заключается в том, что царапание инициирует кристаллизацию, выделяя энергию от высокочастотных колебаний. Другая теория состоит в том, что крошечные фрагменты стекла смещаются во время царапания, что обеспечивает места зарождения кристаллов. Другая гипотеза состоит в том, что растворитель может испариться со стеклянной палочки для перемешивания после того, как она будет удалена, а частичка твердого вещества может упасть в раствор и действовать как «затравочный кристалл» (см. Следующий абзац).Не совсем понятно, как царапина инициирует кристаллизацию, но это есть в арсенале “хитростей” каждого химика.
Есть несколько других методов, которые можно использовать для инициирования кристаллизации, когда царапина не дает результата:
- Добавьте «затравочный кристалл»: маленькое пятнышко сырого твердого вещества, сохраненное до начала кристаллизации, или кусочек чистого твердого вещества из емкости с реагентом. Затравочные кристаллы создают место зарождения, где кристаллы могут начать рост.
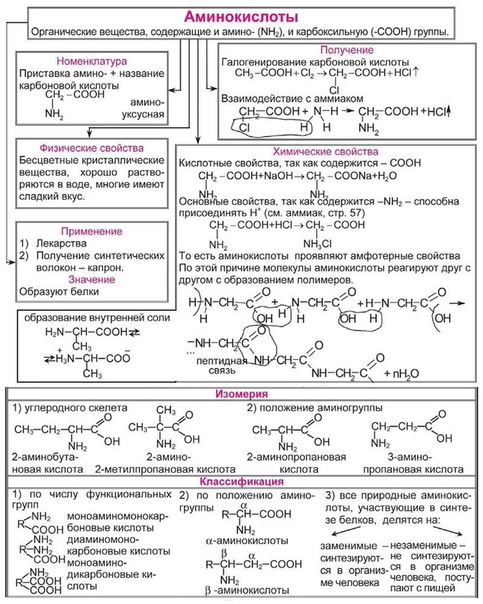
- Опустите стеклянную палочку для перемешивания в перенасыщенный раствор, извлеките ее и дайте растворителю испариться, чтобы на стержне образовался тонкий остаток кристаллов (Рисунок 3.47а). Затем коснитесь стержнем поверхности раствора или перемешайте раствор стержнем, чтобы удалить мелкие затравочные кристаллы.
- Если царапины и затравочные кристаллы не инициируют кристаллизацию, возможно, присутствует слишком много растворителя, и соединение остается полностью растворимым (Рисунок 3.48). Чтобы проверить, так ли это, снова доведите раствор до кипения и уменьшите объем растворителя, возможно, наполовину (рис. 3.48c). Дайте восстановленному раствору остыть и посмотрите, не образуется ли твердое вещество.
 Если это так (рис. 3.48d), количество растворителя определенно было проблемой, и с его объемами можно экспериментировать, чтобы добиться наилучшего роста кристаллов.
Если это так (рис. 3.48d), количество растворителя определенно было проблемой, и с его объемами можно экспериментировать, чтобы добиться наилучшего роста кристаллов.
Автор
Лиза Николс (Общественный колледж Бьютта). Organic Chemistry Laboratory Techniques находится под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License. Полный текст доступен онлайн.
химических экспериментов для детей и родителей, которые можно проводить дома
* Этот пост содержит партнерские ссылки. Вещи, которые вы покупаете по нашим ссылкам, могут приносить нам комиссию.
Веселые, простые химические эксперименты и простые проекты, которые дети и подростки в старшей школе могут выполнять дома, используя бытовые материалы для создания действительно интересных химических реакций.
Поскольку химия – это процесс, а не просто набор фактов, детей на дому следует поощрять делать то, что делают настоящие химики: делать прогнозы, разрабатывать и изменять эксперименты, делать наблюдения и делать разумные выводы. Перед тем как начать, убедитесь, что вы понимаете правила безопасности в лаборатории.
от Теодора Грея
В своем долгожданном продолжении «Элементов» Теодор Грей демонстрирует, как элементы периодической таблицы объединяются, чтобы сформировать молекулы, из которых состоит наш мир.
Все физическое состоит из элементов и бесконечного разнообразия молекул, которые они образуют, когда соединяются друг с другом. В книге «Молекулы» Теодор Грей делает следующий шаг в великой истории, которая началась с периодической таблицы в его бестселлере «Элементы: визуальное исследование каждого известного атома во Вселенной». Здесь он исследует через увлекательные истории и потрясающие фотографии самые интересные, важные, полезные и красивые из миллионов химических структур, из которых состоит каждый материал в мире.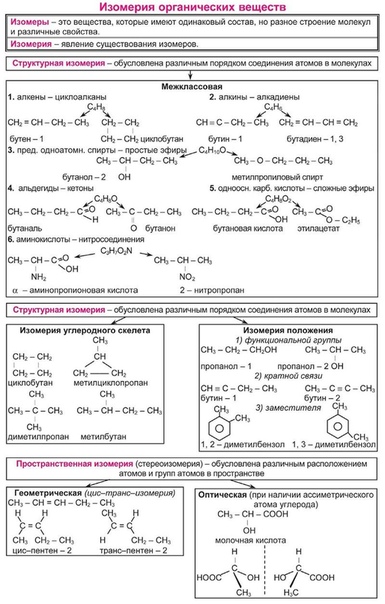
Химическое моделирование
Интерактивная библиотека – это «настоящая интерактивность»! База данных содержит сотни действий, в которых используются сложные программы java, vrml и shockwave. Для тех, кто не может себе позволить беспорядок.
Кислоты и основания
Эксперименты с кислотными дождями
Начните с изучения того, как измерять pH обычных веществ, а затем переходите к определению количества кислоты в почве и ручьях. Руководство для учителей.
Научные эксперименты студентов Alka-Seltzer
Знакомое шипение, которое вы слышите, когда бросаете таблетку Alka-Seltzer в стакан с водой, является результатом химической реакции.Это также идеальный инструмент для демонстрации некоторых изящных научных принципов; такие вещи, как факторы, влияющие на скорость химических реакций, или цвета, полученные в результате химической реакции. Ниже приведены некоторые научные эксперименты, подходящие для использования в школе или дома.
Капустный сок – индикатор pH
Сделайте свой собственный кислотно-щелочной индикатор путем кипячения красной капусты. Используйте сок для проверки pH различных жидкостей.
Используйте сок для проверки pH различных жидкостей.
Кристаллы
Хрустальный орнамент
СТРАНИЦА ОТ А ДО Я
Рождество или нет, кристаллы буры легко создать, и на них приятно смотреть.
Сад кристаллов древесного угля
Цветные, маленькие, нежные кристаллы растут на поверхности древесного угля или кирпича. Вы также можете использовать кусочки губки, угля или раскрошенную пробку, чтобы вырастить кристаллы. Кристаллы образуются из-за того, что пористые материалы, на которых они растут, вытягивают раствор за счет капиллярного действия.
Синяя магия госпожи Стюарт Original Magic Salt Crystal Garden
Синяк миссис Стюарт представляет собой коллоидную суспензию мельчайших частиц синего порошка (гексацианоферрата железа). При желании вы можете заказать воронение или весь комплект на этом сайте.
Горячие и холодные
Эксперименты с сухим льдом
Научный директор ERock-it Джон Макчесни представляет несколько научных экспериментов в домашних условиях, демонстрирующих удивительные свойства сухого льда. Это видео также включает одну из безумных историй Джона «Семь подземелий», в которой Джек и Джилл должны использовать сухой лед, чтобы сбежать от своего врага, «Злой мистер Фред». Rock-it Science – некоммерческая организация, обслуживающая территорию Кремниевой долины.
Heat
Демонстрации в этой главе представляют особую опасность, поскольку в большинстве случаев используются очень горячие или очень холодные вещества, летучие химические вещества, хрупкая стеклянная посуда, газы под высоким давлением или откачанные емкости.
Стальная вата, выделяющая тепло
Химические реакции происходят каждый день вокруг нас.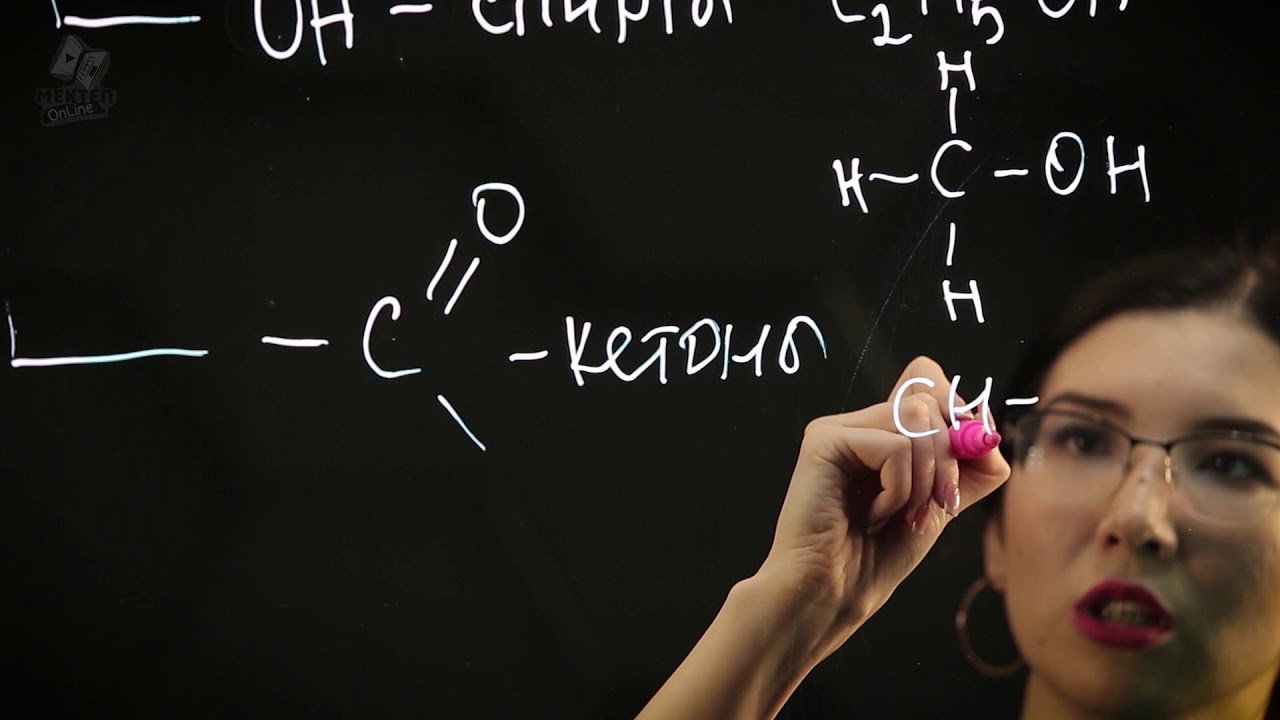 Химическая реакция – это процесс, при котором один тип вещества химически превращается в другое вещество.
Химическая реакция – это процесс, при котором один тип вещества химически превращается в другое вещество.
Бытовая химия
Улучшение волос с помощью химии
Я понял, что немного понимания может уменьшить количество дней с плохими волосами, которые я испытываю. Научные знания и несколько химических смесей помогут мне через полторы недели, пока я не верну волосам приемлемую форму.
Химия окрашивания: реактивные красители
Как вообще происходит связующее окрашивание? Почему краска постоянно держится на хлопковом материале? Для больших и маленьких детей.
Креативная химия
Есть полноцветные рабочие листы и обучающие заметки для увлекательных занятий, подходящих для химического клуба, а также около трехсот страниц вопросников и практических руководств для GCSE и A Level Chemistry.
The Exploratorium Science Snacks about Chemistry
Пузыри, создающие камеру тумана, почему молоко вызывает у некоторых людей тошноту, как действует вкус и многое другое.
Gak Recipe
СТРАНИЦА ОТ А К Я
Вязко-эластичное вещество, похожее на замазку, с которым весело готовить и с которым можно играть. Рецепты Oobleck и Glorax включены. Ресурсы для получения большого количества химикатов.
Как сделать забавное глицериновое мыло
Вы можете быстро и легко сделать набор забавного и симпатичного или элегантного глицеринового мыла. Я учитель химии, поэтому делаю их, чтобы мои ученики использовали их для мытья рук после лабораторных работ. Поскольку я использую их в школе, я не добавляю никаких ароматов, но я объясню, как и когда это можно сделать.
Роберт Брюс Томпсон
Чтение изнутри
Для студентов, любителей DIY и любителей науки, которые больше не могут получить настоящие химические наборы, это единственное в своем роде руководство объясняет, как создать и использовать домашнюю химическую лабораторию, с пошаговыми инструкциями по проведению эксперименты по основам химии – не только для получения красивых цветов и неприятных запахов, но и для того, чтобы научиться выполнять настоящую лабораторную работу.
Потенциальные опасности в вашем доме
План урока для школьного эксперимента по выявлению бытовых химикатов и пониманию их возможных последствий.
Химия мыла
Чтобы понять, что необходимо для эффективной очистки, полезно иметь базовые знания в области химии мыла и моющих средств.
Составы и смеси
Карманный справочник по химическим опасностям NIOSH
Национальный институт профессиональной безопасности и здоровья предоставляет эту базу данных по химическим веществам. Используйте его, чтобы обезопасить себя и свою семью при экспериментах с химическими веществами.
Элементы
Element Games
Вы можете играть в эти игры онлайн и вне дома, чтобы помочь вам запомнить элементы.
элементов в Walmart (31)
Поразительно, сколько элементов вы можете купить в достаточно чистом виде в Walmart: в настоящее время мой список содержит 31 элемент. (Когда я говорю «Walmart», я на самом деле имею в виду любую комбинацию продуктового магазина, строительного магазина и аптеки.
Самодельный водород
Существует огромная разница между наблюдением за тем, как кто-то использует специальный аппарат для производства водорода перед классом или по телевизору, и тем, как вы делаете это самостоятельно, используя то, чего у вас нет дома прямо сейчас.
Структура металла
В основе атома металла лежит кристаллическая структура с плотно упакованными атомами, расположенными в упорядоченные ряды. Эта функция исследует это сердце и показывает, что придает металлу его особые характеристики и как металл ведет себя под воздействием тепла и внешних сил.
Периодические таблицы
Chemical Elements
Меня зовут Йинон Бентор, и несколько лет назад я создал Chemical Elements. com в качестве своего научного проекта для 8-го класса.С тех пор я продолжал обновлять сайт в свободное время, и теперь сайт сильно отличается от первоначального дизайна.
com в качестве своего научного проекта для 8-го класса.С тех пор я продолжал обновлять сайт в свободное время, и теперь сайт сильно отличается от первоначального дизайна.
Книга комиксов Периодическая таблица элементов
Приходите познакомиться с металлическими мужчинами, милой Платиной и другими супергероями Таблицы элементов.
The Elements, by Tom Lehrer
Пойте вместе с профессором Томом Лерером, пока он поет элементы периодической таблицы в этой флэш-анимации.
Периодическая таблица
Файлы Acrobat Периодической таблицы, расположенные в различных форматах.Вы можете сделать их копии и распространить среди студентов.
Таблица Менделеева.
Таблица Менделеева – это природный розеттский камень. Для химиков таблица Менделеева открывает организующие принципы материи, то есть организующие принципы химии. На фундаментальном уровне вся химия содержится в периодической таблице.
Периодическая таблица элементов для печати
Включает атомный номер, атомную массу, символ, имя, электроотрицательность, плотность, энергию ионизации, точку кипения, точку плавления, электронную конфигурацию, состояния окисления, уровень основного состояния, ковалентный радиус и радиус Ван-дер-Ваальса . Если вы обычно работаете с другим набором свойств, вы можете загрузить электронную таблицу и добавить свои собственные числа.
Если вы обычно работаете с другим набором свойств, вы можете загрузить электронную таблицу и добавить свои собственные числа.
The WebElements Scholar Edition
Высококачественный источник информации в Интернете о периодической таблице для студентов. Вы найдете множество изображений, показывающих структуру элементов и периодические свойства.
Деревянная таблица Менделеева
Настоящая таблица с чашками под каждым деревянным бруском, удерживающими сам элемент. Множество информации о каждом элементе, если вы захотите собрать свой собственный.
Бесплатные уроки химии
Chem4Kids
Итак, вы спрашиваете, что такое ХИМИЯ? Что ж … вот наше лучшее определение. Химия – это изучение МАТЕРИИ и изменений, которые происходят с ней .
Chemistry 11
Джереми Шнайдер приложил согласованные усилия, чтобы использовать учебник как можно реже (на случай, если он снова изменится в будущем). Таким образом, для большинства этих уроков не требуется учебник. Любые ссылки на Нельсона, которые действительно появляются, обычно могут быть заменены другим текстом по основам химии.
Любые ссылки на Нельсона, которые действительно появляются, обычно могут быть заменены другим текстом по основам химии.
Chemtutor
Это руководство начинается с основ и дает экспертную помощь на самых сложных этапах понимания вашего первого курса химии.
Курсы по химии на Coursera
Эти курсы постоянно меняются и ведутся на многих языках со всего мира, поэтому выберите свой предпочтительный язык. Для подростков сначала поищите курсы общих понятий, а затем продолжайте работу. Когда я посмотрел, мне предложили курс судебной медицины.
Creative Chemistry
Химические головоломки, интерактивные контрольные опросы, молекулярные модели и гараж настройки Sc1, которые помогут улучшить ваши научные исследования GCSE.Все, что вам нужно для вашего химического клуба.
Общая химия онлайн
Для целеустремленных подростков это бесплатный полный курс химии прямо в сети.
Chemistry
MIT курсы, но подходят для подростков.
Другие идеи по химии
Пузыри
Расследование на месте преступления
Пищевая химия
Рецепт Гака
Мороженое
Теги: химия, наука
Вычислительная техника | Кафедра химии
Dr. Дэйв Хроват
Дэйв Хроват
Менеджер – Компьютерное оборудование
Офис: Химический корпус 321A
Телефон: (940) 565-4041
[email protected]
Химический факультет предоставляет компьютерное оборудование как для исследований, так и для преподавания. Для исследования доступны высокопроизводительные вычислительные мощности, обеспечивающие 269 узлов с общим объемом процессора 521 (1484 ядра), 3,8 ТБ памяти и ~ 150 ТБ дискового пространства. В дополнение к обширному оборудованию существует широкий выбор программного обеспечения для вычислительной химии, доступного для исследований, в том числе AbInit, Crystal, Gamess, Guassian, Molcas, Molpro и NWChem.Учебные помещения включают учебную лабораторию вычислительной химии (CCIL). CCIL предоставляет ресурсы как для бакалавриата, так и для последипломного образования.
Кластер Dell из 142 узлов с гигабитным межсоединением. Главный узел – это PowerEdge 2950 с двумя четырехъядерными процессорами Intel Xeon / EM64T [2,66 ГГц], памятью 16 Гбайт и двумя дисками SCSI 146 Гбайт (raid-1). Имеется 128 вычислительных узлов PowerEdge 1950, каждый из которых оснащен двумя четырехъядерными процессорами Intel Xeon / EM64T [2,66 ГГц], памятью 16 Гбайт и одним диском SCSI на 400 Гбайт.Имеется 8 вычислительных узлов PowerEdge R900, каждый из которых оснащен четырьмя четырехъядерными процессорами Intel Xeon / EM64T [2,66 ГГц], памятью 128 ГБ и двумя дисками SCSI 146 ГБ (raid-1). Кроме того, каждый вычислительный узел R900 оснащен внешней системой хранения SAS Dell MD3000 с дисками SCSI 15–300 Гб (raid-0), обеспечивающими каждому узлу 4 Тбайт рабочего дискового пространства. Имеется 4 вычислительных узла PowerEdge 6850, каждый из которых оснащен четырьмя двухъядерными процессорами Intel Xeon / EM64T [3,4 ГГц], памятью 32 ГБ и двумя дисками SCSI 146 ГБ (raid-1).Кроме того, каждый вычислительный узел 6850 оснащен внешним хранилищем SAS Dell MD1000 с дисками SCSI 15–300 Гб (raid-0), предоставляя каждому узлу 4 ТБ рабочего дискового пространства.
Имеется 128 вычислительных узлов PowerEdge 1950, каждый из которых оснащен двумя четырехъядерными процессорами Intel Xeon / EM64T [2,66 ГГц], памятью 16 Гбайт и одним диском SCSI на 400 Гбайт.Имеется 8 вычислительных узлов PowerEdge R900, каждый из которых оснащен четырьмя четырехъядерными процессорами Intel Xeon / EM64T [2,66 ГГц], памятью 128 ГБ и двумя дисками SCSI 146 ГБ (raid-1). Кроме того, каждый вычислительный узел R900 оснащен внешней системой хранения SAS Dell MD3000 с дисками SCSI 15–300 Гб (raid-0), обеспечивающими каждому узлу 4 Тбайт рабочего дискового пространства. Имеется 4 вычислительных узла PowerEdge 6850, каждый из которых оснащен четырьмя двухъядерными процессорами Intel Xeon / EM64T [3,4 ГГц], памятью 32 ГБ и двумя дисками SCSI 146 ГБ (raid-1).Кроме того, каждый вычислительный узел 6850 оснащен внешним хранилищем SAS Dell MD1000 с дисками SCSI 15–300 Гб (raid-0), предоставляя каждому узлу 4 ТБ рабочего дискового пространства.
Кластер Dell из 47 узлов с гигабитным соединением Ethernet. Главный узел – PowerEdge 1850 с двумя процессорами Intel Xeon / EM64T [3,6 ГГц], памятью 4 ГБ и двумя дисками SCSI 146 ГБ (raid-1). 46 вычислительных узлов PowerEdge SC1425 сконфигурированы с двумя процессорами Intel Xeon / EM64T [3,6 ГГц], памятью 4 Гбайт и одним диском SATA 250 Гбайт. Кластер PSSC Labs на 26 узлов с гигабитным Ethernet и высокоскоростными межсоединениями Myrinet. Главный узел оснащен двумя процессорами AMD Opteron 252 [2,6 ГГц], памятью 8 ГБ и двумя дисками SATA 120 ГБ (raid-1). Отдельный файловый сервер 1,7 ТБ содержит два процессора AMD Opteron 246 [2,0 ГГц], память 4 ГБ, два диска SATA 80 ГБ (raid-1) и восемь дисков SATA 300 ГБ (raid-5). Каждый из 24 вычислительных узлов оснащен двумя процессорами AMD Opteron 252 [2,6 ГГц], памятью 8 ГБ и одним диском SATA 300 ГБ.Основным вычислительным ресурсом для использования в курсе и для сотрудников является кластер Dell из 49 узлов с гигабитным соединением Ethernet. Главный узел – это PowerEdge 850 с одним двухъядерным процессором Intel Xeon / EM64T [3,2 ГГц], памятью 1 ГБ и двумя дисками SCSI 73 ГБ (raid-1).
Главный узел – PowerEdge 1850 с двумя процессорами Intel Xeon / EM64T [3,6 ГГц], памятью 4 ГБ и двумя дисками SCSI 146 ГБ (raid-1). 46 вычислительных узлов PowerEdge SC1425 сконфигурированы с двумя процессорами Intel Xeon / EM64T [3,6 ГГц], памятью 4 Гбайт и одним диском SATA 250 Гбайт. Кластер PSSC Labs на 26 узлов с гигабитным Ethernet и высокоскоростными межсоединениями Myrinet. Главный узел оснащен двумя процессорами AMD Opteron 252 [2,6 ГГц], памятью 8 ГБ и двумя дисками SATA 120 ГБ (raid-1). Отдельный файловый сервер 1,7 ТБ содержит два процессора AMD Opteron 246 [2,0 ГГц], память 4 ГБ, два диска SATA 80 ГБ (raid-1) и восемь дисков SATA 300 ГБ (raid-5). Каждый из 24 вычислительных узлов оснащен двумя процессорами AMD Opteron 252 [2,6 ГГц], памятью 8 ГБ и одним диском SATA 300 ГБ.Основным вычислительным ресурсом для использования в курсе и для сотрудников является кластер Dell из 49 узлов с гигабитным соединением Ethernet. Главный узел – это PowerEdge 850 с одним двухъядерным процессором Intel Xeon / EM64T [3,2 ГГц], памятью 1 ГБ и двумя дисками SCSI 73 ГБ (raid-1). 48 вычислительных узлов представляют собой PowerEdge 850, каждый из которых оснащен одним двухъядерным процессором Intel Xeon / EM64T [3,2 ГГц], памятью 1 ГБ и одним диском SATA 80 ГБ.
48 вычислительных узлов представляют собой PowerEdge 850, каждый из которых оснащен одним двухъядерным процессором Intel Xeon / EM64T [3,2 ГГц], памятью 1 ГБ и одним диском SATA 80 ГБ.
Учебная лаборатория вычислительной химии (CCIL)
CCIL содержит 28 ПК малого форм-фактора, каждый из которых оснащен процессором Intel Pentium4 [3.2 ГГц], 2 ГБ памяти, диск SATA на 120 ГБ и привод DVD R / RW. Аналогично оборудованное место для инструктора доступно с проектором для показа монитора инструктора классу. Для печати материалов по химии доступны два принтера (цветной, черный и белый). Доступно программное обеспечение для операционной системы Windows XP (например, MS Office, Adobe Acrobat, Media Player, Firefox и т. Д.). Кроме того, доступно следующее программное обеспечение, связанное с химией и наукой: Spartan, Gaussian03W, PC Gamess, GaussView, упражнения по органической номенклатуре, реакции и спектроскопии, система онлайн-обучения (OWL), SciFinder, Mathematica, Matlab, Maple и программное обеспечение для молекулярной визуализации (i. е. Молден и РасМол). Лаборатория открыта для всех студентов и аспирантов, обучающихся на курсах химии, а лаборант доступен для помощи пользователям в установленные часы.
е. Молден и РасМол). Лаборатория открыта для всех студентов и аспирантов, обучающихся на курсах химии, а лаборант доступен для помощи пользователям в установленные часы.
Командное обучение – Университет Кил
Недавно мы разработали здесь, в Килле, средство, меняющее правила игры, чтобы вы могли проводить TBL онлайн, используя стандартную учебную платформу вашего университета или школы. Основным камнем преткновения было отсутствие электронной скретч-карты, которую можно было бы легко интегрировать в обучающие платформы.Эта проблема теперь решена с помощью новой онлайн-скретч-карты с мгновенной обратной связью.
Карточка была разработана в Килле Космой Готтарди во время отпуска по беременности и родам. Мы тестировали его в Килле в течение года, и он надежен, прост в использовании и нравится как сотрудникам, так и студентам. Лучше всего то, что это бесплатно!
Существует три отдельных этапа командного обучения: подготовка к занятиям, процесс обеспечения готовности и действия по применению, как показано в таблице ниже:
| 1-й этап | 2-й этап | 3-й этап |
|---|---|---|
| Предклассовая подготовка | Процесс обеспечения готовности | Действия приложения |
| Лекции | iRAT: индивидуальные MCQ | Команды используют концепции, изученные в RAP, для решения сложных задач |
| Скринкасты | tRAT: командное обсуждение ответов на вопросы MCQ, выявленных с помощью скретч-карт | Командные дебаты и обсуждения |
| Чтение перед классом | Инструкция репетитора | Проблемы, связанные с вопросами экзаменационного типа |
| Ресурсы электронного обучения | Апелляции |
TBL – отличная структура для целых классов проблемных когорт. Это обеспечивает низкое соотношение сотрудников и студентов, стимулирует участие студентов и создает индивидуальную и командную ответственность за участие в обучении – TBL действительно создает активных учащихся. Вы можете либо отказаться от всех лекций и посвятить все время общения студентов TBL, либо вы можете поддерживать лекции и использовать TBL как часть регулярных проблемных сессий на протяжении всего курса.
Это обеспечивает низкое соотношение сотрудников и студентов, стимулирует участие студентов и создает индивидуальную и командную ответственность за участие в обучении – TBL действительно создает активных учащихся. Вы можете либо отказаться от всех лекций и посвятить все время общения студентов TBL, либо вы можете поддерживать лекции и использовать TBL как часть регулярных проблемных сессий на протяжении всего курса.
Основные характеристики:
- Стабильные смешанные команды, которые продержатся целый модуль
- Регулярное тестирование базовых знаний
- Групповое решение задач в структурированном формате
- Петли обратной связи с коллегами и инструкторами
- Эффективный контроль успеваемости студентов преподавателем
- Навыки, улучшенные с помощью TBL, взяты из списка будущих навыков Всемирного экономического форума
Когда 80% класса говорят, что они чему-то научились у своих сверстников через TBL, что-то должно быть правильно.

