Урок по химии на тему “Задачи на сплавы и растворы”(9 класс)
Тема: «Задачи на сплавы и растворы» (интегрированный здоровьесберегающий урок химия-математика)
Цель: показать возможность подготовки обучающихся к ГИА и ЕГЭ на примере решения задач на сплавы и растворы различными способами через интегрированные уроки.
Ход урока:
При решении задач на получение нового раствора из исходных или нового сплава из металлов или сплавов (если дополнительные условия не оговорены в условии задачи) необходимо использовать закон сохранения массы, открытый М.В.Ломоносовым (1748), в общем виде сформулирован А.Лавуазье (1789):
общая масса веществ, вступающих в химическую реакцию, равна общей массе продуктов реакции,
или масса сплава равна сумме масс составляющих его частей и общая масса каждого вещества в сплаве равна сумме масс этого вещества во всех составляющих частях, аналогично и для растворов.
Классификация задач на проценты:
Расчеты по уравнению реакций.
Задачи на смеси.
Задачи на “тип соли” (определение состава продукта реакции).
Нахождение массовой доли одного из продуктов реакции в растворе.
Нахождение массы одного из исходных веществ по уравнению.
Схема решения задачи по химии
Условие задачи
Запись уравнения химической реакции
Расчеты по химическим уравнениям реакции
Запись и интерпретация ответа
Химическая часть задачи:
Чтение текста
Запись условия задачи
Определение типа задачи
Анализ задачи – составление плана решения
Математическая часть задачи:
Выбор способа решения
Решение
Запись ответа
Анализ решения
Задача (учитель математики)
Первый сплав содержит 5% меди, второй – 13 % меди.
1 сплав 5% 2 сплав 13% новый сплав11%
Решение:
Пусть х кг масса 1 сплава.
% меди
Масса сплава
Масса меди
1 сплав
5
х
0,05х
2 сплав
13
х+9
0,13(х+9)
3 сплав
11
х+х+9
0,11(х+х+9)
Составим и решим уравнение.
0,05х+0,13(х+9)= 0,11(х+х+9),
0,18х+1,17=0,22х+0,99,
0,04х=0,18,
х=4,5.
4,5+4,5+9=18(кг)- масса третьего сплава.
Ответ: масса третьего сплава 18 килограмм.
Химический опыт и решение задачи по нему (учитель химии).
Задача
Смешали 300 мл 20%-ного раствора CuCl2 и 400 мл 30%-ного раствора Na OH. Определите массу полученного раствора.
Определите массу полученного раствора.
m р-ра= 300 г CuCl2 + 2 NaOH → Cu(OH)
ω(CuCl2) = 20%= 0,2
m р-ра= 400 г m в-ва = ω· m р-ра
ω(NaOH) = 30%= 0,3 m (CuCl2) = 300·0,2 = 60 (г)
m (NaOH) = 400·0,3=120 (г)
m(Cu(OH)2) – ? n (CuCl2) =
n (CuCl2) =
n (NaOH)=
Задачу решаем по недостатку CuCl2.
n (CuCl2) = n (Cu(OH)2) = 0,45 моль.
m(Cu(OH)2) =0,45 моль · 98 г/моль =44,1 (г)
Ответ: m(Cu(OH)2 ) =44,1 г.
Физкультминутка на движение( можно танцевальную)
Задача
В сосуд, содержащий 10 литров 24%-го водного раствора некоторого вещества, добавили 5 литров воды. Сколько процентов составит концентрация получившегося раствора?
Решение:
Химия
Vр-ра=10 л Vв-ва= φVр-ра
φ=24%=0,24 Vв-ва=0,24·10=2,4л
V(H2O)=5л V2р-ра=V1р-ра+V(H2O)
V2р-ра=10+5=15л
φ2в-ва=2,4/15=0,16=16%
Математика
0,24·10=2,4(л)-объём вещества.

10+5=15(л)-объём второго раствора.
2,4:15·100=16%-концентрация нового раствора.
Ответ: 16%.
Задача
Смешали 14 литров 30-процентного водного раствора некоторого вещества с 10 литрами 18-процентного раствора этого же вещества. Сколько процентов составляет концентрация получившегося раствора?
Задача
Смешали 30% и 10% растворы соленой кислоты и получили 600г 15% раствора. Сколько граммов каждого вещества взяли?
Решение:
“Конверт Пирсона”:
30%
5%
3 – 450г
15%
5
10%
15%
1 – 150г
600 : (1+3) = 150(г) – 10% раствор.
150·3 = 450(г) – 30% раствор.
Ответ: 150 г и 450 г.
Раствор
масса р-ра
масса к-ты
30%
x
0,3x
10%
y
0,1y
15%
600
0,15·600
I раствор – х г, кислоты – 0,3х г
II раствор – у г, кислоты – 0,1у г
Новый раствор 600 г, кислоты 0,15·600 г
Ответ: 150 г и 450 г.
Аналогичные задачи из ЕГЭ.
Задача В13 (В14)
В сосуд, содержащий 20 литров 15-процентного водного раствора некоторого вещества, добавили 5 литров воды. Сколько процентов концентрация получившегося раствора?
В сосуд, содержащий 7 литров 24-процентного водного раствора некоторого вещества, добавили 7 литров воды. Сколько процентов составляет концентрация получившегося раствора?
Смешали некоторое количество 15-процентного раствора некоторого вещества с таким же количеством 19-процентного раствора этого же вещества.
 Сколько процентов составляет концентрация получившегося раствора?
Сколько процентов составляет концентрация получившегося раствора?Смешали 4 литра 15-процентного водного раствора некоторого вещества с 6 литрами 25-процентного водного раствора этого же вещества. Сколько процентов составляет концентрация получившегося раствора?
Первый сплав содержит 10 % меди, второй — 40 % меди. Масса второго сплава больше массы первого на 3 кг. Из этих двух сплавов получили третий сплав, содержащий 30 % меди. Найдите массу третьего сплава. Ответ дайте в килограммах.
Смешав 30-процентный и 60-процентный растворы кислоты и добавив 10 кг чистой воды, получили 36-процентный раствор кислоты. Если бы вместо 10 кг воды добавили 10 кг 50-процентного раствора той же кислоты, то получили бы 41-процентный раствор кислоты. Сколько килограммов 30-процентного раствора использовали для получения смеси?
Имеются два сосуда, содержащие 42 кг и 6 кг раствора кислоты различной концентрации.
 Если эти растворы смешать, то получится раствор, содержащий 40% кислоты. Если же смешать равные массы этих растворов, то получится раствор, содержащий 50% кислоты. Сколько кг кислоты содержится в первом растворе?
Если эти растворы смешать, то получится раствор, содержащий 40% кислоты. Если же смешать равные массы этих растворов, то получится раствор, содержащий 50% кислоты. Сколько кг кислоты содержится в первом растворе?
В разработке показано применение «Конверта Пирсона» для решения задач по химии.
Данная тема очень важна в реальной жизни. Ведь часто мы сталкиваемся с необходимостью приготовления раствора нужной концентрации, рассчитать массу вещества в продукте, чистого металла, содержание вредных веществ в воздухе и т.д.
Групповая работа на уроке при закреплении материала. Помимо интегрированного, этот урок и здоровьесберегающий (с физкультминуткой, сменой работы, опытом по химии и т.д.), что так важно в наше время и соответствует требованиям.
Урок на тему «Решение задач на определение массовой доли вещества в сплавах и растворах»
Тема урока: Решение задач на сплавы и растворы.
Цели:
Образовательные:
Актуализировать понятие процента, массовой доли вещества и концентрации вещества.
. Рассмотреть алгоритм решения задач на сплавы и растворы: познакомиться с приемами решения задач в математике и химии.
Выявить уровень овладения учащихся комплексом знаний и умений по решению задач на смеси химическими и математическими способами.
Развивающие:
Развивать способности к самостоятельному выбору метода решения задач.
Умение обобщать, абстрагировать и конкретизировать знания.
Умение оценивать собственные возможности.
Воспитательные:
Воспитывать познавательный интерес к химии и математике, культуру общения, способность к коллективной работе.
Задачи урока.
Обобщить знания учащихся по теме « Расчетные задачи с использованием понятия «доля», «процентная концентрация».
Продолжить развивать умения решать задачи, используя алгебраический метод решения.
Ход урока
I. Организационный момент (Слайд №1 )
Учитель математики: Здравствуйте! Сегодня мы проводим необычный урок. Урок по структуре называется интегрированным. Прежде всего мы сформулируем тему урока. А чтобы сформулировать тему урока, давайте вспомним олимпиаду зимних олимпийских игр 2018. Олимпиада проводилась с 9 по 25 февраля 2018 года в городе Пхёнчхане Южной Кореи. Это небольшой курортный городок численность населения не превышает 50 тысяч человек, был выбран столицей 23-й Олимпиады-2018. Медали Пхенчхана весят около полкилограмма и имеют толщину 0,8 см. Золотые медали олимпийцев содержат 1% (6 граммов) чистого золота, серебряные сделаны из чистого серебра, а бронзовые – из медного сплава. С учетом рыночной цены металлов стоимость медалей такова: золотая – $577, серебряная – $320, бронзовая – $3,50.
Обратимся к таблице.
Всего участвовало 87 стран. 1м-Норвегия, 2м-Германия, 3м-Канада, а Россия заняла 13 место. Наши спортсмены завоевали 2 золотые, 6 серебряных и 9 бронзовых медалей. За всю историю проведения олимпийских игр медали были самыми крупными.
1м-Норвегия, 2м-Германия, 3м-Канада, а Россия заняла 13 место. Наши спортсмены завоевали 2 золотые, 6 серебряных и 9 бронзовых медалей. За всю историю проведения олимпийских игр медали были самыми крупными.
Учитель химии:
Учитель химии: Золотая медаль содержит 580 г серебра и 6 грамм золота. Медаль массазы 586 г.
Итак, тема урока…. « Решение задач на сплавы и расстворы» (учащиеся формулируют сами)
Какова цель нашего урока? (Обобщить знания учащихся по теме « Расчетные задачи с использованием понятия «доля», «процентная концентрация»)
Эпиграф: (Слайд № 2)
«Только из союза двух работающих вместе и при помощи друг друга рождаются великие вещи»
Антуан деСент- Экзюпери
Учитель математики: Задачам на растворы в школьной программе по математике уделяется очень мало времени, но эти задачи встречаются на экзаменах в 9 и 11 классах. На этом уроке мы посмотрим с вами на задачи с двух точек зрения – с химической и математической, и выясним: как математика помогает в решении химических задач и как химия решает некоторые математические задачи.
Учитель математики: Для урока необходимо повторить некоторые определения .Устная разминка: начнем с кроссворда
Кроссворд:
1. Сотая часть числа называется …(процент)
2. Частное двух чисел называют …(отношение)
3. Верное равенство двух отношений называют …(пропорция)
4. В химии определение этого понятия звучало бы так: гомогенная смесь, образованная не менее чем двумя компонентами … (раствор). Один из которых называется растворителем, а другой растворимым веществом.
5. Отношение массы растворимого вещества к массе раствора называют массовой долей вещества в растворе или …(концентрация)
Вырази в процентах числа
Представь в виде десятичных дробей
Учитель химии: Золотая медаль содержит 580 г серебра и грамм золота. Медаль массазы 586 г.
Серебряная медаль серебро 99.9 олово-0,1
Бронзовая медаль- Си- 90%, цинк- 10%,
Задача 1. Масса олимпийских медалей составляет 586 г. Массовая доля золота в золотой медали равна 1,024%. Какова масса чистого золота в золотой медали?
Какова масса чистого золота в золотой медали?
Дано: Решение:
m (медали)= 586г
W (Au)= 1,024% W (в-ва)= m (в-ва)/ m (сплава)
m (Au)= m( ) x w (Au)
(Au) -7
m (Au)=586×0,01024= 6г
Ответ: m (Au)= 6г
Задача 2
Дано: Решение:
m (медали)= 586г
W (Ag)= 99,9% W (в-ва)= m (в-ва)/ m (сплава)
m (Ag)= m( ) x w (Ag)
(Ag) -7
m (Ag)=586x 0,999= 585,41
Ответ: m (Ag)= 585,41
Это химическое решение задачи на содержания металла в сплаве основываясь на формулу вычисления массовой доли вещества.
m (Au)=586×0,01024= 6г
m (Ag)=586x 0,999= 585,41
Давайте, попробуем составить другое выражение
показывающее соотношение трех данных данной формулы.
ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, m | |
СПЛАВ |
Учитель математики: (Слайд №24)
Задача №3:Для изготовления ювелирной продукции используют сплав золота с медью.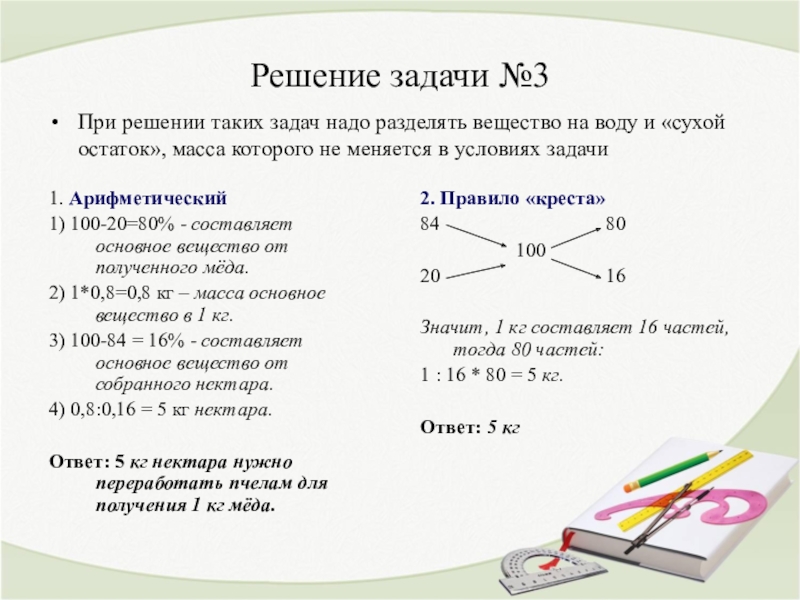
Определите процентное содержание(массовую долю)золота в сплаве, полученном из 1 кг золота и 715г меди.
СПЛАВ | ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, m |
Х | 1,715кг | 1 кг |
W (в-ва)= m (в-ва)/ m (сплава )
(1:1,715) *100%=58%
Задача 4
Изюм получается в процессе сушки винограда. Сколько кг винограда потребуется для получения 20 кг изюма, если виноград содержит 90% воды, а изюм содержит 5% воды
ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, | |
Изюм | 1-0,05= 0,95 | 20кг | 0,95 *20= 19кг |
Виноград | 1-0. | Х | 0,1Х |
0,1Х=19
Х=190 кг
5) Исследовательская работа .
ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, m | |
серьги | 0,585 | Х | |
Чайная ложка | 0,15 | Х |
Задача и6
Имеется два сплава. Первый содержит 10% никеля, второй -30% никеля. Из этих двух сплавов получили 3 сплав, массой 200 кг, содержащий 25% никеля. На сколько кг масса первого сплава была меньше массы второго?
сплавы | ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, m |
I | 0,1 | Х | 0,1х |
II | 0,3 | У | 0,3у |
III | 0,25 | 200 | 50 |
Составляем систему уравнений:
Х+У=200
0,1х+0, 3у=50
Задача 7.
Имеется 2 сплава. Первый сплав содержит 10% Си и Второй 40% Си. Масса второго сплава больше массы первого на 3 кг. Из этих двух сплавов получили третий сплав, содержащий 30 % Си. Найдите массу 3 его сплава. Ответ дайте в кг
сплавы | ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, m |
I | 0,1 | Х | 0,1х |
II | 0,4 | Х+3 | 0,4( Х+3) |
III | 0,3 | 2Х+3 | 0,3( 2Х+3) |
0,1Х+ 0,4(Х+3)= 0,3( 2Х+3)
Задачи на растворы.
Задача 8
Смешали некоторое количествр15-пролцентного
р-ра некоторого вещества с таким же количеством 19-процентного р-ра этого вещества. Сколько процентов составляет концентрация полечившегося раствора?
сплавы | ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА сплава | масса вещества, m |
I | 0,15 | А | 0,15А |
II | 0,19 | А | 0,19 А |
III | Х | 2А | 2АХ |
0,15А+0,19А= 2АХ
Задача 8.
Имеется два сосуда.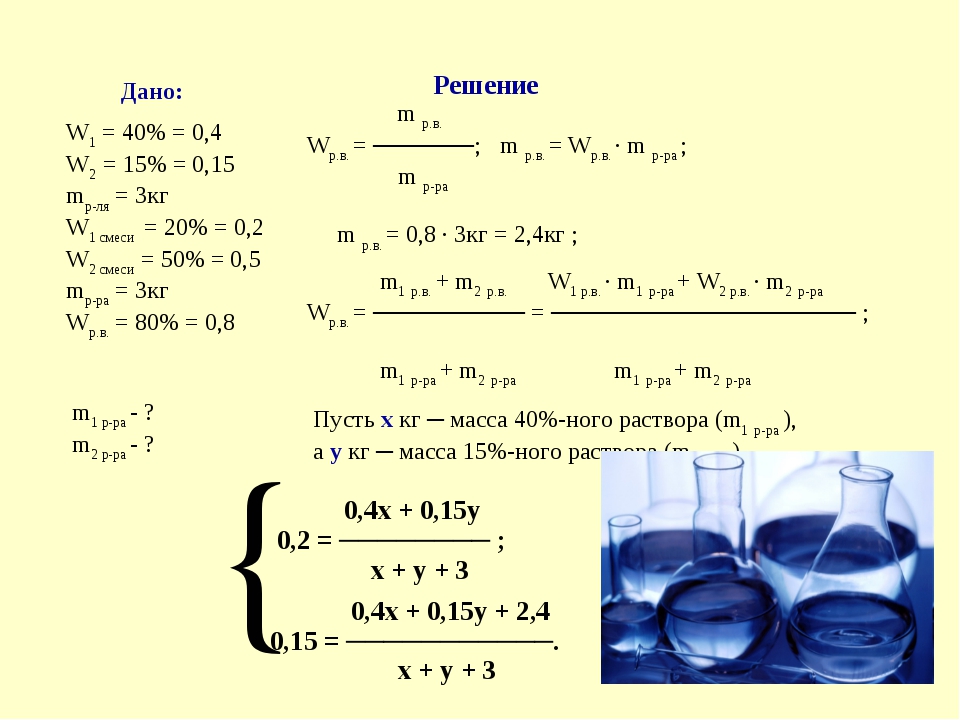 Первый содержит 30 кг, а второй -20 кг раствора кислоты различной концентрации
Первый содержит 30 кг, а второй -20 кг раствора кислоты различной концентрации
Определите массу никеля и хрома в столовых приборах
если массовая доля никеля составляет 10 %, хрома 18%.
Вес приборов представлен в таблице:
№ | Название прибора | вес | Масса никеля | Масса хрома |
1. | Чайная ложка | 25г | 25*0,1=2,5 | 25*0,18=4,5 |
2. | Столовая ложка | 55г | 55*0,1=5,5 | 55*0,18=9,9 |
3. | Нож | 60г | 60*0,1=6 | 60*0,18=10,8 |
4. | Вилка | 35г | 35*0,1=3,5 | 35*0,18=6,3 |
Учитель химии:
Итак, чтобы найти массу вещества в смеси (сплаве), нужно массу смеси(сплава) умножить на долю содержания вещества
Учитель математики:
Задача №3:Для изготовления ювелирной продукции используют сплав золота с медью.
Определите процентное содержание(массовую долю)золота в сплаве, полученном из 1 кг золота и 715г меди.
Алгебраический | химический |
w = m (р.в.)/m (р-ра ) | |
(1:1,715) *100%=58% | W=(1000/1715)*100%=58% |
ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА СМЕСИ, М | масса основного вещества, m | |
СПЛАВ | ПРОЦЕНТНОЕ СОДЕРЖАНИЕ ОЛОВА | МАССА СПЛАВА, г. | МАССА ОЛОВА,г. |
100% = 100% = 28%
Ответ: 28 %
Имеется два сплава. Первый содержит 10% никеля, второй -30% никеля. Из этих двух сплавов получили 3 сплав, массой 200 кг, содержащий 25% никеля. На сколько кг масса первого сплава была меньше массы второго?
Имеется 2 сплава. Первый сплав содержит 10% Си и Второй 40% Си. Масса второго сплава больше массы первого на 3 кг. Из этих двух сплавов получили третий сплав, содержащий 30 % Си. Найдите массу 3 его сплава. Ответ дайте в кг
Смешали некоторое количествр15-пролцентного
р-ра некоторого вещества с таким же количеством 19-процентного р-ра этого вещества. Сколько процентов составляет концентрация полечившегося раствора?
Смешали 4 литра 25-процентного водного раствора некоторого вещества с 6 литрами 25- процентного водного раствора этого же вещества. Сколько процентов составляет концентрация получившегося раствора?
Задача 2. (Габриелян О.С. «Химия», 9 класс).
Вычислите массу меди и никеля, необходимые для производства 25 кг мельхиора. Мельхиор-сплав, содержащий 80% меди и 20% никеля.
Части | ДОЛЯ ОСНОВНОГО ВЕЩЕСТВА, | ОБЩАЯ МАССА СМЕСИ, М | масса основного вещества, m |
Медь | 80%=0,8 | ? (0,8 25 = 20 кг) | |
Никель | 20%=0,2 | ? (0,2 25 = 5 кг) | |
Сплав | 100%=1 | 25 | 25 кг |
Х = 0,8 25 = 20 кг.
Золотая медаль олимпиады 2018 года весит 586 г . Содержание золота в этой медали 1%. Найдите массу драгоценного металла-золота в этой медали.
адача 20 — металл для завода
2 сентября 2016
Условие
В двух областях есть по 20 рабочих, каждый из которых готов трудиться по 10 часов в сутки на добыче алюминия или никеля. В первой области один рабочий за час добывает 0,2 кг алюминия или 0,2 кг никеля. Во второй области для добычи xx кг алюминия в день требуется x2x2 человеко-часов труда, а для добычи yy кг никеля в день требуется y2y2 человеко-часов труда.
В первой области один рабочий за час добывает 0,2 кг алюминия или 0,2 кг никеля. Во второй области для добычи xx кг алюминия в день требуется x2x2 человеко-часов труда, а для добычи yy кг никеля в день требуется y2y2 человеко-часов труда.
Обе области поставляют добытый металл на завод, где для нужд промышленности производится сплав алюминия и никеля, в котором на 1 кг алюминия приходится 1 кг никеля. При этом области договариваются между собой вести добычу металлов так, чтобы завод мог произвести наибольшее количество сплава. Сколько килограммов сплава при таких условиях ежедневно сможет произвести завод?
Решение
Для производства сплава заводу необходимо получить равное количество алюминия и никеля, поэтому рабочие из первой области должны разделиться на две бригады по 10 человек. Работая по 10 часов в сутки, бригады добудут 0,2⋅10⋅10=200,2⋅10⋅10=20 кг алюминия и 20 кг никеля в сутки. Из них на заводе изготовят 40 кг сплава.
Человеко-час = Кол-во работников ⋅ Кол-во часов на рабочих местах Человеко-час = Кол-во работников ⋅ Кол-во часов на рабочих местах . Поэтому x2=10⋅10×2=10⋅10.
Поэтому x2=10⋅10×2=10⋅10.
Значит, во второй области за 10 часов в сутки 10 рабочих добудут x=10⋅10−−−−−√=10x=10⋅10=10 (кг) любого из металлов. Поскольку заводу необходимо получить равное количество металлов, необходимо разделить рабочих поровну, тогда они произведут 10 кг алюминия и 10 кг никеля. Из них на заводе изготовят 20 кг сплава.
Тем самым, завод сможет производить 40+20=6040+20=60 кг сплава ежедневно.
Правильный ответ
60
Подведение итогов урока
Учитель химии.
– Посмотрите на содержание всех решенных сегодня задач. Что их объединяет? (Задачи на растворы.)
– Действительно, во всех задачах фигурируют водные растворы; расчеты связаны с массовой долей растворенного вещества; и если вы обратили внимание, задачи касаются разных сторон нашего быта.
Учитель математики.
– Посмотрите на эти задачи с точки зрения математики. Что их объединяет? (Задачи на проценты.)
При решении всех этих задач мы используем правило нахождения процента от числа.
Оценки за урок.
Критерии оценивания: всего было 6 задач: максимальное кол-во заработанных жетонов-6Значит:
5-6 жетонов-«5»
3-4 – «4»
1-2 – «3»
Домашнее задание. : (Слайд31)
Текстовые задачи на смеси, сплавы, растворы
из сборника
«МАТЕМАТИКА. ПОДГОТОВКА К ЕГЭ-2014»
Под редакцией Ф. Ф. Лысенко, С. Ю. Кулабухова:
Смешали 30%-ный раствор соляной кислоты с 10%-ным и получили 600 г 15%-го раствора. Сколько граммов 10%-го раствора было взято?
Имеется кусок сплава меди с оловом общей массой 24 кг, содержащий 45% меди. Сколько чистого олова надо прибавить к этому куску сплава, чтобы полученный новый сплав содержал 40% меди?
Рефлексия
Критерии | Показатели | |||
Знаю и умею – 3 балла | Затрудняюсь – 2 балла | |||
Знаю | – определение процента | |||
– основное свойство пропорции; | ||||
определение массовой доли | ||||
Умею | – решать задачи на растворы и сплавы старинным способом; | |||
– решать задачи алгебраическим способом | ||||
– решать задачи с помощью химических формул; | ||||
Полезным ли для вас оказался этот интегрированный урок?
Смогли ли вы выбрать наиболее подходящий для вас способ решения?
Будете ли вы использовать эти методы в дальнейшем и при решении заданий ЕГЭ?
Наш урок подошел к концу.
Спасибо за урок!
Смеси исходных веществ с параллельно протекающими реакциями | Задачи 1
Задача 1.
Раствор, содержащий 34 г смеси гидроксида калия и гидроксида натрия нейтрализовали избытком соляной кислоты. В результате образовалось 47,9 г солей. Определите массу каждого из гидроксидов в исходной смеси.
Дано:
масса смеси гидроксидов в исходном р-ре: m(КОН+NаОН) = 34 г;
масса солей после нейтрализации раствора: mсмеси солей = 47,9 г.
Найти:
массу гидроксида калия в исходной смеси: m(КОН) = ?
массу гидроксида натрия в исходной смеси: m(NаОН) = ?
Решение:
Оба компонента смеси (КОН и NаОН) одновременно взаимодействуют с соляной кислотой. Записываем для каждого из веществ смеси свою химическую реакцию:
КОН + НС1 = КС1 + Н2О
NаОН + НС1 = NаС1 + Н2О
Решить данную задачу можно, применив встречный алгоритм.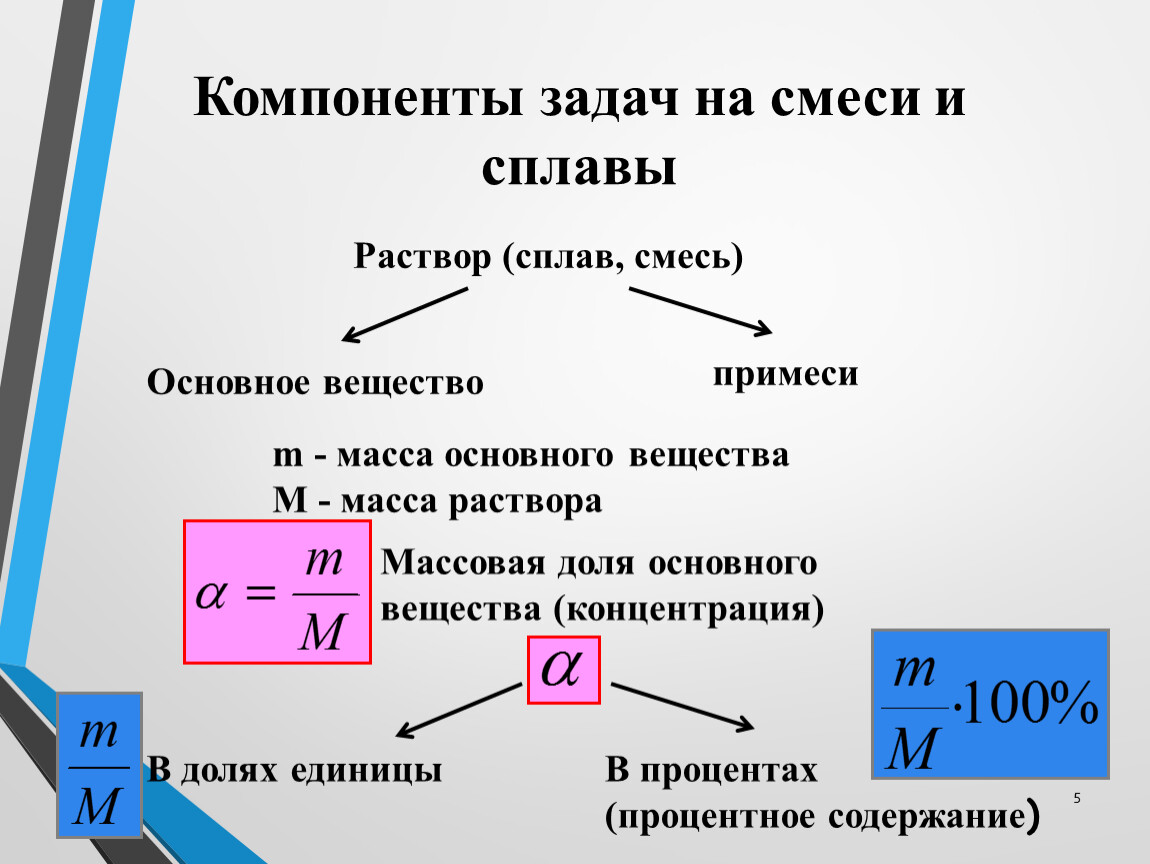 Его можно представить следующим образом:
Его можно представить следующим образом:
В условии требуется определить массу каждого из гидроксидов, поэтому обозначим массу КОН величиной «а» и массу NаОН величиной «в».
1. Используя введенные значения, составим первое математическое уравнение. Для этого приравняем сумму масс гидроксидов к общей их массе в исходном растворе:
а + b= m(КОН + NаОН) = 34 г,
а +b = 34.
Получилось одно математическое уравнение с двумя неизвестными.
2. Теперь, используя величины «а» и «в» как известные, по уравнениям реакций нейтрализации определяем массы полученных солей:
Составляем пропорцию:
а г КОН дают x г КСl (по условию)
56 г КОН дают 74,5 г КС1 (по уравнению)
Составляем пропорцию:
в г NаОН дают х г NаС1 (по условию)
40 г NаОН дают 58,5 г NаС1 (по уравнению)
3. Из условия известно, что суммарная масса полученных солей составляет 47,9 г. Используя полученные в предыдущем действии значения, составляем второе математическое уравнение с двумя неизвестными:
m(КС1) + m(NаС1) = (1,33 . а) + (1,46 . b) = 47,9 г
а) + (1,46 . b) = 47,9 г
(1,33 . а) + (1,46 . b) = 47,9
4. Объединяем два математических уравнения в систему:
Решение этой системы уравнений дает значения:
а = 13,4 г; в = 20,6 г.
Величиной «а» мы обозначали массу КОН, следовательно:
m(КОН) = 13,4 г;
величиной «в» мы обозначали массу NаОН, следовательно:
m(NаОН) =20,6 г.
Ответ: m(КОН) = 13,4 г; m(NаОН) =20,6 г.
Задача 2.
92 г смеси карбоната кальция и безводного нитрата кальция прокалили до окончания выделения газов. В результате выделилась смесь газов с относительной плотностью по водороду 21,63. Определите массу каждой соли в исходной смеси.
Дано:
масса смеси солей: mисход. cмеси[СаСО3) + Са(NО3)2] = 92 г;
относительная плотность смеси газов по водороду: D(Н2) = 21,63.
Найти:
массу карбоната кальция в исходной смеси: m(СаСО3) = ?
массу нитрата кальция в исходной смеси: m[Са(NО3)2] = ?
Решение:
Запишем реакции разложения каждой из солей:
СаСО3 = СаО + СО2 ↑
2Са(NO3)2 = 2СаО + 4NO2 ↑ + О2 ↑
Для решения придется использовать встречный алгоритм:
Применим представленный алгоритм.
1. Искомыми величинами являются массы солей в исходной смеси. Для большего удобства дальнейших расчетов разумнее величиной «а» обозначать количество вещества (n, моль) карбоната кальция: n(СаСО3) = а моль.
Величиной «b» обозначим количество вещества (n, моль) нитрата кальция: n[Са(NO3)2] = b моль.
Соответственно, через молярные массы этих солей можно перейти к массам самих солей:
m(CaCO3) = М(СаСОз) . n(СаСO3) = (100 . а) г;
n(СаСO3) = (100 . а) г;
m[Са(NO3)2] = М[Са(NO3)2] . n[Са(NO3)2] = (164 . b) г.
2. Общая масса исходных солей указана в условии. Это позволяет составить первое математическое уравнение с двумя неизвестными:
(100 . а) + (164 . b) = 92
3. Далее, используя введенные величины «а» и «в», по уравнениям реакций разложения определяем количество вещества каждого из газов:
n = a моль n = x моль
CaCO3 = CaO + CO2 ↑
n = 1 моль n = 1моль
Составим пропорцию:
а моль СаСО3 дают х моль СО2 (по данным условия)
1 моль СаСО3 дают 1 моль СО2 (по уравнению)
Составим пропорции:
b моль Са(NO3)2 дают х моль NО2 (по данным условия)
2 моль Са(NO3)2 дают 4 моль NО2 (по уравнению)
b моль Са(NO3)2 дают у моль О2 (по данным условия)
2 моль Са(NO3)2 дают 1 моль О2 (по уравнению)
4. Определим мольную долю каждого из газов в смеси (в долях от единицы).
Определим мольную долю каждого из газов в смеси (в долях от единицы).
5. Определим среднюю молярную массу смеси газов по значениям их мольных долей в смеси.
Мcр.смеси газов = М(СО2) . (СО2) + М(NО2) . (NO2) + М(O2) . (О2)
По закону Авагадро мольная доля газа в смеси численно равна объемной доле (только для газов), поэтому в формулу для определения Мcредн. вместо объемной доли (Z) подставляем
значение мольной доли ( ) соответствующего газа.
6. Определим среднюю молярную массу смеси газов по данным об относительной плотности.
7. Приравнивая друг другу выражения Мср. смеси газов полученные в двух предыдущих действиях, составляем второе математическое уравнение:
8. Объединяем уравнения, полученные во втором и седьмом действиях в систему
При ее решении получаются значения: а = 0,1; b = 0,5.
Величинами «а» и «b» мы обозначали количество вещества СаСО3 и Са(NO3)2 в исходной смеси солей, следовательно:
n(СаСО3) = 0,1 моль; n[Са(NO3)2] = 0,5 моль.
9. Определяем массы солей в исходной смеси:
m(СаСО3) = n(СаСО3) . М(СаСО3) = 0,1 . 100 = 10 г;
m[Са(NO3)2] = n[Са(NO3)2] . M[Са(NO3)2]) = 0,5 . 164 = 82 г.
Ответ: m(СаСО3) = 10 г; m[Са(NO3)2] = 82 г.
Комментарии:
1 С химической точки зрения в задачах этой группы происходит взаимодействие какого-либо одного реактива со смесью веществ. Причем все вещества смеси участвуют в реакции, но для каждого из них записывается свое химическое уравнение.
Это, так называемые, параллельные реакции. Селективные же реактивы, для выявления количества какого-либо одного участника смеси не используются. В условии задачи чаще всего присутствует информация об общем количестве исходной смеси и об общем количестве расходовавшегося реактива либо образовавшегося продукта. По этим данным обычно требуется выявить количественный состав исходной смеси.
Основная особенность этих задач заключается в том, что при их решении применяют встречный алгоритм с составлением системы математических уравнений. Рассмотрим несколько примеров решения подобных задач.
Тема №8135 Решение задач по химии смеси
Различные способы решения задач на смеси.
Задача. (на смешивание растворов)
Один раствор содержит 20% соли, а второй 70%. Сколько граммов первого и второго растворов нужно взять, чтобы получить 100 г 50%-го солевого раствора?
Способ 1.
1. Составим таблицу:
| α | М (г) | m (г) |
1-й раствор | 20% или 0,2 | x | 0,2 x |
2-й раствор | 70% или 0,7 | 100 – x | 0,7 (100 – x) |
смесь | 50 % или 0,5 | 100 | 50 |
2. Составим и решим уравнение:
Составим и решим уравнение:
0,2 х + 0,7 (100 – x) = 50
х = 40
Ответ: 60 г – 70% раствора и 40 г -20% раствора.
Способ 2.
1. Составим таблицу:
| α | М (г) | m (г) |
1-й раствор | 20% или 0,2 | x | 0,2 x |
2-й раствор | 70% или 0,7 | y | 0,7 y |
смесь | 50 % или 0,5 | 100 | 50 |
(α – доля основного вещества в смеси, М – общая масса смеси, m – масса основного вещества в смеси).
2. Составим и решим систему уравнений:
х + у = 100 х = 40
0,2 х + 0,7 у = 50 у = 60
Ответ: 60 г – 70% раствора и 40 г -20% раствора.
Способ 3.
Решим эту задачу старинным способом по правилу «креста». Составим схему:
20 20
50
70 30
Значит , 100 г смеси составляют 50 частей .
100 : (30+20)= 2 г.(одна часть)
2*30=60 г. (70% р-р)
2*20=40 г. (20% р-р)
Ответ: 60 г – 70% раствора и 40 г -20% раствора.
Правило «креста»:
В левой колонке схемы записаны процентные содержания соли в имеющихся растворах. Посередине – процентное содержание соли в полученной смеси. В правой – разности процентных содержаний имеющихся растворов и полученной смеси (вычитаем из большего числа меньшее и записываем разность на ту диагональ, где находятся, соответственно, уменьшаемое и вычитаемое).
Решите самостоятельно.
1. Имеется два раствора некоторого вещества. Один 15%-ный, а второй 65%-ный. Сколько нужно взять литров каждого раствора, чтобы получить 200л раствора, содержание вещества в котором равно 30%?
2. Имеется два сплава никеля с другой сталью, в которых содержание никеля составляет 5% и 40%. Сколько тонн каждого сплава нужно сплавить, чтобы получилось 140 тонн новой стали с 30-ным содержанием никеля?
Имеется два сплава никеля с другой сталью, в которых содержание никеля составляет 5% и 40%. Сколько тонн каждого сплава нужно сплавить, чтобы получилось 140 тонн новой стали с 30-ным содержанием никеля?
3. Имеется два разных сплава меди, процент содержания которой в первом сплаве на 40% меньше, чем во втором. Когда оба сплава соединили вместе, то новый сплав получился с 36-ным содержанием меди. Известно, что в первом сплаве было 6 кг меди, а во втором в 2 раза больше. Каково процентное содержание меди в обоих сплавах?
4. Смешали 30-ный раствор соляной кислоты с 10-ным. В итоге получилось 600г раствора с 15-ным содержанием соляной кислоты. Найдите, сколько взято было каждого раствора.
5. Бронза – сплав меди и олова. В древности из бронзы отливали колокола, если в ней содержалось 75% меди. К куску бронзы 500кг и содержащему 72% добавили некоторое количество бронзы, содержащей 80% меди, и получили бронзу, необходимую для изготовления колокола. Определите, сколько добавили 80% бронзы.
6. Имеется 600г сплава золота и серебра содержащего золото и серебро в отношении 1:5 соответственно. Сколько грамм золота необходимо добавить к этому сплаву чтобы получить новый сплав, содержащий 50% серебра.
7. Имеется стальной лом двух сортов с содержанием никеля 5% и 40%. Сколько нужно взять металла каждого из этих сортов, чтобы получить 140 т стали с содержанием 30% никеля?
8. 40% раствор серной кислоты разбавили 60% раствором, после чего добавили 5кг воды и получили раствор 20% концентрации. Если бы вместо 5кг воды добавили 5 кг 80% раствора серной кислоты, то получился бы 70% раствор. Сколько было 40% и 60% раствора серной кислоты?
9. Смешали 30%-й раствор соляной кислоты с ее 10%-м раствором и получили 600 г 15%-го раствора. Сколько граммов 30 % -го раствора было взято?
Задачи на добавление (удаление) одного вещества.
Задача 1.
Сироп содержит 18% сахара. Сколько килограммов воды нужно добавить к 40 г сиропа, чтобы содержание сахара составило 15%?
Решение.
Пусть надо добавить кг воды. Составим таблицу:
| α | М (г) | m (г) |
Было | 18% или 0,18 | 40 | 0,18 · 40 |
Стало | 15% или 0,18 | 40 + х | 0,15 (40 + х) |
Так как масса сахара не изменилась, то составим и решим уравнение:
0,15 (40 + х) = 0,18 · 40, х = 8.
Ответ: 8 кг.
Задача 2.
Сколько граммов 35%-го раствора марганцовки надо добавить к 325 г воды, чтобы концентрация марганцовки в растворе составила 10%?
Решение.
Решим задачу по правилу «креста»:
35 10
10
0 25
Значит, 325 г воды составляют 25 частей, а 35%-й раствор – 10 частей, или 325 : 25 · 10 = 130 г.
Ответ: 130 г.
Решите самостоятельно.
1. В 5 кг сплава олова и цинка содержится 80% цинка. Сколько килограммов олова надо добавить к этому сплаву, чтобы процентное содержание цинка стало 40%?
2. Имеется 4 литра 20%-го раствора спирта. Сколько воды него нужно, чтобы получился 10%-й раствор спирта?
3. К 40%-му раствору соляной кислоты добавили 50 г чистой соляной кислоты, в силу чего концентрация такого раствора стала равной 60%. Найти первоначальный вес раствора.
4. К раствору, содержащему 30 г соли, добавили 400 г воды, после чего концентрация соли уменьшилась на 10%/. Найти начальную концентрацию соли.
5. К 5 килограмм сплава олова и цинка добавили 4 кг олова. Найдите первоначальное процентное содержание цинка в первоначальном сплаве, если в новом сплаве цинка стало в 2 раза меньше олова.
6. При выплавке стали из чугуна, выжигается углерод. Содержание углерода в чугуне 4%. Сколько тонн углерода нужно выжечь из 245т чугуна, чтобы получилась сталь с содержанием углерода 2%?
7. Слиток сплава меди и цинка массой 36 кг содержит 45% меди. Какую массу меди надо добавить к этому куску, чтобы полученный сплав содержал 60% меди?
Слиток сплава меди и цинка массой 36 кг содержит 45% меди. Какую массу меди надо добавить к этому куску, чтобы полученный сплав содержал 60% меди?
8. Сколько чистого спирта нужно добавить к 735 г 16%-ного раствора йода и спирта, чтобы получить 10%-ный раствор?
Задачи к разделу Основные понятия и законы химии
Здесь собраны примеры задач с решениями на нахождение молекулярной формулы вещества, эквивалента, парциального давления и другие задачи. Теоретическую часть вы найдете в разделе Основные понятия и законы химии.
Задача 1. Какой объем (н.у.) занимает 5∙10-3 кг углекислого газа?
Показать решение »
Решение.
Найдем молекулярную массу СО2:
Mr(CO2)= 12+2∙16=44 г.
Tакже нам известен молярный объем газа, который равен 22,4 м3.
Составим следующую пропорцию:
44 кг СО2 занимает объем 22,4 м3
5∙10-3 кг СО2 занимает объем – х
откуда х=(5∙10-3∙22,4)/44=2,5∙10-3 м3
Таким образом, 5∙10-3 кг углекислого газа занимает объем равный 2,5∙10-3 м3.
Задача 2. Определить массу 0,9∙10-3 м3 кислорода при 21 °С и давлении 96000 Па, если масса 10-3 м3 кислорода равна 1,5∙10-3 кг при нормальных условиях.
Показать решение »
Решение:
Найдем температуру в Кельвинах Т=273+21=294 К;
Найдем объем газа, приведенный к н.у. по формуле
P1V1 / T1 = P2V2 / T2;
V1= T1P2V2/ T2P1=(273∙96000∙0.9∙10-3)/(294∙101325)=0.8∙10-3 м3
Теперь рассчитаем массу вычисленного объема:
10-3 м3 кислорода имеют массу равную 1,5∙10-3 кг
0,8∙10-3 м3 кислорода имеют массу равную х
х = 0,8∙10-3∙1,5∙10-3/10-3=1,2∙10-3 кг
Таким образом, 0,8∙10-3 м3 кислорода имеют массу равную 1,2∙10-3 кг.
Задача 3. Рассчитайте объем атома железа, если его плотность равна 7900 кг/ м3
Показать решение »
Решение:
Найдем молярный объем железа (M(Fe)=56 г.)
V=n/ρ=56/7900=7,1∙10-3 м3
Условно примем, что атомы имеют форму шара и в кристалле касаются друг друга, то истинный объем будет составлять только 74% от общего объема:
V=0,071∙0,74=5,25∙10-3 м3
Тогда объем одно атома железа будет равен:
VА=5,25∙10-3/6,02∙1026=8,7∙10-30 м3
Задача 4. Определить массу молекулы газа, если масса 10-3 м3 газа, при н.у., равна 0,3810-3 кг.
Показать решение »
Решение:
Число молекул 1 кмоль любого вещества равна числу Авогадро (6,02*1026 ), поэтому для начала определим 1 кмоль газа:
10-3 м3 газа имеют массу равную 0,3810-3 кг
22,4 м3 газа имеют массу равную — х
х=22,4∙0,3810-3/10-3=7,6 кг,
Далее определяем массу молекулы газа:
m=7,6/6,02∙1026=1,26∙10-26 кг.
Задача 5. Рассчитайте молярную массу эквивалента металла, если при соединении 7,2 г. металла с хлором было получено 28,2 г. соли. Молярная масса эквивалента хлора равна 35,45 г/моль
Показать решение »
Решение:
Согласно закону эквивалента отношение массы металла и соли должно быть равно отношению их молярных масс эквивалентов. Обозначим молярную массу эквивалента металла через х, тогда:
7,2/28,2=х/(х+35,45)
Решая уравнение, находим, что х=12,15 г/моль.
Таким образом, молярная масса эквивалента металла Мэкв=12,15 г/моль.
Задача 6. Определение молярной массы эквивалента сложных веществ в реакциях обмена
Определите молярные массы эквивалентов H2SO4 в следующих реакциях:
А) H2SO4+2KOH = K2SO4+2H2O
Б) H2SO4+KOH = KHSO4+H2O
Показать решение »
Решение: Значение эквивалента вещества зависит от того, в какой именно реакции оно участвует.
В реакции А) 1 моль H2SO4 взаимодействует с 2 моль KOH, а эквивалент H2SO4 с 2 эквивалентами KOH. Молярная масса эквивалента KOH равна его молекулярной массе, следовательно, молярная масса эквивалента H2SO4 равна половине ее молекулярной массы:
Мэкв=98/2=49 г/моль
В реакции Б) 1 моль H2SO4 взаимодействует с 1 моль KOH, а эквивалент H2SO4 с 1 эквивалентами KOH. Молярная масса эквивалента KOH равна его молекулярной массе, следовательно, молярная масса эквивалента H2SO4 равна ее молекулярной массе: 98 г/моль.
Задача 7. Рассчитайте молярную массу эквивалента кислоты, если на нейтрализацию 9 г. ее израсходовано 8 г. гидроксида натрия.
Показать решение »
Молярная масса эквивалента гидроксида натрия равна его молекулярной массе Мэкв=40 г/моль.
Вещества взаимодействуют между собой в массах, пропорциональных из молярным массам эквивалента, т.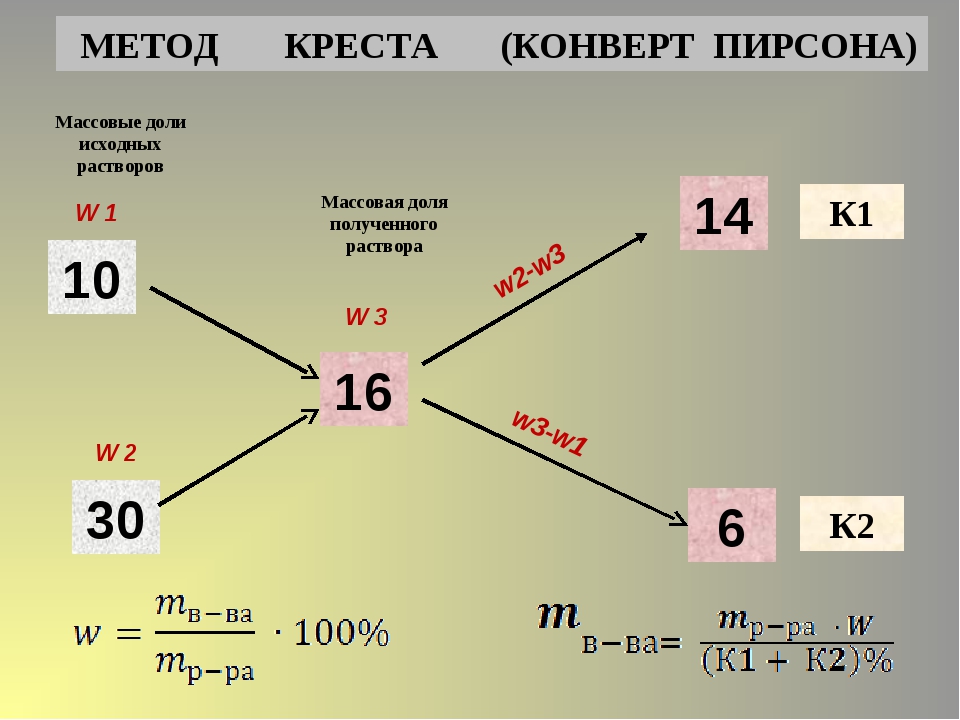 е.:
е.:
Обозначим молярную массу эквивалента кислоты – х, тогда
9/8=х/40
х=45 г/моль
Таким образом , молярная масса эквивалента кислоты Мэкв=45 г/моль.
Задача 8. Найдите молекулярную формулу вещества, если относительная плотность паров этого вещества по водороду равна 67,5, а массовые доли элементов (%) в веществе следующие: серы – 23,7, кислорода – 23,7, хлора – 52.
Показать решение »
Решение:
Формулу искомого соединения можно представить как SxOyClz. Найдем соотношение между числом атомов S, O, Cl делением его содержания на его атомную массу:
x:y:z = 23,7/32 : 23,7/16 : 52/35,5 = 0,74 : 1,48 : 1,46
Делим все полученные соотношения на наименьшее, получаем:
x:y:z =1:2:2
Простейшая формула вещества SO2Cl2
Его молекулярная масса равна
Mr = 32+16∙2+35,5∙2 = 135 г.
Теперь найдем молекулярную массу вещества по плотности паров этого вещества по водороду:
Mr = 2Dh3= 2∙67,5 = 135 г.
Следовательно, истинная формула вещества совпадает с простейшей: SO2Cl2
Задача 9. Рассчитайте молекулярную массу газа, если 7∙10-3 кг. его при 20°С и 0,253∙105 Па занимают объем 22,18∙10-3 м3
Показать решение »
Решение:
В данном случае, вычислить молярную массу газа можно, используя уравнение Клапейрона – Менделеева:
pV = nRT = (m/M)RT;
R=8,3144∙103 Дж/моль∙К
Т=273+20=293 К
М=mRT/pV=7∙10-3∙8,3144∙103293/(0,253∙105∙22,18∙10-3)=30,35 г/моль
Молярная масса газа равна 30,35 г/моль
Задача 10. При 0°С в сосуде объемом 14∙10-3 м3 содержится 0,8∙10-3 кг водорода и 6,3∙10-3 кг азота. Определите парциальное давление азота и общее давление смеси.
Показать решение »
Решение:
Найдем количества вещества водорода и азота:
n=m/Mn(H2)=0,8∙10-3/2=0,4∙10-3моль
n(N2)= 6,3∙10-3/28=0,225∙10-3моль
Далее, с помощью уравнения Клапейрона – Менделеева, найдем парциальное давление каждого газа в смеси:
pV = nRT = (m/M)RT;
p = nRT/V;
p(H2)=n(H2)
RT/V=0,4∙10-3∙8,3144*103∙273/14∙10-3=64,85∙103 Па
p(N2)= n(N2)
RT/V=0,225∙10-3∙8,3144∙103∙273/14∙10-3=36,479∙103 Па
pобщ=p(H2)+p(N2)= 64,85∙103+36,479∙103=101329 Па
Задача 11. Газовая смесь составлена из 5∙10-3 м3 метана под давлением 96000 Па, 2∙10-3 м3 водорода под давлением 84000 Па и 3∙10-3 м3 диоксида углерода под давлением 109000 Па. Объем смеси 8∙10-3 м3. Определите парциальные давления газов в смеси и общее давление смеси.
Показать решение »
Решение:
Сначала найдем парциальное давление каждого из газов:
p(CH4)=P(CH4)∙V(CH4)/Vобщ=96000∙5∙10-3/8∙10-3=60000 Па
p(H2)=P(H2)∙V(H2)/Vобщ=84000∙2∙10-3/8∙10-3=21000 Па
p(CО2)=P(CО2)∙V(CО2)/Vобщ=109000∙3∙10-3/8∙10-3=40875 Па
Общее давление:
pобщ= p(CH4)+ p(H2)+ p(CО2)= 60000+21000+40875=121875 Па
Задача 12.Газовая смесь состоит из оксида и диоксида азота. Вычислите парциальные давления газов в смеси, если объемные доли газов соответственно равны (%) 37,5 и 62,5. Общее давление газовой смеси 106640 Па.
Вычислите парциальные давления газов в смеси, если объемные доли газов соответственно равны (%) 37,5 и 62,5. Общее давление газовой смеси 106640 Па.
Показать решение »
Решение:
Парциальное давление газа в смеси равно произведению общего давления на его объемную долю в смеси:
p(NO)= pобщ∙φNO=106640∙0,375=39990 Па
p(NO2)= pобщ∙φNO2=106640∙0,625=66650 Па
Задачи на смеси (задание № 33)
1. ЗАДАЧИ НА СМЕСИ (задание № 33)
Выполнила учитель химииМАОУ СОШ №25
Журавлева Л.А.
2. ЗАДАЧИ НА СМЕСИ
Тип IВ реакцию
вступает
один компонент
смеси
Тип II
В реакцию
вступает
несколько компонентов
смеси
(параллельные реакции)
Тип III
Комбинированные задачи
3. Типичные ошибки
• Попытка записать оба вещества в однуреакцию. «Смесь оксидов кальция и бария
растворили в соляной кислоте…»
Уравнение реакции составляется так:
СаО + ВаО + 4HCl = СаCl2 + BaCl2 + 2h3O
Это ошибка, ведь в этой смеси могут быть
любые количества каждого оксида.
 А в
А вприведенном уравнении предполагается, что
их равное количество.
• Предположение, что мольное соотношение веществ соответствует
коэффициентам в уравнениях
реакций.
Например:
Zn + 2HCl = ZnCl2 + h3
2Al + 6HCl = 2AlCl3 + 3h3
Количество цинка принимается за х, а
количество алюминия — за 2х (в
соответствии с коэффициентом в уравнении
реакции). Это тоже неверно. Эти количества
могут быть любыми, и они никак между
собой не связаны.
• Попытки найти «количество вещества
смеси», поделив её массу на сумму
молярных масс компонентов.
Это действие вообще никакого смысла не
имеет. Каждая молярная масса может
относиться только к отдельному веществу
(если это не газовая смесь – молярная масса
смеси!).
6. РЕШЕНИЕ ЗАДАЧ I ТИПА (в реакцию вступает один компонент смеси)
• I. 1. Смесь алюминия и железа обработали избытком соляной кислоты,при этом выделилось 8,96 л газа (н.у.).
Это же количество смеси обработали
избытком раствора гидроксида натрия,
выделилось 6,72 л газа (н.
 у.). Найти
у.). Найтимассовую долю железа в исходной
смеси.
7. РЕШЕНИЕ ЗАДАЧ I ТИПА (в реакцию вступает один компонент смеси)
• I. 2. Смесь карбоната и гидрокарбоната калия массой 320г прокалили допостоянной массы. Масса остатка
после прокаливания составила 293,6г.
Определите массовую долю средней
соли в смеси.
8. РЕШЕНИЕ ЗАДАЧ II ТИПА (параллельные реакции)
• C реагентом (реагентами) взаимодействуют всекомпоненты смеси. Для определения порций
отдельных компонентов используется
алгебраический алгоритм.
Решают задачи такого типа с использованием
двух (х и у) или одной (х) переменной.
В качестве неизвестной величины лучше всего
выбрать количество вещества.
9. Алгоритм 1. Решение через систему уравнений с двумя неизвестными (подходит для любой задачи такого типа)
1. Составить уравнения реакций.2. Количества веществ (ν) в исходной смеси
обозначить через х, у моль и, согласно мольным соотношениям в уравнениях реакций
выразить через х, у моль количества веществ
в образовавшейся смеси.

3. Составить математические уравнения. Для
этого следует выразить массу (или объем) веществ через х, у и молярную массу (молярный объем) по формулам:
m = ν • M;
V = ν•Vm.
4. Составить систему уравнений и решить ее.
5. Далее решать согласно условию задачи.
11. РЕШЕНИЕ ЗАДАЧ II ТИПА (параллельные реакции)
• II. 1. Пластинку из магниево-алюминиевого сплава массой 3,9 г поместилив раствор соляной кислоты. Пластинка
растворилась, и выделилось 4,48 л
газа. Найти массовые доли металлов в
сплаве.
12. РЕШЕНИЕ ЗАДАЧ II ТИПА (параллельные реакции)
• II. 2. К раствору, содержащему 5,48гсмеси сульфата и силиката натрия,
прибавили избыток хлорида бария, в
результате образовалось 9,12г осадка.
Найти массы солей в исходной смеси.
13. Алгоритм 2. Решение через уравнение с одним неизвестным (подходит только для задач, в которых можно найти общее количество
продукта,образующегося во всех
параллельных реакциях)
1.
 Составить уравнения реакций.
Составить уравнения реакций.2. Найти количество образовавшегося
вещества.
3. Обозначить количество вещества, получившегося в результате одной реакции, через х
моль, тогда количество вещества, получившегося в результате второй реакции, будет
равно: (νобщ – х) моль. Выразить, согласно
уравнениям реакций, количества веществ в
исходной смеси.
4. Выразить массы веществ, составить и
решить уравнение с одним неизвестным.
15. ТИП III. КОМБИНИРОВАННЫЕ ЗАДАЧИ
• III. 1. При обработке 17,4 г смесиалюминия, железа и меди избытком
соляной кислоты выделилось 8,96 л
(н.у.). Не растворившийся в соляной
кислоте остаток растворился в
концентрированной азотной кислоте с
выделением 4,48 л газа (н.у.). Определите состав исходной смеси (в %).
16. ЗАДАЧИ НА КИСЛЫЕ СОЛИ
Эти задачи можно решать разными способами.В любом случае вначале нужно составить уравнения всех возможных реакций, найти количества реагирующих веществ и, сравнив их соотношение с числом моль по уравнению, определить,
какие соли получаются.

При более простом варианте (алгоритм 1)
можно не учитывать последовательность протекания реакций, исходить из предположения,
что одновременно происходят две реакции, и
использовать алгебраический способ решения.
17. Алгоритм 1 (Параллельные реакции)
1. Составить уравнения всех возможных реакций.2. Найти количества реагирующих веществ и по
их соотношению определить уравнения двух
реакций, которые происходят одновременно.
3. Обозначить количество вещества одного из
реагирующих веществ в первом уравнении как х
моль, во втором – у моль.
4. Выразить через х и у количества веществ реагентов или получившихся солей согласно молярным соотношениям по уравнениям.
5. Составить и решить систему уравнений с двумя
неизвестными, найти количества реагирующих
веществ, затем количества получившихся солей.
Далее решать задачу согласно условию.
19. ЗАДАЧИ НА КИСЛЫЕ СОЛИ
• Задача 1. Газ, полученный при сжигании 19,2 г серы в избытке кислорода,без остатка прореагировал с 682,5 мл
5%-го раствора гидроксида натрия
(плотность 1,055 г/мл).
 Определите
Определитесостав полученного раствора и рассчитайте массовые доли веществ в этом
растворе.
• При более сложном для понимания, но более
глубоко раскрывающем химизм происходящих
процессов способе решения нужно учитывать то,
что в некоторых случаях продукты реакции зависят от порядка смешивания веществ. Нужно
учитывать последовательность реакций, протекающих при взаимодействии многоосновной
кислоты и щелочи. Так, при постепенном
добавлении гидроксида натрия к раствору
фосфорной кислоты будут протекать реакции:
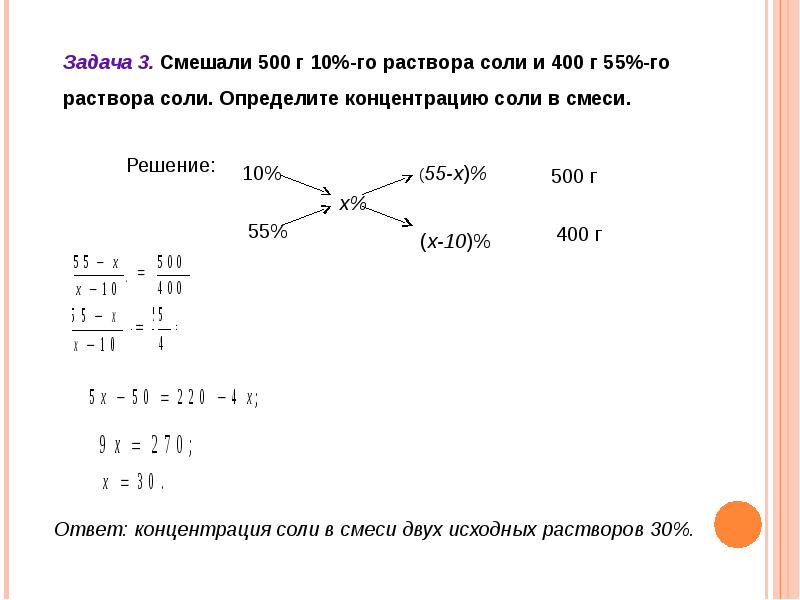
h4PO4 + NaOH = Nah3PO4 + h3O
Nah3PO4 + NaOH = Na2HPO4 + h3O
Na2HPO4 + NaOH = Na3PO4 + h3O
• При обратном же порядке смешивания
реагентов последовательность протекания и
сами реакции будут иными:
3NaOH + h4PO4 = Na3PO4 + 3h3O
2Na3PO4 + h4PO4 = 3Na2HPO4
Na2HPO4 + h4PO4 = 2Nah3PO4
Если образующаяся соль нерастворима, то
вначале образуется осадок – средняя соль, а
затем кислая соль.
22. Алгоритм 2 (Последовательные реакции. Нейтрализация щелочи)
1. Составить уравнение реакции образованиясредней соли.
Количество вещества средней соли и количество
вещества прореагировавшей кислоты или кислотного оксида рассчитывается по количеству
вещества щелочи.
2. Найти количество вещества оставшейся
(непрореагировавшей) кислоты или кислотного
оксида:
νост = νисх – νпрореаг
Составить уравнение реакции избытка кислоты
или оксида со средней солью.
3. По количеству вещества избытка кислоты или
кислотного оксида найти количество вещества
кислой соли и количество прореагировавшей
средней соли.
4. Найти количество вещества оставшейся средней соли.
Алгоритм 3
(Последовательные реакции.
Нейтрализация кислоты.)
1. Составить уравнение реакции образования
кислой соли.
2. Найти количество вещества избытка
щелочи (оставшейся):
νост = νисх – νпрореаг
Составить уравнение реакции избытка
щелочи с кислой солью.

3. По количеству щелочи найти количество
вещества средней соли и количество
прореагировавшей кислой соли.
4. Найти количество вещества оставшейся
кислой соли.
|
Решение:
Отсюда: n = M/µ или М = n * µ = 29,02 кмоль* 36,5 кг/кмоль =1059,23 кг
ri = Ni / Σ Ni = (gi /μi)/Σ gi /μi
Для конечного состава:
|
Идентификация смесей и растворов – Химия для старших классов
Если вы считаете, что контент, доступный через Веб-сайт (как определено в наших Условиях обслуживания), нарушает одно
или больше ваших авторских прав, сообщите нам, отправив письменное уведомление («Уведомление о нарушении»), содержащее
в
информацию, описанную ниже, назначенному ниже агенту. Если репетиторы университета предпримут действия в ответ на
ан
Уведомление о нарушении, оно предпримет добросовестную попытку связаться со стороной, которая предоставила такой контент
средствами самого последнего адреса электронной почты, если таковой имеется, предоставленного такой стороной Varsity Tutors.
Если репетиторы университета предпримут действия в ответ на
ан
Уведомление о нарушении, оно предпримет добросовестную попытку связаться со стороной, которая предоставила такой контент
средствами самого последнего адреса электронной почты, если таковой имеется, предоставленного такой стороной Varsity Tutors.
Ваше Уведомление о нарушении прав может быть отправлено стороне, предоставившей доступ к контенту, или третьим лицам, таким как в виде ChillingEffects.org.
Обратите внимание, что вы будете нести ответственность за ущерб (включая расходы и гонорары адвокатам), если вы существенно искажать информацию о том, что продукт или действие нарушает ваши авторские права. Таким образом, если вы не уверены, что контент находится на Веб-сайте или по ссылке с него нарушает ваши авторские права, вам следует сначала обратиться к юристу.
Чтобы отправить уведомление, выполните следующие действия:
Вы должны включить следующее:
Физическая или электронная подпись правообладателя или лица, уполномоченного действовать от их имени;
Идентификация авторских прав, которые, как утверждается, были нарушены;
Описание характера и точного местонахождения контента, который, по вашему мнению, нарушает ваши авторские права, в \
достаточно подробностей, чтобы позволить репетиторам Varsity найти и точно идентифицировать этот контент; например нам требуется
а
ссылка на конкретный вопрос (а не только на название вопроса), который содержит содержание и описание
к какой конкретной части вопроса – изображению, ссылке, тексту и т. д. – относится ваша жалоба;
Ваше имя, адрес, номер телефона и адрес электронной почты; и
Ваше заявление: (а) вы добросовестно считаете, что использование контента, который, по вашему утверждению, нарушает
ваши авторские права не разрешены законом, владельцем авторских прав или его агентом; (б) что все
информация, содержащаяся в вашем Уведомлении о нарушении, является точной, и (c) под страхом наказания за лжесвидетельство вы
либо владелец авторских прав, либо лицо, уполномоченное действовать от их имени.
д. – относится ваша жалоба;
Ваше имя, адрес, номер телефона и адрес электронной почты; и
Ваше заявление: (а) вы добросовестно считаете, что использование контента, который, по вашему утверждению, нарушает
ваши авторские права не разрешены законом, владельцем авторских прав или его агентом; (б) что все
информация, содержащаяся в вашем Уведомлении о нарушении, является точной, и (c) под страхом наказания за лжесвидетельство вы
либо владелец авторских прав, либо лицо, уполномоченное действовать от их имени.
Отправьте жалобу нашему уполномоченному агенту по адресу:
Чарльз Кон
Varsity Tutors LLC
101 S. Hanley Rd, Suite 300
St. Louis, MO 63105
Или заполните форму ниже:
Глава 9 – Раздел 6: Проблемы со смесью
% PDF-1.3
%
327 0 объект
> / Metadata 324 0 R / OCProperties> / OCGs [368 0 R] >> / OpenAction [329 0 R / XYZ null null null] / Outlines 7 0 R / PageLabels 322 0 R / PageMode / UseNone / Pages 325 0 R / PieceInfo >>> / StructTreeRoot 328 0 R / Тип / Каталог >>
эндобдж
367 0 объект
> / Шрифт >>> / Поля 372 0 R >>
эндобдж
324 0 объект
> поток
Акробат Дистиллятор 5. 0 (Windows) 2001-10-24T16: 09: 57Z2013-04-18T09: 55: 40-05: 002013-04-18T09: 55: 40-05: 00 Acrobat PDFMaker 5.0 для Wordapplication / pdf
0 (Windows) 2001-10-24T16: 09: 57Z2013-04-18T09: 55: 40-05: 002013-04-18T09: 55: 40-05: 00 Acrobat PDFMaker 5.0 для Wordapplication / pdf
«Смесь»
Проблемы со словами: Примеры (стр. Обычно эти упражнения довольно легко решить, как только вы найдете уравнения.Чтобы помочь вам посмотрите, как настроить эти проблемы, ниже приведены еще несколько проблем с их сетки (но не решения).
От
в последнем столбце вы получите уравнение 0.
Из последнего столбца вы
получить уравнение 7.5
= 0,1 (50 + x ).
Решите относительно x . (Примечание процент для воды. «Чистая вода» не содержит соли, поэтому процент соли равен нулю. Если, с другой стороны, вы пытались увеличьте содержание соли, добавив чистую соль, процент будет было сто.)
От
в последней строке вы видите, что у вас есть 20 фунтов за 139,60 доллара,
или 139,60 $ / (20 фунтов).
От
в последнем столбце вы получите уравнение $ 0.
От
последний столбец, вы
получите уравнение 70 + 300 x = 100.
Из последней строки вы
посмотрите, что на 50 граммов в чаше 22 грамма сахара, или 22 / 50 . << Предыдущий Наверх | 1 | 2 | Вернуться к индексу
| Этот урок можно распечатать для личного пользования. |
Задачи о смесях (системы уравнений с двумя переменными)
Задачи о смесях (системы уравнений с двумя переменными) Проблемы со смесью Сколько унций 20% раствора соляной кислоты и
70% раствор соляной кислоты необходимо смешать, чтобы получить 20 унций 50% раствора. раствор соляной кислоты?
раствор соляной кислоты?
Что мы пытаемся найти в этой проблеме? Мы хотим знать необходимое количество 20% раствора кислоты, и мы хотим знать необходимое количество 70% раствора кислоты.Нам понадобится переменная для представляют каждое из этих неизвестных:
x = необходимо 20% раствораг = необходимо унции 70% раствора
Поскольку у нас есть два неизвестных, нам придется написать систему двух переменных для поиска неизвестных.
Чтобы помочь нам организовать информацию в задаче, давайте
представьте, что мы находимся в лаборатории и смотрим на две бутылки с кислотой, которые мы
собирается смешаться вместе. На одной из бутылок написано «20%», и на ней
в нем x унций жидкости.Другая бутылка помечена надписью «70%», и
в нем y унций жидкости. Вот как выглядят две бутылки
как; количество кислоты в каждой бутылке указано под бутылками:
Если мы объединим две бутылки с кислотой, мы получим 20
унций 50% раствора кислоты. Объединение (сложение) двух
бутылки с кислотой можно показать, добавив к нашему рисунку:
| х унций | + | y унций | = | 20 унций |
Первое из наших уравнений будет происходить от суммы жидкость в бутылках – добавление жидкости в две бутылки приведет к дайте нам 20 унций раствора:
х + у = 20Второе из наших двух уравнений будет происходить от суммы чистой кислоты в каждой бутылке.
В первой бутылке 20% x унций жидкости чистая кислота, поэтому количество чистой кислоты в первой бутылке составляет 0,20x.
Во второй бутылке 70% годовых жидкость представляет собой чистую кислоту, поэтому количество чистой кислоты во второй бутылке равно .70г.
В комбинированной смеси 50% от 20 унций жидкости – это чистая кислота, поэтому количество чистой кислоты в комбинированной смеси составляет 0,50 (20).
| чистая кислота в первой бутылке | + | чистая кислота во втором баллоне | = | кислота чистая в смеси |
Так .20x + 0,70y = 0,50 (20)или
.20x + .70y = 10
Умножьте обе части этого уравнения на 10, чтобы очистить десятичные дроби:2x + 7y = 100
Это второе уравнение, которое мы будем использовать.
Теперь решите систему уравнений.
2х + 7у = 100х + у = 20
Умножьте второе уравнение на -2, затем сложите два уравнения. вместе:
вместе:
-2x – 2y = -40
5лет = 60
у = 12
Нам понадобится 12 унций 70% раствора кислоты.
Чтобы найти необходимое количество 20% раствора кислоты, замените 12 для y в любом уравнении; мы воспользуемся более простым уравнением:
х + у = 20х + 12 = 20
х = 8
Итак, потребуется 8 унций 20% раствора кислоты.
6.1: Растворы и концентрация растворов
Навыки для развития
- Опишите основные свойства решений
- Рассчитать концентрацию раствора с использованием молярности и массовых процентов
- Выполните расчеты разбавления, используя уравнение разбавления
В предыдущих разделах мы сосредоточились на составе веществ: образцы вещества, содержащие только один тип элемента или соединения.Однако смеси – образцы вещества, содержащие два или более вещества, соединенных физически, – встречаются в природе чаще, чем чистые вещества. Как и в случае с чистым веществом, относительный состав смеси играет важную роль в определении ее свойств. Относительное количество кислорода в атмосфере планеты определяет ее способность поддерживать аэробную жизнь. Относительные количества железа, углерода, никеля и других элементов в стали (смеси, известной как «сплав») определяют ее физическую прочность и устойчивость к коррозии.Относительное количество активного ингредиента в лекарстве определяет его эффективность в достижении желаемого фармакологического эффекта. Относительное количество сахара в напитке определяет его сладость (Рисунок \ (\ PageIndex {1} \)). В этом разделе мы опишем один из наиболее распространенных способов количественной оценки относительного состава смесей.
Как и в случае с чистым веществом, относительный состав смеси играет важную роль в определении ее свойств. Относительное количество кислорода в атмосфере планеты определяет ее способность поддерживать аэробную жизнь. Относительные количества железа, углерода, никеля и других элементов в стали (смеси, известной как «сплав») определяют ее физическую прочность и устойчивость к коррозии.Относительное количество активного ингредиента в лекарстве определяет его эффективность в достижении желаемого фармакологического эффекта. Относительное количество сахара в напитке определяет его сладость (Рисунок \ (\ PageIndex {1} \)). В этом разделе мы опишем один из наиболее распространенных способов количественной оценки относительного состава смесей.
Рисунок \ (\ PageIndex {1} \): Сахар – один из многих компонентов сложной смеси, известной как кофе.Количество сахара в данном количестве кофе является важным фактором, определяющим сладость напитка. (кредит: Джейн Уитни)
Решения
Видео \ (\ PageIndex {1} \): Введение в решения ускоренного курса химии.
Ранее мы определили растворы как гомогенные смеси, что означает, что состав смеси (и, следовательно, ее свойства) одинаковы во всем ее объеме. Решения часто встречаются в природе, а также были реализованы во многих формах искусственных технологий.Мы рассмотрим более подробное рассмотрение свойств растворов в главе, посвященной растворам и коллоидам, но здесь мы познакомим вас с некоторыми из основных свойств растворов.
Относительное количество данного компонента раствора называется его концентрацией. Часто, хотя и не всегда, раствор содержит один компонент с концентрацией, значительно превышающей концентрацию всех других компонентов. Этот компонент называется растворителем и может рассматриваться как среда, в которой другие компоненты диспергированы или растворены.Растворы, в которых растворителем является вода, конечно, очень распространены на нашей планете. Раствор, в котором вода является растворителем, называется водным раствором.
Растворенное вещество – это компонент раствора, который обычно присутствует в гораздо более низкой концентрации, чем растворитель. Концентрации растворенных веществ часто описываются качественными терминами, такими как разбавленный (относительно низкой концентрации) и концентрированный (относительно высокой концентрации).
Концентрации растворенных веществ часто описываются качественными терминами, такими как разбавленный (относительно низкой концентрации) и концентрированный (относительно высокой концентрации).
Видео \ (\ PageIndex {2} \): Введение в молярность из ускоренного курса химии.
Концентрации растворов
Концентрации могут быть количественно оценены с использованием большого количества единиц измерения, каждая из которых удобна для конкретного применения. Некоторые из общих измерений концентраций, наблюдаемых в научных лабораториях, включают в себя доли на миллион (ppm), доли на миллиард (ppb), массово-массовый процент (m / m%), молярность (M), моляльность ( м) и мольных процентов. В этой единице мы будем использовать две наиболее распространенные единицы измерения: молярность и массово-массовый процент.
Молярность
Молярность ( M ) – полезная единица измерения концентрации для многих приложений в химии. Молярность определяется как количество молей растворенного вещества ровно в 1 литре (1 л) раствора:
Молярность определяется как количество молей растворенного вещества ровно в 1 литре (1 л) раствора:
\ [M = \ mathrm {\ dfrac {mol \: solute} {L \: solution}} \ label {3.4.2} \]
Таким образом, единицами молярности являются моль на литр раствора (моль / л), сокращенно \ (М \). Водный раствор, содержащий 1 моль (342 г) сахарозы в достаточном количестве воды, чтобы получить конечный объем 1.00 л имеет концентрацию сахарозы 1,00 моль / л или 1,00 М. В химической записи квадратные скобки вокруг названия или формулы растворенного вещества представляют молярную концентрацию растворенного вещества. Следовательно,
\ [[\ rm {сахароза}] = 1,00 \: M \]
читается как «концентрация сахарозы 1,00 молярная».
Пример \ (\ PageIndex {1} \): расчет молярных концентраций
Образец безалкогольного напитка объемом 355 мл содержит 0,133 моль сахарозы (столовый сахар). Какая молярная концентрация сахарозы в напитке?
Решение
Поскольку даны молярное количество растворенного вещества и объем раствора, молярность можно рассчитать, используя определение молярности. Согласно этому определению, объем раствора должен быть преобразован из мл в л:
Согласно этому определению, объем раствора должен быть преобразован из мл в л:
\ [\ begin {align *} M & = \ dfrac {mol \: solute} {L \: solution} \\ [5pt] & = \ dfrac {0.133 \: mol} {355 \: mL \ times \ dfrac {1 \: L} {1000 \: mL}} \\ [5pt] & = 0.375 \: M \ label {3.4.1} \ end {align *} \]
Упражнение \ (\ PageIndex {1} \)
Чайная ложка столового сахара содержит около 0,01 моль сахарозы. Какова молярность сахарозы, если чайная ложка сахара была растворена в чашке чая объемом 200 мл?
- Ответ
0.05 M
Пример \ (\ PageIndex {2} \): получение молей и объемов из молярных концентраций
Сколько сахара (моль) содержится в небольшом глотке (~ 10 мл) безалкогольного напитка из примера \ (\ PageIndex {1} \)?
Решение
В этом случае мы можем изменить определение молярности, чтобы выделить искомое количество в молях сахара. Затем подставляем значение молярности, полученное в примере 3. 4.2, 0,375 M :
4.2, 0,375 M :
\ [M = \ mathrm {\ dfrac {mol \: solute} {L \: solution}} \ label {3.4.3} \ nonumber \]
\ [\ begin {align *} \ mathrm {mol \: solute} & = \ mathrm {M \ times L \: solution} \ label {3.4.4} \\ [5pt] \ mathrm {mol \: solute} & = \ mathrm {0.375 \: \ dfrac {mol \: sugar} {L} \ times \ left (10 \: mL \ times \ dfrac {1 \: L} {1000 \: mL} \ right)} & = \ mathrm {0.004 \: mol \: sugar} \ label {3.4.5} \ end {align *} \]
Упражнение \ (\ PageIndex {2} \)
Какой объем (мл) подслащенного чая, описанного в примере \ (\ PageIndex {1} \), содержит такое же количество (моль) сахара (моль), что и 10 мл безалкогольного напитка в этом примере?
- Ответ
80 мл
Пример \ (\ PageIndex {3} \): расчет молярных концентраций по массе растворенного вещества
Дистиллированный белый уксус (Рисунок \ (\ PageIndex {2} \)) – это раствор уксусной кислоты \ (CH_3CO_2H \) в воде. Раствор 0,500 л уксуса содержит 25,2 г уксусной кислоты. Какова концентрация раствора уксусной кислоты в единицах молярности?
Раствор 0,500 л уксуса содержит 25,2 г уксусной кислоты. Какова концентрация раствора уксусной кислоты в единицах молярности?
Рисунок \ (\ PageIndex {3} \): Дистиллированный белый уксус – это раствор уксусной кислоты в воде.
Решение
Как и в предыдущих примерах, определение молярности является основным уравнением, используемым для расчета искомого количества. В этом случае указывается масса растворенного вещества вместо его молярного количества, поэтому мы должны использовать молярную массу растворенного вещества, чтобы получить количество растворенного вещества в молях:
\ [\ mathrm {\ mathit M = \ dfrac {mol \: solute} {L \: solution} = \ dfrac {25.2 \: g \: \ ce {Ch4CO2H} \ times \ dfrac {1 \: mol \: \ ce {Ch4CO2H}} {60.052 \: g \: \ ce {Ch4CO2H}}} {0.500 \: L \: раствор } = 0.839 \: \ mathit M} \ label {3.4.6} \]
\ [\ mathrm {\ mathit M = \ dfrac {mol \: solute} {L \: solution} = 0. 839 \: \ mathit M} \ label {3.4.7} \]
839 \: \ mathit M} \ label {3.4.7} \]
\ [M = \ mathrm {\ dfrac {0.839 \: mol \: solute} {1.00 \: L \: solution}} \ label {3.4.8} \]
Упражнение \ (\ PageIndex {3} \)
Рассчитайте молярность 6,52 г \ (CoCl_2) (128,9 г / моль), растворенного в водном растворе общим объемом 75.0 мл.
- Ответ
0,674 M
Пример \ (\ PageIndex {4} \): определение массы растворенного вещества в заданном объеме раствора
Сколько граммов NaCl содержится в 0,250 л раствора 5,30- M ?
Решение
Объем и молярность раствора указаны, поэтому количество (моль) растворенного вещества легко вычислить, как показано в примере \ (\ PageIndex {3} \):
\ [M = \ mathrm {\ dfrac {mol \: solute} {L \: solution}} \ label {3.4.9} \]
\ [\ mathrm {mol \: solute = \ mathit M \ times L \: solution} \ label {3.4.10} \]
\ [\ mathrm {mol \: solute = 5. 30 \: \ dfrac {mol \: NaCl} {L} \ times 0.250 \: L = 1.325 \: mol \: NaCl} \ label {3.4.11} \]
30 \: \ dfrac {mol \: NaCl} {L} \ times 0.250 \: L = 1.325 \: mol \: NaCl} \ label {3.4.11} \]
Наконец, это молярное количество используется для определения массы NaCl:
\ [\ mathrm {1.325 \: mol \: NaCl \ times \ dfrac {58.44 \: g \: NaCl} {mol \: NaCl} = 77.4 \: g \: NaCl} \ label {3.4.12} \]
Упражнение \ (\ PageIndex {4} \)
Сколько граммов \ (CaCl_2 \) (110,98 г / моль) содержится в 250.0 мл 0,200-М раствора хлорида кальция?
- Ответ
5,55 г \ (CaCl_2 \)
При пошаговом выполнении вычислений, как в примере \ (\ PageIndex {3} \), важно воздерживаться от округления любых промежуточных результатов вычислений, которые могут привести к ошибкам округления в конечном результате. В примере \ (\ PageIndex {4} \) молярное количество NaCl, вычисленное на первом этапе, 1,325 моль, будет правильно округлено до 1.32 моль, если нужно сообщить; однако, хотя последняя цифра (5) не имеет значения, ее необходимо сохранить как защитную цифру в промежуточных вычислениях. Если бы мы не сохранили эту защитную цифру, окончательный расчет массы NaCl составил бы 77,1 г, то есть разница в 0,3 г.
Если бы мы не сохранили эту защитную цифру, окончательный расчет массы NaCl составил бы 77,1 г, то есть разница в 0,3 г.
Помимо сохранения защитной цифры для промежуточных вычислений, мы также можем избежать ошибок округления, выполняя вычисления за один шаг (Пример \ (\ PageIndex {5} \)). Это исключает промежуточные этапы, поэтому округляется только конечный результат.
Пример \ (\ PageIndex {5} \): определение объема раствора
В примере \ (\ PageIndex {3} \) мы обнаружили, что типичная концентрация уксуса составляет 0,839 M . В каком объеме уксуса содержится 75,6 г уксусной кислоты?
Решение
Сначала используйте молярную массу, чтобы вычислить количество молей уксусной кислоты из заданной массы:
\ [\ mathrm {g \: solute \ times \ dfrac {mol \: solute} {g \: solute} = mol \: solute} \ label {3.4.13} \]
Затем используйте молярность раствора для расчета объема раствора, содержащего это молярное количество растворенного вещества:
\ [\ mathrm {mol \: solute \ times \ dfrac {L \: solution} {mol \: solute} = L \: solution} \ label {3. 4.14} \]
4.14} \]
Объединение этих двух этапов в одно дает:
\ [\ mathrm {g \: solute \ times \ dfrac {mol \: solute} {g \: solute} \ times \ dfrac {L \: solution} {mol \: solute} = L \: solution} \ label {3.4.15} \]
\ [\ mathrm {75.6 \: g \: \ ce {Ch4CO2H} \ left (\ dfrac {mol \: \ ce {Ch4CO2H}} {60.05 \: g} \ right) \ left (\ dfrac {L \: solution} {0.839 \: mol \: \ ce {Ch4CO2H}} \ right) = 1.50 \: L \: solution} \ label {3.4.16 } \]
Упражнение \ (\ PageIndex {5} \):
Какой объем 1,50-М раствора KBr содержит 66,0 г KBr?
- Ответ
0,370 л
Массово-массовый процент
Проценты также обычно используются для выражения состава смесей, включая растворы. Массовый процент (м / м%) компонента раствора определяется как отношение массы компонента к массе раствора, выраженное в процентах:
\ [\ mathrm {\% \: m / m = \ dfrac {масса \: of \: solute} {масса \: of \: solution} \ times100 \%} \]
масса раствора = масса растворенного вещества + масса растворителя
Если вы можете измерить массы растворенного вещества и раствора, определение массы / массовых процентов будет несложным. Каждая масса должна быть выражена в одних и тех же единицах, чтобы определить правильную концентрацию.
Каждая масса должна быть выражена в одних и тех же единицах, чтобы определить правильную концентрацию.
Предположим, что раствор был приготовлен растворением \ (25.0 \: \ text {g} \) сахара в \ (100.0 \: \ text {g} \) воды.
Масса раствора
масса раствора = 25,0 г сахара + 100,0 г воды = 125,0 г
Массовый процент рассчитывается по формуле:
\ [\ text {Массовый процент} = \ frac {25.0 \: \ text {g сахара}} {125.0 \: \ text {g solution}} \ times 100 \% = 20.0 \% \: \ text {сахар} \]
Массовый процент также упоминается схожими названиями, такими как массовых процентов, массовых процентов, массовых процентов и других вариаций на эту тему. Наиболее распространенный символ массового процента – это просто знак процента,%, хотя часто используются более подробные символы, включая% массы,% веса и (вес / вес)%. Использование этих более подробных символов может предотвратить смешение массовых процентов с другими типами процентов, такими как объемные проценты (которые будут обсуждаться позже в этом разделе).
Массовые проценты – популярные единицы концентрации для потребительских товаров. На этикетке типичного флакона с жидким отбеливателем (, рис. 3.17, ) указано, что концентрация его активного ингредиента, гипохлорита натрия (NaOCl), составляет 7,4%. Таким образом, образец отбеливателя весом 100,0 г будет содержать 7,4 г NaOCl.
Рисунок \ (\ PageIndex {4} \): Дистиллированный белый уксус – это раствор уксусной кислоты в воде.
{6} \): Определение объема раствора
А 5.Образец спинномозговой жидкости 0 г содержит 3,75 мг (0,00375 г) глюкозы. Каков процент глюкозы в спинномозговой жидкости по массе?
Решение
Образец спинномозговой жидкости содержит примерно 4 мг глюкозы в 5000 мг жидкости, поэтому массовая доля глюкозы должна быть немного меньше одной части из 1000, или примерно 0,1%. Подставляя данные массы в уравнение, определяющее массовые проценты, получаем:
\ [\ mathrm {\% \, глюкоза = \ dfrac {3,75 \; мг \; глюкоза \ раз \ frac {1 \; g} {1000 \; мг}} {5. 0 \; г \; спинной \; жидкость} = 0,075 \%} \]
0 \; г \; спинной \; жидкость} = 0,075 \%} \]
Рассчитанный массовый процент согласуется с нашей приблизительной оценкой (немного меньше 0,1%).
Обратите внимание, что хотя любая единица массы может использоваться для вычисления массового процента (мг, г, кг, унция и т. Д.), Одна и та же единица должна использоваться как для растворенного вещества, так и для раствора, чтобы единицы массы исключались, давая безразмерное соотношение. В этом случае мы преобразовали единицы растворенного вещества в числителе из мг в г, чтобы они соответствовали единицам в знаменателе. С таким же успехом мы могли бы вместо этого преобразовать знаменатель с г в мг.Если для растворенного вещества и раствора используются одинаковые единицы массы, вычисленный массовый процент будет правильным.
Упражнение \ (\ PageIndex {6} \):
Флакон средства для чистки плитки содержит 135 г HCl и 775 г воды. Какой процент по массе HCl в этом очищающем средстве?
- Ответ
14,8%
Пример \ (\ PageIndex {7} \): вычисления с использованием массового процента
«Концентрированная» соляная кислота – водный раствор 37. 2% HCl, который обычно используется в качестве лабораторного реактива. Плотность этого раствора 1,19 г / мл. Какая масса HCl содержится в 0,500 л этого раствора?
2% HCl, который обычно используется в качестве лабораторного реактива. Плотность этого раствора 1,19 г / мл. Какая масса HCl содержится в 0,500 л этого раствора?
Решение
Концентрация HCl составляет около 40%, поэтому порция этого раствора в 100 г будет содержать около 40 г HCl. Поскольку плотность раствора не сильно отличается от плотности воды (1 г / мл), разумная оценка массы HCl в 500 г (0,5 л) раствора примерно в пять раз больше, чем в 100 г порции, или \ (\ mathrm {5 \ times 40 = 200 \: g} \).Чтобы получить массу растворенного вещества в растворе из его массового процента, нам нужно знать соответствующую массу раствора. Используя заданную плотность раствора, мы можем преобразовать объем раствора в массу, а затем использовать данный массовый процент для расчета массы растворенного вещества. Этот математический подход представлен на этой блок-схеме:
Для правильной отмены единицы объем 0,500 л преобразуется в 500 мл, а массовый процент выражается как отношение, 37,2 г HCl / г раствора:
\ [\ mathrm {500 \; мл \; решение \ left (\ dfrac {1. 19 \; g \; solution} {mL \; solution} \ right) \ left (\ dfrac {37.2 \; g \; HCl} {100 \; g \; solution} \ right) = 221 \; g \; HCl} \]
19 \; g \; solution} {mL \; solution} \ right) \ left (\ dfrac {37.2 \; g \; HCl} {100 \; g \; solution} \ right) = 221 \; g \; HCl} \]
Эта масса HCl соответствует нашей приблизительной оценке примерно в 200 г.
Упражнение \ (\ PageIndex {7} \)
В каком объеме концентрированного раствора HCl содержится 125 г HCl?
- Ответ
282 мл
Разведение растворов
Видео \ (\ PageIndex {3} \): Введение в разведения из ускоренного курса химии.
Разбавление – это процесс уменьшения концентрации раствора за счет добавления растворителя. Например, мы можем сказать, что стакан холодного чая становится все более разбавленным по мере таяния льда. Вода из тающего льда увеличивает объем растворителя (воды) и общий объем раствора (холодный чай), тем самым уменьшая относительные концентрации растворенных веществ, которые придают напитку его вкус (Рисунок \ (\ PageIndex {2}) \)).
Рисунок \ (\ PageIndex {5} \): Оба раствора содержат одинаковую массу нитрата меди.Раствор справа более разбавлен, потому что нитрат меди растворен в большем количестве растворителя. (кредит: Марк Отт).
Разбавление также является обычным способом приготовления растворов желаемой концентрации. Добавляя растворитель к отмеренной порции более концентрированного маточного раствора , мы можем достичь определенной концентрации. Например, коммерческие пестициды обычно продаются в виде растворов, в которых активные ингредиенты гораздо более концентрированы, чем это необходимо для их применения.Прежде чем их можно будет использовать на сельскохозяйственных культурах, пестициды необходимо разбавить. Это также очень распространенная практика для приготовления ряда обычных лабораторных реагентов (Рисунок \ (\ PageIndex {3} \)).
Рисунок \ (\ PageIndex {6} \) : Раствор \ (KMnO_4 \) готовят путем смешивания воды с 4,74 г KMnO4 в колбе. (кредит: модификация работы Марка Отта)
(кредит: модификация работы Марка Отта)
Простое математическое соотношение может использоваться для соотнесения объемов и концентраций раствора до и после процесса разбавления.Согласно определению молярности, молярное количество растворенного вещества в растворе равно произведению молярности раствора на его объем в литрах:
\ [n = ML \]
Подобные выражения могут быть записаны для раствора до и после его разбавления:
\ [n_1 = M_1L_1 \]
\ [n_2 = M_2L_2 \]
, где нижние индексы «1» и «2» относятся к раствору до и после разбавления соответственно. Поскольку процесс разбавления не изменяет количество растворенного вещества в растворе, n 1 = n 2 .Таким образом, эти два уравнения могут быть приравнены друг к другу:
\ [M_1L_1 = M_2L_2 \]
Это соотношение обычно называют уравнением разбавления. Хотя мы вывели это уравнение, используя молярность в качестве единицы концентрации и литров в качестве единицы объема, можно использовать другие единицы концентрации и объема, при условии, что эти единицы должным образом сокращаются в соответствии с методом метки фактора. Отражая эту универсальность, уравнение разбавления часто записывается в более общей форме:
Отражая эту универсальность, уравнение разбавления часто записывается в более общей форме:
где \ (C \) и \ (V \) – концентрация и объем соответственно.
Пример \ (\ PageIndex {8} \): определение концентрации разбавленного раствора
Если 0,850 л 5,00- M раствора нитрата меди, Cu (NO 3 ) 2 , разбавить до объема 1,80 л путем добавления воды, какова молярность разбавленного раствора?
Решение
Нам даны объем и концентрация основного раствора, V 1 и C 1 , и объем полученного разбавленного раствора V 2 .Нам нужно найти концентрацию разбавленного раствора, C 2 . Таким образом, мы изменяем уравнение разбавления, чтобы выделить C 2 :
\ [C_1V_1 = C_2V_2 \]
\ [C_2 = \ dfrac {C_1V_1} {V_2} \]
Поскольку основной раствор разбавляется более чем в два раза (объем увеличивается с 0,85 л до 1,80 л), можно ожидать, что концентрация разбавленного раствора будет меньше половины 5 M . Мы сравним эту приблизительную оценку с расчетным результатом, чтобы проверить наличие грубых ошибок в вычислениях (например, таких как неправильная замена заданных величин).Подставляя указанные значения в члены в правой части этого уравнения, получаем:
Мы сравним эту приблизительную оценку с расчетным результатом, чтобы проверить наличие грубых ошибок в вычислениях (например, таких как неправильная замена заданных величин).Подставляя указанные значения в члены в правой части этого уравнения, получаем:
\ [C_2 = \ mathrm {\ dfrac {0.850 \: L \ times 5.00 \: \ dfrac {mol} {L}} {1.80 \: L}} = 2.36 \: M \]
Этот результат хорошо согласуется с нашей приблизительной оценкой (это чуть меньше половины концентрации запасов, 5 M ).
Упражнение \ (\ PageIndex {8} \)
Какова концентрация раствора, полученная при разбавлении 25,0 мл 2,04-М раствора Ch4OH до 500,0 мл?
- Ответ
0.102 M \ (CH_3OH \)
Пример \ (\ PageIndex {9} \): объем разбавленного раствора
Какой объем 0,12 M HBr можно получить из 11 мл (0,011 л) 0,45 M HBr?
Решение
Нам даны объем и концентрация основного раствора, V 1 и C 1 , и концентрация полученного разбавленного раствора C 2 . Нам нужно найти объем разбавленного раствора, V 2 . Таким образом, мы изменяем уравнение разбавления, чтобы выделить V 2 :
Нам нужно найти объем разбавленного раствора, V 2 . Таким образом, мы изменяем уравнение разбавления, чтобы выделить V 2 :
\ [C_1V_1 = C_2V_2 \]
\ [V_2 = \ dfrac {C_1V_1} {C_2} \]
Поскольку концентрация разбавленного раствора (0,12 M ) составляет чуть более одной четвертой исходной концентрации (0,45 M ), мы ожидаем, что объем разбавленного раствора будет примерно в четыре раза больше исходного объема, или около 44 мл. .Подставляя заданные значения и решая неизвестный объем, получаем:
\ [V_2 = \ dfrac {(0,45 \: M) (0,011 \: \ ce L)} {(0,12 \: M)} \]
\ [V_2 = \ mathrm {0,041 \: L} \]
Объем раствора 0,12- M составляет 0,041 л (41 мл). Результат разумный и хорошо согласуется с нашей приблизительной оценкой.
Упражнение \ (\ PageIndex {9} \)
Лабораторный эксперимент требует 0,125 M \ (HNO_3 \). Какой объем 0,125 М \ (HNO_3 \) можно приготовить из 0. 250 л 1.88 М \ (HNO_3 \)?
250 л 1.88 М \ (HNO_3 \)?
- Ответ
3,76 л
Пример \ (\ PageIndex {10} \): объем концентрированного раствора, необходимый для разведения
Какой объем 1,59 M KOH требуется для приготовления 5,00 л 0,100 M KOH?
Решение
Нам дана концентрация исходного раствора C 1 , а также объем и концентрация полученного разбавленного раствора V 2 и C 2 .Нам нужно найти объем основного раствора, V 1 . Таким образом, мы изменяем уравнение разбавления, чтобы выделить V 1 :
\ [C_1V_1 = C_2V_2 \]
\ [V_1 = \ dfrac {C_2V_2} {C_1} \]
Поскольку концентрация разбавленного раствора 0,100 M составляет примерно одну шестнадцатую от концентрации исходного раствора (1,59 M ), мы ожидаем, что объем исходного раствора будет примерно в одну шестнадцатую от объема разбавленного раствора, или около 0. 3 литра. Подставляя заданные значения и решая неизвестный объем, получаем:
3 литра. Подставляя заданные значения и решая неизвестный объем, получаем:
\ [V_1 = \ dfrac {(0,100 \: M) (5,00 \: \ ce L)} {1,59 \: M} \]
\ [V_1 = 0,314 \: \ ce L \]
Таким образом, нам потребуется 0,314 л раствора 1,59- M для приготовления желаемого раствора. Этот результат согласуется с нашей приблизительной оценкой.
Упражнение \ (\ PageIndex {10} \)
Какой объем 0,575-М раствора глюкозы, C 6 H 12 O 6 , можно приготовить из 50.00 мл 3,00-М раствора глюкозы?
- Ответ
0,261 л
Резюме
Растворы представляют собой однородные смеси. Многие растворы содержат один компонент, называемый растворителем, в котором растворены другие компоненты, называемые растворенными веществами. Водный раствор – это раствор, в котором растворителем является вода. Концентрация раствора – это мера относительного количества растворенного вещества в данном количестве раствора. Концентрации могут быть измерены с использованием различных единиц, одна очень полезная единица – молярность, определяемая как количество молей растворенного вещества на литр раствора.Концентрация растворенного вещества в растворе может быть уменьшена путем добавления растворителя, этот процесс называется разбавлением. Уравнение разбавления представляет собой простую связь между концентрациями и объемами раствора до и после разбавления.
Концентрации могут быть измерены с использованием различных единиц, одна очень полезная единица – молярность, определяемая как количество молей растворенного вещества на литр раствора.Концентрация растворенного вещества в растворе может быть уменьшена путем добавления растворителя, этот процесс называется разбавлением. Уравнение разбавления представляет собой простую связь между концентрациями и объемами раствора до и после разбавления.
Видео \ (\ PageIndex {4} \): Обзор расчета молярности.
Видео \ (\ PageIndex {5} \): Обзор расчета разведений. Кроме того, в Англии пьют апельсиновый кабачок.
Ключевые уравнения
- \ (M = \ mathrm {\ dfrac {mol \: solute} {L \: solution}} \)
- C 1 V 1 = C 2 V 2
Глоссарий
- водный раствор
- Раствор, растворителем которого является вода
- концентрированный
- качественный термин для раствора, содержащего растворенное вещество в относительно высокой концентрации
- концентрация
- количественная мера относительных количеств растворенного вещества и растворителя, присутствующих в растворе
- разбавленный
- качественный термин для раствора, содержащего растворенное вещество в относительно низкой концентрации
- разведение
- Процесс добавления растворителя в раствор с целью снижения концентрации растворенных веществ
- растворено
- описывает процесс диспергирования растворенных компонентов в растворителе.

- молярность ( M )
- единица концентрации, определяемая как количество молей растворенного вещества, растворенных в 1 литре раствора
- растворенное вещество
- компонент раствора присутствует в концентрации меньше, чем у растворителя
- растворитель
- компонент раствора присутствует в концентрации, которая выше по сравнению с другими компонентами
растворов, представляющих собой смеси кислот и оснований, проблема A
4.Рассчитайте pH раствора, приготовленного смешиванием 45 мл 0,224 М 3-хлорбензойной кислоты с 30 мл 0,187 М этиламина.
Хлорбензойная кислота (Hcba) является слабой кислотой со значением pK и , равным 3,824. Этиламина нет в таблице, а его сопряженная кислота – этиламмоний (pK a = 10,63). Следовательно, этиламин (EA) является слабым основанием (pK b = 3,37). Этот раствор состоит из смеси слабой кислоты и слабого основания.
Этот раствор состоит из смеси слабой кислоты и слабого основания.
Что происходит, когда мы смешиваем кислоту с основанием? Из предшествующего материала мы должны знать, что кислота и основание взаимодействуют друг с другом в так называемой реакции нейтрализации .Реакция нейтрализации между хлорбензойной кислотой и этиламином показана ниже.
\ [\ ce {Hcba + EA \ leftrightarrow cba- + EAH +} \ hspace {60px} \ mathrm {K_n} \]
Мы можем рассчитать начальные количества Hcba и EA, которые существуют в растворе, но некоторые из них будут реагировать в соответствии с реакцией нейтрализации. Что нам нужно знать, так это степень реакции нейтрализации, другими словами, значение K для этой реакции. Таблиц со значениями K n не существует, поэтому нам нужно посмотреть, есть ли способ придумать выражение K n , сложив серии реакций, для которых у нас есть значения K.
У нас есть реакции на Hcba и EA, которые мы можем найти в таблице. Это следующие:
Это следующие:
\ [\ begin {align}
& \ ce {Hcba + h3O \ leftrightarrow cba- + h4O +} \ hspace {60px} && \ mathrm {K_a \: of \: Hcba} \\
& \ ce {EA + H_2O \ leftrightarrow EAH + + OH-} \ hspace {60px} && \ mathrm {K_b \: of \: EA}
\ end {align} \]
Сложение этих двух вместе дает следующую реакцию:
\ [\ ce {Hcba + EA + 2h3O \ leftrightarrow cba- + EAH + + h4O + + OH-} \ hspace {40px} \ mathrm {K = K_a (кислота) \ times K_b (основание)} \]
Это почти похоже на K n , но это не совсем то же самое.На стороне реагента есть две молекулы воды, а на стороне продукта – ион гидроксония и гидроксид-ион. Обратите внимание, что эти частицы не проявляются в реакции нейтрализации, описанной выше. Как ни заманчиво было бы сказать, что гидроксоний и гидроксид будут реагировать с образованием молекул воды (тем самым просто отбрасывая их и игнорируя), они являются реальными частицами реакции, которые необходимо учитывать в окончательной форме K n. . Чтобы устранить их, добавьте следующую реакцию:
. Чтобы устранить их, добавьте следующую реакцию:
\ [\ ce {h4O + + OH- \ leftrightarrow 2h3O} \ hspace {60px} \ mathrm {K = \ dfrac {1} {K_w}} \]
Эта реакция противоположна реакции K w , реакции, которую мы видели ранее.6} \]
Это значение K n чуть больше шести миллионов очень велико. Это говорит о том, что эта реакция для всех практических целей будет завершена.
Прежде чем решать эту проблему, стоит сделать небольшое отступление и в более общем плане изучить, что мы можем ожидать от значения K n . Всегда ли можно ожидать, что K n будет большим, так что реакции нейтрализации всегда будут завершаться? Или бывают случаи, когда K n может быть относительно небольшим, так что реакция не дойдет до завершения?
Следует помнить о растворе с чрезмерно разбавленной концентрацией кислоты или основания.Например, предположим, что концентрации кислоты и основания порядка 10 -10 М. В этом случае кислоты и основания так мало, что даже если бы значение K n было большим, фактическая степень реакции еще может быть мало. Не так часто мы можем встретить такие растворы в лабораторных условиях, где мы обычно используем гораздо более высокие концентрации. Но это могло произойти в образцах окружающей среды для некоторых видов.
В этом случае кислоты и основания так мало, что даже если бы значение K n было большим, фактическая степень реакции еще может быть мало. Не так часто мы можем встретить такие растворы в лабораторных условиях, где мы обычно используем гораздо более высокие концентрации. Но это могло произойти в образцах окружающей среды для некоторых видов.
Если предположить, что растворы с заметными концентрациями кислоты и основания, получим ли мы когда-нибудь небольшое значение K n ? Вспоминая, мы говорили о слабых кислотах как имеющих значения K и в порядке от самого сильного к самому слабому, 10 -3 , 10 -5 , 10 -7 и 10 -9 .Аналогично слабые основания имели значения K b от самого сильного до самого слабого по той же шкале (от 10 -3 до 10 -9 ). Запомнив уравнение для K n :
К n = К a \ (\ times \) K b \ (\ times \) 10 14
Мы видим, что для получения небольшого значения K n потребуется смесь чрезмерно слабой кислоты и основания. Например, смешивание чрезвычайно слабой кислоты с K a из 10 -9 с чрезвычайно слабым основанием с K b из 10 -9 даст K n из 10 -4 , небольшое количество.Эта реакция нейтрализации вообще не будет протекать долго. Если бы кислота имела значение K , a , равное 10 -7 , а основание, a, K b, значение , равное 10 -7 , значение K n было бы 1, промежуточным значением. Эта реакция нейтрализации будет продолжаться до некоторой степени.
Например, смешивание чрезвычайно слабой кислоты с K a из 10 -9 с чрезвычайно слабым основанием с K b из 10 -9 даст K n из 10 -4 , небольшое количество.Эта реакция нейтрализации вообще не будет протекать долго. Если бы кислота имела значение K , a , равное 10 -7 , а основание, a, K b, значение , равное 10 -7 , значение K n было бы 1, промежуточным значением. Эта реакция нейтрализации будет продолжаться до некоторой степени.
Если мы рассмотрим реакцию нейтрализации, в которой либо кислота, либо основание были сильными (сильная кислота или основание могут иметь значение K a или K b порядка 10 6 или выше), вам потребуется другие виды должны иметь значение K 10 -20 или ниже, чтобы получить небольшое значение K n .Поскольку это необоснованно низкое значение для слабой кислоты или основания, любая кислотно-основная реакция, в которой участвует сильная кислота или сильное основание, будет завершена.
Первый шаг – вычислить начальные концентрации Hcba и EA, помня, что смешивание двух растворов разбавляет каждый из видов.
\ [\ textrm {[Hcba]:} \ mathrm {(0,224 \: M) \ times \ dfrac {45 \: ml} {75 \: ml} = 0,1344 \: M} \]
\ [\ textrm {[EA]:} \ mathrm {(0,187 \: M) \ times \ dfrac {30 \: ml} {75 \: ml} = 0.0748 \: M} \]
Следующий шаг, поскольку K n велик, должен позволить реакции пройти до завершения. Это взаимно однозначная реакция, поэтому вещества с более низкой концентрацией будут израсходованы и ограничат количество образующегося продукта.
\ [\ begin {align}
& && \ ce {Hcba} \ hspace {25px} + && \ ce {EA} \ hspace {25px} \ leftrightarrow && \ ce {cba-} \ hspace {25px} + && \ ce {EAH +} \ nonumber \\
& \ ce {Начальное} && 0,1344 && 0,0748 && 0 && 0 \ nonumber \\
& \ ce {Завершение} && 0.0596 && 0 && 0,0748 && 0,0748 \ nonumber
\ end {align} \]
Конечно, количество EA не может быть нулевым, поскольку K n – это конечное значение и должно быть какое-то конечное количество EA. Следующим шагом в этой проблеме является предположение, что происходит небольшая обратная реакция.
Следующим шагом в этой проблеме является предположение, что происходит небольшая обратная реакция.
\ [\ begin {align}
& && \ ce {Hcba} \ hspace {25px} + && \ ce {EA} \ hspace {25px} \ leftrightarrow && \ ce {cba-} \ hspace {25px} + && \ ce {EAH +} \ nonumber \\
& \ ce {Initial} && 0.1344 && 0,0748 && 0 && 0 \ nonumber \\
& \ ce {Завершение} && 0,0596 && 0 && 0,0748 && 0,0748 \ nonumber \\
& \ ce {Назад \: реакция} && 0,0596 + \ ce {x} && \ ce {x} && 0,0748 – \ ce {x} && 0,0748 – \ ce {x} \ nonumber
\ end {align} \]
И теперь мы можем подумать, можно ли сделать какие-либо приближения. Учитывая, что K n настолько велик, степень обратной реакции очень мала. Это означает, что, вероятно, x очень мало по сравнению с 0.0596 и 0,0748, так что 0,0596 \ (\ gg \) x и 0,0748 \ (\ gg \) x.
\ [\ begin {align}
& && \ ce {Hcba} \ hspace {25px} + && \ ce {EA} \ hspace {25px} \ leftrightarrow && \ ce {cba-} \ hspace {25px} + && \ ce {EAH +} \ nonumber \\
& \ ce {Начальное} && 0,1344 && 0,0748 && 0 && 0 \ nonumber \\
& \ ce {Завершение} && 0,0596 && 0 && 0,0748 && 0,0748 \ nonumber \\
& \ ce {Back \: response} && 0,0596 + \ ce {x} && \ ce {x} && 0. 0748 – \ ce {x} && 0,0748 – \ ce {x} \ nonumber \\
0748 – \ ce {x} && 0,0748 – \ ce {x} \ nonumber \\
& \ ce {Допущение} && 0,0596 \ gg \ ce {x} && && 0,0748 \ gg \ ce {x} && 0. 0748 \ gg \ ce {x} \ nonumber \\
& \ ce {Приближение} && 0,0596 && \ ce {x} && 0,0748 && 0,0748 \ nonumber
\ end {align} \]
Прежде чем мы продолжим, стоит изучить эти окончательные концентрации. Следует отметить одну интересную вещь: у нас есть заметные количества Hcba и cba –. Эти два являются сопряженными парами, и мы знаем, что решение с заметными количествами обоих членов сопряженной пары представляет собой буфер.{-8}} \]
Это число очень мало и явно меньше 5% от 0,0596 и 0,0748. Если мы предположим, что 1,46 \ (\ times \) 10 -8 – это окончательное значение EA после обратной реакции, и что 0,0748 – это окончательное значение EAH + , у нас есть окончательные значения для обоих членов сопряженной пары. . Если мы подставим их в уравнение Хендерсона-Хассельбаха для этиламмония, мы должны получить такой же pH, как указано выше. (Обратите внимание, EA и EAH + не являются буфером, поскольку количество EA незначительно.{-8}} {0,0748} \ справа) = 3,92} \]
(Обратите внимание, EA и EAH + не являются буфером, поскольку количество EA незначительно.{-8}} {0,0748} \ справа) = 3,92} \]
Неудивительно, что эти два значения идентичны.
6.8 Задачи со смесью и решением слов – Промежуточная алгебра
Решение смешанных задач обычно включает решение систем уравнений. Проблемы смешения – это проблемы, в которых два разных решения смешиваются вместе, в результате чего получается новое окончательное решение. Использование стола поможет установить и решить эти проблемы. Базовая структура этой таблицы показана ниже:
| Имя | Сумма | Значение | Уравнение |
|---|---|---|---|
Первый столбец в таблице (Имя) используется для определения жидкостей или объектов, смешанных в проблеме. Во втором столбце (Количество) указывается количество каждой жидкости или объекта. Третий столбец (Значение) используется для значения каждого объекта или процента концентрации каждой жидкости. Последний столбец (Уравнение) содержит произведение суммы на значение или концентрацию.
Во втором столбце (Количество) указывается количество каждой жидкости или объекта. Третий столбец (Значение) используется для значения каждого объекта или процента концентрации каждой жидкости. Последний столбец (Уравнение) содержит произведение суммы на значение или концентрацию.
Ясна содержит 70 мл 50% раствора метана. Сколько 80% раствора она должна добавить, чтобы окончательный раствор состоял из 60% метана? Найдите уравнение.
- Имена решений: 50% (S 50 ), 60% (S 60 ) и 80% (S 80 ).
- Суммы: S 50 = 70 мл, S 80 и S 60 = 70 мл + S 80 .
- Концентрации S 50 = 0,50, S 60 = 0,60 и S 80 = 0,80.
| Имя | Сумма | Значение | Уравнение |
|---|---|---|---|
| S 50 | 70 мл | 0,50 | 0,50 (70 мл) |
| S 80 | S 80 | 0. 80 80 | 0,80 (S 80 ) |
| S 60 | 70 мл + S 80 | 0.60 | 0,60 (70 мл + S 80 ) |
Уравнение, полученное из этих данных: 0,50 (70 мл) + 0,80 (S 80 ) = 0,60 (70 мл + S 80 ).
У Ника и Хлои есть два сорта молока от их небольшого молочного стада: одно с 24% молочным жиром, а другое с 18% молочным жиром. Сколько каждого из них они должны использовать, чтобы получить 42 литра 20% жира?
| Имя | Сумма | Значение | Уравнение |
|---|---|---|---|
| В 24 | В 24 | 0.24 | 0,24 (В 24 ) |
| В 18 | 42 L – B 24 | 0,18 | 0,18 (42 L – B 24 ) |
| В 20 | 42 л | 0,20 | 0,20 (42 л) |
Уравнение, полученное на основе этих данных:
Это означает, что необходимо 14 литров пахты 24% и 28 литров пахты 18%.
В кондитерской Наташи шоколад, который продается за килограмм, смешивают с орехами, которые продаются за килограмм.Шоколад и орехи соединяются в шоколадно-ореховую конфету, которая продается за килограмм. Из какого количества каждого из них получается 30 кг смеси?
Уравнение, полученное из этих данных:
Следовательно, для смеси необходимо 20 кг шоколада.
Проблемы со смешиванием часто возникают при смешивании с чистым раствором или с использованием воды, которая не содержит ни одного интересующего химического вещества. Для чистых растворов концентрация составляет 100%.Для воды концентрация составляет 0%. Это показано в следующем примере.
Джои делает 65% раствор антифриза, используя чистый антифриз, смешанный с водой. Сколько каждого из них нужно использовать, чтобы получить 70 литров?
| Имя | Сумма | Значение | Уравнение |
|---|---|---|---|
| Антифриз (А) | А | 1,00 | 1,00 (А) |
| Вода (Вт) | 70 л – А | 0. 00 00 | 0,00 (70 л – А) |
| 65% раствор | 70 л | 0,65 | 0,65 (70 л) |
Уравнение, полученное на основе этих данных:
Это означает, что количество добавленной воды составляет 70 л – 45,5 л = 24,5 л.
Для вопросов с 1 по 9 напишите уравнения, определяющие взаимосвязь.
- Бак вмещает 8000 литров раствора 40% кислоты. Сколько воды нужно добавить, чтобы приготовить раствор, содержащий 30% кислоты?
- Сколько чистого антифриза нужно добавить к 5 литрам 30% смеси антифриза, чтобы получился раствор, содержащий 50% антифриза?
- У вас есть 12 кг 10% физиологического раствора и еще один 3% раствор.Сколько килограммов второго нужно добавить к первому, чтобы получился 5% раствор?
- Сколько чистого спирта нужно добавить к 24 литрам 14% раствора спирта, чтобы получить 20% раствор?
- Сколько литров синего красителя, которое стоит за литр, необходимо смешать с 18 литрами пурпурного красителя, который стоит за литр, чтобы приготовить смесь, которая стоит за литр?
- Сколько граммов чистой кислоты нужно добавить к 40 граммам 20% раствора кислоты, чтобы получить раствор, содержащий 36% кислоты?
- 100-килограммовый мешок корма для животных состоит на 40% из овса.
 Сколько килограммов чистого овса необходимо добавить в этот корм, чтобы получить 50% овсяную смесь?
Сколько килограммов чистого овса необходимо добавить в этот корм, чтобы получить 50% овсяную смесь? - 20-граммовый сплав платины, который стоит за грамм, смешивают со сплавом, который стоит за грамм. Сколько граммов сплава нужно использовать для изготовления сплава, который стоит грамм?
- Сколько килограммов чая, стоимость одного килограмма, необходимо смешать с 12 килограммами чая, которые стоят за килограмм, чтобы приготовить смесь, которая стоит за килограмм?
Ответьте на вопросы с 10 по 21.
- Сколько литров растворителя, которое стоит за литр, необходимо смешать с 6 литрами растворителя, который стоит за литр, чтобы получить растворитель, который стоит за литр?
- Сколько килограммов карамели, стоящей за килограмм, необходимо смешать с 24 килограммами мармелада, которые стоят за килограмм, чтобы приготовить смесь, которая продается за килограмм?
- Сколько килограммов почвенной добавки, которая стоит на килограмм, необходимо смешать с 20 килограммами нитрата алюминия, которая стоит за килограмм, чтобы получить удобрение, которое стоит за килограмм?
- Конфетная смесь продается за кг.
 Он содержит шоколадные конфеты стоимостью за кг и другие конфеты стоимостью за кг. Сколько каждого в 15 кг смеси?
Он содержит шоколадные конфеты стоимостью за кг и другие конфеты стоимостью за кг. Сколько каждого в 15 кг смеси? - Молоко определенного сорта содержит 10% молочного жира, а сливки определенного сорта – 60% молочного жира. Сколько литров каждого нужно взять, чтобы получить смесь из 100 литров, содержащую 45% молочного жира?
- Раствор A на 50% состоит из кислоты, а раствор B на 80%. Сколько каждого из них нужно использовать, чтобы приготовить 100 мл раствора, который содержит 68% кислоты?
- Краска, содержащая 21% зеленого красителя, смешивается с краской, содержащей 15% зеленого красителя.Сколько литров каждого нужно израсходовать, чтобы приготовить 600 литров краски, содержащей 19% зеленого красителя?
- Сколько килограммов кофе, на 40% состоящего из зерен явы, необходимо смешать с кофе, который на 30% состоит из зерен, чтобы приготовить 80 кг кофейной смеси, состоящей из 32% зерен?
- Ресторану необходимо приготовить фруктовый пунш с легким содержанием алкоголя и крепостью 6%.


 9 = 0,1
9 = 0,1


 2 из 2)
2 из 2)  70
70 7 x + 20 = 0,5 (50 + x ).
Решите относительно x .
7 x + 20 = 0,5 (50 + x ).
Решите относительно x . 15
15
 США)
= 73,60 долл. США
США)
= 73,60 долл. США Упростите деление, чтобы найти удельную стоимость.
Авторские права © Элизабет
Stapel 1999-2011 Все права защищены.
Упростите деление, чтобы найти удельную стоимость.
Авторские права © Элизабет
Stapel 1999-2011 Все права защищены. 90
90 90 x + 8 долларов = (16 + x ) (0,65 доллара).
Решите относительно x .
90 x + 8 долларов = (16 + x ) (0,65 доллара).
Решите относительно x . 35
35 Решите для x ,
а затем преобразовать десятичный ответ в процент.
Решите для x ,
а затем преобразовать десятичный ответ в процент. 00
00 Упростите, а затем преобразуйте в проценты.
Упростите, а затем преобразуйте в проценты.