2.1 Образование иминов и оксимов:
При реакции самого аммиака с карбонильными соединениями образуются неустойчивые и склонные к полимеризации имины. Имины, содержащие хотя бы один ароматический заместитель у карбонильного углерода (Аr–СН=N–R), являются устойчивыми продуктами. Они известны как основания Шиффа (часть 2, глава 2).
2.1.1 Гидролиз иминов. Имины легко гидролизуются в кислой или щелочной среде, что позволяет отделить карбонильные соединения от соединений других классов и выделить их в чистом виде:
2.1.2 Гидролиз оксимов. Оксимы, как и многие производные карбонильных соединений, в водных растворах кислот могут подвергаться гидролизу, регенерируя исходное карбонильное соединение и гидроксиламин. В присутствии сильных кислот альдоксимы могут подвергаться дегидратации:
2. 2.3
Перегруппировка Бекмана (1886 г.). Оксимы кетонов под действием
сильных кислот (концентрированной H2SO4,
полифосфорной кислоты) или РОСl3, РСl5 претерпевают перегруппировку с
образованием амидов кислот:
2.3
Перегруппировка Бекмана (1886 г.). Оксимы кетонов под действием
сильных кислот (концентрированной H2SO4,
полифосфорной кислоты) или РОСl3, РСl5 претерпевают перегруппировку с
образованием амидов кислот:
Следует отметить две характерные особенности механизма перегруппировки:
миграция углеводородного заместителя и разрыв связи N–О протекают как одновременный процесс, так что атом азота не получает в процессе реакции полного положительного заряда;
в протонированном оксиме обычно мигрирует R–группа, находящаяся в транс-положении к ОН-группе.
Оксимы,
как и все другие продукты взаимодействия
карбонильных соединений с N-нуклеофилами,
благодаря π-связи
могут существовать в виде цис–транс-изомеров,
называемых в отличие от алкенов син–
и анти-формами.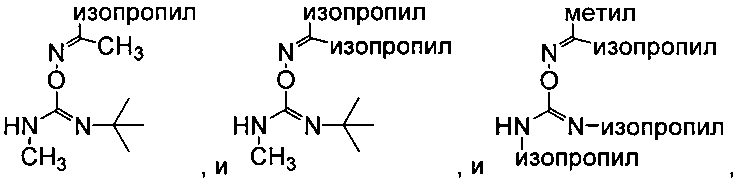 Роль второго заместителя у атома азота
выполняет электронная пара. Если ОН-группа
и меньший заместитель находятся по одну
сторону плоскости
Роль второго заместителя у атома азота
выполняет электронная пара. Если ОН-группа
и меньший заместитель находятся по одну
сторону плоскости
Получающиеся амиды легко гидролизуются с образованием первичного амина и карбоновой кислоты, поэтому эта реакция дает возможность по структре установить строение исходного кетона, а также конфигурацию оксимов. Кроме того, перегруппировка Бекмана может быть использована в синтезе амидов, первичных аминов и кислот, в частности, нашла применение в промышленности перегруппировка оксима циклогексанона с целью получения капролактама – исходного соединения для производства полиамидного синтетического волокна капрон:
3. Реакции с
галогенцентрированными нуклеофилами. Альдегиды
и кетоны при взаимодействии с РСl5 образуют геминальные дигалогенуглеводороды
через внутримолекулярное нуклеофильное
замещение:
Реакции с
галогенцентрированными нуклеофилами. Альдегиды
и кетоны при взаимодействии с РСl5 образуют геминальные дигалогенуглеводороды
через внутримолекулярное нуклеофильное
замещение:
4. Реакции восстановления альдегидов и кетонов. Альдегиды и кетоны могут быть восстановлены в зависимости от условий реакции до соответствующих спиртов либо углеводородов, если в молекуле имеются связи
4.1
4.2
4.3 Метод Клеменсена (1913 г.). Восстановление карбонильной группы активными металлами (или амальгамами) в кислой среде приводит к образованию углеводородов:
4.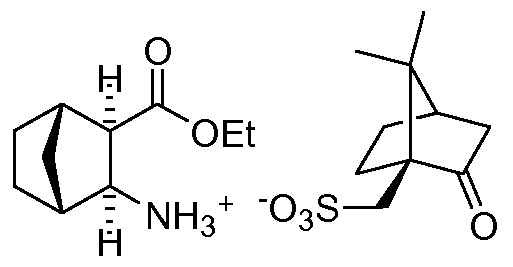 4
Восстановление по Кижнеру-Вольфу (1911
г.). Прямое нагревание оксосоединения
с гидразином и КОН в высококипящем полярном растворителе:
4
Восстановление по Кижнеру-Вольфу (1911
г.). Прямое нагревание оксосоединения
с гидразином и КОН в высококипящем полярном растворителе:
4.5 Восстановление комплексными гидридами металлов (NaBН4, LiAlН4). Реакции восстановления карбонильной группы гидридами металлов по механизму могут быть отнесены к типичным ANреакциям:
Атакующей частицей служит анион
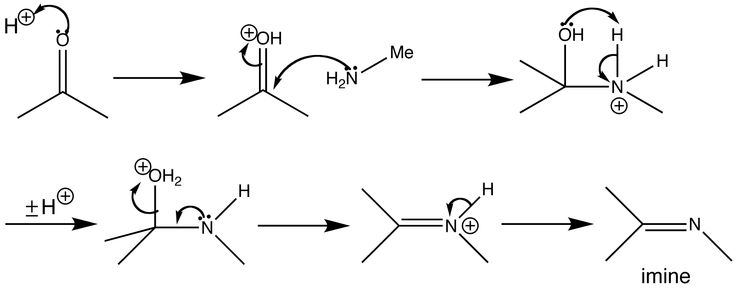
4.5.1 Алюмогидрид лития – мощный и поэтому недостаточно селективный восстановитель. В его присутствии восстанавливаются параллельно с карбонильной группой и кратные связи, группы
4.5.2 Борогидрид натрия – более мягкий восстановитель, селективно восстанавливающий карбонильные группы, не затрагивающий сопряженные с ними двойные связи. Это позволяет получать дефицитные ненасыщенные спирты:
Амин Функциональная группа Имин Химия Атом водорода, 2d, угол, текст, треугольник png
Амин Функциональная группа Имин Химия Атом водорода, 2d, угол, текст, треугольник pngтеги
- угол,
- текст,
- треугольник,
- логотип,
- другие,
- химия,
- число,
- черный,
- химическая реакция,
- параллель,
- органическое соединение,
- органическая химия,
- заместитель,
- символ,
- третичный,
- линия,
- кетон,
- имин,
- альдегид,
- алкил,
- амин,
- аммиак,
- площадь,
- атом,
- черно-белое,
- марка,
- схема,
- функциональная группа,
- атом водорода,
- 2д,
- png,
- прозрачный,
- бесплатная загрузка
Об этом PNG
- Размер изображения
- 1024x652px
- Размер файла
- 15.

- MIME тип
- Image/png
изменить размер PNG
ширина(px)
высота(px)
Лицензия
Некоммерческое использование, DMCA Contact Us
- Химическое соединение Химический синтез Химия Органическое соединение Молекула, химическая формула, угол, белый, текст png 1917x1466px 134.17KB
- Глюкоза Органическое соединение Химия Химическое соединение Сахароза, сахар, угол, белый, текст png
1920x1280px
58.
 33KB
33KB - Водородный текст, Водород Химический элемент Символ Периодическая таблица Химический состав, элемент, разное, угол, белый png 1024x1024px 27.52KB
- Ацетон Химическое соединение Химическая формула Структурная формула Диметилсульфоксид, другие, угол, текст, другие png 1200x713px 22.38KB
- Эфир Функциональная группа Амин Нитросоединение Органическое соединение, колибри, разное, угол, белый png 849x971px 9.06KB
 61KB
61KB- Функциональная группа Спирт Оксигруппа Метильная группа Химия, др., угол, текст, прямоугольник png 1200x1061px 16.24KB
- Этанол Химическая формула Алкоголь Химия Химическое вещество, другие, угол, белый, текст png 1280x837px 18.88KB
- Допамин молекула химия нейротрансмиттер серотонин, информация об элементе, угол, белый, текст png 800x328px 12.14KB
- Кофеин Кофеин Молекулы Химическая структура Молекулярная геометрия, Кофе, угол, белый, текст png 1200x987px 40.58KB
- Молекула Химическое соединение Химическая формула Аминокислота Леводопа, дофамин, угол, белый, текст png
1280x546px
25.
 57KB
57KB - Этаноловое топливо Алкоголь Структурная формула Структура, стоимость, организационная структура, угол, белый, текст png 1280x783px 14.72KB
- Формальдегид Химическое строение Химическое вещество, холодная кислота Линг, разное, угол, текст png 1104x1024px 23.69KB
- Этанол Спирт Химическое соединение Структурная формула Химия, Растворение, разное, угол, белый png 1208x747px 1.64KB
- Альдегид Функциональная группа Структура Кетон Химия, Альдегид, угол, химия, структура png 657x600px 10.16KB
- Кетон Функциональная группа Альдегид Карбонильная группа Органическая химия, другие, угол, текст, логотип png
760x665px
14.
 03KB
03KB - Ацетон Скелетная формула Карбонильная группа Структура Кетон, скелет, разное, угол, другие png 787x768px 11.98KB
- Кофеин Кофеин Молекула Химия Химическое вещество, Кофе, угол, белый, текст png 748x615px 25.92KB
- Органическое соединение Химическое соединение Органическая химия Метан, другие, угол, белый, текст png 1100x788px 26.69KB
- Химический состав Химический состав Химия Химическая номенклатура Амин, другие, химический элемент, угол, текст png 1280x927px 43.85KB
- Ацетальдегид кетон Функциональная группа Химия, Esmalte, угол, текст, другие png
1100x847px
27.
 42KB
42KB - Молекула Химическая структура Тиамин Химическая формула, другие, угол, белый, текст png 1200x420px 22.19KB
- Химия Химическая структура Химический синтез Соединение диазония, никотин, угол, белый, текст png 1280x875px 34.45KB
- Бензол Химия Химическая структура Структурная формула, каучуки, угол, белый, текст png 880x1040px 38.73KB
- Структура Льюиса Схема атома водорода, символ, разное, угол, текст png 768x768px 5.31KB
- Этанол Структурная формула Алкоголь Скелетная формула Химическое соединение, абсолют, разное, угол, белый png
1200x742px
10.
 61KB
61KB - Периодическая таблица Химический элемент Химия Символ, символ, разное, химический элемент, угол png 2000x1148px 13.08KB
- Химия Химический элемент Химическая реакция Лаборатория Периодическая таблица, символ, разное, химический элемент, белый png 600x564px 18.98KB
- Глюкоза Химия Органическое соединение Химическое соединение Фруктоза, молекулярная структура фона, угол, белый, текст png 946x1024px 34.06KB
- Молекулы дейтерированного бензола Ароматичность Химия, химия, Разное, другие, сфера png 1000x1100px 212.92KB
- Носкапин Молекула Химическое соединение Химическая формула Химия, Структура, угол, белый, текст png
1060x958px
23.
 77KB
77KB - шестигранная форма, циклогексановая конформация структурная формула химическое вещество молекула, шестиугольник, разное, угол, белый png 1200x1380px 28.68KB
- Химическая формула Алкоголь Химическое вещество Химия Структурная формула, другие, угол, белый, текст png 800x558px 18.2KB
- газообразный водород атом атом водорода, другие, синий, текст, другие png 600x600px 42.41KB
- Ароматичность Фенолы Ароматические углеводороды Миндальная кислота Бензол, др., угол, прямоугольник, треугольник png 670x767px 17.25KB
- Фенолы Органическая химия Бензоильная группа Химический синтез, бензольное кольцо, разное, угол, прямоугольник png
1034x1192px
10.
 86KB
86KB - Химическое равновесие Химия Обратимая реакция Химическая реакция Динамическое равновесие, динамический удар, разное, угол, треугольник png 822x670px 5.1KB
- Метанол Структурная формула Структура Бутанол Спирт, молекулярная цепь, разное, угол, белый png 1208x747px 1.65KB
- Серотонин молекула химия химическая структура мелатонин, другие, угол, белый, текст png 800x587px 16.54KB
- Частичный заряд Электрический заряд Вода Молекула Химическая полярность, вода Химия, угол, текст, логотип png 2000x1356px 45.67KB
- Органическая химия Нейротрансмиттер Дофамин, Серотонин, Адренал, угол, белый, текст png
1138x609px
18.
 83KB
83KB - Периодическая таблица Химия Химический элемент Рабочий лист, динамические элементы, химический элемент, угол, мебель png 1920x1080px 357.83KB
- Периодическая таблица Атомный номер Химия Химический элемент, периодический, химический элемент, угол, мебель png 3840x2160px 177.66KB
- Углевод Моносахарид Фишер Проекция Альдоза Рибоза, рибонуклеиновая кислота, разное, угол, текст png 500x833px 16.33KB
- Химическая формула Молекула Вода Химия Химическое соединение, вода, угол, текст, логотип png 1280x549px 12.36KB
- Этилен Структурная формула Пропен Химическая связь Двойная связь, 21, разное, угол, белый png
1200x893px
38.
 06KB
06KB - Ацетальдегид Химия Структурная формула Структура, о, разное, угол, текст png 1392x1200px 39.04KB
- Гликоген Химическая структура Молекула Полисахарид, другие, угол, белый, текст png 1280x564px 47.44KB
Я добываю
Общая структура имина
An я добываю (/ɪˈмяп/ или же /ˈɪмɪп/) это функциональная группа или же химическое соединение содержащий углерод –азот двойная связь. Атом азота может быть присоединен к водороду (H) или к органической группе (R). Если эта группа нет атом водорода, тогда соединение иногда может называться База Шиффа.[1] Атом углерода имеет две дополнительные одинарные связи.[2][3][4] Термин «имин» был изобретен в 1883 году немецким химиком. Альберт Ладенбург.[5]
Содержание
- 1 Номенклатура и классификация
- 1.
 1 Алдимин
1 Алдимин
- 1.
- 2 Синтез иминов
- 2.1 Более специализированные методы
- 3 Иминные реакции
- 3.1 Предшественники гетероциклов
- 3.2 Кислотно-основные реакции
- 3.3 Как лиганды
- 3.4 Imine редукции
- 4 Биологическая роль
- 5 Смотрите также
- 6 Рекомендации
Номенклатура и классификация
Обычно имины относятся к соединениям со связностью R2C = NR, как обсуждается ниже. В более ранней литературе имин относится к аза-аналогу эпоксида. Таким образом, этиленимин представляет собой трехчленное кольцо C2ЧАС4NH.[6]
Имины связаны с кетоны и альдегиды заменой кислорода группой NR. Когда R = H, соединение представляет собой первичный имин, когда R представляет собой гидрокарбил, соединение представляет собой вторичный имин. Имины обладают разнообразной реакционной способностью и обычно встречаются в химии.[4] Когда R3 является ОН, имин называется оксим, а когда R3 NH2 Имин называется гидразон.
Первичный имин, в котором C присоединен как к гидрокарбилу, так и к H, называется первичный альдимин; вторичный имин с такими группами называется вторичный альдимин.[7] Первичный имин, в котором C присоединен к двум гидрокарбилам, называется первичный кетимин; вторичный имин с такими группами называется вторичный кетимин.[8]
Один из способов назвать альдимины – взять имя радикала, убрать окончательную букву «е» и добавить «-имин», например этанимин. В качестве альтернативы имин называют производным карбонила, добавляя слово «имин» к названию карбонильного соединения, оксогруппа которого заменена иминогруппой, например Сидноне Имин и ацетон имин (промежуточный продукт в синтезе ацетон азин ).
N-сульфинилимины представляют собой особый класс иминов, имеющих сульфинильную группу, присоединенную к атому азота.
An катион иминия представляет собой родственную функциональную группу, в которой азот имеет четвертую связь, придающую ей положительный заряд.
Алдимин
An альдимин это imine, который является аналог из альдегид.[9]Таким образом, альдимины имеют общую формулу R – CH = N – R ‘. Алдимины похожи на кетимины, являющиеся аналогами кетоны.
Важным подмножеством альдиминов являются Базы Шиффа, в котором заместитель на азот атом (R ‘) является алкил или же арильная группа (т.е. нет а водород атом).[10]
| Номенклатура | CH3–CH2–CH2–CH = NH | CH3–CH = N – CH3 |
|---|---|---|
| 1 | бутанимин | N-метилэтанимин |
| 2 | бутилиденазан | этилиден (метил) азан |
| 3 | бутилиденамин | N-метилэтилиденамин |
| обычное использование | бутиральдегид имин | ацетальдегид N-метилимин |
Алдимины можно называть тремя разными способами:[11]
- путем замены последнего -e в родительский гидрид, R – CH3, с суффиксом “-я добываю“;
- в качестве алкилиден производные от азане;
- (редкий) как алкилиденовые производные «амина».
Устаревшая номенклатура рассматривает альдимины как производные исходного альдегида.
Синтез иминов
Синтез имина из первичного амина и карбонильного соединения.
Имины обычно получают конденсацией первичных аминов и альдегидов, реже кетонов. С точки зрения механизма, такие реакции протекают через нуклеофильное присоединение давая полуаминальный -C (OH) (NHR) – промежуточное соединение, за которым следует устранение воды с образованием имина (см. алкилимино-дезоксо-бис-замещение для подробного механизма). Равновесие в этой реакции обычно благоприятствует карбонил соединение и амин, так что азеотропная дистилляция или использование дегидратирующего агента, такого как молекулярные сита или же сульфат магния, требуется для ускорения реакции в пользу образования имина. В последние годы появилось несколько реагентов, таких как Трис (2,2,2-трифторэтил) борат [B (OCH2CF3)3],[12] пирролидин[13] или же этоксид титана [Ti (OEt)4][14] было показано, что они катализируют образование имина.
Более специализированные методы
Существует несколько других методов синтеза иминов.
- Реакция органических азидов с карбеноидами металлов (получаемыми из диазокарбонильных соединений).[15]
- Конденсация угольные кислоты с нитрозо соединения.
- Перегруппировка тритил-N-галогенаминов в Перестановка Штиглица.
- Обезвоживание полуаминалы.[16]
- По реакции алкены с гидразойная кислота в Реакция Шмидта.
- По реакции нитрила, соляной кислоты и арена в Реакция Хёша.
- Многокомпонентный синтез 3-тиазолинов в Реакция Азингера.
- Начальный кетимины могут быть синтезированы через Реакция Гриньяра с нитрил.[17][18]
Иминные реакции
Гексафторацетонимин – необычный первичный кетимин, который легко выделить.[16]
Имины восприимчивы к гидролиз к соответствующему амин и карбонил сложный.
Имины участвуют во многих реакциях, аналогичных реакциям альдегидов и кетонов:
- Имин восстанавливается в восстановительное аминирование.

- Имин реагирует с амин для аминальный см. например синтез кукурбитурил.
- Имин реагирует с диены в Реакция Азы Дильс-Альдер к тетрагидропиридину.
Предшественники гетероциклов
Беспрепятственные имины склонны к олигомеризации. Такое поведение характерно для иминов, полученных из формальдегида, таких как CH3N = CH2, который тримеризуется к гексагидротриазин.
Имины широко используются в качестве промежуточных продуктов в синтезе гетероциклов. Ароматические имины реагируют с енольный эфир к хинолин в Поварова реакция. Связь C = N в иминах реактивна по отношению к циклоприсоединениям. Имины термически реагируют с кетены в [2 + 2] циклоприсоединения с образованием β-лактамы в Синтез Штаудингера. Имин может быть окислен мета-хлорпероксибензойная кислота (mCPBA), чтобы дать оксазиридин
А тозилимин реагирует с α, β-ненасыщенное карбонильное соединение для аллильный амин в Реакция Азы-Бейлиса – Хиллмана.
Имины являются промежуточными продуктами алкилирования аминов муравьиной кислотой в Реакция Эшвайлера-Кларка.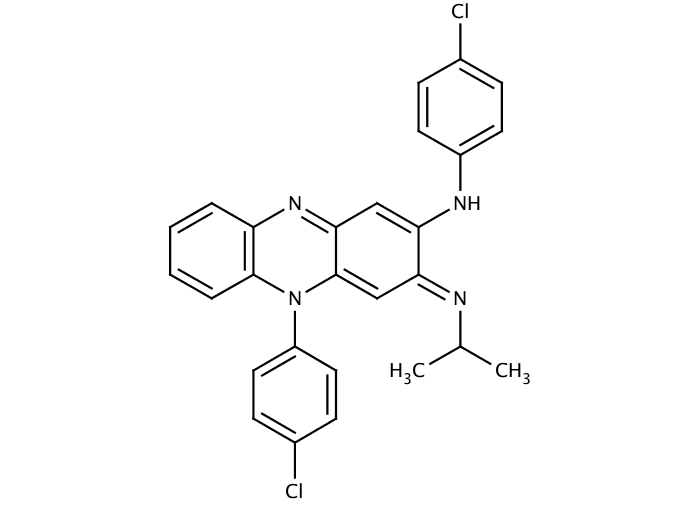
Перегруппировка в химии углеводов с участием имина – это Перестановка Амадори.
Реакция переноса метилена имина нестабилизированным сульфонием илида может дать азиридин system.Imine реагировать с диалкилфосфит в Пудовик реакция и Реакция Кабачника – Филдса.
Кислотно-основные реакции
Как и исходные амины, имины являются умеренно основными и обратимо протонируются с образованием солей иминия. Производные иминия особенно подвержены восстановлению до аминов с использованием перенос гидрирования или стехиометрическим действием цианоборгидрид натрия. Поскольку имины, полученные из несимметричных кетонов, являются прохиральный, их восстановление является полезным методом синтеза хиральных аминов.
Как лиганды
Имины распространены лиганды в координационная химия. Конденсация салициловый альдегид и этилендиамин дают семейства иминсодержащих хелатирующих агентов, таких как Сален.
Imine редукции
Основная статья: Гидрирование двойных связей углерод-азот
Имин можно свести к амин через гидрирование например в синтезе м-толилбензиламин:[19]
Другие восстановители: литийалюминийгидрид и борогидрид натрия.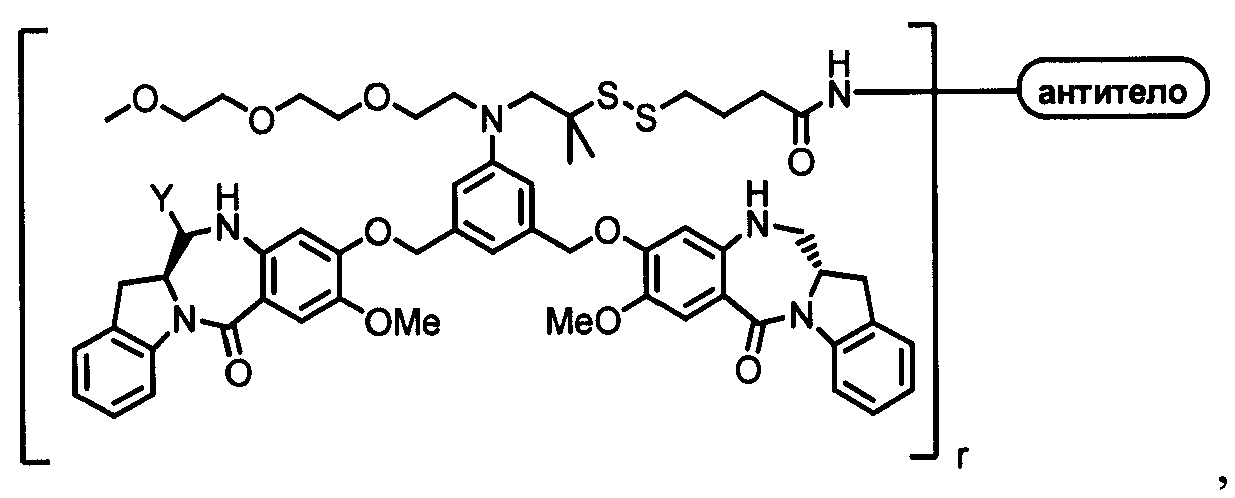 J. Martens: Reduction of Imino Groups (C = N) in (G. Helmchen, RW Hoffmann, J. Mulzer, E. Schaumann) Стереоселективный синтез Хубена-Вейля, Workbench Edition E21 Volume 7, S. 4199-4238, Thieme Verlag Штутгарт, 1996 г., ISBN 3-13-106124-3.
J. Martens: Reduction of Imino Groups (C = N) in (G. Helmchen, RW Hoffmann, J. Mulzer, E. Schaumann) Стереоселективный синтез Хубена-Вейля, Workbench Edition E21 Volume 7, S. 4199-4238, Thieme Verlag Штутгарт, 1996 г., ISBN 3-13-106124-3.
Восстановление иминов
Имины, которые образуются из альдегидов или кетонов и аммиака, могут восстанавливаться до первичных аминов при гидрировании в присутствии обычных катализаторов гетерогенного гидрирования. Эти реакции проводят в одну стадию, восстанавливая смеси карбонильных соединений и аммиака водородом под давлением над никелем Ренея. Поэтому весь процесс получил название “восстановительное аминирование” карбонильных соединений:
Рисунок 1.
Замещение кислорода карбонильной группы
Взаимодействие альдегидов и кетонов с аммиаком и аминами сначала приводит к образованию неустойчивых продуктов присоединения по двойной $C = O$ связи – оксиаминосоединениям. Последние в результате отщепления воды переходят в соответствующие иминосоединения – альдимины или кетимины.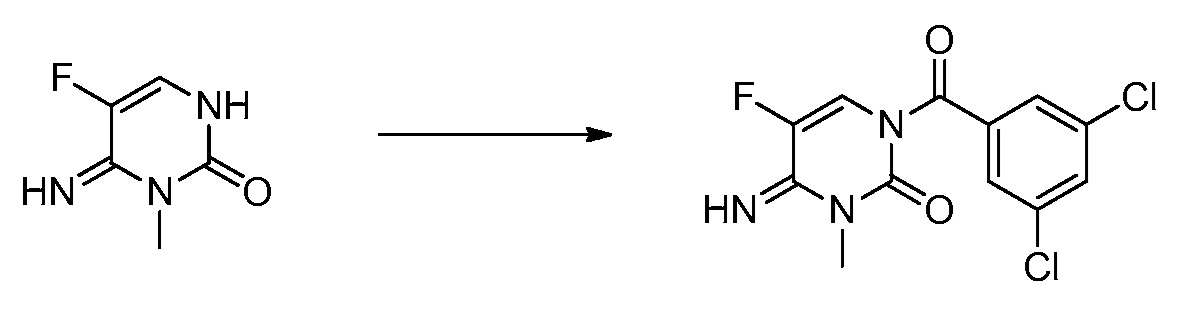 \circ$ С. Это эффективный метод синтеза али-циклических, жирноароматичних и ароматических кетиминов. Например, дифенил-кетимин ($R = R’ = Ph$) получают из бензофенона почти с количественным выходом.
\circ$ С. Это эффективный метод синтеза али-циклических, жирноароматичних и ароматических кетиминов. Например, дифенил-кетимин ($R = R’ = Ph$) получают из бензофенона почти с количественным выходом.
Рисунок 2.
Замещение кислорода иминогруппы в альдегидах и кетонах с одновременным восстановлением имина в присутствии восстановителя – муравьиной кислоты – один из случаев восстановительного аминирования альдегидов или кетонов при действии аммиака или первичных и вторичных аминов (реакция Валлаха-Лейкарта).
Реакция Валлаха-Лейкарта
Реакция Валлаха (1905) – Лейкарта (1885) является важным методом получения первичных, а особенно, вторичных или третичных аминов. Она широко применяется в органическом синтезе, поскольку позволяет сохранить имеющиеся в исходной составе группы, легко восстанавливаются (например, $C = C$, $NO_2$, $CN$). В реакцию вступают алифатические, алициклические, жирноароматические, ароматические и гетероциклические альдегиды и кетоны.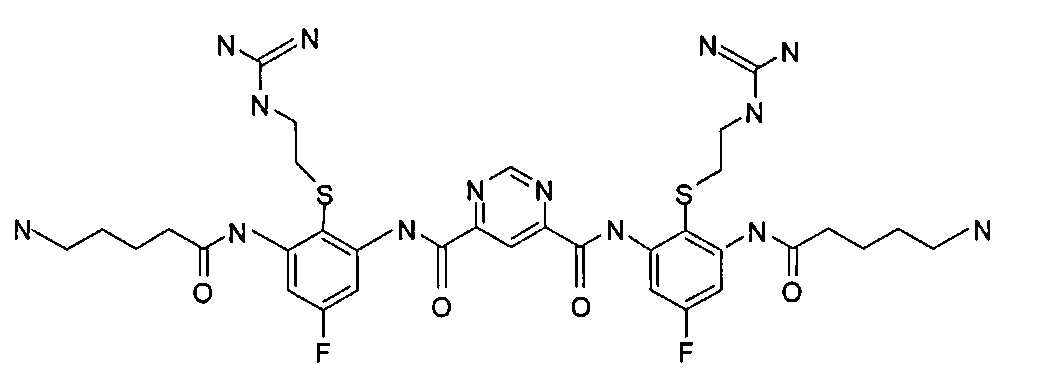 Синтез проводят при нагревании карбонильного соединения с аммонийной солью муравьиной кислоты ($HCOONH_4$) или формамидом ($HCONH_2$) или с первичным или вторичным амином и муравьиной кислотой. Считают, что процесс может происходить по одному из приведенных механизмов.
Синтез проводят при нагревании карбонильного соединения с аммонийной солью муравьиной кислоты ($HCOONH_4$) или формамидом ($HCONH_2$) или с первичным или вторичным амином и муравьиной кислотой. Считают, что процесс может происходить по одному из приведенных механизмов.
По первому механизму, при взаимодействии карбонильной соединения с аммиаком или амином (образующегося при термической диссоциации соли муравьиной кислоты) образуется в соответствии оксиамин или имин. При восстановительном воздействии на них муравьиной кислоты образуется сначала карбокатион, который далее присоединяет гидрид-ион от аниона муравьиной кислоты и образует амин.
Рисунок 3.
Другой механизм предусматривает создание циклического переходного состояния, при взаимодействии карбон-имониевого катиона 1.2 с муравьиной кислотой.
Рисунок 4.
Замечание 1
Следует отметить, что при реакции с аммиаком или первичными аминами могут происходить побочные процессы – дальнейшее восстановительное аминирование соответствующими первичными или вторичными аминами (которые образовались в первом цикле реакции) исходных альдегидов или кетонов с образованием более высокоалкилированных аминов.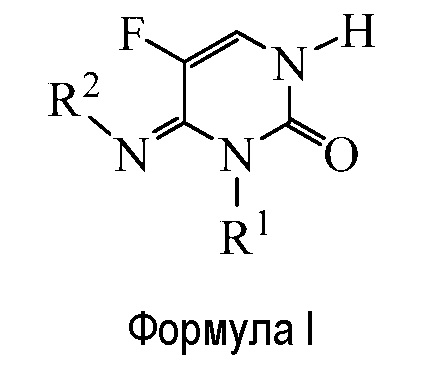
В определенных условиях (например, на холоде, в присутствии поташа) альдегиды и кетоны реагируют со вторичными аминами по другой схеме: происходит отщепление воды и образования диаминопороизводных, при перегонке которых отщепляется одна молекула амина и образуются енамины.
Можно проводить синтез енаминов и в других условиях, например, при кипячении реагентов в бензоле в присутствии $п$-толуолсульфокислоты (для облегчения дегидратации). Во время реакции отгоняется азеотропная смесь воды с бензолом.
Рисунок 5.
Если в реакцию вводить циклические кетоны и циклические амины, то образуются циклические енамины:
Рисунок 6.
Полученные енамины (в частности, циклические) можно использовать для синтеза третичных аминов (восстановлением муравьиной кислотой):
Рисунок 7.
Енамины легко гидролизуются разбавленными кислотами с отщеплением вторичного амина и образованием исходного карбонильного соединения:
Рисунок 8.
Это свойство енаминов часто используют для защиты одной из карбонильных групп в дикетонах от действия различных агентов (например, албмомогидрида лития). После проведения реакции регенерируют карбонильную группу посредством гидролиза енаминной группы.
Каталитическое гидроаминирование альдегидов и кетонов
Путем каталитического гидроаминирования альдегидов и кетонов в присутствии аммиака, первичных или вторичных аминов при повышенном давлении можно получить соответствующие первичные, вторичные или третичные амины.
Реакция восстановительного каталитического аминирования включает стадию дегидратации промежуточного продукта, образовавшегося вследствие присоединения амина по карбонильной группе. Образованный имин или азометин (основа Шиффа) в присутствии катализатора восстанавливается водородом до насыщенного амина.
Рисунок 9.
Например, таким образом можно получить бензиламины из бензальдегида. Для этого бензальдегид растворяют в метаноле, насыщенном аммиаком, добавляют никель Ренея и гидрируют при 90 $^\circ$ С и давлении водорода 100 атм:
Рисунок 10.
Такое преобразование можно провести и с аминокислотами:
Рисунок 11.
Научно-исследовательская работа преподавателей
Основные публикации за последние 6 лет
2021
Конференции
Данилова Е.А., Суворова Ю.В., Иванов Е.Н., Юнникова Л.П., Акентьева Т.А., Исляйкин М.К. Синтез и тестирование биологических свойств тропилированных 2-аминопиримидинов // XXVII Симпозиум «Биоинформатика и компьютерное конструирование лекарств»– 2021. – С. 77.
Юнникова Л.П., Фомина А.Г., Акентьева Т.А., Якимова И.Д Развитие представлений о роли аналогов никотинамидных коферментов в органическом синтезе // Всероссийская научнопрактическая конференция «Агротехнологии XXI века: стратегия развития, технологии и инновации», 16-18 ноября 2021 г. – Пермь: ИПЦ «Прокростъ», 2021. – С. 558-562.
Якимова И.Д., Горохов В.Ю., Стряпунина О.Г. Потенциометрическое определение содержания ионов металлов в растворах (обзор методов анализа) // Всероссийская научнопрактическая конференция «Агротехнологии XXI века: стратегия развития, технологии и инновации», 16-18 ноября 2021 г. – Пермь: ИПЦ «Прокростъ», 2021. – С. 562-565.
– Пермь: ИПЦ «Прокростъ», 2021. – С. 562-565.
Акентьева Т.А., Маннапова Л.Р., Мальцева Е.И. 1,3,5-циклогептатриен и 5Н-дибензо[a,d]циклогептен как структурные аналоги и перспективы применения их производных в сельском хозяйстве в качестве пестицидов, росторегуляторов и лекарственных препаратов // Всероссийская научнопрактическая конференция «Агротехнологии XXI века: стратегия развития, технологии и инновации», 16-18 ноября 2021 г. – Пермь: ИПЦ «Прокростъ», 2021. – С. 527-529.
Журналы и сборники
Леснов А.Е., Кудряшова О.С., Чухланцева Е.Ю. Двухфазные водные системы на основе хлорида алкилбензилдиметиламмония и неорганических высаливателей // Химия в интересах устойчивого развития. – 2021. – Т. 29. – № 1. – С. 61-68.
Кудряшова О.С., Елохов А.М. Фазовые равновесия в системах диантипирилметан–органическая кислота–хлороводород–вода // Журнал физической химии. – 2021. – Т. 95. – № 2. – С. 165-169.
Драчев А.М., Денисова С.А., Леснов А.Е. Комплексообразование эриохромцианина R с ионами алюминия и железа (III) в присутствии пав // Вестник Пермского университета. Серия: Химия. – 2021. – Т. 11. – № 2. – С. 114-125.
Серия: Химия. – 2021. – Т. 11. – № 2. – С. 114-125.
Кудряшова О.С., Елохов А.М., Хайрулина Е.А., Богуш А.А. Состав для затирки горных пород на основе нерастворимых солей кальция для защиты грунтовых вод // Экологические науки о Земле. – 2021. – Т. 80. – № 205. – С. 8.
Старкова Е.В., Неустроев Д.А., Боброва А.В. Дибензосуберенол и тетрафторборат тропилия в реакциях с пара-замещёнными ариламинами // Научный аспект № 1., Т.3. – Самара: изд-во ООО «Аспект», 2021 . – С.322-327.
2020
Конференции
Лысцова Е.А., Горохов В.Ю., Шуров С.Н. Синтез и свойства 7,7-диметил-2-(2,4-диметоксифенил)-5-оксо-5,6,7,8-тетрагидрохинолин-4-карбоновой кислоты // Современные аспекты химии. Материалы VII молодежной школы-конференции. – 2020. – С. 210-214.
Журналы и сборники
Горохов В.Ю., Махова Т.В. (Аза,тио)ксантенилированные амины и имины: синтез, свойства и биологическая активность // Известия Академии наук. Серия химическая. – 2020. – № 3. – С. 425-434.
– 2020. – № 3. – С. 425-434.
Елохов А.М., Белова Д.С., Денисова С.А., Кудряшова О.С. Оптимизация параметров экстракции в системах неорганическая соль–ethomeen C/15–вода Журнал физической химии. – 2020. – Т. 94. – № 7. – С. 1011-1016.
Исаева Ю.И., Елохов А.М., Денисова С.А., Кудряшова О.С. Фазовые равновесия и экстракция ионов металлов в системах на основе смесей хлорида алкилбензилдиметиламмония и оксиэтилированных нонилфенолов // Журнал физической химии. – 2020. – Т. 94. – № 7. – С. 1006-1010.
Кондаков Д.Ф., Фролова Е.А., Кудряшова О.С., Данилов В.П. Противогололедные реагенты на основе хлоридов натрия и кальция и формиата натрия // Химическая технология. – 2020. – Т. 21. – № 7. – С. 297-300.
Кудряшова О.С., Елохов А.М., Гарбуз Е.Э., Распопова Ю.А. Фазовые равновесия в системах K+, Na+//H HCOO––H2O И K+, Na+// HCOO––H2O при 25°С // Журнал неорганической химии. – 2020. – Т. 65. – № 12. – С. 1683-1690.
Станкова А.В., Елохов А.М., Кудряшова О.С., Леснов А.Е. Температурная трансформация фазовых диаграмм систем вода–оксиэтилированный нонилфенол–MgCl2 // Журнал неорганической химии. – 2020. – Т. 65. – № 12. – С. 1691-1696.
Юнникова Л.П., Лихарева Ю.Е., Исляйкин М.К., Данилова Е.А. Соли ксантилия, тиоксантилия или тропилия в реакциях с имидазолом и бензимидазолом // Журнал органической химии. – 2020. – Т. 56. – № 5. – С. 783-788.
Kudryavtsev P., Kudryashova O., Elokhov A., Kudryavtsev N. New biodegradable surfactants: properties and prospects of use // Scientific Israel – Technological Advantages. – 2020. – Т. 22. – № 2. – С. 27-45.
Каталоги или справочники:
Юнникова Л.П., Горохов В.Ю., Акентьева Т.А. Каталог органических реагентов. – Пермь: ИПЦ «Прокростъ», 2017. – 36 с.
Учебные пособия:
Яганова Н.Н., Быков Я.В., Трапезникова Н.Н. Практикум по органической химии: учебное издание. – Пермь: ИПЦ «Прокростъ», 2016. – 116 с.
Юнникова Л.П., Горохов В.Ю., Акентьева Т.А. Органический синтез. – Пермь: ИПЦ «Прокростъ», 2017. – 126 с.
Махова Т.В., Горохов В.Ю. Неорганическая и аналитическая химия. – Пермь: ИПЦ «Прокростъ», 2019. – 155 с.
Методические указания:
Юнникова Л.П., Яганова Н.Н., Якимова И.Д. Физическая и коллоидная химия: лабораторный практикум. – Пермь: ИПЦ «Прокростъ», – 2017. – 102 с.
Якимова И.Д., Быков Я.В. Общая химия: теоретические аспекты, семинары и лабораторные работы. – Пермь: ИПЦ «Прокростъ», – 2018. – 175 с.
Горохов В.Ю., Акентьева Т.А., Юнникова Л.П. Лабораторный практикум по химии(органическая химия). – Пермь: ИПЦ «Прокростъ», – 2019. – 88 с.
2019
Журналы и сборники
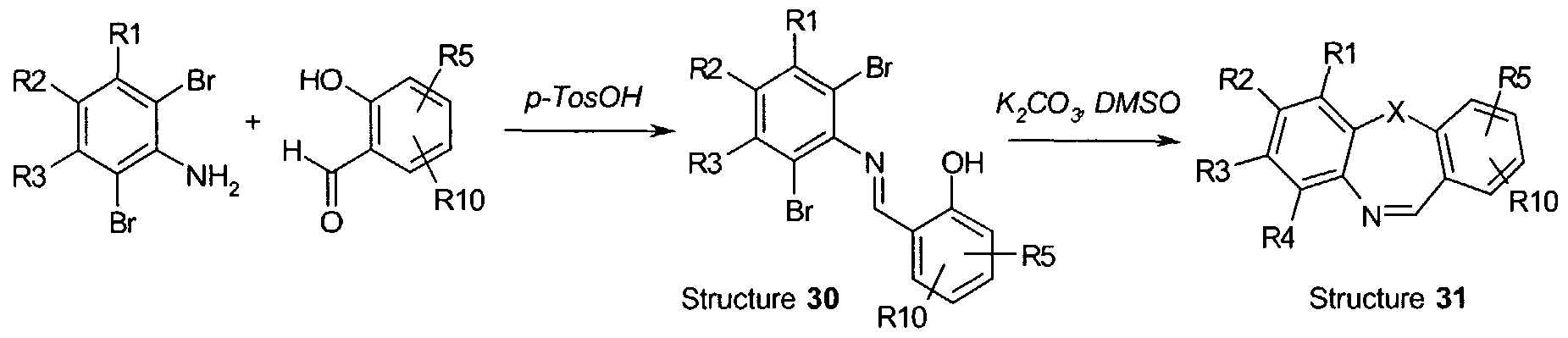
Горохов В.Ю., Быков Я.В., Батуев С.А., Лысцова Е.А., Горохова С.М., Яганова Н.Н. Однореакторный метод синтеза 2-гидроксибензилиден-4-[(аза,тио)ксантенил]анилинов и возможность их применения в качестве регуляторов роста растений // Журнал общей химии. – 2019. – Т. 89. – № 4. – С. 522-527.
– 2019. – Т. 89. – № 4. – С. 522-527.
Горохов В.Ю., Махова Т.В. Пара-(аза,тио)ксантенилированные анилины в реакции переаминирования // Бутлеровские сообщения. – 2019. – Т. 60. – № 10. – С. 32-35.
Юнникова Л.П., Лихарева Ю.Е. Иодид 1,3-диметилбензимидазолиния и 1,3-диметилбензимидазолин в процессах восстановления С=N группы иминов // Бутлеровские сообщения. – 2019. – Т. 60. – № 11. – С. 151-155.
Юнникова Л.П., Лихарева Ю.Е., Баландина С.Ю. N-тропилирование ариламинов // Известия высших учебных заведений. Серия: Химия и химическая технология. – 2019. – Т. 62. – № 2. – С. 79-84.
Юнникова Л.П., Лихарева Ю.Е., Эсенбаева В.В. Электрофильное тропилирование аминопиридинов и 4-аминохинолина // Журнал общей химии. – 2019. – Т. 89. – № 9. – С. 1462-1466.
Юнникова Л.П., Эсенбаева В.В. Соли тропилия как реагенты для модификации гидразидов монокарбоновых кислот // Журнал органической химии. – 2019. – Т. 55. – № 12. – С. 1950-1952.
Юнникова Л.П., Эсенбаева В.В., Акентьева Т. А. Применение 1,3-диоксолана в синтезе замещенных 3,4-дигидрохиназолинов, диарилметанов или метилендиаминов // Бутлеровские сообщения. – 2019. – Т. 58. – № 4. – С. 48-52.
А. Применение 1,3-диоксолана в синтезе замещенных 3,4-дигидрохиназолинов, диарилметанов или метилендиаминов // Бутлеровские сообщения. – 2019. – Т. 58. – № 4. – С. 48-52.
Юнникова Л.П., Эсенбаева В.В., Данилова Е.А., Исляйкин М.К. Катион тиоксантилия в реакциях с фармакофорными аминами гетероциклического ряда // Журнал органической химии. – 2019. – Т. 55. – № 12. – С. 1953-1956.
Yunnikova L.P., Esenbaeva V.V., Danilova E.A., Islyaikin M.K. Reaction of thioxanthylium cation with pharmacophoric heterocyclic amines // Russian Journal of Organic Chemistry. – 2019. – Т. 55. – № 12. – С. 1985-1987.
2018
Журналы и сборники
Акентьева Т.А., Юнникова Л.П., Эсенбаева В.В. Модифицированный синтез 4-(7-циклогепта-1,3,5-триенил)анилина // Бутлеровские сообщения. – 2018. – Т. 56. – № 11. – С. 128-130.
Быков Р.А., Трапезникова Н.Н., Баландина С.Ю., Комарова О.А., Махмудов Р.Р., Пулина Н.А., Собин Ф.В., Рубцов А.Е. Синтез и биологическая активность амидов 4-арил-2-[(2-оксо-1,2-дифенилэтилиден)гидразинил]-4-оксобут-2-еновых кислот // Химико-фармацевтический журнал. – 2018. – Т. 52. – № 5. – С. 33-36.
– 2018. – Т. 52. – № 5. – С. 33-36.
Быков Я.В., Якимова И.Д., Яганова Н.Н. Потенциометрическое определение РКА азотистых органических оснований в среде ацетонитрила // Бутлеровские сообщения. – 2018. – Т. 56. – № 11. – С. 75-81.
Горохов В.Ю., Горохова С.М., Лысцова Е.А. Синтез 4-метил-2,6-ди(9н-тиоксантен-9-ил)анилина // Журнал органической химии. – 2018. – Т. 54. – № 8. – С. 1246-1247.
Эсенбаева В.В., Юнникова Л.П. Амиды сульфаниловой, тио- и угольной кислот в реакции с солями тропилия // Журнал общей химии. – 2018. – Т. 88. – № 4. – С. 683-685.
Эсенбаева В.В., Юнникова Л.П., Кудаярова Т.В., Данилова Е.А. Новые реакции солей тропилия с гетероциклическими диаминами // Журнал общей химии. – 2018. – Т. 88. – № 12. – С. 2087-2090.
Юнникова Л.П., Эсенбаева В.В. Ионы карбения в реакции замещения у атома азота аминогруппы // Журнал органической химии. – 2018. – Т. 54. – № 7. – С. 1015-1018.
Yunnikova L.P., Esenbaeva V.V., Shklyaeva E.V. Tropylium and tritylium salts in reactions with 2-amino-4,6-disubstituted pyrimidines // Russian Journal of Chemistry and Chemical Technology. – 2018. – Т. 61. – № 8. – С. 47-52.
– 2018. – Т. 61. – № 8. – С. 47-52.
Конференции
Волков А.Т., Трапезникова Н.Н., Абрамова Л.П., Петухова А.С., Боровиков М.Ф. Ветеринарно-санитарная оценка продуктов убоя кроликов при экспериментальном заражении животных PER OS микроскопическими грибами (плесенями) // В сборнике: Международная учебно-методическая и научно-практическая конференция, посвященная 140-летию со дня рождения академика Скрябина Константина Ивановича. – 2018. – С. 75-77.
2017
Журналы и сборники
Акентьева Т.А., Махмудов Р.Р. Однореакторный многокомпонентный синтез производных 4-(7-циклогепта-1,3,5-триенил)анилина // Журнал общей химии. – 2017. – Т. – 87. – № 7. – С. 1204-1206.
Игошева Е.В., Трапезникова Н.Н. Из опыта обучения приёмам сравнения и прогнозирования // Химия в школе. Учредители: ООО “Центрхимпресс”. – 2017. – №5. – С. 21-22.
Лихарева Ю.Е., Акентьева Т.А., Юнникова Л.П. Электрофильное тропилирование 2-аминопиридина // Журнал общей химии. – 2017. – Т. 87. – № 2. – С. 333-335.
– 2017. – Т. 87. – № 2. – С. 333-335.
Пак В.Д., Быков Я.В., Яганова Н.Н., Горбунов А.А., Глушков В.А., Дмитриев М.В., Слепухин П.А. Синтез бензо[G]- и бензо[F]хинолинов региоселективной реакцией халконов с нафталин-2-амином // Журнал органической химии. – 2017. – Т. – 53. – № 4. – С. 557-562.
Chao K.L., Yunnikova (Kulakova) L., Herzberg O. Gene polymorphism linked to increased asthma and IBD risk alters gasdermin-B structure, a sulfatide and phosphoinositide binding protein // Proceedings of the National Academy of Sciences of the United States of America. – 2017. – Т. 114. – № 7. – С. E1128-E1137.
Yunnikova L.P., Likhareva Y.E., Akent’eva T.A. Electrophilic tropylation of 2-aminopyridine Russian Journal of General Chemistry. – 2017. – Т. – 87. – № 2. – С. 347-349.
2016
Журналы и сборники
Горохов В.Ю., Махова Т.В. Синтез и антибактериальная активность аминов и иминов, содержащих циклы (аза, тио)ксантенов // Химико-фармацевтический журнал. – 2016. – Т. 50. – № 8. – С. 33-35.
– 2016. – Т. 50. – № 8. – С. 33-35.
Юнникова Л.П., Эсенбаева В.В. 3,5- и 3,6-дизамещенные 3,4-дигидрохиназолины // Журнал общей химии. – 2016. – Т. 86. – № 7. – С. 1223-1225.
Конференции
Акентьева Т.А., Горохов В.Ю. Катионы тропилия и ксантилия в синтезе новых аминов и их производных // ХХ Менделеевский съезд по общей и прикладной химии: тезисы докладов в пяти томах. Уральское отделение Российской академии наук. – 2016. – С. 392.
Быков Я.В., Яганова Н.Н., Пак В.Д. Региоселективность и региоспецифичность реакции халконов с моно- и биядерными первичными ароматическими аминами // ХХ Менделеевский съезд по общей и прикладной химии: тезисы докладов в пяти томах. Уральское отделение Российской академии наук. – 2016. – С. 408.
Юнникова Л.П., Эсенбаева В.В., Лихарева Ю.Е. Новые реакции аналогов тропилидена // ХХ Менделеевский съезд по общей и прикладной химии. тезисы докладов в пяти томах. Уральское отделение Российской академии наук. – 2016. – С. 387.
387.
Имин Енамин Функциональная группа Сульфоний Органическая химия, другие, угол, текст png
Имин Енамин Функциональная группа Сульфоний Органическая химия, другие, угол, текст pngтеги
- угол,
- текст,
- логотип,
- другие,
- химия,
- число,
- азот,
- двойная связь,
- таутомер,
- символ,
- окисление,
- сульфоний,
- заместитель,
- марка,
- органическое соединение,
- органическая химия,
- химическое соединение,
- химический синтез,
- площадь,
- линия,
- имин,
- функциональная группаенамин,
- атом,
- png,
- прозрачный png,
- без фона,
- бесплатная загрузка
- Размер изображения
- 1920x990px
- Размер файла
- 37.17KB
- MIME тип
- Image/png
изменить размер PNG
ширина(px)
высота(px)
Некоммерческое использование, DMCA Contact Us
- org/ImageGallery” align=”middle”>
- Химическое соединение Химический синтез Химия Органическое соединение Молекула, химическая формула, угол, белый png 1917x1466px 134.17KB
- Органическая химия Окситоцин Молекула Химическая формула, Окситоцин, угол, белый png 702x446px 10.83KB
- Водородный текст, Водород Химический элемент Символ Периодическая таблица Химический состав, элемент, разное, угол png 1024x1024px 27.52KB
- Глюкоза Химия Органическое соединение Химическое соединение Фруктоза, молекулярная структура фона, угол, белый png 946x1024px 34.06KB
- Бензол Химия Химическая структура Структурная формула, каучуки, угол, белый png
880x1040px
38.
 73KB
73KB - Бензол Скелетная формула Органическая химия Ароматический углеводород, бензольное кольцо, разное, угол png 1280x701px 24.86KB
- Химия Колледж Публико Мигель де Сервантес Научная лаборатория Окислительное состояние, наука, химический элемент, текст png 1393x592px 534.57KB
- Химия Химическая связь Химическое вещество Ионная связь Атом, молекула, разное, химический элемент png 1009x1280px 325.24KB
- Ион Магний карбонат Химическое соединение Неорганическое соединение, информационный символ, текст, товарный знак png 1280x983px 27.53KB
- Периодическая таблица Химический элемент Химия Атомный номер, физические элементы, разное, угол png
1920x1080px
75.
 43KB
43KB - Ацетальдегид Химическая формула Химия Структурная формула, Брожение этанола, угол, белый png 1100x948px 23.52KB
- Азот Химия Периодическая таблица Химический элемент Химический состав, другие, Разное, химический элемент png 2376x1624px 116.63KB
- Периодическая таблица Химия Состояние окисления Атом, периодическая, разное, химический элемент png 3320x2197px 1.01MB
- Метан Молекула Алкан, 3, разное, химический элемент png 1091x1100px 145.15KB
- Молекула Химия Углеводы Биология Наука, наука, угол, белый png 1070x679px 19.25KB
- org/ImageObject”> Напиток с кофеином Кофеин Кофеин Химическая структура Молекула, Кофе, угол, белый png 2000x1645px 75.2KB
- Амин Функциональная группа Химия Карбоновая кислота Карбонильная группа, другие, угол, белый png 525x600px 5.82KB
- Карбоновая кислота Функциональная группа Карбоксильная группа Химия, День Освобождения О, угол, текст png 742x768px 14.98KB
- Химический инструмент, Химическая лаборатория Эксперимент Химический элемент Иконка, Колба на железной платформе, электроника, текст png 2452x1677px 136.85KB
- Молекула Молекулярная геометрия Химия Шестиугольник, здравый смысл, химический элемент, угол png
615x679px
75.
 31KB
31KB - Уксусная кислота Кислотно-щелочная реакция Химия, др., угол, текст png 640x428px 11.45KB
- Органическая химия Химическая субстанция Лаборатория примесей, НДС, угол, текст png 1164x1024px 41.82KB
- Ацетон Химическое соединение Химическая формула Структурная формула Диметилсульфоксид, другие, угол, текст png 1200x713px 22.38KB
- Молекула Химия Вода Материя Жизнь, вода, химия, твердый png 1100x945px 167.17KB
- Метан Структура Льюиса Структурная формула Простая связь Химическая структура, другие, разное, угол png 800x829px 6.98KB
- org/ImageObject”> Структура Льюиса Ковалентная связь Химическая связь Хлористый водород Валентный электрон, соляная кислота, угол, текст png 1100x600px 21.41KB
- Химическая связь Химия Ковалентная связь Вода Электрон, вода, фиолетовый, химический элемент png 2000x559px 111.16KB
- Атомная теория Периодическая таблица Атомы в молекулах Химия, наука, разное, химический элемент png 1500x1600px 592.81KB
- Структура бензола Льюиса Резонанс Химическая структура, другие, угол, белый png 800x945px 22.86KB
- Тройная связь Химическая связь Азот Ковалентная связь Атом, Оксид бора, текст, другие png 508x567px 12.04KB
- org/ImageObject”> Альдегид Функциональная группа Карбонильная группа Grupa aldehydowa Органическое соединение, другие, текст, другие png 1200x1116px 26.02KB
- Креатин Химическая структура Молекула Креатинин Химия, Назначение Применение, угол, текст png 876x436px 8.86KB
- Оксигруппа Алкоголь Функциональная группа Химия Атом, спирт, текст, другие png 1280x623px 17.46KB
- Молекула Органическая химия, другие, оранжевый, другие png 807x1024px 237.36KB
- Этанол Структурная формула Скелетная формула Структура спирта, другие, Разное, угол png 800x495px 7.97KB
- org/ImageObject”> Орбитальная гибридизация этилена Двойная связь Атомная орбитальная связь Pi, уплощенная, разное, угол png 1040x971px 11.82KB
- Эфир 4-хлоранилин Органическая химия 4-метилбензальдегид Бензол, бензольное кольцо, разное, угол png 534x599px 1.46KB
- Геосмин Органическая химия Бензол Скелетная формула Ароматический углеводород, другие, разное, угол png 1920x1051px 42.1KB
- Бензол Ароматический углеводород Молекула Химическое соединение, бензин, угол, текст png 600x534px 8.18KB
- Кофе Напиток с кофеином Кофеин Химическая структура Молекула, Кофе, угол, белый png 992x816px 18.2KB
- org/ImageObject”> Этанол Спирт Химическое соединение Структурная формула Химия, Растворение, разное, угол png 1208x747px 1.64KB
- Кетоновый эфир Карбонильная группа Функциональная группа Структура, наука, угол, английский png 2000x1626px 49.33KB
- Структура Льюиса Метан Простая связь Химическая связь Валентный электрон, молекулярная цепь, разное, угол png 1041x1079px 10.8KB
- Структурная формула Пропан Химическая формула Скелетная формула Химическое соединение, другие, угол, белый png 800x470px 8.42KB
- Ионная связь Ковалентная связь Химическая связь Химия, химия, разное, оранжевое png 567x720px 127.93KB
- org/ImageObject”> Бензол Ароматический углеводород Ароматичность Органическая химия, другие, угол, белый png 1200x1449px 53.91KB
- Формиат Химия Функциональная группа Этилен Химическая связь, другие, угол, белый png 1200x1173px 14.77KB
- шестигранная форма, циклогексановая конформация структурная формула химическое вещество молекула, шестиугольник, разное, угол png 1200x1380px 28.68KB
- Ковалентная связь Химическая связь Химическое соединение Тройная связь Молекула, морской элемент, разное, текст png 1895x1189px 647.93KB
- Символ Атомное ядро Наука, скрипка, разное, химический элемент png 6792x7659px 110.02KB
Свойства, образование, реакции и механизмы – Master Organic Chemistry
Имины – их свойства, образование, реакции и механизмы
- Имины являются азотистыми аналогами альдегидов и кетонов, содержащими связь C=N вместо связи С=О.

- Они образуются при добавлении первичного амина к альдегиду или кетону , при этом выделяется молекула воды (H 2 O).
- В этом посте мы покажем несколько примеров синтеза иминов, пройдемся по механизму их образования, приведем некоторые из их реакций и сравним их свойства со свойствами альдегидов и кетонов.
Содержание
- Имины – азотсодержащие «родственники» альдегидов и кетонов
- Синтез иминов из альдегидов и кетонов0010
- Механизм образования иминов – ADPED (присоединение-депротонирование-протонирование-отщепление-депротонирование)
- Внутримолекулярное образование иминов
- Реакции иминов – гидролиз и гидразоны
- Почему мы не можем использовать вторичные амины для получения иминов? (соли и энамины иминиума)
- Заключение
- Примечания
- Проверьте себя!
- (Дополнительно) Ссылки и дополнительная литература
1.
 Имины
ИминыСегодня мы рассмотрим альдегиды и кетоны и спросим: что, если мы заменим кислород азотом?
Это даст нам « имин »: [ Примечание 1 – вы также можете встретить термин «основание Шиффа» используется для обозначения имина, полученного из альдегида, и «кетимин» для обозначения имина, полученного из кетона, но мы будем использовать общий термин «имин» для обозначения обоих здесь.)
2. Синтез иминов из альдегидов и кетоновСинтез иминов в большинстве случаев достаточно прост. Первичный амин добавляют к раствору альдегида или кетона , выделяется вода (H 2 O) и образуется соответствующий имин . Возможно, вы помните, что реакцию образования воды можно назвать реакцией -конденсации . Это классический пример.
Вот конкретный пример образования имина из бензальдегида и этиламина из Organic Syntheses Coll.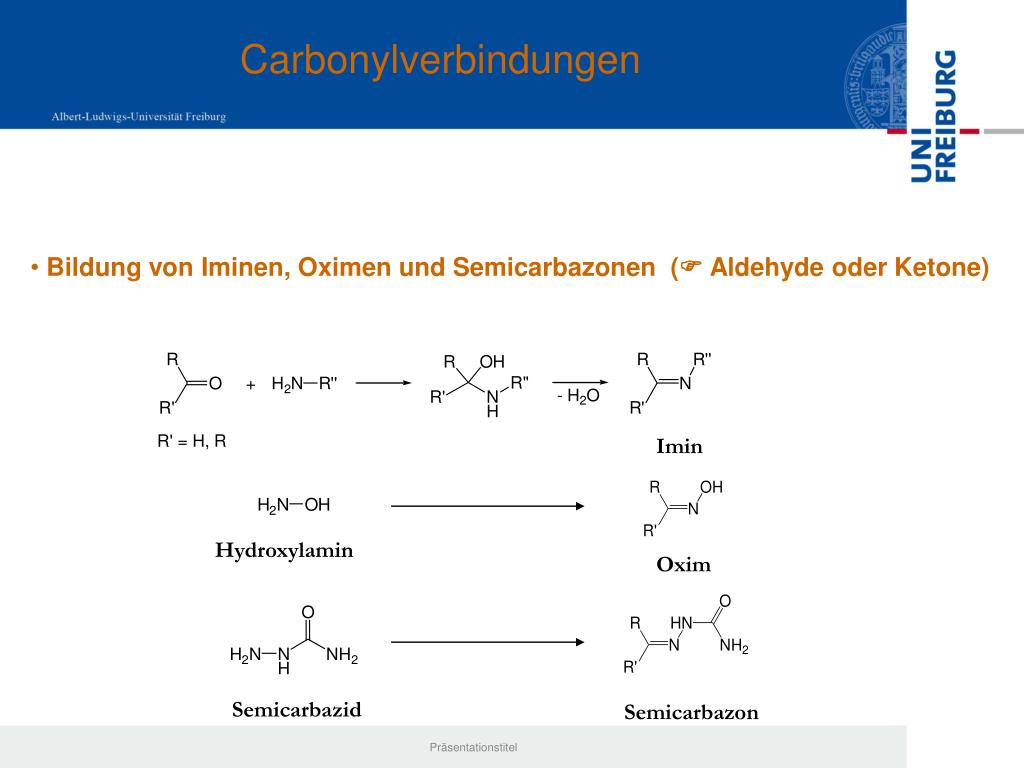 Том. 5, 736 (открытый доступ, нажмите, чтобы увидеть процедуру).
Том. 5, 736 (открытый доступ, нажмите, чтобы увидеть процедуру).
В этом случае конденсация происходит очень быстро. Образовавшуюся воду затем удаляют путем перегонки с получением кристаллического имина с высоким выходом.
Хотя в большинстве случаев не требуется , реакция значительно ускоряется при добавлении кислоты катализатора , и далее мы будем предполагать, что используется кислота. [ Примечание 2 ]
Если вы помните, существует два основных пути, с помощью которых кислотный катализ может способствовать ускорению реакций.
- Кислота ускоряет реакции элиминирования , превращая потенциальные уходящие группы в сопряженные с ними кислоты и, таким образом, превращая их в лучше уходящие группы. [“Сопряженная кислота всегда является лучшей уходящей группой”]
- Кислота ускоряет реакции присоединения , протонируя карбонильный кислород, тем самым делая карбонильный углерод лучшим электрофилом.

Вот общий пример образования имина, показывающий образующиеся и разрывающиеся связи.
Как вы с готовностью можете увидеть,
- Две новые связи C-N и две связи O-H сформированы , а
- Две C-O и две связи N-H – разбиты .
Еще одно замечание. Исходные вещества (альдегид/кетон и первичный амин) и продукты (имин и вода) находятся в равновесии .
Как мы могли бы направить реакцию на желаемый иминовый продукт?
Как можно было бы предположить, применяя принцип Ле Шателье, это поможет удалить воду по мере образования имина , чтобы предотвратить возникновение обратной реакции. ( На практике это часто делается с помощью осушителя, такого как MgSO 4 или молекулярных сит, или путем отделения воды с помощью ловушки Дина-Старка.)
3.
 Механизм
МеханизмЭто приводит нас к следующий большой вопрос. Как работает эта реакция?
Какие механистические стадии могут происходить на пути образования имина из альдегида или кетона?
Прежде чем я «испорчу» его, показав, что было определено экспериментально, было бы забавным упражнением сделать прогноз. Так что я призываю вас принять удар для себя. Некоторые вещи, которые следует иметь в виду:
- Любой предполагаемый механизм этой реакции должен учитывать разрыв из двух связей C-O и двух связей N-H , а также образование двух связей C-N и связей O-H .
- Напомним, что карбонильный углерод альдегидов и кетонов является отличным электрофилом и может подвергаться реакциям присоединения с хорошими нуклеофилами. (Подсказка: амины являются нуклеофилами).
- Для наших целей предположим, что в реакции используется кислотный катализатор.
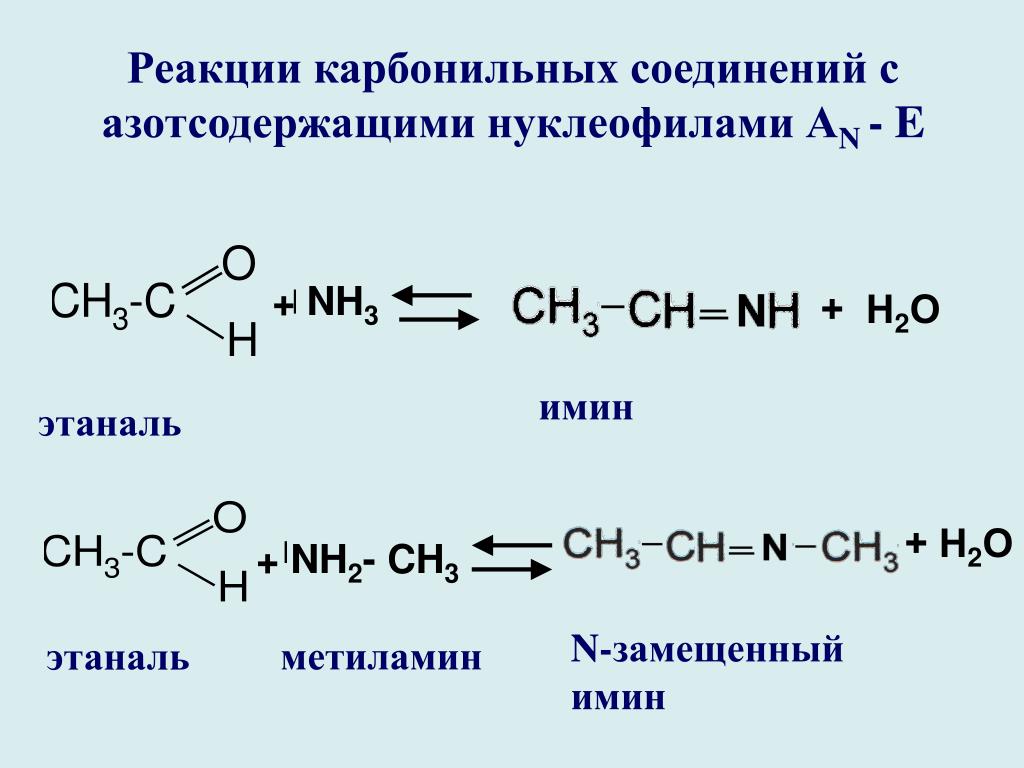 Вспомним, что кислота превращает связи С=О в лучшие электрофилы и что кислота, сопряженная с любым основанием, является лучшей уходящей группой.
Вспомним, что кислота превращает связи С=О в лучшие электрофилы и что кислота, сопряженная с любым основанием, является лучшей уходящей группой.
Как вы думаете, что происходит?
Давайте углубимся.
В присутствии слабой кислоты будет существовать равновесие между нейтральным альдегидом/кетоном и сопряженной кислотой альдегида/кетона, поэтому шаг 1 показан как протонирование кислорода ( форма О-Н). [ Примечание 3 ]
После протонирования карбонил может подвергаться присоединению аминового нуклеофила к электрофильному карбонильному углероду, образуя CN и разрывая СО (pi).
Гибридизация углерода изменилась с sp 2 на sp 3 . Теперь у нас есть тетраэдрический промежуточный продукт с нейтральным ОН и положительно заряженным амином (то есть аммонием). [ Примечание 4]
Что дальше?
- Нам еще предстоит образовать O-H и C-N (пи), и нам еще нужно разорвать связи C-O и две связи N-H.

- Отщепление в этот момент маловероятно, потому что у азота нет доступной неподеленной пары, с которой можно было бы образовать C-N (pi), а уходящей группой будет гидроксид-ион HO(-), относительно сильное основание.
Было бы очень здорово иметь возможность перевести протон из азота (перерыв N-H) в кислород (O-H)!
Депротонирование (Этап 3, разрыв N-H) азота основанием (например, избыток амина, хотя можно просто написать B: так как многие другие виды могут это сделать) с последующим протонированием (Этап 4, форма O-H) кислорода кислотой достигает этого.
Осторожно – обычно ошибочно показывать, как это происходит за один шаг, используя OH для депротонирования N-H. Более корректно показывать двухэтапный процесс.
Вместе эти две стадии вызывают сдвиг протона (H+) от азота к кислороду. По этой причине процесс депротонирования-протонирования (или его обратный) обычно называют переносом протона .
Протонирование OH с получением OH 2 (+) привело к получению намного лучшей уходящей группы .
Наш контрольный список связей для образования и разрыва по-прежнему требует образования C-N (pi) и разрыва C-O. Теперь это можно сделать через элиминация воды с сопутствующим образованием C-N (pi) (Стадия 5, форма C-N, разрыв C-O)/
В отсутствие кислоты элиминация является определяющей стадией образования большинства иминов; добавление кислоты значительно ускоряет скорость этой стадии. [ Примечание 5 ]
Еще одно примечание: если присутствует кислота, важно указать уходящую группу как H 2 O, а не HO-, поскольку HO- является сильным основанием и не будет существовать в наличие сильной кислоты.
В результате элиминирования образуется конъюгированная кислота имина, именуемая солью иминия (или ионом иминия). D эпротонирование положительно заряженного азота (этап 6, перерыв N-H) дает нам нейтральный имин .
Объединив эти шаги, мы получим Протонирование- Добавление – Депротонирование – Протонирование – Удаление – Депротонирование или P ADPED. (Запомните эту мнемонику, потому что она часто встречается!)
4. Внутримолекулярное образование иминаВполне возможно, что амин и альдегид/кетон присутствуют в одной и той же молекуле, присоединенной через углеродную цепь. Образование циклического имина особенно вероятно, если может образоваться пяти- или шестичленное кольцо.
Точно такая же последовательность стадий, как и в межмолекулярном случае, просто так получилось, что амин и альдегид связаны через углеродную цепь; вот пример.
Чтобы найти механизм, наведите курсор сюда или нажмите на эту ссылку.
5. Реакции иминов
Для наших целей, вероятно, наиболее важной реакцией иминов является гидролиз , где обработка имина водой (обычно водной кислотой) восстанавливает исходный альдегид/кетон и первичный амин.
Как и следовало ожидать, образование имина происходит в обратном порядке: две связи C-O (и две связи N-H) образуются, а две связи C-N (и две связи O-H) разрываются.
Водная кислота (H 3 O + ) обычно используется для установления равновесия в сторону гидролиза. В этих условиях механизм гидролиза с использованием водной кислоты составляет P Ротонация – A DDITION – D EPROTONATION – P ROTONATION – E Ограничение – D EPROTONAT не опечатка!
Гидролиз иминов имеет точно такую же последовательность стадий как образование иминов, за исключением того, что идентичность нуклеофила, электрофила и уходящей группы меняется местами.
Наведите здесь, чтобы увидеть механизм, или нажмите на эту ссылку.
Имины способны вступать в реакции присоединения так же, как альдегиды и кетоны.
Одной из важных реакций иминов является восстановление с источником гидрида (H-) с получением аминов. Особое значение имеет процесс, известный как восстановительное аминирование , при котором альдегид или кетон объединяют с первичным амином и восстанавливающим агентом, что приводит к прямому образованию аминов. [ Примечание 6]
Особое значение имеет процесс, известный как восстановительное аминирование , при котором альдегид или кетон объединяют с первичным амином и восстанавливающим агентом, что приводит к прямому образованию аминов. [ Примечание 6]
6. Свойства иминов
Рассмотрев реакции образования (и разрушения) иминов, мы переходим к самому интересному. Продумывая периодические тренды!
Как вы думаете, чем свойства иминов могут отличаться от свойств альдегидов/кетонов? Каков может быть эффект удаления кислорода и замены его атомом, находящимся непосредственно слева от него в периодической таблице?
Давайте начнем с простого вопроса. Какая функциональная группа имеет больший дипольный момент – имин или кетон?
Учитывая более высокую электроотрицательность кислорода, это не должно удивлять.
Давайте думать в другом направлении. Как вы думаете, что может быть более основным : альдегид или имин ?
Вспомним, что основность увеличивается по мере продвижения влево по периодической таблице; электроны менее прочно удерживаются (электроотрицательность уменьшается) и, следовательно, легче отдаются электрофилам.
Имины значительно более просты. ПК a типичного иминия (протонированного имина) составляет около 4 или 5. pK a протонированного альдегида составляет около –7 [ссылка].
Поскольку «чем сильнее кислота, тем слабее сопряженное основание», это делает имины примерно на 11 или 12 pK a единиц (= 12 порядков, 10 12 ) более щелочными!
Третий вопрос.
Как вы думаете, что более электрофильно (т.е. более реакционноспособно по отношению к нуклеофилам): альдегиды или имины?
При прочих равных следует ожидать альдегиды/кетоны более электрофильны, чем их иминовые аналоги.
- Кислород более электроотрицателен, чем азот , поэтому больший дипольный момент должен приводить к большему частичному положительному заряду углерода, что делает его более электрофильным.
- Тот же аргумент, но наоборот: N является лучшим донором электронов, чем O, что сделает присоединенный углерод более богатым электронами и, следовательно, менее электрофильным.

- Также стоит подумать о «второстепенных» формах резонанса как для альдегида, так и для имина, которые так часто определяют их реакционную способность. Может быть полезно думать о «более высокой основности» как о замене «более нестабильного» и, следовательно, «менее вероятного вклада в резонансный гибрид». С альдегидом у нас есть O (-) (сопряженное основание спирта, pK a около 16 ) справа, тогда как с имином RN (-) находится справа (сопряженное основание амина, pK a около 38).
Вот бонусный вопрос, который я оставлю в сносках: Как вы думаете, что более электрофильно (т.е. реактивно по отношению к нуклеофилам) – имин, или протонированный имин («иминий»). [ Примечание 8 ]
7. Двоюродные братья иминов: оксимы и гидразоны
Говоря об иминах, стоит отметить, что у этих функциональных групп есть «двоюродные братья», которые появляются эпизодически во вводных курсах и поэтому не должны быть оставленным.
Оксимы и гидразоны образуются из альдегидов/кетонов по механизму, сходному с механизмом образования иминов.
- Оксимы образуются посредством обработки альдегидов или кетонов с гидроксиламином (NH 2 OH), тогда как гидразоны образуются посредством обработки альдегидов/кетонов с гидризонами 2
- 8 2
- 8 2
- 8 2
- 8. Как и в случае с другими иминами, кислотный катализ ускоряет реакцию (особенно стадию отщепления).
- Оксимы являются субстратами перегруппировки Бекмана, очень важными в производстве нейлона [ Примечание 9 ]
- Гидразоны используются в реакции Вольфа-Кишнера, которая восстанавливает связь C=O до CH 2 .
Механизм образования оксимов и гидразонов точно такой же, как и образования иминов.
Если присутствует кислота, механизм P ротация- A добавление- D эпротонирование- P ротация- E лиминация- D эпротонация ( P ADPED ).
Наведите курсор здесь, чтобы открыть оксимовый механизм. или нажмите на эту ссылку.
Наведите указатель мыши здесь, чтобы увидеть механизм гидразона, или нажмите на эту ссылку.
Часто встречаются на лабораторных курсах. ДНФГ (2,4-динитрофенилгидразин) и семикарбазидные производные альдегидов и кетонов часто дают высококристаллические, ярко окрашенные осадки гидразона с резкими температурами плавления. [ Примечание 10]
8. Почему вторичные амины используются для получения иминов?
Выше мы упомянули, что имин получают путем обработки альдегида или кетона первичным амином .
Почему только первичные амины? Почему мы не можем вместо этого использовать вторичный амин ?
Обработка альдегида или кетона вторичным амином приводит к иминиевой соли , которая может или не может (в зависимости от ее структуры, см. ниже) вступать в дальнейшую реакцию с образованием енамин .
Почему?
Стоит пройтись подробно, потому что добавление вторичных аминов напоминает добавление первичных аминов – до самого конца.
Пройдемся по механизму.
Предполагая, что кислота присутствует, первой стадией будет протонирование карбонильного кислорода (с образованием O–H), за которым следует присоединение неподеленной пары амина к карбонильному углероду, (форма C-N, разрыв C-O (pi) ) .
Далее идет этап переноса протона. Депротонирование N (разрыв N-H) с последующим Протонирование O (форма O-H) дает нам превосходную уходящую группу R-OH 2 (+)
С водой в качестве уходящей группы, теперь гораздо более вероятно, что это приведет к образованию CN (пи) и разрыву СО.
Это дает нам положительно заряженную соль иминия, показанную ниже.
Если мы следим за P ADPED , следующим шагом должно быть D эпротонирование, верно? Вот в чем проблема.
Азот уже связан с тремя атомами углерода. Нет протона, который можно было бы оторвать от азота!
В случае такой молекулы, как формальдегид (и другие «неенолизируемые» альдегиды/кетоны, в которых отсутствует протон на альфа-углероде), здесь все заканчивается . В качестве конечного продукта мы получаем иминиевую соль. [ Примечание 11 ]
Однако если на альфа-углероде иминия есть протон (т.
Депротонирование (брейк C-H, форма C-C (pi), брейк C-N (pi) дает нам следующие виды: комбинация ложки и вилки дает нам лопатку , обычай требует, чтобы это называлось enamine (имя, впервые придуманное лауреатом Нобелевской премии Джорджем Виттигом еще в 1927 году).
Если вы ведете счет, это по-прежнему P A D P E D для образования енамина. Однако на этот раз эпротонирование D происходит на альфа-углероде.
Енамины являются отличными нуклеофилами и подвергаются совершенно другому набору реакций. Наверное, лучше на этом остановиться и разобраться с ними в отдельной статье.
Просто чтобы дать вам представление, вот пример образования енамина от Organic Syntheses.
Ссылка: Органические синтезы , 1968 , 48 , 556.
9. Заключение
Итак, что мы узнали об иминах?
- Имины являются азотсодержащими родственниками альдегидов и кетонов
- Они образуются при обработке альдегида или кетона первичным амином . Кислота помогает катализировать реакцию.
- Механизм образования в слегка кислотных условиях составляет P Ротонация- A DDITION- D EPROTONATION- P ROTONATION- E ограничение- D Eprotonation, OR P A D. D. , или P A D.
 D.
D. - Если альдегид/кетон и первичный амин находятся в одной и той же молекуле, может произойти образование внутримолекулярного имина, что даст циклический имин.
- Имины могут быть гидролизованы обратно в исходный альдегид/кетон с помощью H 2 O (на практике обычно водная кислота H 3 O+), снова через P A D P E D .
- Имины также могут восстанавливаться источником гидрида (H – ) с получением аминов . Сочетание образования имина с восстановлением называется восстановительным аминированием .
- Имины более основные , чем альдегиды/кетоны, и обычно менее реакционноспособны по отношению к нуклеофилам.
- Оксимы и 9Гидразоны 0003 являются химическими родственниками иминов, которые образуются по тому же механизму.
- Обработка альдегидов/кетонов вторичными аминами приводит к получению иминиевых солей, которые могут подвергаться дальнейшему депротонированию (например, по альфа-углероду) с образованием енаминов .
 Механизм образования енаминов также P A D P E D .
Механизм образования енаминов также P A D P E D .
Вот потенциально полезная цифра, обобщающая механизмы прямой и обратной реакции:
Мы углубимся в химию енаминов в следующей статье этой серии, здесь .
Примечания
Примечание 1- Термин « основание Шиффа » часто ограничивается иминами, полученными из ароматических альдегидов (например, бензальдегида), которые значительно более устойчивы к гидролизу (и, следовательно, их легче выделить), чем те, из алкильных («алифатических») альдегидов. Более редко встречающийся термин « анил » относится к иминам, полученным путем конденсации ароматических аминов (например, анилина) с альдегидами. Как ни странно, термин « азометин » также находит применение для иминов, особенно в старой литературе.
Примечание 2 – Кислота не является строго необходимой для образования имина, особенно для алкиламинов (и других нуклеофильных аминов, таких как гидроксиламин/гидразин), где константы равновесия >200 были измерены в водном растворе [Ссылка]. Для целей этой статьи мы будем предполагать умеренно кислые условия, хотя в других частях курса (например, образование гидразона в реакции Вольфа-Кишнера) вы можете наблюдать реакции конденсации с образованием C=N в нейтральных или даже щелочных условиях.
Для целей этой статьи мы будем предполагать умеренно кислые условия, хотя в других частях курса (например, образование гидразона в реакции Вольфа-Кишнера) вы можете наблюдать реакции конденсации с образованием C=N в нейтральных или даже щелочных условиях.
Примечание 3 – Для алкиламинов протонирование альдегида не требуется для того, чтобы произошло присоединение, а удаление воды является определяющим фактором. Для слабонуклеофильных аминов (например, PhNH 2 и других аминов с pK a H, равным 3–5) скорость определяется прибавлением, и для того, чтобы присоединение происходило с разумной скоростью, необходимо протонирование карбонильного кислорода [см. Anslyn & Догерти, 2006, с. 597 для дальнейшего обсуждения]. Мы верим, что в большинстве вводных курсов не проводится строгого различия между этими двумя случаями, поэтому показано «сначала протонирование».
Примечание 4 – По аналогии с «полуацеталем» нейтральные частицы, которые могут образовываться в результате присоединения амина к альдегиду или кетону, известны как «полуаминаль» или карбиноламин.
Примечание 5 – Образование иминов сильно зависит от pH, при этом типичный максимум возникает при pH 4–5 [например, Ссылка]. Когда реакции контролируются с помощью УФ, обычно наблюдается быстрое исчезновение поглощения C=O (т.е. быстрое добавление), за которым следует очень медленное появление поглощения C=N. Это означает, что устранение является определяющим фактором.
Что еще интересно, скорость начинает падать, когда рН становится ниже 4. Как вы думаете, почему это может быть?
Примечание 6 – Восстановительное аминирование – это процесс, посредством которого альдегиды/кетоны превращаются в имины и затем восстанавливаются без выделения промежуточного имина. Классический метод для проведения этого заключается в использовании восстановителя цианборгидрида натрия (NaCNBH 3 ) при слегка кислом pH (6 или около того). В этих условиях альдегид/кетон восстанавливается очень медленно, тогда как иминий (сопряженная кислота имина) восстанавливается плавно.
Подумайте об этом. Это означает, что соли иминия более активны по отношению к нуклеофилам, чем нейтральные альдегиды!
Примечание 7 – При прочих равных условиях альдегиды на более электрофильны, чем (альды) имины, , а кетоны более электрофильны, чем (кет)имины.
Примечание 8 – Что более электрофильно – иминий (протонированный имин) или имин?
Нейтральные резонансные формы гораздо важнее (т.е. вносят больший вклад в резонансный гибрид), чем заряженные резонансные формы. Вклад формы иминного резонанса, несущей два точечных заряда, будет очень мал по сравнению с вкладом формы нейтрального резонанса.
Сравните это с иминиумом, где обе наиболее важные формы резонанса имеют один точечный заряд. В то время как резонансная форма, в которой углерод имеет полный октет, будет более важной, правосторонняя резонансная форма (карбокатион) будет вносить гораздо больший вклад, чем в случае нейтрального имина.
Примечание 9 – Циклогексанон превращается в оксим циклогексанона, который подвергается перегруппировке Бекмана при обработке сильной кислотой с образованием капролактама. Ежегодно для производства нейлона-6 производится около 5 миллионов тонн капролактама.
Почему название капролактам? Шестиуглеродная карбоновая кислота Ch4Ch3Ch3Ch3Ch3CO2H называется капроновой кислотой по имени запаха коз (особенно вонючие старые козы). Эфиры карбоновых кислот называются капроатами; соответствующий циклический эфир (лактон) называется капролактоном. Циклические амиды называются лактамами. Таким образом, капролактам представляет собой циклический амид, полученный из капроновой кислоты.
Примечание 10 – Гидразины 2,4-динитрофенилгидразин (ДНФГ) и семикарбазид являются классическими реагентами для определения наличия альдегидов/кетонов в неизвестном образце. Это все еще делается в учебных лабораториях (и при окраске методом ТСХ). До появления спектрометрии точки плавления были одним из немногих доступных инструментов для определения характеристик. Превращение жидких кетонов/альдегидов в высококристаллические производные ДНФГ или семикарбазона было полезным диагностическим инструментом.
До появления спектрометрии точки плавления были одним из немногих доступных инструментов для определения характеристик. Превращение жидких кетонов/альдегидов в высококристаллические производные ДНФГ или семикарбазона было полезным диагностическим инструментом.
Примечание 11 – Соли иминия могут быть достаточно стабильными, чтобы их можно было разливать по бутылкам и продавать в коммерческих целях. Приведенная ниже иминиевая соль в просторечии известна как соль Эшенмозера. Он реагирует как электрофил с енолами в реакциях Манниха.
Проверьте себя! Ссылки и дополнительная литература63 , 63 , 489-510DOI: 10.1021/cr60225a003
Хороший обзор ключевых свойств, реакций и синтезов иминов, от первого выделения имина Шиффом в 1864 г. до
г. Некоторые основные моменты из вводного раздела:
– Характерная ИК-частота для C=N находится в диапазоне 1650-1670 см -1 , в отличие от 1600-1650 см -1 у алкенов и 1710-1750 см -1 у алкенов.
 C = O
C = O – Среднее расстояние C = N составляет около 1,24 Å для кетиминов по сравнению со средним расстоянием C = O около 1,21 Å для кетонов
– Если не соблюдать осторожность, первичные алифатические альдегиды могут легко давать полимерные материалы с аминами из-за легкости альдольных конденсаций. Тенденция снижается по мере увеличения стерических затруднений альдегида/амина.
-Ароматические альдегиды легко и количественно реагируют с аминами с образованием соответствующих иминов даже при комнатной температуре.
– Для кетонов требуется более длительное время реакции, чем для альдегидов; Кислотные катализаторы полезны, а удаление воды определенно необходимо. Ароматические кетоны реагируют с аминами еще медленнее, чем алифатические кетоны.
– Альдимины имеют более низкий измеренный дипольный момент (1,4 Д), чем кетоны (2,5 Д). [Ссылка]
Mittheilungen aus dem Universitätslaboratorium в Пизе: Eine neue Reihe organischer Basen
Schiff, H. Ann. 1864 , 131, 118.
Ann. 1864 , 131, 118.
DOI: dx.doi.org/10.1002/jlac.18641310113
Первое сообщение об имине, Хьюго Шифф.
ДУГЛАС Г. НОРТОН, ВЕРНОН Э. ХОРИ, ФРАНК К. ДЭВИС, ЛЛОЙД Дж. МИТЧЕЛЛ и СИВЕР А. БАЛЛАРД
J. Org. Chem., 1954, 19 (7), 1054-1066
DOI: 10.1021/jo01372a010
. удалить воду (например, используя ловушку Дина-Старка и азеотропную перегонку воды с бензолом или толуолом).
W. P. Jencks
J. Am. хим. соц. 1959 , 81 , 475-481
DOI: 10.1021/ja01511a053
Классическое исследование зависимости рН от образования оксима/семикарбазона около рН 4,5. Предлагается, чтобы определяющей скорость стадией была потеря воды (этап удаления), а не протонирование карбонильного кислорода.

Brian E. Love and Jianhua Ren
The Journal of Organic Chemistry 1993, 58 (20), 5556-5557
DOI: 1021/jo00072a051
A удобный синтез пространственно затрудненных иминов с использованием тетраэтилортосиликата (Si(OEt) 4 ) в качестве дегидратирующего агента, так как он образует некислотный побочный продукт.
RF Borch, M.D. Bernstein и H. Dupont Durst
J. Am. хим. соц. 1971 , 93 , 2897-2904
doi: 10.1021/ja00741a013
Первое подробное исследование об общем исследовании общего числа. Показывает, что NaCNBH 3 является плохим восстановителем для типичных альдегидов и кетонов при pH 6, но быстро восстанавливает имины, образованные из этих предшественников в тех же условиях.

Образование енамина:
Georg Wittig, Hermann Blumenthal
Ber. 1927 , 60 (5), 1085-1094
doi: 10.1002/cber.1
Нобелевский лауреат профессор. 2,2-(ТРИМЕТИЛЕНДИТИО)ЦИКЛОГЕКСАНОН
Р. Б. Вудворд, И. Дж. Пахтер и М. Л. Шейнбаум
Орг. Синтез. 1974, 54 , 39
DOI: 10.15227/orgsyn.054.0039
Первый шаг в этой процедуре, представленной химиком-органиком профессором Робертом Бернсом Вудвордом (Гарвардский университет), представляет собой синтез енамина.
D. Burpitt and J.G. Thweatt
Org. Синтез. 1968, 48 , 56
DOI: 10.15227/orgsyn.048.0056
Первый шаг в этой процедуре из Organic Syntheses представляет собой синтез енамина.

Брайан Капон и Чжэнь Пин Ву
: 1021/jo00295a017
Исследование стабильности различных енаминов в растворе.
Анжю. Хими. Междунар. Эд. англ. 10 1971 330-331
J. Schrieber, H. Maag, N. Hashimoto, A. Eschenmoser
DOI: 10.1002/ani.197103301
Первый отчет о полезных реакциях с эссенмозолами и энмозолами еноляты.
Один вопрос, на который я хотел бы получить ответ и указать в литературе – энергетика имин-енаминной таутомерии.
10.6: Имины – Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 106355
- Тим Содерберг
- Университет Миннесоты Моррис
Электрофильный атом углерода альдегидов и кетонов может быть мишенью нуклеофильной атаки аминов, а также спиртов. Конечным результатом атаки аминового нуклеофила является функциональная группа, в которой двойная связь C=O заменена двойной связью C=N, известная как имин. (Эквивалентный термин — «основание Шиффа», но в этой книге мы будем использовать термин «имин»). Напомним из раздела 7.5B, что имины имеют pKa примерно 7, поэтому при физиологическом pH они могут быть точно определены либо как протонированные (иминиевая ионная форма), либо как нейтральные (имин).
Конечным результатом атаки аминового нуклеофила является функциональная группа, в которой двойная связь C=O заменена двойной связью C=N, известная как имин. (Эквивалентный термин — «основание Шиффа», но в этой книге мы будем использовать термин «имин»). Напомним из раздела 7.5B, что имины имеют pKa примерно 7, поэтому при физиологическом pH они могут быть точно определены либо как протонированные (иминиевая ионная форма), либо как нейтральные (имин).
Иминиум образование ионов:
Механизм (ферментативный):
Механически образование имина включает две стадии. Во-первых, азот амина атакует карбонильный углерод на стадии нуклеофильного присоединения (стадия 1), которая очень похожа на образование полуацеталей и полукеталей. Основываясь на ваших знаниях о механизме образования ацеталей и кеталей, вы могли бы ожидать, что следующим шагом будет атака второго амина с образованием соединения с углеродом, связанным с двумя аминогруппами — азотной версией кеталя или ацеталя. Вместо этого то, что происходит дальше (шаг 2 выше), заключается в том, что электроны неподеленной пары азота «отталкивают» кислород от углерода, образуя двойную связь \(C=N\) (иминиум) и смещенную молекулу воды.
Вместо этого то, что происходит дальше (шаг 2 выше), заключается в том, что электроны неподеленной пары азота «отталкивают» кислород от углерода, образуя двойную связь \(C=N\) (иминиум) и смещенную молекулу воды.
Превращение иминия обратно в альдегид или кетон представляет собой гидролитический процесс (связи разрываются молекулой воды), и механически это просто обратный процесс образования иминия:
Гидролиз иониевого иона:
Механизм (ферментативный):
Ферменты, образующие углерод-углеродные связи, называемые альдолазами (которые мы подробно рассмотрим в главе 12), часто образуют иминиевые связи между карбонильным углеродом на субстрате и остатком лизина в активном центре фермента, как в этой альдолазной реакции из цикл Кальвина:
После завершения углерод-углеродной связи, образующей часть альдолазной реакции, иминиевая связь гидролизуется, высвобождая продукт, так что он может диффундировать из активного центра и позволить начать другой каталитический цикл.
В главе 17 мы узнаем о реакциях, которые зависят от кофермента, называемого пиридоксальфосфатом (\(PLP\)), также известного как витамин \(B6\). В этих реакциях альдегидный углерод \(PLP\) соединяется с ферментативным лизином в активном центре:
Затем \(PLP\)-лизиниминная связь заменяется иминной связью между \(PLP\) и аминогруппой на субстрате, что можно назвать трансиминированием.
Механизм трансиминирования очень похож на механизм образования имина:
Реакция трансформации:
Механизм:
Упражнение 10.6.1
Изобразите имин, который может образоваться между каждой парой соединений.
а.
б.
в.
Упражнение 10.6.2
Нарисуйте продукт гидролиза имминия для каждого из следующих соединений.
- Ответить
Добавьте сюда текст ответа, и он будет автоматически скрыт, если на странице активен шаблон “AutoNum”.

Упражнение 10.6.3
- Показанный ниже промежуточный продукт метаболизма подвергается внутримолекулярному образованию имина в качестве стадии биосинтеза лизина (EC 4.3.3.7). Нарисуйте продукт этой стадии образования внутримолекулярного имина.
- Предскажите продукт этой стадии гидролиза иминия (EC 2.3.1.117) по пути деградации пролина.
Эта страница под названием 10.6: Imines распространяется под лицензией CC BY-NC-SA 4.0 и была создана, изменена и/или курирована Тимом Содербергом с использованием исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Автор
- Тим Содерберг
- Лицензия
- СС BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.

- Метки
- фермент
- Имин
- механизм
- источник@https://digitalcommons.morris.umn.edu/chem_facpubs/1/
- Трансмиссионная реакция
21.4. Образование имина | Органическая химия II
Цели
После завершения этого раздела вы должны уметь
- писать уравнения для описания реакций, происходящих между альдегидами или кетонами и первичными или вторичными аминами.
- идентифицирует продукт, образованный в результате реакции данного альдегида или кетона с данным первичным или вторичным амином.
- идентифицируют альдегид или кетон, амин или и то, и другое, необходимые для синтеза данного имина или енамина.

- напишите подробный механизм реакции альдегида или кетона с первичным амином.
- напишите подробный механизм реакции альдегида или кетона со вторичным амином.
Ключевые термины
Убедитесь, что вы можете определить и использовать в контексте приведенные ниже ключевые термины.
- 2,4‑динитрофенилгидразон
- енамин
- имин
Study Notes
Имин представляет собой соединение, содержащее структурную единицу
Енамин представляет собой соединение, содержащее структурную единицу
. Оба этих типа соединений могут быть получены реакцией альдегида или кетона с амином.
У вас может быть возможность наблюдать за реакцией альдегида и кетона с 2,4-динитрофенилгидразином (реактив Брэди) с образованием 2,4-динитрофенилгидрозоны в лаборатории. Это классический тест органической химии для подтверждения наличия карбонильной группы. В результате реакции образуются очень красочные и яркие осадки желтого, оранжевого и красного цвета.
Если вы понимаете, почему две реакции образования имина и енамина по существу идентичны, и можете написать подробный механизм каждой из них, вы уже на пути к освоению органической химии. Если вы понимаете, как и почему происходят эти реакции, вы можете свести к минимуму объем материала, который вам необходимо запомнить.
Реакция с первичными аминами с образованием иминов
Реакция альдегидов и кетонов с аммиаком или 1º-аминами приводит к образованию производных имина, также известных как основания Шиффа (соединения, имеющие функцию C=N). Вода удаляется в реакции, катализируемой кислотой и обратимой в том же смысле, что и образование ацеталя. Необходимо тщательно контролировать рН для реакций, в которых образуются иминовые соединения. Скорость, с которой образуются эти иминовые соединения, обычно максимальна при рН 5 и падает при более высоких и более низких значениях рН. При высоком pH не будет достаточно кислоты для протонирования ОН в промежуточном продукте, чтобы можно было удалить его в виде H 2 O. При низком pH большая часть аминового реагента будет связана в виде его конъюгированной с аммонием кислоты и станет ненуклеофильной.
При низком pH большая часть аминового реагента будет связана в виде его конъюгированной с аммонием кислоты и станет ненуклеофильной.
Преобразование реагентов в продукты просто
Примеры реакций формирования имин
Механизм образования иминов
1) Я нуклеофильная добавление
2) Перевод протона
3) Проонания OH
40002 2). (элиминация нуклеофила)
5) Депротонирование
Обратимость реакций образования имина
Имины могут гидролизоваться обратно в соответствующий первичный амин в кислых условиях.
Реакции с участием других реагентов типа Y-NH
2 Имины иногда трудно выделить и очистить из-за их чувствительности к гидролизу. Следовательно, были изучены другие реагенты типа Y–NH 2 , и было обнаружено, что они дают стабильные продукты (R 2 C=N–Y), полезные для характеристики альдегидов и кетонов, из которых они получены. Некоторые из этих реагентов перечислены в следующей таблице вместе со структурой и названиями продуктов их карбонильной реакции. Гидразоны используются как часть восстановления Вольфа-Кишнера и будут обсуждаться более подробно в разделе 21.6.
Гидразоны используются как часть восстановления Вольфа-Кишнера и будут обсуждаться более подробно в разделе 21.6.
За исключением незамещенных гидразонов, эти производные легко получают и часто представляют собой кристаллические твердые вещества, даже если исходный альдегид или кетон являются жидкими. Поскольку точки плавления можно определить быстрее и точнее, чем точки кипения, подобные производные полезны для сравнения и идентификации карбонильных соединений. Следует отметить, что хотя семикарбазид имеет две аминогруппы (-NH 2 ), только одна из них является реакционноспособным амином. Другой является амидоподобным и дезактивируется соседней карбонильной группой.
Упражнения
1)Нарисуйте продукты следующих реакций.
2) Нарисуйте структуру реагента, необходимого для получения указанного продукта.
3) Нарисуйте продукты следующих реакций.
Ответы
Показать ответ
Авторы
Проф. Стивен Фармер (Университет штата Сонома)
Стивен Фармер (Университет штата Сонома)
Уильям Ройш, почетный профессор (Университет штата Мичиган), Виртуальный учебник органической химии
Реакция с вторичными аминами с образованием енаминов
Большинство альдегидов и кетонов реагируют с 2º-аминами с образованием продуктов, известных как енаминов . Следует отметить, что, как и образование ацеталей, это катализируемые кислотой обратимые реакции с потерей воды. Следовательно, енамины легко превращаются обратно в их карбонильные предшественники путем гидролиза, катализируемого кислотой.
Механизм
1) Нуклеофильное присоединение
2) Перенос протона
3) Протонирование OH
4) Удаление воды (элиминация нуклеофилов)
5) ДеПротонация
Обратимость эмаминов
Упражнения
1). Пожалуйста, нарисуйте продукты.
2) Укажите структуру реагента, необходимого для получения следующего продукта
Ответы
Показать ответ
Авторы
- Д-р Дитмар Кеннеполь FCIC (профессор химии, Университет Атабаски)
- Проф.
 Стивен Фармер (Государственный университет Сономы)
Стивен Фармер (Государственный университет Сономы)
Динамическая иминная химия. | Semantic Scholar
- DOI: 10.1039/c2cs15305j
- Идентификатор корпуса: 205815103
@article{Belowich3012DynamicIC,
title={Динамическая иминовая химия.},
автор = {Мэттью Э. Белович и Дж. Фрейзер Стоддарт},
journal={обзоры химического общества},
год = {2012},
объем={41 6},
страницы={
2003-24
}
} - M. Belowich, J. F. Stoddart
- Опубликовано 27 февраля 2012 г.
- Chemistry
- Обзоры Chemical Society
что образование кинетически конкурентоспособных промежуточных продуктов со временем заменяется термодинамически наиболее стабильным продуктом (продуктами). По этой фундаментальной причине иминная связь оказалась необычайно разнообразной и полезной в руках химиков-синтетиков. Образование иминной связи — одна из немногих реакций, определяющих известную дисциплину…
Образование иминной связи — одна из немногих реакций, определяющих известную дисциплину…
Просмотр на PubMed
doi.org
Динамическая химия имины
- М. ниже, J. F. Stoddart
Химия
- 2012
Формация ИМИНА – ФЛЕКТИЯ – FROM AMININE и ALDE. реакция, протекающая под термодинамическим контролем, так что образование кинетически конкурентных промежуточных соединений происходит в…
Кинетическая селективность и термодинамические особенности конкурентного образования иминов в динамической ковалентной химии.
- Sirinan Kulchat, M. Chaur, J. Lehn
Chemistry
Chemistry
- 2017
Полученные в результате этих экспериментов данные о селективности образования моноаминов дериватизируют смеси, а также полифункциональные соединения, содержащие различные типы аминогрупп.
Индуцированная деформацией реактивность в динамической ковалентной химии макроциклических иминов.

- Lars Ratjen, G. Vantomme, J. Lehn
Химия
Химия
- 2015
Стабилизация высокоэнергетических молекулярных форм путем координации ионов металлов с последующим удалением последних предлагает общую процедуру неравновесные молекулярные состояния, судьба которых затем может быть исследована, в частности, в сочетании с динамическими ковалентными химическими процессами.
Количественные шкалы реактивности для динамической ковалентной и системной химии.
Впервые разработаны количественные шкалы реактивности, способные коррелировать и предсказывать равновесие динамических ковалентных реакций (ДКР), основанные на универсальных ДКР между иминами, одним из наиболее используемых структурных мотивов в ДКК, и рядом O- и S-мононуклеофилы.
Универсальный подход к формированию динамической амидной связи с иминными нуклеофилами.
- Х. Эргувен, Эван Н.
 Кейзер, Б. Арндтсен
Кейзер, Б. Арндтсен Химия, биология
Химия
- 2020
В этой работе описывается метод образования стабильных и широко используемых амидных связей путем использования обратимого сочетания иминов и ацилхлоридов, который предлагает подход к созданию широкого семейства амидных продуктов под термодинамическим контролем, включая селективное образование амидных макроциклов или полимеров.
Динамическое нуклеофильное ароматическое замещение тетразинов
- Т. Сантос, Дэвид С. Риверо, Ромен Каррильо
Химия
Angewandte Chemie
- 2021
Высокий потенциал этой методологии был доказан путем построения двух реагирующих надмолекулярных систем: макроцикла, демонстрирующего индуцированное светом высвобождение ацетилхолина; и усеченную [4 + 6] тетраэдрическую флуоресцентную клетку, сохраняющую форму, которая разбирается тиолами, если только она не пост-стабилизирована IEDDA.
Почти количественный синтез макроциклов мочевины с помощью объемного N-заместителя
Использование динамической затрудненной мочевинной связи (HUB) для построения макроциклов мочевины с очень высокой эффективностью, а объемный N-трет-бутил может быть легко удален кислотой для устранения динамичности HUB и стабилизации структур макроцикла.
Энантиоселективные реакции динамического обмена иминов.
Реакции энантиоселективного обмена аминов были продемонстрированы в качестве первого примера посредством реакции энантиомерных хиральных аминов, таких как природные аминокислоты, с рядом инновационных аксиально-хиральных иминов на основе 1,1′-бинафтил-2,2′-диамина, которые были получены из реакций конденсации между BNDA и салициловым альдегидом или его производными.
Контролируемый молекулярный брак в ковалентных клетках, управляемый водородными связями.
- Koushik Acharyya, P.
 Mukherjee
Mukherjee Химия
Химия
- 2014
Супрамолекулярный подход, основанный на исключительной невалентности
. обсуждаются органические клетки и приводится пример нетрадиционного метатезиса иминной связи при трансформации органических клеток в клетки.
Динамическая ковалентная химия, основанная на реакционной способности: обратимое связывание и различение моноспиртов по хиральности.
Генерируемые in situ простые общие иминиевые ионы были использованы для динамического ковалентного связывания моноспиртов с высоким сродством, а субстраты, которые могут участвовать в π-π и полярных π-взаимодействиях, способны обеспечивать кажущиеся константы равновесия величиной 10 (4) M(-2), демонстрирующая способность слабых супрамолекулярных сил стабилизировать динамическую ковалентную сборку.
ПОКАЗАНЫ 1-10 ИЗ 99 ССЫЛОК
СОРТИРОВАТЬ ПОРелевантности Наиболее влиятельные документыНедавность
Матричный синтез с использованием обратимого образования иминной связи.

Иминная связь, образованная обратимой конденсацией амина и альдегида, и ее применение в качестве динамической ковалентной связи в синтезе молекулярных соединений, направленном на матрицу, будет…
Стабильность иминсодержащих динамических [2]ротаксаны к гидролизу.
- К. Леунг, В. Вонг, Ф. Арико, Филип К. Османн, Дж. Ф. Стоддарт
Химия
Органическая и биомолекулярная химия
- 2010
Предложен механизм частичной разборки двух динамичных [2]ротаксанов, включающий разрыв кинетически лабильных иминных связей молекулами воды.
Динамическая ковалентная химия.
- С. Роуэн, С. Кантрилл, Г. Р. Казинс, Дж. Сандерс, Дж. Ф. Стоддарт
Химия
Angewandte Chemie
- 2002
Некоторые недавние примеры демонстрации динамической ковалентной химии подчеркивают основные концепции этой области науки.
Соединение металломакроциклов с помощью динамической ковалентной химии: универсальный метод синтеза молекулярных клеток.

Описан модульный подход к синтезу каркасных структур, а процесс аминового обмена с этилендиамином позволяет чистое преобразование додекадерных каркасов в шестиядерные без разрушения металло-макроциклических структур.
Приключения в области молекулярного распознавания.
- Дж. Сандерс
Химия
- 2000
Резюме Описаны два различных подхода к созданию супрамолекулярных систем, потенциально способных к распознаванию и катализу. Используя подход к дизайну, мы смогли ускорить…
Сворачивание донорно-акцепторного полиротаксана с использованием нековалентных связывающих взаимодействий
Синтез и характеристика полиротаксанов, содержащих π-электронодонорные звенья 1,5-диоксинафталина (ДНФ), обведенные кружком циклобис(паракват-п-фенилен) (CBPQT4+), заложив основу для подготовки ранее неописанного класса макромолекулярных архитектур.
Самосортировка динамических библиотек иминов во время дистилляции.

- K. Osowska, O. Miljanić
Chemistry
Angewandte Chemie
- 2011
. Продемонстрируется, что вакуумная дистилляция может использоваться для сортировки комплексных библиотек [N N]. основе летучести отдельных иминов.
Молекулярные кольца Борромео
- К. Чичак, С. Кантрилл, Дж. Ф. Стоддарт
Химия
Наука
- 2004
Совместное использование координационной, супрамолекулярной и динамической ковалентной химии позволило создать высокоэффективное конструирование с помощью нескольких совместных процессов самосборки наноразмерной додекакации с приблизительной диаметром 2,5 нанометра и внутренней камерой объемом 250 Å3, выстланной 12 атомами кислорода.
Эффективное производство [n]ротаксанов с использованием шаблонных реакций клиппирования
Некоторые из динамичных [n]ротаксанов были превращены в их кинетически стабильные аналоги сначала путем восстановления («фиксации») иминных связей комплексом Bh4·THF, а затем путем протонирования комплекса добавлением кислоты.
Конфигурационный поворотный переключатель с активацией pH: управление изомеризацией E/Z в гидразонах.
Замена одной из карбонильных групп в 1,2,3-трикетон-2-нафтилгидразоне пиридиновым кольцом дает оригинальный молекулярный переключатель, который можно полностью, эффективно и обратимо переключать…
Имин против енамина — Органическая химия Видео
Имины и енамины представляют собой продукты, образованные нуклеофильным присоединением первичного (1˚) амина, вторичного (2˚) амина или аммиака (NH 3 ) к карбонилам, таким как кетоны или альдегиды.
Нажмите здесь, чтобы посмотреть полное видео!
Имине и Энамин: в чем разница?
Имины выглядят как карбонилы и образуются из первичного амина (или аммиака), реагирующего с некоторым типом кислоты (H + , H 3 O + ) с карбонилом. Проще говоря, это похоже на карбонил с двойной связью с азотом вместо кислорода.
Проще говоря, это похоже на карбонил с двойной связью с азотом вместо кислорода.
Структура имина
Обратите внимание, что после завершения реакции у вас останется структура, которая выглядит следующим образом (выше выделено зеленым цветом). Отходящая 3-углеродная цепь — это просто группа R, которая была присоединена к исходному первичному амину до того, как он прореагировал.
С другой стороны, енамины образуются из карбонилов, реагирующих со вторичным амином, и имеют двойную связь не с азотом, а с углеродом.
Вы можете запомнить это, потому что азот уже имеет 2 группы R в начале и, следовательно, был бы положительно заряжен, если бы он содержал двойную связь. Например:
Структура енамина
Обратите внимание, что двойная связь здесь находится между 2 атомами углерода: 1 из карбонильного углерода, который ее образовал, а другой представляет собой альфа-углерод.
Енамины образуются по тому же механизму, что и имины, за исключением последней стадии, которая представляет собой депротонирование катиона иминия (подробнее об этом позже).
Реакция:
A. Реагенты
Реакция имина
Реагенты, необходимые для образования имина, просты и на самом деле сводятся к трем вещам: 3 , тип амина 0˚
Обычно считается, что части 2 и 3 объединяют, NH 3 и H + , так что у нас нет дополнительного шага. Если бы мы сделали это, реакция выглядела бы просто так:
Препарат аммония
Для енаминов используется амин с температурой 2˚, и поэтому обычно встречается циклический амин, такой как азетидин:
Вторичный циклический амин
Предполагая протонирование, как мы делали ранее, мы получим реакцию, показанную ниже и будьте готовы запустить наш механизм.
Протонированный амин
Теперь, когда мы углубимся в механизм, мы сосредоточимся на образовании имина через амины 0˚ или 1˚. Однако, если мы используем описанный выше циклический протонированный амин, механизм будет таким же, пока мы не дойдем до конца
B.
 Обзор механизма
Обзор механизмаПротонирование — это первая стадия, на которой кислород из карбонила реагирует с протонированным амином, который мы образовали выше. Как вы можете видеть ниже, мы уже взяли протон и сформировали наши + ОН.
Отсюда мы можем нарисовать резонансную структуру, чтобы у нас был положительный заряд не на кислороде, как раньше, а теперь на углероде исходного карбонила.
Резонансные структуры
Зеленую резонансную структуру не обязательно рисовать, потому что стрелки будут точно такими же, как только мы выполним следующий шаг, однако это более полная картина и иногда ее легче визуализировать.
Затем происходит нуклеофильная атака [1,2-присоединение] с неподеленной парой от исходного нейтрального амина до положительного заряда на углероде. Отсюда мы получаем тетраэдрическое промежуточное соединение с новой связью C-N, а азот теперь снова имеет положительный заряд.
Тетраэдрический Промежуточный
*Примечание. Вам это знакомо? Это очень распространенный промежуточный продукт для реакций нуклеофильного присоединения, таких как механизм ацеталя/полуацеталя.
Теперь вы можете нарисовать NH 3 + с одной из букв H, свисающей в сторону, потому что мы пытаемся устранить воду и, следовательно, произвести протонный обмен, который является нашим следующим шагом. Это означает, что кислород из OH захватит один из H из H-NH 2 + (это просто NH 3 + , расположенные по-другому) и сформирует –H 2 O + .
Этап переноса протона
Как только мы сформируем воду, мы можем выгнать нашу уходящую группу или устранить воду. Мы делаем это, используя электроны азота, образуя двойную связь между углеродом и азотом и в процессе образуя ион иминия. Продукт теперь выглядит знакомо?
Этап устранения
На данный момент у нас есть катион иминия, который будет вашей контрольной точкой для этих типов реакций. Если вы не понимаете эту структуру, вы, скорее всего, сделали что-то не так и должны вернуться к своему механизму и различным шагам, чтобы выяснить, где вы хотите отклониться от курса.
Для енаминного механизма это будет тетраэдрический интермедиат, образованный до переноса протона и образования воды. Отсюда вода снова станет нашей покидающей группой, которая будет удалена на следующем шаге.
Енамин тетраэдрический промежуточный продукт
C. Промежуточные продукты
Это общая формула катиона иминия (R2C=NR 2 + ), который является ключевым промежуточным продуктом для иминовых и енаминовых реакций.
Общая структура иминиевого катиона
Образование иминиевого катиона будет нашим последним промежуточным продуктом, прежде чем мы получим конечный продукт, который может быть имином или енамином. Отсюда мы можем использовать воду или сопряженную основу нашего исходного NH 9.0018 4 + , который представляет собой NH 3 (аммиак), чтобы депротонировать конечный H на азоте, чтобы получить наш конечный продукт, имин.
Катион иминия
Катион иминия для енаминов выглядит очень похоже. Ниже приведен пример, когда используемый амин был вторичным (2˚) и циклическим.
Ниже приведен пример, когда используемый амин был вторичным (2˚) и циклическим.
Иминий Катион енамина
D. Продукты
Имин Продукт
Общая формула имина: R 2 C=NR
Продукт иминного механизма будет выглядеть как карбонил, за исключением того, что он содержит N (азот) , вместо O (кислород) и дополнительный H (водород). Остальное будет просто нашим побочным продуктом.
Также обратите внимание, что NH 4 + был воспроизведен, но если бы мы использовали воду для депротонирования катиона иминия, вместо этого мы получили бы H 3 O + и NH 3 в качестве побочных продуктов. Оба будут правильными!
Продукт енамина
Для енаминов наш продукт не будет иметь двойную связь с азотом, а вместо этого будет иметь двойную связь от исходного положения карбонильного углерода до одного из альфа-углеродов (подробнее об этом ниже).
Специально для енаминов:
Все шаги выше были описаны для случаев, когда используется амин 0˚ или 1˚, однако, когда используется амин 2˚, мы получаем другую последнюю стадию. Это потому, что если мы посмотрим на наш катион иминия (зеленый выше), у нас нет водорода для депротонирования на азоте.
Это потому, что если мы посмотрим на наш катион иминия (зеленый выше), у нас нет водорода для депротонирования на азоте.
Вопрос, который мы задаем себе, будет следующим: откуда взять водород (H), который нужно удалить? Ответ на этот вопрос находится в нашем альфа-положении от нашего исходного карбонила.
Как и раньше, помните, что мы можем депротонировать с сопряженным основанием, которым в данном случае будет циклический амин (см. ниже) или вода.
Стадия депротонирования енаминов
Связанные темы:
1. Альфа-положение (α)
Мы кратко упомянули альфа-положение, когда говорили об енаминах, но почему это важно? Оказывается, енамины могут вступать в реакции в своем альфа-положении, как и многие другие соединения в органической химии, такие как енолы и еноляты.
Альфа-положение благодаря своей уникальной кислотности (pka ~ 20) позволяет таким соединениям, как еноляты и енамины, вступать в различные реакции (алкилирование и ацилирование) по альфа-углероду.
Енамины способны использовать свое нуклеофильное альфа-положение для добавления различных групп R и образования альфа-замещенных карбонилов. Это происходит через промежуточную соль иминия, которая может гидролизоваться обратно до карбонила.
Алкилирование и гидролиз енамина
2. Гидролиз
Гидролиз в данном случае относится к способности переходить от нашей иминиевой соли обратно к нашему карбонилу с использованием воды и небольшого количества кислоты. Механизм включает 5 стадий: протонирование, присоединение Н3О, перенос протона, отщепление, депротонирование. Кажется знакомым?
Вот видео этого механизма, используемого для превращения сложного эфира обратно в карбоновую кислоту.
Гидролиз можно проводить как для иминов, так и для енаминов, чтобы снова превратить их в карбонилы, как показано ниже при гидролизе енамина.
Гидролиз енамина
Этот механизм гидролиза будет важен при решении задач алкилирования и ацилирования енамина, поскольку гидролиз обратно до карбонила обычно является последней стадией.
3. Таутомеризация
Еще одна важная тема возникает при обсуждении енолов, альфа-углерода и, в частности, кетонов, а именно таутомеров и таутомеризации. Причина, по которой это применимо, заключается в том, что имины и енамины могут таутомеризоваться друг с другом.
Во-первых, у нас есть кето-енольная таутомеризация, которая может катализироваться кислотой или основанием. Помните, что эти 2 соединения являются просто конституциональными изомерами.
Кето-енольная таутомеризация
То же правило применяется к иминам и енаминам. Обратите внимание, что единственная разница между 2 заключается в том, что двойная связь и 1 H (водород) поменялись местами.
Таутомеризация имина и енамина
Эта концепция таутомеризации с иминами и енаминами будет приобретать все большее значение при рассмотрении реакций синтеза, где необходимо добавлять группы R в альфа-положение.
4. Основания Шиффа и другие соединения азота
Теперь, говоря об иминах, мы должны признать, что их также можно назвать основаниями Шиффа, когда группа, присоединенная к N, представляет собой не водород, а алкильную группу.
Возьмем, к примеру, приведенную ниже структуру, которая является общей структурой имина.
Общая структура имина
На самом деле мы можем называть это соединение разными именами в зависимости от того, что такое R1, R2 и R3. Давайте рассмотрим некоторые из наиболее распространенных названий:
- Если R3 ≠ H, это называется основанием Шиффа
- Если R3 = H и R1 или R2 = H, это называется первичным альдимином, что означает, что имин был получен из альдегида
- Если R3 ≠ H и R1 или R2 = H, это называется вторичным альдимином
- Если R3 = H и R1 и R2 ≠ H, это называется первичным кетимином, что означает, что имин был получен из кетона
- Если R3 ≠ H и R1 и R2 ≠ H, это называется вторичным кетимином
-
Некоторые другие названия, которые вы можете встретить, это азиридины, полуаминали, азиды и нитрозосоединения.
- Полуаминали — это просто первое промежуточное соединение, которое мы видим в иминном механизме, где центральный углерод присоединен к гидроксильной (ОН), аминной (NR2) и 2 группам R.

- Нитрозосоединения содержат группу «–N=O», где N (азот) присоединен к группе R, такой как углерод, азот и даже иногда кислород.
- Азиридин относится к структуре с химической формулой C2H5N. Это в основном 3-членное кольцо с группой NH, присоединенной к 2 Ch3. Его также можно увидеть под названием этиленимин.
- Наконец, азиды обозначаются просто N3- или иногда называются азид-ионами. Возможно, вы уже видели эту структуру, когда узнали о формальных обвинениях. Структурно это может быть представлено тремя различными способами, если мы включим резонансные структуры.
5. Альдольная конденсация
Наконец, просто имейте в виду, что еноляты, которые реагируют очень похоже на енамины, могут подвергаться реакции конденсации, известной как альдольная конденсация. Это когда енолят-1 действует как нуклеофил (Nu-) и атакует электрофил (E+), такой как другой карбонил.
Это образует то, что известно как β-гидроксикарбонил, который может дегидратироваться по 2 механизмам с образованием сопряженного ненасыщенного карбонила.
Вот пример: (подробнее об этом позже)
Механизм альдольной конденсации
Вопросы и ответы:
Почему необходимо рисовать стрелки равновесия или реверса?
- Это потому, что это обратимая реакция по механизму гидролиза. Мы можем взаимодействовать между карбонилом и имин/енамином с помощью кислотного катализа и воды.
Что мы получим, если воспользуемся третичным амином?
- Третичные амины не имеют связи N-H и, следовательно, не могут образовывать первое промежуточное соединение в реакциях имина и енамина, которым является полуаминаль. Хотя группы NR3 являются хорошими нуклеофилами, они не будут эффективно реагировать с альдегидами и кетонами.
Можем ли мы перейти от имина к енамину?
- Да, через таутомеризацию. Это может катализироваться кислотой или основанием, и в результате получаются два структурных изомера, которые могут взаимно преобразовываться.
Каков механизм обратной реакции от имина или енамина к исходному карбонилу?
- Это называется гидролизом, и его механизм можно найти выше в разделе, посвященном енаминам.
 Единственная разница для иминов заключается в том, что первая стадия включает протонирование азота с образованием катиона иминия.
Единственная разница для иминов заключается в том, что первая стадия включает протонирование азота с образованием катиона иминия.
Какие еще были 5 шагов для механизма?
- 5 стадий механизма имина и енамина: протонирование, нуклеофильная атака, перенос протона, отщепление и депротонирование.
Краткое описание механизма имина и енамина:
I. Механизм имина:
Механизм имина
Вот краткое описание механизма имина. Обратите внимание на 5 этапов: протонирование, нуклеофильная атака, перенос протона, элиминация и депротонирование.
II. Энамин:
Механизм енамина
Вот краткое описание механизма енамина. Здесь можно увидеть те же 5 стадий иминного механизма, за исключением стадии депротонирования катиона иминия, где наше сопряженное основание захватывает водород из альфа-углерода.
Скрининг и характеристика разнообразной панели метагеномных иминредуктаз для биокаталитического восстановительного аминирования
- Статья
- Опубликовано:
- Джеймс Р. Маршалл 1 na1 ,
- Пейюань Яо ORCID: orcid.org/0000-0003-4029-5985 1,2 na1 ,
- Сара Л. Монтгомери 1 ,
- Джеймс Д. Финниган ORCID: orcid.org/0000-0002-8514-784X 3 ,
- Томас В. Торп 1 ,
- Райан Б. Палмер 1 ,
- Хуан Мангас-Санчес 1 ,
- Ричард А. М. Дункан ORCID: orcid.org/0000-0002-6822-7039 3 ,
- Рэйчел С. Хит ORCID: orcid.org/0000-0003-1910-8268 1 ,
- Kirsty M. Graham 3 ,
- Darren J. Cook 3 ,
- Simon J. Charnock 3 &
- …
- Николас Дж.
 Тернер
ORCID: orcid.org/0000-0002-8708-0781 1
Тернер
ORCID: orcid.org/0000-0002-8708-0781 1
Химия природы том 13 , страницы 140–148 (2021 г.)Процитировать эту статью
9617 Доступ
38 цитирований
22 Альтметрический
Сведения о показателях
Предметы
- Биокатализ
- Катализ
- Зеленая химия
- Органическая химия
- Химический синтез
Abstract
Поиск более быстрых и простых способов скрининга пространства белковых последовательностей, позволяющих идентифицировать новые биокатализаторы для асимметричного синтеза, остается как проблемой, так и ограничивающим шагом в открытии ферментов. Биокаталитические стратегии синтеза хиральных аминов становятся все более привлекательными и включают ферментативное асимметричное восстановительное аминирование, которое предлагает эффективный способ получения многих из этих ценных соединений. Здесь мы сообщаем об открытии более 300 новых иминредуктаз и производстве большой (384 фермента) и разнообразной по последовательности панели иминредуктаз, доступных для скрининга. Мы также сообщаем о разработке удобного высокопроизводительного экрана для проверки их активности. С помощью этого подхода мы идентифицировали биокатализаторы иминредуктазы, способные принимать структурно требовательные кетоны и амины, которые включают препаративный синтез N -замещенные производные β-аминоэфира с помощью процесса динамического кинетического разрешения с превосходными выходами и стереохимической чистотой.
Биокаталитические стратегии синтеза хиральных аминов становятся все более привлекательными и включают ферментативное асимметричное восстановительное аминирование, которое предлагает эффективный способ получения многих из этих ценных соединений. Здесь мы сообщаем об открытии более 300 новых иминредуктаз и производстве большой (384 фермента) и разнообразной по последовательности панели иминредуктаз, доступных для скрининга. Мы также сообщаем о разработке удобного высокопроизводительного экрана для проверки их активности. С помощью этого подхода мы идентифицировали биокатализаторы иминредуктазы, способные принимать структурно требовательные кетоны и амины, которые включают препаративный синтез N -замещенные производные β-аминоэфира с помощью процесса динамического кинетического разрешения с превосходными выходами и стереохимической чистотой.
Это предварительный просмотр содержимого подписки, доступ через ваше учреждение
Варианты доступа
Подписаться на журнал
Получить полный доступ к журналу на 1 год
118,99 €
всего 9,92 € за выпуск
Подписаться
Расчет налогов будет завершен во время оформления заказа.
Купить артикул
Получите ограниченный по времени или полный доступ к статье на ReadCube.
32,00 $
Купить
Все цены указаны без учета стоимости.
Рис. 1: Рабочий процесс и приблизительные сроки создания метагеномной библиотеки с примерами того, как эта платформа использовалась для расширения набора биокаталитических инструментов применительно к IRED. Рис. 2: 384 IREDy-to-go скрининг амина 2b в сочетании с данными биотрансформации для восстановительного аминирования 2 с b филогенетически нанесен на карту, чтобы показать общее распределение активности. Рис. 3: Высокопроизводительная характеристика с использованием колориметрического скрининга, диаграмма, показывающая субстраты, представляемые на колориметрический скрининг, наряду с количеством окончательных попаданий фермента; метод расчета количества попаданий приведен в дополнительном разделе 4. 5. Рис. 4: Восстановительное аминирование в аналитическом масштабе. Рис. 5: Асимметричное восстановительное аминирование β-кетоэфиров в препаративном масштабе.
5. Рис. 4: Восстановительное аминирование в аналитическом масштабе. Рис. 5: Асимметричное восстановительное аминирование β-кетоэфиров в препаративном масштабе. Доступность данных
Данные, подтверждающие результаты и выводы, доступны в этом документе и в дополнительной информации. Как скрининг IREDy-to-go, так и дубликат планшета для скрининга без компонентов колориметрического скрининга, содержащий 0,5 мг неочищенного лизата каждого IRED в каждой лунке, свободно доступны через Prozomix Ltd.
Ссылки
Кан, С. Б. Дж., Льюис, Р. Д., Чен, К. и Арнольд, Ф. Х. Направленная эволюция цитохрома С для образования связи углерод-кремний: оживление кремния. Наука 354 , 1048–1051 (2016).
КАС пабмед ПабМед Центральный Статья Google ученый
“>Burke, A.J. et al. Дизайн и эволюция фермента с неканоническим органокаталитическим механизмом. Природа 570 , 219–223 (2019).
КАС пабмед Статья Google ученый
Zeymer, C., Zschoche, R. & Hilvert, D. Оптимизация ферментативного механизма вдоль эволюционной траектории компьютерно разработанной (ретро-)альдолазы. Дж. Ам. хим. соц. 139 , 12541–12549 (2017).
КАС пабмед Статья Google ученый
Сандовал, Б. А., Мейхан, А. Дж. и Хайстер, Т. К. Энантиоселективный перенос атома водорода: открытие каталитической неразборчивости во флавин-зависимых «ен»-редуктазах.
 Дж. Ам. хим. соц. 139 , 11313–11316 (2017).
Дж. Ам. хим. соц. 139 , 11313–11316 (2017).КАС пабмед Статья Google ученый
Сандовал, Б. А. и Хайстер, Т. К. Новые стратегии расширения набора инструментов ферментов в биокатализе. Курс. мнение хим. биол. 55 , 45–51 (2020).
КАС пабмед ПабМед Центральный Статья Google ученый
Devine, P. N. et al. Расширение применения биокатализа для решения задач разработки лекарств. Нац. Преподобный Хим. 2 , 409–421 (2018).
Артикул Google ученый
Xiao, H., Bao, Z. & Zhao, H. Высокопроизводительные методы скрининга и отбора для направленной эволюции ферментов. Индивидуальный инж. хим. Рез. 54 , 4011–4020 (2015).
КАС пабмед Статья Google ученый
“>Friedfeld, M. R. et al. Прекурсоры кобальта для высокопроизводительного обнаружения катализаторов гидрирования асимметричных алкенов из неблагородных металлов. Наука 342 , 1076 (2013).
КАС пабмед Статья Google ученый
Коллинз, К. Д., Генш, Т. и Глориус, Ф. Современные скрининговые подходы к открытию и развитию реакций. Нац. хим. 6 , 859–871 (2014).
КАС пабмед Статья Google ученый
Кабрера-Пардо, Дж., Чай, Д.И., Лю, С., Мрксич, М. и А. Козьмин, С.
 Масс-спектрометрия с использованием меток для ускорения обнаружения и оптимизации реакций. Нац. хим. 5 , 423–427 (2013).
Масс-спектрометрия с использованием меток для ускорения обнаружения и оптимизации реакций. Нац. хим. 5 , 423–427 (2013).КАС пабмед ПабМед Центральный Статья Google ученый
Ваначек, П. и др. Изучение разнообразия ферментов путем интеграции биоинформатики с анализом экспрессии и биохимической характеристикой. ACS Катал. 8 , 2402–2412 (2018).
КАС Статья Google ученый
Yan, C. et al. Скрининг биокатализаторов в реальном времени в живых бактериальных колониях. Дж. Ам. хим. соц. 139 , 1408–1411 (2017).
КАС пабмед Статья Google ученый
Вальехо, Д., Никооманзар, А., Паегель, Б. М. и Чапут, Дж. К. Флуоресцентно-активированная сортировка капель для направленной эволюции одной клетки.
 Синтезатор ACS. биол. 8 , 14:30–14:40 (2019).
Синтезатор ACS. биол. 8 , 14:30–14:40 (2019).КАС пабмед ПабМед Центральный Статья Google ученый
Гилен, Ф. и др. Эволюция ферментов, направленная на сверхвысокую производительность, путем сортировки капель, активируемой абсорбцией (AADS). Проц. Натл акад. науч. США 113 , E7383–E7389 (2016).
КАС пабмед Статья ПабМед Центральный Google ученый
Дэвидс Т., Шмидт М., Бётчер Д. и Борншойер Ю. Т. Стратегии открытия и разработки ферментов для биокатализа. Курс. мнение хим. биол. 17 , 215–220 (2013).
КАС пабмед Статья Google ученый
Бунзель, Х. А., Гаррабу, X., Потт, М. и Хилверт, Д. Ускорение открытия и разработки ферментов с помощью методов сверхвысокой производительности.
 Курс. мнение Структура биол. 48 , 149–156 (2018).
Курс. мнение Структура биол. 48 , 149–156 (2018).КАС пабмед Статья Google ученый
Ghislieri, D. & Turner, N.J. Биокаталитические подходы к синтезу энантиомерно чистых хиральных аминов. Верх. Катал. 57 , 284–300 (2014).
КАС Статья Google ученый
Weise, N., Parmeggiani, F., Ahmed, S. & Turner, NJ. Открытие и исследование мутазоподобной активности фенилаланин-аммиачной лиазы из Anabaena variabilis . Топ. Катал. 61 , 288–295 (2018).
КАС пабмед ПабМед Центральный Статья Google ученый
Гроган Г. Синтез хиральных аминов с использованием окислительно-восстановительного биокатализа. Курс. мнение хим. биол. 43 , 15–22 (2018).
КАС пабмед Статья Google ученый
“>Jia, Z.-J., Gao, S. & Arnold, F.H. Ферментативное первичное аминирование бензильных и аллильных C( sp 3 )-H связей. Дж. Ам. хим. соц. 142 , 10279–10283 (2020).
КАС пабмед Статья Google ученый
Schrittwieser, JH, Velikogne, S. & Kroutil, W. Биокаталитическое восстановление имина и восстановительное аминирование кетонов. Доп. Синтез. Катал. 357 , 1665–1685 (2015).
Google ученый
Hyslop, J. F. et al. Биокаталитический синтез хиральных N -функционализированных аминокислот. Анжю. хим.
 Междунар. Эд. 57 , 13821–13824 (2018).
Междунар. Эд. 57 , 13821–13824 (2018).КАС Статья Google ученый
Шталь, Л. Справочник по гомогенному гидрированию, тома 1–3, под редакцией Йоханнеса Г. де Вриса (DSM Pharmaceutical Products, Гелен, Нидерланды) и Корнелиса Дж. Эльзевира (Амстердамский университет, Нидерланды). Wiley-VCH Verlag GmbH & Co. KGaA: Вайнхайм. 2007. 1632 стр. 625 долларов США. ISBN 978-3-527-31161-3. Дж. Ам. хим. соц. 129 , 10297–10298 (2007 г.).
КАС Статья Google ученый
Ли, В. Стереоселективное образование аминов (Springer, 2014).
Роули, С. Д. и Джордан, А. М. Набор инструментов химика-медика: анализ реакций, используемых при поиске потенциальных лекарств. Ж. Мед. хим. 54 , 3451–3479 (2011).
КАС пабмед Статья Google ученый
“>Хоу, Г. и др. Энантиоселективное гидрирование N–H иминов. Дж. Ам. хим. соц. 131 , 9882–9883 (2009 г.).
КАС пабмед Статья Google ученый
Аурелио, Л., Браунли, Р. и Хьюз, А. Б. Синтетический препарат N -метил-ɑ-аминокислоты. Хим. 104 , 5823–5846 (2004 г.).
КАС пабмед Статья Google ученый
Алеку А.Г. и др. Восстановительная аминаза из Aspergillus oryzae . Нац. хим. 9 , 961–969 (2017).
КАС пабмед Статья Google ученый
“>Scheller, P.N., Lenz, M., Hammer, S.C., Hauer, B. & Nestl, B.M. Катализируемое иминредуктазой межмолекулярное восстановительное аминирование альдегидов и кетонов. ChemCatChem 7 , 3239–3242 (2015).
КАС Статья Google ученый
Wetzl, D. et al. Асимметричное восстановительное аминирование кетонов, катализируемое иминредуктазами. ChemCatChem 8 , 2023–2026 (2016).
КАС Статья Google ученый
Maugeri, Z. & Rother, D. Восстановительное аминирование кетонов, катализируемое цельноклеточными биокатализаторами, содержащими иминредуктазы (IRED).
 Дж. Биотехнология. 258 , 167–170 (2017).
Дж. Биотехнология. 258 , 167–170 (2017).КАС пабмед Статья Google ученый
Roiban, G.D. et al. Эффективное биокаталитическое восстановительное аминирование за счет расширения набора инструментов иминредуктазы. ChemCatChem 9 , 4475–4479 (2017).
КАС Статья Google ученый
Шарма, М. и др. Механизм восстановительного аминирования, катализируемый грибковыми восстановительными аминазами. ACS Катал. 8 , 11534–11541 (2018).
КАС Статья Google ученый
Мицукура К., Сузуки М., Тада К., Йошида Т. и Нагасава Т. Асимметричный синтез хирального циклического амина из циклического имина с помощью бактериального цельноклеточного катализатора энантиоселективной иминредуктазы. Орг.
 биомол. хим. 8 , 4533–4535 (2010).
биомол. хим. 8 , 4533–4535 (2010).КАС пабмед Статья Google ученый
Мицукура, К. и др. Очистка и характеристика романа ( R )-иминредуктаза из Streptomyces sp. GF3587. Бионауч. Биотехнолог. Биохим. 75 , 1778–1782 (2011).
КАС пабмед Статья Google ученый
Слабу И., Галман Дж. Л., Ллойд Р. К. и Тернер Н. Дж. Открытие, разработка и синтетическое применение трансаминазных биокатализаторов. ACS Катал. 7 , 8263–8284 (2017).
КАС Статья Google ученый
Мангас-Санчес, Дж. и др. Иминредуктазы (IRED). Курс. мнение хим. биол. 37 , 19–25 (2017).
КАС пабмед Статья Google ученый
“>Шобер, М. и др. Хиральный синтез ингибитора LSD1 GSK2879552 возможен за счет направленной эволюции иминредуктазы. Нац. Катал. 2 , 909–915 (2019).
КАС Статья Google ученый
Wetzl, D. et al. Расширение набора инструментов иминредуктазы путем изучения пространства последовательностей бактериальных белков. ChemBioChem 16 , 1749–1756 (2015).
КАС пабмед Статья Google ученый
Франция, S. P. et al. Идентификация новых бактериальных членов семейства ферментов иминредуктаз, которые выполняют восстановительное аминирование.
 ChemCatChem 10 , 510–514 (2018).
ChemCatChem 10 , 510–514 (2018).КАС Статья Google ученый
Георге-Дору Р. и др. Эффективное биокаталитическое восстановительное аминирование за счет расширения набора инструментов иминредуктазы. ChemCatChem 9 , 4475–4479 (2017).
Артикул КАС Google ученый
Zhu, J. et al. Энантиоселективный синтез 1-арилзамещенных тетрагидроизохинолинов с использованием иминредуктазы. ACS Катал. 7 , 7003–7007 (2017).
КАС Статья Google ученый
Li, H., Luan, Z.J., Zheng, G.W. & Xu, J.H. Эффективный синтез хиральных индолинов с использованием иминредуктазы из Paenibacillus lactis . Доп. Синтез. Катал. 357 , 1692–1696 (2015).
КАС Статья Google ученый
“>Бод, Д., Джеффрис, Дж. У. Э., Муди, Т. С., Уорд, Дж. М. и Хейлс, Х. К. Метагеномный подход к открытию нового биокатализатора: применение к трансаминазам и синтезу аллильных аминов. Зеленый хим. 19 , 1134–1143 (2017).
КАС Статья Google ученый
Эрнандес, К., Секреньи, А. и Клапес, П. Нуклеофильная неразборчивость природных и искусственных альдолаз. ChemBioChem 19 , 1353–1358 (2018).
ПабМед Статья КАС Google ученый
Лейпольд, Л.
 и др. Идентификация и использование надежных трансаминаз из метагенома внутренней канализации. Зеленый хим. 21 , 75–86 (2019).
и др. Идентификация и использование надежных трансаминаз из метагенома внутренней канализации. Зеленый хим. 21 , 75–86 (2019).КАС пабмед Статья Google ученый
Капарко, А. и др. Метагеномный майнинг для открытия аминдегидрогеназы. Доп. Синтез. Катал. 362 , 2427 (2020).
КАС Статья Google ученый
Нагойский протокол о доступе к генетическим ресурсам и совместном использовании на справедливой и равной основе выгод от их использования к Конвенции о биологическом разнообразии (Министерство иностранных дел и по делам Содружества Парламента Великобритании, 2010 г.).
Zawodny, W. et al. Химиоферментативный синтез замещенных азепанов путем последовательного биокаталитического восстановления и литийорганической перегруппировки. Дж.
 Ам. хим. науч. 140 , 17872–17877 (2018).
Ам. хим. науч. 140 , 17872–17877 (2018).КАС Статья Google ученый
Montgomery, S.L. et al. Характеристика иминредуктаз в восстановительном аминировании для изучения взаимосвязей структура-активность. Науч. Доп. 6 , eaay9320 (2020).
КАС пабмед ПабМед Центральный Статья Google ученый
Майер, К. М. и Арнольд, Ф. Х. Колориметрический анализ для количественного определения активности дегидрогеназы в неочищенных клеточных лизатах. Дж. Биомол. Screen 7 , 135–140 (2002).
КАС пабмед Статья Google ученый
Peng, H. et al. Расшифровка образования пиперидина в индолизидинах, полученных из поликетидов, показывает восстановление тиоэфира, трансаминирование и необычный процесс восстановления имина.
 АСУ Хим. биол. 11 , 3278–3283 (2016).
АСУ Хим. биол. 11 , 3278–3283 (2016).КАС пабмед Статья Google ученый
Ye, S. et al. Идентификация методом геномного анализа кластера генов поликетидов I типа из Streptomyces argillaceus , участвующих в биосинтезе пиридиновых и пиперидиновых алкалоидов аргимицинов P. Front. микробиол. 8 , 194 (2017).
ПабМед ПабМед Центральный Google ученый
Lenz, M. et al. Асимметричное восстановление кетонов иминредуктазами. ChemBioChem 18 , 253–256 (2017).
КАС пабмед Статья Google ученый
Гонсалес-Мартинес, Д. и др. Асимметричный синтез первичных и вторичных β-фторариламинов с использованием восстановительных аминаз грибов. ChemCatChem 12 , 2421 (2020).

Артикул КАС Google ученый
Smith, J. A. et al. в A101 Advances in Cough, Dyspnea, and Interventional Legmonary A2672–A2672 (American Thoracic Society, 2017).
Darcsi, A., Tóth, G., Kökösi, J. & Béni, S. Выяснение структуры связанной с процессом примеси дапоксетина. Дж. Фарм. Биомед. Анальный. 96 , 272–277 (2014).
КАС пабмед Статья Google ученый
Fuchs, M., Koszelewski, D., Tauber, K., Kroutil, W. & Faber, K. Химиоферментативный асимметричный полный синтез ( S )-ривастигмина с использованием омега-трансаминаз. Хим. коммун. 46 , 5500–5502 (2010).
КАС Статья Google ученый
Чжан, Д. и др. Разработка дегидрогеназы β-аминокислот для синтеза β-аминокислот путем восстановительного аминирования β-кетокислот.
 САУ Катал. 5 , 2220–2224 (2015).
САУ Катал. 5 , 2220–2224 (2015).КАС Статья Google ученый
Мидельфорт, К. и др. Реконструкция и характеристика субстратной специфичности и активности аминотрансферазы Vibrio fluvialis для синтеза имагабалина. Белок Eng. Дес. Сел. 26 , 25–33 (2013).
КАС пабмед Статья Google ученый
Юраисти Э. и Солошонок В. Энантиоселективный синтез β-аминокислот 2-е изд. (Wiley, 2005).
Иглесиас, Э. Реакции гидролиза сложных эфиров и нитрозирования енолов этилциклогексанон-2-карбоксилата, ингибируемые β-циклодекстрином. Дж. Орг. хим. 65 , 6583–6594 (2000).
КАС пабмед Статья Google ученый
Борнадель, А. и др. Технические соображения по расширению масштабов восстановительного аминирования, катализируемого иминредуктазой: тематическое исследование.
 Организационный процесс. Рез. Дев. 23 , 1262–1268 (2019).
Организационный процесс. Рез. Дев. 23 , 1262–1268 (2019).КАС Статья Google ученый
Мангас-Санчес, Дж. и др. Асимметричный синтез первичных аминов, катализируемый грибковыми восстановительными аминазами. Хим. науч. 11 , 5052–5057 (2020).
КАС Статья пабмед ПабМед Центральный Google ученый
Сутин Л. и др. Оксазолоны как мощные ингибиторы 11β-гидроксистероиддегидрогеназы типа 1. Биоорг. Мед. хим. лат. 17 , 4837–4840 (2007).
КАС пабмед Статья Google ученый
Афанасьев О.И., Кучук Э., Усанов Д.Л., Чусов Д. Восстановительное аминирование в синтезе лекарственных средств. Хим. Ред. 119 , 11857–11911 (2019).
КАС пабмед Статья Google ученый
“>
Wijma, H.J. et al. Энантиоселективные ферменты с помощью компьютерного дизайна и скрининга in silico. Анжю. хим. Междунар. Эд. 54 , 3726–3730 (2015).
КАС Статья Google ученый
Роббинс Д. В. и Хартвиг Дж. Ф. Простой многомерный подход к высокопроизводительному открытию каталитических реакций. Science 333 , 1423–1427 (2011).
КАС пабмед ПабМед Центральный Статья Google ученый
Turner, NJ. Энантиоселективное окисление связей C–O и C–N с использованием оксидаз. Хим. 111 , 4073–4087 (2011).
КАС пабмед Статья Google ученый
Ван, Л. и Сяо, Дж. Реакции переноса атома водорода. Топ. Курс. хим. 374 , 1–55 (2016).
Артикул КАС Google ученый
Тобиас Х. и др. Прямое восстановительное аминирование кетонов: структура и активность S -селективные иминредуктазы из Streptomyces . ChemCatChem 6 , 2248–2252 (2014).
Артикул КАС Google ученый
Ленц М., Борлингхаус Н., Вайнманн Л. и Нестл Б.М. Последние достижения в реакциях, катализируемых иминредуктазой. World J. Microbiol. Биотехнолог. 33 , 199 (2017).
ПабМед Статья КАС Google ученый
Nugent, T.C. & El-Shazly, M. Синтез хирального амина – последние разработки и тенденции восстановления енамида, восстановительного аминирования и восстановления имина. Доп. Синтез. Катал. 352 , 753–819 (2010).
КАС Статья Google ученый
Salzmann, T.N., Ratcliffe, R.W., Christensen, B.G. & Bouffard, F.A. Стереоконтролируемый синтез (+)-тиенамицина. Дж. Ам. хим. науч. 102 , 6161–6163 (1980).
КАС Статья Google ученый
Скачать ссылки
Благодарности
Мы благодарим Инновационный центр промышленных биотехнологий (IBioIC) и Исследовательский совет по биотехнологии и биологическим наукам (BBSRC) за предоставление стипендии CASE J.R.M. от Prozomix Ltd. был поддержан стипендией CSC и Ассоциацией содействия инновациям молодежи Китайской академии наук (грант № 2016166). Т.В.Т. была поддержана стипендией BBSRC CASE, присуждаемой Pfizer. С.Л.М. был поддержан стипендией BBSRC CASE от Johnson Matthey. Р.Б.П. и Р.Ш.Х. были поддержаны Европейским исследовательским советом (грант ERC № 742987). Дж. М.-С. финансировался за счет гранта BB/M006832/1 Британского исследовательского совета по биотехнологии и биологическим наукам. S.J.C., D.J.C., J.D.F., R.A.M.D. и К.М.Г. признать Седьмую рамочную программу Европейского Союза по исследованиям, технологическим разработкам и демонстрациям в соответствии с соглашением о гранте №. 685474 за поддержку MetaFluidics. Нью-Джерси выражает благодарность ERC за присуждение расширенного гранта (грант № 742987). Мы благодарим Д. Хейса из Манчестерского института биотехнологии (MIB) за помощь в сборе данных кругового дихроизма. Мы благодарим Y. Qi из Prozomix Ltd за скрининг диафораз Prozomix. Prozomix и J.R.M., P.Y., S.L.M., T.W.T., R.B.P., J.M.-S., R.S.H. и Н.Дж.Т. также поблагодарите других сотрудников Prozomix за их поддержку.
S.J.C., D.J.C., J.D.F., R.A.M.D. и К.М.Г. признать Седьмую рамочную программу Европейского Союза по исследованиям, технологическим разработкам и демонстрациям в соответствии с соглашением о гранте №. 685474 за поддержку MetaFluidics. Нью-Джерси выражает благодарность ERC за присуждение расширенного гранта (грант № 742987). Мы благодарим Д. Хейса из Манчестерского института биотехнологии (MIB) за помощь в сборе данных кругового дихроизма. Мы благодарим Y. Qi из Prozomix Ltd за скрининг диафораз Prozomix. Prozomix и J.R.M., P.Y., S.L.M., T.W.T., R.B.P., J.M.-S., R.S.H. и Н.Дж.Т. также поблагодарите других сотрудников Prozomix за их поддержку.
Информация об авторе
Примечания автора
Эти авторы внесли равный вклад: Джеймс Р. Маршалл, Пейюань Яо.
Авторы и организации
Химический факультет Манчестерского университета, Манчестерский институт биотехнологии, Манчестер, Великобритания
Джеймс Р.
 Маршалл, Пейюань Яо, Сара Л. Монтгомери, Томас У. Торп, Райан Б. Палмер, Хуан Мангас-Санчес, Рэйчел С. Хит и Николас Дж. Тернер
Маршалл, Пейюань Яо, Сара Л. Монтгомери, Томас У. Торп, Райан Б. Палмер, Хуан Мангас-Санчес, Рэйчел С. Хит и Николас Дж. ТернерНациональная инженерная лаборатория промышленных ферментов, Тяньцзиньский инженерно-исследовательский центр биокаталитических технологий, Тяньцзиньский институт промышленных биотехнологий, Китайская академия наук, Тяньцзиньский экономический парк аэропорта, Тяньцзинь, Китайская Народная Республика
Пейюань Яо
Prozomix, Building 4, West End Ind. Estate, Haltwhistle, UK
Джеймс Д. Финниган, Ричард А. М. Дункан, Кирсти М. Грэм, Даррен Дж. Кук и Саймон Дж. Чарнок
Авторы
- Джеймс Р. Маршалл
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Peiyuan Yao
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Sarah L.
 Montgomery
MontgomeryПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Джеймс Д. Финниган
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Thomas W. Thorpe
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Ryan B. Palmer
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Хуан Мангас-Санчес
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Richard A. M. Duncan
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Rachel S. Heath
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Kirsty M.
 Graham
GrahamПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Даррен Дж. Кук
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Simon J. Charnock
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Николас Дж. Тернер
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Contributions
N.J.T. и С.Дж.К. разработал и курировал проект. Дж. М.-С. и Р.Ш.Х. руководил проектом. JRM, JDF, KMG, SLM и D.J.C. выполнили идентификацию, клонирование и экспрессию ферментов. J.R.M., J.D.F., R.A.M.D. и С.Дж.К. принимали участие в проектировании, разработке и внедрении колориметрического экрана и 384-луночных планшетов. Дж. Р. М. и П.Ю. провели высокопроизводительную характеристику ферментов. Дж. Р. М. и П.Ю. выполнили аналитическую шкалу биотрансформаций. П.Ю. проведены препаративно-масштабные биотрансформации. П.Ю. и Р.Б.П. синтезированы химические стандарты. Дж. Р. М. и Т.В.Т. провел исследования термостабильности. N.J.T., S.J.C., JRM, P.Y., RSH, JM-S., J.D.F. и Т.В.Т. написал рукопись и сгенерировал цифры.
Дж. Р. М. и П.Ю. выполнили аналитическую шкалу биотрансформаций. П.Ю. проведены препаративно-масштабные биотрансформации. П.Ю. и Р.Б.П. синтезированы химические стандарты. Дж. Р. М. и Т.В.Т. провел исследования термостабильности. N.J.T., S.J.C., JRM, P.Y., RSH, JM-S., J.D.F. и Т.В.Т. написал рукопись и сгенерировал цифры.
Автор, ответственный за переписку
Переписка с Николас Дж. Тернер.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Дополнительная информация
Дополнительная информация
Дополнительные разделы 1 (1.1–1.4), 2, 3 (3.1, 3.2.1–3.2.7, 3.3.1–3.3.4, 3.4.1 и 3.4.2), 4 (4.1–4.4, 4.4. 1-4.4.5, 4.5 и 4.6), 5 (5.1, 5.2, 5.2.1–5.2. 4, 5.3–5.5), 6, 7 (7.1–.7.5), 8 и 9.
4, 5.3–5.5), 6, 7 (7.1–.7.5), 8 и 9.
Права и разрешения
Перепечатка и разрешения
Об этой статье
Дополнительная литература
Многофункциональный биокатализатор для сопряженного восстановления и восстановительного аминирования
- Томас В. Торп
- Джеймс Р. Маршалл
- Николас Дж. Тернер
Природа (2022)
Купи один и один получи бесплатно
- Майкл А.

- Майкл А.
