Имины – Справочник химика 21
Гетероциклические соединения [79, 81, 154] могут присутствовать и в группе соединений основного характера и в группе соединений остаточного азота. Для качественного определения азотных гетероциклов в инфракрасной области можно пользоваться табл. 68 [79, 207]. Гетероциклические соединения с атомом азота в кольце, как правило, имеют характер вторичных аминов или иминов (пирролы, пиридины, хинолины). В их спектрах поглощения присутствуют полосы поглощения вторичных аминов или иминов, отличающихся, как уже говорилось, повышенной интенсивностью. Кроме того, присутствуют интенсивные полосы поглощения, соответствующие скелетным колебаниям кольца, валентным колебаниям замещенных колец, валентным и деформационным колебаниям водородного атома кольца. [c.134]Внутреннее строение и физико-химические свойства полимеров. Свойства полимеров зависят от особенностей их внутреннего строения и в” первую очередь от вида структурной единицы полимера, степени полимеризации, строения цепей, а также от характера и интенсивности взаимодействия между ними.
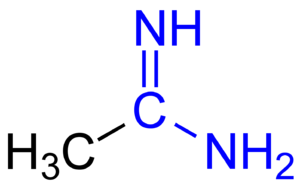
Восстановлением нитропроизводных можно группу NO2 превратить в NHs н получить имины. [c.41]
При действии системы К02/18-краун-6 в эфире при комнатной температуре (перемешивание в течение 4—6 ч) вторичные Ы-хлорамины превращаются в имины и далее в карбонильные соединения [977] [c.397]
Имины = NH имино- -имин [c.82]
Кроме того, нитрилы образуются из альдегидов и аммиака через промежуточную стадию дегидрирования иминов [c.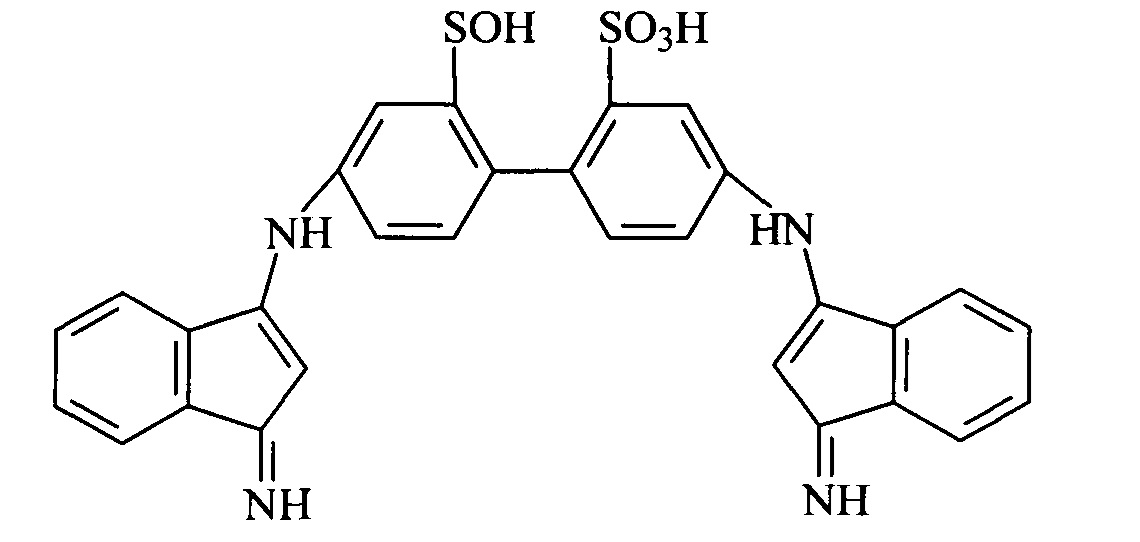
Азотсодержащие органические соединения объединяют несколько классов, важнейшими из которых являются амины с функциональной группой —Nh3, имины с группой =NH, цианистые соединения или нитрилы с группой—N, нитросоедипения с группой —NO2, нитрозосоединепня с группой —NO. [c.152]
Наблюдающаяся высокая химическая активность )адикалов обусловлена незаполненностью их электронных оболочек. Характерна аналогия между химическими свойствами гидридов углерода, азота, кислорода и фтора и химическими свойствами атомов с тем же числом электронов. Так, радикал СН (метин) является химическим аналогом атома Н, радикалы СНа (метилен) и NH (имин) — аналогами атома О, радикалы СН3 (метил), НН2 (аминогруппа) и ОН (гидроксил) — аналогами атома К и, наконец, молекулы СН4, N1 3, Н2О и НГ в известном смысле (инертность) аналогичны атому N6. Благодаря химической ненасыщенности радикалов энергия активации нроцессов, протекающих с их участием, имеет порядок величины энергии активации атомных реакций.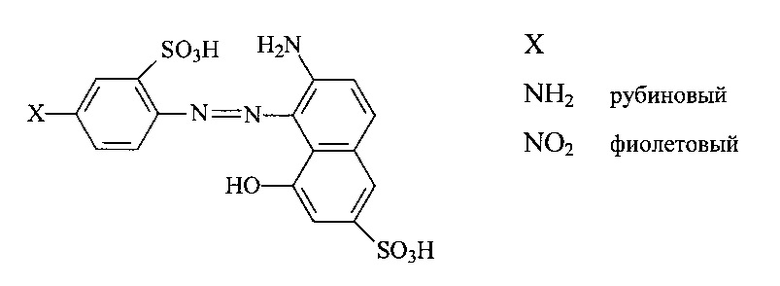
Названия соединений, в которых двухвалентная группа >NH замыкает цепь атомов угле )ода, образуют, добавляя суффикс -имин к названию соответствующего углеводорода с тем же числом атомов углерода и водорода, что и в данном соединении
Этиленимин. Действием тионилхлорида на мопоэтанола1 ипгид-рохлорид при 80—90° или действием газообразного хлористого водорода па моноэтаноламин при 160° [311 получают Р-хлорэтиламингидрохлорид, который под действием водных щелочей при 90—100° переходит в этилеп-имин [c.195]
Связь = N. В спектрах алифатических иминов полоса С = N-связи обычно расположена в области 1G70 см и смещена в сторону меньших частот в случае сопряженных и ароматических [c.133]
ПАВ, содержащие функциональные группы с положительным суммарным электронным эффектом (например, амины, амиды, имины и др.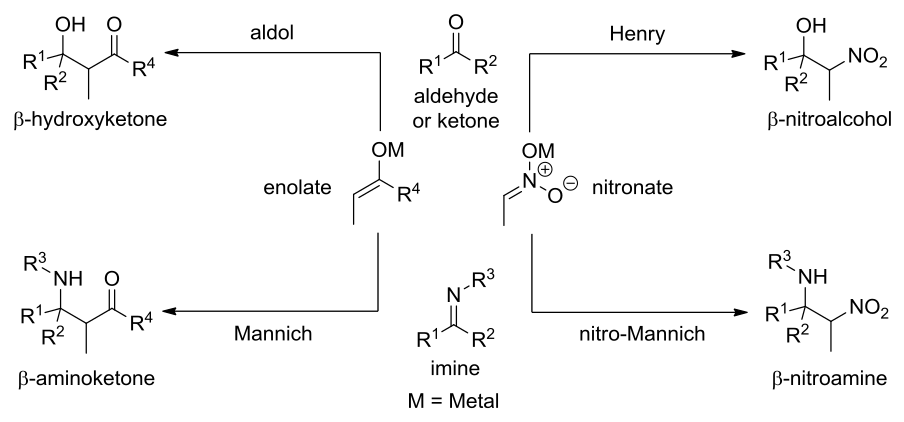 ), несколько меньше, чем ПАВ первой группы, повышают диэлектрическую проницаемость бензола (табл. 6.5). В их присутствии увеличивается энергия выхода электрона из металла (ДКРП отрицательна) (см. рис. 6.13), в [c.300]
), несколько меньше, чем ПАВ первой группы, повышают диэлектрическую проницаемость бензола (табл. 6.5). В их присутствии увеличивается энергия выхода электрона из металла (ДКРП отрицательна) (см. рис. 6.13), в [c.300]
Для осуществления реакции между аммиаком и спиртами мож-1 0 применять н дегидрирующие катализаторы (медь, никель, кобальт, нанесенные, например, на оксид алюминия). В этом случае лгехагтзм реакции совершенно иной —вначале происходит дегидрирование спирта в альдегид, а затем конденсация альдегида с аммиаком и гидрирование образующегося имина
Выбор температурного интервала окисления. Окисление будет протекат цепным путем (о и,) при небольшом и,. Из условия и = получаем для цепного режима условия и иманометрическая установка позволяет измерять достаточно надежно скорости поглощения кислорода и>Цмин. Следовательно, измерить а можно только в таких условиях, когда а2>и>и ин, т. е. Иминповышением температуры.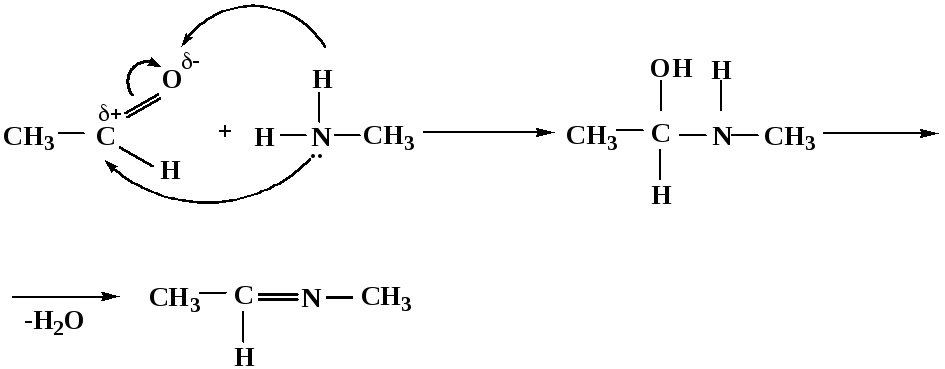 Поэтому существует такая температура Гмин, ниже которой на данной установке параметр а определить уже нельзя, и опыты надо проводить при 7 >7 мнн. Если известен температурный ход а (lga=lgЛa— —Ед/2,ЗНТ), то можно вычислить Т МИН используя Н0рЭ.В6НСТВО
Поэтому существует такая температура Гмин, ниже которой на данной установке параметр а определить уже нельзя, и опыты надо проводить при 7 >7 мнн. Если известен температурный ход а (lga=lgЛa— —Ед/2,ЗНТ), то можно вычислить Т МИН используя Н0рЭ.В6НСТВО
Если реакция (2) протекает быстро, то скорость окислительного аммонолиза, как и наблюдалось на опыте, равна скорости образования акролеина. Пока еще не установлено, является реакция (2) гомогенной или гетерогенной. Ее можно представить как образование имина СН2=СН— H=NH с последующей окислительной дегидрогенизацией, но эти соединения весьма неустойчивы и легко полимеризуются. Известно, однако, что на катализаторе М0О3 в присутствии аммиака протекает превращение акролеина в нитрил.
Для первичных и вторичных аминов (имеющих подвижный атом водорода в аминной группе) механизм ингибирующего действия заключается в линейном обрыве цепи в результате образования иминных радикалов [c.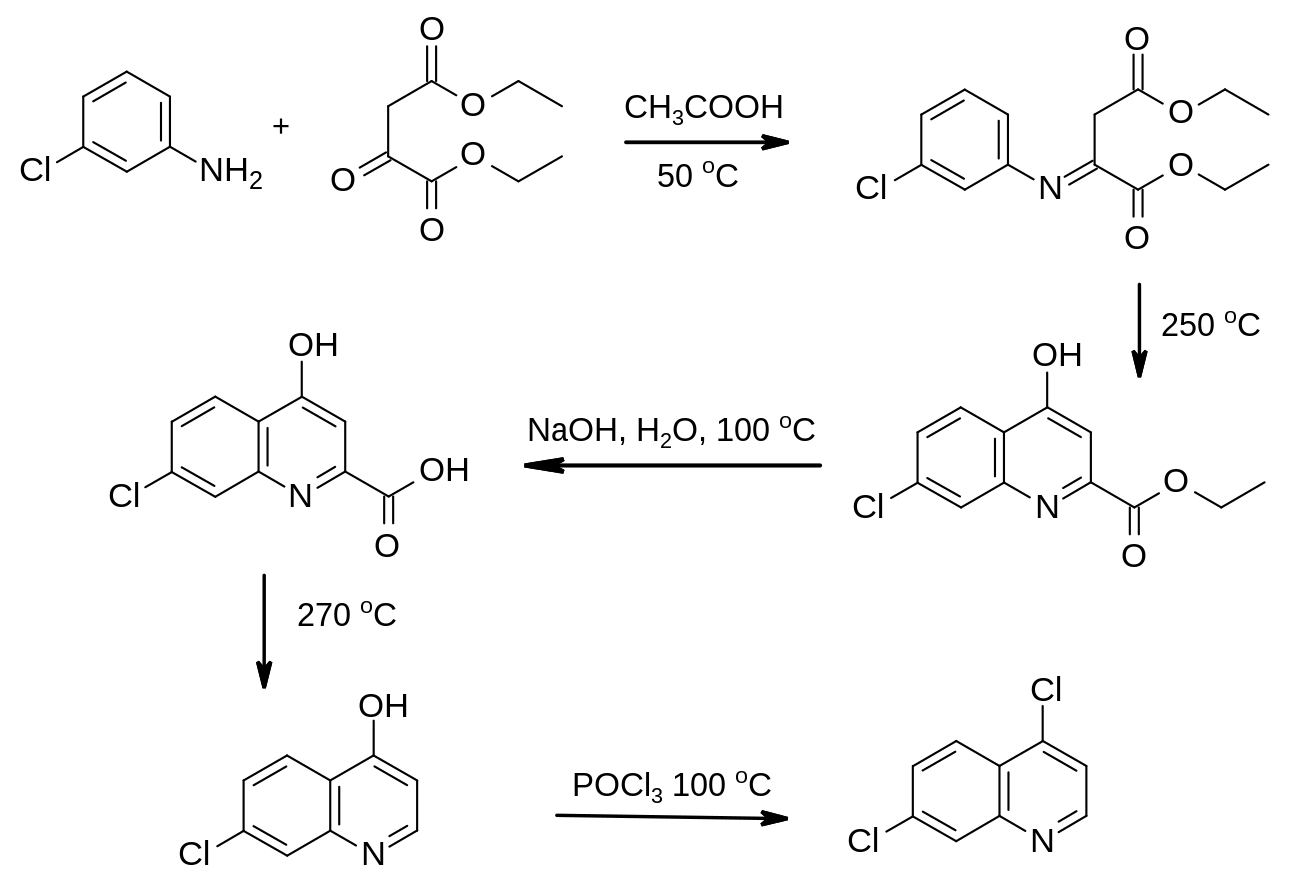 61]
61]
Указанный механизм подтверждается присутствием иминных радикалов, а также структурой ожидаемых конечных продуктов окисления. Иминный радикал в свою очередь взаимодействует С пероксидным, в результате чего образуются алкоксильные и азо-токсидные радикалы
Все эти катализаторы работают по рассмотренному ранее окислительно-восстановительному механизму, и скорость реакции зависит только от парциального давления пропилена (г = йЯсзНб )> свидетельствуя о лимитирующей стадии взаимодействия пропилена с окисленным активным центром катализатора, где образуется хе-мосорбированный аллильный радикал. В свою очередь, на другом активном центре сорбируется аммиак, вероятно, в виде иминного радикала NH. Взаимодействие их друг с другом с участием кислорода решетки и дает акрилонитрил. [c.424]
Основы неорганической химии для студентов нехимических специальностей (1989) — [ c.102 , c.

Органикум. Практикум по органической химии. Т.2 (1979) — [ c.58 ]
Химический энциклопедический словарь (1983) — [ c.218 ]
Синтезы органических препаратов Сб.3 (1952) — [ c.0 ]
Углублённый курс органической химии книга2 (1981) — [ c.25 ]
Названия органических соединений (1980) — [ c.191 , c.195 , c.280 ]
Синтетические методы органической химии (1982) — [ c.90 , c.112 , c.215 , c.277 ]
Органическая химия (1974) — [
c. 698
,
c.699
]
698
,
c.699
]
Общая органическая химия Т.7 (1984) — [ c.65 , c.71 ]
Количественный органический анализ по функциональным группам (1983) — [ c.0 ]
Биоорганическая химия (1991) — [ c.189 , c.190 , c.228 , c.333 ]
Органическая химия Часть 2 (1994) — [ c.225 , c.226 ]
Химия Краткий словарь (2002) — [ c.124 ]
Основы современной химии гетероциклических соединений (1971) — [ c.0 ]
Органическая химия Том1 (2004) — [
c. 58
]
58
]
Справочник Химия изд.2 (2000) — [ c.498 ]
Катализ в неорганической и органической химии книга вторая (1949) — [ c.40 , c.601 ]
Органическая химия (1964) — [ c.82 , c.83 ]
Алюмогидрид лития и его применение в органической химии (1957) — [ c.135 ]
Основы органической химии (1983) — [ c.153 , c.155 , c.166 , c.184 , c.323 ]
Механизмы реакций в органической химии (1991) — [ c.245 ]
Межфазный катализ в органическом синтезе (1980) — [
c. 71
,
c.309
]
71
,
c.309
]
Электрохимический синтез органических веществ (1976) — [ c.170 ]
Методы эксперимента в органической химии Часть 2 (1950) — [ c.274 ]
Основы органической химии 1 Издание 2 (1978) — [ c.488 ]
Органикум Часть2 (1992) — [ c.2 , c.69 ]
Химия илидов (1969) — [ c.0 ]
Органическая химия (1972) — [ c.304 ]
Комплексные гидриды в органической химии (1971) — [ c.224 ]
Электрохимический синтез органических веществ (1976) — [ c.170 ]
Химия координационных соединений (1985) — [
c.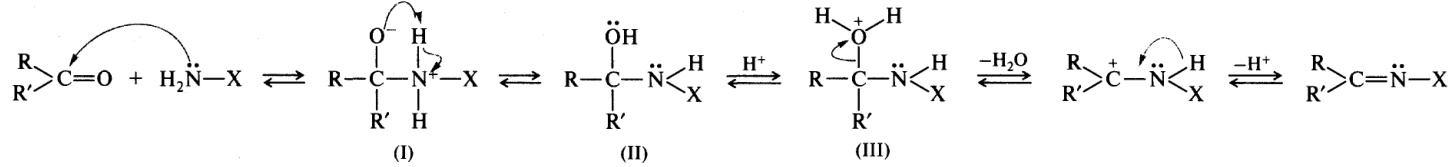 354
,
c.355
]
354
,
c.355
]
Органическая химия (1972) — [ c.304 ]
Органическая химия Издание 2 (1976) — [ c.312 ]
Органическая химия Том 1 (1963) — [ c.537 , c.631 ]
Новые воззрения в органической химии (1960) — [ c.297 ]
Катализ в химии и энзимологии (1972) — [ c.152 , c.157 , c.192 ]
Органическая химия (1964) — [ c.82 , c.83 ]
Справочное руководство по эпоксидным смолам (1973) — [ c.87 ]
Акваметрия (1952) — [
c. 397
]
397
]
Органическая химия Том 1 (1962) — [ c.537 , c.631 ]
Курс физической органический химии (1972) — [ c.481 ]
Синтезы органических препаратов Сборник 3 (1952) — [ c.0 ]
Биохимия Издание 2 (1962) — [ c.360 ]
Определение строения органических соединений (2006) — [ c.12 , c.130 , c.217 , c.278 ]
Иммобилизованные ферменты (1987) — [ c.91 ]
Имины получение – Справочник химика 21
Его применяют при аллергиях (бронхиальной астме, сенной лихорадке и др. ) так же, как и адреналин. Синтезируют рацемический эфедрин (псевдоэфедрин) действием метиламина на I-фенил-1,2-пропандион с последующим восстановлением промежуточного имина. Адренэргическим и сосудосуживающим действием обладает также и норэфедрин (7). Первая стадия его синтеза заключается в конденсации бензальдегида с нитроэтаном, которая проводится в присутствии водного карбоната калия при комнатной температуре в атмосфере азота. Полученный при этом нитроспирт затем восстанавливают в амин (7) в системе 2п/АсОН [c.57]
) так же, как и адреналин. Синтезируют рацемический эфедрин (псевдоэфедрин) действием метиламина на I-фенил-1,2-пропандион с последующим восстановлением промежуточного имина. Адренэргическим и сосудосуживающим действием обладает также и норэфедрин (7). Первая стадия его синтеза заключается в конденсации бензальдегида с нитроэтаном, которая проводится в присутствии водного карбоната калия при комнатной температуре в атмосфере азота. Полученный при этом нитроспирт затем восстанавливают в амин (7) в системе 2п/АсОН [c.57]
При реакции аминов с альдегидами и кетонами образуются продукты присоединения, известные под названием иминов или оснований Шиффа (разд. 7.3,Г и 8.4,В). Имины, полученные из алифатических альдегидов и первичных аминов, обычно неустойчивы и полимеризуются или реагируют далее с амином с образованием более сложных продуктов. Однако имины, полученные из ароматических альдегидов, таких, как бензальдегид, часто стабильны, так же как и оксимы и гидразоны (разд.
 7.3,Г). Образование иминов — процесс обратимый, и из них часто можно регенерировать альдегиды или кетоны гидролизом водной кислотой. [c.155]
7.3,Г). Образование иминов — процесс обратимый, и из них часто можно регенерировать альдегиды или кетоны гидролизом водной кислотой. [c.155]Основания Шиффа легко алкилируются с образованием четвертичной соли имина, при гидролизе которой получается вторичный амин. Этот метод особенно часто используют для получения смешанных алифатических вторичных аминов. На первой стадии удовлетворительные результаты получаются только для иодистого метила [35]. Используя на первой стадии диалкилсульфат [36], удается успешно ввести как метилвную, так и этильную группы. Второй метод более прост, поскольку для его выполнения не требуется аппаратуры, способной выдерживать давление, но он дает более низкие выходы и более загрязненные продукты, чем метод с применением иодистого алкила [37]. Для ряда смешанных алифатических вторичных аминов, полученных алкилированием иодистым метилом, выходы составляли 52—93% [37]. [c.502]
Механизм реакции довольно сложен и не до конца выяснен [323]. На первой стадии субстрат атакуется частицей, содержащей нитрил и НС1 (и кислоту Льюиса, если таковая присутствует), давая соль имина (39). Атакующими частицами могут быть 37 или 38. На второй стадии полученная соль гидролизуется до продуктов [c.371]
Получение и реакции иминов [c.215]
В СВОЮ очередь вторичный амин может реагировать либо с альдегидом, либо с имином полученные продукты восставав вливаются в третичные амины [c.348]
Своеобразную пространственную структуру имеют имины, полученные из кетенов их кумулированные двойные связи создают условия для существования оптических антиподов (34а) и (346), напоминающих алленовые. Барьер рацемизации невелик (40—50 кДж/моль). [c.339]
Производное пятичленного гетероцикла, содержащее в цикле четыре атома азота, – 1,5-пентаметилентетразол (коразол, 172) применяют в качестве аналептика ( пробуждающего средства центрального действия) при угнетении сердечно-сосудистой системы и дыхания, а также при отравлениях наркотиками и снотворными. Синтезируют коразол действием избытка азотистоводородной кислоты на циклогексанон в присутствии хлорида цинка или пентаоксида фосфора. Полагают, что вначале образуется иминная форма капролактама, циклоконденсация которой со второй молекулой исходной кислоты приводит к получению сти.мулятора (172) [c.110]
Синтезируют коразол действием избытка азотистоводородной кислоты на циклогексанон в присутствии хлорида цинка или пентаоксида фосфора. Полагают, что вначале образуется иминная форма капролактама, циклоконденсация которой со второй молекулой исходной кислоты приводит к получению сти.мулятора (172) [c.110]
Нитрилы гидрируются в амины на платиновых и родиевых катализаторах при температуре 25 °С и давлении 1-3 атм и на скелетном никеле при 25-150 °С и 1-270 атм. Применяются также бориды никеля, кобальтовые и поверхностные палладиевые катализаторы. Восстановление протекает ступенчато. Первичный амин, образующийся в результате присоединения к нитрилу 2 моль водорода, способен присоединяться к промежуточному имину, что в конечном счете приводит к получению смеси первичного, вторичного и даже третичного аминов реакции конденсации с повышением температуры интенсифицируются [c.62]
Принципиально новым и оригинальным направлением в области создания ингибиторов, пригодных для одновременной защиты черных и цветных металлов, является получение солей аминов, иминов и других органических оснований с нитро- и динитробензойными кислотами.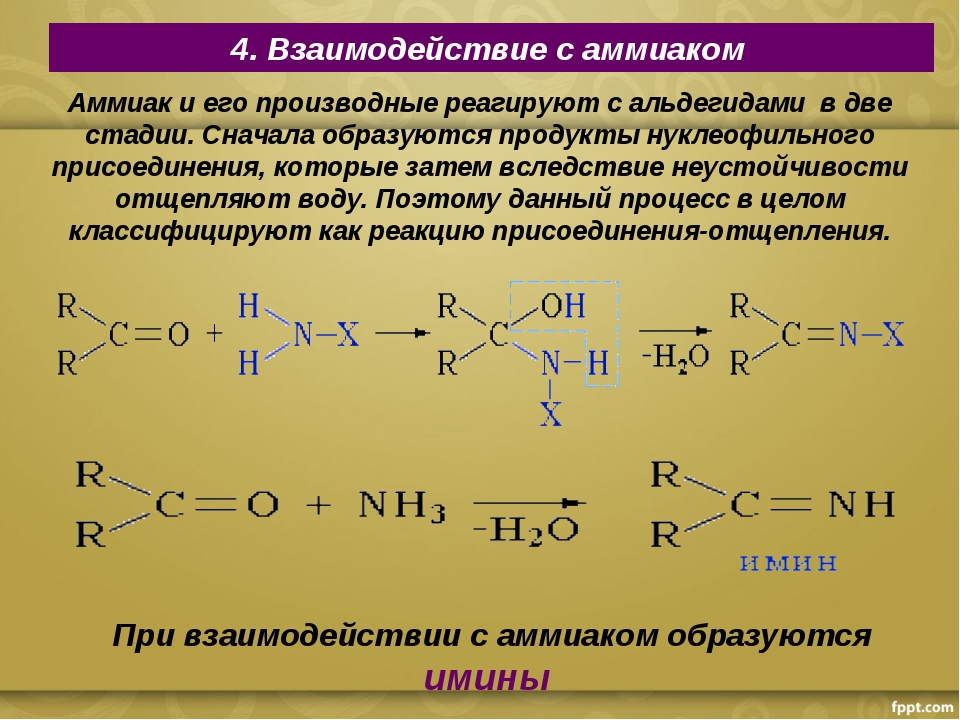 Данное направление детально разработано Институтом физической химии АН СССР [93 144]. [c.124]
Данное направление детально разработано Институтом физической химии АН СССР [93 144]. [c.124]
Несимметрично замещенные по атому углерода оксазиридины имеют асимметрический атом углерода, и частичное разделение 2-бутил-З-изобутил-З-метилоксазиридина на оптические изомеры при стереоселективном окислении его в присутствии бруцина является доказательством циклического строения этих соединений. Оксазиридины с хиральностью, обусловленной только асимметрией при трехковалентном атоме азота, были получены окислением иминов оптически активными пероксикислотами, например ( + )-пероксикамфорной кислотой. Окисление пероксикислотами иминов, полученных из оптически активных аминов, дало высокие оптические выходы диастереомеров, что свидетельствует о хиральности как при атоме азота, так и в углеродной цепи исходного амина. [c.675]
Для амидов или иминов, полученных при взаимодействии 2-арилэтиламинов с производными карбоновых кислот или альдегидами, возможно замыкание цикла, приводящее к 3,4-дигидро- или 1,2,3,4-тетрагидроизохинолинам соответственно. Последующее окисление позволяет получать таким образом ароматические производные изохинолина. [c.186]
Последующее окисление позволяет получать таким образом ароматические производные изохинолина. [c.186]
Это объяснение, которое, возможно, и оправедливо для КО М- нлек сообразования с объемистым триметилбором, не в скрывает, однако, общих закономерностей изменения электронодонорных сво йств циклических иминов в зависимости от величины цикла. Соответствующие причины, скорее, следует искать в различном характере распределения электронов, присущем этим циклам. Эта наиболее общая и фундаментальная причина была вскрыта при исследовании [82] химических сдвигов в ЯМР-спектрах циклических иминов. Полученные результаты представляют прямое физическое доказательство распределения электронов у атома азота в зависимости от величины цикла и показывают, что минимальную электронную плотность имеет атом азота трехчленного цикла этиленимина. В силу этого для него следует ожидать минимальной способности к присоединению протона и, следовательно, минимальной основности. [c. 65]
65]
Используя менее активные производные, например НЬ1А1(ОС2Н5)з, можно задержать реакцию на первой стадии имин, полученный таким образом, гидролизуется до альдегида. [c.490]
В разд. 6-3.1. Другой пример обращения копфр1гурации при изменении природы растворителя найден при изучении гидрирования и гидрогенолиза имина, полученного из (В)- (+)-а-метилбензил-амина и а-кетоглутаровой кислоты [126]. В среде этанола образуется (5 )-(+)-глутаминовая кис.тота (13% и.э.), а в диоксане получается избыток i -(—)-энантиомера (19% и.э. ср. разд. 7-2.2). [c.54]
Харада и сотр. [33, 40], Хиски и Нортроп [30] изучили гидрирование оксимов и иминов, полученных из менти.лпирувата или из хиральных амидов пировиноградной кислоты. [c.370]
На первой стадии под действием сильно кислой среды (безводная фосфорная кислота) происходит отщепление иона гидроксила. Образовавшийся положительно заряженный атом азота присоединяет гидридион, отщепляющийся от соседнего атома углерода, а полученный при этом карбокатион V теряет протон и образует имин VI. В присутствии уксусного ангидрида образуется ацетильное производное а-комплекса VII, из которого при изомеризации получается 3,4-диалкилацетанилид. [c.134]
В присутствии уксусного ангидрида образуется ацетильное производное а-комплекса VII, из которого при изомеризации получается 3,4-диалкилацетанилид. [c.134]
В синтезе азотсодержащих производных очень важны пеизогипсические трансформации азотсодержащих функций различных уровней окис.тения. Так, обычным путем получения аминов является восстановление производных кислот (нитри.тов или амидов) или карбопи, гьных соеди-пепий (иминов), [c.114]
Обычные первичные и вторичные галогениды дают главным образом продукты М-алкилирования, особенно в случае енаминов, полученных из альдегидов. Продукты алкилирования первичными и вторичными галогенидами можно получить с хорошими выходами другим методом, а именно алкилированием солей енаминов, которые получают [173] обработкой имина этил-магнийбромидом в тетрагидрофуране [174] [c.444]
Имины получают по реакции 16-14. Метод, основанный на реакции с солью енамина, был также успешно использован для моно-а-алкилирования а,р-ненасыщенных кетонов [175].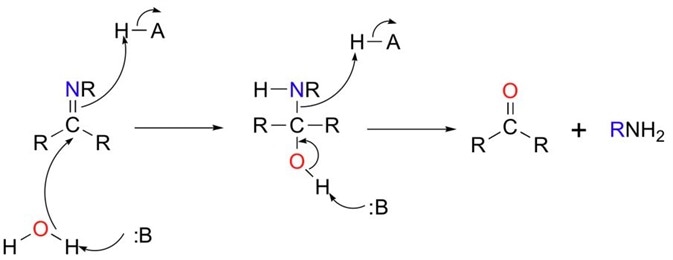 Енамины, полученные из альдегидов и бутилизобутиламина, можно алкилировать с хорошими выходами простыми первичными алкилгалогенидами [176]. В этом случае Ы-алкилированию, по-видимому, препятствуют стерические затруднения. [c.444]
Енамины, полученные из альдегидов и бутилизобутиламина, можно алкилировать с хорошими выходами простыми первичными алкилгалогенидами [176]. В этом случае Ы-алкилированию, по-видимому, препятствуют стерические затруднения. [c.444]
Соединение состава N2F2 — дифтордиазин — образуется в качестве одного из продуктов при электролизе аммоний-гидродифторида (доп. 73) или действии фтора на натрийазид. Более прямым путем его получения является взаимодействие фто[> имина (доп. 81) с очень тщательно высушенным калийфторидом по уравнению [c.405]
Из электрохимических производств, основанных на использовании электролиза для проведения окислительных или восстановительных реакций, можно назвать электрохимическое окисление Na l в Na lOa производство перхлоратов окислением хлоратов электрохимическое получение хлорной кислоты при обессоливании морской и минерализованных вод электролизным методом получение диоксида хлора и т.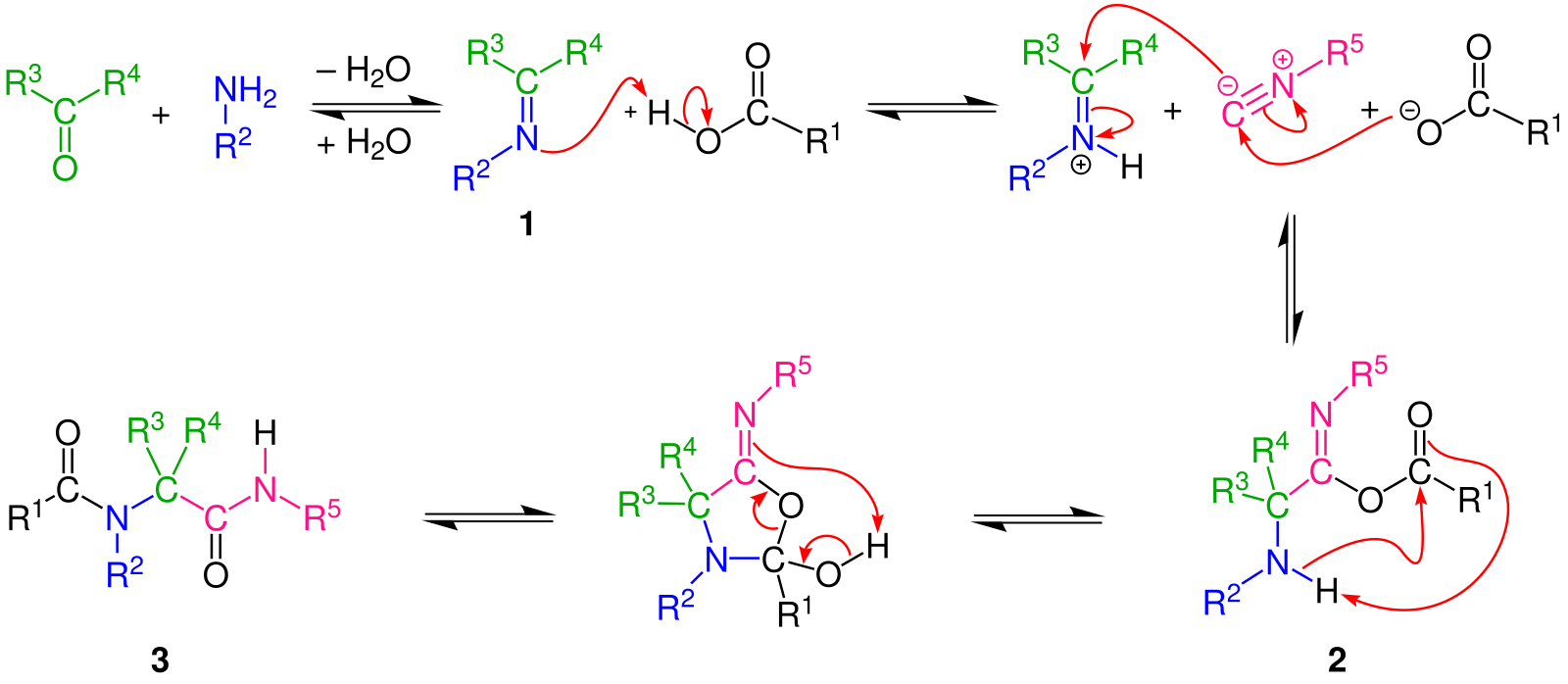 д. В органической химии процессы электролиза используются в реакциях катодного восстановления нитросоединений, иминов, имидоэфиров, альдегидов и кетонов, карбоновых кислот, сложных эфиров, а также в реакциях анодного окисления жирных кислот и их солей, ненасыщенных кислот ароматического ряда, ацетилирова-ния, алкилирования и др. [c.357]
д. В органической химии процессы электролиза используются в реакциях катодного восстановления нитросоединений, иминов, имидоэфиров, альдегидов и кетонов, карбоновых кислот, сложных эфиров, а также в реакциях анодного окисления жирных кислот и их солей, ненасыщенных кислот ароматического ряда, ацетилирова-ния, алкилирования и др. [c.357]
Иминный водородный атом амидной связи подвижен и может быть замещен на различные радикалы. На этом основаны многочисленные реакции полиамидов, например реакция оксиэтилирования, которая приводит к получению производных с ценными свойствами. [c.260]
Рассмотрены реакции олигомеров е-аминокапроновой кислоты для получения иминов с широким спектром медико-биологической активности. Так, оротовый альдегид образует имины с указанными олигомерами, обладающие высокой антивирусной и антитоксичной активностью. Установлено, что каталитическая реакция аллилового спирта и его сложных эфиров с е-капролактамом сопровождается аллильной перегруппировкой. что способствует олигомеризации аллиловым спиртом и получению Ы-ацилпроизводных аллилтовых эфиров е-аминокапроновой кислоты. [c.53]
что способствует олигомеризации аллиловым спиртом и получению Ы-ацилпроизводных аллилтовых эфиров е-аминокапроновой кислоты. [c.53]
С целью разработки методов получения молекулярно-организованных металлокомплексных систем с векторным фото- и элеюростимуллированным переносом заряда и энергии в настоящей работе на основе смешанно-лигандньпс циклометаллированных комплексов платиновых металлов 1ТЧ(11), Ргетероциклическими иминами – депротонированные формы 2- [c.51]
Более далекое расположение иминного фрагмента от фуранового цикла повышает антибактериальное действие нитрофуранов. Получен ряд препаратов, например фурагин (12), его водо- [c.89]
Оно также обладает ненаркотическим анальгетическим действием и ингибирует биосинтез простагландинов. В основе промышленного метода его синтеза лежит реакция Фишера. Необходимое для этого основание Шиффа получают конденсацией параметоксифенилгидразина (78) с метилатом 3-ацетилпропио-новой кислоты (79) в уксусной кислоте. Образовавшийся имин кипятят в смеси этанола с соляной кислогой, а полученный таким образом эфир индолилуксусной кислоты подвергают ше-лочному гидролизу до свободной кислоты (80). Затем индол (80) ацилируют п-хлорбензоилхлоридом в присутствии гидрида натрия до индометацина (81) [c.99]
Образовавшийся имин кипятят в смеси этанола с соляной кислогой, а полученный таким образом эфир индолилуксусной кислоты подвергают ше-лочному гидролизу до свободной кислоты (80). Затем индол (80) ацилируют п-хлорбензоилхлоридом в присутствии гидрида натрия до индометацина (81) [c.99]
Разработано несколько промышленных путей синтеза цикло-серина. Один из них основан на хлорировании акрилата (91) до дигалогенида (92), в котором региоселективно замещают атом хлора при С-3 на аминооксигруппу [действием О-натриевого производного оксима ацетона (93) с последующим гидролизом имина (94)[. Затем второй атом хлора в промежуточном монохлориде замещают на аминофуппу и полученный таким образом аминоэфир (95) циклизуют в щелочной среде в циклосерин (96) [c.102]
Общая схема получения барбитуратов (211) основана на циклоконденсации замещенных эфиров малоновой кислоты с мочевиной или гуанидином в присутствии этоксида натрия В первом случае образуется промежуточная натриевая соль (210), а во втором – промежуточный имин (212), которые затем переводят в уреиды (211) [c. 148]
148]
Триаминозамещенный птерин (315) используют в качестве диуретика под названием триамтерен. Его синтезируют из пиримидина (310) конденсацией с бензальдегидом. Основание Шиффа образуется региоселективно с наиболее основной из четырех присутствующих аминогрупп, а именно с той, которая находится в (З-положении к циклическим атомам азота и не может участвовать в образовании таутомерных иминов. Альди-минную фуппу затем цианируют и полученный продукт (314) конденсируют внутримолекулярно под действием щелочи [c.170]
Имины
01 марта 2011Издательство полиграфия зеленоград Типография Копи77.
Оглавление:
1. Имины
2. Синтез
Структура иминов. Иминогруппа выделена синим.
органические соединения общей формулы RRC=NR, где R, R H, Alk, Ar и R H, Alk, Ar, азотистые аналоги альдегидов и кетонов, содержащие фрагмент NR, соединенный двойной связью с атомом углерода.
К иминам относятся также азометины.
В систематической номенклатуре IUPAC суффикс -имин используется для обозначения группы C=NH.
Реакционная способность
Атом азота в иминах слабонуклеофилен, атом углерода – электрофилен.
Имины обладают слабоосновными свойствами и в отсутствие воды могут протонироваться и алкилироваться по атому азота с образованием иминиевых солей:
- R2C=NR + RHal R2C=NRR•Hal
Иминиевые соли также образуются при алкилировании и ацилировании иминов, продукты алкилирования могут быть выделены, в случае ацилирования промежуточно образующиеся ацилиминиевые соли циклизуются в β-лактамы
Реакции иминов с нуклеофилами протекают по атому углерода, весьма разнообразны и широко используются в органическом синтезе.
Так, имины гидролизуются водой с образованием карбонильных соединений и аминов, эта реакция обратна реакции синтеза иминов:
- R2C=NR + H2O R2C=O + RNH2
Реакции иминов с аминами приводят к образованию аминалей:
- R2C=NR + RNH2 R2C2
Реакция иминов с цианистым водородом либо триметилсилилцианидом является вариантом реакции Штреккера и, в случае N-замещенных иминов, может служить методом синтеза N-замещенных α-аминокислот:
- R2C=NR + HCN R2CCN
- R2CCN + 2H2O R2CCOOH + NH3
Взаимодействие реактивов Гриньяра и литийорганических соединений с иминами ведет к C-алкилированию последних с образованием аминов:
- R2C=NR + RLi R2RCN R Li
- R2RCN R Li + H2O R2RCNHR + LiOH
Имины вступают в различные реакции циклоприсоединения, образуя с карбенами продукты-циклоприсоединения – азиридины, с кетенами идет-циклоприсоединение с образованием азетидин-2-оны:
С 1,3-диполярными соединениями образуются пятичленные гетероциклы – продукты-циклоприсоединения.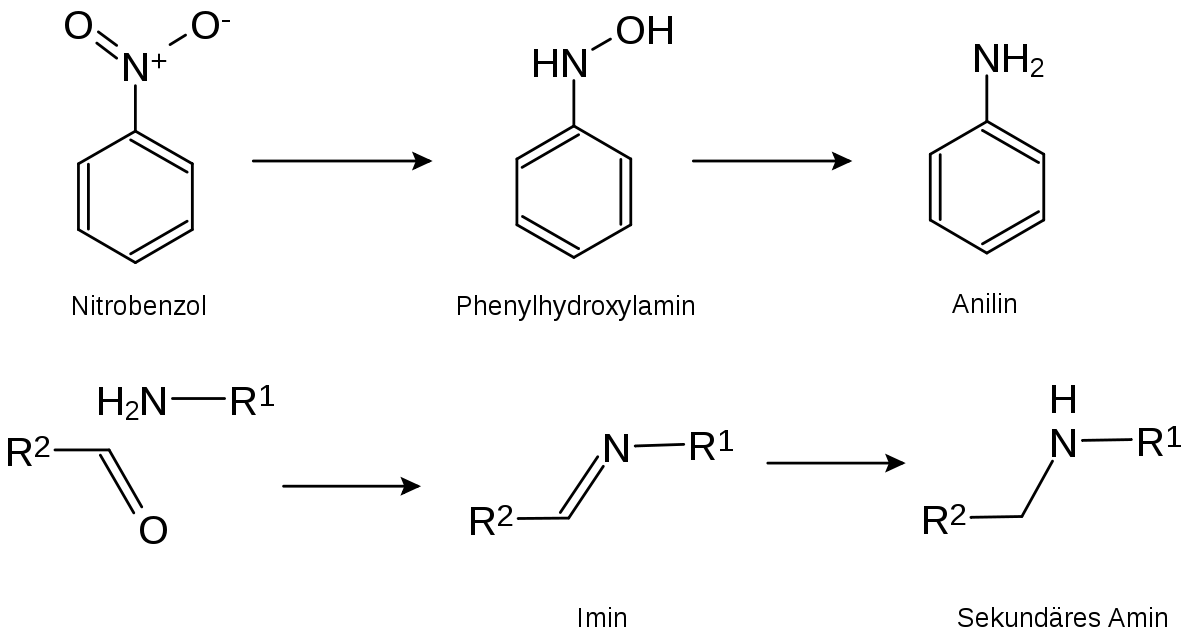
Имины также могут выступать в роли диенофилов в реакции Дильса-Альдера:
Под действием энергичных восстановителей имины восстанавливаются до вторичных аминов:
- R2C=NR + R2CH-NHR
Имины, образованные из енолизирующихся карбонильных соединений, способны к имин-енаминной таутомерии:
Просмотров: 4273
Изучение влияния компексообразования на реакционную способность оснований Шиффа и диастереоселективность реакции имин-кетенового циклоприсоединения по Штаудингеру
Да, при использовании комплексообразования суммарный химический выход β-лактамов уменьшается. Мы предполагаем, что это связано с неполной конверсией на стадии комплексообразования, необходимостью проведения реакций имин-кетенового циклоприсоединения при повышенной температуре, обеспечивающей разрушение комплекса и образование свободного имина, а также введением дополнительной стадии очистки от соединений меди путем экстракции. При исследовании возможностей комплексообразования целевых β-лактамов также было обнаружено, что они способны образовывать координационные соединения меди (II), однако такие реакции протекают очень медленно и с очень низкой степенью конверсии (контроль осуществлялся по ТСХ, выделить комплекс β-лактама пока не удалось).
При исследовании возможностей комплексообразования целевых β-лактамов также было обнаружено, что они способны образовывать координационные соединения меди (II), однако такие реакции протекают очень медленно и с очень низкой степенью конверсии (контроль осуществлялся по ТСХ, выделить комплекс β-лактама пока не удалось).
В дальнейшем планируется предпринять ряд мер для увеличения суммарного выхода реакций. Во-первых, планируется вводить комплексообразователь на стадии получения имина для смещения направления реакции в сторону образования E-изомера. Во-вторых, для связывания меди планируется при проведении экстракции использовать водный раствор ЭДТА. В-третьих, планируется оптимизировать финальную стадию для поиска оптимальных условий получения β-лактамов из комплексов иминов.
Из литературы известно, что имины VI могут образовывать кординационные соединения с различными металлами (Cu, Pr, Co, Ni, Zn и др.), поэтому мы также рассматриваем возможность использования другого комплексообразователя и руководствуемся при этом некоторыми наблюдениями. Поскольку имин является достаточно крупным бидентатным лигандом, мы предполагаем, что использование комплексов, включающих трех и более иминовых лигандов будет приводить к меньшим выходам из-за стерической затрудненности вхождения имина в координационную сферу металла (для комплекса PrL3 выход составил всего 52%). К тому же, более приоритетными являются диамагнитные комплексообразователи, которые позволят избежать уширения сигналов в спектрах ЯМР 1Н, затрудняющего идентификацию и анализ продукта. Также необходимо, чтобы комплекс разрушался в условиях проведения реакции циклоприсоединения, что накладывает определенные ограничения на прочность комплекса. Поэтому следующим металлом, который планируется опробовать в качестве комплексообразователя, является Cu (I), соответствующий вышеперечисленным требованиям.
Поскольку имин является достаточно крупным бидентатным лигандом, мы предполагаем, что использование комплексов, включающих трех и более иминовых лигандов будет приводить к меньшим выходам из-за стерической затрудненности вхождения имина в координационную сферу металла (для комплекса PrL3 выход составил всего 52%). К тому же, более приоритетными являются диамагнитные комплексообразователи, которые позволят избежать уширения сигналов в спектрах ЯМР 1Н, затрудняющего идентификацию и анализ продукта. Также необходимо, чтобы комплекс разрушался в условиях проведения реакции циклоприсоединения, что накладывает определенные ограничения на прочность комплекса. Поэтому следующим металлом, который планируется опробовать в качестве комплексообразователя, является Cu (I), соответствующий вышеперечисленным требованиям.
Preparation of Chitosan-based Injectable Hydrogels and Its Application in 3D Cell Culture
Гидрогель, представленные в настоящем Протоколе (рис. 1) имеет два основных компонента: Хитозан гликоль природный полимер и синтетических бензальдегида прекращено полимера gelator DF PEG, которые оба биосовместимых материалов.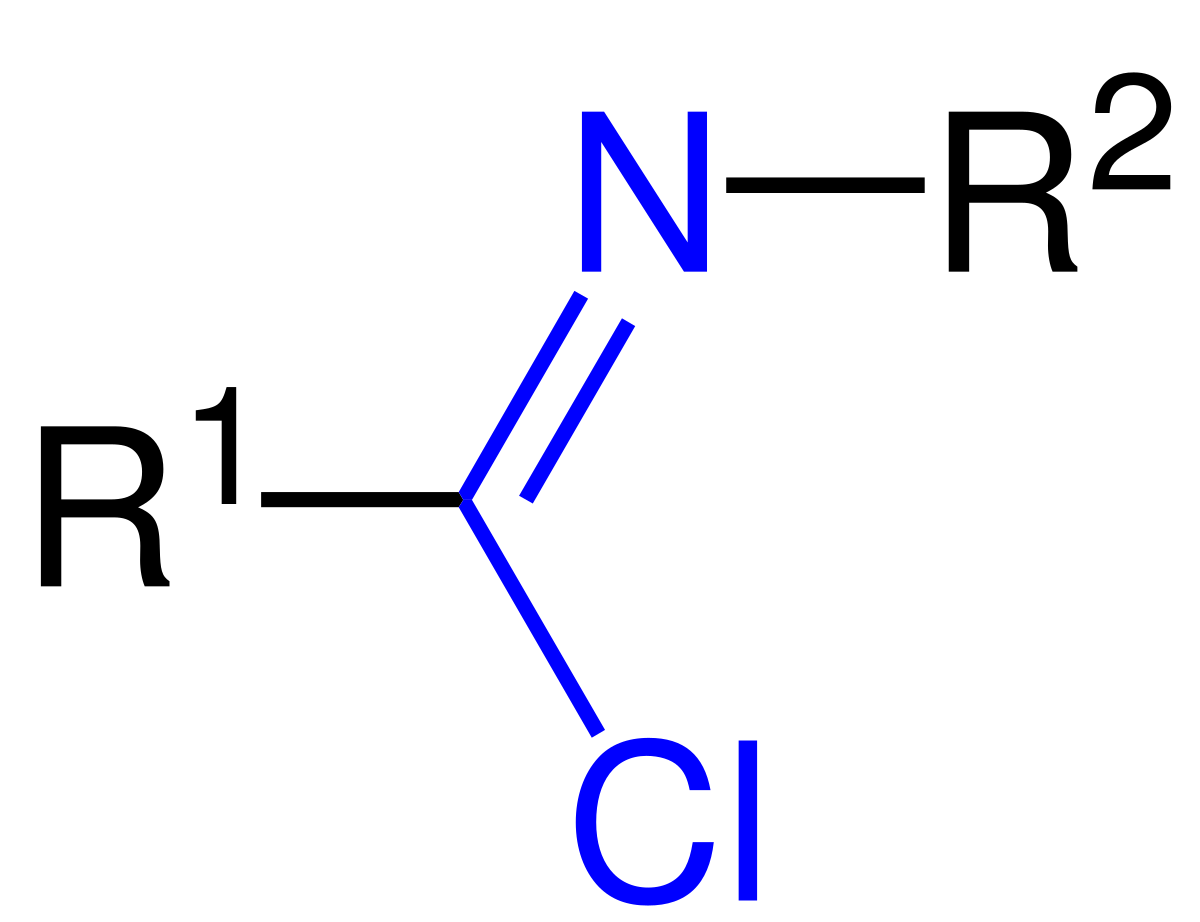 Синтез DF PEG представлены с использованием реакции модификации одношаговый. PEG молекулярной массой 4000 был выбран в этом протоколе проблемы растворимость, эффективность модификации, а также жесткость гидрогеля. Серия гидрогели с различных механических сильные были подготовлены с использованием различных твердых содержание и соотношения гликоль хитозана и DF КОЛЫШЕК. Однородной гидрогели быстро были сформированы в минутах, смешивая гелеобразования решения при комнатной температуре, хотя гелеобразования скорость может также замедлить, растворы. Реологические свойства теста использовалась для оценки механических сильные стороны различных гидрогели. Хранения модулей (G’) этих гидрогелей были обнаружены приблизительно отличаются от 900 ПА (мягкие), 2100 ПА (средний) 4700 ПА (жесткая) (Таблица 1 и рис. 2A). Это привело к более высокой плотности сшивки, добавив больше полимера gelators в сети гидрогеля, что приводит к более высоких хранения модуля (большей жесткости).
Синтез DF PEG представлены с использованием реакции модификации одношаговый. PEG молекулярной массой 4000 был выбран в этом протоколе проблемы растворимость, эффективность модификации, а также жесткость гидрогеля. Серия гидрогели с различных механических сильные были подготовлены с использованием различных твердых содержание и соотношения гликоль хитозана и DF КОЛЫШЕК. Однородной гидрогели быстро были сформированы в минутах, смешивая гелеобразования решения при комнатной температуре, хотя гелеобразования скорость может также замедлить, растворы. Реологические свойства теста использовалась для оценки механических сильные стороны различных гидрогели. Хранения модулей (G’) этих гидрогелей были обнаружены приблизительно отличаются от 900 ПА (мягкие), 2100 ПА (средний) 4700 ПА (жесткая) (Таблица 1 и рис. 2A). Это привело к более высокой плотности сшивки, добавив больше полимера gelators в сети гидрогеля, что приводит к более высоких хранения модуля (большей жесткости). Свойство самостоятельно обратимо подтверждается также восстановления гидрогеля модуль (рис. 2B). Известно, что жесткость ECM, отличается для различных тканей, таким образом гидрогеля может предложить регулируемый механический подсказки и требованиям различных исследовательских разнообразный соотношения между гликоль хитозана и DF PEG полимера gelators18.
Свойство самостоятельно обратимо подтверждается также восстановления гидрогеля модуль (рис. 2B). Известно, что жесткость ECM, отличается для различных тканей, таким образом гидрогеля может предложить регулируемый механический подсказки и требованиям различных исследовательских разнообразный соотношения между гликоль хитозана и DF PEG полимера gelators18.
L929 клетки, линии клеток фибробластов обычно мышь с в естественных условиях окружающей среды ткани жесткость ~ 5600 ПА19, была использована в качестве модели клетки должен быть внедрен в гидрогеля. После инкапсуляции клеток в гидрогели, его можно легко заметить что клетки в гидрогели показали чрезвычайно высокой жизнеспособности (> 99%) на протяжении всего процесса культуры, подтверждающий отличная биосовместимость гидрогеля на основе хитозана. Значительное увеличение плотности клеток в гидрогеля подразумевает, что этот Гидрогель может поддержать пролиферации L929 клеток, даже без загородный Добавлено факторы роста (Рисунок 3А).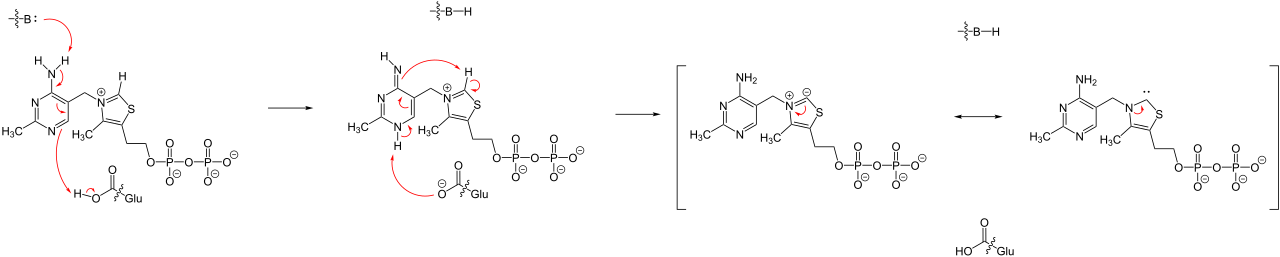 После 7 дней в культуре в гидрогеля 300% (рис. 3B) увеличение числа клеток. Сообщается, что клетки культивировали в леса можно различать следующие механические сигналы20,21, который может подразумевать дальнейшие исследования, с помощью этого метода культуры 3D гидрогеля.
После 7 дней в культуре в гидрогеля 300% (рис. 3B) увеличение числа клеток. Сообщается, что клетки культивировали в леса можно различать следующие механические сигналы20,21, который может подразумевать дальнейшие исследования, с помощью этого метода культуры 3D гидрогеля.
Имплантация клеток с инъекционными гидрогели приобрела несравненный преимущества значительно повысить эффективность поставок и жизнеспособности имплантированные клетки14. В рамках сети высокоструктурированные динамической иминного гидрогеля может self-heal после инъекции. Самостоятельно обратимо свойство позволяет Гидрогель для инъекций, который подразумевает потенциальных приложений для гидрогели как инъекционные несколько перевозчиков. Для дальнейшей оценки этот Гидрогель как носитель инъекционные ячейки, подражая инъекции и после культивирования эксперимент была выполнена. Гидрогель клетки встроенных была загружена в шприц и выдавливается через 48 G иглу в чашку Петри, после 7 день после культивирования процесса с ячейки жизнеспособность и распространения ставкой учился.
Как показано на рисунке 4A, сплющенные гидрогеля штук может self-heal реформы комплексной гидрогеля около 1 ч после инъекции, которая полезна в ячейке доставки. Для ячеек в гидрогеля когда по сравнению с изображения взял сразу после инкапсуляции (Рисунок 4A, левый Вставка), плотность ячеек, резко после 7 дней (Рисунок 4A, средняя Вставка). В расширенном видения, более подробный клеток fissional процесс, в котором находятся некоторые клетки должен быть разделен на два (рис. 4A, правый Вставка), непосредственно подтверждается 3D пролиферации в гидрогеля. Рисунок 4B показывает конфокальный изображения жить мертвых клеток анализов после инъекции и культуры после эксперимента. Плотность клеток вводили увеличилась очевидно с жизнеспособность высокой клеток (> 99%), демонстрируя успешное пролиферации в 3D гидрогеля после инъекции. Чтобы узнать, был ли инъекции влияют темпы распространения клеток, сравнение количественного статистического анализа для ставок распространения клеток в гидрогели, с или без инъекций выполнена (рис.
Мы описали Типичная процедура применения гидрогеля, но исследователи могут изменить протокол в соответствии с требованиями конкретных исследований. Полимерные gelators имеют значительное влияние на гидрогеля и легко изменяемые. Например жесткость этот Гидрогель могут быть легко манипулировать различных соотношениях гликоль хитозана и DF PEG gelator. Между тем использование ПЭГ DF других молекулярных масс также может выполнить эту цель. Мы использовали PEG 4K в настоящем Протоколе, но может также работать PEG 2K до 10K. При использовании других колышки, важно контролировать время гелеобразования и жесткость специально. Другие функциональные полимерные gelators также могут работать, если исследователи имеют навыки синтеза для подготовки конкретных функциональных полимеров Бензойный альдегид прекращено17.
Этот протокол имеет ряд ограничений. Во-первых из-за динамической структуры, жесткость этот Гидрогель ограничен по сравнению с ковалентной связи высокоструктурированные гидрогеля. Один могут возникать сбои подготовить гидрогели с слишком высокий модуль упругости конструкции. Во-вторых этот Гидрогель био разложению, ограничивая таким образом долгосрочные клеточной культуры в рамках гидрогеля. В-третьих гидрогеля предлагает 3D высокоструктурированные культивирования среды, которая имеет проблемы распространения. На сегодняшний день, большинство из био анализы основаны на 2D культуры. 3D структура может помешать дальнейшему клеток, связанных в vivo исследований.
При использовании данного протокола, существует несколько важных шагов, чтобы следовать. Во-первых во время синтеза полимеров gelator DF PEG, обезвоживание очень важно. Во-вторых при выполнении процедуры, связанные с клеток, стерильные операция имеет решающее значение. В-третьих окрашивание время следует хорошо контролируется в гидрогели получить хороший конфокальный изображения.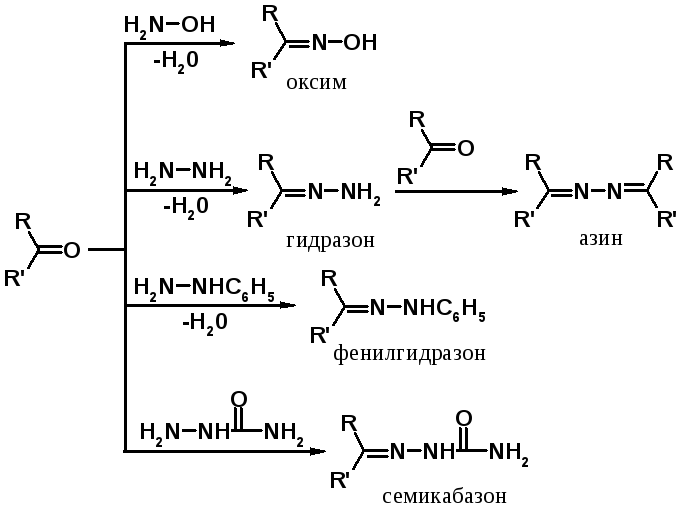
Таким образом протокол представил снисходительный подготовка инъекционные гидрогели на основе хитозана, которые применяются в качестве платформы для 3D клеточной культуры и могли бы предложить регулируемый механический подсказки для различных исследований. Она уже применялась в областях, касающихся доставки лекарств, клеточной терапии и химиотерапии опухоль, которая не только является свидетельством ее производительность, но также увеличивает свой потенциал для биомедицинских apзаявки.
Subscription Required. Please recommend JoVE to your librarian.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie.
 Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie. - Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
10.6: Имины – Химия LibreTexts
Электрофильный атом углерода альдегидов и кетонов может быть мишенью нуклеофильной атаки аминов, а также спиртов. Конечным результатом атаки аминового нуклеофила является функциональная группа, в которой двойная связь C=O заменена двойной связью C=N, известная как имин. (Эквивалентный термин — «основание Шиффа», но в этой книге мы будем использовать термин «имин»). Напомним из раздела 7.5B, что имины имеют pKa примерно 7, поэтому при физиологическом pH они могут быть точно определены как протонированные (форма иминиум-иона) или нейтральные (имин).
Конечным результатом атаки аминового нуклеофила является функциональная группа, в которой двойная связь C=O заменена двойной связью C=N, известная как имин. (Эквивалентный термин — «основание Шиффа», но в этой книге мы будем использовать термин «имин»). Напомним из раздела 7.5B, что имины имеют pKa примерно 7, поэтому при физиологическом pH они могут быть точно определены как протонированные (форма иминиум-иона) или нейтральные (имин).
Образование ионов иминия:
Механизм (ферментативный):
Механически образование имина включает две стадии. Во-первых, азот амина атакует карбонильный углерод на стадии нуклеофильного присоединения (стадия 1), которая очень похожа на образование полуацеталей и полукеталей. Основываясь на ваших знаниях о механизме образования ацеталей и кеталей, вы могли бы ожидать, что следующим шагом будет атака второго амина с образованием соединения с углеродом, связанным с двумя аминогруппами — азотной версией кеталя или ацеталя. Вместо этого то, что происходит дальше (шаг 2 выше), заключается в том, что электроны неподеленной пары азота «отталкивают» кислород от углерода, образуя двойную связь \(C=N\) (иминиум) и смещенную молекулу воды.
Вместо этого то, что происходит дальше (шаг 2 выше), заключается в том, что электроны неподеленной пары азота «отталкивают» кислород от углерода, образуя двойную связь \(C=N\) (иминиум) и смещенную молекулу воды.
Превращение иминия обратно в альдегид или кетон представляет собой гидролитический процесс (связи разрываются молекулой воды), и механически это просто обратный процесс образования иминиума:
Гидролиз иона иминия:
Механизм (ферментативный):
Ферменты, образующие углерод-углеродные связи, называемые альдолазами (которые мы подробно рассмотрим в главе 12), часто образуют иминиевые связи между карбонильным углеродом на субстрате и остатком лизина в активном центре фермента, как в этой альдолазной реакции из Цикл Кальвина:
После завершения углерод-углеродной связи, образующей часть альдолазной реакции, иминиевая связь гидролизуется, высвобождая продукт, так что он может диффундировать из активного центра и позволить начать другой каталитический цикл.
В главе 17 мы узнаем о реакциях, которые зависят от кофермента, называемого пиридоксальфосфатом (\(PLP\)), также известного как витамин \(B6\). В этих реакциях альдегидный углерод \(PLP\) соединяется с ферментативным лизином в активном центре:
Затем \(PLP\)-лизиниминная связь заменяется иминной связью между \(PLP\) и аминогруппой на субстрате, что можно назвать трансиминированием.
Механизм трансиминирования очень похож на механизм образования имина:
Реакция трансформации:
Механизм:
Упражнение 10.6.1
Изобразите имин, который может образоваться между каждой парой соединений.
а.
б.
в.
Упражнение 10.6.2
Нарисуйте продукт гидролиза имминия для каждого из следующих соединений.
- Ответить
Добавьте сюда текст ответа, и он будет автоматически скрыт, если на странице активен шаблон “AutoNum”.

Упражнение 10.6.3
- Метаболический промежуточный продукт, показанный ниже, подвергается внутримолекулярному образованию имина на стадии биосинтеза лизина (КФ 4.3.3.7). Нарисуйте продукт этой стадии образования внутримолекулярного имина.
- Предскажите продукт этой стадии гидролиза иминия (EC 2.3.1.117) по пути деградации пролина.
Авторы и авторство
Имины и енамины
Имины и енамины
Имины представляют собой азотсодержащие аналоги альдегидов и кетонов, содержащие связь C=N вместо связи C=O.Они образуются в результате реакции дегидратации альдегида или кетона с амином. Имины, полученные из альдегидов, иногда называют альдиминами, имины, полученные из кетонов, иногда называют кетиминами. Енамины являются азотистыми аналогами енолов.
В этом посте мы рассмотрим синтез иминов и енаминов и механизм образования иминов.
(часть 5 серии о реакциях нейтральных нуклеофилов с карбонильными соединениями)
Имины и энамины
Люблю органическую химию азота, особенно алкалоиды.На мой взгляд, имины — одна из самых красивых функциональных групп. Я хотел бы рассказать вам обо всех удивительных вещах, которые могут делать имины, но сегодня мы будем очень простыми: мы поговорим о механизмах, участвующих в их формировании.
Что еще за имины? Ну, они выглядят так:
Это имине слева. Справа его химические родственники: оксимы и гидразоны. Их всех объединяет двойная связь C=N, и все они образуются в результате одного и того же процесса.Давайте поговорим о том, как создается C=N.
Реакция начинается с перемешивания альдегида или кетона в растворе с небольшим количеством кислоты. [примечание 1] Вы, возможно, помните, что кислота делает карбонильные атомы углерода более электрофильными — она связывается с карбонильным кислородом и ослабляет связь C=O. Теперь начинается захватывающая часть. При добавлении амина карбонильный углерод (электрофил) атакуется азотом амина (нуклеофил), и происходит 1,2-присоединение. Следующим шагом является перенос протона. Это служит двум целям.Во-первых, OH протонируется с образованием Oh3(+), что является гораздо лучшей уходящей группой. Во-вторых, перенос протона освобождает неподеленную пару азота амина.
Теперь начинается захватывающая часть. При добавлении амина карбонильный углерод (электрофил) атакуется азотом амина (нуклеофил), и происходит 1,2-присоединение. Следующим шагом является перенос протона. Это служит двум целям.Во-первых, OH протонируется с образованием Oh3(+), что является гораздо лучшей уходящей группой. Во-вторых, перенос протона освобождает неподеленную пару азота амина.
Оказавшись снова на свободе, неподеленная пара аминов теперь спускается на соседний углерод подобно рогатой сове, пикирующей на залитую лунным светом полевку, выбрасывая Oh3(+) в виде нейтральной молекулы воды. Последним этапом является простое депротонирование полученного положительно заряженного имина (мы называем его иминий — большинство положительно заряженных органических молекул оканчивается на -ium), в результате чего получается наш нейтральный продукт — имин.На практике эту реакцию обычно проводят с осушителем, таким как сульфат магния, чтобы впитать воду, которая образуется по пути. Это снова принцип Ле Шателье в действии: вы заметите, что реакция представляет собой равновесие. Если вы возьмете свой имин, а затем растворите его в воде, вы можете получить исходный альдегид/кетон плюс амин.
Это снова принцип Ле Шателье в действии: вы заметите, что реакция представляет собой равновесие. Если вы возьмете свой имин, а затем растворите его в воде, вы можете получить исходный альдегид/кетон плюс амин.
Итак, разбивая механистическую последовательность, мы получаем: протонирование/1,2-присоединение/перенос протона/1,2-отщепление/депротонирование . Если присмотреться, то может показаться знакомым: — это точная последовательность из 5 стадий образования сложного эфира из карбоксильной кислоты, гидролиза сложного эфира и гидролиза амида.о которых мы говорили в прошлый раз. Вот: u Под этими четырьмя, казалось бы, разными реакциями вы найдете единство их механизма.
Кстати, реакции образования оксимов и гидразонов протекают точно так же. Основное отличие состоит в том, что гидроксиламин и гидразины более нуклеофильны, чем амины (не на экзамене: альфа-эффект), а продукты более стабильны. В учебных лабораториях вам, возможно, приходилось характеризовать альдегид или кетон, образуя гидразон и измеряя температуру плавления. В частности, гидразоны, образованные 2,4-динитрофенилгидразином (ДНФГ), имеют ярко-красный цвет и часто являются высококристаллическими, что обеспечивает еще один метод анализа.
В частности, гидразоны, образованные 2,4-динитрофенилгидразином (ДНФГ), имеют ярко-красный цвет и часто являются высококристаллическими, что обеспечивает еще один метод анализа.
До сих пор вы могли заметить, что имин, с которым мы имели дело, был первичным амином: связанным только с одним атомом углерода. Что происходит, когда мы имеем дело со вторичным амином? Ну, они тоже образуют связь C=N, но есть ключевое отличие: их нельзя депротонировать на конце, так как у них две связи NC (кстати, это , также называется иминиумом). сделать это соединение нейтральным.Что вы делаете?
Вот как это сделать: депротонировать альфа-углерод. Полученное химическое соединение называется енамин. Енамины во многом похожи на своих химических собратьев, енолов: они нуклеофильны по альфа-углероду и реагируют с электрофилами. Ключевое отличие состоит в том, что они на самом деле более реактивны. Это делает очень полезными химические промежуточные соединения. Вот пример енамина в действии – процесс, впервые подробно продемонстрированный профессором Гилбертом Сторком из Колумбии в 1963 году.Иногда их называют енаминными реакциями Аиста.
Вот пример енамина в действии – процесс, впервые подробно продемонстрированный профессором Гилбертом Сторком из Колумбии в 1963 году.Иногда их называют енаминными реакциями Аиста.
Обратите внимание, что в конце реакции происходит еще одно депротонирование, чтобы вернуть вам нейтральный енамин. Если вам нужно вернуть свой кетон, они будут реагировать с водной кислотой: вы переходите к иминиуму, который затем гидролизуется по механизму, обратному механизму, который я нарисовал для гидролиза имина.
Дополнительная литература: ознакомьтесь с некоторыми удивительными достижениями, которые были обнаружены в каталитической химии енаминов за последние 10 лет или около того.
Примечания
[примечание 1] – кислота не является абсолютным требованием для этой реакции, особенно при образовании имина из альдегидов. Однако кислота ускоряет реакцию при условии, что рН не настолько низок, чтобы амин протонировался.
Проверьте себя!
(Расширенные) Ссылки и дальше чтения
Иминообразование из кетонов (синтез кетимина):
- UEBER DAS Auftreten Von Stereoisomerie Bei Nicht Oximartigen Stickstoffverbindungen
A.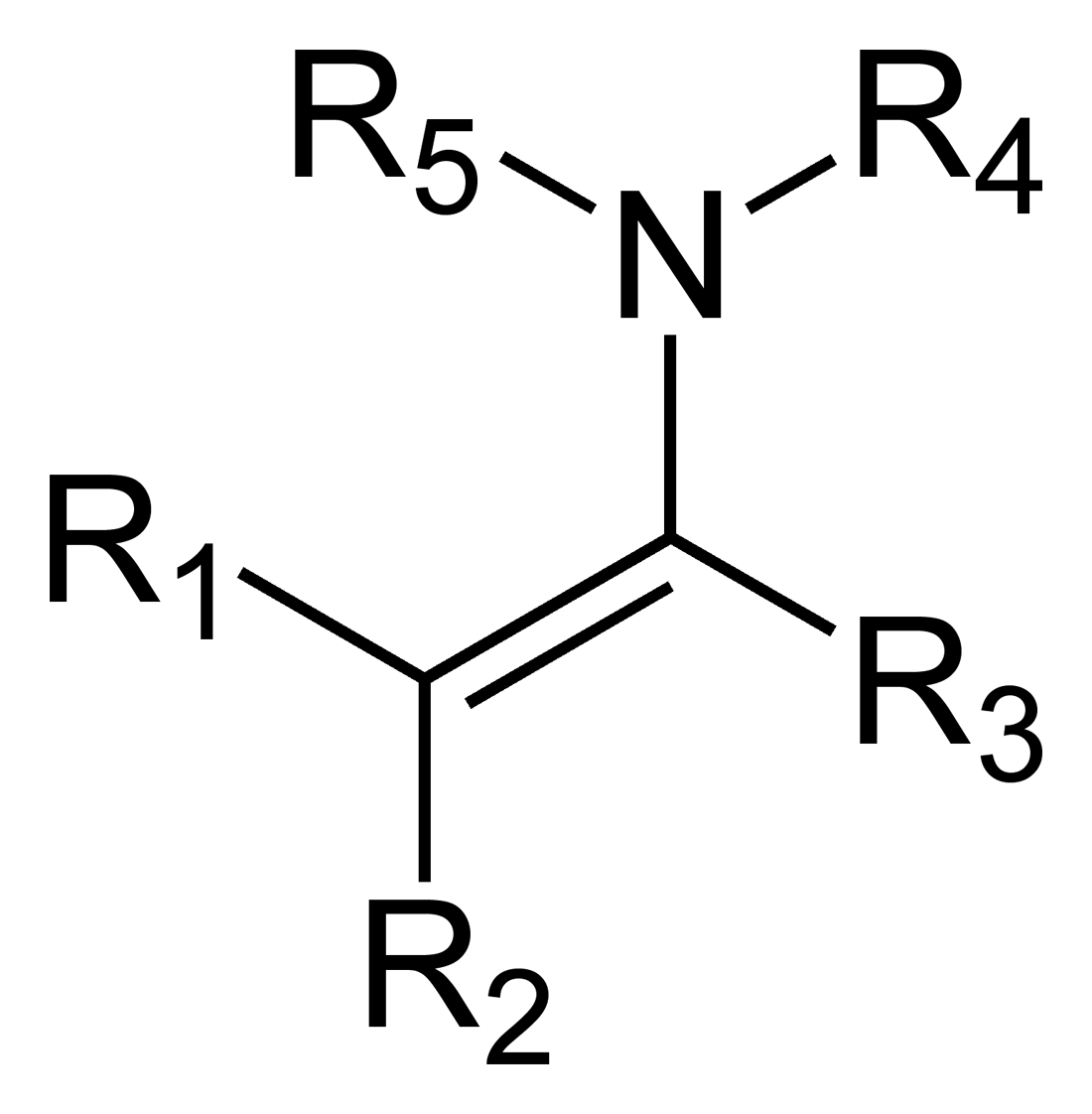 Hantzsch, Friedrich Kraft
Hantzsch, Friedrich Kraft
Chem. Бер. 1891 ; 24 (2): 3511-3528
СООТВЕТСТВУЮЩИЕ ВТОРИЧНЫЕ АМИНЫ
DOUGLAS G. NORTON, VERNON E. HAURY, FRANK C. DAVIS, LLOYD J. MITCHELL и SEAVER A. BALLARD
J. Org.Chem., 1954, 19 (7), 1054-1066
. DOI: 10.1021/jo01372a010
. удалить воду (например, используя ловушку Дина-Старка и азеотропную перегонку воды с бензолом или толуолом). - Стабильные ионы карбония. L. Протонированные имины
Джордж А. Олах и Пол. Kreienbuehl
Journal of the American Chemical Society 1967, 89 (18), 4756-4759
DOI: 10.1021/ja00994a033
Эта статья лауреата Нобелевской премии профессора Джорджа Олаха посвящена ЯМР-исследованиям протонирования иминов в суперкислотах. В экспериментальной части приведены подробности синтеза исследованных иминов.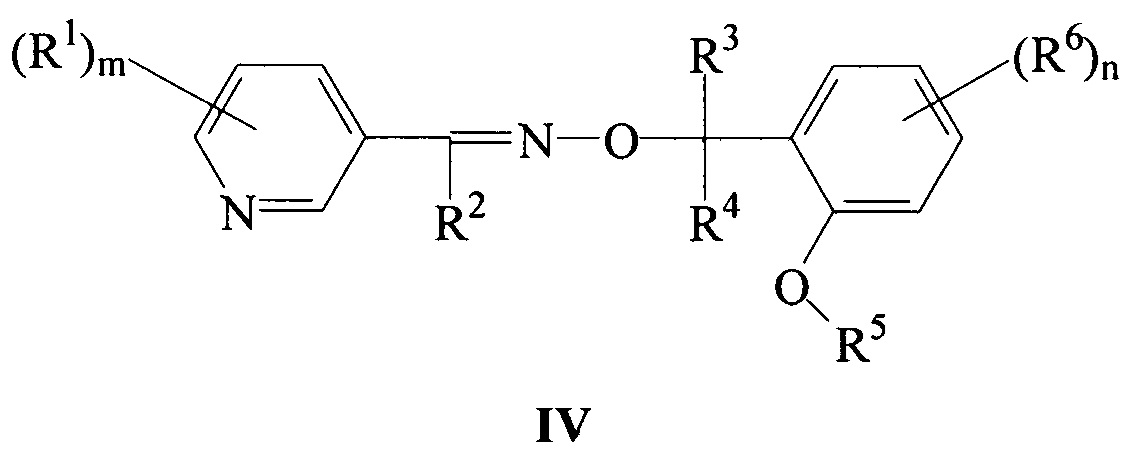
-
- Синтез стерически затрудненных иминов
Brian E. Love и Jianhua REN
Журнал органической химии 1993, 58 (20), 5556-5557
DOI: 1021 / jo00072a051
Удобный синтез пространственно затрудненных иминов с использованием тетраэтилортосиликата (Si(OEt) 4 ) в качестве дегидратирующего агента, поскольку он образует некислотный побочный продукт.Формирование энамина: - Ueber die Einwirkung des Ammoniaks auf Acetessigester
Norman Collie
Just. Либих. Аня. хим. 1884, 226 (3), 294-322
DOI: 10.1002/jlac.18842260306
Эта статья демонстрирует, что реакционная способность виниламина была известна еще в 1884 году! - Über die Einwirkung von Ammoniak und Ammoniak-Derivaten auf o-Acetylaceto-phenole
Georg Wittig, Hermann Blumenthal
Ber. 1927 , 60 (5), 1085-1094
1927 , 60 (5), 1085-1094
DOI: 10.1002/cber.19270600515
Лауреат Нобелевской премии профессор Г. Виттиг ввел термин «енаминол азота» в статье. - Über einfache Enamine mit tertiär gebundenem Stickstoff
Mannich, H. Davidsen
Chem. Бер. 1936 1936 69 (9), 2106-2112
DOI: 10.1002 / CBER19360690921
Enamine Praction была впервые практикована Маннихом в этой публикации - новый синтез 2-алкил и 2-ацилкетонов
Гилберт аист, Росс Террелл и Джейкоб Szmuskovicz
Журнал американского химического общества 1954 76 (7), 2029-2030
DOI: 1021 / JA01636A103
Первый документ проф.Аист о новом методе а-замещения кетонов через енамины. - Энаминное алкилирование и ацилирование карбонильных соединений
аист, А. Бризолара, H. Landesman, J. Szmuskovicz, и R. Terrell
Бризолара, H. Landesman, J. Szmuskovicz, и R. Terrell
Журнал американского химического общества 1963 85 (2 ), 207-222
DOI: 10.1021/ja00885a021
Еще одна классическая статья проф. Сторка об образовании енаминов и их использовании в органическом синтезе для -замещения альдегидов и кетонов. - универсальный новый синтез энамина
Уильям Эндрю белый и Гарольд Weingarten
Журнал органической химии 1967, 32 (1), 213-214
DOI: 1021 / JO01277A052
A краткое сообщение, описывающее метод синтеза енаминов с использованием TiCl 4 в качестве дегидратирующего агента. - Усовершенствованная методика синтеза енамина с тетрахлоридом титана. II. Объем реакции.
Карлсон, Рольф; Nilsson, åsa
acta Chemica Scandinavica 1984, 38b , 49-53
, 49-53
doi: 3891 / acta.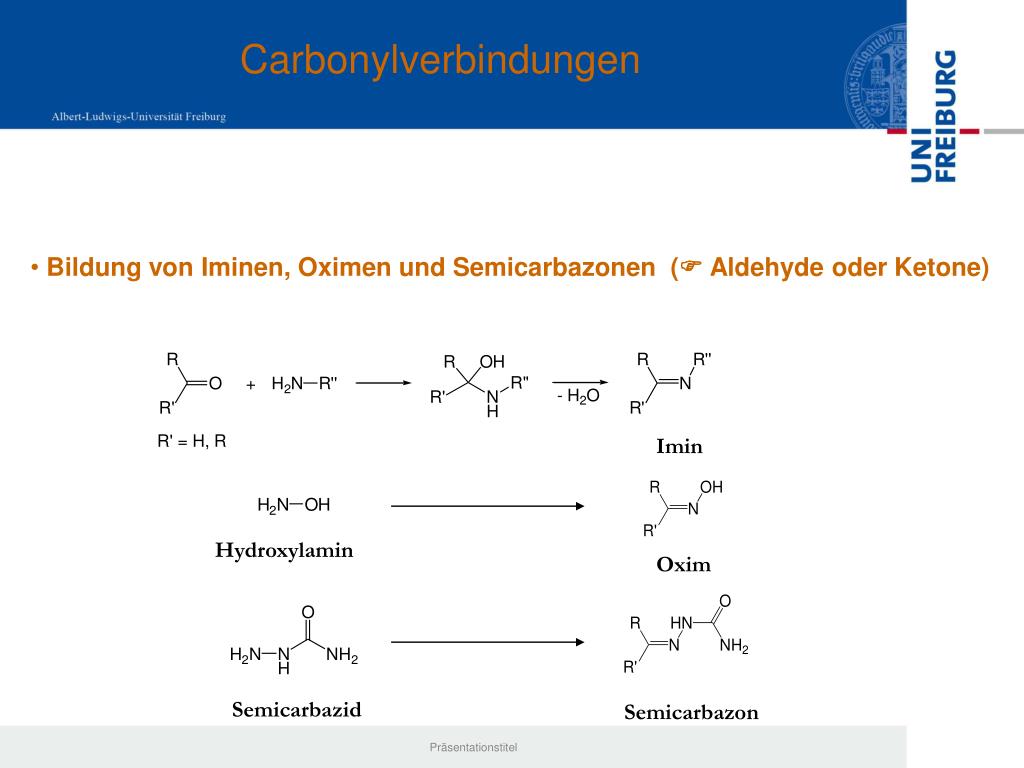 chem.scand.38B-0049
chem.scand.38B-0049
Другая статья, описывающая использование TICL 4 в качестве Льюиса Кислота и дегидратирующий агент для синтеза енамина. - 2,2-(ТРИМЕТИЛЕНДИТИО)ЦИКЛОГЕКСАНОН
R. B. Woodward, I. J. Pachter, and M. L. Scheinbaum
Org. Синтез. 1974, 54 , 39
DOI: 10.15227/orgsyn.054.0039
Первым этапом этой процедуры, предложенной легендарным химиком-органиком профессором Робертом Бернсом Вудвордом (Гарвард), является синтез енамина. - ЦИКЛОДЕКАНОН
D. Burpitt and J.G. Thweatt
Org. Синтез. 1968, 48 , 56
DOI: 10.15227/orgsyn.048.0056
Первым этапом этой процедуры из Organic Syntheses является синтез енамина. - Сравнение тавтомеризации и гидролиза некоторых вторичных и третичных энаминов
Brian Capon и Zhen Ping Wu
Журнал органической химии 1990, 55 (8), 2317-2324
Doi : 1021/jo00295a017
Исследование стабильности различных енаминов в растворе.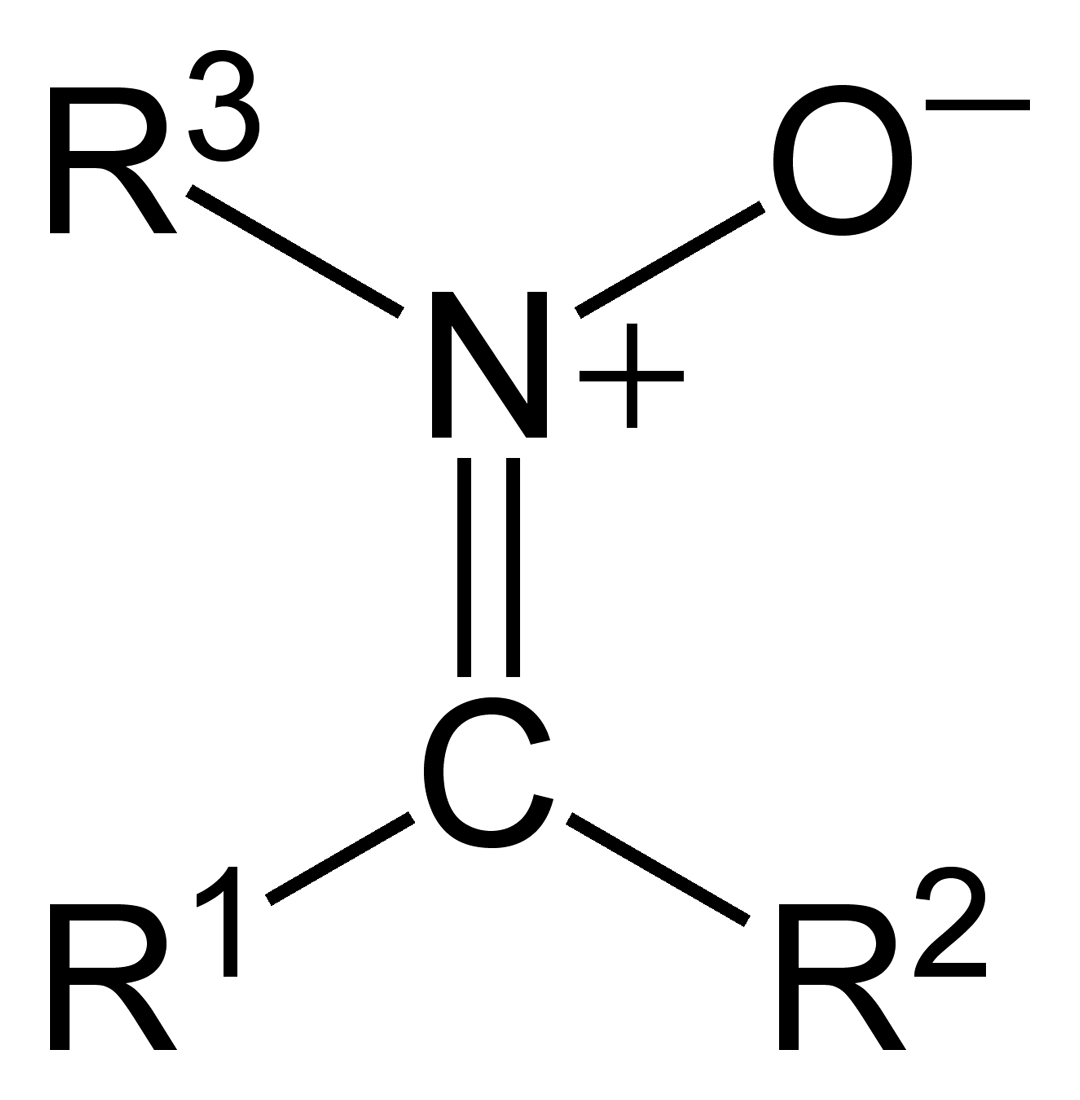
Динамическая иминная химия – Обзоры химического общества (RSC Publishing)
Образование имина из амина и альдегида представляет собой обратимую реакцию, которая протекает под термодинамическим контролем, так что образование кинетически конкурентоспособных промежуточных соединений со временем заменяется термодинамически наиболее стабильным продуктом (продуктами). По этой фундаментальной причине иминная связь оказалась необычайно разнообразной и полезной в руках химиков-синтетиков.Образование иминной связи является одной из немногих реакций, определяющих дисциплину, известную как динамическая ковалентная химия (ДКК), которая в настоящее время широко используется при конструировании экзотических молекул и протяженных структур из-за присущей им «вычитки» и «ошибки». «проверка», связанная с этими обратимыми реакциями. В то время как и супрамолекулярная химия, и DCC работают в режиме обратимости, DCC имеет дополнительное преимущество, заключающееся в построении прочных молекул за счет образования ковалентных связей, а не хрупких супермолекул, возникающих в результате нековалентных связующих взаимодействий.
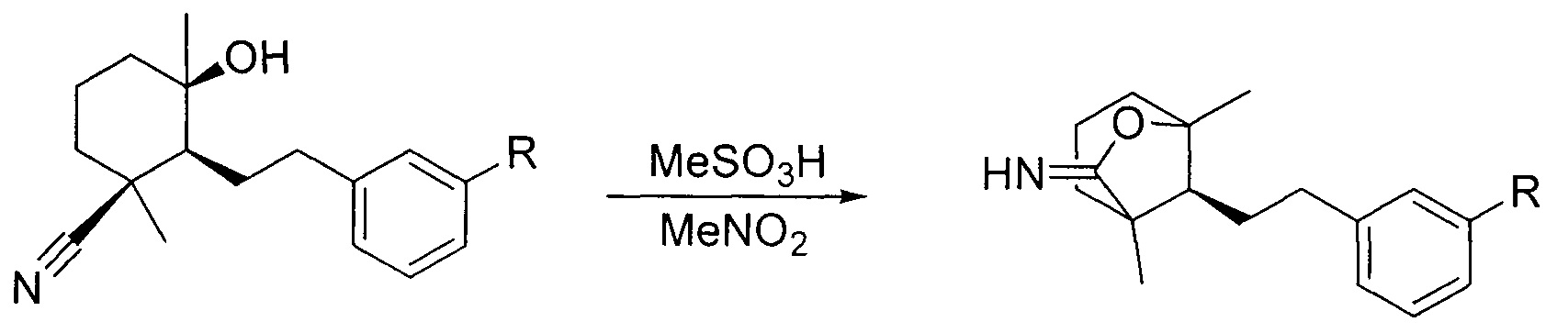 С другой стороны, для образования этих продуктов требуется больше времени — иногда дни или даже месяцы, — но их образование часто можно катализировать. Таким образом, из относительно простых предшественников могут быть получены высокосимметричные молекулы и протяженные структуры. Когда DCC используется в сочетании с протоколами, ориентированными на шаблон, которые основаны на использовании нековалентных связывающих взаимодействий между молекулярными строительными блоками, чтобы предварительно организовать их в определенные относительные геометрические формы в качестве прелюдии к образованию ковалентных связей под контролем равновесия, возникает дополнительный уровень контроля над структурой и топологией, который предлагает обезоруживающе простой способ конструирования механически взаимосвязанных молекул, таких как ротаксаны, катенаны, кольца Борромео и узлы Соломона.В этом учебном обзоре основное внимание уделяется использованию динамических иминных связей в конструировании соединений и продуктов, образованных с помощью дополнительных шаблонов и без них.
С другой стороны, для образования этих продуктов требуется больше времени — иногда дни или даже месяцы, — но их образование часто можно катализировать. Таким образом, из относительно простых предшественников могут быть получены высокосимметричные молекулы и протяженные структуры. Когда DCC используется в сочетании с протоколами, ориентированными на шаблон, которые основаны на использовании нековалентных связывающих взаимодействий между молекулярными строительными блоками, чтобы предварительно организовать их в определенные относительные геометрические формы в качестве прелюдии к образованию ковалентных связей под контролем равновесия, возникает дополнительный уровень контроля над структурой и топологией, который предлагает обезоруживающе простой способ конструирования механически взаимосвязанных молекул, таких как ротаксаны, катенаны, кольца Борромео и узлы Соломона.В этом учебном обзоре основное внимание уделяется использованию динамических иминных связей в конструировании соединений и продуктов, образованных с помощью дополнительных шаблонов и без них. В то время как синтез под термодинамическим контролем дает новую жизнь области химической топологии, он также обеспечивает доступ к бесконечному множеству новых материалов, которые во многих случаях просто недоступны с использованием более традиционных синтетических методологий, где кинетический контроль управляет процессом. насест. Одним из самых привлекательных качеств химии является ее способность заново изобретать себя, чтобы создать свой собственный объект, на что впервые указал Бертло полтора века назад.
В то время как синтез под термодинамическим контролем дает новую жизнь области химической топологии, он также обеспечивает доступ к бесконечному множеству новых материалов, которые во многих случаях просто недоступны с использованием более традиционных синтетических методологий, где кинетический контроль управляет процессом. насест. Одним из самых привлекательных качеств химии является ее способность заново изобретать себя, чтобы создать свой собственный объект, на что впервые указал Бертло полтора века назад.У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент.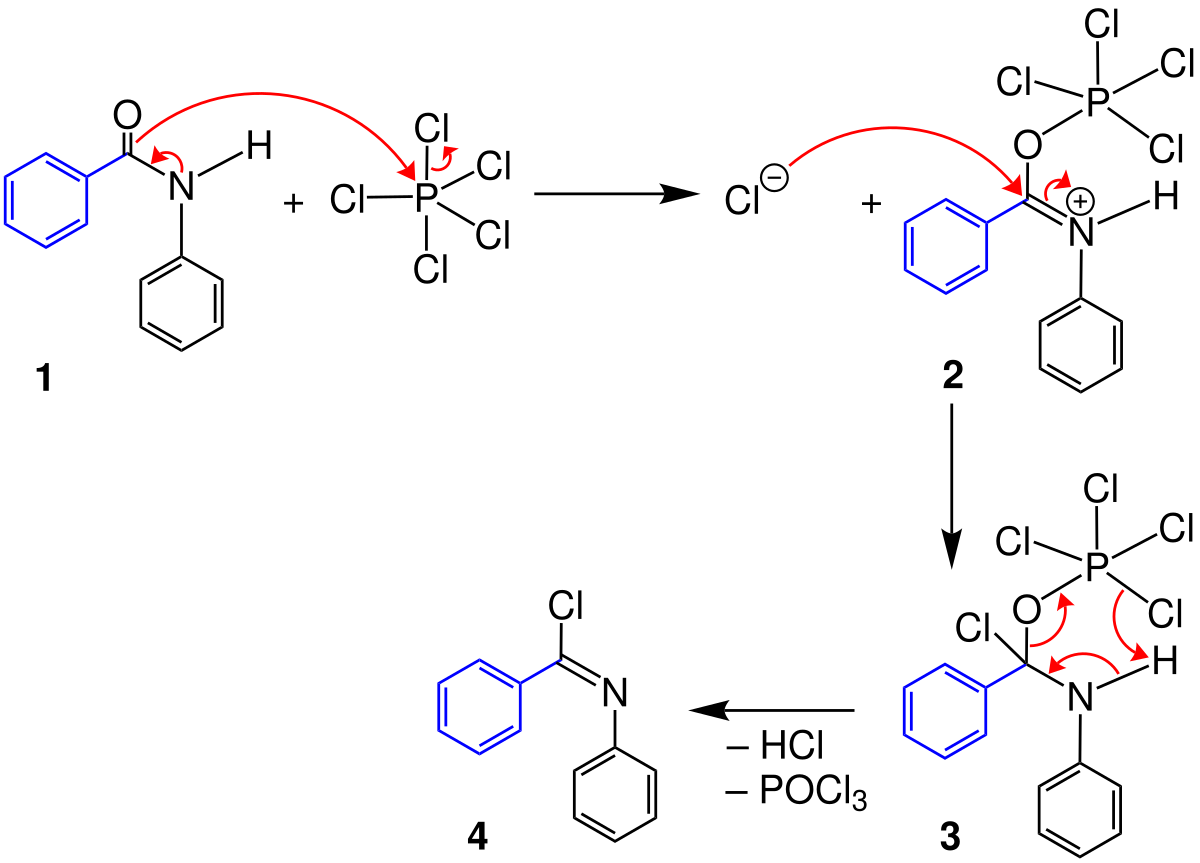 ..
Что-то пошло не так. Попробуй снова?
..
Что-то пошло не так. Попробуй снова?Динамическая иминная химия – Обзоры химического общества (издательство RSC)
Образование имина из амина и альдегида представляет собой обратимую реакцию, которая протекает под термодинамическим контролем, так что образование кинетически конкурентоспособных промежуточных соединений со временем заменяется термодинамически наиболее стабильным продуктом (продуктами).По этой фундаментальной причине иминная связь оказалась необычайно разнообразной и полезной в руках химиков-синтетиков. Образование иминной связи является одной из немногих реакций, определяющих дисциплину, известную как динамическая ковалентная химия (ДКК), которая в настоящее время широко используется при конструировании экзотических молекул и протяженных структур из-за присущей им «вычитки» и «ошибки».
 «проверка», связанная с этими обратимыми реакциями. В то время как и супрамолекулярная химия, и DCC работают в режиме обратимости, DCC имеет дополнительное преимущество, заключающееся в построении прочных молекул за счет образования ковалентных связей, а не хрупких супермолекул, возникающих в результате нековалентных связующих взаимодействий.С другой стороны, для образования этих продуктов требуется больше времени — иногда дни или даже месяцы, — но их образование часто можно катализировать. Таким образом, из относительно простых предшественников могут быть получены высокосимметричные молекулы и протяженные структуры. Когда DCC используется в сочетании с протоколами, ориентированными на шаблон, которые основаны на использовании нековалентных связывающих взаимодействий между молекулярными строительными блоками, чтобы предварительно организовать их в определенные относительные геометрические формы в качестве прелюдии к образованию ковалентных связей под контролем равновесия, возникает дополнительный уровень контроля над структурой и топологией, который предлагает обезоруживающе простой способ конструирования механически взаимосвязанных молекул, таких как ротаксаны, катенаны, кольца Борромео и узлы Соломона.
«проверка», связанная с этими обратимыми реакциями. В то время как и супрамолекулярная химия, и DCC работают в режиме обратимости, DCC имеет дополнительное преимущество, заключающееся в построении прочных молекул за счет образования ковалентных связей, а не хрупких супермолекул, возникающих в результате нековалентных связующих взаимодействий.С другой стороны, для образования этих продуктов требуется больше времени — иногда дни или даже месяцы, — но их образование часто можно катализировать. Таким образом, из относительно простых предшественников могут быть получены высокосимметричные молекулы и протяженные структуры. Когда DCC используется в сочетании с протоколами, ориентированными на шаблон, которые основаны на использовании нековалентных связывающих взаимодействий между молекулярными строительными блоками, чтобы предварительно организовать их в определенные относительные геометрические формы в качестве прелюдии к образованию ковалентных связей под контролем равновесия, возникает дополнительный уровень контроля над структурой и топологией, который предлагает обезоруживающе простой способ конструирования механически взаимосвязанных молекул, таких как ротаксаны, катенаны, кольца Борромео и узлы Соломона. В этом учебном обзоре основное внимание уделяется использованию динамических иминных связей в конструировании соединений и продуктов, образованных с помощью дополнительных шаблонов и без них. В то время как синтез под термодинамическим контролем дает новую жизнь области химической топологии, он также обеспечивает доступ к бесконечному множеству новых материалов, которые во многих случаях просто недоступны с использованием более традиционных синтетических методологий, где кинетический контроль управляет процессом. насест. Одним из самых привлекательных качеств химии является ее способность заново изобретать себя, чтобы создать свой собственный объект, на что впервые указал Бертло полтора века назад.
В этом учебном обзоре основное внимание уделяется использованию динамических иминных связей в конструировании соединений и продуктов, образованных с помощью дополнительных шаблонов и без них. В то время как синтез под термодинамическим контролем дает новую жизнь области химической топологии, он также обеспечивает доступ к бесконечному множеству новых материалов, которые во многих случаях просто недоступны с использованием более традиционных синтетических методологий, где кинетический контроль управляет процессом. насест. Одним из самых привлекательных качеств химии является ее способность заново изобретать себя, чтобы создать свой собственный объект, на что впервые указал Бертло полтора века назад.У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент. ..
Что-то пошло не так. Попробуй снова?
..
Что-то пошло не так. Попробуй снова?Недавние применения иминов в качестве ключевых промежуточных соединений в синтезе алкалоидов и новых гетероциклов азота
Легкий путь к хинолизидинам и индолизидинам посредством каскадных реакций иминов что аллилсиланы действуют как нуклеофилы для присоединения ионов иминия, мы разработали план синтеза хинолизидинов и индолизидинов, который в общих чертах изложен в .А именно, мы предполагали, что монозащищенные дикарбонильные соединения общей формы
5 могут вступать в каскад реакций с аллилсиланами 8 или 9 , в которых предпоследний промежуточный ион иминия захватывается другим нуклеофилом с образованием бициклических азотистых гетероциклов 6 . Точно так же разветвленный аллилсилан 10 может реагировать с 5 с образованием 7 . Размеры колец продуктов можно было варьировать, просто изменяя количество атомов углерода в исходных материалах.Примечательной особенностью этого подхода к хинолизидинам и индолизидинам является то, что процесс является конвергентным, что позволяет включать два ациклических исходных материала в бициклический продукт за одну химическую операцию.
Точно так же разветвленный аллилсилан 10 может реагировать с 5 с образованием 7 . Размеры колец продуктов можно было варьировать, просто изменяя количество атомов углерода в исходных материалах.Примечательной особенностью этого подхода к хинолизидинам и индолизидинам является то, что процесс является конвергентным, что позволяет включать два ациклических исходных материала в бициклический продукт за одну химическую операцию.Чтобы проверить жизнеспособность этого подхода к синтезу хинолизидина, мы сначала конденсировали известный аминоаллилсилан 9 5 с известным монозащищенным диальдегидом 11 6 с получением имина 10 ( 14) .Дальнейшее превращение 14 в предполагаемый иминиевый ион 17 , которое предположительно происходило через 15 и 16 , лучше всего достигалось действием трифторуксусной кислоты при -40°С.
 Прекращение каскада с использованием триэтилсилана или иона цианида в качестве улавливающего агента для 17 дало 12 или 13 соответственно с превосходным общим выходом. Для того, чтобы изучить объем этой химии, монозащищенный диальдегид 11 и линейный аминоаллилсилан 8 7 дали прореагировать, и реакцию погасили триэтилсиланом с получением 19 .Точно так же применение этой последовательности к 9 и моноацеталю диальдегида 18 6 привело к 20 . Эти две последние реакции не были оптимизированы. Несколько предварительных экспериментов по распространению этой каскадной последовательности на синтез пирролизидинов не увенчались успехом.
Прекращение каскада с использованием триэтилсилана или иона цианида в качестве улавливающего агента для 17 дало 12 или 13 соответственно с превосходным общим выходом. Для того, чтобы изучить объем этой химии, монозащищенный диальдегид 11 и линейный аминоаллилсилан 8 7 дали прореагировать, и реакцию погасили триэтилсиланом с получением 19 .Точно так же применение этой последовательности к 9 и моноацеталю диальдегида 18 6 привело к 20 . Эти две последние реакции не были оптимизированы. Несколько предварительных экспериментов по распространению этой каскадной последовательности на синтез пирролизидинов не увенчались успехом.Как отмечалось ранее, истинной проверкой любой новой стратегии или методологии является возможность ее применения для подготовки представляющих интерес мишеней, и не ускользнуло от внимания то, что соединения 12 и 20 могут быть легко преобразованы в встречающиеся в природе хинолизины.
 и индолизины.Действительно, соединение 12 было известным промежуточным соединением в предыдущем синтезе (±)-эпилупинина ( 1 ), 8 , 9 , но мы разработали улучшенный протокол для осуществления этого превращения, который включал озонолиз трифторацетатной соли 12 с последующим гидридным восстановлением промежуточного озонида (уравнение 1). Аналогичным образом соединение 20 было преобразовано в природный продукт (±)-таширомин ( 2 ) (уравнение 2). 10
и индолизины.Действительно, соединение 12 было известным промежуточным соединением в предыдущем синтезе (±)-эпилупинина ( 1 ), 8 , 9 , но мы разработали улучшенный протокол для осуществления этого превращения, который включал озонолиз трифторацетатной соли 12 с последующим гидридным восстановлением промежуточного озонида (уравнение 1). Аналогичным образом соединение 20 было преобразовано в природный продукт (±)-таширомин ( 2 ) (уравнение 2). 10 (1)
(2)
Затем мы хотели исследовать каскадные процессы с участием разветвленных аминоаллилсиланов и моноацеталей кетоальдегидов.В этом случае конденсация известного разветвленного аминоаллилсилана 10 11 с монозащищенным диальдегидом 11 с последующей последовательной обработкой полученного in situ имина ТФУ, а затем водным раствором NaCN дает эпимерную смесь (88:12) аминонитрилов 23 с отличным выходом ().
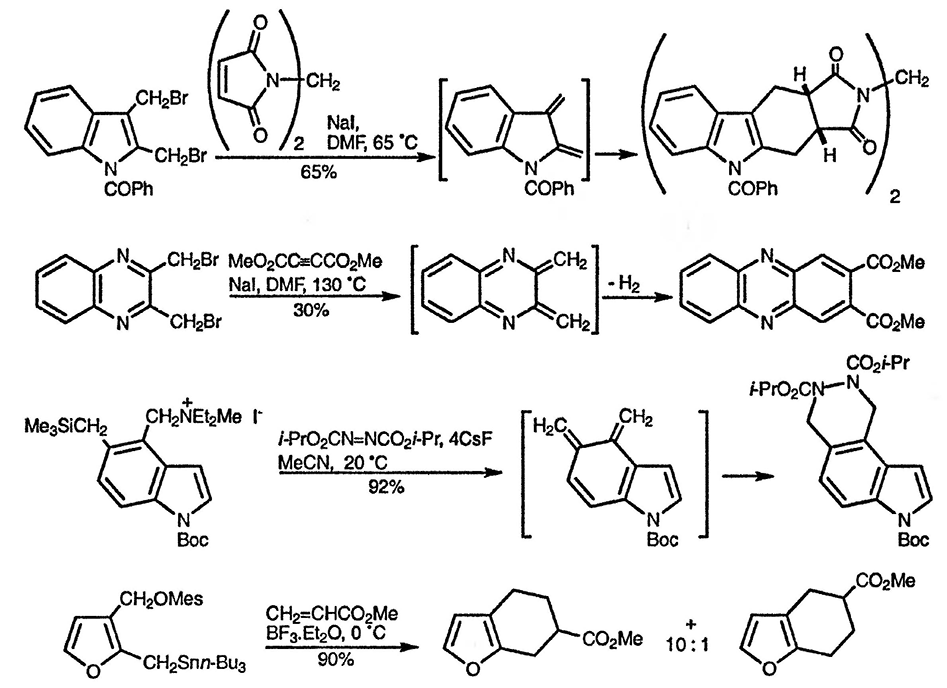 Мы также были рады обнаружить, что моноацетали кетоальдегида также являются подходящими партнерами для реакции. Например, 21 и 22 каждый конденсировали с аллилсиланом 10 , а промежуточные имины обрабатывали трифторуксусной кислотой для инициирования циклизации; обрыв каскада добавлением цианид-иона дал аминонитрилы 24 и 25 .
Мы также были рады обнаружить, что моноацетали кетоальдегида также являются подходящими партнерами для реакции. Например, 21 и 22 каждый конденсировали с аллилсиланом 10 , а промежуточные имины обрабатывали трифторуксусной кислотой для инициирования циклизации; обрыв каскада добавлением цианид-иона дал аминонитрилы 24 и 25 .Чтобы проиллюстрировать полезность этого процесса, он был применен к краткому энантиоселективному синтезу хинолизидинового алкалоида (-)-эпимиртина ( 3 ) (). Так, известный аминоаллилсилан 26 12 конденсировали с моноацеталем диальдегида 11 с получением имина, который затем последовательно обрабатывали трифторуксусной кислотой и водным раствором NaCN с получением 27 , восстановление которого NaCNBH 3 предоставили смесь (95:5) эпимерных хинолизидинов 28a,b .
 Озонолиз экзоциклического олефина в трифторацетатной соли 28a,b дал неразделимую смесь (95:5) (-)-эпимиртина ( 3 ) и (+)-миртина ( 29 ). 13
Озонолиз экзоциклического олефина в трифторацетатной соли 28a,b дал неразделимую смесь (95:5) (-)-эпимиртина ( 3 ) и (+)-миртина ( 29 ). 13 Потенциальная полезность α-аминонитрилов, образованных в последовательностях, изображенных на рис., не ускользнула от нашего внимания. Например, α-аминонитрилы могут быть депротонированы сильными основаниями с образованием стабилизированных карбанионов, которые могут вступать в реакции с рядом различных электрофилов, и они также могут служить эквивалентами ионов иминия в бруилантах и родственных процессах. 14 Например, полезность α-аминонитрила 25 подтверждается его легкой конверсией в 31 , которые содержат трициклическое ядро галихлорина ( 33 ). 15 Соответственно, ent- 25 давали возможность реагировать с 3-бутенилмагнийбромидом с получением хинолизидина 30 в виде единственного диастереомера с практически количественным выходом ().
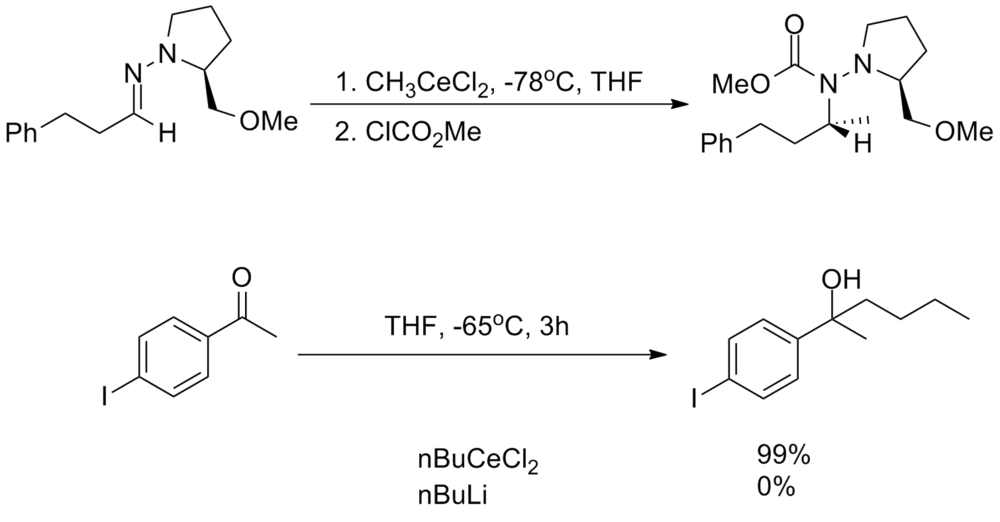 Гидрохлоридная соль 30 подвергалась легкому метатезису с замыканием енинового цикла в присутствии катализатора Граббса II ( 32 ) с получением 31 .Синтез 31 примечателен своей краткостью, всего тремя стадиями из ациклических исходных материалов и эффективностью (общий выход 64%).
Гидрохлоридная соль 30 подвергалась легкому метатезису с замыканием енинового цикла в присутствии катализатора Граббса II ( 32 ) с получением 31 .Синтез 31 примечателен своей краткостью, всего тремя стадиями из ациклических исходных материалов и эффективностью (общий выход 64%).Имины и синтез, ориентированный на разнообразие
Синтез, ориентированный на разнообразие (DOS) и его различные проявления представляют собой области значительной важности на стыке областей органического синтеза и химической биологии. 16 Одной из важнейших задач DOS является эффективное создание коллекций функционально и стереохимически разнообразных малых молекул, особенно тех, которые обладают скелетами, присутствующими в натуральных продуктах или молекулах, подобных лекарствам.Один привлекательный и мощный метод, недавно появившийся для создания таких наборов молекул, включает использование многокомпонентных реакций (MCR) 17 для создания подходящим образом замещенных промежуточных соединений, которые можно легко трансформировать путем циклизации и рефункционализации, что приводит к дальнейшему увеличению молекулярной сложности и разнообразия.
 4
4 Несколько лет назад мы открыли многокомпонентную реакцию, включающую винилогенные реакции Манниха богатых электронами диенов с ионами N -ацилиминия, образующимися in situ путем N -ацилирования иминов с образованием аддуктов, которые легко превращаются в ряд сложных алкалоидов, представляющих разные семейства. 1f В контексте DOS мы предполагали, что родственный четырехкомпонентный процесс, включающий комбинацию амина 34 , альдегида 35 и ацилирующего агента 36 , может генерировать реакционноспособный N -ацилиминий. ион, который впоследствии может быть захвачен нуклеофилом 37 с образованием функционализированного амида 38 (). Вариант этого протокола повлечет за собой добавление нуклеофила к промежуточному имину с последующим N -ацилированием для получения 38 . 18 Эта экспериментальная гибкость вместе с доступностью многочисленных реагентов 34 – 37 позволяет вводить продукты 38 с высоким уровнем функционального и структурного разнообразия, так что впоследствии может быть проведен ряд различных циклизаций.
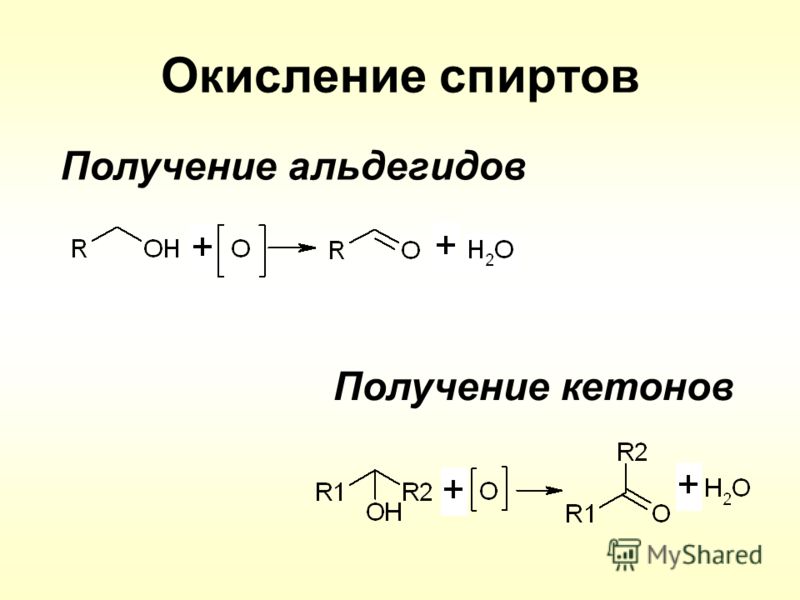 выполнено для создания массива гетероциклических каркасов всего за несколько стадий из коммерчески доступных исходных материалов.
выполнено для создания массива гетероциклических каркасов всего за несколько стадий из коммерчески доступных исходных материалов.Вопрос на данном этапе заключался в том, можем ли мы на самом деле организовывать такие реакции для быстрой сборки гетероциклических систем, которые представляли бы интерес для DOS.С этой целью мы сосредоточились на объединении ненасыщенных аминов, арилальдегидов, простых хлорангидридов, а также аллильных и π-нуклеофилов для получения аддуктов, которые можно было бы дополнительно преобразовать циклизациями, включающими реакции RCM, реакции Дикмана и Хека, а также реакции Дильса-Альдера и диполярные циклоприсоединения. Например, конденсация метил-2-формилбензоата ( 40 ) с аллилом и пропаргиламином дает промежуточные имины, которые последовательно обрабатывают ацетилхлоридом и аллилцинкбромидом с получением аддуктов 41 и 42 в одном реакторе ().Соединение 41 превращали в бензазепин 43 с помощью RCM с использованием катализатора Граббса 32 с последующей циклизацией Дикмана.
 В родственном процессе 42 и стирол, который служил в качестве пятого компонента в процессе, подвергались ениновому каскаду RCM/CM при обработке катализатором Ховейда-Граббса ( 45 ) с получением промежуточного продукта, который подвергался циклизации с помощью Конденсация Дикмана для получения 44 . Эти два примера хорошо иллюстрируют, как простое изменение одного из входов в начальном многокомпонентном процессе позволяет дифференцированно обрабатывать аддукты в мишени различной сложности и структуры.
В родственном процессе 42 и стирол, который служил в качестве пятого компонента в процессе, подвергались ениновому каскаду RCM/CM при обработке катализатором Ховейда-Граббса ( 45 ) с получением промежуточного продукта, который подвергался циклизации с помощью Конденсация Дикмана для получения 44 . Эти два примера хорошо иллюстрируют, как простое изменение одного из входов в начальном многокомпонентном процессе позволяет дифференцированно обрабатывать аддукты в мишени различной сложности и структуры.Изменение функциональности альдегидного компонента позволяет получить доступ к другим коллекторам циклизации и, следовательно, к другим гетероциклическим системам. Иллюстрацией этой особенности является использование 2-бромбензальдегида ( 48 ) в четырехкомпонентном процессе для получения субстратов, поддающихся циклизации Хека (). Образовавшийся таким образом третичный амид 47 подвергали двухстадийной последовательности циклизаций, включающей RCM с последующей реакцией Хека, с получением 46 .
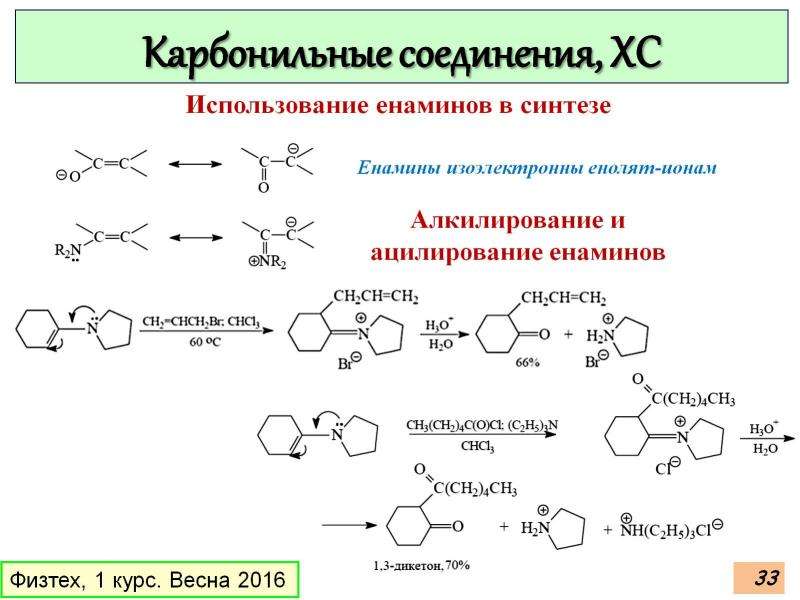
Другой аспект этой стратегии для DOS включает использование силиленоловых эфиров в качестве исходных материалов в начальном четырехкомпонентном процессе для получения альдегидов, которые затем можно использовать в качестве предшественников 1,3-диплолов, которые могут претерпевать внутримолекулярные [3+2] диполярные циклоприсоединения с проксимальными двойными или тройными связями для создания разнообразных гетероциклических каркасов.Например, взаимодействие бромальдегида 46 с бис(триметилсилил)аллиламином в присутствии каталитических количеств ТМСОТф с последующей обработкой полученного имина in situ ацетилхлоридом и эфиром енола 49 привело к получению аддукта 50 (). Когда 50 конденсировали с саркозином в кипящем толуоле, промежуточный азометинилид легко подвергался [3+2] циклоприсоединению с образованием 51 . нитрон, который подвергся легкому [3+2] циклоприсоединению с образованием 52 .

Внутримолекулярная реакция Дильса-Альдера (IMDA) — еще одна мощная реакция для синтеза сложных молекул. Следовательно, мы обратили наше внимание на использование исходных материалов в четырехкомпонентном процессе, которые обеспечили бы субстраты, способные подвергаться таким преобразованиям. В данном случае мы обнаружили, что при добавлении пентадиенилсилана 55 и акрилоилхлорида к имину, образующемуся in situ при конденсации бензальдегида 53 с бис(триметилсилил)аллиламином в присутствии TMSOTf, полученный продукт подвергался самопроизвольному [ 4+2] циклизация с получением 56 ().В связанной каскадной реакции конденсация 2-азидобензальдегида ( 54 ) с пропаргиламином с последующей обработкой промежуточного имина ацетилхлоридом и ацеталем кетена 57 приводит к получению триазола 58 через [3+2] диполярный циклоприсоединение. Примечательным аспектом этих конструкций является то, что сложные гетероциклические системы быстро генерируются в простых однореакторных операциях.

Поскольку мы всегда заинтересованы в применении новых стратегий синтеза гетероциклов к натуральным продуктам, мы задались вопросом, можно ли использовать эту новую стратегию для DOS для получения сложных алкалоидов.Таким образом, мы предполагали, что четырехкомпонентная реакция может быть использована для сборки 62 и их аналогов, которые прекрасно послужат предшественниками бензолированного ядра азабицикло[3.2.2]нонана, присутствующего в алкалоидах изопавина. 19 К счастью, мы обнаружили, что конденсация пипероналя ( 59 ) с метиламином дает промежуточный имин, который последовательно обрабатывают на месте реактивом Гриньяра 60 , а затем хлорангидридом 61 с получением 62 () .Когда 62 обрабатывали водной кислотой, он подвергался легкой циклизации с образованием (±)-роэлактамина ( 4 ), алкалоида, который был выделен в 1992 году из Roemeria refracta DC.
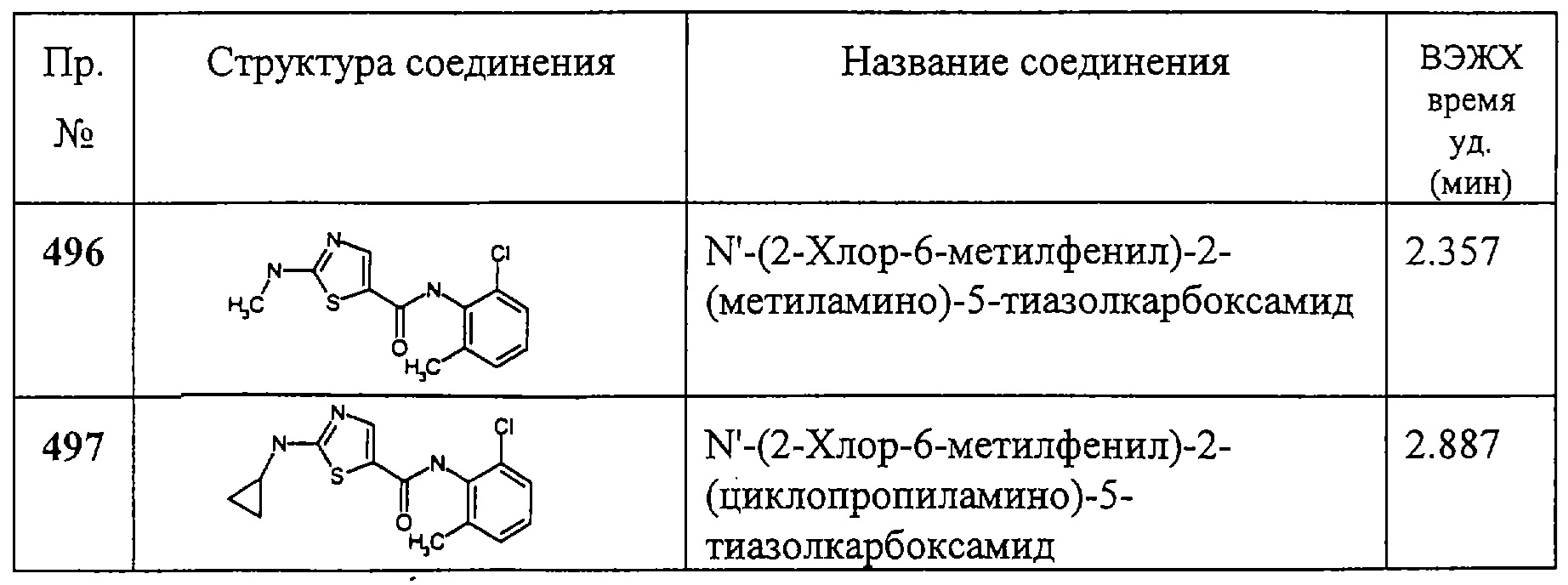 20
20 Imine и Enamine Гидролиза механизма гидролиза
Имины и энамины могут быть гидролизованы на альдегиды и кетоны в кислых условиях:
Запомнить, Реакции из альдегидов и кетонов с спиртов и аминов все обратимы и, следовательно, продукты этих реакций – ацетали, имины и енамины могут снова превращаться в карбонильные соединения при использовании большого избытка воды.
Вы можете найти механизм гидролиза ацеталя в этой статье, поэтому теперь давайте обсудим механизм гидролиза имина и енамина один за другим.
В реакции участвуют те же промежуточные продукты, что и при образовании иминов, только стадии меняются местами. Он начинается с протонирования азота, превращающего имин в ион иминия, который является очень электрофильным и подвергается атаке водой на следующем этапе:
После переноса протона от кислорода к азоту (вероятно, межмолекулярный процесс), ион аммония выбрасывается в виде нейтрального амина.
 На этом этапе образуется ион оксония, который после депротонирования дает желаемый кетон.
На этом этапе образуется ион оксония, который после депротонирования дает желаемый кетон.Гидролиз енаминов также начинается с протонирования, однако на этот раз в этой стадии участвует углерод с двойной связью: атакуется водой с образованием нестабильного тетраэдрического интермедиата.
После этого происходит протонирование азота, превращающее его в хорошую уходящую группу, которая выбивается неподеленными парами кислорода.
Кетон получают после депротонирования иона оксония.
В этих реакциях довольно много стадий, но, к счастью, вам не нужно запоминать их все , чтобы предсказать структуру альдегида и кетона , образующихся после гидролиза.
Вот ярлык; проведите линию между атомами азота и углерода .
Это связи, которые расщепляются во время гидролиза. Азот является частью амина, и связанный с ним углерод представляет собой атом углерода C=O:
Дополнительные примеры гидролиза имина и енамина, а также ацеталя рассматриваются в этой практической задаче .

- Синтез стерически затрудненных иминов
