История открытия таблицы Менделеева – BrainApps.ru
Открытие Дмитрием Менделеевым периодической таблицы химических элементов в марте 1869 года стало настоящим прорывом в химии. Российскому ученому удалось систематизировать знания о химических элементах и представить их в виде таблицы, которую и сейчас обязательно изучают школьники на уроках химии. Периодическая таблица стала фундаментом для бурного развития этой сложной и интересной науки, а история ее открытия окутана легендами и мифами. Для всех увлекающихся наукой будет интересно узнать правду о том, как Менделеев открыл таблицу периодических элементов.
История таблицы Менделеева: как все начиналось
Попытки классифицировать и систематизировать известные химические элементы предпринимались задолго до Дмитрия Менделеева. Свои системы элементов предлагали такие известные ученые, как Деберейнер, Ньюлендс, Мейер и другие. Однако из-за нехватки данных о химических элементах и их правильных атомных массах предложенные системы были не совсем достоверными.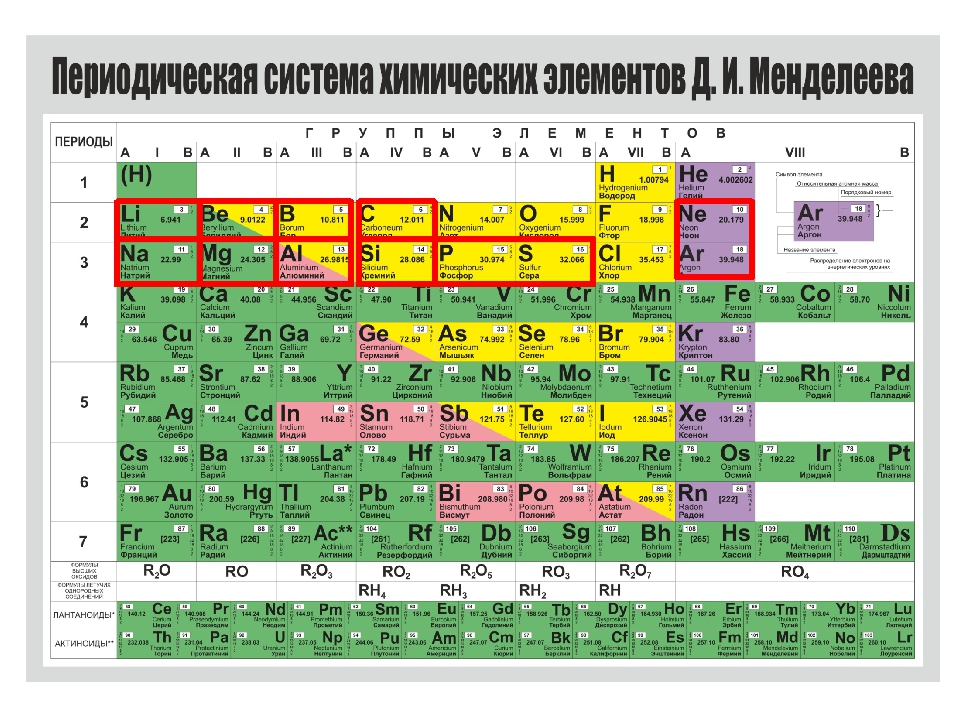
История открытия таблицы Менделеева начинается в 1869 году, когда российский ученый на заседании Русского химического общества рассказал своим коллегам о сделанном им открытии. В предложенной ученым таблице химические элементы располагались в зависимости от их свойств, обеспечивающихся величиной их молекулярной массы.
Интересной особенностью таблицы Менделеева было также наличие пустых клеток, которые в будущем были заполнены открытыми химическими элементами, предсказанными ученым (германий, галлий, скандий). После открытия периодической таблицы в нее много раз вносились добавления и поправки. Совместно с шотландским химиком Уильямом Рамзаем Менделеев добавил в таблицу группу инертных газов (нулевую группу).
В дальнейшем история периодической таблицы Менделеева была напрямую связана с открытиями в другой науке – физике. Работа над таблицей периодических элементов продолжается до сих пор, и современные ученые добавляют новые химические элементы по мере их открытия. Значение периодической системы Дмитрия Менделеева сложно переоценить, так как благодаря ей:
- Систематизировались знания о свойствах уже открытых химических элементов;
- Появилась возможность прогнозирования открытия новых химических элементов;
- Начали развиваться такие разделы физики, как физика атома и физика ядра;
Существует множество вариантов изображения химических элементов согласно периодическому закону, однако наиболее известный и распространенный вариант – это привычная для каждого таблица Менделеева.
Мифы и факты о создании периодической таблицы
Самым распространенным заблуждением в истории открытия таблицы Менделеева является то, что ученый увидел ее во сне. На самом деле сам Дмитрий Менделеев опроверг этот миф и заявил, что размышлял над периодическим законом на протяжении многих лет. Чтобы систематизировать химические элементы он выписывал каждый из них на отдельную карточку и многократно комбинировал их между собой, расставляя в ряды в зависимости от их схожих свойств.
Миф о «вещем» сне ученого можно объяснить тем, что Менделеев работал над систематизацией химических элементов сутками напролет, прерываясь на непродолжительный сон. Однако только упорный труд и природный талант ученого дал долгожданный результат и обеспечил Дмитрию Менделееву всемирную известность.
Многих учащихся в школе, а иногда и в университете, заставляютзаучивать или хотя бы примерно ориентироваться в таблице Менделеева. Для этого человек должен не только иметь хорошую память, но и логически мыслить, связывая элементы в отдельные группы и классы. Изучение таблицы легче всего дается тем людям, которые постоянно поддерживают мозг в тонусе, проходя тренинги на BrainApps.
Изучение таблицы легче всего дается тем людям, которые постоянно поддерживают мозг в тонусе, проходя тренинги на BrainApps.
Год таблицы Менделеева: как это будет?
Из мероприятий, которые планирует провести наш университет — осенью, — у нас запланировано открытие первого химического технопарка «Mendeleev Центр»(https:// muctr.ru/upload/university/us/plan/18_19/technopark.pdf). Сергей Семенович Собянин подписал соответствующее распоряжение. Это будет четыре лаборатории. Первая лаборатория «Химия. Старт» — химия для самых маленьких, начиная с 3-4 класса, когда ребята могут прийти осуществить безопасные химические эксперименты. В школе у них такой предмета еще нет, а к нам они могут прийти и понять, что такое химия, для чего нужно становиться химиком. Остальные лаборатории — для ребят более старшего возраста – начиная с восьмого класса, когда химия изучается в школе. Одна лаборатория будет посвящена материаловедению, материалам для фотоники, композитные материалы; одна лаборатория посвящена неорганической химии, одна — проблемам органической химии. Помимо этого, в технопарке будет экспозиция, посвященная наследию и творчеству Дмитрия Ивановича Менделеева, и развитию химии и химической технологии в нашей стране, плюс будет ряд экспонатов, где можно будет пощупать, потрогать, посмотреть, что такое химия.
Помимо этого, в технопарке будет экспозиция, посвященная наследию и творчеству Дмитрия Ивановича Менделеева, и развитию химии и химической технологии в нашей стране, плюс будет ряд экспонатов, где можно будет пощупать, потрогать, посмотреть, что такое химия.
— А где будет находиться технопарк?
— Он будет располагаться на нашей площадке, для этого у нас есть трехэтажное здание с отдельным входом с улицы, которое мы сейчас начали переоборудовать.
— А как можно будет попасть на экскурсию? Это право школьник должен заслужить, или билеты будут продаваться свободно?
— У нас будут заключаться договоры со школами, чтобы классы могли приезжать, заниматься экспериментами, делать свои проекты. В выходные мы планируем, что технопарк будет работать как интерактивный музей, куда можно будет просто приходить и смотреть. Но мы еще подумаем о музейной концепции, как мы будем приглашать, привлекать ребят. Я думаю, что это должно быть доступно максимальному числу школьников и их родителей.
— Вы упомянули открытые уроки – а как вы выбирали школы для участия в этой программе?
— У нас есть обширная сеть школ Москвы и Московской области, которые с нами сотрудничают. Мы хотим расширять географию и выезжать в другие в регионы. Помимо этого, мы сотрудничаем с Ивановским химико-технологическим университетом с Казанским национально-исследовательским технологическим университетом. Мы будем передавать дидактические материалы им, и они могут ими пользоваться.
— Представим, что где-то в соседнем регионе есть какая-то школа, которая хочет с вами сотрудничать. Что они должны сделать?
— Нужно написать нам письмо. Мы рассмотрим заявку. Мы готовы сотрудничать, взаимодействовать с новыми школами, приезжать и читать лекции. И приглашаем к себе: мы уже в конце прошлого года открыли лабораторию (при финансовой поддержке DOW Chemicals). Это лабораторный практикум для работы со школьниками – отдельное помещение, хорошо оборудованное.
— Вернемся к празднованию года Периодической системы химических элементов. Будут ли мероприятия в России согласованы с тем, что проходит за рубежом? Или они отличаются?
Будут ли мероприятия в России согласованы с тем, что проходит за рубежом? Или они отличаются?
— Есть план, утвержденный оргкомитетом. Оргкомитет есть в России и за рубежом. В планах около 60 мероприятий. Истории развиваются параллельно, где-то они пересекаются. В основном это научные конференции, и только в России делается акцент на популяризацию. Среди таких мероприятий – издание юбилейных марок, написание книги про Дмитрия Ивановича Менделеева. Сейчас есть только одна книга из серии «Жизнь замечательных людей».
В этом году исполнилось 150 лет с даты открытия таблицы Менделеева — Российская газета
В 1869 году профессор Санкт-Петербургского университета Николай Меншуткин на заседании Русского химического общества прочел доклад профессора того же университета Д.И. Менделеева “Соотношение свойств с атомным весом элементов”, который затем был опубликован в “Журнале Русского физико-химического общества”. Так человечество узнало об одном из фундаментальных законов природы – Периодическом законе химических элементов.
На портрете, висящем во всех школьных кабинетах химии, мы видим пожилого ученого с неровно подстриженной бородой, благородным лбом и волосами до плеч – это наш российский гений Дмитрий Иванович Менделеев. Строгого определения гениальности не существует, но в данном случае сомнений нет – он не просто решил проблему, над которой бились лучшие умы лучших научных школ Европы. Это тем удивительнее, что открыть Периодический закон на основании имевшихся тогда экспериментальных данных было совершенно невозможно, а он это непостижимым образом сделал.
Про Дмитрия Ивановича рассказывают две легенды: что он придумал водку, и что Периодическая таблица привиделась ему во сне. Первая – обычная городская легенда с подсознательной попыткой опростить великого человека, сблизить его с выпивающим населением. А ссылка многочисленных авторов на докторскую диссертацию Менделеева “О соединении спирта с водой”, в которой он якобы описал рецепт “правильной” водки, говорит лишь о том, что ни один из них не удосужился в эту работу заглянуть. В ней приведено множество данных о различных показателях таких растворов, но для самых разных концентраций спирта. Вторая история – из того же ряда. Если Таблица приснилась, то и это сближает Менделеева с нами, простыми людьми. Может быть, ему что-то подобное и снилось.
В ней приведено множество данных о различных показателях таких растворов, но для самых разных концентраций спирта. Вторая история – из того же ряда. Если Таблица приснилась, то и это сближает Менделеева с нами, простыми людьми. Может быть, ему что-то подобное и снилось.
Может быть, ему что-то и снилось, вот только над решением этой загадки природы, по его собственному признанию, он “лет двадцать думал”. Это некоторое преувеличение, потому что на момент открытия Менделееву только-только исполнилось 35 лет. И его портрет именно в таком возрасте – молодого в сущности человека – и следовало бы помещать в кабинетах химии.
Посмотрим на нарисованную им рукописную Таблицу. К тому времени было известно всего чуть более 60 элементов с их атомными весами (сейчас почти вдвое больше). Идея расположить элементы по возрастанию их атомных весов совершенно естественна. Сложнее было заметить периодические закономерности в этом ряду, но и здесь было немало сделано до Менделеева. Уже существовало “правило октетов” (химические свойства каждого восьмого элемента очень близки), “правило триад” (в каждой тройке близких по свойствам элементов средний элемент обладает и средним атомным весом). Однако никому не удавалось построить систему для всех известных элементов. Тогда и свойства многих из них были неизвестны, и атомные веса некоторых были измерены неправильно.
Однако никому не удавалось построить систему для всех известных элементов. Тогда и свойства многих из них были неизвестны, и атомные веса некоторых были измерены неправильно.
За основу своей системы Менделеев взял химические свойства элементов и расположил химически похожие друг под другом, при этом соблюдая принцип возрастания атомных весов. Но ничего не выходило! Бериллий нарушил всю картину уже в первой строчке будущей Таблицы – получалось, что углерод является аналогом алюминия, а немного дальше таким аналогом оказывался и титан. С точки зрения их химических свойств это было нонсенсом.
Этот год провозглашен Международным годом Периодической таблицы – IYPT 2019
Вот тут он мог бы и прекратить поиски системы – все крупнейшие ученые того времени так и поступили. Но не Менделеев. Он взял и изменил атомный вес бериллия, а между кальцием и титаном оставил пустую клеточку и тем самым предсказал элемент скандий. Самое поразительное, что так же он поступил чуть ли не с третью всех тогда известных элементов! Например, присвоил урану атомный вес 240 вместо принятого 60 (увеличил в четыре раза!), переставил местами кобальт и никель, теллур и йод. Опубликовав в 1869 году первый вариант своей Таблицы, он предсказал сразу три элемента, изменил атомные веса у десятка, и при этом открыл закон, что “свойства элементов стоят в периодической зависимости от их атомного веса”.
Опубликовав в 1869 году первый вариант своей Таблицы, он предсказал сразу три элемента, изменил атомные веса у десятка, и при этом открыл закон, что “свойства элементов стоят в периодической зависимости от их атомного веса”.
И только через 44 года, в 1913 году английский физик Мозли выяснил, что менделеевский номер в Таблице – это количество протонов в ядре каждого элемента (заряд ядра), подтвердив тем самым правоту гениальной интуиции ее автора.
Уже через 6 лет после публикации статьи о Таблице была заполнена в ней первая пустая клетка – был открыт галлий, который прекрасно встал после цинка и под алюминием.
Он прожил 73 года, написал почти 500 статей по химии, физической химии, технике, физике, экономике, геодезии. Организовал и стал первым директором Палаты мер и весов, был профессором университета и действительным статским советником (т.е. генералом), ушел из университета в знак протеста против сокращения университетской автономии, был избран в 90 иностранных академий наук и забаллотирован при выборах в российскую. Наши академики сочли его труды недостаточно фундаментальными…
Наши академики сочли его труды недостаточно фундаментальными…
Американские физики синтезировали 101-й элемент Таблицы и назвали его менделевием, на Земле есть минерал менделеевит, вулкан и подводный горный хребет имени Менделеева, а на обратной стороне Луны – кратер Менделеева. 2019 год провозглашен ООН Международным годом Периодической таблицы – IYPT 2019.
Самую большую в Евразии таблицу Менделеева открыли в Дубне
Гигантскую таблицу химических элементов Менделеева разместили на фасаде бассейна в Дубне, на набережной Волги. Она будет самым крупным на материке Евразия путеводителем по тайнам Природы для туристов.
Самой большой стационарной таблицей Менделеева с 2017 года считалась таблица площадью 150 м2, размещенная на стенах испанского университета в Мурсии. В 2019 году рекорд Испании обогнала Австралия. Там на фасаде нового здания Университета Эдит Коуэн (Edith Cowan University) открыли таблицу Менделеева площадью 660 м2.
“Что может быть лучшей презентацией истории и будущего науки, чем периодическая таблица?”, – сказал тогда о событии вице-канцлер этого университета, химик Стив Чэпмен (Steve Chapman).
23 июля на второе место в мире и на первое в Евразии вышла таблица Менделеева, которую соорудили в Дубне. Ее составили из 121 клеточки общей площадью 284 м2 и разместили на фасаде бассейна “Архимед” Объединенного института ядерных исследований (ОИЯИ). Бассейн стоит на набережной Волги, поэтому с любого судна можно в подробностях разглядеть содержание таблицы химических элементов, десять из которых были созданы в Дубне, учеными ОИЯИ.
Торжественное открытие таблицы Менделеева в Дубне приветствовали в онлайн-формате министр науки и высшего образования РФ Валерий Фальков, президенты Международного союза чистой и прикладной химии (IUPAC) Кристофер Бретт (Christopher Brett) и Международного союза чистой и прикладной физики (IUPAP) Мишель Спиро (Michel Spiro), губернатор Московской области Андрей Воробьев.
Сейчас в таблице Менделеева содержится 118 химических элементов. Еще три клеточки в огромной дубненской таблице химических элементов оставили пустыми в ожидании трех новых кандидатов с номерами 119, 120, 121. Их синтез скоро начнется на новой Фабрике сверхтяжелых ионов в ОИЯИ.
“Что нас ждет? Предсказания теоретиков мира разнообразны и порою экстравагантны, – сказал об этом на церемонии открытия “отец” элемента №118, живая легенда науки, академик Юрий Оганесян. – Но мне кажется, что матушка-таблица и на этот раз преподнесет нам сюрпризы, которые трудно предсказать. Таблица не стареет. Спустя полтора столетия она, как Джоконда Леонардо, своей загадочной улыбкой влечет исследователей в волшебный мир науки, оставаясь полной тайн и открытий…”
Все дело в том, что таблица Менделеева – не застывший памятник науке. Она – живая картина многовековой истории познания законов Природы. А познание не имеет конца.
Ранее мы рассказывали, что тайну таблицы Менделеева открыла странная звезда Млечного Пути, и что таблицу Менделеева хотят расширить до 173 элементов. А еще мы писали о том, что композитор Олег Трояновский перевел таблицу Менделеева на язык музыки.
А еще мы писали о том, что композитор Олег Трояновский перевел таблицу Менделеева на язык музыки.
Больше новостей из мира науки вы найдёте в разделе “Наука” на медиаплатформе “Смотрим”.
Великая химическая война. Как СССР и США заполняли таблицу Менделеева | События | ОБЩЕСТВО
2019-й стал Международным годом периодической таблицы химических элементов. 8 февраля отмечается 185-летие её автора Дмитрия Менделеева, и самой таблице Менделеева в этом году исполняется 150 лет.
К этому юбилею в российском издательстве вышла книга доцента кафедры высокомолекулярных и элементоорганических соединений КФУ, популяризатора науки Аркадия Курамшина «Элементы: замечательный сон профессора Менделеева».
В 1869 году, когда Дмитрий Менделеев придумал периодическую систему, в ней было всего 63 элемента. К своему 150-летию таблица Менделеева пополнилась до 118 элементов. На минувшей неделе учёный Юрий Оганесян, именем которого назвали последний из открытых химических элементов – оганесон, – объявил, что началась погоня за 119-м и 120-м элементами.
Факт №1. «Русский» элемент
«Казанский след» в таблице Менделеева яркий и конкретный, – рассказывает Аркадий Курамшин. – Единственный элемент из существующих в земной коре, открытый в России, – это рутений (44-й). Он был известен ещё во времена Дмитрия Менделеева. Его название происходит от позднелатинского Ruthenia, что в переводе – Русь или Россия. И открыт он в стенах Казанского университета профессором Карлом Клаусом в 1844 году. В традициях российской химической школы была сильна минералогия, органическая химия, а вот с открытием новых элементов не повезло. Позже в нашей стране открывали сверхтяжёлые элементы, созданные искусственно.
Факт №2. «Трансфермиевые войны»
Со сверхтяжёлыми элементами связаны «трансфермиевые войны» – период состязаний российских и американских физиков-ядерщиков в открытии химических элементов./imgs/2019/08/05/10/3489939/b210986d372c08253b7647f6928441111a87d79b.jpg) Он совпал с годами холодной войны.
Он совпал с годами холодной войны.
«104-й элемент (резерфордий) в СССР назывался курчатовий в честь «отца» советской атомной бомбы, 102-й (нобелий) – именовался жолиотий в честь учёного и борца за мир Фредерика Жолио-Кюри, – продолжает химик. – Во время перестройки в советских школах даже висели таблицы Менделеева с жолиотием, курчатовием и другими советскими наименованиями. Международный союз теоретической и прикладной химии (ИЮПАК) был возмущён. Именно он с 1913 года был единственной в мире организацией, которая имела право давать названия новым элементам.
– Во время перестройки в советских школах даже висели таблицы Менделеева с жолиотием, курчатовием и другими советскими наименованиями. Международный союз теоретической и прикладной химии (ИЮПАК) был возмущён. Именно он с 1913 года был единственной в мире организацией, которая имела право давать названия новым элементам.
Факт №3. 10 открытий «технеция»
«43-й элемент – технеций – не могли обнаружить в природе долгое время, – говорит Аркадий Курамшин. – Сам Дмитрий Менделеев оставил для него место в таблице, предсказав, что его займёт «экомарганец». Его открывали раз 10, причём несколько раз даже успевали давать ему имя. Немецкие исследователи назвали его мазурий (от Мазурских озёр, где полегла 10-я русская армия во время Первой мировой войны – то есть в честь победы над русской армией). А японский исследователь Масатака Огава назвал его ниппоний (Ниппон – в переводе «страна восходящего солнца»)».
– Сам Дмитрий Менделеев оставил для него место в таблице, предсказав, что его займёт «экомарганец». Его открывали раз 10, причём несколько раз даже успевали давать ему имя. Немецкие исследователи назвали его мазурий (от Мазурских озёр, где полегла 10-я русская армия во время Первой мировой войны – то есть в честь победы над русской армией). А японский исследователь Масатака Огава назвал его ниппоний (Ниппон – в переводе «страна восходящего солнца»)».
Открытия не подтвердились. Технеций стал первым элементом, полученным искусственно на циклотроне в 1930-х. Но японцы всё-таки умудрились не только оставить свой след в таблице Менделеева, но и назвать один из элементов в честь своей страны. Оказалось, что у них есть ещё один перевод «страны восходящего солнца» – Нихон. Отсюда и название 113-го элемента – нихоний.
«К слову, Менделеева потому и считали первооткрывателем периодического закона, что он предсказал свойства некоторых элементов, – продолжает химик. – Признание к нему пришло, когда эти элементы открыли, и их свойства совпали с предсказаниями. Так, ещё при жизни Менделеева, обнаружили галлий, скандий и германий. Кстати, в самой старой из сохранившихся аудиторных таблиц на месте германия – пустота. По этой детали и установили примерный возраст документа».
Так, ещё при жизни Менделеева, обнаружили галлий, скандий и германий. Кстати, в самой старой из сохранившихся аудиторных таблиц на месте германия – пустота. По этой детали и установили примерный возраст документа».
Факт №4. «Безопасная» радиация
Последний элемент, который можно найти в земной коре в заметных количествах – это уран (93-й). Все элементы, начиная с 94-го, получены искусственно. Это сверхтяжёлые, радиоактивные металлы. Например, нептуний и плутоний используют на атомных электростанциях. Но некоторые радиоактивные элементы можно найти в квартирах.
«Так, америций применяют в противопожарных датчиках, – уточняет Аркадий Курамшин. – В отличие от более дешёвых оптических такие датчики реагируют не на появление дыма, а на сами продукты горения. Как правило, их устанавливают в отделах редких рукописей в библиотеках, музеях. Ведь если там заметят дым, то спасать уже будет нечего. Некоторые ставят датчики с америцием в офисах и даже квартирах. Бояться этого не нужно, ведь в этих приборах такое мизерное количество вещества, что оно не угрожает жизни и здоровью. Что касается испускаемых америцием альфа-частиц, то они легко задерживаются корпусом датчика».
Что касается испускаемых америцием альфа-частиц, то они легко задерживаются корпусом датчика».
Факт №5. Шведский «чудо-камушек»
Больше всего неорганических элементов открыла Шведская королевская академия наук. Впрочем, это не столько заслуга, сколько везение.
«Большая часть лантаноидов в таблице Менделеева (ряд с 57-го по 71-й элемент) была открыта в составе одного минерала – иттербита, который обнаружили на шведском острове, – поясняет Аркадий Курамшин. – Поскольку все они очень похожи, то их открытие напоминало известное стихотворение: «Вот дом, который построил Джек. А это пшеница, которая в тёмном чулане хранится в доме, который построил Джек…». Сначала в этом минерале обнаружили иттербий, дальше в примесях нашли тербий и эрбий, а в их примесях – ещё элементы. Так, благодаря одному минералу открыли семь химических элементов. Повезло с камушком!»
Факт №6. Элементы-земляки
Химическим элементам часто дают названия, связанные с топонимами. Из-за этого, к примеру, школьники и студенты постоянно путают марганец с магнием.
Из-за этого, к примеру, школьники и студенты постоянно путают марганец с магнием.
«У этих элементов похожи не только символы, записанные в таблицу Менделеева, но и названия, и это не просто так, – говорит Аркадий Курамшин. – Ведь, по сути, они названы в честь одного и того же географического объекта – фессалийской Магнесии – области на севере Греции, которая существовала во времена античности, Византии. Возле Магнесии находилось месторождение солей магния, который из-за цвета называли белой магнесией. А рядом было месторождение оксида марганца – он чёрного цвета. Недолго думая, его назвали чёрной магнесией. Так что марганец и магний получили название от одного корня».
Факт №7. Гномы и духи-«помощники»
Мало кто знает, что элемент кобальт назван так в честь кобольдов – злобных гномов из германского фольклора.
«Кобальт более тугоплавкий, чем железо, – объясняет Аркадий Курамшин. – Так что в Средневековье и в эпоху Возрождения плавильные печи не могли его полностью расплавить. Тем самым он мешал выплавке железа. А поскольку людям свойственно перекладывать ответственность на других, то они решили, что это кобольды подмешивают какой-то плохой материал, мешающий честным рудокопам зарабатывать на хлеб. Кстати, никель тоже назван в честь злого духа. У немецких горняков в Средневековье была легенда про рабочего, которого звали Николас. Когда шахта обрушилась, товарищи успели выскочить, а ему не помогли. По легенде он превратился в бесплотного духа и начал мстить шахтёрам – подбрасывал какой-то тугоплавкий состав, мешавший выплавке железа. Это вещество позже назвали никелем».
Тем самым он мешал выплавке железа. А поскольку людям свойственно перекладывать ответственность на других, то они решили, что это кобольды подмешивают какой-то плохой материал, мешающий честным рудокопам зарабатывать на хлеб. Кстати, никель тоже назван в честь злого духа. У немецких горняков в Средневековье была легенда про рабочего, которого звали Николас. Когда шахта обрушилась, товарищи успели выскочить, а ему не помогли. По легенде он превратился в бесплотного духа и начал мстить шахтёрам – подбрасывал какой-то тугоплавкий состав, мешавший выплавке железа. Это вещество позже назвали никелем».
Факт №8.
 Теллур со вкусом чеснока
Теллур со вкусом чеснокаНеизвестно, кто из учёных это проверил, но, если человек проглотит половину микрограмма теллура, то от него сутки будет пахнуть так, будто бы он съел несколько долек чеснока.
«При этом это не скажется отрицательно на здоровье, – уверен Аркадий Курамшин. – В общем-то, проверять полученные вещества на вкус какое-то время было официально необходимо, чтобы описать его характеристики. Традиция эта закончилась в 1786 году после смерти шведского химика Карла Шееле, который получил синильную кислоту и попробовал её на вкус. Самое печальное, что он сделал это буквально за несколько часов до собственной свадьбы. Перед встречей с невестой решил не тратить время и поработать. Вот и доэкспериментировался. После его смерти обязательная проверка на вкус из химических протоколов исчезла, потому что стало понятно, что неизвестные вещества могут быть ядовитыми».
Факт №9. «Беспристрастные» названия
До появления ИЮПАК каждый мог назвать элемент, как вздумается. К примеру, осмий с греческого переводится как «вонючий». Теперь же одно из правил – нельзя давать элементам названия, имеющие эмоциональную окраску. Также запрещено назвать вещества в честь людей, вызывающих неоднозначную историческую оценку.
К примеру, осмий с греческого переводится как «вонючий». Теперь же одно из правил – нельзя давать элементам названия, имеющие эмоциональную окраску. Также запрещено назвать вещества в честь людей, вызывающих неоднозначную историческую оценку.
«Учёные придумали хитрый ход, как соблюсти это правило, – говорит Аркадий Курамшин. – Многие думают, что 114-й элемент назвали флеровием в честь Георгия Флёрова, стоящего у истоков советской ядерной химии. На самом деле он назван в честь Лаборатории ядерных реакций имени Флёрова. Ведь сам учёный участвовал в модернизации ядерного оружия и создании термоядерного оружия, да к тому же его личность могла бы вызвать неоднозначную оценку у конкурентов по «трансфермиевым войнам». А вот название в честь лаборатории вопросов не вызвало».
Похожей ошибкой было бы считать, что 102-й элемент – нобелий – назвали в честь Альфреда Нобеля. На самом деле – в честь Шведского института имени Нобеля. Ведь ИЮПАК рекомендует использовать в названиях новых элементов топонимы и имена великих учёных. А Нобель всё-таки был промышленником и химиком-практиком, а не великим учёным.
А Нобель всё-таки был промышленником и химиком-практиком, а не великим учёным.Интересна история названия полония. «В СССР любили говорить, что Мария Склодовская-Кюри патриотично назвала открытый ею элемент в честь Польши, – рассказывает Аркадий Курамшин. – Вряд ли эту инициативу в Российской империи восприняли бы на ура. Ведь страны с названием Польша на карте тогда не было, да и термин такой в Российской Империи, где училась Мария, не упоминали. Саму эту территорию называли губерниями Привисленского края. Так что, назвав элемент полонием, Склодовская-Кюри действительно могла привлечь внимание к Польше».
Кстати
«Таблица Менделеева для химиков – всё равно, что теория относительности Эйнштейна для физиков или теория эволюции для биологов, – говорит Аркадий Курамшин. – Многие норовят доказать неверность этих теорий, переделать периодическую систему. В 2007 году на Менделеевском съезде в Москве я встретил порядка 10 человек, каждый из которых предлагал свой вариант «таблицы Менделеева». Как правило, это были кандидаты технических наук на пенсии, пожилые изобретатели с устаревшей теоретической базой знаний. Таблица давно стала поводом для спекуляций. Неслучайно одно из старейших российских профильных периодических изданий «Журнал общей химии», одним из основателей которого был Дмитрий Менделеев (при нём – это был журнал Русского химического общества) в наше время взял за правило не принимать к публикации статьи, посвящённые созданию очередной версии Периодической системы.
Как правило, это были кандидаты технических наук на пенсии, пожилые изобретатели с устаревшей теоретической базой знаний. Таблица давно стала поводом для спекуляций. Неслучайно одно из старейших российских профильных периодических изданий «Журнал общей химии», одним из основателей которого был Дмитрий Менделеев (при нём – это был журнал Русского химического общества) в наше время взял за правило не принимать к публикации статьи, посвящённые созданию очередной версии Периодической системы.
день рождения IUPAC и история открытия периодического закона
Публикуем еще один текст по следам конференции Mendeleev 150, прошедшей в Университете ИТМО с 26 по 28 июля. В эти дни участники международного события чествовали не только годовщину создания периодической таблицы, но и день рождения Международного союза теоретической и прикладной химии (International Union of Pure and Applied Chemistry — IUPAC), под эгидой которого проходила конференциях. Об организации, водке «Менделеев» и истории открытия периодического закона – в нашем тексте.
Об организации, водке «Менделеев» и истории открытия периодического закона – в нашем тексте.
Международная конференция Mendeleev 150 состоялась в рамках года Периодической таблицы химических элементов, объявленного ООН, и проходила при поддержке двух организаций: UNESCO и Международного союза теоретической и прикладной химии (International Union of Pure and Applied Chemistry — IUPAC).
IUPAC занимает место центрального органа в мире по делам химической номенклатуры и терминологии: сотрудники организации устанавливают стандарты в областях методологии исследований, атомных весов и оценки других данных. Кроме того, IUPAC занимается публикацией научных докладов и книг, а также помогает в проведении крупных конференций по химии, таких как Mendeleev-150. В этом году организации исполнилось 100 лет.
Мартин Полякофф«IUPAC и его официальная поддержка имеют большое значение для конференции. Ведь именно эгида IUPAC является гарантом качества организации и научной программы мероприятий в области химии.
Поддержка IUPAC является весомым поводом для ученых мирового уровня посетить конференцию по химии, кроме того, организация активно распространяет информацию о поддерживаемом мероприятии по всем существующим в распоряжении союза каналам. Отдельной особенностью Mendeleev 150 стал тот факт, что столетие союза пришлось на третий день конференции. Со словами поздравления выступили экс-президент IUPAC Наталия Тарасова (Россия) и член исполнительного комитета IUPAC Mei-Hung Chiu (Китай). Специальное видеообращение по просьбе организаторов записал действующий президент IUPAC Qi-Feng Zhou (Китай)», – прокомментировал председатель оргкомитета Михаил Курушкин.
На день ранее свои поздравления передал и член программного комитета конференции, сэр Мартин Полякофф – профессор химии Ноттингемского университета, обладатель ордена Британской империи (командор), медали Леверхалма от Лондонского королевского общества и титула рыцаря-бакалавра. Авторитетному ученому не удалось приехать в Санкт-Петербург, и он записал специальное видеообращение для участников Mendeleev 150. Он поздравил всех присутствующих с годовщиной периодической таблицы химических элементов и поднял в честь праздника рюмку с водкой под названием «Менделеев».
Ученый известен как активный популяризатор науки: он является одним из создателей научно-популярного проекта Periodic Videos, где авторы роликов знакомят зрителей с химическими элементами. Члены команды YouTube-канала создали видео в честь начала года Периодической таблицы, которое транслировалось во время Mendeleev 150.
Кроме Полякоффа, во второй день международной конференции перед гостями выступили и другие ученые со всего мира. В их числе Пекка Пююкке, профессор Хельсинского университета. Он рассказал о внутренних механизмах и истоках происхождения периодической таблицы. По словам финского исследователя, еще до фундаментальной работы Менделеева проводились попытки сортировки химических элементов на основе их физических свойств. Одним из первых предложенных способов стали триады Йиоганна Вольганга Деберейнера (Döbereiner’s triads). В 1817 году он обнаружил, что стронций обладал свойствами, промежуточными по отношению к кальцию и барию. Затем к 1829 году Доберейнер нашел и другие группы из трех элементов. Отсюда название «триады». После, в 1862 году, французский геолог и химик Александр Эмиль Шанкуртуа предложил систематизацию химических элементов, основанную на закономерном изменении атомных масс — «земную спираль» (vis tellurique) или «цилиндр Бегуйе».
Он рассказал о внутренних механизмах и истоках происхождения периодической таблицы. По словам финского исследователя, еще до фундаментальной работы Менделеева проводились попытки сортировки химических элементов на основе их физических свойств. Одним из первых предложенных способов стали триады Йиоганна Вольганга Деберейнера (Döbereiner’s triads). В 1817 году он обнаружил, что стронций обладал свойствами, промежуточными по отношению к кальцию и барию. Затем к 1829 году Доберейнер нашел и другие группы из трех элементов. Отсюда название «триады». После, в 1862 году, французский геолог и химик Александр Эмиль Шанкуртуа предложил систематизацию химических элементов, основанную на закономерном изменении атомных масс — «земную спираль» (vis tellurique) или «цилиндр Бегуйе».
На протяжение шестидесятых годов 19 века свои работы представляли Юлиас Лотар Мейер и Дмитрий Менделеев, которые впоследствии совместно получили медаль от Лондонского международного общества. Менделеев же, рассказывает Пююкке, предсказал элементы, еще не открытые на тот момент: скандий, галлий и германий.
Менделеев же, рассказывает Пююкке, предсказал элементы, еще не открытые на тот момент: скандий, галлий и германий.
«Я уважаю исследователей, которые смотрят в будущее. Знаменитый русский физик-кристаллограф Александр Китайгородский говорил, что существуют три класса теорий. Теории первого класса прогнозируют, второго — запрещают, а третьего — объясняют. Лично я ценю прогнозирующие», — заметил Пекка Пююкке.
Об истории открытия периодического закона также рассказывал профессор СПбГУ Игорь Дмитриев. Историк вспомнил, что основой для написания работы Менделеева послужили результаты конгресса в Карлсруэ 1860 года, а также работы Жана Батиста Дюма, который много занимался классификацией органических соединений.
Международная конференция Mendeleev 150«В октябре 1867 года Менделеев начинает читать курс лекций по химии для студентов первого курса Санкт-Петербургского университета.
Ему, естественно, нужно было что-то порекомендовать в качестве учебника или пособия. Но он не смог выбрать ничего подходящего, и поэтому, отчасти по уговору друзей, начал писать свой учебник. Это версия самого Менделеева. Но была еще одна причина, толкавшая его к написанию учебника, — деньги. Менделеев к тому времени был женат, уже рос сын, осенью того года выяснилось, что родится еще один ребенок. К тому же ученый купил имение в Тверской губернии и решил сделать его образцовым. На все это нужны были деньги. Если удастся написать большой толстый учебник и переиздавать его время от времени, то это издание может давать очень хороший дополнительный доход. Так оно и случилось», — рассказывает Игорь Дмитриев.
Периодический закон — один из самых странных законов, и история его открытия тоже очень странная. Во всяком случае, необычная во многих отношениях, продолжает Дмитриев. В первой публикации Менделеев употребляет слово «закон» всего один раз, и относится это определение отнюдь не к тому, что мы сейчас называем периодическим законом. Автор отнес слово «закон» к тому утверждению, что свойства элемента находятся в зависимости от атомного веса. А уже второе утверждение, что эта зависимость имеет периодический характер, конкретизирует первое. Для Менделеева первое утверждение было гораздо важнее второго. Оно, говорил ученый, органично вписывалось во все его химическое мировоззрение.
Автор отнес слово «закон» к тому утверждению, что свойства элемента находятся в зависимости от атомного веса. А уже второе утверждение, что эта зависимость имеет периодический характер, конкретизирует первое. Для Менделеева первое утверждение было гораздо важнее второго. Оно, говорил ученый, органично вписывалось во все его химическое мировоззрение.
Со временем Менделеев развивает работу, посылает ее за границу и получает известность. Дальше ученый делает шаг, который станет трагедией его жизни. Любой исследователь на его месте всю жизнь после открытия закона занимался бы двумя вещами: приоритетными спорами и изучением закономерностей в системе, как меняются различные свойства. А Менделеев в конце 1871 года в рабочем дневнике делает запись о насосах. Он начинает изучать новую тему: ищет мировой эфир. Подробнее о дальнейшей жизни Менделеева можно прочитать в материале ITMO.NEWS.
Игорь ДмитриевВо время второго дня проведения Mendeleev 150 другие ученые также рассказывали о способах применения таблицы в современной работе. Например, профессор Кристофер Хендон из Университета Орегона рассказал, как с помощью таблицы создает материалы и проводит каталитические превращения. А другой исследователь из США, профессор химии в Университете Техаса Кит Паннелл, поделился опытом изучения 14-ой подгруппы таблицы (углерод, кремний, германий, олово и свинец) и их общего свойства, известного как конкатенация — способность формировать связи.
Например, профессор Кристофер Хендон из Университета Орегона рассказал, как с помощью таблицы создает материалы и проводит каталитические превращения. А другой исследователь из США, профессор химии в Университете Техаса Кит Паннелл, поделился опытом изучения 14-ой подгруппы таблицы (углерод, кремний, германий, олово и свинец) и их общего свойства, известного как конкатенация — способность формировать связи.
Интересные факты о таблице Менделеева
Благодаря Генеральной Ассамблее ООН 2019 официально стал Международным годом таблицы Менделеева. Расскажем несколько интересных фактов о периодической таблице химических элементов.
Таблица МенделееваРодители смогут вспомнить школьную программу, а школьники узнают полезную информацию для расширения кругозора и успехов на уроках и олимпиадах по химии.
Интересные факты об истории таблицы Менделеева
Факт #1. Создателем таблицы считается Дмитрий Менделеев, но до него похожую схему представил научному сообществу Джон Ньюленд. Правда, его не восприняли всерьез.
Факт #2. Российский ученый Дмитрий Иванович впервые опубликовал свой вариант таблицы в 1869 году, окончательный вид с доработками и улучшениями открытие приобрело только в 1871 году.
Факты об элементах таблицы Менделеева
У большинства элементов таблицы Менделеева есть своя увлекательная история открытия и необычные свойства. Опишем некоторые из них.
Факт #1. Благодаря урану (U) ученый Анри Беккерель получил Нобелевскую премию. Он понял, что вещество радиоактивно, когда случайно положил соли урана на фотопластинку. А еще уран — последний по номеру природный элемент в таблице, остальные вещества можно создать только искусственным путем.
Факт #2. 200 лет назад исследователи Льюис и Кларк прошли через всю Америку к Тихому океану. Они взяли с собой в путь ртутное слабительное. А современные ученые по следам ртути (Hg), которая со временем не разлагается, смогли узнать точное место лагеря путешественников.
Они взяли с собой в путь ртутное слабительное. А современные ученые по следам ртути (Hg), которая со временем не разлагается, смогли узнать точное место лагеря путешественников.
Факт #3. Галлий (Ga) стал первым пробелом в таблице, заполненным уже после смерти ученого. Металлический галлий известен тем, что он сохраняет твердость при комнатной температуре, но в руках плавится.
Факт #4. Одни наименования химических элементов произошли от латинских слов, связанных со свойствами веществ. Некоторые элементы получили названия в честь ученых. А часть веществ носит имена героев мифов.
Факт #5. Элемент титан (Ti) назвали именем могучих сыновей богини Геи. Это один из самых твердых металлов. А его диаксид переливаетсямвсеми цветами радуги.
Факт #6. Тантал (Ta) носит имя героя древнегреческих мифов, совершившего несколько непростительных преступлений.
Факт #7. Торий (Th) назвали в честь бога грома Тора.
Факт #8. Ванадий (V) отличается соединениями с необычной окраской, поэтому назван именем древнескандинавской богини красоты.
Факт #9. Уран (U), Нептуний (Np) и Плутоний (Pu) также носят имена богов Урана, Нептуна (Посейдона) и Плутона (Аида).
Мифы о таблице Менделеева
Факт #1. Периодическая таблица химических элементов также известна распространенными мифами. Самый популярный гласит, что ученый однажды увидел сразу всю таблицу во сне. Но исследование жизни Менделеева говорит о том, что на самом деле он потратил немало времени и сил на свое открытие.
Факт #2. По другой легенде буквы армянского алфавита связаны с таблицей Менделеева. В разборе армянских названий таких веществ, как золото, серебро, свинец и ртуть, некая связь действительно прослеживается. Но это, скорее, совпадение. Армянские ученые вряд ли могли заранее предугадать открытие всех элементов таблицы.
Открытие Менделеева — огромный вклад в науку. И хороший повод для появления интересных фактов и мифов. А что еще вы знаете о таблице Менделеева? Пишите свои дополнения в комментариях.
И хороший повод для появления интересных фактов и мифов. А что еще вы знаете о таблице Менделеева? Пишите свои дополнения в комментариях.
НАЦИОНАЛЬНЫЙ ПЕРИОДИЧЕСКИЙ ДЕНЬ – 7 февраля
НАЦИОНАЛЬНЫЙ ПЕРИОДИЧЕСКИЙ ДЕНЬ7 февраля Национальный день таблицы Менделеева отмечает публикацию первой таблицы элементов. Мы также посмотрим, как периодическая таблица Менделеева изменилась с годами.
Периодическая таблица Менделеева имеет долгую историю. Это и открытие элементов во многом повлияли на науку. Древний человек знал лишь несколько элементов. Однако к I веку нашей эры.человечество знало о таких элементах, как золото, серебро, медь, железо, свинец, олово, ртуть, сера и углерод. Со временем мы добавили в свои открытия мышьяк, сурьму, фосфор и цинк. К 1809 году было обнаружено 47 элементов. Пришло время организовать, и Иоганн Дёберейнер сделал одну из первых попыток сделать это. В 1817 году он организовал элементы в группы по три, или триады, на основе сходных качеств.
7 февраля 1863 года английский химик Джон Ньюлендс опубликовал одну из первых таблиц элементов.Ньюлендс разделил известные 56 элементов на 11 групп на основе «Закона октав». Его таблица предполагает, что любой элемент будет иметь свойства, аналогичные свойствам элементов на восемь позиций до и после него в таблице.
Расположив элементы в соответствии с возрастающим атомным весом, Ньюлендс был одним из первых ученых, обнаруживших закономерность в свойствах элементов. В результате его стол оставил место для новых открытий. Он даже предсказал, что будущие открытия дополнят таблицу. Фактически, Ньюлендс правильно предсказал открытие германия.
Открытия будущего В то время как некоторые части периодической таблицы Ньюлендса содержали недостатки, то же самое было и в других таблицах, предложенных позже. В 1869 году химик Дмитрий Менделеев опубликовал статью о разработке новой таблицы Менделеева. В таблице Менделеева элементы также расположены по атомной массе. К этому времени были обнаружены только 60 из более чем 100 элементов, которые мы знаем сегодня.
В таблице Менделеева элементы также расположены по атомной массе. К этому времени были обнаружены только 60 из более чем 100 элементов, которые мы знаем сегодня.
Как и в предыдущих таблицах, некоторым из этих элементов были приписаны неточности. Менделеев исправил некоторые из этих неточностей, но не все.Менделеев делал предположения о других, из-за чего элементы неправильно размещались на столе. Как и Ньюлендс, Менделеев также предсказал открытия, и он правильно предсказал свойства пяти элементов и их соединений.
Открытия на протяжении всей карьеры шотландца Уильяма Рамзи с 1892 по 1910 год, наряду с Джоном Уильямом Струттом, Моррисом Трэверсом и Фредериком Содди, привели к идентификации благородных газов. В 1904 году Рамзи была присуждена Нобелевская премия за открытие пяти элементов.
Генри Мозли Генри Мозли, физик-экспериментатор, внес свой вклад в разработку современной таблицы Менделеева. В 1913 году Мозли обнаружил, что каждый элемент имеет определенное количество протонов. В результате позже, хотя и не при его жизни, были обнаружены четыре новых химических элемента.
В результате позже, хотя и не при его жизни, были обнаружены четыре новых химических элемента.
С начала 20 века таблица Менделеева практически не изменилась. Однако 21 век еще молод. Некоторые исследователи предлагают новые подходы к периодической таблице Менделеева, сохраняя при этом ее целостность, как к одному из самых ценных инструментов в химической науке.Текущая таблица насчитывает 118 элементов.
КАК СОБЛЮДАТЬ #PeriodicTableDayПроверьте свои знания таблицы Менделеева. Празднуйте с помощью мелочей с Периодической таблицей или предлагайте друг другу называть элементы. Сделайте еще один шаг и назовите количество протонов в каждом элементе.
Узнайте больше об элементах периодической таблицы, прочитав 7 элементов, создающих историю.
Посетите www.PeriodicTableDay.org для получения дополнительной информации. Используйте #PeriodicTableDay для публикации в социальных сетях.
Педагоги, посетите страницы классной комнаты с Национальным календарем, чтобы узнать, как включить День национальной таблицы Менделеева в свой класс.
7 февраля 2016 года, первый Национальный день таблицы Менделеева, был учрежден 7 февраля 2016 года. Этот день призван способствовать преодолению трудностей, преодолеваемых при разработке современной таблицы Менделеева. Г-н Дэвид Т. Стейнекер, писатель, изобретатель и учитель химии в государственных школах округа Джефферсон в Кентукки, вдохновлен этими проблемами.Он выступил с инициативой отметить Национальный день таблицы Менделеева на основе первой таблицы элементов Джона Ньюлендса, опубликованной 7 февраля 1863 года.
Существует более 1500 национальных дней. Не пропустите ни одного. Празднуйте каждый день® с Национальным календарем®!
Периодическая таблица (1865-1934) | Химия
Рождение Периодической таблицы произошло на химическом конгрессе (химическом конгрессе) 3-5 сентября 1860 года в Карлсруэ, Германия.
Со времен Лавуазье ученые искали способы объяснить химическое и физическое сходство элементов, которое таинственным образом повторялось через равные промежутки времени с увеличением атомного веса.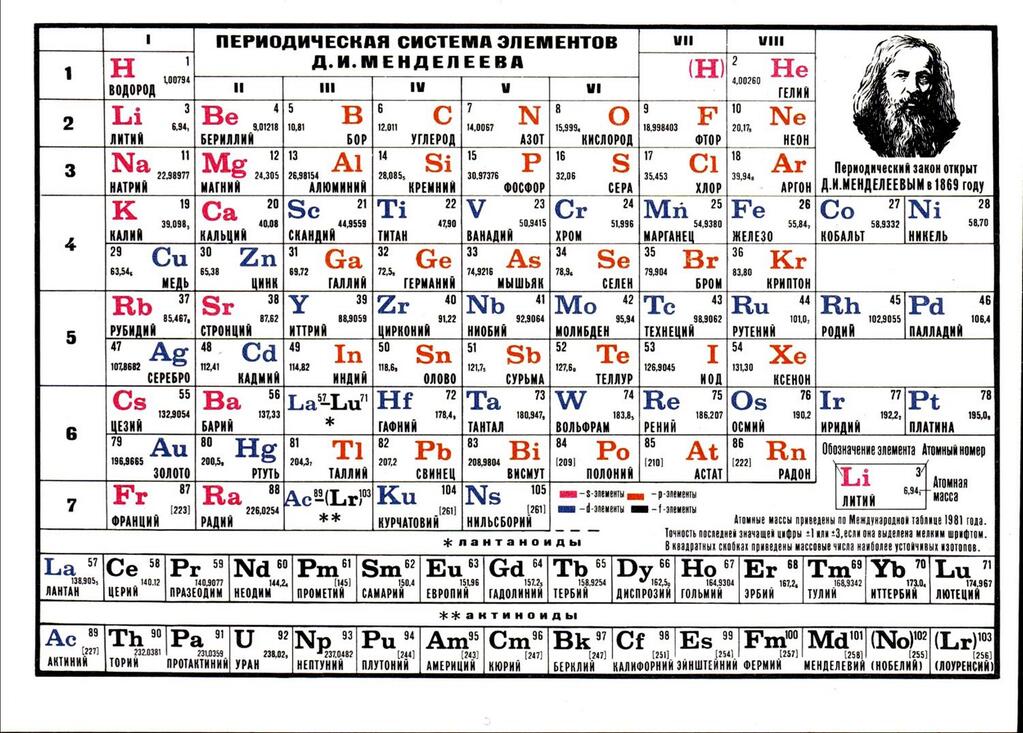 Схемы включали все, от спирали в 45 градусов – теллурической спирали – до закона «Закона октав». Частично проблема заключалась в том, что атомный вес часто рассчитывался как кратное (или дробное) значение кажущегося эквивалентного веса элемента. Даже формула для воды – H 2 O, 2 атома водорода на 1 атом кислорода – была предметом обсуждения.
Схемы включали все, от спирали в 45 градусов – теллурической спирали – до закона «Закона октав». Частично проблема заключалась в том, что атомный вес часто рассчитывался как кратное (или дробное) значение кажущегося эквивалентного веса элемента. Даже формула для воды – H 2 O, 2 атома водорода на 1 атом кислорода – была предметом обсуждения.
Именно на этой встрече итальянский химик Станислао Канниццаро (1826-1910) вновь представил теорию, предложенную Амедео Авогадро (1776-1856), в которой валентность может быть использована для установления самосогласованного набора истинных, абсолютных атомных атомов. веса.Два химика в аудитории, немецкий химик Лотар Мейер (1830-1895) и русский химик Димитрий Менделеев (1834-1907), быстро поняли, как эти исправленные числа позволили установить новый порядок элементов.
Каждая из них впоследствии предложила свои собственные периодические таблицы, но именно версия Менделеева, опубликованная на год раньше Мейера, в конечном итоге стала стандартной. Менделеев был настолько смел, что предсказал не только существование новых элементов, включая скандий, галлий и германий, но и свойств каждого из них.Периодическая таблица в том виде, в каком мы ее знаем сегодня, приобрела свою окончательную форму с введением атомных чисел в 1912 году.
Менделеев был настолько смел, что предсказал не только существование новых элементов, включая скандий, галлий и германий, но и свойств каждого из них.Периодическая таблица в том виде, в каком мы ее знаем сегодня, приобрела свою окончательную форму с введением атомных чисел в 1912 году.
1865-1874: гелий
Гелий, 2
Школа колледжа сенатора О’Коннора
Северный Йорк, Онтарио, Канада
Учитель: Алисия Копрянюк
Художник: Якуб Брол
Мое изображение гелия следующее: с правой стороны шестиугольника находится воздушный шар, на котором изображен французский флаг. Я выбрал для воздушного шара французский флаг, потому что гелий был открыт французским астрономом Пьером Жюлем Сезаром Янссеном.На другой стороне шестиугольника я нарисовал Солнце, потому что именно там впервые был обнаружен гелий. В частности, это было обнаружено как желтая линия на границе Солнца. Кроме того, я добавил пурпурное свечение в качестве пламени, представляющего цвет, который гелий излучает в газоразрядной трубке.
Примечание. В исходный плакат были внесены исправления. Тулий (Tm, 69) был перемещен с 1865-1874 гг. На 1875-1884 гг. Веб-сайт, интерактивный PDF-файл и загружаемый плакат обновлены, чтобы отразить это изменение.
Вернуться к началу.
1875-1884: галлий, гольмий, иттербий, скандий, самарий, гадолиний, тулий
Галлий, 31
Средняя школа Хадсонвилля
Хадсонвилл, Мичиган, США
Учитель: Дуг Раган
Художник: София Путман
Галлий был открыт в 1875 году Полем-Эмилем ЛеКок де Буабодран с помощью спектроскопа, который пропускает белый свет через призму, разделяя свет на отдельные цветовые длины волн за счет преломления.Мой дисплей включает отдельные цвета радуги, чтобы показать, как он обнаружил элемент. Атомный номер галлия (Ga) равен 31. Галлий – это металл, который является хрупким твердым телом при низких температурах и жидким при температурах выше 85,57 ⁰F (29,76 ⁰C). Я сделал вырез капающей жидкости, чтобы представить жидкое состояние элементов, и вырезал твердые вырезки, чтобы показать это как твердое тело.
Гольмий, 67
Католический колледж Нэгл
Джералдтон, Западная Австралия, Австралия
Учитель: миссис.Элизабет Коста
Художник: Эшли Нейсбитт и Эмили Макферсон
Наш дизайн отражает открытие и магнитные свойства гольмия. Трое мужчин, открывших элемент, изображены спектральными цветными линиями гольмия. Наиболее распространенной фигурой является швед Пер Теодор Клеве, главный первооткрыватель стихии. Атомы гольмия представлены в виде разноцветных кружков из белых и желтых точек. Магнит и окружающие магнитные поля иллюстрируют магнитные свойства элемента.Линейный спектр в основании рисунка представляет собой линии поглощения гольмия. Длины волн линий поглощения позволили открыть гольмий. Синий и желтый оттенки символизируют флаг Швеции.
Иттербий, 70
Ранний / средний колледж в GTCC Jamestwon
Джеймстаун, Северная Каролина, США
Учитель: Элизабет Саншайн
Художник: Хна Агилера
Создавая свои работы, я исследовал элемент иттербий, его историю и открытие. Иттербий открыл Жан Шарль Галиссар де Мариньяк, и я решил, что он заслуживает похвалы за этот вклад в науку, поэтому нарисовал его справа. Поскольку иттербий был открыт в шведском городе, я добавил шведский флаг. Эксперименты, в ходе которых был обнаружен иттербий, проводились в Женевском университете, поэтому я нарисовал профиль университета внизу. Справа я нарисовал, как иттербий появляется в природе, и доработал все, добавив представление символа в середине рисунка.
Иттербий открыл Жан Шарль Галиссар де Мариньяк, и я решил, что он заслуживает похвалы за этот вклад в науку, поэтому нарисовал его справа. Поскольку иттербий был открыт в шведском городе, я добавил шведский флаг. Эксперименты, в ходе которых был обнаружен иттербий, проводились в Женевском университете, поэтому я нарисовал профиль университета внизу. Справа я нарисовал, как иттербий появляется в природе, и доработал все, добавив представление символа в середине рисунка.
Скандий, 21
Средняя школа Эйвонворта
Питтсбург, Пенсильвания, США
Учитель: Бриттни Ливси
Художник: Ава Калли
Скандий – двадцать первый элемент периодической таблицы Менделеева. Он был открыт в 1879 году Ларсом Ф. Нильсоном. Элемент получил название «Скандий», потому что он был найден в Швеции, которая является частью Скандинавского региона. Причина, по которой на плитке изображен горный хребет, заключается в том, что в Скандинавском регионе есть горы.Розово-голубой велосипед – обычное хобби шведских граждан. Скандий также используется в велосипедах, наряду с бейсбольными битами. Шведский флаг в велосипедной корзине показывает страну, где был обнаружен скандий.
Скандий также используется в велосипедах, наряду с бейсбольными битами. Шведский флаг в велосипедной корзине показывает страну, где был обнаружен скандий.
Самарий, 62
Coláiste Choilm
Swords, Дублин, Ирландия
Учитель: Шон Келлехер
Художник: Студенты естественных наук 1-го класса переходного периода
Джон Джоли, ирландский геолог и физик, «открыл» элемент гиберниум, изучая кусок гранита в 1907 году.(Самарий был открыт ранее в 1853 году). Джоли был пионером в области радиоактивного датирования Земли и соавтором «Дублинского метода» внутривенной лучевой терапии: самарий – бета-излучатель, используемый в радиотерапии рака костей. Миниатюризация магнитов в динамиках, используемых при переходе от отдельно стоящих радиоприемников к Walkman и другим портативным аудиоустройствам, включала добавление самария.
Гадолиний, 64
Озель Шисли Теракки Тепеорен Анадолу Лизеси
Стамбул, Тузла, Турция
Учитель: Гюльсен Сокуллу
Художник: Алара Айдын
Я начал рисовать с телевизора, потому что гадолиний используется в цветном телевидении. Сначала я хотел нарисовать вены (поскольку в МРТ используются соединения гадолиния), но подумал, что это будет немного сложно. Цвета символа и числа взяты с изображения гадолиния. И последнее, но не менее важное: первооткрыватель гадолиния (Жан Шарль Галиссар де Мариньяк) определенно должен занять место в произведении искусства.
Сначала я хотел нарисовать вены (поскольку в МРТ используются соединения гадолиния), но подумал, что это будет немного сложно. Цвета символа и числа взяты с изображения гадолиния. И последнее, но не менее важное: первооткрыватель гадолиния (Жан Шарль Галиссар де Мариньяк) определенно должен занять место в произведении искусства.
Примечание. В исходный плакат были внесены исправления. Торий (Th, 90) был перенесен из десятилетия 1875-1884 гг. В 1825-1834 гг. Веб-сайт, интерактивный PDF-файл и загружаемый плакат обновлены, чтобы отразить это изменение.
Тулий, 69
King High School
Тампа, Флорида, США
Учитель: Эллисон Мерсер
Художник: Харрисон Альстер
Пер Теодор Клев обнаружил тулий, он изображен в центре произведения искусства. Вверху – рисунок тулия, а вокруг Пер Теодора Клеве – атомный номер 69, символ Tm и классическая плитка тулия в периодической таблице. Ручка и чернила.
Вернуться к началу.
1885-1894: празеодим, неодим, германий, диспрозий, аргон, фтор
празеодим, 59
Средняя школа Вайса
Пфлюгервилль, Техас, U. S.A.
S.A.
Учитель: Кристина Хотчкина
Художники: Анастасия Т., Кайла К. и Бренда О.
Мы выяснили, что наш элемент используется в сценическом освещении, часть его лампочки, и был открыт Карлом Ауэром фон Вельсбахом. В греческом переводе это «зеленый близнец» из-за того, что он производит зеленый оксид. Мы решили сделать фон сценой с типами сценического освещения, в которых присутствует наш элемент, и на сцене у нас есть символ для зеленых близнецов (римская цифра для двух зеленых цветов).Мы раскрасили плитку так, чтобы она выглядела так, как будто она светится от сценического освещения.
Неодим, 60
Сеульская зарубежная британская школа
Сеул, Южная Корея, Южная Корея
Учитель: Ким Стюарт
Художник: Ирен Чо
Неодим используется в предметах, которые мы используем в повседневной жизни, например, в зажигалках и магнитах. Зеленый край странной формы напоминал северную часть Австрии, где в 1885 году Карл Ауэр фон Вельсбах открыл неодим. В центре большой рисунок металлического неодима в стеклянной пробирке. Я попытался сделать его более похожим на настоящую вещь, используя металлический серебристый маркер и добавив карандашные пометки (серебристый цвет не проявился на отсканированной копии).
В центре большой рисунок металлического неодима в стеклянной пробирке. Я попытался сделать его более похожим на настоящую вещь, используя металлический серебристый маркер и добавив карандашные пометки (серебристый цвет не проявился на отсканированной копии).
Германий, 32
5-я гимназия Митилини
Митилини, Лесбос, Греция
Учителя: Василики Томаиди и Мария Яннику
Художник: Анна – Мария Цокару
Этот рисунок был сделан на уроках химии и искусства.Когда я услышал об этой теме, первое, что пришло мне в голову, была настольная игра, в которую я играл со своими друзьями. Речь шла о нескольких горняках, которые пытались найти золото, точно так же, как Клеменс Винклер, открывший германий в шахте в 1886 году. Итак, первая часть моего рисунка изображает шахтера. Затем я решил нарисовать еще несколько применений германия. В общем, мой рисунок разворачивает в хронологическом порядке всю историю Германии.
Диспрозий, 66
Средняя школа Лексингтона
Лексингтон, Южная Каролина, U. S.A.
S.A.
Учитель: Сэм Оксли
Художник: Элизабет Маллиган
На изображении диспрозия справа изображена большая Эйфелева башня, потому что химик, открывший этот элемент, Поль Эмиль Лекок де Буабодран, был французом. На одной из опор башни написан год обнаружения диспрозия (1886 г.). Атомный номер свисает с верхней части плитки. Диспрозий обладает сильным магнитным полем, поэтому символ показан обращенным к магниту. Внизу есть рисунок естественного серого цвета элемента.На рисунках показаны красные лазеры и ветряные турбины, чтобы подчеркнуть практическое применение элемента.
Аргон, 18
Средняя школа округа Арнприор
Арнприор, Онтарио, Канада
Учитель: Шерил Уэлбэнкс
Художник: Кейлин Пру
Название аргон происходит от греческого слова, означающего ленивый или инертный, потому что элемент не очень легко реагировал. Мы изобразили лень стихии изображением ленивца. Корона означает, что элемент представляет собой благородный газ.Лампочка показывает, как аргон используется в лампах накаливания, чтобы нити не перегорели. Цвет фона был выбран, поскольку он представляет диапазон цветов, которые аргон проявляет в электрическом поле. Наконец, нижнее изображение представляет собой баллон с газом, поскольку аргон используется в качестве защитного газа при сварке.
Цвет фона был выбран, поскольку он представляет диапазон цветов, которые аргон проявляет в электрическом поле. Наконец, нижнее изображение представляет собой баллон с газом, поскольку аргон используется в качестве защитного газа при сварке.
фтор, 9
Техасский университет A&M Сан-Антонио
Сан-Антонио, Техас, Соединенные Штаты Америки
Учитель: доктор Дж. Роберт Шелтон
Художник: Киара Крафт
Фтор был впервые обнаружен французским химиком Анри Муассаном в 1886 году.Он выделил и открыл этот элемент, пропустив электричество через фтористоводородную кислоту и фторид калия с помощью электролиза.
Вернуться к началу.
1895-1904: европий, неон, криптон, ксенон, полоний, радий, радон, актиний
европий, 63
Колледж доктора Алетты Якобс
Хугезанд, Гронинген, Нидерланды
Учитель: доктор Мишель Вийнхольд
Художник: Кейтлин Вийлбриф
Европий – один из наиболее реактивных элементов из ряда лантанидов. Он был обнаружен в ходе ранних спектроскопических экспериментов в 1890 году П.Е. Лекок де Буабодран, но его открытие приписывают Эжену-Анатолю Демарсе, который первым выделил элемент в чистом виде в 1896 году.
Он был обнаружен в ходе ранних спектроскопических экспериментов в 1890 году П.Е. Лекок де Буабодран, но его открытие приписывают Эжену-Анатолю Демарсе, который первым выделил элемент в чистом виде в 1896 году.
Когда страны Европейского Союза ввели свою общую валюту (евро), элемент, названный в честь Европы, был выбран для защиты банкнот 5 евро, поскольку соединения Eu излучают флуоресцентный свет. Этот секрет был раскрыт голландскими химиками, когда они игрались в лаборатории с новой валютой.Они так и не определили точное соединение, потому что это повлечет за собой уничтожение банкноты, что является преступлением.
В моем классе у меня очень тихая ученица, которая постоянно что-то рисует и зарисовывает. Поэтому я попросил ее изготовить эту плитку, так как она сочетала бы ее любовь к искусству с уроками химии.
Неон, 10
Канадская международная школа Вьетнам
Хошимин, Вьетнам
Учитель: Алекс Лав
Художник: Нгуен Чыонг Тху Нгок
Английские ученые сэр Уильям Рамзи и Моррис Траверс, две грани в центре плитки, заморозили образец аргона с помощью жидкого воздуха в 1898 году. Они собрали первое количество испарившегося газа, поместили образец в атомный спектрометр и наблюдали красный свет, светящийся от газа. Этот яркий цвет является фоном, представленным на иллюстрации. Более того, неон является пятым по распространенности элементом во Вселенной, но на Земле он встречается редко. Этот элемент используется для создания ярких и ярких неоновых огней, которые можно увидеть на рекламных вывесках.
Они собрали первое количество испарившегося газа, поместили образец в атомный спектрометр и наблюдали красный свет, светящийся от газа. Этот яркий цвет является фоном, представленным на иллюстрации. Более того, неон является пятым по распространенности элементом во Вселенной, но на Земле он встречается редко. Этот элемент используется для создания ярких и ярких неоновых огней, которые можно увидеть на рекламных вывесках.
Криптон, 36
A.L. Fortune Secondary
Эндерби, Британская Колумбия, Канада
Учитель: Mrs.Аннетт Тоуп
Художник: Тристан Баумле
Моя первоначальная идея заключалась в том, чтобы символ элемента располагался посередине, как в обычной таблице Менделеева. В ходе своего исследования я решил включить как можно больше различных вариантов использования криптона. Я начал с флуоресцентного света в верхней части произведения искусства. В качестве фона я добавил лазеры – еще одно использование криптона. Зеленый кубический кристалл показывает криптон в его кристаллизованной форме. Наконец, я поставил флаг Великобритании и год его открытия, 1898 год.
Наконец, я поставил флаг Великобритании и год его открытия, 1898 год.
Ксенон, 54
Франкфуртская международная школа
Оберурзель, Гессен, Германия
Учитель: Mr.Ви Куммари
Автор: Бронвин Сэндфилд
В верхней части плитки я нарисовал фотопленку, показывающую открытие элемента. На первом изображении показано расположение Университетского колледжа Лондона. На втором изображены два первооткрывателя, Уильям Рамзи и Моррис Траверс. Последнее изображение показывает время, когда оно было обнаружено. Я также написал некоторые его характеристики на стороне пленки; бесцветный, без запаха и инертный. Я также добавил точки кипения и плавления газа и показал, что это один из благородных газов.
Полоний, 84
Пекинский университет Цзяотун (BJTU) (через Университет Ватерлоо)
Ватерлоо, Онтарио, Канада
Учитель: Рик Марта
Художник: Синенг (Винсент) Чжао; представляющий класс 2018 студентов BJTU Nano
1. В 1898 году польский ученый Мария Кюри впервые выделила полоний (Po) путем обработки многих тонн радиоактивной урановой руды, называемой ураном.
2. По имеет уникальную простую кубическую кристаллическую структуру.
3. Po – первый радиоактивный элемент естественного происхождения, встречающийся в периодической таблице.По является излучателем альфа-частиц.
4. В честь 150-летия Периодической системы Менделеева русского ученого написано 150 лет на русском языке.
5. Отмечено 100-летие ИЮПАК.
6. Табак может содержать следовые количества Po; Показано, что сигарета указывает на другую опасность для здоровья, связанную с курением.
Радий, 88
Mount Royal University
Калгари, Альберта, Канада
Учитель: Крис Ловалло
Художник: Алия МакКракен, Кейси Хейрман
Студенты начали с вопросника «Кто-что-где-когда-почему» , чтобы направлять свои исследования радия.Выдержки идей относительно того, как визуально выразить свои исследования, приведены ниже:
Что? Радиоактивный символ – рисунок руки, держащей радий, изображающий повреждение клеток и ДНК.
Кто? Рисунок Мари и Пьера Кюри – Портреты людей, участвовавших в открытии
Где? Рисунок радиевых шахт или Ecole de Physique – Рисунок радиевых горячих источников
Когда? Цитируя Марию Кюри: «Радий – это элемент, он принадлежит людям» – Рисунок радиоактивных бумаг Мари и Пьера
Почему? Светящиеся в темноте часы – люди, использующие радий в повседневной жизни.
Радон, 86
Средняя школа Сикамора
Цинциннати, Огайо, США
Учитель: Майкл Гейер
Художник: SHS Chemistry Club
Рисунок на этой плитке, нарисованный от руки, является результатом работы очень небольшой группы студентов из химического клуба нашей школы и одного художника из класса химии в нашей школе. На нем изображены два ученых, открывших радон, а именно Эрнест Резерфорд и его научный сотрудник Гарриет Брукс из Университета Макгилла. Универсальный символ излучения включен из-за природы этого элемента.
Актиний, 89
Средняя школа Эмили Карр
Вудбридж, Онтарио, Канада
Учитель: Адриана ДиПьетро
Художник: ECSS STEM Club
Актиний был открыт в 1899 году французским химиком Андре-Луи Дебьерном. Дебьерн выделил актиний из богатой ураном минеральной руды. В 1902 году немецкий химик Фридрих Оскар Гизель независимо открыл этот элемент. Поскольку Дебьерн первым открыл элемент, именно он назвал его имя.Актиний – это радиоактивное вещество, которое светится синим светом. Его можно использовать при лечении рака, но он также может вызывать повреждение ДНК. Актиний также можно использовать в качестве источника нейтронов.
Его можно использовать при лечении рака, но он также может вызывать повреждение ДНК. Актиний также можно использовать в качестве источника нейтронов.
Вернуться к началу.
1905-1914: лютеций
Лютеций, 71
Иствудский университетский институт
Китченер, Онтарио, Канада
Учитель: Панда Марш
Художник: Лейли Рохани
Лютеций – химический элемент с символом Lu и атомным номером 71.Это серебристо-белый металл, устойчивый к коррозии в сухом, но не влажном воздухе. Лютеций – последний элемент в ряду лантанидов, и он традиционно считается одним из редкоземельных металлов. Честь открытия лютеция досталась Жоржу Урбену в Сорбонне в Париже, поскольку он был первым, кто сообщил об этом. Другие химики, а именно Карл Ауэр в Германии и Чарльз Джеймс в США, приступив к выделению лютеция, собирались сделать то же открытие.
Вернуться к началу.
1915-1924: гафний, протактиний
Гафний, 72
Средняя школа штата Уранган
Торки, Квинсленд, Австралия
Учитель: Стефани Уайтхед
Художник: Талия Брукс
Я придумал дизайн элемента плитки гафния, узнав об истории элемента и его свойствах. Гафний был открыт в 1923 году Георгом фон Хевеши и Дирком Костером в Хафнии, ныне известной как Копенгаген. Город часто известен своими яркими домами, выстилающими каналы, как показано на моих работах.Также я раскрасил эти дома в цвета радуги, потому что, когда гафний окисляется, он образует поверхность цвета радуги.
Гафний был открыт в 1923 году Георгом фон Хевеши и Дирком Костером в Хафнии, ныне известной как Копенгаген. Город часто известен своими яркими домами, выстилающими каналы, как показано на моих работах.Также я раскрасил эти дома в цвета радуги, потому что, когда гафний окисляется, он образует поверхность цвета радуги.
Protactinium, 91
Старшая средняя школа Плано Вест
Плано, Техас, США
Учитель: Николь Лисси
Художник: Эмили Рен
Я использовал черную микронную и белую гелевую ручку на тонированной бумаге для создания своих работ. Протактиниум был впервые идентифицирован в 1913 году Казимиром Фаянсом и О. Геринг, пока они изучали цепочку распада урана. На картине изображен Казимир Фаянс, окруженный увеличенной диаграммой цепочки распада урана.Его руки окружают элемент Па, который является центром художественного произведения. На фоне изображения есть классная доска, на которой тонко написано «временная шкала элементов 2019» как дополнительный штрих к произведению искусства.
Вернуться к началу.
1925-1934: рений
Рений, 75
Strathcona-Tweedsmuir School
Окотокс, Альберта, Канада
Учитель: Дебра Карлсон
Художник: Джейк Бэверсток
Дизайн рениевых элементов был создан с использованием черно-белого негатива и позитивного графического дизайна, наложенного на карту долины Рейна 1690 года в Германии (картограф Де Витт).Финальная постановка рассматривает историю элемента, но изображает ее в современной стилизованной работе. Три перьевых ручки олицетворяют каждого из главных первооткрывателей этого элемента и первые образцы рения, использованные в наконечниках для ручек. Стилизованное «Ре» и компасная роза гармонично сочетаются с произведениями искусства и создают ощущение временного периода. Пунктирные линии отделяют карту от графического оформления.
Вернуться к началу.
Периодическая таблица Хронология Лист для учителя
Фото: Clipart. ком
комВведение
Цель этого урока – представить и сосредоточить внимание на ранней истории периодической таблицы Менделеева. Студенты должны использовать информацию из Краткой истории развития Периодической таблицы, чтобы заполнить график. На этом листе представлены ключевые даты, факты, цифры и события для временной шкалы. Ответы на оставшиеся вопросы можно найти в основной части урока.
Временная шкала периодической таблицы
Учащиеся должны заполнить пропуски, указав правильные даты, факты и цифры.
1649 – Hennig Brand обнаружил фосфор .
1829 – Иоганн Доберейнер открыл триаду галогенов и триаду щелочных металлов.
1862 – Первая таблица Менделеева была создана де Шанкуртуа . Он собрал стол к
.классификации химических элементов в порядке, основанном на их периодичности химической и
физические свойства .
1864 – Джон Ньюлендс опубликовал свою версию периодической таблицы Менделеева, а разработал Закон
октав.
1869 – Дмитрий Менделеев опубликовал свою периодическую таблицу, в конечном итоге став «отцом
». Таблица Менделеева».
1870 – Лотар Мейер опубликовал свою версию периодической таблицы Менделеева (после Менделеева) .
1895 – Лорд Рэлей открыл аргон , новый газообразный элемент, который был химически инертен.
1898 – Уильям Рэмси помог установить «нулевую» группу (для «нулевой валентности») и предсказал
будущее открытие элемента неон .
1911 – Эрнест Резерфорд установил, что «ядерный заряд на ядре был пропорционален
.
к атомному весу элемента ».
1911 – А. ван ден Брук установил, что атомный вес элемента равен приблизительно
равно заряду на атоме .Этот заряд стал «атомным номером», по которому
элементов таблицы Менделеева классифицируются как .
1913 – Генри Мозли открыл изотопов элементов . Это открытие установило, что
«свойства элементов периодически менялись в зависимости от атомного номера», а не атомного
вес , который ранее был принят в соответствии с периодическим законом.
1940 – Гленн Сиборг обнаружил плутония и трансурановых элементов от 94 до 102 .
Его открытия представляют собой последние (и самые последние) изменения в таблице Менделеева.
Иллюстрированная история Периодической таблицы (важные события: 100 достижений, изменивших историю). Пересмотренное и обновленное издание (100 значимых): Том Джексон: 9781627
В 1869 году Дмитрий Менделеев подарил миру Периодическую таблицу. Он содержал 63 элемента, что намного больше, чем четыре элемента – земля, вода, огонь и воздух – установленных в древнем мире, но менее половины от общего количества в нашей современной таблице. Менделеев считал, что впереди еще много элементов. Он был прав.
Этот важный справочник по Периодической таблице, содержащий более 300 иллюстраций, отслеживает историю мощного, но элегантного инструмента, который обнажает строительные блоки Вселенной. Путешествие начинается в момент формирования первых городов и следует за вкладом философов, алхимиков, промышленников и великих ученых, которые собирают силы для создания этого шедевра накопленных знаний. История включает Демокрита из Древней Греции, который сказал, что четыре элемента природы должны состоять из атомов; в остальном наш мир – всего лишь иллюзия, и французский аристократ Антуан Лавуазье первым показал, что вода вообще не стихия.
Путешествие начинается в момент формирования первых городов и следует за вкладом философов, алхимиков, промышленников и великих ученых, которые собирают силы для создания этого шедевра накопленных знаний. История включает Демокрита из Древней Греции, который сказал, что четыре элемента природы должны состоять из атомов; в остальном наш мир – всего лишь иллюзия, и французский аристократ Антуан Лавуазье первым показал, что вода вообще не стихия.
От древнегреческих философов до алхимика, который кипятил мочу до тех пор, пока она не засветилась в темноте, до британского изобретателя, описавшего мощное воздействие электричества на труп, Мэри Шелли (до того, как она написала Франкенштейна), до теолога, наблюдавшего за мышами. теряет сознание, когда болтается над пивом, открытие элементов – это история с множеством глав.Из мыслей и поступков великих мыслителей всегда складываются великие истории, и вот сотня самых значительных. Каждая история связана с запутанной головоломкой, которая стала открытием и изменила наш взгляд на мир. Мы называем их Значимыми.
Мы называем их Значимыми.
Древность | Углерод | К | 6 | Неизвестно | |
Античность | Медь | Cu | 29 | Халдеи (Ирак) (10 000 до н. | |
Античность | Сера | S | 16 | Греки | |
С.5000 г. до н.э. | Золото | Au | 79 | Египтяне | |
С. | Серебро | Ag | 47 | халдеи (Ирак), греки | |
С.2500 г. до н.э. | Утюг | Fe | 26 | Египтяне, хетты (Турция) | |
С. | Олово | Sn | 50 | Египтяне, инки | |
С.1600 г. до н.э. | Сурьма | Сб | 51 | Египтяне, халдеи | |
С. | Меркурий | Hg | 80 | Египтяне, китайцы, греки | |
С.1000 г. до н.э. | Свинец | Пб | 82 | Египтяне | |
С. | цинк | Zn | 30 | Римлянам | |
Парацельс (немецкий алхимик и врач) | Обозначается как металл в 1526 | ||||
До этого момента идентифицированные элементы либо встречались естественным образом, либо легко извлекались из руд путем плавки.Более тысячи лет в этот список не добавлялось никаких новых элементов. Хотя некоторые из оставшихся неоткрытых элементов были очень редкими, основная причина задержки с открытием этих новых элементов заключалась в том, что многие из них были гораздо более реактивными и обнаруживались только в химических соединениях, удерживаемых вместе с гораздо более прочными химическими связями между составляющими элементами соединения. Параллельный перерыв в развитии науки произошел в истории механики. Между тем, как Архимед объяснил Mechanical Advantage в 269 году до нашей эры, было очень мало теоретических успехов. и законы движения Ньютона в 1687 году. | |||||
С.1250 г. н.э. | Мышьяк | Как | 33 | Альбертус Магнус | Немецкий монах |
С. | Висмут | Би | 83 | Василий Валентин | Немецкий монах Описано в 1500 |
Клод Франсуа Жоффруа | Французский химик Идентифицировано в 1753 | ||||
1669 н.э. | Фосфор | п. | 15 | Henning Марка | Немецкий алхимик |
До 1700 | Платина | Pt | 78 | Индейцы Южной Америки | |
Антонио де Уллоа | Испанский исследователь и администратор Идентифицировано в 1741 | ||||
Чарльз Вуд | Британский химик Идентифицировано в 1741 | ||||
1735 | Кобальт | Co | 27 | Георг Брандт | Шведский химик и минералог |
1751 | Никель | Ni | 28 | Аксель Фредрик Кронштедт | Шведский химик и минералог |
1755 | Магний | мг | 12 | Joseph Черный | Шотландский физик и химик |
1766 | Водород | H | 1 | Генри Кавендиш | Английский аристократ |
1772 | Азот | N | 7 | Дэниел Резерфорд | Шотландский химик и врач |
1772/4 | Кислород | О | 8 | Карл Вильгельм Шееле | Шведский химик в Уппсальском университете |
Джозеф Пристли | Английский химик и философ | ||||
1774 | Хлор | Класс | 17 | Шееле | |
1774 | Марганец | млн | 25 | Иоганн Готтлиб Gahn | Шведский химик |
1780 | Хром | Cr | 24 | Луи-Николас Воклен | Французский фармацевт |
1781 | Молибден | Пн | 42 | Питер Хьельм | Шведский химик |
1783 | Теллур | Te | 52 | Франц Мюллер фон Райхенштайн | Венгерский минералог |
1783 | Вольфрам | Вт | 74 | Хуан и Фаусто Эльхуяр | Испанские химики и минералоги |
1787 | Стронций | Sr | 38 | Адэр Кроуфорд | Шотландский врач Открытие 1787 |
Томас Чарльз Хоуп | Идентифицировано 1791 в Эдинбурге | ||||
Дэви | Изолированный 1808 | ||||
1789 | Цирконий | Zr | 40 | Мартин Генрих Клапрот | Немецкий химик-минералог |
1789 | Уран | U | 92 | Клапрот | Обнаруженный оксид урана (Предполагается, что это элемент) |
Эжен Пелиго | Французский химик Изолированный элемент в 1841 г. | ||||
1791 | Титан | Ti | 22 | Уильям Грегор | Английский викарий |
Клапрот | Идентифицировано в 1795 | ||||
1794 | Иттрий | Y | 39 | Йохан Гадолин | Финский химик и минералог |
1797 | Бериллий | Be | 4 | Vauquelin | Французский минералог Обнаружено 1797 |
Фридрих Вёлер | Немецкий химик Изолированный 1828 г. в Берлине | ||||
Антуан-Александр-Брут Бюсси | Французский химик Изолированный 1828 г. в Париже | ||||
1801 | Ванадий | В | 23 | Андрес Мануэль дель Рио | Мексиканский ученый и натуралист испанского происхождения Мексиканский горный колледж Initilly с названием Panchromium Позже назван Erythronium |
Ипполит-Виктор Цанга-Дескотиль Барон Александр фон Гумбольдт | Французский химик, поддержанный прусским дворянином, в 1805 году оспорил требование дель Рио.Считается, что это Chromium . | ||||
Нильс Габриэль Сефстрём | Открыт заново в 1831 году и назван шведским химиком ванадием | ||||
1801 | Ниобий | Nb | 41 | Чарльз Хэтчетт | Английский химик |
1802 | Тантал | Ta | 73 | Андерс Густав Экеберг | Шведский химик |
1803 | Родий | Правый | 45 | Уильям Хайд Волластон | Английский химик и врач Кембридж |
1803 | Палладий | Pd | 46 | Волластон | |
1803 | Осмий | Ос | 76 | Смитсон Теннант | Английский химик Кембридж |
1803 | Индий | В | 77 | Теннант | |
1803 | Церий | CE | 58 | Йенс Якоб Берцелиус и Вильгельм Хизингер | Шведский химик и шведский геолог В Уппсальском университете |
1807 | Калий | К | 19 | Хамфри Дэви | Английский химик и физик |
1807 | Натрий | Na | 11 | Дэви | |
1808 | Бор | В | 5 | Луи-Жозеф Гей-Люссак и Луи-Жак Тенар | Французские химики |
Дэви | |||||
1808 | Кальций | Ca | 20 | Дэви | |
1808 | Рутений | Ру | 44 | Енджей Андрей Снядецкий | Польский химик Обнаружен в 1808 году в Вильно (не подтверждено) |
Карл Клаус | Русский химик Изолированный 1844 г. при Казанском государственном университете | ||||
1808 | Барий | Ba | 56 | Дэви | |
1811 | Йод | Я | 53 | Бернар Куртуа | Французский химик |
1815 | Торий | Чт | 90 | Берцелиус | |
1817 | Литий | Ли | 3 | Йохан Август Арфведсон | Шведский химик Упсала |
1817 | Селен | SE | 34 | Берцелиус | |
1817 | Кадмий | Кд | 48 | Фридрих Штромайер | Немецкий химик |
Карл Самуэль Леберехт Герман | Немецкий химик | ||||
1824 | Кремний | Si | 14 | Берцелиус | |
1825 | Алюминий | Al | 13 | Ганс Кристиан Эрстед | датский физик Копенгаген |
1825/6 | Бром | Br | 35 | Карл Лёвиг | Гейдельберг, Германия |
Антуан-Жером Балар | Монтпилиер, Франция | ||||
1839 | Лантан | La | 57 | Карл Мосандер | Шведский химик и минералог |
1842 | Эрбий | Er | 68 | Мосандер | |
1843 | Тербий | ТБ | 65 | Мосандер | |
1860 | Цезий | CS | 55 | Роберт Бунзен и Густав Кирхгоф | Немецкие химики и немецкий физик в Гейдельбергском университете |
1861 | Рубидий | руб. | 37 | Bunsen & Kirchhoff | |
1861 | Таллий | Тл | 81 | Уильям Крукс | Английский химик Лондон |
1863 | Индуим | В | 77 | Фердинанд Рейх и Иероним Рихтер | Немецкие химики |
1868 | Гелий | He | 2 | Пьер Жюль Сезар Янссен | Французский астроном |
Джозеф Норман Локьер | Английский астроном | ||||
1869 Периодическая таблица элементов предложена независимо Мейером и Менделеевым .(См. Современный пример Периодической таблицы ) | |||||
1871 | Галлий | Ga | 31 | Дмитрий Иванович Менделеев | Русский химик Прогноз 1871 |
Поль Эмиль Лекок де Буабодран | Французский химик Обнаружено 1875 г. | ||||
1871 | Скандий | SC | 21 | Менделеева | Прогноз 1871 |
Ларс Нильсон | Шведский химик Обнаружено 1879 | ||||
1871 | Германий | Ge | 32 | Менделеев | Прогноз 1871 |
Клеменс Винклер | Немецкий химик Обнаружено 1886 Фрайбургский университет | ||||
1871 | Протактиний | Па | 91 | Менделеев | Прогноз 1871 |
Казимир Фаянс и Отто Геринг | Карлсруэ, Германия 1913 | ||||
Отто Хан и Лиз Мейтнер | Институт Кайзера-Вильгема, Берлин 1918 | ||||
Фредерик Содди , Джон Крэнстон и Эндрю Флек | Глазго, Шотландия 1918 | ||||
1878 | Гольмий | Ho | 67 | Per Teodor Cleve | Шведский химик Упсала |
Марк Делафонтен и Жак-Луи Соре | Швейцарские химики Женева | ||||
1878 | Иттербий | Yb | 70 | Жан Шарль Галиссар де Мариньяк | Швейцарский химик Женева |
1879 | Самарий | см | 62 | de Boisbaudran | |
1879 | Тулий | ТМ | 69 | Клив | |
1880 | Гадолиний | Gd | 64 | де Мариньяк | |
1885 | Празеодим | Пр | 59 | Carl Auer Freiherr von Welsbach | Австрийский ученый и изобретатель |
1885 | Неодим | Nd | 60 | фон Вельсбах | |
1886 | Фтор | Ф. | 9 | Джозеф Анри Муассан | Французский химик Париж |
1886 | Диспрозий | Ду | 66 | de Boisbaudran | |
1894 | Аргон | Ар | 18 | Джон Уильям Стратт ( лорд Рэлей ) и Уильям Рамзи | Английский физик и шотландский химик Кембридж и Калифорнийский университет в Лондоне |
1895 | Гелий | He | 2 | Рамзи | Университетский колледж Лондона |
1898 | Криптон | Кр | 36 | Рамзи и Моррис Уильям Трэверс | Шотландские и английские химики Калифорнийский университет в Лондоне |
1898 | Неон | Ne | 10 | Ramsay & Travers | Калифорнийский университет в Лондоне |
1898 | Ксенон | Xe | 54 | Ramsay & Travers | Калифорнийский университет в Лондоне |
1898 | Полоний | Po | 84 | Мария Кюри | Польско-французский физик и химик Сорбонна, Париж |
1898 | Радий | Ra | 88 | Мари и Пьер Кюри | |
1899 | Актиний | Ac | 89 | Андре Дебьерн | Французский химик Париж |
1900 | Радон | Rn | 86 | Фридрих Эрнст Дорн | Немецкий физик Университет Галле |
1901 | Европий | ЕС | 63 | Эжен Анатоль Демарсе | Французский химик |
1907 | Лютеций | Лю | 71 | Georges Urbain | Французский химик Сорбонна, Париж |
Чарльз Джеймс | Английский химик Университет Нью-Гэмпшира, США | ||||
Карл Ауэр | Австрийский химик Германия | ||||
1923 | Гафний | Hf | 72 | Дирк Костер и Дьёрдь Хевеси | Датские и венгерские химики Копенгагенский университет |
1925 | Рений | Re | 75 | Уолтер Ноддак , Ида Тэке и Отто Карл Берг | Берлин, Германия |
1925 | Технеций (Мазур) | Тс | 43 | Noddack, Tacke & Berg | Берлин, Германия |
1938 | Прометий | мкм | 61 | H.B. Law , J. D. Pool , Kurbatov & L. L. Quill | (заявлено в 1938 г.) Государственный университет Огайо |
J.A. Маринский , Л.Е. Гленденин , Чарльз Д. Кориелл | (доказано в 1945 г.) Oak Ridge Labs, Теннесси | ||||
1939 | Франций | Пт | 87 | Маргарита Перей | Институт Кюри, Париж |
1940 | Астатин | по адресу | 85 | Дейл Р. Corson , K. R. Mackenzie & Emilio Segré (итальянский) | Калифорнийский университет |
Следующие элементы с атомным номером больше 92 (уран) известны как трансурановые элементы . Все они радиоактивны и, кроме нептуния и плутония, ни один из них не встречается на Земле в естественных условиях, а период полураспада намного короче ее возраста. | |||||
1940 | Нептуний | НП | 93 | Эдвин М. Макмиллан и Филип Х. Абельсон | Беркли, Калифорния |
1940 | Плутоний | Pu | 94 | Гленн Т. Сиборг , Артур К. Валь , Джозеф У. Кеннеди , Майкл Сефола и Макмиллан | Радиационная лаборатория Лоуренса (LRL), Калифорнийский университет, Беркли |
1944 | Кюрий | см | 96 | Сиборг, Ральф А. Джеймс и Альберт Гиорсо | LRL, Беркли |
1944 | Америций | Am | 95 | Сиборг, Леон О. Morgan et al. | Аргоннская национальная лаборатория, Чикаго |
1949 | Беркелиум | Bk | 97 | Гиорсо, Сиборг, Стэнли Г. Томпсон и Кеннет улица | LRL, Беркли |
1950 | Калифорний | Cf | 98 | Ghiorso, Seaborg et al. | LRL, Беркли |
1952 | Эйнштейний | Es | 99 | Ghiorso et al. | LRL, Беркли |
G. R. Choppin et al. | Национальная лаборатория Лос-Аамос | ||||
1952 | Фермий | FM | 100 | Гиорсо с большой командой | LRL, Беркли, совместно с Аргоннской национальной лабораторией и Лос-Аламосской национальной лабораторией |
Следующие элементы с атомными номерами больше 100 известны как Трансфермиевые элементы .У них очень короткий период полураспада, иногда всего доли секунды, и во многих случаях было создано всего несколько атомов. | |||||
1955 | Менделевий | Md | 101 | Ghiorso, Bernard Harvey et al. | LRL, Беркли |
1956 | Нобелий | № | 102 | Коллектив Объединенного института ядерных исследований (ОИЯИ) | ЮНИР, Дубна, СССР 1956 |
Гиорсо, Сиборг, Джон Р. Walton и Torbjørn Sikkeland | LRL, Беркли 1958 | ||||
1961 | Лоуренсий | Lr | 103 | Гиорсо, Алмон Ларш, Роберт М. Латимер и др. | LRL, Беркли |
1964 | Резерфордий | Rf | 104 | Дьёрдь Флеров и др. | ЮНИР, Дубна, СССР |
Ghiorso et al. | LRL, Беркли | ||||
1967 | Дубний | Дб | 105 | Flerov et al. | ЮНИР, Дубна, СССР, 1967 |
Ghiorso et al. | LRL, Беркли 1969 | ||||
1974 | Сиборгий | Sg | 106 | Флеров Юрий Органес и др. | ЮНИР, Дубна, СССР |
Ghiorso et al. | LRL, Беркли | ||||
1976 | Бориум | Bh | 107 | Organessian et al. | ЮНИР, Дубна, СССР 1976 |
Питер Армбрустер , Готфрид Мюнценберг et al. | GSI Labs, Дармштадт, Германия 1981 | ||||
1982 | Мейтнерий | млн тонн | 109 | Армбрустер, Мюнценберг и др. | GSI Labs, Дармштадт, Германия |
1984 | Калий | HS | 108 | Армбрустер, Мюнценберг и др. | GSI Labs, Дармштадт, Германия |
1994 | Дармштадтиум | DS | 110 | Армбрустер, Хорхе Ригол и др. | GSI Labs, Дармштадт, Германия |
1994 | Рентген | Rg | 111 | Armbruster et al. | Имя заполнителя GSI Labs, Дармштадт, Германия |
1996 | Коперникум | Cn | 112 | Армбрустер, Сигурд Хофманн и др. | GSI Labs, Дармштадт, Германия |
1998 | Флеровий | эт. | 114 | Органессиан Владимир Утёнков и др. | JNIR |
Кентон Муди и др. | Ливерморская национальная лаборатория им. Лоуренса (LLNL), Калифорния | ||||
2001 | Ливерморий | Уровень | 116 | Органессиан, Утёнков, Муди и др. | Совместные группы JNIR и LLNL |
2004 | Унунтриум | Уут | 113 | Organessian et al. | Имя заполнителя Совместные команды JNIR и LLNL |
2004 | Унунпентиум | Uup | 115 | Organessian et al. | Имя заполнителя Совместные команды JNIR и LLNL |
2006 | Унуноктиум | Uuo | 118 | Organessian et al. | Имя заполнителя Совместные группы JNIR и LLNL |
2010 | Ununseptium | Uus | 117 | Органессиан, Джим Роберто и др. | Имя заполнителя Объединенные бригады ОНРЛ, ЛЛНЛ, JNIR |
Унуннний | Ууэ | 119 | Роберт Смоланчук (Прогноз) | Имя заполнителя | |
История Периодической таблицы
7.1 История Периодической таблицы
Цель обучения
- Ознакомиться с историей периодической таблицы Менделеева.
Современная таблица Менделеева сформировалась в результате долгой истории попыток химиков расположить элементы в соответствии с их свойствами в качестве средства предсказания химического поведения. Одним из первых, кто предложил такое расположение, был немецкий химик Йоханнес Доберейнер (1780–1849), который заметил, что многие из известных элементов могут быть сгруппированы в триады – набор из трех элементов, которые имеют схожие свойства., наборы из трех элементов, которые имеют похожие свойства, например, хлор, бром и йод; или медь, серебро и золото. Доберейнер предложил сгруппировать все элементы в такие триады, но последующие попытки расширить его концепцию оказались безуспешными. Теперь мы знаем, что части таблицы Менделеева – в частности, блок d – содержат триады элементов с существенным сходством. Средние три члена большинства других столбцов, такие как сера, селен и теллур в группе 16 или алюминий, галлий и индий в группе 13, также имеют удивительно похожий химический состав.
К середине 19 века атомные массы многих элементов были определены. Английский химик Джон Ньюлендс (1838–1898), выдвинув гипотезу о том, что химический состав элементов может быть связан с их массами, расположил известные элементы в порядке увеличения атомной массы и обнаружил, что каждый седьмой элемент имеет аналогичные свойства (рис. 7.1. элементов в октавы по предложению Ньюлендса »). (Благородные газы все еще были неизвестны.) Поэтому Ньюлендс предположил, что элементы можно разделить на октавы – группу из семи элементов, соответствующих горизонтальным рядам в элементах основной группы (не считая благородных газов, которые в то время были неизвестны)., соответствующие горизонтальным строкам в элементах основной группы. К сожалению, «закон октав» Ньюлендса, похоже, не работал для элементов тяжелее кальция, и его идея публично высмеивалась. На одной из научных встреч Ньюлендса спросили, почему он не расположил элементы в алфавитном порядке, а не по атомной массе, поскольку это имело бы такой же смысл! Фактически, Ньюлендс был на правильном пути – за некоторыми исключениями, атомная масса действительно увеличивается с атомным номером, и аналогичные свойства возникают каждый раз, когда заполняется набор из нс 2 np 6 подоболочек.Несмотря на то, что в таблице Ньюлендса не было логического места для элементов блока d , в 1887 году Лондонское королевское общество наградило его идею за свою идею.
Джон Ньюлендс (1838–1898)
Ньюлендс заметил, что свойства элемента повторяются каждый седьмой (или кратный семи) элемент, как музыкальные ноты повторяются каждую восьмую ноту.
Рисунок 7.1 Расположение элементов в октавах, предложенное Newlands
Приведенная здесь таблица сопровождает письмо 27-летнего Ньюлендса редактору журнала Chemical News , в котором он написал: «Если элементы расположены в порядке их эквивалентов с небольшими перестановками, Как и в прилагаемой таблице, можно заметить, что элементы, принадлежащие к одной группе, обычно появляются на одной горизонтальной линии.Также будет видно, что количество аналогичных элементов обычно различается либо на 7, либо на несколько кратных семи; другими словами, члены одной и той же группы стоят по отношению друг к другу в таком же отношении, как концы одной или нескольких октав в музыке. Таким образом, в группе азота между азотом и фосфором находится 7 элементов; между фосфором и мышьяком – 14; между мышьяком и сурьмой – 14; и, наконец, между сурьмой и висмутом, 14 также. Я предлагаю условно обозначить это своеобразное отношение закон октав как .Я и т. Д. Джон А. Р. Ньюлендс, F.C.S. Лаборатория, 19, Грейт-Сент-Хеленс, штат Коннектикут, 8 августа 1865 года.
Периодическая таблица приобрела свою современную форму благодаря работам немецкого химика Юлиуса Лотара Мейера (1830–1895) и русского химика Дмитрия Менделеева (1834–1907), оба из которых сосредоточились на взаимосвязи между атомной массой и различными физическими и химическими веществами. характеристики. В 1869 году они независимо друг от друга предложили по существу идентичное расположение элементов. Мейер выровнял элементы в своей таблице в соответствии с периодическими изменениями простых атомных свойств, таких как «атомный объем» (рис. 7.2 «Изменение атомного объема с атомным номером, адаптированное из графика Мейера 1870 года»), который он получил делением атомной массы (молярной массы) в граммах на моль на плотность элемента в граммах на кубический сантиметр. Это свойство эквивалентно тому, что сегодня определяется как молярный объем – молярная масса элемента, деленная на его плотность. (измеряется в кубических сантиметрах на моль):
Уравнение 7.1
молярная масса (г / моль) плотность (г / см3) = молярный объем (см3 / моль)Как показано на Рисунке 7.2 «Изменение атомного объема с атомным номером, адаптировано из графика Мейера 1870 года», щелочные металлы имеют самые высокие молярные объемы твердых элементов. На графике Мейера зависимости атомного объема от атомной массы неметаллы находятся на восходящей части графика, а металлы – на пиках, во впадинах и на спусках.
Дмитрий Менделеев (1834–1907)
Когда стеклянный завод его семьи был разрушен пожаром, Менделеев переехал в Санкт-Петербург, Россия, изучать науку.Он заболел и не ожидал, что выздоровеет, но защитил докторскую диссертацию с помощью своих профессоров и сокурсников. Помимо таблицы Менделеева, еще одним вкладом Менделеева в науку стал выдающийся учебник Принципы химии , которым пользовались многие годы.
Рис. 7.2. Изменение атомного объема в зависимости от атомного номера, адаптировано из графика Мейера 1870 г.
Обратите внимание на периодическое увеличение и уменьшение атомного объема.Поскольку на момент составления этого графика благородные газы еще не были обнаружены, пики соответствуют щелочным металлам (группа 1).
Периодическая таблица Менделеева
Менделеев, который впервые опубликовал свою периодическую таблицу в 1869 году (рис. 7.3 «Периодическая таблица Менделеева, опубликованная в Немецком журнале»), обычно считается создателем современной периодической таблицы. Ключевое различие между его расположением элементов и расположением элементов Мейера и других состоит в том, что Менделеев не предполагал, что все элементы были обнаружены (на самом деле в то время было известно только около двух третей встречающихся в природе элементов).Вместо этого он намеренно оставил пробелы в своей таблице с атомными массами 44, 68, 72 и 100 в надежде, что элементы с такими атомными массами будут обнаружены. Эти заготовки соответствуют элементам, которые мы теперь знаем как скандий, галлий, германий и технеций.
Рисунок 7.3 Периодическая таблица Менделеева, опубликованная в немецком журнале Annalen der Chemie und Pharmacie в 1872 г.
Заголовки столбцов «Reihen» и «Gruppe» на немецком языке означают «строка» и «группа».Формулы указывают тип соединений, образованных каждой группой, где «R» означает «любой элемент», и используются верхние индексы там, где мы теперь используем нижние индексы. Атомные массы показаны после знаков равенства и увеличиваются в каждой строке слева направо.
Наиболее убедительным свидетельством в пользу расположения элементов Менделеева было открытие двух ранее неизвестных элементов, свойства которых полностью соответствовали его предсказаниям (Таблица 7.1 «Сравнение свойств, предсказанных Менделеевым в 1869 году для»).Два пустых места, которые Менделеев оставил в своей исходной таблице, находились под алюминием и кремнием в ожидании открытия двух еще неизвестных элементов, eka -алюминий и eka -силикон (от санскрита eka , что означает « один, как в слове «один за пределами алюминия»). Наблюдаемые свойства галлия и германия соответствовали свойствам алюминия eka и кремния eka настолько хорошо, что, как только они были открыты, периодическая таблица Менделеева быстро получила признание.
Таблица 7.1 Сравнение свойств, предсказанных Менделеевым в 1869 г. для eka -Aluminium и eka -Silicon со свойствами галлия (обнаруженного в 1875 г.) и германия (обнаруженного в 1886 г.)
| Имущество | eka -Алюминий (прогнозируемый) | Галлий (наблюдаемый) | eka -Кремний (прогноз) | Германий (наблюдается) |
|---|---|---|---|---|
| атомная масса | 68 | 69.723 | 72 | 72,64 |
| элемент | металл | металл | грязно-серый металл | серо-белый металл |
| низкий mp * | т.пл. = 29,8 ° C | высокая МП | т.пл. = 938 ° C | |
| d = 5.9 г / см 3 | d = 5,91 г / см 3 | d = 5,5 г / см 3 | d = 5,323 г / см 3 | |
| оксид | E 2 O 3 | Ga 2 O 3 | EO 2 | GeO 2 |
| d = 5.5 г / см 3 | d = 6,0 г / см 3 | d = 4,7 г / см 3 | d = 4,25 г / см 3 | |
| хлорид | ECl 3 | GaCl 3 | ECl 4 | GeCl 4 |
| летучие | т.пл. = 78 ° C т.кип. * = 201 ° C | т.кип. <100 ° C | точка кипения = 87 ° C | |
| * т.пл. = точка плавления; bp = точка кипения. | ||||
Когда химические свойства элемента показали, что ему могло быть отведено неправильное место в более ранних таблицах, Менделеев тщательно пересмотрел его атомную массу. Он обнаружил, например, что ранее сообщенные атомные массы бериллия, индия и урана были неверными. Первоначально сообщалось, что атомная масса индия составляет 75,6, исходя из предполагаемой стехиометрии InO для его оксида. Если бы эта атомная масса была правильной, то индий нужно было бы поместить в середину неметаллов, между мышьяком (атомная масса 75) и селеном (атомная масса 78).Тем не менее, поскольку элементарный индий представляет собой серебристо-белый металл , Менделеев предположил, что стехиометрия его оксида на самом деле была In 2 O 3 , а не InO. Это означало бы, что атомная масса индия на самом деле составляла 113, что помещало этот элемент между двумя другими металлами, кадмием и оловом.
Одна группа элементов, отсутствующая в таблице Менделеева, – это благородные газы. Все они были открыты более 20 лет спустя, между 1894 и 1898 годами, сэром Уильямом Рамзи (1852–1916; Нобелевская премия по химии 1904 года).Изначально Рамзи не знал, где разместить эти элементы в периодической таблице. Аргон, первый открытый, имел атомную массу 40. Это было больше, чем у хлора и сравнимо с массой калия, поэтому Рамзи, используя те же рассуждения, что и Менделеев, решил поместить благородные газы между галогенами и атомами калия. щелочные металлы.
Роль атомного номера в Периодической таблице
Несмотря на свою полезность, периодическая таблица Менделеева была полностью основана на эмпирических наблюдениях, подкрепленных очень слабым пониманием.Только в 1913 году молодой британский физик Х. Дж. Мозли (1887–1915), анализируя частоты рентгеновских лучей, испускаемых элементами, обнаружил, что в основе порядка элементов лежит атомный номер , а не атомная масса. Мозли предположил, что размещение каждого элемента в его серии соответствовало его атомному номеру Z , который представляет собой количество положительных зарядов (протонов) в его ядре. Например, аргон, хотя и имеет атомную массу больше, чем у калия (39.9 а.е.м. по сравнению с 39,1 а.е.м. соответственно), в периодической таблице калия находилось с до . Анализируя частоты испускаемых рентгеновских лучей, Мозли заметил, что атомный номер аргона равен 18, а калия – 19, что указывает на то, что они действительно были размещены правильно. Мозли также заметил три пробела в своей таблице частот рентгеновского излучения, поэтому он предсказал существование трех неизвестных элементов: технеция ( Z = 43), открытого в 1937 году; прометий ( Z = 61), открытый в 1945 г .; и рений ( Z = 75), открытый в 1925 году.
Х. Дж. Мозли (1887–1915)
Мозли оставил свою исследовательскую работу в Оксфордском университете, чтобы присоединиться к британской армии в качестве офицера связи во время Первой мировой войны. Он был убит во время битвы при Галлиполи в Турции.
Пример 1
До его открытия в 1999 году некоторые теоретики полагали, что в природе существует элемент с Z из 114. Используйте рассуждения Менделеева, чтобы назвать элемент 114 как eka -______; затем определите известный элемент, химический состав которого, по вашему мнению, будет наиболее близок к химическому составу элемента 114.
Дано: атомный номер
Запрошено: имя с префиксом eka –
Стратегия:
A Используя периодическую таблицу (см. Главу 32 «Приложение H: Периодическая таблица элементов»), найдите строку n = 7. Определите местонахождение неизвестного элемента с помощью Z = 114; затем определите известный элемент, который находится прямо над этим местом.
B Назовите неизвестный элемент, используя префикс eka – перед именем известного элемента.
Решение:
A Строку n = 7 можно заполнить, предположив наличие элементов с атомными номерами больше 112, которые находятся под ртутью (Hg). Если подсчитать три прямоугольника вправо, получим элемент 114, который находится непосредственно под свинцом (Pb). B Если бы Менделеев был жив сегодня, он бы назвал элемент 114 eka свинцом.
Упражнение
Используйте рассуждения Менделеева, чтобы назвать элемент 112 как eka -______; затем определите известный элемент, химический состав которого, по вашему мнению, будет наиболее близок к химическому составу элемента 112.
Ответ: эка -ртуть
Сводка
В периодической таблице элементы расположены в соответствии с их электронными конфигурациями, так что элементы в одном столбце имеют одинаковые валентные электронные конфигурации.Периодические изменения размера и химических свойств являются важными факторами, определяющими типы химических реакций, которым подвергаются элементы, и типы химических соединений, которые они образуют. Современная таблица Менделеева была основана на эмпирических корреляциях таких свойств, как атомная масса; Ранние модели, использующие ограниченные данные, отметили существование триад и октав элементов с аналогичными свойствами. Периодическая таблица приобрела свою нынешнюю форму благодаря работе Дмитрия Менделеева и Юлиуса Лотара Мейера, которые оба сосредоточили внимание на взаимосвязи между атомной массой и химическими свойствами.Мейер расположил элементы по их атомному объему, который сегодня эквивалентен молярному объему , определяемому как молярная масса, деленная на молярную плотность. Корреляция с электронной структурой атомов была сделана, когда Г. Дж. Мозли показал, что периодическое расположение элементов определяется атомным номером, а не атомной массой.
Ключевые вынос
- Элементы в таблице Менделеева расположены в соответствии с их свойствами, а таблица Менделеева служит помощником в прогнозировании химического поведения.
Концептуальные проблемы
Йоханнесу Доберейнеру приписывают разработку концепции химических триад. Какие из 15 элементов группы вы ожидаете составить триаду? Ожидаете ли вы, что B, Al и Ga будут действовать как триада? Обоснуйте свои ответы.
Несмотря на то, что Доберейнер, Ньюлендс, Мейер и Менделеев внесли свой вклад в разработку современной таблицы Менделеева, Менделеев приписывают ее происхождение.Почему периодическая таблица Менделеева была принята так быстро?
Как вклад Мозли в разработку таблицы Менделеева объяснил расположение благородных газов?
Схема именования eka , разработанная Менделеевым, использовалась для описания неоткрытых элементов.
- Используйте этот метод присвоения имен, чтобы предсказать атомный номер eka -ртути, eka -астатина, eka -таллия и eka -гафния.
- Используя префикс eka , идентифицируйте элементы с этими атомными номерами: 79, 40, 51, 117 и 121.
Числовая задача
На основании предоставленных данных заполнить таблицу.
Виды Молярная масса (г / моль) Плотность (г / см 3 ) Молярный объем (см 3 / моль) А 40.078 25.85 B 39,09 0,856 С 32,065 16,35 D 1.823 16,98 E 26,98 9,992 Ф 22,98 0,968 Постройте график зависимости молярного объема от молярной массы этих веществ.Согласно Мейеру, какие металлы, а какие – неметаллы?
Ответ
Виды Молярная масса (г / моль) Плотность (г / см 3 ) Молярный объем (см 3 / моль) А 40.078 1,550 25,85 B 39.09 0.856 45,67 С 32.065 1,961 16.35 D 30,95 1,823 16,98 E 26.98 2,700 9.992 Ф 22,98 0.968 23,7 Мейер обнаружил, что щелочные металлы имеют самые высокие молярные объемы, и что молярные объемы неуклонно уменьшаются с увеличением атомной массы, затем выравниваются и, наконец, снова возрастают. Элементы, расположенные на восходящей части графика зависимости молярного объема от молярной массы, обычно были неметаллами.Если мы посмотрим на график данных в таблице, мы можем сразу идентифицировать те элементы с наибольшими молярными объемами (A, B, F) как металлы, расположенные в левой части периодической таблицы. Элемент с наименьшим молярным объемом (E) – алюминий. График показывает, что последующие элементы (C, D) имеют молярные объемы, которые больше, чем у E, но меньше, чем у A и B. Таким образом, C и D, скорее всего, будут неметаллами (что имеет место: C = Сера, D = фосфор).
| Атомный Номер | Имя | Символ | Год открытия | Первооткрыватель | Производное от Наименование / символ |
|---|---|---|---|---|---|
| 1 | водород | H | 1766 | Генри Кавендиш | От греческого слова «гидро» – «вода» и гены «формирования», поскольку она сгорала на воздухе, образуя воду. |
| 2 | гелий | He | 1868 | Пьер-Жюль-Сезар Янссен | От греческого слова helios, означающего «солнце». Он был обнаружен методом спектроскопии во время солнечного затмения в хромосфере Солнца. |
| 3 | литий | Ли | 1818 | Йохан Август Арфведсон | От латинского lithos для «камня», потому что считалось, что литий существует только в минералах, поскольку он был впервые обнаружен в минерале петалит. |
| 4 | бериллий | Be | 1798 | Николас-Луи Воклен | От греческого слова berryllos, означающего «берилл», драгоценный камень, в котором он был впервые найден. |
| 5 | бор | B | 1808 (изолированный) | Хамфри Дэви | От арабского слова «бурак» – «белый».Впервые он был изолирован в нечистом состоянии Луи-Жозефом Гей-Люссаком и Луи-Жаком Тенаром, но именно Хамфри Дэви первым получил чистый бор с помощью электролиза. |
| 6 | углерод | С | – | известно с древних времен | От латинского “уголь” – “уголь”. В 1797 году Смитсон Теннант показал, что алмаз – это чистый углерод. |
| 7 | азот | N | 1772 | Дэниел Резерфорд | От латинского слова «нитрий» и греческого «нитрон» для «природной соды» и генов «формирования», поскольку он содержится в нитрате калия, селитре, селитре или природной соде. |
| 8 | кислород | O | 1774 | Джозеф Пристли | От греческого oxys для «кислоты» и генов для «образования», поскольку Антуан-Лоран Лавуазье первоначально думал, что кислород является продуцентом кислоты, потому что, когда он сжигал фосфор и серу и растворял их в воде, они производили кислоты. |
| 9 | фтор | F | 1886 (изолированный) | Фердинанд Фредерик, Анри Муассан | От латинского fluere для «потока или флюса», поскольку минеральный плавиковый шпат использовался в качестве флюса в металлургии из-за его низкой температуры плавления. |
| 10 | неон | Ne | 1898 | Сэр Уильям Рамзи, Моррис М.Траверс | От греческого neos для «новый». |
| 11 | натрий | Na | 1807 | Сэр Хамфри Дэви | От английского soda и латинского sodanum для «средства от головной боли». Химический символ происходит от латинского natrium для соды. |
| 12 | магний | мг | 1808 (отделение от минерала) | Сэр Хамфри Дэви | Из Магнезии, района в Фессалии на северо-востоке Греции. |
| 13 | алюминий | Al | 1825 (изолированный) | Ганс Кристиан Эрстед | От латинского alum и alumen, что означает «строгий», так как ранние римляне называли любое вещество со строгим вкусом квасцами. |
| 14 | кремний | Si | 1924 | Йонс Якоб Берцелиус | От латинского silx и silicis для «кремень».Первоначально считалось, что это металл и он назывался кремнием, но когда выяснилось, что это неверно, название было изменено на кремний. |
| 15 | фосфор | P | 1669 | Хенниг Бренд | От греческого слова «фосфор», что означает «приносить свет», поскольку белый фосфор самопроизвольно окисляется на воздухе и светится в темноте. |
| 16 | сера (сера) | S | – | известно с древних времен | От латинского сульфурия и санскритского сульвери.Сера была известна как камень Бренне, горючий камень, из которого получают полевой камень. |
| 17 | хлор | Класс | 1774 | Карл Вильгельм Шееле | От греческого слова «хлорос», означающего «бледно-зеленый», цвет элемента. |
| 18 | аргон | Ar | 1894 | Сэр Уильям Рамзи, лорд Роли | От греческого argos для «ленивый», потому что не сочетается с другими элементами. |
| 19 | калий | К | 1807 (изолированный) | Сэр Хамфри Дэви | От английского поташа, так как он был найден в каустическом калийном (KOH). Химический символ происходит от латинского kalium через арабское qali, означающее щелочь. |
| 20 | кальций | Ca | 1808 (изолированный) | Сэр Хамфри Дэви | От латинского calx, означающего «известь или известняк», в котором он встречается. |
| 21 | скандий | сбн | 1879 | Ларс Фредрик Нильсон | От латинского слова scandia, обозначающего Скандинавию, где был найден минерал. |
| 22 | титан | Ti | 1791 | Преподобный Уильям Грегор | От латинских титанов, мифологических первых сыновей земли. |
| 23 | ванадий | В | 1801/1830 | Андрес Мануэль дель Рио-и-Фернандес / Нильс Габриэль Сефстрем | От скандинавской богини любви и красоты Фрейи Ванадис из-за множества красивых цветных составов. |
| 24 | хром | Cr | 1797 | Луи-Николас Воклен | От греческого «цвет», означающего «цвет», так как существует много цветных соединений хрома. |
| 25 | марганец | Mn | 1774 (изолированный) | Йохан Готлиб Ган | От латинского magnes для «магнита», поскольку минерал пиролюзит (MnO 2 ) обладает магнитными свойствами. |
| 26 | утюг | Fe | – | известно с древних времен | От англосаксонского железа.Этот символ происходит от латинского ferrum, означающего «твердость». |
| 27 | кобальт | Co | 1739 | Георг Брандт | От немецкого кобольда, обозначающего «злых духов», которые, как считалось, доставляли проблемы шахтерам, поскольку минерал содержал элемент мышьяк, вредный для их здоровья. |
| 28 | никель | Ni | 1751 | Аксель Фредрик Кронштедт | От немецкого слова «никель», что означает «обманчивый дух», как горняки называли минерал никколит купферникель (ложная медь), поскольку он напоминал медную руду по внешнему виду, но в руде не было обнаружено меди. |
| 29 | медь | Cu | – | известно с древних времен | От латинского «cuprum», означающего «Кипр», где римляне впервые получили медь. |
| 30 | цинк | Zn | – | известно с древних времен | Из немецкого цинка. |
| 31 | галлий | Ga | 1875 | Поль-Эмиль Лекок де Буабодран | От латинского gallia для Франции или, возможно, от латинского gallus для «le coq or cock» в честь его первооткрывателя Фенча. Предсказано Менделеевым, назвавшим его эка-алюминием. |
| 32 | германий | Ge | 1886 | Клеменс Винклер | Из латинского germania для Германии в честь немецкого первооткрывателя.Предсказано Менделеевым, назвавшим его эка-кремнием. |
| 33 | мышьяк | как | – | известно с древних времен | От латинского arsenicum и греческого arsenikos для желтой мышьяковой руды звучит похоже на греческое arsenikon, означающее «мужской или мощный», возможно, из-за его токсичности. |
| 34 | селен | SE | 1817 | Йонс Якоб Берцелиус | От греческого Селена, богиня луны, потому что элемент найден в теллуре (названном в честь Теллуса, римской богини земли). |
| 35 | бром | Br | 1826 | Антуан-Жером Балар | От греческого слова bromos, означающего «зловоние». |
| 36 | криптон | Кр | 1898 | Сэр Уильям Рамзи, Моррис М. Траверс | От греческого kryptos означает «скрытый». |
| 37 | рубидий | руб. | 1861 | Роберт Бунзен, Густав Кирхгоф | От латинского rubidus, что означает самый глубокий красный из-за двух темно-красных линий в его спектре. |
| 38 | стронций | Sr | 1792 | Томас Чарльз Хоуп | Из Стронтиана, города в Шотландии, где найден минерал стронтианит. |
| 39 | иттрий | Y | 1794 | Йохан Гадолин | Из шведской деревни Иттерби, где был обнаружен минерал гадолинит (иттербит). |
| 40 | цирконий | Zr | 1789 | Мартин Генрих Клапрот | От арабского zargun означает «подобный золоту». |
| 41 | ниобий | Nb | 1801 | Чарльз Хэтчетт | От греческого Ниобы, дочери Тантала, поскольку элементы ниобий и тантал изначально считались идентичными элементами. |
| 42 | молибден | Пн | 1778 | Карл Велхельм Шееле | От греческого слова «молибдос», означающего «свинец», поскольку древние греки использовали этот термин для обозначения любого черного минерала, оставившего след. |
| 43 | технеций | Tc | 1937 (синтезировано) | Карло Перье, Эмилио Сегре | От греческого technetos для «искусственного». |
| 44 | рутений | Ру | 1844 (изолированный) | Карл Карлович Клаус | От латинского ruthenia, старого названия России. |
| 45 | родий | Rh | 1803 | Уильям Хайд Волластон | От греческого слова rhodon, означающего роза, из-за розовых растворов ее солей. |
| 46 | палладий | Pd | 1803 | Уильям Хайд Волластон | От второго по величине астероида Солнечной системы Паллуса, названного в честь богини мудрости и искусства Афины Паллады, поскольку элемент был обнаружен через год после открытия астероида. |
| 47 | серебро | Ag | – | известно с древних времен | От англосаксонских seofor и siolfur. Химический символ происходит от латинского argentum и санскритского argunas, означающего «яркий». |
| 48 | кадмий | Cd | 1817 | Фридрих Штромайер | От греческого слова kadmeia, что означает «каламин, карбонат цинка», поскольку он был обнаружен как примесь с карбонатом цинка в природе. |
| 49 | индий | В | 1863 | Фердинанд Райх, Иероним Теодор Рихтер | Цвет индиго для индиго-синей линии в спектре элемента. |
| 50 | банка | Sn | – | известно с древних времен | Из англосаксонской олова.Химический символ происходит от латинского олова, обозначающего сплавы, содержащие свинец. |
| 51 | сурьма | Сб | – | известно с древних времен | От греческого «анти» и «монос», что означает «не один», потому что он был найден во многих соединениях. Символ Sb происходит от первоначального названия stibium. |
| 52 | теллур | Te | 1782 | Франц Йозеф Мюллер фон Райхенштейн | От латинского Tellus, римской богини земли. |
| 53 | йод | I | 1811 | Барнард Куртуа | От греческого ioeides для «фиолетового цвета» из-за его паров фиолетового цвета. |
| 54 | ксенон | Xe | 1898 | Сэр Уильям Рамзи, Моррис М.Траверс | От греческого «ксенон», что означает «незнакомец». |
| 55 | цезий (цезий) | CS | 1860 | Роберт Вильгельм Бунзен, Густав Роберт Кирхгоф | От латинского caesius для «небесно-голубого цвета», который был цветом линии цезия на спектроскопе. |
| 56 | барий | Ba | 1808 (изолированный) | Сэр Хамфри Дэви | От греческого слова barys для «тяжелый», так как он был найден в минеральном тяжелом шпате. |
| 57 | лантан | Ла | 1839 | Карл Густав Мосандер | От греческого lanthanein – «ускользать от внимания», потому что он прятался в цериевой руде, и его было трудно отделить. |
| 58 | церий | CE | 1803 | Йонс Якоб Берцелиус, Вильгельм фон Хизингер, Мартин Генрих Клапрот | С планетоида Церера, названного в честь римской богини земледелия. |
| 59 | празеодим | Pr | 1885 | Карл Ф. Ауэр фон Вельсбах | От греческого prasios для «зеленого» и Didymos для «близнеца» из-за образующихся бледно-зеленых солей. Карл Ф. Ауэр фон Вельсбах выделил празеодим и неодим из пробы дидима. |
| 60 | неодим | Nd | 1885 (изолирован от минерала) | Карл Ф.Ауэр фон Вельсбах | От греческого слова neos для «нового» и «didymos» для близнеца после того, как Карл Ауэр фон Вельсбах разделил дидимий на новые элементы, один из которых он назвал неодимом. |
| 61 | прометий | Pm | 1944 (синтезировано) | Джейкоб А. Марински, Лоуренс Э. Гленденин, Чарльз Д. Кориелл | От Прометея, который украл огонь с небес и передал его человечеству, поскольку он был найден путем использования ядерной энергии, что также представляет угрозу. |
| 62 | самарий | см | 1878 | Марк Делафонтэн | Из минерала самарскит, в котором он был найден и который был назван в честь полковника фон Самарского, русского горного чиновника. |
| 63 | европий | Eu | 1896 (отделение от минерала) | Эжен-Антоль Демаркай | С континента Европа.Демаркай изолировал европий в 1901 году. |
| 64 | гадолиний | Gd | 1880 | Жан Шарль Галиссар де Мариньяк | Из минерала гадолинита, в котором он найден и который был назван в честь Йохана Гадолина. |
| 65 | тербий | Tb | 1843 | Карл Густав Мосандер | Из деревни Иттерби в Швеции, где впервые был обнаружен минерал иттербит. |
| 66 | диспрозий | Dy | 1886 | Поль-Эмиль Лекок де Буабодран | От греческого dysprositos – «трудно добраться», потому что диспрозий трудно отделить от минерала гольмия, в котором он содержится. |
| 67 | гольмий | Ho | 1879 | Per Theodor Cleve | От латинского holmia, обозначающего Стокгольм, или, возможно, от имени Холмберга, который первым выделил его. |
| 68 | эрбий | Er | 1843 | Карл Густав Мосандер | Из шведского города Иттерби, где впервые была добыта руда гадолинита. |
| 69 | тулий | ТМ | 1879 | Per Theodor Cleve | От Thule, самого раннего названия Скандинавии. |
| 70 | иттербий | Yb | 1878 | Жан Шарль Галиссар де Мариньяк | Из шведской деревни Иттерби, где был найден минерал иттербит. |
| 71 | лютеций | Лю | 1907 | Жорж Урбен | От латинского lutetia – латинское название города Париж. |
| 72 | гафний | Hf | 1923 | Дирк Костер, Шарль де Хевеши | От латинского слова hafnia, обозначающего Копенгаген, где он был впервые обнаружен. |
| 73 | тантал | Ta | 1802 | Андерс Густав Экеберг | Из греческого слова tantalos, мифологический персонаж, изгнанный в Аид, не мог есть или пить, потому что элемент был нерастворим в кислотах. |
| 74 | вольфрам | Вт | 1783 (изолированный) | Дон Хуан Хосе и Дон Фаусто д’Эльхуяр | От шведского слова tungsten, означающего «тяжелый камень». Химический символ происходит от немецкого вольфрама, который был обнаружен с оловом и мешал плавлению олова. Говорят, что он поедает олово, как волк поедает овцу. |
| 75 | рений | Re | 1925 | Ида Таке-Ноддак, Уолтер Ноддак, Отто Карл Берг | От латинского rhenus, обозначающего Рейнский Раллей в Германии. |
| 76 | осмий | Ос | 1803 | Смитсон Теннант | От греческого «запах» из-за резкого запаха летучей окиси. |
| 77 | иридий | Ir | 1803 | Смитсон Теннант | От латинского Ирис, греческой богини радуги, из-за разнообразия цветов соляных растворов элемента. |
| 78 | платина | Pt | 1735 | Антонио де Уллоа | От испанской платины для «серебра». |
| 79 | золото | Au | – | известно с древних времен | От санскритского jval «сиять».Символ Au происходит от латинского aurum, обозначающего Аврору, римскую богиню рассвета. |
| 80 | ртуть | Hg | – | известно с древних времен | От римского бога Меркурия, посланника богов. Символ происходит от греческого «гидрагириум», что означает «жидкое серебро» или «быстрое серебро». |
| 81 | таллий | Тл | 1861 | Сэр Уильям Крукс | От греческого thallos для «зеленого побега» из-за ярко-зеленых линий в его спектре. |
| 82 | свинец | Пб | – | известно с древних времен | От англосаксонского лидера. Символ происходит от латинского plumbum, означающего «свинец». |
| 83 | висмут | Би | 1753 | Клод-Франсуа Жоффруа Младший | От немецкого weisse masse для «белой массы», цвета ее оксидов. |
| 84 | полоний | Po | 1898 | Пьер и Мария Кюри | Из Польши, родины Марии Склодовской Кюри. |
| 85 | астатин | по адресу | 1940 (синтезировано) | Дейл Р. Карсон, К.Р. Маккензи, Эмилио Сегре, | От греческого astatos для «нестабильного», поскольку это нестабильный элемент. |
| 86 | радон | Rn | 1900 | Фридрих Эрнст Дорн | Первоначально назывался излучением радия, Em, потому что он был продуктом распада радия. Название радон отражает его происхождение от радия. |
| 87 | франций | Fr | 1939 | Маргарита Кэтрин Перей | Из Франции, страны, в которой он был впервые обнаружен. |
| 88 | радий | Ra | 1898 | Мария Склодовская Кюри, Пьер Кюри | От латинского радиуса, означающего «луч или луч», из-за его способности испускать лучи. |
| 89 | актиний | Ac | 1899 | Андре-Луи Дебьерн | От греческого слова «актис» или «акинис», что означает «луч или луч», потому что это хороший источник альфа-излучения. |
| 90 | торий | Чт | 1828 | Йонс Якоб Берцелиус | От Тора, скандинавского бога грома. |
| 91 | протактиний | Па | 1913 | Kasimir Fajans, O.H. Геринг | Фаянс назвал элемент «бревиум», потому что он обнаружил только короткоживущие атомы. |
| 1917 | Lise Meitner и Otto Hahn | Мейтнер и Хан обнаружили, что большинство атомов «бревиума» имеют долгую жизнь, поэтому они переименовали его в протактиний, от греческого protos, означающего «первый» и актиний, поскольку было обнаружено, что он является родоначальником актиния. | |||
| 92 | уран | U | 1789 | Мартин Генрих Клапрот | На планете Уран, названной в честь римского «Небесного Отца», Уран был открыт в 1781 году. |
| 93 | нептуний | Np | 1940 (синтезировано) | Эдвин М. Макмиллан, Филип Х. Абельсон | От Нептуна, римского бога моря, поскольку это следующая самая удаленная планета в Солнечной системе после Урана, и этот элемент является следующим после Урана в Периодической таблице элементов. |
| 94 | плутоний | Pu | 1941 (синтезировано) | Гленн Т.Сиборг, Джозеф В. Кеннеди, Эдвард М. Макмиллан, Артур К. Уол | С планеты Плутон, римского бога подземного мира, поскольку Плутон является следующей планетой в Солнечной системе после Нептуна, а элемент плутоний – следующий элемент после нептуния в Периодической таблице элементов. |
| 95 | америций | Am | 1944 (синтезировано) | Гленн Т.Сиборг, Ральф А. Джеймс, Леон О. Морган, Альберт Гиорсо | По аналогии с европием, шестым элементом в ряду лантаноидов (лантаноидов), поскольку америций является шестым элементом в ряду актиноидов (актинидов). |
| 96 | кюрий | см | 1944 (синтезировано) | Гленн Т. Сиборг, Ральф А. Джеймс, Альберт Гиорсо | Из книги «Пьер и Мария Кюри», открывших элементы радий и полоний. |
| 97 | берклий | Bk | 1949 (синтезировано) | Гленн Т. Сиборг, Стэнли Г. Томпсон, Альберт Гиорсо | Из Беркли, Калифорния, где он был впервые синтезирован. |
| 98 | калифорний | Cf | 1950 (синтезировано) | Стэнли Г.Томпсон, Гленн Т. Сиборг, Кеннет-стрит, младший, Альберт Гиорсо | Из штата и университета Калифорнии, где этот элемент был впервые синтезирован. |
| 99 | эйнштейний | Es | 1952 (синтезировано) | Альберт Гиорсо | Из «Альберта Эйнштейна». Эйстейний-252 впервые обнаружен в обломках термоядерного оружия. |
| 100 | фермий | Fm | 1952 (синтезировано) | Альберт Гиорсо | От Энрико Ферми, физика, построившего первый ядерный реактор. Впервые обнаружен в обломках взрыва термоядерного оружия. |
| 101 | менделевий | Md | 1955 (синтезировано) | Стэнли Г.Томпсон, Гленн Т. Сиборг, Барнард Г. Харви, Грегори Р. Чоппин, Альберт Гиорсо | От Дмитрия Менделеева, разработавшего Периодическую таблицу элементов. Первоначальный химический символ был My, но был изменен в 1955 году. |
| 102 | нобелий | № | 1958 (синтезировано) | Альберт Гиорсо, Гленн Т. Сиборг, Торбьорн Сиккеланд, Джон Р. Уолтон | От Альфреда Нобеля, первооткрывателя динамита и основателя Нобелевской премии. |
| 103 | лоуренсий | Lr | 1961 (синтезировано) | Альберт Гиорсо, Торбьорн Сиккеланд, Алмон Э. Ларш, Роберт М. Латимер | От Эрнеста О. Лоуренса, создавшего циклотрон. Первоначальный символ был Lw, но был изменен на Lr. |
| 104 | резерфордий | РЭ | 1964/1969 (синтезировано) | Российские ученые в Дубне / Альберт Гиорсо | От Эрнеста Резерфорда, разработавшего теорию радиоактивных превращений. |
| 105 | дубний | Db | 1967/1970 (синтезировано) | Российские ученые в Дубне / Лаборатория Лоуренса Беркли | Из местонахождения Российского научного центра в Дубне. |
| 106 | сиборгий | Sg | 1974 (синтезировано) | Альберт Гиорсо | От Гленна Теодора Сиборга, возглавлявшего команду, впервые синтезировавшую ряд трансурановых элементов. |
| 107 | бориум | Bh | 1981 (синтезировано) | Центр исследований тяжелых ионов, Германия | От Нилса Бора, который разработал теорию электронного строения атома. |
| 108 | хассий | HS | 1984 (синтезировано) | Питер Армбрустер, Готфрид Мюнценбер | От латинского hassia, обозначающего немецкую землю Гессен, бывшей столицей которой был Дармштадт, где этот элемент был впервые синтезирован. |
| 109 | мейтнерий | Mt | 1980 (синтезировано) | Питер Армбрустер, Готфрид Мюнценбер | От Лизы Мейтнер, открывшей протактиний. |
| 110 | дармштадтий | DS | 1994 (синтезировано) | Питер Армбрустер, Готфрид Мюнценбер | Из Дармштадта, региона, где расположен исследовательский центр. |
| 111 | рентген | Rg | 1994 (синтезировано) | многонациональная группа ученых в Центре исследований тяжелых ионов, Дармштадт, Германия | От Рентгена, первооткрывателя рентгеновских лучей. |
| 112 | коперниций | Cn | 1996 (синтезировано) | многонациональная группа ученых в Центре исследований тяжелых ионов, Дармштадт, Германия | Название, предложенное в 2009 году, Международном году астрономии, в честь Николая Коперника, который постулировал, что Земля вращается вокруг Солнца. |
| 113 | нихоний | Nh | 2004 | Японские ученые RIKEN (приоритет открытия над ОИЯИ) | Назван в честь японского японского слова «Нихон». |
| 114 | флеровий | эт. | 1998 (синтезировано) | многонациональный коллектив ученых Объединенного института ядерных исследований, Дубна, Россия | Названа в честь Лаборатории Флерова, которая носит имя русского физика Георгия Флёрова. |
| 115 | московский | Mc | 2003 (синтезировано) | Объединенный институт ядерных исследований (ОИЯИ), Дубна, Россия | Назван в честь Московской области, где расположен ОИЯИ. |
| 116 | ливерморий | Уровень | 2000 (синтезировано) | многонациональный коллектив ученых Объединенного института ядерных исследований, Дубна, Россия | Назван в честь Ливерморской национальной лаборатории Лоуренса в Ливерморе, США. |

 э.)
э.) 5000 г. до н.э.
5000 г. до н.э. 2100 г. до н.э.
2100 г. до н.э. 1500 г. до н.э.
1500 г. до н.э. 0 BC / AD
0 BC / AD . Выделение этих новых элементов зависело от знаний о более сложных процессах химического разложения или механического разделения, которые были разработаны только в более поздние годы.Открытие ускорилось в девятнадцатом веке с появлением электрических методов.
. Выделение этих новых элементов зависело от знаний о более сложных процессах химического разложения или механического разделения, которые были разработаны только в более поздние годы.Открытие ускорилось в девятнадцатом веке с появлением электрических методов. 1500 г. н.э.
1500 г. н.э.