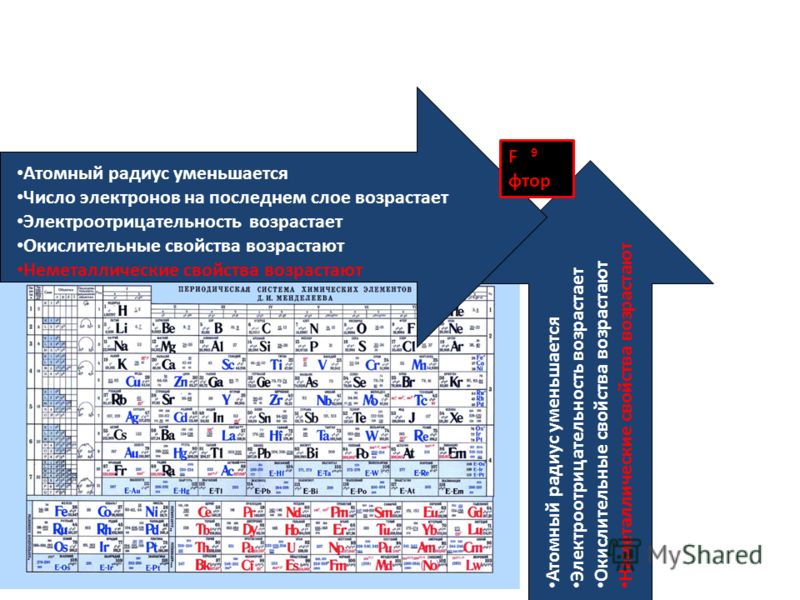
Периодическая таблица: как использовать, элементы, группы и многое другое!
В звонке периодическая таблица мы можем видеть химические элементы, которые упорядочены по их атомным номерам, а также по их электронной конфигурации, не забывая об их химических свойствах. Все это означает, что перед нами устройство в виде таблицы.
Вот почему мы можем определить периодическую таблицу как своего рода схема, позволяющая лучше понять каждый из элементов, при изучении химии. Но сегодня вам предстоит открыть для себя гораздо больше.
Индекс
- 1 Что такое таблица Менделеева и для чего она нужна?
- 2 Разработка атомных элементов, свойств и весов
- 3 Структура таблицы Менделеева и ее элементов
- 3.1 Группы или семьи
- 3.2 Периоды
- 3.3 Блочное деление
- 4 В чем важность таблицы элементов?
- 5 Как пользоваться периодической таблицей
- 6 Новые химические элементы в таблице
Наверняка вы уже знали, что это схема, в которой появляются химические элементы. Но они не случайно, но их размещение и данные, которые дает нам указанная таблица, имеют определенную цель. Эта цель будет заключаться в том, чтобы узнать как сходства, так и все, что отличает каждый из основных элементов. Все это для практического применения.
Но они не случайно, но их размещение и данные, которые дает нам указанная таблица, имеют определенную цель. Эта цель будет заключаться в том, чтобы узнать как сходства, так и все, что отличает каждый из основных элементов. Все это для практического применения.
Элементы распределяются как слева направо, так и сверху вниз, но всегда в порядке возрастания их атомные номера, то есть количество протонов. Горизонтальные ряды периодической таблицы элементов называются периодами, а 18 вертикальных столбцов – группами или семействами.
Разработка атомных элементов, свойств и весовНадо сказать, что некоторые элементы были хорошо известны еще в древности. Основными из них были золото, серебро, а также медь или ртуть. Но на самом деле первое открытие химического элемента произошло в XNUMX веке. Именно благодаря Хеннингу Брэнду он открыл фосфор. Уже в XNUMX веке стали известны другие, такие как водород или кислород. Это было так Антуан Лавуазье составил список из 33 пунктов. , который сгруппировал их в газы, металлы, неметаллы и землю. В начале XIX века новую идею разработал Джон Далтон. Это была формулировка химического атомизма, таким образом создавая систему относительные атомные массы. Хотя Дальтон предпочитал называть их атомными весами. Позже его идеи также были изменены, поскольку в них были неточности.
, который сгруппировал их в газы, металлы, неметаллы и землю. В начале XIX века новую идею разработал Джон Далтон. Это была формулировка химического атомизма, таким образом создавая систему относительные атомные массы. Хотя Дальтон предпочитал называть их атомными весами. Позже его идеи также были изменены, поскольку в них были неточности.
После всех исследований и достижений у нас в общей сложности 118 элементов. Мы найдем их разделенными на так называемые группы или семьи и периоды. Вы хотите знать, что символизирует каждый из них?
Группы или семьи
Это вертикальные столбцы, которые мы видим в таблице. В таблице, которую мы все знаем сегодня, их всего 18, и, как мы видим, они пронумерованы должным образом. Элементы в каждой группе имеют очень похожие физические и химические свойства.
- Grupo 1: В нем мы встретим щелочных металлов.
 Он состоит из элементов: лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs), франция (Fr).
Он состоит из элементов: лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs), франция (Fr). - Grupo 2: В этой второй группе мы увидим щелочноземельные металлы. Они тверже предыдущих и хорошо проводят электричество. Здесь мы найдем бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (ra).
- Grupo 3: Семья Эскандио. Среди них скандий (Sc) и иттрий (Y). Хотя они несколько противоречивы, мы должны также упомянуть лантан (La) и актиний (Ac).
- Grupo 4: Это семейство титана. В нем мы находим титан (ti), цирконий (Zr), гафний (Hf) и резерфорд (Rf).
- Grupo 5: Внутри семья ванадия, мы собираемся найти ванадий (V), ниобий (Nb), тантал (Ta), дубний (Db).
- Grupo 6: В этой группе мы находим хромовая семья. Там мы увидим хром (Cr), молибден (Mo), вольфрам (W), сиборгий (Sg).
- Grupo 7: марганец (Mn), технеций (Tc) и рений (Re), все они принадлежат к семейству марганцевых.

- Grupo 8: железная семья Он состоит из железа (Fe), рутения (Ru), осмия (Os), калия (Hs).
- Grupo 9: Здесь мы находим кобальт (Co), родий (Rh), иридий (Ir), мейтнерий (Mt).
- Grupo 10: Семейство никеля состоит из никеля (Ni), палладия (Pd), платины (Pt), дармштадция (Ds).
- Grupo 11: Медь (Cu), серебро (Ag) и золото (Au) известны как чеканка металлов, хотя не все принимают этот термин.
- Grupo 12: Цинк (Zn), кадмий (Cd) и ртуть (Hg).
- Grupo 13: Так называемая группа 13 также соответствует группе бора. Название происходит от земли, потому что именно там их больше всего. Мы находим бор (B), алюминий (Al), галлий (Ga), индий (In), таллий (Ti) и нихоний (nh).
- Grupo 14: В углерод или карбонидная группа, мы находим углерод (C), кремний (Si), германий (Ge), олово (Sn), свинец (Pb), флеровий (FI).
- Grupo 15: В этом случае мы приходим к группа азота. Конечно, мы начинаем с азота (N), фосфора (P), мышьяка (As), сурьмы (Sb), висмута (Bi) и мускусной кислоты (Mc).
- Grupo 16: Он известен как группа амфигенов, хотя они не могут скрыть свой статус кислородной семьи. Итак, мы находим кислород (O), серу (S), селен (Se), теллур (Te), полоний (Po), ливерморио (Lv).
- Grupo 17: галогены находятся в этой группе. Фтор (F), хлор (CI), бром (Br), йод (I), астат (At), тенезе (Ts).
- Grupo 18: Звонки благородные газы Это еще одна группа элементов, имеющих очень похожие свойства. В нормальных условиях это газы без цвета и запаха. Это гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe), радон (Rn) и органезон (Og).
Чтобы понять эту организацию, вы должны знать, что каждый из членов группы имеет очень похожие характеристики как их электронная конфигурация и та же валентность, то есть количество электронов, которые они имеют в последней оболочке. Конечно, если мы посмотрим сверху вниз и на одну и ту же группу, мы увидим, как увеличиваются атомные радиусы каждого из составляющих ее элементов.
Конечно, если мы посмотрим сверху вниз и на одну и ту же группу, мы увидим, как увеличиваются атомные радиусы каждого из составляющих ее элементов.
Периоды
Если теперь сосредоточиться на горизонтальные ряды, которые составляют периодическую таблицу, тогда это заставляет нас говорить о периодах. В зависимости от того, к какому периоду принадлежит каждый элемент, он будет указывать количество энергетических уровней атома. Они организованы по уровням и подуровням, но всегда элементы будут организованы в соответствии с их атомными номерами.
- Период 1: В период один у нас есть только два химических элемента. Водород и гелий.
- Период 2: В этом случае атомный номер немного увеличивается, и мы обнаруживаем в общей сложности восемь элементов, среди которых, среди прочих, литий, бор, углерод или азот, как мы видим на изображении.
- Период 3: В этот период находятся натрий, магний, алюминий, кремний, фосфор или сера.
- Период 4: Четвертая строка таблицы Менделеева уже содержит больше элементов. Всего в нем разместится 18 человек. Мы можем упомянуть как калий и кальций, так и железо и цинк.
- Период 5Что ж, как мы уже знаем, это соответствует пятой строке таблицы элементов. Их также всего 18. Здесь мы найдем стронций или палладий.
- Период 6: Еще 18 элементов находятся в так называемом шестом ряду или периоде 6. Некоторые из них – цезий, вольфрам или ртуть.
- Период 7: Наиболее радиоактивные и нестабильные элементы обнаружены в этот период 7. Актиниды также включены.
Блочное деление
Для выполнения разбивки таблицы элементов блока учитывается орбиталь, на которой находится последний электрон.
- Блок s: Блок s соответствует первым двум группам, то есть щелочным и щелочноземельным группам, не забывая при этом гелий и водород.
- Блок p: Соответствует шести последним группам.
 Содержит все металлоиды.
Содержит все металлоиды. - Блок d: Группы с 3 по 12 будут в этом блоке. Можно сказать, что в нем есть переходные металлы.
- Блок f: Он состоит из лантаноидов и актинидов.
Как мы видели, таблица показывает нам и представляет элементы в простой форме. С одной стороны, мы обнаруживаем, что элементы, собственно говоря, представлены символом. В самой распространенной таблице мы можем видеть, как ее сопровождают всего две цифры. Один из них будет относиться к его массовому числу, то есть сумма протонов и нейтронов. С другой стороны, атомный номер (количество протонов), обычно ставится в нижнем индексе слева от элемента. При всем этом таблица – идеальный инструмент для нашего обучения.
Как пользоваться периодической таблицей
Для многих таблица Менделеева – это больше, чем иероглиф. Вот почему все его деления, числа и даже цвета имеют значение. Вы должны знать, что говорит вам каждый из этих разделов:
Вы должны знать, что говорит вам каждый из этих разделов:
- Символы: Символ представление элемента. Он состоит из прописных букв и иногда сопровождается другими строчными буквами, в зависимости от регистра.
- Классификация: Как мы видели ранее, классификация или группы, в которых появляется каждый из элементов, также важны.
- Атомная масса: Это масса атома, выраженная в единицах (а.е.м.).
- Количество протонов: Число протонов любого атома совпадает с его атомным номером.
- Количество нейтронов: Равно атомная масса минус количество протонов.
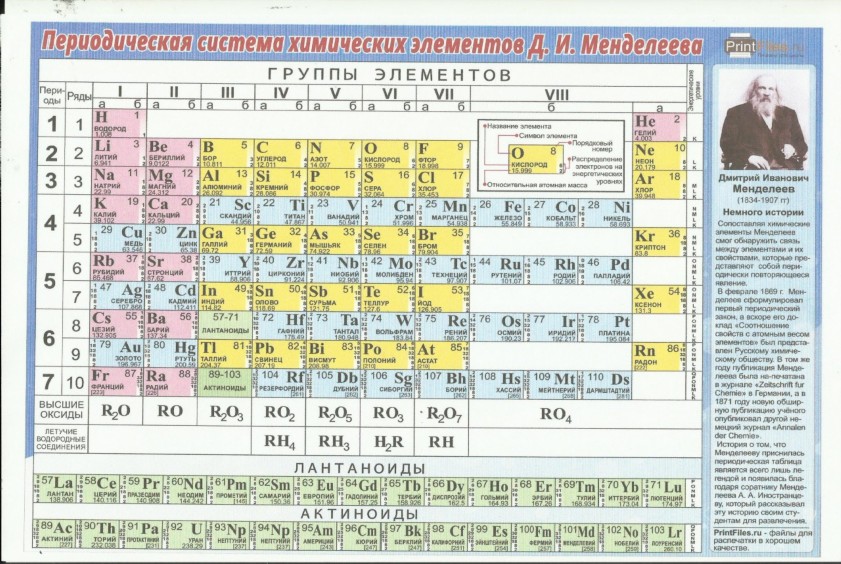
- Цвет элементов: Указывает на отражение света, когда мы говорим о нормальных условиях.
- Атомный объем: Определяется как объем, занимаемый моль атомов элемента.
Кажется, что когда мы выучили обычную таблицу Менделеева, появляются какие-то новые элементы. В частности, они расположены в седьмом ряду, и вам необходимо знать их четыре. Они названы в честь: Московио, Тенесо, Нихониум и Оганесон. Надо сказать, что элемент Nihonium был открыт некоторыми японскими учеными, а остальные разделены между Россией и США.
Периодическая таблица менделеева свойства элементов.
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.
При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.
Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
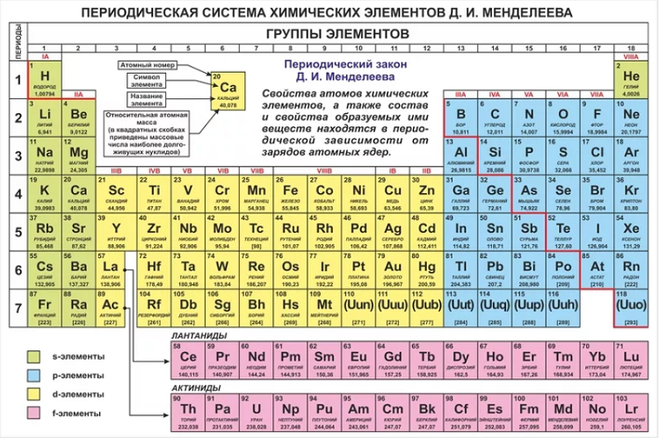
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
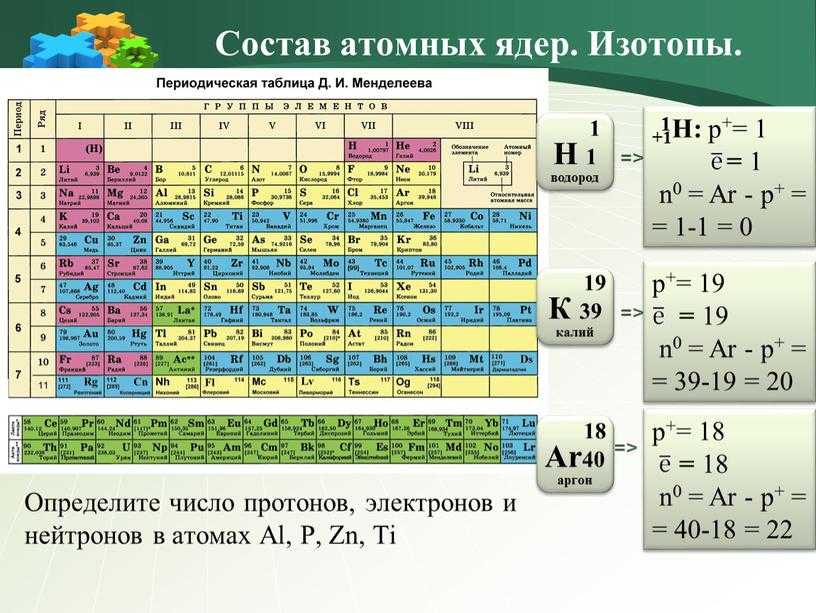
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.
Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс “Таблица Менделеева для чайников”. В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о , который с радостью поделится с вами своими знаниями и опытом.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
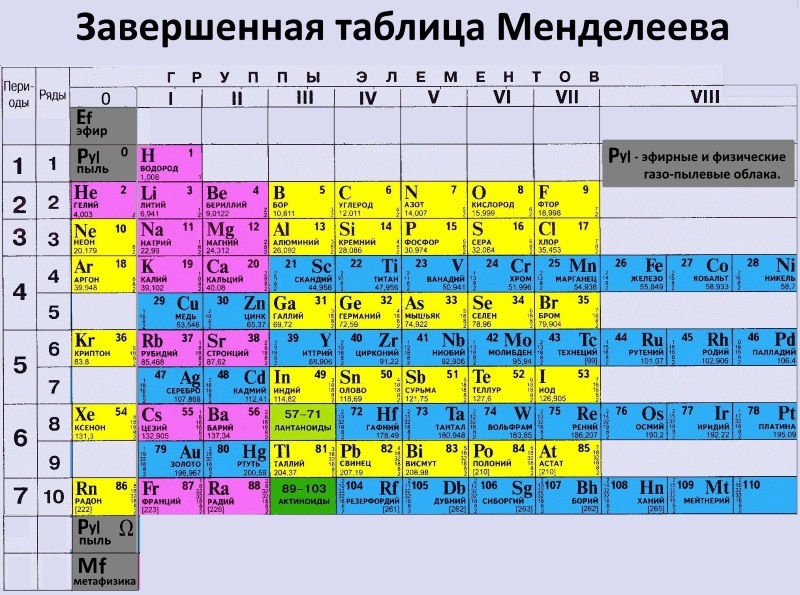
Графическим изображением периодического закона является периодическая таблица. Она содержит 7 периодов и 8 групп.
Короткая форма таблицы Д.И. Менделеева.
Полудлинный вариант таблицы Д.И. Менделеева.
Существует ещё и длинный вариант таблицы, он похож
на полудлинный, но только лантаноиды и актиноиды не вынесены за пределы
таблицы.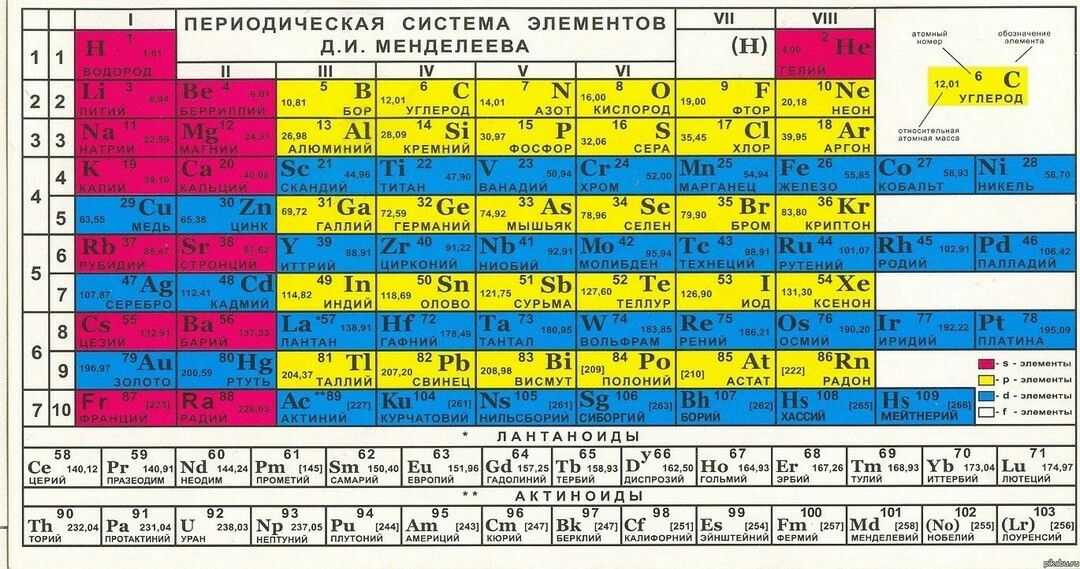
Оригинал таблицы Д. И. Менделеева
1. Период –химические элементы, расположенные в строчку (1 – 7)
Малые (1, 2, 3) – состоят из одного ряда элементов
Большие (4, 5, 6, 7) – состоят из двух рядов – чётного и нечётного
Периоды могут состоять из 2 (первый), 8 (второй и третий), 18 (четвертый и пятый) или 32 (шестой) элементов. Последний, седьмой период незавершен.
Все периоды (кроме первого) начинаются щелочным металлом, а заканчиваются благородным газом.
Во всех периодах с увеличением относительных атомных
масс элементов наблюдается усиление неметаллических и ослабление металлических
свойств. В больших периодах переход свойств от активного металла к благородному
газу происходит более медленно (через 18 и 32 элемента), чем в малых периодах
(через 8 элементов). Кроме того, в малых периодах слева направо
валентность в соединениях с кислородом возрастает от 1 до 7 (например, от
Na
до
Cl
). В больших периодах вначале
валентность возрастает от 1 до 8 (например, в пятом периоде от рубидия к
рутению), затем происходит резкий скачок, и валентность уменьшается до 1 у
серебра, потом снова возрастает.
В больших периодах вначале
валентность возрастает от 1 до 8 (например, в пятом периоде от рубидия к
рутению), затем происходит резкий скачок, и валентность уменьшается до 1 у
серебра, потом снова возрастает.
2. Группы – вертикальные столбцы элементов с одинаковым числом валентных электронов, равным номеру группы. Различают главные (А) и побочные подгруппы (Б).
Главные подгруппы состоят из элементов малых и больших периодов.
Побочные подгруппы состоят из элементов только больших периодов.
В главных подгруппах сверху вниз металлические свойства усиливаются, а неметаллические ослабевают. Элементы главных и побочных групп сильно отличаются по свойствам.
Номер группы показывает высшую валентность элемента (кроме N, O , F ).
Общими для элементов главных и побочных подгрупп
являются формулы высших оксидов (и их гидратов). У высших оксидов и их гидратов
элементов
I
–
III
групп (кроме бора) преобладают основные свойства, с
IV
по
VIII
– кислотные.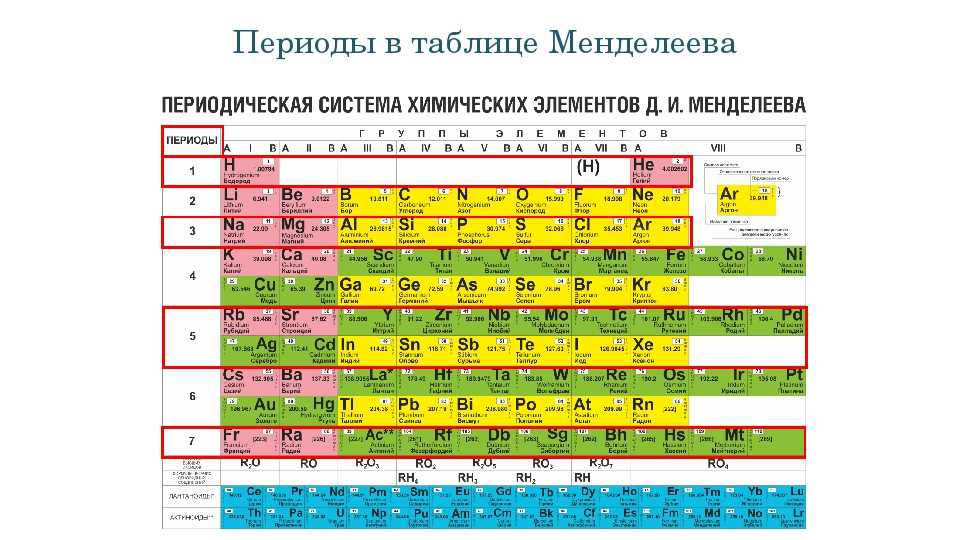
Группа | III | VII | VIII (кроме инертных газов) | |||||
Высший оксид | Э 2 О | ЭО | Э 2 О 3 | ЭО 2 | Э 2 О 5 | ЭО 3 | Э 2 О 7 | ЭО 4 |
Гидрат высшего оксида | ЭОН | Э(ОН) 2 | Э(ОН) 3 | Н 2 ЭО 3 | Н 3 ЭО 4 | Н 2 ЭО 4 | НЭО 4 | Н 4 ЭО 4 |
Для элементов главных подгрупп общими
являются формулы водородных соединений. Элементы главных подгрупп
I
–
III
групп образуют твердые вещества –
гидриды (водород в степени окисления – 1), а
IV
–
VII
групп – газообразные. Водородные
соединения элементов главных подгрупп
IV
группы (ЭН 4) – нейтральны,
V
группы (ЭН 3) –
основания,
VI
и
VII
групп (Н 2 Э и НЭ) – кислоты.
Водородные
соединения элементов главных подгрупп
IV
группы (ЭН 4) – нейтральны,
V
группы (ЭН 3) –
основания,
VI
и
VII
групп (Н 2 Э и НЭ) – кислоты.
Таблица Менделеева является одним из величайших открытий человечества, позволившим упорядочить знания об окружающем мире и открыть новые химические элементы . Она является необходимой для школьников, а так же для всех, кто интересуется химией. Кроме того, данная схема является незаменимой и в других областях науки.
Данная схема содержит все известные человеку элементы, причем они группируются в зависимости от атомной массы и порядкового номера . Эти характеристики влияют на свойства элементов. Всего в коротком варианте таблицы имеется 8 групп, элементы, входящие в одну группу, обладают весьма сходными свойствами. Первая группа содержит водород, литий, калий, медь, латинское произношение на русском которой купрум. А так же аргентум — серебро, цезий, золото — аурум и франций. Во второй группе расположены бериллий, магний, кальций, цинк, за ними идут стронций, кадмий, барий, заканчивается группа ртутью и радием.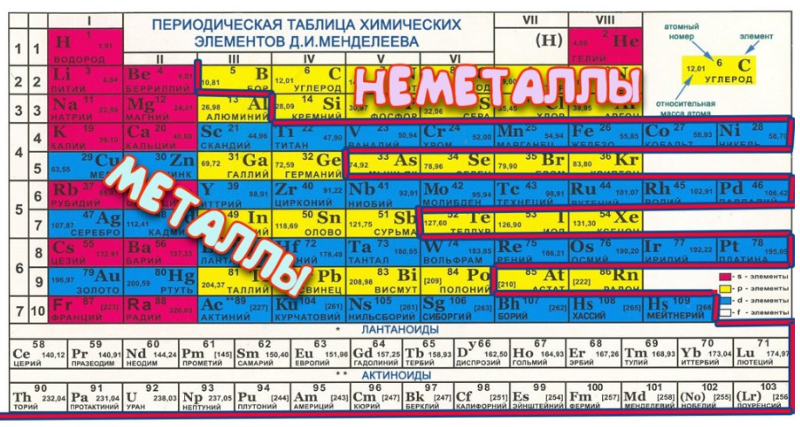
В состав третьей группы вошли бор, алюминий, скандий, галлий, потом следуют иттрий, индий, лантан, завершается группа таллием и актинием. Четвертая группа начинается с углерода, кремния, титана, продолжается германием, цирконием, оловом и завершается гафнием, свинцом и резерфордием. В пятой группе имеются такие элементы, как азот, фосфор, ванадий, ниже расположены мышьяк, ниобий, сурьма, потом идут тантал висмут и завершает группу дубний. Шестая начинается с кислорода, за которым лежат сера, хром, селен, потом следуют молибден, теллур, далее вольфрам, полоний и сиборгий.
В седьмой группе первый элемент – фтор, потом следует хлор, марганец, бром, технеций, за ним находится йод, потом рений, астат и борий. Последняя группа является самой многочисленной . В нее входят такие газы, как гелий, неон, аргон, криптон, ксенон и радон. Так же к данной группе относятся металлы железо, кобальт, никель, родий, палладий, рутений, осмий, иридий, платина. Далее идут ханний и мейтнерий. Отдельно расположены элементы, которые образуют ряд актиноидов и ряд лантаноидов . Они обладают сходными свойствами с лантаном и актинием.
Отдельно расположены элементы, которые образуют ряд актиноидов и ряд лантаноидов . Они обладают сходными свойствами с лантаном и актинием.
Данная схема включает в себя все виды элементов, которые делятся на 2 большие группы – металлы и неметаллы , обладающие разными свойствами. Как определить принадлежность элемента к той или иной группе, поможет условная линия, которую необходимо провести от бора к астату. Следует помнить, что такую линию можно провести только в полной версии таблицы. Все элементы, которые находятся выше этой линии, и располагаются в главных подгруппах считаются неметаллами. А которые ниже, в главных подгруппах – металлами. Так же металлами являются вещества, находящиеся в побочных подгруппах . Существуют специальные картинки и фото, на которых можно детально ознакомиться с положением этих элементов. Стоит отметить, что те элементы, которые находятся на этой линии, проявляют одинаково свойства и металлов и неметаллов.
Отдельный список составляют и амфотерные элементы, которые обладают двойственными свойствами и могут образовывать в результате реакций 2 вида соединений. При этом у них проявляются одинаково как основные, так и кислотные свойства . Преобладание тех или иных свойств зависит от условий реакции и веществ, с которыми амфотерный элемент реагирует.
При этом у них проявляются одинаково как основные, так и кислотные свойства . Преобладание тех или иных свойств зависит от условий реакции и веществ, с которыми амфотерный элемент реагирует.
Стоит отметить, что данная схема в традиционном исполнении хорошего качества является цветной. При этом разными цветами для удобства ориентирования обозначаются главные и побочные подгруппы . А так же элементы группируются в зависимости от схожести их свойств.
Однако в настоящее время наряду с цветной схемой очень распространенной является периодическая таблица Менделеева черно белая. Такой ее вид используется для черно-белой печати. Несмотря на кажущуюся сложность, работать с ней так же удобно, если учесть некоторые нюансы. Так, отличить главную подгруппу от побочной в таком случае можно по отличиям в оттенках, которые хорошо заметны. К тому же в цветном варианте элементы с наличием электронов на разных слоях обозначаются разными цветами .
Стоит отметить, что в одноцветном исполнении ориентироваться по схеме не очень трудно. Для этого будет достаточно информации, указанной в каждой отдельной клеточке элемента.
Для этого будет достаточно информации, указанной в каждой отдельной клеточке элемента.
Егэ сегодня является основным видом испытания по окончанию школы, а значит, подготовке к нему необходимо уделять особое внимание. Поэтому при выборе итогового экзамена по химии , необходимо обратить внимание на материалы, которые могут помочь в его сдаче. Как правило, школьникам на экзамене разрешено пользоваться некоторыми таблицами, в частности, таблицей Менделеева в хорошем качестве. Поэтому, чтобы она принесла на испытаниях только пользу, следует заблаговременно уделить внимание ее строению и изучению свойств элементов, а так же их последовательности. Необходимо научиться, так же пользоваться и черно-белой версией таблицы , чтобы на экзамене не столкнуться с некоторыми трудностями.
Помимо основной таблицы, характеризующей свойства элементов и их зависимость от атомной массы, существуют и другие схемы, которые могут оказать помощь при изучении химии.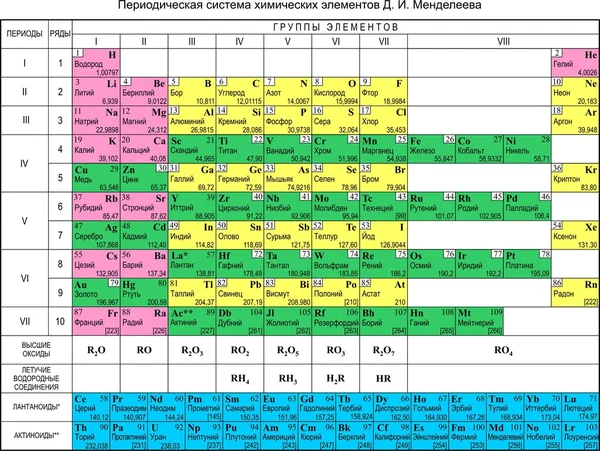 Например, существуют таблицы растворимости и электроотрицательности веществ . По первой можно определить, насколько растворимо то или иное соединение в воде при обычной температуре. При этом по горизонтали располагаются анионы – отрицательно заряженные ионы, а по вертикали – катионы, то есть положительно заряженные ионы. Чтобы узнать степень растворимости того, или иного соединения, необходимо по таблице найти его составляющие. И на месте их пересечения будет нужное обозначение.
Например, существуют таблицы растворимости и электроотрицательности веществ . По первой можно определить, насколько растворимо то или иное соединение в воде при обычной температуре. При этом по горизонтали располагаются анионы – отрицательно заряженные ионы, а по вертикали – катионы, то есть положительно заряженные ионы. Чтобы узнать степень растворимости того, или иного соединения, необходимо по таблице найти его составляющие. И на месте их пересечения будет нужное обозначение.
Если это буква «р», то вещество полностью растворимо в воде в нормальных условиях. При наличии буквы «м» — вещество малорастворимое, а при наличии буквы «н» — оно почти не растворяется. Если стоит знак «+», — соединение не образует осадок и без остатка реагирует с растворителем. Если присутствует знак «-», это означает, что такого вещества не существует. Иногда так же в таблице можно увидеть знак «?», тогда это обозначает, что степень растворимости этого соединения доподлинно не известна. Электроотрицательность элементов может варьироваться от 1 до 8, для определения этого параметра так же существует специальная таблица.
Еще одна полезная таблица – ряд активности металлов. В нем располагаются все металлы по увеличении степени электрохимического потенциала. Начинается ряд напряжения металлов с лития, заканчивается золотом. Считается, что чем левее занимает место в данном ряду металл, тем он более активен в химических реакциях. Таким образом, самым активным металлом считается металл щелочного типа литий. В списке элементов ближе к концу так же присутствует водород. Считается, что металлы, которые расположены после него, являются практически неактивными. Среди них такие элементы, как медь, ртуть, серебро, платина и золото.
Таблица Менделеева картинки в хорошем качестве
Данная схема является одним из крупнейших достижений в области химии. При этом существует немало видов этой таблицы – короткий вариант, длинный, а так же сверхдлинный. Самой распространенной является короткая таблица, так же часто встречается и длинная версия схемы. Стоит отметить, что короткая версия схемы в настоящее время не рекомендуется ИЮПАК для использования.
Всего было разработано больше сотни видов таблицы , отличающихся представлением, формой и графическим представлением. Они используются в разных областях науки, либо совсем не применяются. В настоящее время новые конфигурации схемы продолжают разрабатываться исследователями. В качестве основного варианта используется либо короткая, либо длинная схема в отличном качестве.
Химия – увлекательный, но сложный предмет. А если в школе еще и не было принадлежностей для проведения экспериментов, то можно сказать, что она и вовсе прошла мимо. Но есть то, в чём должен хотя бы минимально ориентироваться каждый человек. Это таблица Менделеева.
Для школьников выучить ее – настоящая пытка. Если они видят ее в снах, то только кошмарных. Так много элементов, у каждого свой номер… Но одна многодетная мать придумала занимательный способ, как выучить таблицу Менделеева . Он подойдет как для детей, так и для взрослых, и о нём тебе с радостью расскажет реакция «Так Просто!» .
Периодическая таблица химических элементов
Как показывает опыт матери четверых детей Карин Трипп, при правильном подходе возможно выучить всё. Чтобы приобщить к изучению химии даже маленьких детей, она решила превратить периодическую таблицу элементов в поле для морского боя.
Игра содержит четыре страницы с таблицей Менделеева – по две для каждого игрока. Каждому игроку на одной таблице необходимо нарисовать свои корабли, а на другой – обозначать точками свои выстрелы и подбитые корабли соперника.
Правила морского боя такие же, как в классической игре. Только для того, чтобы подстрелить кораблик соперника, нужно назвать не букву c цифрой, а соответствующий химический элемент.
Такая методика позволит детям не только усвоить названия химических элементов. Она способствует развитию памяти и логического мышления. Ведь дети будут анализировать порядковые номера и цвета.
Для того чтобы детям на первых порах было проще найти нужный элемент, ряды и столбцы следует пронумеровать цифрами. Но, по словам Карин, ее дети уже через несколько дней игры в «химический морской бой» стали прекрасно ориентироваться в таблице Менделеева. Они знали даже атомные массы и порядковые номера элементов.
Но, по словам Карин, ее дети уже через несколько дней игры в «химический морской бой» стали прекрасно ориентироваться в таблице Менделеева. Они знали даже атомные массы и порядковые номера элементов.
Со временем правила игры можно усложнить. Например, размещать корабль только в пределах одного семейства химических элементов.
В эту игру с удовольствием играет даже восьмилетняя дочь изобретательной матери, которая еще не изучала химию в школе. Да и для взрослых это отличный способ занимательно провести время.
Все страницы таблицы Менделеева для игры в морской бой можно распечатать на обычном или цветном принтере и использовать неограниченное количество раз.
7.11: Серия заданий — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 98037
Цели обучения
- Используйте ряд действий, чтобы предсказать, произойдет ли реакция.

Ниже мы видим два металла, которые могут подвергаться воздействию воды. На картинке слева изображен натрий, который бурно реагирует при контакте с водой. На изображении справа изображено серебро, металл, настолько не вступающий в реакцию с водой, что из него можно делать сосуды для питья. Оба металла имеют один электрон \(s\) во внешней оболочке, так что вы можете предсказать одинаковую реакционную способность каждого из них. Однако у нас есть инструмент, который позволяет нам лучше предсказывать, как одни элементы будут реагировать на другие.
Рисунок \(\PageIndex{1}\): слева натрий реагирует с водой. Справа серебро в виде чашечек с водой не реагирует.Серия действий
Реакции одиночной замены происходят только тогда, когда элемент, который выполняет замену, более реактивен, чем элемент, который замещается. Поэтому полезно иметь список элементов в порядке их относительной реакционной способности. Ряд активности представляет собой список элементов в порядке убывания их реактивности. Поскольку металлы заменяют другие металлы, а неметаллы заменяют другие неметаллы, каждый из них имеет отдельный ряд активности. Таблица \(\PageIndex{1}\) ниже представляет собой ряд активности наиболее распространенных металлов, а таблица \(\PageIndex{2}\) представляет собой ряд активности галогенов.
Поскольку металлы заменяют другие металлы, а неметаллы заменяют другие неметаллы, каждый из них имеет отдельный ряд активности. Таблица \(\PageIndex{1}\) ниже представляет собой ряд активности наиболее распространенных металлов, а таблица \(\PageIndex{2}\) представляет собой ряд активности галогенов.
| Элементы в порядке убывания реакционной способности | Происходит реакция |
|---|---|
\(\ce{Li}\) \(\се{К}\) \(\ce{Ba}\) \(\ce{Sr}\) \(\се{Са}\) \(\ce{Na}\) | Прореагировать с холодной водой, заменив водород. |
\(\ce{Mg}\) \(\ce{Al}\) \(\ce{Zn}\) \(\ce{Cr}\) \(\ce{Fe}\) \(\ce{Cd}\) | Реагировать с паром, но не с холодной водой, замещая водород. |
\(\ce{Co}\) \(\ce{Ni}\) \(\ce{Sn}\) \(\ce{Pb}\) | Не реагировать с водой. Реагировать с кислотами, замещая водород. |
| \(\ce{H_2}\) | |
\(\ce{Cu}\) \(\ce{Hg}\) \(\ce{Ag}\) \(\ce{Pt}\) \(\ce{Au}\) | Не реагирует с водой или кислотами. |
| Элементы, от наиболее реакционноспособных к наименее реакционноспособным |
|---|
| \(\ce{F_2}\) |
| \(\ce{Cl_2}\) |
| \(\ce{Br_2}\) |
| \(\ce{I_2}\) |
Для реакции с одинарным замещением данный элемент способен заменить элемент, стоящий ниже него в ряду активности. Это можно использовать, чтобы предсказать, произойдет ли реакция. Предположим, что небольшие кусочки металлического никеля были помещены в два отдельных водных раствора: нитрата железа (III) и нитрата свинца (II).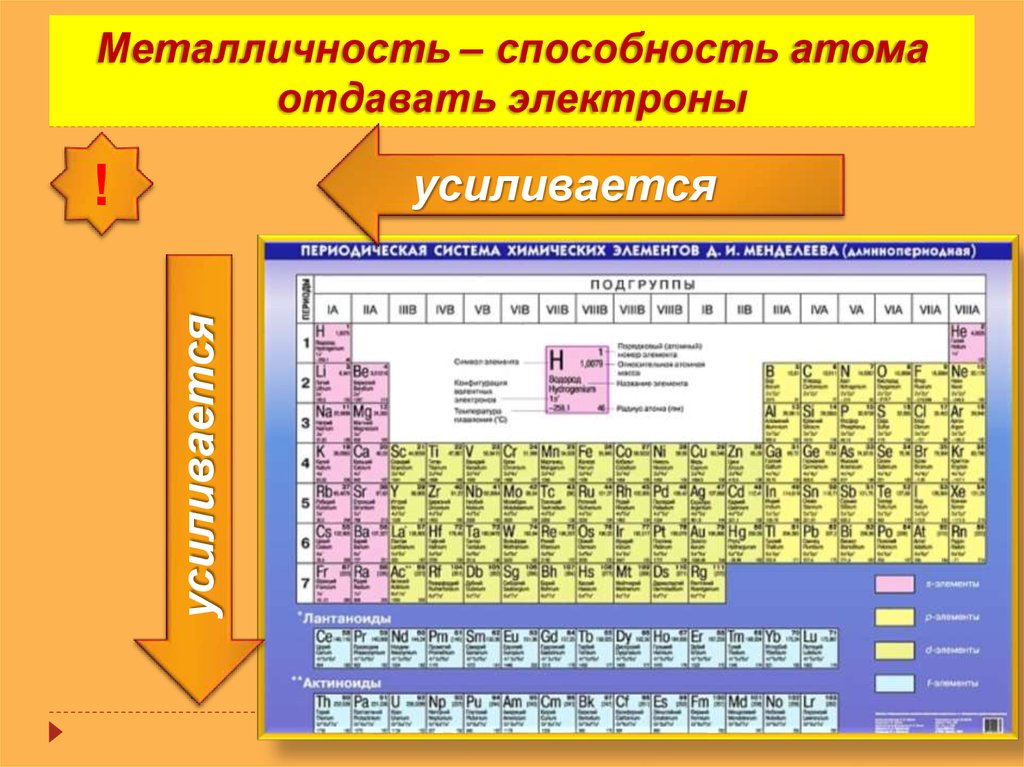 Глядя на ряд активности, мы видим, что никель ниже железа, но выше свинца. Следовательно, металлический никель будет способен заменить свинец в реакции, но не сможет заменить железо.
Глядя на ряд активности, мы видим, что никель ниже железа, но выше свинца. Следовательно, металлический никель будет способен заменить свинец в реакции, но не сможет заменить железо.
\[\ce{Ni} \left( s \right) + \ce{Pb(NO_3)_2} \left( aq \right) \rightarrow \ce{Ni(NO_3)_2} \left( aq \right ) + \ce{Pb} \left( s \right) \nonumber \]
\[\ce{Ni} \left( s \right) + \ce{Fe(NO_3)_3} \left( aq \right ) \rightarrow \text{NR (нет реакции)} \nonumber \]
В описаниях, сопровождающих ряд активности металлов, данный металл также способен вступать в реакции, описанные ниже в этом разделе. Например, литий будет реагировать с холодной водой, замещая водород. Он также будет реагировать с паром и кислотами, так как для этого требуется более низкая степень реакционной способности.
Примеры \(\PageIndex{1}\)
Используйте ряд действий, чтобы предсказать, произойдут ли следующие реакции. Если нет, напишите \(\text{NR}\). Если реакция идет, запишите продукты реакции и составьте уравнение.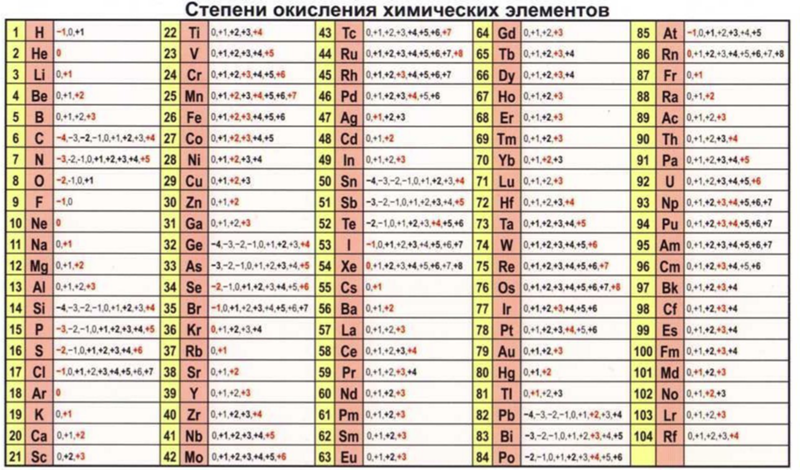
- \(\ce{Al} \left( s \right) + \ce{Zn(NO_3)_2} \left( aq \right) \rightarrow\)
- \(\ce{Ag} \left( s \right) + \ce{HCl} \left( aq \right) \rightarrow\)
Раствор
| Шаги | Пример \(\PageIndex{1A}\) \(\ce{Al} \left( s \right) + \ce{Zn(NO_3)_2} \left( aq \right) \rightarrow\) | Пример \(\PageIndex{1B}\) \(\ce{Ag} \left( s \right) + \ce{HCl} \left( aq \right) \rightarrow\) |
|---|---|---|
| Спланируйте задачу. | Сравните места алюминия и цинка в ряду активности (таблица \(\PageIndex{1}\)) | Сравните размещение серебра и водорода (таблица \(\PageIndex{1}\)) |
Решить.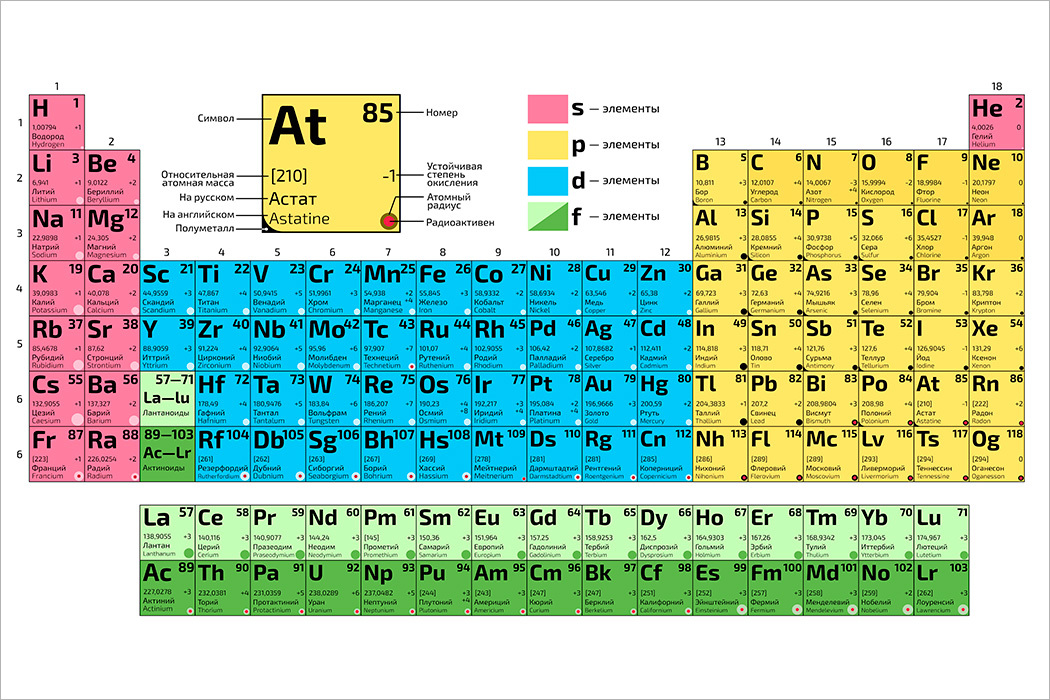 | Поскольку алюминий выше цинка, он способен заменить его и произойдет реакция. Продуктами реакции будут водный раствор нитрата алюминия и твердый цинк. Позаботьтесь о том, чтобы написать правильные формулы для продуктов, прежде чем сбалансировать уравнение. Алюминий принимает заряд \(+3\) в ионном соединении, поэтому формула нитрата алюминия имеет вид \(\ce{Al(NO_3)_3}\). Сбалансированное уравнение: \(2 \ce{Al} \left( s \right) + 3 \ce{Zn(NO_3)_2} \left( aq \right) \rightarrow 2 \ce{Al(NO_3)_3} \left( aq \right) + 3 \ce{Zn} \left( s \right)\) | Поскольку серебро ниже водорода, оно не способно заменить водород в реакции с кислотой. \(\ce{Ag} \left( s \right) + \ce{HCl} \left( aq \right) \rightarrow \text{NR}\) |
Упражнение \(\PageIndex{1}\)
Используйте ряд действий для прогнозирования продуктов каждого уравнения, если они есть.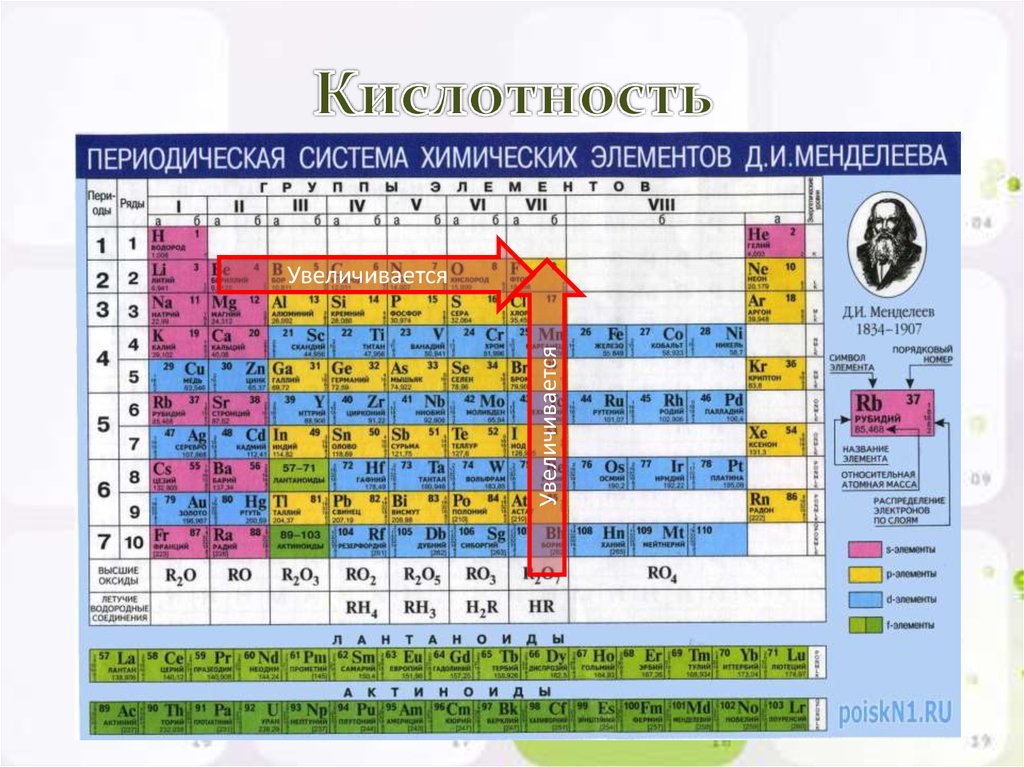
- \(\ce{FeCl2 + Zn →}\)
- \(\ce{HNO3 + Au →}\)
- Ответить на
- Продукты ZnCl 2 + Fe.
- Ответ б
- Нет реакции.
Резюме
- Металлы и галогены классифицируются по их способности вытеснять другие металлы или галогены, находящиеся ниже их в ряду активности.
7.11: Серия действий распространяется под лицензией CC BY-NC-SA 4.0 и была создана, изменена и/или курирована LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.
- Теги
Периодическая таблица элементов: отсортировано по сериям (EnvironmentalChemistry.com)
- Skip to page content
- Skip to site menu on this page
Sorted by Series
Actinides
| Name | Sym | # | ||||||
|---|---|---|---|---|---|---|---|---|
| Actinium | Ac | 89 | ||||||
| Americium | AM | 95 | ||||||
| Berkelium | BK | 97 | ||||||
| 9 | 97977 | |||||||
| 9 | 97 | 9777 | 9 | 977 | .0067Cf | 98 | ||
| Curium | Cm | 96 | ||||||
| Einsteinium | Es | 99 | ||||||
| Fermium | Fm | 100 | ||||||
| Lawrencium | LR | 103 | ||||||
| Mendelevium | MD | 101 | ||||||
| NEPTUNIUM | NP | 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 93 930067 | ||||||
| Nobelium | No | 102 | ||||||
| Plutonium | Pu | 94 | ||||||
| Protactinium | Pa | 91 | ||||||
| Thorium | Th | 90 | ||||||
| Уран | U | 92 |
Щелочноземельные металлы
| Наименование | Sym
| ||
|---|---|---|---|
| Barium | Ba | 56 | |
| Beryllium | Be | 4 | |
| Calcium | Ca | 20 | |
| Magnesium | Mg | 12 | |
| Radium | RA | 88 | |
| Стронтий | SR | 38 |
ALKALI Metalls
ALKALI
ALKALI
9.
 0127
0127Halogens
| Name | Sym | # | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Astatine | At | 85 | |||||||||||||||||||||||
| Bromine | Br | 35 | |||||||||||||||||||||||
| Chlorine | CL | 17 | |||||||||||||||||||||||
| Флуорин | F | ||||||||||||||||||||||||
| йод | I | 539 | I | 53 | I | I | I | I | I | I | |||||||||||||||
| 0067 |
Lanthanides
| Name | Sym | # | ||||
|---|---|---|---|---|---|---|
| Cerium | Ce | 58 | ||||
| Dysprosium | Dy | 66 | ||||
| Erbium | Er | 68 | ||||
| Europium | EU | 63 | ||||
| Gadolinium | GD | 64 | GD | 64 | 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007. 0050 0050 | |
| Holmium | Ho | 67 | ||||
| Lanthanum | La | 57 | ||||
| Lutetium | Lu | 71 | ||||
| Neodymium | Nd | 60 | ||||
| Praseodymium | PR | 59 | ||||
| PROMETHIUM | PM | 61 | ||||
| SAMARIM0067 | Sm | 62 | ||||
| Terbium | Tb | 65 | ||||
| Thulium | Tm | 69 | ||||
| Ytterbium | Yb | 70 |
Metalloids (Metals)
| Наименование | SYM | # | ||||
|---|---|---|---|---|---|---|
| Возратность | SB | 51 | ||||
| 9 | ||||||
| 9 | ||||||
| 9 | | Ge | 32 | Polonium | Po | 84 | |
Metalloids (Nonmetals)
| Name | Sym | # | |
|---|---|---|---|
| Arsenic | As | 33 | |
| Boron | B | 5 | |
| Кремний | SI | 14 | |
| 7 | 7 | 1752 |
Metals
| Name | Sym | # | ||
|---|---|---|---|---|
| Aluminum | Al | 13 | ||
| Bismuth | Bi | 83 | ||
| Gallium | GA | 31 | ||
| Индий | в | 49 | ||
| ВЫСОВАНИЕ | PB | . 0067 0067 | ||
| Thallium | Tl | 81 | ||
| Tin | Sn | 50 |
Noble Gasses
| Name | Sym | # | |
|---|---|---|---|
| Argon | Ar | 18 | |
| Helium | He | 2 | |
| Krypton | Kr | 36 | |
| Neon | Ne | 10 | |
| Radon | Rn | 86 | |
| Xenon | Xe | 54 |
Nonmetals
| Name | Sym | # | |
|---|---|---|---|
| углерод | C | 6 | |
| Водород | H | 1 | 1 |
| 1 | 1 | ||
| 1 | |||
| 0067 | N | 7 | |
| Oxygen | O | 8 | |
| Phosphorus | P | 15 | |
| Selenium | Se | 34 | |
| Sulfur | S | 16 |
Трансактиниды
| Наименование | SYM | # | ||||
|---|---|---|---|---|---|---|
| BOHRIUM 9007 | 50 | |||||
| 9007 | 9007 | 9007 | 9007 | 9007 | ||
. 0067 0067 | 107 | |||||
| Darmstadtium | Ds | 110 | ||||
| Dubnium | Db | 105 | ||||
| Hassium | Hs | 108 | ||||
| Meitnerium | Mt | 109 | ||||
| Рентгений | Rg | 111 | ||||
| Резерфордий 7 | Rf| Seaborgium | Sg | 106 | |
Transition Metals
| Name | Sym | # | |
|---|---|---|---|
| Cadmium | Cd | 48 | |
| Chromium | Cr | 24 | |
| Кобальт | CO | 27 | |
| МОП | CU | 29 | CU | 29 | CU | 29 | CU | 29 | 0041Gold | Au | 79 |
| Hafnium | Hf | 72 | |
| Iridium | Ir | 77 | |
| Iron | Fe | 26 | |
| марганец | MN | 25 | |
| Mercury | HG | 80 | |
| Molybdenum | |||
| Molybdenum | 1 | ||