|
Цели урока: |
Все учащиеся смогут – понимать модель строения атома. Большинство учащихся сможет – объяснять поведение потока протонов, нейтронов и электронов в электрическом поле. Некоторые учащиеся могут – анализировать существовавшие в различные периоды времени модели атома, определяя преимущества и недостатки каждой модели. |
Критерии оценивания: |
Учащиеся, достигнут целей обучения если: – Определять и описывать протоны, нейтроны и электроны с точки зрения их относительного заряда и относительной массы. – Описывать распределение массы и заряда внутри атома. – Понять модель строения атома. – Прогнозировать поведение потока протонов, нейтронов и электронов в электрическом поле. |
Языковые цели: |
Учащиеся смогут описывать строение атома, используя термины, специфичные для данной темы. Лексика и терминология, специфичная для предмета: Атом, нейтральный, ядро, протон, нейтрон, электрон, заряд, относительная масса, планетарная модель. Полезные выражения для диалогов и письма: В состав атома… входит… Ядро атома… состоит из…. |
Межпредметные связи: |
История (работа с историческими фактами, различные этапы развития строения атома). Физика – строение атома, ядро, заряд, электрическое поле. |
Предварительные знания: |
Вещество, элемент, молекула, атом. |
Основные сведения о строении атома. состав атомных ядер
«Химия – это область чудес, в ней скрыто счастье человечества, величайшие завоевания разума будут сделаны именно в этой области».
А.М. Горький
Наиболее точную и полную модель строения атома предложил Эрнест Резерфорд, хотя понятие «атом» было известно еще в античном мире. Свою модель строения атома ученый назвал планетарной, потому что атом как крошечная Солнечная система, в центре которого ядро, а вокруг ядра вращаются электроны.
Крошечное
ядро состоит из элементарных частиц – протонов и нейтронов. Рассмотрим
таблицу, в которой указан символ этой частицы, её масса и заряд.
Состав ядра
Из таблицы видно, что протон имеет заряд +1, масса протона равна 1, как и у водорода, поэтому он имеет символ р (пэ). Нейтроны тоже имеют массу равную 1, не имеют заряда, он равен 0 и обозначаются буквой n (эн). Электроны обозначаются буквой е, заряд их равен –1, т.к. масса их ничтожна мала, то ей можно пренебречь.
Сумма чисел протонов и нейтронов называется массовым числом и обозначается буквой А, которая численно равна относительной атомной массе, округленной до целого значения.
Для того чтобы определить число протонов и электронов,
Для нахождения числа нейтронов можно использовать следующую формулу:
N = A – Z
т. к.
A =
Z +
N, где N
–
число нейтронов, а Z
–
число протонов.
к.
A =
Z +
N, где N
–
число нейтронов, а Z
–
число протонов.
Несмотря на то, что атом очень малы, швейцарские учёные Биннинг и Рорер
Строение атома и валентность элементов
Рассматривая электронное строение атомов различных элементов в порядке возрастания их порядкового номера, мы убедились (с. 28), что атом водорода (1в ) одновалентен, тогда как валентность атома гелия (1з ) равна нулю. Валентность атома лития (ls 2s ) во всех соединениях равна единице, тогда как бериллий (18 2в ) становится двухвалентным благодаря переходу атома в возбужденное состояние (18 28 2р ).
Нельзя отождествлять степень окисления с валентностью элемента, если даже абсолютные их значения совпадают. Валентность атома, определяемая как число химических связей, которыми данный атом соединен с другими атомами, не может иметь знака (+ или —) и равняться нулю. Поэтому особенно неудачны выражения положительная и отрицательная валентность и тем более нулевая валентность , бытующие поныне в химической литературе. Рассмотрим пример метана СНд, метилового спирта СНзОН, формальдегида НСОН, муравьиной кислоты ИСООН и диоксида углерода СОа, в которых валентность углерода равна четырем, а степени окисления его равны соответственно —4, —2, О, + 2 и -1-4. Кроме того, для установления валентности атома требуется знание химического строения соединения, а определение степени окисления производится в отрыве от строения вещества, т.

Монооксид углерода представляет собой пример химического соединения, когда валентность элементов превышает число неспаренных электронов. Углерод и кислород трехвалентны, хотя атомы этих элементов имеют по два неспаренных электрона. Не следует думать, что монооксид углерода — исключение. Наоборот, подавляюш,ее большинство неорганических соединений образуется или на основе донорно-акцепторного механизма ковалентной связи, или одновременно сочетает в себе обменный и донорно-акцепторный механизмы. Рассмотрим сульфид цинка, кристаллохимическое строение которого показано на рис. 4. Каждый атом цинка связан с четырьмя атомами серы, и, наоборот, каждый атом серы — с четырьмя атомами цинка. Поэтому атомы цинка и серы проявляют одинаковую валент ность, равную четырем. Между тем атом цинка в нормальном состоянии не имеет ни одного неспаренного электрона, а атом серы характеризуется двумя одиночными электронами. При возбуждении атома цинка происходит промотирование 45-электрона на 4р-уровень и появляются два неспаренных электрона  73]
73]
Классическая теория рассматривала вопрос о числе валентности, которое можно было приписать атому определенного элемента, входящему в состав определенной молекулы (или определенного ряда молекул). Согласно классической теории атом одного и того же элемента в двух разных молекулах (или разных рядах молекул) может иметь разные числа валентности. Что же касается валентности атома в изолированном состоянии, то такой вопрос не имел смысла в классической теории химического строения .
Валентность элементов с точки зрения теории строения атома. Сопоставление валентности элементов, устанавливаемой изучением химического состава и формул сложных веществ, с зарядом ионов, образуемых атомами данного элемента, приводит к заключению, что валентность элемента, по существу, и определяется зарядом иона. Так, водород одновалентен. Это связано с тем, что атом водорода в процессе [c.

Электронное строение атома бериллия в газообразном состоянии — 15 25% Увеличение заряда ядра атома бериллия по сравнению с зарядом ядра атома лития наряду с тем, что 25-электроны только частично экранируют друг друга, приводит к двум эффектам 1) атом Ве имеет металлический радиус только 0,89 А, значительно меньше, чем в случае лития (1,22 А) 2) потенциалы ионизации Ве, 9,32 и 18,21 эв, гораздо большие, чем у Ы (5,39 эе), делают Ве значительно менее электроположительным, если рассматривать его хилшческие свойства в сравнении со свойствами Действительно, не существует никаких кристаллических соединений или растворов, в которых ионы Ве + существовали бы как таковые. Все соединения, строение которых было определено, даже соединения с наиболее электроотрицательными элементами, такие, как ВеО и ВеР.,, по крайней мере частично обладают ковалентным характером связи. Электронное строение атомов других элементов II группы (Mg, Са, 5г, Ва и Ка) подобно строению атома Ве. Однако больший размер этих ато.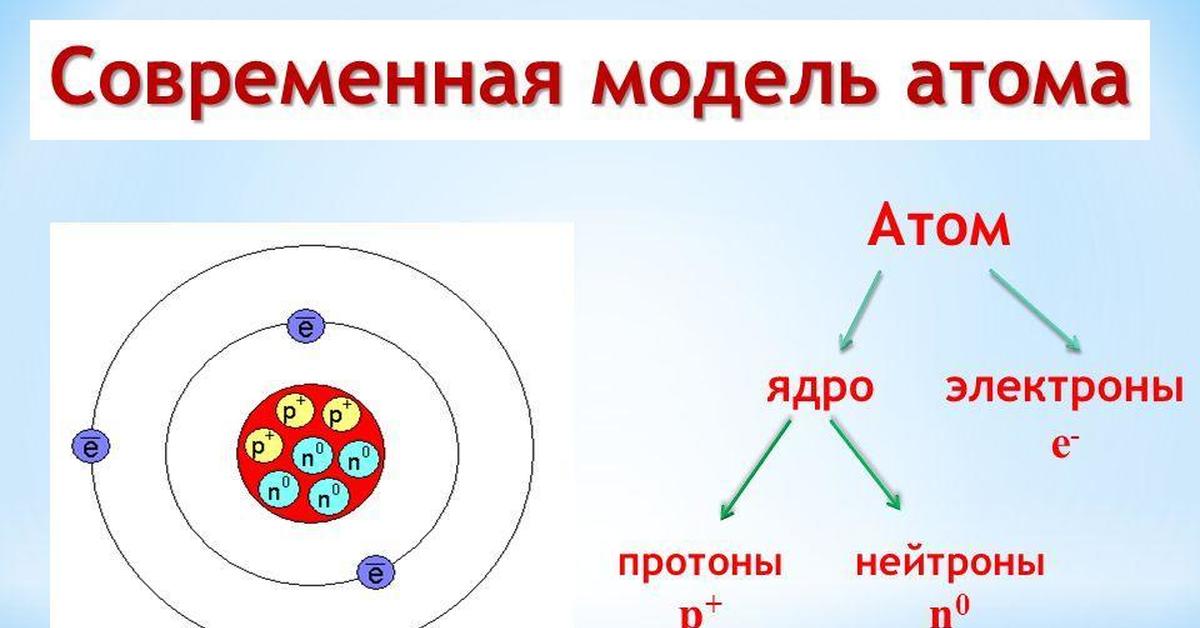
Вскоре появляется работа, результаты которой привели к мысли об определенном строении молекул. В 1852 г. английский исследователь Франкланд на основании изучения образования некоторых металлорганических соединений (СНзЫа, (СНз)2Н , (СНз)зА1, (СНз)480 и др.] ввел понятие о валентности (атомности), численно выражающей способность атома данного элемента вступать в соединение с определенным числом атомов другого элемента. Приняв валентность водорода равной единице, можно считать, что валентность других элементов является числом, показывающим, со сколькими атомами водорода (или иного одновалентного элемента) может соединиться атом данного элемента. [c.110]
Валентность элементов зависит от строения их атомов. Согласно данным современной науки, атомы представляют собой сложные системы. Б центре атома находится ядро, имеющ,ее положительные электрические заряды. Вокруг ядра вращаются электроны (наименьшие частицы отрицательного электричества). Число положительных зарядов ядра равно числу отрицательно заряженных электронов атома. Поэтому атом в целом является электронейтраль-ным. Электроны располагаются вокруг ядра слоями, причем во внешнем слое не бывает больше 8 электронов. [c.50]
Б центре атома находится ядро, имеющ,ее положительные электрические заряды. Вокруг ядра вращаются электроны (наименьшие частицы отрицательного электричества). Число положительных зарядов ядра равно числу отрицательно заряженных электронов атома. Поэтому атом в целом является электронейтраль-ным. Электроны располагаются вокруг ядра слоями, причем во внешнем слое не бывает больше 8 электронов. [c.50]
В металлических проводниках электрический ток представляет собой движение этих электронов при силе тока в 1 ампер 6,3 10 электронов протекают в секунду через поперечное сечение проводника. Для того чтобы понять это, мы должны воспользоваться нашими познаниями в строении атомов химических элементов. Явления радиоактивности, а также исследования с помощью рентгеновских лучей, привели к заключению, что атомы состоят из положительно заряженного ядра, окруженного системой отрицательно заряженных электронов, которые мы можем сравнить с планетами нашей солнечной системы ). Несмотря на то, что носителем атомной массы является ядро, объем последнего ничтожен по сравнению с измерениями атома диаметр ядра для различных элементов выражается величиной порядка 10 см. Кроме положительных зарядов ядро содержит также и отрицательные электроны, которые можно рассматривать как связующее вещество . Избыток положительных зарядов указывает порядковое число данного элемента оно определяет такке и количество электронов, вращающихся вокруг ядра, так как по отношению к внешней среде атом является электрически нейтральным,. Электроны вращаются вокруг ядра нормального атома на более или менее отдаленных и наклоненных друг к другу эллиптических орбитах — так называемых дискретных и свободных от излучения квантовых орбитах. Внешние воздействия могут перебрасывать электроны с одной орбиты на другую. Часто (но не всегда) ) электроны, находящиеся на внешней орбите, легче всего отщепляются. Эти легко отщепляющиеся электроны играют роль при многих реакциях, поскольку последние вообще возможны с точки зрения общих законов энергетики, и поэтому их назы- вают у электроположительных элементов электронами валентности.
Несмотря на то, что носителем атомной массы является ядро, объем последнего ничтожен по сравнению с измерениями атома диаметр ядра для различных элементов выражается величиной порядка 10 см. Кроме положительных зарядов ядро содержит также и отрицательные электроны, которые можно рассматривать как связующее вещество . Избыток положительных зарядов указывает порядковое число данного элемента оно определяет такке и количество электронов, вращающихся вокруг ядра, так как по отношению к внешней среде атом является электрически нейтральным,. Электроны вращаются вокруг ядра нормального атома на более или менее отдаленных и наклоненных друг к другу эллиптических орбитах — так называемых дискретных и свободных от излучения квантовых орбитах. Внешние воздействия могут перебрасывать электроны с одной орбиты на другую. Часто (но не всегда) ) электроны, находящиеся на внешней орбите, легче всего отщепляются. Эти легко отщепляющиеся электроны играют роль при многих реакциях, поскольку последние вообще возможны с точки зрения общих законов энергетики, и поэтому их назы- вают у электроположительных элементов электронами валентности. [c.18]
[c.18]
Впоследствии было показано (Г. Си бор г. Актинидные элементы. М., Атом-издат, 1960), что строение периодической системы элементов сложнее. Химические свойства элементов закономерно меняются с изменением электронной оболочки атома, и хотя уран имеет шести валентные соединения, он принадлежит не к VI группе, а к группе тяжелых редкоземельных элементов, аналогов группы элементов от лантана до лютеция. [c.8]
Такие формулы правильно отражают фактическую сторону, но ничего не говорят ни о причине четырехвалентности углерода, ни о природе химической связи между атомами, образующими молекулу. Когда с развитием учения о строении атома стало ясно, что свойства элементов находятся в периодической зависимости не от их ато.много веса, а от порядкового номера, то есть от количества положительных зарядов их ядра, начала выясняться и природа химической связи и причина, определяющая валентность элементов.
 [c.15]
[c.15] Рассмотрим теперь математическое представление реактантов, учитывающее явление геометрической изомерии. Отметим сразу, что современные формулы строения химических веществ непригодны для проведения расчетов на ЭВМ химических реакций, так как их нельзя непосредственно ввести в оперативную намять ЭВМ или записать на внешние носители информации. Далее, для этой цели нецелесообразно использовать и векторное представление молекул, которое строилось на основе их брутто-формул. Следовательно, требуются дальнейшие обобщения, связанные с представлением молекул в виде матриц определенной размерности, равной числу содержащихся в молекуле атомов. При формировании элементов этой матрицы, называемой В-матрицей, учитывается, что каждый атом состоит из атомного остова, составленного из ядра атома и внутренних электронов и имеющего некоторый формальный заряд, и электронов валентной оболочки. Последние менее сильно связаны с атомным остовом и участвуют в образовании химических связей. [c.174]
[c.174]
Структура и характер химической связи металлов и неметаллических элементов соверщенно отличны друг от друга. Строение металлов будет подробно рассмотрено в гл. 23. Здесь же следует лишь заметить, что в металлах каждый атом окружен большим числом ближайших соседей (обычно 8 или 12), причем атомы образуют плотно-упакованную структуру или структуру, близкую к плотноупакованной, например кубическую объемноцентрированную (см. рис. 11.15, ч. 1). В металлах валентные электроны легко перемещаются по всему кристаллу, что и придает металлам характерный блеск, а также высокие тепло- и электропроводность. [c.282]
Еще не изжито до конца мнение, согласно которому теория химического строения сводится к формальной схеме, позволяющей рисовать органические молекулы, приписав атому водорода одну черточку валентности, кислороду и сере — две, азоту и фосфору — три, а углероду — четыре. Бутлеров был бесконечно далек от такого подхода к делу и считал валентность атома углерода, как и других элементов, переменной. Труды Бутлерова сохранили свое значение до сего времени, поскольку он верно решил коренные методологические проблемы органической химии, над которыми безуспешно бились его современники. [c.9]
Труды Бутлерова сохранили свое значение до сего времени, поскольку он верно решил коренные методологические проблемы органической химии, над которыми безуспешно бились его современники. [c.9]
Чаще, чем валентность, используется почти равноценное понятие степень окисления. Это положительное или отрицательное число, выражающее заряд, который будет иметь атом, если электроны в молекуле соединения распределить между атомами определенным образом. Так как это распределение часто несколько произвольно, степень окисления не всегда численно равна валентности. Тем не менее это понятие чрезвычайно полезно. Ниже приведены правила для установления степени окисления каждого атома в соединении, но следует помнить, что они не являются безупречными степень окисления атома в элементе в свободном виде равна нулю , степень окисления одноатомного иона есть его заряд степень окисления каждого атома в ковалентном соединении известного строения есть заряд, который останется на атоме, после того как все общие электронные пары полностью сместились бы в сторону наиболее электроотрицательного атома (электронная пара, обобщенная одинаковыми атомами, делится пополам) степень окисления атома элемента в молекуле соединения с неизвестным строением обычно оценивают по степеням окисления атомов других элементов в молекуле соединения.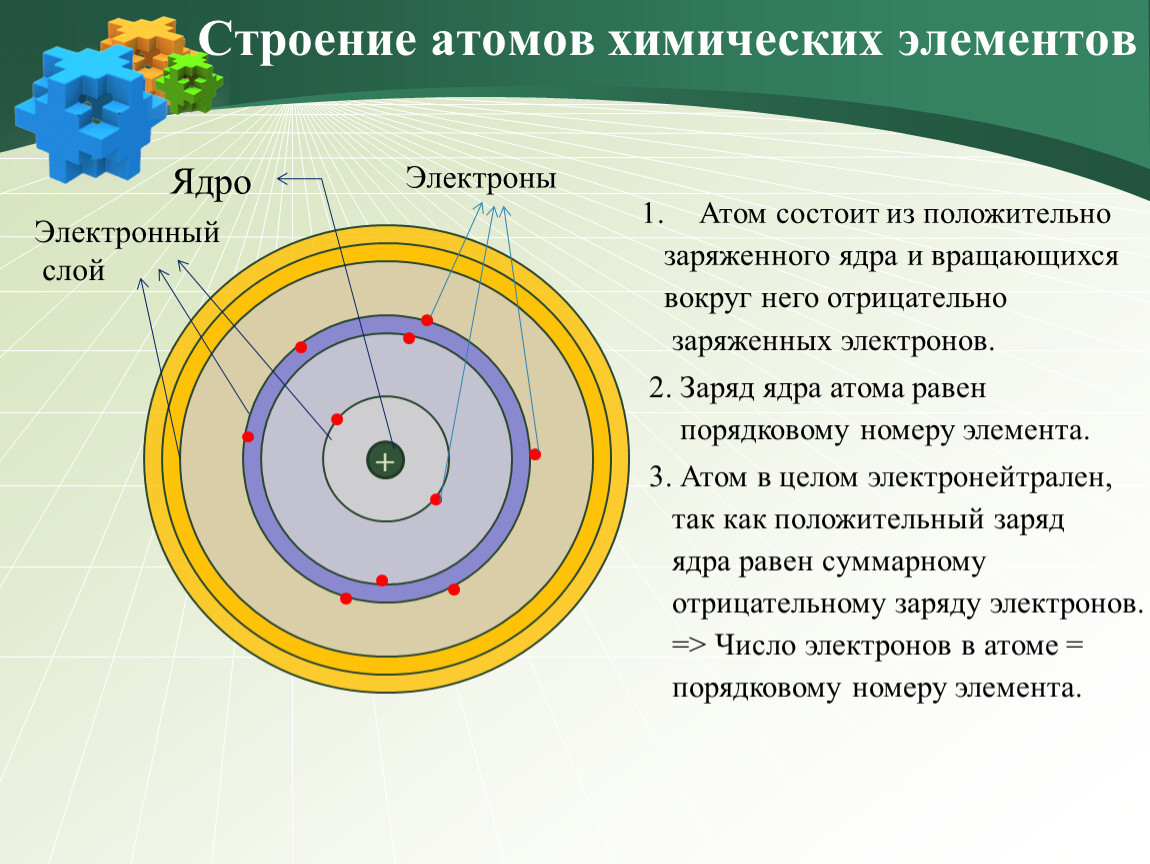 [c.126]
[c.126]
Первые данные о строении силикатов были получены с помощью химических методов. На основании исследований учеными из школ И. И. Лемберга и В. И. Вернадского удалось сделать важные выводы о строении силикатов и выявить связь между строением и реакционной способностью отдельных групп силикатов. В алюмосиликатах удалось установить наличие стойких комплексов, переходящих при химических превращениях без изменения от одного соединения к другому. Однако в изучении силикатов наибольшие успехи были достигнуты в результате применения рентгеноструктурного и электронографического анализов, а также электронной микроскопии. К настоящему времени можно считать установленным, что основным элементом пространственной группировки кристаллических силикатов является группа 8104 в форме тетраэдра, в которой каждый атом кремния связан с четырьмя атомами кислорода. Связи 51 — О, играющие главную роль в силикатах, можно считать ковалентными. Однако полярность таких связей значительна. Как в 5102, так и в силикатах атомы кислорода располагаются вокруг атома кремния в вершинах тетраэдра, используя свою вторую валентность большей частью или на связь с другим атомом кремния или на связь с атомом металла. В последнем случае атомы кислорода переходят в состояние однозарядных отрицательных ионов. [c.59]
Как в 5102, так и в силикатах атомы кислорода располагаются вокруг атома кремния в вершинах тетраэдра, используя свою вторую валентность большей частью или на связь с другим атомом кремния или на связь с атомом металла. В последнем случае атомы кислорода переходят в состояние однозарядных отрицательных ионов. [c.59]
Строение электронных уровней атомов этих элементов характеризуется почти полной достройкой -подуровня предпоследнего уровня шесть —у железа, семь — у кобальта и восемь — у никеля. Заполнение -подуровня у атомов этих элементов сказывается на уменьшении окислительного числа, поскольку на /-подуровне содержится меньшее число непарных электронов (см. Курс химии, ч. 1. Общетеоретическая, гл. 11, стр. 86). Поэтому если марганцу свойственно еще окислительное число +7. то атом железа может отдавать не более 6 электронов и, следовательно, его окислительное число не может быть больше +6. Окислительное число кобальта не можег быть больше +5, а никеля -1-4. Таким образом, у атомов этих элементов уже нельзя считать все электроны незаполненных уровней валентными. Одновременно с повышением устойчивости почти зг(полненного /-подуровня снижается склонность этих элементов к металлообразным соединениям с электронной проводимостью. [c.126]
Одновременно с повышением устойчивости почти зг(полненного /-подуровня снижается склонность этих элементов к металлообразным соединениям с электронной проводимостью. [c.126]
Таким образом, общие и специфические свойства определяются схожестью электронного строения атомов ( в свободном или связанном состоянии), проявляемой в близости радиусов, величин электроотрицательности атомов, в изоморфизме соединений, равенстве и однотипности валентных возможностей атомов и т. д. Индивидуальные свойства — это свойства, присущие только данному атому это результат проявления всех особенностей его электронной структуры, его заряда ядра и всех вытекающих особенностей (энергии, геометрии атомных орбиталей). Электронная структура атома в свободном состоянии индивидуальна, неповторима. Атом занимает определенное место в непрерывном ряду элементов и обладает физической индивидуальностью спектром, атомной массой, набором изотопов и т. д. и т. п. [c.48]
Попять физический смысл валентности помогло учение о строении атомов и химической связл.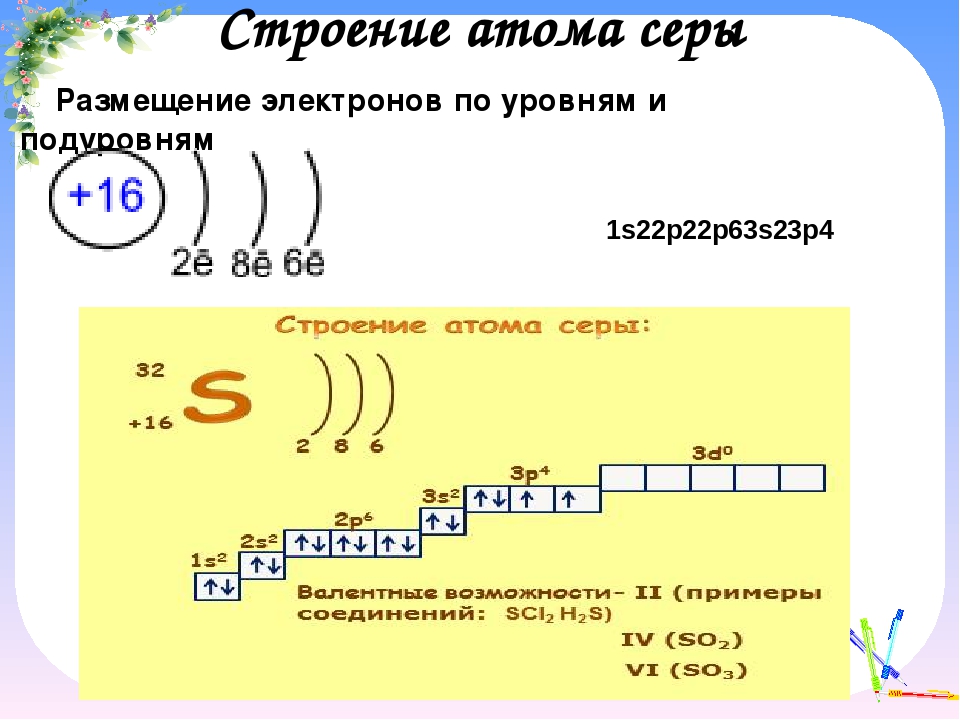 Как уже отмечалось, электроны, которые участвуют в образовании химических связей между атомами, называются валентными. Зто электроны, наиболее слабо связанные с ядром. У химических элементов общее число валентных электронов в атоме, как правило, равно номеру группы периодической системы элементов Д. И. Менделеева. Так, атом серы (элемент VI группы) содержит всего 16 электронов, нз них валентных 6. К валентным относятся прежде всего электроны внешних незавершенных уровней. Однако валентными могут быть и электроны второго снаружи уровня (например, у -элементов), а также электроны третьего снаружи уровня (например, у /-элементов). [c.58]
Как уже отмечалось, электроны, которые участвуют в образовании химических связей между атомами, называются валентными. Зто электроны, наиболее слабо связанные с ядром. У химических элементов общее число валентных электронов в атоме, как правило, равно номеру группы периодической системы элементов Д. И. Менделеева. Так, атом серы (элемент VI группы) содержит всего 16 электронов, нз них валентных 6. К валентным относятся прежде всего электроны внешних незавершенных уровней. Однако валентными могут быть и электроны второго снаружи уровня (например, у -элементов), а также электроны третьего снаружи уровня (например, у /-элементов). [c.58]
Важнейшим представлением класситеской теории химиче ского строения является представление о том, что атом определенного элемента в определенном ряду химических частиц может быть охарактеризован некоторым постоянным целым положительным числом — числом валентности. Это число в классической теории имело смысл числа единиц сродства, которое затрачивает данный атом на образование химических связей с другими атомами в рассматриваемом ряду соединений. Установление значения числа валентности некоторого атома в определенном ряду соединений в классической теории может быть проведено двумя путями. [c.135]
Установление значения числа валентности некоторого атома в определенном ряду соединений в классической теории может быть проведено двумя путями. [c.135]
Основные научные исследования посвяш,ены развитию электронных представлений в химии. Предложил (1916) статическую электронную теорию строения атомов и молекул, согласно которой а) атомы благородных газов обладают особенно устойчивой восьмиэлектронной внешней оболочкой (атом гелия — двухэлектронной) б) атомы других элементов во внешней оболочке имеют неполный электронный октет в) образование химического соединения происходит вследствие перехода электронов от атома одного элемента к атому другого элемента и появления ионной химической связи, то есть благодаря электростатическому притяжению. Наиболее устойчивыми должны быть те соединения, в которых валентные электроны распределяются так, чтобы каждый атом был окружен оболочкой, имитирующей электронную оболочку благородного газа. Гипотеза Косселя о гетерополярных связях легла в основу теории ионной связи и гетеровалентности. [22, 324[ [c.258]
[22, 324[ [c.258]
Если бы не было определенной закономерности, в соответствии с которой атомы различных элементов соединяются, образуя молекулы и кристаллические соединения, то приходилось бы запоминать формулы тысяч соединений. Однако формулы различных веществ в значительной мере поддаются систематизации, в основе которой лежит тот факт, что некоторые элементы имеют вполне определенную способность образовывать соединения или обладают определенной валентностью (от латинского слова valentia — сила или способность), определяющей число других атомов, с которыми может соединяться атом данного элемента. Другие элементы, более слондвух или большего числа присущих им валентностей. Данная глава посвящена вопросам природы валентности, валентности элементов и ее связи со строением атомов, систематизации валентностей и других свойств элементов, достигаемой периодической системой все эти вопросы — очень важная часть химической науки. [c.159]
Высшая положительная валентность элемента определяется максимальным количеством электронов, которые может отдать атом данного элемента при его окислении. Во многих случаях высшая положительная валентность элемента определяется структурой внешнего электронного слоя его атома. Так, согласно схеме строения атома азота 4-7 2)5), на внешнем электронном слое содержится 5 электронов. Высшая положительная валентность азота, как указано, численно равна той же величине (-Ь5). Такое, же соотношение наблюдается для многих элементов. Так, сера образует соединения ЗОг и 80з, в которых она – -4 и -[-6-валентна. Схема строения атома 8 + 16 2)8)6). Эта схема показывает, что на внешнем слое атома серы содержится 6 электронов и высшая положительная валентность серы равна Ц- 6. Высшая положительная валентность хлора +7, и атом хлора на внешнем слое содержит 7 электронов и т. д. К числу подобных элементов относятся все типичные неметаллы. [c.95]
Во многих случаях высшая положительная валентность элемента определяется структурой внешнего электронного слоя его атома. Так, согласно схеме строения атома азота 4-7 2)5), на внешнем электронном слое содержится 5 электронов. Высшая положительная валентность азота, как указано, численно равна той же величине (-Ь5). Такое, же соотношение наблюдается для многих элементов. Так, сера образует соединения ЗОг и 80з, в которых она – -4 и -[-6-валентна. Схема строения атома 8 + 16 2)8)6). Эта схема показывает, что на внешнем слое атома серы содержится 6 электронов и высшая положительная валентность серы равна Ц- 6. Высшая положительная валентность хлора +7, и атом хлора на внешнем слое содержит 7 электронов и т. д. К числу подобных элементов относятся все типичные неметаллы. [c.95]
Металличность и неметалличность в значительной степени определяются структурой атома, т. е. зарядом его ядра и особенностями строения электронной оболочки. Как известно, атомы состоят из положительно заряженного ядра и отрицательно заряженньтсилы притяжение— между разноименными зарядами и отталкивание— между одноименными.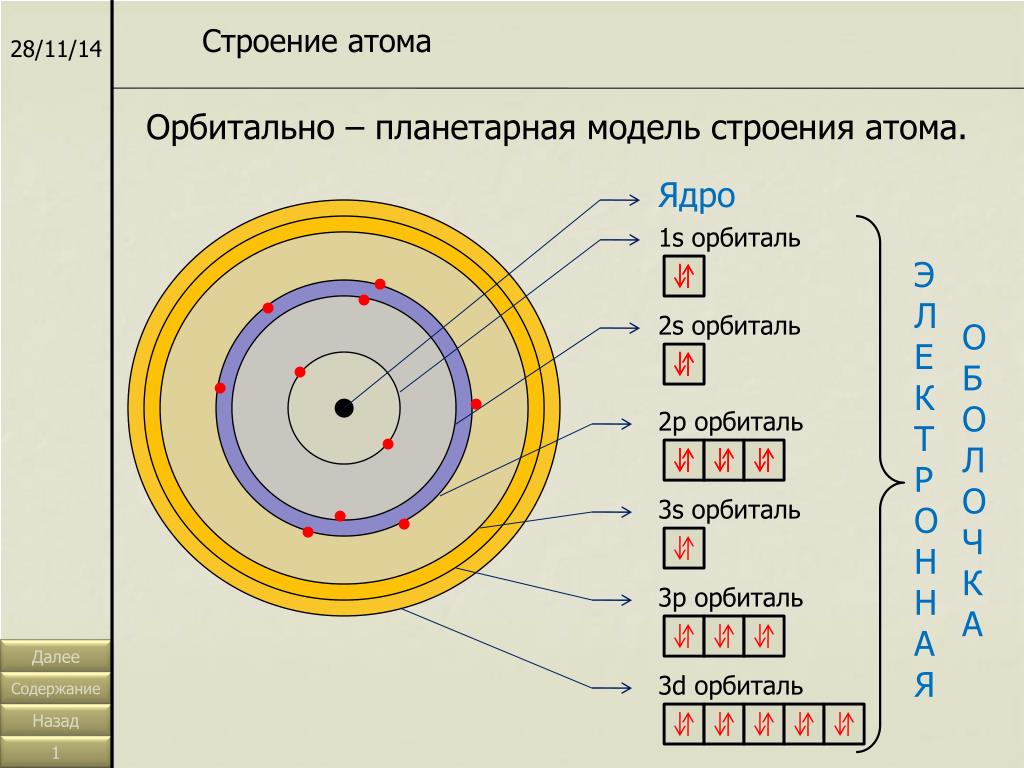 Наличие и взаимодействие этих сил обеспечивает, во-первых, устойчивое существование атома, во-вторых, открывает возможность таких химических реакций, в процессе которых в зависимости от условий I, р и химической природы другого реагента) от атома отделяется или к нему притягивается то или иное количество электронов. Факты показывают, что проявление металлических свойств в простейшем виде связано с отдачей электронов, а неметаллических— с приобретением. Поскольку атом химического элемента способен в принципе как к приему, так и к отдаче валентных электронов, то вполне понятным становится сосуществование в атоме металлических и неме- [c.127]
Наличие и взаимодействие этих сил обеспечивает, во-первых, устойчивое существование атома, во-вторых, открывает возможность таких химических реакций, в процессе которых в зависимости от условий I, р и химической природы другого реагента) от атома отделяется или к нему притягивается то или иное количество электронов. Факты показывают, что проявление металлических свойств в простейшем виде связано с отдачей электронов, а неметаллических— с приобретением. Поскольку атом химического элемента способен в принципе как к приему, так и к отдаче валентных электронов, то вполне понятным становится сосуществование в атоме металлических и неме- [c.127]
Со времен М. В. Ломоносова ученых занимал вопрос о причинах химического сродства между элементами, о природе сил, вызывающих образование химических соединений. Но решить этот вопрос удалось только на основе теории строения ато.ма. Оказалось, что наибольшее значение для возникновения химической связи имеют силы взаимодействия между электронами атомов, их движения и перегруппировки. При этом особенно ваншую роль играют валентные электроны, т. е. внешние, наиболее подвижные электроны незавершенных слоев атомов. Электроны же внутренних, завершенных энергетических уровней не участвуют в осуществлении химической связи. Поведение элемента в реакции зависит от свойств его атома терять свои электроны или приобретать чу>кие, от прочности связи между валентными электронами и атомом. [c.55]
При этом особенно ваншую роль играют валентные электроны, т. е. внешние, наиболее подвижные электроны незавершенных слоев атомов. Электроны же внутренних, завершенных энергетических уровней не участвуют в осуществлении химической связи. Поведение элемента в реакции зависит от свойств его атома терять свои электроны или приобретать чу>кие, от прочности связи между валентными электронами и атомом. [c.55]
После открытия электронов немецкий физико-химик Рихард Абегг в 1904 г. предположил, что, поскольку инертные газы не образуют химических соединений, то они должны иметь устойчивую электронную конфигурацию. Ученый утверждал, что химическая реакция представляет собой взаимодействие между электронами, а ядра атомов при этом остаются без изменения. Равным образом электронное строение должно определять валентность элементов в зависимости от того, сколько электронов может отдать или принять атом. Таким образом, речь шла об электронных оболочках, которые должны содержать определенное количество электронов. [c.106]
[c.106]
Теория типов имела, однако, и несомненные заслуги. В связи с ней были созданы предпосылки для возникновения теории химического строения учение о валентности элементов и представление о цепеобразном соединении атомов друг с другом. В самом деле, уже из формул четырех основных типов, предложенных Жераром, следует, что водород и хлор могут соединяться с одним атомом водорода, кислород —с двумя, а азот — с тремя. Такие же выводы можно было бы сделать и для других элементов, в том числе и для углерода. Приняв атом водорода за единицу, можно считать, что сам водород и галогены — элементы одноатомные (или, как стали говорить позднее, одновалентные), кислород и сера — двухатомные (двухвалентные), азот и фосфор — трехатомные (трехвалентные), углерод — четьцрехатомен (четырехвалентен). Атомность элементов отождествлялась с числом единиц сродства, которыми обладали их атомы. Соединение двух атомов, образование химической связи происходит, как тогда говорили, в результате взаимной нейтрализации ( потребления ) двух единиц сродства, по одной от каждого атома. Рассматривая формулы углеводородов и их производаых, [c.56]
Рассматривая формулы углеводородов и их производаых, [c.56]
Итак, каждый эле.мент характеризуется двумя основными свойства.ми — весом его атомов и валентностью. Но чем же определяется валентность атома Как устроен ато.м Что общего и какие различия в строении атомов разных элементов — На все эти вопросы ответа ещё не было. Ко времени вступления Менделеева в науку химикам были известны 64 элемента. Поиски новых элементов проводились бессисте.мно, открытия их совершались случайно, и было не ясно, есть ли вообще конец открытию новых элементов. [c.65]
Свойства и получение. Атом углерода в валентном состоя-ВИИ s 2spxPgPz имеет четыре, неспаренных электрона и во внешнем электронном слое отсутствуют как свободные квантовые ячейки, так и неподеленные электронные пары (только для одного элемента, кроме углерода,— водорода характерно состояние атома, имеющее з ти особенности). Такое электронное строение атома и расположение углерода посередине шкалы электроотрицательностей обусловливают уникальные свойства данного элемента, благодаря которым существует огромное многообразие органических соединений. [c.352]
[c.352]
Строение электронных уровней атомов железа, кобальта и никеля характеризуется почти полной достройкой -подуровня предпоследнего электронного уровня шесть электронов — у железа, семь—у кобальта и восемь — у никеля. Заполнение -подуровня у атомов этих элементов сказывается на уменьшении окислительного числа, поскольку на -подуровне содержится меньшее число непарных электронов. Поэтому если марганцу свойственна еще степень окисления 4-7, то атом железа может отдавать не более шести электронов и, следовательно, его степень окисления не может быть больше 4-6. Окислительное число кобальта не может быть больше 4-5, а никеля 4-4, Таким образом, у атомов этих элементов нельзя считать все электроны незаполненных уровней валентными. Одновременно с повышением устойчивости почти заполненного -подуровня снижается склонность этих элементов к образованию металлоподобных соединений с электронной проводимостью. Электрической проводимостью такого типа обладают только силиды этих металлов. [c.297]
[c.297]
В чем причина появления оптической активности у некоторых органических вешеста Ответ на этот вопрос был дан на основании тетраэдрической теории Я. Вант-Гоффа и Л. Ле-Беля (1874). Согласно этой теории оптической активностью обладают соединения, молекулы которых имеют асимметрическое строение. В состав таких молекул входит асимметрический атом углерода, т. е. атом, у которого все четыре валентности затрачены на соединение с различными атомами или группами атомов (рис. 2.3). Такой атом не имеет ни одного элемента симметрии — ни центров, ни осей, ни плоскости. [c.217]
Подобная близость свойств объясняется тем, что в высшей степени окисления атом элемента, находящегося в третьем периоде (в главной подгруппе) и атомы элементов побочной подгруппы приобретают сходное электронное строение. Например, атом хрома имеет электронную конфигурацию 1з Когда хром находится в степени окисления 4-6 (например, в оксиде СгОз), шесть электронов его атома (пять М- и один 4б-электрон) вместе с валентными электронами соседних атомов (в случае СгОз — атомов кислорода) образуют общие электронные пары, осуществляющие химические связи.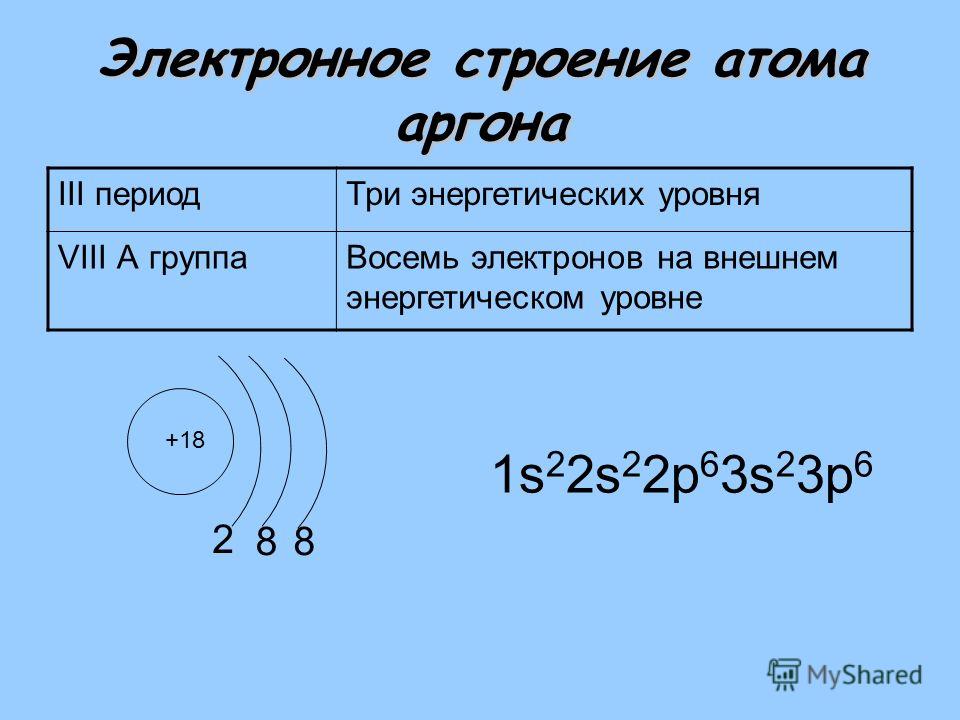 Остальные электроны, непосредственно не участвующие в образовании связей, имеют конфигурацию отвечающую электронной структуре благородного газа. Аналогично у атома серы, находящегося в степени окисления -Ьб (например, в триокси-де серы ЗОз), шесть электронов участвуют в образовании ковалентных связей, а конфигурация остальных (1з 28 р ) также соответствует электронной структуре благородного газа. Короче говоря, сходство в свойствах соединений элементов побочной подгруппы и элемента третьего периода той же группы обусловлено тем, что их ионы, отвечающие высшим степеням окисления, являются электронными анапогами. Это легко видеть из данных табл. 21.1. [c.497]
Остальные электроны, непосредственно не участвующие в образовании связей, имеют конфигурацию отвечающую электронной структуре благородного газа. Аналогично у атома серы, находящегося в степени окисления -Ьб (например, в триокси-де серы ЗОз), шесть электронов участвуют в образовании ковалентных связей, а конфигурация остальных (1з 28 р ) также соответствует электронной структуре благородного газа. Короче говоря, сходство в свойствах соединений элементов побочной подгруппы и элемента третьего периода той же группы обусловлено тем, что их ионы, отвечающие высшим степеням окисления, являются электронными анапогами. Это легко видеть из данных табл. 21.1. [c.497]
Бор – первый р-элемент в периодической системе элементов. Строение внешней электронной оболочки его атома в невозбужлениом состоянии 2х 2р . Возбуждение переводит атом в состояние 2f 2p p и далее в ip -тбридное валентное состояние, в котором орбитали расположены под углом 120. Этому состоянию отвечает структура соединений бора, в которых атом В связан с тремя другими атомами (три Образование донорно-акцепторной ж-связи (акцептор – атом бора) стабилизирует ip -гибридное состояние. Это приводит к уменьшению межатомных расстояний В-Г, В-О и др. Благодаря наличию в небольшом по размеру атоме бора свободной орбитали бор – один из сильнейших акцепторов неподеленных электронных пар. Многие соединения бора являются кислотами Льюиса, они энергично взаимодействуют с основаниями Льюиса, например [c.343]
Это приводит к уменьшению межатомных расстояний В-Г, В-О и др. Благодаря наличию в небольшом по размеру атоме бора свободной орбитали бор – один из сильнейших акцепторов неподеленных электронных пар. Многие соединения бора являются кислотами Льюиса, они энергично взаимодействуют с основаниями Льюиса, например [c.343]
Свойства и получение. Внешняя электронная оболочка атома углерода в основном и возбужденном состоянии имеет строение 2s 2p и s2pxPfPi. Таким образом, в валентном состоянии атом углерода имеет четыре неспарениых электрона и во внешнем электронном слое отсутствуют как свободные атомные орбитали, так и неподеленные электронные пары (только для одного элемента, кроме углерода, – водорода характерно подобное состояние атома). Такое электронное строение атома углерода обусловливает две характерных его особенности возможность образовывать четыре ковалентные связи и неспособность к донорно-акцепторному взаимодействию. [c.363]
Теории валентности и стереохимия развивались в прошлом столетии в очень тесной связи, так что достижения одной обычно были результатом успехов другой. В 1852 г. Фрэнкленд предложил концепцию валентности и показал, что элементы при образовании соединений реагируют с определенными количествами других элементов, и эти количества теперь называют эктшвалентными. Кекуле в 1858 г. и Кольбе в 1859 г. расширили представление о валентности и постулировали, что атом углерода четырехвалентен. В 1858 г. Кекуле предположил, что атомы углерода соединяются друг с другом в неограниченном числе, образуя цепи в том же году Купер ввел концепцию валентной связи и нарисовал первые структурные формулы. Термин химическое строе-ние ввел в 1861 г. Бутлеров, который отметил важность написания простейших формул соединений, показывающих, как соединены атомы в молекулах. Он также установил, что свойства соединений определяются их молекулярным строением, п если известно строение, то можно предсказать свойства. Однако только в 1874 г. был сделан первый основной шаг к наглядному представлению молекулярного строения в трех измерениях. В этом же году Вант-Гофф и ле Бель независимо друг от друга постулировали тетраэдрическое расположение четырех связей атома углерода и таким образом дали возможность классической органической стереохимии по крайней мере.
В 1852 г. Фрэнкленд предложил концепцию валентности и показал, что элементы при образовании соединений реагируют с определенными количествами других элементов, и эти количества теперь называют эктшвалентными. Кекуле в 1858 г. и Кольбе в 1859 г. расширили представление о валентности и постулировали, что атом углерода четырехвалентен. В 1858 г. Кекуле предположил, что атомы углерода соединяются друг с другом в неограниченном числе, образуя цепи в том же году Купер ввел концепцию валентной связи и нарисовал первые структурные формулы. Термин химическое строе-ние ввел в 1861 г. Бутлеров, который отметил важность написания простейших формул соединений, показывающих, как соединены атомы в молекулах. Он также установил, что свойства соединений определяются их молекулярным строением, п если известно строение, то можно предсказать свойства. Однако только в 1874 г. был сделан первый основной шаг к наглядному представлению молекулярного строения в трех измерениях. В этом же году Вант-Гофф и ле Бель независимо друг от друга постулировали тетраэдрическое расположение четырех связей атома углерода и таким образом дали возможность классической органической стереохимии по крайней мере.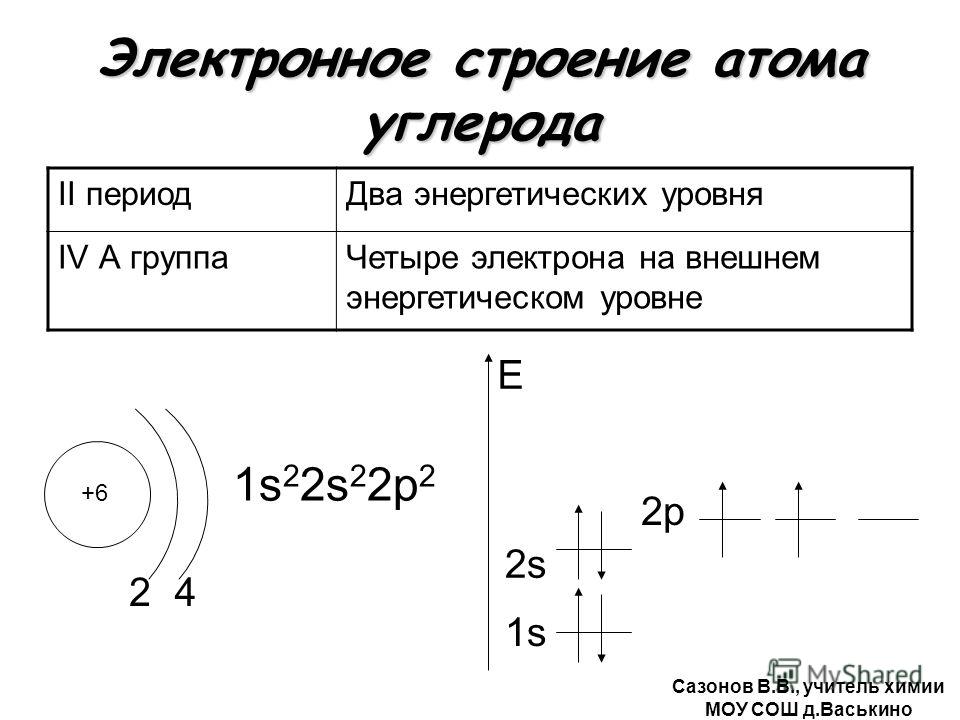 на двадцать лет опередить неорганическую стереохимию. [c.191]
на двадцать лет опередить неорганическую стереохимию. [c.191]
Элементы фтор F, хлор С1, бром Вг, иод I и астат At составляют V1IA группу Периодической системы Д. И. Менделеева. Групповое название этих элементов — галогены. Строение валентного электронного уровня атомов галогенов одинаково ns np атом фтора не имеет /г -подуровня, поэтому он образует только одну ковалентную связь. Фтор — самый электроотрицательный элемент и встреч ается только в состояниях Р- и F . [c.219]
Элементы подгруппы титана относятся к числу переходных — они содержат недостроенную электронную оболочку п—Электронная подкладка у атомов таких элементов, т. е. оболочка, предшествующая слою валентных электронов, относится к 8-электронному типу (имеет благороднотазовое строение). Как известно, в подгруппах таких элементов, ввиду жесткости (малой деформируемости) 8-злект-ронных оболочек (в отличие от 18-электронных, характерных для ностпереходных элементов), с ростом атомного номера и радиуса ато-ма (иона) наблюдается уменьшение поляризующего действия. Наиболее сильным поляризующим действием (при прочих равных усло виях) обладает титан из-за малого размера атома (иона) в этой подгруппе он сильнее всего удерживает валентные электроны и поэтому относительно легко может быть переведен в состояние с более низкой степенью окисления, чем обычное валентное состояние, характеризуемое степенью окисления +4. [c.105]
Наиболее сильным поляризующим действием (при прочих равных усло виях) обладает титан из-за малого размера атома (иона) в этой подгруппе он сильнее всего удерживает валентные электроны и поэтому относительно легко может быть переведен в состояние с более низкой степенью окисления, чем обычное валентное состояние, характеризуемое степенью окисления +4. [c.105]
Урок «Строение атома. Опыт Резерфорда», (физика, 8 класс)
Урок физики 8 класс
Строение атома. Опыт Резерфорда
Подготовила и провела
учитель физики МОУ «Луховский лицей»
Смирнова С.Г.
Цели урока: обеспечить усвоение учащимися знаний о строении атома и атомного ядра; дать представление о научных экспериментах, которые привели к построению планетарной модели атома; учить применять полученные знания на практике: научить пользоваться периодической системой химических элементов Менделеева для определения состава атома; реализовать межпредметные связи физика- химия; расширить кругозор учащихся.
Организационный момент
Фронтальный опрос по пройденной теме, актуализация знаний для изучения нового материала
– Какой физической величиной характеризуют действие одного тела на другое?
– Почему мы считаем, что электрический заряд- физическая величина?
– Как называется единица физического заряда?
– Опишите опыт, иллюстрирующий, что заряд тела можно многократно делить на порции
– Как называется наименьшая порция заряда?
– Может ли существовать заряд без частицы?
– Частица без заряда?
– Чему равен заряд электрона?
– Можно ли «снять» заряд с электрона?
– Перечислите известные вам микрочастицы, имеющие заряд, и не имеющие его
Изучение нового материала
Учитель. После того как был открыт электрон, встал вопрос: где искать электроны. Где было бы естественным их искать?
Ученики: может быть, в атомах?
Учитель. Это верное предположение. И эпиграфом к нашему уроку я взяла слова:
И эпиграфом к нашему уроку я взяла слова:
Еще, быть может, каждый атом-
Вселенная, где сто планет,
Там все, что есть, в объеме сжатом,
Но также то, чего здесь нет
Разные ученые предложили разные модели строения атома. Рассмотрим модель Томсона (слайд с диска «Физика -9», урок «Строение атома»)
Модель Томсона. Отрицательный заряд равно распределен внутри положительного атома. Электроны- изюмины в кексе
Проверить правильность этой модели взялся Э. Резерфорд. Он догадался, что атом каким-то образом нужно «разбить», чтобы заглянуть внутрь. Как вы думаете, возможно ли это? (выслушиваются предложения учащихся)
Учитель. Если через атомы пролетают очень маленькие, сравнимые по размерам с самими атомами, заряженные частицы, то по их движению можно судить о строении атома. Встал вопрос: чем обстрелять атом? (выслушиваются предложения учащихся)
Учитель. Оказалось, что есть вещества (уран, радий и др.), из которых непрерывно вылетают положительные частицы, масса которых очень мала, а скорость велика, 15000 км/с. Расстояние от Земли до Луны они пролетели бы за 25 сек. Но как заметить альфа-частицу? Воспользовались экраном, покрытым особым составом, который светился, когда на него попадали частицы. Каждая частица, попавшая на экран, создавала на нем маленькую вспышку (частицы можно было обнаружить и сосчитать)
Расстояние от Земли до Луны они пролетели бы за 25 сек. Но как заметить альфа-частицу? Воспользовались экраном, покрытым особым составом, который светился, когда на него попадали частицы. Каждая частица, попавшая на экран, создавала на нем маленькую вспышку (частицы можно было обнаружить и сосчитать)
Затем перед экраном была поставлена тончайшая золотая фольга толщиной 0,001 мкм (3300 слоев атомов золота)
Результаты опыта Резерфорда
Учитель. 1-й результат: почти все альфа-частицы пролетели через все 3300 слоев атомов золота так, как будто на их пути ничего не было. Как бы вы объяснили этот результат?
Учащиеся в ходе рассуждений находят ответ: в атоме есть пустоты, не заполненные частицами вещества
Учитель. Как велики эти пустоты?
Учащиеся доходят до верного ответа, что пустоты составляют значительную часть атома, иначе альфа-частицы не пролетели бы прямо сквозь пластину, а разбрасывались бы в разные стороны.
Учитель. 2-й результат: небольшая часть частиц отклонилась от своего пути, когда частицы прошли сквозь пластину. Как бы вы объяснили этот результат?
Учащиеся. Те частицы, которые отклонились, очевидно прошли около каких-то заряженных тел, но далеко от них, т.к. притяжение или отталкивание было не очень сильным
Учитель. Верно,молодцы.3-й результат: несколько альфа-частиц отклонились на большой угол, а некоторые из них (33 из 150000) были отброшены назад. Как бы вы объяснили этот результат?
Учащиеся. Эти частицы налетели на другую частицу, которая ее оттолкнула
Учитель: Как была заряжена та частица?
Ученик. Если оттолкнула, значит была заряжена так же как и альфа- частица, т.е. положительно
Учитель. При взаимодействии двух тел какое из них больше изменит скорость?
Ученик. То, у которого масса меньше, следовательно, масса альфа-частицы меньше массы той, которой она была отброшена.
Учитель. Молодцы. Вы сделали правильные выводы из результатов опыта Резерфорда.
Молодцы. Вы сделали правильные выводы из результатов опыта Резерфорда.
Итак, опыт Резерфорда показал, что внутри атома имеются положительно заряженная частица- ядро. Именно от ядра и оттолкнулись те немногие частицы, которые пролетали вблизи от него. На большом расстоянии от ядра в атоме находятся отрицательно заряженные частицы- электроны. Они притягиваются, но не приближаются вплотную к ядру, потому что вращаются вокруг него
Закрепление и углубление изученного материала. Составляется таблица строения атома, учащиеся зарисовывают в тетрадь
Строение атома (планетарная модель по Резерфорду) | ||
ядро(99,98% массы атома) | оболочка атома ( R=0, 00000001см) | |
протоны | нейтроны | электроны (0,02% от массы атома) |
Работа с таблицей Д. И. Менделеева
И. Менделеева
Учитель. Пользуясь таблицей Д.И. Менделеева, научимся определять строение атома любого химического элемента
Число протонов в ядре равно порядковому номеру элемента, для бора 5
Массовое число, округленное до целых, определяет число всех частиц в ядре (протонов и нейтронов), 10, 811= 11
11-5=6-число нейтронов в ядре
В нейтральном атоме электронов вращается вокруг ядра столько, сколько в ядре протонов, для атома бора 5
Тестовые задания
- Заряд ядра атома азота равен:
а) 7 б) 13 в) 4 г) 29 д) 11 - Число протонов в ядре атома криптона:
а) 36 б) 17 в) 4 г) 31 д) 6 - Число нейтронов в ядре атома цинка:
а) 8 б) 35 в)11 г)30 д)4 - Число электронов в атоме железа:
а) 11 б)8 в)56 г)26 д)30
Поменяйтесь заданиями с соседом по парте, проверим ответы:
- Заряд ядра атома азота равен:
а) 7 б) 13 в) 4 г) 29 д) 11 - Число протонов в ядре атома криптона:
а) 36 б) 17 в) 4 г) 31 д) 6 - Число нейтронов в ядре атома цинка:
а) 8 б) 35 в)11 г)30 д)4 - Число электронов в атоме железа:
а) 11 б)8 в)56 г)26 д)30
Это интересно!
1)m (атома) =m (ядра)- вся масса атома сосредоточена в ядре!
2) (атома) \ r (ядра) = 100000- сплошная пустота!
3) Если все частицы, из которых вы состоите, сложить вплотную, то вы уменьшитесь в 100000 раз, и под микроскопом вас не будет видно. А масса- те же 50 кг!. Вот это кроха!. Но самое потрясающее то, что объекты с такой чудовищной плотностью нашлись в природе. Не на Земле, не в солнечной системе. Это нейтронные звезды, расположенные в разных местах Вселенной. Они состоят из одних ядер, уложенных вплотную.
А масса- те же 50 кг!. Вот это кроха!. Но самое потрясающее то, что объекты с такой чудовищной плотностью нашлись в природе. Не на Земле, не в солнечной системе. Это нейтронные звезды, расположенные в разных местах Вселенной. Они состоят из одних ядер, уложенных вплотную.
4)Чайная ложка вещества нейтронной звезды весит 100 млрд тонн!
5)Если бы плотность Земли уменьшилась до плотности нейтронной звезды, то в поперечнике осталось бы не более 100 метров
6)Поперек ногтя мизинца могло бы уместиться 100000000 атомов
4.Подведение итогов урока
5. Задание на дом: п. 29, нарисовать схему строения атомов лития, бериллия
Химическая связь — основные виды, типы и характеристики
Статья находится на проверке у методистов Skysmart.
Если вы заметили ошибку, сообщите об этом в онлайн-чат (в правом нижнем углу экрана).
Химическая связь и строение вещества
Все системы стремятся к равновесию и к уменьшению свободной энергии — так гласит один из постулатов химической термодинамики. Атомы, взаимодействующие в молекуле вещества, тоже подчиняются этому закону. Они стремятся образовать устойчивую конфигурацию — 8-электронную или 2-электронную внешнюю оболочку. Этот процесс взаимодействия называется химической связью, благодаря ему получаются молекулы и молекулярные соединения.
Атомы, взаимодействующие в молекуле вещества, тоже подчиняются этому закону. Они стремятся образовать устойчивую конфигурацию — 8-электронную или 2-электронную внешнюю оболочку. Этот процесс взаимодействия называется химической связью, благодаря ему получаются молекулы и молекулярные соединения.
| Химическая связь — это взаимодействие между атомами в молекуле вещества, в ходе которого два электрона (по одному от каждого атома) образуют общую электронную пару либо электрон переходит от одного атома к другому. |
Как понятно из определения химической связи, при взаимодействии двух атомов один из них может притянуть к себе внешние электроны другого. Эта способность называется электроотрицательностью (ЭО). Атом с более высокой электроотрицательностью (ЭО) при образовании химической связи с другим атомом может вызвать смещение к себе общей электронной пары.
Важно!
Существует несколько систем измерения ЭО, но пользоваться для расчетов можно любой из них. Для образования химической связи важно не конкретное значение ЭО, а разница между этими показателями у двух атомов.
Для образования химической связи важно не конкретное значение ЭО, а разница между этими показателями у двух атомов.
Механизм образования химической связи
Существует два механизма взаимодействия атомов:
обменный — предполагает выделение по одному внешнему электрону от каждого атома и соединение их в общую пару;
донорно-акцепторный — происходит, когда один атом (донор) выделяет два электрона, а второй атом (акцептор) принимает их на свою свободную орбиталь.
Независимо от механизма химическая связь между атомами сопровождается выделением энергии. Чем выше ЭО атомов, т. е. их способность притягивать электроны, тем сильнее и этот энергетический всплеск.
Энергией связи называют ту энергию, которая выделяется при взаимодействии атомов. Она определяет прочность химической связи и по величине равна усилию, необходимому для ее разрыва. |
Также на прочность влияют следующие показатели:
Длина связи — расстояние между ядрами атомов. С уменьшением этого расстояния растет энергия связи и увеличивается ее прочность.
Кратность связи — количество электронных пар, появившихся при взаимодействии атомов. Чем больше это число, тем выше энергия и, соответственно, прочность связи.
На примере химической связи в молекуле водорода посмотрим, как меняется энергия системы при сокращении расстояния между ядрами атомов. По мере сближения ядер электронные орбитали этих атомов начинают перекрывать друг друга, в итоге появляется общая молекулярная орбиталь. Неспаренные электроны через области перекрывания смещаются от одного атома в сторону другого, возникают общие электронные пары. Все это сопровождается нарастающим выделением энергии. Сближение происходит до тех пор, пока силу притяжения не компенсирует сила отталкивания одноименных зарядов.
Основные типы химических связей
Различают четыре вида связей в химии: ковалентную, ионную, металлическую и водородную. Но в чистом виде они встречаются редко, обычно имеет место наложение нескольких типов химических связей. Например, в молекуле фосфата аммония (NH4)3PO4присутствует одновременно ионная связь между ионами и ковалентная связь внутри ионов.
Также отметим, что при образовании кристалла от типа связи между частицами зависит, какой будет кристаллическая решетка. Если это ковалентная связь — образуется атомная решетка, если водородная — молекулярная решетка, а если ионная или металлическая — соответственно, будет ионная или металлическая решетка. Таком образом, влияя на тип кристаллической решетки, химическая связь определяет и физические свойства вещества: твердость, летучесть, температуру плавления и т. д.
Основные характеристики химической связи:
насыщенность — ограничение по количеству образуемых связей из-за конечного числа неспаренных электронов;
полярность — неравномерная электронная плотность между атомами и смещение общей пары электронов к одному из них;
направленность — ориентация связи в пространстве, расположение орбиталей атомов под определенным углом друг к другу.

Ковалентная связь
Как уже говорилось выше, этот тип связи имеет два механизма образования: обменный и донорно-акцепторный. При обменном механизме объединяются в пару свободные электроны двух атомов, а при донорно-акцепторном — пара электронов одного из атомов смещается к другому на его свободную орбиталь.
| Ковалентная связь — это процесс взаимодействия между атомами с одинаковыми или близкими радиусами, при котором возникает общая электронная пара. Если эта пара принадлежит в равной мере обоим взаимодействующим атомам — это неполярная связь, а если она смещается к одному из них — это полярная связь. |
Как вы помните, сила притяжения электронов определяется электроотрицательностью атома. Если у двух атомов она одинакова, между ними будет неполярная связь, а если один из атомов имеет большую ЭО — к нему сместится общая электронная пара и получится полярная химическая связь.
Важно!
В зависимости от того, сколько получилось электронных пар, химические связи могут быть одинарными, двойными или тройными.
Ковалентная неполярная связь образуется в молекулах простых веществ, неметаллов с одинаковой ЭО: Cl2, O2, N2, F2 и других.
Посмотрим на схему образования этой химической связи. У атомов водорода есть по одному внешнему электрону, которые и образуют общую пару.
Ковалентная полярная связь характерна для неметаллов с разным уровнем ЭО: HCl, NH3,HBr, H2O, H2S и других.
Посмотрим схему такой связи в молекуле хлороводорода. У водорода имеется один свободный электрон, а у хлора — семь. Таким образом, всего есть два неспаренных электрона, которые соединяются в общую пару. Поскольку в данном случае ЭО выше у хлора, эта пара смещается к нему.
Другой пример — молекула сероводорода H2S. В данном случае мы видим, что каждый атом водорода имеет по одной химической связи, в то время как атом серы — две. Количество связей определяет валентность атома в конкретном соединении, поэтому валентность серы в сероводороде — II.
В данном случае мы видим, что каждый атом водорода имеет по одной химической связи, в то время как атом серы — две. Количество связей определяет валентность атома в конкретном соединении, поэтому валентность серы в сероводороде — II.
Число связей, которые могут быть у атома в молекуле вещества, называется валентностью. |
Характеристики ковалентной связи:
- насыщена,
- направлена,
- имеет полярность.
Ионная связь
Как понятно из названия, данный тип связи основан на взаимном притяжении ионов с противоположными зарядами. Он возможен между веществами с большой разницей ЭО — металлом и неметаллом. Механизм таков: один из атомов отдает свои электроны другому атому и заряжается положительно. Второй атом принимает электроны на свободную орбиталь и получает отрицательный заряд. В результате этого процесса образуются ионы.
| Ионная связь — это такое взаимодействие между атомами в молекуле вещества, итогом которого становится образование и взаимное притяжение ионов. |
Разноименно заряженные ионы стремятся друг к другу за счет кулоновского притяжения, которое одинаково направлено во все стороны. Благодаря этому притяжению образуются ионные кристаллы, в решетке которых заряды ионов чередуются. У каждого иона есть определенное количество ближайших соседей — оно называется координационным числом.
Обычно ионная связь появляется между атомами металла и неметалла в таких соединениях, как NaF, CaCl2, BaO, NaCl, MgF2, RbI и других. Ниже схема ионной связи в молекуле хлорида натрия.
Важно!
Все соли образованы с помощью ионных связей, поэтому в задачах, где нужно определить тип химической связи в веществах, в качестве подсказки можно использовать таблицу растворимости.
Характеристики ионной связи:
Ковалентная и ионная связь в целом похожи, и одну из них можно рассматривать, как крайнее выражение другой. Но все же между ними есть существенная разница. Сравним эти виды химических связей в таблице.
Ковалентная связь | Ионная связь |
|---|---|
Характеризуется появлением электронных пар, принадлежащих обоим атомам. | Характеризуется появлением и взаимным притяжением ионов. |
Общая пара электронов испытывает притяжение со стороны обоих ядер атомов. | Ионы с противоположными зарядами подвержены кулоновскому притяжению. |
Имеет направленность и насыщенность. | Ненасыщенна и не имеет направленности. |
Количество связей, образуемых атомом, называется валентностью. | Количество ближайших соседей атома называется координационным числом. |
Образуется между неметаллами с одинаковой или не сильно отличающейся ЭО. | Образуется между металлами и неметаллами — веществами со значимо разной ЭО. |
Металлическая связь
Отличительная особенность металлов в том, что их атомы имеют достаточно большие радиусы и легко отдают свои внешние электроны, превращаясь в положительно заряженные ионы (катионы). В итоге получается кристаллическая решетка, в узлах которой находятся ионы, а вокруг беспорядочно перемещаются электроны проводимости, образуя «электронное облако» или «электронный газ».
Свободные электроны мигрируют от одного иона к другому, временно соединяясь с ними и снова отрываясь в свободное плавание. Этот механизм по своей природе имеет сходство с ковалентной связью, но взаимодействие происходит не между отдельными атомами, а в веществе.
| Металлическая связь — это взаимодействие положительных ионов металлов и отрицательно заряженных электронов, которые являются частью «электронного облака», рассеянного по всему объему вещества. |
Наличие такого «электронного облака», которое может прийти в направленное движение, обусловливает электропроводность металлов. Другие их качества — пластичность и ковкость, объясняются тем, что ионы в кристаллической решетке легко смещаются. Поэтому металл при ударном воздействии способен растягиваться, но не разрушаться.
Характеристики металлической связи:
ненаправленность,
делокализованный характер,
многоэлектронность.
Металлическая связь присуща как простым веществам — таким как Na, Ba, Ag, Cu, так и сложным сплавам — например, AlCr2, CuAl11Fe4, Ca2Cu и другим.
Схема металлической связи:
M — металл,
n — число свободных внешних электронов.
К примеру, у железа в чистом виде на внешнем уровне есть два электрона, поэтому его схема металлической связи выглядит так:
Обобщим все полученные знания. Таблица ниже описывает кратко химические связи и строение вещества.
2.2: Структура атома и как мы ее представляем
Развитие современной атомной теории многое раскрыло о внутренней структуре атомов. Стало известно, что атом содержит очень маленькое ядро, состоящее из положительно заряженных протонов и незаряженных нейтронов, окруженное гораздо большим объемом пространства, содержащим отрицательно заряженные электроны. Ядро содержит большую часть массы атома, потому что протоны и нейтроны намного тяжелее электронов, тогда как электроны занимают почти весь объем атома.Диаметр атома составляет порядка 10 −10 м, тогда как диаметр ядра примерно 10 −15 м – примерно в 100 000 раз меньше. Чтобы получить представление об их относительных размерах, рассмотрим следующее: если бы ядро было размером с чернику, атом был бы размером с футбольный стадион (рисунок \ (\ PageIndex {1} \)).
Чтобы получить представление об их относительных размерах, рассмотрим следующее: если бы ядро было размером с чернику, атом был бы размером с футбольный стадион (рисунок \ (\ PageIndex {1} \)).
Рисунок \ (\ PageIndex {1} \): Если бы атом можно было расширить до размеров футбольного стадиона, ядро было бы размером с одну чернику.(в середине фото: модификация работы «babyknight» / Wikimedia Commons; право на кредит: изменение работы Паксона Вельбера).
Атомы и составляющие их протоны, нейтроны и электроны чрезвычайно малы. Например, атом углерода весит менее 2 \ (\ times \) 10 −23 г, а электрон имеет заряд менее 2 \ (\ times \) 10 −19 C (кулонов). При описании свойств крошечных объектов, таких как атомы, мы используем соответственно небольшие единицы измерения, такие как атомная единица массы (а.е.м.) и фундаментальная единица заряда (е).Первоначально аму определяли на основе водорода, самого легкого элемента, а затем – кислорода. С 1961 года он был определен в отношении наиболее распространенного изотопа углерода, атомам которого приписываются массы ровно 12 а.е.м. (Этот изотоп известен как «углерод-12», как будет обсуждаться позже в этом модуле.) Таким образом, одна а.е.м. составляет ровно \ (1/12 \) массы одного атома углерода-12: 1 а.е.м. = 1,6605 \ ( \ раз \) 10 −24 г. (Дальтон (Да) и единая атомная единица массы (u) являются альтернативными единицами, эквивалентными аму.) Фундаментальная единица заряда (также называемая элементарным зарядом) равна величине заряда электрона (e) с e = 1,602 \ (\ times \) 10 −19 C.
С 1961 года он был определен в отношении наиболее распространенного изотопа углерода, атомам которого приписываются массы ровно 12 а.е.м. (Этот изотоп известен как «углерод-12», как будет обсуждаться позже в этом модуле.) Таким образом, одна а.е.м. составляет ровно \ (1/12 \) массы одного атома углерода-12: 1 а.е.м. = 1,6605 \ ( \ раз \) 10 −24 г. (Дальтон (Да) и единая атомная единица массы (u) являются альтернативными единицами, эквивалентными аму.) Фундаментальная единица заряда (также называемая элементарным зарядом) равна величине заряда электрона (e) с e = 1,602 \ (\ times \) 10 −19 C.
Протон имеет массу 1,0073 а.е.м. и заряд 1+. Нейтрон – это немного более тяжелая частица с массой 1,0087 а.е.м. и нулевым зарядом; как следует из названия, он нейтрален. Электрон имеет заряд 1− и является гораздо более легкой частицей с массой около 0,00055 а.е.м. (потребуется около 1800 электронов, чтобы равняться массе одного протона.Свойства этих фундаментальных частиц сведены в Таблицу \ (\ PageIndex {1} \). (Наблюдательный студент может заметить, что сумма субатомных частиц атома не равна реальной массе атома: общая масса шести протонов, шести нейтронов и шести электронов составляет 12,0993 а.е.м., что немного больше, чем 12,00 а.е.м. реального углерода. 12 атома. Эта «недостающая» масса известна как дефект массы, и вы узнаете об этом в главе, посвященной ядерной химии.)
(Наблюдательный студент может заметить, что сумма субатомных частиц атома не равна реальной массе атома: общая масса шести протонов, шести нейтронов и шести электронов составляет 12,0993 а.е.м., что немного больше, чем 12,00 а.е.м. реального углерода. 12 атома. Эта «недостающая» масса известна как дефект массы, и вы узнаете об этом в главе, посвященной ядерной химии.)
| Имя | Расположение | Заряд (К) | Стоимость единицы | Масса (а.е.м.) | Масса (г) |
|---|---|---|---|---|---|
| электрон | вне ядра | \ (- 1.{−24} \) |
Число протонов в ядре атома – это его атомный номер (Z). Это определяющая черта элемента: его значение определяет идентичность атома. Например, любой атом, содержащий шесть протонов, является элементом углерода и имеет атомный номер 6, независимо от того, сколько нейтронов или электронов он может иметь. Нейтральный атом должен содержать одинаковое количество положительных и отрицательных зарядов, поэтому количество протонов равно количеству электронов.Следовательно, атомный номер также указывает количество электронов в атоме. Общее количество протонов и нейтронов в атоме называется его массовым числом (А). Таким образом, количество нейтронов – это разница между массовым числом и атомным номером: A – Z = количество нейтронов.
Это определяющая черта элемента: его значение определяет идентичность атома. Например, любой атом, содержащий шесть протонов, является элементом углерода и имеет атомный номер 6, независимо от того, сколько нейтронов или электронов он может иметь. Нейтральный атом должен содержать одинаковое количество положительных и отрицательных зарядов, поэтому количество протонов равно количеству электронов.Следовательно, атомный номер также указывает количество электронов в атоме. Общее количество протонов и нейтронов в атоме называется его массовым числом (А). Таким образом, количество нейтронов – это разница между массовым числом и атомным номером: A – Z = количество нейтронов.
\ [\ begin {align *}
\ ce {atomic \: number \ 🙁 Z) \: & = \: number \: of \: protons \\
mass \: number \ 🙁 A) \: & = \: число \: из \: протонов + число \: из \: нейтронов \\
AZ \: & = \: число \: из \: нейтронов}
\ end {align *} \]
Атомы электрически нейтральны, если они содержат одинаковое количество положительно заряженных протонов и отрицательно заряженных электронов. Когда количество этих субатомных частиц равно , а не , атом электрически заряжен и называется ионом. Заряд атома определяется следующим образом:
Когда количество этих субатомных частиц равно , а не , атом электрически заряжен и называется ионом. Заряд атома определяется следующим образом:
Заряд атома = количество протонов – количество электронов
Как будет обсуждаться более подробно позже в этой главе, атомы (и молекулы) обычно приобретают заряд, приобретая или теряя электроны. Атом, который получает один или несколько электронов, будет иметь отрицательный заряд и называется анионом. Положительно заряженные атомы, называемые катионами, образуются, когда атом теряет один или несколько электронов.Например, нейтральный атом натрия (Z = 11) имеет 11 электронов. Если этот атом потеряет один электрон, он станет катионом с зарядом 1+ (11-10 = 1+). Нейтральный атом кислорода (Z = 8) имеет восемь электронов, и если он получит два электрона, он станет анионом с зарядом 2− (8-10 = 2−).
Пример \ (\ PageIndex {1} \): состав атома
Йод – важный микроэлемент в нашем рационе; он необходим для выработки гормона щитовидной железы. Недостаток йода в рационе может привести к развитию зоба, увеличению щитовидной железы (Рисунок \ (\ PageIndex {2} \)).
Недостаток йода в рационе может привести к развитию зоба, увеличению щитовидной железы (Рисунок \ (\ PageIndex {2} \)).
Рисунок \ (\ PageIndex {2} \): (a) Недостаток йода в рационе может вызвать увеличение щитовидной железы, называемое зобом. (б) Добавление к соли небольшого количества йода, предотвращающего образование зоба, помогло устранить эту проблему в США, где потребление соли велико. (кредит а: модификация работы «Алмази» / Wikimedia Commons; кредит б: модификация работы Майка Моцарта)
Добавление небольшого количества йода к поваренной соли (йодированной соли) по существу устранило эту проблему для здоровья в Соединенных Штатах, но до 40% населения мира по-прежнему подвержены риску дефицита йода.Атомы йода добавляются в виде анионов, и каждый из них имеет заряд 1- и массовое число 127. Определите количество протонов, нейтронов и электронов в одном из этих анионов йода.
Решение
Атомный номер йода (53) говорит нам, что нейтральный атом йода содержит 53 протона в своем ядре и 53 электрона вне ядра. Поскольку сумма числа протонов и нейтронов равна массовому числу 127, число нейтронов равно 74 (127 – 53 = 74).Поскольку йод добавляется в виде аниона 1−, количество электронов равно 54 [53 – (1–) = 54].
Поскольку сумма числа протонов и нейтронов равна массовому числу 127, число нейтронов равно 74 (127 – 53 = 74).Поскольку йод добавляется в виде аниона 1−, количество электронов равно 54 [53 – (1–) = 54].
Упражнение \ (\ PageIndex {1} \)
Ион платины имеет массовое число 195 и содержит 74 электрона. Сколько протонов и нейтронов он содержит и каков его заряд?
- Ответ
78 протонов; 117 нейтронов; заряд 4+
Химические символы
Химический символ – это сокращение, которое мы используем для обозначения элемента или атома элемента.Например, ртуть обозначается символом Hg (Рисунок \ (\ PageIndex {3} \)). Мы используем один и тот же символ для обозначения одного атома ртути (микроскопический домен) или для обозначения контейнера из многих атомов элемента ртути (макроскопический домен).
Рисунок \ (\ PageIndex {3} \) : символ Hg представляет элемент ртуть независимо от количества; он может представлять один атом ртути или большое количество ртути. Изображение использовано с разрешения Википедии (пользователь: Materialscientist).
Изображение использовано с разрешения Википедии (пользователь: Materialscientist).
Символы для нескольких общих элементов и их атомов перечислены в Таблице \ (\ PageIndex {2} \). Некоторые символы являются производными от общего имени элемента; другие – это аббревиатуры имени на другом языке. Символы состоят из одной или двух букв, например H для водорода и Cl для хлора. Чтобы избежать путаницы с другими обозначениями, заглавными являются только первые буквы символа. Например, Co – это символ элемента кобальта, а CO – это обозначение соединения монооксида углерода, которое содержит атомы элементов углерода (C) и кислорода (O).Все известные элементы и их символы находятся в периодической таблице.
| Элемент | Обозначение | Элемент | Обозначение |
|---|---|---|---|
| алюминий | Al | утюг | Fe (из железа ) |
| бром | руб. | свинец | Пб (из свинца ) |
| кальций | Ca | магний | мг |
| углерод | С | ртуть | Hg (из гидраргирум ) |
| хлор | Класс | азот | N |
| хром | Cr | кислород | O |
| кобальт | Co | калий | К (из калия ) |
| медь | Cu (из меди ) | кремний | Si |
| фтор | F | серебро | Ag (из argentum ) |
| золото | Au (из aurum ) | натрия | Na (из натрия ) |
| гелий | He | сера | S |
| водород | H | банка | Sn (с олова ) |
| йод | I | цинк | Zn |
Традиционно первооткрыватель (или первооткрыватели) нового элемента дает ему имя. Однако до тех пор, пока название не будет признано Международным союзом теоретической и прикладной химии (IUPAC), рекомендуемое название нового элемента основано на латинских словах, обозначающих его атомный номер. Например, элемент 106 назывался уннилгексием (Unh), элемент 107 назывался unnilseptium (Uns), а элемент 108 назывался уннилоктиум (Uno) в течение нескольких лет. Эти элементы теперь названы в честь ученых или мест; например, элемент 106 теперь известен как seaborgium (Sg) в честь Гленна Сиборга, лауреата Нобелевской премии, который принимал активное участие в открытии нескольких тяжелых элементов.
Однако до тех пор, пока название не будет признано Международным союзом теоретической и прикладной химии (IUPAC), рекомендуемое название нового элемента основано на латинских словах, обозначающих его атомный номер. Например, элемент 106 назывался уннилгексием (Unh), элемент 107 назывался unnilseptium (Uns), а элемент 108 назывался уннилоктиум (Uno) в течение нескольких лет. Эти элементы теперь названы в честь ученых или мест; например, элемент 106 теперь известен как seaborgium (Sg) в честь Гленна Сиборга, лауреата Нобелевской премии, который принимал активное участие в открытии нескольких тяжелых элементов.
ИЮПАК
Посетите этот сайт, чтобы узнать больше об ИЮПАК, Международном союзе теоретической и прикладной химии, и изучить его периодическую таблицу.
Структура атома | Обзор биологии [видео]
Атомы – строительные блоки Вселенной; они составляют все, что вы видите вокруг себя. Но что составляет атом?
В самом центре атома находится ядро , которое состоит из маленьких частиц, называемых протонами и нейтронами . Протоны – очень маленькие положительно заряженные частицы, а нейтроны – нейтральные частицы, не имеющие заряда.
Протоны – очень маленькие положительно заряженные частицы, а нейтроны – нейтральные частицы, не имеющие заряда.
Атомы могут иметь только один протон или несколько. Группа атомов, каждая из которых имеет одинаковое количество протонов, называется элементом. Например, водород – это элемент с одним протоном в ядре, а углерод – это элемент с 6 протонами.
В общем, у атома будет определенное количество нейтронов в ядре, что означает, что атом не будет терять или приобретать нейтроны в течение очень долгого времени.Это называется стабильным атомом . Обычно в стабильном атоме равное количество нейтронов и протонов, но есть исключения. Чтобы найти массовое число элемента, вы складываете количество протонов и нейтронов вместе, так что протоны + нейтроны = массовое число. Это дает нам такие названия, как Углерод-12 или Углерод-14, которые представляют собой типы атомов углерода, используемые при датировании по углероду!
Вращающиеся вокруг положительно заряженного центра атома частицы с отрицательным зарядом называются электронами . Электроны притягиваются к положительному ядру, но они могут покинуть свою орбиту под действием внешней силы.
Электроны притягиваются к положительному ядру, но они могут покинуть свою орбиту под действием внешней силы.
У атома есть определенное количество электронов, вращающихся вокруг ядра. Если количество электронов равно количеству протонов, общий электрический заряд атома нейтрален. Если в атоме больше электронов, чем протонов, его заряд будет отрицательным. С меньшим количеством электронов, чем протонов, атом будет иметь положительный заряд.
Электроны определяют, как атомы взаимодействуют друг с другом. Атомы могут обмениваться электронами, образуя молекул , которые представляют собой частицы, состоящие из множества атомов.Вода состоит из двух атомов водорода и одного атома кислорода. Эти три атома имеют общие электроны.
Теперь, когда мы поговорили о различных частях атома, давайте резюмируем некоторые свойства атомов. Атомы имеют атомный номер, который представляет собой количество протонов в ядре. В периодической таблице и атомы расположены в порядке возрастания атомного номера. Заряд атома рассчитывается на основе разницы между количеством протонов в ядре и количеством электронов, вращающихся вокруг ядра.
Заряд атома рассчитывается на основе разницы между количеством протонов в ядре и количеством электронов, вращающихся вокруг ядра.
Обзор
Атом состоит из протонов, электронов и нейтронов. Количество электронов определяет, как атомы взаимодействуют друг с другом, и решает, является ли атом в целом положительным, отрицательным или нейтральным. Массовое число атома находится путем сложения количества протонов и нейтронов. И, наконец, заряд атома определяется количеством протонов и электронов в атоме.
Большое спасибо за просмотр, и увидимся в следующий раз!
Анализ структуры элементов
СПРАВОЧНАЯ ИНФОРМАЦИЯ:Изучение минералов требует знания атомов, молекулы, элементы и соединения.Скалы состоят из минералов. Минералы из элементов. Элементы состоят из молекул, а молекулы состоят из атомы.
Элементы состоят из очень мелких частиц
называется атомами. Атом – это наименьшая часть элемента, которая сохраняет все
характеристики элемента. Атомы состоят из протонов, нейтронов,
и электроны, которые состоят из основных строительных блоков материи,
лептоны и кварки. . Эти субатомные частицы лишены отчетливой
характеристики элементов.
Атомы состоят из протонов, нейтронов,
и электроны, которые состоят из основных строительных блоков материи,
лептоны и кварки. . Эти субатомные частицы лишены отчетливой
характеристики элементов.
Протоны и нейтроны состоят из различные комбинации кварков. Есть шесть различных типов кварки, известные как ароматы: верхний, нижний, очаровательный, странный, верхний и нижний. Протоны заряжены положительно, а нейтроны электрически нейтральны. Нейтроны и протоны находятся в ядре атома.
Электроны – это один из шести типов
лептоны. Электроны в элементах находятся в пространстве от
ядро в различных
расстояния называются атомными орбиталями .Каждая из орбиталей может содержать заданное количество
электронов, но в этой модели трудно описать, где находятся электроны.
можно найти. Водород имеет один электрон, который представляет
самый низкий уровень энергии. Неон с атомным номером 10 имеет
атомарная конфигурация 1s 2 2s 2 2p 6 . Неон – один из благородных газов, потому что на его внешних орбиталях достаточно
электроны должны быть полными. Однако некоторые элементы, такие как Магний имеют неоноподобную орбитальную структуру, за исключением того, что они имеют 2 электрона в одной трети
оболочка (1s 2 2s 2 2p 6 3s 2 ).
Третья оболочка магния не заполнена.
Неон – один из благородных газов, потому что на его внешних орбиталях достаточно
электроны должны быть полными. Однако некоторые элементы, такие как Магний имеют неоноподобную орбитальную структуру, за исключением того, что они имеют 2 электрона в одной трети
оболочка (1s 2 2s 2 2p 6 3s 2 ).
Третья оболочка магния не заполнена.
Большинство веществ, обнаруживаемых на Земле, обычно состоят из более одного атома. Когда два или более атома образуют химическую связь, они создают молекула. Молекула может состоять из двух или более атомов одного и того же элемента. (O 2 ) или атомов двух или более различных элементов (H 2 O). Когда два или более элемента объединяются, они образуют так называемое соединение. А Молекула – это наименьшая отдельная часть элемента или соединения.
В этой лабораторной работе студенты будут рассматривать галит (поваренную соль).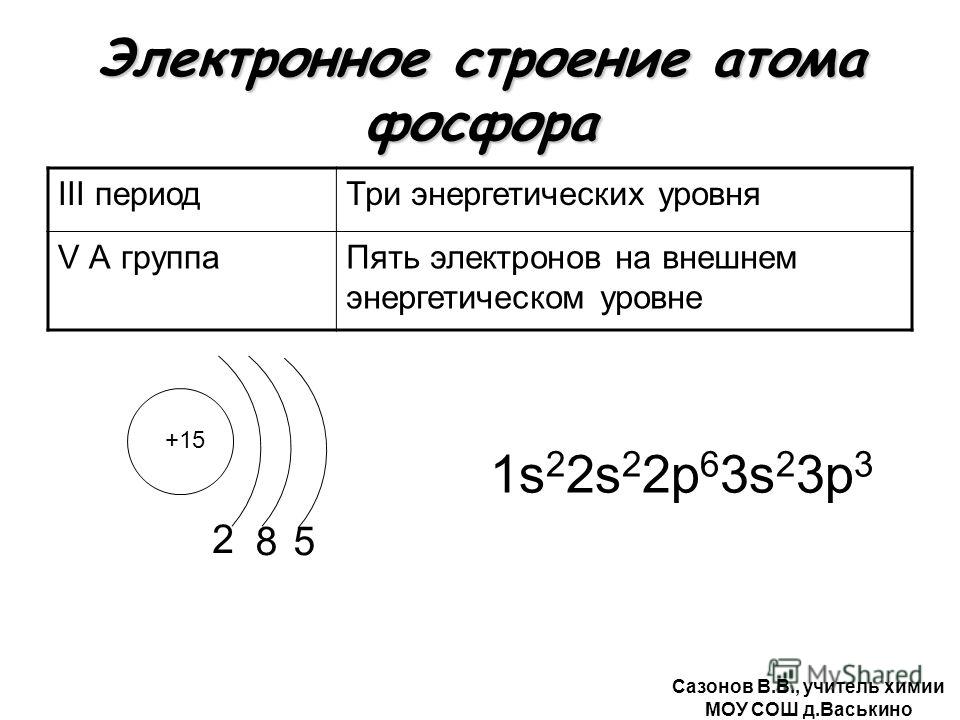 который имеет химическую формулу NaCl. Натрий (Na) и хлор (Cl) очень
разные элементы.
который имеет химическую формулу NaCl. Натрий (Na) и хлор (Cl) очень
разные элементы.
В элементарном состоянии хлор представляет собой зеленовато-желтый газ с температурой плавления -101 градус по Цельсию и точка кипения -34,1 градуса по Цельсию. В нем 17 электронов в трех снаряды. Он также имеет атомный диаметр 3,62 единицы (не беспокойтесь о тип юнитов). Натрий плавится при 98 градусах Цельсия и закипает при 889 градусах. градусов по Цельсию.Элементарный натрий – серебристо-белый металл, который может быть разрезать ножом. Очень бурно реагирует с воздухом или водой. Это отличный проводник тепла и электричества. Он имеет 11 электронов, также в три снаряда. Атомный диаметр натрия 1,81 единицы (размер атом хлора).
Хотя натрий и хлор очень разные, они
объединяются, чтобы сформировать соединение, называемое галитом (NaCl), широко известное как столовый
соль. Кристаллы галита растут в кубической форме, которая отражает, как хлор и
натриевый комбинат. Поскольку размер атома натрия составляет половину атома хлора,
два элемента идеально сочетаются в кубический узор, как показано слева.
Поскольку размер атома натрия составляет половину атома хлора,
два элемента идеально сочетаются в кубический узор, как показано слева.
- Обсудите с учащимися структуру атомов. Раздайте
салфетки периодической таблицы. Просмотрите общие элементы и их символы.
Назовите название элемента и попросите учеников дать вам
символ. Вы можете задать другие вопросы, например об атомном весе.
или является ли элемент обычно твердым, жидким или газообразным.
- Попросите учащихся найти натрий (Na) и хлор (Cl) на
салфетки. Обсудите их подробно, как указано выше. Попросите студентов
заполните рабочий лист, используя информацию из периодической диаграммы.
Просмотрите электроны, протоны и нейтроны.
- Дайте учащимся немного соли для проверки. Спросите их, есть ли соль
кубический. (ответ – да). Предложите ученикам найти кристалл.
это не кубический.(Могут быть скопления кубиков, но они все еще
кубической.
 ) Спросите их, кристаллы ли это или кристаллы, которые
разбита на маленькие кубики. (Ответ может отличаться, но если он сломан или
«расколотая» соль по-прежнему будет образовывать кубики.)
) Спросите их, кристаллы ли это или кристаллы, которые
разбита на маленькие кубики. (Ответ может отличаться, но если он сломан или
«расколотая» соль по-прежнему будет образовывать кубики.)
Chem4Kids.com: Атомы: структура
Атомы – основа химии. Они являются основой всего во Вселенной. Как известно, материя состоит из атомов. Твердые тела состоят из плотно упакованных атомов, а газы – из рассредоточенных атомов.Мы собираемся охватить такие основы, как атомная структура и связь между атомами. По мере того, как вы узнаете больше, вы можете перейти на страницы реакций и биохимии и увидеть, как атомы образуют соединения, которые помогают выжить биологическому миру.
Есть ли куски материи меньше атомов? Конечно, есть. Сверхмалые частицы можно найти внутри кусочков атомов. Эти субатомные частицы включают нуклонов и кварков . Химики-ядерщики и физики работают вместе на ускорителях частиц , чтобы обнаружить присутствие этих крошечных, крошечных кусочков материи. Однако наука основана на атоме, потому что это мельчайшая отдельная единица материи.
Однако наука основана на атоме, потому что это мельчайшая отдельная единица материи.
В периодической таблице Менделеева почти 120 известных элементов. (117, пока мы пишем это) Химики и физики каждый день пытаются создавать новые в своих лабораториях. Атомы разных элементов имеют разное количество электронов, протонов и нейтронов. Каждый элемент уникален и имеет атомный номер. Это число говорит вам количество протонов в каждом атоме элемента. Атомный номер также называется числом протона.
Вы можете видеть, что каждая часть атома помечена знаком «+», «-» или «0». Эти символы относятся к заряду частицы. Вы когда-нибудь слышали о поражении электрическим током от розетки, статическом электричестве или молнии? Все это связано с электрическими зарядами. Заряды также находятся в крошечных частицах материи.
Эти символы относятся к заряду частицы. Вы когда-нибудь слышали о поражении электрическим током от розетки, статическом электричестве или молнии? Все это связано с электрическими зарядами. Заряды также находятся в крошечных частицах материи.Электрон всегда имеет «-» или отрицательный заряд. Протон всегда имеет «+» или положительный заряд. Если заряд всего атома равен «0» или нейтрален, имеется равное количество положительных и отрицательных зарядов.У нейтральных атомов одинаковое количество электронов и протонов. Третья частица – нейтрон. Он имеет нейтральный заряд, также известный как нулевой заряд.
Поскольку количество протонов в атоме не меняется, меньшее количество или больше электронов могут создать особый атом, называемый ионом. Катионы имеют меньше электронов и положительный заряд. Анионы имеют лишние электроны, которые создают отрицательный заряд.
Самая маленькая письменность в мире (Stanford Univ.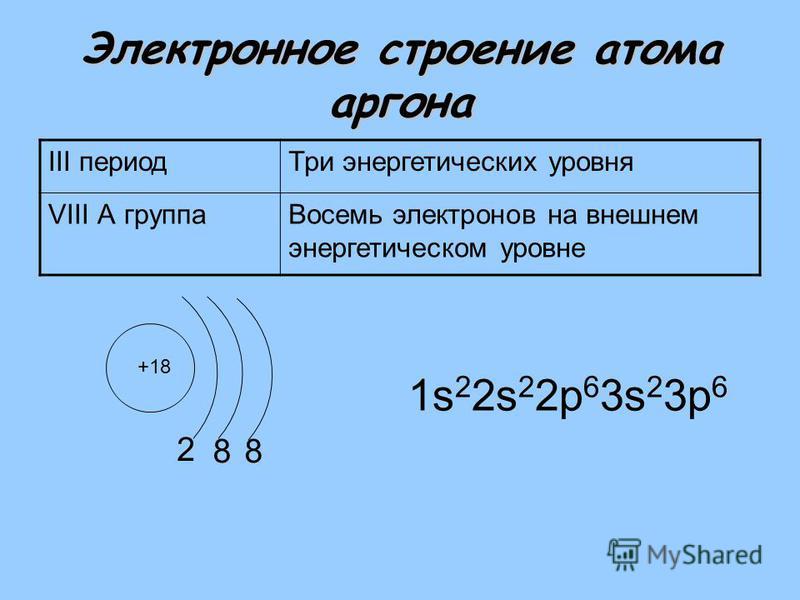 Видео)
Видео)
Заряд и структура материи
Строение материи
Изучая химию, вы знаете, что материя состоит из атомов, которые объединяются в молекулы и кристаллы. Чтобы понять, как образуются молекулы и кристаллы, а также свойства макроскопической материи, нам нужно более глубоко изучить атомную структуру. Ключевые идеи, которые нам необходимо знать, следующие:
- Атомы состоят из электронов и ядер;
- Размеры атомов определяются распределением электронов в атоме;
- Ядра маленькие, но содержат почти всю массу атома;
- Связь между атомами, которая формирует молекулы и кристаллы, возникает из-за электрических сил между электронами и ядрами и распределения электронов между разными атомами.
Ядра в атоме можно рассматривать для большей части химии и биологии, как если бы они были классическими «точечными массами» в ньютоновском смысле – объектами, которые можно моделировать как не имеющие структуры и значительного размера. Единственное, что имеет значение для нас, – это то, как они взаимодействуют (создают и ощущают) дальнодействующие силы – гравитацию (у них есть масса), электрические силы (у них есть заряд) и магнитные силы (у них есть магнитный момент). Фактически, мы знаем, что они состоят из нейтронов и протонов, и мы даже много знаем о структуре нейтронов и протонов.Но структура ядра и структура нейтронов и протонов не играют роли в поведении молекул при нормальных температурах. Они не играют никакой роли в понимании биологии (за исключением того, что субструктуры объясняют радиоактивность, и мы можем использовать их как зонды обычного вещества).
Единственное, что имеет значение для нас, – это то, как они взаимодействуют (создают и ощущают) дальнодействующие силы – гравитацию (у них есть масса), электрические силы (у них есть заряд) и магнитные силы (у них есть магнитный момент). Фактически, мы знаем, что они состоят из нейтронов и протонов, и мы даже много знаем о структуре нейтронов и протонов.Но структура ядра и структура нейтронов и протонов не играют роли в поведении молекул при нормальных температурах. Они не играют никакой роли в понимании биологии (за исключением того, что субструктуры объясняют радиоактивность, и мы можем использовать их как зонды обычного вещества).
Электроны сложнее. Они намного легче ядер (электрон имеет массу ~ 1/2000 массы нейтрона или протона) и, в результате, распределяются по гораздо большему объему, чем ядро.Здесь фраза «в результате» – пустая фраза. Это происходит из-за квантовой природы материи и из того факта, что квантовые свойства тем важнее, чем легче объект. Это совсем не очевидно и выходит за рамки того, что мы можем здесь обсудить. Полезно подумать об этом: поскольку он такой легкий, электрон движется очень быстро – вращаясь вокруг и заполняя пространство атома, как лопасти электрического вентилятора. Это не совсем правильно – электрон может находиться во многих местах одновременно, но это не так уж и плохо в качестве отправной точки.
Полезно подумать об этом: поскольку он такой легкий, электрон движется очень быстро – вращаясь вокруг и заполняя пространство атома, как лопасти электрического вентилятора. Это не совсем правильно – электрон может находиться во многих местах одновременно, но это не так уж и плохо в качестве отправной точки.
Что для нас важно, как для электронов, так и для ядер, так это их электрический характер.
Заряд и электрическая сила
Мы выделили три силы, действующие на расстоянии: гравитацию, электричество и магнетизм. Откуда они? Почему они случаются? Трудно представить, какой ответ мы можем дать на этот вопрос. Почему объекты оказывают друг на друга силу, когда сталкиваются друг с другом? Мы можем ответить, что объекты не могут занимать одно и то же пространство, и поэтому они отталкивают друг друга с пути.Но это предполагает особое свойство материи – они не могут занимать одно и то же пространство. Ответ для наших войск, действующих на расстоянии, таков:
Основные частицы, из которых состоит материя, обладают свойствами – массой, зарядом и магнитным моментом.
Каждое из этих свойств создает силы, действующие на расстоянии, и реагирует на них.
Вот и все. Это аналог «объекты не могут занимать одно и то же пространство», который должен удовлетворять нас – на данный момент – относительно того, почему при взаимодействии объектов возникают нормальные силы.(В конце концов, мы увидим эти макроскопические контактные силы как следствие электрического взаимодействия и законов квантовой механики.) Результатом будет
Каждый заряд оказывает действие на расстоянии друг от друга электрическими силами на каждый второй заряд. Именно эта сила удерживает атомы вместе.
В нашей модели материи вся материя состоит из электронов и ядер, а ядра – из протонов и нейтронов. Заряд электрона в некотором смысле противоположен заряду протона в том смысле, что электрон и протон в одном и том же месте будут создавать силы на третьем заряде, которые компенсируются.Это хорошо отображается на положительные и отрицательные числа, которые отменяются, когда мы их складываем. Мы называем заряд протона положительным, а заряд электрона отрицательным.
Мы называем заряд протона положительным, а заряд электрона отрицательным.
Поскольку большая часть материи состоит из равного числа положительных и отрицательных зарядов, в основном все электрические силы взаимно нейтрализуются, и мы обычно не видим их эффектов. Но поскольку силы между зарядами зависят от расстояния, распределение положительных и отрицательных зарядов может быть важным.
Для биологических и химических систем тот факт, что электроны легкие и могут перемещаться от одного атома к другому или совместно использоваться между атомами, играет решающую роль.Просто чтобы напомнить вам о важном моменте, который вы выучили по химии:
Атом или молекула, у которых больше или меньше электронов, чем протонов, имеет общий заряд и называется ионом. Электроны и ионы являются основными источниками электрических эффектов в веществе.
Верно также, что для некоторых молекул распределение заряда в молекуле неоднородно. Одна сторона или конец могут иметь больше отрицательного заряда, а другая – положительного.Поскольку расстояние имеет значение в электрических силах, ориентация множества таких молекул вместе может иметь значительный эффект.
Одна сторона или конец могут иметь больше отрицательного заряда, а другая – положительного.Поскольку расстояние имеет значение в электрических силах, ориентация множества таких молекул вместе может иметь значительный эффект.
[Вы можете создать такой макроскопический объект, взяв что-нибудь из таких молекул и выровняв их. Вы можете сделать это с воском, поместив его в электрическое поле, когда он расплавлен, а затем заморозить. В этом случае брусок из замороженного воска будет иметь встроенный электрический эффект – например, на одном конце будет положительный заряд, а на другом – отрицательный. Он действует как стержневой магнит, но с электрическими, а не магнитными силами.Такой объект получил название электрет . ]
Мы рассмотрим эти вопросы более подробно в дальнейшем.
Джулия Гувеа, Марк Эйхенлауб и Джо Редиш 21.08.13
Отображение химической структуры отдельных молекул, атом за атомом
Физик из Брукхейвенской лаборатории Перси Зал с бесконтактным атомно-силовым микроскопом, который он адаптировал и использовал в Центре функциональных наноматериалов (CFN), для изображения азот- и серосодержащих молекул в нефти.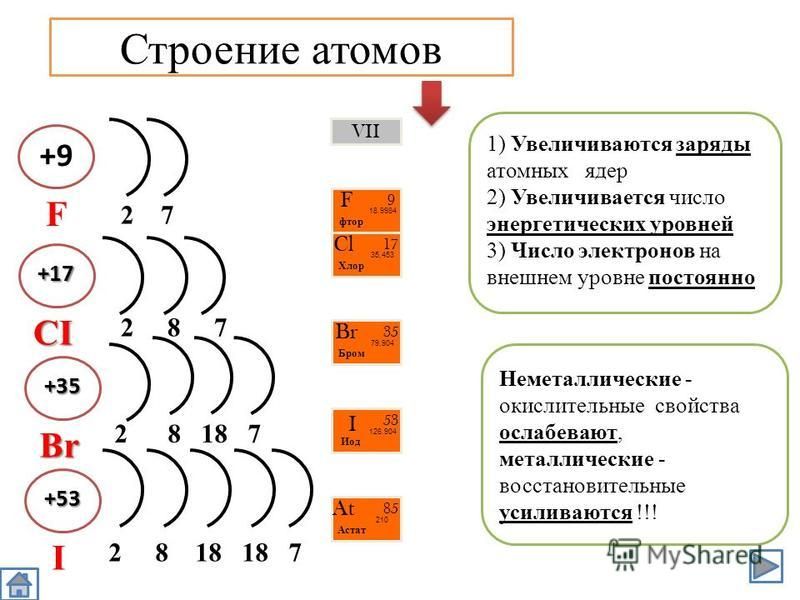 Предоставлено: Брукхейвенская национальная лаборатория.
Предоставлено: Брукхейвенская национальная лаборатория.Для физика Перси Зала оптимизация и подготовка бесконтактного атомно-силового микроскопа (nc-AFM) для прямой визуализации химической структуры одиночной молекулы немного похожа на игру в видеоигру в виртуальной реальности. Процесс требует навигации и манипулирования кончиком инструмента по миру атомов и молекул, в конечном итоге подбирая некоторые из них в нужном месте и правильным способом. Если эти задачи будут выполнены успешно, вы перейдете на высший уровень, получив изображения, которые точно показывают, где расположены отдельные атомы и как они химически связаны с другими атомами.Но сделайте один неверный ход, и игра окончена. Пора начинать заново.
“NC-AFM имеет очень чувствительный наконечник из одной молекулы, который сканирует тщательно подготовленную чистую поверхность монокристалла на постоянной высоте и” чувствует “силы между молекулой наконечника и отдельными атомами и связями молекул, размещенных на нем.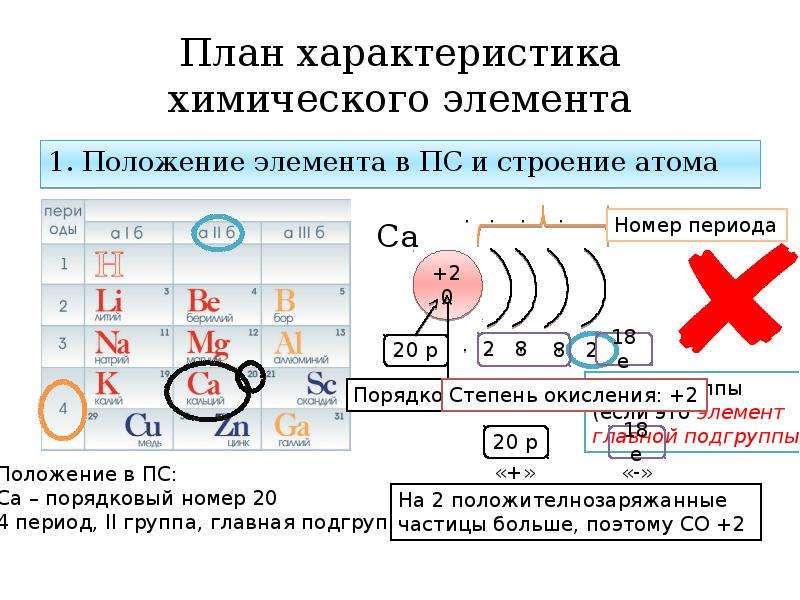 чистая поверхность », – пояснил Заль, который является частью группы по изучению интерфейсов и катализу в Центре функциональных наноматериалов (CFN), США.S. Департамент энергетики (DOE) Научно-исследовательский центр Брукхейвенской национальной лаборатории. «На то, чтобы этот датчик заработал должным образом, может потребоваться час или дни. Вы не можете просто нажать кнопку; требуется точная настройка. Но все эти усилия определенно окупаются, когда вы видите изображения, похожие на молекулы в учебнике химии. ”
чистая поверхность », – пояснил Заль, который является частью группы по изучению интерфейсов и катализу в Центре функциональных наноматериалов (CFN), США.S. Департамент энергетики (DOE) Научно-исследовательский центр Брукхейвенской национальной лаборатории. «На то, чтобы этот датчик заработал должным образом, может потребоваться час или дни. Вы не можете просто нажать кнопку; требуется точная настройка. Но все эти усилия определенно окупаются, когда вы видите изображения, похожие на молекулы в учебнике химии. ”
История определения химической структуры
С самого начала в области химии ученые могли определять элементный состав молекул.Что было труднее, так это выяснить их химическую структуру или конкретное расположение атомов в пространстве. Знание химической структуры важно, потому что она влияет на реакционную способность молекулы и другие свойства.
Например, Майкл Фарадей в 1825 г. выделил бензол из остатков нефтяного газа. Вскоре было установлено, что бензол состоит из шести атомов водорода и шести атомов углерода, но его химическая структура оставалась спорной до 1865 года, когда Фридрих Август Кекуле предложил циклическую структуру.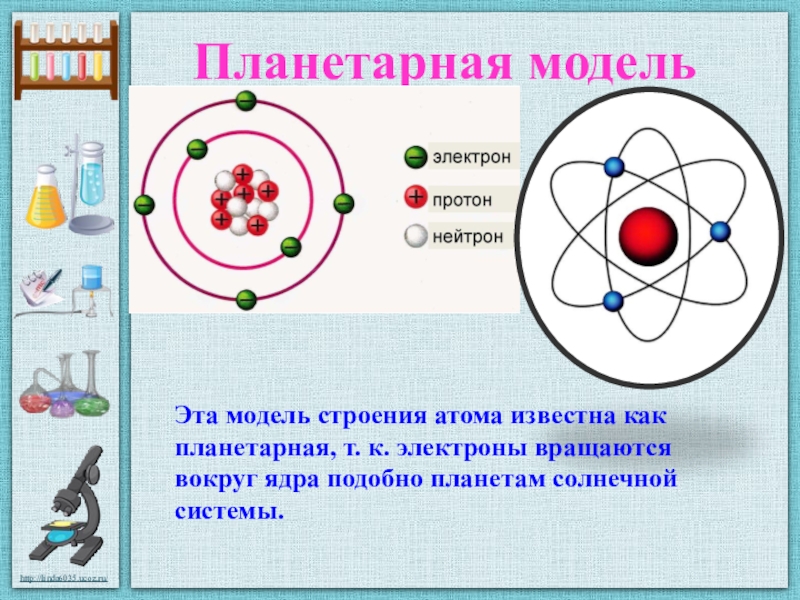 Однако его предложение было основано не на прямом наблюдении, а скорее на логическом выводе из числа изомеров (соединений с одной и той же химической формулой, но с разными химическими структурами) бензола. Правильная симметричная гексагональная структура бензола была наконец обнаружена посредством его дифракционной картины, полученной Кэтлин Лонсдейл с помощью рентгеновской кристаллографии в 1929 году. В 1931 году Эрих Хюкель использовал квантовую теорию для объяснения происхождения «ароматичности» в бензоле. Ароматичность – это свойство плоских кольцевых молекул, в которых электроны разделены между атомами.Благодаря такому уникальному расположению электронов ароматические соединения обладают особой стабильностью (низкой реакционной способностью).
Однако его предложение было основано не на прямом наблюдении, а скорее на логическом выводе из числа изомеров (соединений с одной и той же химической формулой, но с разными химическими структурами) бензола. Правильная симметричная гексагональная структура бензола была наконец обнаружена посредством его дифракционной картины, полученной Кэтлин Лонсдейл с помощью рентгеновской кристаллографии в 1929 году. В 1931 году Эрих Хюкель использовал квантовую теорию для объяснения происхождения «ароматичности» в бензоле. Ароматичность – это свойство плоских кольцевых молекул, в которых электроны разделены между атомами.Благодаря такому уникальному расположению электронов ароматические соединения обладают особой стабильностью (низкой реакционной способностью).
Сегодня рентгеновская кристаллография продолжает оставаться основным методом определения химической структуры наряду со спектроскопией ядерного магнитного резонанса. Однако для обоих методов требуются кристаллы или относительно чистые образцы, и модели химической структуры должны быть выведены путем анализа полученных дифракционных картин или спектров.
Первое реальное изображение химической структуры было получено всего десять лет назад. В 2009 году ученые из IBM Research – Zurich Lab в Швейцарии использовали nc-AFM для разрешения атомной основы отдельной молекулы пентацена, увидев ее пять конденсированных бензольных колец и даже углерод-водородные связи. Этот прорыв стал возможным благодаря выбору подходящей молекулы для конца наконечника – такой, которая могла бы подходить очень близко к поверхности пентацена, не вступая с ней в реакцию или не связываясь с ней.Также потребовалась оптимизированная электроника для считывания показаний датчика при криогенных температурах для измерения небольших частотных сдвигов в колебаниях зонда (которые связаны с силой) при сохранении механической и термической стабильности с помощью устройств гашения вибрации, сверхвысоковакуумных камер и низкотемпературных систем охлаждения.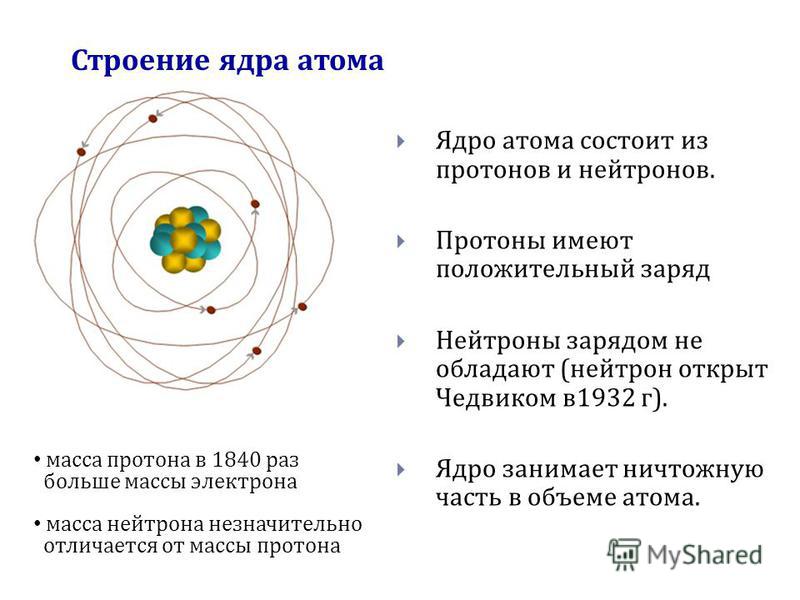
«Низкотемпературная nc-AFM – единственный метод, который может напрямую отображать химическую структуру одиночной молекулы», – сказал Заль. «С помощью nc-AFM вы можете визуализировать положения отдельных атомов и расположение химических связей, которые влияют на реакционную способность молекулы.«
Кекуле утверждает, что идея кольцевой структуры бензола пришла к нему во сне о змее, поедающей собственный хвост. Предоставлено: Брукхейвенская национальная лаборатория. Однако в настоящее время все еще существуют некоторые требования к молекулам, чтобы они подходили для визуализации с помощью nc-AFM. Молекулы должны быть в основном плоскими (плоскими), поскольку сканирование происходит на поверхности, и поэтому они не подходят для больших трехмерных (3-D) структур, таких как белки. Кроме того, из-за медленного характера сканирования за один эксперимент практически можно исследовать только несколько сотен молекул.Заль отмечает, что это ограничение может быть преодолено в будущем с помощью искусственного интеллекта, который проложит путь к автоматизированной сканирующей зондовой микроскопии.
По словам Зала, хотя NC-AFM с тех пор применялся несколькими группами по всему миру, он не получил широкого распространения, особенно в Соединенных Штатах.
«Этот метод все еще относительно новый, и для получения молекулярных структур на основе наконечников CO требуется долгое обучение», – сказал Заль. «Требуется большой опыт в сканирующей зондовой микроскопии, а также терпение.«
Уникальные возможности и опыт
NC-AFM в CFN представляет собой один из немногих в этой стране. За последние несколько лет Заль модернизировал и настроил прибор, в первую очередь с помощью программного и аппаратного обеспечения с открытым исходным кодом GXSM (для сканирующей микроскопии Gnome X). Заль занимается разработкой GXSM более двух десятилетий. Система управления обработкой сигналов в реальном времени и программное обеспечение непрерывно записывают рабочие условия и автоматически регулируют положение наконечника по мере необходимости, чтобы избежать нежелательных столкновений, когда прибор работает в режиме сканирования, специфичного для АСМ, для регистрации сил, воздействующих на молекулы. Поскольку Заль сам написал программное обеспечение, он может программировать и внедрять новые режимы визуализации или работы для новых измерений и добавлять функции, которые помогут операторам лучше исследовать атомный мир.
Поскольку Заль сам написал программное обеспечение, он может программировать и внедрять новые режимы визуализации или работы для новых измерений и добавлять функции, которые помогут операторам лучше исследовать атомный мир.
Например, недавно Заль применил специальный режим «нарезки» для определения трехмерной геометрической конфигурации, в которой одна молекула дибензотиопена (DBT) – серосодержащая ароматическая молекула, обычно встречающаяся в нефти, – адсорбируется на поверхности золота. Молекула DBT не совсем плоская, а скорее наклонена под углом, поэтому он объединил серию изображений силы (срезов), чтобы создать топографическое представление всей структуры молекулы.
«В этом режиме препятствия, такие как торчащие атомы, автоматически избегаются», – сказал Захл. «Эта возможность важна, поскольку измерения силы в идеале производятся в одной фиксированной плоскости, при этом необходимо находиться очень близко к атомам, чтобы почувствовать силы отталкивания и, в конечном итоге, добиться детального контраста изображения. Когда части выступают из плоскости молекулы, они, вероятно, негативно повлияют на качество изображения “.
Когда части выступают из плоскости молекулы, они, вероятно, негативно повлияют на качество изображения “.
Это изображение DBT было выполнено в рамках сотрудничества с Юньлуном Чжаном, физиком-органическим химиком из компании ExxonMobil Research and Engineering Corporate Strategic Research в Нью-Джерси.Чжан встретился с Залом на конференции два года назад и понял, что возможности и опыт в области NC-AFM в CFN будут иметь большой потенциал для его исследований в области химии нефти.
DBT (левая колонка) – одно из серосодержащих соединений нефти; CBZ и ACR (правая и средняя колонки соответственно) представляют собой азотсодержащие соединения. Вверху каждого столбца показаны иллюстрации и модели их химических структур в виде шариков и палочек (черный цвет означает атомы углерода; желтый означает серу, а синий означает азот).Смоделированные изображения с помощью атомно-силовой микроскопии (a, b, d, e, g и h) хорошо совпадают с изображениями, полученными экспериментально (c, f и i). Предоставлено: Брукхейвенская национальная лаборатория.
Предоставлено: Брукхейвенская национальная лаборатория.Захл и Чжан использовали nc-AFM для визуализации химической структуры не только DBT, но и двух азотсодержащих ароматических молекул – карбазола (CBZ) и акридина (ACR), которые широко наблюдаются в нефти. Анализируя изображения, они разработали набор шаблонов общих черт в кольцевых молекулах, которые можно использовать для поиска атомов серы и азота и отличия их от атомов углерода.
Нефть: сложная смесь
Химический состав нефти широко варьируется в зависимости от того, где и как она образовалась, но в целом она содержит в основном углерод и водород (углеводороды) и меньшие количества других элементов, включая серу и азот. При сгорании топлива эти «гетероатомы» производят оксиды серы и азота, которые способствуют образованию кислотных дождей и смога – загрязнителей воздуха, вредных для здоровья человека и окружающей среды.Гетероатомы также могут снижать стабильность топлива и вызывать коррозию компонентов двигателя. Хотя существуют процессы очистки, не вся сера и азот удаляются. Выявление наиболее распространенных структур нечистых молекул, содержащих атомы азота и серы, может привести к оптимизации процессов очистки для производства более чистого и более эффективного топлива.
Хотя существуют процессы очистки, не вся сера и азот удаляются. Выявление наиболее распространенных структур нечистых молекул, содержащих атомы азота и серы, может привести к оптимизации процессов очистки для производства более чистого и более эффективного топлива.
«Наши предыдущие исследования с группой IBM в Цюрихе по нефтяным асфальтенам и смесям тяжелой нефти позволили впервые« заглянуть »в многочисленные структуры нефти», – сказал Чжан.«Однако необходимы более системные исследования, особенно в отношении присутствия гетероатомов и их точного расположения в каркасах ароматических углеводородов, чтобы расширить область применения этого нового метода для выявления сложных молекулярных структур в нефти».
Чтобы отобразить атомы и связи в DBT, CBZ и ACR, ученые подготовили наконечник nc-AFM с монокристаллом золота на вершине и одиночной молекулой монооксида углерода (CO) на конце ( молекула того же типа, что использовалась в первоначальном эксперименте IBM).Металлический кристалл обеспечивает атомарно чистую и плоскую основу, с которой может быть захвачена молекула CO.
После «функционализации» иглы они нанесли несколько каждой из молекул (количество пыли) на поверхность золота внутри нк-АСМ в сверхвысоком вакууме при комнатной температуре посредством сублимации. Во время сублимации молекулы переходят прямо из твердой фазы в газовую.
Хотя полученные ими изображения поразительно напоминают рисунки химической структуры, вы не можете напрямую сказать по этим изображениям, присутствует ли в определенном месте атом азота, серы или углерода.Чтобы вычесть эту информацию, требуются некоторые исходные знания.
«В качестве отправной точки мы визуализировали небольшие хорошо известные молекулы с типичными строительными блоками, которые встречаются в более крупных полициклических ароматических углеводородах – в данном случае в нефти», – пояснил Заль. «Наша идея заключалась в том, чтобы увидеть, как выглядят основные строительные блоки этих химических структур, и использовать их для создания набора шаблонов для их обнаружения в более крупных неизвестных молекулярных смесях».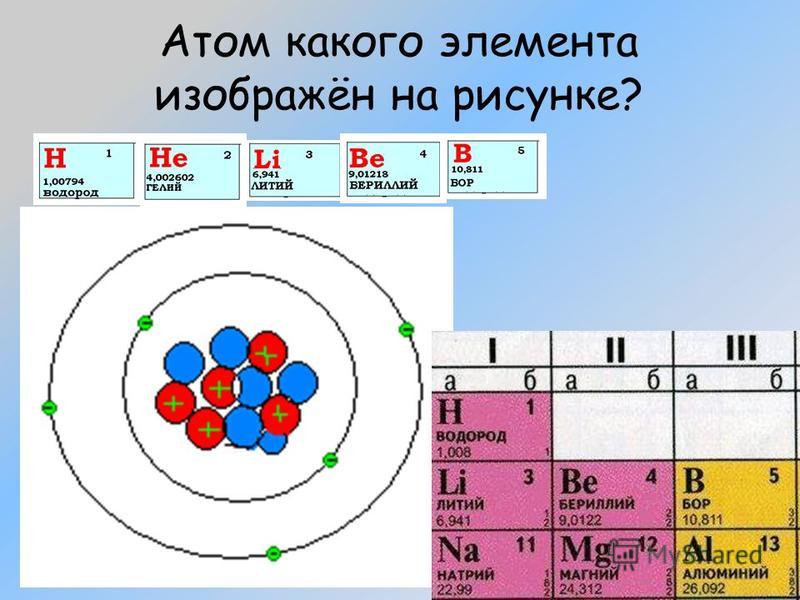
Например, для серо- и азотсодержащих молекул в нефти сера присутствует только в кольцевых структурах с пятью атомами (пятиугольная кольцевая структура), в то время как азот может присутствовать в кольцах с пятью или шестью (гексагональная кольцевая структура) атомами. В дополнение к этой геометрии соединения, относительный «размер» или атомный радиус элементов может помочь различить их. Сера относительно больше азота и углерода, а азот немного меньше углерода.АСМ чрезвычайно чувствителен именно к этому размеру или «высоте».
В дополнение к этой геометрии соединения, относительный «размер» или атомный радиус элементов может помочь различить их. Сера относительно больше азота и углерода, а азот немного меньше углерода.АСМ чрезвычайно чувствителен именно к этому размеру или «высоте».
«Проще говоря, сила, которую АСМ регистрирует в непосредственной близости от атома, связана с расстоянием и, следовательно, с размером этого атома; по мере того, как АСМ сканирует молекулу с фиксированной высотой, более крупные атомы больше выступают из самолет “, – пояснил Захл. «Следовательно, чем больше размер атома в молекуле, тем больше сила, которую регистрирует АСМ, когда он приближается к своей атомной оболочке, и отталкивание резко возрастает.Поэтому на изображениях сера выглядит как яркая точка, а азот – чуть слабее ».
Захл и Чжан затем сравнили свои экспериментальные изображения с изображениями, смоделированными на компьютере, которые они получили с помощью метода моделирования механической частицы.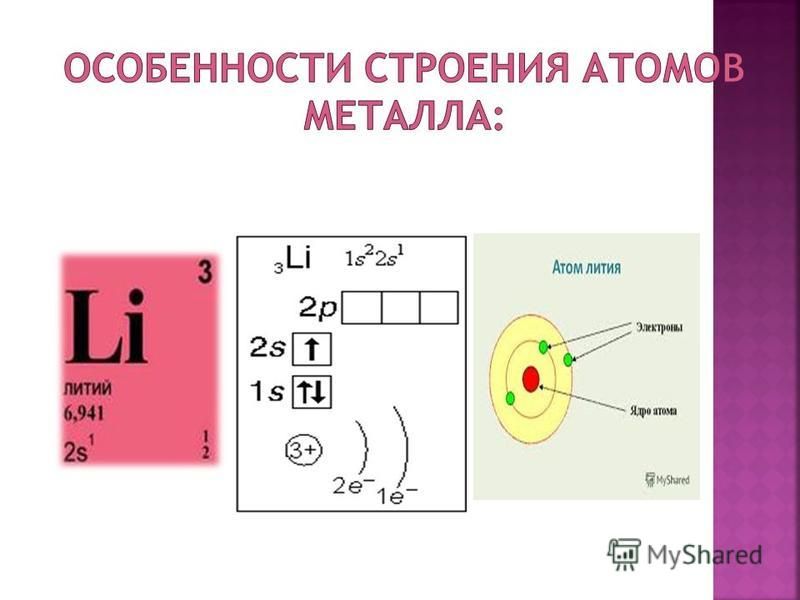 Этот метод имитирует действительные силы, действующие на молекулу CO на конце наконечника, когда она сканирует молекулы и изгибается в ответ. Они также выполнили теоретические расчеты, чтобы определить, как электростатический потенциал (распределение заряда) молекул влияет на измеренную силу и соотносится с их появлением на изображениях нк-АСМ.
Этот метод имитирует действительные силы, действующие на молекулу CO на конце наконечника, когда она сканирует молекулы и изгибается в ответ. Они также выполнили теоретические расчеты, чтобы определить, как электростатический потенциал (распределение заряда) молекул влияет на измеренную силу и соотносится с их появлением на изображениях нк-АСМ.
«Мы использовали теорию функционала плотности, чтобы изучить, как силы, ощущаемые молекулой зонда CO, ведут себя в присутствии зарядовой среды, окружающей молекулы», – сказал Заль. «Нам нужно знать, как распределяются электроны, чтобы понять атомную силу и механизм контраста связей. Эти идеи даже позволяют нам определять одинарные или двойные связи между атомами, анализируя детали изображения».
В дальнейшем Zahl продолжит разработку и совершенствование режимов визуализации nc-AFM и связанных с ними технологий для исследования многих видов интересных, неизвестных или новых молекул в сотрудничестве с различными пользователями.К наиболее интересным молекулам-кандидатам относятся молекулы с большим магнитным моментом и особыми спиновыми свойствами для квантовых приложений, а также новые графеноподобные (графен – это лист атомов углерода толщиной в один атом, расположенный в гексагональной решетке) материалы с необычными электронными свойствами.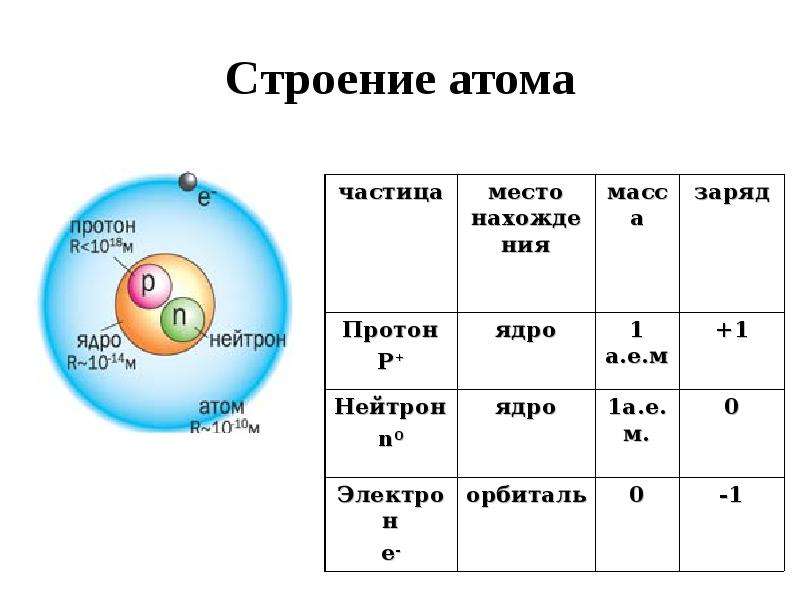
«CFN обладает уникальными возможностями и опытом в области NC-AFM, который может быть применен к широкому кругу молекул», – сказал Заль. «В ближайшие годы я считаю, что искусственный интеллект окажет большое влияние на эту область, помогая нам автономно управлять микроскопом для выполнения наиболее трудоемких, утомительных и подверженных ошибкам частей экспериментов.Благодаря этой особой способности наши шансы на победу в «игре» значительно увеличатся ».
Исследователи представляют молекулы, впервые меняющие зарядовые состояния
Дополнительная информация: Перси Заль и др.Руководство по анализу изображений с помощью атомно-силовой микроскопии для различения гетероатомов в ароматических молекулах, Energy & Fuels (2019). DOI: 10.1021 / acs.
 energyfuels.9b00165 Предоставлено
Брукхейвенская национальная лаборатория
energyfuels.9b00165 Предоставлено
Брукхейвенская национальная лабораторияСсылка : Визуализация химической структуры отдельных молекул, атом за атомом (2019, 22 июля) получено 21 декабря 2021 г. с https: // физ.org / news / 2019-07-imaging-chemical-индивидуальные-молекулы-atom.html
Этот документ защищен авторским правом. За исключением честных сделок с целью частного изучения или исследования, никакие
часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в информационных целях.
Контент предоставляется только в информационных целях.
Lewis StructuresСтруктуры Льюиса – это простой способ отслеживать связывающие электроны, несвязывающие электроны и формальные заряды в молекулах. Чтобы создать структуру Льюиса, сложите все валентные электроны составляющих атомов молекулы или иона. Расположите эти электроны в виде двухэлектронных связей и несвязывающих пар так, чтобы каждый атом имел конфигурацию заполненной оболочки. Вы видели, как рисовать структуры Льюиса некоторых простых молекул. Давайте посмотрим на более сложный пример – азид калия. Это соль, и ее можно записать в виде KN 3 или [K] [N 3 ]. По соглашению в формуле катион стоит перед анионом.
Официальное обвинениеФормальный заряд может показать нам богатые электронами и бедные электронами области соединения.Это важная часть структуры Льюиса.На каждый атом в структуре:
Счетчик электроновПодсчет электронов вокруг атома говорит нам о его реакционной способности. Если количество электронов меньше количества, необходимого для заполнения валентной оболочки, атом является реактивным. Все атомы будут искать заполненную валентную оболочку.Для каждого атома:
Обратите внимание, что NO 3 является радикалом. На кислороде есть неспаренный электрон, и у этого атома кислорода меньше электронов, чем необходимо для заполнения валентной оболочки. Это ключ к химическому составу этой молекулы. Назад Компас Таблицы Показатель Введение Следующий |





 (О зарядах мы поговорим позже.)
(О зарядах мы поговорим позже.)
