Год таблицы Менделеева: как это будет?
Каким будет год периодической таблицы, сколько всего пройдет мероприятий в его рамках, как школьнику попасть на экскурсию в новый технопарк и как оставаться ученым, будучи ректором РХТУ, рассказал в интервью Indicator.Ru Александр Мажуга.
— Александр Георгиевич, 2019 год был объявлен годом таблицы Менделеева. Однако сегодня таблицу Менделеева проходят в школе, и каждый пятиклассник хотя бы визуально помнит, как она выглядит. Как вы считаете, зачем объявлять год этой таблицы, в чем главный посыл?
— Это мероприятие не только российское, это мероприятие международное. Российского химическое общество им. Д.И. Менделеева и Российская академия наук выступили в ЮНЕСКО, ООН с инициативой проведения года Периодической таблицы химических элементов. История открытия таблицы достаточно запутанная: есть английские ученые, американские, французские, которые внесли свой вклад. Но исторические данные, публикации, по которым легко определить первенство, указывают, что открытие было сделано в России, Дмитрием Ивановичем 150 лет назад.
Дмитрий Иванович — первый, кто в этом порядке нашел закон периодичности, и в этом весь смысл. Таблица — не просто удобный способ расположения элементов. Это закон периодичности, который гласит, что свойства элементов повторяются в рядах и в периодах. На самом деле, только в России, на пространстве союзных республик и бывших социалистических стран таблица носит имя Менделеева. В других странах она не имеет имени. Задача Российской Федерации и химиков нашей страны — сделать так, чтобы на международной арене таблице официально присвоили имя Менделеева. Для этого наша страна должна приложить все усилия. Это научная дипломатия, способ еще раз показать, что наша наука, в первую очередь, естественно-научный блок, имеет вес на международной арене. Если вы помните, открытие новых трех тяжелых элементов было сделано либо в нашей стране (в Дубне), либо в сотрудничестве с российскими учеными.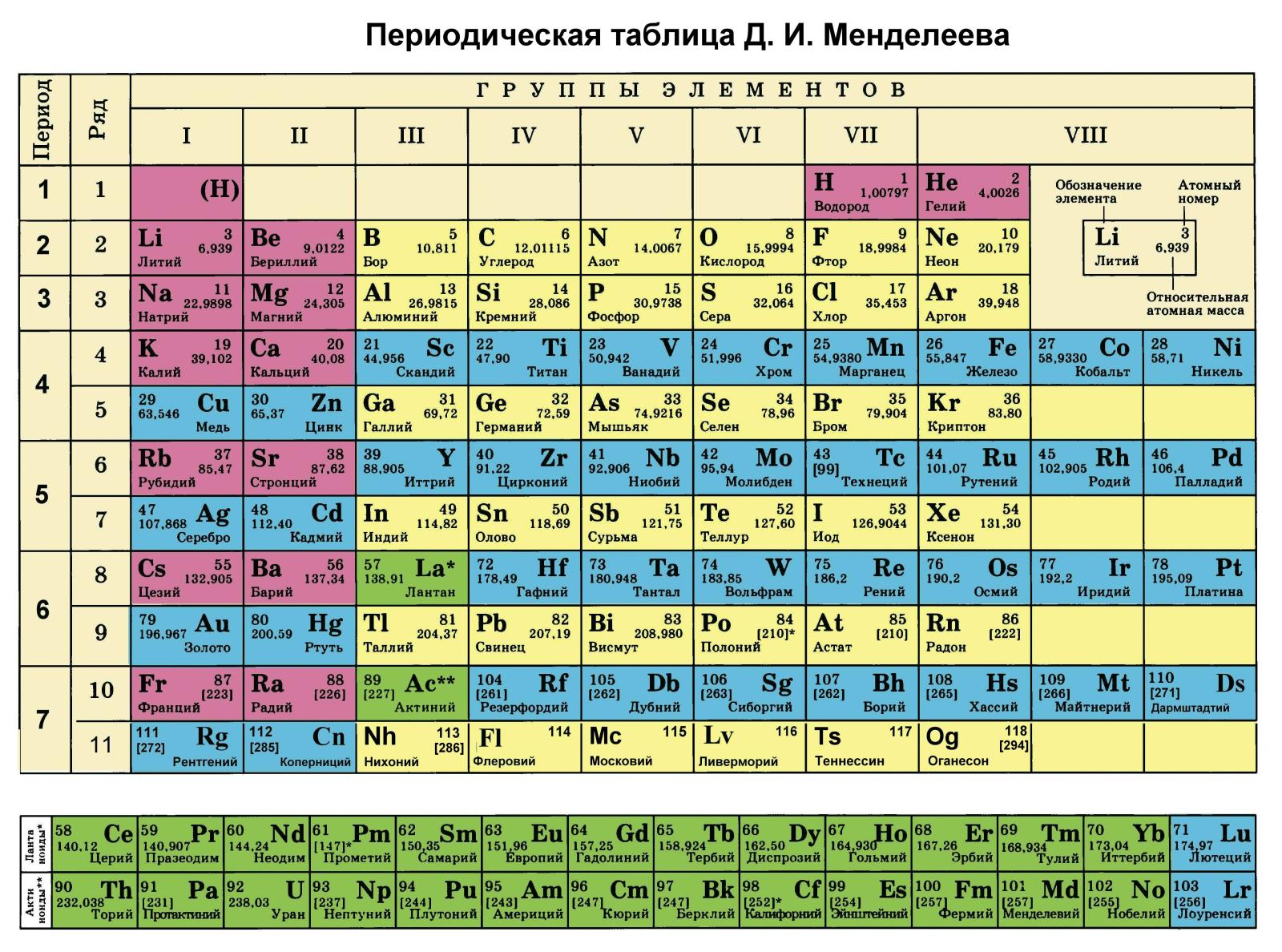
— А какие мероприятия планируются в рамках этого года? Кто их организует?
— Надо разделять две категории мероприятий: те, которые будут проходить в мире, и те, которые будут проходить на территории Российской Федерации. У вас была публикация, что председатель правительства Дмитрий Анатольевич Медведев подписал приказ о проведении года Периодической таблицы Химических элементов и об организации оргкомитета, который как раз возглавил Дмитрий Анатольевич. Наш университет, РХТУ, стал соорганизатором, головной организатор, естественно — Российская академия наук, Российское химическое общество, Министерство науки и высшего образования. РХТУ, как подведомственная организация Минобра, выступает соорганизатором-оператором проведения года – не только в России, но и за рубежом.
— Кстати, про главу российского оргкомитета. Как вам работается под таким руководством?
— Дмитрий Анатольевич возглавляет «большой» оргкомитет. Туда входят представители правительства, министерств, представители химического бизнеса. Я вхожу в рабочую группу при Министерстве науки и высшего образования, но могу сказать, что очень комфортно, очень хорошо. У нас много мероприятий, много идей. Одна из важных задач — найти под них финансирование. А так — оргкомитет работает в штатном рабочем режиме. К организации открытия года в Париже и Москве привлекается команда, которая занимается Фестивалем науки «Наука 0+».
Туда входят представители правительства, министерств, представители химического бизнеса. Я вхожу в рабочую группу при Министерстве науки и высшего образования, но могу сказать, что очень комфортно, очень хорошо. У нас много мероприятий, много идей. Одна из важных задач — найти под них финансирование. А так — оргкомитет работает в штатном рабочем режиме. К организации открытия года в Париже и Москве привлекается команда, которая занимается Фестивалем науки «Наука 0+».
Открытие планируется грандиозным. Международная часть торжества пройдет 29 января в Париже, в ЮНЕСКО. На торжественной части мероприятия будут присутствовать около 1500 человек. Большая представительская делегация Российской Федерации — около 200 человек, среди которых будут и студенты профильных вузов. Конечно же, среди вузов — наш университет и МГУ. Параллельно с торжественным открытием три дня, начиная с 28 января, будет проходить выставка, которая будет посвящена Периодическому закону. Будет представлена история и факты, подтверждающие, что открытие было сделано Дмитрием Ивановичем Менделеевым, также будет экспозиция об истории открытия разных элементов..jpg)
— А на открытии будет большая делегация от вашего университета?
— Порядка 20 человек. Учитывая, что вся делегация от России будет около 200 человек, это составит 10%. Самая большая делегация от университетов, насколько я знаю. Также будет большая делегация от МГУ. Кстати, еще из важных моментов: в прошлом году наш университет впервые вошел в Шанхайский рейтинг вузов. Кроме него только три наших вуза туда попали: МГУ, Новосибирский государственный университет и РГУ нефти и газа имени Губкина. Это хорошая победа. И мероприятие в Париже тоже поможет продвинуться на международной арене. У нас будет стенд своего университета, который носит имя Менделеева (по-английски мы называемся Mendeleev University).
— Получается, выставкой в Париже вы рассчитываете привлечь больше иностранных студентов?
— Да, у нас уже увеличилось количество иностранных студентов. Для нас важно заниматься экспортом нашего образования. Тем более, что оно у нас достойное — особенно в области естественнонаучных дисциплин и, в частности, химической технологии.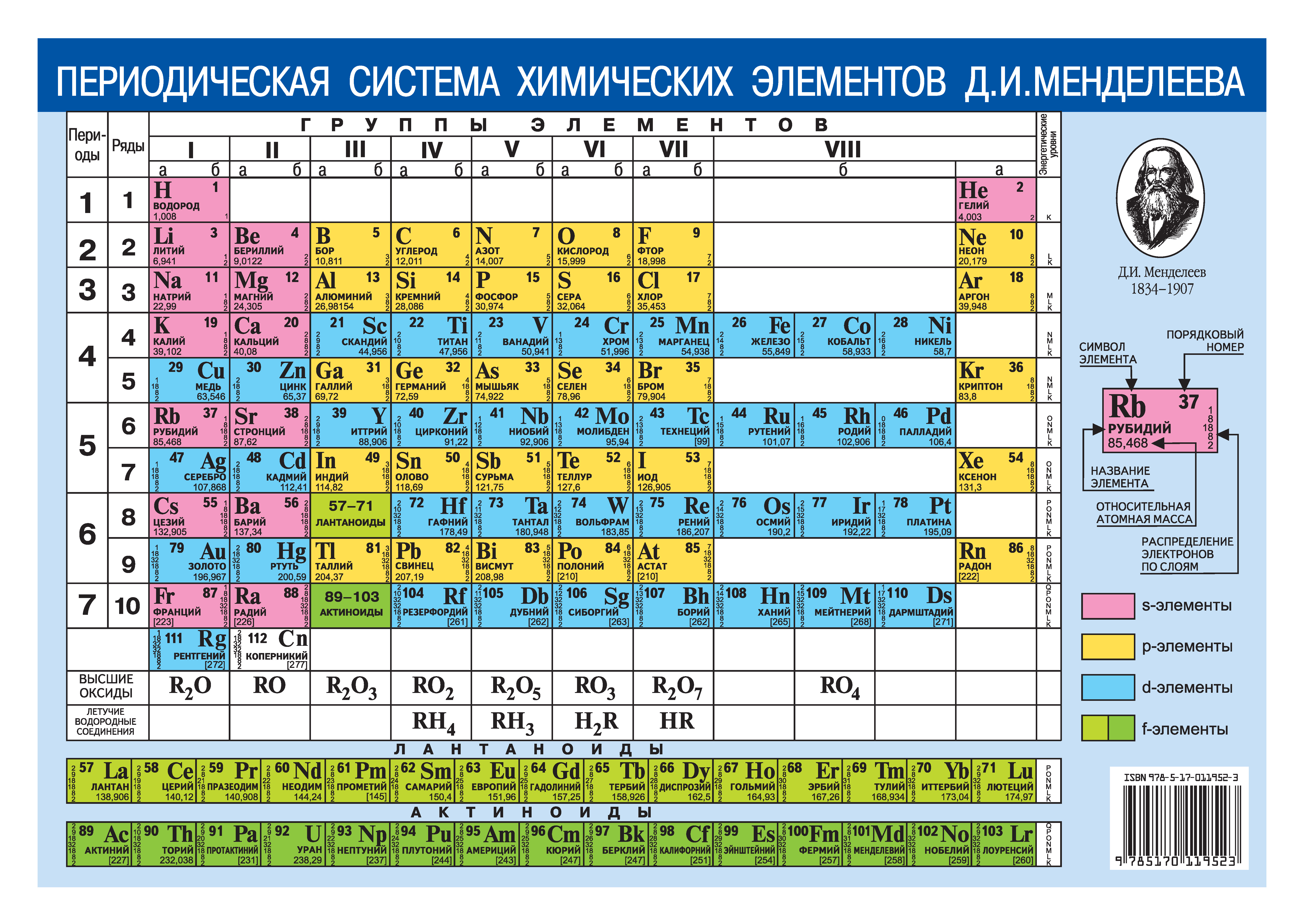 Так что популяризация вуза на международной арене тоже очень важная цель мероприятий года. Как и популяризация химии, даже для школьников.
Так что популяризация вуза на международной арене тоже очень важная цель мероприятий года. Как и популяризация химии, даже для школьников.
— И что вы подготовили для школьников к торжественному открытию?
— Для школьников во время выставки будут проходить химические мастер-классы. Наш университет будет делать VR-зону, которая будет демонстрировать интерактивный практикум по неорганической химии и интерактивный химический завод. Можно будет побродить по нефтеперерабатывающему заводу, посмотреть, как он устроен. На выставке будет много студентов и школьников, большей частью, конечно, из Франции, но и из других европейских стран тоже. И наш университет везет туда интерактивный практикум по химии, настоящую химическую лабораторию. Ребенок сможет надеть очки, почувствовать себя настоящим ученым, узнать некоторые новые вещи о химических элементах и Периодическом законе.
— А какие задания там будут?
Еще одна важная для нас дата — 6 февраля, официальное открытие года в Москве, в Российской академии наук. Будет проходить выставка, пройдет торжественная часть, на которой запланировано выступление представителей нашего академического сообщества, один из открывателей элементов — Юрий Цолакович Оганесян из Дубны — прочитает лекцию. Приедет известный химик Мартин Полякофф из Великобритании, из Ноттингема. У профессора корни в России. Пройдет выставка, будет интерактив, представят экспозицию, где показывает химические элементы в различных областях: в космонавтике, в экологических аспектах, в «зеленой» химии, в здравоохранении, в химической технологии.
Дальше, в течение года, как в России, так и во всем мире, будут проходить разные мероприятия. Это съезды ассоциации химиков (самая большая ассоциация — ИЮПАК). В России самым большим мероприятием будет Менделеевский съезд осенью. Это самое большое собрание, конференция химиков нашей страны с международным участием. Что касается популяризации таблицы, наследия нашей страны, будет проведен ряд открытых уроков по химии на базе вузов и на базе школ.
— Рутений.
— Да. Много элементов названы в честь ученых: мендеелевий, кюрий. Много элементов названы в честь городов: дубний, московий. Эти факты мы также хотим рассказать. В прошлом году наш университет проводил первый Химический диктант. Химический факультет МГУ также проводил. Я думаю, в этом году мы сделаем вместе Химический диктант на всю страну, когда в любой точке страны можно будет через компьютер подсоединиться дистанционно, оценить свои знания по химии и узнать новое о Периодической таблице, Периодическом законе.
Из мероприятий, которые планирует провести наш университет — осенью, — у нас запланировано открытие первого химического технопарка «Mendeleev Центр». Сергей Семенович Собянин подписал соответствующее распоряжение. Это будет четыре лаборатории. Первая лаборатория «Химия. Старт» — химия для самых маленьких, начиная с 3-4 класса, когда ребята могут прийти осуществить безопасные химические эксперименты. В школе у них такой предмета еще нет, а к нам они могут прийти и понять, что такое химия, для чего нужно становиться химиком. Остальные лаборатории — для ребят более старшего возраста – начиная с восьмого класса, когда химия изучается в школе. Одна лаборатория будет посвящена материаловедению, материалам для фотоники, композитные материалы; одна лаборатория посвящена неорганической химии, одна — проблемам органической химии. Помимо этого, в технопарке будет экспозиция, посвященная наследию и творчеству Дмитрия Ивановича Менделеева, и развитию химии и химической технологии в нашей стране, плюс будет ряд экспонатов, где можно будет пощупать, потрогать, посмотреть, что такое химия.
Это будет четыре лаборатории. Первая лаборатория «Химия. Старт» — химия для самых маленьких, начиная с 3-4 класса, когда ребята могут прийти осуществить безопасные химические эксперименты. В школе у них такой предмета еще нет, а к нам они могут прийти и понять, что такое химия, для чего нужно становиться химиком. Остальные лаборатории — для ребят более старшего возраста – начиная с восьмого класса, когда химия изучается в школе. Одна лаборатория будет посвящена материаловедению, материалам для фотоники, композитные материалы; одна лаборатория посвящена неорганической химии, одна — проблемам органической химии. Помимо этого, в технопарке будет экспозиция, посвященная наследию и творчеству Дмитрия Ивановича Менделеева, и развитию химии и химической технологии в нашей стране, плюс будет ряд экспонатов, где можно будет пощупать, потрогать, посмотреть, что такое химия.
— А где будет находиться технопарк?
— Он будет располагаться на нашей площадке, для этого у нас есть трехэтажное здание с отдельным входом с улицы, которое мы сейчас начали переоборудовать.
— А как можно будет попасть на экскурсию? Это право школьник должен заслужить, или билеты будут продаваться свободно?
— У нас будут заключаться договоры со школами, чтобы классы могли приезжать, заниматься экспериментами, делать свои проекты. В выходные мы планируем, что технопарк будет работать как интерактивный музей, куда можно будет просто приходить и смотреть. Но мы еще подумаем о музейной концепции, как мы будем приглашать, привлекать ребят. Я думаю, что это должно быть доступно максимальному числу школьников и их родителей.
— Вы упомянули открытые уроки – а как вы выбирали школы для участия в этой программе?
— У нас есть обширная сеть школ Москвы и Московской области, которые с нами сотрудничают. Мы хотим расширять географию и выезжать в другие в регионы. Помимо этого, мы сотрудничаем с Ивановским химико-технологическим университетом с Казанским национально-исследовательским технологическим университетом. Мы будем передавать дидактические материалы им, и они могут ими пользоваться.
— Представим, что где-то в соседнем регионе есть какая-то школа, которая хочет с вами сотрудничать. Что они должны сделать?
— Нужно написать нам письмо. Мы рассмотрим заявку. Мы готовы сотрудничать, взаимодействовать с новыми школами, приезжать и читать лекции. И приглашаем к себе: мы уже в конце прошлого года открыли лабораторию (при финансовой поддержке DOW Chemicals). Это лабораторный практикум для работы со школьниками – отдельное помещение, хорошо оборудованное.
— Вернемся к празднованию года Периодической системы химических элементов. Будут ли мероприятия в России согласованы с тем, что проходит за рубежом? Или они отличаются?
— Есть план, утвержденный оргкомитетом. Оргкомитет есть в России и за рубежом. В планах около 60 мероприятий. Истории развиваются параллельно, где-то они пересекаются. В основном это научные конференции, и только в России делается акцент на популяризацию. Среди таких мероприятий – издание юбилейных марок, написание книги про Дмитрия Ивановича Менделеева. Сейчас есть только одна книга из серии «Жизнь замечательных людей».
Сейчас есть только одна книга из серии «Жизнь замечательных людей».
Всего в России пройдет около 600 мероприятий, и если за рубежом подавляющее большинство (кроме открытия) – это научные конференции, мы делаем чуть больший упор на популяризацию.
— Тогда давайте поговорим об итогах года для РХТУ. В прошлом интервью Indicator.Ru вы говорили, что собираетесь сделать РХТУ первым проектным вузом в сфере химической технологии. Есть ли какие-то успехи?
— 2018 год был для нашего университета удачным. Во-первых, в области образования, а образование и подготовка высококвалифицированных кадров – все-таки наша первостепенная задача. К нам пришли очень хорошие ребята в этом году. Средний балл ЕГЭ сильно возрос. Если до этого он составлял 72 балла, во время приемной кампании 2018 он составил 80 баллов. Это очень большой подъем.
Мы активно пересматриваем учебные программы. И действительно, мы хотим сделать так, чтобы наш вуз готовил кадры для конкретной отрасли. Мы отвечаем за химическую технологию, химическую промышленность, и должны отвечать на запросы химпрома. Прошлый год был удачным с точки зрения развития инфраструктуры. В нашем университете давно не было ремонта и обновления материально-технической базы, оборудования. В этом году нам удалось за счет привлеченных средств и заработанных денег отремонтировать все внешние корпуса, крыши, помещения изнутри. В этом году запланировано много ремонтных работ внутри зданий, что тоже очень важно. Когда ты приходишь на работу, и университет выглядит красиво и хорошо, всегда приятно приходить пораньше и уходить попозже. Социокультурная среда для работы сотрудников и учебы студентов тоже очень важна. Мы выиграли достаточно много проектов, которые были объявлены в прошлом году, и много проектов продолжается. Были подписаны соглашений, которые должны перейти в более тесное взаимодействие с нашим бизнесом. Я думаю, это большая заслуга, что мы стали ближе к работодателям и нашей промышленности. Мы подписали соглашение о создании научно-образовательного центра с компаниями «Уралхим», «Уралкалий» и ИРЕА «Курчатовский институт» в рамках предстоящего конкурса на НОЦы.
Мы отвечаем за химическую технологию, химическую промышленность, и должны отвечать на запросы химпрома. Прошлый год был удачным с точки зрения развития инфраструктуры. В нашем университете давно не было ремонта и обновления материально-технической базы, оборудования. В этом году нам удалось за счет привлеченных средств и заработанных денег отремонтировать все внешние корпуса, крыши, помещения изнутри. В этом году запланировано много ремонтных работ внутри зданий, что тоже очень важно. Когда ты приходишь на работу, и университет выглядит красиво и хорошо, всегда приятно приходить пораньше и уходить попозже. Социокультурная среда для работы сотрудников и учебы студентов тоже очень важна. Мы выиграли достаточно много проектов, которые были объявлены в прошлом году, и много проектов продолжается. Были подписаны соглашений, которые должны перейти в более тесное взаимодействие с нашим бизнесом. Я думаю, это большая заслуга, что мы стали ближе к работодателям и нашей промышленности. Мы подписали соглашение о создании научно-образовательного центра с компаниями «Уралхим», «Уралкалий» и ИРЕА «Курчатовский институт» в рамках предстоящего конкурса на НОЦы. Мы наладили взаимодействия с представителями фармацевтической отрасли, где очень много химии, тонкого органического синтеза фармсубстанций, и подписали ряд соглашений по разработке технологий получения важных препаратов.
Мы наладили взаимодействия с представителями фармацевтической отрасли, где очень много химии, тонкого органического синтеза фармсубстанций, и подписали ряд соглашений по разработке технологий получения важных препаратов.
— Можете привести конкретные примеры?
— Один из примеров — препарат Лопинавир, предназначенный для лечения вирусных заболеваний, прежде всего ВИЧ. Мы помогаем решить одну из проблем национальной безопасности – проблему импортозамещения. Много говорят о том, что санкции – это угроза потери лекарственных субстанций.
Наш университет готов включиться в работу и помогать стране создавать отечественные субстанции. Такая же ситуация сейчас и с композитными материалами. Сейчас громкая история — импортозамещение материалов для МС-21 (новый российский пассажирский авиалайнер – прим. Indicator.Ru): композиты под санкциями, а компонентной базы отечественной нет. Опять же, тут наш университет выполняет ряд проектов по разработке технологий получения композитных материалов.
Сейчас мы работаем над крупными проектами, которые, надеюсь, будут реализованы. Мы активно включились в проект по 216-му ФЗ («Об инновационных научно-технологических центрах и о внесении изменений в отдельные законодательные акты Российской Федерации» – прим. Indicator.Ru). В рамках этого проекта в Тульской области наш филиал, а также Тульский государственный университет и МГУ создают Композитную долину. Это отечественные композиты, прежде всего для аэрокосмической промышленности, на основе углеродных материалов и не только, разнообразные конструкционные материалы.
— Также в интервью вы упоминали, что собираетесь составить программу развития вуза до 2025 года. Как продвигается работа?
— Что касается стратегии — мы не приняли ее в прошлом году. Чем больше мы погружаемся в специфику нашей отрасли и деятельность университета, тем больше появляется дополнений и изменений. Мы понимаем, что этот процесс может быть бесконечным, но в этом году надо остановиться и принять это решение.
— Желательно до 2025 года ее принять.
— Да, я надеюсь, что в этом году мы ее точно сделаем. Мы сейчас активно работаем над стратегией.
— А что вы можете сказать о научной деятельности университета в 2018 году? Находили ли вы сами время заниматься наукой?
— Было опубликовано много статей (больше, чем в предыдущие годы). Для РХТУ год был очень удачный, хотя и непростой. Выиграны проекты рффи, рнф, намечены планы на будущее.
В принципе, год был удачным и в моей научной лаборатории, где мы тоже опубликовали рекордное количество статей. Мы провели первые доклинические испытания контрастного средства для визуализации опухоли головного мозга (это уже моя наука), надеюсь, что скоро клинические испытания начнутся. Проблема импортозамещения в диагностике тоже решается в соответствии с майскими указами президента и запросами Министерства здравоохранения.
— С точки зрения научной работы стало ли менее «обидно быть ученым», как вы выразились в прошлый раз?
— Нам нужно сделать так, чтобы наши преподаватели старались больше заниматься наукой. В моем понимании (и эту политику я продвигаю в университете), любой преподаватель – это ученый. Среди наших преподавателей есть «чистые ученые», ведущие активную научно- исследовательскую работу, коллеги публикуют научные труды, получают гранты, эти умения передают студентам, прививают студентам любовь к науке. Но мы вуз технологический, и большое внимание уделяем разработке новых технологических решений, в данном случае кафедры больше направлены на работу с промышленностью. И по-другому быть не должно: либо преподаватель двигает науку, либо очень близок к технологии. Мы стараемся помогать нашим преподавателям, чтобы они могли уделить больше времени науке.
В моем понимании (и эту политику я продвигаю в университете), любой преподаватель – это ученый. Среди наших преподавателей есть «чистые ученые», ведущие активную научно- исследовательскую работу, коллеги публикуют научные труды, получают гранты, эти умения передают студентам, прививают студентам любовь к науке. Но мы вуз технологический, и большое внимание уделяем разработке новых технологических решений, в данном случае кафедры больше направлены на работу с промышленностью. И по-другому быть не должно: либо преподаватель двигает науку, либо очень близок к технологии. Мы стараемся помогать нашим преподавателям, чтобы они могли уделить больше времени науке.
— И последний вопрос. РХТУ получил право самостоятельно присуждать ученые степени (об этом вам тоже задавали вопрос в предыдущем интервью). Вы говорили, что вам больше импонирует модель МГУ. Как вы воплотили этот план? Присуждены ли уже какие-то ученые степени?
— Нет, пока не присуждены, мы работаем по ВАКовской системе. Мы должны перейти на собственное присуждение ученых степеней с 1 сентября 2019 года. Сейчас мы разрабатываем и практически согласовали установочные документы. И действительно, мы выбрали модель, которая максимально приближена к модели МГУ и ВАКа, но подняли требования по количеству публикаций, и я думаю, что близко к системе МГУ и ВАКа и останемся, и уже в начавшемся году перейдем на собственные диссоветы. У нас будет ряд объединенных советов (по биотехнологии) и закрытый совет (по спецтематикам), которые будут работать по ВАКу.
Мы должны перейти на собственное присуждение ученых степеней с 1 сентября 2019 года. Сейчас мы разрабатываем и практически согласовали установочные документы. И действительно, мы выбрали модель, которая максимально приближена к модели МГУ и ВАКа, но подняли требования по количеству публикаций, и я думаю, что близко к системе МГУ и ВАКа и останемся, и уже в начавшемся году перейдем на собственные диссоветы. У нас будет ряд объединенных советов (по биотехнологии) и закрытый совет (по спецтематикам), которые будут работать по ВАКу.
Источник: Индикатор
Найдена связь сверхпроводимости с таблицей Менделеева / Интерфакс
Высокотемпературная сверхпроводимость — это утрата материалом электрического сопротивления при температуре выше температуры жидкого азота (−196 С). Это удивительное свойство интересует физиков, химиков и материаловедов уже несколько десятилетий, так как сверхпроводящие материалы, работающие при комнатной температуре, открывают огромные возможности для электроэнергетики, транспорта и многих других технологий. На сегодняшний день рекорд критической температуры сверхпроводимости принадлежит веществу h4S: при давлении 1.5 миллиона атмосфер оно является сверхпроводником при температурах до −70 С. Такие давления можно воспроизвести в лаборатории, но невозможно использовать в реальной жизни, да и температура ещё далека от комнатной, поэтому поиски продолжаются. Возможно, даже ещё более высокотемпературная сверхпроводимость может быть получена для соединений металла и водорода — гидридов. Но само явление сверхпроводимости до сих пор во многом загадка, и учёные были вынуждены пользоваться методом проб и ошибок.
На сегодняшний день рекорд критической температуры сверхпроводимости принадлежит веществу h4S: при давлении 1.5 миллиона атмосфер оно является сверхпроводником при температурах до −70 С. Такие давления можно воспроизвести в лаборатории, но невозможно использовать в реальной жизни, да и температура ещё далека от комнатной, поэтому поиски продолжаются. Возможно, даже ещё более высокотемпературная сверхпроводимость может быть получена для соединений металла и водорода — гидридов. Но само явление сверхпроводимости до сих пор во многом загадка, и учёные были вынуждены пользоваться методом проб и ошибок.
Группа химиков под руководством профессора Сколтеха и МФТИ Артёма Оганова обнаружила закономерность в распределении в таблице Менделеева элементов, способных к образованию сверхпроводимых соединений. Оказалось, что высокотемпературная сверхпроводимость возникает у веществ, в состав которых входят атомы металлов, близких к заселению новой электронной подоболочки. В этом случае атом в кристалле будет очень чувствителен к положению окружающих атомов, а это создаст сильное электрон-фононное взаимодействие — тот самый эффект, который лежит в основе традиционной сверхпроводимости. Основываясь на таком предположении, учёные предположили высокотемпературную сверхпроводимость для гидридов актиния. Проверка подтвердила это предположение: для Ach26 сверхпроводимость предсказана при температурах вплоть до −69 С при давлении в 1.5 миллиона атмосфер.
Основываясь на таком предположении, учёные предположили высокотемпературную сверхпроводимость для гидридов актиния. Проверка подтвердила это предположение: для Ach26 сверхпроводимость предсказана при температурах вплоть до −69 С при давлении в 1.5 миллиона атмосфер.
«Сама идея связи сверхпроводимости с таблицей Менделеева принадлежит моему студенту Дмитрию Семенку. Найденный им принцип настолько простой, что удивительно, что никто не заметил его раньше», — рассказывает Артём Оганов.
Результаты исследования опубликованы в журнале The Journal of Physical Chemistry Letters.
Источник: mipt.ru
Зачем нужна таблица Менделеева | Решаем химию: вопросы и ответы
Изучая неорганическую химию в школе или вузе, вы всегда будете иметь перед глазами огромную и совершенно законную подсказку – таблицу Менделеева. Таблица – справочный материал, который выдают на любом экзамене, будь то егэ по химии или сессия на первом курсе института.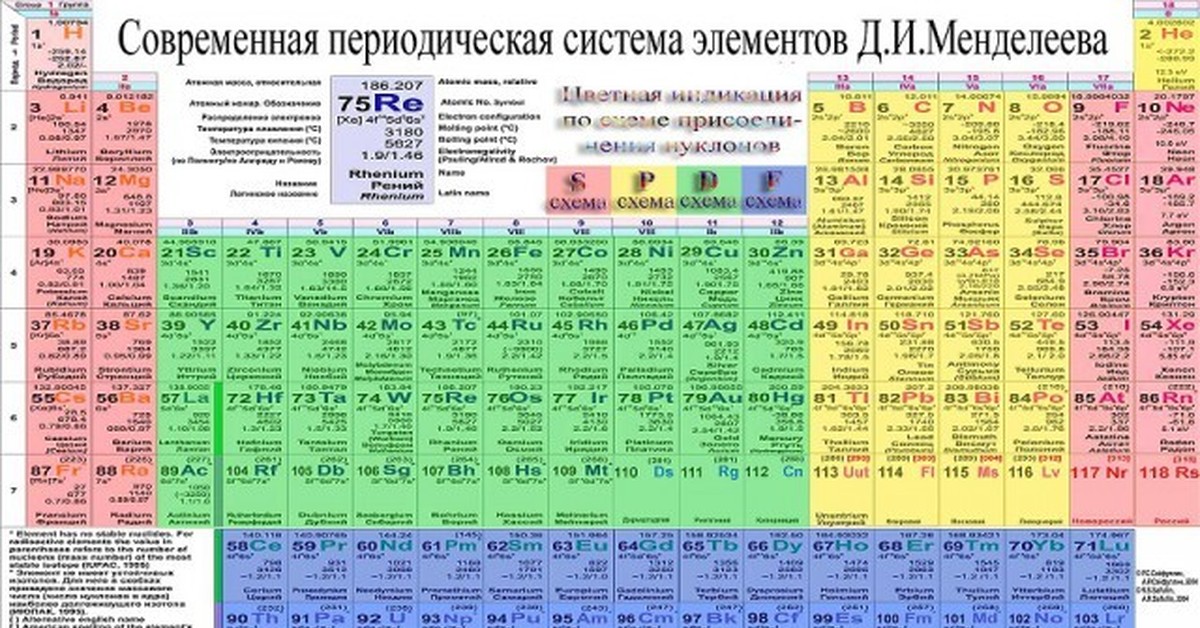 Самое главное – научиться пользоваться этой подсказкой.
Самое главное – научиться пользоваться этой подсказкой.
Бродит миф, что Дмитрий Иванович Менделеев увидел таблицу во сне. Но вот сам Менделеев, говорят, недюжинно обижался на эти домыслы и отвечал, что периодическая система химических элементов – результат многолетней работы. В итоге этой работы и появились таблица и периодический закон, согласно которому
свойства элементов находятся в периодической зависимости от их атомного веса.
Что таблица наглядно и отражает.
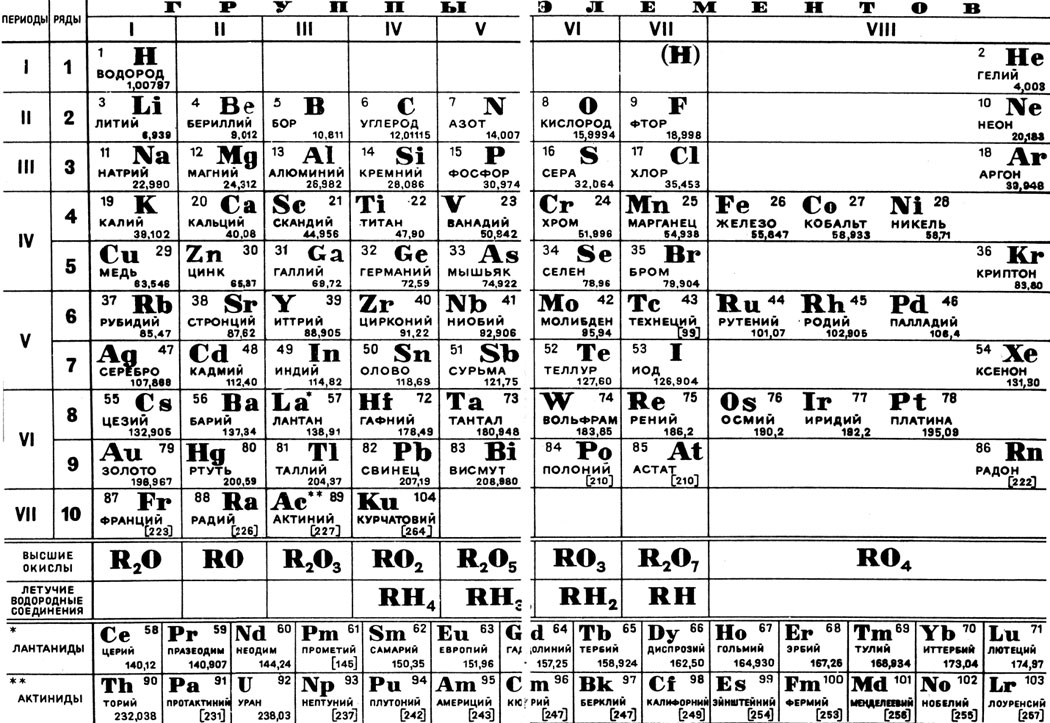
В учебниках химии и классах обычно представлен короткий вариант периодической таблицы. Но существуют ещё и длинный и сверхдлинный. Но самый компактный и удобный для школьников и студентов – короткий. Его особенность в том, что актиноиды и лантаноиды вынесены вниз, а периоды, начиная с четвёртого, имеют две строки. А вот так выглядит длинный вариант:
Фото: chem-mind.comФото: chem-mind.com
Теперь посмотрите на любой элемент. У него есть порядковый номер, и он (это уже подсказка) показывает заряд ядра атома. Зная заряд атома, мы может сказать, сколько протонов составляют ядро и сколько электронов имеется в атоме. Кроме того, в таблице указаны атомные массы всех элементов. И это вторая подсказка, потому что без атомных масс нельзя проводить расчёты. И ещё, зная заряд ядра (то есть число протонов) и массу атома, можно с лёгкостью узнать число нейтронов. Таким образом, даже беглый взгляд на ячейку позволяет нам многое узнать о строении атома конкретного элемента.
Зная заряд атома, мы может сказать, сколько протонов составляют ядро и сколько электронов имеется в атоме. Кроме того, в таблице указаны атомные массы всех элементов. И это вторая подсказка, потому что без атомных масс нельзя проводить расчёты. И ещё, зная заряд ядра (то есть число протонов) и массу атома, можно с лёгкостью узнать число нейтронов. Таким образом, даже беглый взгляд на ячейку позволяет нам многое узнать о строении атома конкретного элемента.
Как пользоваться таблицей Менделеева
В таблице есть группы (колонки, которые обозначаются римскими цифрами) и периоды (строки, которые обозначаются арабскими цифрами). Чтобы было проще, давайте рассмотрим пару примеров.
Пример 1.
Кальций имеет порядковый номер 20. В какой группе и каком периоде он находится?
Ответ: Кальций находится во II группе в 4 периоде.
Пример 2.
Элемент находится в VIII группе в 3 периоде. Что это за элемент? Каков его порядковый номер?
Ответ: это аргон и его порядковый номер 18.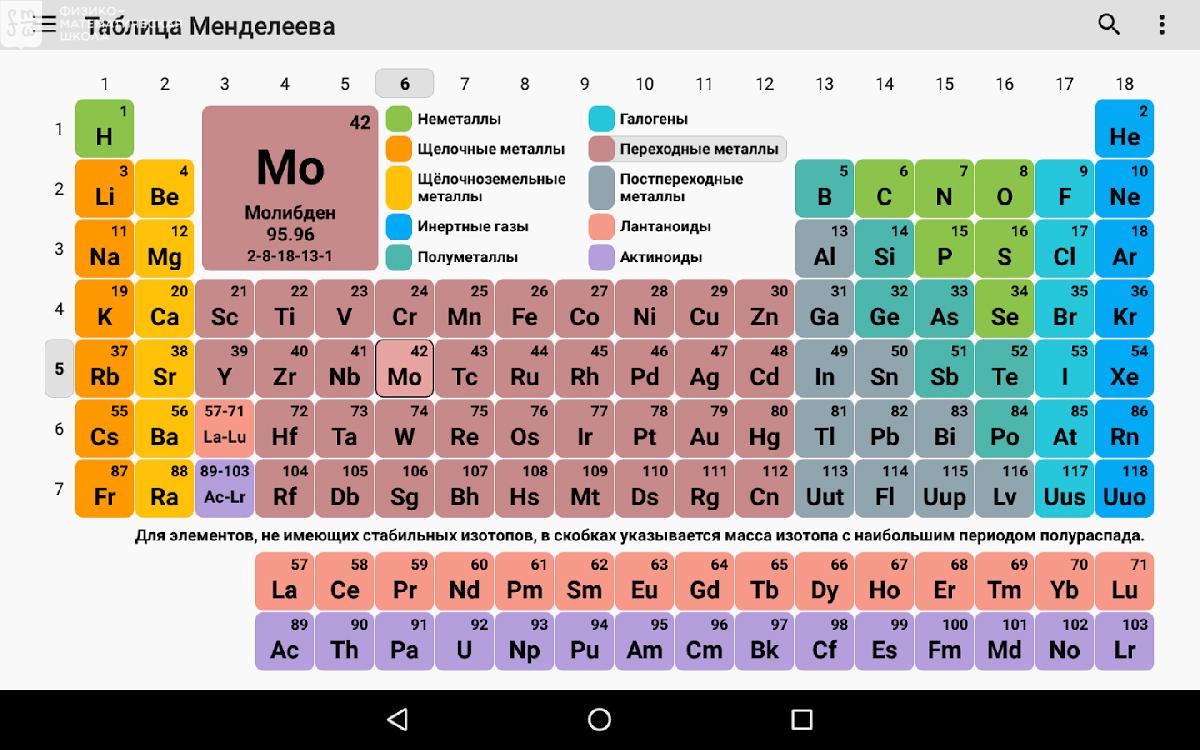
Таким образом, мы можем найти элемент, зная его порядковый номер либо зная номер группы и периода.
Теперь важная ремарка. Элементы в таблице расположены в порядке увеличения заряда ядра, начиная с самого простого атома – атома водорода. Периодический закон в формулировке Менделеева говорил, что свойства элементов находятся в периодической зависимости от атомной массы. То есть элементы должны располагаться в таблице в порядке увеличения атомной массы. Но это нет всегда так: посмотрите на кобальт (порядковый номер 28) и никель (порядковый номер 29) и убедитесь, что атомная масса никеля меньше атомной массы кобальта. Значит, никель должен стоять перед кобальтом? Почему же тогда он стоит после него? Все дело в том, что в 20 веке учёные доказали, что
свойства элементов находятся в периодической зависимости от заряда ядра атома.
Именно так звучит современная формулировка периодического закона (и именно поэтому кобальт стоит перед никелем).
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Периодическая система химических элементов – таблица Менделеева
Периодическая система химических элементов
Периодическая система сформирована из разделенных на группы и периоды химических элементов, отсортированных по определенной закономерности. Попытки составить таблицу химических элементов предпринимали многие ученые, но в известном нам виде, это получилось именно у русского химика Дмитрия Менделеева в 1869 году. Именно по его имени она и получила название таблицы Менделеева. Семействами химических элементов являются щелочные, щёлочноземельные, переходные, постпереходные металлы, полуметаллы, галогены, лантаноиды, актиноиды, благородные газы, и халькогены.
Список химических элементов
| Номер | Название | Символ |
|---|---|---|
| 1 | Водород | H |
| 2 | Гелий | He |
| 3 | Литий | Li |
| 4 | Бериллий | Be |
| 5 | Бор | B |
| 6 | Углерод | C |
| 7 | Азот | N |
| 8 | Кислород | O |
| 9 | Фтор | F |
| 10 | Неон | Ne |
| 11 | Натрий | Na |
| 12 | Магний | Mg |
| 13 | Алюминий | Al |
| 14 | Кремний | Si |
| 15 | Фосфор | P |
| 16 | Сера | S |
| 17 | Хлор | Cl |
| 18 | Аргон | Ar |
| 19 | Калий | K |
| 20 | Кальций | Ca |
| 21 | Скандий | Sc |
| 22 | Титан | Ti |
| 23 | Ванадий | V |
| 24 | Хром | Cr |
| 25 | Марганец | Mn |
| 26 | Железо | Fe |
| 27 | Кобальт | Co |
| 28 | Никель | Ni |
| 29 | Медь | Cu |
| 30 | Цинк | Zn |
| 31 | Галлий | Ga |
| 32 | Германий | Ge |
| 33 | Мышьяк | As |
| 34 | Селен | Se |
| 35 | Бром | Br |
| 36 | Криптон | Kr |
| 37 | Рубидий | Rb |
| 38 | Стронций | Sr |
| 39 | Иттрий | Y |
| 40 | Цирконий | Zr |
| 41 | Ниобий | Nb |
| 42 | Молибден | Mo |
| 43 | Технеций | Tc |
| 44 | Рутений | Ru |
| 45 | Родий | Rh |
| 46 | Палладий | Pd |
| 47 | Серебро | Ag |
| 48 | Кадмий | Cd |
| 49 | Индий | In |
| 50 | Олово | Sn |
| 51 | Сурьма | Sb |
| 52 | Теллур | Te |
| 53 | Иод | I |
| 54 | Ксенон | Xe |
| 55 | Цезий | Cs |
| 56 | Барий | Ba |
| 57 | Лантан | La |
| 58 | Церий | Ce |
| 59 | Празеодим | Pr |
| 60 | Неодим | Nd |
| 61 | Прометий | Pm |
| 62 | Самарий | Sm |
| 63 | Европий | Eu |
| 64 | Гадолиний | Gd |
| 65 | Тербий | Tb |
| 66 | Диспрозий | Dy |
| 67 | Гольмий | Ho |
| 68 | Эрбий | Er |
| 69 | Тулий | Tm |
| 70 | Иттербий | Yb |
| 71 | Лютеций | Lu |
| 72 | Гафний | Hf |
| 73 | Тантал | Ta |
| 74 | Вольфрам | W |
| 75 | Рений | Re |
| 76 | Осмий | Os |
| 77 | Иридий | Ir |
| 78 | Платина | Pt |
| 79 | Золото | Au |
| 80 | Ртуть | Hg |
| 81 | Таллий | Tl |
| 82 | Свинец | Pb |
| 83 | Висмут | Bi |
| 84 | Полоний | Po |
| 85 | Астат | At |
| 86 | Радон | Rn |
| 87 | Франций | Fr |
| 88 | Радий | Ra |
| 89 | Актиний | Ac |
| 90 | Торий | Th |
| 91 | Протактиний | Pa |
| 92 | Уран | U |
| 93 | Нептуний | Np |
| 94 | Плутоний | Pu |
| 95 | Америций | Am |
| 96 | Кюрий | Cm |
| 97 | Берклий | Bk |
| 98 | Калифорний | Cf |
| 99 | Эйнштейний | Es |
| 100 | Фермий | Fm |
| 101 | Менделевий | Md |
| 102 | Нобелий | No |
| 103 | Лоуренсий | Lr |
| 104 | Резерфордий | Rf |
| 105 | Дубний | Db |
| 106 | Сиборгий | Sg |
| 107 | Борий | Bh |
| 108 | Хассий | Hs |
| 109 | Мейтнерий | Mt |
| 110 | Дармштадтий | Ds |
| 111 | Рентгений | Rg |
| 112 | Коперниций | Cn |
| 113 | Нихоний | Nh |
| 114 | Флеровий | Fl |
| 115 | Московий | Mc |
| 116 | Ливерморий | Lv |
| 117 | Теннессин | Ts |
| 118 | Оганесон | Og |
Таблица мирового значения – Поиск-НН
В Москве
Открывая 28 ноября в Фундаментальной библиотеке МГУ им. М. В. Ломоносова торжественную церемонию закрытия года Периодической таблицы химических элементов в России, завершившую отечественную серию мероприятий в рамках Международного года таблицы Менделеева, ректор Виктор Садовничий подчеркнул, что Дмитрий Иванович Менделеев был гениальным человеком, проявившим талант исследователя не только в химии, но и в физической химии и экономике. Сравнив его с гением Максвелла, Фарадея, Кюри, ректор отметил, что русского ученого Менделеева знают во всем мире: его труды показали всему миру, как фундаментальная наука позволяет на столетия вперед предопределять развитие экономики и общества в целом.
М. В. Ломоносова торжественную церемонию закрытия года Периодической таблицы химических элементов в России, завершившую отечественную серию мероприятий в рамках Международного года таблицы Менделеева, ректор Виктор Садовничий подчеркнул, что Дмитрий Иванович Менделеев был гениальным человеком, проявившим талант исследователя не только в химии, но и в физической химии и экономике. Сравнив его с гением Максвелла, Фарадея, Кюри, ректор отметил, что русского ученого Менделеева знают во всем мире: его труды показали всему миру, как фундаментальная наука позволяет на столетия вперед предопределять развитие экономики и общества в целом.
Показанный на церемонии видеоролик напомнил, что, когда 1 марта 1869 г. Д. И. Менделеев закончил свой труд «Опыт системы элементов, основанной на их атомном весе и химическом сходстве», было известно около 60 элементов. Сегодня в таблице их 118, из которых 94 встречаются в природе, а остальные являются синтетическими. Таким образом уже полтора века сбываются слова ученого: «Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются».
Президент РАН Александр Сергеев отметил на церемонии, что благодаря большой работе в рамках Менделеевского года общественное восприятие научной деятельности продвинулось значительно. Различные мероприятия, вошедшие в программу Года, разбудили любопытство сотен тысяч и даже миллионов человек. Предметом этого интереса стала не только сама таблица, сколько тот факт, что все на Земле и в космосе состоит из ограниченного набора элементов, который люди уже знают. Благодаря осмыслению этого обстоятельства, любопытный ум уже задается вопросами: одиноки ли мы во Вселенной, возможны ли другие взаимодействия у тех пяти элементов, из которых состоит ДНК, как на основе знаний о связях уже известных кирпичиков природы создавать принципиально новые материалы и соединения.
По словам Сергеева, это и является самым главным итогом года таблицы Менделеева в России. Благодаря ему люди самых разных занятий и возрастов по-иному посмотрели на мир. И это дает основание быть уверенным в том, что толчок, данный этим проектом, приведет в науку молодежь и безусловно отразится на новых научных успехах. «Спасибо году Менделеева!», — подытожил президент РАН.
«Спасибо году Менделеева!», — подытожил президент РАН.
Первый замминистра науки и высшего образования РФ Григорий Трубников отметил, что закрытие Менделеевского года и достижения в пропаганде химической науки, достигнутые в его рамках, обязательно должны получить свое развитие в десятилетии и даже столетии химии. «Чего бы мы ни касались — это химия!», — заметил он и добавил, что благодаря году таблицы Менделеева люди открыли красоту фундаментальной химии как науки будущего, без которой невозможно развитие человечества.
Как известно, первым масштабным событием в рамках года таблицы Менделеева стала международная образовательно-просветительская акция «Открытая лабораторная», состоявшаяся 9 февраля в 120 городах России и 30 странах; среди вопросов «Лабы» была рубрика, посвященная не только Периодической системе, но и мифам вокруг химии. В целом в России в 2019 г. состоялось более 500 научно-популярных и образовательных мероприятий для школьников, студентов, молодых ученых и людей всех возрастов, приуроченных к 150-летию таблицы Менделеева и направленных на привлечение внимания общества к химии и науке в целом. Среди наиболее значимых событий — Всероссийский фестиваль NAUKA 0+, Всероссийский съезд учителей химии, Всероссийский открытый урок по химии, Всероссийский химический диктант, XXI Менделеевский съезд по общей и прикладной химии, ХХIХ Менделеевская школа-конференция молодых ученых в Иваново, химические турниры ученых и учреждение оргкомитетом V Всероссийской премии «За верность науке» спецноминации «Популяризация химии». Продолжая традиции международного научного сотрудничества, заложенные Менделеевым, по инициативе России учреждена международная премия ЮНЕСКО-России им. Д. И. Менделеева за достижения в области фундаментальных наук. Прием заявок заканчивается 15 марта 2020 г., и первое вручение премии в том же году.
Среди наиболее значимых событий — Всероссийский фестиваль NAUKA 0+, Всероссийский съезд учителей химии, Всероссийский открытый урок по химии, Всероссийский химический диктант, XXI Менделеевский съезд по общей и прикладной химии, ХХIХ Менделеевская школа-конференция молодых ученых в Иваново, химические турниры ученых и учреждение оргкомитетом V Всероссийской премии «За верность науке» спецноминации «Популяризация химии». Продолжая традиции международного научного сотрудничества, заложенные Менделеевым, по инициативе России учреждена международная премия ЮНЕСКО-России им. Д. И. Менделеева за достижения в области фундаментальных наук. Прием заявок заканчивается 15 марта 2020 г., и первое вручение премии в том же году.
Оператором проведения Международного года таблицы Менделеева в России стал Всероссийский фестиваль NAUKA 0+, генеральным партнером — Благотворительный Фонд «Искусство, наука и спорт».
В Токио
Церемония закрытия Международного года Периодической таблицы химических элементов состоялась в Токио 5 декабря. Подвести итоги проекта и обсудить перспективы развития химической науки собрались организаторы Менделеевского года и все причастные к его празднованию: представители мирового научного сообщества, политики, бизнесмены, общественные деятели. По словам председателя исполнительного комитета Международного года Таблицы в Японии Кохэя Тамао, церемония дала возможность оглянуться на многие мероприятия, проведенные во всем мире в честь празднования юбилея таблицы. Эти события прославили работу ученых и инженеров, внесших свой вклад в открытие и развитие Периодической таблицы, и работу тех, кто изучает новые элементы.
Подвести итоги проекта и обсудить перспективы развития химической науки собрались организаторы Менделеевского года и все причастные к его празднованию: представители мирового научного сообщества, политики, бизнесмены, общественные деятели. По словам председателя исполнительного комитета Международного года Таблицы в Японии Кохэя Тамао, церемония дала возможность оглянуться на многие мероприятия, проведенные во всем мире в честь празднования юбилея таблицы. Эти события прославили работу ученых и инженеров, внесших свой вклад в открытие и развитие Периодической таблицы, и работу тех, кто изучает новые элементы.
В церемонии приняла участие представительная делегация из России. Первый замминистра науки и высшего образования РФ Григорий Трубников подчеркнул, что масштабное проведение Международного года таблицы Менделеева позволило расширить области сотрудничества в химии и активизировать обмен высококвалифицированными научными кадрами. Десятки миллионов людей узнали про историю открытия Периодической таблицы, про ее роль в развитии фундаментальной науки. Многочисленные открытые уроки в школах и ряд интерактивных мероприятий позволили вовлечь в атмосферу науки и познания мира огромное количество детей и молодежи. Он обратился к Международному союзу теоретической и прикладной химии (IUPAC) и ЮНЕСКО с просьбой и в дальнейшем привлекать внимание к наследию Д. И. Менделеева, распространив наглядные пособия о Периодическом законе в школах развивающихся стран.
Многочисленные открытые уроки в школах и ряд интерактивных мероприятий позволили вовлечь в атмосферу науки и познания мира огромное количество детей и молодежи. Он обратился к Международному союзу теоретической и прикладной химии (IUPAC) и ЮНЕСКО с просьбой и в дальнейшем привлекать внимание к наследию Д. И. Менделеева, распространив наглядные пособия о Периодическом законе в школах развивающихся стран.
Часть церемонии закрытия была посвящена перспективам развития Периодической таблицы. С докладами на эту тему выступили ученые с мировым именем, работающие над созданием новых элементов. Президент РАН Александр Сергеев дал молодым исследователям пять советов, ставя в пример личность Менделеева, и поделился с участниками церемонии взглядами на будущее Периодической таблицы. Также прозвучали выступления лауреатов Нобелевской премии Макото Кобаяси (физика, 2008 г.) и Акира Есино (химия, 2019 г.). С видеообращением выступил известный популяризатор химии сэр Мартин Поляков, вице-президент Лондонского королевского общества.
В рамках церемонии прошла секция под названием «Создание сверхтяжелых элементов», в ходе которой ученые из научных центров, внесших существенный вклад в синтез и открытие сверхтяжелых элементов, вышли на сцену, чтобы отпраздновать завершение 7-го периода таблицы Менделеева, и обратились с приветствиями к собравшимся. Директор Объединенного института ядерных исследований (Дубна) Виктор Матвеев рассказал об истории и перспективах синтеза новых элементов в институте. Завершил работу секции Юрий Оганесян (единственный живущий на Земле человек, в честь которого назван оганесон, 118-й элемент таблицы Менделеева), отметивший от имени первооткрывателей элементов большой вклад многих научных институтов, международных организаций и стран в синтез и признание открытия новых сверхтяжелых элементов. «Во время церемонии был трогательный момент, когда на сцену вышли руководители шести мировых лабораторий, ведущих синтез таких элементов (Россия, Германия, Япония, три лаборатории из США), с названиями тех элементов таблицы Менделеева, которые они открыли. И все говорили о важности международного научного сотрудничества, которое существенно ускоряет научный поиск. Теперь перед нами стоит следующая задача — сделать так, чтобы премия Менделеева, которая впервые будет присуждаться в следующем году, со временем вошла в число наиболее престижных мировых премий в области фундаментальной науки», — написал в Faсebook вице-президент РАН Алексей Хохлов.
И все говорили о важности международного научного сотрудничества, которое существенно ускоряет научный поиск. Теперь перед нами стоит следующая задача — сделать так, чтобы премия Менделеева, которая впервые будет присуждаться в следующем году, со временем вошла в число наиболее престижных мировых премий в области фундаментальной науки», — написал в Faсebook вице-президент РАН Алексей Хохлов.
Самым ярким итогом празднования Международного года Периодической таблицы стала интерактивная выставка, представленная на церемонии закрытия. Основное внимание в экспозиции было приковано к таблице Менделеева — ее показали в различных формах и исполнении, в том числе самых неожиданных. Российская часть экспозиции была также посвящена таблице и современным достижениям российских ученых, в том числе инновационным разработкам в области ядерной физики и ядерной медицины. ОИЯИ продемонстрировал макет ДЦ-280, являющийся «сердцем» «фабрики сверхтяжелых элементов». Научно-исследовательский физико-химический институт им. Л. Я. Карпова представил макет генератора технеция. Ученые МГУ показали посетителям, как с помощью новых технологий оказаться в кабинете Менделеева и провести опыт в химлаборатории XIX в. Частью экспозиции стала историческая зона с собранием архивных документов и личных вещей ученого. Выставку украсил Молекулярный бар с «химическими» коктейлями.
Члены РАН выступили в Токио с лекциями перед школьниками и студентами, посетили знаменитый японский научный центр RIKEN (Институт физико-химических исследований), провели встречи с коллегами из других стран. «Российская химическая наука очень уважаема во всем мире. Мы это почувствовали на себе во время посещения научного центра RIKEN, в ходе встреч с коллегами, во время открытых уроков и лекций для молодых научных сотрудников, студентов и школьников. Один из пригородов Токио был обширно украшен скульптурами и различными изображениями Периодической таблицы. Российский вклад в науку ценят в Японии», — подчеркнул президент РАН Александр Сергеев. По его мнению, Международный год Периодической таблицы приведет к большому притоку молодежи в науку во всем мире. «Я абсолютно уверен, что через короткое время мы станем свидетелями того, как в науку, прежде всего в химию, придет большой поток талантливой молодежи, увлеченной научным поиском. Этому способствовали мероприятия 2019 года, посвященные таблице Менделеева, и, что немаловажно, Россия в данном процессе сыграла одну из ключевых ролей», — резюмировал он.
По его мнению, Международный год Периодической таблицы приведет к большому притоку молодежи в науку во всем мире. «Я абсолютно уверен, что через короткое время мы станем свидетелями того, как в науку, прежде всего в химию, придет большой поток талантливой молодежи, увлеченной научным поиском. Этому способствовали мероприятия 2019 года, посвященные таблице Менделеева, и, что немаловажно, Россия в данном процессе сыграла одну из ключевых ролей», — резюмировал он.
Международный год таблицы Менделеева укрепил сотрудничество между учеными и различными научными объединениями всего мира, учебными заведениями и промышленностью, позволил установить прочные партнерские отношения для достижений целей в будущем на благо развития химической науки.
Справка 2019 г. был объявлен Генеральной ассамблеей ООН Международным годом Периодической таблицы химических элементов в честь 150-летия открытия Периодического закона великим русским ученым Д. И. Менделеевым. Инициатива о проведении юбилейного года принадлежала Российскому химическому обществу им. Д. И. Менделеева, РАН, Министерству науки и высшего образования РФ, российским и зарубежным ученым и была поддержана десятками национальных и международных научных объединений. Цель инициативы — подчеркнуть научное и технологическое значение системы химических элементов в устойчивом развитии человечества. В результате Международный год таблицы Менделеева прошел под эгидой ЮНЕСКО во многих странах, в том числе в России, Франции, Германии, Испании, США, Японии, ЮАР, Индии, Великобритании, и на шести континентах, включая Антарктиду.
Д. И. Менделеева, РАН, Министерству науки и высшего образования РФ, российским и зарубежным ученым и была поддержана десятками национальных и международных научных объединений. Цель инициативы — подчеркнуть научное и технологическое значение системы химических элементов в устойчивом развитии человечества. В результате Международный год таблицы Менделеева прошел под эгидой ЮНЕСКО во многих странах, в том числе в России, Франции, Германии, Испании, США, Японии, ЮАР, Индии, Великобритании, и на шести континентах, включая Антарктиду.
Свою первую схему таблицы в статье «Соотношение свойств с атомным весом элементов» Д. И. Менделеев опубликовал в 1869 г. в журнале Русского химического общества. С тех пор Периодическая таблица химических элементов является одним из самых значительных достижений в науке, охватывая сущность не только химии, но и всех естественных наук.
Церемония открытия Международного года таблицы Менделеева состоялась 29 января 2019 г. в Париже, в штаб-квартире ЮНЕСКО.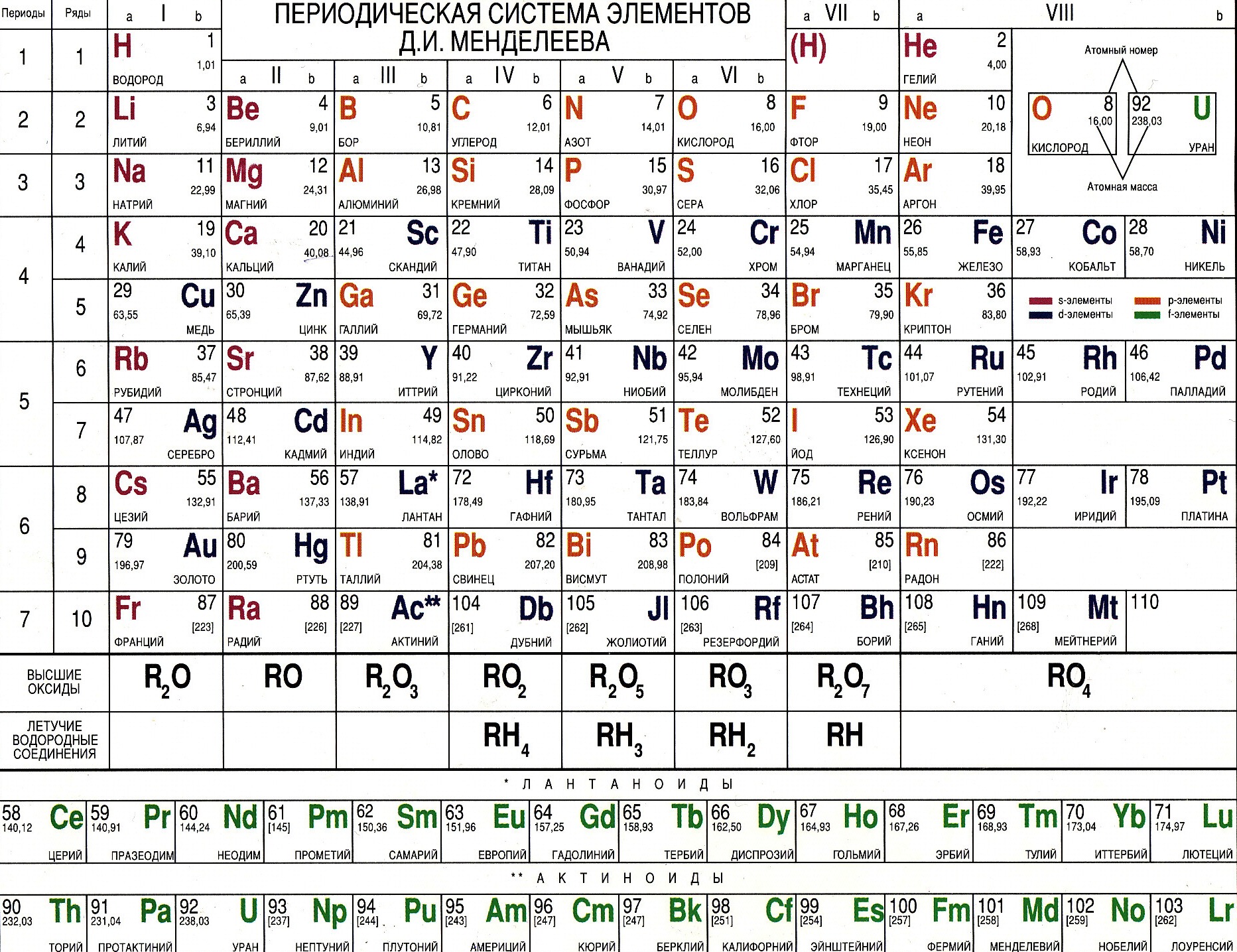 Участниками и гостями открытия стали более 1300 человек из 80 стран — ученые, политики, руководители международных, научных, образовательных организаций, представители бизнеса и общественных объединений.
Участниками и гостями открытия стали более 1300 человек из 80 стран — ученые, политики, руководители международных, научных, образовательных организаций, представители бизнеса и общественных объединений.
Открытие Международного года таблицы Менделеева в России состоялось 6 февраля в Москве, в главном здании РАН. Международный год объединил множество заинтересованных сторон, включая ЮНЕСКО, научные общества в области химии и физики, научные союзы, образовательные и научно-исследовательские учреждения, технологические платформы, некоммерческие организации и частный бизнес для продвижения Периодической таблицы и укрепления ее значимости в мире. Десятки тысяч мероприятий — выставки, фестивали, конференции, презентации, творческие конкурсы, викторины и многие другие, посвященные 150-летию таблицы, — были проведены в школах и вузах.
На ЕНТ по “химии” разрешили носить с собой бумажную таблицу Менделеева
Принято решение допустить пронос бумажных версий таблиц Менделеева и Растворимости солей.

Школьникам, проходящим Единое национальное тестирование (ЕНТ) по предмету “химия”, разрешено проносить с собой привычные бумажные версии Периодической таблицы Дмитрия Менделеева. Об этом, как передает BaigeNews.kz, сообщило в своих аккаунтах в соцсетях РГКП “Национальный центр тестирования” Министерства образования и науки РК.
Как поясняется в сообщении Центра тестирования, адресованном экзаменующимся, в электронном формате тестирования уже были предусмотрены таблицы Менделеева и Растворимости солей в самой программе.
“На экране компьютера отображаются данные таблицы, при наведении на них. Однако, некоторые из Вас обращались к министру Образования и науки РК А. Аймагамбетову с просьбой разрешить использование бумажных таблиц. По поручению министра, нами изучен данный вопрос и использование бумажных версий таблиц не противоречит Правилам. Чтобы Вам было удобнее пользоваться на тестировании своими привычными таблицами Менделеева и Растворимости солей, было принято решение допустить пронос бумажных версий вышеуказанных таблиц.
Все для Вас. Все для того, чтобы Вам было удобно“, — говорится в тексте заявления.
Однако, организаторы ЕНТ предупреждают: “Имейте ввиду, что мы не пропустим бумажные таблицы, в которых есть надписи, формулы и прочие “подсказки”. Мы отнеслись к Вам с пониманием, ждем от Вас такой же реакции”.
Напоминаем, что 6 мая в Казахстане стартовало Единое национальное тестирование, с результатами которого можно участвовать в конкурсе на присуждение государственного образовательного гранта, причем в этом году ЕНТ впервые проводится в электронном формате.
На ЕНТ для поступления в вузы на грант зарегистрировались более 120 тысяч человек, из них в первый день тестирование будут сдавать порядка восьми тысяч выпускников. Абитуриенты могут сдать ЕНТ два раза, при этом они сами выбирают дату и время тестирования. Для участия в конкурсе на получение государственного образовательного гранта поступающие могут предъявить сертификат с лучшим результатом. Это увеличивает шансы претендентов на присуждение гранта.
Абитуриенты могут сдать ЕНТ два раза, при этом они сами выбирают дату и время тестирования. Для участия в конкурсе на получение государственного образовательного гранта поступающие могут предъявить сертификат с лучшим результатом. Это увеличивает шансы претендентов на присуждение гранта.
О том же, что ЕНТ полностью переведут на электронный формат, 26 января сообщил Премьер-министр Аскар Мамин. Полные ответы на вопросы о том, как будет проходить ЕНТ в 2021 году, BaigeNews.kz писало здесь.
Таблица менделеева название знак произношение. Обозначение, произношение, названия и символы химических элементов. Химические вещества и их произношение
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов.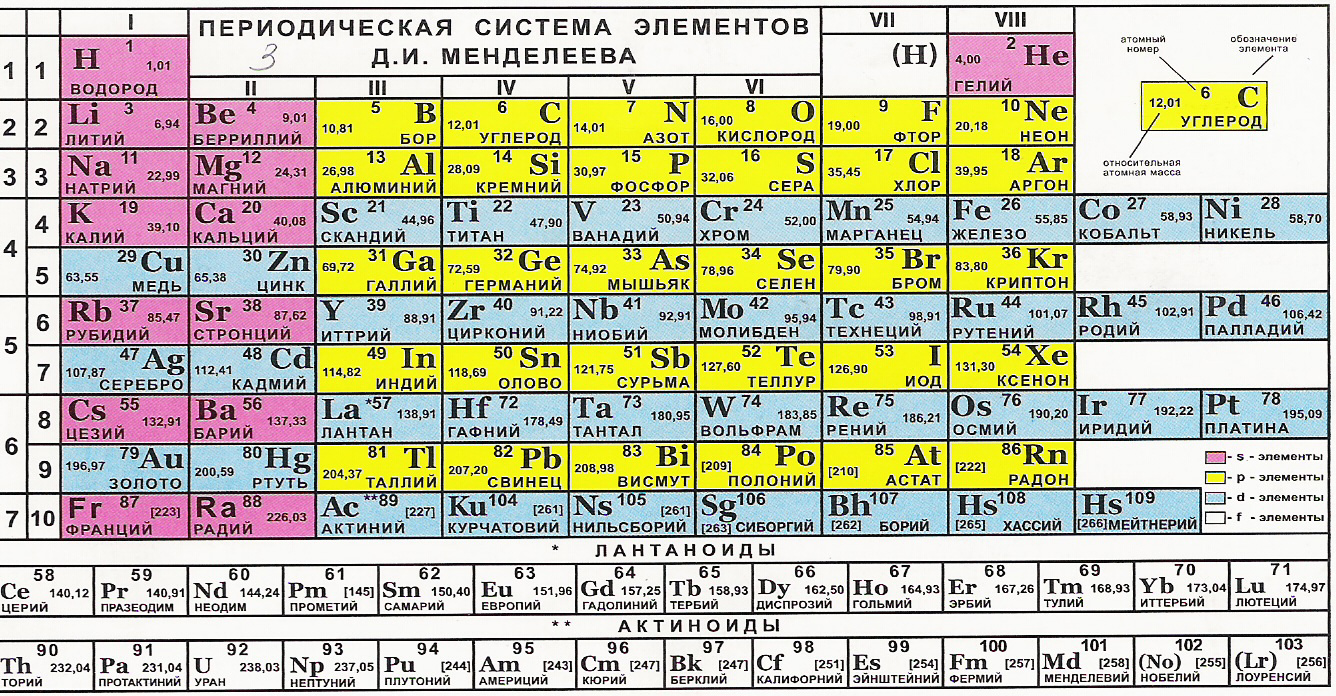 При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.
При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.
Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.
Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс “Таблица Менделеева для чайников”. В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе , который с радостью поделится с вами своими знаниями и опытом.
2.1. Химический язык и его части
Человечество использует много разных языков.
Кроме естественных языков (японского,
английского, русского – всего более 2,5 тысяч),
существуют еще и искусственные языки ,
например, эсперанто. Среди искусственных языков
выделяются языки различных наук .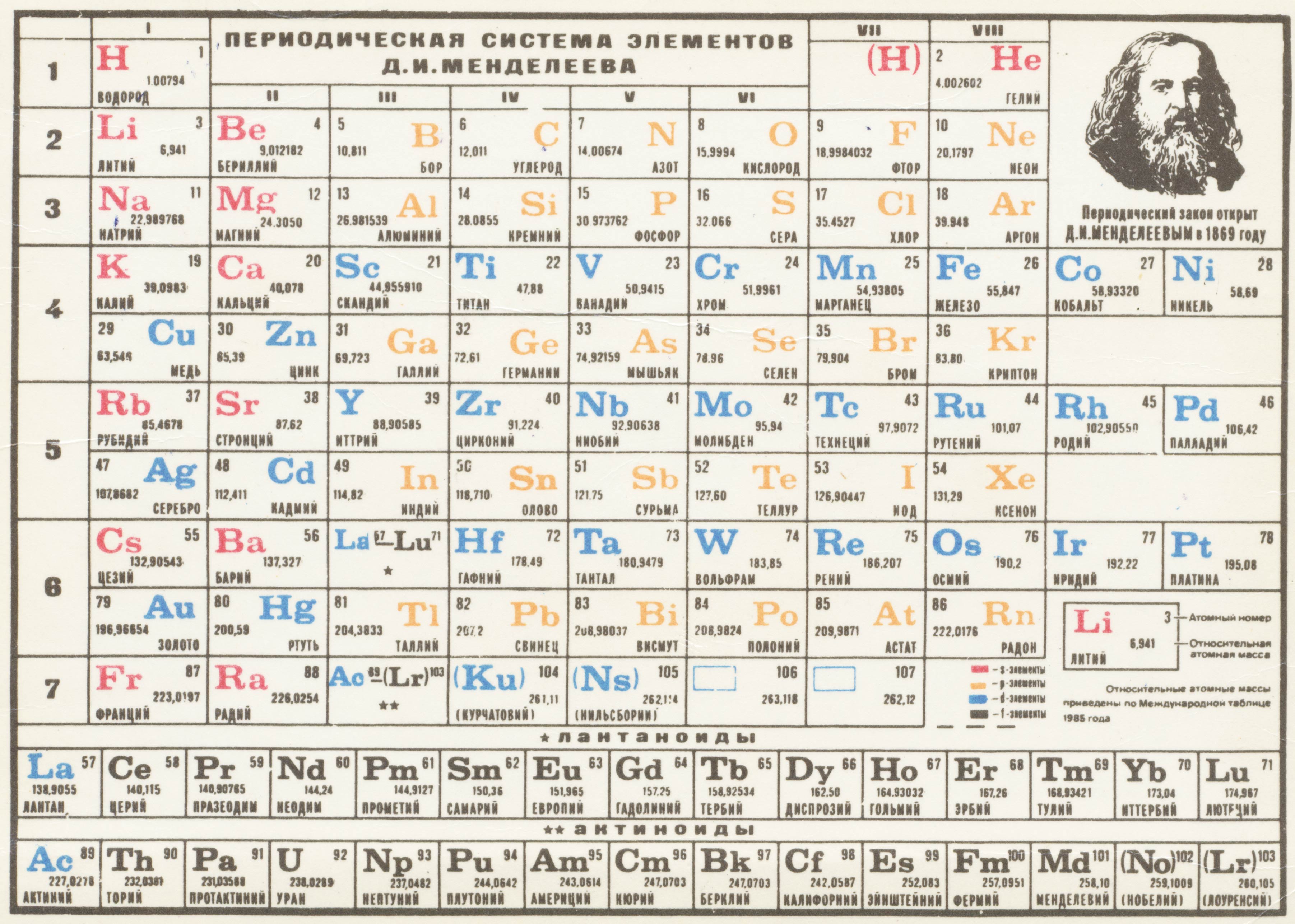 Так, в
химии используется свой, химический язык .
Так, в
химии используется свой, химический язык .
Химический язык – система условных
обозначений и понятий, предназначенная для
краткой, ёмкой и наглядной записи и передачи
химической информации.
Сообщение, написанное на большинстве
естественных языков, делится на предложения,
предложения – на слова, а слова – на буквы. Если
предложения, слова и буквы мы назовем частями
языка, то тогда мы сможем выделить аналогичные
части и в химическом языке (таблица 2).
Таблица 2. Части химического языка
Любым языком овладеть сразу невозможно, это относится и к химическому языку. Поэтому пока вы познакомитесь только с основами этого языка: выучите некоторые ” буквы” , научитесь понимать смысл ” слов” и” предложений” . В конце этой главы вы познакомитесь с названиями химических веществ – неотъемлемой частью химического языка. По мере изучения химии ваше знание химического языка будет расширяться и углубляться.
ХИМИЧЕСКИЙ ЯЗЫК.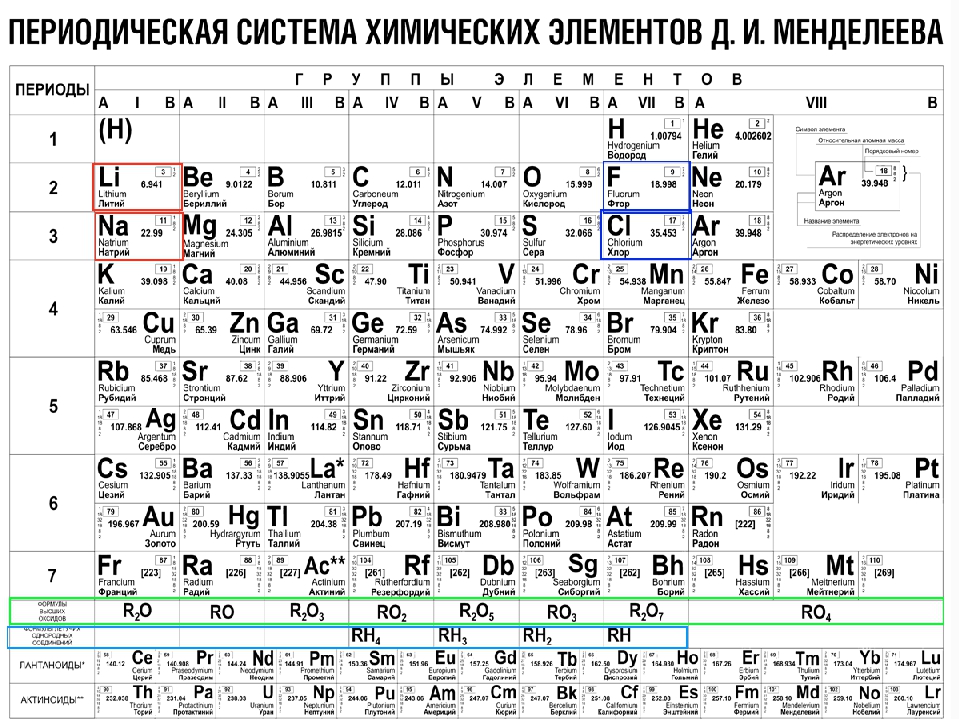
1.Какие искусственные языки вы знаете (кроме
названных в тексте учебника)?
2.Чем естественные языки отличаются от
искусственных?
3.Как вы думаете, можно ли при описании химических
явлений обходиться без использования
химического языка? Если нет, то почему? Если да, то
в чем будут заключаться преимущества, а в чем
недостатки такого описания?
2.2. Символы химических элементов
Символ химического элемента обозначает сам
элемент или один атом этого элемента.
Каждый такой символ представляет собой
сокращенное латинское название химического
элемента, состоящее из одной или двух букв
латинского алфавита (латинский алфавит см. в
приложении 1). Символ пишется с прописной буквы.
Символы, а также русские и латинские названия
некоторых элементов, приведены в таблице 3. Там же
даны сведения о происхождении латинских
названий. Общего правила произношения символов
не существует, поэтому в таблице 3 приводится и
” чтение” символа, то есть, как этот символ
читается в химической формуле.
Заменять символом название элемента в устной
речи нельзя, а в рукописных или печатных текстах
это допускается, но не рекомендуется.В настоящее
время известно 110 химических элементов, у 109 из
них есть названия и символы, утвержденные
Международным союзом теоретической и прикладной
химии (ИЮПАК).
В таблице 3 приведена информация только о 33
элементах. Это те элементы, которые при изучении
химии вам встретятся в первую очередь. Русские
названия (в алфавитном порядке) и символы всех
элементов приведены в приложении 2.
Таблица 3. Названия и символы некоторых химических элементов
Название | ||||
Латинское | Написание | |||
| – | Написание | Происхождение | – | – |
| Азот | N itrogenium | От греч. ” рождающий селитру” ” рождающий селитру” | ” эн” | |
| Алюминий | Al uminium | От лат. ” квасцы” | ” алюминий” | |
| Аргон | Ar gon | От греч. ” недеятельный” | ” аргон” | |
| Барий | Ba rium | От греч. ” тяжелый” | ” барий” | |
| Бор | B orum | От арабск. ” белый минерал” | ” бор” | |
| Бром | Br omum | От греч. ” зловонный” | ” бром” | |
| Водород | H ydrogenium | От греч. ” рождающий воду” ” рождающий воду” | ” аш” | |
| Гелий | He lium | От греч. ” Солнце” | ” гелий” | |
| Железо | Fe rrum | От лат. ” меч” | ” феррум” | |
| Золото | Au rum | От лат. ” горящий” | ” аурум” | |
| Йод | I odum | От греч. ” фиолетовый” | ” йод” | |
| Калий | K alium | От арабск. ” щёлочь” | ” калий” | |
| Кальций | Ca lcium | От лат. ” известняк” ” известняк” | ” кальций” | |
| Кислород | O xygenium | От греч. ” рождающий кислоты” | ” о” | |
| Кремний | Si licium | От лат. ” кремень” | ” силициум” | |
| Криптон | Kr ypton | От греч. ” скрытый” | ” криптон” | |
| Магний | M ag nesium | От назв. полуострова Магнезия | ” магний” | |
| Марганец | M an ganum | От греч. ” очищающий” | ” марганец” | |
| Медь | Cu prum | От греч. назв. о. Кипр назв. о. Кипр | ” купрум” | |
| Натрий | Na trium | От арабск, ” моющее средство” | ” натрий” | |
| Неон | Ne on | От греч. ” новый” | ” неон” | |
| Никель | Ni ccolum | От нем. ” медь святого Николая” | ” никель” | |
| Ртуть | H ydrarg yrum | Лат. ” жидкое серебро” | ” гидраргирум” | |
| Свинец | P lumb um | От лат. названия сплава свинца с
оловом. | ” плюмбум” | |
| Сера | S ulfur | От санскриттского ” горючий порошок” | ” эс” | |
| Серебро | A rg entum | От греч. ” светлый” | ” аргентум” | |
| Углерод | C arboneum | От лат. ” уголь” | ” цэ” | |
| Фосфор | P hosphorus | От греч. ” несущий свет” | ” пэ” | |
| Фтор | F luorum | От лат. глагола ” течь” | ” фтор” | |
| Хлор | Cl orum | От греч.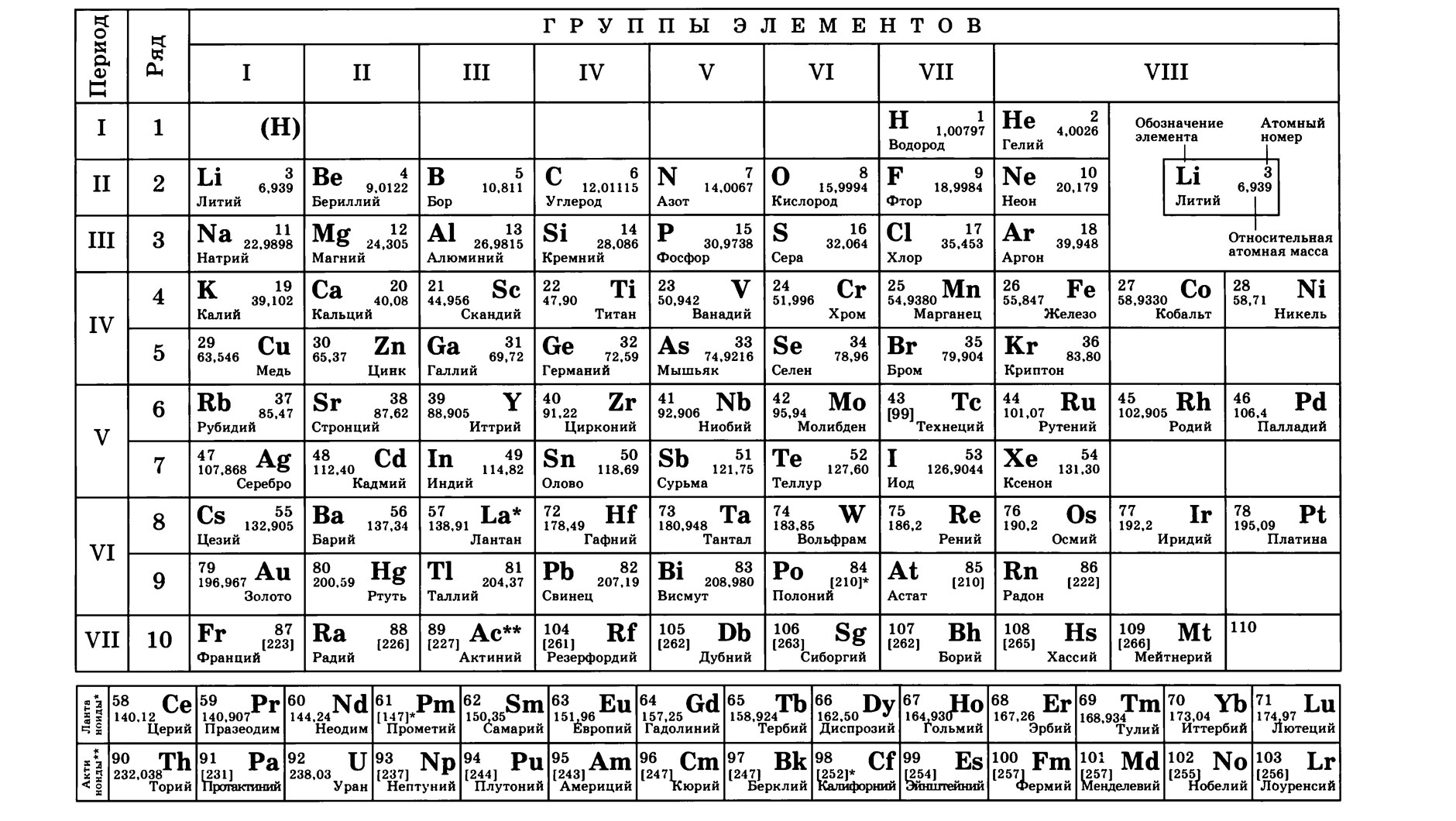 ” зеленоватый” ” зеленоватый” | ” хлор” | |
| Хром | C hr omium | От греч. ” краска” | ” хром” | |
| Цезий | C aes ium | От лат. ” небесно-голубой” | ” цезий” | |
| Цинк | Z in cum | От нем. ” олово” | ” цинк” | |
2.3. Химические формулы
Для обозначения химических веществ используют химические формулы .
Для молекулярных веществ химическая формула
может обозначать и одну молекулу этого вещества.
Информация о веществе может быть разной, поэтому
существуют разные типы химических формул .
В зависимости от полноты информации химические
формулы делятся на четыре основных типа: простейшие , молекулярные , структурные и пространственные .
Подстрочные индексы в простейшейформуле не
имеют общего делителя.
Индекс ” 1″ в формулах не ставится.
Примеры простейших формул: вода – Н 2 О,
кислород – О, сера – S, оксид фосфора – P 2 O 5 ,
бутан – C 2 H 5 , фосфорная кислота – H 3 PO 4 ,
хлорид натрия (поваренная соль) – NaCl.
Простейшая формула воды (Н 2 О) показывает,
что в состав воды входит элемент водород (Н) и
элемент кислород (О), причем в любой порции
(порция – часть чего-либо, что может быть
разделено без утраты своих свойств.) воды число
атомов водорода в два раза больше числа атомов
кислорода.
Число частиц , в том числе и число атомов ,
обозначается латинской буквой N . Обозначив
число атомов водорода – N H , а число
атомов кислорода – N O , мы можем
записать, что
Или N H: N O = 2: 1.
Простейшая формула фосфорной кислоты (Н 3 РО 4) показывает, что в состав фосфорной кислоты входят атомы водорода , атомы фосфора и атомы кислорода , причем отношение чисел атомов этих элементов в любой порции фосфорной кислоты равно 3:1:4, то есть
N H: N P: N O = 3: 1: 4.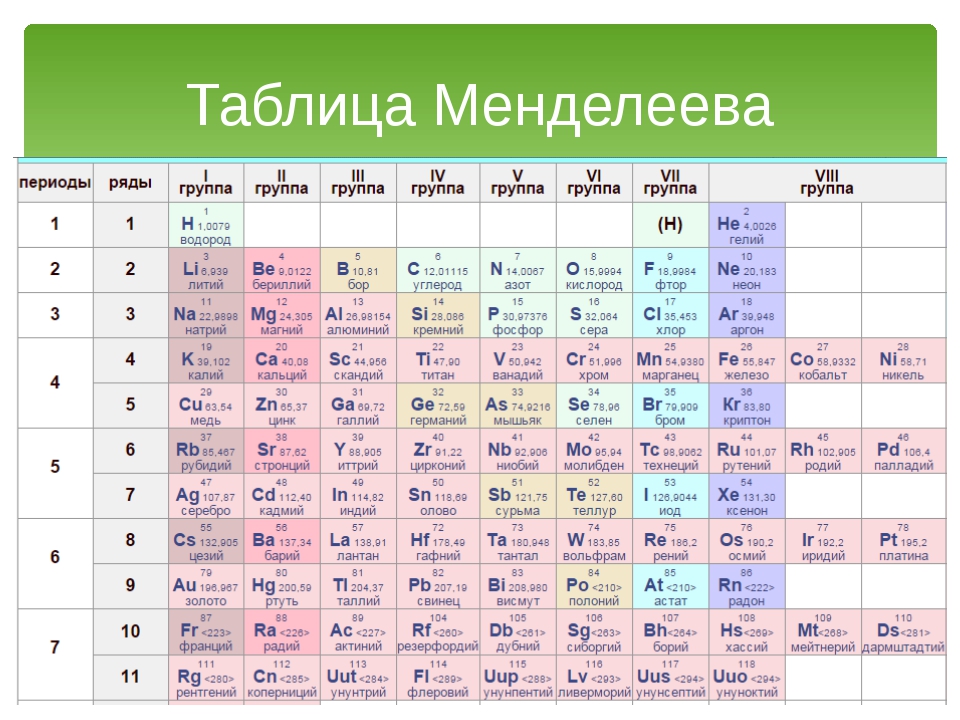
Простейшая формула может быть составлена для любого индивидуального химического вещества, а для молекулярного вещества, кроме того, может быть составлена молекулярная формула .
Примеры молекулярных формул: вода – H 2 O, кислород – O 2 , сера – S 8 , оксид фосфора – P 4 O 10 , бутан – C 4 H 10 , фосфорная кислота – H 3 PO 4 .
У немолекулярных веществ молекулярных формул нет.
Последовательность записи символов элементов в простейших и молекулярных формулах определяется правилами химического языка, с которыми вы познакомитесь по мере изучения химии. На информацию, передаваемую этими формулами, последовательность символов влияния не оказывает.
Из знаков, отражающих строение веществ, мы будем использовать пока только валентный штрих (” черточку”). Этот знак показывает наличие между атомами так называемой ковалентной связи (что это за тип связи и каковы его особенности, вы скоро узнаете).
В молекуле воды атом кислорода связан простыми
(одинарными) связями с двумя атомами водорода, а
атомы водорода между собой не связаны. Именно это
наглядно показывает структурная формула воды.
Именно это
наглядно показывает структурная формула воды.
Другой пример: молекула серы S 8 . В этой молекуле 8 атомов серы образуют восьмичленный цикл, в котором каждый атом серы связан с двумя другими атомами простыми связями. Сравните структурную формулу серы с объемной моделью ее молекулы, показанной на рис. 3. Обратите внимание на то, что структурная формула серы не передает форму ее молекулы, а показывает только последовательность соединения атомов ковалентными связями.
Структурная формула фосфорной кислоты показывает, что в молекуле этого вещества один из четырех атомов кислорода связан только с атомом фосфора двойной связью, а атом фосфора, в свою очередь, связан еще с тремя атомами кислорода простыми связями. Каждый из этих трех атомов кислорода, кроме того, связан простой связью с одним из трех имеющихся в молекуле атомов водорода./p>
Сравните приведенную ниже объемную модель молекулы метана с его пространственной, структурной и молекулярной формулой:
В пространственной формуле метана
клиновидныевалентные штрихи как бы в
перспективе показывают, какой из атомов водорода
находится ” ближе к нам” , а какой ” дальше
от нас” .
Иногда в пространственной формуле указывают длины связей и значения углов между связями в молекуле, как это показано на примере молекулы воды.
Немолекулярные вещества не содержат молекул. Для удобства проведения химических расчетов в немолекулярном веществе выделяют так называемую формульную единицу .
Примеры состава формульных единиц некоторых веществ: 1) диоксид кремния (кварцевый песок, кварц) SiO 2 – формульная единица состоит из одного атома кремния и двух атомов кислорода; 2) хлорид натрия (поваренная соль) NaCl – формульная единица состоит из одного атома натрия и одного атома хлора; 3) железо Fe – формульная единица состоит из одного атома железа.Как и молекула, формульная единица – наименьшая порция вещества, сохраняющая его химические свойства.
Таблица 4
Информация, передаваемая формулами разных типов
Тип формулы | Информация,
передаваемая формулой. | |
| Простейшая Молекулярная Структурная Пространственная |
| |
Рассмотрим теперь на примерах, какую информацию дают нам формулы разных типов.
1. Вещество: уксусная кислота . Простейшая формула – СН 2 О, молекулярная формула – C 2 H 4 O 2 , структурная формула
Простейшая формула говорит нам, что
1) в состав уксусной кислоты входит углерод,
водород и кислород;
2) в этом веществе число атомов углерода
относится к числу атомов водорода и к числу
атомов кислорода, как 1:2:1, то есть N H: N C:N O = 1:2:1.
Молекулярная формула добавляет, что
3) в молекуле уксусной кислоты – 2 атома углерода,
4 атома водорода и 2 атома кислорода.
Структурная формула добавляет, что
4, 5) в молекуле два атома углерода связаны между
собой простой связью; один из них, кроме этого,
связан с тремя атомами водорода, с каждым простой
связью, а другой – с двумя атомами кислорода, с
одним – двойной связью, а с другим – простой;
последний атом кислорода связан еще простой
связью с четвертым атомом водорода.
2. Вещество: хлорид натрия . Простейшая формула – NaCl.
1) В состав хлорида натрия входит натрий и хлор.
2) В этом веществе число атомов натрия равно числу
атомов хлора.
3. Вещество: железо . Простейшая
формула – Fe.
1) В состав этого вещества входит только железо,
то есть это простое вещество.
4. Вещество: триметафосфорная кислота . Простейшая формула – HPO 3 , молекулярная формула – H 3 P 3 O 9 , структурная формула
1) В состав триметафосфорной кислоты входит
водород, фосфор и кислород.
2) N H: N P:N O = 1:1:3.
3) Молекула состоит из трех атомов водорода, трех
атомов фосфора и девяти атомов кислорода.
4, 5) Три атома фосфора и три атома кислорода,
чередуясь, образуют шестичленный цикл. Все связи
в цикле простые. Каждый атом фосфора, кроме того,
связан еще с двумя атомами кислорода, причем с
одним – двойной связью, а с другим – простой.
Каждый из трех атомов кислорода, связанных
простыми связямис атомами фосфора, связан еще
простой связью с атомом водорода.
Фосфорная кислота – H 3 PO 4 (другое название – ортофосфорная кислота) –
прозрачное бесцветное кристаллическое вещество
молекулярного строения, плавящееся при 42 o С.
Это вещество очень хорошо растворяется в воде и
даже поглощает пары воды из воздуха
(гигроскопично). Фосфорную кислоту производят в
больших количествах и используют прежде всего в
производстве фосфорных удобрений, а также в
химической промышленности, при производстве
спичек и даже в строительстве. Кроме того,
фосфорная кислота применяется при изготовлении
цемента в зубоврачебной технике, входит в состав
многих лекарственных средств. Эта кислота
достаточно дешева, поэтому в некоторых странах,
например в США, очень чистая сильно разбавленная
водой фосфорная кислота добавляется в
освежающие напитки для замены дорогой лимонной
кислоты. Кроме того,
фосфорная кислота применяется при изготовлении
цемента в зубоврачебной технике, входит в состав
многих лекарственных средств. Эта кислота
достаточно дешева, поэтому в некоторых странах,
например в США, очень чистая сильно разбавленная
водой фосфорная кислота добавляется в
освежающие напитки для замены дорогой лимонной
кислоты. |
Метан – CH 4 . Если у вас
дома есть газовая плита, то с этим веществом вы
сталкиваетесь ежедневно: природный газ, который
горит в конфорках вашей плиты, на 95 % состоит из
метана. Метан – газ без цвета и запаха с
температурой кипения –161 o С. В смеси с
воздухом он взрывоопасен, этим и объясняются
происходящие иногда в угольных шахтах взрывы и
пожары (другое название метана – рудничный газ).
Третье название метана – болотный газ – связано
с тем, что пузырьки именно этого газа поднимаются
со дна болот, где он образуется в результате
деятельности некоторых бактерий. В
промышленности метан используется как топливо и
сырье для производства других веществ. Метан
является простейшим углеводородом . К этому
классу веществ относятся также этан (C 2 H 6),
пропан (C 3 H 8), этилен (C 2 H 4),
ацетилен (C 2 H 2) и многие другие
вещества. Метан
является простейшим углеводородом . К этому
классу веществ относятся также этан (C 2 H 6),
пропан (C 3 H 8), этилен (C 2 H 4),
ацетилен (C 2 H 2) и многие другие
вещества. |
Таблица 5 . Примеры формул разных типов для некоторых веществ –
Все названия химических элементов происходят из латинского языка. Это необходимо в первую очередь для того, чтобы ученые разных стран могли понимать друг друга.
Химические знаки элементов
Элементы принято обозначать химическими знаками (символами). По предложению шведского химика Берцелиуса (1813 г.) химические элементы обозначают начальной или начальной и одной из последующих букв латинского названия данного элемента; первая буква всегда прописная, вторая строчная. Например, водород (Hydrogenium) обозначается буквой H, кислород (Oxygenium) – буквой O, сера (Sulfur) – буквой S; ртуть (Hydrargyrum) – буквами Hg, алюминий (Aluminium) – Al, железо (Ferrum) – Fe и т. д.
Рис.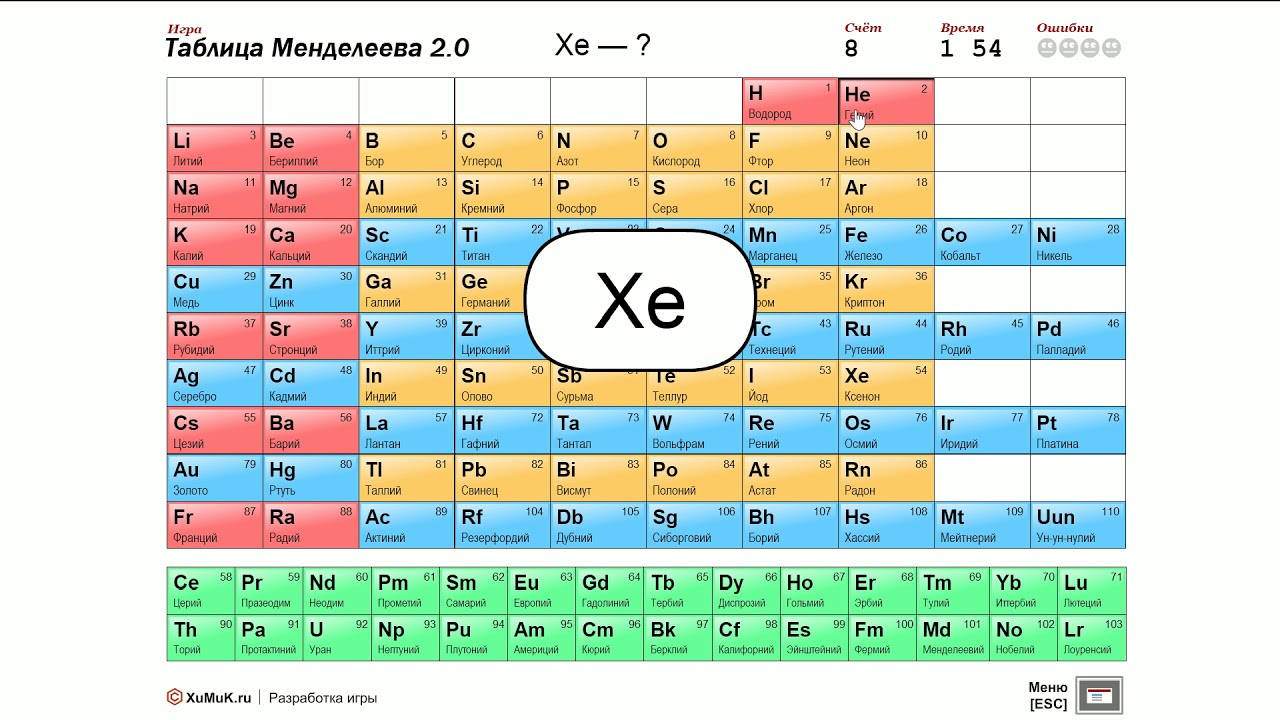 1. Таблица химических элементов с названиями на латинском и русском языке.
1. Таблица химических элементов с названиями на латинском и русском языке.
Русские названия химических элементов зачастую представляют собой латинские названия с видоизмененными окончаниями. Но также существует множество элементов, произношение которых отличается от латинского первоисточника. Это либо коренные русские слова (например, железо), либо слова, которые являются переводом (пример – кислород).
Химическая номенклатура
Химическая номенклатура – правильное наименование химических веществ. Латинское слово nomenclatura переводится как «перечень имен, названий»
На ранней стадии развития химии веществам давались произвольные, случайные наименования (тривиальные названия). Легколетучие жидкости назывались спиртами, к ним относились «соляной спирт» – водный раствор соляной кислоты, «силитряный спирт» – азотная кислота, «нашатырный спирт» – водный раствор аммиака. Маслообразные жидкости и твердые вещества назывались маслами, например, концентрированная серная кислота носила название «купоросное масло», хлорид мышьяка – «мышьяковое масло».
Иногда вещества получали название по имени его первооткрывателя, например, «глауберова соль» Na 2 SO 4 *10H 2 O, открытая немецким химиком И. Р. Глаубером в XVII веке.
Рис. 2. Портрет И. Р. Глаубер.
В старинных названиях могли указываться вкус веществ, цвет, запах, внешний вид, медицинское действие. Одно вещество иногда имело несколько наименований.
К концу XVIII века химикам было известно не более 150-200 соединений.
Первую систему научных названий в химии выработала в 1787 г. комиссия химиков во главе с А. Лавуазье. Химическая номенклатура Лавуазье послужила основой для создания национальных химических номенклатур. Для того, чтобы химики разных стран понимали друг друга, номенклатура должна быть единой. В настоящее время построение химических формул и названий неорганических веществ подчиняется системе номенклатурных правил, созданной комиссией Международного союза теоретической и прикладной химии (ИЮПАК). Каждое вещество изображается формулой, в соответствии с ней строится систематическое название соединения.
Рис. 3. А. Лавуазье.
Что мы узнали?
Все химические элементы имеют латинские корни. Латинские названия химических элементов являются общепринятыми. В русский язык они переносятся с помощью калькирования или перевода. однако некоторые слова имеют изначально русское значение, например, медь или железо. Химической номенклатуре подчиняются все химические вещества, состоящие из атомов и молекул. впервые система научных названий была разработана А. Лавуазье.
Тест по теме
Оценка доклада
Средняя оценка: 4.2 . Всего получено оценок: 768.
Инструкция
Периодическая система представляет собой многоэтажный «дом», в котором располагается большое количество квартир. Каждый «жилец» или в своей собственной квартире под определенным номером, который является постоянным. Помимо этого элемент имеет «фамилию» или название, например кислород, бор или азот. Кроме этих данных в каждой «квартире» или указана такая информация, как относительная атомная масса, которая может иметь точные или округленные значения.
Как в любом доме, здесь имеются «подъезды», а именно группы. Причем в группах элементы располагаются слева и справа, образуя . В зависимости от того, с какой стороны их больше, та называется главной. Другая подгруппа, соответственно, будет побочной. Также в таблице имеются «этажи» или периоды. Причем периоды могут быть как большими (состоят из двух рядов) так и малыми (имеют только один ряд).
По таблице можно показать строение атома элемента, каждый из которых имеет положительно заряженное ядро, состоящее из протонов и нейтронов, а также вращающихся вокруг него отрицательно заряженных электронов. Число протонов и электронов численно совпадает и определяется в таблице по порядковому номеру элемента. Например, химический элемент сера имеет №16, следовательно, будет иметь 16 протонов и 16 электронов.
Чтобы определить количество нейтронов (нейтральных частиц, также расположенных в ядре) вычтите из относительной атомной массы элемента его порядковый номер. Например, железо имеет относительную атомную массу равную 56 и порядковый номер 26. Следовательно, 56 – 26 = 30 протонов у железа.
Следовательно, 56 – 26 = 30 протонов у железа.
Электроны находятся на разном расстоянии от ядра, образуя электронные уровни. Чтобы определить число электронных (или энергетических) уровней, нужно посмотреть на номер периода, в котором располагается элемент. Например, алюминий находится в 3 периоде, следовательно, у него будет 3 уровня.
По номеру группы (но только для главной подгруппы) можно определить высшую валентность. Например, элементы первой группы главной подгруппы (литий, натрий, калий и т.д.) имеют валентность 1. Соответственно, элементы второй группы (бериллий, магний, кальций и т.д.) будут иметь валентность равную 2.
Также по таблице можно проанализировать свойства элементов. Слева направо металлические свойства ослабевают, а неметаллические усиливаются. Это хорошо видно на примере 2 периода: начинается щелочным металлом натрием, затем щелочноземельный металл магний, после него амфотерный элемент алюминий, затем неметаллы кремний, фосфор, сера и заканчивается период газообразными веществами – хлором и аргоном. В следующем периоде наблюдается аналогичная зависимость.
В следующем периоде наблюдается аналогичная зависимость.
Сверху вниз также наблюдается закономерность – металлические свойства усиливаются, а неметаллические ослабевают. То есть, например, цезий гораздо активнее по сравнению с натрием.
Как пользоваться Периодической таблицей элементов
Периодическая таблица элементов содержит самую разнообразную информацию. В большинстве таблиц указаны как минимум символы элементов, атомный номер и атомная масса. Таблица Менделеева организована таким образом, чтобы вы могли сразу увидеть тенденции в свойствах элементов. Вот как использовать периодическую таблицу для сбора информации об элементах.
Организация периодической таблицы
Zoky10ka / Getty Images
Таблица Менделеева содержит информационные ячейки для каждого элемента, упорядоченные по возрастанию атомного номера и химических свойств.Ячейка каждого элемента обычно содержит много важной информации об этом элементе.
Символы элемента – это аббревиатуры имени элемента. В некоторых случаях аббревиатура происходит от латинского названия элемента. Каждый символ состоит из одной или двух букв. Обычно символ представляет собой аббревиатуру имени элемента, но некоторые символы относятся к более старым названиям элементов (например, символ серебра – Ag, что соответствует его старому имени, argentum) .
В некоторых случаях аббревиатура происходит от латинского названия элемента. Каждый символ состоит из одной или двух букв. Обычно символ представляет собой аббревиатуру имени элемента, но некоторые символы относятся к более старым названиям элементов (например, символ серебра – Ag, что соответствует его старому имени, argentum) .
Современная таблица Менделеева организована в порядке возрастания атомного номера.Атомный номер – это количество протонов в атоме этого элемента. Количество протонов является решающим фактором при различении одного элемента от другого. Изменение количества электронов или нейтронов не меняет тип элемента. При изменении количества электронов образуются ионы, а при изменении количества нейтронов – изотопы.
Атомная масса элемента в атомных единицах массы – это средневзвешенная масса изотопов элемента. Иногда в таблице Менделеева указывается одно значение атомного веса.Другие таблицы включают два числа, которые представляют диапазон значений. Диапазон указан потому, что содержание изотопов варьируется от одного места отбора проб к другому. В оригинальной периодической таблице Менделеева элементы организованы в порядке увеличения атомной массы или веса.
Диапазон указан потому, что содержание изотопов варьируется от одного места отбора проб к другому. В оригинальной периодической таблице Менделеева элементы организованы в порядке увеличения атомной массы или веса.
Вертикальные столбцы называются группами. Каждый элемент в группе имеет одинаковое количество валентных электронов и обычно ведет себя аналогичным образом при соединении с другими элементами. Горизонтальные ряды называются периодами.Каждый период указывает на самый высокий уровень энергии, который электроны этого элемента занимают в основном состоянии. Две нижние строки – лантаноиды и актиниды – все относятся к группе 3B и указаны отдельно.
Многие периодические таблицы включают название элемента, чтобы помочь тем, кто не помнит все символы элементов. Многие периодические таблицы идентифицируют типы элементов, используя разные цвета для разных типов элементов. К ним относятся щелочные металлы, щелочноземельные металлы, основные металлы, полуметаллы и переходные металлы.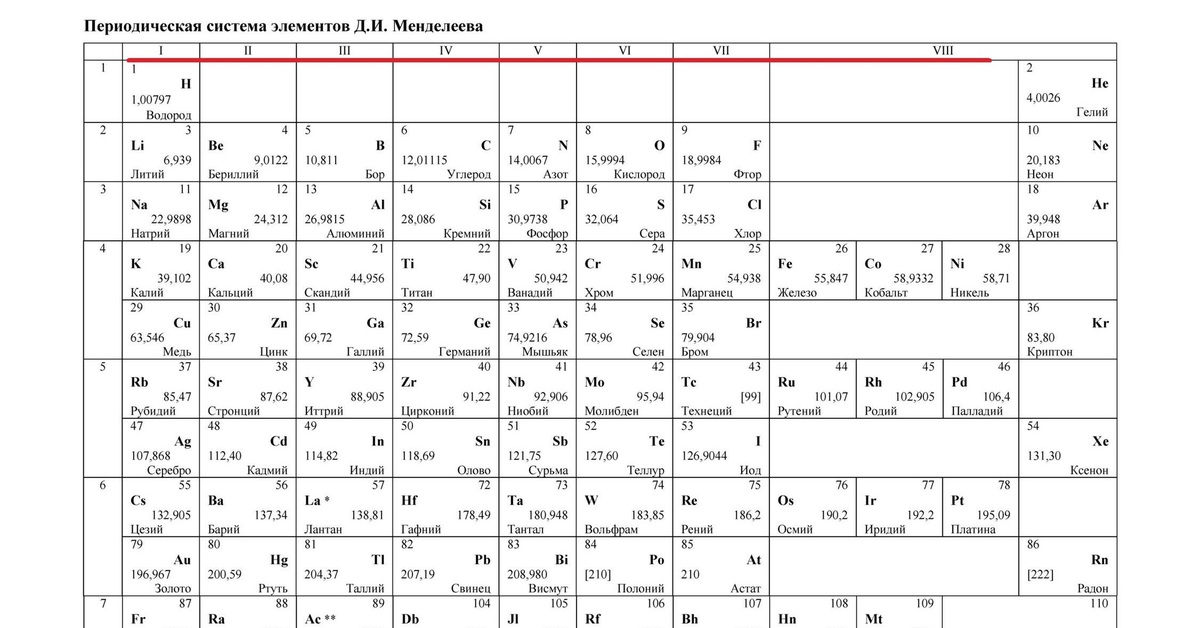
Тенденции периодической таблицы
ThoughtCo / Марица Патринос
Таблица Менделеева организована таким образом, чтобы продемонстрировать различные тенденции (периодичность).
- Атомный радиус (половина расстояния между центрами двух атомов, просто соприкасающихся друг с другом)
- увеличивает перемещение сверху вниз по таблице
- уменьшается при перемещении слева направо по таблице
- Энергия ионизации (энергия, необходимая для удаления электрона из атома)
- убывает, двигаясь сверху вниз
- увеличивается при перемещении слева направо
- Электроотрицательность (мера способности образовывать химическую связь)
- убывает, двигаясь сверху вниз
- увеличивается при перемещении слева направо
Сродство к электрону
Способность принимать электрон, сродство к электрону можно предсказать на основе групп элементов.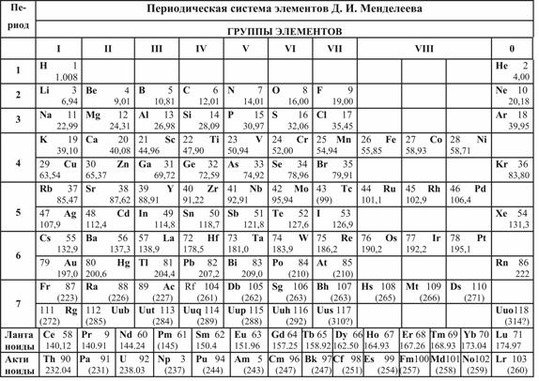 Благородные газы (например, аргон и неон) имеют близкое к нулю сродство к электрону и не принимают электроны. Галогены (например, хлор и йод) обладают высоким сродством к электрону. Большинство других групп элементов имеют сродство к электрону ниже, чем у галогенов, но больше, чем у благородных газов.
Благородные газы (например, аргон и неон) имеют близкое к нулю сродство к электрону и не принимают электроны. Галогены (например, хлор и йод) обладают высоким сродством к электрону. Большинство других групп элементов имеют сродство к электрону ниже, чем у галогенов, но больше, чем у благородных газов.
Большинство элементов – металлы. Металлы, как правило, являются хорошими электрическими и теплопроводными, твердыми и блестящими. Неметаллы сгруппированы в верхнем правом углу таблицы Менделеева. Исключение составляет водород, который находится в верхнем левом углу таблицы.
Таблица Менделеева: быстрые факты
- Периодическая таблица представляет собой графическую коллекцию данных об элементах.
- В таблице перечислены химические элементы в порядке возрастания атомного номера, который представляет собой количество протонов в атоме элемента.
- Строки (точки) и столбцы (группы) организуют элементы в соответствии с аналогичными свойствами.
 Например, все элементы в первом столбце представляют собой химически активные металлы с валентностью +1. Все элементы в ряду имеют одинаковую внешнюю электронную оболочку.
Например, все элементы в первом столбце представляют собой химически активные металлы с валентностью +1. Все элементы в ряду имеют одинаковую внешнюю электронную оболочку.
Хорошая таблица Менделеева – отличный инструмент для решения задач химии. Вы можете использовать онлайн-таблицу Менделеева или распечатать свою собственную. Как только вы освоитесь с частями таблицы Менделеева, поинтересуйтесь, насколько хорошо вы ее читаете.
Стратегия теста SAT Chemistry: как пользоваться периодической таблицей
Что можно найти в таблице Менделеева?
Давайте посмотрим на элемент рубидий (Rb), чтобы рассмотреть типы информации, которую вы можете найти в периодической таблице:
- Атомарный символ – это сокращение имени элемента.
- Имя элемента – это общее имя элемента.
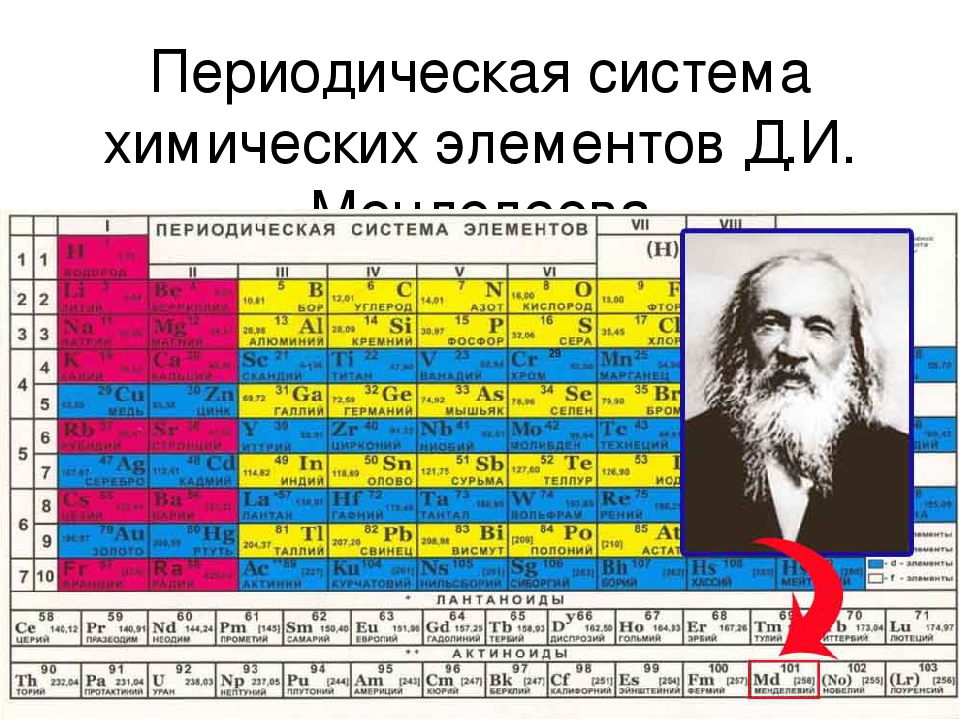
- Вверху находится атомный номер , который представляет количество протонов в атомном ядре элемента. Он также представляет собой количество электронов в электронном облаке, окружающем атомное ядро.
- Внизу, под названием элемента, вы увидите атомную массу . Это размер атома.
Periodic Trending
Тенденции периодической таблицы позволяют нам узнать еще больше о свойствах элемента, а также о том, насколько он реагирует с другими элементами. Давайте рассмотрим несколько различных периодических тенденций:
Атомный радиус – это измерение размера атомов в элементе. Обычно это расстояние от ядра до внешнего края электронного облака. (Вы также можете думать об этом как о половине расстояния между ядрами двух атомов.) Так каков тренд атомного радиуса в периодической таблице? Атомный радиус увеличивается при перемещении справа налево по таблице периодов, а также при перемещении сверху вниз.
Электроотрицательность – это свойство, которое говорит вам о тенденции атома притягивать электроны. Молекула образуется, когда два или более атома соединяются вместе.Часто эти атомы разделяют электроны, образуя эту связь. Однако это распределение не всегда равнозначно. Если вы можете предсказать электроотрицательность, то вы сможете определить, какие атомы будут разделять больше всего электронов, какие просто жадные и даже украдут электроны у других атомов.
Как показано на изображении ниже, тенденция электроотрицательности противоположна тенденции атомного радиуса. Электроотрицательность увеличивается, когда вы перемещаетесь от снизу вверх и слева направо .
Энергия ионизации – это количество энергии, необходимое для отвода электрона от атома.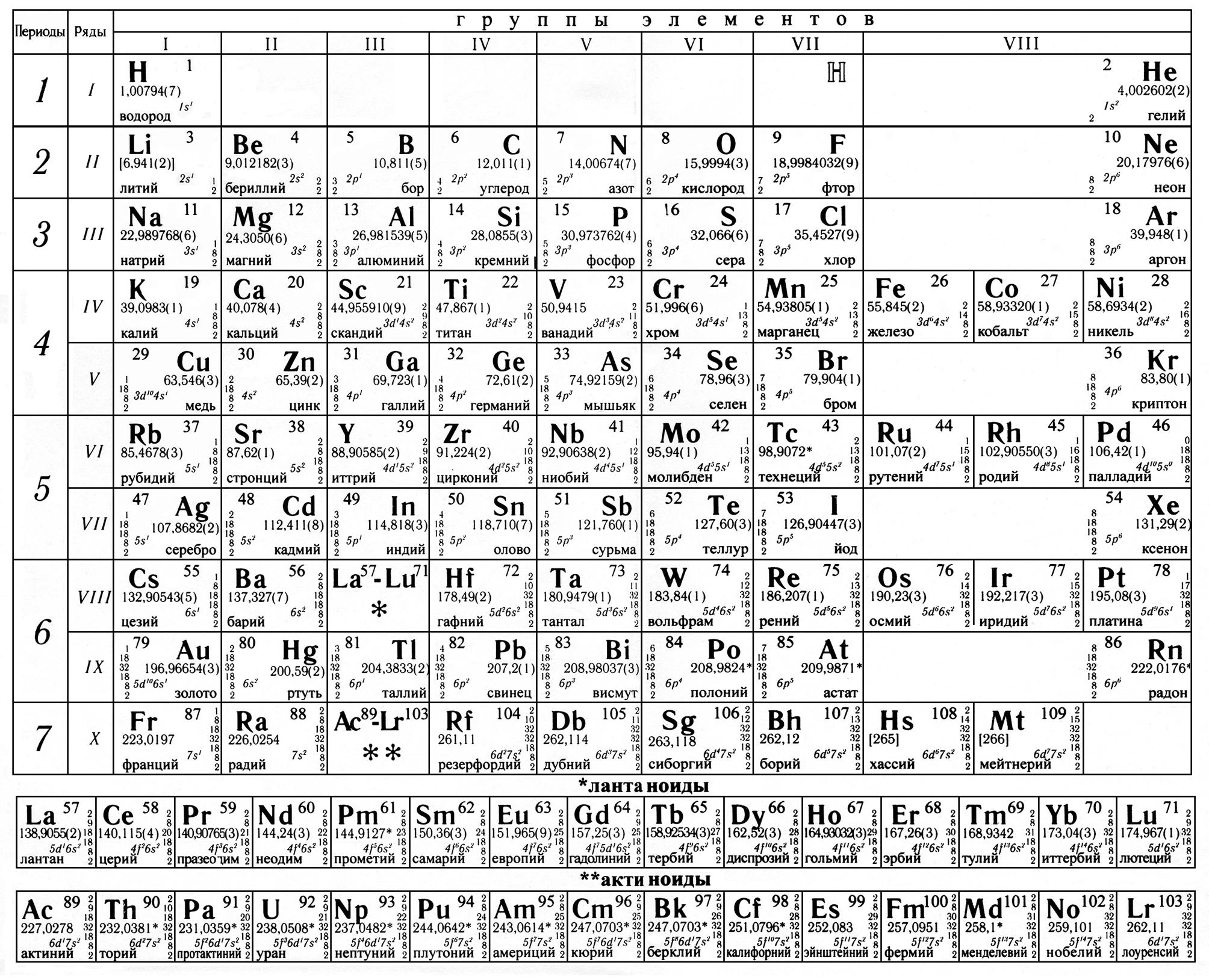 Сродство к электрону – это мера изменения энергии, когда атом получает или теряет энергию из-за принятия лишнего электрона. Поскольку они тесно связаны с электроотрицательностью, оба этих измерения следуют той же тенденции, что и электроотрицательность – энергия ионизации и сродство к электрону увеличиваются снизу вверх и слева направо.
Сродство к электрону – это мера изменения энергии, когда атом получает или теряет энергию из-за принятия лишнего электрона. Поскольку они тесно связаны с электроотрицательностью, оба этих измерения следуют той же тенденции, что и электроотрицательность – энергия ионизации и сродство к электрону увеличиваются снизу вверх и слева направо.
Рассмотрение исключений
Теперь, когда мы рассмотрели тенденции в периодической таблице Менделеева, следует указать на один отказ от ответственности: бывают исключения. Например, благородные газы и переходные металлы имеют небольшие различия в значениях электроотрицательности, поэтому вы не сможете предсказать их электроотрицательность, энергию ионизации и сродство к электрону в соответствии с тенденциями.
Краткое содержание урока
Периодическая таблица Менделеева может использоваться, чтобы узнать о свойствах элемента, таких как атомный символ атома, имя элемента, атомный номер и атомная масса.Вы также можете найти тенденции в периодической таблице, которые позволяют вам предсказать атомный радиус элемента, электроотрицательность, энергию ионизации и сродство к электрону.
Помните следующее: когда вы двигаетесь справа налево и сверху вниз, атомный радиус увеличивается. Когда вы двигаетесь в противоположном направлении – снизу вверх и слева направо, электроотрицательность, энергия ионизации и сродство к электрону увеличиваются.
от классического дизайна для использования в массовой культуре
Периодическая таблица Менделеева – одно из тех классических изображений, которые можно найти во многих научных лабораториях и классах.Это изображение почти каждый видел когда-либо в своей жизни.
Вы также можете найти таблицу Менделеева на футболках, кружках, пляжных полотенцах, наволочках, пододеяльниках и многих других предметах. Он даже вдохновил меня на сборник рассказов.
Кто может забыть таблицу Менделеева, положенную на музыку американцем Томом Лерером, профессором математики из Гарварда, который также был певцом / автором песен и сатириком. Его песня The Elements включает в себя все элементы, которые были известны на момент написания в 1959 году.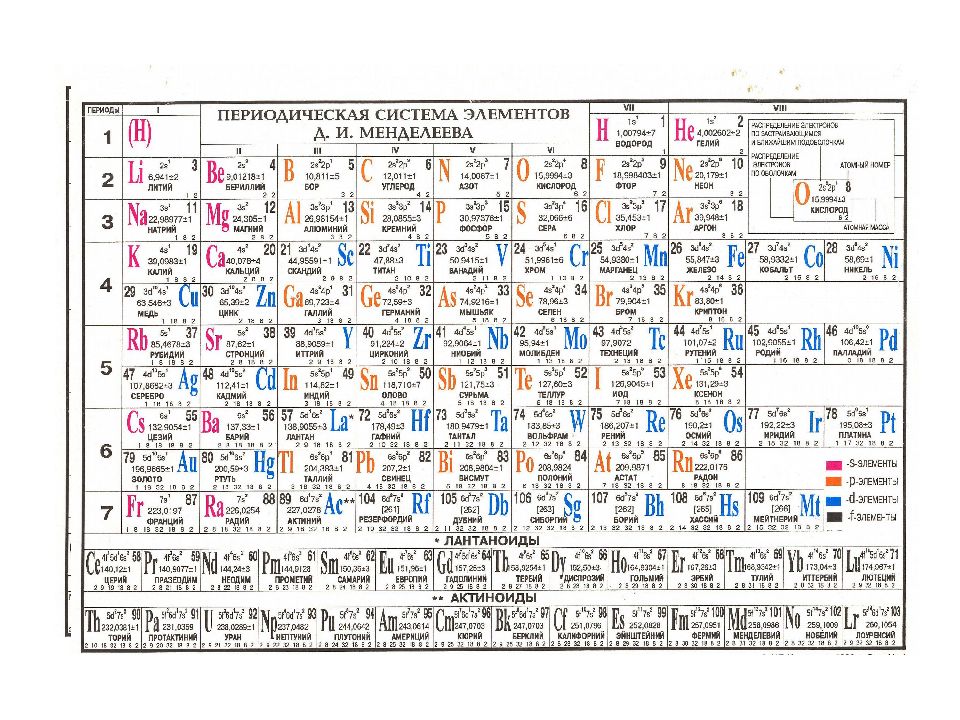
С тех пор в периодическую таблицу Менделеева было добавлено несколько новых элементов, в том числе четыре, которые были официально одобрены в прошлом году Международным союзом чистой и прикладной химии (IUPAC).
Но что именно показывает таблица Менделеева?
Короче говоря, это попытка организовать совокупность элементов – всех известных чистых соединений, состоящих из одного типа атомов.
Есть два способа посмотреть, как устроена таблица Менделеева, основанная либо на наблюдаемых свойствах содержащихся в ней элементов, либо на субатомном строении атомов, образующих каждый элемент.
Основная современная таблица Менделеева. Shutterstock / duntaroЭлементы
Когда ученые начали собирать элементы в 1700-х и 1800-х годах, медленно выявляя новые в течение десятилетий исследований, они начали замечать закономерности и сходство в их физических свойствах. Некоторые были газами, некоторые – блестящими металлами, некоторые бурно реагировали с водой и так далее.
В то время, когда элементы были впервые открыты, структура атомов не была известна.Ученые начали искать способы систематизировать их, чтобы схожие свойства можно было сгруппировать вместе, точно так же, как кто-то, собирающий ракушки, может попытаться организовать их по форме или цвету.
Задача осложнялась тем, что не все элементы были известны. В результате оставались пробелы, из-за которых расшифровка шаблонов немного напоминала попытку собрать головоломку с недостающими частями.
Разные ученые придумали разные типы таблиц. Первую версию нынешней таблицы обычно приписывают русскому профессору химии Дмитрию Менделееву в 1869 году, а обновленную версию – в 1871 году.
Периодическая таблица Менделеева впервые опубликована за пределами России в Zeitschrift für Chemie (1869, страницы 405-6). Викимедиа / Дмитрий Менделеев Важно отметить, что Менделеев оставил пробелы в таблице, куда, по его мнению, следует поместить недостающие элементы. Со временем эти пробелы были заполнены, и появилась окончательная версия, которую мы знаем сегодня.
Со временем эти пробелы были заполнены, и появилась окончательная версия, которую мы знаем сегодня.
Атомы
Чтобы действительно понять окончательную структуру периодической таблицы, нам нужно немного понять об атомах и о том, как они устроены.У атомов есть центральное ядро (ядро), состоящее из более мелких частиц, называемых протонами и нейтронами.
Это число протонов, которое дает элементу его атомный номер – число, которое обычно находится в верхнем левом углу каждого прямоугольника в периодической таблице.
Свойства водорода указаны в периодической таблице. Shutterstock / duntaroТаблица Менделеева расположена в порядке возрастания атомных номеров (слева направо, сверху вниз).Он варьируется от элемента 1 (водород H) в верхнем левом углу до недавно утвержденного элемента 118 (oganesson Og) в правом нижнем углу.
Количество нейтронов в ядре может быть разным. Это дает начало различным изотопам для каждого элемента.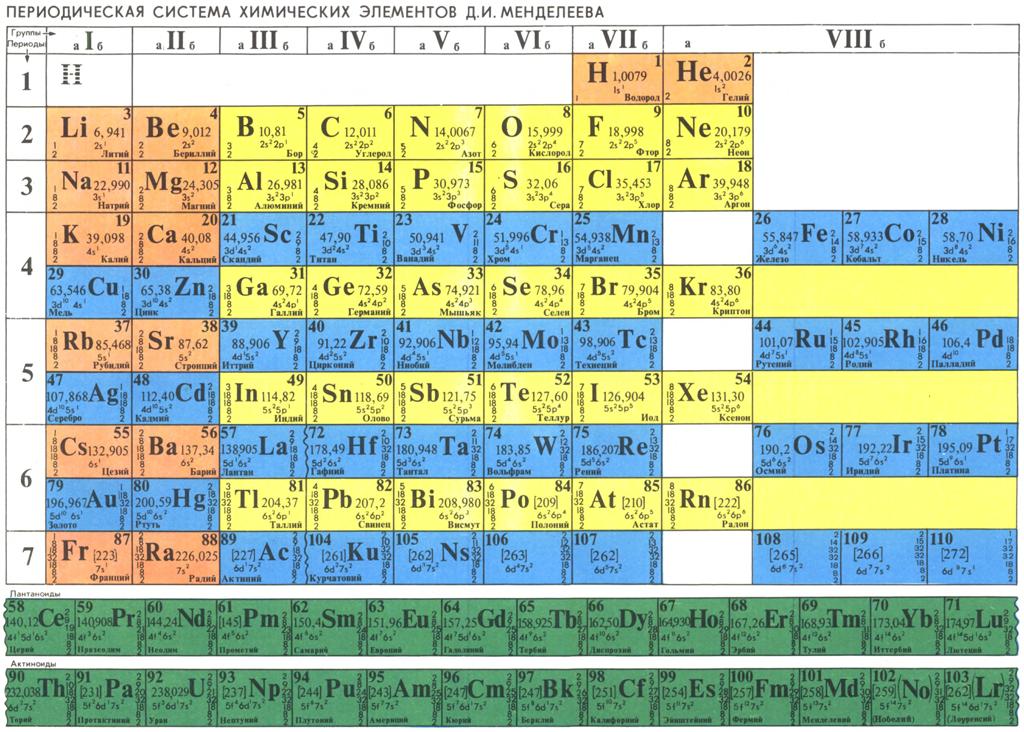
Например, вы, возможно, слышали о датировании по углероду-14 для определения возраста объектов. Этот изотоп представляет собой радиоактивную версию обычного углерода C (или углерода-12), который имеет два дополнительных нейтрона.
Но почему под основной таблицей находится отдельный блок элементов, и почему основная таблица имеет странную форму с выступом наверху? Это сводится к тому, как устроен другой компонент атома – электроны.
Электроны
Мы склонны думать, что атомы устроены чем-то вроде луковицы, с семью слоями электронов, называемыми «оболочками», обозначенными K, L, M, N, O, P и Q, окружающими ядро ядра.
Представьте атом с центральным ядром, содержащим все протоны и нейтроны, окруженным серией оболочек, содержащих электроны. Разговор, CC BY-ND Каждая строка в периодической таблице как бы соответствует заполнению одной из этих оболочек электронами.У каждой оболочки есть подоболочки, и порядок, в котором они заполняются, зависит от требуемой энергии, хотя это сложный процесс. Мы вернемся к ним позже.
Мы вернемся к ним позже.
Проще говоря, первый элемент в каждой строке начинает новую оболочку, содержащую один электрон, в то время как последний элемент в каждой строке имеет две (или одну для первой строки) подоболочек во внешней оболочке, полностью занятых. Эти различия в электронах также объясняют некоторые сходства свойств между элементами.
С одной или двумя подоболочками во внешнем слое, заполненными электронами, последние элементы каждого ряда совершенно инертны, поскольку во внешней оболочке нет дыр или щелей для взаимодействия с другими атомами.
Вот почему элементы в последнем столбце, такие как гелий He, неон (Ne), аргон (Ar) и т. Д., Называются благородными газами (или инертными газами). Все они газы, и они «благородны», потому что редко связываются с другими элементами.
Напротив, элементы первого столбца, за исключением водорода (как и в грамматике английского языка, всегда есть исключения!), Называются щелочными металлами.Элементы первого столбца похожи на металл по своему характеру, но имея только один электрон во внешней оболочке, они очень реактивны, поскольку этот одинокий электрон очень легко задействовать в химической связи. При добавлении в воду они быстро реагируют с образованием щелочного (основного) раствора.
При добавлении в воду они быстро реагируют с образованием щелочного (основного) раствора.
Каждая оболочка может вместить все большее количество электронов. Первая оболочка (K) подходит только для двух, поэтому в первой строке периодической таблицы всего два элемента: водород (H) с одним электроном и гелий (He) с двумя.
Вторая оболочка (L) вмещает восемь электронов. Таким образом, вторая строка периодической таблицы содержит восемь элементов с зазором между водородом и гелием для размещения дополнительных шести.
Третья оболочка (M) вмещает 18 электронов, но третий ряд по-прежнему содержит только восемь элементов. Это связано с тем, что дополнительные десять электронов не добавляются к этому слою до тех пор, пока первые два электрона не будут добавлены к четвертой оболочке (N) (почему мы узнаем позже).
Таким образом, зазор в четвертом ряду увеличен для размещения дополнительных десяти элементов, что приводит к «отрыву» от верхней части стола.Дополнительные десять соединений в средней части называются переходными металлами.
Четвертая оболочка содержит 32 электрона, но, опять же, дополнительные электроны не добавляются к этой оболочке до тех пор, пока некоторые из них также не будут добавлены к пятой (O) и шестой (P) оболочкам, что означает, что и четвертый, и пятый ряды содержат 18 элементов.
Для следующих двух строк (шестой и седьмой) вместо дальнейшего расширения таблицы в сторону для включения этих дополнительных 14 элементов, которые сделают ее слишком широкой, чтобы ее было легко читать, они были вставлены как блок из двух строк, называемый лантаноидами. (элементы с 57 по 71) и актиноиды (элементы с 89 по 103) под основной таблицей.
Таблица Менделеева выглядела бы иначе, если бы в нее были включены лантаноиды и актиноиды. Разговор, CC BYВы можете увидеть, где они могли бы поместиться, если бы периодическая таблица была расширена, если вы посмотрите на два нижних квадрата в третьем столбце таблицы выше.
По столбцам
Есть еще один усложняющий фактор, определяющий окончательную форму стола. Как упоминалось ранее, по мере того, как электроны добавляются к каждому слою, они переходят в разные подоболочки (или орбитали), которые описывают места вокруг ядра, где они с наибольшей вероятностью могут быть обнаружены.Они известны под буквами s, p, d и f.
Как упоминалось ранее, по мере того, как электроны добавляются к каждому слою, они переходят в разные подоболочки (или орбитали), которые описывают места вокруг ядра, где они с наибольшей вероятностью могут быть обнаружены.Они известны под буквами s, p, d и f.
Буквы, используемые для орбиталей, фактически получены из описаний излучения или поглощения света электронами, движущимися между орбиталями: s harp, p rincipal, d iffuse и f main.
Каждая оболочка имеет свою собственную конфигурацию подоболочек с именами от 1s до 7p, что дает общее количество электронов в каждой оболочке по мере продвижения по периодической таблице.
Разговор, CC BY-ND Как упоминалось ранее, порядок, в котором подоболочки заполняются электронами, не так прост. Вы можете увидеть порядок, в котором они заполняются, на изображении ниже, просто следуйте порядку, как вы читали бы слева направо.
Существует интерактивная таблица Менделеева, которая также хорошо иллюстрирует последовательность заполнения, если вы щелкаете по атомам.
Элементы в столбце обычно имеют схожие свойства, но в некоторых местах элементы, расположенные рядом, также могут быть похожими. Например, в переходных металлах кластеры драгоценных металлов вокруг меди (Cu), серебра (Ag), золота (Au), палладия (Pd) и платины (Pt) очень похожи.
Большинство существующих элементов с высокими атомными номерами, включая четыре сверхтяжелых элемента, добавленных в прошлом году, очень нестабильны и никогда не были обнаружены в природе или изолированы от нее.
Вместо этого они создаются и анализируются в ничтожных количествах в сильно искусственных условиях. Теоретически могут быть и другие элементы, помимо известных сейчас 118 (есть дополнительные суборбитали g, h и i), но мы пока не знаем, будет ли какой-либо из них достаточно стабильным, чтобы быть изолированным.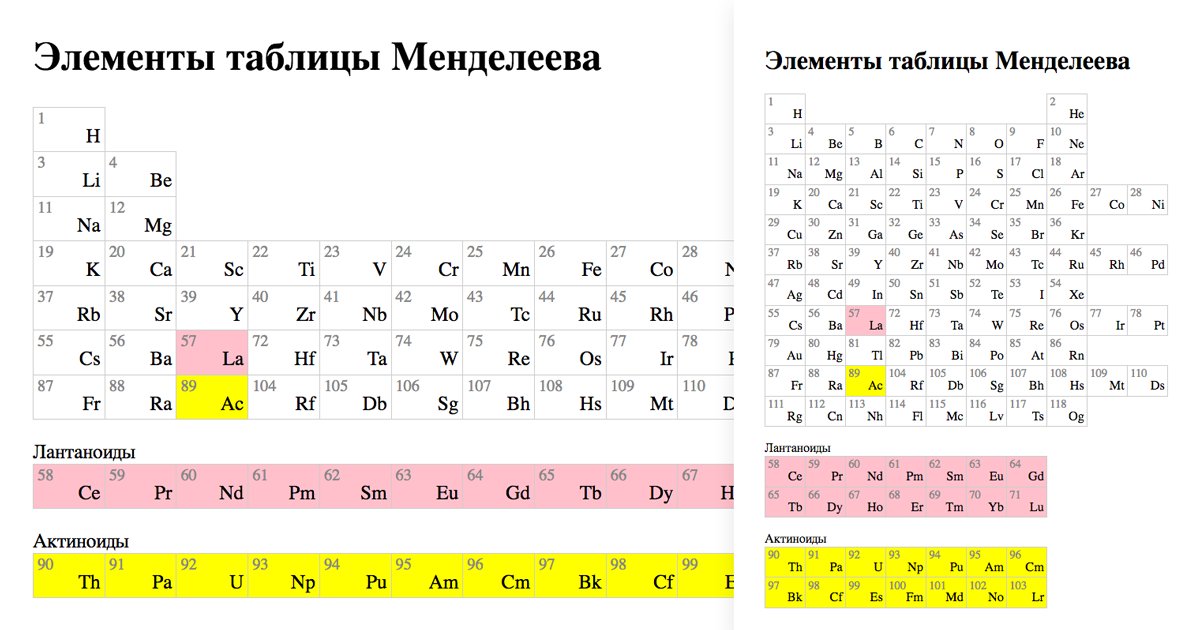
Классический дизайн
Периодическая таблица Менделеева видела много красочных и информативных версий, созданных за эти годы.
Периодическая таблица украшает такси в Великобритании.Flickr / Отец Гаурав Шрофф, CC BY-NC-NDОдна из моих любимых – художественная версия с оригинальными произведениями искусства для каждого элемента, заказанная Королевским химическим институтом Австралии по случаю Международного года химии в 2011 году.
Другой фаворит – интерактивная версия с изображениями элементов. Создатели этого сайта также опубликовали журнальный столик под названием The Elements и приложение Apple с видеороликами о каждом элементе.
Интерактивные версиибыли также созданы Королевским химическим обществом (их также можно загрузить как приложение) и ChemEd DL среди других.
Классический дизайн таблицы Менделеева можно использовать для игры в версию игры «Морской бой».
Играем в боевые корабли с периодической таблицей на первом Всемирном научном фестивале в Брисбене в 2016 году. Разговор, CC BY-NC-ND
Разговор, CC BY-NC-NDСуществует также множество забавных версий, помогающих организовать множество объектов, включая еду, пиво, смайлики, приложения для iPad и птиц.
Что касается The Elements Тома Лерера, песня еще не обновлена, чтобы включить все элементы, известные сегодня, но на протяжении многих лет на нее делали каверы.
Актер Дэниел Рэдклифф, прославившийся о Гарри Поттере, исполнил версию во время выступления в качестве гостя на шоу Грэма Нортона BBC.
Существуют и другие музыкальные версии элементов, но они тоже еще не обновлены, чтобы включить все записи периодической таблицы.
Таким образом, периодическая таблица – это химическая систематика всех элементов. Его триумф в том, что он по-прежнему актуален для ученых, а также становится частью популярной культуры.
Наизнанку Откройте для себя элементы: Периодическая таблица
Периодическая таблица Менделеева представляет собой систему классификации для элементы. Каждый элемент имеет уникальные свойства, и вы может предсказать физические и химические свойства элемента в зависимости от его положения в периодической таблице.
Когда вы смотрите на таблицу Менделеева, символы и числа выглядят как изображение слева. Символы являются сокращениями. происхождения слова для каждого элемента.Например, Символ свинца, Pb, происходит от латинского слова plumbum. что означает «жидкое серебро».
Число над символом – это атомная масса (или атомный вес). Это общее количество протонов и нейтроны в атоме.
Число под символом – это атомный номер и это отражает количество протонов в ядре
атома каждого элемента. Каждый элемент имеет уникальный атомный
номер.Свинец имеет 82 протона, поэтому его атомный номер
равно 82. Затем элементы располагаются в порядке возрастания
атомные номера – так водород (H), который имеет только
один протон, расположен первым в таблице, а натрий
(Na), который имеет 11 протонов и находится ниже
Таблица.
Затем элементы располагаются в порядке возрастания
атомные номера – так водород (H), который имеет только
один протон, расположен первым в таблице, а натрий
(Na), который имеет 11 протонов и находится ниже
Таблица.
Мы можем использовать атомный номер и атомную массу, чтобы узнать
количество протонов, нейтронов и электронов там
находятся в атоме. Вычитая атомный номер из
атомная масса, мы можем узнать количество нейтронов
Есть.
Есть 18 основных столбцов элементов
в периодической таблице. Их называют группами или семьями.
Элементы в одной группе или семье имеют одинаковые
– но не идентичные – свойства. Например литий,
натрий и калий являются членами семьи 1. Они
все очень реактивны и поэтому могут легко сочетаться с
другие элементы для образования соединений. Каждый горизонтальный ряд
называется периодом. В отличие от элементов в семье, элементы
в период не похожи по свойствам.Есть 7
периоды стихий. 2 строки, которые были разделены
из основной таблицы – редкоземельные элементы или лантаноны
(лантаноиды) в первом периоде и актиноны (актиниды)
в следующем периоде.
Путешествие к созданию таблица Менделеева может быть прослежена еще в Древние греки 400 г. до н.э., которые использовали слово «элемент» и “атом” для описания различий между вещи.
Периодическая таблица, известная нам сегодня, была создан четырьмя отдельными европейскими учеными во время 1860-е гг. В 1863 г. 44-летний французский геолог А. Э. Бегайе. де Шанкуртуа составил список элементов, измеренных по их атомному весу. Между тем в Англии химик Джон А. Р. Ньюлендс заметил, что химические группы повторяются. каждые 8 элементов. Он назвал это правилом октавы, сравнивая это к музыкальным нотам.
Между
1868 и 1869 гг., Работая самостоятельно, русский химик.
Дмитрий И.Менделеев и немецкий химик Лотар Мейер
расположил элементы в 7 столбцов в соответствии с их
химические свойства. Их таблицы были похожи, но
была принята таблица Менделеева. Он собран
наблюдения и открытия более ранних химиков, показывающие
символы химических элементов в порядке
их атомные массы, но его таблица была огромным научным
прорыв, потому что он оставил пробелы и точно предсказал
неоткрытые элементы. Это значительно ускорило
открытие новых элементов и наше понимание их
свойства, и это позволило ученым точно
предсказывать элементы – многие элементы были
обнаруженные или искусственно созданные, которые вписались в
пробелы в таблице. Менделеев предсказал свойства
скандия, галлия и германия: в течение 20 лет
ученые обнаружили существование этих элементов
и его предсказания оказались точными.Современное
версии таблицы Менделеева содержат 109 элементов,
но новый
элементы обнаруживаются все время.
Это значительно ускорило
открытие новых элементов и наше понимание их
свойства, и это позволило ученым точно
предсказывать элементы – многие элементы были
обнаруженные или искусственно созданные, которые вписались в
пробелы в таблице. Менделеев предсказал свойства
скандия, галлия и германия: в течение 20 лет
ученые обнаружили существование этих элементов
и его предсказания оказались точными.Современное
версии таблицы Менделеева содержат 109 элементов,
но новый
элементы обнаруживаются все время.
Периодическая таблица: это больше, чем просто химия и физика
Кредит: welcomia / shutterstock.com
Это Международный год Периодической таблицы Менделеева, и хотя меня (точно) обвиняли в том, что я фанат физики, я здесь, чтобы сказать вам, что эта знаменитая диаграмма касается не только физики, химии и других наук. .Это также касается математики, инженерии и даже ненаучных областей знаний, включая историю, географию и происхождение слов.
Во-первых, краткий обзор того, что такое таблица Менделеева. Это таблица всех химических строительных блоков вещества. На сегодняшний день люди наблюдали 118 как естественных, так и искусственно созданных. Каждый из этих строительных блоков, известных как атомные элементы, содержит положительно заряженное ядро (известное как ядро), которое (обычно) окружено облаком отрицательно заряженных частиц, называемых электронами.Если немного приблизить ядро, мы находим положительно заряженные частицы, известные как протоны, и нейтральные частицы, известные как нейтроны.
Единственная особенность, которая определяет атомный элемент, – это его атомный номер, то есть количество протонов в его ядре. Водород имеет один протон, поэтому его атомный номер равен 1, а уран имеет 92, поэтому его атомный номер… 92. Если имеется равное количество электронов и протонов, атом электрически нейтрален. Если электронов меньше или больше, чем протонов, атом электрически заряжен и известен как ион.
Официальная таблица Менделеева NIST.
Кредит: Н. Ганачек / NIST
У каждого атома может быть несколько различных версий, известных как изотопы, в которых в ядре разное количество нейтронов. Например, водород обычно имеет только один протон и не имеет нейтронов, но изотоп, известный как дейтерий или «тяжелый водород», также содержит один нейтрон.
Изотоп дейтерия помогает создавать более тяжелые элементы внутри звезд, делает некоторые лекарства более эффективными и может быть ключевым ингредиентом для получения чистой термоядерной энергии.Он был обнаружен в 1930-х годах в Национальном институте стандартов и технологий (NIST, тогда известный как Национальное бюро стандартов), где он был обнаружен Гарольдом Юри из Колумбийского университета, который получил Нобелевскую премию за свой подвиг.
(Увы, Фердинанд Брикведде из NIST не получил приза. Это нормально.)
Итак, вы уже можете увидеть важность этого изотопа в астрономии, фармацевтике и энергетике. И все же, несмотря на свою важность, это большая редкость по сравнению с обычным водородом, самым распространенным ингредиентом воды, большинства звезд и Вселенной в целом.Удивительно, как один элемент в таблице Менделеева содержится в таком количестве разных вещей в нашем мире.
В 1869 году русский химик Дмитрий Менделеев создал первую периодическую таблицу, расположив атомные элементы в столбцы и строки. Атомарные элементы в одних и тех же столбцах и строках имеют определенные общие свойства. Например, атомы в крайнем правом столбце, известные как благородные газы, могут сильно различаться по массе от легких (гелий) до тяжелых (например, радон), но их объединяет то, что они обычно не участвуют в химических реакциях. .
Гений Менделеева состоял в том, что он оставил места для элементов, которые еще не были открыты, и тем самым он предсказал их существование, например, галлий в 1875 году и германий в 1886 году. Как вы, возможно, догадались, последний был назван в честь Германии ( родина первооткрывателя Клеменса Винклера). Что касается первого, Поль Эмиль Лекок де Буабодран назвал элемент «галлией» в честь Галлии, региона железного века, который включает современную Францию.
Итак, если вы любите историю, литературу и слова, таблица Менделеева для вас.Некоторые элементы названы в честь городов: Стронций происходит из шотландской деревни Стронтиан, где был обнаружен минерал, содержащий элемент. Некоторые взяли свои имена из мифологии. Элемент ванадий назван в честь норвежской богини Ванадис. Недавно открытые элементы, как правило, называются в честь реальных людей, таких как мейтнерий (австрийско-шведский физик Лизе Мейтнер была соавтором ядерного деления). Именование элементов после мест также было в тренде. Например, теннессин поступает из штата Теннесси, где находится Национальная лаборатория Ок-Ридж, которая выполнила ключевую работу по производству этого конкретного элемента.
Крупным планом – сфера из почти чистого кремния.
Кредит: NIST
Если вам нравится инженерное дело, таблица Менделеева – идеальное место для инноваций. Полупроводниковая промышленность использовала периодическую таблицу, чтобы выйти за рамки стандартных устройств на основе кремния. Инженеры-полупроводники использовали различные комбинации элементов из столбцов III и V периодической таблицы для создания новых полупроводниковых сплавов, таких как нитрид галлия (GaN) и нитрид индия (InN), каждый из которых имеет разные преимущества.Например, нитрид галлия может излучать свет с большим количеством длин волн, включая синий свет, используемый в экранах смартфонов. Нитрид индия может поглощать свет в более узком диапазоне длин волн, что делает его отличным кандидатом для солнечных элементов, поскольку он поглощает определенные длины волн света, наиболее распространенного от солнца.
И, конечно же, материаловедение. Инженеры любят комбинировать легкий металлический титан с другими элементами, такими как алюминий, для создания сплавов для самолетов и других транспортных средств.Сплавы магния и других элементов, таких как золото, находят применение в медицинских имплантатах для восстановления костей. Эти сплавы хороши тем, что они поддаются биологическому разложению, поэтому они исчезают после того, как послужили опорой для роста новых костей.
NIST’s Materials Genome Initiative – это современное воплощение духа периодической таблицы Менделеева, использующее вычислительные мощности, в том числе искусственный интеллект, для объединения элементов в новые материалы для желаемых приложений, таких как менее дорогие в производстве никелевые монеты и «Металлические стекла» для более прочных строительных материалов.
Точность хронометража может быть не тем, что вы ассоциируете с периодической таблицей, но исследователям NIST, создающим современные атомные часы, это может быть первое, что приходит на ум. С 1967 года второй определяли атомные часы с использованием атомов цезия. Если на атомы цезия воздействовать микроволновым излучением с частотой 9 192 631 770 герц (циклов в секунду), они изменят квантовые энергетические состояния. Используя электронный детектор для измерения изменения состояния атомов, ученые NIST удерживают генерируемую частоту привязанной к атомному переходу, обеспечивая очень стабильный частотный выход.
Атомные часы позволяют нам точно разделить секунду на миллиардные доли и более. Точные измерения времени полезны для отметки времени финансовых транзакций, синхронизации обмена данными и данных, а также для навигации с использованием глобальной системы позиционирования (GPS). В последнее время исследователи NIST создают часы с другими атомами, такими как стронций, иттербий, ртуть и алюминий. Исследователи изменяют квантовые состояния этих атомов с помощью оптического излучения с частотами в сотни триллионов циклов в секунду (намного выше, чем микроволновое излучение, используемое в цезиевых часах).Эти «оптические часы» позволяют разделить секунды на еще меньшие интервалы, что может быть полезно для таких вещей, как обнаружение подземных геологических отложений и даже темной материи.
Трехмерные (3-D) квантовые газовые атомные часы JILA состоят из световой сетки, образованной тремя парами лазерных лучей. Пакет из двух столов используется для настройки оптических компонентов вокруг вакуумной камеры. Здесь показан верхний стол, на котором устанавливаются линзы и другая оптика. Синий лазерный луч возбуждает кубическое облако атомов стронция, расположенное за круглым окном в центре стола.Атомы стронция сильно флуоресцируют при возбуждении синим светом.
Кредит: G.E. Марти / Джила
Если вы любите числа, ну, конечно, таблица Менделеева ими заполнена. Каждый атом в таблице имеет множество величин. Помимо атомного номера, есть атомный вес и энергия ионизации (количество энергии, необходимое для удаления электрона из этого атома).
Как мы получили такие точные цифры? По мере того, как физики разрабатывали квантовую теорию, они производили высокоточные (и удивительно правильные) вычисления уровней энергии электронов в атомах.Среди прочего, химики определили, как расположение электронов в атомах влияет на химические реакции. Вся эта работа ученых была связана с современной математикой.
Однако после того, как ученые разработали основы, оставалось еще много работы для понимания свойств каждого из элементов. Кто причастен? Ученые-измерители, такие как люди, работающие в NIST.
МатематикNIST Джим Симс объяснил мне: «Как люди« стандартов », мы те, кто собирает в мире экспериментальные и теоретические данные об атомных свойствах элементов и критически оценивает их, чтобы получить наилучшую оценку чисел в стол в любое время.Математика, безусловно, входит в этот анализ, и, что более важно, любое вычисление атомной структуры в значительной степени зависит как от математики, так и от вычислительной науки ».
Я спросил Джима, какие достижения в математике привели к созданию таблицы Менделеева, которую мы знаем сегодня. «Скорее, чем какой-либо конкретный пример, – сказал он, – все, что я могу придумать, – это тот факт, что современная физика, химия и математика тесно взаимосвязаны».
И я сделаю еще один шаг, сказав, что в периодической таблице взаимосвязано так много других полей.Одна небольшая таблица – это одновременно источник знаний и плацдарм для творчества во многих областях. Это гораздо больше, чем просто плакат на уроке химии в старшей школе; это план на будущее.
Печатную версию официальной таблицы Менделеева NIST можно скачать здесь.
Смотрите видеоролики NIST и другие ресурсы по Международному году Периодической таблицы элементов здесь.
применений в реальной жизни каждого элемента периодической таблицы
Элементы периодической таблицы находятся повсюду, фактически, они составляют все.
Понимание того, как читать таблицу Менделеева – это одно, но оно не говорит вам, полезен ли элемент, как он выглядит или даже как он используется.
Чтобы ответить на некоторые из этих вопросов, мы составили это «краткое руководство», которое поможет вам легко читать и перемещаться по ресурсам для некоторых применений каждого элемента в периодической таблице.
Все элементы периодической таблицы включены ниже и расположены по атомным номерам от 1 до 118.
** Совет: если вы хотите перейти к определенному элементу, используйте функцию поиска (CTRL + F) в браузере, чтобы быстро определить то, что вы ищете **
Руководство
Каждый Заголовок элемента имеет имя, атомный номер, атомный символ, а также цветовой код, обозначающий группу, к которой он принадлежит.
Например, водород зеленого цвета, поэтому он принадлежит к группе «прочие неметаллы».
Используйте это руководство, чтобы помочь вам определить группу каждого металла по мере того, как вы узнаете о них больше.
Водород
Символ: H
Атомный вес: 1.008
Описание: Водород – взрывоопасный газ, а также самый легкий элемент.
Где он используется: Водород составляет около 90 процентов атомов во всей Вселенной. Химикат широко используется как в газовом, так и в жидком топливе. Водород использовался НАСА в качестве основного топлива для программы Space Shuttle, а в настоящее время активно используется в нефтяной и обрабатывающей промышленности.
Вспомогательное видео:
Гелий
Символ: He
Атомный вес: 4.002602 (2)
Описание: Гелий является самым инертным газом и вторым легким элементом .
Где он используется: Гелий обычно легче воздуха, что приводит к его использованию в погодных и праздничных воздушных шарах. Он также используется в качестве инертной защиты при дуговой сварке и для создания избыточного давления в баках с жидким топливом в ракетах.Из-за его широкого использования в рекреационных целях природные источники гелия могут быть полностью истощены в следующем десятилетии, что вызывает опасения у научного сообщества.
Литий
Символ: Li
Атомный вес: 6,94
Описание: В стандартных условиях литий является самым легким металлом, мягким и химически активным.
Где он используется: Литий, как известно, чаще всего используется в батареях.Он также используется в алюминиевых сплавах, чтобы сделать посуду более долговечной, и, что самое удивительное, в психиатрических лекарствах в качестве стабилизатора настроения.
Бериллий
Символ: Be
Атомный вес: 9.012183 (5)
Описание: Бериллий – легкий металл.
Где используется: Этот элемент чаще всего используется в качестве легирующего агента для меди. В сочетании, полученный металл, бериллиевая медь, используется для изготовления пружин и различных электрических применений.Благодаря легким металлическим свойствам он конструктивно используется в аэрокосмической промышленности.
Бор
Символ: B
Атомный вес: 10,81
Описание: Бор представляет собой порошкообразное твердое вещество черного цвета.
Где применяется: Бор применяется в пиротехнике. При сгорании выделяет зеленый цвет в пламени. Чаще используются борная кислота и бура. Вы можете найти бор в антисептических средствах, моющих средствах, керамической глазури и глазных каплях.
Углерод
Символ: C
Атомный вес: 12.011
Описание: Существует ряд чистых форм этого элемента, включая графит, алмаз, фуллерены и графен. Наноформы, фуллерены и графен выглядят как черные или темно-коричневые, похожие на сажу порошки.
Где он используется: Углерод уникален среди элементов своей способностью образовывать прочно связанные цепи, запечатанные атомами водорода.Эти углеводороды в основном используются в качестве топлива и сырья для производства полимеров, волокон, красок, растворителей, пластмасс и т. Д. Загрязненный углерод в виде древесного угля (из древесины) и кокса (из угля) используется при выплавке металлов. .
Графит используется для изготовления карандашей, тиглей и электродов. Чистый алмаз также полностью состоит из атомов углерода. Открытие углеродных нанотрубок, фуллеренов и листов графена толщиной до атома привело к их использованию в электронной промышленности и в нанотехнологиях в целом.
Азот
Символ: N
Атомный вес: 14.007
Описание: Азот – бесцветный газ.
Где используется: 78 процентов всей атмосферы Земли состоит из азота. Этот элемент важен для химической промышленности, поскольку он является ключевым питательным веществом в удобрениях и ключевым компонентом азотной кислоты, нейлона и взрывчатых материалов. Процесс Габера – это хорошо известный метод реакции азота с водородом с образованием аммиака.
Кислород
Символ: O
Атомный вес: 15.999
Описание: Кислород – бесцветный газ.
Где он используется: Многие живые существа, в том числе люди, используют кислород для дыхания. Чистый кислород используется для лечения проблем с дыханием и делает космический корабль пригодным для жизни. Кислород в промышленности в основном используется при производстве стали и других металлических сплавов. В больших количествах также используются такие химические вещества, как азотная кислота и перекись водорода.
Он также используется в качестве антифриза и для производства полиэфира и хлорэтилена, прекурсора ПВХ. Кислородный газ используется для кислородно-ацетиленовой сварки. Растет использование для очистки сточных вод и промышленных стоков.
Фтор
Символ: Fl
Атомный вес: 18.998403163 (6)
Описание: Фтор – желтоватый ядовитый газ и наиболее реактивный элемент.
Где используется: Фтор – обычная добавка к питьевой воде и используется в качестве чистящего средства в зубной пасте.В поп-культуре плавиковая кислота использовалась в качестве растворяющего агента в популярном телешоу «Во все тяжкие». Химикат может растворять стекло и используется в основном как травильный состав.
Он также используется для производства гексафторида урана, используемого в атомной энергетике для разделения изотопов урана, и для производства гексафторида серы, изоляционного газа для силовых трансформаторов электроэнергии.
Фтор также используется во многих растворителях и высокотемпературных пластмассах, таких как тефлон и Gore-Tex®.
Неон
Символ: Ne
Атомный вес: 20,1797 (6)
Описание: Неон – инертный газ.
Где он используется: Неон – четвертый по численности элемент во всей Вселенной. Сегодня этот элемент чаще всего используется в рекламных знаках. Когда стекло соблазняется электричеством, оно обычно светится, что приводит к его использованию в соответствующей индустрии вывесок, а также в высоковольтных индикаторах и лазерах.Жидкий неон – важный криогенный хладагент.
Диаграмма:
Источник: BruceBlaus / WikimediaНатрий
Символ: Na
Атомный вес: 22.98976928 (2)
Описание: Натрий – очень реактивный мягкий металл.
Где он используется: Натрий используется в уличных фонарях для получения желтого света, а также является компонентом многих соединений, таких как поваренная соль, кальцинированная сода, бура и пищевая сода.
Магний
Символ: Mg
Атомный вес: 24.305
Описание: Магний – легкий металл.
Где он используется: Магний находит множество применений в медицине в виде английской соли, магнезиального молока, хлорида и цитрата. Магний также необходим как для животных, так и для растений. Поскольку он менее плотный, чем алюминий, его часто легируют алюминием для использования в конструкциях самолетов и автомобилей.Его также добавляют в расплавленное железо и сталь для удаления серы.
Поскольку магний легко воспламеняется в воздухе и горит ярким светом, его используют в осветительных ракетах, фейерверках и бенгальских огнях. Оксид магния используется для изготовления жаропрочного кирпича для каминов и печей. Его также добавляют в корм для крупного рогатого скота и удобрения.
Вспомогательное видео:
Алюминий
Символ: Al
Атомный вес: 26.9815385
Описание: Алюминий – легкий нержавеющий металл.
Где используется: Алюминий – это мягкий и податливый металл, который используется для изготовления консервных банок и мусорных баков, посуды, деталей самолетов и автомобилей, а также других структурных применений.
Кремний
Символ: Si
Атомный вес: 28.085
Описание: Кремний – твердый металлоид.
Где он используется: Кремний широко используется в полупроводниковой промышленности в твердотельной электронике.Для таких применений кремний должен быть легирован бором, галлием, фосфором или мышьяком.
Фосфор
Символ: P
Атомный вес: 30.973761998 (5)
Описание: Фосфор – это светящееся белое воскообразное твердое вещество.
Где используется: Белый фосфор используется в факелах и зажигательных устройствах, а красный фосфор находится в материале, наклеенном на стороны спичечных коробок. Однако больше всего фосфорные соединения используются для удобрений.Фосфор также важен при производстве стали.
Сера
Символ: S
Атомный вес: 32,06
Описание: Сера представляет собой хрупкое твердое вещество желтого цвета.
Где используется: Сера используется в порохе и другой пиротехнике, производстве резины, а также в качестве инсектицида, фунгицида и фумиганта. Его также можно использовать для лечения кожных заболеваний, однако его основное применение – разделение соединений.
Хлор
Символ: Cl
Атомный вес: 35,45
Описание: Хлор – это зеленоватый ядовитый газ.
Где используется: Хлор используется для очистки воды и как антисептик. При производстве бумаги, пластмасс, растворителей и тканей также используются большие количества хлора.
Аргон
Символ: Ar
Атомный вес: 39.948 (1)
Описание: Аргон – инертный газ.
Где он используется: Аргон используется в лампах накаливания и люминесцентных лампах в качестве защитного слоя вокруг нити, чтобы кислород не разъедал ее. Он также используется в качестве защитного экрана при дуговой сварке и полупроводниковых кристаллах.
Калий
Символ: K
Атомный вес: 39.0983
Описание: Калий – мягкий металл и является реактивным.
Где используется: Калий в основном используется в соединениях. В сочетании с хлором он образует хлорид калия, который используется в удобрениях, фармацевтических препаратах и солевых растворах. Гидроксид калия также используется в мыле и чистящих средствах, а карбонат калия используется в производстве стекла.
Кальций
Символ: Ca
Атомный вес: 40.078 (4)
Описание: Кальций – мягкий металл.
Где используется: Кальций используется для получения тория и урана в качестве восстановителя. Он также используется в качестве легирующего агента для алюминия, меди, свинца и магния.
Скандий
Символ: Sc
Атомный вес: 44.955908
Описание: Скандий – мягкий легкий металл.
Где используется: Скандий, широко используемый в ртутных лампах, является ключевым элементом освещения стадионов.Его радиоактивный изотоп также используется в качестве отслеживающего агента.
Титан
Символ: Ti
Атомный вес: 47,867 (1)
Описание: Титан – самый прочный легкий металл и жаропрочный.
Где используется: Титан – невероятно прочный металл, используемый в сплавах с алюминием, железом и другими металлами. Этот прочный металл используется в аэрокосмической промышленности, а также в двигателях отчасти из-за его способности сохранять прочность при экстремальных температурах.
Ванадий
Символ: V
Атомный вес: 50.9415 (1)
Описание: Ванадий – твердый металл.
Где используется: Этот элемент используется в реактивных двигателях и компонентах самолетов. Все его применения требуют, чтобы он был объединен с другим металлом или элементом, таким как ванадиево-галлиевая лента, используемая в магнитах. Около 80 процентов произведенного ванадия используется в качестве добавки к стали для получения очень прочного сплава.
Диаграмма:
Источник: СтэнфордХром
Символ: Cr
Атомный вес: 51,9961 (6)
Описание: Хром – твердый блестящий металл.
Где используется: Хром используется в нержавеющей стали, а также в процессе хромирования. Различные соединения хрома известны своими яркими цветами.
Марганец
Символ: Mn
Атомный вес: 54.938044 (3)
Описание: Марганец – твердый металл.
Где используется: Двуокись марганца составляет около 0,14 процента земной коры. Он используется в стекле для удаления зеленого цвета, присутствующего в соединениях железа. Он слишком хрупкий, чтобы использовать его самостоятельно, и в основном используется в качестве сплава.
Железо
Символ: Fe
Атомный вес: 55,845 (2)
Описание: Железо – это металл средней твердости, обладающий магнитными свойствами.
Где используется: Основное применение железа – производство стали. Когда сталь сочетается с хромом, получается нержавеющая сталь, стойкая к коррозии.
Кобальт
Символ: Co
Атомный вес: 58.933194 (4)
Описание: Кобальт – твердый металл и обладает магнитными свойствами.
Где он используется: Кобальт используется в основном для лечения рака и лучевой терапии. Металлический кобальт иногда используется в гальванике из-за его привлекательного внешнего вида, твердости и устойчивости к коррозии.
Никель
Символ: Ni
Атомный вес: 58,6934 (4)
Описание: Никель – металл средней твердости и обладает магнитными свойствами.
Где он используется: Никель используется в нержавеющей стали и других антикоррозионных металлических сплавах. Другие известные применения включают производство трубопроводов и насосно-компрессорных труб, а также в процессе опреснения воды.
Медь
Символ: Cu
Атомный вес: 63.546 (3)
Описание: Медь – цветной металл, хорошо проводящий тепло и электричество.
Где используется: Медь – один из лучших проводников электричества, поэтому ее используют в электронике и двигателях. Металл также очень теплопроводен, поэтому его используют в радиаторах, кондиционерах и системах отопления.
Цинк
Символ: Zn
Атомный вес: 65,38 (2)
Описание: Цинк не подвержен коррозии.
Где используется: Цинк используется в качестве легирующего агента для латуни, никеля, серебра и алюминия. Краски, каучуки, косметика, батарейки, текстиль и чернила также нуждаются в этом элементе.
Галлий
Символ: Ga
Атомный вес: 69,723 (1)
Описание: Галлий – мягкий металл с низкой температурой плавления.
Где используется: Поскольку галлий имеет низкую температуру плавления, он часто используется в медицинских термометрах в качестве заменителя ртути.В сочетании с мышьяком он используется в полупроводниках, лазерах и солнечных батареях. Его также можно использовать при изготовлении зеркал.
Вспомогательное видео:
Германий
Символ: Ge
Атомный вес: 72,630 (8)
Описание: Германий – хрупкий металлоид.
Где используется: Германий находит применение в полупроводниковой промышленности. Когда он легирован другими элементами, он дает высокоэффективные транзисторы.Продолжая использовать его в электронике, он также реализован в люминесцентных лампах.
Мышьяк
Символ: As
Атомный вес: 74.
5 (6)
Описание: Мышьяк – хрупкий металлоид.
Где используется: Этот элемент используется в качестве легирующего агента в транзисторах, в основном с галлием. Многие соединения мышьяка используются в качестве инсектицидов и ядов.
Селен
Символ: Se
Атомный вес: 78.971 (8)
Описание: Селен – хрупкое твердое вещество серого цвета.
Где он используется: В основном селен используется в стекольной промышленности. Его свойства позволяют обесцвечивать класс, а также делать красное стекло. Используется в солнечных и фотоэлементах. В пленочной фотографии он также используется в качестве фототонера.
Бром
Символ: Br
Атомный вес: 79,904
Описание: Бром – жидкость темно-красного цвета.
Где он используется: Бром используется в качестве замедлителя горения в пластмассах и электронике. Его также можно использовать для очистки и дезинфекции воды, что позволяет использовать его в плавательных бассейнах и гидромассажных ваннах.
Криптон
Символ: Kr
Атомный вес: 83,798 (2)
Описание: Криптон – инертный газ.
Где он используется: Около 0,0001 процента атмосферы Земли составляет криптон, что делает его получение относительно трудным.Элемент используется для вспышек в высокоскоростной фотографии, а также в качестве проводящего газа в люминесцентных лампах. Фторид криптона используется в некоторых лазерах.
Рубидий
Символ: Rb
Атомный вес: 85,4678 (3)
Описание: Рубидий – это мягкий металл, обладающий реакционной способностью.
Где используется: Рубидий используется в вакуумных трубках для удаления примесей газов. Он также широко используется в фотоэлементах и специализированных очках.Его можно легко ионизировать, поэтому его часто используют в качестве топлива в космических кораблях.
Диаграмма:
Источник: Ahazard / WikimediaСтронций
Символ: Sr
Атомный вес: 87,62 (1)
Описание: Стронций – мягкий металл.
Где он используется: Стронций используется в пиротехнике для получения ярко-красных оттенков. Его также можно использовать в производстве ферритовых магнитов и рафинировании цинка.
Иттрий
Символ: Y
Атомный вес: 88.
(2)
Описание: Иттрий – мягкий металл.
Где используется: Оксид иттрия используется для изготовления телевизионных трубок с красным фосфором. Наряду с этим он используется для повышения прочности алюминиевых и магниевых сплавов.
Цирконий
Символ: Zr
Атомный вес: 91,224 (2)
Описание: Цирконий – коррозионностойкий металл.
Где используется: Цирконий используется в качестве антикоррозионного состава в насосах и клапанах.Он не поглощает нейтроны, поэтому также широко используется в ядерных реакторах.
Ниобий
Символ: Nb
Атомный вес: 92.
(2)Описание: Ниобий – нержавеющий металл с высокой температурой плавления.
Где он используется: Ниобий используется в сплавах нержавеющей стали. Сплавы, произведенные с ниобием, очень прочны и часто используются в трубопроводах и реактивных двигателях.
Молибден
Символ: Mo
Атомный вес: 95.95 (1)
Описание: Молибден – металл с высокой температурой плавления.
Где используется: Молибден используется для изготовления сплавов, используемых в деталях ракет и самолетов, а также в ядерной энергетике и в нагревательных элементах. Его можно использовать для очистки нефти, но в основном он используется в качестве легирующего агента для очистки стали. Дисульфид молибдена используется в качестве присадки к смазочным материалам.
Технеций
Символ: Tc
Атомный вес: [98]
Описание: Технеций – долгоживущий радиоактивный элемент.
Где используется: Технеций – это синтезированный элемент, который можно использовать в качестве радиоактивного индикатора.
Рутений
Символ: Ru
Атомный вес: 101,07 (2)
Описание: Рутений – твердый металл, который не вызывает коррозии.
Где используется: Рутений используется в качестве катализатора для упрочнения металлов. Он также используется в электрических контактах и для цветного стекла.
Родий
Символ: Rh
Атомный вес: 102.
(2)
Описание: Родий – не корродирующий твердый блестящий металл.
Где используется: Родий используется для производства электрических контактов. Это использование распространяется на каталитические нейтрализаторы, но в основном оно используется в качестве легирующего агента. Сплавы родия можно использовать в печах, электродах и свечах зажигания.
Палладий
Символ: Pd
Атомный вес: 106,42 (1)
Описание: Палладий – это не подверженный коррозии твердый металл, который легко поглощает водород.
Где используется: Палладий – важный элемент процесса каталитической конверсии. Он также используется в украшениях и зубных пломбах.
Серебро
Символ: Ag
Атомный вес: 107,8682 (2)
Описание: Серебро – мягкий блестящий металл, который является лучшим проводником электричества.
Где используется: Серебро используется в ювелирных изделиях и посуде. Это лучший отражатель видимого света, хотя он и тускнеет.Он используется в паяльных и паяльных смесях, а также в аккумуляторах. Серебряные краски используются для изготовления печатных схем. Серебро также обладает антибактериальными свойствами, и недавно наночастицы серебра стали использовать в одежде для предотвращения роста бактерий и создания неприятных запахов.
Кадмий
Символ: Cd
Атомный вес: 112,414 (4)
Описание: Кадмий – это некорродирующий мягкий металл, который токсичен.
Где используется: Кадмий ядовит, поэтому практического применения у него мало. Его можно использовать для предотвращения коррозии или поглощения нейтронов в ядерных реакторах. Одно из его наиболее коммерческих применений – перезаряжаемые никель-кадмиевые батареи.
Индий
Символ: In
Атомный вес: 114,818 (1)
Описание: Индий – это мягкий металл класса .
Где он используется: Индий в основном используется в качестве легирующего агента для германия в процессе производства транзисторов.Он также используется для изготовления зеркал с высокой отражающей способностью и легкоплавких сплавов.
Олово
Символ: Sn
Атомный вес: 118,710 (7)
Описание: Олово – это мягкий металл, не подверженный коррозии.
Где используется: Олово хорошо полируется и не подвержено коррозии. Он в основном используется для покрытия других металлов или в качестве сплава припоя и олова. Магниты ниобий-олово известны своей сверхпроводящей способностью.
Сурьма
Символ: Sb
Атомный вес: 121,760 (1)
Описание: Сурьма – хрупкий металлоид.
Где используется: Сурьма в основном используется в аккумуляторах, оболочках кабелей и других металлических изделиях. Его можно использовать для изготовления огнестойких материалов и красок. Древние египтяне использовали этот элемент в качестве макияжа для глаз.
Изображение:
Источник: MindatТеллур
Символ: Te
Атомный вес: 127.60 (3)
Описание: Теллур – хрупкий металлоид.
Где используется: Теллур обеспечивает лучшую обрабатываемость меди и нержавеющей стали. Используется как базовый компонент чугуна и капсюлей-детонаторов.
Йод
Символ: I
Атомный вес: 126.
(3)Описание: Йод представляет собой фиолетово-черное твердое вещество.
Где используется: Соли йода используются в фотопленке и как антисептик для ран.Радиоактивный изотоп йода-131 используется для лечения рака щитовидной железы. Его часто добавляют в небольших количествах в поваренную соль, чтобы избежать дефицита йода.
Ксенон
Символ: Xe
Атомный вес: 131,293 (6)
Описание: Ксенон – инертный газ.
Где он используется: Ксенон используется в фотографических вспышках и дуговых лампах для съемок фильмов. Под давлением в дуговой лампе он может излучать ультрафиолетовый свет.Он также используется для обнаружения радиации и в счетчиках рентгеновского излучения.
Цезий
Символ: Cs
Атомный вес: 132.
196 (6)Описание: Цезий (цезий) – это мягкий металл, который является реактивным и имеет самые большие стабильные атомы.
Где используется: Цезий используется в вакуумных трубках для удаления следовых газов. Чаще всего он используется в качестве соединения в буровом растворе. Одно из наиболее важных применений – в «цезиевых часах» (атомных часах) и в качестве катализатора процесса гидрирования.
Вспомогательное видео:
Барий
Символ: Ba
Атомный вес: 137,327 (7)
Описание: Барий – мягкий металл, поглощающий рентгеновские лучи.
Где используется: Барий используется для получения зеленого свечения в пиротехнике. Он также используется для удаления газов из вакуумных трубок. Соединения бария используются в качестве контрастного вещества в рентгеновских лучах.
Лантан
Символ: La
Атомный вес: 138. (7)
Описание: Лантан – мягкий металл.
Где он используется: Лантан используется вместе с редкоземельными элементами для изготовления дуговых ламп. Он также составляет около 20 процентов мишметала, сплава, используемого в кремне зажигалок. Сплав лантана и никеля используется для хранения газообразного водорода для использования в транспортных средствах, работающих на водороде, а лантан также используется в никель-металлогидридных батареях.
Церий
Символ: Ce
Атомный вес: 140.116 (1)
Описание: Церий – мягкий металл.
Где используется: Церий также используется в качестве компонента мишметалла для производства кремня для зажигалок. Его можно использовать в качестве катализатора для очистки масла. Оксид церия также используется в качестве компонента стенок самоочищающихся духовок.
Празеодим
Символ: Pr
Атомный вес: 140.
(2)Описание: Празеодим – мягкий металл.
Где используется: Празеодим используется для изготовления очков из желтого стекла для сварщиков. Празеодим также используется в кремневых зажигалках. Однако в основном он используется для окрашивания стекла и эмали.
Неодим
Символ: Nd
Атомный вес: 144,242 (3)
Описание: Неодим – мягкий металл.
Где он используется: Наиболее важным применением неодима является сплав железа и бора для создания очень сильных постоянных магнитов.Неодим используется для изготовления кремня для зажигалок и входит в состав специализированных защитных очков сварщика. Неодимовое стекло используется для изготовления лазеров, а оксид и нитрат неодима используются в качестве катализаторов в реакциях полимеризации.
Прометий
Символ: Pm
Атомный вес: [145]
Описание: Прометий – долгоживущий радиоактивный элемент.
Где используется: Прометий используется в основном для исследований в области радиации.Его можно использовать в ядерных батареях и как источник света для сигналов. Исследователи полагают, что вскоре его можно будет использовать в портативных рентгеновских аппаратах.
Самарий
Символ: Sm
Атомный вес: 150,36 (2)
Описание: Самарий – это мягкий металл класса .
Где используется: Самарий используется в качестве катализатора дегидратации и дегидрирования этанольного топлива. Его также можно использовать для поглощения инфракрасных лучей и при лечении рака.
Европий
Символ: Eu
Атомный вес: 151.964 (1)
Описание: Европий – мягкий металл.
Где используется: Европий является хорошим поглотителем нейтронов, поэтому его часто используют в ядерных реакторах. Одно из его соединений также используется для производства красного фосфора в телевизорах.
Гадолиний
Символ: Gd
Атомный вес: 157.25 (3)
Описание: Гадолиний – мягкий металл, который является лучшим поглотителем нейтронов и обладает магнитными свойствами.
Где он используется: Гадолиний часто используется в приложениях, где присутствуют микроволны. Его также можно использовать в телевизионных трубках с зеленым люминофором. Элемент является магнитным, что привело к его использованию в аппаратах МРТ.
Диаграмма:
Источник: Грег РобсонТербий
Символ: Tb
Атомный вес: 158. (2)
Описание: Тербий – мягкий металл.
Где используется: Тербий используется в качестве стабилизатора высокотемпературных топливных элементов. Его сплавы также используются в электронных устройствах и в качестве индикаторов магнитного поля.
Диспрозий
Символ: Dy
Атомный вес: 162,500 (1)
Описание: Диспрозий – мягкий металл.
Где он используется: В сочетании с редкоземельными элементами диспрозий используется в качестве материала для лазеров.Его также можно использовать в стержнях ядерных реакторов.
Гольмий
Символ: Ho
Атомный вес: 164.93033 (2)
Описание: Гольмий – мягкий металл.
Где используется: Гольмий используется в производстве магнитов в качестве концентратора потока. Он также используется в желтом или красном цвете при производстве фианита.
Эрбий
Символ: Er
Атомный вес: 167.259 (3)
Описание: Эрбий – мягкий металл
Где он используется: Эрбий является хорошим поглотителем нейтронов, что позволяет использовать его в стержнях ядерного контроля. Его также можно использовать для снижения твердости металлов, а также для применения в усилителях и лазерах.
Тулий
Символ: Tm
Атомный вес: 168.93422 (2)
Описание: Тулий – мягкий металл.
Где используется: Тулий – наименее встречающийся в природе элемент на Земле.При облучении тулий производит изотоп, который испускает рентгеновские лучи, и его можно использовать для изготовления легкого портативного рентгеновского аппарата. Тулий также используется в некоторых хирургических лазерах.
Иттербий
Символ: Yb
Атомный вес: 173,045 (10)
Описание: Иттербий – мягкий металл.
Где он используется: Иттербий считается полезным для измельчения зерна в стали. Его также можно использовать в качестве промышленного катализатора.
Лютеций
Символ: Lu
Атомный вес: 174.9668 (1)
Описание: Лютеций – мягкий металл, самый плотный и твердый редкоземельный металл.
Где используется: Лютеций очень редок и дорог. После очистки его можно использовать в процессе крекинга нефти. Есть несколько других коммерческих приложений.
Гафний
Символ: Hf
Атомный вес: 178.49 (2)
Описание: Гафний – это нержавеющий металл, поглощающий нейтроны.
Где используется: Гафний является хорошим поглотителем нейтронов, поэтому он используется в стержнях ядерного управления на атомных подводных лодках. Благодаря высокой температуре плавления он также используется в горелках для плазменной сварки. Оксид гафния используется в микрочипах.
Тантал
Символ: Ta
Атомный вес: 180.94788 (2)
Описание: Тантал – это металл с высокой температурой плавления, не подверженный коррозии.
Где он используется: Тантал используется в электронной промышленности для изготовления конденсаторов и резисторов. Его можно использовать для увеличения прочности металлических сплавов, а также для повышения коррозионной стойкости. Металл также используется в хирургических инструментах, поскольку не вызывает иммунного ответа.
Вольфрам
Символ: W
Атомный вес: 183,84 (1)
Описание: Вольфрам – металл с самой высокой температурой плавления.
Где он используется: Вольфрам имеет самую высокую температуру плавления из всех металлов, что позволяет использовать его в качестве нитей накаливания в лампах накаливания. Он также используется в стали для придания прочности.
Рений
Символ: Re
Атомный вес: 186.207 (1)
Описание: Рений – это плотный металл с высокой температурой плавления.
Где используется: Рений – распространенный катализатор при производстве высокооктанового бензина.Он также используется в сплавах для реактивных двигателей и в качестве нитей для масс-спектрографов.
Осмий
Символ: Os
Атомный вес: 190,23 (3)
Описание: Осмий – это некорродирующий твердый металл с высокой температурой плавления и самый плотный элемент.
Где он используется: Осмий в основном используется для изготовления твердых сплавов. Вы можете найти его в наконечниках шариковых ручек, иглах для записей, электрических контактах и других металлических компонентах, где необходимо уменьшить трение.
Иридий
Символ: Ir
Атомный вес: 192.217 (3)
Описание: Иридий – твердый металл, не подверженный коррозии, а также самый плотный элемент (такой же, как Os).
Где он используется: Иридий в основном используется в качестве отвердителя для платины. Этот элемент также используется в качестве сплава в наконечниках перьевых ручек и подшипниках компаса, а также в контактах свечей зажигания.
Платина
Символ: Pt
Атомный вес: 195.084 (9)
Описание: Платина – не корродирующий плотный металл.
Где используется: Платина известна своими антикоррозийными свойствами и уже давно используется для изготовления ювелирных изделий. Его основное применение – каталитические нейтрализаторы для автомобилей.
Золото
Символ: Au
Атомный вес: 196.966569 (5)
Описание: Золото является наиболее пластичным элементом и представляет собой плотный не тускнеющий цветной металл.
Где оно используется: Золото – один из самых востребованных металлов в мире, потому что ему легко придавать форму и скульптуру, он хорошо проводит электричество и не тускнеет. Помимо использования в чеканке монет и ювелирных изделий, он используется в механизмах для часов, суставов протезов и электрических соединителей. Наночастицы золота используются в качестве промышленных катализаторов.
Ртуть
Символ: Hg
Атомный вес: 200,592 (3)
Описание: Ртуть является жидким металлом и токсична.
Где используется: Ртуть используется для изготовления термометров, барометров, электрических переключателей и других инструментов. Он часто используется в уличных и люминесцентных лампах, а также в химической промышленности в качестве катализатора.
Таллий
Символ: Tl
Атомный вес: 204,38
Описание: Таллий – токсичный мягкий металл.
Где используется: Таллий используется для образования стекла с низкой температурой плавления.Когда-то его использовали как крысиный яд, но теперь его запрещено использовать в домашних условиях.
Свинец
Символ: Pb
Атомный вес: 207,2 (1)
Описание: Свинец – это плотный, мягкий, не подверженный коррозии токсичный металл.
Где он используется: Многие ранее распространенные виды использования свинца теперь запрещены из-за его токсических эффектов. Он по-прежнему широко используется для автомобильных аккумуляторов, пигментов, боеприпасов, оболочки кабелей, свинцового хрусталя, радиационной защиты и некоторых припоев.
Висмут
Символ: Bi
Атомный вес: 208.98040 (1)
Описание: Висмут – хрупкий металл с низкой температурой плавления.
Где используется: Висмут обычно используется в пожарных извещателях и системах пожаротушения из-за его низкой температуры плавления. Это также привело к его использованию в электрических предохранителях.
Полоний
Символ: Po
Атомный вес: [209]
Описание: Полоний – долгоживущий радиоактивный элемент.
Где он используется: Полоний используется в качестве атомного источника тепла для краткосрочного использования. Это также видно в антистатических щетках и в пленке.
Астатин
Символ: At
Атомный вес: [210]
Описание: Астатин – это короткоживущий радиоактивный элемент.
Где он используется: Астатин используется в качестве радиоактивного индикатора и при лечении рака.
Радон
Символ: Rn
Атомный вес: [222]
Описание: Радон – короткоживущий радиоактивный газ.
Где он используется: Радон используется для лечения рака. Его часто производили в больницах, выкачивая радон из радия, а затем запечатывая его в трубках.
Франций
Символ: Fr
Атомный вес: [223]
Описание: Франций является радиоактивным и короткоживущим элементом с атомами больше, чем цезий.
Где используется: Самый стабильный изотоп франция, франций-223, имеет период полураспада 22 минуты.Из-за короткого срока службы этот элемент не имеет коммерческого использования.
Радий
Символ: Ra
Атомный вес: [226]
Описание: Радий – долгоживущий радиоактивный элемент.
Где он используется: Радий используется в качестве источника нейтронов, а также используется для производства радона. Один грамм радия-226 будет производить 0,0001 мл радона каждый день. Элемент в 1000000 раз активнее урана.
Актиний
Символ: Ac
Атомный вес: [227]
Описание: Актиний – долгоживущий радиоактивный элемент.
Где используется: Актиний применяется в медицине для радиоиммунотерапии. Он встречается только в урановой руде, что делает его очень дорогим. Одна тонна урана производит эквивалент 1/10 грамма актиния.
Торий
Символ: Th
Атомный вес: 232.0377 (4)
Описание: Торий – долгоживущий радиоактивный элемент.
Где он используется: Торий используется для покрытия нитей в лампах накаливания. Его можно использовать в качестве ядерного топлива в ториевых реакторах, хотя это совершенно новая технология. Торий также является легирующим агентом в магнии, а оксид тория используется в качестве промышленного катализатора.
Протактиний
Символ: Па
Атомный вес: 231.03588 (2)
Описание: Протактиний – долгоживущий радиоактивный элемент.
Где он используется: В настоящее время протактиний не используется в коммерческих целях из-за его относительной редкости.
Уран
Символ: U
Атомный вес: 238.02891 (3)
Описание: Уран – долгоживущий радиоактивный элемент.
Где он используется: Уран используется в качестве ядерного топлива для ядерных энергетических реакторов и производит материал, необходимый для ядерного оружия.Он также используется как краситель для стекла. Это также основной материал, из которого сделаны другие синтетические трансурановые элементы.
Нептуний
Символ: Np
Атомный вес: [237]
Описание: Нептуний – долгоживущий радиоактивный элемент.
Где используется: Нептуний не имеет известных коммерческих применений.
Плутоний
Символ: Pu
Атомный вес: [244]
Описание: Плутоний – долгоживущий радиоактивный элемент.
Где он используется: Плутоний используется в качестве ядерного топлива и в ядерном оружии.
Вспомогательное видео:
Америций
Символ: Am
Атомный вес: [243]
Описание: Америций – долгоживущий радиоактивный элемент.
Где используется: Америций используется в детекторах дыма и в качестве портативного источника гамма-излучения.
Кюрий
Символ: Cm
Атомный вес: [247]
Описание: Кюрий – долгоживущий радиоактивный элемент.
Где используется: Кюрий в основном используется для исследований, но в будущем он может производить больше ядерной энергии на грамм, чем плутоний.
Берклий
Символ: Bk
Атомный вес: [247]
Описание: Берклий – это долгоживущий радиоактивный элемент.
Где используется: Berkelium не используется в коммерческих целях из-за своей редкости.
Калифорний
Символ: Cf
Атомный вес: [251]
Описание: Калифорний – долгоживущий радиоактивный элемент.
Где используется: Калифорний – сильный излучатель нейтронов. Используется в металлоискателях на серебро и золото. Его также можно использовать для определения подземных нефтяных пластов и определения усталости металла в аэрокосмической сфере.
Эйнштейний
Символ: Es
Атомный вес: [252]
Описание: Эйнштейний – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Фермий
Символ: Fm
Атомный вес: [257]
Описание: Фермий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Менделевий
Символ: Md
Атомный вес: [258]
Описание: Менделевий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Нобелий
Символ: №
Атомный вес: [259]
Описание: Нобелий – короткоживущий радиоактивный элемент
Где он используется: Не используется вне исследований .
Лоуренсий
Символ: Lr
Атомный вес: [266]
Описание: Лоуренсий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Резерфордий
Символ: Rf
Атомный вес: [267]
Описание: Резерфордий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Дубний
Символ: Db
Атомный вес: [268]
Описание: Дубний – короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Сиборгий
Символ: Sg
Атомный вес: [269]
Описание: Сиборгий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Bohrium
Символ: Bh
Атомный вес: [270]
Описание: Bohrium – это короткоживущий радиоактивный элемент .
Где используется: Не используется вне исследований.
Калий
Символ: Hs
Атомный вес: [277]
Описание: Калий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Мейтнерий
Символ: Mt
Атомный вес: [278]
Описание: Мейтнерий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Дармштадций
Символ: Ds
Атомный вес: [281]
Описание: Дармштадций – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Рентгений
Символ: Rg
Атомный вес: [282]
Описание: Рентгений – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Copernicium
Символ: Cn
Атомный вес: [285]
Описание: Copernicium – это короткоживущий радиоактивный элемент .
Где используется: Не используется вне исследований.
Nihonium
Symbol: Nh
Атомный вес: [286]
Описание: Nihonium – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Флеровий
Символ: Fl
Атомный вес: [289]
Описание: Флеровий – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Московий
Символ: Mc
Атомный вес: [290]
Описание: Московий – это короткоживущий радиоактивный элемент .
Где используется: Не используется вне исследований.
Вспомогательное видео:
Livermorium
Символ: Lv
Атомный вес: [293]
Описание: Ливерморий является короткоживущим радиоактивным элементом.
Где используется: Не используется вне исследований.
Tennessine
Символ: Ts
Атомный вес: [294]
Описание: Tennessine – это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Оганессон
Символ: Ог
Атомный вес: [294]
Описание: Оганессон – это короткоживущий радиоактивный элемент.Это самый тяжелый элемент, известный человеку (на момент написания).
Где используется: Не используется вне исследований.
Периодическая таблица показывает, как мы используем каждый элемент
Согласно опросу, проведенному базирующейся в Филадельфии некоммерческой организацией The Science History Institute, большинство американцев (59% из нас) не могут назвать более 10 из 118 элементов периодической таблицы. По данным Live Science, каждый пятый американец не может назвать ни одного элемента.
Даже если вы можете назвать все элементы на столе, знаете ли вы, что они на самом деле делают в реальной жизни? Если пришло время пройти курс повышения квалификации по периодической таблице, вам могут помочь эти графические изображения, созданные инженером-программистом Boeing Китом Эневольдсеном.
Во-первых, краткое резюме: периодическая таблица – это диаграмма, в которой химические элементы расположены в порядке возрастания атомного номера, выстроенные так, чтобы элементы, обладающие схожими свойствами, располагались в той же строке или столбце, что и другие. Таблица Менделеева считается одним из самых полезных научных инструментов.
Adobe
ВерсияЭневольдсена, названная «Периодическая таблица элементов в картинках и словах», содержит всю информацию, содержащуюся в традиционной периодической таблице, но включает пиктограммы и ярлыки, показывающие, где вы можете встретить каждый элемент в повседневной жизни.
Он был создан, чтобы помочь учащимся начальных классов средней школы, но также может использоваться взрослыми, которые хотят освежить свои знания в области химии.
Например, иттрий сочетается с лазерами, а осмий находится рядом с изображением точек пера. Довольно круто, правда?
Кейт Эневольдсен
А знаете ли вы, что бор используется для изготовления спортивного инвентаря, а сера содержится в яйцах?
Кейт Эневольдсен
Согласно веб-сайту Эневольдсена, элементы имеют цветовую кодировку в таблице в соответствии с химическими группами.
«Другие информационные панели описывают атомную структуру, химические связи и радиоактивность», – продолжает пояснение на веб-сайте.