Знаменитая таблица Менделеева
ДМИТРИЙ ИВАНОВИЧ МЕНДЕЛЕЕВ
Автор: Сергей НЕЧАЕВ
30.12.2021
История науки знает множество открытий, однако немногие из них можно сопоставить с тем, что было сделано Дмитрием Ивановичем Менделеевым. В самом деле, хотя со времени открытия периодического закона химических элементов прошло немало лет, никто не может сказать, когда будет до конца понято все глубочайшее содержание знаменитой «таблицы Менделеева». Только вот вопрос: а кто же все-таки придумал ее первым?
Дмитрий Иванович Менделеев родился 27 января (8 февраля) 1834 года в Тобольске. В январе 1865 года он защитил докторскую диссертацию и был утвержден профессором кафедры технической химии Петербургского университета.
ОТКРЫТИЕ, СДЕЛАННОЕ «ВО СНЕ»
Принято считать, что свою периодическую таблицу Менделеев увидел во сне, и ему оставалось лишь записать ее и обосновать.
Дмитрий Иванович говорил своему другу философу И.И. Лапшину, посетившему его незадолго перед открытием: «Все в голове сложилось, а выразить таблицей не могу».
Получается, что Менделеев работал, как сумасшедший, три дня и три ночи не ложась спать. Доведя себя до крайней степени нервного истощения, он, как сейчас говорят, «отключился», и тут-то его и посетило «озарение».
Скорее всего, вся эта история с вещим сном лишь подтверждает тот факт, что люди, которые очень интенсивно работают над какой-либо проблемой, просто продолжают решать ее и во сне, только в этом случае к мыслительной деятельности подключается уже подсознание. Именно оно способно на такие величайшие научные «подвиги».
Конечно же, открытие Менделеева было совершено им не случайно, и уж точно не во сне. Всему этому предшествовала огромная работа, основанная на сочетании знаний физической стороны исследуемого явления, математической интуиции и философского осмысления. 17 февраля (1 марта) 1869 года Менделеев отправил в типографию рукопись, в которой был изложен его «Опыт системы элементов, основанной на их атомном весе и химическом сходстве». Уже через две недели он представил в Русское химическое общество статью «Соотношение свойств с атомным весом элементов».
В конечном итоге, Менделеев составил несколько вариантов периодической системы и на ее основе исправил атомные веса некоторых известных элементов.
С этого момента все другие проблемы отошли для него на задний план. В частности, он забросил работу над учебником «Основы химии» (труд этот будет закончен лишь в 1871 году). Распределение элементов в составленной им таблице каждый раз казалось ему несовершенным.
Закончилось все это тем, что Менделеев сумел предсказать существование нескольких до того неизвестных элементов. Более того, в одной из своих статей он подробно описал свойства трех из них: он назвал эти элементы «экабором», «экаалюминием» и «экакремнием» (или «экасилицием»). Чтобы было понятно: «эка» – на санскрите означает «первый», так что название, например, «экаалюминий» означает «первый аналог алюминия».
Так на свет появилась фундаментальная схема, которой до сих пор пользуются как школьники, так и ученые во всем мире.
ЮЛИУС ЛОТАР МЕЙЕР
И все же, справедливости ради, возвращаясь к знаменитой таблице Менделеева, необходимо отметить, что у нее был еще один «автор». Его звали Юлиус Лотар Мейер, и был он доктором медицины, занимавшимся вопросами теоретической и физической химии.
Этот человек родился 19 августа 1830 года в семье врача в маленьком городке Фарель, что в провинции Ольденбург.
Работая в Гейдельберге, Мейер поддерживал научные контакты с химиками-органиками Августом Кекуле и Фридрихом Бейльштейном, и это привело Мейера к решению серьезно заняться химией.
В 1859 году Мейер защитил как диссертацию на право чтения лекций историко-критическую работу «Химические теории от Бертолле до Берцелиуса».
В 1860 году Мейер, как и Д.И. Менделеев, принял участие в Международном конгрессе химиков в Карлсруэ, на котором обсуждались определения основных понятий химии. На этом конгрессе, в частности, было решено четко разграничить понятия «атом», «молекула» и «эквивалент». В результате, была в основном решена проблема атомных масс, что открыло дорогу для систематизации химических элементов и создания периодического закона.
На этом конгрессе, в частности, было решено четко разграничить понятия «атом», «молекула» и «эквивалент». В результате, была в основном решена проблема атомных масс, что открыло дорогу для систематизации химических элементов и создания периодического закона.
В «Краткой истории химии» Айзека Азимова сказано: «Мейер опубликовал свою работу в 1870 году. А за год до этого русский химик Дмитрий Иванович Менделеев (1834–1907) установил порядок изменения длины периодов элементов и наглядно продемонстрировал значение своего открытия».
Это не совсем так. На самом деле, Менделеев не был первым человеком, который построил научную классификацию элементов. Юлиус Лотар Мейер на основании данных об атомных весах предложил таблицу, показывающую соотношение атомных весов для нескольких характерных групп элементов, намного раньше – в 1864 году.
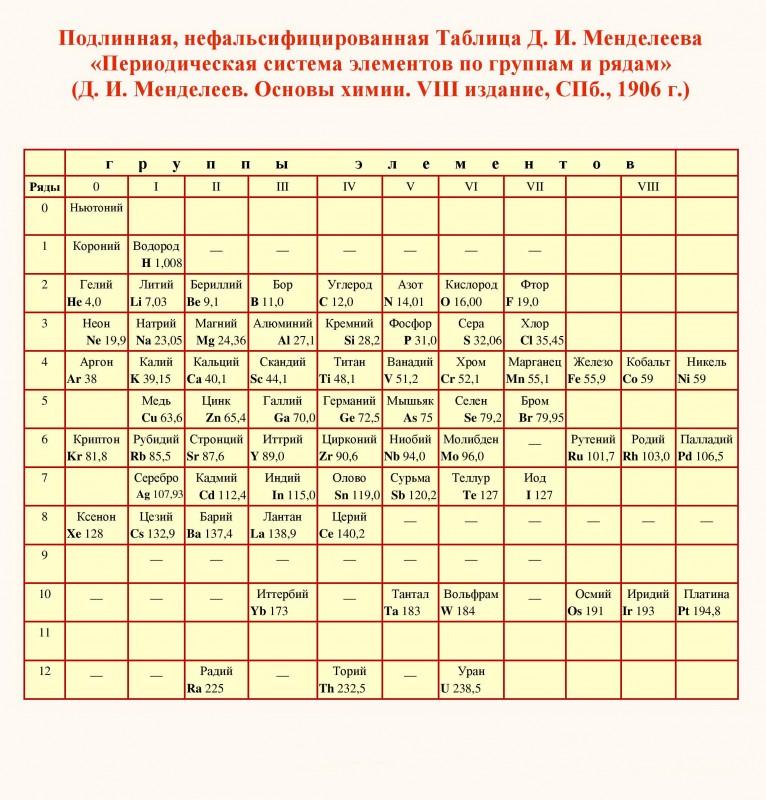
В таблице Мейера было 28 элементов, размещенных в шесть столбцов согласно их валентностям.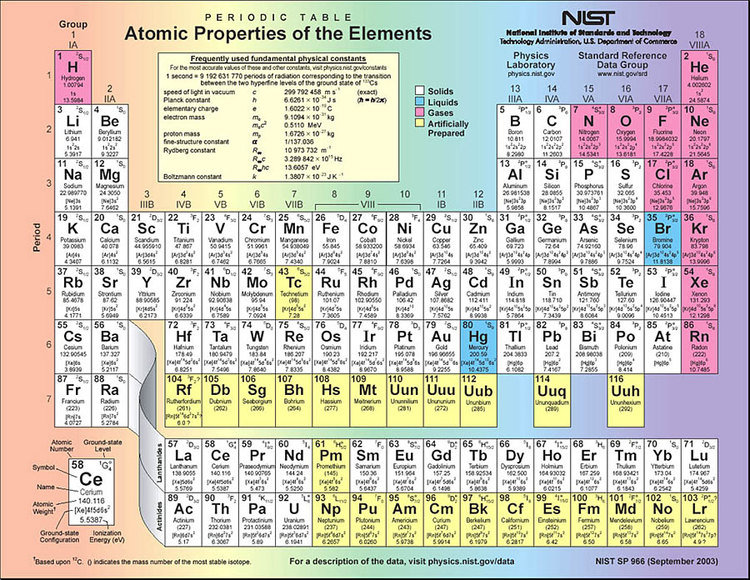
Специалисты совершенно справедливо считают эту таблицу Мейера сокращенной, ибо в ней ученый отобразил только те 28 элементов, в свойствах которых он был уверен. Всего 28 элементов, а это – меньше половины известных в то время. Расположение остальных элементов оставалось неясным, и что делать с ними, Мейер не знал.
Более того, в 1864 году Мейер предложил располагать элементы по группам, но дальше этого предложения не пошел и понятие «группа элементов» не раскрыл.
ТАБЛИЦА МЕЙЕРА 1870 ГОДА
В 1870 году Мейер опубликовал еще одну работу, называвшуюся «Природа химических элементов как функция их атомного веса» и содержавшую новую таблицу, состоявшую уже из девяти вертикальных столбцов (сходные элементы располагались в горизонтальных рядах, а некоторые ячейки таблицы Мейер оставил незаполненными). В новой таблице отображалось уже 55 элементов, и она была понятна и удобна для отображения в книгах.
В новой таблице отображалось уже 55 элементов, и она была понятна и удобна для отображения в книгах.
В своей работе Мейер систематизировал элементы и изобразил их в виде кривой, где атомные объемы являются периодической функцией от значений атомных масс. Он так характеризовал эту зависимость: «Правильно определив различные атомные веса (из плотностей их соединений в газообразном состоянии или из теплоемкостей), можно в этой схеме расположить все известные до настоящего времени элементы».
ТАБЛИЦА МЕЙЕРА И ТАБЛИЦА МЕНДЕЛЕЕВА: ЗА КЕМ ПРИОРИТЕТ?
Как уже говорилось, Д.И. Менделеев составил и опубликовал свою знаменитую таблицу в феврале-марте 1869 года. Точнее, это был некий отдаленный прототип ныне всем известной периодической системы элементов. Он выстроил символы известных ему 63 элементов в прообраз периодической таблицы элементов вертикальной формы, а потом эту свою таблицу он корректировал и совершенствовал всю жизнь.
Мейер опубликовал свою редакцию периодической таблицы химических элементов в 1864 году, то есть на пять лет раньше Менделеева.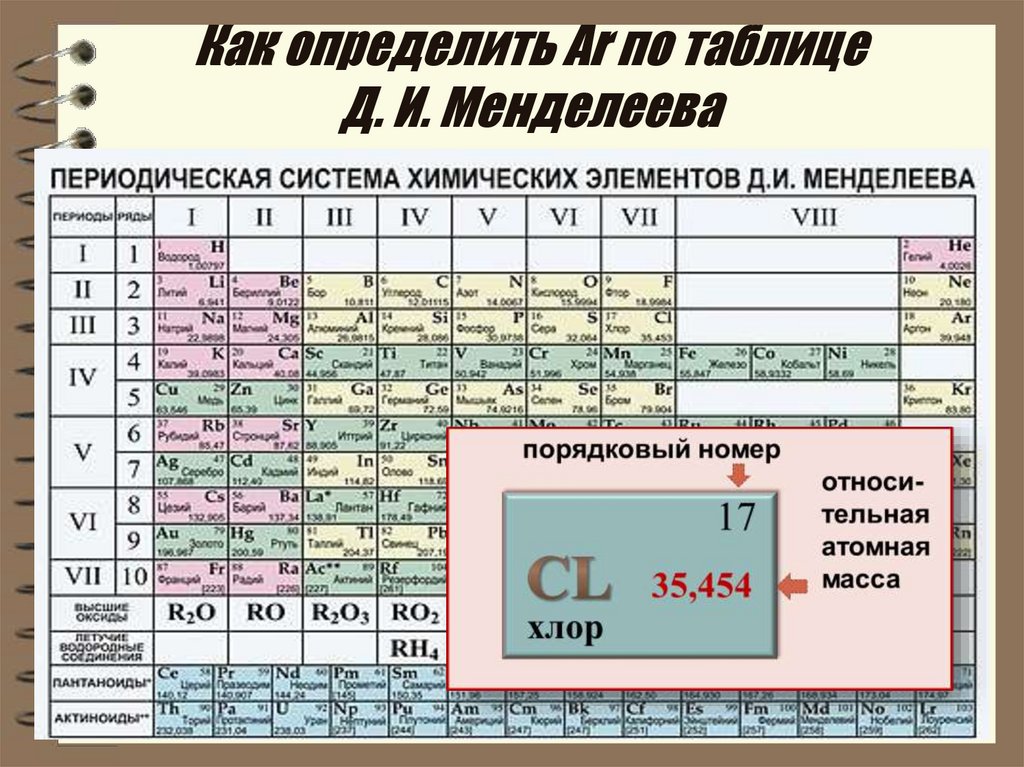
В 1870 году, то есть уже после опубликования Менделеевым периодического закона, появилась статья Мейера, в которой он рассмотрел общую систему химических элементов, расположив их по возрастанию атомных масс. По мнению ряда специалистов, таблица Мейера 1870 года была в некоторых отношениях совершеннее первых вариантов таблицы Менделеева. При этом сам Дмитрий Иванович в одной из своих статей заявил, что таблица Мейера представляла собой только простое сопоставление элементов, на что Мейер отвечал, что его таблица «в существенном идентична данной Менделеевым».
Дмитрий Иванович возмущенно писал: «Господин Мейер раньше меня не имел в виду периодического закона, а после меня ничего нового к нему не прибавил».
Более того, согласно Менделееву, Мейер не стал развивать свое открытие и даже не сделал попыток на его основе дать предсказания свойств еще не открытых элементов. Свое мнение по этому вопросу Дмитрий Иванович сформулировал так: «По праву творцом научной идеи должно того считать, кто понял не только философскую, но и практическую сторону дела, сумел так его поставить, что в новой истине все могли убедиться, и она стала всеобщим достоянием. Тогда только идея, как материя, не пропадет».
Тогда только идея, как материя, не пропадет».
Получается, что Мейер был все еще очень далек даже от понимания истинного смысла периодической системы. Менделеев же открывал элементы и предсказывал их свойства, опираясь на пустые клетки в созданной им таблице.
На самом деле, Мейер был очень осторожен в оглашении своих научных суждений. И поначалу он избегал публиковать свои прогнозы свойств еще неоткрытых элементов. И именно отсутствие у Мейера успешных научных прогнозов свойств еще неоткрытых элементов некоторые ученые расценили как намного меньшую научную достоверность его периодической таблицы по сравнению с таблицей Менделеева.
Тем не менее, Мейер уже через несколько месяцев после появления первых сообщений Менделеева об открытом им периодическом законе выступил с претензией на свой приоритет. И многие, особенно в Германии (это и понятно), до сих пор считают именно Мейера первооткрывателем периодической системы.
В свое время вокруг имен Мейера и Менделеева разгорелась весьма острая дискуссия, кто же из них первым сделал великое открытие. И до сих пор в зарубежных изданиях имена Менделеева и Мейера ставят рядом там, где речь идет о периодическом законе и периодической системе химических элементов, причем имя Мейера выдвигают на «полкорпуса вперед».
И до сих пор в зарубежных изданиях имена Менделеева и Мейера ставят рядом там, где речь идет о периодическом законе и периодической системе химических элементов, причем имя Мейера выдвигают на «полкорпуса вперед».
Кстати
Фигура Менделеева всегда была окружена всевозможными мифами. Один из самых распространенных – якобы Менделеев сделал научное обоснование стандарта русской водки в 40 градусов. Связано это с тем, что тема его докторской диссертации звучала так: «Рассуждение о соединении спирта с водою». Но к водке это не имело никакого отношения. Работа была посвящена очень узкой научной проблематике, связанной с теорией растворов.
А в 1882 году Лондонское королевское общество присудило золотые медали совместно Менделееву и Мейеру. Наградам сопутствовала формулировка: «За открытие периодических соотношений атомных весов».
ГЛАВНОЕ – ОТКРЫТИЕ ПЕРИОДИЧЕСКОЙ ЗАВИСИМОСТИ
Дмитрий Иванович Менделеев умер 20 января (2 февраля) 1907 года. Юлиус Лотар Мейер умер намного раньше – в апреле 1895 года.
Юлиус Лотар Мейер умер намного раньше – в апреле 1895 года.
Юлиус Лотар Мейер
Когда Менделеев придумывал свою таблицу, было известно лишь 63 химических элемента. В год смерти ученого был открыт «лютеций», получивший 71-й номер. Сотым элементом стал «фермий», впервые полученный в конце 1952 года. А в 1955 году американские ученые синтезировали элемент № 101, и ему было дано название «менделевий» (Md) – в честь Д.И. Менделеева.
Интересно отметить, что на сегодняшний день официально известно уже 118 химических элементов, из них 94 было обнаружено в природе, а остальные получены искусственно, и это уже исключительно ядерная физика.
Химические элементы делятся на металлы и неметаллы, причем к металлам относятся 85% из них. 99% земной коры по массе составляют лишь восемь химических элементов: кислород, калий, натрий, магний, кальций, железо, алюминий, кремний. Водород и гелий – элементы, преобладающие в космосе. В живых организмах наиболее распространенные элементы – это азот, водород, кислород, углерод.
В живых организмах наиболее распространенные элементы – это азот, водород, кислород, углерод.
Джон Ньюлендс
Как видим, наука шагнула очень далеко вперед. В свое время Менделеев так сформулировал текст предполагаемого им периодического закона: «Свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Современная формулировка такова: «Свойства химических элементов, а также формы и свойства, образуемых ими простых веществ и соединений, находятся в периодической зависимости от величины зарядов ядер их атомов».
Что же касается Мейера, то он в свое время опубликовал кривую изменения атомных объемов элементов. Она действительно отражала одно из свойств периодического закона, и этим Мейер существенно содействовал систематизации элементов. Но все дело в том, что сам Мейер не смог разглядеть общей закономерности природы – периодичности. Менделеев же совершенно правильно предположил, что свойствами элементов управляет периодический закон, и алгоритм этого периодического закона был реализован им в графической форме в виде его периодической таблицы элементов.
Менделеев же совершенно правильно предположил, что свойствами элементов управляет периодический закон, и алгоритм этого периодического закона был реализован им в графической форме в виде его периодической таблицы элементов.
А ВЕДЬ БЫЛ ЕЩЕ И ДЖОН НЬЮЛЕНДС
В данном контексте следует также упомянуть о британском химике Джоне Ньюлендсе (1837–1898). В 1864 году он тоже составил таблицу, в которой расположил все известные тогда элементы в порядке увеличения их атомных весов. Пронумеровав элементы (элементы, имевшие одинаковые веса, имели у него один и тот же номер), Ньюлендс сделал следующий вывод: «Разность в номерах наименьшего члена группы и следующего за ним равна семи; иначе говоря, восьмой элемент, начиная с данного элемента, является своего рода повторением первого, подобно восьмой ноте октавы в музыке».
Через год Ньюлендс опубликовал новую таблицу, назвав ее «законом октав», который формулировался следующим образом: «Номера аналогичных элементов, как правило, отличаются или на целое число семь, или на кратное семи; другими словами, члены одной и той же группы соотносятся друг с другом в том же отношении, как и крайние точки одной или больше октав в музыке».
После 1866 года Джон Ньюлендс больше не предпринимал попыток дальнейшей разработки своей систематики, тем не менее, именно его в Великобритании считают тем, кто впервые высказал идею о периодичности изменения свойств элементов. В любом случае, в 1887 году, через пять лет после Менделеева и Мейера, Лондонское королевское общество вручило свою медаль и ему. Награде сопутствовала формулировка: «За открытие периодического закона химических элементов».
Дмитрий Иванович Менделеев на это отреагировал следующей оценкой работы Ньюлендса: «В этих трудах видны некоторые зародыши периодического закона».
ТАК КТО ЖЕ ВСЕ-ТАКИ?
И все же у знаменитого русского естествоиспытателя К.А. Тимирязева мы читаем: «Едва ли не самым выдающимся шагом вперед собственно химии явилась возможность естественной классификации элементов в периодическую систему (Ньюлендс, Лотар Мейер и особенно Менделеев), дозволяющих рассматривать все свойства как функции их атомного веса».
Ключевыми для нас тут являются слова: «особенно Менделеев»…
А вот мнение Лотара Кольдица, известного немецкого химика, издателя учебников по химии и профессора Берлинского университета: «Никто из ученых, занимавшихся до Менделеева или одновременно с ним исследованиями соотношений между атомными весами и свойствами элементов, не смог сформулировать эту закономерность так ясно, как это сделал он. В частности, это относится к Ньюлендсу и Мейеру. Предсказание еще неизвестных элементов, их свойств и свойств их соединений является исключительно заслугой Д.И. Менделеева».
Тем не менее, чтобы не путаться во взаимных претензиях, в большинстве химических сообществ западного мира периодическая таблица не носит имени первооткрывателя, а словосочетание «таблица Менделеева» существует только в России.
Фото предоставлены
сайтом Wikipedia.org
Автор: Сергей НЕЧАЕВ
| ||||||
С днем рождения, Дубна! 23 июля в рамках мероприятий, посвященных 65-летнему юбилею ОИЯИ и города Дубны, состоится торжественное открытие панно “Периодическая таблица Д.И.Менделеева”. Ее площадь составляет более 284 кв. м, что делает ее самой большой в Европе. Таблица расположена на стене плавательного бассейна “Архимед” на набережной Волги и будет хорошо видна как жителям и гостям города, так и пассажирам многочисленных круизных теплоходов, проплывающих по реке. Таблица отражает выдающийся вклад ученых подмосковной Дубны в открытие новых химических элементов и призвана способствовать повышению интереса общества к достижениям современной науки.Об идее создания панно мы побеседовали с Юрием Цолаковичем Оганесяном – специалистом в области экспериментальной ядерной физики, академиком РАН, научным руководителем Лаборатории ядерных реакций имени Г. Юрий Цолакович, в день рождения нашего наукограда состоится знаковое событие – открытие в Дубне самой большой в мире таблицы Менделеева на фасаде бассейна “Архимед”. Да, это панно станет новой достопримечательностью нашего города. У Дубны славная история: когда построили канал, то здесь установили памятник Ленину работы великого скульптора С.Д.Меркурова, затем был снят кинофильм “Волга-Волга” с Любовью Орловой – часть съемок прошла на канале Москва-Волга и Московском море, а теперь на набережной будет столь знаменательный объект – панно “Периодическая таблица Менделеева”. Панно – не просто украшение, это, прежде всего, популяризация науки, своеобразный рассказ дубненцам и гостям города о достижениях ОИЯИ. Именно так. Достопримечательность всегда имеет много граней. На панно можно смотреть с архитектурной, документальной, познавательной, с глубоко научной точек зрения. Мы увидим, как Таблица будет меняться, какие элементы еще будут появляться и так далее. На ваш взгляд, наступит ли время, когда Периодическая таблица Менделеева заполнится и замкнется? Вообще, ядерной физике сто с небольшим лет. Говоря об элементах, следует вспомнить, что когда в марте 1869 года Менделеев отдал свой труд в печать, считалось, что элементы, сколько бы их ни было, являются кирпичиками мироздания, и мир построен из этих элементов. А у великого ученого Дальтона – 1808 год, когда было известно всего 36 элементов, – кирпичики соединяются в молекулы, далее в более сложные формы – кристаллы. Всего 36 элементов, как буквы алфавита. И этими буквами вы можете описать все, что угодно. Но когда Менделеев начал исследовать свойства этих элементов, их было уже 63, он заметил, что свойства этих элементов периодически повторяются. Однако такое поведение явно не согласуется с понятием “кирпичики мироздания”. Буквы в алфавите не должны быть похожи друг на друга! А если они похожи, подчиняясь какой-то закономерности, то это значит, что они сами имеют сложную структуру, которая, собственно, и дает эту периодичность… Менделеев понял, что рассматриваемый набор элементов это не кирпичики мироздания. Он стал искать эфир, в котором рождаются элементы, и был целиком поглощен поисками этих истоков материального мира. И теперь, как ни странно, 150 лет спустя, мы стали задаваться теми же вопросами: что такое таблица и как толкуется периодичность, что будет дальше, могут ли быть какие-то элементы более тяжелыми, можно ли считать ли элементы, которые созданы искусственно, настоящими? Если мы пойдем дальше, то сам закон будет видоизменяться, потому что, согласно теории относительности, если электроны будут двигаться вокруг этого ядра со скоростью близкой к скорости света, то станет расти их масса, и это должно быть учтено. По этой причине орбиты будут уплотняться, и тогда самая последняя орбита, где крутится тот самый электрон, который ответственен за химические свойства, изменит свои характеристики. Благодаря этим открытиям, весь научный мир еще раз убедился, что можно сделать то, что раньше казалось невозможным. Большой прогресс случится, когда начнут строить квантовые компьютеры, это уже мы говорим о технике, а вот как это будет выглядеть… Есть разные сценарии, они зависят от указанного взаимодействия и эффектов теории относительности. То есть процесс поиска новых элементов бесконечен… Таблица сама по себе неисчерпаема. Она продолжает жить в научном мире, будут добавляться элементы, открываться новые ее формы, строиться новые лаборатории по поиску элементов. Юрий Цолакович, любопытно, при каких обстоятельствах возникла сама идея? С чем связан выбор пространства для размещения панно? Подобные таблицы уже есть в мире, в Испании, например, она занимает площадь150 квадратных метров, наша будет больше! Я показал эту таблицу Виктору Анатольевичу Матвееву в 2017 году, тогда мы обсуждали возможность ее появления на заднем фасаде Дома культуры “Мир”. Я иногда гуляю по этому парку, сажусь на скамейку как раз напротив. Если говорить о деталях создания панно – как разрабатывался дизайн, почему он именно такой? Познавательный аспект превыше остального и главенствует в данном объекте? Если вы поищете таблицу Менделеева в интернете – там их огромное количество, по-моему, 1500 видов. Таблица имеет разные формы, из всех мы с Сергеем Николаевичем Дмитриевым выбрали ту, которая имеет научное содержание. Панно “Периодическая таблица имени Д.И.Менделеева” сделано не просто декоративно, но и содержательно с точки зрения науки. Наша Таблица будет очень хорошо смотреться ночью, с подсветкой. Кроме того, рядом слева есть свободное поле, на нем можно транслировать лекции, рассказывать об истории открытия элементов, об их химических свойствах, а на правой стороне демонстрировать различные элементы Таблицы. Юрий Цолакович, круг ваших научных интересов описан не в одной статье. А что помогает Вам отвлекаться от рабочего процесса, от науки. Может быть, театральное, музыкальное искусство? Все, о чем вы сейчас сказали, – это все духовное: и мышление, и творчество связаны с духовностью человека. Вы знаете, мне часто задают вопрос, на который сложно отвечать. Меня спрашивают о пользе открытия элементов. Это неосязаемое понимание, которое нельзя купить или продать, оно приходит как открытие, ты вдруг по-новому видишь мир. Насколько, на ваш взгляд, взаимосвязаны наука и культура? Одно без другого очень бедно, и, безусловно, они взаимосвязаны. Поэтому своим ученикам я говорю – оставьте ваши книги, забудьте о них на некоторое время, идите в театр, послушайте музыку, посмотрите, что делается вокруг. Это так важно, это расширяет горизонты. После соприкосновения с искусством ученые возвращаются к работе уже другими людьми? Именно так, я им говорю, что могу все простить, но не могу простить того, если они ничего не знают кроме своей области. Если посмотреть на ученых прошлого, они были многогранны. Тот же Менделеев – он не был членом Академии наук, а был членом Академии художеств! Он жил в квартире, выделенной петербургским университетом, и в ней по субботам принимал гостей, накрывая стол белой скатертью. А потом, когда они собирались расходиться, Дмитрий Иванович просил, чтобы они на этой скатерти расписались. А дальше его жена вышивала эти подписи – Репин, Мусоргский, кто только там не был. Это потрясающе. Он устраивал на Соловках раз в месяц семинары. И один из них был посвящен цвету. Приглашал физиков, химиков, артистов, художников, театральных деятелей, и каждый из них выступал на этом семинаре, рассказывал, что он понимает под словом “цвет”. Физик говорит, что это излучение, химик, что это смешение таких-то компонентов, художник рассуждал, как красный цвет напоминает ему кровь и он не может спокойно смотреть на красные полотнища. И это все интересно людям. Беседовала Элеонора ЯМАЛЕЕВА, | ||||||
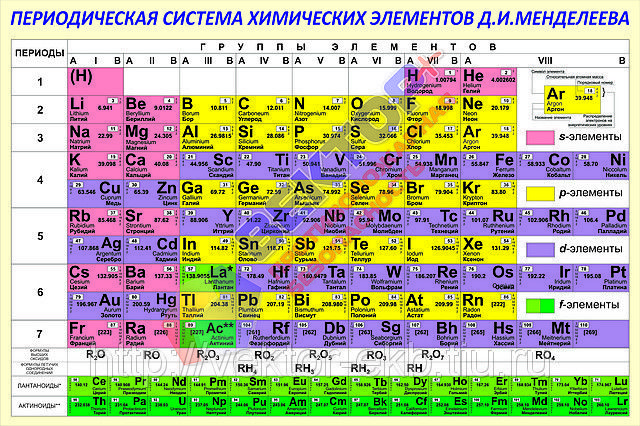
Таблица Менделеева. Периодическая система химических элементов Д.И.Менделеева, химические элементы
| H | 1 | 1 |
| 1.00794±7 | ||
| 1s1 | ||
| Водород | ||
| He | 2 | 2 |
4. 002602±2 002602±2 | ||
| 1s2 | ||
| Гелий | ||
| Li | 3 | 1 2 |
| 6.941±2 | ||
| 2s1 | ||
| Литий | ||
| Be | 4 | 2 2 |
| 9.01218±1 | ||
| 2s2 | ||
| Бериллий | ||
| B | 5 | 3 2 |
10. 811±5 811±5 | ||
| 2s22p1 | ||
| Бор | ||
| C | 6 | 4 2 |
| 12.011±1 | ||
| 2s22p2 | ||
| Углерод | ||
| N | 7 | 5 2 |
| 14.0067±1 | ||
| 2s22p3 | ||
| Азот | ||
| O | 8 | 6 2 |
15. 9994±3 9994±3 | ||
| 2s22p4 | ||
| Кислород | ||
| F | 9 | 7 2 |
| 18.998403±1 | ||
| 2s22p5 | ||
| Фтор | ||
| Ne | 10 | 8 2 |
| 20.179±1 | ||
| 2s22p6 | ||
| Неон | ||
| Na | 11 | 1 8 2 |
22. 98977±1 98977±1 | ||
| 3s1 | ||
| Натрий | ||
| Mg | 12 | 2 8 2 |
| 24.305±1 | ||
| 3s2 | ||
| Магний | ||
| Al | 13 | 3 8 2 |
| 26.98154±1 | ||
| 3s23p1 | ||
| Алюминий | ||
| Si | 14 | 4 8 2 |
28. 0855±3 0855±3 | ||
| 3s23p2 | ||
| Кремний | ||
| P | 15 | 5 8 2 |
| 30.97376±1 | ||
| 3s23p3 | ||
| Фосфор | ||
| S | 16 | 6 8 2 |
| 32.066±6 | ||
| 3s23p4 | ||
| Сера | ||
| Cl | 17 | 7 8 2 |
35. 453±1 453±1 | ||
| 3s23p5 | ||
| Хлор | ||
| Ar | 18 | 8 8 2 |
| 39.948±1 | ||
| 3s23p6 | ||
| Аргон | ||
| K | 19 | 1 8 8 2 |
| 39.0983±1 | ||
| 4s1 | ||
| Калий | ||
| Ca | 20 | 2 8 8 2 |
40. 078±4 078±4 | ||
| 4s2 | ||
| Кальций | ||
| 2 9 8 2 | 21 | Sc |
| 44.95591±1 | ||
| 3d14s2 | ||
| Скандий | ||
| 2 10 8 2 | 22 | Ti |
47. 88±3 88±3 | ||
| 3d24s2 | ||
| Титан | ||
| 2 11 8 2 | 23 | V |
| 50.9415±1 | ||
| 3d34s2 | ||
| Ванадий | ||
| 1 13 8 2 | 24 | Cr |
51. 9961±6 9961±6 | ||
| 3d54s1 | ||
| Хром | ||
| 2 13 8 2 | 25 | Mn |
| 54.9380±1 | ||
| 3d54s2 | ||
| Марганец | ||
| 2 14 8 2 | 26 | Fe |
55. 847±3 847±3 | ||
| 3d64s2 | ||
| Железо | ||
| 2 15 8 2 | 27 | Co |
| 58.9332±1 | ||
| 3d74s2 | ||
| Кобальт | ||
| 2 16 8 2 | 28 | Ni |
58. 69±1 69±1 | ||
| 3d84s2 | ||
| Никель | ||
| 1 18 8 2 | 29 | Cu |
| 63.546±3 | ||
| 3d104s1 | ||
| Медь | ||
| 2 18 8 2 | 30 | Zn |
65. 39±2 39±2 | ||
| 3d104s2 | ||
| Цинк | ||
| Ga | 31 | 3 18 8 2 |
| 69.723±4 | ||
| 4s24p1 | ||
| Галлий | ||
| Ge | 32 | 4 18 8 2 |
72. 59±3 59±3 | ||
| 4s24p2 | ||
| Германий | ||
| As | 33 | 5 18 8 2 |
| 74.9216±1 | ||
| 4s24p3 | ||
| Мышьяк | ||
| Se | 34 | 6 18 8 2 |
| 78.96±3 | ||
| 4s24p4 | ||
| Селен | ||
| Br | 35 | 7 18 8 2 |
79. 904±1 904±1 | ||
| 4s24p5 | ||
| Бром | ||
| Kr | 36 | 8 18 8 2 |
| 83.80±1 | ||
| 4s24p6 | ||
| Криптон | ||
| Rb | 37 | 1 8 18 8 2 |
| 85.4678±3 | ||
| 5s1 | ||
| Рубидий | ||
| Sr | 38 | 2 8 18 8 2 |
| 87,62±1 | ||
| 5s2 | ||
| Стронций | ||
| 2 9 18 8 2 | 39 | Y |
88. 9059±1 9059±1 | ||
| 4d15s2 | ||
| Иттрий | ||
| 2 10 18 8 2 | 40 | Zr |
| 91.224±2 | ||
| 4d25s2 | ||
| Цирконий | ||
| 1 12 18 8 2 | 41 | Nb |
92. 9064±1 9064±1 | ||
| 4d45s1 | ||
| Ниобий | ||
| 1 13 18 8 2 | 42 | Mo |
| 95.94±1 | ||
| 4d55s1 | ||
| Молибден | ||
| 2 13 18 8 2 | 43 | Tc |
97. 9072 9072 | ||
| 4d55s2 | ||
| Технеций | ||
| 1 15 18 8 2 | 44 | Ru |
| 101.07±2 | ||
| 4d75s1 | ||
| Рутений | ||
| 1 16 18 8 2 | 45 | Rh |
102. 9055±1 9055±1 | ||
| 4d85s1 | ||
| Родий | ||
| 0 18 18 8 2 | 46 | Pd |
| 106.42±1 | ||
| 4d105s0 | ||
| Палладий | ||
| 1 18 18 8 2 | 47 | Ag |
107. 8682±3 8682±3 | ||
| 4d105s1 | ||
| Серебро | ||
| 2 18 18 8 2 | 48 | Cd |
| 112.41±1 | ||
| 4d105s2 | ||
| Кадмий | ||
| In | 49 | 3 18 18 8 2 |
114.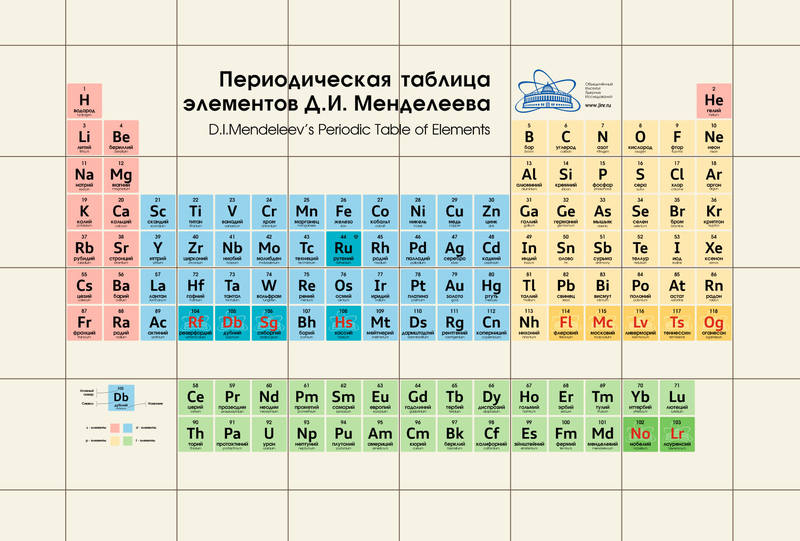 82±1 82±1 | ||
| 5s25p1 | ||
| Индий | ||
| Sn | 50 | 4 18 18 8 2 |
| 118.710±7 | ||
| 5s25p2 | ||
| Олово | ||
| Sb | 51 | 5 18 18 8 2 |
| 121.75±3 | ||
| 5s25p3 | ||
| Сурьма | ||
| Te | 52 | 6 18 18 8 2 |
127. 60±3 60±3 | ||
| 5s25p4 | ||
| Теллур | ||
| I | 53 | 7 18 18 8 2 |
| 126.9045±1 | ||
| 5s25p5 | ||
| Иод | ||
| Xe | 54 | 8 18 18 8 2 |
| 131.29±3 | ||
| 5s25p6 | ||
| Ксенон | ||
| Cs | 55 | 1 8 18 18 8 2 |
132. 9054±1 9054±1 | ||
| 6s1 | ||
| Цезий | ||
| Ba | 56 | 2 8 18 18 8 2 |
| 137.33±1 | ||
| 6s2 | ||
| Барий | ||
| 2 9 18 18 8 2 | 57 | La* |
138. 9055±3 9055±3 | ||
| 5d16s2 | ||
| Лантан | ||
| 2 10 32 18 8 2 | 72 | Hf |
| 178.49±3 | ||
| 5d26s2 | ||
| Гафний | ||
| 2 11 32 18 8 2 | 73 | Ta |
180. 9479±1 9479±1 | ||
| 5d36s2 | ||
| Тантал | ||
| 2 12 32 18 8 2 | 74 | W |
| 183.85±3 | ||
| 5d46s2 | ||
| Вольфрам | ||
| 2 13 32 18 8 2 | 75 | Re |
186. 207±1 207±1 | ||
| 5d56s2 | ||
| Рений | ||
| 2 14 32 18 8 2 | 76 | Os |
| 190.2±1 | ||
| 5d66s2 | ||
| Осмий | ||
| 2 15 32 18 8 2 | 77 | Ir |
192. 22±3 22±3 | ||
| 5d76s2 | ||
| Иридий | ||
| 1 17 32 18 8 2 | 78 | Pt |
| 195.08±3 | ||
| 5d96s1 | ||
| Платина | ||
| 1 18 32 18 8 2 | 79 | Au |
196. 9665±1 9665±1 | ||
| 5d106s1 | ||
| Золото | ||
| 2 18 32 18 8 2 | 80 | Hg |
| 200.59±3 | ||
| 5d106s2 | ||
| Ртуть | ||
| Tl | 81 | 3 18 32 18 18 8 2 |
204.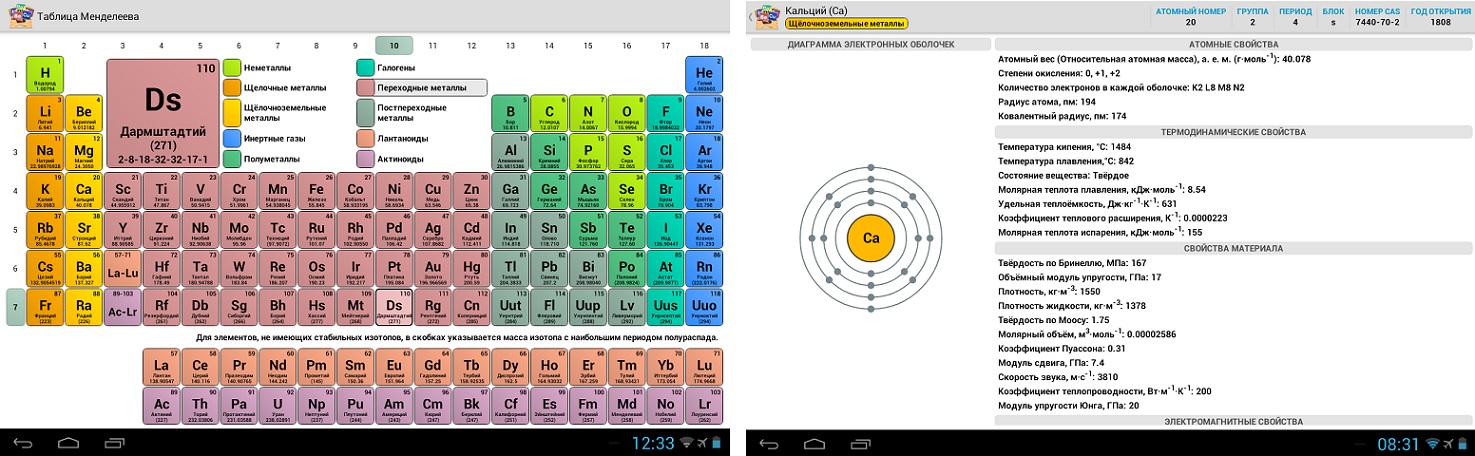 383±1 383±1 | ||
| 6s26p1 | ||
| Таллий | ||
| Pb | 82 | 4 18 32 18 18 8 2 |
| 207.2±1 | ||
| 6s26p2 | ||
| Свинец | ||
| Bi | 83 | 5 18 32 18 18 8 2 |
208.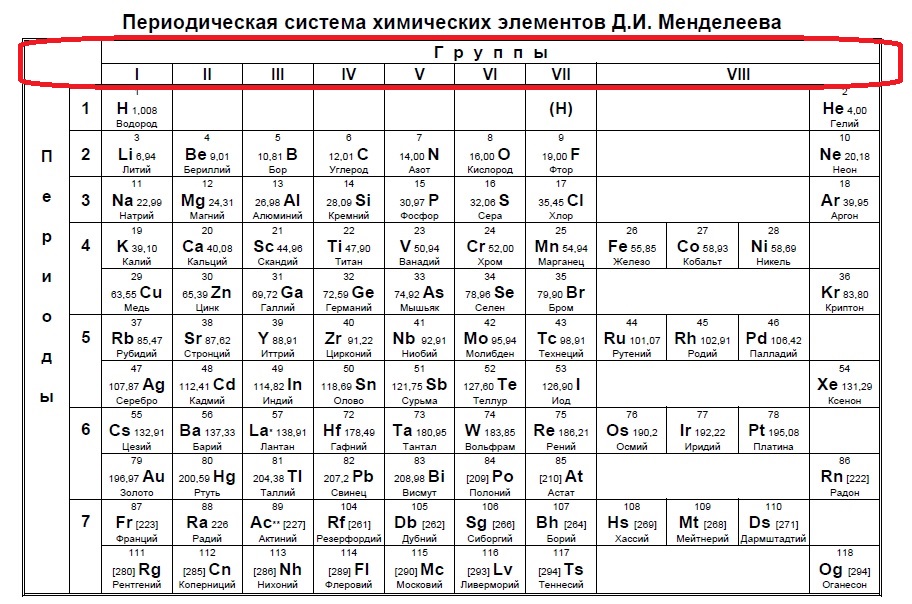 9804±1 9804±1 | ||
| 6s26p3 | ||
| Висмут | ||
| Po | 84 | 6 18 32 18 18 8 2 |
| 208.9824 | ||
| 6s26p4 | ||
| Полоний | ||
| At | 85 | 7 18 32 18 18 8 2 |
209. 9871 9871 | ||
| 6s26p5 | ||
| Астат | ||
| Rn | 86 | 8 18 32 18 18 8 2 |
| 222.0176 | ||
| 6s26p6 | ||
| Радон | ||
| Fr | 87 | 1 8 18 32 18 18 8 2 |
223. 0197 0197 | ||
| 7s1 | ||
| Франций | ||
| Ra | 88 | 2 8 18 32 18 18 8 2 |
| 226.0254 | ||
| 7s2 | ||
| Радий | ||
| 2 8 18 32 18 8 2 | 89 | Ac** |
227. 0278 0278 | ||
| 6d17s2 | ||
| Актиний | ||
| 2 10 32 32 18 8 2 | 104 | Rf |
| [261] | ||
| 6d27s2 | ||
| Резерфордий | ||
| 2 11 32 32 18 8 2 | 105 | Db |
| [262] | ||
| 6d37s2 | ||
| Дубний | ||
| 2 12 32 32 18 8 2 | 106 | Sg |
| [263] | ||
| 6d47s2 | ||
| Сиборгий | ||
| 2 13 32 32 18 8 2 | 107 | Bh |
| [262] | ||
| 6d57s2 | ||
| Борий | ||
| 2 14 32 32 18 8 2 | 108 | Hs |
| [265] | ||
| 6d67s2 | ||
| Хассий | ||
| 2 15 32 32 18 8 2 | 109 | Mt |
| [266] | ||
| 6d77s2 | ||
| Мейтнерий | ||
| 1 17 32 32 18 8 2 | 110 | Ds |
| (281) | ||
| 5f146d97s1 | ||
| Дармштадтий | ||
| 1 18 32 32 18 8 2 | 111 | Rg |
| (281) | ||
| 5f146d107s1 | ||
| Рентгений | ||
| 112 | Cn | |
| 285 | ||
| 5f146d107s2 | ||
| Коперниций | ||
| Nh | 113 | |
| (286) | ||
| 5f146d107s27p1 | ||
| Нихоний | ||
| Fl | 114 | |
| 289 | ||
| 5f146d107s27p2 | ||
| Флеровий | ||
| Mc | 115 | |
| 289 | ||
| 5f146d107s27p3 | ||
| Московий | ||
| Lv | 116 | 6 18 32 32 18 8 2 |
| 293 | ||
| 5f146d107s27p4 | ||
| Ливерморий | ||
| Ts | 117 | 2 8 18 32 32 18 7 |
| [294] | ||
| 5f146d107s27p5 | ||
| Теннессин | ||
| Og | 118 | |
| [294] | ||
| 5f146d107s27p6 | ||
| Оганесон | ||
Высшие оксиды
Летучие водородные соединения
Лантаноиды
| Ce | 58 | 2 9 19 18 8 2 |
140.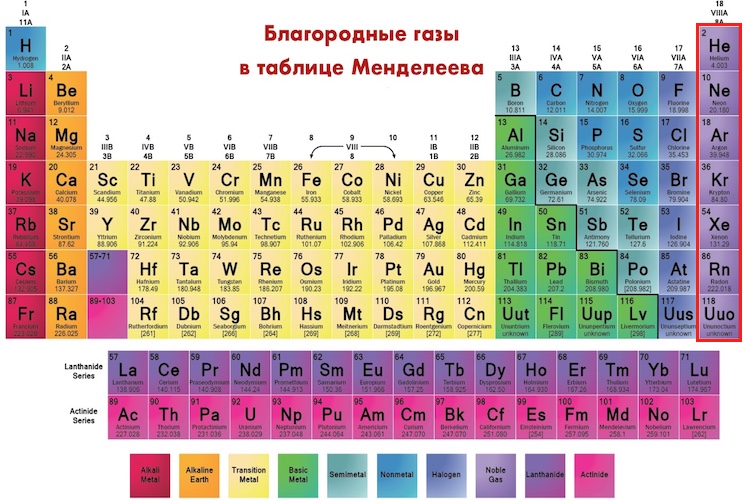 12±1 12±1 | ||
| 4f15d16s2 | ||
| Церий | ||
| Pr | 59 | 2 8 21 18 8 2 |
| 140.9077±1 | ||
| 4f36s2 | ||
| Празеодим | ||
| Nd | 60 | 2 8 22 18 8 2 |
144. 24±3 24±3 | ||
| 4f46s2 | ||
| Неодим | ||
| Pm | 61 | 2 8 23 18 8 2 |
| 144.9128 | ||
| 4f56s2 | ||
| Прометий | ||
| Sm | 62 | 2 8 24 18 8 2 |
150. 36±3 36±3 | ||
| 4f66s2 | ||
| Самарий | ||
| Eu | 63 | 2 8 25 18 8 2 |
| 151.96±1 | ||
| 4f76s2 | ||
| Европий | ||
| Gd | 64 | 2 9 25 18 8 2 |
157. 25±3 25±3 | ||
| 4f75d16s2 | ||
| Гадолиний | ||
| Tb | 65 | 2 8 27 18 8 2 |
| 159.9254±1 | ||
| 4f96s2 | ||
| Тербий | ||
| Dy | 66 | 2 8 28 18 8 2 |
162. 50±3 50±3 | ||
| 4f106s2 | ||
| Диспрозий | ||
| Ho | 67 | 2 8 29 18 8 2 |
| 164.9304±1 | ||
| 4f116s2 | ||
| Гольмий | ||
| Er | 68 | 2 8 30 18 8 2 |
167. 26±3 26±3 | ||
| 4f126s2 | ||
| Эрбий | ||
| Tm | 69 | 2 8 31 18 8 2 |
| 168.9342±1 | ||
| 4f136s2 | ||
| Тулий | ||
| Yb | 70 | 2 8 32 18 8 2 |
173. 04±3 04±3 | ||
| 4f146s2 | ||
| Иттербий | ||
| Lu | 71 | 2 9 32 18 8 2 |
| 174.967±1 | ||
| 4f145d16s2 | ||
| Лютеций | ||
Актиноиды
| Th | 90 | 2 10 18 32 18 8 2 |
232. 0381±1 0381±1 | ||
| 6d27s2 | ||
| Торий | ||
| Pa | 91 | 2 9 20 32 18 8 2 |
| 231.0359 | ||
| 5f26d17s2 | ||
| Протактиний | ||
| U | 92 | 2 9 21 32 18 8 2 |
238. 0289±1 0289±1 | ||
| 5f36d17s2 | ||
| Уран | ||
| Np | 93 | 2 9 22 32 18 8 2 |
| 237.0482 | ||
| 5f46d17s2 | ||
| Нептуний | ||
| Pu | 94 | 2 8 24 32 18 8 2 |
244. 0642 0642 | ||
| 5f67s2 | ||
| Плутоний | ||
| Am | 95 | 2 8 25 32 18 8 2 |
| 243.0614 | ||
| 5f77s2 | ||
| Амерций | ||
| Cm | 96 | 2 9 25 32 18 8 2 |
247. 0703 0703 | ||
| 5f7d617s2 | ||
| Кюрий | ||
| Bk | 97 | 2 9 26 32 18 8 2 |
| 247.0703 | ||
| 5f8d617s2 | ||
| Берклий | ||
| Cf | 98 | 2 8 28 32 18 8 2 |
251. 0796 0796 | ||
| 5f107s2 | ||
| Калифорний | ||
| Es | 99 | 2 8 29 32 18 8 2 |
| 252.0828 | ||
| 5f117s2 | ||
| Эйнштейний | ||
| Fm | 100 | 2 8 30 32 18 8 2 |
257. 0951 0951 | ||
| 5f127s2 | ||
| Фермий | ||
| Md | 101 | 2 8 31 32 18 8 2 |
| 258.0986 | ||
| 5f137s2 | ||
| Менделевий | ||
| No | 102 | 2 8 32 32 18 8 2 |
259. 1009 1009 | ||
| 5f147s2 | ||
| Нобелий | ||
| Lr | 103 | 2 9 32 32 18 8 2 |
| 260.1054 | ||
| 5f146d17s2 | ||
| Лоуренсий | ||
236
проверенных автора готовы помочь в написании работы любой сложности
Мы помогли уже 4 396 ученикам и студентам сдать работы от решения задач до дипломных на отлично! Узнай стоимость своей работы за 15 минут!
Полтора века — от таблицы Менделеева к Периодической системе
Наука и жизньНаука
Кандидат химических наук Аркадий Курамшин, Казанский федеральный университет.
Сейчас, спустя сто пятьдесят лет после формулировки Д. И. Менделеевым Периодического закона мы можем назвать его графическое изображение — Периодическую систему химических элементов одним из наиболее мощных «артефактов» не только химии, но и всей науки в целом. В таблице, которую можно найти на стене в каждой химической лаборатории или аудитории, всего 118 заполненных ячеек и в то же время это концентрат большей части наших знаний о химии. Никакой другой раздел естественных наук не может похвастаться столь высоким содержанием знаний в одном небольшом документе.
Естественно, таблицы в современных аудиториях не всегда выглядели так, как сейчас. За полтора столетия, прошедших от первых набросков периодической системы, сделанных Менделеевым, до дня сегодняшнего (особенно за первые полвека существования Периодического закона), таблица значительно изменилась. Более того, до сих пор появляются предложения улучшить её, сделать более удобной. Большая часть изменений была внесена в периодическую систему уже после смерти Д. И. Менделеева, когда наконец стали понятны причины выполнения Периодического закона. Возможно, зайди Дмитрий Иванович сейчас в школьный кабинет химии, ему бы не сразу удалось узнать своё детище. Скорее всего, именно поэтому профессиональные химики редко используют термин «Таблица Менделеева», предпочитая термин «периодическая система». Давайте посмотрим, как за эти полтора века менялась основная «икона» химии и как её предлагают изменить.
И. Менделеева, когда наконец стали понятны причины выполнения Периодического закона. Возможно, зайди Дмитрий Иванович сейчас в школьный кабинет химии, ему бы не сразу удалось узнать своё детище. Скорее всего, именно поэтому профессиональные химики редко используют термин «Таблица Менделеева», предпочитая термин «периодическая система». Давайте посмотрим, как за эти полтора века менялась основная «икона» химии и как её предлагают изменить.
Первая таблица Менделеева
Разработка принципов классификации химических элементов, открытие Периодического закона и в конечном счёте создание периодической системы вряд ли можно назвать внезапным озарением одного-единственного человека — скорее это закономерная кульминация химической мысли второй половины XIX века. Мы знаем, когда открытие было сделано. Днём рождения прообраза современной периодической системы, первой таблицы Менделеева, считается 17 февраля (1 марта) 1869 года. Этим днём датируется первая рукописная менделеевская таблица, озаглавленная «Опыт системы элементов, основанной на их атомном весе и химическом сходстве».
Через пару недель, 6 марта (18 марта) 1869 года, на заседании Русского химического общества председатель общества Николай Александрович Меншуткин зачитывает менделеевское сообщение о «Соотношении свойств с атомным весом элементов». Вскоре после этого статья Менделеева с соответствующим названием выходит в журнале общества. В том же издании 29 ноября (11 декабря) 1870 года Д. И. Менделеев публикует статью «Естественная система элементов и применение её к указанию свойств неоткрытых элементов», которая, пожалуй, оказывается самой важной публикацией определения приоритета Дмитрия Ивановича как автора Периодического закона. Во-первых, в этой статье Менделеев впервые вводит термин «Периодический закон», а во-вторых, использует этот закон для предсказания существования атомных масс, а также физических и химических свойств нескольких ещё не открытых химических элементов. Как показали последовавшие десять лет, именно предсказания свойств и оказались самой важной находкой Дмитрия Ивановича — периодическую повторяемость свойств химических элементов через определённый интервал в 1860-е годы химики наблюдали и до Менделеева.
В 1862 году такую периодичность отметил французский химик и геолог Александр-Эмиль Бегье де Шанкуртуа. Он представил систему элементов в виде спиральной линии, образованной элементами в порядке увеличения их атомной массы на поверхности цилиндра. Элементы «спирали де Шанкуртуа», совпадавшие по вертикали, обладали близкими свойствами (например, кислород и сера), подобная близость свойств элементов, находящихся в одной группе (также по вертикали), стала визитной карточкой менделеевской системы. Однако работы де Шанкуртуа не произвели впечатления на его современников: система была сложной, для публикации в журнале спиралевидную диаграмму с трудом удалось изобразить в плоскости, так что близость химических свойств элементов оказалась далеко не очевидной.
В 1864 году английский химик и музыкант Джон Ньюлендс также расставил элементы в порядке увеличения атомных весов, обнаружив при этом, что свойства химических элементов повторяются через каждые семь элементов, как и сходные ноты чередуются в октаве через каждые семь нот.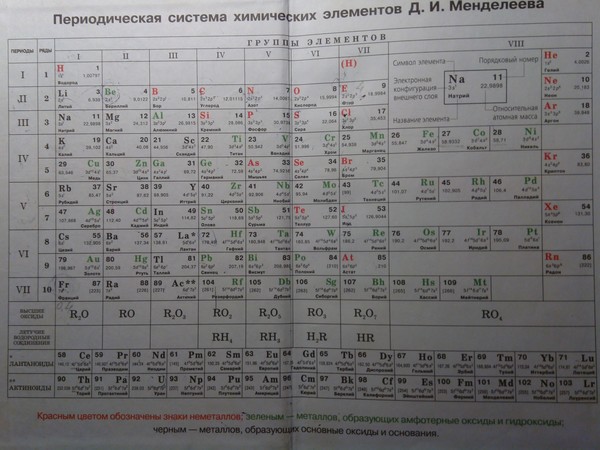 Считая, что основы гармонии мира едины и в музыке и в химии, Ньюлендс назвал обнаруженную закономерность «законом октав». Сначала он составил таблицу, очень похожую на менделеевскую, в том числе и с пустыми клетками на месте ещё не открытых элементов, однако сам же испугался этих пустот и в 1866 году, представляя своё открытие Лондонскому химическому обществу, показал таблицу без «белых пятен». Гармония рухнула — по закону октав оказывались сходными углерод и ртуть, и британский химик, первый ректор Университетского колледжа Лондона Джордж Кэри Фостер язвительно поинтересовался у Ньюлендса, не пробовал ли тот найти закономерности в свойствах элементов, просто расставив их по алфавиту. После обсуждения журнал Лондонского химического общества отказался публиковать «закон октав», и Ньюлендс сменил направление исследований.
Считая, что основы гармонии мира едины и в музыке и в химии, Ньюлендс назвал обнаруженную закономерность «законом октав». Сначала он составил таблицу, очень похожую на менделеевскую, в том числе и с пустыми клетками на месте ещё не открытых элементов, однако сам же испугался этих пустот и в 1866 году, представляя своё открытие Лондонскому химическому обществу, показал таблицу без «белых пятен». Гармония рухнула — по закону октав оказывались сходными углерод и ртуть, и британский химик, первый ректор Университетского колледжа Лондона Джордж Кэри Фостер язвительно поинтересовался у Ньюлендса, не пробовал ли тот найти закономерности в свойствах элементов, просто расставив их по алфавиту. После обсуждения журнал Лондонского химического общества отказался публиковать «закон октав», и Ньюлендс сменил направление исследований.
Нельзя сказать, что к выводам Дмитрия Ивановича первоначально отнеслись более доброжелательно. Выслушав доклад, сделанный Меншуткиным от имени Менделеева, президент Русского химического общества Николай Николаевич Зинин посоветовал Менделееву «заняться делом, достойным настоящего исследователя», хотя через пару лет и изменил своё мнение: «Очень, очень хорошо, премного отличных сближений, даже весело читать, дай Бог Вам удачи в опытном подтверждении Ваших выводов». Профессор Лейпцигского университета Герман Кольбе в 1870 году назвал открытие Менделеева «спекулятивным», а Роберт Бунзен говорил, что Менделеев увлекает химиков «в надуманный мир чистых абстракций».
Профессор Лейпцигского университета Герман Кольбе в 1870 году назвал открытие Менделеева «спекулятивным», а Роберт Бунзен говорил, что Менделеев увлекает химиков «в надуманный мир чистых абстракций».
Однако Менделеев был уверен в правоте своего Периодического закона, и последовавшее скоро подтверждение его предсказаний убедило в этом и коллег. И если первое сообщение о Периодическом законе Менделеева сделано в марте 1869 года, днём его рождения как фундаментального химического закона, скорее, стоит считать 1875 год. В этот год произошла первая верификация закона — французский учёный Лекок де Буабодран открыл элемент, которому дал название «галлий», и определённые экспериментальным путём свойства галлия оказались близки предсказанным свойствам менделеевского экаалюминия.
Последовавшие в 1879 году открытия скандия (экабора) и в 1886 году германия (экакремния) показали, что свойства галлия и экабора совпали не случайно, а значит, менделеевский закон действительно фундаментальный, а не какая-то удачная форма классификации элементов и не «надуманный мир чистых абстракций».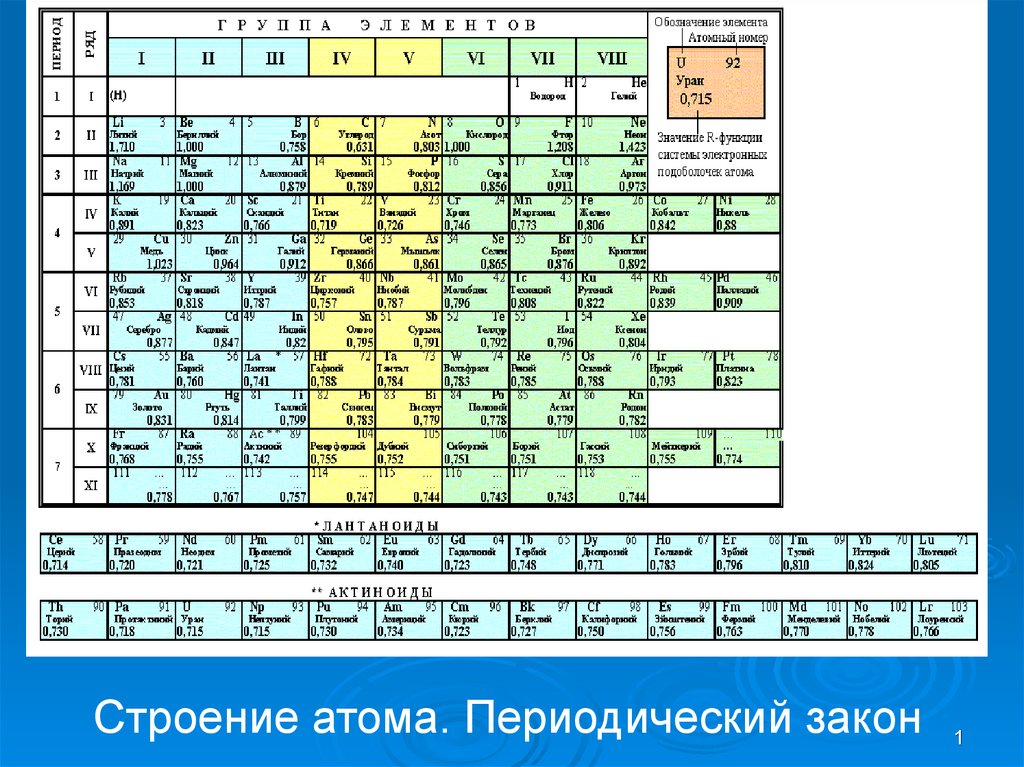
В 1882 году Лондонское королевское общество присудило Менделееву и главному его конкуренту в приоритете открытия периодической системы Лотару Мейеру высшие награды — золотые медали Дэви — «За открытие периодических соотношений атомных весов». Ученик Бунзена Лотар Мейер, независимо от Менделеева, в 1870 году предложил практически аналогичную менделеевской таблицу, систематизирующую химические элементы. Мейер, в отличие от Ньюлендса, не побоялся оставить в своей таблице пустые ячейки для ещё неизвестных химических элементов, но, в отличие от Менделеева, не пытался предсказать их свойства. После открытия германия в 1886 году и Ньюлендс и Мейер всё реже упоминаются в связи с созданием и Периодического закона, и его графического отображения — периодической системы, а типографии Европы признали первенство Дмитрия Ивановича и начали печатать учебные пособия под названием «Таблица Менделеева», даже не дожидаясь открытия германия.
Последняя таблица Менделеева
Если 1880-е годы стали триумфом предсказательной способности Периодического закона, то 1890-е — первой (правда, на настоящий момент и последней) проверкой закона на прочность.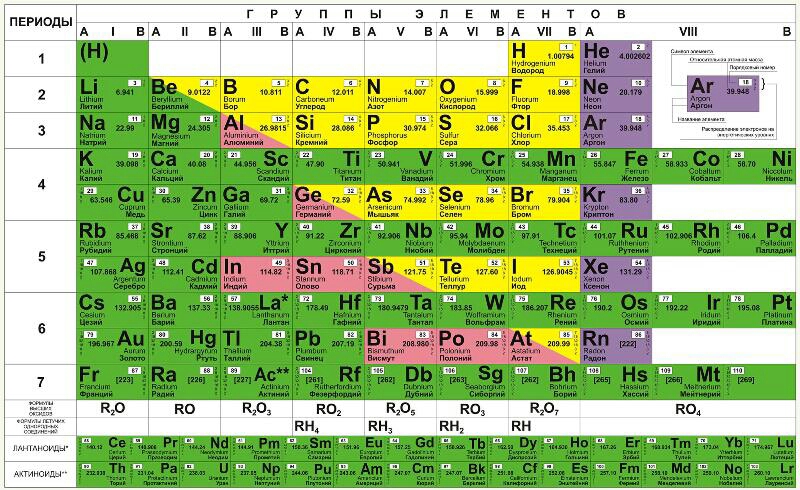 В 1894 году Джон Стретт, лорд Рэлей и Уильям Рамзай сделали открытие, угрожавшее предложенному Менделеевым строгому порядку периодической системы: они открыли аргон, новый газ, которому не было места в периодической системе. Химикам не удавалось заставить реагировать аргон с чем-либо, этот газ оставался полностью инертным, и Менделеев первоначально предположил, что аргон не химический элемент, а чрезвычайно устойчивое соединение, образованное в результате комбинации уже известных элементов.
В 1894 году Джон Стретт, лорд Рэлей и Уильям Рамзай сделали открытие, угрожавшее предложенному Менделеевым строгому порядку периодической системы: они открыли аргон, новый газ, которому не было места в периодической системе. Химикам не удавалось заставить реагировать аргон с чем-либо, этот газ оставался полностью инертным, и Менделеев первоначально предположил, что аргон не химический элемент, а чрезвычайно устойчивое соединение, образованное в результате комбинации уже известных элементов.
Лингвистический и культурологический взгляд на таблицу Менделеева
О таблице Менделеева слышал каждый, кто доучился до старших классов. А тот, кто связал жизнь с химией, – не расстаётся с ней ни на день. А я вот решил вам рассказать, как видят периодическую таблицу не химики и физики, а лингвисты и лирики. Ведь таблица Менделеева – это «словарь» всей материи во Вселенной. Это живая латынь и дополнительные 118 слов языка. Стихи и каламбуры…
Ну, приступим.
Вечно живой мёртвый язык
Латынь называют мёртвым языком, но учёными всего мира она используется постоянно и постепенно пополняется словами из русского, немецкого, английского…
Всё дело в том, что выражение «мёртвый язык» означает лишь то, что дети не учат этот язык с младенчества в качестве родного. Вот так и получается, что живые языки пополняют мёртвые.
Вот так и получается, что живые языки пополняют мёртвые.
Элементы таблицы Менделеева даются на латыни, и когда открывались новые элементы, их нарекали на языках того времени, в честь учёных, городов и стран той эпохи.
Так что не только латынь влияет на современные языки, но и наоборот.
Например, названия химических элементов флеровий, московий, дубний, оганесон пришли в латынь из России. Есть ещё Менделевий. Кстати, о Менделееве.
Менделеев
Не во всех странах таблицу называют именно «Таблицей Менделеева». Имя пусть не первого пытавшегося, но всё же автора, наконец подарившего миру таблицу, конечно, не скрывается, но скромно умалчивается. Как и портрет Дмитрия Ивановича на таблице за пределами России встретишь редко.
«Золото, оно и в Африке золото», или Польза от таблицы Менделеева для изучения языков
100 с лишним элементов имеют названия, и похожие в разных языках, и нет.
Пусть у некоторых названий элементов в некоторых языках есть разные значения (в английском –Lead можно прочитать как «свинец», а можно как «вести», iron – «железо», и «утюг», и «гладить»).
Но главное, «химическое» значение остаётся прежним. Поэтому элементы периодической таблицы – это дополнительная сотня к вашему лексикону изучаемого языка!
На японской таблице Менделеева названия «давно известных» металлов и прочих элементов обозначены иероглифами, а новые, открытые учёными и названные в честь их имён, городов и стран – на катакане (японской слоговой азбукой, в основном для заимствованных слов).
В китайской же – все элементы имеют иероглифическое обозначение.
Золото по-литовски Auksas, поэтому обозначение Au смотрится как родное.
В русском языке формула воды «аш два о» звучит как «аж два о», то есть кого-то удивляет наличие двух О, хотя на самом деле кислород-то (О) как раз один, а два атома (Н) водорода. CuSO4 для простоты запоминания читают как «кусоч».
Песня
Про химические элементы сочиняют стихи и песни, но самой известной из них была и остаётся песня Тома Лерера « Элементы». То она влетит в топы интернет-мемов, то её вдруг исполнит молодой актёр, Дэниэл Рэдклифф, например.
То она влетит в топы интернет-мемов, то её вдруг исполнит молодой актёр, Дэниэл Рэдклифф, например.
https://www.youtube.com/watch?v=rSAaiYKF0c
There’s antimony, arsenic, aluminum, selenium,
And hydrogen and oxygen and nitrogen and rhenium,
And nickel, neodymium, neptunium, germanium,
And iron, americium, ruthenium, uranium,
Europium, zirconium, lutetium, vanadium,
And lanthanum and osmium and astatine and radium,
And gold and protactinium and indium and gallium,
And iodine and thorium and thulium and thallium.
There’s yttrium, ytterbium, actinium, rubidium,
And boron, gadolinium, niobium, iridium,
And strontium and silicon and silver and samarium,
And bismuth, bromine, lithium, beryllium, and barium.
There’s holmium and helium and hafnium and erbium,
And phosphorus and francium and fluorine and terbium,
And manganese and mercury, molybdenum, magnesium,
Dysprosium and scandium and cerium and cesium.
And lead, praseodymium, and platinum, plutonium,
Palladium, promethium, potassium, polonium,
And tantalum, technetium, titanium, tellurium,
And cadmium and calcium and chromium and curium.
There’s sulfur, californium, and fermium, berkelium,
And also mendelevium, einsteinium, nobelium,
And argon, krypton, neon, radon, xenon, zinc, and rhodium,
And chlorine, carbon, cobalt, copper, tungsten, tin, and sodium.
These are the only ones of which the news has come to Ha’vard,
And there may be many others, but they haven’t been discavard.
Перевод
Есть место Мышьяку, Сурьме, Селену, Алюминию
И Водороду, Кислороду, Углероду, Рению,
И Неодиму, Никелю, Нептунию, Германию,
Железу, Америцию, Рутению, Уранию
Европию, Цирконию, Лютецию, Ванадию,
Лантану вместе с Осмием, Астату вместе с Радием,
Золоту, Протактинию и Индию и Галлию,
И Йоду вместе с Торием, и Тулию и Таллию.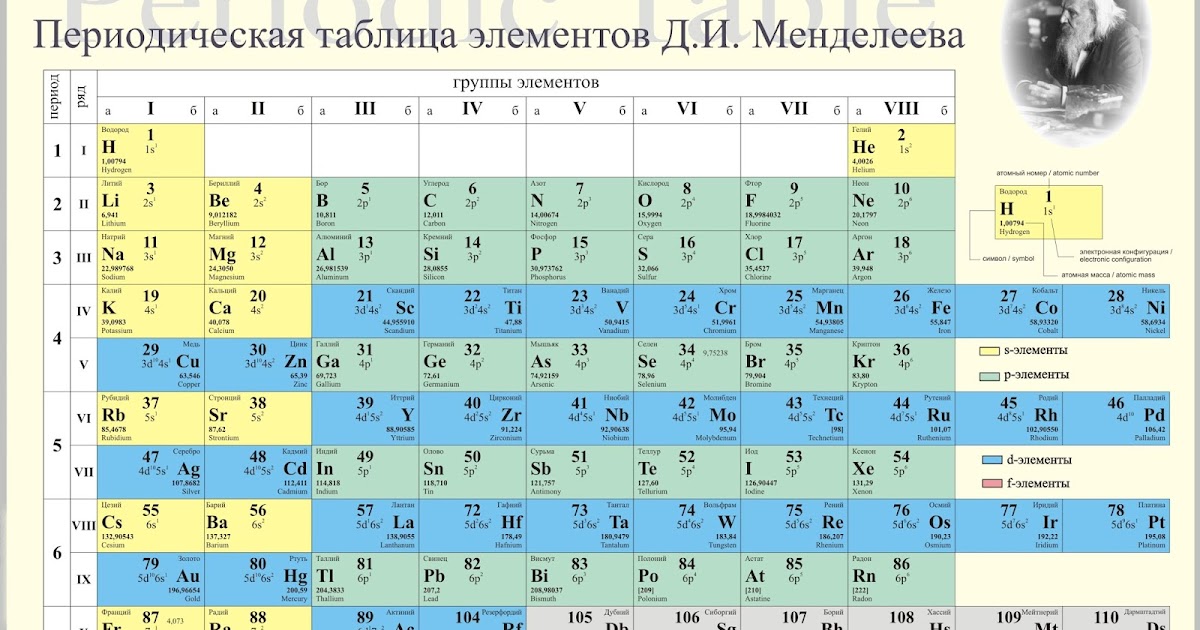
И Иттрию, Иттербию, Актинию, Рубидию,
И Бору, Гадолинию, Ниобию, Иридию,
И Стронцию и Кремнию, Серебру и Самарию,
И Висмуту и Брому, Литию, Бериллию и Барию.
И Гольмию, и Гелию, и Гафнию, и Эрбию,
И Фосфору, и Францию, и Фтору вместе с Тербием,
И Ртути с Молибденом, также Марганцу, и Магнию,
Диспрозию, и Церию, и Цезию, и Скандию.
Свинцу, Празеодимию, и Платине, Плутонию,
Палладию, Прометию и Калию, Полонию,
И Танталу, и Теллуру, Технецию и Кадмию,
Титану, Хрому, Кюрию и непременно Кальцию
И Сере, Калифорнию, и Фермию, и Берклию,
И также Менделевию, Эйнштейнию, Нобелию,
Аргон, Криптон, Неон, Радон, Ксенон, Цинк, Медь, Хлор, Родий,
Азот, Вольфрам и Натрий, Кобальт, Олово есть вроде.
Об этом сообщили мне из Гарварда студенты
Но есть и неоткрытые другие элементы.
Попробуйте перевести эту песню на языки, которые знаете вы.
Так что познавать мир языков можно и через таблицу Менделеева!
Полезные ссылки
1) Элементы таблицы по-китайски с произношением: https://www.youtube.com/watch?v=IL2CLP1RyDQ
2) Статья китайской Википедии о таблице Менделеева: 元素周期表 – 维基百科,自由的百科全书 (wikipedia.org)
3) Статья японской Википедии о таблице Менделеева: 周期表 – Wikipedia
4) Учим языки химиков мира с Language Heroes! Школа самостоятельного изучения иностранных языков – Language Heroes (lh22.ru)
PictureCredit
Основной курс: Редкие языки
6,000 ₽ Купить
Теги по теме:латынь Языки и наука
Периодическая таблица: определение, элементы, группы
Периодическая таблица: определение, элементы, группы | StudySmarterВыберите язык
Предлагаемые языки для вас:
Европа
английский (DE) английский (Великобритания)
StudySmarter — универсальное учебное приложение.
4.8 • Рейтинг +11k
Более 3 миллионов загрузок
Бесплатно
Сохранять
Распечатать
Редактировать
Периодическая таблица
Содержание :
ОГЛАВЛЕНИЕ
Представьте, что вы собираете пазл. По мере того, как часы тикают, вы систематизируете каждую часть, сопоставляя каждую часть вместе, пока, в конце концов, с облегчением и чувством выполненного долга не сформируете картину. Довольно сложно, правда?
Теперь представьте, что вы собираете ту же головоломку, но без половины частей и без готовой картинки, которая вам поможет. Это то, что, должно быть, чувствовали химики, когда пытались расположить все элементы в том, что мы теперь знаем как периодическую таблицу .
Это то, что, должно быть, чувствовали химики, когда пытались расположить все элементы в том, что мы теперь знаем как периодическую таблицу .
- Мы рассмотрим периодическую таблицу в физической химии.
- Мы начнем с определения периодической таблицы, а затем рассмотрим ее структуру.
- Затем мы изучим его историю.
- К концу этой статьи вы должны быть в состоянии объяснить, как устроена периодическая таблица, сравнить строки, столбцы и блоки в периодической таблице и описать, как таблица Менделеева изменилась с течением времени.
Периодическая таблица элементов
Вот определение периодической таблицы:
Периодическая таблица представляет собой отображение элементов, упорядоченных в соответствии с их атомным номером.
Таблица Менделеева. Олив Одагбу, StudySmarter Originals
Периодическая таблица удобна, потому что она упорядочивает элементы в строки и столбцы на основе их свойств. Это означает, что когда вы знаете положение элемента в таблице Менделеева, вы можете предсказать, как он ведет себя и реагирует . Начнем с рассмотрения его структуры.
Это означает, что когда вы знаете положение элемента в таблице Менделеева, вы можете предсказать, как он ведет себя и реагирует . Начнем с рассмотрения его структуры.
Как устроена периодическая таблица?
Прежде всего, периодическая таблица состоит из элементов . Эти элементы собраны в рядов , столбцов, и блоки . Это не всегда было так , но мы узнаем, как оно изменилось позже, когда мы будем обсуждать историю периодической таблицы. На данный момент мы углубимся в то, как устроена периодическая таблица.
Элементы
Как мы определили выше, периодическая таблица представляет собой набор из элементов . Помните, что элемент — это чистое химическое вещество, состоящее из атомов с одинаковым числом протонов в ядрах. Его точное количество протонов определяет количество электронов; это то, что делает элемент, ну, элемент !
Элементы в периодической таблице показаны с использованием их химического символа. Это одно- или двухбуквенное сокращение, уникальное для каждого элемента. Первая буква всегда заглавная, а вторая строчная. Например, медь известна как Cu, кальций как Ca, а углерод как C. Элементы также показаны с их атомным номером и относительной атомной массой .
Это одно- или двухбуквенное сокращение, уникальное для каждого элемента. Первая буква всегда заглавная, а вторая строчная. Например, медь известна как Cu, кальций как Ca, а углерод как C. Элементы также показаны с их атомным номером и относительной атомной массой .
Атомный номер элемента — это число протонов в его ядре, в то время как его относительная атомная масса – это средняя масса одного атома в элементе. Это масса протонов и нейтронов в ядре атома. Относительная атомная масса измеряется по определенной шкале, где атом углерода-12 имеет массу ровно 12.
Элемент. На основе оригинала StudySmarter Олив Одабгу
Перейдите к Масс-спектрометрия , чтобы узнать больше об относительной атомной массе. Вы также можете узнать больше о том, как протоны и электроны атома влияют на его свойства в Фундаментальные частицы .
Периоды
Элементы в периодической таблице объединяются в строки .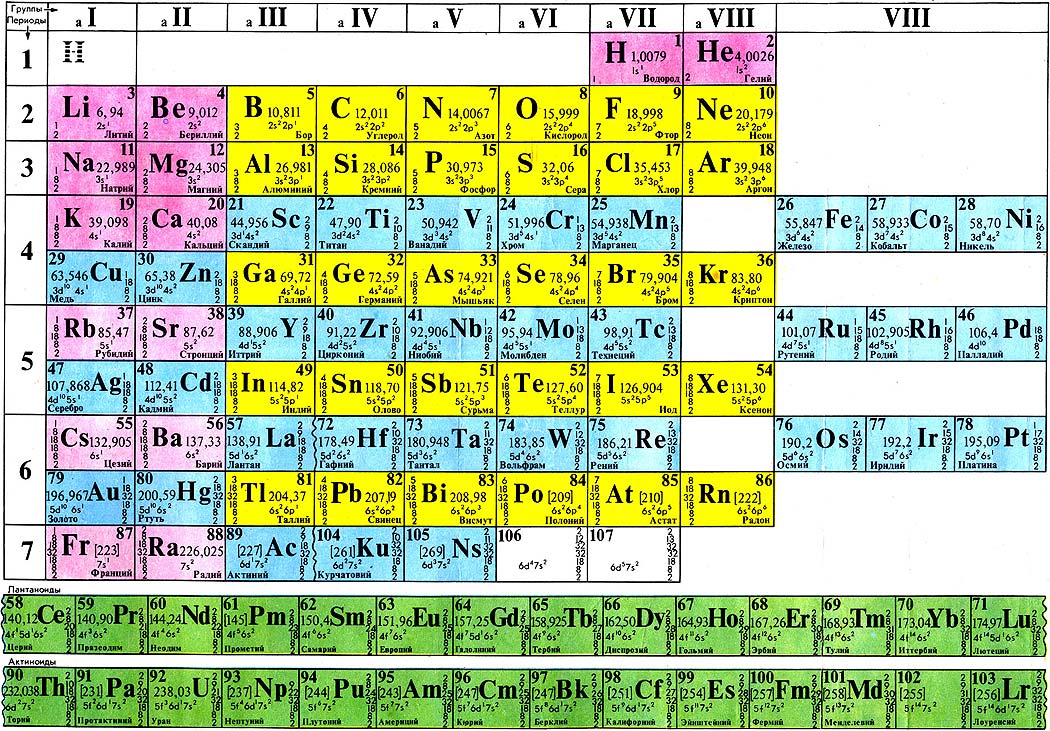 Строка в периодической таблице известна как период ; отсюда происходит слово периодический . Строки периодической таблицы показывают периодичность .
Строка в периодической таблице известна как период ; отсюда происходит слово периодический . Строки периодической таблицы показывают периодичность .
Периодичность относится к тенденциям, которые вы видите по мере прохождения периода (строки) в периодической таблице. Эти тенденции повторяются с каждым новым периодом.
Элементы в периоде упорядочены по возрастанию атомного номера . Помните, что атомный номер — это количество протонов в элементе. Атомный номер увеличивается на 1 каждый раз, когда вы перемещаетесь слева направо по периоду в таблице. Когда вы достигаете конца периода, вы перемещаетесь вниз и влево к началу нового периода и продолжаете считать атомные числа оттуда. Всего в периодической таблице периодов 7 .
Периоды в периодической таблице. Основано на оригинале StudySmarter Олив Одагбу
Атомный номер увеличивается по мере прохождения периода. На основе исследования StudySmarter Original Олив Одагбу
На основе исследования StudySmarter Original Олив Одагбу
Элементы одного периода имеют одинаковое количество электронных оболочек. Например, элементы периода 1 имеют только одну электронную оболочку, тогда как элементы периода 5 имеют пять электронных оболочек.
Группы периодической таблицы
Элементы периодической таблицы также собраны в столбцах . Эти столбцы называются группами . Всего в периодической таблице 18 групп с официальной нумерацией IUPAC 1-18. Однако для целей вашего курса мы будем следовать традиционной системе нумерации, которая равна 9.0034 1-0 или 1-8 . Это часто изображается римскими цифрами. Группы:
Алочные металлы (группа I)
Алочные металлы Земли (Группа II)
Группа Борона (группа III)
Группа углерода (группа IV)
15 9041 9041Группа углерода (группа IV)
15 9041.
 пниктогены (группа V)
пниктогены (группа V)0005
Группы в периодической таблице. Основано на исследовании StudySmarter Original Олив Одагбу. Электроны внешней оболочки также известны как валентных электрона. Валентные электроны определяют химические свойства и реакционную способность элемента. Это означает, что все элементы одной группы реагируют одинаково. Однако обратите внимание, что каждый элемент в группе имеет на одну электронную оболочку больше, чем элемент над ним.
Валентные электроны — это электроны, находящиеся на внешней оболочке атома.
Старая система нумерации полезна, потому что она дает нам представление о том, сколько валентных электронов имеет элемент в определенной группе. Например, все элементы группы I, щелочные металлы, имеют один валентный электрон. Напротив, все элементы группы VII, галогены, имеют семь валентных электронов. Все благородные газы группы VIII имеют восемь валентных электронов, что дает им полные внешние электронные оболочки.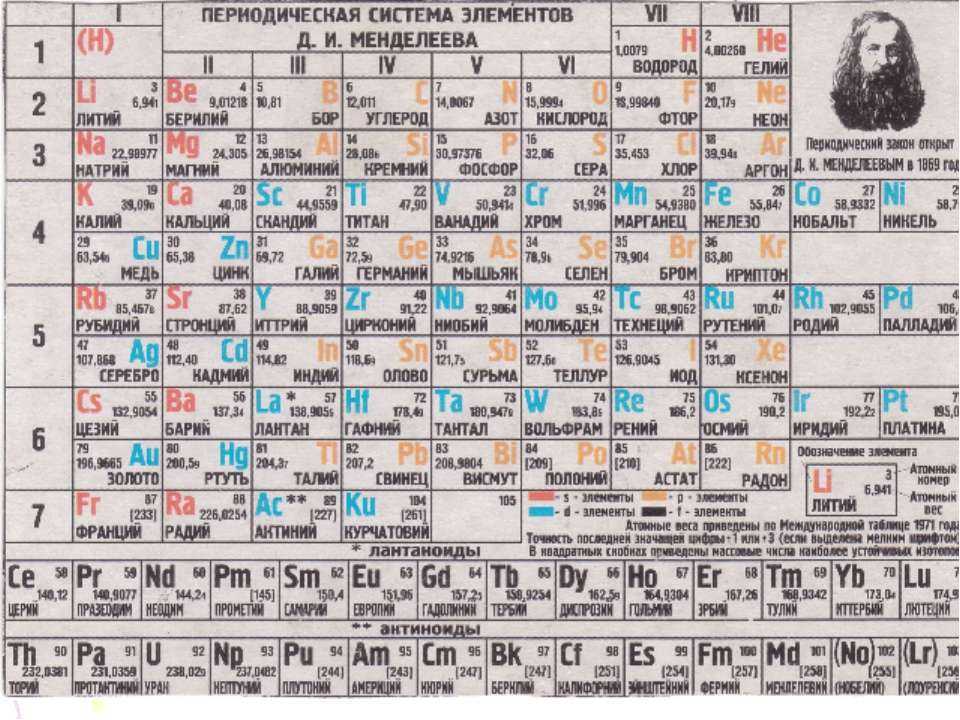
Группа I также включает водород, хотя он не является щелочным металлом и реагирует совершенно иначе, чем другие члены группы. С атомным номером 1 водород является самым легким из существующих элементов. У него всего один протон и один электрон. Поэтому вы можете ожидать, что следующий по легкости элемент, гелий, будет находиться по соседству в группе II, так как у него всего два протона и два электрона. Однако вместо этого гелий находится в группе VIII. Это связано с тем, что в оболочке валентных электронов гелия есть место только для двух электронов, а это означает, что у гелия на самом деле есть полная внешняя оболочка электронов. Это заставляет его вести себя как другие элементы группы VIII.
Количество групп в периодической таблице, равное 18, было рекомендовано Международным союзом теоретической и прикладной химии ( IUPAC) в 1988 году. Оно заменило старую систему нумерации, 1–0 или 1–. 8 (который исключает элементы d- и f-блоков, к которым мы вернемся позже). Старая система все еще широко используется, особенно в экзаменационных комиссиях по английскому (AQA) и шотландскому (SQA), и это та версия, которую вам необходимо знать.
Старая система все еще широко используется, особенно в экзаменационных комиссиях по английскому (AQA) и шотландскому (SQA), и это та версия, которую вам необходимо знать.
Блоки
Вы могли заметить, что при использовании старой системы нумерации групп отсутствуют два больших фрагмента таблицы Менделеева. А как насчет элементов между группами II и III, которые находятся в группах IUPAC с 3 по 12? Как насчет тех двух рядов элементов под таблицей Менделеева — где они вписываются? Ну, еще один способ взглянуть на периодическую таблицу — разделить ее на 9 частей.0034 блоков .
Блоки в периодической таблице представляют собой группы элементов, у которых валентный электрон с наивысшей энергией находится в одной и той же подоболочке.
В периодической таблице есть четыре блока:
- Элементы s-блока имеют самую высокую энергию валентного электрона в s-подоболочке. S-блок включает группы I и II.

- элементы p-блока все имеют валентный электрон с наивысшей энергией в p-подоболочке. Р-блок включает группы с III по VIII, или, по терминологии ИЮПАК, с 13 по 18, и в основном состоит из неметаллов.
- Элементы d-блока имеют самую высокую энергию валентного электрона в d-подоболочке. D-блок включает группы с 3 по 12, а также переходных металла .
- Элементы f-блока имеют валентный электрон с наивысшей энергией в f-подоболочке. F-блок включает лантаноидов и актинидов . Это две строки, показанные под основной частью таблицы Менделеева. Ниже мы показали, как они соотносятся с другими элементами периодической таблицы.
Да, мы знаем, что мы сказали, что гелий находится в группе VIII, но вместо того, чтобы быть в p-блоке, как все другие элементы в группе VIII, он находится в s-блоке. Помните, на его внешней оболочке есть место только для двух электронов? Это связано с тем, что оболочка содержит только s-подоболочку, в то время как все остальные члены группы VIII также имеют p-подоболочку. Это означает, что валентный электрон гелия с самой высокой энергией находится в s-подоболочке, что делает его элементом s-блока.
Это означает, что валентный электрон гелия с самой высокой энергией находится в s-подоболочке, что делает его элементом s-блока.
Чтобы узнать больше об электронных подоболочках, взгляните на Электронные оболочки и Электронная конфигурация .
Блоки периодической таблицы. На основе StudySmarter Original by Olive Odagbu
Периодическая таблица Металлы, неметаллы и металлоиды
Последний способ структурирования периодической таблицы, который мы рассмотрим сегодня, включает разделение таблицы зигзагообразной линией. Он начинается слева от бора и извивается вниз и вправо, пробираясь между кремнием и германием, затем между мышьяком и сурьмой, теллуром и полонием. Наконец, он отделяет астатин от теннессина, прежде чем добить слева от оганесона.
Эта линия имеет разные названия: линия металл-неметалл, амфотерная линия, металлоидная линия и лестничная. Он делит таблицу на металлы, неметаллы и металлоиды.
- Элементы слева от линии классифицируются как металлы.
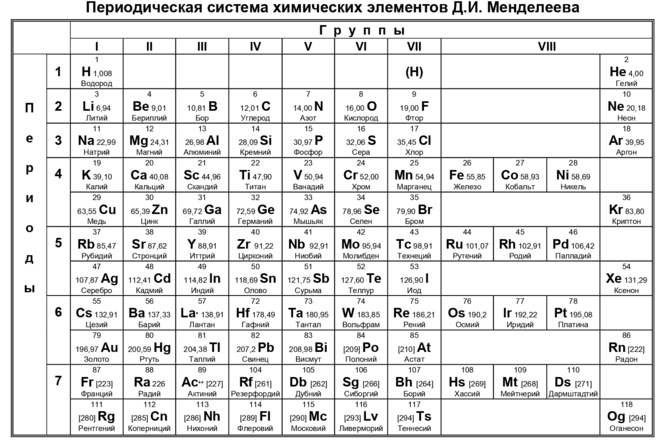
- Элементы справа от черты (а также водород) относятся к неметаллам.
- Некоторые элементы, соприкасающиеся с линией, классифицируются как металлоиды.
Металлы, неметаллы и металлоиды в периодической таблице. Основано на оригинале StudySmarter Олив Одагбу
Металлы
Металлы появляются в левой части периодической таблицы. Они обладают некоторыми характерными свойствами.
- Металлы обычно теряют электроны с образованием положительных катионов.
- Имеют высокие температуры плавления и кипения.
- Имеют низкие значения электроотрицательности.
- В свежесрезанном виде они блестят и блестят.
- Они податливы и пластичны.
- Они являются хорошими проводниками тепла и электричества.
Неметаллы
Неметаллы находятся в правой части периодической таблицы (за исключением водорода, который также является неметаллом). Как следует из названия, они противоположны металлам. На самом деле, вы можете думать о них просто как об отсутствии металлических характеристик.
Как следует из названия, они противоположны металлам. На самом деле, вы можете думать о них просто как об отсутствии металлических характеристик.
- Неметаллы обычно приобретают электроны с образованием отрицательных анионов.
- Имеют высокие значения электроотрицательности.
- Они имеют диапазон температур плавления и кипения. Некоторые из них, такие как кремний, имеют чрезвычайно высокую температуру плавления, в то время как другие, такие как кислород, имеют низкую температуру плавления.
- Твердые неметаллы хрупкие.
- Плохие проводники тепла и электричества.
Металлоиды
Металлоиды находятся в середине периодической таблицы. Они пересекают разделительную линию, отделяющую металлы от неметаллов, и их свойства находятся на полпути между ними.
- Обычно металлоиды блестят и блестят при разрезании, но по своей природе являются хрупкими.
- Имеют средние значения электроотрицательности.
- Являются средними проводниками электричества.

Не существует фиксированного научного определения металлов, неметаллов и металлоидов. Из-за этого разные источники могут классифицировать определенные элементы по-разному, и на самом деле некоторые ученые даже проводят разделительную линию в другом месте. Например, углерод и селен иногда признаются металлоидами.
Теперь мы знаем, как выглядит таблица Менделеева и как она устроена. Но как так получилось?
История периодической таблицы
В начале статьи мы сравнили создание первой версии таблицы Менделеева с попыткой собрать головоломку, в которой отсутствует половина частей и нет картинки, которая поможет вам. Для химиков в годы, предшествовавшие 19 веку, это было проблемой, с которой они столкнулись. Давайте сосредоточимся на трех ученых и их вкладе в современную периодическую таблицу.
Иоганн Вольфганг Доберейнер
В 1817 году немецкий физик Иоганн Вольфганг Доберейнер первым попытался классифицировать элементы.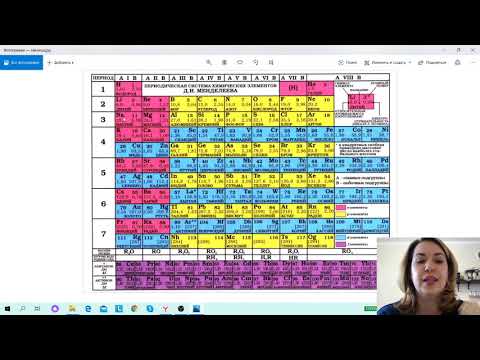 Он заметил, что некоторые элементы можно поместить в группы по три, называемые 9.0034 триады , и что элементы внутри триады имеют сходные свойства. На самом деле свойства второго элемента в триаде находились на полпути между свойствами первого и третьего. Например, он сгруппировал вместе литий, натрий и калий — все металлы, которые, как мы теперь знаем, относятся к группе I.
Он заметил, что некоторые элементы можно поместить в группы по три, называемые 9.0034 триады , и что элементы внутри триады имеют сходные свойства. На самом деле свойства второго элемента в триаде находились на полпути между свойствами первого и третьего. Например, он сгруппировал вместе литий, натрий и калий — все металлы, которые, как мы теперь знаем, относятся к группе I.
Джон Ньюлендс
В 1864 г. элементы. Он увидел, что если расположить все элементы в таблице по атомной массе, их свойства повторяются через равные промежутки времени. Эти свойства повторяются через каждые восемь элементов, что привело к названию «закон октав».
Однако в то время было открыто только около 60 элементов. Ньюлендс ошибочно предположил, что это были единственные существующие элементы. Он не оставил пробелов для каких-либо неоткрытых элементов, поэтому его таблица не имела особого смысла после кальция. Он также иногда помещал два элемента в одну и ту же коробку. В целом его идеи высмеивались сверстниками.
Версия периодической таблицы Ньюленда. Изображение предоставлено: commons.wikimedia.org
Дмитрий Менделеев
Наконец, в 1869 г., русский химик Дмитрий Менделеев пришел к той версии таблицы Менделеева, которую мы знаем сегодня. Он взял идею Ньюлендса о законе октав, но оставил пробелы для неоткрытых элементов, предсказывая их свойства по поведению окружающих их элементов. Хотя он в основном расположил элементы в порядке атомной массы, он поменял местами некоторые из них, чтобы они лучше соответствовали его закону октав.
Например, аргон был намного тяжелее калия, но размещение калия перед аргоном означало бы, что высокореакционноспособный металл калий будет в группе с нереакционноспособными неметаллическими газами, а нереакционноспособный аргон будет в группе с химически активными металлами. Его таблица постепенно была принята, когда были обнаружены новые элементы, которые соответствовали предсказанным им свойствам. Вопрос об атомной массе был решен, когда в 20 веке были открыты субатомные частицы, и ученые поняли, что элементы действительно должны быть упорядочены по атомным 9. 0064 номер , а не масс.
0064 номер , а не масс.
Менделеевская версия периодической таблицы с пробелами, оставленными для неоткрытых элементов. Изображение предоставлено: commons.wikimedia.org
Периодическая таблица — основные выводы
- Периодическая таблица представляет собой отображение элементов, упорядоченных в соответствии с их атомными номерами.
- Периодическая таблица состоит из строк, столбцов и блоков.
- Строка в периодической таблице называется периодом. Периоды показывают периодичность, то есть они показывают тенденции в своих свойствах, которые повторяются в каждой строке. Атомный номер увеличивается по мере того, как вы перемещаетесь по периоду в периодической таблице.
- Столбец периодической таблицы называется группой. Элементы одной группы имеют одинаковое количество валентных электронов и реагируют сходным образом.
- Периодическая таблица разделена на блоки. Блоки — это группы элементов, каждый из которых имеет валентный электрон с наивысшей энергией в одной и той же подоболочке.

- Вы также можете классифицировать элементы как металлы, неметаллы и металлоиды. Металлы находятся в левой части таблицы Менделеева, а неметаллы — в правой. Между ними находятся металлоиды.
- Предыдущие версии периодической таблицы упорядочивали элементы по атомной массе, а не по атомному номеру. Современная периодическая таблица, какой мы ее знаем сегодня, была создана Дмитрием Менделеевым в 1869 году.
Часто задаваемые вопросы о периодической таблице
Табличное расположение химических элементов, которое упорядочено по возрастанию атомного номера и группирует элементы в соответствии с повторяющимися свойствами.
Элементы в периодической таблице расположены в порядке возрастания атомного номера.
Химик Дмитрий Менделеев изобрел периодическую таблицу.
Строки называются периодами.
Итоговая викторина по таблице Менделеева
Вопрос
Какова правильная классификация элемента Zr, циркония
Показать ответ
Ответ
Блок d
Показать вопрос
Вопрос
Что такое поправка на энергию
9000 рубидия?
Показать ответ
Ответ
Rb + (g) → Rb2 + (g) + e–
Показать вопрос
Вопрос
Какова единица атомного радиуса?
Показать ответ
Ответить
Показать вопрос
Вопрос
В каком порядке расположены элементы в периодической таблице?
Показать ответ
Ответ
Увеличение атомного номера
Показать вопрос
Вопрос
Почему атомный радиус уменьшается с течением времени?
Показать ответ
Ответ
Увеличение заряда ядра
Показать вопрос
Вопрос
Почему электроотрицательность увеличивается в течение периода?
Показать ответ
Ответ
Электрон в той же оболочке, похожей на экран
Показать вопрос
Вопрос
Какой из этих элементов имеет наибольший атомный радиус?
Показать ответ
Ответ
Показать вопрос
Вопрос
Атомный номер ____ при перемещении по периоду периодической таблицы.
Показать ответ
Ответить
Увеличить
Показать вопрос
Вопрос
Правда или ложь? Элементы одной группы имеют одинаковое количество электронных оболочек.
Показать ответ
Ответ
Показать вопрос
Вопрос
Сколько валентных электронов имеют элементы группы I?
Показать ответ
Ответить
Показать вопрос
Вопрос
Сколько валентных электронов имеют элементы VII группы?
Показать ответ
Ответить
Показать вопрос
Вопрос
Какая группа периодической таблицы имеет полную внешнюю оболочку электронов?
Показать ответ
Ответ
Группа VIII, также известная как группа 0
Показать вопрос
Вопрос
Сколько электронных оболочек имеют элементы периода 3?
Показать ответ
Ответить
Показать вопрос
Вопрос
Сколько электронов на внешней оболочке имеют элементы периода 3?
Показать ответ
Ответить
Это зависит от
Показать вопрос
Вопрос
Как называются столбцы периодической таблицы?
Показать ответ
Ответить
Группы
Показать вопрос
Вопрос
Как называются строки периодической таблицы?
Показать ответ
Ответ
Периоды
Показать вопрос
Вопрос
Сколько групп в периодической таблице согласно номенклатуре ИЮПАК?
Показать ответ
Ответ
Показать вопрос
Вопрос
Все элементы в одном блоке имеют _____.
Показать ответ
Ответ
Одинаковое количество электронов на внешней оболочке
Показать вопрос
Вопрос
Какие из следующих свойств являются типичными для металлов?
Показать ответ
Ответить
Высокие температуры плавления и кипения
Показать вопрос
Вопрос
Какие из следующих свойств являются типичными свойствами неметаллов?
Показать ответ
Ответ
Высокая электроотрицательность
Показать вопрос
Подробнее о периодической таблице
Откройте для себя подходящий контент для ваших тем
Не нужно обманывать, если у вас есть все необходимое для успеха! Упаковано в одно приложение!
Учебный план
Будьте идеально подготовлены вовремя с индивидуальным планом.
Тесты
Проверьте свои знания с помощью игровых тестов.
Карточки
Создавайте и находите карточки в рекордно короткие сроки.
Заметки
Создавайте красивые заметки быстрее, чем когда-либо прежде.
Учебные наборы
Все учебные материалы в одном месте.
Документы
Загружайте неограниченное количество документов и сохраняйте их в Интернете.
Study Analytics
Определите сильные и слабые стороны вашего исследования.
Еженедельные цели
Ставьте индивидуальные учебные цели и зарабатывайте баллы за их достижение.
Умные напоминания
Хватит откладывать на потом наши напоминания об учебе.
Награды
Зарабатывайте очки, открывайте значки и повышайте уровень во время учебы.
Волшебный маркер
Создавайте карточки в заметках полностью автоматически.
Умное форматирование
Создавайте самые красивые учебные материалы, используя наши шаблоны.
Периодическая таблица элементов: использование каждого элемента периодической таблицы в реальной жизни
Элементы периодической таблицы повсюду, на самом деле они составляют все.
Понимание того, как читать периодическую таблицу, — это одно, но оно не говорит вам, полезен ли элемент, как он выглядит или даже как он используется.
Чтобы ответить на некоторые из этих вопросов, мы составили это краткое руководство, которое поможет вам легко читать и ориентироваться в ресурсах для некоторых применений каждого элемента периодической таблицы.
Все элементы периодической таблицы перечислены ниже и упорядочены по атомному номеру от 1 до 118.
**Совет: если вы хотите перейти к определенному элементу, используйте поиск (CTRL + F ) функция в вашем браузере, чтобы быстро определить, что вы ищете**
Руководство
Каждый заголовок элемента имеет свое имя, атомный номер, атомный символ, а также цветовой код для обозначения группы, к которой он принадлежит .
Например, водород имеет зеленый цвет, поэтому он относится к группе «другие неметаллы».
Используйте это руководство, чтобы определить группу каждого металла, когда вы узнаете о них больше.
Водород
Обозначение: H
Атомный вес: 1,008
Описание: Водород является легким взрывоопасным газом.
Где используется: Водород составляет около 90 процентов атомов во всей Вселенной. Химическое вещество активно используется как в виде газа, так и в качестве жидкого топлива. Водород использовался НАСА в качестве основного топлива для программы Space Shuttle, а также в настоящее время активно используется в нефтяной и обрабатывающей промышленности. 9
Атомный вес:
Где используется: Газообразный гелий, как известно, легче воздуха, поэтому его используют в метеорологических и праздничных воздушных шарах. Он также используется в качестве инертного экрана при дуговой сварке и для герметизации баков с жидким топливом в ракетах. Из-за его широкого рекреационного использования природные источники гелия рискуют полностью истощиться в следующем десятилетии, что вызовет опасения у научного сообщества.
Из-за его широкого рекреационного использования природные источники гелия рискуют полностью истощиться в следующем десятилетии, что вызовет опасения у научного сообщества.
Литий
Символ: Li
Атомный вес: 6,94
Описание: Легкий и реактивный металл.
Где используется: Известно, что литий чаще всего используется в батареях. Он также используется в алюминиевых сплавах, чтобы сделать посуду более прочной, и, что самое удивительное, в психиатрических препаратах в качестве стабилизатора настроения.
Бериллий
Обозначение: Be
Атомный вес: 9.012183(5)
Описание: Бериллий — легкий металл.
Где используется: Этот элемент чаще всего используется в качестве легирующей добавки для меди. В сочетании полученный металл, бериллиевая медь, используется для изготовления пружин и различных электрических устройств. Благодаря легким свойствам металла он используется в конструкции в аэрокосмической промышленности.
Благодаря легким свойствам металла он используется в конструкции в аэрокосмической промышленности.
Бор
Обозначение: B
Атомный вес: 10,81
Описание: Бор представляет собой порошкообразное твердое вещество черного цвета.
Где используется: Бор используется в пиротехнике. При горении он дает зеленый цвет в пламени. Более распространено использование борной кислоты и буры. Вы можете найти бор в антисептиках, моющих средствах, керамической глазури и глазных каплях.
Углерод
Символ: C
Атомный вес: 12,011
Описание: Существует ряд чистых форм этого элемента, включая графит, алмаз, фуллерены и графен. Наноформы, фуллерены и графен выглядят как черные или темно-коричневые сажеподобные порошки.
Где используется: Углерод уникален среди элементов своей способностью образовывать прочно связанные цепи, скрепленные атомами водорода. Эти углеводороды в основном используются в качестве топлива и сырья для производства полимеров, волокон, красок, растворителей, пластмасс и т. д. Примесный углерод в виде древесного угля (из древесины) и кокса (из угля) используется при выплавке металлов. .
Эти углеводороды в основном используются в качестве топлива и сырья для производства полимеров, волокон, красок, растворителей, пластмасс и т. д. Примесный углерод в виде древесного угля (из древесины) и кокса (из угля) используется при выплавке металлов. .
Графит используется для изготовления карандашей, тиглей и электродов. Чистый алмаз также полностью состоит из атомов углерода. Открытие углеродных нанотрубок, фуллеренов и листов графена толщиной в атом привело к их использованию в электронной промышленности и в нанотехнологиях в целом.
Азот
Символ: N
Атомный вес: 14,007
Описание: Азот — бесцветный газ.
Где используется: 900:35 78 процентов всей атмосферы Земли состоит из азота. Этот элемент имеет важное значение для химической промышленности, поскольку он является ключевым питательным веществом в удобрениях и ключевым компонентом азотной кислоты, нейлона и взрывчатых веществ. Процесс Габера — это хорошо известный метод взаимодействия азота с водородом с образованием аммиака.
Процесс Габера — это хорошо известный метод взаимодействия азота с водородом с образованием аммиака.
Кислород
Символ: O
Атомный вес: 15,999
Описание: Кислород — бесцветный газ.
Где используется: Многие живые существа, включая людей, используют кислород для дыхания. Чистый кислород используется для лечения проблем с дыханием и делает космический корабль пригодным для жизни. Кислород в промышленности в основном используется при производстве стали и других металлических сплавов. Большие количества также используются в производстве химических веществ, таких как азотная кислота и перекись водорода.
Он также используется в качестве антифриза и для производства полиэстера и хлорэтилена, предшественника ПВХ. Газообразный кислород используется для кислородно-ацетиленовой сварки. Растет использование в очистке сточных вод и промышленных стоков.
Фтор
Обозначение: Fl
Атомный вес: 18,998403163(6)
Наиболее активный и ядовитый газ .
Где используется: Фтор является обычной добавкой к питьевой воде и используется в качестве чистящего средства в зубной пасте. В поп-культуре плавиковая кислота использовалась в качестве растворителя в популярном телешоу «Во все тяжкие». Химическое вещество может растворять стекло и используется в основном в качестве травильного состава.
Он также используется для производства гексафторида урана, используемого в ядерной энергетике для разделения изотопов урана, и для производства гексафторида серы, изолирующего газа для мощных электрических трансформаторов.
Фтор также используется во многих растворителях и высокотемпературных пластмассах, таких как тефлон и Gore-Tex®.
Неон
Обозначение: Ne
Атомный вес: 20.1797(6)
Описание: Неон — инертный газ.
Где используется: Неон — четвертый по распространенности элемент во всей вселенной.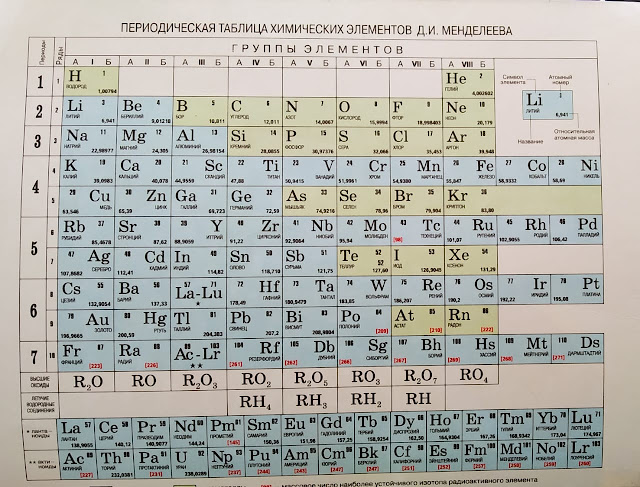 Безусловно, наиболее заметное использование этого элемента сегодня используется в рекламных вывесках. Под влиянием электричества стекло обычно светится, что приводит к его использованию в соответствующей индустрии вывесок, а также в высоковольтных индикаторах и лазерах. Жидкий неон является важным криогенным хладагентом.
Безусловно, наиболее заметное использование этого элемента сегодня используется в рекламных вывесках. Под влиянием электричества стекло обычно светится, что приводит к его использованию в соответствующей индустрии вывесок, а также в высоковольтных индикаторах и лазерах. Жидкий неон является важным криогенным хладагентом.
Диаграмма:
Источник: BruceBlaus/WikimediaНатрий
Символ: Na
Атомный вес: 22,98976928(2)
Описание: Натрий — очень реакционноспособный мягкий металл.
Где используется: Натрий используется в уличных фонарях для получения желтого света, а также является компонентом многих соединений, таких как поваренная соль, кальцинированная сода, бура и пищевая сода.
Магний
Обозначение: Mg
Атомный вес: 24,305
Описание: Магний – легкий металл.
Где используется: Магний находит широкое применение в медицине в виде соли Эпсома, магнезиального молока, хлорида и цитрата.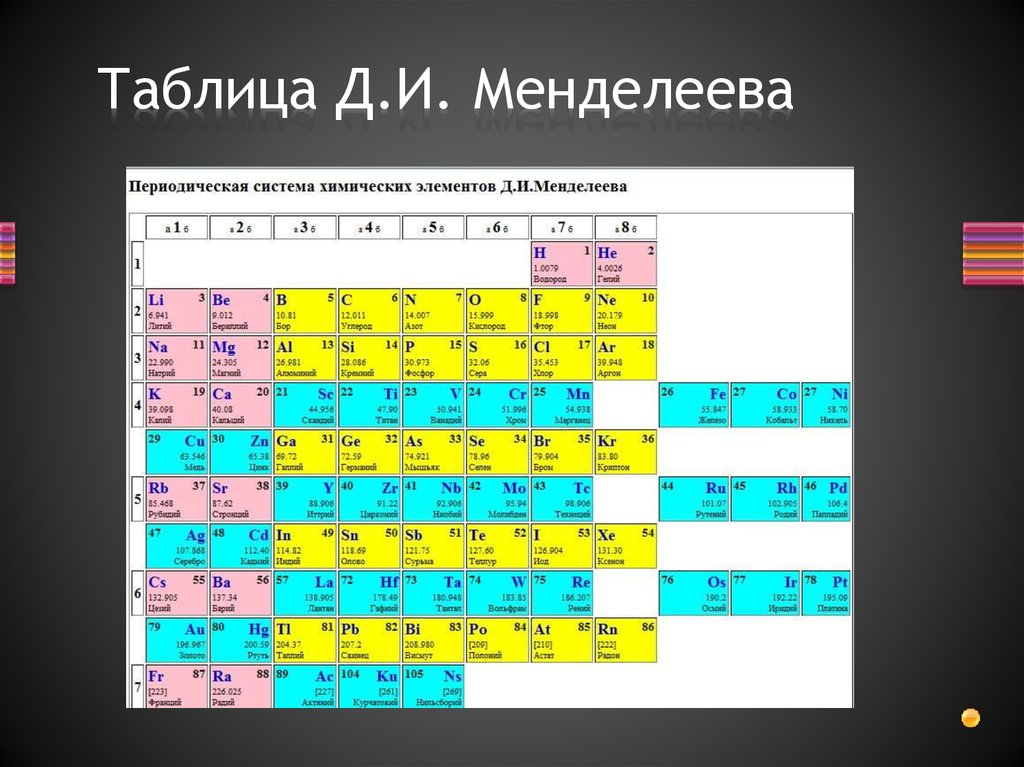 Магний также необходим как животным, так и растениям. Поскольку он менее плотный, чем алюминий, его часто сплавляют с алюминием для использования в конструкциях самолетов и автомобилей. Его также добавляют в расплавленный чугун и сталь для удаления серы.
Магний также необходим как животным, так и растениям. Поскольку он менее плотный, чем алюминий, его часто сплавляют с алюминием для использования в конструкциях самолетов и автомобилей. Его также добавляют в расплавленный чугун и сталь для удаления серы.
Поскольку магний легко воспламеняется на воздухе и горит ярким светом, он используется в сигнальных ракетах, фейерверках и бенгальских огнях. Оксид магния используется для изготовления жаростойких кирпичей для каминов и печей. Его также добавляют в корма для скота и удобрения.
Алюминий
Обозначение: Al
Атомный вес: 26,9815385
5 Описание: 90 034
Где используется: Алюминий — это мягкий и ковкий металл, который используется в консервных банках и мусорных баках, посуде, деталях самолетов и автомобилей, а также в других конструкциях.
Кремний
Обозначение: Si
Атомный вес: 28,085
Описание: Кремний — это твердый металлоид.
Где используется: Кремний широко используется в полупроводниковой промышленности в твердотельной электронике. Для таких применений кремний должен быть легирован бором, галлием, фосфором или мышьяком.
Самый популярный
Фосфор
Символ: P
Атомный вес: 30,973761998(5)
Описание: Фосфор — это светящееся белое воскообразное твердое вещество.
Где используется: Белый фосфор используется в сигнальных ракетах и зажигательных устройствах, а красный фосфор используется в материалах, наклеиваемых на бока спичечных коробков. Однако соединения фосфора чаще всего используются в качестве удобрений. Фосфор также важен в производстве стали.
Сера
Символ: S
Атомный вес: 32,06
Описание: Сера представляет собой хрупкое твердое вещество желтого цвета.
Где используется: Сера используется в порохе и другой пиротехнике, производстве резины, а также в качестве инсектицида, фунгицида и фумиганта. Его также можно использовать для лечения кожных заболеваний, однако его основное применение заключается в разделении соединений.
Хлор
Обозначение: Cl
Атомный вес: 35,45
Описание: Хлор — это ядовитый газ зеленоватого цвета.
Где используется: Хлор используется для очистки воды и в качестве антисептика. При производстве бумаги, пластмасс, растворителей и текстиля также используется большое количество хлора.
Аргон
Обозначение: Ar
Атомный вес: 39,948(1)
Описание: Аргон — инертный газ.
Где используется: Аргон используется в лампах накаливания и люминесцентных лампах в качестве защитного слоя вокруг нити накала, чтобы предотвратить ее коррозию кислородом. Он также используется в качестве защитного экрана при дуговой сварке и полупроводниковых кристаллах.
Он также используется в качестве защитного экрана при дуговой сварке и полупроводниковых кристаллах.
Калий
Обозначение: K
Атомный вес: 39,0983
Описание: Калий — это мягкий металл.
Где используется: Калий в основном используется в соединениях. Он сочетается с хлором для производства хлорида калия, который используется в удобрениях, фармацевтических препаратах и солевых каплях. Гидроксид калия также используется в мыле и чистящих средствах, а карбонат калия используется в производстве стекла.
Кальций
Обозначение: Ca
Атомный вес: 40.078(4)
Описание: Кальций — мягкий металл.
Где используется: Кальций используется для получения тория и урана в качестве восстановителя. Он также используется в качестве легирующего агента для алюминия, меди, свинца и магния.
Скандий
Символ: Sc
Атомный вес: 44,8
Описание: Скандий — мягкий легкий металл.
Где используется: Широко используемый в ртутных лампах скандий является ключевым элементом в освещении стадионов. Его радиоактивный изотоп также используется в качестве трассирующего агента.
Титан
Обозначение: Ti
Атомный вес: 47,867(1)
Описание: Титан – самый легкий и жаропрочный металл.
Где используется: Титан — невероятно прочный металл, используемый в сплавах с алюминием, железом и другими металлами. Этот прочный металл используется в аэрокосмической промышленности, а также в двигателях отчасти из-за его способности сохранять свою прочность в экстремальных температурных условиях.
Ванадий
Обозначение: V
Атомный вес: 50,9415(1)
Описание: Ванадий представляет собой металл.
Где используется: Этот элемент используется в реактивных двигателях и компонентах самолетов. Все его применения требуют, чтобы он сочетался с другим металлом или элементом, таким как ванадиево-галлиевая лента, используемая в магнитах. Около 80 процентов произведенного ванадия используется в качестве добавки к стали для производства очень прочного сплава.
Диаграмма:
Источник: СтэнфордХром
Символ: CR
Атомный вес: 51.9961 (6)
Описание: 51.9961 (6)
.0035 Хром — твердый блестящий металл.
Где используется: Хром используется в нержавеющей стали, а также в процессе хромирования. Различные соединения хрома известны своими яркими цветами.
Марганец
Обозначение: Mn
Атомный вес: 54,4(3)
Описание: Марганец представляет собой твердый металл.
Где используется: Диоксид марганца составляет около 0,14% земной коры. Он используется в стекле для удаления зеленого цвета, присутствующего в соединениях железа. Он слишком хрупок, чтобы использоваться сам по себе, и в основном используется в виде сплава.
Железо
Обозначение: Fe
Атомный вес: 55,845(2)
Описание: Железо является металлом средней твердости.
Где используется: Железо в основном используется для производства стали. Когда сталь соединяется с хромом, получается нержавеющая сталь, устойчивая к коррозии.
Кобальт
Символ: Co
Атомный вес: 58.4(4)
Описание: Кобальт — это твердый металл, обладающий магнитными свойствами.
Где используется: Кобальт в основном используется для лечения рака и лучевой терапии. Металлический кобальт иногда используется в гальванике из-за его привлекательного внешнего вида, твердости и устойчивости к коррозии.
Металлический кобальт иногда используется в гальванике из-за его привлекательного внешнего вида, твердости и устойчивости к коррозии.
Никель
Обозначение: Ni
Атомный вес: 58,6934(4)
Описание: -Нельзь является магнитно-твердым металлом.
Где используется: Никель используется в нержавеющей стали и других антикоррозионных металлических сплавах. Другие известные области применения включают производство труб и трубок, а также в процессе опреснения.
Медь
Обозначение: Cu
Атомный вес: 63,546(3)
Описание: Медь — окрашенный при нагревании металл, который хорошо проводит электричество.
Где используется: Медь является одним из лучших проводников электричества, поэтому ее используют в электронике и двигателях. Металл также очень теплопроводен, поэтому он используется в радиаторах, кондиционерах и системах отопления.
Цинк
Обозначение: Zn
Атомный вес: 65,38(2)
Описание: Цинк — это некорродирующий металл.
Где он используется: Цинк используется в качестве легирующего агента для латуни, никеля, серебра и алюминия. Краски, каучуки, косметика, батареи, текстиль и чернила также нуждаются в этом элементе.
Галлий
Обозначение: Ga
Атомный вес: 69,723(1)
Описание: Галлий — это мягкий металл с низкой температурой плавления.
Где используется: Поскольку галлий имеет низкую температуру плавления, его часто используют в медицинских термометрах вместо ртути. В сочетании с мышьяком он используется в полупроводниках, лазерах и солнечных панелях. Его также можно использовать в производстве зеркал.
Германий
Обозначение: Ge
Атомный вес: 72,630(8)
Описание: Германий — хрупкий металлоид.
Где используется: Германий находит применение в полупроводниковой промышленности. Когда он легирован другими элементами, из него получаются высокоэффективные транзисторы. Продолжая использовать его в электронике, он также реализован в люминесцентных лампах.
Мышьяк
Обозначение: As
Атомный вес: 74,
5(6)
Описание: Мышьяк — это хрупкий металлоид.
Где используется: Этот элемент используется в качестве легирующего агента в транзисторах, в основном с галлием. Многие соединения мышьяка используются в качестве инсектицидов и ядов.
Селен
Обозначение: Se
Атомный вес: 78,971(8)
Описание: Селен представляет собой хрупкое вещество серого цвета.
Где используется: Селен в основном используется в стекольной промышленности. Его свойства позволяют обесцвечивать класс, а также изготавливать красное стекло. Используется в солнечных батареях и фотоэлементах. В пленочной фотографии он также используется в качестве фотографического тонера.
Его свойства позволяют обесцвечивать класс, а также изготавливать красное стекло. Используется в солнечных батареях и фотоэлементах. В пленочной фотографии он также используется в качестве фотографического тонера.
Бром
Символ: Br
Атомный вес: 79,904
Описание: Бром представляет собой жидкость темно-красного цвета.
Где используется: Бром используется в качестве антипирена в пластмассах и электронике. Его также можно использовать для очистки и дезинфекции воды, что приводит к его использованию в бассейнах и джакузи.
Криптон
Символ: Kr
Атомный вес: 83,798(2)
Описание: Криптон представляет собой газ.
Где используется: Примерно 0,0001% атмосферы Земли составляет криптон, что делает его получение относительно сложным. Этот элемент используется для вспышек в высокоскоростной фотографии, а также в качестве проводящего газа в люминесцентных лампах. Фторид криптона используется в некоторых лазерах.
Фторид криптона используется в некоторых лазерах.
Рубидий
Обозначение: Rb
Атомный вес: 85.4678(3)
Описание: Рубидий – это мягкий, реакционноспособный металл.
Где используется: Рубидий используется в вакуумных трубках для удаления следов газов. Он также широко используется в фотоэлементах и специализированных очках. Он легко ионизируется, поэтому его часто используют в качестве топлива в космических кораблях.
Диаграмма:
Источник: Ahazard/WikimediaСтронций
Обозначение: Sr
Атомный вес: 87,62(1)
Описание: Стронций — мягкий металл.
Где используется: Стронций используется в пиротехнике для получения ярко-красного цвета. Его также можно использовать в производстве ферритовых магнитов и рафинировании цинка.
Иттрий
Обозначение: Y
Атомный вес: 88,
(2)Описание:
35 Иттрий – мягкий металл.

Где используется: Оксид иттрия используется для изготовления телевизионных ламп с красным фосфором. Наряду с этим его применяют для повышения прочности алюминиевых и магниевых сплавов.
Цирконий
Обозначение: Zr
Атомный вес: 91.224(2)
Описание: Цирконий является нейтронно-стойким металлом.
Где используется: Цирконий используется в качестве антикоррозионного состава в насосах и клапанах. Он не поглощает нейтроны, поэтому также широко используется в ядерных реакторах.
Ниобий
Обозначение: Nb
Атомный вес: 92,
(2)
Описание: Ниобий – металл с высокой температурой плавления.
Где используется: Ниобий используется в сплавах из нержавеющей стали. Сплавы, изготовленные с использованием ниобия, очень прочны и часто используются в трубопроводах и реактивных двигателях.
Молибден
Обозначение: Mo
Атомный вес: 95.95(1)
Описание: Молибден — это металл с высокой температурой плавления.
Где используется: Молибден используется для изготовления сплавов, используемых в деталях ракет и самолетов, а также в атомной энергетике и в нагревательных элементах. Его можно использовать для очистки нефти, но в основном он используется в качестве легирующего агента для очистки стали. Дисульфид молибдена используется в качестве присадки к смазочным материалам.
Технеций
Символ: Tc
Атомный вес: [98]
Описание: Технеций – это долгоживущий радиоактивный элемент.
Где используется: Технеций — синтезированный элемент, который можно использовать в качестве радиоактивного индикатора.
Рутений
Обозначение: Ru
Атомный вес: 101. 07(2)
07(2)
Описание: Рутений представляет собой некоррозионно-твердый металл.
Где используется: Рутений используется в качестве катализатора для упрочнения металлов. Он также используется в электрических контактах и для окрашивания стекла.
Родий
Обозначение: Rh
Атомный вес: 102,
(2)Описание: Rh блестящий, некорродирующий металл.
Где используется: Родий используется для изготовления электрических контактов. Это использование распространяется на каталитические нейтрализаторы, но его основное применение – в качестве легирующего агента. Сплавы родия можно использовать в печах, электродах и свечах зажигания.
Палладий
Обозначение: Pd
Атомный вес: 106,42(1)
Описание: Палладий является твердым металлом, не подверженным коррозии.
Где используется: Палладий является важным элементом процесса каталитической конверсии. Он также используется в ювелирных изделиях и зубных пломбах.
Серебро
Символ: Ag
Атомный вес: 107.8682(2)
Описание: Серебро — это мягкий блестящий металл, который является лучшим проводником электричества.
Где используется: Серебро используется в ювелирных изделиях и посуде. Это лучший отражатель видимого света, хотя и тускнеет. Он используется в соединениях для пайки и пайки, а также в батареях. Серебряные краски используются для изготовления печатных плат. Серебро также обладает антибактериальными свойствами, и недавно наночастицы серебра стали использоваться в одежде для предотвращения роста бактерий и создания неприятных запахов.
Кадмий
Обозначение: Cd
Атомный вес: 112. 414(4)
414(4)
Описание: Кадмий является мягким, некорродирующим металлом.
Где используется: Кадмий ядовит, поэтому практического применения у него мало. Его можно использовать для предотвращения коррозии или для поглощения нейтронов в ядерных реакторах. Одним из наиболее коммерческих применений является перезаряжаемые никель-кадмиевые батареи.
Индий
Обозначение: In
Атомный вес: 114.818(1)
Описание: Индий — мягкий металл .
Где используется: Индий в основном используется в качестве легирующей добавки для германия в процессе производства транзисторов. Он также используется для изготовления зеркал с высокой отражающей способностью и легкоплавких сплавов.
Олово
Обозначение: Sn
Атомный вес: 118,710(7)
Описание: Олово — мягкий металл, не подверженный коррозии.
Где используется: Олово хорошо полируется и не подвержено коррозии. Он в основном используется для покрытия других металлов или в качестве сплава припоя и олова. Ниобиево-оловянные магниты известны своими сверхпроводящими способностями.
Сурьма
Обозначение: Sb
Атомный вес: 121,760(1)
Описание: Сурьма представляет собой металлолом.
Где используется: Сурьма в основном используется в батареях, оболочке кабелей и других металлических изделиях. Его можно использовать для изготовления огнеупорных материалов и красок. Древние египтяне использовали этот элемент в качестве черного макияжа для глаз.
Изображение:
Источник: MindatTellurium
Символ: TE
Атомный вес: 127,60 (3)
Описание: .
Где используется: Теллур улучшает обрабатываемость меди и нержавеющей стали. Он используется в качестве основного компонента чугуна и капсюлей-детонаторов.
Он используется в качестве основного компонента чугуна и капсюлей-детонаторов.
Йод
Обозначение: I
Атомный вес: 126,
(3)
Описание: йод фиолетово-черный.
Где используется: Соли йода используются в фотопленке и в качестве антисептика для ран. Радиоактивный изотоп йода-131 используется для лечения рака щитовидной железы. Его часто добавляют в небольших количествах в поваренную соль, чтобы избежать дефицита йода.
Ксенон
Обозначение: Xe
Атомный вес: 131,293(6)
Описание: в ксеноне представляет собой газ.
Где используется: Ксенон используется в фотовспышках и дуговых лампах для съемок фильмов. Под давлением в дуговой лампе он может излучать ультрафиолетовый свет. Он также используется для обнаружения излучения и в счетчиках рентгеновского излучения.
Цезий
Символ: Cs
Атомный вес: 132,
196(6)
Описание: Цезий (Цезий) — это мягкий металл, который является реакционноспособным и имеет самые большие стабильные атомы.
Где используется: Цезий используется в вакуумных трубках для удаления следовых газов. Чаще всего используется в качестве соединения в буровом растворе. Одно из его наиболее важных применений — в «цезиевых часах» (атомных часах) и в качестве катализатора процесса гидрогенизации.
Барий
Символ: Ba
Атомный вес: 137,327(7)
Описание: Барий – это мягкий металл, поглощающий рентгеновские лучи.
Где используется: Барий используется для получения зеленого свечения в пиротехнике. Он также используется для удаления газов из вакуумных трубок. Соединения бария используются в качестве контрастного вещества в рентгеновских лучах.
Он также используется для удаления газов из вакуумных трубок. Соединения бария используются в качестве контрастного вещества в рентгеновских лучах.
Лантан
Обозначение: La
Атомный вес: 138,
(7)
Описание: Лантан — мягкий металл.
Где используется: Лантан используется вместе с редкоземельными элементами для изготовления дуговых ламп. Он также составляет около 20 процентов мишметалла, сплава, используемого в кремне для зажигалок. Сплав лантана и никеля используется для хранения газообразного водорода для использования в транспортных средствах с водородным двигателем, а лантан также используется в никель-металлогидридных батареях.
Церий
Обозначение: Ce
Атомный вес: 140,116(1)
Описание: Церий — мягкий металл.
Где используется: Церий также используется в качестве компонента мишметалла для производства кремня для зажигалок. Его можно использовать в качестве катализатора для очистки нефти. Оксид церия также используется в качестве компонента стенок в самоочищающихся печах.
Его можно использовать в качестве катализатора для очистки нефти. Оксид церия также используется в качестве компонента стенок в самоочищающихся печах.
Празеодим
Символ: Pr
Атомный вес: 140,(2)
Описание: Празеодим — это мягкий металл.
Где используется: Празеодим используется для изготовления очков из желтого стекла для сварщиков. Празеодим также используется в кремневых зажигалках. Однако его основное применение – окрашивание стекла и эмалей.
Неодим
Обозначение: Nd
Атомный вес: 144,242(3)
Описание: Неодим представляет собой мягкий металл.
Где используется: Наиболее важное применение неодима — сплав с железом и бором для изготовления очень сильных постоянных магнитов. Неодим используется для изготовления кремня для зажигалок и входит в состав специальных очков сварщика. Неодимовое стекло используется для изготовления лазеров, а оксид и нитрат неодима используются в качестве катализаторов в реакциях полимеризации.
Неодимовое стекло используется для изготовления лазеров, а оксид и нитрат неодима используются в качестве катализаторов в реакциях полимеризации.
Прометий
Символ: Pm
Атомный вес: [145]
Описание: Прометий — это радиоактивный долгоживущий элемент.
Где используется: Прометий используется в основном для исследований в области радиации. Его можно использовать в ядерных батареях и в качестве источника света для сигналов. Исследователи считают, что вскоре его можно будет использовать в портативных рентгеновских аппаратах.
Самарий
Обозначение: Sm
Атомный вес: 150,36(2)
Описание: Самарий представляет собой0034 мягкий металл.
Где используется: Самарий используется в качестве катализатора для дегидратации и дегидрирования этанолового топлива. Его также можно использовать для поглощения инфракрасных световых лучей и при лечении рака.
Его также можно использовать для поглощения инфракрасных световых лучей и при лечении рака.
Европий
Обозначение: Eu
Атомный вес: 151,964(1)
Описание: Европий представляет собой мягкий металл.
Где используется: Европий является хорошим поглотителем нейтронов, поэтому его часто используют в ядерных реакторах. Одно из его соединений также используется в производстве красного фосфора в телевизорах.
Гадолиний
Символ: Gd
Атомный вес: 157,25(3)
Описание:
Где он используется: Гадолиний часто используется в приложениях, где присутствуют микроволны. Его также можно использовать в телевизионных трубках с зеленым люминофором. Элемент является магнитным, что привело к его использованию в аппаратах МРТ.
Диаграмма:
Источник: Грег Робсон.
Где используется: Тербий используется в качестве стабилизатора высокотемпературных топливных элементов. Его сплавы также используются в электронных устройствах и в качестве индикаторов магнитного поля.
Диспрозий
Символ: Dy
Атомный вес: 162.500(1)
Описание: Диспрозий — это мягкий металл.
Где используется: В сочетании с редкоземельными элементами диспрозий используется в качестве лазерного материала. Его также можно использовать в стержнях ядерных реакторов.
Гольмий
Символ: Ho
Атомный вес: 164,
(2)
Описание: – мягкий металл.
Где используется: Гольмий используется в производстве магнитов в качестве концентратора магнитного потока. Он также используется в качестве желтого или красного цвета в производстве кубического циркония.
Erbium
Символ: ER
Атомный вес: 167,259 (3)
Описание: Эрбиум – это мягкий металл
, где он используется: Эрбиум – это необработанный металл. к его использованию в ядерных управляющих стержнях. Его также можно использовать для уменьшения твердости металлов, а также в усилителях и лазерах.
Тулий
Символ: Tm
Атомный вес: 168.
Описание: Тулий — мягкий металл.
Где используется: Тулий — наименее встречающийся в природе элемент на Земле. При облучении тулий образует изотоп, излучающий рентгеновские лучи, и его можно использовать для изготовления легкого портативного рентгеновского аппарата. Тулий также используется в некоторых хирургических лазерах.
Иттербий
Обозначение: Yb
Атомный вес: 173,045(10)
Описание: Иттербий — мягкий металл.
Где используется: Считается, что иттербий можно использовать для измельчения зерна в стали. Он также может быть использован в качестве промышленного катализатора.
Лютеций
Обозначение: Lu
Атомный вес: 174,9668(1)
Описание: Лютеций — самый редкий и плотный металл.
Где используется: Лютеций очень редкий и дорогой. После очистки его можно использовать в процессе крекинга нефти. Есть несколько других коммерческих приложений.
Гафний
Обозначение: Hf
Атомный вес: 178,49(2)
Описание: Гафний является некорродирующим металлом.
Где используется: Гафний является хорошим поглотителем нейтронов, поэтому он используется в стержнях управления атомными подводными лодками. Из-за высокой температуры плавления он также используется в горелках для плазменной сварки. Оксид гафния используется в микросхемах.
Оксид гафния используется в микросхемах.
Тантал
Обозначение: Ta
Атомный вес: 180,(2)
Описание: Тантал — это коррозионностойкий металл с высокой температурой плавления.
Где используется: Тантал используется в электронной промышленности для изготовления конденсаторов и резисторов. Его можно использовать для увеличения прочности металлических сплавов, а также для повышения коррозионной стойкости. Металл также используется в хирургических инструментах, потому что он не вызывает иммунного ответа.
Вольфрам
Обозначение: W
Атомный вес: 183,84(1)
Описание: Вольфрам — плотный металл с самой высокой температурой плавления.
Где используется: Вольфрам имеет самую высокую температуру плавления среди всех металлов, что привело к его использованию в качестве нити накала в лампах накаливания. Он также используется в стали для придания прочности.
Он также используется в стали для придания прочности.
Рений
Символ: Re
Атомный вес: 186.207(1)
Описание: Рений — это плотный металл с высокой температурой плавления.
Где используется: Рений — распространенный катализатор в производстве высокооктанового бензина. Он также используется в сплавах для реактивных двигателей и в качестве нитей накала для масс-спектрографов.
OSMIUM
Символ: OS
Атомный вес: 190.23 (3)
Описание: Осмий является некорродирующим жестким металлом с высоким содержанием мельтинг-точков и является элементом DENest.
Где используется: Осмий в основном используется для изготовления сплавов твердых металлов. Вы можете найти его в наконечниках шариковых ручек, иглах для грампластинок, электрических контактах и других металлических компонентах, где необходимо уменьшить трение.
Iridium
Символ: IR
Атомный вес: 192.217 (3)
Описание: Иридий является некоррезирующим жестким металлом и также является элементом Densest (то же самое.
Где используется: Иридий в основном используется в качестве отвердителя для платины. Этот элемент также используется в качестве сплава в наконечниках перьевых ручек и подшипниках компаса, а также для контактов в свечах зажигания.
Платина
Обозначение: Pt
Атомный вес: 195.084(9)
Описание: плотный металл, не подверженный коррозии.
Где используется: Платина известна своими коррозионно-стойкими свойствами и уже давно используется в ювелирных изделиях. Его основное применение в каталитических нейтрализаторах для автомобилей.
Золото
Обозначение: Au
Атомный вес: 196,
9(5)
Описание: металл, который не тускнеет, является самым ковким металлом.
Где используется: Золото — один из самых желанных металлов в мире, потому что ему легко придавать форму и лепить, оно хорошо проводит электричество и не тускнеет. Помимо использования в чеканке монет и ювелирных изделиях, он используется в шестернях для часов, суставах искусственных конечностей и электрических разъемах. Наночастицы золота используются в качестве промышленных катализаторов.
Ртуть
Обозначение: Hg
Атомный вес: 200.592(3)
Описание: Ртуть представляет собой токсичную жидкость.
Где используется: Ртуть используется для изготовления термометров, барометров, электрических переключателей и других приборов. Он часто используется в уличных фонарях и люминесцентных лампах, а также в химической промышленности в качестве катализатора.
Таллий
Символ: Tl
Атомный вес: 204,38
Описание: Таллий — это токсичный мягкий металл.
Где используется: Таллий используется для производства легкоплавкого стекла. Когда-то его использовали как крысиный яд, но теперь его запрещено использовать в быту.
Свинец
Обозначение: Pb
Атомный вес: 207,2(1)
Описание: Свинец представляет собой металлическую плотную, некорродирующую, некорродирующую,
Где он используется: Многие ранее распространенные виды использования свинца теперь запрещены из-за его токсического воздействия. Он по-прежнему широко используется для автомобильных аккумуляторов, пигментов, боеприпасов, оболочки кабелей, свинцового хрусталя, радиационной защиты и некоторых припоев.
Висмут
Обозначение: Bi
Атомный вес: 208,98040(1)
Описание: Висмут представляет собой металл с низкой температурой плавления.
Где используется: Висмут обычно используется в пожарных извещателях и системах пожаротушения из-за его низкой температуры плавления. Это также привело к его использованию в электрических предохранителях.
Это также привело к его использованию в электрических предохранителях.
Полоний
Символ: Po
Атомный вес: [209]
Описание: Полоний является долгоживущим радиоактивным элементом.
Где используется: Полоний используется в качестве источника атомного тепла для краткосрочного использования. Это также видно в антистатических щетках и в пленке.
Астатин
Обозначение: At
Атомный вес: [210]
Описание: Астат является радиоактивным короткоживущим элементом.
Где используется: Астат используется в качестве радиоактивного индикатора и при лечении рака.
Радон
Обозначение: Rn
Атомный вес: [222]
Описание: Радон – это короткоживущий радиоактивный газ.
Где используется: Радон используется для лечения рака. Его часто производили в больницах, выкачивая радон из радия и затем запечатывая его в трубки.
Франций
Обозначение: Fr
Атомный вес: [223]
Описание: Франций является радиоактивным и короткоживущим элементом.
Где используется: Самый стабильный изотоп франция, франций-223, имеет период полураспада 22 минуты. Из-за короткого срока службы этот элемент не используется в коммерческих целях.
Радий
Символ: Ra
Атомный вес: [226]
Описание: Радий — долгоживущий радиоактивный элемент.
Где используется: Радий используется в качестве источника нейтронов, а также для производства радона. Один грамм радия-226 производит 0,0001 мл радона каждый день. Этот элемент в 1 000 000 раз активнее урана.
Актиний
Символ: Ac
Атомный вес: [227]
Описание: Актиний – это долгоживущий радиоактивный элемент.
Где используется: Актиний используется в медицине для радиоиммунотерапии. Он содержится только в урановой руде, что делает его очень дорогим. Одна тонна урана дает эквивалент 1/10 грамма актиния.
Торий
Обозначение: Th
Атомный вес: 232,0377(4)
Описание: Торий – это долгоживущий радиоактивный элемент.
Где используется: Торий используется для покрытия нитей в лампах накаливания. Его можно использовать в качестве ядерного топлива в ториевых реакторах, хотя это очень новая технология. Торий также является легирующим агентом магния, а оксид тория используется в качестве промышленного катализатора.
Протактиний
Символ: Па
Атомный вес: 231. 03588(2)
03588(2)
Описание: Протактиний – это долгоживущий радиоактивный элемент.
Где используется: В настоящее время протактиний не используется в коммерческих целях из-за его относительной редкости.
Уран
Обозначение: U
Атомный вес: 238,02891(3)
Описание: Уран является долгоживущим радиоактивным элементом.
Где используется: Уран используется в качестве ядерного топлива для ядерных энергетических реакторов и производит материал, необходимый для ядерного оружия. Он также используется в качестве красителя для стекла. Это также основной материал, из которого изготавливаются другие синтетические трансурановые элементы.
Нептуний
Обозначение: Np
Атомный вес: [237]
Описание: Нептуний – радиоактивный элемент-долгожитель.
Где используется: Нептуний не используется в коммерческих целях.
Плутоний
Символ: Pu
Атомный вес: [244]
Описание: Плутоний — долгоживущий радиоактивный элемент.
Где используется: Плутоний используется в качестве ядерного топлива и в ядерном оружии.
Америций
Символ: Am
Атомный вес: [243]
Описание: Америций — радиоактивный долгоживущий элемент.
Где используется: Америций используется в детекторах дыма и в качестве переносного источника гамма-излучения.
Кюрий
Символ: Cm
Атомный вес: [247]
Описание: Кюрий является долгоживущим радиоактивным элементом.
Где используется: Кюрий в основном используется для исследований, но в будущем он может производить больше ядерной энергии на грамм, чем плутоний.
Берклий
Обозначение: Bk
Атомный вес: [247]
Описание: Берклий — долго радиоактивный элемент.
Где используется: Berkelium не имеет коммерческого применения из-за своей редкости.
Калифорний
Символ: Cf
Атомный вес: [251]
Описание: Калифорний является долгоживущим элементом.
Где используется: Калифорний является сильным источником нейтронов. Используется в металлоискателях для серебра и золота. Его также можно использовать для обнаружения нефтяных слоев под землей и обнаружения усталости металла в аэрокосмических приложениях.
Эйнштейний
Обозначение: Es
Атомный вес: [252]
Описание: Эйнштейн является короткоживущим элементом.
Где используется: Не использовать вне исследований.
Фермий
Обозначение: Fm
Атомный вес: [257]
Описание: Фермий — короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Менделевий
Обозначение: Md
Атомный вес: [258]
Описание: Менделевий является короткоживущим элементом.
Где используется: Не используется вне исследований.
Nobelium
Символ: no
Атомный вес: [259]
Описание: Нобелия-это радиоактивный элемент, который является недолгим
, где он использовался: -это радиоактивный элемент, который используется на расстоянии
, где он использовался: -это радиоактивный элемент. .
.
Lawrencium
Символ: Lr
Атомный вес: [266]
Описание: Лоуренсий – это недолговечный радиоактивный элемент.
Где используется: Не используется вне исследований.
Резерфордий
Обозначение: Rf
Атомный вес: [267]
Описание: Резерфордий является короткоживущим радиоактивным элементом.
Где используется: Не используется вне исследований.
Дубний
Символ: Db
Атомный вес: [268]
Описание: Дубний — короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Сиборгий
Обозначение: Sg
Атомный вес: [269]
Описание: Сиборгий — короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Борий
Обозначение: Bh
Атомный вес: [270]
Описание: Борий является короткоживущим5 радиоактивным элементом4.
Где используется: Не используется вне исследований.
Хассий
Обозначение: Hs
Атомный вес: [277]
Описание: Хассий является короткорадиоактивным элементом.
Где используется: Не используется вне исследований.
Мейтнерий
Обозначение: Mt
Атомный вес: [278]
Описание: Мейтнерий — короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Darmstadtium
Обозначение: Ds
Атомный вес: [281]
Описание: Дармштадтий — это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Рентгений
Обозначение: Rg
Атомный вес: [282]
Описание: Рентген является короткоживущим элементом.
Где используется: Не используется вне исследований.
Копернициум
Обозначение: Cn
Атомный вес: [285]
Описание: Коперниций представляет собой радиоактивный элемент, который является короткоживущим.
Где используется: Не используется вне исследований.
Нигоний
Обозначение: Nh
Атомный вес: [286]
Описание: Нигоний — короткоактивный элемент.
Где используется: Не использовать вне исследований.
Флеровий
Обозначение: Fl
Атомный вес: [289]
Описание: Флеровий является короткорадиоактивным элементом.
Где используется: Не используется вне исследований.
Московий
Обозначение: Mc
Атомный вес: [290]
Описание: Московий 4
Где используется: Не используется вне исследований.
Ливерморий
Символ: Lv
Атомный вес: [293]
5 короткорадиоактивный элемент, который является ливермориоактивным.
Где используется: Не используется вне исследований.
Теннессин
Символ: Ts
Атомный вес: [294]
Описание: Теннессин — это короткоживущий радиоактивный элемент.
Где используется: Не используется вне исследований.
Оганесон
Обозначение: Og
Атомный вес: [294]
Описание: Оганесон — короткоживущий радиоактивный элемент. Это самый тяжелый элемент, известный человеку (на момент написания статьи).
Где используется: Не используется вне исследований.
More Stories
наука
Прорыв в долголетии: ученые открывают способ обратить старение в скелетных мышцах
Стивен Вичинанца| 20.09.2022
инновации
Безвоздушные шины, в которых используются технологии НАСА, могут положить конец проколам, сократить количество отходов и революционизировать отрасль
Крис Янг| 15.09.2022
транспорт
Первый в мире летающий велосипед может находиться в воздухе 40 минут
Лукия Пападопулос| 17.09.2022
Химические элементы таблицы Менделеева, отсортированные по символу
- Главная
- Периодическая таблица
- Элементы по символу
Элементы периодической таблицы, отсортированные по символу
клик по любому элементу 9003 название для дальнейших химических свойств, данных об окружающей среде или воздействии на здоровье.
Этот список содержит 118 химических элементов.
| The chemical elements of the periodic chart sorted by: | Symbol | Name chemical element | Atomic number | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Name alphabetically | Ac | Актиний | 89 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Атомный номер | Ag | 3150 Silver | 47 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Symbol | Al | Aluminum | 13 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Atomic Mass | Am | Americium | 95 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – электроотрицательность | Ar | аргон | 18 | As | Arsenic | 33 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Melting point | At | Astatine | 85 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Boiling point | Au | Золото | 79 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Вандерваальсов радиус | Ba | 5 Барий3154| 56 | | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Year of discovery | B | Boron | 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Inventor surname | Be | Beryllium | 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Элементы в земной коре | Bh | Борий | 107 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bi | Bismuth | 83 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Covalenz radius | Bk | Berkelium | 97 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| – Ionization energy | Br | Бром | 35 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Для студентов и преподавателей химии: Таблица справа выделена символом . Первым химическим элементом является актиний, а последним – цирконий. Обратите внимание, что элементы не показывают своего естественного отношения друг к другу, как в периодической системе. Там вы можете найти металлы, полупроводники, неметаллы, инертный благородный газ (ы), галогены, лантаноиды, актиноиды (редкоземельные элементы) и переходные металлы. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Са | Кальций | 20 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cd | Cadmium | 48 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C | Carbon | 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ce | Cerium | 58 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cf | Калифорния | 98 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cl | Хлор | 19 314 50 9314 0034 Cn | Copernicium | 112 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cm | Curium | 96 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Co | Cobalt | 27 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cr | Хром | 24 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cs | Цезий | 55 9317 1 9147 1 | 0034 CuCopper | 29 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ds | Darmstadtium | 110 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Db | Dubnium | 105 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dy | Диспрозий | 66 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Er | Эрбий | 68 | Einsteinium | 99 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eu | Europium | 63 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fm | Fermium | 100 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fl | Flerovium | 114 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| F | Фтор | 9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Iron | 26 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fr | Francium | 87 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ga | Gallium | 31 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gd | Gadolinium | 64 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ge | Германий | 32 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | |||||||
| He | Helium | 2 | |||||
| Hg | Mercury | 80 | |||||
| Hf | Hafnium H | 72 | |||||
| Ho | Гольмий | 67 | Hassium | 108 | |||
| I | Iodine | 53 | |||||
| In | Indium | 49 | |||||
| Ir | Иридий | 77 | |||||
| К | Калий | 4 19 | Kr | Krypton | 36 | ||
| La | Lanthanum | 57 | |||||
| Li | Lithium | 3 | |||||
| Lr | Лоуренсиум | 103 | |||||
| Lv | Ливермориум 3154 | 116 | |||||
| Lu | Lutetium | 71 | |||||
| Md | Mendelevium | 101 | |||||
| Mg | Magnesium | 12 | |||||
| Mn | Марганец | 25 | |||||
Mt3154 | Meitnerium | 109 | |||||
| Mo | Molybdenum | 42 | |||||
| Mc | Moscovium | 115 | |||||
| N | Азот | 7 | |||||
| Na | Натрий | 11 | 11Nb | Niobium | 41 | ||
| Nd | Neodymium | 60 | |||||
| Ne | Neon | 10 | |||||
| Ni | Никель | 28 | |||||
| Nh | Нигоний 5 113 | | |||||
| No | Nobelium | 102 | |||||
| Np | Neptunium | 93 | |||||
| O | Oxygen | 8 | |||||
| Ог | Оганессонм | 118 | |||||
| 53 Ос0034 Osmium | 76 | ||||||
| Pb | Lead | 82 | |||||
| P | Phosphorus | 15 | |||||
| Pa | Protactinium | 91 | |||||
| Pd | Палладий | 46 | 1 30034 Po | Polonium | 84 | ||
| Pr | Praseodymium | 59 | |||||
| Pm | Promethium | 61 | |||||
| Pt | Платина | 78 | |||||
| Пу | Плутоний | 4 94 | |||||
| Ra | Radium | 88 | |||||
| Rb | Rubidium | 37 | |||||
| Re | Rhenium | 75 | |||||
| Rf | Резерфордий | 104 | |||||
| 34 Rg | 5 Roentgenium111 | ||||||
| Rh | Rhodium | 45 | |||||
| Rn | Radon | 86 | |||||
| Ru | Ruthenium | 44 | |||||
| S | Сера | 16 | Antimony | 51 | |||
| Sc | Scandium | 21 | |||||
| Sm | Samarium | 62 | |||||
| Sg | Сиборгиум | 106 | |||||
| Se | Селен | 43154 | |||||
| Si | Silicon | 14 | |||||
| Sn | Tin | 50 | |||||
| Sr | Strontium | 38 | |||||
| Ta | Тантал | 73 | |||||
| Tb | 035 | 65 | |||||
| Tc | Technetium | 43 | |||||
| Te | Tellurium | 52 | |||||
| Th | Thorium | 90 | |||||
| Тс | Теннессин | 117 | |||||
| Тл0035 | Thallium | 81 | |||||
| Ti | Titanium | 22 | |||||
| Tm | Thulium | 69 | |||||
| W | Вольфрам | 74 | |||||
| Уран | Уран | 94 3145V | Vanadium | 23 | |||
| Xe | Xenon | 54 | |||||
| Y | Yttrium | 39 | |||||
| Yb | Иттербий | 70 | |||||
| Zn | 30 915 3 Цинк 54 | ||||||
| Zr | Zirconium | 40 | |||||
Click here: for a schematic overview of the periodic table of elements in chart form
Вам нужно знать вес некоторых молекул? Попробуйте наш калькулятор молекулярного веса!
Пожалуйста, сообщайте о любой случайной ошибке в приведенной выше статистике по химическим элементам.
Проект злоупотребления периодической таблицей
Вот текущий проект, в рамках которого я намерен каталогизировать злоупотребление периодической таблицей. Пожалуйста, добавьте в проект The Periodic Table Abuse Project, предупредив меня о злоупотреблениях!
Периодическая таблица — красивая, упорядоченная, организованная вещь, и, хотя споры о некоторых ее аспектах продолжают бушевать, основная привлекательность таблицы остается вне времени.
Итак, почему люди так часто ругают стол?
С одной стороны у нас есть « Периодическая таблица… “ , злоупотребление. Эти «таблицы» — это те, которые собирают связанные фрагменты данных, а затем «организуют» их в форме периодической таблицы. Самая большая проблема здесь заключается в том, что данные расположены не в духе оригинала или не согласуются с ним. Например, когда нет очевидной связи между фрагментами информации, которые появляются в каждом столбце и каждой строке, периодическая таблица является «злоупотреблением». Одним из таких примеров является Периодическая таблица текстовых сообщений, которая представляет собой не что иное, как алфавитное расположение текстовых терминов. Возможно, менее вопиющим примером является Периодическая таблица пива, которая, по крайней мере, группирует связанные стили пива в столбцах.
Одним из таких примеров является Периодическая таблица текстовых сообщений, которая представляет собой не что иное, как алфавитное расположение текстовых терминов. Возможно, менее вопиющим примером является Периодическая таблица пива, которая, по крайней мере, группирует связанные стили пива в столбцах.
Как правило, я , а не собираю здесь ‘ Периодическая таблица… ‘ примеров, отчасти потому, что это уже было сделано раньше, но главным образом потому, что я ищу более конкретное злоупотребление, чем просто использование таблицы в качестве шаблон для организации. Сказав это, я, безусловно, буду рассматривать такие таблицы с точки зрения злоупотребления символами, но я не буду рассматривать их, если они не злоупотребляют такими символами, как Периодическая таблица слонов. Это тонкая грань, и я ожидаю, что иногда буду непоследовательным — потерпите меня!
Со временем и по мере того, как я буду собирать больше примеров, я думаю, что злоупотребления нужно будет организовать в подкатегории и, вероятно, отображать иначе, чем я ниже. Я уже думаю о нескольких названиях для подкатегорий злоупотреблений, таких как; злоупотребление символами, злоупотребление атомными номерами, злоупотребление массовыми числами, организационные злоупотребления, опечатки и т. д. Во всяком случае, на данный момент, вот что у нас есть.
Я уже думаю о нескольких названиях для подкатегорий злоупотреблений, таких как; злоупотребление символами, злоупотребление атомными номерами, злоупотребление массовыми числами, организационные злоупотребления, опечатки и т. д. Во всяком случае, на данный момент, вот что у нас есть.
Кафе-мороженое Subzero в Индианаполисе изобретает элемент и ошибается в атомных числах. С кальцием в моем мороженом я могу справиться (и ожидать), но с большой дозой кобальта тоже? Спасибо, не надо. Спасибо Джозефу Варго за ролик.
|
Ртуть на куриных крылышках? Buffalo Wild Wings считает, что это отличная идея! Честно? Я менее уверен. @compoundchem указывает на это.
|
Не довольствуясь использованием только ртути для отравления, Buffalo Wild Wings предлагает дополнительные элементы! Другой от @compoundchem.
|
Нижний регистр? Верхний регистр? Какая разница? Считает ли гелий, что он более важен, чем остальные элементы? Спасибо @TeacherChemist за это, который также сообщает об исправлении.
|
| @WPIBurdette систематически уничтожает вирусную периодическую таблицу. Похоже, ЛСД повлиял не только на внешний вид этой таблицы. Щелкните здесь, чтобы получить полную информацию об удалении. |
@_razza указывает, что ее кружка с периодической таблицей нуждается в небольшом уходе за опечатками. Это лучше, чем иметь таллий на внутри !
|
We Love Jelly похоже, что они немного перестарались с коктейлями. Это НЕ МОЖЕТ закончиться хорошо. Больше новых элементов? Я так не думаю, хотя ‘ Pornstar Martini ’ — это интересный взгляд на Прометий! Спасибо @sbrattonuk за публикацию. Это НЕ МОЖЕТ закончиться хорошо. Больше новых элементов? Я так не думаю, хотя ‘ Pornstar Martini ’ — это интересный взгляд на Прометий! Спасибо @sbrattonuk за публикацию. |
Часть 1 лаборатории кофейных коктейлей в любом случае вызовет у вас головную боль! Если вам все равно, я не буду употреблять церий в своем кофе, большое спасибо, и вам лучше выпить этот напиток с мейтнерием побыстрее, так как период полувыведения довольно короткий. Спасибо @KazMitch за предупреждение из двух частей.
|
Вот вторая часть невероятной кофейной смеси от @KazMitch. Одна проблема здесь заключается в том, что Cc означает две разные вещи… эээ…. ну и еще куча всего. По крайней мере, в этом молочном капучино много кальция, но я пропущу хлорированный кофе, радиоактивные напитки с америцием или курием, и эйнштейний с моим кофеином кажется мне немного рискованным.
|
Нужно быть довольно наглым, чтобы звать Королевский институт… особенно, если учесть перечисленные ниже злоупотребления! Но, по крайней мере, я в хорошей компании!
|
| Упс! Немного близко к дому, на мой вкус! Моя защита? Их предложили веб-дизайнеры, и они мне понравились. Ирония, капает. Моя вина. |
| Там должно быть ТОННА пародий на сериал «Во все тяжкие». Это для телешоу/фильма/телефильма «Доктор Куинн, знахарка », прославленного актрисой Джейн Сеймур. Как ни странно, я чувствую, что на самом деле должно быть элементов с символами Dr и Qu, даже если им не разрешено принимать атомные и массовые числа Br и Ba. |
Чудо науки Гриль-бар в Массачусетсе действительно должен знать лучше! Спасибо NomNomDePlume на Reddit за это дополнение. Есть целая куча вещей, которые я не хочу на шпажках, бутербродах или чем-то еще. Кстати, что там с двухатомным ванадием, бором и углеродом?? Фото Кредит. Есть целая куча вещей, которые я не хочу на шпажках, бутербродах или чем-то еще. Кстати, что там с двухатомным ванадием, бором и углеродом?? Фото Кредит. |
| Музей науки и промышленности в Чикаго производит тербий — упс! (по состоянию на 16.04.15). Спасибо @JennyE_OHare за вклад. |
| Эти магниты от Target просто, эээ…. пропустите цель! Спасибо Шери Ферби за внимание к ним. |
| Честно говоря, я знаю, что такие вещи случаются, но это ужасно для обложки учебника по химии. Спасибо Кейси Джиллетт за ролик. |
Мэтью Кеннеди предупреждает меня о некоторых серьезных нарушениях в отношении символов, формы и вставки значков со стороны JCC в Колумбусе, штат Огайо. Ой! Ой! |
| Ребята из МОЛЕКУЛ-Р творят всякие гадости во имя Молекулярной Гастрономии – что бы ЭТО ни было! (Нет, я тоже никогда не слышал об этом). Вы тоже можете испытать гелеобразование , сферификацию , эмульгирование и « другие трансформации »! |
| Люди из МОЛЕКУЛ-Р расширяют символы, добавляя букву «Т» для инструментов — достаточно сказано! |
| Больше чепухи про Уолтера Уайта, на этот раз от HQ Wallpapers. «Во» — это элемент? Кто скажет ИЮПАК и/или Калифорнии? |
Это опасно близко к « Периодической таблице… », которую я НЕ документирую здесь, но злоупотребление символами просто вынуждает меня включить ее. |
| Спасибо Брэндону Бойду за вызов Veritasium — они утверждают, что знают лучше! «Элемент истины»? Нет, все ложь! |
| Обнаружение этого старого каштана было лишь вопросом времени, и нам не пришлось долго ждать благодаря твиттеру Каплана о подготовке к MCAT. О, как я ненавидел это много лет. |
| @altotus (и его отец) держат меня в курсе событий во Флориде в ресторане Toasted в Винтер-парке. Еще один, который близок к ‘ The Periodic Table of… ’ (которую я стараюсь не документировать здесь), это связано со злоупотреблением символами. Надеюсь, что их бутерброды лучше, чем их уважение к таблице Менделеева! |
Ужас из ужасов, теперь в дело вступает Американский химический совет. Когда закончится безумие? Когда закончится безумие? |
| Возможно, вы помните это из относительно недавней рекламной кампании Dow TV. Спасибо @chris_sy за напоминание. |
| Да, вы можете купить эту китайскую кружку для еды на zazzle.com. Пожалуйста, проявите уважение и не делайте этого. Хотя я полагаю, что есть жареный рис лучше, чем потреблять Francium! |
| Опять же, если честно, если выбирать между миской, полной кюриума, или миской, полной чау-мейн, я выбираю вариант с глутаматом натрия. |
Возможно, вы знаете книгу Science Ink , написанную Карлом Циммером (еще одна книга, которую я хотел бы написать), в которой перечислены татуировки, основанные на науке. Я не уверен, есть ли это в той книге, но злоупотребление символами заставляет меня съеживаться почти так же сильно, как игла! Кстати, эта нижняя молекула выглядит так, как будто это дофамин, но я думаю, что они упустили двойную связь. Я не уверен, есть ли это в той книге, но злоупотребление символами заставляет меня съеживаться почти так же сильно, как игла! Кстати, эта нижняя молекула выглядит так, как будто это дофамин, но я думаю, что они упустили двойную связь. |
| Что меня больше раздражает: назидательный бред 21-го века или злоупотребление символами? Галстук — это тупо в квадрате. Спасибо @dprindle за предупреждение. |
| О, смотри, ненаука похищает НАСТОЯЩУЮ науку – обычное дело в причудливом мире образования. Спасибо @TheOtherDrX за бдительность в мире образования. |
| Как и я, Билл Най злоупотребляет столом, но почему-то я чувствую, что он нравится людям, и я должен получить пропуск! Еще раз спасибо @TheOtherDrX. |
Еще больше чепухи из «Во все тяжкие» — держу пари, из этого конкретного источника будет еще НАМНОГО больше! Спасибо Скотту Энглеру за это. |
| Да, это «Периодическая таблица … » (которую я стараюсь не документировать), но опять же, это действительно должно быть связано со злоупотреблением символами. Спасибо, Пенни. |
| Это злоупотребление? Не уверен, но пока коробка «LuNCH» Крисси Брамер входит в проект злоупотреблений. Может быть, один для обзора? |
| Чрезмерное злоупотребление символами квалифицируется как « Периодическая таблица победителей Тур де Франс ». На шестипенсовике начинает злоупотреблять и едва знает, когда остановиться, и я просто задокументирую здесь три из них. Честно говоря, некоторые принты действительно весьма привлекательны. |
Больше злоупотреблений на велосипеде, на этот раз из итальянской версии «Le Tour» для второго, На входе по шестипенсовику . |
| И, наконец, третья версия велосипедного безумия, подытоживающая испанскую гонку. |
| Организация учителей химии Юго-Восточного Мичигана составляет элемент! Мммммм….. |
| Еще странные кружки. Не уверен, где это оставляет водород и гелий, или даже Ekaaluminium! |
| Хотя Эмпедокл мог бы одобрить это, я не уверен, откуда он берет свои атомные веса. |
Я думал, что символом воды является ▽, но, похоже, ИЮПАК изменил ситуацию! Если вы не знакомы с фильмом «Пятый элемент » и персонажем Лилу (как и я), то каламбур для вас потерян. Теперь я образован в таких вопросах. Спасибо, Дэн! Спасибо, Дэн! |
| Меньше о злоупотреблениях и больше о некоторых вольностях. Scandium = «Научный центр» Университета Дрекселя на 34-й улице и рынке в Филадельфии. |
| Согласно городскому словарю, нинтендиум — это «самый прочный и долговечный материал, известный человечеству, обнаруженный нинтендо для использования в своей консоли Nintendo Entertainment System». Другие источники говорят нам, что это 133-й элемент и он имеет символ Nn! Не стесняйтесь полностью игнорировать оба. Спасибо @CCanfield100 за ролик. |
| Еще один файл под заголовком «они должны знать лучше», Тринити-колледж искусств и наук в Дьюке делает грязные дела с На и Се и создает два новых «элемента». Спасибо @cjt217 за ролик. |
ATOMAS от Max Gittel отменяет интересную работу с неприятным символом для Br. (Кстати, я до сих пор не понимаю игру). (Кстати, я до сих пор не понимаю игру). |
| Сегодня (5 июня) национальный день пончиков, поэтому я предлагаю отпраздновать это, никогда не делая этого. Спасибо @overheardinchem. |
| Ну, это воняет! Спасибо @bhgross144 за эту огромную кучу сплошных оскорблений! |
| Честно говоря, я ненавижу это. Все бензол и группы разрушены. Издевательства высшей степени! |
| Значит, вас беспокоили сульфиты и прочие «химии» в вине? Как насчет нескольких кусочков цезия? Charles Smith Wines предлагает металл группы 1 в качестве дополнения к вашему доступному Cab Sav! |
Не удовлетворившись Cs, Чарльз Смит продолжает предлагать ваш рений и пару новых элементов. |
| Я отнесу это к категории «злоупотребление служебным положением» @CHI_Healthtech. Думаю, это для вас «Учёные жизни»! |
| Нет, @MaddChemistry, вы не можете злоупотреблять символами и именами таким образом, даже во имя #GaGa. |
| @scburdet указывает на эту раздражающую поздравительную открытку ко Дню святого Валентина. Отягчающие? Да, потому что все шло хорошо до «М» (ну это и то, что там делают 2, 3, 5 и 2). |
| Bodybuilding.com использует старый прием, ссылаясь на периодическую таблицу (или, по крайней мере, на ее внешний вид), чтобы придать больше научного доверия продукту. Спасибо @Meachteach за место. |
«Слияние элементов»? Это трансфермиевая ручка? Как отмечает @flugrol, это действительно «идеальный шторм злоупотребления элементами и маркетинговой чуши». Предоставлено нам @scburdet. Предоставлено нам @scburdet. |
| @scburdet снова заметил злоупотребление острым соусом. Конечно, Ca будет полной противоположностью острому соусу, верно? Верно? |
| Связь с Джеки Робинсон на @nightlyshow? Спрашивает, @scburdet. В любом случае, куда, черт возьми, делся молибден? |
| Эээ… на самом деле нет, Барракуда, у тебя есть все НЕПРАВИЛЬНО элементов. Спасибо @overheardinchem за место в международном аэропорту Рино-Тахо. |
| Честно говоря, сладкое научное мороженое, это не «сладкое» и не «научное». |
Ред. «гуру», Томас К. Мюррей злоупотребляет технецием. Или это углерод, или есть новые элементы? Неа. Мюррей злоупотребляет технецием. Или это углерод, или есть новые элементы? Неа. |
| Wehrd науке лучше знать! |
| Нет, нет, нет Химической Арены, времена года не стихия! |
| Muscle Elements пытается связать «науку» со своим продуктом через название и символику — предположительно. |
| Это действительно очень «непослушно», например, «непослушно не быть элементом». На. Спасибо @vancew за место |
| Вот еще ерунда про йогурт, на этот раз от Yogurt Lab в Миннесоте. Спасибо @MeachTeach за место. |
Злоупотребление секвенированием и дублированием со стороны Dow (снова) и Accenture. Ту ту. Спасибо @chembones за ролик. Ту ту. Спасибо @chembones за ролик. |
| Случайный алфавит появляется на этой футболке, по-видимому, перечисляя соответствующие штрафы Roller Derby – да, это тоже ничего не значит для меня. |
| Натан из Массачусетса вывешивает оскорбления спереди и по центру груди на выставке ChemEd 2015. |
| Скотт Энглер идет за пиццей в Pie Five и очень разочарован. Однако ни слова о том, какой была пицца. |
| Рубашки «Да, ботан», в них нет элемента ниндзя, но все равно спасибо. |
Да, не в восторге от этого по множеству причин. но я думаю, что это очень хорошо подходит для «нарушения последовательности». Только не носите это в классе. ХОРОШО? Только не носите это в классе. ХОРОШО? |
| Тяжелые металлы? Злоупотребление последовательностью, или железо действительно тяжелый металл? Думаю, нет. В любом случае, я бы сказал, что это злоупотребление футболками Bd Idea. Спасибо Рою Ловеллу за ролик. |
| Боб Уорли видит немного больше злоупотреблений последовательностью и предполагает, что некоторых людей могут беспокоить другие аспекты этого — меня нет. |
| Даремское научное кафе добавляет в периодическую таблицу несколько ложных элементов. Ди и Ле дебютируют! |
Tide повторно окрестить кобальтом и ртутью в интересах порки стирального порошка. Спасибо доктору Мишель за место. |
| Послушайте, у вас действительно не может быть никакой «таблицы Менделеева» до середины-конца 19-го века. Спасибо @scburdet за указание на глупость цыплят Дуга Сэвиджа! |
| Извините, но на диаграмме Венна действительно нет взаимосвязи между аббревиатурами состояний в верхнем регистре и символами элементов. Любимая мозоль @Andrew_Taylor |
| Люди в @UnQuarkedWine изо всех сил злоупотребляют символами и таблицей в целом. Гррр… |
| И так далее. Двойной гррр… |
По-видимому, перекись водорода имеет формулу «HP» в калифорнийских супермаркетах. Спасибо @ramusallam за место. Спасибо @ramusallam за место. |
| Бен Дикман предупреждает меня о злоупотреблении символами, ужас из ужасов, во имя «науки»! Кстати, что такое элемент «е»? |
| Сезонное, последовательность злоупотреблений. Во всем виноват Сайнфелд. |
Еще одно злоупотребление последовательностью, даже если оно сделано по уважительной причине, на этот раз от @AgilentChem. Не уверен, что хочу эти элементы в своем вине! Не уверен, что хочу эти элементы в своем вине! |
Вы знаете, что что-то не так, когда ЧЕТЫРЕ разных человека предупреждают вас о злоупотреблениях, И каждый из этих людей прокомментирует мою потенциальную крайнюю неприязнь к edubabble в сочетании с злоупотреблением периодической таблицей! Не то чтобы мне не нравился Эд. Технология как таковая, на самом деле, наоборот, заключается в том, что я презираю ее использование в качестве троянского коня для внедрения назидательной чуши и ошибочных педагогических концепций. Как я НЕНАВИЖУ это двойное насилие! Спасибо, что решили убить меня, @cgchemK, @S_J_Lancaster, @altotus и @Media_Barber! |
| Спасибо Фиби Лю за то, что она помогла мне разобраться с символами и надругательствами над столом, вдохновленными Minecraft. |
Спасибо @scburdet за то, что продолжаете оскорблять. На этот раз @is_chris находит ПРОТИВНУЮ кофейную чашку. Я бы не доверял содержимому! На этот раз @is_chris находит ПРОТИВНУЮ кофейную чашку. Я бы не доверял содержимому! |
| Еще от всегда бдительного @scburdet и еще от кухни. На этот раз он следит за @jeremymberg и его дурацкой медно-куминовой чушью. |
| Извиняюсь, но я забыл, кто меня предупредил об этой неэлементарной ерунде. Соответственно, я действительно понятия не имею, о чем идет речь (кроме того факта, что насилие свирепствует). Знаю, что это из The Atlantic 1999 года, но я правда вообще в этом не разбираюсь. |
| Да, научный лагерь Cougar, здесь слишком много математики, физики и уравнений для периодической таблицы. Извините, мне не нравится. Спасибо @pchemstud. |
Судя по всему, существует «официальная периодическая таблица Майнкрафт». Эррр, нет! Спасибо Лойс Бергин за то, что передала мне этого маленького обидчика. Эррр, нет! Спасибо Лойс Бергин за то, что передала мне этого маленького обидчика. |
| Запутался? Да, я скажу, что ты. |
| No Brewing Technologies, нет такого элемента, как нержавеющий, а если бы он был, то он, наверное, назывался бы хромом! |
| Да ладно, IU, давайте не будем злоупотреблять жизненной силой того, что мы делаем! Разве злоупотребление средней атомной массой не должно сопровождаться злоупотреблением атомным номером? |
| Спасибо @MonashMONster за это вкусное, но вопиющее, полное оскорблений. |
Мои карандаши были бы несчастливы, если бы их разместили здесь. |
| Старое, старое, старое оскорбление, на этот раз переделанное (из «элемента неожиданности») Чеггом. Зевать. |
| Точно так же, как STEAM является вымышленным, выдуманным маркетинговым инструментом, так и логотип BK Consulting. Идеальная синергия, как сказали бы в мире консалтинга! |
| Как и IU, BU делает все грязное. |
| Лучше бы эти картинки были недостающими элементами! Мне они не кажутся. |
Несмотря на то, что обычно я стараюсь избегать искажений, связанных с « Периодическая таблица… », одни символы на этом листе вызывают у меня изжогу. Спасибо Шерри Линн Макгрегор. Спасибо Шерри Линн Макгрегор. |
| О Боже, теперь за дело взялись канадцы. Еще раз спасибо Шерри Линн МакГрегор. |
| Вот это мне ОЧЕНЬ не нравится. В нем ругань Периодической таблицы сочетается с одной из моих любимых ненавистей — приторно-сладкой утопической подачей работы преподавателя. ОТВРАТ! А что вообще происходит с номером 3?? |
| Есть идеи, какое отношение имеют 94 и 63? Пу, Эу? |
| Я должен признать, что @onasixpence проделывает прекрасную работу, и это представляет для меня особый интерес, но, тем не менее, это больше злоупотребление! |
Брэндон Бойд обращает мое внимание на злоупотребление символами. |
| В этом так много неправильного, что сложно понять, с чего начать, если честно. Спасибо Мэтту за место. |
| Спасибо Ивану Апрахамяну (и другим) за то, что они заметили этот чушь от людей из Cole Haan. |
| Старый анекдот. Я могу принять ругань Na, но не бред про Бэтмена. Как по мне, слишком “Теория большого взрыва”. Не фанат супергероев/комиксов, и это не поднимает мне настроения. |
| Трудно понять, с чего начать, но достаточно сказать, что это настоящий хулиган! Спасибо @cjt217 за наводку. |
Неправильно, неправильно и еще раз неправильно, доктор Пеппер. Ванадий в моей газировке? Ванадий в моей газировке? |
| Я не большой поклонник Джона Оливера (просто не нахожу его особенно забавным), а к мистеру Лохте я отношусь еще меньше, поэтому, когда пловец продолжает получать прессу за то, что он придурок, а Оливер злоупотребляет столом , Я несчастлив. Спасибо Кристиану Кэнфилду за предупреждение. |
| Да уж, “вкусовой лаборатории” лучше избегать! Позовите Тая Уоллинга на место. |
| Старая проблема, немного новый контекст, все еще раздражает. |
Time Out разрушает Периодическую таблицу всеми способами, которые я могу себе представить. С чего начать? Я даже не могу понять этого безумного отсутствия логики. Спасибо @BenningtonChem за освещение страданий. |
| Целый ДРУГОЙ набор из основных элементов? Спасибо @paulcoxon за понимание! |
Обычно я избегаю злоупотреблений « Периодическая таблица… », но злоупотребление символами здесь настолько распространено, что я действительно должен включить его. @magicmolly и @teddyblanks создают еще больший беспорядок, чем сам мусор на улицах Нью-Йорка. Это действительно «мусор». Спасибо нескольким людям, которые указали на это, включая @reneewebs. |
| Old Navy нанесет на футболку ВСЕ, что угодно, включая злоупотребление галогенами! Спасибо @hawkwing12 за модную оплошность. |
Uncommongoods.com производит миксологический набор, который, безусловно, имеет свою привлекательность, однако он просто неправильный. |
| Хотя я одобряю то, что они означают, я решительно не одобряю злоупотребления. |
| Кристиан Кэнфилд предупреждает меня о злоупотреблении символами. Это химическая формула кокоса? 😉 |
| Быть милым? Конечно, но как насчет того, чтобы быть правым? |
Нравится периодическая таблица? Спасибо женщинам-ученым
Обсуждение периодической таблицы элементов часто заканчивается простым упоминанием Дмитрия Менделеева, русского химика, сформулировавшего Периодический закон и использовавшего его для исправления свойств некоторых уже открытых элементов, не говоря уже о предсказании свойств восьми элементов, которые еще предстоит открыть.
Но вместо того, чтобы быть основой, это была бы просто причудливая статья в горном журнале. на этом его развитие закончилось. Менделеев был назначен ему профессором общей химии в 1867 году и должен был читать лекции по неорганической химии. Не имея хорошего русского учебника, он решил написать его, а для этого требовалось правильно расположить химические элементы, что ускользало от других ученых.
на этом его развитие закончилось. Менделеев был назначен ему профессором общей химии в 1867 году и должен был читать лекции по неорганической химии. Не имея хорошего русского учебника, он решил написать его, а для этого требовалось правильно расположить химические элементы, что ускользало от других ученых.
Так началась история таблицы Менделеева в том виде, в каком мы ее знаем, но на этом пути она получила много помощи.
Все слышали о Марии Кюри , потому что она получила две Нобелевские премии за исследования радиоактивности и открытие полония и радия в 1898 году. неидентифицируемый осадок. Позже выяснилось, что этот остаток состоит из двух новых элементов: самария и гадолиния.
Авторы и права: Science Photo Library
Другая менее известная женщина — австрийский шведский физик-ядерщик.0034 Лиза Мейтнер . Она и ее коллега Отто Ган впервые доказали открытие элемента 91, протактиния, в 1917-1918 гг. Во время их исследовательской работы в Институте химии им. Кайзера-Вильгельма в Берлине она была вынуждена работать в подвале, потому что женщин не должны были видеть.
Кайзера-Вильгельма в Берлине она была вынуждена работать в подвале, потому что женщин не должны были видеть.
В 1925 году немецкая пара Ида и Вальтер Ноддак совместно открыли элемент 75, рений. Элемент, названный в честь реки Рейн, является одним из самых редких веществ на земле. Пара также считала, что они нашли элемент, который они назвали масарием, но им так и не удалось воспроизвести и изолировать его. В отличие от Марии Кюри, которая получила признание за свои открытия сама по себе, Ида Ноддак всю свою жизнь работала гостем в лаборатории своего мужа, потому что в Германии замужним женщинам запрещалось иметь оплачиваемую работу.
В 1934 году физик Энрико Ферми из Римского университета объявил, что он и его коллеги открыли элементы 93 и 94, обстреляв уран нейтронами. Ида указал в журнальной статье в Angewandte Chemie, что Ферми не удалось доказать, что новые элементы были получены. «Возможно, что ядро распадается на несколько больших фрагментов, — сказала она, —
процесс, который мы сейчас называем делением. В 1938 году Мейтнер и Ган обнаружили, что одним из веществ, полученных Ферми, был барий, элемент, известный более ста лет, и что ядро урана действительно расщепилось, как указал Ноддак.
В 1938 году Мейтнер и Ган обнаружили, что одним из веществ, полученных Ферми, был барий, элемент, известный более ста лет, и что ядро урана действительно расщепилось, как указал Ноддак.
Мейтнер, еврейка, была вынуждена бежать в Швецию во время Второй мировой войны, но когда Ган получил Нобелевскую премию по химии в 1945 году, Мейтнер даже не была признана. Ее имя также не фигурировало в публикации, вышедшей в 1939 году, хотя она и пришла к результату.
В 1939 году французский физик Маргарита Перей открыла франций, последний природный элемент, который можно было извлечь из минералов.
В 1980-х годах американский химик Дарлин Хоффман стала первой женщиной в США, возглавившей исследовательскую группу, занимавшуюся производством и изучением сверхтяжелых элементов, веществ с атомным номером больше 100. Одна из ее коллег, Дон Шонесси , сейчас ведет исследование группа, которая участвовала в открытии шести таких сверхтяжелых элементов с атомными номерами от 113 до 118.
Когда в конце XIX века была открыта радиоактивность, был обнаружен целый ряд новых веществ, гораздо больше, чем было место для в периодической системе. Британский радиохимик Фредерик Содди развил идею о том, что несколько элементов могут иметь одинаковую атомную массу, но именно польский химик Стефани Горовиц , которая представила экспериментальные доказательства существования изотопов. Кроме того, шотландский врач Маргарет Тодд предложила термин «изотоп», что в переводе с греческого означает «то же самое место». Они занимали одно и то же место в периодической таблице и были вариантами одного и того же элемента. Позже к открытию новых изотопов были привлечены многие женщины, например, Берта Карлик и ее помощница Трауде Бернерт в Вене, доказавшие открытие стабильных изотопов астата в 1919 году.43.
Gertrud Woker в Швейцарии и Alice Hamilton в США предоставили информацию об опасности отравления свинцом в начале 1900-х годов.
Ряд женщин также внесли свой вклад в правильное размещение элементов в периодической таблице. Русский ученый Юлия Лермонтова работала над разделением металлов платиновой группы (рутения, родия, палладия, осмия, иридия и платины) еще в 1870-х годах, вскоре после того, как Менделеев представил свою первую версию периодической таблицы.
Периодическая система явно создана не одним человеком, как об этом часто говорят популярные представления. Над системой многих элементов и их изотопов бок о бок с мужчинами работали многие женщины на всех уровнях.
Поздравляем со 150-летием периодической таблицы и поздравляем всех мужчин и женщин, которые сделали это возможным.
Шаблон периодической таблицы | Бесплатно редактируемый пример
Научитесь отличать углерод от кобальта с помощью этой интерактивной таблицы Менделеева — одного из многих образовательных инструментов от семьи FigJam.
Попробуйте FigJam бесплатно
Шаблон периодической таблицы
Станьте похожим на валентный электрон и объединитесь с другими в этом шаблоне периодической таблицы элементов.
Начать диаграмму
Откройте для себя стандарт Au для виртуальных периодических таблиц
Потратьте время на навигацию по периодической таблице, чтобы изучить группы, запомнить символы, свойства элементов или даже узнать, что такое атомный номер, и понять, почему Менделеев расположил элементы как он сделал.
Подбор при позиционировании: Используйте интерактивные изображения, чтобы понять, как отдельные элементы классифицируются по химическим свойствам.
Систематическое изучение: Опирайтесь на структуру периодической таблицы элементов, чтобы направлять свои исследования (или ваших учеников).
Расчет соединений: Предсказать тип соединения двух элементов, изучив положение каждого элемента на столе по отношению к их сходным свойствам.
Начало работы
FigJam
Свяжись со своими лучшими друзьями Изучайте периодическую таблицу вместе в виртуальном пространстве и наблюдайте за реальными результатами, которые помогут решить химические задачи, понять различные группы или понять отдельные элементы. Когда вы переключаетесь на доску FigJam, каждый может подключиться через Lil’ Notes и Anonymous Thoughts и внести свой уникальный вклад в вещи с помощью Emoji, штампов, цветных маркеров и многого другого. Сотрудничество? Все дело в химии.
Когда вы переключаетесь на доску FigJam, каждый может подключиться через Lil’ Notes и Anonymous Thoughts и внести свой уникальный вклад в вещи с помощью Emoji, штампов, цветных маркеров и многого другого. Сотрудничество? Все дело в химии.
Начало построения диаграммы
Найдите растворы для исследований от Al до Zn
Покорите химию, как ученый, с интерактивной, удобной для чтения периодической таблицей. Затем обратите внимание на все остальные темы с помощью дополнительных инструментов и руководств от нашего сообщества.
Часто задаваемые вопросы
Самый простой способ создать виртуальную периодическую таблицу — начать с шаблона от FigJam. Периодические таблицы состоят из 118 специально расположенных ячеек, каждая из которых заполнена точными числами и символами, поэтому лучше всего начинать с полностью проверенного готового продукта. Оттуда вы можете настроить его по своему усмотрению.
Если вы изо всех сил пытаетесь усвоить урок химии, вы можете попробовать превратить учебное время в игровое. Как так? Сделайте периодическую таблицу интерактивной. Вот несколько забавных занятий и конкурсов:
Как так? Сделайте периодическую таблицу интерактивной. Вот несколько забавных занятий и конкурсов:
– Поиск элементов
– Игра в составление слов из символов элементов
– Задание по добавлению рисунка общего употребления под каждым элементом
– Раунд «Морской бой периодической таблицы»
Помните: При обучении элементам лучше собрать всех за столом
Элементы в шаблоне каждого элемента периодической таблицы в порядке сверху вниз:
H — водород
He — гелий
Li — литий
Be — бериллий
B — бор
4 C — 5 углерод
N – азот
O – кислород
F – фтор
NE – NEON
NA – натрия
мг – магний
Al – Алюминий
SI – Silicon
P -Фосфор
SI -SULF
P -Фосфор 9000
SI -SULF
.0005
CL – хлор
AR – Argon
K – калий
CA – кальций
SC – Scandium
TI – Титан
V – Vanadium
CR – Хром
MN – Манганский
FE -Ird -Irad -Irder -Ird.
Co – Cobalt
Ni – Nickel
Cu – Copper
Zn – Zinc
GA – Gallium
GE – Германия
AS – Arsenic
SE – Selenium
Brromine
SE – Selenium
Brromin
RB – Rubidium
SR – Strontium
Y – Yttrium
Zr – Zirconium
NB – Niobium
MO – Molybdenum
TC – Technetium
RU -MORALIUM
RH -rh -Plodium
40004
RH -rh -Plodiu
AG – Silver
CD – Cadmium
дюйм – индий
SN – TIN
SB – Отвания
TE – Tellurium
I – йодин
XE – XENON
CS – CS -CESIUD
9.0004 BA – BariumLA – Lanthanum
CE – Cerium
Pr – Praseodymium
ND – Neodymium
PM – PraseThium
SM – Самарий
EU – Europium
GD -GadOlium
DY – Dysprosium
HO – Holmium
ER – Erbium
TM – Thulium
YB – Ytterbium
Lu – Lutetium
HF – Hafnium
TA -Tantalum
W -Tungsten
TA -Tantalum 9000
W -Tungsten
0005
Re – Rhenium
OS – OSMIUM
IR – IRIDIUM
PT – Платину
AU – GOLD
HG – Mercury
TL – Thallium
PB – LEAD
BI -BISMUTH
4.

 ..
.. Н.Флерова в Объединенном институте ядерных исследований. Под руководством Юрия Цолаковича в Дубне получены все известные к настоящему времени сверхтяжелые элементы от 113-го до 118-го, последний из которых назван в честь ученого – оганесон.
Н.Флерова в Объединенном институте ядерных исследований. Под руководством Юрия Цолаковича в Дубне получены все известные к настоящему времени сверхтяжелые элементы от 113-го до 118-го, последний из которых назван в честь ученого – оганесон. Здесь, в Дубне, великое открытие Менделеева имело продолжение – учеными ОИЯИ синтезированы новые химические элементы. Таблица, которую будет видно пассажирам всех проплывающих по Волге теплоходов, отражает выдающийся вклад ученых нашего города в развитие науки, и, надеюсь, будет способствовать повышению интереса прежде всего молодежи к новым научным достижениям.
Здесь, в Дубне, великое открытие Менделеева имело продолжение – учеными ОИЯИ синтезированы новые химические элементы. Таблица, которую будет видно пассажирам всех проплывающих по Волге теплоходов, отражает выдающийся вклад ученых нашего города в развитие науки, и, надеюсь, будет способствовать повышению интереса прежде всего молодежи к новым научным достижениям.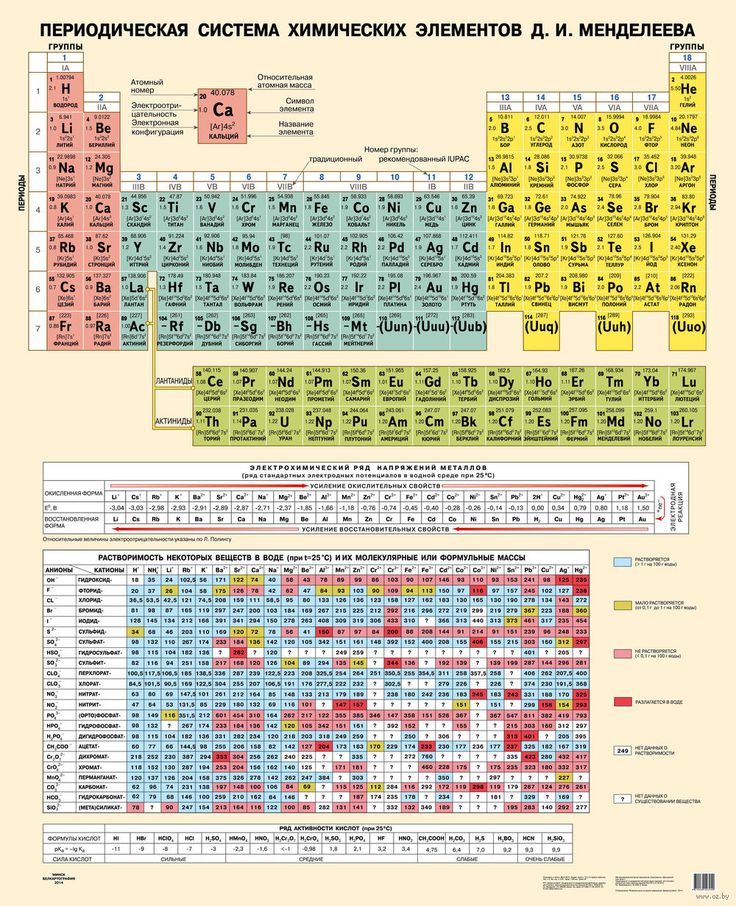 И они, эти кирпичики, неделимы. Их еще Демокрит за 400 лет до нашей эры назвал атомами, тогда это было чисто философское понятие.
И они, эти кирпичики, неделимы. Их еще Демокрит за 400 лет до нашей эры назвал атомами, тогда это было чисто философское понятие. А таблица осталась.
А таблица осталась. Этим мы будем заниматься, это большой путь, сейчас пока мы поняли, что те средства, которые использовали для открытия новых элементов, не годятся, чтобы идти дальше. Сейчас все развивается очень быстро: то, что на данный момент считается передним краем науки, через 10 лет будет обычным делом.
Этим мы будем заниматься, это большой путь, сейчас пока мы поняли, что те средства, которые использовали для открытия новых элементов, не годятся, чтобы идти дальше. Сейчас все развивается очень быстро: то, что на данный момент считается передним краем науки, через 10 лет будет обычным делом. И однажды подходит ко мне Андрей Владимирович Тамонов, и мы обсуждаем, что бы такое монументальное сделать на этой стене. И я посвящаю его в свою идею. А когда я поделился мыслями с Григорием Владимировичем Трубниковым, то он уже имел это в планах, только имел в виду фасад бассейна, чтобы было видно с Волги.
И однажды подходит ко мне Андрей Владимирович Тамонов, и мы обсуждаем, что бы такое монументальное сделать на этой стене. И я посвящаю его в свою идею. А когда я поделился мыслями с Григорием Владимировичем Трубниковым, то он уже имел это в планах, только имел в виду фасад бассейна, чтобы было видно с Волги.
 Тогда они и в будущем мало что узнают и откроют.
Тогда они и в будущем мало что узнают и откроют. В этом смысле, конечно, то что в Дубне будет такая достопримечательность – панно “Периодическая таблица Менделеева” – это замечательно. Будут разные люди смотреть на нее со своей точки зрения, по-разному воспринимать, это очень хорошо!
В этом смысле, конечно, то что в Дубне будет такая достопримечательность – панно “Периодическая таблица Менделеева” – это замечательно. Будут разные люди смотреть на нее со своей точки зрения, по-разному воспринимать, это очень хорошо!