Физика 8 класс. Количество теплоты. Удельная теплоемкость. Топливо.
Физика 8 класс Конспект Количество теплотыКоличество теплоты. Удельная теплоемкость. Топливо.
Внутренняя энергия тела может изменяться как при совершении работы, так и путем теплопередачи (без совершения работы). Если изменение внутренней энергии происходит путем теплопередачи, то переход энергии от одних тел к другим осуществляется теплопроводностью, конвекцией или излучением.
Количество энергии, переданной от одного тела к другому в процессе теплопередачи, называют количеством теплоты.
Количество теплоты, которое необходимо для нагревания тела (или выделяемое при остывании), зависит от массы этого тела, от изменения его температуры и рода вещества.
Количество теплоты обозначают буквой Q, измеряют в джоулях (Дж) или в килоджоулях (кДж).
1 кДж = 1 000 Дж
Количество теплоты измеряют также в
1 ккал = 1 000 кал.
Калория – это количество теплоты, которое необходимо для нагревания 1 г воды на 1 ºС.
1 кал = 4,19 Дж
1 ккал = 4190 Дж = 4,19 кДж.
Физическая величина равная количеству теплоты, которое необходимо передать телу массой 1 кг для того, чтобы его температура изменилась на 1ºС, называется удельной теплоёмкостью вещества.
Удельная теплоемкость обозначается буквой с и измеряется в Дж/кг ºС.
Пример удельной теплоемкости:
удельная теплоемкость воды 4200 Дж/кг ºС — это означает, что для нагревания воды массой 1 кг на 1 ºС необходимо количество теплоты, равное 4200 Дж.
Удельная теплоемкость вещества, находящегося в различных агрегатных состояниях, различна.
Количество теплоты. Удельная теплоемкостьЧтобы рассчитать количество теплоты, необходимое для нагревания тела или выделяемое при охлаждении, следует:
удельную теплоемкость умножить на массу тела и на разность между конечной и начальной температурами.
где с – удельная теплоемкость, m – масса, t2 – конечная температура,
t1 – начальная температура тела.
Топливо — это горючее вещество, которое используется для получения некоторого количества теплоты.
Топливо используют для кипячения воды, приготовления пищи, обогревания жилища, езды на автомобиле.
Самые распространенные виды топлива: газ, нефть, дерево, уголь, бензин.
Топливо — источник энергииПримеры топлива:
твердые виды топлива: уголь, сера, фосфор
жидкие виды топлива: нефть, бензин, керосин, эфир, спирт, ацетонгазообразные виды топлива: водород, метан, пропан, ацетилен.
Основные свойства топлива
- горючее вещество, которое при сгорании выделяет тепло
- вещество должно иметь небольшую температуру воспламенения
- топливом может быть горючее вещество, продукты сгорания которого безвредны
- топливом могут стать только широко распространенные, сравнительно лёгкие в добыче и удобные для транспортировки вещества.

Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется
Удельная теплота сгорания топлива обозначается буквой q. Единицей удельной теплоты сгорания является 1 Дж/кг.
Общее количество теплоты Q, выделяемое при сгорании m кг топлива, вычисляется по формуле
где q — удельная теплота сгорания топлива, m — масса топлива.
Пример удельной теплоты топлива:
удельная теплота сгорания бензина 4,6 · 107 Дж/кг – это значит, что при полном сгорании бензина массой 1 кг выделяется 4,6 · 107 Дж энергии.
Конспект составлен на основании теоретического материала учебника «Физика 8 класс» А.В. Перышкин, «Физика 8 класс»А.В.Грачев.
Скачать конспект:
Похожие записи:
Страница не найдена |
Страница не найдена | 404. Страница не найдена
Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
22232425262728
2930
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
22232425262728
2930
Архивы
Метки
Настройки
для слабовидящих
Количество теплоты.
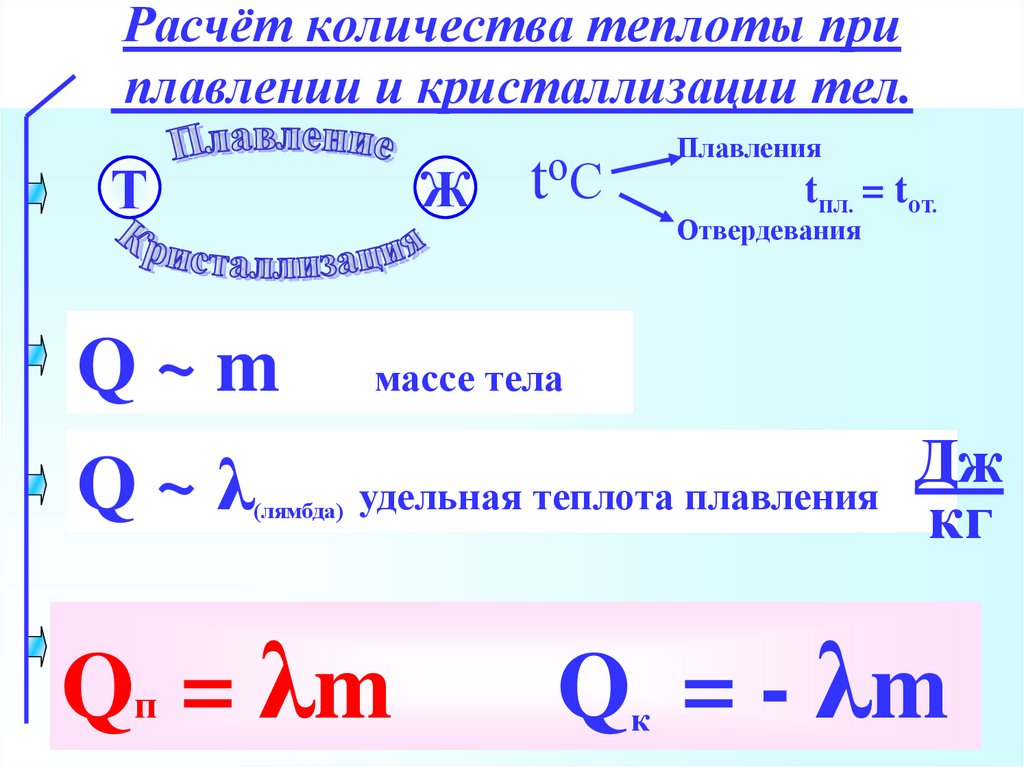 Единица количества теплоты
Единица количества теплотыКак мы уже знаем, внутренняя энергия тела может изменяться как при совершении работы, так и при помощи теплопередачи (не совершая работу). Главное различие между работой и количеством теплоты заключается в том, что работа определяет процесс преобразования внутренней энергии системы, который сопровождается трансформацией энергии из одного вида в другой.
В том случае, если изменение внутренней энергии протекает с помощью теплопередачи
Энергия, которую тело теряет или получает во время теплопередачи, называется количеством теплоты.
При вычислении количества теплоты, необходимо знать, какие величины влияют на него.
От двух одинаковых горелок будем нагревать два сосуда. В одном сосуде 1 кг воды, в другом – 2 кг. Температура воды в двух сосудах изначально одинакова. Мы можем видеть, что за одно и тоже время вода в одном из сосудов нагревается быстрее, хотя оба сосуда получают равное количество теплоты.
Мы можем видеть, что за одно и тоже время вода в одном из сосудов нагревается быстрее, хотя оба сосуда получают равное количество теплоты.
Таким образом, делаем вывод: чем больше масса данного тела, тем большее количество теплоты следует затратить, для того чтобы понизить, или повысить его температуру на такое же количество градусов.
Когда тело остывает, оно отдает соседним предметам тем большее количество теплоты, чем больше его масса.
Мы все знаем, что если нужно нагреть полный чайник воды до температуры 50°C, мы затратим меньше времени на это действие, чем для нагревания чайника с тем же объемом воды, но только до 100 °C. В случае номер один воде будет отдано меньшее количество теплоты, нежели во втором.
Таким образом, количество теплоты, требуемое для нагревания, напрямую зависит от того, на сколько градусов

Но возможно ли определить количество теплоты, требуемой не для нагревания воды, а какого-нибудь другого вещества, допустим, масла, свинца или железа.
Наполним один сосуд водой, а другой наполним растительным маслом. Массы воды и масла равные. Оба сосуда будем равномерно подогревать на одинаковых горелках. Начнем опыт при равной начальной температуре растительного масла и воды. Через пять минут, измерив температуры нагревшихся масла и воды, мы заметим, что температура масла намного выше температуры воды, хотя обе жидкости получали одинаковое количество тепла.
Напрашивается очевидный вывод: при нагревании равных масс масла и воды при одинаковой температуре нужно разное количество теплоты.
И мы тут же делаем еще одни вывод: количество теплоты, которое требуется для нагревания тела, напрямую зависит от вещества, из которого состоит само тело (рода вещества).
Таким образом, количество теплоты, нужное для нагревания тела (либо выделяемое при остывании), напрямую зависит от массы данного тела, вариативности его температуры, а также рода вещества.
Количество теплоты обозначают символом Q. Как и другие различные виды энергии, количество теплоты измеряется в джоулях (Дж) либо в килоджоулях (кДж).
1 кДж = 1000 Дж
Однако история показывает, что ученые стали измерять количество теплоты задолго того, как в физике появилось такое понятие как энергия. В то время, была выведена специальная единица для измерения количества теплоты – калория (кал) либо килокалория (ккал). Слово имеет латинские корни, калор – жара.
1 ккал = 1000 кал
Калория – это то количество теплоты, которое нужно для нагревания 1 г воды на 1°C
1 кал = 4,19 Дж ≈ 4,2 Дж
1 ккал = 4190 Дж ≈ 4200 Дж ≈ 4,2 кДж
Остались вопросы? Не знаете, как сделать домашнее задание?
Чтобы получить помощь репетитора – зарегистрируйтесь.
Первый урок – бесплатно!
Зарегистрироваться
© blog. tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
тепла | Определение и факты
тепло , энергия, которая передается от одного тела к другому в результате разницы температур. Если два тела с разными температурами сближаются, энергия передается, то есть потоки тепла, от более горячего тела к более холодному. Эффект этой передачи энергии обычно, но не всегда, заключается в повышении температуры более холодного тела и понижении температуры более горячего тела. Вещество может поглощать тепло без повышения температуры за счет перехода от одного физического состояния (или фазы) к другому, например, от твердого к жидкому (плавление), от твердого к парообразному (сублимация), от жидкости к пару. (кипение) или из одной твердой формы в другую (обычно это называется кристаллическим переходом).Важное различие между теплом и температурой (тепло является формой энергии, а температура – мерой количества этой энергии, присутствующей в теле) было прояснено в 18-19 веках.
Тепло как форма энергии
Изучите теплопередачу и узнайте разницу между теплом и температурой
Узнайте о теплопередаче и взаимосвязи между теплом и температурой.
Encyclopædia Britannica, Inc. Посмотреть все видео для этой статьи Поскольку все многочисленные формы энергии, включая тепло, могут быть преобразованы в работу, количество энергии выражается в единицах работы, таких как джоули, фут-фунты , киловатт-часы или калории.Существуют точные отношения между количеством тепла, добавляемого к телу или отводимого от него, и величиной воздействия на состояние тела. Две наиболее часто используемые единицы тепла – это калория и британская тепловая единица (БТЕ). Калория (или грамм-калория) – это количество энергии, необходимое для повышения температуры одного грамма воды с 14,5 до 15,5 ° C; BTU – это количество энергии, необходимое для повышения температуры одного фунта воды с 63 до 64 ° F. Одна БТЕ составляет примерно 252 калории.Оба определения указывают, что изменения температуры должны измеряться при постоянном давлении в одну атмосферу, поскольку количество задействованной энергии частично зависит от давления. Калория, используемая для измерения содержания энергии в продуктах, – это большая калория, или килограмм-калория, равная 1000 грамм-калориям.
Калория, используемая для измерения содержания энергии в продуктах, – это большая калория, или килограмм-калория, равная 1000 грамм-калориям.
Британская викторина
Викторина “Все о физике”
Кто был первым ученым, проведшим эксперимент по управляемой цепной ядерной реакции? Какая единица измерения для циклов в секунду? Проверьте свою физическую хватку с помощью этой викторины.
В общем, количество энергии, необходимое для подъема единицы массы вещества через заданный температурный интервал, называется теплоемкостью или удельной теплоемкостью этого вещества. Количество энергии, необходимое для повышения температуры тела на один градус, варьируется в зависимости от наложенных ограничений. Если тепло добавляется к газу, находящемуся в постоянном объеме, количество тепла, необходимое для повышения температуры на один градус, меньше, чем если бы тепло добавлялось к тому же газу, свободному для расширения (как в цилиндре, оснащенном подвижным поршнем). ) и так работаю.В первом случае вся энергия идет на повышение температуры газа, но во втором случае энергия не только способствует повышению температуры газа, но и обеспечивает энергию, необходимую для работы, совершаемой газом над газом. поршень. Следовательно, теплоемкость вещества зависит от этих условий. Чаще всего определяют удельную теплоемкость при постоянном объеме и удельную теплоемкость при постоянном давлении. Французские ученые Пьер-Луи Дюлон и Алексис-Тереза Пети в 1819 году показали, что теплоемкость многих твердых элементов тесно связана с их атомным весом.Так называемый закон Дюлонга и Пти был полезен для определения атомного веса некоторых металлических элементов, но из него есть много исключений; Позднее было обнаружено, что отклонения можно объяснить на основе квантовой механики.
) и так работаю.В первом случае вся энергия идет на повышение температуры газа, но во втором случае энергия не только способствует повышению температуры газа, но и обеспечивает энергию, необходимую для работы, совершаемой газом над газом. поршень. Следовательно, теплоемкость вещества зависит от этих условий. Чаще всего определяют удельную теплоемкость при постоянном объеме и удельную теплоемкость при постоянном давлении. Французские ученые Пьер-Луи Дюлон и Алексис-Тереза Пети в 1819 году показали, что теплоемкость многих твердых элементов тесно связана с их атомным весом.Так называемый закон Дюлонга и Пти был полезен для определения атомного веса некоторых металлических элементов, но из него есть много исключений; Позднее было обнаружено, что отклонения можно объяснить на основе квантовой механики.
Неверно говорить о тепле в теле, потому что тепло ограничивается передачей энергии. Энергия, хранящаяся в теле, – это не тепло (и не работа, так как работа также является энергией в пути). Однако принято говорить о явном и скрытом тепле.Скрытая теплота, также называемая теплотой испарения, – это количество энергии, необходимое для превращения жидкости в пар при постоянной температуре и давлении. Энергия, необходимая для плавления твердого тела в жидкость, называется теплотой плавления, а теплота сублимации – это энергия, необходимая для преобразования твердого тела непосредственно в пар, эти изменения также происходят в условиях постоянной температуры и давления.
Однако принято говорить о явном и скрытом тепле.Скрытая теплота, также называемая теплотой испарения, – это количество энергии, необходимое для превращения жидкости в пар при постоянной температуре и давлении. Энергия, необходимая для плавления твердого тела в жидкость, называется теплотой плавления, а теплота сублимации – это энергия, необходимая для преобразования твердого тела непосредственно в пар, эти изменения также происходят в условиях постоянной температуры и давления.
Воздух представляет собой смесь газов и водяного пара, и вода, присутствующая в воздухе, может изменять фазу; я.е., он может стать жидким (дождь) или твердым (снег). Чтобы различать энергию, связанную с фазовым переходом (скрытое тепло), и энергию, необходимую для изменения температуры, было введено понятие явного тепла. В смеси водяного пара и воздуха явное тепло – это энергия, необходимая для создания определенного изменения температуры, за исключением энергии, необходимой для фазового перехода.
Расчет тепла, энергии и изменений температуры – видео и стенограмма урока
Удельная теплоемкость
Мы собираемся посмотреть, как тепло и температура взаимодействуют, вычислив, сколько тепла нужно, чтобы взять 50 граммов льда с температурой -20 ° F и превратить их в воду с температурой 80 ° F.Для этого нам придется использовать две разные формулы энергии; один для удельной теплоемкости и один для скрытой теплоты. Формула удельной теплоемкости, которую вы можете увидеть на своем экране, говорит нам, сколько добавленного тепла ( Q ) требуется для изменения температуры вещества.
Здесь m – масса, ΔT – изменение температуры и c – удельная теплоемкость. Удельная теплоемкость – это количество тепла, необходимое для повышения температуры вещества на один градус Цельсия.
Скрытое тепло
Хотя формула теплоемкости говорит нам, сколько тепла требуется для повышения температуры вещества, она не говорит нам, сколько тепла требуется для изменения фазы вещества. Для этого мы используем формулу скрытой теплоты.
Для этого мы используем формулу скрытой теплоты.
Скрытая теплота ( l ) – это теплота, необходимая для изменения фазы вещества на единицу массы. Существует два различных типа скрытой теплоты: скрытая теплота плавления и скрытая теплота испарения .Первый имеет дело с изменением вещества между твердым телом и жидкостью, а второй – с изменением между жидкостью и газом.
Удельная и скрытая теплоемкость уникальна для каждого вещества. В нашем примере вода имеет следующие значения удельной и скрытой теплоты, которые вы можете видеть на своем экране, пока мы говорим.
«J» означает джоули, которые представляют собой единицы измерения энергии. В этом случае мы видим Дж / г или Джоули на грамм, что относится к единицам тепловой энергии, расходуемой на массу объекта.
Завершение задачи
Мы используем уравнения удельной и скрытой теплоты вместе, когда повышение температуры вещества переводит его из одной фазы в другую. В нашем примере общее добавленное тепло ( Qtot ) будет представлять собой количество тепла, необходимое для повышения температуры льда до точки, где он тает ( Qi ), плюс количество тепла, необходимое для превращения льда в воду ( Qitw ), плюс количество тепла, необходимое для повышения температуры воды ( Qw ) до 80o F.
В нашем примере общее добавленное тепло ( Qtot ) будет представлять собой количество тепла, необходимое для повышения температуры льда до точки, где он тает ( Qi ), плюс количество тепла, необходимое для превращения льда в воду ( Qitw ), плюс количество тепла, необходимое для повышения температуры воды ( Qw ) до 80o F.
Прежде чем мы включим всю информацию о нашей проблеме, нам нужно сделать еще одну вещь. Нам нужно преобразовать нашу температуру из Фаренгейта в Цельсия. Для этого преобразования мы используем следующую формулу.
Для этой задачи нам нужно преобразовать нашу начальную температуру -20o F и нашу конечную температуру 80o F.
Теперь мы используем всю информацию, которую мы дали в разделе, для решения нашей проблемы.
Наконец, давайте кратко отметим, как были выбраны наши температурные интервалы для ΔT , или конечная температура минус начальная температура. Эти температурные интервалы были выбраны потому, что лед тает при температуре выше 0 ° C. Таким образом, тепло, добавляемое для льда, может применяться только при температуре от -29 ° C до 0 ° C, а тепло, добавляемое для воды, может применяться только при температуре от 0 ° C до 27 ° C ».
Эти температурные интервалы были выбраны потому, что лед тает при температуре выше 0 ° C. Таким образом, тепло, добавляемое для льда, может применяться только при температуре от -29 ° C до 0 ° C, а тепло, добавляемое для воды, может применяться только при температуре от 0 ° C до 27 ° C ».
Кривая нагрева
В предыдущих разделах мы подробно рассмотрели взаимосвязь между теплотой и температурой, изучив формулы удельной и скрытой теплоты.Однако, сосредоточившись исключительно на формулах, легко остаться без интуитивного понимания того, что именно происходит. Мы можем помочь выработать более интуитивное понимание, глядя на так называемую кривую нагрева. Кривая нагрева показывает взаимосвязь между температурой и добавленным теплом. На диаграмме на экране вы можете видеть, что температура вещества повышается по мере того, как к нему добавляется больше тепла.
Вы также заметите, что большие участки графика представляют собой горизонтальные линии. Здесь добавляется тепло, но температура не повышается. Это происходит потому, что в этот момент все тепло уходит на изменение фазы вещества, а не на его нагревание. Таким образом, первый горизонтальный сегмент представляет точку плавления , где вещество переходит из твердого в жидкое, а второй горизонтальный сегмент представляет точку кипения , при которой вещество переходит из жидкости в газ.
Здесь добавляется тепло, но температура не повышается. Это происходит потому, что в этот момент все тепло уходит на изменение фазы вещества, а не на его нагревание. Таким образом, первый горизонтальный сегмент представляет точку плавления , где вещество переходит из твердого в жидкое, а второй горизонтальный сегмент представляет точку кипения , при которой вещество переходит из жидкости в газ.
Краткое содержание урока
Тепло и температура, хотя на первый взгляд кажутся похожими, на самом деле представляют собой два разных понятия. Тепло – это энергия, которая передается от горячего вещества к холодному, а температура – это мера средней кинетической энергии молекул в системе. Их можно связать друг с другом с помощью уравнений удельной и скрытой теплоты.
Уравнение удельной теплопроводности используется для определения количества тепла, добавляемого ( Q ) к веществу при изменении температуры ( ΔT ).
Здесь m – масса вещества, а c – его удельная теплоемкость , которая сообщает нам, сколько тепла требуется, чтобы повысить температуру вещества на один градус Цельсия.
Уравнение скрытой теплоты используется для определения количества тепла, добавляемого для изменения фазы вещества.
Скрытая теплота ( l ) – это теплота, необходимая для изменения фазы вещества на единицу массы. Скрытая теплота может быть либо скрытой теплотой плавления, для переключения между твердым телом и жидкостью, либо скрытой теплотой парообразования, для переключения между жидкостью и газом.
Наконец, то, как тепло и температура взаимодействуют в веществе, также можно увидеть графически на так называемой кривой нагрева , которая показывает взаимосвязь между температурой и добавленным теплом.Он также показывает точку плавления , при которой вещество превращается из твердого тела в жидкость, и точку кипения , при которой вещество превращается из жидкости в газ.
По мере добавления тепла температура повышается, за исключением горизонтальных участков кривой, где вместо этого все тепло уходит на изменение фазы вещества.
14.2 Изменение температуры и теплоемкость – Физика колледжа: OpenStax
Глава 14 Методы теплопередачи и теплопередачи
Сводка
- Наблюдайте за теплопередачей и изменением температуры и массы.
- Расчет конечной температуры после передачи тепла между двумя объектами.
Одним из основных эффектов теплопередачи является изменение температуры: нагревание увеличивает температуру, а охлаждение снижает ее. Мы предполагаем, что фазового перехода нет и что система не выполняет никаких работ. Эксперименты показывают, что передаваемое тепло зависит от трех факторов: изменения температуры, массы системы, а также вещества и фазы вещества.
Рисунок 1. Тепло Q , передаваемое для изменения температуры, зависит от величины изменения температуры, массы системы, а также от вещества и фазы. (а) Количество переданного тепла прямо пропорционально изменению температуры. Чтобы удвоить изменение температуры массы м , вам нужно добавить вдвое больше тепла. (б) Количество передаваемого тепла также прямо пропорционально массе. Чтобы вызвать эквивалентное изменение температуры в удвоенной массе, вам нужно добавить в два раза больше тепла.(c) Количество передаваемого тепла зависит от вещества и его фазы. Если требуется количество тепла в размере Q , чтобы вызвать изменение температуры Δ T в данной массе меди, потребуется в 10,8 раза больше тепла, чтобы вызвать эквивалентное изменение температуры при той же массе меди. вода при условии отсутствия фазового перехода ни в одном из веществ.Зависимость от изменения температуры и массы легко понять. Поскольку (средняя) кинетическая энергия атома или молекулы пропорциональна абсолютной температуре, внутренняя энергия системы пропорциональна абсолютной температуре и количеству атомов или молекул.Благодаря тому, что переданное тепло равно изменению внутренней энергии, тепло пропорционально массе вещества и изменению температуры. Передаваемое тепло также зависит от вещества, так что, например, количество тепла, необходимое для повышения температуры, меньше для спирта, чем для воды. Для одного и того же вещества передаваемое тепло также зависит от фазы (газ, жидкость или твердое тело).
ТЕПЛООБМЕН И ИЗМЕНЕНИЕ ЭНЕРГИИ
Количественная связь между теплопередачей и изменением температуры включает все три фактора:
[латекс] \ boldsymbol {Q = mc \ Delta {T}}, [/ латекс]
где [латекс] \ boldsymbol {Q} [/ latex] – это символ теплопередачи, [latex] \ boldsymbol {m} [/ latex] – масса вещества, а [латекс] \ boldsymbol {\ Delta { T}} [/ latex] – это изменение температуры.{\ circ} \ textbf {C)}}. [/ latex]
Значения удельной теплоемкости обычно нужно искать в таблицах, потому что нет простого способа их вычислить. Как правило, удельная теплоемкость также зависит от температуры. В таблице 1 приведены типичные значения теплоемкости для различных веществ. За исключением газов, температурная и объемная зависимость удельной теплоемкости большинства веществ слабая. Из этой таблицы видно, что удельная теплоемкость воды в пять раз больше, чем у стекла, и в десять раз больше, чем у железа, что означает, что требуется в пять раз больше тепла, чтобы повысить температуру воды на такую же величину, что и у стекла, и в десять раз больше. много тепла для повышения температуры воды, как для утюга.{\ circ} \ textbf {C}}. [/ latex] (a) Сколько тепла требуется? Какой процент тепла используется для повышения температуры (б) сковороды и (в) воды?
Стратегия
Кастрюля и вода всегда имеют одинаковую температуру. Когда вы ставите кастрюлю на плиту, температура воды и кастрюли увеличивается на одинаковую величину. Мы используем уравнение теплопередачи для данного изменения температуры и массы воды и алюминия. Значения удельной теплоемкости воды и алюминия приведены в таблице 1.4 \ textbf {J} = 27.0 \ textbf {кДж}}. [/ Latex]
[латекс] \ boldsymbol {Q _ {\ textbf {Total}} = Q _ {\ textbf {W}} + Q _ {\ textbf {Al}} = 62.8 \ textbf {kJ} + 27.0 \ textbf {kJ} = 89.8 \ textbf {кДж}}. [/ latex]
Таким образом, количество тепла, идущего на нагревание сковороды, равно
.[латекс] \ boldsymbol {\ frac {27.0 \ textbf {kJ}} {89.8 \ textbf {kJ}}} [/ latex] [латекс] \ boldsymbol {\ times100 \% = 30.1 \%}, [/ латекс]
, а на подогрев воды –
.[латекс] \ boldsymbol {\ frac {62.8 \ textbf {kJ}} {89.8 \ textbf {kJ}}} [/ latex] [latex] \ boldsymbol {\ times100 \% = 69.9 \%}. [/ Latex]
Обсуждение
В этом примере тепло, передаваемое контейнеру, составляет значительную долю от общего переданного тепла. Хотя вес кастрюли в два раза больше, чем у воды, удельная теплоемкость воды более чем в четыре раза больше, чем у алюминия.Следовательно, для достижения заданного изменения температуры воды требуется чуть более чем в два раза больше тепла по сравнению с алюминиевым поддоном.
Рисунок 2. Дымящиеся тормоза этого грузовика – видимое свидетельство механического эквивалента тепла.Пример 2: Расчет повышения температуры в результате работы, проделанной с веществом: перегрев тормозов грузовика на спуске
Тормоза грузовика, используемые для контроля скорости на спуске, работают, преобразуя гравитационную потенциальную энергию в повышенную внутреннюю энергию (более высокую температуру) тормозного материала.{\ circ} \ textbf {C}} [/ latex], если материал сохраняет 10% энергии от грузовика массой 10 000 кг, спускающегося на 75,0 м (в вертикальном перемещении) с постоянной скоростью.
Стратегия
Если тормоза не применяются, потенциальная гравитационная энергия преобразуется в кинетическую энергию. При срабатывании тормозов потенциальная гравитационная энергия преобразуется во внутреннюю энергию тормозного материала. Сначала мы вычисляем гравитационную потенциальную энергию [latex] \ boldsymbol {(Mgh)} [/ latex], которую весь грузовик теряет при спуске, а затем находим повышение температуры, возникающее только в тормозном материале.{\ circ} \ textbf {C}}. [/ latex]
Обсуждение
Эта температура близка к температуре кипения воды. Если бы грузовик ехал какое-то время, то непосредственно перед спуском температура тормозов, вероятно, была бы выше, чем температура окружающей среды. Повышение температуры при спуске, вероятно, приведет к повышению температуры тормозного материала выше точки кипения воды, поэтому этот метод непрактичен. Однако та же самая идея лежит в основе недавней гибридной технологии автомобилей, в которой механическая энергия (гравитационная потенциальная энергия) преобразуется тормозами в электрическую энергию (аккумулятор).
| Вещества | Удельная теплоемкость ( c ) | |
|---|---|---|
| Твердые вещества | Дж / кг⋅ºC | ккал / кг⋅ºC 2 |
| Алюминий | 900 | 0,215 |
| Асбест | 800 | 0,19 |
| Бетон, гранит (средний) | 840 | 0,20 |
| Медь | 387 | 0.0924 |
| Стекло | 840 | 0,20 |
| Золото | 129 | 0,0308 |
| Человеческое тело (в среднем при 37 ° C) | 3500 | 0,83 |
| Лед (в среднем, от -50 ° C до 0 ° C) | 2090 | 0,50 |
| Чугун, сталь | 452 | 0,108 |
| Свинец | 128 | 0,0305 |
| Серебро | 235 | 0.0562 |
| Дерево | 1700 | 0,4 |
| Жидкости | ||
| Бензол | 1740 | 0,415 |
| этанол | 2450 | 0,586 |
| Глицерин | 2410 | 0,576 |
| Меркурий | 139 | 0,0333 |
| Вода (15,0 ° C) | 4186 | 1.000 |
| Газы 3 | ||
| Воздух (сухой) | 721 (1015) | 0,172 (0,242) |
| Аммиак | 1670 (2190) | 0,399 (0,523) |
| Двуокись углерода | 638 (833) | 0,152 (0,199) |
| Азот | 739 (1040) | 0,177 (0,248) |
| Кислород | 651 (913) | 0.156 (0,218) |
| Пар (100 ° C) | 1520 (2020) | 0,363 (0,482) |
| Таблица 1. Удельная теплоемкость 1 различных веществ | ||
Обратите внимание, что Пример 2 является иллюстрацией механического эквивалента тепла. В качестве альтернативы повышение температуры может быть произведено с помощью паяльной лампы, а не механически.
Пример 3: Расчет конечной температуры при передаче тепла между двумя телами: заливка холодной воды в горячую кастрюлю
Допустим, вы налили 0.{\ circ} \ textbf {C}}. [/ latex] Предположим, что кастрюля стоит на изолированной подушке и выкипает незначительное количество воды. Какова температура, когда вода и поддон через короткое время достигают теплового равновесия?
Стратегия
Сковорода помещается на изолирующую подкладку так, чтобы теплоотдача с окружающей средой была незначительной. Изначально кастрюля и вода не находятся в тепловом равновесии: кастрюля имеет более высокую температуру, чем вода. Затем теплообмен восстанавливает тепловое равновесие, когда вода и поддон соприкасаются.Поскольку теплопередача между поддоном и водой происходит быстро, масса испарившейся воды незначительна, а величина тепла, теряемого поддоном, равна теплу, полученному водой. Обмен тепла прекращается, когда достигается тепловое равновесие между кастрюлей и водой. Теплообмен можно записать как [латекс] \ boldsymbol {| Q _ {\ textbf {hot}} | = Q _ {\ textbf {cold}}}. [/ Latex]
Решение
- Используйте уравнение теплопередачи [латекс] \ boldsymbol {Q = mc \ Delta {T}} [/ latex], чтобы выразить тепло, теряемое алюминиевой сковородой, через массу сковороды, удельную теплоемкость алюминия. , начальная температура сковороды и конечная температура:
[латекс] \ boldsymbol {Q _ {\ textbf {hot}} = m _ {\ textbf {Al}} c _ {\ textbf {Al}} (T _ {\ textbf {f}} – 150 ^ {\ circ} \ textbf {C})}.{\ circ} \ textbf {C})}. [/ latex]
- Обратите внимание, что [latex] \ boldsymbol {Q _ {\ textbf {hot}} 0} [/ latex] и что их сумма должна быть равна нулю, потому что тепло, теряемое горячей сковородой, должно быть таким же, как тепло, полученное холодной водой. :
[латекс] \ begin {array} {rcl} \ boldsymbol {Q _ {\ textbf {cold}} + Q _ {\ textbf {hot}}} & \ boldsymbol {=} & \ boldsymbol {0,} \\ \ boldsymbol {Q _ {\ textbf {cold}}} & \ boldsymbol {=} & \ boldsymbol {-Q _ {\ textbf {hot}},} \\ \ boldsymbol {m _ {\ textbf {W}} c _ {\ textbf {W }} (T _ {\ textbf {f}} – 20.{\ circ} \ textbf {C}}? [/ latex] Причина в том, что вода имеет большую удельную теплоемкость, чем большинство обычных веществ, и поэтому претерпевает небольшое изменение температуры при данной теплопередаче. Большой водоем, например озеро, требует большого количества тепла для значительного повышения температуры. Это объясняет, почему температура в озере остается относительно постоянной в течение дня, даже когда изменение температуры воздуха велико. Однако температура воды действительно меняется в течение длительного времени (например, с лета на зиму).
ЭКСПЕРИМЕНТ НА ДОМУ: ИЗМЕНЕНИЕ ТЕМПЕРАТУРЫ ЗЕМЛИ И ВОДЫ
Что нагревается быстрее, земля или вода?
Для изучения разницы в теплоемкости:
- Поместите равные массы сухого песка (или почвы) и воды одинаковой температуры в две небольшие банки. (Средняя плотность почвы или песка примерно в 1,6 раза больше плотности воды, поэтому вы можете получить примерно равную массу, используя [латекс] \ boldsymbol {50 \%} [/ латекс] больше воды по объему.)
- Нагрейте оба предмета (с помощью духовки или нагревательной лампы) одинаковое время.
- Запишите конечную температуру двух масс.
- Теперь доведите обе банки до одинаковой температуры, нагревая в течение более длительного периода времени.
- Снимите банки с источника тепла и измеряйте их температуру каждые 5 минут в течение примерно 30 минут.
Какой образец остывает быстрее всего? Это упражнение воспроизводит явления, ответственные за ветер с суши и с моря. {\ circ} \ textbf {C}}? [/ latex]
- Передача тепла [латекс] \ boldsymbol {Q} [/ latex], которая приводит к изменению [латекса] \ boldsymbol {\ Delta {T}} [/ latex] температуры тела с массой [латекс] \ boldsymbol {m} [/ latex] – это [латекс] \ boldsymbol {Q = mc \ Delta {T}}, [/ latex], где [latex] \ boldsymbol {c} [/ latex] – удельная теплоемкость материала. .Это соотношение также можно рассматривать как определение удельной теплоемкости.
Концептуальные вопросы
1: Какие три фактора влияют на теплопередачу, необходимую для изменения температуры объекта?
2: Тормоза в автомобиле повышают температуру на [латекс] \ boldsymbol {\ Delta {T}} [/ latex] при остановке автомобиля на скорости [латекс] \ boldsymbol {v}. [/ latex] Насколько лучше был бы [latex] \ boldsymbol {\ Delta {T}} [/ latex], если бы автомобиль изначально имел в два раза большую скорость? Вы можете предположить, что автомобиль останавливается достаточно быстро, чтобы не отводить тепло от тормозов.{\ circ} \ textbf {C}}: [/ latex] (а) вода; (б) бетон; (в) сталь; и d) ртуть.
5: Потирание рук согревает их, превращая работу в тепловую энергию. Если женщина трет руки взад и вперед в общей сложности 20 движений на расстоянии 7,50 см на каждый натирание и со средней силой трения 40,0 Н, каково повышение температуры? Масса согреваемых тканей всего 0,100 кг, в основном в ладонях и пальцах.
6: Блок чистого материала массой 0,250 кг нагревается от [латекса] \ boldsymbol {20.{\ circ} \ textbf {C}} [/ latex] путем добавления 4,35 кДж энергии. Вычислите его удельную теплоемкость и определите вещество, из которого он, скорее всего, состоит.
7: Предположим, что одинаковые количества тепла передаются различным массам меди и воды, вызывая одинаковые изменения температуры. Какое отношение массы меди к воде?
8: (a) Количество килокалорий в пище определяется калориметрическими методами, при которых пища сжигается и измеряется теплоотдача.{\ circ} \ textbf {C}} [/ latex] через 30,0 мин, если предположить, что тело продолжает вырабатывать энергию со скоростью 150 Вт? [латекс] \ boldsymbol {(1 \ textbf {watt} = \: 1 \ textbf {джоуль в секунду или} 1 \ textbf {W} = \: 1 \ textbf {Дж / с})}. [/ latex]
10: Даже при остановке после периода нормальной эксплуатации большой промышленный ядерный реактор передает тепловую энергию со скоростью 150 МВт за счет радиоактивного распада продуктов деления. Эта теплопередача вызывает быстрое повышение температуры, если система охлаждения выходит из строя [латекс] \ boldsymbol {(1 \ textbf {watt} = \: 1 \ textbf {джоуль в секунду или} 1 \ textbf {W} = \: 1 \ textbf {Дж / с и} 1 \ textbf {MW} = \: 1 \ textbf {мегаватт})}.{\ circ} \ textbf {C}}, [/ latex], если не указано иное, и при среднем давлении 1,00 атм. В скобках указаны значения [латекс] \ boldsymbol {c _ {\ textbf {p}}} [/ latex] при постоянном давлении 1,00 атм.
Глоссарий
- удельная теплоемкость
- количество тепла, необходимое для изменения температуры 1,00 кг вещества на 1,00 ºC
Решения
Проверьте свое понимание
1: Теплопередача зависит только от разницы температур.{\ circ} \ textbf {C}} [/ latex]
7:
10,8
9:
617 Вт
Измерение тепла – видео по физике от Brightstorm
Измерение тепла выполняется в калориях. Одна калория – это количество энергии, необходимое для того, чтобы поднять один грамм воды на один градус Цельсия. Чтобы измерить тепло, нужно разделить изменение температуры образца воды на массу воды.
Измерение тепла, как же нам измерить тепло? Помните, что тепло – это поток энергии от горячего объекта к холодному или от чего-то более горячего к более холодному. Мы можем измерить это тепло с помощью того, что называется калорийностью. Калория – это мера количества тепла в веществе, и это, по сути, количество энергии, необходимое для поднятия одного грамма воды на один градус Цельсия, и формула, которую мы можем использовать для расчета, представляет собой изменение температуры, деленное на Цельсия. массой нагретой им воды.
Давайте рассмотрим пример того, как можно вычислить меру тепла, как можно вычислить калории. Допустим, у нас есть образец пищи, и когда образец пищи сгорает и нагрев поднимает 25 граммов воды с 10 до 85 градусов по Цельсию, сколько калорий было высвобождено этой пищей? И давайте предположим, что мы получили всю энергию от этой пищи для нагрева воды, мы не сильно потеряли окружающую среду и другие места, что вся эта энергия была передана непосредственно воде, хорошо, поэтому мы можем просто установить это вверх.У нас есть изменение температуры в пределах нашей массы воды, хорошо, что, как вы знаете, мы собираемся использовать, затем граммы наших научных единиц, поэтому изменение температуры, наша конечная температура составила 85 градусов по Цельсию, наша начальная температура была, я извините, 10 градусов по Цельсию, а масса нашей воды составляла 25 граммов, хорошо, поэтому, если мы разделим это, мы получим 75 градусов по Цельсию, это наше изменение температуры, деленное на 25 граммов воды, которое будет равно 3 калориям, так что образец пищи произвел 3 Калории и 3 калории – это измерение тепла, которое было передано от пищи в воду, или переданное тепло – измерение тепла.
Physlet Physics Кристиана и Беллони: Исследование 20.6
Exploration 20.6: Удельная теплоемкость при постоянном давлении и постоянном объеме
Подождите, пока анимация полностью загрузится.
Существует задержка по времени – поскольку система должна находиться в равновесии – до того, как произойдет изменение состояния.
В этой анимации N = nR (т.е. k B = 1). Это дает закон идеального газа как PV = NT.Рестарт.
Для идеального одноатомного газа изменение внутренней энергии зависит только от температуры, ΔU = (3/2) nRΔT = (3/2) NΔT.
- Рассчитайте изменение внутренней энергии для трех случаев.
- Какая работа выполняется в каждом конкретном случае? Напоминаем, что W = ∫ P dV, и давление может (и во многих случаях зависит) от объема. Подсчитайте проделанную работу в каждом случае, используя следующие два метода, а затем сравните свои ответы.
- Графически: Чтобы найти проделанную работу, нужно определить площадь под кривой («площадь» красной области на графике).После оценки площади путем подсчета блоков сетки установите флажок выше, чтобы отобразить расчет площади (путем численного интегрирования) в моделировании. Объясните любые существенные различия между вашей оценкой и численным интегрированием.
- Аналитическое решение (требуется немного расчетов): Когда тепло добавляется при постоянном давлении (изобарический процесс), тогда P, давление, в приведенном выше уравнении для работы просто постоянная интегрирования. Когда тепло добавляется в постоянном объеме (изохорный процесс), проделанная работа равна нулю.Почему? Когда тепло добавляется при постоянной температуре (изотермический), используйте закон идеального газа (PV = NT) и запишите давление как функцию объема: NT / V (где N и T постоянны), а затем вы можете интегрировать ( ответ включает натуральный логарифм).
- Используя первый закон термодинамики, Q = W + ΔU, рассчитайте подвод тепла и покажите, что оно одинаково для всех трех случаев.
Удельная теплоемкость материала – это мера количества тепла, необходимого для получения грамма (или заданного количества) материала 1 o C.Для газа требуется разное количество тепла для повышения того же количества газа до той же температуры в зависимости от обстоятельств, при которых добавляется тепло. Если добавлено одинаковое количество тепла, конечные температуры расширения при постоянном давлении и постоянном объеме будут совершенно разными (и при постоянной температуре тепло добавляется, но температура не изменяется!).
- В каком случае подвод тепла увеличивает температуру больше всего? Почему?
Итак, если удельная теплоемкость идеального газа вообще должна иметь какое-либо значение, она должна быть определена в терминах процесса: удельная теплоемкость при постоянном объеме или удельная теплоемкость при постоянном давлении.
- Вернитесь к расчету тепла в (c). Рассчитайте константу пропорциональности между подводимой теплотой и изменением температуры для случаев постоянного объема и постоянного давления: Q = (Constant) NΔT.
- Какая константа в каждом случае? Почему постоянная для расширения при постоянном давлении больше? (Подсказка: подумайте, используется ли тепло только для изменения температуры или для изменения температуры и выполняйте работу.)
Обычно мы записываем теплоемкость как молярную теплоемкость (где n – число молей) и находим, что для постоянного давления Q = C P nΔT и C P = (5/2) R, и для постоянного объема Q = C V nΔT и C V = (3/2) R.
Мы начали это обсуждение с того, что для идеального одноатомного газа средняя внутренняя энергия составляет (3/2) Тл. Это происходит из кинетической теории и равноправия энергии, где 3 происходит от 3 степеней свободы. Для двухатомного газа средняя внутренняя энергия составляет (5/2) Тл, потому что есть еще две степени свободы (вращения).
- Чем отличаются теплоемкость при постоянном давлении и теплоемкость при постоянном объеме для двухатомного газа?
Когда вы получите красивый график, щелкните его правой кнопкой мыши, чтобы клонировать график и изменить его размер для лучшего обзора.
Исследование автором Энн Дж. Кокс.
Physlets были разработаны в колледже Дэвидсона и преобразованы с Java на JavaScript с использованием системы SwingJS, разработанной в колледже Св. Олафа.
Видео с вопросом: Расчет энергии, необходимой для нагрева массы по известному изменению температуры
Стенограмма видео
Определите, сколько энергии необходимо для нагрева двух килограммов воды на три градуса Цельсия.Используйте значение 4184 джоулей на килограмм градусов Цельсия для удельной теплоемкости воды. Дайте свой ответ двум значащим цифрам.
Хорошо, в этом упражнении мы начнем с двух килограммов воды. И мы хотим нагреть эту воду так, чтобы ее температура повысилась на три градуса по Цельсию. Итак, какой бы ни была температура сейчас, мы хотим увеличить ее на три градуса по Цельсию. Назовем это изменение температуры Δ𝑇. И мы обозначим массу этой воды, два килограмма, 𝑚.Учитывая удельную теплоемкость воды, мы хотим знать, сколько энергии необходимо, чтобы нагреть это количество воды на столько.
Мы можем вспомнить математическое соотношение, которое поможет нам решить эту проблему. Это соотношение говорит нам, что количество энергии, необходимое для повышения температуры на некоторую величину, Δ𝑇, некоторого количества вещества, 𝑚, равно произведению этих двух величин на удельную теплоемкость этого вещества. И мы напоминаем, что в целом удельная теплоемкость говорит нам, сколько энергии необходимо для нагрева одного килограмма данного материала на один градус Цельсия.Для жидкой воды это 4184 джоуля.
Другими словами, если мы прибавим это количество джоулей энергии к одному килограмму воды, то мы повысим ее температуру на один градус Цельсия. Итак, зная массу воды, изменение температуры, на которое мы хотим повлиять, Δ𝑇 и удельную теплоемкость воды, мы готовы рассчитать необходимую энергию. Подставляя эти значения для 𝑚, 𝐶 и Δ𝑇, давайте на мгновение взглянем на единицы измерения.
Обратите внимание, что у нас есть единицы массы в килограммах как в числителе, так и в знаменателе.Это означает, что эти единицы будут отменены. У нас также есть единицы измерения температуры в градусах Цельсия как в знаменателе, так и в числителе. Так что и эти отряды тоже отменяются. При вычислении этого продукта у нас останутся просто джоули, единицы энергии. Это подтверждает, что мы на правильном пути. И когда мы рассчитываем это произведение, мы находим результат 25104 джоулей.
Это не окончательный ответ, потому что в постановке задачи мы видим, что мы должны дать ответ в виде двух значащих цифр.Первая значимая цифра в этом числе – два. Следующая значимая цифра – пятерка. И третья значимая цифра – это единица. Мы оставим только два таких. А поскольку наша третья значащая цифра меньше пяти, это означает, что мы не будем округлять. Мы оставим наши первые две значащие цифры такими, какие они есть, два и пять. Округляя наш результат до двух значащих цифр, мы получаем 25000 джоулей. Именно столько энергии потребуется, чтобы нагреть два килограмма воды на три градуса Цельсия.
14.2 Изменение температуры и теплоемкость – Физика колледжа, главы 1-17
14 Методы нагрева и передачи
Сводка
- Наблюдайте за теплопередачей и изменением температуры и массы.
- Расчет конечной температуры после передачи тепла между двумя объектами.
Одним из основных эффектов теплопередачи является изменение температуры: нагревание увеличивает температуру, а охлаждение снижает ее.Мы предполагаем, что фазового перехода нет и что система не выполняет никаких работ. Эксперименты показывают, что передаваемое тепло зависит от трех факторов: изменения температуры, массы системы, а также вещества и фазы вещества.
Рисунок 1. Тепло Q , передаваемое для изменения температуры, зависит от величины изменения температуры, массы системы, а также от вещества и фазы. (а) Количество переданного тепла прямо пропорционально изменению температуры.Чтобы удвоить изменение температуры массы м , вам нужно добавить вдвое больше тепла. (б) Количество передаваемого тепла также прямо пропорционально массе. Чтобы вызвать эквивалентное изменение температуры в удвоенной массе, вам нужно добавить в два раза больше тепла. (c) Количество передаваемого тепла зависит от вещества и его фазы. Если требуется количество тепла Q , чтобы вызвать изменение температуры Δ T в данной массе меди, потребуется 10.В 8 раз больше тепла, чтобы вызвать эквивалентное изменение температуры в той же массе воды, при условии отсутствия фазовых изменений ни в одном из веществ.Зависимость от изменения температуры и массы легко понять. Поскольку (средняя) кинетическая энергия атома или молекулы пропорциональна абсолютной температуре, внутренняя энергия системы пропорциональна абсолютной температуре и количеству атомов или молекул. Благодаря тому, что переданное тепло равно изменению внутренней энергии, тепло пропорционально массе вещества и изменению температуры.Передаваемое тепло также зависит от вещества, так что, например, количество тепла, необходимое для повышения температуры, меньше для спирта, чем для воды. Для одного и того же вещества передаваемое тепло также зависит от фазы (газ, жидкость или твердое тело).
ТЕПЛООБМЕН И ИЗМЕНЕНИЕ ЭНЕРГИИ
Количественная связь между теплопередачей и изменением температуры включает все три фактора:
[латекс] \ boldsymbol {Q = mc \ Delta {T}}, [/ латекс]
где [латекс] \ boldsymbol {Q} [/ latex] – это символ теплопередачи, [latex] \ boldsymbol {m} [/ latex] – масса вещества, а [латекс] \ boldsymbol {\ Delta { T}} [/ latex] – это изменение температуры.{\ circ} \ textbf {C)}}. [/ latex]
Значения удельной теплоемкости обычно нужно искать в таблицах, потому что нет простого способа их вычислить. Как правило, удельная теплоемкость также зависит от температуры. В таблице 1 приведены типичные значения теплоемкости для различных веществ. За исключением газов, температурная и объемная зависимость удельной теплоемкости большинства веществ слабая. Из этой таблицы видно, что удельная теплоемкость воды в пять раз больше, чем у стекла, и в десять раз больше, чем у железа, что означает, что требуется в пять раз больше тепла, чтобы повысить температуру воды на такую же величину, что и у стекла, и в десять раз больше. много тепла для повышения температуры воды, как для утюга.{\ circ} \ textbf {C}}. [/ latex] (a) Сколько тепла требуется? Какой процент тепла используется для повышения температуры (б) сковороды и (в) воды?
Стратегия
Кастрюля и вода всегда имеют одинаковую температуру. Когда вы ставите кастрюлю на плиту, температура воды и кастрюли увеличивается на одинаковую величину. Мы используем уравнение теплопередачи для данного изменения температуры и массы воды и алюминия. Значения удельной теплоемкости воды и алюминия приведены в таблице 1.4 \ textbf {J} = 27.0 \ textbf {кДж}}. [/ Latex]
[латекс] \ boldsymbol {Q _ {\ textbf {Total}} = Q _ {\ textbf {W}} + Q _ {\ textbf {Al}} = 62.8 \ textbf {kJ} + 27.0 \ textbf {kJ} = 89.8 \ textbf {кДж}}. [/ latex]
Таким образом, количество тепла, идущего на нагревание сковороды, равно
.[латекс] \ boldsymbol {\ frac {27.0 \ textbf {kJ}} {89.8 \ textbf {kJ}}} [/ latex] [латекс] \ boldsymbol {\ times100 \% = 30.1 \%}, [/ латекс]
, а на подогрев воды –
.[латекс] \ boldsymbol {\ frac {62.8 \ textbf {kJ}} {89.8 \ textbf {kJ}}} [/ latex] [latex] \ boldsymbol {\ times100 \% = 69.9 \%}. [/ Latex]
Обсуждение
В этом примере тепло, передаваемое контейнеру, составляет значительную долю от общего переданного тепла. Хотя вес кастрюли в два раза больше, чем у воды, удельная теплоемкость воды более чем в четыре раза больше, чем у алюминия.Следовательно, для достижения заданного изменения температуры воды требуется чуть более чем в два раза больше тепла по сравнению с алюминиевым поддоном.
Рисунок 2. Дымящиеся тормоза этого грузовика – видимое свидетельство механического эквивалента тепла.Пример 2: Расчет повышения температуры в результате работы, проделанной с веществом: перегрев тормозов грузовика на спуске
Тормоза грузовика, используемые для контроля скорости на спуске, работают, преобразуя гравитационную потенциальную энергию в повышенную внутреннюю энергию (более высокую температуру) тормозного материала.{\ circ} \ textbf {C}} [/ latex], если материал сохраняет 10% энергии от грузовика массой 10 000 кг, спускающегося на 75,0 м (в вертикальном перемещении) с постоянной скоростью.
Стратегия
Если тормоза не применяются, потенциальная гравитационная энергия преобразуется в кинетическую энергию. При срабатывании тормозов потенциальная гравитационная энергия преобразуется во внутреннюю энергию тормозного материала. Сначала мы вычисляем гравитационную потенциальную энергию [latex] \ boldsymbol {(Mgh)} [/ latex], которую весь грузовик теряет при спуске, а затем находим повышение температуры, возникающее только в тормозном материале.{\ circ} \ textbf {C}}. [/ latex]
Обсуждение
Эта температура близка к температуре кипения воды. Если бы грузовик ехал какое-то время, то непосредственно перед спуском температура тормозов, вероятно, была бы выше, чем температура окружающей среды. Повышение температуры при спуске, вероятно, приведет к повышению температуры тормозного материала выше точки кипения воды, поэтому этот метод непрактичен. Однако та же самая идея лежит в основе недавней гибридной технологии автомобилей, в которой механическая энергия (гравитационная потенциальная энергия) преобразуется тормозами в электрическую энергию (аккумулятор).
| Вещества | Удельная теплоемкость ( c ) | |
|---|---|---|
| Твердые вещества | Дж / кг⋅ºC | ккал / кг⋅ºC 2 |
| Алюминий | 900 | 0,215 |
| Асбест | 800 | 0,19 |
| Бетон, гранит (средний) | 840 | 0,20 |
| Медь | 387 | 0.0924 |
| Стекло | 840 | 0,20 |
| Золото | 129 | 0,0308 |
| Человеческое тело (в среднем при 37 ° C) | 3500 | 0,83 |
| Лед (в среднем, от -50 ° C до 0 ° C) | 2090 | 0,50 |
| Чугун, сталь | 452 | 0,108 |
| Свинец | 128 | 0,0305 |
| Серебро | 235 | 0.0562 |
| Дерево | 1700 | 0,4 |
| Жидкости | ||
| Бензол | 1740 | 0,415 |
| этанол | 2450 | 0,586 |
| Глицерин | 2410 | 0,576 |
| Меркурий | 139 | 0,0333 |
| Вода (15,0 ° C) | 4186 | 1.000 |
| Газы 3 | ||
| Воздух (сухой) | 721 (1015) | 0,172 (0,242) |
| Аммиак | 1670 (2190) | 0,399 (0,523) |
| Двуокись углерода | 638 (833) | 0,152 (0,199) |
| Азот | 739 (1040) | 0,177 (0,248) |
| Кислород | 651 (913) | 0.156 (0,218) |
| Пар (100 ° C) | 1520 (2020) | 0,363 (0,482) |
| Таблица 1. Удельная теплоемкость 1 различных веществ | ||
Обратите внимание, что Пример 2 является иллюстрацией механического эквивалента тепла. В качестве альтернативы повышение температуры может быть произведено с помощью паяльной лампы, а не механически.
Пример 3: Расчет конечной температуры при передаче тепла между двумя телами: заливка холодной воды в горячую кастрюлю
Допустим, вы налили 0.{\ circ} \ textbf {C}}. [/ latex] Предположим, что кастрюля стоит на изолированной подушке и выкипает незначительное количество воды. Какова температура, когда вода и поддон через короткое время достигают теплового равновесия?
Стратегия
Сковорода помещается на изолирующую подкладку так, чтобы теплоотдача с окружающей средой была незначительной. Изначально кастрюля и вода не находятся в тепловом равновесии: кастрюля имеет более высокую температуру, чем вода. Затем теплообмен восстанавливает тепловое равновесие, когда вода и поддон соприкасаются. {\ circ} \ textbf {C})}.{\ circ} \ textbf {C})}. [/ latex]
[латекс] \ begin {array} {rcl} \ boldsymbol {Q _ {\ textbf {cold}} + Q _ {\ textbf {hot}}} & \ boldsymbol {=} & \ boldsymbol {0,} \\ \ boldsymbol {Q _ {\ textbf {cold}}} & \ boldsymbol {=} & \ boldsymbol {-Q _ {\ textbf {hot}},} \\ \ boldsymbol {m _ {\ textbf {W}} c _ {\ textbf {W }} (T _ {\ textbf {f}} – 20.{\ circ} \ textbf {C}}? [/ latex] Причина в том, что вода имеет большую удельную теплоемкость, чем большинство обычных веществ, и поэтому претерпевает небольшое изменение температуры при данной теплопередаче. Большой водоем, например озеро, требует большого количества тепла для значительного повышения температуры. Это объясняет, почему температура в озере остается относительно постоянной в течение дня, даже когда изменение температуры воздуха велико. Однако температура воды действительно меняется в течение длительного времени (например, с лета на зиму).
ЭКСПЕРИМЕНТ НА ДОМУ: ИЗМЕНЕНИЕ ТЕМПЕРАТУРЫ ЗЕМЛИ И ВОДЫ
Что нагревается быстрее, земля или вода?
Для изучения разницы в теплоемкости:
- Поместите равные массы сухого песка (или почвы) и воды одинаковой температуры в две небольшие банки. (Средняя плотность почвы или песка примерно в 1,6 раза больше плотности воды, поэтому вы можете получить примерно равную массу, используя [латекс] \ boldsymbol {50 \%} [/ латекс] больше воды по объему.)
- Нагрейте оба предмета (с помощью духовки или нагревательной лампы) одинаковое время.
- Запишите конечную температуру двух масс.
- Теперь доведите обе банки до одинаковой температуры, нагревая их в течение более длительного периода времени.
- Снимите банки с источника тепла и измеряйте их температуру каждые 5 минут в течение примерно 30 минут.
Какой образец остывает быстрее всего? Эта деятельность воспроизводит явления, ответственные за дующий с суши и морской бриз. {\ circ} \ textbf {C}}? [/ латекс]
- Передача тепла [латекс] \ boldsymbol {Q} [/ latex], которая приводит к изменению [латекса] \ boldsymbol {\ Delta {T}} [/ latex] температуры тела с массой [латекс] \ boldsymbol {m} [/ latex] – это [латекс] \ boldsymbol {Q = mc \ Delta {T}}, [/ latex], где [latex] \ boldsymbol {c} [/ latex] – удельная теплоемкость материала. .Это соотношение также можно рассматривать как определение удельной теплоемкости.
Концептуальные вопросы
1: Какие три фактора влияют на теплопередачу, необходимую для изменения температуры объекта?
2: Тормоза в автомобиле повышают температуру на [латекс] \ boldsymbol {\ Delta {T}} [/ latex] при остановке автомобиля на скорости [латекс] \ boldsymbol {v}. [/ latex] Насколько лучше был бы [latex] \ boldsymbol {\ Delta {T}} [/ latex], если бы автомобиль изначально имел в два раза большую скорость? Вы можете предположить, что автомобиль останавливается достаточно быстро, чтобы не отводить тепло от тормозов.{\ circ} \ textbf {C}}: [/ latex] (а) вода; (б) бетон; (в) сталь; и d) ртуть.
5: Потирание рук согревает их, превращая работу в тепловую энергию. Если женщина трет руки взад и вперед в общей сложности 20 движений на расстоянии 7,50 см на каждый натирание и со средней силой трения 40,0 Н, каково повышение температуры? Масса согреваемых тканей всего 0,100 кг, в основном в ладонях и пальцах.
6: Блок чистого материала массой 0,250 кг нагревается от [латекса] \ boldsymbol {20.{\ circ} \ textbf {C}} [/ latex] путем добавления 4,35 кДж энергии. Вычислите его удельную теплоемкость и определите вещество, из которого он, скорее всего, состоит.
7: Предположим, что одинаковые количества тепла передаются различным массам меди и воды, вызывая одинаковые изменения температуры. Какое отношение массы меди к воде?
8: (a) Количество килокалорий в пище определяется калориметрическими методами, при которых пища сжигается и измеряется теплоотдача.{\ circ} \ textbf {C}} [/ latex] через 30,0 мин, если предположить, что тело продолжает вырабатывать энергию со скоростью 150 Вт? [латекс] \ boldsymbol {(1 \ textbf {watt} = \: 1 \ textbf {джоуль в секунду или} 1 \ textbf {W} = \: 1 \ textbf {Дж / с})}. [/ latex]
10: Даже при остановке после периода нормальной эксплуатации большой промышленный ядерный реактор передает тепловую энергию со скоростью 150 МВт за счет радиоактивного распада продуктов деления. Эта теплопередача вызывает быстрое повышение температуры, если система охлаждения выходит из строя [латекс] \ boldsymbol {(1 \ textbf {watt} = \: 1 \ textbf {джоуль в секунду или} 1 \ textbf {W} = \: 1 \ textbf {Дж / с и} 1 \ textbf {MW} = \: 1 \ textbf {мегаватт})}.{\ circ} \ textbf {C}}, [/ latex], если не указано иное, и при среднем давлении 1,00 атм. Значения в скобках: [латекс] \ boldsymbol {c _ {\ textbf {p}}} [/ latex] при постоянном давлении 1,00 атм.
Глоссарий
- удельная теплоемкость
- количество тепла, необходимое для изменения температуры 1,00 кг вещества на 1,00 ºC
Решения
Проверьте свое понимание
1: Теплопередача зависит только от разницы температур.
