Как определить металлические свойства по таблице Менделеева
Статьи › Находится › Где находятся металлы в таблице менделеева
Металлические свойства усиливаются в группах сверху вниз. В каждой главной подгруппе наиболее выражены металлические свойства у элементов седьмого периода. В периодах происходит ослабление металлических свойств. В каждом периоде самые сильные металлические свойства у элементов IA группы, то есть у щелочных металлов.
- Как определить металлические свойства элементов
- Как усиливаются металлические свойства в таблице
- Как определить свойства химических элементов
- Как по таблице Менделеева определить кислотные свойства
- Как определить у какого элемента наиболее выражены металлические свойства
- Как определять металлические и неметаллические свойства
- Как определить металл в таблице
- Как определить возрастание металлических свойств
- Как определить металл или не металл
- Что такое металлические свойства
- Что определяет химические свойства металлов
- Как определить кислотные или основные свойства
- Как доказать кислотные свойства
- Какие элементы в таблице Менделеева металлы
- Как определить порядок возрастания металлических свойств
- Какой элемент имеет более выраженные металлические свойства
- Какие неметаллы проявляют металлические свойства
Как определить металлические свойства элементов
Металлические свойства — способность атомов отдавать электроны. Именно наличием свободных электронов объясняются общие физические свойства металлов: высокая электропроводность и теплопроводность, характерный металлический блеск, ковкость. Металлические свойства усиливаются в группах сверху вниз.
Именно наличием свободных электронов объясняются общие физические свойства металлов: высокая электропроводность и теплопроводность, характерный металлический блеск, ковкость. Металлические свойства усиливаются в группах сверху вниз.
Как усиливаются металлические свойства в таблице
При перемещении вдоль периода СПРАВА НАЛЕВО металлические свойства элементов УСИЛИВАЮТСЯ. В обратном направлении возрастают неметаллические.
Как определить свойства химических элементов
Химические свойства элемента, его способность вступать в реакции с другими веществами и элементами, полностью определяются строением электронной оболочки атома. Именно процессы взаимодействия оболочек и изучает химия. Строение электронной оболочки в свою очередь полностью определяется количеством электронов в атоме.
Как по таблице Менделеева определить кислотные свойства
Основные свойства зависят от металлических свойств и меняются точно так же — в периодах увеличиваются справа налево, а в группах — сверху вниз. Кислотные свойства зависят уже от неметаллических свойств и меняются соответствующим образом — увеличиваются слева направо в периодах, а в группах — снизу вверх.
Кислотные свойства зависят уже от неметаллических свойств и меняются соответствующим образом — увеличиваются слева направо в периодах, а в группах — снизу вверх.
Как определить у какого элемента наиболее выражены металлические свойства
Наиболее ярко металлические свойства выражены у щелочных металлов (Li, Na, K, Rb, Cs, Fr), что обусловлено низким значением энергий ионизации их атомов. Это очень мягкие металлы (можно резать ножом), обладающие чрезвычайно высокой химической активностью.
Как определять металлические и неметаллические свойства
При перемещении вдоль периода СПРАВА НАЛЕВО металлические свойства элементов УСИЛИВАЮТСЯ. В обратном направлении возрастают неметаллические.
Как определить металл в таблице
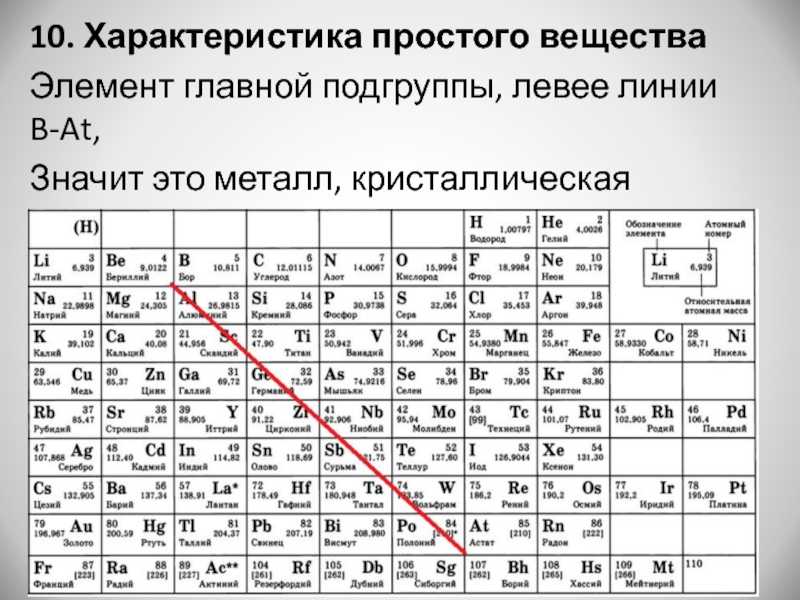
В нашей периодической таблице символы неметаллов красные, а металлов — синие. Если провести диагональ примерно из левого верхнего угла в правый нижний, то элементы главных подгрупп выше диагонали будут неметаллами, а ниже — металлами.
Как определить возрастание металлических свойств
Чем выше порядковый номер, тем выше металлические свойства.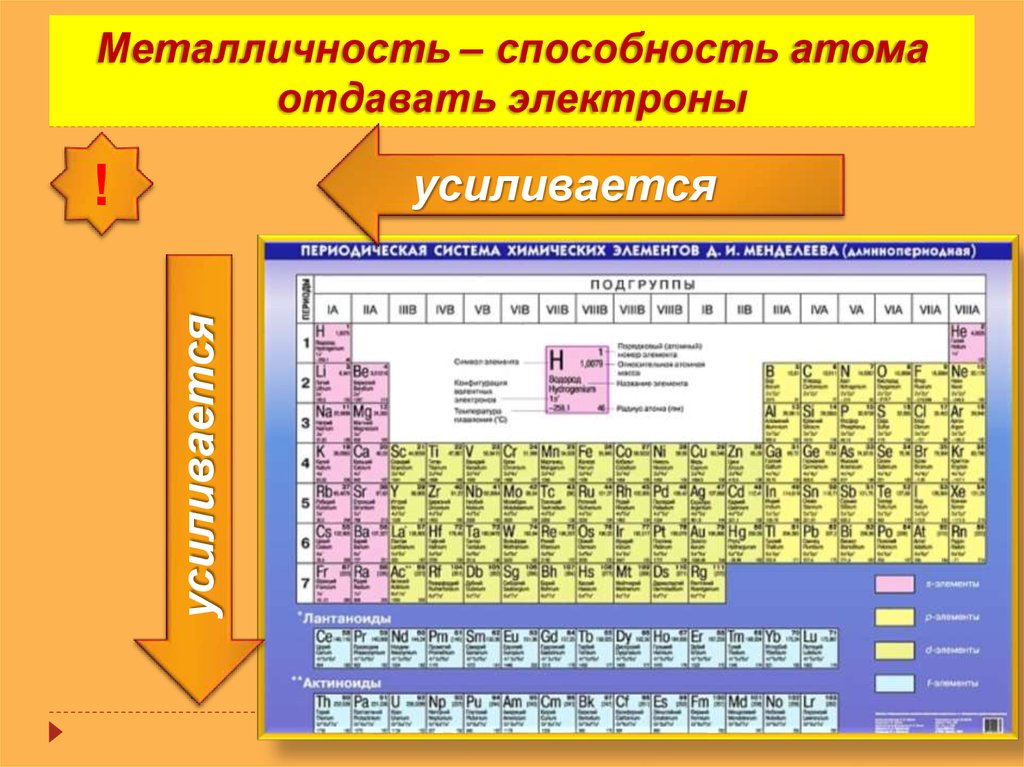 Записываем в порядке возрастания металлических свойств: B (бор), Mg (магний), Al (алюминий), Ca (кальций), Rb (рубидий), Ba (барий).
Записываем в порядке возрастания металлических свойств: B (бор), Mg (магний), Al (алюминий), Ca (кальций), Rb (рубидий), Ba (барий).
Как определить металл или не металл
Металлы можно ковать, прокатывать в листы, вытягивать в проволоку. Неметаллы не имеют общих физических свойств и не похожи на металлы. У них отсутствует металлический блеск. У большинства неметаллов низкие электропроводность и теплопроводность.
Как определить в таблице Менделеева металлы и неметаллы
Металлы расположены в левом нижнем углу таблицы, неметаллы — в правом верхнем углу. Между ними находятся полуметаллы. Все периоды, кроме первого, начинается щелочным металлом. Каждый период заканчивается инертным газом.
Что такое металлические свойства
Металлические свойства — способность атомов отдавать электроны. Именно наличием свободных электронов объясняются общие физические свойства металлов: высокая электропроводность и теплопроводность, характерный металлический блеск, ковкость. Металлические свойства усиливаются в группах сверху вниз.
Металлические свойства усиливаются в группах сверху вниз.
Что определяет химические свойства металлов
От активности металлов зависит их химические свойства. Простые вещества — металлы в окислительно-восстановительных реакциях являются восстановителями. По положению металла в электрохимическом ряду можно судить о том, насколько активно он способен вступать в химические реакции (т.
Как определить кислотные или основные свойства
По Аррениусу кислотно-основные свойства (КОС) определяются характером диссоциации веществ в водном растворе. Кислотно-основные свойства оксидов определяют по их отношению к кислотам и основаниям. Если оксид реагирует с кислотой, то ему присущи основные свойства, если с основанием − кислотные.
Как доказать кислотные свойства
Для того, что бы доказать ее кислотные свойства нам надо провести реакцию нейтрализацию ее с щелочью. Например с гидроксидом натрия. Если в результате реакции мы получим соль и воду, то можно считать свойства кислотные доказаны.
Какие элементы в таблице Менделеева металлы
Список химических элементов
№ | Название | Атомная масса (а.е.м.) |
|---|---|---|
5 | Бор | |
6 | Углерод | 12,0107 (8) |
7 | Азот | 14,0067 (2) |
8 | Кислород | 15,9994 (3) |
Как определить порядок возрастания металлических свойств
Металлические свойства элементов возрастают сверху вниз если идти по группе и уменьшаются если идти справа налево по периоду, тогда: 1)Na, Ca, Sr, Ba. Неметаллические свойства элементов возрастают справа налево, если идти по периоду, но уменьшаются при движении сверху вниз по группе, тогда: 1)С, N, S, O.
Какой элемент имеет более выраженные металлические свойства
Так как металлические свойства в ряду периодической системы уменьшаются слава на право, то в данном вопросе правильным ответом будет вариант 1- Магний. Уменьшение металлических свойств связано с тем, что число электронов на внешнем энергетическом уровне увеличивается.
Уменьшение металлических свойств связано с тем, что число электронов на внешнем энергетическом уровне увеличивается.
Какие неметаллы проявляют металлические свойства
Углерод, фосфор, селен, иод граничат с металлоидами и проявляют некоторый металлический характер, как и водород. Среди благородных газов радон является наиболее металлическим и начинает проявлять некоторое катионное поведение, что необычно для неметалла.
Оксиды — что это такое? Химические свойства и классификация
Поможем понять и полюбить химию
Начать учиться
124.6K
Знакомство с оксидами обычно начинается на уроках химии в 8 классе. Из этой статьи вы узнаете, что такое оксиды в химии, их классификацию и свойства, а также способы получения.
Определение оксидов
Оксиды — это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2.
е. бинарные соединения), один из которых — кислород в степени окисления −2.
Общая формула оксидов: ЭxOy, где Э – химический элемент, а x и y — индексы, определяемые степенью окисления химических элементов.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Виды оксидов
Все оксиды делятся на солеобразующие и несолеобразующие.
Несолеобразующие оксиды — это оксиды, которые не взаимодействуют с кислотами и щелочами, то есть не способны образовать соли.
К несолеобразующим оксидам относят: CO, SiO, N2O, NO.
Солеобразующие оксиды — это оксиды, которые взаимодействуют с кислотами и щелочами с образованием солей.
Солеобразующие оксиды делятся на три группы:
Основные оксиды — это оксиды, образованные металлами со степенью окисления +1 или +2.
Примеры основных оксидов: Na+12O, Ca+2O, Ba+2O.
Амфотерные оксиды — оксиды, образованные металлами со степенью окисления +3 или +4.
К амфотерным оксидам относят также: ZnO, BeO, PbO, SnO.
Несмотря на то, что эти металлы проявляют степень окисления +2 в данных соединениях, их оксиды проявляют амфотерные свойства.
Примеры амфотерных оксидов: Al+32O3, Fe2+3O3.
Кислотные оксиды — оксиды, образованные металлами с валентностью V и более или неметаллами с любой валентностью (за исключением несолеобразующих оксидов, то есть CO, SiO, N2O, NO).
Примеры кислотных оксидов: S+6O3, N2+5O5, Mn2+7O7.
Если один и тот же химический элемент образовывает несколько оксидов, то с увеличением степени окисления основные свойства оксидов ослабевают и усиливаются кислотные.
Например:
CrO (оксид хрома (II)) — проявляет основные свойства;
Cr2O3 (оксид хрома (III)) — проявляет амфотерные свойства;
CrO3 (оксид хрома (VI)) — проявляет кислотные свойства.
Закрепим знания о типах оксидов, изучив схему:
Номенклатура оксидов
Названия оксидов строятся по систематической номенклатуре следующим образом:
Пишем слово «оксид».

Указываем название второго химического элемента в родительном падеже.
Если этот элемент имеет переменную валентность, то указываем валентность элемента в этом соединении в скобках римской цифрой.
Примеры названий оксидов:
Fe2O3 — оксид железа (III). Читается: феррум два о три.
Na2O — оксид натрия. Читается: натрия два о.
SO3 — оксид серы (VI). Читается: эс о три.
До появления систематической номенклатуры вещества называли по присущим им специфическим свойства (цвету, запаху и т. д.). Такой способ названия веществ — тривиальная номенклатура. Некоторые названия используются и сейчас.
Названия некоторых оксидов: таблица
Химическая формула оксида | Бытовое (тривиальное название) | Возможное научное название |
|---|---|---|
| H2O | Вода | Оксид водорода |
| CO2 | Углекислый газ | Оксид углерода (IV), диоксид углерода |
| CO | Угарный газ | Оксид углерода (II), монооксид углерода |
| SO3 | Серный газ | Оксид серы (VI), триоксид серы |
| SO2 | Сернистый газ | Оксиды серы (IV), диоксид серы |
| SiO2 | Кварц, горный хрусталь, песок кварцевый, речной и морской | Оксид кремния |
| Al2O3 | Глинозем | Оксид алюминия |
| Fe2O3 | Гематит (крокус) | Оксид железа (III) |
| CaO | Негашеная известь | Оксид кальция |
Химические свойства основных оксидов
1.
 Взаимодействие с водой
Взаимодействие с водойС водой способны реагировать оксиды тех металлов, которым соответствуют растворимые гидроксиды. То есть с водой реагируют только оксиды щелочных и щелочноземельных металлов.
Основный оксид + вода = основание Например: Na |
|---|
Оксид магния взаимодействует с водой только при нагревании.
2. Взаимодействие с кислотными оксидами и кислотами
Основные оксиды, соответствующие щелочам, взаимодействуют со всеми кислотными оксидами и кислотами. Оксиды неактивных металлов взаимодействуют только с кислотными оксидами, соответствующими сильным кислотам, или с сильными кислотами.
Основный оксид + кислотный оксид = соль Например: BaO + SO3 = BaSO4
Например: Mg(OH)2 + 2HNO3 = Mg(NO3)2 + 2H2O |
|---|
3.
 Взаимодействие с амфотерными оксидами
Взаимодействие с амфотерными оксидамиВ эту реакцию могут вступать только основные оксиды щелочных или щелочноземельных металлов. При сплавлении двух оксидов образуется соль.
Основный оксид + амфотерный оксид = соль |
|---|
Как составлять такие соли: металл в этой соли берем из основного оксида, а кислотный остаток из амфотерного оксида (они проявляют более кислотные свойства).
Химические свойства кислотных оксидов
1. Взаимодействие с водой
Кислотные оксиды взаимодействуют с водой с образованием соответствующих кислот. За исключением SiO2, которому соответствует нерастворимая кремниевая кислота.
Кислотный оксид + вода = кислота Например: SO3 + H2O = H2SO4 |
|---|
2.
 Взаимодействие с основными оксидами и щелочами
Взаимодействие с основными оксидами и щелочамиКислотные оксиды сильных кислот способны взаимодействовать с любыми основными оксидами или основаниями.
Кислотный оксид + основный оксид = соль Например: SO3 + CuO = CuSO4 Кислотный оксид + основание = соль + вода Например: N2O5 + 2NaOH = 2NaNO3 + H2O |
|---|
Кислотные оксиды, соответствующие слабым кислотам (такие как CO2, SO2), способны взаимодействовать с основными оксидами, соответствующим щелочам, а также с щелочами.
3. Взаимодействие с амфотерными оксидами и гидроксидами
С амфотерными оксидами в реакцию вступают кислотные оксиды — как правило, сильных кислот.
Кислотный оксид + амфотерный оксид = соль Например: SO3 + Al2O3 = Al2(SO4)3 Кислотный оксид + амфотерный оксид = соль + вода Например: SO3 + Al(OH)3 = Al2(SO4)3 + H2O |
|---|
Химические свойства амфотерных оксидов
1. Взаимодействие с водой
Амфотерные оксиды не взаимодействуют с водой — даже при нагревании!
Амфотерный оксид + вода ≠ |
|---|
2. Взаимодействие с кислотными оксидами и кислотой
Амфотерные оксиды взаимодействуют только с сильными и средними кислотами и их оксидами.
Амфотерный оксид + кислотный оксид = соль Например: Al2O3 + N2O5 = 2Al(NO3)3 Амфотерный оксид + кислота = соль + вода Например: Al2O3 + 6HCl = 2AlCl3 + 3H2O |
|---|
3. Взаимодействие с основными оксидами
Амфотерные оксиды взаимодействуют только с теми оксидами, которые соответствуют щелочам. Реакция протекает только в расплаве, так как в растворе такие оксиды взаимодействуют преимущественно с водой с образованием щелочей.
Амфотерный оксид + основный оксид (расплав) = соль Например: Al2O3 + Na2O = 2NaAlO2 |
|---|
4.
 Взаимодействие со щелочами
Взаимодействие со щелочамиПродукты взаимодействия амфотерных оксидов со щелочами зависят от условий проведения реакции. В растворе образуются комплексные соли, а при сплавлении – средние соли.
Амфотерный оксид + щелочь (раствор) + вода = комплексная соль Например: Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4] Амфотерный оксид + щелочь (расплав) = средняя соль + вода Например: ZnO + 2KOH = K2ZnO2 + H2O |
|---|
Получение оксидов
1. Окисление металлов
Почти все металлы окисляются кислородом до устойчивых степеней окисления.
Например: 4Al + 3O2 = 2Al2O3
Исключение
Не взаимодействуют с кислородом: платина, золото и палладий.
Металлы с переменной степенью окисления, как правило, образуют соединения в степени окисления +3:
4Cr + 3O2 = 2Cr2O3
При взаимодействии щелочных металлов (элемента IA группы) образуются пероксиды Me2O2 или надпероксиды MeO2, где Ме — щелочной металл.
2. Окисление простых веществ — неметаллов
При окислении неметаллов в избытке кислорода, как правило, образуются высшие оксиды (это оксиды, в которых неметалл проявляют высшую степень окисления):
4P + 5O2 (избыток) = 2P2O5
При недостаточном количестве кислорода образуются оксиды неметаллов в промежуточной степени окисления:
4P + 3O2 (недостаток) = 2P2O3
Существуют и исключения. Например, сера окисляется лишь до оксида серы (IV) даже в избытке кислорода:
S + O2 = SO2
Или азот, который взаимодействует с кислородом только при температуре 2 000̊С или под действием электрического разряда с образованием оксида азота (II):
N2 + O2 = 2NO
Запомнить
Галогены (элементы VIIA группы) вовсе не взаимодействуют с кислородом, так же как и инертные газы (элементы VIIIA группы).
3. Разложение гидроксидов
Некоторые кислоты и гидроксиды неустойчивы и самопроизвольно разлагаются по схеме:
Гидроксид (кислота) = оксид + вода
Например:
H2SO3 = SO2↑ + H2O
H2CO3 = CO2↑ + H2O
Ag(OH) = Ag2O + H2O
NH4OH = NH3↑ + H2O
Оксиды тяжелых металлов (нерастворимые гидроксиды) и кремниевая кислота разлагаются при нагревании по той же самой схеме.
Например:
4. Окисление сложных веществ
Сложные бинарные (состоящие из двух химических элементов) соединения окисляются с образованием двух оксидов этих элементов в устойчивых степенях окисления.
Например:
2H2S + 3O2 = 2SO2 + 2H2O
4NH3 + 5O2 = 4NO + 6H2O
Также оксиды получают разложением солей, например, карбонатов, нитратов сульфатов и т. д.
д.
Например, Li2CO3 = Li2O + CO2↑
Мы узнали, какие вещества в химии называют оксидами, какие бывают оксиды, а также разобрали свойства каждого вида. Осталось подкрепить теорию практикой — а сделать это можно на курсах по химии в онлайн-школе Skysmart!
Татьяна Сосновцева
К предыдущей статье
Ковалентные неполярные и полярные связи
К следующей статье
121.2K
Химические свойства металлов
Получите план обучения, который поможет понять и полюбить химию
На вводном уроке с методистом
Выявим пробелы в знаниях и дадим советы по обучению
Расскажем, как проходят занятия
Подберём курс
Свойства кислот и оснований
Основные понятия
Что такое кислота? В этом уроке вы узнаете об отличительных свойствах кислот и оснований, о том, что отличает кислоту от основания, а также о том, что такое амфотерное соединение. Если вам понравилась эта статья, обязательно ознакомьтесь с другими нашими руководствами по кислотно-щелочной технике, ссылка на которые приведена ниже.
Если вам понравилась эта статья, обязательно ознакомьтесь с другими нашими руководствами по кислотно-щелочной технике, ссылка на которые приведена ниже.
Связанные статьи
- Сильные кислоты и основания
- Что такое рН?
- Кислотно-основная химия
- Кислотно-основные теории
Что такое кислоты и основания?
В настоящее время существует три определения кислот и оснований, определяющих их поведение в растворах. Это определения Льюиса, Бренстеда-Лоури и Аррениуса. Итак, что такое кислота ? По сути, кислоты принимают электронные пары и отдают протоны водорода. Напротив, основания отдают электроны и принимают протоны водорода. В дополнение к этим определениям кислоты и основания можно классифицировать по их свойствам. Эти свойства включают pH, вкус, текстуру, реакционную способность и электропроводность.
Название «кислота» происходит от латинского acidus , что означает «кислый», и относится к кислому вкусу и резкому запаху многих кислот. Узнайте, как называть кислоты здесь.
Узнайте, как называть кислоты здесь.
рН кислот и оснований
Шкала рН представляет собой меру кислотности или щелочности раствора и варьируется от 0 до 14. Как вы можете видеть на изображении выше, кислые растворы имеют рН менее 7, тогда как основания имеют pH выше 7. Растворы с pH 7, такие как вода (H 2 O), считаются нейтральный . Существует множество различных способов измерения рН раствора, но наиболее распространенными являются два метода: использование индикаторов и зондов. Зонды, как правило, более точны, потому что устройство помещается в раствор и считывается в цифровом виде. Между тем, с индикаторами вы должны использовать свои глаза, чтобы наблюдать за любым изменением цвета и сравнивать его со шкалой pH. Одним из видов индикатора является лакмусовая бумага. Кислоты окрашивают синюю лакмусовую бумагу в красный цвет, а основания окрашивают красную лакмусовую бумагу в синий цвет. Обратите внимание, как это соотносится с цветами на изображении выше.
Итак, что означает, что раствор является кислым или щелочным? Кислые растворы имеют высокую концентрацию протонов водорода, в то время как основные растворы имеют высокую концентрацию ионов гидроксида. Когда эти два раствора объединяются, они компенсируют друг друга в так называемой реакции нейтрализации . В этой реакции продуктами являются соли и вода, которая образуется при объединении протонов водорода и ионов гидроксида.
Вкус и консистенция кислот и оснований
Еще одним отличительным признаком между кислотами и основаниями является вкус и текстура. Следует отметить, что вы всегда должны следовать правилам безопасности в лаборатории, и никогда не потребляйте и не прикасайтесь к химическим веществам . До того, как эти правила были закреплены в камне, чтобы защитить нас, химики пробовали химические вещества на вкус. На самом деле, известный физик и математик сэр Исаак Ньютон попробовал более сотни различных химических веществ, когда занимался алхимией. Среди них был элемент ртуть, который очень токсичен и был приписан его смерти. Как упоминалось ранее, кислые растворы имеют высокую концентрацию ионов водорода. Это делает вкус кислот терпким или кислым. Хотя вы никогда не должны употреблять кислоты в лаборатории, вы можете связать это со вкусом лимона. Лимоны кислые, так как содержат большое количество лимонной кислоты. Кроме того, лимоны имеют рН около 2-3, что хорошо относится к кислой категории по шкале рН. Что касается основ, то они имеют тенденцию быть горькими на вкус. Примером этого может быть, если вы когда-либо пробовали мыльный пузырь.
Среди них был элемент ртуть, который очень токсичен и был приписан его смерти. Как упоминалось ранее, кислые растворы имеют высокую концентрацию ионов водорода. Это делает вкус кислот терпким или кислым. Хотя вы никогда не должны употреблять кислоты в лаборатории, вы можете связать это со вкусом лимона. Лимоны кислые, так как содержат большое количество лимонной кислоты. Кроме того, лимоны имеют рН около 2-3, что хорошо относится к кислой категории по шкале рН. Что касается основ, то они имеют тенденцию быть горькими на вкус. Примером этого может быть, если вы когда-либо пробовали мыльный пузырь.
Опять же, вы никогда не должны преднамеренно прикасаться к химическим веществам на коже, так как они могут быть вредными и абразивными. Однако, если бы это произошло в лаборатории, вы могли бы определить, является ли это кислотой или основанием на основе прикосновения. Если раствор кажется мыльным или скользким, это основа. Это связано с тем, что основания растворяют жирные кислоты из нашей кожи и, по сути, превращают нашу кожу в мыло. Между тем, кислоты обычно грубы на ощупь.
Между тем, кислоты обычно грубы на ощупь.
Реакционная способность кислот и оснований
Реакция омыленияРеакции с металлами
Когда кислоты реагируют с металлами, результат очень похож на реакцию нейтрализации. Единственная разница в том, что вместо воды вы будете получать газообразный водород. Независимо от того, какая кислота или металл используются, они всегда будут производить соль и H 2 газ. Одним из примеров этого является реакция между магнием и соляной кислотой. При объединении в результате образуются хлорид магния и газообразный водород. Что касается оснований, то они обычно не реагируют с металлами, но есть несколько металлов, которые составляют исключения, такие как цинк и алюминий. Эти реакции также приводят к солям и газообразному водороду.
Реакции с карбонатами
Кислоты также могут реагировать с карбонатами, в этом случае образуются соль, вода и углекислый газ. Карбонаты образуются при соединении с металлами или органическими соединениями. Уникальной особенностью здесь является производство углекислого газа. Этим можно манипулировать в лаборатории, чтобы определить, является ли неизвестный раствор щелочным или кислым. Просто добавьте раствор карбоната, и если образуется углекислый газ, раствор, вероятно, будет кислым.
Уникальной особенностью здесь является производство углекислого газа. Этим можно манипулировать в лаборатории, чтобы определить, является ли неизвестный раствор щелочным или кислым. Просто добавьте раствор карбоната, и если образуется углекислый газ, раствор, вероятно, будет кислым.
Реакции с жирами/маслами
Ранее в статье упоминалось, что основы растворяют масла на нашей коже и, по сути, превращают нашу кожу в мыло. Этот процесс растворения жиров и масел называется гидролизом, а в присутствии основания — омылением. По сути, эта реакция означает, что основания соединяются с жирами с образованием глицерина или мыла.
Проводимость кислот и оснований
В этой статье мы говорили о том, как кислоты и основания могут ионизироваться в протоны водорода и ионы гидроксида при помещении в раствор. Электролиты представляют собой соли/молекулы, которые полностью ионизируются в полярных веществах, таких как вода. По этой причине сильные кислоты и основания также являются сильными электролитами. Эти электролиты способны проводить электричество в водном состоянии, потому что их ионы подвижны.
Эти электролиты способны проводить электричество в водном состоянии, потому что их ионы подвижны.
Сводная карта сравнения
| Свойства | кислоты | Основы |
| Вкус | ||
| Вкус | 70080 | |
| 0080 | Горьба | |
| Текстура | Грубая | SOPURE и Slippery |
| PH | Менее 7 | больше 7 |
| LIPMAR | . —->Синий | |
| Реакционная способность | – Реагирует с металлами с образованием газа h3 – Реагирует с карбонизированными соединениями с образованием CO2 | – Обычно не реагирует с металлами или с карбонизированными соединениями – Реагирует с маслами и жирами |
| Проводит электричество в воде | да | да |
| Примеры | аммиачная вода (гидроксид аммиака) |
Что такое амфотерное соединение?
Если соединение является амфотерным, оно может реагировать либо как кислота, либо как основание. Амфотерные соединения обычно представляют собой оксиды или гидроксиды металлов. Они реагируют с кислотами с образованием соли металла и с сильным основанием с образованием многоатомного иона металла. Для реакции с основанием амфотерный гидроксид часто должен быть получен свежеприготовленным, а основание должно быть горячим и концентрированным. В следующем примере оксид цинка превращается в ион цинката Zn(OH) 4 – в составе растворимого цинката натрия при добавлении к концентрированной основе.
Амфотерные соединения обычно представляют собой оксиды или гидроксиды металлов. Они реагируют с кислотами с образованием соли металла и с сильным основанием с образованием многоатомного иона металла. Для реакции с основанием амфотерный гидроксид часто должен быть получен свежеприготовленным, а основание должно быть горячим и концентрированным. В следующем примере оксид цинка превращается в ион цинката Zn(OH) 4 – в составе растворимого цинката натрия при добавлении к концентрированной основе.
- в кислоте: Zno + H 2 SO 4 → ZnSO 4 + H 2 O
- в основании: Zno + 2 NaOH + H 2 O → Na 2 (ZN (ZN + H 2 O → Na 2 (ZN + H 2 O → NA 2 OH) 4 ]
Примеры амфотерных соединений
Гидроксид хрома, гидроксид олова, гидроксид свинца, гидроксид кобальта, гидроксид цинка, оксид цинка, гидроксид алюминия и оксид алюминия.
Что такое полипротонная кислота?
Некоторые кислоты имеют более одного кислотного протона, например серная кислота или фосфорная кислота. Эти соединения имеют много интересных свойств и применений. Для получения дополнительной информации см. наш учебник по полипротоновым кислотам.
Видео, показывающее свойства кислоты
В этом видео ChemTalk соляная кислота, сильная кислота, реагирует с элементарным самарием, редкоземельным металлом. Вы можете видеть, как концентрированная и разбавленная кислота дают разные результаты. Подписывайтесь на наш канал на Youtube — скоро будет больше потрясающих видео!Дополнительная литература
- Что такое pKa?
- Количественное определение протонов, нейтронов и электронов
- Расчет молярной массы
Кислотно-основные характеристики оксидов и гидроксидов
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 68247
Слева направо в таблице Менделеева кислотно-щелочной характер оксидов и гидроксидов переходят от основного к кислому. (3+) (водн.)
(3+) (водн.)
–(OH-)–> [Al(OH)4]-(водн.)
Оксиды неметаллов
– Ковалентная связь: почти полное распределение электронной волновой функции
– Ковалентные оксиды обычно кислые (элементы действуют как кислота при взаимодействии с h3O)
SO3 + h3O(ж) -> h3SO4(водн.) -> H+ + HSO4-
A. Оксид A Гидроксид
Ионные гидриды
Типы гидридов– Ионная связь: нет распределения волновой функции электронов
– Основные вещества Бренстеда, потому что они будут реагировать с протоном
– Основной Льюис, поскольку они могут быть лигандами
Cah3 + 2h3O -> 2h3 + Ca(OH)2
Н- Н+ h3
– В этом случае Cah3 является основным, потому что он реагирует с водой (в данном случае с кислотой) с образованием многих гидридов путем восстановления протона.
Ковалентные гидриды
– Ковалентная связь: почти полное распределение волновой функции электрона
HF + h3O -> F- + h4O+ ….также может быть записано как HF(aq) <--> H+(aq) + F-(водн. )
)
H+ H+ H+
– HF является слабой кислотой, которая является кислотой бронстеда, потому что она теряет протон. Следовательно, HF — это слабая кислота, где вода действует как тихая вода, а F- — это слабое сопряженное основание.
Участники
- Шаблон:ContribChem230
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Лицензия
- СС BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.

