Количество теплоты: формула, расчет
Что быстрее нагреется на плите – чайник или ведро воды? Ответ очевиден – чайник. Тогда второй вопрос – почему?
Ответ не менее очевиден – потому что масса воды в чайнике меньше. Отлично. А теперь вы можете проделать самостоятельно самый настоящий физический опыт в домашних условиях. Для этого вам понадобится две одинаковые небольшие кастрюльки, равное количество воды и растительного масла, например, по пол-литра и плита. На одинаковый огонь ставите кастрюльки с маслом и водой. А теперь просто наблюдайте, что быстрее будет нагреваться. Если есть градусник для жидкостей, можно применить его, если нет, можно просто пробовать температуру время от времени пальцем, только осторожно, чтобы не обжечься. В любом случае вы вскоре убедитесь, что масло нагревается значительно быстрее воды. И еще один вопросик, который тоже можно реализовать в виде опыта. Что быстрее закипит – теплая вода или холодная? Все снова очевидно – теплая будет на финише первой.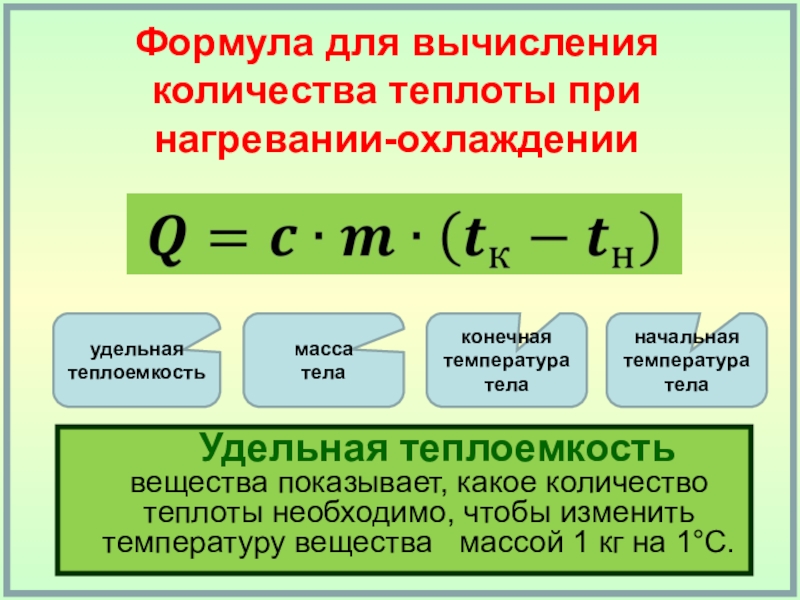
Количество теплоты
Количество теплоты – это энергия, которую тело теряет или приобретает при теплопередаче. Это понятно и из названия. При остывании тело будет терять некое количество теплоты, а при нагревании – поглощать. А ответы на наши вопросы показали нам, от чего зависит количество теплоты? Во-первых, чем больше масса тела, тем большее количество теплоты надо затратить на изменение его температуры на один градус. Во-вторых, количество теплоты, необходимое для нагревания тела, зависит от того вещества, из которого оно состоит, то есть от рода вещества. И в-третьих, разность температур тела до и после теплопередачи также важна для наших расчетов. Исходя из всего вышесказанного, мы можем
Q=cm(t_2-t_1 ) ,
где Q – количество теплоты,
m – масса тела,
(t_2-t_1 ) – разность между начальной и конечной температурами тела,
c – удельная теплоемкость вещества, находится из соответствующих таблиц.
По этой формуле можно произвести расчет количества теплоты, которое необходимо, чтобы нагреть любое тело или которое это тело выделит при остывании.
Измеряется количество теплоты в джоулях (1 Дж), как и всякий вид энергии. Однако, величину эту ввели не так давно, а измерять количество теплоты люди начали намного раньше. И пользовались они единицей, которая широко используется и в наше время – калория (1 кал). 1 калория – это такое количество теплоты, которое потребуется для нагреванияь 1 грамма воды на 1 градус Цельсия. Руководствуясь этими данными, любители подсчитывать калории в съедаемой пище, могут ради интереса подсчитать, сколько литров воды можно вскипятить той энергией, которую они потребляют с едой в течение дня.
Нужна помощь в учебе?
Предыдущая тема: Излучение: сущность, опыт, энергия
Следующая тема:   Удельная теплоёмкость: расчет количества теплоты
Количество теплоты. Удельная теплоемкость вещества :: Класс!ная физика
КОЛИЧЕСТВО ТЕПЛОТЫ
При теплопередаче (теплообмене) внутренняя энергия одних тел уменьшается, а других – увеличивается, без изменения механической энергии тел и без совершения работы.
При этом уменьшается внутренняя энергия тела-нагревателя, а внутренняя энергия нагреваемого тела увеличивается .
Процесс теплопередачи характеризуется количеством теплоты.
Количеством теплоты (Q) называется изменение внутренней энергии тела, происходящее в результате теплопередачи.
Количество теплоты измеряется в системе СИ в джоулях.
[Q] = 1Дж.
Кроме того, для измерения количества теплоты (вне системы СИ) используется единица, называемая калорией (кал).
1 калория равна количеству теплоты, необходимому для нагревания 1 г воды на 1 градус С.
Опытным путем было установлено, что для нагревания 1 г воды на 1 градус требуется
совершить работу в 4,18 Дж, следовательно 1кал = 4,18Дж.
УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ ВЕЩЕСТВА
Удельная теплоемкость вещества показывает, какое количество теплоты необходимо, чтобы изменить температуру единицы массы данного вещества на 1°С.
Единица удельной теплоемкости в системе СИ :
[c] = 1Дж/кг·градусС.
Удельную теплоемкость данного вещества можно приближенно считать постоянной величиной.
У разных веществ удельная теплоемкость имеет разные значения.
Если одинаковым по массе телам из разных веществ передать одно и то же количество теплоты, то они нагреются до разной температуры. Вещество с меньшей теплоемкостью нагреется сильнее,
а вещество с большей теплоемкостью – слабее.
КНИЖНАЯ ПОЛКА
Глобальное потепление. Ведет ли оно к катастрофе?
ИНТЕРЕСНО
что песок обладает малой удельной теплоемкостью, поэтому быстро нагревается и охлаждается.
Устали? – Отдыхаем!
Количество теплоты – материалы для подготовки к ЕГЭ по Физике
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: количество теплоты, удельная теплоёмкость вещества, уравнение теплового баланса.
Как мы знаем, одним из способов изменения внутренней энергии является теплопередача (теплообмен). Предположим, что тело участвует в теплообмене с другими телами, и при этом не совершается механическая работа — ни самим телом, ни другими телами над этим телом.
Если в процессе теплообмена внутренняя энергия тела изменилась на величину , то говорят, что тело получило соответствующее количество теплоты: .
Если при этом величина отрицательна, т.е. тело отдавало энергию, то говорят также, что тело отдавало тепло. Например, вместо формально верной, но несколько нелепой фразы «тело получило —5 Дж тепла» мы скажем: «тело отдало 5 Дж тепла».
Удельная теплоёмкость вещества
Предположим, что в процессе теплообмена агрегатное состояние вещества тела не изменяется (не происходит плавление, кристаллизация, парообразование или конденсация). Начальную температуру тела обозначим , конечную температуру — .
Опыт показывает, что количество теплоты, полученное телом, прямо пропорционально массе тела и разности конечной и начальной температур:
Коэффициент пропорциональности c называется удельной теплоёмкостью вещества тела. Удельная теплоёмкость не зависит от формы и размеров тела. Удельные теплоёмкости различных веществ можно найти в таблицах.
Удельная теплоёмкость не зависит от формы и размеров тела. Удельные теплоёмкости различных веществ можно найти в таблицах.
Введя обозначение , получим также:
Чтобы понять физический смысл удельной теплоёмкости, выразим её из последней формулы:
Мы видим, что удельная теплоёмкость численно равна количеству теплоты, которое необходимо для нагревания 1кг данного вещества на
Чем больше удельная теплоёмкость вещества, тем большее количество теплоты требуется для нагревания тела данной массы на заданное количество градусов.
В задачах часто фигурируют вода и лёд. Их удельные теплоёмкости желательно помнить.
Вода: Дж/(кг·C).
Лёд: Дж/(кг·C).
Произведение удельной теплоёмкости вещества на массу тела называется теплоёмкостью тела и обозначается :
Соответственно, для количества теплоты имеем:
Уравнение теплового баланса
Рассмотрим два тела (обозначим их 1 и 2), которые образуют замкнутую систему.
Имеется фундаментальный закон природы, подтверждаемый всевозможными экспериментами — закон сохранения энергии. Он гласит, что полная энергия замкнутой системы тел не меняется со временем.
В данном случае закон сохранения энергии утверждает, что внутренняя энергия нашей системы будет оставаться одной и той же: . Если изменение внутренней энергии первого тела равно , а изменение внутренней энергии второго тела равно , то суммарное изменение внутренней энергии будет равно нулю:
Но — количество теплоты, полученное первым телом в процессе теплообмена; аналогично — количество теплоты, полученное вторым телом в процессе теплообмена. Стало быть,
(1)
Попросту говоря, сколько джоулей тепла отдало одно тело, ровно столько же джоулей получило второе тело. Так как система замкнута, ни один джоуль наружу не вышел. Соотношение (1) называется уравнением теплового баланса. В общем случае, когда тел образуют замкнутую систему и обмениваются энергией только с помощью теплопередачи, из закона сохранения энергии с помощью тех же рассуждений получаем общее уравнение теплового баланса:
Так как система замкнута, ни один джоуль наружу не вышел. Соотношение (1) называется уравнением теплового баланса. В общем случае, когда тел образуют замкнутую систему и обмениваются энергией только с помощью теплопередачи, из закона сохранения энергии с помощью тех же рассуждений получаем общее уравнение теплового баланса:
(2)
В качестве простого примера применения уравнения теплового баланса рассмотрим следующую задачу.
Смешали г воды при температуре и г воды при температуре . Найти установившуюся температуру смеси.
Обозначим искомую установившуюся температуру через . Запишем уравнение теплового баланса (1):
где — удельная теплоёмкость воды. Раскрываем скобки и находим:
Урок 23. внутренняя энергия. работа. количество теплоты – Физика – 10 класс
Работа и теплопередача как способы изменения внутренней энергии
Выражение для внутренней энергии одноатомного идеального или разреженного реального газов имеет следующий вид: $U = \frac{3}{2} \cdot \nu \cdot R \cdot T$.
Для идеального газа из молекул с двумя, тремя или большим числом атомов требуется учёт кинетической энергии вращения молекул (их уже нельзя считать материальными точками), поэтому выражение для их внутренней энергии отличается от $U = \frac{3}{2} \cdot \nu \cdot R \cdot T$, но только числовым коэффициентом.
Для двухатомного газа (например, H2, O2, CO и пр.):
$U = \frac{5}{2} \cdot \nu \cdot R \cdot T$.
Для газа с тремя атомами и более (например, CO2, CH4):
$U = 3 \cdot \nu \cdot R \cdot T$.
Чтобы изменить внутреннюю энергию вещества, нужно передать ему некоторое количество теплоты либо совершить над ним работу.
Существует три вида теплопередачи:
Теплопроводность – это процесс переноса энергии от более нагретых частей тела к менее нагретым, осуществляемый хаотически движущимися частицами тела (атомами, молекулами, электронами и т. п.). Простой пример – нагревание ложки в горячем чае.
п.). Простой пример – нагревание ложки в горячем чае.
Конвекция – вид теплопередачи, при котором внутренняя энергия передаётся струями или потоками жидкости, или газа. Пример: проветривание комнаты.
Излучение – процесс переноса энергии посредством электромагнитного излучения. Простой пример: солнечный свет.
Механическая работа меняет механическую энергию тела. В термодинамике то же самое. К примеру, если газ двигает поршень, расширяясь, то у нас, как и в механике, есть и сила, и перемещение. Разница только в том, что при совершении работы в термодинамике меняется не кинетическая или потенциальная энергия газа как целого тела, а кинетическая энергия его молекул, то есть внутренняя энергия газа.
Если газ расширяется, то работу газа принято считать положительной. Если же сжимается – то отрицательной.
Формула для нахождения работы газа при изобарном процессе примет следующий вид: $A = p \cdot \Delta V$.
Для изотермического процесса формула принимает следующий вид: $A = \nu \cdot R \cdot T \cdot ln \frac{V_2}{V_1}$.
Количество теплоты. Удельная теплоёмкость – FIZI4KA
1. Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количеством теплоты.
Количеством теплоты называется изменение внутренней энергии тела в процессе теплопередачи без совершения работы.
Количество теплоты обозначают буквой \( Q \). Так как количество теплоты является мерой изменения внутренней энергии, то его единицей является джоуль (1 Дж).
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
2. Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. \circ C) \) температур: \( Q\sim(t_2-t_1) \).
\circ C) \) температур: \( Q\sim(t_2-t_1) \).
4. Если теперь в один сосуд налить 100 г воды, а в другой такой же сосуд налить немного воды и положить в неё такое металлическое тело, чтобы его масса и масса воды составляли 100 г, и нагревать сосуды на одинаковых плитках, то можно заметить, что в сосуде, в котором находится только вода, температура будет ниже, чем в том, в котором находятся вода и металлическое тело. Следовательно, чтобы температура содержимого в обоих сосудах была одинаковой нужно воде передать большее количество теплоты, чем воде и металлическому телу. Таким образом, количество теплоты, необходимое для нагревания тела зависит от рода вещества, из которого это тело сделано.
5. Зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К), называется удельной теплоёмкостью вещества.
Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой \( c \). Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Удельная теплоёмкость свинца 140 Дж/кг °С. Это значит, что для нагревания 1 кг свинца на 1 °С необходимо затратить количество теплоты 140 Дж. Такое же количество теплоты выделится при остывании 1 кг воды на 1 °С.
Поскольку количество теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж. \circ) \]
\circ) \]
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
6. Пример решения задачи. В стакан, содержащий 200 г воды при температуре 80 °С, налили 100 г воды при температуре 20 °С. После чего в сосуде установилась температура 60 °С. Какое количество теплоты получила холодная вода и отдала горячая вода?
При решении задачи необходимо выполнять следующую последовательность действий:
- записать кратко условие задачи;
- перевести значения величин в СИ;
- проанализировать задачу, установить, какие тела участвуют в теплообмене, какие тела отдают энергию, а какие получают;
- решить задачу в общем виде;
- выполнить вычисления;
- проанализировать полученный ответ.
1. Условие задачи.
Дано:
\( m_1 \) = 200 г
\( m_2 \) = 100 г
\( t_1 \) = 80 °С
\( t_2 \) = 20 °С
\( t \) = 60 °С
______________
\( Q_1 \) — ? \( Q_2 \) — ?
\( c_1 \) = 4200 Дж/кг · °С
2. СИ: \( m_1 \) = 0,2 кг; \( m_2 \) = 0,1 кг.
СИ: \( m_1 \) = 0,2 кг; \( m_2 \) = 0,1 кг.
3. Анализ задачи. В задаче описан процесс теплообмена между горячей и холодной водой. Горячая вода отдаёт количество теплоты \( Q_1 \) и охлаждается от температуры \( t_1 \) до температуры \( t \). Холодная вода получает количество теплоты \( Q_2 \) и нагревается от температуры \( t_2 \) до температуры \( t \).
4. Решение задачи в общем виде. Количество теплоты, отданное горячей водой, вычисляется по формуле: \( Q_1=c_1m_1(t_1-t) \).
Количество теплоты, полученное холодной водой, вычисляется по формуле: \( Q_2=c_2m_2(t-t_2) \).
5. Вычисления.
\( Q_1 \) = 4200 Дж/кг · °С · 0,2 кг · 20 °С = 16800 Дж
\( Q_2 \) = 4200 Дж/кг · °С · 0,1 кг · 40 °С = 16800 Дж
6. В ответе получено, что количество теплоты, отданное горячей водой, равно количеству теплоты, полученному холодной водой. При этом рассматривалась идеализированная ситуация и не учитывалось, что некоторое количество теплоты пошло на нагревание стакана, в котором находилась вода, и окружающего воздуха. В действительности же количество теплоты, отданное горячей водой, больше, чем количество теплоты, полученное холодной водой.
При этом рассматривалась идеализированная ситуация и не учитывалось, что некоторое количество теплоты пошло на нагревание стакана, в котором находилась вода, и окружающего воздуха. В действительности же количество теплоты, отданное горячей водой, больше, чем количество теплоты, полученное холодной водой.
ПРИМЕРЫ ЗАДАНИЙ
Часть 1
1. Удельная теплоёмкость серебра 250 Дж/(кг · °С). Что это означает?
1) при остывании 1 кг серебра на 250 °С выделяется количество теплоты 1 Дж
2) при остывании 250 кг серебра на 1 °С выделяется количество теплоты 1 Дж
3) при остывании 250 кг серебра на 1 °С поглощается количество теплоты 1 Дж
4) при остывании 1 кг серебра на 1 °С выделяется количество теплоты 250 Дж
2. Удельная теплоёмкость цинка 400 Дж/(кг · °С). Это означает, что
1) при нагревании 1 кг цинка на 400 °С его внутренняя энергия увеличивается на 1 Дж
2) при нагревании 400 кг цинка на 1 °С его внутренняя энергия увеличивается на 1 Дж
3) для нагревания 400 кг цинка на 1 °С его необходимо затратить 1 Дж энергии
4) при нагревании 1 кг цинка на 1 °С его внутренняя энергия увеличивается на 400 Дж
3. \circ \)
\circ \)
4. На рисунке приведён график зависимости количества теплоты, необходимого для нагревания двух тел (1 и 2) одинаковой массы, от температуры. Сравните значения удельной теплоёмкости (\( c_1 \) и \( c_2 \)) веществ, из которых сделаны эти тела.
1) \( c_1=c_2 \)
2) \( c_1>c_2 \)
3) \( c_1<c_2 \)
4) ответ зависит от значения массы тел
5. На диаграмме представлены значения количества теплоты, переданного двум телам равной массы при изменении их температуры на одно и то же число градусов. Какое соотношение для удельных теплоёмкостей веществ, из которых изготовлены тела, является верным?
1) \( c_1=c_2 \)
2) \( c_1=3c_2 \)
3) \( c_2=3c_1 \)
4) \( c_2=2c_1 \)
6. На рисунке представлен график зависимости температуры твёрдого тела от отданного им количества теплоты. Масса тела 4 кг. Чему равна удельная теплоёмкость вещества этого тела?
1) 500 Дж/(кг · °С)
2) 250 Дж/(кг · °С)
3) 125 Дж/(кг · °С)
4) 100 Дж/(кг · °С)
7. При нагревании кристаллического вещества массой 100 г измеряли температуру вещества и количество теплоты, сообщённое веществу. Данные измерений представили в виде таблицы. Считая, что потерями энергии можно пренебречь, определите удельную теплоёмкость вещества в твёрдом состоянии.
При нагревании кристаллического вещества массой 100 г измеряли температуру вещества и количество теплоты, сообщённое веществу. Данные измерений представили в виде таблицы. Считая, что потерями энергии можно пренебречь, определите удельную теплоёмкость вещества в твёрдом состоянии.
1) 192 Дж/(кг · °С)
2) 240 Дж/(кг · °С)
3) 576 Дж/(кг · °С)
4) 480 Дж/(кг · °С)
8. Чтобы нагреть 192 г молибдена на 1 К, нужно передать ему количество теплоты 48 Дж. Чему равна удельная теплоёмкость этого вещества?
1) 250 Дж/(кг · К)
2) 24 Дж/(кг · К)
3) 4·10-3 Дж/(кг · К)
4) 0,92 Дж/(кг · К)
9. Какое количество теплоты необходимо для нагревания 100 г свинца от 27 до 47 °С?
1) 390 Дж
2) 26 кДж
3) 260 Дж
4) 390 кДж
10. На нагревание кирпича от 20 до 85 °С затрачено такое же количество теплоты, как для нагревания воды такой же массы на 13 °С. Удельная теплоёмкость кирпича равна
1) 840 Дж/(кг · К)
2) 21000 Дж/(кг · К)
3) 2100 Дж/(кг · К)
4) 1680 Дж/(кг · К)
11. Из перечня приведённых ниже высказываний выберите два правильных и запишите их номера в таблицу.
Из перечня приведённых ниже высказываний выберите два правильных и запишите их номера в таблицу.
1) Количество теплоты, которое тело получает при повышении его температуры на некоторое число градусов, равно количеству теплоты, которое это тело отдаёт при понижении его температуры на такое же число градусов.
2) При охлаждении вещества его внутренняя энергия увеличивается.
3) Количество теплоты, которое вещество получает при нагревании, идёт главным образом на увеличение кинетической энергии его молекул.
4) Количество теплоты, которое вещество получает при нагревании, идёт главным образом на увеличение потенциальной энергии взаимодействия его молекул
5) Внутреннюю энергию тела можно изменить, только сообщив ему некоторое количество теплоты
12. В таблице представлены результаты измерений массы \( m \), изменения температуры \( \Delta t \) и количества теплоты \( Q \), выделяющегося при охлаждении цилиндров, изготовленных из меди или алюминия.
Какие утверждения соответствуют результатам проведённого эксперимента? Из предложенного перечня выберите два правильных. Укажите их номера. На основании проведенных измерений можно утверждать, что количество теплоты, выделяющееся при охлаждении,
1) зависит от вещества, из которого изготовлен цилиндр.
2) не зависит от вещества, из которого изготовлен цилиндр.
3) увеличивается при увеличении массы цилиндра.
4) увеличивается при увеличении разности температур.
5) удельная теплоёмкость алюминия в 4 раза больше, чем удельная теплоёмкость олова.
Часть 2
C1.Твёрдое тело массой 2 кг помещают в печь мощностью 2 кВт и начинают нагревать. На рисунке изображена зависимость температуры \( t \) этого тела от времени нагревания \( \tau \). Чему равна удельная теплоёмкость вещества?
1) 400 Дж/(кг · °С)
2) 200 Дж/(кг · °С)
3) 40 Дж/(кг · °С)
4) 20 Дж/(кг · °С)
Ответы
Количество теплоты. Удельная теплоёмкость
Удельная теплоёмкость
Удельная теплоемкость вещества — формулы, определение, обозначение
Нагревание и охлаждение
Эти два процесса знакомы каждому. Вот нам захотелось чайку, и мы ставим чайник, чтобы нагреть воду. Или ставим газировку в холодильник, чтобы охладить.
Логично предположить, что нагревание — это увеличение температуры, а охлаждение — ее уменьшение. Все, процесс понятен, едем дальше.
Но не тут-то было: температура меняется не «с потолка». Все завязано на таком понятии, как количество теплоты. При нагревании тело получает количество теплоты, а при нагревании — отдает.
- Количество теплоты — энергия, которую получает или теряет тело при теплопередаче.
Виу-виу-виу! Внимание!
Обнаружено новое непонятное слово — теплопередача.
Минуточку, давайте закончим с количеством теплоты.
В процессах нагревания и охлаждения формулы для количества теплоты выглядят так:
Нагревание Q = cm(tконечная – tначальная) Охлаждение Q = cm(tначальная – tконечная) Q — количество теплоты [Дж] c — удельная теплоемкость вещества [Дж/кг*˚C] m — масса [кг] tконечная — конечная температура [˚C] tначальная — начальная температура [˚C] |
В этих формулах фигурирует и изменение температуры, о котором мы сказали выше, и удельная теплоемкость, речь о которой пойдет дальше.
А вот теперь поговорим о видах теплопередачи.
Виды теплопередачи
- Теплопередача — это физический процесс передачи тепловой энергии от более нагретого тела к менее нагретому.
Здесь все совсем несложно, их всего три: теплопроводность, конвекция и излучение.
Теплопроводность
Тот вид теплопередачи, который можно охарактеризовать, как способность тел проводить энергию от более нагретого тела к менее нагретому.
Речь о том, чтобы передать тепло с помощью соприкосновения. Признавайтесь, грелись же когда-нибудь возле батареи. Если вы сидели к ней вплотную, то согрелись вы благодаря теплопроводности. Обниматься с котиком, у которого горячее пузо, тоже эффективно.
Порой мы немного перебарщиваем с возможностями этого эффекта, когда на пляже ложимся на горячий песок. Эффект есть, только не очень приятный. Ну а ледяная грелка на лбу дает обратный эффект — ваш лоб отдает тепло грелке.
Конвекция
Когда мы говорили о теплопроводности, мы приводили в пример батарею. Теплопроводность — это когда мы получаем тепло, прикоснувшись к батарее. Но все вещи в комнате к батарее не прикасаются, а комната греется. Здесь вступает конвекция.
Дело в том, что холодный воздух тяжелее горячего (холодный просто плотнее). Когда батарея нагревает некий объем воздуха, он тут же поднимается наверх, проходит вдоль потолка, успевает остыть и спуститься обратно вниз — к батарее, где снова нагревается. Таким образом, вся комната равномерно прогревается, потому что все более горячие потоки сменяют все менее холодные.
Излучение
Пляж мы уже упоминали, но речь шла только о горячем песочке. А вот тепло от солнышка — это излучение. В этом случае тепло передается через волны.
Если мы греемся у камина, то получаем тепло конвекцией или излучением?🤔
Обоими способами. То тепло, которое мы ощущаем непосредственно от камина (когда лицу горячо, если вы расположились слишком близко к камину) — это излучение. А вот прогревание комнаты в целом — это конвекция.
То тепло, которое мы ощущаем непосредственно от камина (когда лицу горячо, если вы расположились слишком близко к камину) — это излучение. А вот прогревание комнаты в целом — это конвекция.
Удельная теплоемкость: понятие и формула для расчета
Формулы количества теплоты для нагревания и охлаждения мы уже разбирали, но давайте еще раз:
Нагревание Q = cm(tконечная – tначальная) Охлаждение Q = cm(tначальная – tконечная) Q — количество теплоты [Дж] c — удельная теплоемкость вещества [Дж/кг*˚C] m — масса [кг] tконечная — конечная температура [˚C] tначальная — начальная температура [˚C] |
В этих формулах фигурирует такая величина, как удельная теплоемкость. По сути своей — это способность материала получать или отдавать тепло.
По сути своей — это способность материала получать или отдавать тепло.
С точки зрения математики удельная теплоемкость вещества — это количество теплоты, которое надо к нему подвести, чтобы изменить температуру 1 кг вещества на 1 градус Цельсия:
Удельная теплоемкость вещества c= Q/m(tконечная – tначальная) Q — количество теплоты [Дж] c — удельная теплоемкость вещества [Дж/кг*˚C] m — масса [кг] tконечная — конечная температура [˚C] tначальная — начальная температура [˚C] |
Также ее можно рассчитать через теплоемкость вещества:
Удельная теплоемкость вещества c= C/m c — удельная теплоемкость вещества [Дж/кг*˚C] C — теплоемкость вещества [Дж/˚C] m — масса [кг] |
Величины теплоемкость и удельная теплоемкость означают практически одно и то же. Отличие в том, что теплоемкость — это способность всего вещества к передаче тепла. То есть формулу количества теплоты для нагревания тела можно записать в таком виде:
Отличие в том, что теплоемкость — это способность всего вещества к передаче тепла. То есть формулу количества теплоты для нагревания тела можно записать в таком виде:
Количество теплоты, необходимое для нагревания тела Q = C(tконечная – tначальная) Q — количество теплоты [Дж] c — удельная теплоемкость вещества [Дж/кг*˚C] m — масса [кг] tконечная — конечная температура [˚C] tначальная — начальная температура [˚C] |
Таблица удельных теплоемкостей
Удельная теплоемкость — табличная величина. Часто ее указывают в условии задачи, но при отсутствии в условии — можно и нужно воспользоваться таблицей. Ниже приведена таблица удельных теплоемкостей для некоторых (многих) веществ.
Газы | C, Дж/(кг·К) |
Азот N2 | 1051 |
Аммиак Nh4 | 2244 |
Аргон Ar | 523 |
Ацетилен C2h3 | 1683 |
Водород h3 | 14270 |
Воздух | 1005 |
Гелий He | 5296 |
Кислород O2 | 913 |
Криптон Kr | 251 |
Ксенон Xe | 159 |
Метан Ch5 | 2483 |
Неон Ne | 1038 |
Оксид азота N2O | 913 |
Оксид азота NO | 976 |
Оксид серы SO2 | 625 |
Оксид углерода CO | 1043 |
Пропан C3H8 | 1863 |
Сероводород h3S | 1026 |
Углекислый газ CO2 | 837 |
Хлор Cl | 520 |
Этан C2H6 | 1729 |
Этилен C2h5 | 1528 |
Металлы и сплавы | C, Дж/(кг·К) |
Алюминий Al | 897 |
Бронза алюминиевая | 420 |
Бронза оловянистая | 380 |
Вольфрам W | 134 |
Дюралюминий | 880 |
Железо Fe | 452 |
Золото Au | 129 |
Константан | 410 |
Латунь | 378 |
Манганин | 420 |
Медь Cu | 383 |
Никель Ni | 443 |
Нихром | 460 |
Олово Sn | 228 |
Платина Pt | 133 |
Ртуть Hg | 139 |
Свинец Pb | 128 |
Серебро Ag | 235 |
Сталь стержневая арматурная | 482 |
Сталь углеродистая | 468 |
Сталь хромистая | 460 |
Титан Ti | 520 |
Уран U | 116 |
Цинк Zn | 385 |
Чугун белый | 540 |
Чугун серый | 470 |
Жидкости | Cp, Дж/(кг·К) |
Азотная кислота (100%-ная) Nh4 | 1720 |
Бензин | 2090 |
Вода | 4182 |
Вода морская | 3936 |
Водный раствор хлорида натрия (25%-ный) | 3300 |
Глицерин | 2430 |
Керосин | 2085…2220 |
Масло подсолнечное рафинированное | 1775 |
Молоко | 3906 |
Нефть | 2100 |
Парафин жидкий (при 50С) | 3000 |
Серная кислота (100%-ная) h3SO4 | 1380 |
Скипидар | 1800 |
Спирт метиловый (метанол) | 2470 |
Спирт этиловый (этанол) | 2470 |
Топливо дизельное (солярка) | 2010 |
Задача
Какое твердое вещество массой 2 кг можно нагреть на 10 ˚C, сообщив ему количество теплоты, равное 7560 Дж?
Решение:
Используем формулу для нахождения удельной теплоемкости вещества:
c= Q/m(tконечная – tначальная)
Подставим значения из условия задачи:
c= 7560/2*10 = 7560/20 = 378 Дж/кг*˚C
Смотрим в таблицу удельных теплоемкостей для металлов и находим нужное значение.
Металлы и сплавы | C, Дж/(кг·К) |
Алюминий Al | 897 |
Бронза алюминиевая | 420 |
Бронза оловянистая | 380 |
Вольфрам W | 134 |
Дюралюминий | 880 |
Железо Fe | 452 |
Золото Au | 129 |
Константан | 410 |
Латунь | 378 |
Манганин | 420 |
Медь Cu | 383 |
Никель Ni | 443 |
Нихром | 460 |
Олово Sn | 228 |
Платина Pt | 133 |
Ртуть Hg | 139 |
Свинец Pb | 128 |
Серебро Ag | 235 |
Сталь стержневая арматурная | 482 |
Сталь углеродистая | 468 |
Сталь хромистая | 460 |
Титан Ti | 520 |
Уран U | 116 |
Цинк Zn | 385 |
Чугун белый | 540 |
Чугун серый | 470 |
Ответ: латунь
Количество теплоты, удельная теплоемкость
От чего зависит количество теплотыВнутренняя энергия тела изменяется при совершении работы или теплопередаче. При явлении теплопередачи внутренняя энергия передается теплопроводностью, конвекцией или излучением.
При явлении теплопередачи внутренняя энергия передается теплопроводностью, конвекцией или излучением.
Каждое тело при нагревании или охлаждении (при теплопередаче) получает или теряет какое-то количество энергии. Исходя из этого, принято это количество энергии назвать количеством теплоты.
Итак, количество теплоты – это та энергия, которую отдает или получает тело в процессе теплопередачи.
Какое количество теплоты необходимо для нагревания воды? На простом примере можно понять, что для нагревания разного количества воды потребуется разное количество теплоты. Допустим, возьмем две пробирки с 1 литром воды и с 2-мя литрами воды. В каком случае потребуется большее количество теплоты? Во втором, там, где в пробирке 2 литра воды. Вторая пробирка будет нагреваться дольше, если мы подогреваем их одинаковым источником огня.
Таким образом, количество теплоты зависит от массы тела. Чем больше масса, тем большее количество теплоты требуется для нагрева и, соответственно, на охлаждение тела требуется большее время.
От чего еще зависит количество теплоты? Естественно, от разности температур тел. Но это еще не все. Ведь если мы попытаемся нагреть воду или молоко, то нам потребуется разное количество времени. Т.е получается, что количество теплоты зависит от вещества, из которого состоит тело.
В итоге получается, что количество теплоты, которое нужно для нагревания или количество теплоты, которое выделяется при остывании тела, зависит от его массы, от изменения температуры и от вида вещества, из которого состоит тело.
В чем измеряется количество теплотыЗа единицу количества теплоты принято считать 1 Джоуль. До появления единицы измерения энергии ученые считали количество теплоты калориями. Сокращенно эту единицу измерения принято писать – “Дж”
Калория – это количество теплоты, которое необходимо для того, чтобы нагреть 1 грамм воды на 1 градус Цельсия. Сокращенно единицу измерения калории принято писать – “кал”.
1 кал = 4,19 Дж.
Обратите внимание, что в этих единицах энергии принято отмечать пищевую ценность продуктов питания кДж и ккал.
1 ккал = 1000 кал.
1 кДж = 1000 Дж
1 ккал = 4190 Дж = 4,19 кДж
Что такое удельная теплоемкостьКаждое вещество в природе имеет свои свойства, и для нагрева каждого отдельного вещества требуется разное количество энергии, т.е. количества теплоты.
Удельная теплоемкость вещества – это величина, равная количеству теплоты, которое нужно передать телу с массой 1 килограмм, чтобы нагреть его на температуру 1 0C
Удельная теплоемкость обозначается буквой c и имеет величину измерения Дж/кг*
Например, удельная теплоемкость воды равна 4200 Дж/кг*0C. То есть это то количество теплоты, которое нужно передать 1 кг воды, чтобы нагреть ее на 1 0C
Следует помнить, что удельная теплоемкость веществ в разных агрегатных состояниях различна. То есть для нагревания льда на 1 0C потребуется другое количество теплоты.
То есть для нагревания льда на 1 0C потребуется другое количество теплоты.
Например, необходимо рассчитать количество теплоты, которое нужно потратить для того, чтобы нагреть 3 кг воды с температуры 15 0С до температуры 85 0С. Нам известна удельная теплоемкость воды, то есть количество энергии, которое нужно для того, чтобы нагреть 1 кг воды на 1 градус. То есть для того, чтобы узнать количество теплоты в нашем случае, нужно умножить удельную теплоемкость воды на 3 и на то количество градусов, на которое нужно увеличить температуры воды. Итак, это 4200*3*(85-15) = 882 000.
В скобках мы рассчитываем точное количество градусов, отнимая от конечного необходимого результата начальное
Итак, для того, чтобы нагреть 3 кг воды с 15 до 85 0С, нам потребуется 882 000 Дж количества теплоты.
Количество теплоты обозначается буквой Q, формула для его расчета выглядит следующим образом:
Q=c*m*(t2-t1).
Задача 1. Какое количество теплоты потребуется для нагрева 0,5 кг воды с 20 до 50 0С
Дано:
m = 0,5 кг.,
с = 4200 Дж/кг*0С,
t1 = 20 0С,
t2 = 50 0С.
Величину удельной теплоемкость мы определили из таблицы.
Решение:
количество теплоты определяется по формуле Q=c*m*(t2-t1).
Подставляем значения:
Q=4200*0,5*(50-20) = 63 000 Дж = 63 кДж.
Ответ: Q=63 кДж.
Задача 2. Какое количество теплоты потребуется для нагревания алюминиевого бруска массой 0,5 кг на 85 0С?
Дано:
m = 0,5 кг.,
с = 920 Дж/кг*0С,
t1 = 0 0С,
t2 = 85 0С.
Решение:
количество теплоты определяется по формуле Q=c*m*(t2-t1).
Подставляем значения:
Q=920*0,5*(85-0) = 39 100 Дж = 39,1 кДж.
Ответ: Q= 39,1 кДж.
Изменение температуры и теплоемкость
Цели обучения
К концу этого раздела вы сможете:
- Наблюдать за теплопередачей и изменением температуры и массы.
- Расчет конечной температуры после передачи тепла между двумя объектами.
Одним из основных эффектов теплопередачи является изменение температуры: нагрев увеличивает температуру, а охлаждение снижает ее. Мы предполагаем, что фазового перехода нет, и что система или система не выполняет никаких работ.Эксперименты показывают, что передаваемое тепло зависит от трех факторов: изменения температуры, массы системы, а также вещества и фазы вещества.
Рис. 1. Тепло Q , передаваемое для изменения температуры, зависит от величины изменения температуры, массы системы, а также от вещества и фазы. (а) Количество переданного тепла прямо пропорционально изменению температуры. Чтобы удвоить изменение температуры массы m, вам нужно добавить в два раза больше тепла.(б) Количество переданного тепла также прямо пропорционально массе. Чтобы вызвать эквивалентное изменение температуры в удвоенной массе, вам нужно добавить в два раза больше тепла. (c) Количество передаваемого тепла зависит от вещества и его фазы. Если требуется количество тепла Q , чтобы вызвать изменение температуры Δ T в данной массе меди, потребуется в 10,8 раза больше тепла, чтобы вызвать эквивалентное изменение температуры в той же массе воды, при условии отсутствия фазы изменение любого вещества.
Чтобы удвоить изменение температуры массы m, вам нужно добавить в два раза больше тепла.(б) Количество переданного тепла также прямо пропорционально массе. Чтобы вызвать эквивалентное изменение температуры в удвоенной массе, вам нужно добавить в два раза больше тепла. (c) Количество передаваемого тепла зависит от вещества и его фазы. Если требуется количество тепла Q , чтобы вызвать изменение температуры Δ T в данной массе меди, потребуется в 10,8 раза больше тепла, чтобы вызвать эквивалентное изменение температуры в той же массе воды, при условии отсутствия фазы изменение любого вещества.
Зависимость от изменения температуры и массы легко понять. Поскольку (средняя) кинетическая энергия атома или молекулы пропорциональна абсолютной температуре, внутренняя энергия системы пропорциональна абсолютной температуре и количеству атомов или молекул. Благодаря тому, что переданное тепло равно изменению внутренней энергии, тепло пропорционально массе вещества и изменению температуры. Передаваемое тепло также зависит от вещества, так что, например, количество тепла, необходимое для повышения температуры, меньше для спирта, чем для воды.Для одного и того же вещества передаваемое тепло также зависит от фазы (газ, жидкость или твердое тело).
Передаваемое тепло также зависит от вещества, так что, например, количество тепла, необходимое для повышения температуры, меньше для спирта, чем для воды.Для одного и того же вещества передаваемое тепло также зависит от фазы (газ, жидкость или твердое тело).
Теплопередача и изменение температуры
Количественная связь между теплопередачей и изменением температуры включает все три фактора: Q = mc Δ T , где Q – символ теплопередачи, m – масса вещества и Δ T – изменение температуры. Обозначение c обозначает удельную теплоемкость и зависит от материала и фазы.Удельная теплоемкость – это количество тепла, необходимое для изменения температуры 1,00 кг массы на 1,00 ° C. Удельная теплоемкость c – это свойство вещества; его единица СИ – Дж / (кг К) или Дж / (кг ºC). Напомним, что изменение температуры (Δ T ) одинаково в единицах кельвина и градусов Цельсия. Если теплопередача измеряется в килокалориях, то единицей удельной теплоемкости является ккал / (кг ⋅ ºC).
Значения удельной теплоемкости обычно нужно искать в таблицах, потому что нет простого способа их вычислить.Как правило, удельная теплоемкость также зависит от температуры. В таблице 1 приведены типичные значения теплоемкости для различных веществ. За исключением газов, температурная и объемная зависимость удельной теплоемкости большинства веществ слабая. Из этой таблицы видно, что удельная теплоемкость воды в пять раз больше, чем у стекла и в десять раз больше, чем у железа, что означает, что требуется в пять раз больше тепла, чтобы поднять температуру воды на ту же величину, что и у стекла, и в десять раз больше. много тепла для повышения температуры воды, как для утюга.Фактически, вода имеет одну из самых высоких удельной теплоемкости из всех материалов, что важно для поддержания жизни на Земле.
Пример 1. Расчет необходимого тепла: нагрев воды в алюминиевой кастрюле
Алюминиевая кастрюля массой 0,500 кг на плите используется для нагрева 0,250 литра воды с 20,0 ° C до 80,0 ° C. а) Сколько тепла требуется? Какой процент тепла используется для повышения температуры (б) сковороды и (в) воды?
а) Сколько тепла требуется? Какой процент тепла используется для повышения температуры (б) сковороды и (в) воды?
Стратегия
Кастрюля и вода всегда имеют одинаковую температуру.Когда вы ставите кастрюлю на плиту, температура воды и кастрюли увеличивается на одинаковую величину. Мы используем уравнение теплопередачи для данного изменения температуры и массы воды и алюминия. Значения удельной теплоемкости воды и алюминия приведены в таблице 1.
Решение
Поскольку вода находится в тепловом контакте с алюминием, кастрюля и вода имеют одинаковую температуру.
Рассчитать разницу температур:
Δ T = T f – T i = 60.0ºC.
Рассчитайте массу воды. Поскольку плотность воды составляет 1000 кг / м 3 , один литр воды имеет массу 1 кг, а масса 0,250 литра воды составляет м w = 0,250 кг.
Рассчитайте тепло, передаваемое воде. Используйте удельную теплоемкость воды в таблице 1:
Используйте удельную теплоемкость воды в таблице 1:
Q w = м w c w Δ T = (0,250 кг) (4186 Дж / кгºC) (60,0ºC) = 62.8 кДж.
Рассчитайте тепло, передаваемое алюминию. Используйте удельную теплоемкость алюминия в таблице 1:
.Q Al = м Al c Al Δ T = (0,500 кг) (900 Дж / кгºC) (60,0ºC) = 27,0 × 10 4 Дж = 27,0 кДж . <
Сравните процент тепла, поступающего в сковороду, и в воду. Сначала найдите общее переданное тепло:
Q Итого = Q w + Q Al = 62.8 кДж + 27,0 кДж = 89,8 кДж.
Таким образом, количество тепла, идущего на нагревание сковороды, равно
.[латекс] \ frac {27.0 \ text {kJ}} {89.8 \ text {kJ}} \ times100 \% = 30.1 \% \\ [/ latex]
, а на подогрев воды –
. [латекс] \ frac {62,8 \ text {кДж}} {89,8 \ text {кДж}} \ times100 \% = 69,9 \% \\ [/ latex].
Обсуждение
В этом примере тепло, передаваемое контейнеру, составляет значительную долю от общего переданного тепла. Хотя вес кастрюли в два раза больше, чем у воды, удельная теплоемкость воды более чем в четыре раза больше, чем у алюминия.Следовательно, для достижения заданного изменения температуры воды требуется чуть более чем в два раза больше тепла по сравнению с алюминиевым поддоном.
Пример 2. Расчет повышения температуры в результате работы, проделанной с веществом: перегрев тормозов грузовика на спуске
Рис. 2. Дымящиеся тормоза этого грузовика – видимое свидетельство механического эквивалента тепла.
Тормоза грузовика, используемые для контроля скорости на спуске, работают, преобразуя гравитационную потенциальную энергию в повышенную внутреннюю энергию (более высокую температуру) тормозного материала.Это преобразование предотвращает преобразование потенциальной гравитационной энергии в кинетическую энергию грузовика. Проблема в том, что масса грузовика велика по сравнению с массой тормозного материала, поглощающего энергию, и повышение температуры может происходить слишком быстро, чтобы тепло передавалось от тормозов в окружающую среду.
Рассчитайте повышение температуры 100 кг тормозного материала со средней удельной теплоемкостью 800 Дж / кг ºC, если материал сохраняет 10% энергии от грузовика массой 10 000 кг, спускающегося 75.0 м (при вертикальном перемещении) с постоянной скоростью.
Стратегия
Если тормоза не применяются, потенциальная энергия гравитации преобразуется в кинетическую энергию. При срабатывании тормозов потенциальная гравитационная энергия преобразуется во внутреннюю энергию тормозного материала. Сначала мы вычисляем гравитационную потенциальную энергию ( Mgh ), которую весь грузовик теряет при спуске, а затем находим повышение температуры, возникающее только в тормозном материале.
Решение
- Рассчитайте изменение гравитационной потенциальной энергии при спуске грузовика с горы Mgh = (10,000 кг) (9.{\ circ} C \\ [/ латекс].
Обсуждение
Эта температура близка к температуре кипения воды. Если бы грузовик ехал какое-то время, то непосредственно перед спуском температура тормозов, вероятно, была бы выше, чем температура окружающей среды. Повышение температуры при спуске, вероятно, приведет к повышению температуры тормозного материала выше точки кипения воды, поэтому этот метод непрактичен. Однако та же самая идея лежит в основе недавней гибридной технологии автомобилей, в которой механическая энергия (гравитационная потенциальная энергия) преобразуется тормозами в электрическую энергию (аккумулятор).
Повышение температуры при спуске, вероятно, приведет к повышению температуры тормозного материала выше точки кипения воды, поэтому этот метод непрактичен. Однако та же самая идея лежит в основе недавней гибридной технологии автомобилей, в которой механическая энергия (гравитационная потенциальная энергия) преобразуется тормозами в электрическую энергию (аккумулятор).
| Таблица 1. Удельная теплоемкость различных веществ | ||
|---|---|---|
| Вещества | Удельная теплоемкость ( c ) | |
| Твердые вещества | Дж / кг ⋅ ºC | ккал / кг ⋅ ºC |
| Алюминий | 900 | 0,215 |
| Асбест | 800 | 0,19 |
| Бетон, гранит (средний) | 840 | 0.20 |
| Медь | 387 | 0,0924 |
| Стекло | 840 | 0,20 |
| Золото | 129 | 0,0308 |
| Человеческое тело (в среднем при 37 ° C) | 3500 | 0,83 |
| Лед (в среднем, от −50 ° C до 0 ° C) | 2090 | 0,50 |
| Чугун, сталь | 452 | 0,108 |
| Свинец | 128 | 0. 0305 0305 |
| Серебро | 235 | 0,0562 |
| Дерево | 1700 | 0,4 |
| Жидкости | ||
| Бензол | 1740 | 0,415 |
| Этанол | 2450 | 0,586 |
| Глицерин | 2410 | 0,576 |
| Меркурий | 139 | 0,0333 |
| Вода (15.0 ° С) | 4186 | 1.000 |
| Газы | ||
| Воздух (сухой) | 721 (1015) | 0,172 (0,242) |
| Аммиак | 1670 (2190) | 0,399 (0,523) |
| Двуокись углерода | 638 (833) | 0,152 (0,199) |
| Азот | 739 (1040) | 0,177 (0,248) |
| Кислород | 651 (913) | 0.156 (0,218) |
| Пар (100 ° C) | 1520 (2020) | 0,363 (0,482) |
Обратите внимание, что Пример 2 является иллюстрацией механического эквивалента тепла. В качестве альтернативы повышение температуры может быть произведено с помощью паяльной лампы, а не механически.
В качестве альтернативы повышение температуры может быть произведено с помощью паяльной лампы, а не механически.
Пример 3. Расчет конечной температуры при передаче тепла между двумя телами: заливка холодной воды в горячую кастрюлю
Допустим, вы залили 0,250 кг 20.0ºC воды (около чашки) в алюминиевую кастрюлю весом 0,500 кг, снятую с плиты, при температуре 150ºC. Предположим, что поддон стоит на изолированной подушке и выкипает незначительное количество воды. Какова температура, когда вода и поддон через короткое время достигают теплового равновесия?
Стратегия
Кастрюлю кладут на изолирующую подкладку, чтобы тепло не передавалось с окружающей средой. Изначально кастрюля и вода не находятся в тепловом равновесии: кастрюля имеет более высокую температуру, чем вода.Затем теплообмен восстанавливает тепловое равновесие, когда вода и поддон соприкасаются. Поскольку теплообмен между кастрюлей и водой происходит быстро, масса испарившейся воды незначительна, а величина тепла, теряемого сковородой, равна теплу, полученному водой. Обмен тепла прекращается, когда достигается тепловое равновесие между кастрюлей и водой. Теплообмен можно записать как | Q горячий | = Q холодный .
Обмен тепла прекращается, когда достигается тепловое равновесие между кастрюлей и водой. Теплообмен можно записать как | Q горячий | = Q холодный .
Решение
Используйте уравнение теплопередачи Q = mc Δ T , чтобы выразить тепло, теряемое алюминиевой сковородой, через массу сковороды, удельную теплоемкость алюминия, начальную температуру сковороды и конечная температура: Q горячий = м Al c Al ( T f – 150ºC).
Выразите тепло, полученное водой, через массу воды, удельную теплоемкость воды, начальную температуру воды и конечную температуру: Q холодная = м W c W ( T f – 20,0 ° C).
Обратите внимание, что Q горячий <0 и Q холодный > 0 и что они должны быть в сумме равными нулю, потому что тепло, теряемое горячей сковородой, должно быть таким же, как тепло, полученное холодной водой:
[латекс] \ begin {array} {lll} Q _ {\ text {cold}} + Q _ {\ text {hot}} & = & 0 \\ Q _ {\ text {cold}} & = & – Q _ {\ text {hot}} \\ m _ {\ text {W}} c _ {\ text {W}} \ left (T _ {\ text {f}} – 20. {\ circ} \ text {C} \ end {array} \\ [/ latex]
{\ circ} \ text {C} \ end {array} \\ [/ latex]
Обсуждение
Это типичная проблема калориметрии : два тела при разных температурах приводят в контакт друг с другом и обмениваются теплом до тех пор, пока не будет достигнута общая температура. Почему конечная температура намного ближе к 20,0ºC, чем к 150ºC? Причина в том, что вода имеет большую удельную теплоемкость, чем большинство обычных веществ, и поэтому претерпевает небольшое изменение температуры при данной теплопередаче. Большой водоем, например озеро, требует большого количества тепла для значительного повышения температуры.Это объясняет, почему температура в озере остается относительно постоянной в течение дня, даже когда изменение температуры воздуха велико. Однако температура воды действительно меняется в течение длительного времени (например, с лета на зиму).
Эксперимент на вынос: изменение температуры земли и воды
Что нагревается быстрее, земля или вода?
Для изучения разницы в теплоемкости:
- Поместите равные массы сухого песка (или почвы) и воды одинаковой температуры в две небольшие банки.
 (Средняя плотность почвы или песка примерно в 1,6 раза больше плотности воды, поэтому вы можете получить примерно равную массу, используя на 50% больше воды по объему.)
(Средняя плотность почвы или песка примерно в 1,6 раза больше плотности воды, поэтому вы можете получить примерно равную массу, используя на 50% больше воды по объему.) - Нагрейте оба (в духовке или нагревательной лампе) одинаковое время.
- Запишите конечную температуру двух масс.
- Теперь доведите обе банки до одинаковой температуры, нагревая их в течение более длительного периода времени.
- Снимите банки с источника тепла и измеряйте их температуру каждые 5 минут в течение примерно 30 минут.
Какой образец остывает быстрее всего? Эта деятельность воспроизводит явления, ответственные за дующий с суши и морской бриз.
Проверьте свое понимание
Если 25 кДж необходимо для повышения температуры блока с 25 ° C до 30 ° C, сколько тепла необходимо для нагрева блока с 45 ° C до 50 ° C?
Решение
Теплопередача зависит только от разницы температур. Поскольку разница температур в обоих случаях одинакова, во втором случае необходимы те же 25 кДж.
Сводка раздела
- Передача тепла Q , которая приводит к изменению Δ T температуры тела массой м составляет Q = mc Δ T , где c – удельная теплоемкость материала. Это соотношение также можно рассматривать как определение удельной теплоемкости.
Концептуальные вопросы
- Какие три фактора влияют на теплопередачу, необходимую для изменения температуры объекта?
- Тормоза в автомобиле повышают температуру на Δ T при остановке автомобиля со скорости v .Насколько больше было бы Δ T , если бы автомобиль изначально имел вдвое большую скорость? Вы можете предположить, что автомобиль останавливается достаточно быстро, чтобы не отводить тепло от тормозов.
Задачи и упражнения
- В жаркий день температура в бассейне объемом 80 000 л повышается на 1,50ºC. Какова чистая теплопередача при этом нагреве? Игнорируйте любые осложнения, такие как потеря воды из-за испарения.

- Докажите, что 1 кал / г · ºC = 1 ккал / кг · ºC.
- Для стерилизации 50.Стеклянная детская бутылочка 0 г, мы должны поднять ее температуру с 22,0 ° С до 95,0 ° С. Какая требуется теплопередача?
- Одинаковая передача тепла идентичным массам разных веществ вызывает разные изменения температуры. Рассчитайте конечную температуру, когда 1,00 ккал тепла передается 1,00 кг следующих веществ, первоначально при 20,0 ° C: (a) вода; (б) бетон; (в) сталь; и d) ртуть.
- Потирание рук согревает их, превращая работу в тепловую энергию. Если женщина трет руки взад и вперед в общей сложности 20 движений, на расстоянии 7.50 см на руб, а при средней силе трения 40,0 Н, что такое повышение температуры? Масса согреваемых тканей всего 0,100 кг, в основном в ладонях и пальцах.
- Блок чистого материала массой 0,250 кг нагревают с 20,0 ° C до 65,0 ° C за счет добавления 4,35 кДж энергии. Вычислите его удельную теплоемкость и определите вещество, из которого он, скорее всего, состоит.

- Предположим, что одинаковые количества тепла передаются различным массам меди и воды, вызывая одинаковые изменения температуры.Какое отношение массы меди к воде?
- (a) Количество килокалорий в пище определяется калориметрическими методами, при которых пища сжигается и измеряется теплоотдача. Сколько килокалорий на грамм содержится в арахисе весом 5,00 г, если энергия его горения передается 0,500 кг воды, содержащейся в алюминиевой чашке весом 0,100 кг, что вызывает повышение температуры на 54,9 ° C? (b) Сравните свой ответ с информацией на этикетке, найденной на упаковке арахиса, и прокомментируйте, согласуются ли значения.
- После интенсивных упражнений температура тела человека весом 80,0 кг составляет 40,0 ° C. С какой скоростью в ваттах человек должен передавать тепловую энергию, чтобы снизить температуру тела до 37,0 ° C за 30,0 мин, если предположить, что тело продолжает вырабатывать энергию со скоростью 150 Вт? 1 Вт = 1 Дж / с или 1 Вт = 1 Дж / с.
- Даже после остановки после периода нормальной эксплуатации большой промышленный ядерный реактор передает тепловую энергию со скоростью 150 МВт за счет радиоактивного распада продуктов деления.
 Эта теплопередача вызывает быстрое повышение температуры при выходе из строя системы охлаждения (1 Вт = 1 джоуль / сек или 1 Вт = 1 Дж / с и 1 МВт = 1 мегаватт). (a) Рассчитайте скорость повышения температуры в градусах Цельсия в секунду (ºC / s), если масса активной зоны реактора составляет 1,60 × 10 5 кг, а ее средняя удельная теплоемкость составляет 0,3349 кДж / кг ºC. (b) Сколько времени потребуется, чтобы получить повышение температуры на 2000 ° C, которое может привести к расплавлению некоторых металлов, содержащих радиоактивные материалы? (Начальная скорость повышения температуры будет больше, чем рассчитанная здесь, потому что теплопередача сосредоточена в меньшей массе.Позже, однако, повышение температуры замедлится, потому что стальная защитная оболочка 5 × 10 5 кг также начнет нагреваться.)
Эта теплопередача вызывает быстрое повышение температуры при выходе из строя системы охлаждения (1 Вт = 1 джоуль / сек или 1 Вт = 1 Дж / с и 1 МВт = 1 мегаватт). (a) Рассчитайте скорость повышения температуры в градусах Цельсия в секунду (ºC / s), если масса активной зоны реактора составляет 1,60 × 10 5 кг, а ее средняя удельная теплоемкость составляет 0,3349 кДж / кг ºC. (b) Сколько времени потребуется, чтобы получить повышение температуры на 2000 ° C, которое может привести к расплавлению некоторых металлов, содержащих радиоактивные материалы? (Начальная скорость повышения температуры будет больше, чем рассчитанная здесь, потому что теплопередача сосредоточена в меньшей массе.Позже, однако, повышение температуры замедлится, потому что стальная защитная оболочка 5 × 10 5 кг также начнет нагреваться.)
Рисунок 3. Бассейн с радиоактивным отработавшим топливом на атомной электростанции. Отработанное топливо долго остается горячим. (кредит: Министерство энергетики США)
Глоссарий
удельная теплоемкость: количество тепла, необходимое для изменения температуры 1,00 кг вещества на 1,00 ºC
Избранные решения проблем и упражнения
1. 5,02 × 10 8 Дж
5,02 × 10 8 Дж
3. 3.07 × 10 3 Дж
5. 0,171ºC
7. 10,8
9. 617 Вт
Теплопередача, удельная теплоемкость и калориметрия – University Physics Volume 2
Цели обучения
К концу этого раздела вы сможете:
- Объяснение явлений, связанных с теплом как формой передачи энергии
- Решение проблем, связанных с теплопередачей
В предыдущих главах мы видели, что энергия – одно из фундаментальных понятий физики. Тепло – это тип передачи энергии, который вызывается разницей температур и может изменять температуру объекта. Как мы узнали ранее в этой главе, теплопередача – это движение энергии от одного места или материала к другому в результате разницы температур. Передача тепла имеет фундаментальное значение для таких повседневных действий, как отопление и приготовление пищи, а также для многих промышленных процессов. Он также составляет основу тем, которые будут рассмотрены в оставшейся части этой главы.
Мы также вводим понятие внутренней энергии, которая может быть увеличена или уменьшена за счет теплопередачи.Мы обсуждаем другой способ изменить внутреннюю энергию системы, а именно выполнение работы над ней. Таким образом, мы начинаем изучение взаимосвязи тепла и работы, которая является основой двигателей и холодильников и центральной темой (и источником названия) термодинамики.
Внутренняя энергия и тепло
Тепловая система имеет внутренней энергии (также называемой тепловой энергией ) , которая является суммой механических энергий ее молекул. Внутренняя энергия системы пропорциональна ее температуре.Как мы видели ранее в этой главе, если два объекта с разной температурой приводят в контакт друг с другом, энергия передается от более горячего объекта к более холодному, пока тела не достигнут теплового равновесия (то есть они имеют одинаковую температуру). Ни один из объектов не совершает никакой работы, потому что никакая сила не действует на расстоянии (как мы обсуждали в разделе Работа и кинетическая энергия). Эти наблюдения показывают, что тепло – это энергия, передаваемая самопроизвольно из-за разницы температур. (Рисунок) показывает пример теплопередачи.
Ни один из объектов не совершает никакой работы, потому что никакая сила не действует на расстоянии (как мы обсуждали в разделе Работа и кинетическая энергия). Эти наблюдения показывают, что тепло – это энергия, передаваемая самопроизвольно из-за разницы температур. (Рисунок) показывает пример теплопередачи.
Значение «тепла» в физике отличается от его обычного значения.Например, в разговоре мы можем сказать, что «жара была невыносимой», но в физике мы бы сказали, что температура была высокой. Тепло – это форма потока энергии, а температура – нет. Между прочим, люди чувствительны к тепловому потоку , а не к температуре.
Тепло – это форма потока энергии, а температура – нет. Между прочим, люди чувствительны к тепловому потоку , а не к температуре.
Поскольку тепло – это форма энергии, в системе СИ единицей измерения является джоуль (Дж). Другой распространенной единицей энергии, часто используемой для получения тепла, является калория (кал), определяемая как энергия, необходимая для изменения температуры 1,00 г воды, в частности, между и, поскольку существует небольшая температурная зависимость.Также обычно используется килокалория (ккал), которая представляет собой энергию, необходимую для изменения температуры 1,00 кг воды на. Так как масса чаще всего указывается в килограммах, то килокалория удобна. Как ни странно, пищевые калории (иногда называемые «большими калориями», сокращенно Cal) на самом деле являются килокалориями, что нелегко определить по маркировке упаковки.
Механический эквивалент тепла
Также можно изменять температуру вещества, выполняя работу, которая передает энергию в систему или из нее. Это понимание помогло установить, что тепло – это форма энергии. Джеймс Прескотт Джоуль (1818–1889) провел множество экспериментов, чтобы установить механический эквивалент тепла – работа, необходимая для получения тех же эффектов, что и теплопередача . В единицах, используемых для этих двух величин, эквивалентность равна
Это понимание помогло установить, что тепло – это форма энергии. Джеймс Прескотт Джоуль (1818–1889) провел множество экспериментов, чтобы установить механический эквивалент тепла – работа, необходимая для получения тех же эффектов, что и теплопередача . В единицах, используемых для этих двух величин, эквивалентность равна
Мы считаем, что это уравнение представляет преобразование между двумя единицами энергии. (Другие числа, которые вы можете увидеть, относятся к калориям, определенным для температурных диапазонов, отличных от до.)
(рисунок) показывает одну из самых известных экспериментальных установок Джоуля для демонстрации того, что работа и тепло могут производить одни и те же эффекты, и измерения механического эквивалента тепла. Это помогло установить принцип сохранения энергии. Гравитационная потенциальная энергия ( U ) была преобразована в кинетическую энергию ( K ), а затем рандомизирована по вязкости и турбулентности в увеличенную среднюю кинетическую энергию атомов и молекул в системе, что привело к увеличению температуры. Вклад Джоуля в термодинамику был настолько значительным, что в его честь была названа единица энергии в системе СИ.
Вклад Джоуля в термодинамику был настолько значительным, что в его честь была названа единица энергии в системе СИ.
Увеличение внутренней энергии за счет теплопередачи дает тот же результат, что и увеличение ее за счет выполнения работы.Следовательно, хотя система имеет четко определенную внутреннюю энергию, мы не можем сказать, что она имеет определенное «теплосодержание» или «рабочее содержание». Четко определенная величина, которая зависит только от текущего состояния системы, а не от истории этой системы, называется переменной состояния . Температура и внутренняя энергия являются переменными состояния. Подводя итог этому абзацу, тепло и работа не являются переменными состояния .
Подводя итог этому абзацу, тепло и работа не являются переменными состояния .
Между прочим, увеличение внутренней энергии системы не обязательно увеличивает ее температуру.Как мы увидим в следующем разделе, температура не меняется, когда вещество переходит из одной фазы в другую. Примером может служить таяние льда, которое может быть достигнуто путем добавления тепла или выполнения работы трения, например, когда кубик льда трется о шероховатую поверхность.
Изменение температуры и теплоемкость
Мы отметили, что теплопередача часто вызывает изменение температуры. Эксперименты показывают, что без фазового перехода и без какой-либо работы над системой или ею переданное тепло обычно прямо пропорционально изменению температуры и массы системы в хорошем приближении.(Ниже мы покажем, как действовать в ситуациях, когда приближение неверно.) Константа пропорциональности зависит от вещества и его фазы, которая может быть газом, жидкостью или твердым телом. Мы опускаем обсуждение четвертой фазы, плазмы, потому что, хотя это наиболее распространенная фаза во Вселенной, она редка и недолговечна на Земле.
Мы опускаем обсуждение четвертой фазы, плазмы, потому что, хотя это наиболее распространенная фаза во Вселенной, она редка и недолговечна на Земле.
Мы можем понять экспериментальные факты, заметив, что передаваемое тепло – это изменение внутренней энергии, которая представляет собой полную энергию молекул.В типичных условиях полная кинетическая энергия молекул составляет постоянную долю внутренней энергии (по причинам и за исключениями, которые мы увидим в следующей главе). Средняя кинетическая энергия молекулы пропорциональна абсолютной температуре. Следовательно, изменение внутренней энергии системы обычно пропорционально изменению температуры и количеству молекул, N . Математически зависимость от вещества в значительной степени обусловлена разной массой атомов и молекул.Мы рассматриваем его теплоемкость с точки зрения его массы, но, как мы увидим в следующей главе, в некоторых случаях теплоемкость на молекулу одинакова для разных веществ. Зависимость от вещества и фазы также является результатом различий в потенциальной энергии, связанной с взаимодействиями между атомами и молекулами.
Зависимость от вещества и фазы также является результатом различий в потенциальной энергии, связанной с взаимодействиями между атомами и молекулами.
Значения удельной теплоемкости обычно необходимо измерять, потому что нет простого способа их точно рассчитать. (Рисунок) показывает типичные значения теплоемкости для различных веществ.Из этой таблицы видно, что удельная теплоемкость воды в пять раз больше, чем у стекла и в 10 раз больше, чем у железа, что означает, что для повышения температуры воды на определенное количество требуется в пять раз больше тепла, чем у стекла, и в 10 раз больше. столько, сколько по железу. Фактически, вода имеет одну из самых высоких удельной теплоемкости из всех материалов, что важно для поддержания жизни на Земле.
Удельная теплота газов зависит от того, что поддерживается постоянным во время нагрева – обычно от объема или давления.В таблице первое значение удельной теплоемкости для каждого газа измерено при постоянном объеме, а второе (в скобках) измерено при постоянном давлении. Мы вернемся к этой теме в главе, посвященной кинетической теории газов.
Мы вернемся к этой теме в главе, посвященной кинетической теории газов.
Как правило, удельная теплоемкость также зависит от температуры. Таким образом, точное определение c для вещества должно быть дано в терминах бесконечно малого изменения температуры. Для этого отметим это и заменим на d :
За исключением газов, температурная и объемная зависимость удельной теплоемкости большинства веществ слабая при нормальных температурах.Поэтому мы обычно принимаем удельную теплоемкость постоянными на значениях, указанных в таблице.
(рисунок) иллюстрирует повышение температуры, вызванное работой. (Результат такой же, как если бы такое же количество энергии было добавлено с помощью паяльной лампы, а не механически.)
Расчет повышения температуры в результате работы, проделанной на грузовике с веществом. Тормоза, используемые для управления скоростью на спуске, выполняют свою работу, преобразуя гравитационную потенциальную энергию в повышенную внутреннюю энергию (более высокую температуру) тормозного материала ((рисунок)). Это преобразование предотвращает преобразование потенциальной гравитационной энергии в кинетическую энергию грузовика. Поскольку масса грузовика намного больше, чем масса тормозного материала, поглощающего энергию, повышение температуры может происходить слишком быстро, чтобы тепло от тормозов передавалось в окружающую среду; Другими словами, тормоза могут перегреться.
Это преобразование предотвращает преобразование потенциальной гравитационной энергии в кинетическую энергию грузовика. Поскольку масса грузовика намного больше, чем масса тормозного материала, поглощающего энергию, повышение температуры может происходить слишком быстро, чтобы тепло от тормозов передавалось в окружающую среду; Другими словами, тормоза могут перегреться.
Дымящиеся тормоза тормозной тележки – видимое свидетельство механического эквивалента тепла.
Рассчитайте повышение температуры 10 кг тормозного материала со средней удельной теплоемкостью, если материал удерживает 10% энергии от спускающегося грузовика массой 10 000 кг 75.0 м (при вертикальном перемещении) с постоянной скоростью.
Стратегия Мы вычисляем гравитационную потенциальную энергию ( Mgh ), которую весь грузовик теряет при спуске, приравниваем ее к увеличению внутренней энергии тормозов, а затем находим повышение температуры, возникающее только в тормозном материале.
Решение Сначала мы рассчитаем изменение гравитационной потенциальной энергии при спуске грузовика:
Поскольку кинетическая энергия грузовика не изменяется, закон сохранения энергии говорит нам, что потерянная потенциальная энергия рассеивается, и мы предполагаем, что 10% ее передается внутренней энергии тормозов, так что возьмите.Затем мы рассчитываем изменение температуры от переданного тепла, используя
, где м – масса тормозного материала. Вставьте указанные значения, чтобы найти
Значение Если бы грузовик ехал некоторое время, то непосредственно перед спуском температура тормозов, вероятно, была бы выше, чем температура окружающей среды. Повышение температуры при спуске, вероятно, приведет к очень сильному повышению температуры тормозного материала, поэтому этот метод непрактичен.Вместо этого грузовик использовал бы технику торможения двигателем. Другая идея лежит в основе новейшей технологии гибридных и электрических автомобилей, в которой механическая энергия (кинетическая и гравитационная потенциальная энергия) преобразуется тормозами в электрическую энергию в аккумуляторе. Этот процесс называется регенеративным торможением.
Этот процесс называется регенеративным торможением.
В задачах обычного типа объекты с разными температурами контактируют друг с другом, но изолированы от всего остального, и им позволяют прийти в равновесие.Контейнер, который предотвращает передачу тепла внутрь или наружу, называется калориметром, а использование калориметра для измерения (обычно теплоемкости или удельной теплоемкости) называется калориметрией.
Мы будем использовать термин «проблема калориметрии» для обозначения любой проблемы, в которой рассматриваемые объекты термически изолированы от своего окружения. Важная идея при решении задач калориметрии заключается в том, что во время теплообмена между объектами, изолированными от их окружения, тепло, полученное более холодным объектом, должно равняться теплу, теряемому более горячим объектом, из-за сохранения энергии:
Мы выражаем эту идею, записывая, что сумма тепла равна нулю, потому что полученное тепло обычно считается положительным; тепло потеряно, отрицательное.
Расчет конечной температуры в калориметрии. Предположим, вы наливаете 0,250 кг воды (примерно чашку) в алюминиевую кастрюлю весом 0,500 кг, снятую с плиты, с температурой 0 ° C. Предположим, что теплопередача не происходит ни к чему другому: кастрюлю кладут на изолирующую подкладку, и не учитывают передачу тепла воздуху за короткое время, необходимое для достижения равновесия. Таким образом, это проблема калориметрии, даже если не указан изолирующий контейнер. Также предположим, что выкипает незначительное количество воды.Какова температура, при которой вода и поддон достигают теплового равновесия?
Стратегия Изначально кастрюля и вода не находятся в тепловом равновесии: кастрюля имеет более высокую температуру, чем вода. Теплопередача восстанавливает тепловое равновесие при соприкосновении воды и поддона; он останавливается, когда достигается тепловое равновесие между поддоном и водой. Тепло, теряемое сковородой, равно теплу, полученному водой – это основной принцип калориметрии.
Решение
- Используйте уравнение теплопередачи, чтобы выразить тепло, потерянное алюминиевой сковородой, через массу сковороды, удельную теплоемкость алюминия, начальную температуру сковороды и конечную температуру:
- Выразите тепло, полученное водой, через массу воды, удельную теплоемкость воды, начальную температуру воды и конечную температуру:
- Обратите внимание, что и и что, как указано выше, они должны быть в сумме равными нулю:
- Поместите все термины с левой стороны, а все остальные термины с правой стороны.Решение для
и вставьте числовые значения:
Значение Почему конечная температура намного ближе к, чем к? Причина в том, что вода имеет большую удельную теплоемкость, чем большинство обычных веществ, и, следовательно, претерпевает меньшее изменение температуры при данной теплопередаче. Большой водоем, например озеро, требует большого количества тепла для значительного повышения температуры. Это объясняет, почему температура в озере остается относительно постоянной в течение дня, даже когда изменение температуры воздуха велико.Однако температура воды действительно меняется в течение длительного времени (например, с лета на зиму).
Это объясняет, почему температура в озере остается относительно постоянной в течение дня, даже когда изменение температуры воздуха велико.Однако температура воды действительно меняется в течение длительного времени (например, с лета на зиму).
Проверьте свое понимание Если для повышения температуры породы необходимо 25 кДж, от какого количества тепла необходимо нагреть камень?
В хорошем приближении теплопередача зависит только от разницы температур. Поскольку разница температур в обоих случаях одинакова, во втором случае необходимы те же 25 кДж. (Как мы увидим в следующем разделе, ответ был бы другим, если бы объект был сделан из некоторого вещества, которое меняет фазу где-то между и.)
Температурно-зависимая теплоемкость При низких температурах удельная теплоемкость твердых тел обычно пропорциональна. Первое понимание этого поведения было связано с голландским физиком Питером Дебаем, который в 1912 году рассмотрел атомные колебания с помощью квантовой теории, которую Макс Планк недавно использовал для излучения. Например, хорошее приближение для удельной теплоемкости соли NaCl: Константа 321 K называется температурой Дебая NaCl, и формула хорошо работает, когда Используя эту формулу, сколько тепла требуется для повышения температуры 24.0 г NaCl от 5 К до 15 К?
Например, хорошее приближение для удельной теплоемкости соли NaCl: Константа 321 K называется температурой Дебая NaCl, и формула хорошо работает, когда Используя эту формулу, сколько тепла требуется для повышения температуры 24.0 г NaCl от 5 К до 15 К?
Решение Поскольку теплоемкость зависит от температуры, нам нужно использовать уравнение
Мы решаем это уравнение для Q путем интегрирования обеих частей:
Затем подставляем данные значения и вычисляем интеграл:
Значение Если бы мы использовали уравнение и удельную теплоемкость соли при комнатной температуре, мы получили бы совсем другое значение.
11.2 Тепло, удельная теплоемкость и теплопередача – физика
Теплообмен, удельная теплоемкость и теплоемкость
В предыдущем разделе мы узнали, что температура пропорциональна средней кинетической энергии атомов и молекул в веществе, и что средняя внутренняя кинетическая энергия вещества тем выше, чем выше температура вещества.
Если два объекта с разной температурой соприкасаются друг с другом, энергия передается от более горячего объекта (то есть объекта с более высокой температурой) к более холодному (с более низкой температурой) объекту, пока оба объекта не будут иметь одинаковую температуру. . При равенстве температур нетто-передачи тепла, поскольку количество тепла, передаваемого от одного объекта к другому, равно количеству возвращенного тепла. Одним из основных эффектов теплопередачи является изменение температуры: нагревание увеличивает температуру, а охлаждение снижает ее.Эксперименты показывают, что тепло, передаваемое веществу или от него, зависит от трех факторов: изменения температуры вещества, массы вещества и определенных физических свойств, связанных с фазой вещества.
Уравнение теплопередачи Q равно
Q = mcΔT, Q = mcΔT,11,7
, где м – масса вещества, а Δ T – изменение его температуры в единицах Цельсия или Кельвина. Обозначение c обозначает удельную теплоемкость и зависит от материала и фазы.Удельная теплоемкость – это количество тепла, необходимое для изменения температуры 1,00 кг массы на 1,00 ºC. Удельная теплоемкость c – это свойство вещества; его единица СИ – Дж / (кг К) или Дж / (кг ° C ° C). Изменение температуры (ΔTΔT) одинаково в кельвинах и градусах Цельсия (но не в градусах Фаренгейта). Удельная теплоемкость тесно связана с понятием теплоемкости. Теплоемкость – это количество тепла, необходимое для изменения температуры вещества на 1,00 ° C ° C.В форме уравнения теплоемкость C равна C = mcC = mc, где m – масса, а c – удельная теплоемкость. Обратите внимание, что теплоемкость такая же, как и удельная теплоемкость, но без какой-либо зависимости от массы. Следовательно, два объекта, состоящие из одного и того же материала, но с разной массой, будут иметь разную теплоемкость. Это связано с тем, что теплоемкость – это свойство объекта, а удельная теплоемкость – это свойство любого объекта , изготовленного из того же материала.
Значения удельной теплоемкости необходимо искать в таблицах, потому что нет простого способа их вычислить.В таблице 11.2 приведены значения удельной теплоемкости для некоторых веществ в качестве справочной информации. Из этой таблицы видно, что удельная теплоемкость воды в пять раз больше, чем у стекла, а это означает, что для повышения температуры 1 кг воды требуется в пять раз больше тепла, чем для повышения температуры 1 кг стекла тем же способом. количество градусов.
Поддержка учителей
Поддержка учителей
[BL] [OL] [AL] Объясните, что эта формула работает только в том случае, если фаза вещества не меняется.Передача тепловой энергии, тепла и фазовый переход будут рассмотрены позже в этой главе.
Предупреждение о неправильном представлении
Единицами измерения удельной теплоемкости являются Дж / (кг ° C⋅ ° C) и Дж / (кг K). Однако градусы Цельсия и Кельвина не всегда взаимозаменяемы. В формуле для удельной теплоемкости используется разница в температуре, а не абсолютная температура. Это причина того, что градусы Цельсия могут использоваться вместо Кельвина.
| Вещества | Удельная теплоемкость ( c ) |
|---|---|
| Твердые вещества | Дж / (кг ⋅ ° C⋅ ° C) |
| Алюминий | 900 |
| Асбест | 800 |
| Бетон, гранит (средний) | 840 |
| Медь | 387 |
| Стекло | 840 |
| Золото | 129 |
| Тело человека (среднее) | 3500 |
| Лед (средний) | 2090 |
| Чугун, сталь | 452 |
| Свинец | 128 |
| Серебро | 235 |
| Дерево | 1700 |
| Жидкости | |
| Бензол | 1740 |
| Этанол | 2450 |
| Глицерин | 2410 |
| Меркурий | 139 |
| Вода | 4186 |
| Газы (при постоянном давлении 1 атм) | |
| Воздух (сухой) | 1015 |
| Аммиак | 2190 |
| Двуокись углерода | 833 |
| Азот | 1040 |
| Кислород | 913 |
| Пар | 2020 |
Таблица 11.2 Удельная теплоемкость различных веществ.
Snap Lab
Изменение температуры земли и воды
Что нагревается быстрее, земля или вода? Вы ответите на этот вопрос, проведя измерения для изучения различий в удельной теплоемкости.
- Открытое пламя. Соберите все распущенные волосы и одежду, прежде чем зажечь открытое пламя. Следуйте всем инструкциям своего учителя о том, как зажечь пламя. Никогда не оставляйте открытое пламя без присмотра. Знайте расположение противопожарного оборудования в лаборатории.
- Песок или грунт
- Вода
- Духовка или тепловая лампа
- Две маленькие банки
- Два термометра
Инструкции
Процедура
- Поместите равные массы сухого песка (или почвы) и воды одинаковой температуры в две небольшие банки. (Средняя плотность почвы или песка примерно в 1,6 раза больше плотности воды, поэтому вы можете получить равные массы, используя на 50 процентов больше воды по объему.)
- Нагрейте оба вещества (с помощью духовки или нагревательной лампы) в течение одинакового времени.
- Запишите конечные температуры двух масс.
- Теперь доведите обе банки до одинаковой температуры, нагревая их в течение более длительного периода времени.
- Снимите банки с источника тепла и измеряйте их температуру каждые 5 минут в течение примерно 30 минут.
Контроль захвата
Потребовалось больше времени, чтобы нагреть воду или песок / почву до той же температуры? Какой образец остыл дольше? Что этот эксперимент говорит нам о том, как удельная теплоемкость воды по сравнению с удельной теплотой земли?
- Песок / почва нагревается и остывает дольше.Это говорит нам о том, что удельная теплоемкость земли больше, чем у воды.
- Песок / почва нагревается и остывает дольше. Это говорит нам о том, что удельная теплоемкость воды больше, чем у земли.
- Вода нагревается и остывает дольше. Это говорит нам о том, что удельная теплоемкость земли больше, чем у воды.
- Вода нагревается и остывает дольше. Это говорит нам о том, что удельная теплоемкость воды больше, чем у земли.
Проводимость, конвекция и излучение
Всякий раз, когда есть разница температур, происходит передача тепла. Передача тепла может происходить быстро, например, через сковороду, или медленно, например, через стенки изолированного холодильника.
Существует три различных метода теплопередачи: теплопроводность, конвекция и излучение. Иногда все три могут происходить одновременно. См. Рисунок 11.3.
Рис. 11.3 В камине передача тепла происходит всеми тремя способами: теплопроводностью, конвекцией и излучением.Излучение отвечает за большую часть тепла, передаваемого в комнату. Передача тепла также происходит через теплопроводность в комнату, но гораздо медленнее. Теплообмен за счет конвекции также происходит через холодный воздух, поступающий в комнату вокруг окон, и горячий воздух, покидающий комнату, поднимаясь вверх по дымоходу.
Проводимость – это передача тепла при прямом физическом контакте. Тепло, передаваемое между электрической горелкой плиты и дном сковороды, передается за счет теплопроводности. Иногда мы пытаемся контролировать теплопроводность, чтобы чувствовать себя более комфортно.Поскольку скорость теплопередачи у разных материалов разная, мы выбираем такие ткани, как толстый шерстяной свитер, которые зимой замедляют отвод тепла от нашего тела.
Когда вы идете босиком по ковру в гостиной, ваши ноги чувствуют себя относительно комфортно… пока вы не ступите на кафельный пол кухни. Поскольку ковер и кафельный пол имеют одинаковую температуру, почему один из них холоднее другого? Это объясняется разной скоростью теплопередачи: материал плитки отводит тепло от вашей кожи с большей скоростью, чем ковровое покрытие, что делает его более холодным.
Поддержка учителей
Поддержка учителей
[BL] [OL] [AL] Спросите учащихся, какая сейчас температура в классе. Спросите их, все ли предметы в комнате имеют одинаковую температуру. Как только это будет установлено, попросите их положить руку на стол или на металлический предмет. Стало холоднее? Почему? Если их стол сделан из ламината Formica, то рука будет прохладно, потому что ламинат является хорошим проводником тепла и отводит тепло от руки, создавая ощущение «холода» из-за тепла, покидающего тело.
Некоторые материалы просто проводят тепловую энергию быстрее, чем другие. В целом металлы (например, медь, алюминий, золото и серебро) являются хорошими проводниками тепла, тогда как такие материалы, как дерево, пластик и резина, плохо проводят тепло.
На рис. 11.4 показаны частицы (атомы или молекулы) в двух телах при разных температурах. (Средняя) кинетическая энергия частицы в горячем теле выше, чем в более холодном теле. Если две частицы сталкиваются, энергия передается от частицы с большей кинетической энергией к частице с меньшей кинетической энергией.Когда два тела находятся в контакте, происходит много столкновений частиц, что приводит к чистому потоку тепла от тела с более высокой температурой к телу с более низкой температурой. Тепловой поток зависит от разности температур ΔT = Thot-TcoldΔT = Thot-Tcold. Таким образом, вы получите более сильный ожог от кипятка, чем от горячей воды из-под крана.
Рис. 11.4 Частицы в двух телах при разных температурах имеют разные средние кинетические энергии. Столкновения, происходящие на контактной поверхности, имеют тенденцию передавать энергию из высокотемпературных областей в низкотемпературные области.На этой иллюстрации частица в области более низких температур (правая сторона) имеет низкую кинетическую энергию перед столкновением, но ее кинетическая энергия увеличивается после столкновения с контактной поверхностью. Напротив, частица в области более высоких температур (слева) имеет большую кинетическую энергию до столкновения, но ее энергия уменьшается после столкновения с контактной поверхностью.
Конвекция – это передача тепла движением жидкости. Такой тип теплопередачи происходит, например, в котле, кипящем на плите, или во время грозы, когда горячий воздух поднимается к основанию облаков.
Советы для успеха
В обиходе термин жидкость обычно означает жидкость. Например, когда вы заболели и врач говорит вам «выпить жидкости», это означает только пить больше напитков, а не вдыхать больше воздуха. Однако в физике жидкость означает жидкость или газ . Жидкости движутся иначе, чем твердый материал, и даже имеют свой собственный раздел физики, известный как гидродинамика , который изучает их движение.
При повышении температуры жидкости они расширяются и становятся менее плотными.Например, на рис. 11.4 может быть изображена стенка воздушного шара с газами внутри воздушного шара с другой температурой, чем снаружи в окружающей среде. Более горячие и, следовательно, быстро движущиеся частицы газа внутри воздушного шара ударяются о поверхность с большей силой, чем более холодный воздух снаружи, заставляя воздушный шар расширяться. Это уменьшение плотности по отношению к окружающей среде создает плавучесть (тенденцию к повышению). Конвекция обусловлена плавучестью – горячий воздух поднимается вверх, потому что он менее плотен, чем окружающий воздух.
Иногда мы контролируем температуру своего дома или самих себя, контролируя движение воздуха. Герметизация дверей герметичным уплотнением защищает от холодного ветра зимой. Дом на рис. 11.5 и горшок с водой на плите на рис. 11.6 являются примерами конвекции и плавучести, созданными человеком. Океанские течения и крупномасштабная атмосферная циркуляция переносят энергию из одной части земного шара в другую и являются примерами естественной конвекции.
Рисунок 11.5 Воздух, нагретый так называемой гравитационной печью, расширяется и поднимается вверх, образуя конвективную петлю, которая передает энергию другим частям комнаты. По мере того, как воздух охлаждается у потолка и внешних стен, он сжимается, в конечном итоге становясь более плотным, чем воздух в помещении, и опускается на пол. Правильно спроектированная система отопления, подобная этой, в которой используется естественная конвекция, может быть достаточно эффективной для равномерного обогрева дома.
Рис. 11.6 Конвекция играет важную роль в теплопередаче внутри этого сосуда с водой.Попав внутрь жидкости, передача тепла другим частям горшка происходит в основном за счет конвекции. Более горячая вода расширяется, уменьшается по плотности и поднимается, передавая тепло другим областям воды, в то время как более холодная вода опускается на дно. Этот процесс повторяется, пока в кастрюле есть вода.
Излучение – это форма передачи тепла, которая происходит при испускании или поглощении электромагнитного излучения. Электромагнитное излучение включает радиоволны, микроволны, инфракрасное излучение, видимый свет, ультрафиолетовое излучение, рентгеновские лучи и гамма-лучи, все из которых имеют разные длины волн и количество энергии (более короткие волны имеют более высокую частоту и больше энергии).
Поддержка учителей
Поддержка учителей
[BL] [OL] Электромагнитные волны также часто называют электромагнитными волнами. Мы по-разному воспринимаем электромагнитные волны разной частоты. Так же, как мы можем видеть одни частоты как видимый свет, мы воспринимаем некоторые другие как тепло.
Вы можете почувствовать теплоотдачу от огня и солнца. Точно так же вы иногда можете сказать, что духовка горячая, не касаясь ее дверцы и не заглядывая внутрь – она может просто согреть вас, когда вы пройдете мимо.Другой пример – тепловое излучение человеческого тела; люди постоянно излучают инфракрасное излучение, которое не видно человеческому глазу, но ощущается как тепло.
Излучение – единственный метод передачи тепла, при котором среда не требуется, а это означает, что тепло не должно вступать в прямой контакт с какими-либо предметами или переноситься ими. Пространство между Землей и Солнцем в основном пусто, без какой-либо возможности теплопередачи за счет конвекции или теплопроводности. Вместо этого тепло передается за счет излучения, и Земля нагревается, поскольку она поглощает электромагнитное излучение, испускаемое Солнцем.
Рис. 11.7 Большая часть тепла от этого пожара передается наблюдателям через инфракрасное излучение. Видимый свет передает относительно небольшую тепловую энергию. Поскольку кожа очень чувствительна к инфракрасному излучению, вы можете почувствовать присутствие огня, даже не глядя на него. (Дэниел X. О’Нил)
Все объекты поглощают и излучают электромагнитное излучение (см. Рисунок 11.7). Скорость передачи тепла излучением в основном зависит от цвета объекта. Черный – наиболее эффективный поглотитель и радиатор, а белый – наименее эффективный.Например, люди, живущие в жарком климате, обычно избегают ношения черной одежды. Точно так же черный асфальт на стоянке будет горячее, чем прилегающие участки травы в летний день, потому что черный поглощает лучше, чем зеленый. Верно и обратное – черный цвет излучает лучше, чем зеленый. Ясной летней ночью черный асфальт будет холоднее, чем зеленый участок травы, потому что черный излучает энергию быстрее, чем зеленый. Напротив, белый цвет – плохой поглотитель и плохой радиатор. Белый объект, как зеркало, отражает почти все излучение.
Поддержка учителя
Поддержка учителя
Попросите учащихся привести примеры теплопроводности, конвекции и излучения.
Виртуальная физика
Формы и изменения энергии
В этой анимации вы исследуете теплопередачу с различными материалами. Поэкспериментируйте с нагревом и охлаждением железа, кирпича и воды. Для этого перетащите объект на пьедестал и затем удерживайте рычаг в положении «Нагреть» или «Охлаждать». Перетащите термометр рядом с каждым объектом, чтобы измерить его температуру – вы можете в режиме реального времени наблюдать, как быстро он нагревается или охлаждается.
Теперь попробуем передать тепло между объектами. Нагрейте кирпич и поместите его в прохладную воду. Теперь снова нагрейте кирпич, но затем поместите его поверх утюга. Что ты заметил?
Выбор опции быстрой перемотки вперед позволяет ускорить передачу тепла и сэкономить время.
Контроль захвата
Сравните, насколько быстро различные материалы нагреваются или охлаждаются. Основываясь на этих результатах, какой материал, по вашему мнению, имеет наибольшую удельную теплоемкость? Почему? Какая из них имеет наименьшую удельную теплоемкость? Можете ли вы представить себе реальную ситуацию, в которой вы хотели бы использовать объект с большой удельной теплоемкостью?
- Вода занимает больше всего времени, а железу нужно меньше времени, чтобы нагреться и остыть.Для теплоизоляции желательны объекты с большей удельной теплоемкостью. Например, шерстяная одежда с большой удельной теплоемкостью предотвратит потерю тепла телом.
- Вода занимает меньше всего времени, а железу нужно больше времени, чтобы нагреться и остыть. Для теплоизоляции желательны объекты с большей удельной теплоемкостью. Например, шерстяная одежда с большой удельной теплоемкостью предотвратит потерю тепла телом.
- Кирпич займет меньше всего времени, а железу нужно больше времени, чтобы нагреться и остыть.Для теплоизоляции желательны объекты с большей удельной теплоемкостью. Например, шерстяная одежда с большой удельной теплоемкостью предотвратит потерю тепла телом.
- Вода занимает меньше всего времени, а кирпичу нужно больше времени, чтобы нагреться и остыть. Для теплоизоляции желательны объекты с большей удельной теплоемкостью. Например, шерстяная одежда с большой удельной теплоемкостью предотвратит потерю тепла телом.
Поддержка учителей
Поддержка учителей
Попросите учащихся учесть различия в результатах интерактивных упражнений при использовании разных материалов.Например, спросите их, будет ли изменение температуры больше или меньше, если кирпич заменить железным блоком той же массы, что и кирпич. Попросите студентов рассмотреть одинаковые массы металлов, алюминия, золота и меди. После того, как они заявят, больше или меньше изменение температуры для каждого металла, попросите их обратиться к Таблице 11.2 и проверить, верны ли их прогнозы.
Передача тепла посредством теплопроводности: уравнения и примеры – стенограмма видео и урока
Примеры поведения
В нашей повседневной жизни есть всевозможные примеры поведения.Главное – подумать о том, соприкасаются ли предметы физически. Таким образом, кастрюля с кипящей водой, нагреваемая электрической плитой, получает тепловую энергию от плиты посредством теплопроводности. И когда вы дотрагиваетесь до металлического противня в духовке и обжигаетесь, это тоже произошло из-за кондукции.
Уравнение проводимости
В физике все должно иметь уравнение! Это какое-то неписаное правило. Проведение – не исключение. Насколько быстро происходит проводимость, зависит от нескольких факторов: из какого материала сделаны объекты (проводимости), площади поверхности двух соприкасающихся объектов, разницы температур между двумя объектами и толщины двух объектов.
В форме уравнения это выглядит так.
Q свыше т – это скорость теплопередачи – количество тепла, передаваемого за секунду, измеряемое в Джоулях в секунду или ваттах. k – это теплопроводность материала. Например, медь имеет теплопроводность 390, а шерсть – всего 0,04. T1 – это температура одного объекта, а T2 – температура другого.Поскольку это разница температур, вы можете использовать градусы Цельсия или Кельвина, в зависимости от того, что вам удобнее. А d – это толщина интересующего нас материала.
Таким образом, скорость передачи тепла к объекту равна теплопроводности материала, из которого он сделан, умноженному на площадь соприкасающейся поверхности. умножается на разницу температур между двумя объектами, деленную на толщину материала.
Пример расчета
Хорошо, давайте рассмотрим пример.Допустим, вы собираетесь в аквапарк и собираетесь взять с собой охладитель пенополистирола. Кулер имеет общую площадь 1,2 квадратных метра, толщину стенок 0,03 метра. Температура внутри кулера – 0 по Цельсию, а в самое жаркое время дня 38 градусов по Цельсию. Сколько тепловой энергии в секунду теряет кулер в это время суток? А сколько тепловой энергии теряется за три часа в аквапарке при температуре 38 градусов? (Примечание: теплопроводность пенополистирола равна 0.01.)
Все, что нам нужно сделать, чтобы решить эту проблему, – это подставить числа в уравнение. Потери тепловой энергии в секунду ( Q / t ) равны теплопроводности пенополистирола ( k ), умноженной на площадь поверхности охладителя ( A ), умноженную на разницу температур между охладитель и внешний вид ( T2 – T1 ), разделенные на толщину пенополистирола. Это 0,01, умноженное на 1,2, умноженное на 38, разделенное на 0.03. Введите все это в калькулятор, и вы получите 15,2 Джоулей в секунду или 15,2 Вт.
Q / t = ((0,01) (1,2) (38-0)) / 0,03 = 15,2 Дж / с или 15,2 Вт
Для второй части вопроса нам нужно выяснить, сколько энергия теряется за три часа. Что ж, у нас есть потери энергии за секунду – 15,2 Джоулей. Итак, нам просто нужно знать, сколько секунд осталось в трех часах. Три часа, умноженные на 60 минут, умноженные на 60 секунд, в сумме дают 10800 секунд.15,2 джоулей в секунду в течение 10 800 секунд … умножьте два числа вместе, и вы получите в общей сложности 164 160 джоулей за три часа.
И все – готово.
Краткое содержание урока
Проводимость – это передача тепловой энергии между двумя объектами, находящимися в прямом физическом контакте. Это один из трех типов теплопередачи, два других – конвекция и излучение. Когда два объекта с разной температурой соприкасаются друг с другом, между ними будет проходить тепловая энергия.Чтобы понять это, мы должны понять, что температура – это средняя кинетическая энергия молекул в веществе. Более горячие материалы содержат молекулы, которые движутся быстрее. Поэтому, когда холодный объект соприкасается с горячим объектом, быстро движущиеся горячие молекулы сталкиваются с более холодными молекулами, распространяя тепло от горячего объекта на холодный объект. Это будет продолжаться до тех пор, пока они не достигнут одинаковой температуры.
Некоторые материалы являются лучшими проводниками, чем другие. Вот почему кафельные полы кажутся такими холодными.Ваши ноги почти всегда теплее пола, но кафельный пол лучше проводит тепло. То, что ваша кожа ощущается как «холодная», – это просто передача тепла от ваших ног к полу, и это происходит намного быстрее с плиточным полом, чем с ковром, хотя обычно они имеют одинаковую температуру.
Уравнение проводимости говорит нам, что скорость теплопередачи ( Q / t ) в Джоулях в секунду или ваттах равна теплопроводности материала ( k ), умноженной на площадь поверхности соприкасающихся объектов ( A ), умноженное на разницу температур между двумя материалами ( T2 – T1 ), разделенную на толщину интересующего нас материала ( d ).Вы можете использовать это, чтобы определить скорость теплопередачи, но если вам дан конкретный период времени ( т ), вы также можете рассчитать общее переданное тепло.
Электроэнергия происходит повсюду вокруг нас: когда вы обжигаетесь на горячем противне, когда вы нагреваете кастрюлю на электрической плите, когда у вас установлена внутренняя изоляция стен. Всякий раз, когда тепло передается между двумя предметами, которые соприкасаются напрямую, это происходит из-за теплопроводности.
Результаты обучения
После завершения этого урока у вас должны быть способности:
- Определить проведение и выявить повседневные примеры его
- Объясните, как происходит проводимость, и какие факторы влияют на ее скорость.
- Вспомните уравнение проводимости
Определение, формула, уравнение, расчет и применение
Молярная теплоемкость – это количество тепла, необходимое для повышения температуры 1 моля вещества на 1 единицу, и рассчитывается путем деления теплоемкости на общее количество молей.
Вы когда-нибудь задумывались, почему мы не обжигаемся, пользуясь сковородой?
Конечно, нас защищает ручка, но почему она не так горячая, как сама сковорода? Ведь он подвергается одинаковому воздействию тепла.
Во-первых, ручку-попарку обычно делают из пластика, а это значит, что она плохо проводит тепло. Кроме того, при таком же тепловом воздействии повышение температуры пластиковой ручки намного меньше, чем повышение температуры металлической части.Это связано с высокой теплоемкостью ручки по сравнению с металлом, из которого сделана сковорода.
Теплоемкость определяется как количество тепловой энергии, необходимое для повышения температуры данной массы вещества на одну единицу. Удельная теплоемкость и молярная теплоемкость – это свойства, производные от теплоемкости материала.
Благодаря высокой теплоемкости ручки она не нагревается так, как сама сковорода (Фото: Kzenon / Shutterstock).
Удельная теплоемкость и молярная удельная теплоемкость
Теплоемкость – это обширное свойство, т.е.е., это зависит от количества и размера вещества. Модифицированная форма теплоемкости (называемая удельной теплоемкостью или просто удельной теплоемкостью) обычно используется в физике. Удельная теплоемкость не зависит от количества вещества и, следовательно, является более полезным свойством.
Удельная теплоемкость определяется как количество тепла, необходимое для повышения одной единицы массы вещества на 1 единицу температуры. Математически это теплоемкость вещества, деленная на его массу. Формула для определения теплоемкости:
Здесь c – теплоемкость, выраженная в единицах Дж / кг.K, C – теплоемкость вещества в Дж / К, а m – масса вещества в килограммах. Еще одна очень важная формула, используемая для выражения удельной теплоемкости:
Здесь также c обозначает удельную теплоемкость, ΔQ – разность тепловой энергии в джоулях, m – масса вещества, а ΔT – разница температур. в Кельвине.
В химии, где количество вещества обычно измеряется в молях, а не в граммах, дальнейшее изменение определения и формулы теплоемкости с включением молей значительно упрощает задачу.
Молярная теплоемкость определяется как количество тепла, необходимое для повышения 1 моля вещества на 1 градус Кельвина. Как и удельная теплоемкость, молярная теплоемкость является интенсивным свойством, то есть не зависит от количества вещества .
Математически это теплоемкость вещества, деленная на количество молей, и выражается как:
Здесь см – молярная теплоемкость (Дж / К · моль), C – теплоемкость (Дж / К ), а n – количество молей (моль).
Удельная теплоемкость и молярная теплоемкость могут не изменяться в зависимости от количества или размера вещества, но их значения меняются в зависимости от метода определения.
Когда к веществу, в частности к газам, подводится тепловая энергия, повышение температуры сопровождается увеличением либо объема, либо давления, а иногда и того и другого. Эти явления объясняются законом Шарля и законом Гей-Люссака.
CP, m и CV, m часто используются для обозначения молярной теплоемкости, измеренной при постоянном давлении (изобарический) и постоянном объеме (изохорный).
Значение молярной теплоемкости при постоянном давлении всегда больше, чем измеренное при постоянном объеме. Это связано с тем, что тепло, подаваемое при постоянном давлении, используется для выполнения работы и расширения в объеме. Напротив, тепло, подаваемое при постоянном объеме, полностью используется для повышения температуры вещества.
Отношение CP и CV называется коэффициентом теплоемкости или индексом адиабаты (γ = CP / CV) и является важным термином при работе с обратимыми процессами в термодинамике.С другой стороны, разница между CP, m и CV, m равна универсальной газовой постоянной R. Выражение CP, m – CV, m = R называется соотношением Майера.
Как рассчитать молярную теплоемкость вещества?
Определение теплоемкости вещества и, следовательно, его удельной теплоемкости и молярной теплоемкости – это не совсем ракетная наука. Значения можно вычислить, просто разбив их определения, найдя отдельные величины (количество подаваемого или отведенного тепла, начальную температуру, конечную температуру, массу и количество молей вещества) и подставив их в соответствующие места в формулы.
Шаг 1: Определение теплоемкости
Как уже определено, теплоемкость – это количество тепла, необходимое для повышения температуры известного количества вещества на одну единицу. Определение выражается как:
Здесь C – теплоемкость, Q – тепловая энергия, а ΔT – разница температур. ΔQ также может заменить Q.
ΔT – это T1-T2, где T1 – начальная температура, а T2 – конечная температура вещества. Начните с записи начальной / начальной температуры T1 с помощью термометра.Кроме того, взвесьте образец (м) и запишите значение в кг для дальнейшего использования.
Затем подайте в систему известное количество тепловой энергии (Q). Количество тепловой энергии может быть указано в джоулях или калориях. Когда вы закончите подачу тепла, дождитесь стабилизации температуры и запишите конечную температуру как T2.
Преобразуйте значение температуры в градусы Кельвина, добавив число 273,15 к значению Цельсия (0 ° c = 273,15 K). Если количество поставленной тепловой энергии выражается в калориях, переведите ее в джоули.Умножьте количество тепловой энергии в калориях на 4,184, чтобы получить количество в джоулях (1 кал = 4,184 джоулей).
Наконец, подставьте значения Q, T1 и T2 в формулу теплоемкости. Возьмите калькулятор или используйте свой мозг, чтобы выполнить вычисления и определить теплоемкость образца. Единицы теплоемкости – Дж / К.
Шаг 2: Определение удельной теплоемкости или удельной теплоемкости
Удельную теплоемкость или удельную теплоемкость можно легко найти, разделив теплоемкость образца на его массу (c = C / m).Идите вперед и разделите значение C, найденное на предыдущем шаге, на значение m, также отмеченное на предыдущем шаге, чтобы получить удельную теплоемкость образца. Полученное количество будет иметь единицы Дж / кг. K
Шаг 3: Определение молярной теплоемкости
Если вы прокрутите назад и посмотрите на формулу для молярной теплоемкости (см = C / n), вы найдете термин «n», обозначающее количество молей образца. Чтобы найти количество молей, разделите количество пробы на его молярную массу.
Теперь, когда вы нашли n, подставьте значение теплоемкости (C) и количество молей (n) в формулу и вычислите молярную теплоемкость.
Другой метод определения молярной теплоемкости – это умножение удельной теплоемкости (c) образца на его молярную массу (M). При этом обязательно переводите молярную массу в кг / моль.
Альтернативный метод – использование калориметра
Другой метод определения удельной теплоемкости вещества – использование калориметра.Калориметр – это научный прибор, состоящий из следующих частей: внутреннего и внешнего сосуда, мешалки, термометра, изоляционного материала и т. Д.
Внутренний сосуд или чашка содержит материал образца, удельную теплоемкость которого необходимо определить. Его помещают в середину внешнего сосуда, наполненного водой.
Процедура начинается с регистрации массы и начальной температуры воды и вещества пробы.
Калориметр используется для измерения теплового потока в реакции; этот метод называется калориметрией.(Фотография предоставлена Фуадом А. Саадом / Shutterstock)
Затем образец нагревается с помощью запальной проволоки. Когда температура образца поднимается выше температуры внешней воды, начинается теплообмен между ними. Через некоторое время электрический поток отключается и измеряются конечные температуры воды и образца. Тепловая энергия, теряемая материалом образца, будет равна теплу, полученному водой во внешнем сосуде. Теперь воспользуемся формулой ΔQ = mcΔT.
Для образца ΔQs = (mcΔT) s, а для воды ΔQw = (mcΔT) w.
Но ΔQs = ΔQw. Таким образом, (mcΔT) s = (mcΔT) w.
Замените значения массы образца и воды (ms и mw соответственно), изменения температуры (ΔTs = T1s-T2s и ΔTw = T1w-T2w) и удельной теплоемкости воды (cw) как 4,1796 кДж / кг.К для определения удельной теплоемкости образца (cs). Как только удельная теплоемкость вещества определена, умножив ее на его молярную массу, вы получите молярную теплоемкость вещества.
Области применения теплоемкости
Теплоемкость вещества определяет, где и когда оно может быть использовано. Например, ручки и ручки посуды производятся из материалов с высокой теплоемкостью для обеспечения безопасности пользователя. С другой стороны, термометры изготавливаются из материалов с низкой удельной теплоемкостью, чтобы обнаруживать даже самые незначительные колебания температуры.
Другой пример – использование воды в системах охлаждения двигателя.Вода имеет самую высокую удельную теплоемкость из всех жидкостей. При том же количестве тепла повышение температуры воды минимально, что делает его идеальным выбором для охлаждающей жидкости / агента.
Статьи по теме
Статьи по теме
Явление, когда морская вода остается прохладнее, чем окружающий воздух и песок в жаркий летний день, даже несмотря на то, что она подвергается воздействию такого же количества тепла от солнца, также может быть объяснено концепцией теплоемкости: высокой теплоемкости вода ответственна за многие природные явления, включая климат Земли и выживание водных организмов!
Работа и тепло
7.2 Работа и тепло
Цели обучения
- Определите вид работы по давлению и объему.
- Определите тепло .
- Соотнесите количество тепла с изменением температуры.
Мы уже определили работу как силу, действующую на расстоянии. Оказывается, есть и другие эквивалентные определения работы, которые также важны в химии.
Когда определенный объем газа расширяется, он работает против внешнего давления и расширяется (рисунок 7.2 «Объем в зависимости от давления»). То есть газ должен выполнять работу. Предполагая, что внешнее давление P ext является постоянным, объем работы, выполняемой газом, определяется уравнением
w = – P внешний × Δ V, где Δ V – изменение объема газа. Этот член всегда равен окончательному объему за вычетом начального объема,
. Δ В = В конечная – В начальнаяи может быть положительным или отрицательным, в зависимости от того, V final больше (расширяется) или меньше (сокращается), чем V начальный .Отрицательный знак в уравнении для работы важен и означает, что по мере увеличения объема (Δ V положительно) газ в системе теряет энергию в качестве работы. С другой стороны, если газ сжимается, Δ V отрицательно, и два отрицательных знака делают работу положительной, поэтому в систему добавляется энергия.
Рисунок 7.2 Объем в зависимости от давления
Когда газ расширяется против внешнего давления, газ действительно работает.
Наконец, рассмотрим единицы. Изменения объема обычно выражаются в таких единицах, как литры, тогда как давление обычно выражается в атмосферах. Когда мы используем уравнение для определения работы, единица измерения работы выражается в литрах · атмосферах или л · атм. Это не очень распространенная единица для работы. Однако существует переводной коэффициент между л · атм и обычной единицей работы, джоулями:
. 1 л · атм = 101,32 ДжИспользуя этот коэффициент преобразования и предыдущее уравнение для работы, мы можем рассчитать работу, выполняемую при расширении или сжатии газа.
Пример 2
Какую работу совершает газ, если он расширяется с 3,44 л до 6,19 л при постоянном внешнем давлении 1,26 атм? Выразите окончательный ответ в джоулях.
Решение
Сначала нам нужно определить изменение объема, Δ В . Изменением всегда является конечное значение минус начальное значение:
Δ В = В конечная – В начальная = 6.19 л – 3,44 л = 2,75 лТеперь мы можем использовать определение работы для определения проделанной работы:
w = – P ext · Δ V = – (1,26 атм) (2,75 л) = −3,47 л · атмТеперь мы построим коэффициент преобразования из отношения между литром · атмосферой и джоулями:
−3,47 л⋅атм × 101,32 Дж1 л⋅атм = −351 ДжМы ограничиваем окончательный ответ тремя значащими цифрами, если это необходимо.
Проверьте себя
Какая работа выполняется, когда газ расширяется от 0?66 л до 1,33 л при внешнем давлении 0,775 атм?
Ответ
−53 Дж
Тепло – еще один аспект энергии. Тепло – передача энергии от одного тела к другому из-за разницы температур. это передача энергии от одного тела к другому из-за разницы температур. Например, когда мы касаемся чего-либо руками, мы интерпретируем этот объект как горячий или холодный в зависимости от того, как передается энергия: если энергия передается в ваши руки, объект ощущается горячим.Если энергия передается от ваших рук к объекту, они становятся холодными. Поскольку тепло является мерой передачи энергии, оно также измеряется в джоулях.
Для данного объекта количество тепла ( q ) пропорционально двум вещам: массе объекта ( m ) и изменению температуры (Δ T ), вызванному передачей энергии. Мы можем записать это математически как
q∝m × ΔT, где ∝ означает «пропорционально». Чтобы сделать пропорциональность равенством, мы включаем константу пропорциональности.В этом случае константа пропорциональности обозначена как c и называется удельной теплоемкостью Константа пропорциональности между теплотой, массой и изменением температуры; также называется удельной теплоемкостью, или, более кратко, удельной теплоемкостью :
q = мк Δ T, где масса, удельная теплоемкость и изменение температуры умножаются. Удельная теплоемкость – это мера того, сколько энергии необходимо для изменения температуры вещества; чем больше удельная теплоемкость, тем больше энергии требуется для изменения температуры.Единицы измерения удельной теплоемкости – Jg⋅ ° C или Jg⋅K, в зависимости от единицы измерения Δ T . Вы можете заметить отклонение от требования выражать температуру в Кельвинах. Это связано с тем, что изменение температуры на на имеет одно и то же значение, независимо от того, выражены ли температуры в градусах Цельсия или Кельвинах.
Пример 3
Рассчитайте количество тепла, когда 25,0 г Fe повышают температуру с 22 ° C до 76 ° C. Удельная теплоемкость Fe равна 0.449 Дж / г · ° С.
Решение
Сначала необходимо определить Δ T . Изменением всегда является конечное значение минус начальное значение:
Δ T = 76 ° C – 22 ° C = 54 ° CТеперь мы можем использовать выражение для q , подставить все переменные и решить для тепла:
q = (25,0 г) (0,449 Дж · г⋅ ° C) (54 ° C) = 610 ДжОбратите внимание, как единицы измерения g и ° C отменяются, оставляя J единицей тепла. Также обратите внимание, что это значение q является положительным по своей природе, что означает, что в систему поступает энергия.
Проверьте себя
Рассчитайте количество тепла, возникающее при повышении температуры 76,5 г Ag с 17,8 ° C до 144,5 ° C. Удельная теплоемкость Ag составляет 0,233 Дж / г · ° C.
Ответ
2260 Дж
Как и в случае с любым уравнением, когда вы знаете все переменные, кроме одной, в выражении для q , вы можете определить оставшуюся переменную с помощью алгебры.
Пример 4
Для повышения температуры 373 г Hg на 104 ° C требуется 5 408 Дж тепла.Какова удельная теплоемкость Hg?
Решение
Мы можем начать с уравнения для q , но теперь даны другие значения, и нам нужно решить для удельной теплоемкости. Обратите внимание, что Δ T дается непосредственно как 104 ° C. Подставляющая,
5,408 Дж = (373 г) c (104 ° C)Разделим обе части уравнения на 373 г и 104 ° C:
c = 5408 Дж (373 г) (104 ° C)Соединив числа и собрав все единицы, получим
с = 0.139 мкг⋅ ° CПроверьте себя
Золото имеет удельную теплоемкость 0,129 Дж / г · ° C. Если для повышения температуры образца золота на 99,9 ° C требуется 1377 Дж, какова масса золота?
Ответ
107 г
В таблице 7.1 «Удельная теплоемкость различных веществ» перечислены удельные температуры некоторых веществ. Удельная теплоемкость – это физическое свойство веществ, поэтому это характеристика вещества.Общая идея состоит в том, что чем ниже удельная теплоемкость, тем меньше энергии требуется для изменения температуры вещества на определенную величину.
Таблица 7.1 Удельная теплоемкость различных веществ
| Вещество | Удельная теплоемкость (Дж / г · ° C) |
|---|---|
| вода | 4,184 |
| утюг | 0.449 |
| золото | 0,129 |
| ртуть | 0,139 |
| алюминий | 0,900 |
| спирт этиловый | 2,419 |
| магний | 1,03 |
| гелий | 5.171 |
| кислород | 0,918 |
Ключевые выводы
- Работа может быть определена как изменение объема газа при постоянном внешнем давлении.
- Тепло – это передача энергии из-за разницы температур.
- Теплота может быть рассчитана через массу, изменение температуры и удельную теплоемкость.
Упражнения
Дайте два определения работы.
Какой знак работы при увеличении объема пробы газа? Объясните, почему у работы есть этот знак.
Что происходит, когда газ расширяется с 3,00 л до 12,60 л при внешнем давлении 0,888 атм?
Что происходит, когда газ расширяется от 0?666 л до 2,334 л при внешнем давлении 2,07 атм?
Какова работа, когда газ сжимается с 3,45 л до 0,97 л при внешнем давлении 0,985 атм?
Какова работа, когда газ сжимается с 4,66 л до 1,22 л при внешнем давлении 3,97 атм?
Как и работа, знак тепла может быть положительным или отрицательным.Что происходит с общей энергией системы, если тепло положительно?
Как и работа, знак тепла может быть положительным или отрицательным. Что происходит с полной энергией системы, если тепло отрицательно?
Для повышения температуры до 36 требуется 452 Дж тепла.8 г образца металла от 22,9 ° C до 98,2 ° C. Какова теплоемкость металла?
Требуется 2267 Дж тепла, чтобы поднять температуру образца металла массой 44,5 г с 33,9 ° C до 288,3 ° C. Какова теплоемкость металла?
Неизвестная масса алюминия поглощает 187.9 Дж тепла и увеличивает его температуру с 23,5 ° C до 35,6 ° C. Какая масса у алюминия? Сколько это молей алюминия?
Образец He переходит с 19,4 ° C до 55,9 ° C при добавлении 448 Дж энергии. Какая масса у гелия? Сколько это молей гелия?
ответы
Работа – это сила, действующая на расстоянии или в объеме, изменяющемся против некоторого давления.
При положительном нагреве общая энергия системы увеличивается.
Пример удельной теплоемкости Задача
Энергия, необходимая для нагрева чего-либо, пропорциональна изменению массы и температуры материала.Константа пропорциональности называется удельной теплоемкостью.Фотография Johannes W на Unsplash
Удельная теплоемкость – это количество тепла на единицу массы, необходимое для повышения температуры материала на один градус Цельсия или Кельвина. Эти три примера задач удельной теплоемкости покажут, как найти удельную теплоемкость материала или другую информацию, включающую удельную теплоемкость.
Уравнение удельной теплоемкости
Уравнение, наиболее часто связанное с удельной теплоемкостью:
Q = mcΔT
, где
Q = тепловая энергия
m = масса
c = удельная теплоемкость
ΔT = изменение температуры = (T конечный – T начальный )
Хороший способ запомнить эту формулу: Q = «em cat»
По сути, это уравнение используется для определения количества тепла, добавляемого к материалу для повышения температуры на определенную величину (или количество теряется при остывании материала).
Это уравнение применимо только к материалам, которые остаются в одном и том же состоянии вещества (твердое, жидкое или газообразное) при изменении температуры. Фазовые изменения требуют дополнительных энергетических соображений.
Пример удельной теплоемкости Задача – найти количество тепла
Вопрос : 500-граммовый куб свинца нагревают от 25 ° C до 75 ° C. Сколько энергии требовалось для нагрева свинца? Удельная теплоемкость свинца составляет 0,129 Дж / г ° C.
Решение : Во-первых, давайте перейдем к известным нам переменным.
m = 500 грамм
c = 0,129 Дж / г ° C
ΔT = (T final – T начальный ) = (75 ° C – 25 ° C) = 50 ° C
Вставьте эти значения в уравнение теплоемкости сверху.
Q = mcΔT
Q = (500 грамм) · (0,129 Дж / г ° C) · (50 ° C)
Q = 3225 Дж
Ответ : Для нагрева свинца потребовалось 3225 Джоулей энергии куб от 25 ° C до 75 ° C.
Пример удельной теплоемкости Задача – найти удельную теплоемкость
Вопрос: 25-граммовый металлический шар нагревается до 200 ° C с помощью энергии 2330 Дж.Какова удельная теплоемкость металла?
Решение : Перечислите известную нам информацию.
м = 25 грамм
ΔT = 200 ° C
Q = 2330 Дж
Поместите их в уравнение теплоемкости.
Q = mcΔT
2330 Дж = (25 г) c (200 ° C)
2330 Дж = (5000 г ° C) c
Разделите обе стороны на 5000 г ° C
c = 0,466 Дж / г ° C
Ответ : Удельная теплоемкость металла составляет 0,466 Дж / г ° C.
Пример удельной теплоемкости Задача – определение начальной температуры
Вопрос: Горячему куску меди весом 1 кг дают остыть до 100 ° C.Если медь выделяет 231 кДж энергии, какова начальная температура меди? Удельная теплоемкость меди составляет 0,385 Дж / г ° C.
Решение : Перечислите наши переменные:
m = 1 кг
T final = 100 ° C
Q = -231 кДж (отрицательный знак означает, что медь охлаждается и теряет энергию.)
c = 0,385 Дж / г ° C
Нам нужно привести наши единицы в соответствие с единицами удельной теплоемкости, поэтому давайте преобразуем единицы массы и энергии.
