История развития химии – сообщение доклад кратко (8 класс)
Химия – это наука о составе, строении и свойствах всех веществ и соединений. Данная научная область очень важна в жизни людей. Но как вообще появилась химия? И как она улучшалась до сегодняшних дней?
Зарождение химии.
Это очень долгая история, а потому начать стоит с малого. По сути, химия существовала уже с тех пор, как на свет появились люди. Получение огня путем трения двух палок друг об друга или готовка мяса считается химией. Не скоро, но до нашей эры люди смогли делать многие вещи. Например, изготовление красок, ядов и лекарств, брожение, горение, плавление, металлургия и парфюмерия. В 5 веке до нашей эры появились некоторые умозаключения. Эмпедокл решил огонь, воду, землю и воздух считать основными элементами. Демокрит и Левкипп начали развивать теорию, доказывающую тот факт, что вещества состоят из атомов.
Следующий этап – алхимия.
В современности данной разновидности химии уже, конечно, не существует. Но в древности наука была знаменита. Попала она к людям от арабов. На Востоке был лишь прототип алхимии. Тем не менее, уже тогда появились следующие вещества: ртуть, сера, фосфор, практически все соли, азотная кислота и гидроксид натрия. В 3 веке до нашей эры наука добирается и до Европы. Там главным вопросом был создание золота и получение его из других веществ. Такой интерес к металлу возник в связи с тем, что золото было торговой валютой.
Самыми известными алхимиками принято считать Николу Фламеля, Авиценну, Альберта Великого и Гебера. И, конечно же, все знают о том, как алхимики пытались создать философский камень – вещество, способное превращать что угодно в золото и получить эликсир жизни. Его еще называли пятым элементом.
Кто же ввел термин химии в науку?
Только в 16 веке химия стала известна как научная дисциплина. Но была одна проблема: ввиду того, что химия не выражалась количественно, многие спорили, наука или она вообще или просто вид познания. Ломоносову в своей же первой работе, относящаяся к химии, доказал, что это наука. Естественно, на этом химические достижения людей не закончились. К примеру, Гельмонт открыл углекислый газ, а Менделеев создал всем известную таблицу элементов.
Вариант 2
Химия – это наука о строении, составе и свойствах веществ и их соединений. Химия, как и другие науки, развивались постепенно: открывались ранее неизвестные элементы, получали новые соли и кислоты, создавались материалы. Теории людей, используемые для развития химии, изменили мировоззрение всего человечества. Их вклад трудно оценить. Но кто помог усовершенствовать химию и как это вышло?
Первооткрыватели химии.
Вполне логично, что в первую очередь мы должны быть благодарны тем людям, которые вообще открыли химию.
Затем уже, ближе к 17 веку, химию начали определять как науку. Ну, почти. Дело в том, что между учеными шли споры, наука ли химия или же просто познания. Спор возник по той причине, что в химии нельзя было ничего сосчитать количественно. В конце концов, ссора была разрешена.
Михаил Юрьевич Ломоносов – без него никто бы не смог.
Да, именно он доказал, что химия – это наука, а не обычные практические познания. Он же дал правильное определение науке. Вообще, Ломоносов – писатель, в первую очередь, это да. Но еще он химик, физик и энциклопедист. Ломоносов открыл много чего нового: теория молекулярно – кинетического тепла, закон термодинамики, наука о стекле. Ломоносов даже доказал то, что у Венеры есть атмосфера.
Дмитрий Иванович Менделеев – царь химии.
Ну, без него никак вовсе. Если усилия остальных химиков трудно оценить, то вклад данного человека и вовсе оценить нельзя. Самые главные и великие его открытия – это периодический закон и таблица всех химических элементов, которая, кстати, заполняется и в сегодняшние дни.
Самые главные и великие его открытия – это периодический закон и таблица всех химических элементов, которая, кстати, заполняется и в сегодняшние дни.
Бутлеров и его положения.
Немало важны и его открытия. Является основателем трех теорий строения органических веществ, а еще основал специальную школу для химиков. Изучил изомерию почти всех органических соединений, а также синтезировал вещества.
Кекуле Фридрих Август – органик из Германии.
Уже ясно, что исследования шли на органику. Ему принадлежит идея о том, что валентность – это целая единица сродства, которой обладает атом. Именно он сказал, что углерод четырехвалентен.
История развития химии
Интересные ответы
- Строение и деление клетки – доклад сообщение
 Термин «клетка» предложил Гук еще в 1665 году. Клетка является основой учений цитологии.
Термин «клетка» предложил Гук еще в 1665 году. Клетка является основой учений цитологии. - Сообщение Водоросли в жизни человека (7 класс доклад)
Водоросли – это низшие растения. Их роль в жизни человека достаточно велика. Как и остальные растения, водоросли осуществляют процесс фотосинтеза.
- Лотос – сообщение доклад (из красной книги)
Лотос – цветок небесной красоты, его лепестки бывают чаще всего желтого и розового цвета, но есть и другие цвета, сам он растет из илистой воды. Он имеет мистическое значение во всех народах, о чем и пойдет речь далее.
- Животные
- Коала сообщение доклад 2, 4, 7 класс
Коалу нередко называют сумчатым медведем, но на самом деле австралийский пушистик далек от медведей, но близок вомбатам, чьим близким родственником и является
Урок 4. арены (ароматические углеводороды) – Химия – 10 класс
Химия, 10 класс
Урок № 4. Арены (ароматические углеводороды)
Перечень вопросов, рассматриваемых в теме: урок посвящён ароматическим углеводородам, их номенклатуре, физическим и химическим свойствам, а также роли в жизни человека.
Глоссарий
Ароматический углеводород – соединение, содержащее в молекуле специфическую систему чередующихся одинарных и двойных связей (сопряженных π-связей).
Акцептор – атом или группа атомов, принимающих электроны и образующих химическую связь за счёт своей пустой орбитали и неподелённой пары электронов донора.
Гибридизация – процесс взаимодействия разных, но близких по энергии электронных орбиталей, приводящий к их выравниванию по форме и энергии.
Гомология – явление сходства по составу, строению, химическим свойствам и принадлежности к тому же классу одного вещества с другим веществом, но различающиеся друг от друга на одну или несколько групп СН
Горение – быстро протекающий процесс окисления вещества, сопровождающийся большим выделением тепла и ярким свечением.
Группа функциональная – группа атомов, определяющая наиболее характерные химические свойства вещества и его принадлежность к определенному классу.
Донорное (электронодонорное) свойство – способность атомов элемента отдавать свои электроны другим атомам. Количественной мерой донорных свойств атомов, образующих химическую связь, является их электроотрицательность.
Изомерия – явление существования веществ, одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и вследствие этого по физическим и химическим свойствам. Такие вещества называются изомерами.
Формула структурная – изображение молекулы, в котором показан порядок связывания атомов между собой. Химические связи в таких формулах обозначаются черточками.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тесто по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Арены (ароматические углеводороды) – органические соединения, имеющие общую формулу С
Бензольное кольцо – это цикличная группа шести атомов углерода; структуру в виде кольца предложил Ф. А. Кекуле в 1865 г.
Простейшим представителем аренов является бензол С6Н6. Среди других представителей можно отметить, например, кумол (изопропилбензол) C6H5CH(CH3)2.
Формулы бензола
Полная структурная (формула, предложенная Ф.А. Кекуле) | |
Сокращенная структурная (формула, предложенная Ф.А. Кекуле) | |
Сокращенная структурная с сопряженными связями |
Бензол – первый представитель класса аренов (ароматических углеводородов). Каждый атом углерода в молекуле бензола С6Н6 имеет 4 валентных электрона: s1p3. Тип гибридизации атомов углерода в бензольном кольце молекулы аренов, как и у алкенов, – sp2.
sp2 гибридизация – это смешивание одного s и двух p электронных облаков и образование трёх одинаковых (гибридных). Гибридные облака участвуют в образовании 3 δ-связей, лежащих на плоскости. Оставшееся у каждого из шести атомов углерода негибридизованное третье p-облако имеет форму гантели. Шесть p-облаков, перекрываясь с соседними над и под плоскостью δ-связей, участвует в образовании общего 6-электронного облака, которое является общим для всех атомов углерода.
Шесть p-облаков, перекрываясь с соседними над и под плоскостью δ-связей, участвует в образовании общего 6-электронного облака, которое является общим для всех атомов углерода.
Свойства бензола и других ароматических соединений и их обусловленность электронным строением молекулы бензола.
Физические и химические свойства бензола и его гомологов
Физические свойства бензола
Бензол – бесцветная жидкость с характерным запахом, которая кипит при 80,1 °С, ρ = 0,876 г/cм3. Бензол очень огнеопасен!
Бензол является хорошим растворителем. В пробирку нальем 1 мл дистиллированной воды и добавим несколько капель масла. Масло не растворяется в воде даже после перемешивания содержимого. Во вторую пробирку нальем 1 мл бензола. Перемешаем содержимое. Масло растворяется в бензоле. Однако ввиду высокой токсичности, использование бензола в качестве растворителя нежелательно.
Сопряжение π-связей в молекуле бензола
Образование пи-связей в молекуле бензола обусловлено тем, что негрибридизованные облака образуют общие электронные плотности в виде колец над и под плоскостью молекулы бензола. Обратите внимание, что в результате образуется общее пи-электронное облако, а все связи между атомами углерода в молекуле бензола оказываются одинаковыми (их еще называют полуторными). Именно пи-электронные облака являются объяснением того факта, что – в отличие от первоначального варианта представления молекулярной формулы бензола с чередованием одинарных и двойных связей – бензол не проявляет выраженных свойств алкенов.
Обратите внимание, что в результате образуется общее пи-электронное облако, а все связи между атомами углерода в молекуле бензола оказываются одинаковыми (их еще называют полуторными). Именно пи-электронные облака являются объяснением того факта, что – в отличие от первоначального варианта представления молекулярной формулы бензола с чередованием одинарных и двойных связей – бензол не проявляет выраженных свойств алкенов.
Химические свойства бензола
Реакции замещения (как алканы) | Галогенирование | Реакция происходит в присутствии катализатора (соли FeBr3, AlCl3, AlBr3): |
Нитрование | ||
Алкилирование | ||
Реакции присоединения (как алкены) | Каталитическое гидрирование | |
Радикальное хлорирование | ||
Окисление | Горение | 2С6Н6 + 15О2→12СО2 + 6Н2О |
Взаимодействие с перманганатом калия | Не обесцвечивает раствор перманганата калия (реакция не идёт) |
Горение бензола
Бензол горит жёлтым коптящим пламенем, если внести в пламя стекло, на нем быстро оседает слой копоти.
Электрофилы – это положительно заряженные частицы, имеющие свободную орбиталь на внешнем электронном уровне и способные образовывать новые ковалентные связи за счёт пары электронов другой молекулы. К электрофилам относятся молекулы галогенов, SO3 и молекулы с сильнополяризованной связью (HCOO–Br+).
Электрофильное замещение в ароматических соединениях можно представить реакцией присоединения-отщепления. Эта реакция проходит в несколько стадий.
При инициации реакции молекула хлора распадается на два иона. Катализатор, например, AlCl3, присоединяя ион хлора Cl−, приобретает отрицательный заряд. Оставшийся ион хлора Cl+, который является электрофилом, присоединяется к образовавшемуся на катализаторе отрицательному иону AlCl4−.Образованное соединение называется π-комплексом. Этот комплекс вступает в реакцию с молекулой бензола, обеспечивая присоединение ионов хлора Cl+ к атомам углерода.
Сравнение свойств бензола и толуола
Бензол
Отношение к раствору KMnO4 | Не окисляется |
Горение на воздухе | 2С6Н6 + 15О2 → 12СО2 + 6Н2О |
Реакция гидрирования | |
Присоединение хлора (галогена) | |
Замещение водорода хлором (галогеном) | |
Нитрование |
Толуол
Отношение к раствору KMnO4 | Окисление боковых цепей (в присутствии h3SO4 или KMnO4) |
Горение на воздухе | C6H5–CH3 + 9O2 → 7CO2 + 4H2O |
Реакция гидрирования | |
Присоединение хлора (галогена) | |
Замещение водорода хлором (галогеном) | |
Нитрование |
ПРИМЕРЫ И РАЗБОР РЕШЕНИЯ ЗАДАНИЙ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Определение формулы бензола. Пошаговый тренажер решения задач
Определение формулы бензола. Пошаговый тренажер решения задач
Шаг 1.
Найдите молекулярную формулу бензола, если известно, что его пары в 2,78 раз тяжелее азота.
1. Вывод формулы для нахождения относительной массы бензола из формулы относительной плотности.
D (по N2) = Mr (бензола) / Mr (N2), выведем формулу для расчета относительной массы бензола:
Mr (бензола) = D (по N2) [×] Mr (N2).
Ответ: Mr (бензола) = D (по N2) × Mr (N2)
2. Рассчитаем относительную молекулярную массу азота, используя периодическую систему химических элементов Д.И. Менделеева.
Mr (N2) = 2 · 14 = 28.
Ответ: Mr (N2) = 28.
3. Рассчитаем относительную молекулярную массу бензола (с точностью до целых):
Mr (бензола) = 2,78 · 28 = 77,84 ≈ 78.
Ответ: Mr (бензола) = 78
4. Бензол является углеводородом. Все углеводороды состоят из углерода и водорода.
Бензол является углеводородом. Все углеводороды состоят из углерода и водорода.
5. Нахождение количества атомов углерода в молекуле бензола. Количество атомов углерода в молекуле бензола равно […].
Ответ: 6.
Пусть количество атомов углерода равно x, а количество атомов водорода – y. Поскольку вещество имеет равное количество атомов углерода и водорода, то x = y.
Составим уравнение с учетом значений относительной атомной массы углерода и водорода, а также вычисленной относительной молекулярной массы бензола.
12 ⋅ x + 1 ⋅ y = 78.
x = y = 78 / 13 = 6.
Следовательно, в молекуле содержатся шесть атомов углерода и шесть атомов водорода.
6. Составление молекулярной формулы бензола С6Н6
2. Решение задачи о свойствах толуола
В результате взаимодействия 2,5 моль толуола с бромом образовалось 700 г трибромтолуола. Найдите практический выход реакции (%) от теоретически возможного. Ответ округлите до целого числа.
Ответ: 86 %.
Решение.
1. Запишем уравнение реакции.
С6Н5СН3 + 3Br2 → | С6Н2СН3Br3 + | 3НBr |
Толуол | Трибромтолуол |
2. Рассчитаем молярную массу трибромтолуола.
М (С6Н2СН3Br3) = 329 г/моль
3. Рассчитаем теоретический выход (г) трибромтолуола.
2,5 моль | х г | |
С6Н5СН3 + 3Br2 → | С6Н2СН3Br3 + | 3НBr |
1 моль | 1 моль · 329 г/моль |
2,5 моль / 1 моль = х г / 1 моль · М (С6Н2СН3Br3)
х = 2,5 · 329 / 1 = 815 (г).
4. Рассчитаем теоретический выход (%) трибромтолуола.
Составляем пропорцию:
815 г составляет 100 %
700 г – х %.
Отсюда:
х = 700 · 100 / 815 = 85,88 ≈ 86 (%).
Ученые и изобретатели России – Менделеев Дмитрий Иванович
День рождения: 27 января 1834 г. День смерти: 20 января 1907 г. Место рождения: Тобольск Семейное положение: женат дважды. Первая жена — Феозва Никитична Лещева (1862—1880). Вторая жена — Анна Ивановна Попова (1882—1907). Деятельность и интересы: химия, технология, экономика, метрология, агрохимия и сельское хозяйство, просвещение, физическая химия, химия твердого тела, теория растворов, физика жидкостей и газов, технология нефти, приборостроение, метеорология, воздухоплавание, кораблестроение, освоение Крайнего Севера, педагогика, переплетные работы, картонажные работы Свои «три службы Родине» Менделеев определял так: научная деятельность, преподавание и служба российской промышленности. Еще факты Еще факты |
Образование, степени и звания
1847-1849, Тобольская мужская гимназия
1876, Императорская Санкт-Петербургская Академия Наук: член-корреспондент
Работа
1855, Симферопольская мужская гимназия: старший учитель естественных наук
1903, Киевский политехнический институт: председатель Государственной экзаменационной комиссии
Открытия
В ходе работы над трудом «Основы химии», Д.И. Менделеев в феврале 1869 года открыл один из фундаментальных законов природы — периодический закон химических элементов, позволяющий не только с точностью определить многие свойства уже известных элементов, но и прогнозировать свойства еще не открытых. В ходе работы над периодической таблицей Менделеев уточнил значения атомных масс девяти элементов, а также предсказал существование, атомные массы и свойства ряда элементов, открытых позже (галлия, скандия, германия, полония, астата, технеция и франция). Дополнил таблицу нулевой группой благородных газов в 1900 году.
В 1850-х годах исследовал явления изоморфизма, которые демонстрируют взаимозависимость кристаллической формы и химического состава соединений, а также зависимость свойств элементов от их атомных объемов.
Дополнил таблицу нулевой группой благородных газов в 1900 году.
В 1850-х годах исследовал явления изоморфизма, которые демонстрируют взаимозависимость кристаллической формы и химического состава соединений, а также зависимость свойств элементов от их атомных объемов.
В 1859 году Менделеев сконструировал прибор для определения плотности жидкости — пикнометр.
В 1860 году открыл температуру абсолютного кипения жидкостей — критическую температуру, при которой плотность и давление насыщенного пара максимальны, а плотность жидкости, находящейся в динамическом равновесии с паром, минимальна.
Биография
Русский ученый-энциклопедист, автор фундаментальных работ по химии, физике,
химической технологии, метрологии, воздухоплаванию, метеорологии, сельскому
хозяйству, экономике и т.д. Самое известное открытие Менделеева —
фундаментальный закон природы, периодический закон химических элементов.
Сам полагал, что его имя составили «всего более четыре предмета… периодический закон, исследование упругости газов, понимание растворов как ассоциации и “Основы химии”». Периодический закон был открыт им в ходе работы над «Основами химии». Растворы исследовал всю жизнь, постепенно постигая природу химического соединения как такового, а уравнение Клапейрона—Менделеева (общее уравнение состояния идеального газа) — важная формула, устанавливающая зависимость между давлением, молярным объемом и абсолютной температурой идеального газа.
На протяжении всей жизни регулярно участвовал в производственных предприятиях, где теоретические научные проблемы обладали скорее прикладным значением. Кроме того, интересовался весьма разноплановыми сферами деятельности, включая воздухоплавание, кораблестроение и освоение Крайнего Севера.
Менделеев — автор более полутора тысяч трудов, в том числе классических
«Основ химии», первого систематизированного изложения неорганической химии
(1869—1871). Пользовался огромным научным авторитетом во всем мире и был
удостоен множества наград — российских и зарубежных орденов и медалей,
почетного членства в разнообразных российских и зарубежных научных обществах,
многочисленных научных званий и т.д.
Пользовался огромным научным авторитетом во всем мире и был
удостоен множества наград — российских и зарубежных орденов и медалей,
почетного членства в разнообразных российских и зарубежных научных обществах,
многочисленных научных званий и т.д.
Значение и состав химической промышленности (кратко) | География. Реферат, доклад, сообщение, краткое содержание, лекция, шпаргалка, конспект, ГДЗ, тест
Тема: Химическая промышленность мира
Химическая промышленность имеет огромное значение в развитии народного хозяйства страны. Ее продукция используется практически во всех отраслях хозяйства: от быта и здравоохранения до промышленности, транспорта и сельского хозяйства. Химическая промышленность производит новые материалы, заменяющие природные, она имеет огромные возможности для комбинирования производства и получения различной продукции.
В состав химической промышленности входят:
- Горно-химическая промышленность, осуществляющая добычу минерального химического сырья: апатитов, фосфоритов, серы, поваренной, калийной и глауберовой солей.

- Основная химия, включающая в себя: а) производство кислот, солей и щелочей; б) производство минеральных удобрений.
- Химия органического синтеза.
- Химия полимеров (производство химических волокон, пластмасс и синтетического каучука). Материал с сайта http://worldofschool.ru
- Переработка полимеров (производство изделий из пластмасс, производство резины и изделий из неё).
- Тонкая химия, включающая в себя: а) фармацевтическую промышленность; б) парфюмерную промышленность.
- Бытовая химия (производство моющих средств, лаков и красок).
Конспект о химическая промышленности кратко
Значение химической промышленности доклад
Состав и значение химической промышленности кратко
Химическая промышленность краткое сообщение
Горная химия мира кратко
Влияние алкоголя на здоровье человека
Алкоголь и здоровье человека — не совместимые вещи
Этиловый спирт – это ядовитое наркотическое вещество.
В алкоголе содержатся следующие ядовитые примеси: эфиры, альдегиды сивушные масла, свободные кислоты. Спиртные напитки у всех клеток тела отнимают воду, с которыми он соприкасается.
Спиртное поступает в кровь и человек начинает пьянеть. Слизистой желудка всасывается примерно 90% принятого внутрь алкоголя. Алкоголь разрушает центральную нервную систему. Он изменяет функцию нервных клеток, проникая внутрь их. Каждый второй больной алкоголизмом имеет пораженную сердечно–сосудистую систему.
Алкоголь поражает поджелудочную железу, влияет на печень, желудок, пищевод.
Сильнее всего от алкоголя страдает человеческий мозг.
Алкоголь склеивает эритроциты в крови, что приводит к образованию тромбов.
Доказано, что сто грамм водки убивает 8 000 мозговых клеток. В результате, мозг становится меньше в объеме, на нем появляются рубцы и язвочки, не исключены также кровоизлияния и пустоты.
Наибольшее влияние спиртного приходится на кору головного мозга. Страдает от этого высшая нервная система. Пьяный человек тяжело мыслит и трудно принимает решения.
Воздействие алкоголя на организм человека
Организм человека, употребляющего спиртные напитки, изнашивается в несколько раз быстрее, чем организм здорового, не пьющего. Спиртные напитки влияют абсолютно на все системы и органы без исключения, ослабляют иммунитет, приводят к частым заболеваниям.
Вред алкоголя
45% пьющих людей умирают от инфарктов. Не мал процент и тех пьющих, кто кончает жизнь самоубийством. Смерть наступает и от болезней, которые возникают из-за регулярного приема спиртного. Алкоголь толкает на действия криминального характера, необдуманные проступки.
Алкоголь тесно связан и с потенцией. Спиртное снижает влечение к противоположному полу, снижает сексуальную активность.
Многих алкоголиков со стажем уже не интересуют многие жизненные вопросы, для них важно только одно – где найти выпить!
Берегите свое здоровье! Не пейте! Откажитесь от спиртного вообще!
СПб ГБУЗ «Городская поликлиника № 72» проводит диспансеризацию по адресу СПб. , пос. Металлострой, Пионерская ул., д.1 (взрослое отделение).
, пос. Металлострой, Пионерская ул., д.1 (взрослое отделение).
Куда обращаться:
1) Кабинет профилактики № 308 (3 этаж):
понедельник — 11.00-14.00
вторник — 16.00-20.00
среда — 08.00-12.00
четверг — 13.00-17.00
пятница — 10.00-14.00
2) К участковому терапевту с 8.00-20.00 ежедневно, кроме субботы и воскресенья.
Справки по тел: 241-54-58 (регистратура), 241-54-59 (кабинет № 308).
В 2018 году диспансеризации подлежат граждане следующих годов рождения: 1916, 1919, 1922, 1925, 1928, 1931, 1934, 1937, 1940, 1943, 1946, 1949, 1952, 1955, 1958, 1961, 1964, 1967, 1970, 1973, 1976, 1979, 1982, 1985, 1988, 1991, 1994, 1997.
Трезвость – залог здоровья и долголетия! Если у вас или у близкого вам человека развивается алкоголизм — появилась психологическая и физическая зависимость от алкоголя, признаки похмелья, — обратитесь к врачу (наркологу).
Круглосуточный телефон доверия в Санкт-Петербурге для взрослых: 714-42-10; для детей и подростков: 576-10-10. Антиалкогольные горячие линии 8-800-200-0-200, 8-800-200-00-08.
Бытовая химия загрязняет воздух гораздо больше, чем думали
- Джонатан Эймос
- Корреспондент Би-би-си по вопросам науки
Автор фото, Getty Images
Подпись к фото,Товары бытовой химии – источних загрязнения воздуха летучими органическими соединениями
Проведенное в США исследование показало, что бытовая химия и химические вещества, содержащиеся в продуктах ежедневного использования, стали одним из главных источников загрязнения воздуха в городах. В этом смысле они уже соперничают с выхлопами автомобилей.
Исследование, которое провели ученые Университета Колорадо, было в основном посвящено так называемым летучим органическим соединениям (ЛОС).
Эти вещества содержатся в продуктах на основе нефти, таких как чистящие жидкости и краски. Попадая в воздух, ЛОС могут образовывать вредные для здоровья частицы.
Ученые утверждают, что мы сильно недооцениваем вред, наносимый летучими органическими соединениями, не являющихся частью автомобильных выхлопов.
Это кажется удивительным, поскольку по весу мы используем гораздо больше горючего, чем других химических продуктов.
Меньше бытовой химии
Около 95% сырой нефти идет на производство различных видов топлива и лишь примерно 5% перерабатывается для использования в таких продуктах, как дезодоранты, пестициды и клеи.
Но эксперт американского Национального управления океанических и атмосферных исследований доктор Джессика Гилман утверждает, что выводы исследования не должны удивлять, поскольку автомобильное топливо сгорает (превращаясь в основном в двуокись углерода и воду), а многие продукты бытовой химии просто выделяют эти вещества в воздух, как и было задумано при их создании.
“Чаще всего их используют в качестве растворителей – в таких продуктах, как жидкость для снятия лака или лак для волос, которым я пользовалась сегодня утром. Часто их используют в качестве чистящих веществ, например, для чистки ковров”, – объясняет Джессика Гилман.
“Без них трудно, поскольку альтернатива таким чистящих жидкостям – обычная вода, которая, как вы знаете, не выводит все пятна”, – говорит Джессика Гилман.
Ее коллега доктор Брайан Макдональд тем не менее считает, что сокращение количества химических веществ в домашнем хозяйстве было бы делом полезным.
“Используйте как можно меньше подобных веществ – не больше, чем необходимо”, – советует он.
Анализ
Роджер Харрабин, обозреватель Би-би-си по вопросам экологии
Воздух, которым мы дышим, содержит настолько богатую смесь разнообразных компонентов, что исследователи не могут быть уверены в том, какое химическое вещество вызывает ту или иную проблему.
Установить ограничения по выбросам в атмосферу, которые удовлетворили бы всех, – это еще более сложная задача. Некоторым нравятся освежители воздуха. Другие от них задыхаются.
Чистящие аэрозоли полезны в хозяйстве, но у некоторых от них слезятся глаза. Я знаю человека, у которого в детстве спровоцировали астму химические выделения из сборной мебели в его спальне.
Эта область исследования запущена, поскольку население и СМИ уделяют основное внимание не химическим выделениям в доме, а автомобильным выхлопам на улице.
Ученые из Университета Колорадо собрали воедино большой объем информации по теме своего исследования.
Они заново изучили, какие химические вещества производители используют в своих товарах, и проверили статистику различных надзорных и регулирующих ведомств. Они запустили в небо над Лос-Анджелесом зонды, берущие пробы воздуха и оценили итоги измерений качества воздуха в домах и на улице, собранных другими исследователями.
Исследовательская группа пришла к выводу, что количество ЛОС, выделяемых в США потребительскими и промышленными продуктами, весьма вероятно, в два или три раза выше нынешних оценок. (Существуют также естественные источники ЛОС в окружающей среде).
Ученые также считают, что эти исследования переоценивают значение выбросов в атмосферу автомобильных двигателей.
50 на 50
В качестве примера исследователи приводят нынешние оценки американского Агентства по защите окружающей среды.
Агентство предполагает, что около 75% выбросов основанных на нефти ЛОС приходятся на автомашины и примерно 25% – на химические продукты.
По оценке ученых Университета Колорадо, расклад здесь примерно 50 на 50.
Автор фото, DAVID ILIFF
Подпись к фото,Ученые Университета Колорадо собрали воедино большой объем информации по теме своего исследования
“Использование этих продуктов приводит к тому, что выделения из них ЛОС сравнимы с тем, что вылетает из выхлопной трубы вашего автомобиля. Одна из причин в том, что в США, как и в Европе, меры по контролю над автомобильными выхлопами оказались действительно успешными”, – говорит доктор Макдональд, ведущий автор исследования.
Одна из причин в том, что в США, как и в Европе, меры по контролю над автомобильными выхлопами оказались действительно успешными”, – говорит доктор Макдональд, ведущий автор исследования.
Эксперты утверждают, что результаты американского исследования применимы и к другим развитым странам, в том числе европейским.
“Это исследование – полезное напоминание о том, что дискуссии о чистоте окружающей среды должны принимать во внимание все источники ее загрязнения и что одни лишь меры по снижению автомобильных выхлопов решают только часть проблемы”, – говорит профессор респираторной медицины Медицинской школы Брайтона и Суссекса Энтони Фру:
Автомобили, конечно же, выделяют в атмосферу не только ЛОС. В числе вредных выбросов автомобильных двигателей – оксиды азота (NOx).
Более того, именно соединения ЛОС и NОx создают в атмосфере частицы, наиболее вредные для нашего здоровья.
Исследование Университета Колорадо опубликовано в журнале Science Magazine.
Таблицы DPVA.ru – Инженерный Справочник | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Химический справочник / / Химия для самых маленьких. Шпаргалки. Детский сад, Школа. / / Начала химии. Основные понятия. Классификация веществ. Закон постоянства вещества. Атомно-молекулярное учение. Поделиться:
| |||||||||||||||||||||
| Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. Вложите в письмо ссылку на страницу с ошибкой, пожалуйста. | ||||||||||||||||||||||
| Коды баннеров проекта DPVA.ru Начинка: KJR Publisiers Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | |||||||||||||||||||||
1.5: Краткая история химии
Цели обучения
- Чтобы понять развитие атомной модели.

Только в эпоху древних греков у нас не было никаких записей о том, как люди пытались объяснить химические изменения, которые они наблюдали и использовали. В то время считалось, что природные объекты состоят всего из четырех основных элементов: земли, воздуха, огня и воды. Затем, в четвертом веке до нашей эры, два греческих философа, Демокрит и Левкипп, предположили, что материя не бесконечно делится на более мелкие частицы, а вместо этого состоит из фундаментальных неделимых частиц, называемых атомов .К сожалению, у этих ранних философов не было технологии для проверки своей гипотезы. В любом случае они вряд ли сделали бы это, потому что древние греки не проводили экспериментов и не использовали научный метод. Они считали, что природа Вселенной может быть открыта только рациональным мышлением.
В течение следующих двух тысячелетий алхимиков , которые занимались химией и спекулятивной философией в средние века и эпоху Возрождения, добились многих успехов в химии. Их главной целью было преобразование одних элементов в другие с помощью процесса, который они назвали трансмутацией (рис. \(\PageIndex{1}\)). В частности, алхимики хотели найти способ превратить более дешевые металлы в золото. Хотя большинство алхимиков не подходили к химии систематически, и многие из них, по-видимому, были откровенными мошенниками, алхимики в Китае, арабских королевствах и средневековой Европе внесли большой вклад, включая открытие таких элементов, как ртуть (ртуть) и получение нескольких сильных кислот. .
Их главной целью было преобразование одних элементов в другие с помощью процесса, который они назвали трансмутацией (рис. \(\PageIndex{1}\)). В частности, алхимики хотели найти способ превратить более дешевые металлы в золото. Хотя большинство алхимиков не подходили к химии систематически, и многие из них, по-видимому, были откровенными мошенниками, алхимики в Китае, арабских королевствах и средневековой Европе внесли большой вклад, включая открытие таких элементов, как ртуть (ртуть) и получение нескольких сильных кислот. .
Рисунок \(\PageIndex{1}\) Алхимик за работой
Алхимия была формой химии, которая процветала в средние века и в эпоху Возрождения. Хотя некоторые алхимики были мошенниками, другие внесли большой вклад, включая открытие нескольких элементов и получение сильных кислот.
Современная химия
В 16 и 17 веках зародилось то, что мы теперь называем современной химией. В этот период были достигнуты большие успехи в металлургии , извлечении металлов из руд и проведены первые систематические количественные опыты. В 1661 году англичанин Роберт Бойль (1627–1691) опубликовал книгу «Химик-скептик» , в которой описывалась взаимосвязь между давлением и объемом воздуха. Что еще более важно, Бойль определил элемент как вещество, которое не может быть разделено на два или более простых вещества химическими средствами. Это привело к идентификации большого количества элементов, многие из которых были металлами. По иронии судьбы, сам Бойль никогда не считал металлы элементами.
В 1661 году англичанин Роберт Бойль (1627–1691) опубликовал книгу «Химик-скептик» , в которой описывалась взаимосвязь между давлением и объемом воздуха. Что еще более важно, Бойль определил элемент как вещество, которое не может быть разделено на два или более простых вещества химическими средствами. Это привело к идентификации большого количества элементов, многие из которых были металлами. По иронии судьбы, сам Бойль никогда не считал металлы элементами.
В 18 веке английский священник Джозеф Пристли (1733–1804) открыл газообразный кислород и обнаружил, что многие углеродосодержащие материалы энергично горят в кислородной атмосфере. Этот процесс получил название горение .Пристли также обнаружил, что газ, образующийся при брожении пива, который, как мы теперь знаем, представляет собой углекислый газ, является одним из газообразных продуктов сгорания. Однако исследования этого газа Пристли не продолжились, как ему хотелось бы. После того, как он упал в чан с бродящим пивом, пивовары запретили ему работать на своих заводах. Хотя Пристли не понял, что это такое, он обнаружил, что углекислый газ растворяется в воде, образуя сельтерскую воду. По сути, его можно считать основателем многомиллиардной индустрии газированных безалкогольных напитков.
Хотя Пристли не понял, что это такое, он обнаружил, что углекислый газ растворяется в воде, образуя сельтерскую воду. По сути, его можно считать основателем многомиллиардной индустрии газированных безалкогольных напитков.
Джозеф Пристли (1733–1804)
Пристли был политическим теоретиком и ведущим унитарным министром. Он был назначен в Уоррингтонскую академию в Ланкашире, Англия, где разработал новые курсы по истории, науке и искусству. Во время визитов в Лондон Пристли встречался с ведущими учеными, в том числе с Бенджамином Франклином, который поощрял интерес Пристли к электричеству. Работа Пристли над газами началась, когда он жил рядом с пивоварней в Лидсе, где он заметил «неподвижный воздух», выходящий из чанов с бродящим пивом и элем.Его научные открытия включали взаимосвязь между электричеством и химическими изменениями, 10 новых «воздухов» и наблюдения, которые привели к открытию фотосинтеза. Из-за его поддержки принципов Французской революции дом, библиотека и лаборатория Пристли были разрушены толпой в 1791 году. Он и его жена эмигрировали в Соединенные Штаты в 1794 году, чтобы присоединиться к своим трем сыновьям, которые ранее эмигрировали в Пенсильванию. . Пристли так и не вернулся в Англию и умер в своем новом доме в Пенсильвании.
Он и его жена эмигрировали в Соединенные Штаты в 1794 году, чтобы присоединиться к своим трем сыновьям, которые ранее эмигрировали в Пенсильванию. . Пристли так и не вернулся в Англию и умер в своем новом доме в Пенсильвании.
Несмотря на новаторские исследования Пристли и других, ясное понимание горения оставалось неуловимым. Однако в конце 18 века французский ученый Антуан Лавуазье (1743–1794) показал, что горение — это реакция углеродсодержащего вещества с кислородом с образованием углекислого газа и воды и что жизнь зависит от подобной реакции, которую мы сегодня наблюдаем. звоните дыхание . Лавуазье также написал первый современный текст по химии и широко известен как отец современной химии.Его самым важным вкладом был закон сохранения массы , который гласит, что в любой химической реакции масса реагирующих веществ равна массе образующихся продуктов. То есть в химической реакции масса не теряется и не разрушается. К сожалению, Лавуазье инвестировал в частную корпорацию, которая собирала налоги для короны, а королевские сборщики налогов не пользовались популярностью во время Французской революции. Он был казнен на гильотине в возрасте 51 года, преждевременно прекратив свой вклад в химию.
Он был казнен на гильотине в возрасте 51 года, преждевременно прекратив свой вклад в химию.
Атомная теория материи
В 1803 году английский школьный учитель Джон Дальтон (1766–1844) расширил разработку Прустом закона определенных пропорций ( Раздел 1.2 «Научный метод» ) и выводы Лавуазье о сохранении массы в химических реакциях, чтобы предположить, что элементы состоят из неделимых частиц, которые он назвал атомами (взяв термин от Демокрита и Левкиппа). Атомная теория материи Дальтона содержит четыре фундаментальные гипотезы:
- Вся материя состоит из крошечных неделимых частиц, называемых атомами.
- Все атомы элемента одинаковы по массе и химическим свойствам, тогда как атомы разных элементов различаются по массе и основным химическим свойствам.
- Химическое соединение – это вещество, которое всегда содержит одни и те же атомы в одном и том же соотношении.
- В химических реакциях атомы одного или нескольких соединений или элементов перераспределяются или перестраиваются по отношению к другим атомам с образованием одного или нескольких новых соединений.
 Сами по себе атомы не изменяются в химических реакциях.
Сами по себе атомы не изменяются в химических реакциях.
Эта последняя гипотеза предполагает, что цель алхимиков по превращению других элементов в золото невозможна, по крайней мере, посредством химических реакций. Теперь мы знаем, что атомная теория Дальтона по существу верна, с четырьмя небольшими изменениями:
- Не все атомы элемента должны иметь одинаковую массу.
- Атомы одного элемента могут быть превращены в другой посредством ядерных реакций.
- Составы многих твердых соединений несколько различаются.
- При определенных обстоятельствах некоторые атомы могут делиться (расщепляться на более мелкие частицы).
Эти модификации иллюстрируют эффективность научного метода; более поздние эксперименты и наблюдения были использованы для уточнения первоначальной теории Дальтона.
Закон множественных пропорций
Несмотря на ясность своего мышления, Дальтон не мог использовать свою теорию для определения элементного состава химических соединений, потому что у него не было надежной шкалы атомных масс; то есть он не знал относительных масс таких элементов, как углерод и кислород. Например, он знал, что газ, который мы теперь называем окисью углерода, содержит углерод и кислород в соотношении 1:1,33 по массе, а второе соединение, газ, который мы называем двуокисью углерода, содержит углерод и кислород в соотношении 1:2,66 по массе. . Поскольку 2,66/1,33 = 2,00, второе соединение содержало в два раза больше атомов кислорода на один атом углерода, чем первое. Но какова была правильная формула для каждого соединения? Если первое соединение состояло из частиц, содержащих один атом углерода и один атом кислорода, то второе должно состоять из частиц, содержащих один атом углерода и два атома кислорода.Если первое соединение имело два атома углерода и один атом кислорода, то второе должно иметь два атома углерода и два атома кислорода. Если бы у первого был один атом углерода и два атома кислорода, у второго был бы один атом углерода и четыре атома кислорода и так далее. Дальтон не мог отличить эти или более сложные альтернативы. Однако эти данные привели к общему утверждению, которое теперь известно как закон кратных пропорций : когда два элемента образуют ряд соединений, отношения масс второго элемента, присутствующих на грамм первого элемента, могут почти всегда выражается как отношение целых чисел.
Например, он знал, что газ, который мы теперь называем окисью углерода, содержит углерод и кислород в соотношении 1:1,33 по массе, а второе соединение, газ, который мы называем двуокисью углерода, содержит углерод и кислород в соотношении 1:2,66 по массе. . Поскольку 2,66/1,33 = 2,00, второе соединение содержало в два раза больше атомов кислорода на один атом углерода, чем первое. Но какова была правильная формула для каждого соединения? Если первое соединение состояло из частиц, содержащих один атом углерода и один атом кислорода, то второе должно состоять из частиц, содержащих один атом углерода и два атома кислорода.Если первое соединение имело два атома углерода и один атом кислорода, то второе должно иметь два атома углерода и два атома кислорода. Если бы у первого был один атом углерода и два атома кислорода, у второго был бы один атом углерода и четыре атома кислорода и так далее. Дальтон не мог отличить эти или более сложные альтернативы. Однако эти данные привели к общему утверждению, которое теперь известно как закон кратных пропорций : когда два элемента образуют ряд соединений, отношения масс второго элемента, присутствующих на грамм первого элемента, могут почти всегда выражается как отношение целых чисел. (Тот же закон справедлив для массовых отношений соединений, образующих ряд, содержащий более двух элементов.) Пример 4 показывает, как можно применить закон кратных пропорций для определения идентичности соединения.
(Тот же закон справедлив для массовых отношений соединений, образующих ряд, содержащий более двух элементов.) Пример 4 показывает, как можно применить закон кратных пропорций для определения идентичности соединения.
Пример \(\PageIndex{1}\)
Химик изучает ряд простых соединений углерода и водорода. В следующей таблице перечислены массы водорода, которые соединяются с 1 г углерода с образованием каждого соединения.
| Соединение | Масса водорода (г) |
|---|---|
| А | 0.0839 |
| Б | 0,1678 |
| С | 0,2520 |
| Д |
- Определите, подчиняются ли эти данные закону кратных пропорций.

- Рассчитайте массу водорода, который соединится с 1 г углерода с образованием D , четвертого соединения в ряду.
Дано: масса водорода на грамм углерода для трех соединений
Запрашиваемый:
- отношения масс водорода к углероду
- масса водорода на грамм углерода для четвертого соединения в ряду
Стратегия:
A Выберите наименьшую массу для использования в качестве знаменателя, а затем рассчитайте отношение каждой из других масс к этой массе. При необходимости укажите другие коэффициенты.
B Если отношения представляют собой небольшие целые числа, данные подчиняются закону кратных пропорций.
C Решите, образуют ли коэффициенты числовой ряд. Если да, то определите следующего члена этого ряда и предскажите соотношение, соответствующее следующему соединению в ряду.
D Используйте пропорции для расчета массы водорода на грамм углерода в этом соединении.
Раствор
A Соединение A имеет наименьшую массу водорода, поэтому мы используем его в качестве знаменателя.Соотношения оставшихся масс водорода B и C , которые соединяются с 1 г углерода, следующие:
CA=0,2520g0,0839g=3,00=31BA=0,1678g0,0839g=2,00=21CB=0,2520g0,1678g=1,502≈32
B Отношения масс водорода, которые соединяются с 1 г углерода, действительно состоят из небольших целых чисел (3/1, 2/1, 3/2), как и предсказывает закон кратных пропорций.
C Соотношения B / A и C / A образуют ряды 2/1, 3/1, поэтому следующий член ряда должен быть 6 15 D / /1.
D Таким образом, если соединение D существует, оно будет образовано путем соединения 4 × 0,0839 г = 0,336 г водорода с 1 г углерода. Такое соединение существует; это метан , основная составляющая природного газа.
Такое соединение существует; это метан , основная составляющая природного газа.
Упражнение \(\PageIndex{1}\)
Известны четыре соединения, содержащие только серу и фтор. В следующей таблице перечислены массы фтора, которые соединяются с 1 г серы с образованием каждого соединения.
| Соединение | Масса фтора (г) |
|---|---|
| А | 3.54 |
| Б | 2,96 |
| С | 2,36 |
| Д | 0,59 |
- Определите соотношения масс фтора, которые соединяются с 1 г серы в этих соединениях. Соответствуют ли эти данные закону кратных пропорций?
- Рассчитайте массу фтора, который соединится с 1 г серы с образованием следующих двух соединений в ряду: E и F .
- Ответить
- A / D = 6,0 или 6/1; B / D ≈ 5,0 или 5/1; C / D = 4,0 или 4/1; да
- Соотношения 3,0 и 2,0 дают 1,8 г и 1,2 г фтора/грамм серы соответственно. (Ни одно из этих соединений еще не известно.)
Гипотеза Авогадро
В очередной попытке установить формулы химических соединений французский химик Жозеф Гей-Люссак (1778–1850) провел серию экспериментов с использованием объемных измерений.В условиях постоянной температуры и давления он тщательно измерил объемы газов, которые вступали в реакцию с образованием данного химического соединения, а также объемы продуктов, если они были газами. Гей-Люссак обнаружил, например, что один объем газообразного хлора всегда реагирует с одним объемом газообразного водорода с образованием двух объемов газообразного хлороводорода. Точно так же один объем газообразного кислорода всегда реагировал с двумя объемами газообразного водорода с образованием двух объемов водяного пара (часть (а) на рисунке \(\PageIndex{2}\)).
Рисунок \(\PageIndex{2}\) Эксперименты Гей-Люссака с газообразным хлором и газообразным водородом
(a) Один объем газообразного хлора прореагировал с одним объемом газообразного водорода с образованием двух объемов газообразного хлористого водорода, а один объем газообразного кислорода прореагировал с двумя объемами газообразного водорода с образованием двух объемов водяного пара. (b) Краткое изложение гипотезы Авогадро, которая интерпретировала результаты Гей-Люссака с точки зрения атомов. Обратите внимание, что самый простой способ получить две молекулы хлористого водорода – это если водород и хлор состоят из молекул, содержащих по два атома элемента.
Результаты Гей-Люссака сами по себе не выявили формул для хлористого водорода и воды. Итальянский химик Амадео Авогадро (1776–1856) разработал ключевую идею, которая привела к точным формулам. Он предположил, что при измерении газов при одинаковой температуре и давлении равные объемы различных газов содержат одинаковое количество частиц газа . Гипотеза Авогадро , объясняющая результаты Гей-Люссака, резюмируется здесь и в части (b) на Рисунке \(\PageIndex{2}\):
Гипотеза Авогадро , объясняющая результаты Гей-Люссака, резюмируется здесь и в части (b) на Рисунке \(\PageIndex{2}\):
\( один объем (или частица) водорода + один объем (или частица) хлора → два объема (или частицы) хлористого водорода \)
Если теория атомов Дальтона была верна, то каждая частица водорода или хлора должна была содержать по крайней мере два атома водорода или хлора, потому что были произведены две частицы хлористого водорода.Самое простое, но не единственное объяснение заключалось в том, что водород и хлор содержат по два атома каждый (т. е. они были двухатомными ), а хлороводород содержал по одному атому водорода и хлора. Применение этого рассуждения к результатам Гей-Люссака с водородом и кислородом приводит к выводу, что вода содержит два атома водорода на один атом кислорода. К сожалению, из-за отсутствия данных, подтверждающих гипотезу Авогадро о том, что равные объемы газов содержат одинаковое количество частиц, его объяснения и формулы для простых соединений не были общепринятыми более 50 лет. Дальтон и многие другие продолжали верить, что частицы воды содержат один атом водорода и один атом кислорода, а не два атома водорода и один атом кислорода. Историческое развитие концепции атома обобщено на Рисунке \(\PageIndex{3}\).
Дальтон и многие другие продолжали верить, что частицы воды содержат один атом водорода и один атом кислорода, а не два атома водорода и один атом кислорода. Историческое развитие концепции атома обобщено на Рисунке \(\PageIndex{3}\).
Рисунок \(\PageIndex{3}\) Краткий обзор исторического развития концепции атома
Резюме
Древние греки впервые предположили, что материя состоит из элементарных частиц, называемых атомами .Химия приняла свою нынешнюю научную форму в 18 веке, когда тщательные количественные эксперименты Лавуазье, Пруста и Дальтона привели к закону определенных пропорций, закону сохранения массы и закону кратных пропорций , которые заложили основа атомной теории материи Дальтона. В частности, гипотеза Авогадро обеспечила первую связь между макроскопическими свойствами вещества (в данном случае объемом газа) и числом присутствующих атомов или молекул.
ВЫНОС КЛЮЧЕЙ
- Разработка атомной модели опиралась на применение научного метода на протяжении нескольких столетий.
КОНЦЕПТУАЛЬНЫЕ ПРОБЛЕМЫ
Дайте определение воспламенению и обсудите вклад Пристли и Лавуазье в понимание реакции горения.
Инженеры-химики часто используют в своих расчетах понятие «массового баланса», согласно которому масса реагентов должна равняться массе продуктов.Какой закон поддерживает эту практику?
Применяется ли закон кратных пропорций как к отношениям масс, так и к отношениям атомов? Почему или почему нет?
Каковы четыре гипотезы атомной теории материи?
Большая часть энергии во Франции обеспечивается ядерными реакциями. Согласуются ли такие реакции с гипотезами Дальтона? Почему или почему нет?
Содержит ли 1 л воздуха такое же количество частиц, как 1 л газообразного азота? Поясните свой ответ.

ЧИСЛЕННЫЕ ЗАДАЧИ
Пожалуйста, убедитесь, что вы знакомы с темами, обсуждаемыми в разделе «Основные навыки 1» ( Раздел 1.9 «Основные навыки 1» ), прежде чем переходить к числовым задачам.
Один из минералов, обнаруженных в почве, имеет атомное соотношение Al:Si:O 0,2:0,2:0,5. Соответствует ли это закону кратных пропорций? Почему или почему нет? Соответствует ли соотношение элементов атомной теории материи Дальтона?
Азот и кислород реагируют, образуя три разных соединения, содержащих 0.571 г, 1,143 г и 2,285 г кислорода/грамм азота соответственно. Соответствует ли это закону кратных пропорций? Поясните свой ответ.
Известны три бинарных соединения ванадия и кислорода. В следующей таблице приведены массы кислорода, которые соединяются с 10,00 г ванадия с образованием каждого соединения.
Соединение Масса кислорода (г) А 4.  71
71Б 6,27 С - Определите отношение масс кислорода, который соединяется с 3,14 г ванадия в соединениях А и В .
- Предскажите массу кислорода, который соединится с 3,14 г ванадия с образованием третьего соединения в ряду.
Известны три соединения, содержащие титан, магний и кислород.В следующей таблице приведены массы титана и магния, которые реагируют с 5,00 г кислорода с образованием каждого соединения.
Соединение Масса титана (г) Масса магния (г) А 4,99 2,53 Б 3,74 3.  80
80С - Определите соотношения масс титана и магния, которые соединяются с 5,00 г кислорода в этих соединениях.
- Предскажите массы титана и магния, которые соединились бы с 5,00 г кислорода с образованием другого возможного соединения в ряду: C .
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie.
 Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie. - Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Современная химия и медицина – Атлантика
В наши дни наука больше не нуждается в оправдании как предмет, достойный искренней преданности человека. Все стороны признают, что получение точного знания о силах и веществах во вселенной принесет человечеству неисчислимые блага. Полное значение этого нового света в его отношении к улучшению человеческой судьбы только начинает осознаваться.
Все стороны признают, что получение точного знания о силах и веществах во вселенной принесет человечеству неисчислимые блага. Полное значение этого нового света в его отношении к улучшению человеческой судьбы только начинает осознаваться.
В соответствии с растущим признанием ценности научных исследований для человечества сегодня среди ученых существует стремление связать каждую конкретную науку со всеми другими и связать все вместе в единое целое, не упуская из виду необходимость точности в каждой части.Существование таких сложных разделов науки, как физическая химия, биохимия, физиологическая ботаника и т. д., является одним из признаков более широкого мировоззрения; и некоторые из величайших современных научных достижений происходят на границе между различными науками. Природа, в конце концов, представляет собой единое целое, и наша классификация ее тесно связанных явлений по особым темам отчасти произвольна.
Эта попытка связать различные науки друг с другом полезна не только для науки в целом, но и для отдельного работника. Мировоззрение человека должно быть расширено попыткой проследить отношение его особой задачи к многообразию деятельности и потребностей человечества.
Мировоззрение человека должно быть расширено попыткой проследить отношение его особой задачи к многообразию деятельности и потребностей человечества.
Особая отрасль науки, называемая химией, во многом связана с человеческой жизнью, а также с другими науками. Она составляет существенную часть любой натурфилософии; она служит замечательным средством интеллектуальной дисциплины; он направляет производителя и продавца к эффективности производства и чистоте продукта; но, возможно, самое главное, она содержит ключ, который один может открыть ворота к действительно фундаментальным знаниям о скрытых причинах здоровья и болезней.Это один из самых ценных и жизненно важных способов, которыми любая отрасль науки может служить человечеству в ближайшие годы.
Десять веков назад, во времена алхимиков, химию называли «служанкой медицины»; сегодня эта связь не слабее, а гораздо сильнее. Цель настоящей статьи — очень кратко привлечь внимание к некоторым путям, которыми современная химия может помочь теории и практике медицины.
То, что существует тесная связь между химией и медициной, ясно каждому.Наши тела целиком состоят из химических веществ, и все многообразные функции живого организма зависят, по крайней мере частично, от химических реакций. Химические процессы позволяют нам переваривать пищу, согревать нас, снабжать нас мышечной энергией. Весьма вероятно, что даже впечатления наших чувств и мысли нашего мозга, а также способ передачи их по нервам более или менее тесно связаны с химическими реакциями. Короче говоря, человеческое тело — удивительно сложная химическая машина; а его здоровье и болезнь, его жизнь и смерть существенно связаны с согласованием множества сложных химических превращений.
Эта сложность живого тела требует ясного зрения и глубоких знаний для ее полного понимания; и химия прежних дней была слишком простой и поверхностной, чтобы быть очень полезным проводником в загадочном лабиринте многих сходящихся и пересекающихся путей. Теперь обстоятельства полностью изменились. Химия быстро приближается к физике по точности и выходит за пределы физики по масштабу. По мере роста понимания химии разрыв между более простыми явлениями в химической лаборатории и более сложными изменениями, лежащими в основе органической жизни, становился все меньше и меньше.Разумный врач понимает это и приветствует помощь, которую ему может оказать быстро развивающаяся наука химия. Один выдающийся патологоанатом недавно сказал, что при изучении клетки и ее роста, как нормального, так и ненормального, ученый-медик пришел к тому, что он должен прибегнуть к химическим знаниям, потому что он понимает, что действие клетки зависит от природы и количества различных химических веществ, из которых он сделан. Так как клетка является основой всей жизни и поскольку наши тела состоят просто из скоплений самых разнообразных клеток, каждая из которых подчиняется химическим законам, то ясно, что химия должна лежать в основе всех жизненных функций.
По мере роста понимания химии разрыв между более простыми явлениями в химической лаборатории и более сложными изменениями, лежащими в основе органической жизни, становился все меньше и меньше.Разумный врач понимает это и приветствует помощь, которую ему может оказать быстро развивающаяся наука химия. Один выдающийся патологоанатом недавно сказал, что при изучении клетки и ее роста, как нормального, так и ненормального, ученый-медик пришел к тому, что он должен прибегнуть к химическим знаниям, потому что он понимает, что действие клетки зависит от природы и количества различных химических веществ, из которых он сделан. Так как клетка является основой всей жизни и поскольку наши тела состоят просто из скоплений самых разнообразных клеток, каждая из которых подчиняется химическим законам, то ясно, что химия должна лежать в основе всех жизненных функций.
Химия может быть полезна в медицине как минимум тремя совершенно разными способами. Один из них связан с обнаружением компонентов вещей. Этот вид химии называется аналитической химией. Другой способ, которым химия может помочь медицине, зависит от способности современного химика не только выяснять, из чего сделаны вещи, но и открывать, как соединяются части. Этот раздел химии называется структурной химией, потому что он имеет дело не только с материалами, но и с тем, как эти материалы расположены.Еще один метод оказания помощи исходит из еще более позднего развития химии, обычно называемой физической химией, которая имеет дело с явлениями, лежащими на границе между физикой и химией, особенно с той частью границы, которая касается отношения энергии к материалу. Физический химик должен знать не только то, из чего сделаны вещи и как эти элементы соединяются, но также и то, какая энергия требуется для их соединения, и какая энергия высвобождается при их разложении.
Этот вид химии называется аналитической химией. Другой способ, которым химия может помочь медицине, зависит от способности современного химика не только выяснять, из чего сделаны вещи, но и открывать, как соединяются части. Этот раздел химии называется структурной химией, потому что он имеет дело не только с материалами, но и с тем, как эти материалы расположены.Еще один метод оказания помощи исходит из еще более позднего развития химии, обычно называемой физической химией, которая имеет дело с явлениями, лежащими на границе между физикой и химией, особенно с той частью границы, которая касается отношения энергии к материалу. Физический химик должен знать не только то, из чего сделаны вещи и как эти элементы соединяются, но также и то, какая энергия требуется для их соединения, и какая энергия высвобождается при их разложении.
Каждый из этих трех видов химии может значительно помочь науке и медицинскому искусству — и не нужно никакого философа, чтобы объявить, насколько эффективнее может быть их помощь, чем старый метод наблюдения только за внешним видом жидкости и ткани.
Теперь давайте кратко и подробно рассмотрим различные аспекты этих трех способов оказания помощи, рассматривая их в том порядке, в котором они только что были упомянуты. Сначала идет область химика-аналитика. Как уже было сказано, человеческий организм — это химическая машина.Он полностью состоит из химических веществ и приводится в действие исключительно химической энергией. Химик-аналитик может сообщить нам состав каждого из многочисленных веществ, составляющих эту сложную машину. Он способен не только обнаружить различные присутствующие элементы, но и с большой точностью оценить их точное количество. Он может анализировать пищу, а также различные части и выделения тела, и может определить связь между составом съеденной пищи и полученной телесной субстанцией.Все это, очевидно, имеет большую ценность, так как сразу показывает нам в общих чертах, какие элементы должны входить в пищу; и, кроме того, в случаях болезни он дает нам превосходные ключи к пониманию того, каким образом различные функции тела отклоняются от нормальных, и, таким образом, оказывает важную помощь в диагностике и предложении подходящего лечения. Но это старая и очевидная история, поэтому я не буду больше останавливаться на аналитической стороне применения химии в медицине, какой бы важной она ни была.
Но это старая и очевидная история, поэтому я не буду больше останавливаться на аналитической стороне применения химии в медицине, какой бы важной она ни была.
Обратимся теперь ко второму аспекту предмета, а именно к отношению структурной химии к медицине. Столь недавнее развитие предмета, что сама идея структурной химии еще не является частью оборудования среднего либерально образованного человека.
Структурная химия берет свое начало в открытии того, что два вещества могут состоять из одинаковых процентных количеств одних и тех же элементов, но при этом совершенно отличаться друг от друга. Тот факт, что две вещи могут быть абсолютно одинаковыми в своих составляющих, но очень разными по своим свойствам, подразумевает, что должно быть различие в расположении того или иного рода.Наиболее ясное представление об этой идее мы можем получить с помощью атомарной гипотезы. Если мельчайшие частицы любого данного сложного вещества состоят из еще меньших атомов различных рассматриваемых элементов, то ясно, что мы можем представить себе различное расположение этих атомов, и разумно предположить, что конкретное расположение могло бы существенно различаться. в природе образующихся соединений. Везде в жизни обустройство имеет большое значение. Что касается чисел, то комбинация 191 сильно отличается от комбинации 911, хотя каждая из них содержит те же отдельные знаки.Почему расположение не может иметь значения в случае атомов?
в природе образующихся соединений. Везде в жизни обустройство имеет большое значение. Что касается чисел, то комбинация 191 сильно отличается от комбинации 911, хотя каждая из них содержит те же отдельные знаки.Почему расположение не может иметь значения в случае атомов?
В этом кратком обзоре невозможно точно объяснить, как химики получают представление о расположении атомов, составляющих частицы (или молекулы) каждого вещества. Мы полагаемся на два метода работы: первый — расщепление соединения и определение того, на какие группы оно распадается; во-вторых, попытка построить из этих или подобных групп исходное соединение. Подобно тому, как среди обломков рухнувшего здания вы найдете фрагменты, достаточные для того, чтобы понять, было ли это жилище, конюшня или машинная мастерская, так и среди фрагментов разрушенного вещества вы найдете еще сохранившиеся фрагменты его конструкции. вместе, достаточно, чтобы указать что-то из исходной группировки.Каждая отдельная химическая структура оставит различный химический мусор. Если из подобных фрагментов исходное вещество может быть сконструировано подходящими средствами, то есть убедительные доказательства того, что были получены некоторые знания о структуре.
Если из подобных фрагментов исходное вещество может быть сконструировано подходящими средствами, то есть убедительные доказательства того, что были получены некоторые знания о структуре.
Что касается полезности структурной химии для медицины, то мы не можем не видеть сразу ее огромной важности. Если соединение друг с другом бесконечно малых атомов различными способами изменяет свойства образующихся веществ по-разному, то очевидно, что особый способ соединения каждого из сложных соединений, составляющих наши тела, имеет для нас жизненно важное значение.Более того, в случае с нашей пищей только расположение атомов может иметь решающее значение между пищей и ядом.
Легко понять, почему эти разные структуры должны оказывать разное действие на организм. Жизнь, в случае животных, представляет собой непрерывный процесс разложения более сложных структур на более простые; и ясно, что это разделение будет происходить по-разному в разных группах и, таким образом, приведет к разным результатам.
Знание атомного строения различных веществ, составляющих тело, не только должно дать бесценный путеводитель в изучении физиологии, патологии и гигиены, но уже привело к логическому открытию совершенно новых лекарств, построенных искусственно в лаборатории, чтобы соответствовать особым потребностям конкретных заболеваний и рациональному использованию продуктов питания.В ближайшие годы эти достижения обязательно умножатся.
Таким образом, в будущем врач может работать не с сывороткой или вирусом сомнительного состава и ценности, а с чистыми веществами, полученными в химической лаборатории, — веществами с их группами атомов, организованными тонкой наукой так, как для восстановления изношенных органов или уничтожения злокачественных микробов без какого-либо вреда. Таким образом, мы можем мечтать о достижении искусственного иммунитета от оспы, например, настолько же превосходящего вакцинацию, насколько он превосходит старую прививку.
Полезные вещества такого рода редко обнаруживаются случайно; число возможных аранжировок слишком велико. Чтобы узнать все, что нужно знать о материи, необходимо найти структуру каждой сложной субстанции, существующей в теле, и расположение атомов в каждой частице нашего сложного организма. До тех пор, пока это не будет сделано, мы не сможем с достаточной уверенностью предсказать, что будет происходить с этими веществами в ходе их повседневного функционирования или как на них, вероятно, повлияет болезнь.Это проблема настолько жизненно важная, что трудно преувеличить ее значение для потомков.
Чтобы узнать все, что нужно знать о материи, необходимо найти структуру каждой сложной субстанции, существующей в теле, и расположение атомов в каждой частице нашего сложного организма. До тех пор, пока это не будет сделано, мы не сможем с достаточной уверенностью предсказать, что будет происходить с этими веществами в ходе их повседневного функционирования или как на них, вероятно, повлияет болезнь.Это проблема настолько жизненно важная, что трудно преувеличить ее значение для потомков.
Как я сказал, современные знания теперь требуют от химика, чтобы он знал не только элементы, из которых состоят все вещи, и то, как эти элементы соединяются вместе, но также и то, какой выход энергии связан с каждым изменением, к которому они относятся. может подвергаться.
Нет никаких сомнений в том, что энергия является непосредственной причиной каждого действия в известной вселенной. Без какой-либо энергии вся вселенная была бы неподвижной, темной, пронзительно холодной, спящей.Мир, наполненный физическими энергиями, но лишенный химической энергии, мог бы вращаться и иметь свет и тепло; но в нем не может быть органической жизни, ибо жизнь основана на действии химической энергии. Таким образом, изучение химической энергии представляет собой еще одну очень важную человеческую проблему.
Таким образом, изучение химической энергии представляет собой еще одну очень важную человеческую проблему.
Физическая химия имеет дело с отношением каждого из различных видов энергии к химическому изменению. Он имеет дело с действующими, движущими силами, которые делают жизнь возможной, и в каждом из своих многочисленных аспектов он привносит новый разум в работу живого механизма.
Физическая химия рассматривает, среди прочего, химические связи превращений твердого тела в жидкое и жидкое в газообразное, а также обсуждает природу растворов и смесей всех видов. Поскольку живое тело состоит из твердых тел и жидкостей и зависит от атмосферных газов, способствующих химическим изменениям, оживляющим его, и поскольку растворы и смеси присутствуют в каждой клетке, законы и теории физической химии переплетаются с каждым явлением. факт физиологии.
Опять же, физическая химия имеет дело с отношением тепла к химическому изменению. Выход энергии в виде теплоты при каждой химической реакции достоин изучения, но особенно человеку следует исследовать те ступени, по которым вырабатывается всякая животная теплота, — и это происходит исключительно благодаря химической реакции. Кроме того, физическая химия изучает влияние изменения температуры на скорость и тенденцию химического действия, что имеет большое значение при изучении лихорадок и других ненормальных состояний, а также при отслеживании чудесного скрытого механизма, посредством которого тело поддерживают почти постоянную температуру.
Кроме того, физическая химия изучает влияние изменения температуры на скорость и тенденцию химического действия, что имеет большое значение при изучении лихорадок и других ненормальных состояний, а также при отслеживании чудесного скрытого механизма, посредством которого тело поддерживают почти постоянную температуру.
Однако эта динамическая химия будущего не останавливается на достигнутом. В ее области лежат также недавно открытые отношения химии и электричества, имеющие отношение, быть может, к некоторым тайнам нервной деятельности и дающие много сведений о природе растворов вообще. Важнее, пожалуй, всего этого раздел предмета, называемый фотохимией, химией света, который обещает оказать большую помощь в толковании изменений, происходящих в листьях растений под влиянием солнечного света.Только благодаря свету природа способна создавать сложные соединения, необходимые для обеспечения всех животных пищей; и пока мы не поймем рост растения, мы не можем надеяться понять рост животного.
Немедленное размышление покажет, что эта химия веществ в действии — то есть химия энергии — несет с собой обещание полезности для будущих поколений, которая, возможно, превосходит любую другую науку. Ибо изучение инертной субстанции, от которой отошла жизнь, сколь бы точным ни было это исследование, не может дать нам истинного знания о ее истинном предназначении, так же как мы не можем предсказать по внешнему виду чучела птицы в музее его назначение. полная привычка к жизни.Чтобы понять процесс жизни, нужно видеть вещества в действии и изучать их поведение под влиянием разнообразных сил, действующих вокруг них; и это является целью физической химии.
Я очень кратко обрисовал несколько путей, которыми наука обещает помочь страдающему человечеству в будущем. Некоторым эта точка зрения могла показаться материалистической; однако мы должны помнить, что наука не пытается проникнуть в высшую тайну, а имеет дело только с фактами природы.Величайшие загадки жизни кажутся почти такими же далекими от решения, как и прежде. Какие отношения существуют, например, между химическими изменениями и мышлением, какие постоянные изменения химической структуры вызывают память, мы не знаем. Жизнь мы никогда не могли произвести только из мертвого материала. Личность и наследственность бросают вызов химику, как и физиологу и психологу. Но не будем нетерпеливы. Хотя и невозможно предсказать, насколько далеко мы с помощью нашего ограниченного ума сможем проникнуть в тайны безмерно обширной и прекрасной вселенной, тем не менее мы можем утешать себя мыслью, что каждый сделанный шаг приносит новое благо человечеству и новую жизнь. вдохновение для больших усилий.
Какие отношения существуют, например, между химическими изменениями и мышлением, какие постоянные изменения химической структуры вызывают память, мы не знаем. Жизнь мы никогда не могли произвести только из мертвого материала. Личность и наследственность бросают вызов химику, как и физиологу и психологу. Но не будем нетерпеливы. Хотя и невозможно предсказать, насколько далеко мы с помощью нашего ограниченного ума сможем проникнуть в тайны безмерно обширной и прекрасной вселенной, тем не менее мы можем утешать себя мыслью, что каждый сделанный шаг приносит новое благо человечеству и новую жизнь. вдохновение для больших усилий.
Краткое сообщение: Пространственные и временные вариации химического состава поверхностного снега на маршруте от побережья Восточной Антарктиды до вершины ледяного щита (Купол А)
Бертлер Н., Маевски П. А., Аристараин А., Барретт П., Бекальи С.,
Бернардо Р., Бо С., Сяо С., Карран М. и Цинь Д.: Химия снега
через Антарктиду, Энн. Glaciol., 41, 167–179, 2005.
Bondietti, E.A. and Papastefanou, C.: Оценки времени пребывания сульфатные аэрозоли в атмосферном воздухе // Хим.Total Environ., 136, 25–31, https://doi.org/10.1016/0048-9697(93)-G, 1993.
Дин, М., Сяо, К., Ли, Ю., Рен, Дж., Хоу, С., Джин, Б. и Сунь, Б.: Пространственное изменчивость поверхностного баланса массы на маршруте перехода из Чжуншаня Станция до Купола А, Антарктида, J. Glaciol., 57, 658–666, 2011.
Диксон Д.А., Маевский П.А., Коротких Э., Снид С.Б., Хэндли М.Дж., Интрон Д.С., и Скамбос, TA: Изменения в химическом составе снега и фирна на маршрутах US ITASE и влияние поверхностного остекления, The Cryosphere, 7, 515–535, https://doi.org/10.5194/tc-7-515-2013, 2013.
Du, Z., Xiao, C., Ding, M. и Li, C.: Идентификация множественных природных и антропогенные источники пыли в снегу от станции Чжуншань до купола А, Восточная Антарктида, J. Glaciol., 64, 855–865, https://doi.org/10.1017/jog.2018.72, 2018.
Du, Z., Xiao, C., Handley, MJ, Mayewski, PA, Ли, К. , Лю, С., Ма, X.,
и Янг, Дж.: Характеристики и источники вариации Fe в пробах снега вдоль
поход от станции Чжуншань до купола А, Восточная Антарктида, Sci.Всего
Environ., 675, 380–389, https://doi.org/10.1016/j.scitotenv.2019.04.139, 2019.
, Лю, С., Ма, X.,
и Янг, Дж.: Характеристики и источники вариации Fe в пробах снега вдоль
поход от станции Чжуншань до купола А, Восточная Антарктида, Sci.Всего
Environ., 675, 380–389, https://doi.org/10.1016/j.scitotenv.2019.04.139, 2019.
Финлейсон-Питтс, Б.Дж.: Химия тропосферы морской соли: взгляд на химический состав NaCl и NaBr на молекулярном уровне, Chem. Обр., 103, 4801–4822, 2003.
Граньяни Р., Смиралья К., Стенни Б. и Торчини С.: Химические и изотопные профили из снежных ям и неглубоких кернов фирна на леднике Кэмпбелл, север Земли Виктории, Антарктида, Анн. Glaciol., 27, 679–684, 1998.
Хара, К., Осада, К., и Яманучи, Т.: Измерения аэрозолей с привязанных аэростатов: сезонные и вертикальные вариации компонентов аэрозолей над станцией Сёва, Антарктида, Атмос. хим. Phys., 13, 9119–9139, https://doi.org/10.5194/acp-13-9119-2013, 2013.
Хара К., Наказава Ф., Фудзита С., Фукуи К. , Эномото, Х., и Сугияма, С.: Горизонтальное распределение компонентов аэрозоля и состояния их смешивания в Антарктиде во время прохождения JASE, Atmos. хим. Phys., 14, 10211–10230, https://doi.org/10.5194/acp-14-10211-2014, 2014.
хим. Phys., 14, 10211–10230, https://doi.org/10.5194/acp-14-10211-2014, 2014.
Хоу С., Ли Ю., Сяо С. и Рен Дж.: Недавняя скорость накопления в Куполе А, Антарктида, Китай. науч. Bull., 52, 428–431, 2007.
Keene, W.C., Maring, H., Maben, J.R., Kieber, D.J., Pszenny, A.A., Dahl, Э. Э., Изагирре, М. А., Дэвис, А. Дж., Лонг, М. С., и Чжоу, X .: Химические и физические характеристики зарождающихся аэрозолей, образующихся при лопании пузырьков при модель воздушно-морской границы, J. Geophys. Рез., 112, Д21202, https://doi.org/10.1029/2007JD008464, 2007.
Ходжер Т.В., Голобокова Л.П., Осипов Е.Ю., Шибаев Ю.В. А., Липенков В.Я., Осипова О.П., Пети Дж.Р. Пространственно-временная динамика химического состава поверхностного снега в Восточной Антарктиде на разрезе станция Прогресс – станция Восток, Криосфера, 8, 931–939, https://doi.org/10.5194/tc-8-931-2014, 2014.
Легран, М.: Химия антарктического снега и льда, J. de Phys., 48, 77–86, 1987.
Легран, М. и Дельмас, Р.Ж.: Пространственные и временные вариации снега.
химия на Земле Адели (Восточная Антарктида), Ann. Гласиол., 7, 20–25,
1985.
и Дельмас, Р.Ж.: Пространственные и временные вариации снега.
химия на Земле Адели (Восточная Антарктида), Ann. Гласиол., 7, 20–25,
1985.
Легран, М., Ян, X., Преункерт, С., и Тейс, Н.: Круглогодичные записи морская соль, газообразный и твердый неорганический бром в атмосфере пограничный слой на прибрежном (Дюмон-д’Юрвиль) и центральном (Конкордия) востоке Антарктические участки, J. Geophys. Рез., 121, 2015JD024066, https://doi.org/10.1002/2015JD024066, 2016.
Легран, М., Преункерт, С., Веллер, Р., Зипф Л., Эльзессер К., Мерчел С., Ругель Г. и Вагенбах Д.: Круглогодичная запись объемного и сегрегированного по размеру состава аэрозолей в центральной Антарктиде (участок Конкордия) – Часть 2: Биогенный серный (сульфатный и метансульфонатный) аэрозоль, атм. хим. Phys., 17, 14055–14073, https://doi.org/10.5194/acp-17-14055-2017, 2017a.
Легран, М., Преункерт, С., Вольф, Э., Веллер, Р., Журден, Б., и Вагенбах, Д.: Круглогодичные записи объемного и размерного состава аэрозолей в центральной Антарктиде (Concordia сайт) – Часть 1: Фракционирование частиц морской соли, Атмос. хим. Phys., 17, 14039–14054, https://doi.org/10.5194/acp-17-14039-2017, 2017б.
хим. Phys., 17, 14039–14054, https://doi.org/10.5194/acp-17-14039-2017, 2017б.
Ли, К., Сяо, К., Ши, Г., Дин, М., Цинь, Д. и Рен, Дж.: Пространственные и временная изменчивость вещества морского происхождения на разрезе из Чжуншаня Станция до купола А, Восточная Антарктида, J. Environ. наук, 46, 190–202, https://doi.org/10.1016/j.jes.2015.07.011, 2016.
Марион Г., Фаррен Р. и Комровски А.: Альтернативные пути поступления морской воды замораживание, холодный рег. науч. техн., 29, 259–266, 1999.
Маевский П. А., Карлтон А. М., Биркель С. Д., Диксон Д., Курбатов А. В., Коротких Э., МакКоннелл Дж., Карран М., Коул-Дай Дж., Цзян С., Пламмер, К., Вэнс Т., Мааш К.А., Снид С.Б. и Хэндли М.: Ледяной керн и аналоги реанализа климата для прогнозирования Антарктики и Южного полушария изменения климата, Quaternary Sci. Откр., 155, 50–66, https://doi.org/10.1016/j.quascirev.2016.11.017, 2017.
Малвейни, Р. и Вольф, Э.: Пространственная изменчивость основного химического состава
Антарктический ледяной щит, Ann. Glaciol., 20, 440–447, 1994.
Glaciol., 20, 440–447, 1994.
Нойбауэр, Дж. и Хьюманн, К.Г.: Определение следов нитратов в снегу и фирновые керны шельфовых ледников моря Уэдделла, Антарктида, Атмос. Окружающая среда, 22, 537–545, 1988.
Пропозито, М., Бекальи, С., Кастеллано, Э., Флора, О., Дженони, Л., Граньяни, Р., Стенни Б., Траверси Р., Удисти Р. и Фреззотти М.: Химические и изотопная изменчивость снега на маршруте ITASE 1998 г. из залива Терра Нова до Купола С, Восточная Антарктида, Энн. Гляциол., 35, 187–194, 2002.
Цинь Д., Зеллер Э. Дж. и Дрешхофф Г. А.: Распределение нитратов содержание в поверхностном снегу Антарктического ледяного щита по маршруту Международная трансантарктическая экспедиция 1990 г., J. Geophys. Рез., 97, с. 6277–6284, 1992.
Ранкин, А. М. и Вольф, Э. У.: Аммоний и калий в снегу вокруг Колония императорских пингвинов в Антарктиде. наук, 12, 154–159, https://doi.org/10.1017/S0954102000000201, 2000.
Рассел А. и МакГрегор Г.Р.: Атмосферное Южное полушарие. циркуляция: влияние на антарктический климат и реконструкция антарктического
данные ледяных кернов, Climatic Change, 99, 155–192, 2010.
циркуляция: влияние на антарктический климат и реконструкция антарктического
данные ледяных кернов, Climatic Change, 99, 155–192, 2010.
Саварино Дж., Кайзер Дж., Морин С., Сигман Д.М. и Тименс М.Х. атмосферные нитраты в прибрежной Антарктиде, Атмос. хим. Phys., 7, 1925–1945, https://doi.org/10.5194/acp-7-1925-2007, 2007.
Севери, М., Бекагли, С., Кастеллано, Э., Морганти, А., Траверси, Р., и Удисти, Р.: Тридцать лет снежного покрова в Талос-Доум (Северная Виктория). Земля, Восточная Антарктида): химические профили и климатические последствия, Микрохим. Ж., 92, 15–20, https://doi.org/10.1016/j.microc.2008.08.004, 2009.
Ши, Г.: Набор данных: данные о химическом составе поверхности снега на маршруте от от побережья Восточной Антарктиды до вершины ледяного щита, Купол А, Обмен данными Платформа полярной науки, Национальный центр арктических и антарктических данных, https://doi.org/10.11856/SNS.D.2021.003.v0, 2021.
Ши, Г., Ли, Ю., Цзян, С., Ан, К., Ма, Х. , Сун, Б., и Ван, Ю.:
Крупномасштабная пространственная изменчивость основных ионов во влажной атмосфере
отложение вдоль разреза Китайская Антарктида (31 ∘ с.ш.–69 ∘ ю.ш.), Tellus B, 64, 17134, https://doi.org/10.3402/tellusb.v64i0.17134, 2012.
, Сун, Б., и Ван, Ю.:
Крупномасштабная пространственная изменчивость основных ионов во влажной атмосфере
отложение вдоль разреза Китайская Антарктида (31 ∘ с.ш.–69 ∘ ю.ш.), Tellus B, 64, 17134, https://doi.org/10.3402/tellusb.v64i0.17134, 2012.
Shi, G ., Баффен, А.М., Гастингс, М.Г., Ли, К., Ма, Х., Ли, Ю., Сунь, Б., Ан, С., и Цзян, С.: Исследование обработки нитратов после осаждения в Снег Восточной Антарктики: изотопные ограничения фотолитических потерь, повторного окисления и источников поступления, Atmos.хим. Phys., 15, 9435–9453, https://doi.org/10.5194/acp-15-9435-2015, 2015.
Shi, G., Buffen, AM, Ma, H., Hu, Z., Сунь, Б., Ли, К., Ю, Дж., Ма, Т., Ан, К., Цзян С., Ли Ю. и Гастингс М. Г.: Отличительное летнее время образование нитратов в атмосфере на Восточно-Антарктическом ледяном щите, Геохим. Космохим. Ac., 231, 1–14, https://doi.org/10.1016/j.gca.2018.03.025, 2018.
Sigl, M., Fudge, TJ, Winstrup, M., Cole-Dai, J. ., Феррис Д. , МакКоннелл Дж. Р., Тейлор К. С., Велтен, К.С., Вудрафф, Т.Е., Адольфи, Ф., Бизио, М., Брук, Э.Дж., Бьюзерт, К., Каффи, М.В., Данбар, Н.В., Эдвардс, Р., Генг, Л., Айверсон, Н. , Коффман Б., Лейман Л., Маселли О.Дж., Макгвайр К., Мюшелер Р., Нишиидзуми К., Пастерис Д.Р., Родс Р.Х. и Соуэрс Т.А.: Глубокий ледяной керн WAIS Divide WD2014 хронология – Часть 2: Годовой учет (0–31 тыс. л.н.), Клим. Прошлое, 12, 769–786, https://doi.org/10.5194/cp-12-769-2016, 2016.
, МакКоннелл Дж. Р., Тейлор К. С., Велтен, К.С., Вудрафф, Т.Е., Адольфи, Ф., Бизио, М., Брук, Э.Дж., Бьюзерт, К., Каффи, М.В., Данбар, Н.В., Эдвардс, Р., Генг, Л., Айверсон, Н. , Коффман Б., Лейман Л., Маселли О.Дж., Макгвайр К., Мюшелер Р., Нишиидзуми К., Пастерис Д.Р., Родс Р.Х. и Соуэрс Т.А.: Глубокий ледяной керн WAIS Divide WD2014 хронология – Часть 2: Годовой учет (0–31 тыс. л.н.), Клим. Прошлое, 12, 769–786, https://doi.org/10.5194/cp-12-769-2016, 2016.
Судзуки Т., Иидзука Ю., Мацуока К., Фурукава Т., Камияма К. и Ватанабэ, О.: Распределение компонентов морской соли в снежном покрове вдоль Траверс от побережья до станции Купол Фудзи 1000 км вглубь суши на восток Земля Королевы Мод, Антарктида, Теллус B, 54, 407–411, 2002.
Траверси Р., Бекальи С., Кастеллано Э., Ларджуни О., Мильори А.,
Севери М., Фреззотти М. и Удисти Р.: Пространственное и временное распределение
экологических маркеров от Прибрежных до плато Антарктиды по фирну
химический анализ керна, Int.Дж. Окружающая среда. Анальный. хим., 84, 457–470,
https://doi.org/10.1080/03067310310001640393, 2004.
Окружающая среда. Анальный. хим., 84, 457–470,
https://doi.org/10.1080/03067310310001640393, 2004.
Удисти Р., Даян У., Бекальи С., Бусетто М., Фросини Д., Легран М., Лукарелли Ф., Преункерт С., Севери М. и Траверси Р. Морские брызги аэрозоля в центральной Антарктиде. Настоящее атмосферное поведение и последствия для палеоклиматических реконструкций, Atmos. Окружающая, 52, 109–120, https://doi.org/10.1016/j.atmosenv.2011.10.018, 2012.
Вирккула, А., Тейнила, К., Хилламо, Р., Керминен, В.-М., Саарикоски С., Аурела М., Вииданоя Дж., Паатеро Дж., Копонен И.К. и Кулмала М.: Химический состав аэрозоля пограничного слоя над Атлантическим океаном и на антарктическом участке, Атмос. хим. Phys., 6, 3407–3421, https://doi.org/10.5194/acp-6-3407-2006, 2006.
Wagenbach, D., Ducroz, F., Mulvaney, R., Keck, L. , Миникин А., Легран М., Холл, Дж. С., и Вольф, Э. В.: Аэрозоль морской соли в прибрежных районах Антарктики, Дж. Геофиз. Рез., 103, 10961–10974, 1998.
Веллер Р. , Вагенбах, Д., Легран, М., Эльзассер, К., Тиан-кунце, X.,
и Königlanglo, G.: Непрерывные 25-летние записи аэрозолей в прибрежных водах.
Антарктида: межгодовая изменчивость ионных соединений и связи с
климатические индексы, Tellus B, 63, 901–919,
https://doi.org/10.1111/j.1600-0889.2011.00542.x, 2011.
, Вагенбах, Д., Легран, М., Эльзассер, К., Тиан-кунце, X.,
и Königlanglo, G.: Непрерывные 25-летние записи аэрозолей в прибрежных водах.
Антарктида: межгодовая изменчивость ионных соединений и связи с
климатические индексы, Tellus B, 63, 901–919,
https://doi.org/10.1111/j.1600-0889.2011.00542.x, 2011.
Вольф, Э.В., Фишер, Х., Фундел, Ф., Рут, У., Тварлох, Б., Литтот, ГК, Малвейни Р., Ротлисбергер Р., де Анджелис М., Бутрон С. Ф., Ханссон, М., Джонселл У., Хаттерли М.А., Ламберт Ф., Кауфманн П., Штауффер, Б., Стокер, Т. Ф., Стеффенсен, Дж. П., Биглер, М., Зиггаард-Андерсен, М. Л., Удисти Р., Бекальи С., Кастеллано Э., Севери М., Вагенбах Д., Барбанте, К., Габриэлли, П. и Гаспари, В.: Протяженность морского льда в Южном океане, продуктивность и приток железа за последние восемь ледниковых циклов, Nature, 440, 491–496, https://doi.org/10.1038/nature04614, 2006.
Вольф Э. В., Барбанте С., Бекагл С., Биглер М., Бутрон С. Ф.,
Кастеллано, Э., де Анджелис, М., и Федерер, У.: Изменения в окружающей среде за
последние 800 000 лет из химического анализа ледяного керна EPICA Dome C,
Четвертичная наука. Rev., 29, 285–295, 2010.
Rev., 29, 285–295, 2010.
%PDF-1.4 % 135 0 объект > эндообъект внешняя ссылка 135 74 0000000016 00000 н 0000002214 00000 н 0000002299 00000 н 0000002502 00000 н 0000002838 00000 н 0000002988 00000 н 0000003397 00000 н 0000003500 00000 н 0000003537 00000 н 0000003704 00000 н 0000004210 00000 н 0000004948 00000 н 0000005086 00000 н 0000005496 00000 н 0000008186 00000 н 0000008318 00000 н 0000008479 00000 н 0000008658 00000 н 0000011082 00000 н 0000012484 00000 н 0000012700 00000 н 0000014374 00000 н 0000014675 00000 н 0000014976 00000 н 0000016772 00000 н 0000018620 00000 н 0000018735 00000 н 0000018900 00000 н 0000019126 00000 н 0000021614 00000 н 0000072014 00000 н 0000074134 00000 н 0000074950 00000 н 0000075000 00000 н 0000080255 00000 н 0000080470 00000 н 0000080692 00000 н 0000080976 00000 н 0000081026 00000 н 0000083558 00000 н 0000083751 00000 н 0000083959 00000 н 0000084254 00000 н 0000088376 00000 н 0000088589 00000 н 0000093426 00000 н 0000093632 00000 н 0000099693 00000 н 0000099904 00000 н 0000104737 00000 н 0000104945 00000 н 0000115619 00000 н 0000115827 00000 н 0000120662 00000 н 0000120870 00000 н 0000125165 00000 н 0000125373 00000 н 0000129539 00000 н 0000129750 00000 н 0000129800 00000 н 0000135566 00000 н 0000135763 00000 н 0000135968 00000 н 0000157644 00000 н 0000157858 00000 н 0000193632 00000 н 0000193840 00000 н 0000193890 00000 н 0000197849 00000 н 0000198075 00000 н 0000198285 00000 н 0000198570 00000 н 0000212761 00000 н 0000001776 00000 н трейлер ]/предыдущая 539634>> startxref 0 %%EOF 208 0 объект >поток hdK(Dq 3s2wlȂXI0
Yk#+Ƃac!NJ9s:}@98Ja A:vD؊!wpnPV\t3j|bzh?l-6′)kYJ|fSDC[d. “EGĽ%L@t;40Zcq`E(GGVg4k4Z|3ny!,Lc}1>pI*A&0b泠
ƙ9,8*D
Nc”>IBl+72ϡ?)GP2-24E)L2-
“EGĽ%L@t;40Zcq`E(GGVg4k4Z|3ny!,Lc}1>pI*A&0b泠
ƙ9,8*D
Nc”>IBl+72ϡ?)GP2-24E)L2-
Динамическая комбинаторная химия на основе белков: краткий обзор и экспериментальный протокол – Hartman – 2019 – European Journal of Organic Chemistry
Введение
С момента своего появления более двух десятилетий назад подходы к комбинаторной химии1-5 превратились в целенаправленную динамическую комбинаторную химию (tdDCC) и превратились в инструмент идентификации попаданий6-11 Растущее число групп продемонстрировали общую применимость и область применения tdDCC для идентификации модуляторов мишеней.6, 12-20 tdDCC относится к общим фармакологически значимым мишеням, которые наряду с белками также включают ДНК и РНК, тогда как DCC с белковым шаблоном (ptDCC) относится только к белкам. В последние годы было опубликовано несколько обзоров и глав книг по tdDCC.21-23 Этот мини-обзор охватывает нашу работу над ptDCC и предоставляет ключевые особенности нашего протокола, объясняя основные шаги в разработке успешного эксперимента ptDCC.
Тщательно отобранные строительные блоки соединяются обратимым образом через ковалентные или нековалентные связи, образуя динамическую комбинаторную библиотеку (DCL) (рис. 1).Биосовместимость, зависимость от рН, температуры, растворимости и стабильности компонентов являются важными факторами, которые следует учитывать. Идеальные DCL не требуют сорастворителей, однако может случиться так, что образованные продукты имеют более низкую растворимость, чем строительные блоки, и для того, чтобы удерживать все соединения в растворе, обычно используется сорастворитель, такой как диметилсульфоксид (ДМСО). Осаждение компонентов DCL может привести к нежелательному сдвигу равновесия. Напротив, желаемый сдвиг равновесия может быть получен путем добавления внешнего стимула, такого как белок-мишень.В целом, в ptDCC можно использовать два различных подхода: «адаптивный DCC», при котором мишень присутствует во время формирования DCL, и «предварительно уравновешенный DCC», при котором мишень добавляется после установления DCL. . Преимущество предварительно уравновешенного DCC заключается в том, что химию обмена можно применять в условиях, которые не переносятся белком. Недостатком является то, что этап скрининга выполняется в статических условиях, и нельзя наблюдать никаких эффектов амплификации, поскольку белок не изменяет равновесие.
. Преимущество предварительно уравновешенного DCC заключается в том, что химию обмена можно применять в условиях, которые не переносятся белком. Недостатком является то, что этап скрининга выполняется в статических условиях, и нельзя наблюдать никаких эффектов амплификации, поскольку белок не изменяет равновесие.
Схематическое изображение целевой динамической комбинаторной химии.
При ptDCC член(ы) DCL, которые связываются лучше всего, будут амплифицироваться, что приведет к увеличению их концентрации по сравнению с контрольной реакцией без внешнего стимула. Затем эти связующие могут быть дополнительно оценены на предмет их биохимических свойств.
Чтобы провести сравнительный анализ DCL, холостую реакцию без мишени следует запустить одновременно с реакцией по шаблону.Другой подход DCC – несравнительный, при котором попадания могут анализироваться в комплексе с целью или после выхода из цели. Существуют различные методы, которые можно использовать для анализа ДХЛ: жидкостная и эксклюзионная хроматография в сочетании с масс-спектрометрией, ЯМР-спектроскопия, флуоресцентная спектроскопия и рентгеновская кристаллография. Рисунок 2 иллюстрирует сравнительный подход по сравнению с несравнительным подходом, который может быть принят в DCC. Реакционную смесь можно «заморозить», чтобы предотвратить повторное уравновешивание библиотеки во время анализа.В случае химии ацилгидразона это может быть достигнуто за счет увеличения pH. Денатурация нагреванием, добавлением растворителя или (сверхбыстрым) центрифугированием обеспечивает высвобождение всех связывающих веществ из белка перед анализом.
Существуют различные методы, которые можно использовать для анализа ДХЛ: жидкостная и эксклюзионная хроматография в сочетании с масс-спектрометрией, ЯМР-спектроскопия, флуоресцентная спектроскопия и рентгеновская кристаллография. Рисунок 2 иллюстрирует сравнительный подход по сравнению с несравнительным подходом, который может быть принят в DCC. Реакционную смесь можно «заморозить», чтобы предотвратить повторное уравновешивание библиотеки во время анализа.В случае химии ацилгидразона это может быть достигнуто за счет увеличения pH. Денатурация нагреванием, добавлением растворителя или (сверхбыстрым) центрифугированием обеспечивает высвобождение всех связывающих веществ из белка перед анализом.
 Адаптировано из Frei et al.21
Адаптировано из Frei et al.211. Обратимая реакция Подходит для DCC
До сих пор использовалось лишь ограниченное количество обратимых реакций, они представлены на схеме 1. Одной из наиболее часто используемых реакций является образование (ацил-)гидразона, в котором кетоновые или альдегидные строительные блоки объединяются с (ацил-)гидразидами. . Эта реакция конденсации может происходить в воде, что делает ее биосовместимой.24 Синтез строительных блоков, как правило, прост, или они могут быть коммерчески доступными.
Обратимые реакции, используемые в таргетных ДКК для выявления биоактивных соединений. Адаптировано из Van der Vlag and Hirsch.23 В физиологических условиях, нейтральном рН и комнатной температуре образование и обмен ацилгидразона происходят относительно медленно. При кислом рН равновесие достигается быстро. Однако Грини и его коллеги показали, что на зависимость от pH может влиять добавление нуклеофильного катализатора.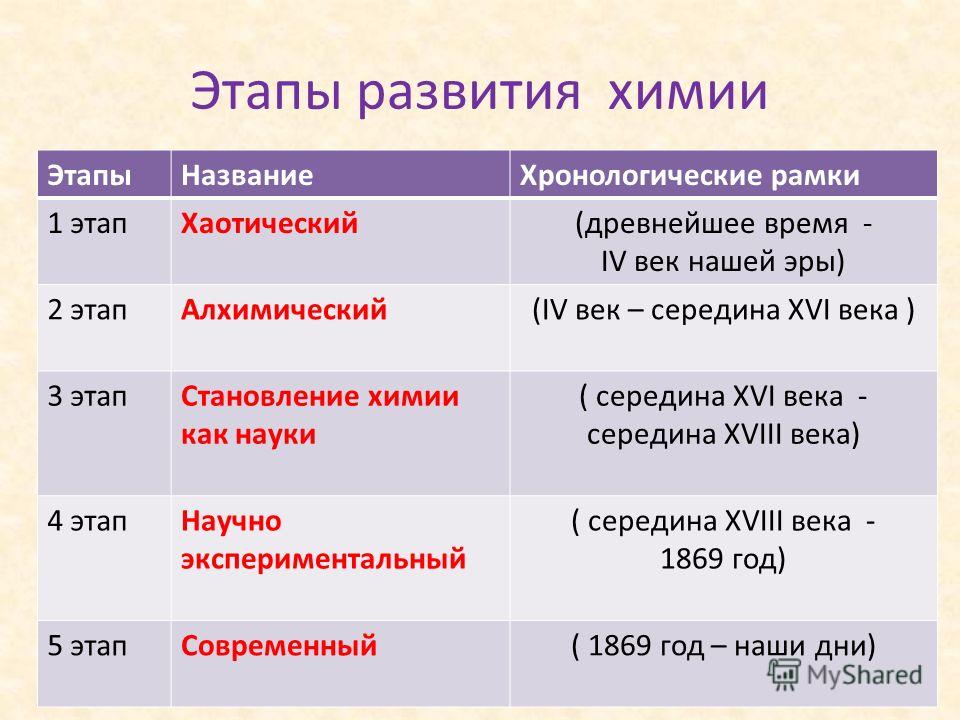 Они смогли достаточно быстро достичь равновесия при сравнительно высоком рН, равном 6.2 с использованием анилина в качестве нуклеофильного катализатора.12 Ранее Доусон с сотрудниками показал, что анилин может служить катализатором образования ацилгидразона и оксимного лигирования.25, 26 Производные анилина, содержащие заместители в арильном кольце, даже более эффективные катализаторы.27
Они смогли достаточно быстро достичь равновесия при сравнительно высоком рН, равном 6.2 с использованием анилина в качестве нуклеофильного катализатора.12 Ранее Доусон с сотрудниками показал, что анилин может служить катализатором образования ацилгидразона и оксимного лигирования.25, 26 Производные анилина, содержащие заместители в арильном кольце, даже более эффективные катализаторы.27
Ацилгидразоновая связь является обратимой, но достаточно стабильной для проведения прямого анализа в кислых условиях и устойчива к гидролизу при физиологических значениях рН, что позволяет «заморозить» обратимую реакцию при повышении рН.24
Обзор исследований, опубликованных за последние пять лет в области ptDCC, приведен в таблице 1. Следует отметить, что было опубликовано гораздо больше работ по применению DCC для формирования разнообразных библиотек в процессе открытия лекарств. Например, соединение DCC с библиотеками, кодируемыми ДНК, с созданием так называемых динамических комбинаторных химических библиотек, кодируемых ДНК (EDCCL). Иминобиотин и гомотетрамерный стрептавидин использовали в качестве модельной системы для идентификации бидентатного взаимодействия белок/лиганд.Добавление внешнего стимула, например целевого белка, может сместить термодинамическое равновесие, и, следовательно, после секвенирования можно наблюдать амплификацию ДНК28
Иминобиотин и гомотетрамерный стрептавидин использовали в качестве модельной системы для идентификации бидентатного взаимодействия белок/лиганд.Добавление внешнего стимула, например целевого белка, может сместить термодинамическое равновесие, и, следовательно, после секвенирования можно наблюдать амплификацию ДНК28
| Цель | Обратимая реакция | Анализ | Размер библиотеки | Время уравновешивания | Метод, применяемый для измерения сходства | Лучшая близость | Арт. |
|---|---|---|---|---|---|---|---|
| Тау-РНК дикого типа | Дисульфид | ВЭЖХ-МС и ЯМР | 21 | 2 дня | Флуоресцентное титрование | EC 50 = 70 нм | Артигас и др.201533 |
| РНК ФСС ВИЧ | Дисульфид | МС | 12 | 4 дня | н. д. д. | н.д. | Макэнани и др.201634 |
| Рецептор сосудистого эндотелиального фактора роста (VEGFR) 2 | Имине | HRMS | 297 | 24 часа | Активность in vitro в отношении линий раковых клеток | ИС 50 = 2.4 мкм | Ян и др. 201635 |
| Эндотиапепсин | Ацилгидразон | ВЭЖХ-МС | 90 | 20 ч | Анализ ингибирования | ИС 50 = 54. 5 нм К i = 25,4 нм 5 нм К i = 25,4 нм | Мондал и др. 201636 |
| ФимХ | Ацилгидразон | ВЭЖХ | 8 | 3 дня | СПР | К D = 273 нм | Фрей и др.201737 |
| УДФ-галактопиранозомутаза | Ацилгидразон | ВЭЖХ | 11 | 24 часа | Анализ на основе флуоресценции и МИК | K D = 3 мкм МИК = 26 мкг мл –1 | Фу и др. 201738 201738 |
| Миелопероксидаза (МПО) | Гидразон | Анализ активности | 6 | н.д. | анализ активности in vivo | IC 50 = 79 нм | Субхье и др.201739 |
| EC FabH | Ацилгидразон | 19 F-ЯМР | 5 | 12 ч | Ферментативный анализ | IC 50 = 3 мм | Эктстрём и др. 201840 201840 |
| Мультибелковая стратегия в отношении оксигеназ AlkB: FTO, ALKBh4 и ALKBH5 | Ацилгидразон | ДСФ и ВЭЖХ | 10 | 5 ч | Анализы деметилазы и DSF на основе ВЭЖХ | ИС 50 = 2.6 мкм | Дас и др. 201841 |
| Trypanosoma cruzi, содержащие бромдомен (Tc BDF3) | Ацилгидразон | ВЭЖХ-МС | 30 | н. д. д. | ДСФ | IC 50 = 13–23 мкм | Гарсия и др.201842 |
| ДНК G-квадруплекса | Иминовое образование | ВЭЖХ и ESI-МС | 10 | 24 часа | н.д. | с.п.а. | Яна и др. 201943 |
2. Пристальный взгляд на шаблонный белок
Для получения значимых результатов экспериментов с DCC критически важно качество входного шаблона. Поскольку равновесие библиотеки смещается из-за шаблонного эффекта добавленного образца белка, она должна состоять из целевого белка, максимально приближенного к его нативному состоянию.Количество используемого шаблона зависит от целевого белка, сообщалось об успешных проектах DCC с использованием от 0,1 до 1,5 эквивалентов белка.29, 44 Эксперименты DCC также возможны со смесью белков, но четко определенный образец упрощает последующие данные. анализа и снижает количество ложноположительных результатов для желаемой цели.41 Состояние образца белка зависит от различных переменных. Для экспериментов DCC особое значение имеют чистота, концентрация, третичная и четвертичная структура белка, добавки и примеси, а также значение pH.Во время эксперимента, который может длиться до нескольких дней, может произойти расщепление белка и его осаждение. Тесты, описанные здесь, должны дать обзор и помочь выбрать подходящие экспериментальные условия для планирования новых экспериментов DCC. В следующих параграфах мы кратко обсудим влияние этих факторов и подходящие аналитические методы для их мониторинга.
Поскольку равновесие библиотеки смещается из-за шаблонного эффекта добавленного образца белка, она должна состоять из целевого белка, максимально приближенного к его нативному состоянию.Количество используемого шаблона зависит от целевого белка, сообщалось об успешных проектах DCC с использованием от 0,1 до 1,5 эквивалентов белка.29, 44 Эксперименты DCC также возможны со смесью белков, но четко определенный образец упрощает последующие данные. анализа и снижает количество ложноположительных результатов для желаемой цели.41 Состояние образца белка зависит от различных переменных. Для экспериментов DCC особое значение имеют чистота, концентрация, третичная и четвертичная структура белка, добавки и примеси, а также значение pH.Во время эксперимента, который может длиться до нескольких дней, может произойти расщепление белка и его осаждение. Тесты, описанные здесь, должны дать обзор и помочь выбрать подходящие экспериментальные условия для планирования новых экспериментов DCC. В следующих параграфах мы кратко обсудим влияние этих факторов и подходящие аналитические методы для их мониторинга.
2.1. Чистота
В случае образца смешанного или нечистого белка может параллельно протекать несколько матричных реакций.Невозможно провести различие между небольшой частью образца, демонстрирующей сильный матричный эффект, и большой частью белкового пула, демонстрирующей лишь слабое усиление связывающего вещества. Это приведет к перекрытию данных, которые трудно анализировать, и может привести к ложным срабатываниям. Поэтому мы рекомендуем начинать с самой высокой доступной чистоты белка.
2.2. Стабильность
Не только исходное состояние, но и стабильность матричного белка в ходе реакции следует проверять предварительными тестами перед проведением DCC-эксперимента.Промежуток времени, в течение которого отслеживается эксперимент DCC, предварительно уравновешенный или адаптивный, может варьироваться. Это зависит от скорости реакции и концентрации и в идеале должно контролироваться до тех пор, пока библиотека не достигнет равновесного состояния. Обычно ДХЛ достигает нового равновесия в течение первых нескольких дней, в зависимости от обратимой реакции и используемых условий (табл. 1). Однако, если белок стабилен в течение более длительного периода времени, возможно более длительное время уравновешивания, например, до 20 дней для очень стабильной протеазы эндотиапепсина (см.4).24
Обычно ДХЛ достигает нового равновесия в течение первых нескольких дней, в зависимости от обратимой реакции и используемых условий (табл. 1). Однако, если белок стабилен в течение более длительного периода времени, возможно более длительное время уравновешивания, например, до 20 дней для очень стабильной протеазы эндотиапепсина (см.4).24
Важно, чтобы белок не осаждался и не разрушался во время эксперимента. Осаждение белка удалит матрицу из раствора. Денатурация шаблона приведет к совершенно новым шаблонам, что повлияет на равновесное состояние DCL. Это может привести к случайной и невоспроизводимой амплификации соединений неупорядоченным белком и уменьшению изначально уже амплифицированных лучших связывателей нативной матрицы.Если белок-мишень является лабильным, поэтому необходимо следить за реакцией во времени, чтобы определить временное матричное равновесие библиотеки DCC. При этом могут быть обнаружены соединения, амплифицированные в нативном состоянии матрицы.
В конце концов, после продолжительного инкубирования, почти каждый белок распадется и, таким образом, снова изменит равновесие DCL. Соединения, амплифицированные на этом этапе, следует игнорировать, поскольку они не были шаблонированы нативным белком.Поэтому следует избегать наблюдения за экспериментом DCC в течение более длительных периодов времени, чем стабильность шаблона в конкретных условиях.
2.3. Буфер и pH
При выборе буфера для DCC-экспериментов необходимо выполнить несколько различных требований. Следует обратить внимание на возможные побочные реакции с ДКЛ или эффекты хелатирования. Например, трис-буфер может образовывать имин с альдегидными строительными блоками, которые могут влиять на формирование DCL.Некоторая стабилизация белка полезна, но также следует избегать сильных взаимодействий буфера с белком-мишенью, например, фосфатного буфера для фосфатсвязывающего белка. Фосфат может конкурировать с возможными связующими; возможные последствия конкуренции более подробно обсуждаются в разделе 2. 5. До сих пор в большинстве случаев использовались общие буферные системы, которые показаны в таблице 2 и на схеме 2. Однако выбор буфера не ограничивается установленными системами.
5. До сих пор в большинстве случаев использовались общие буферные системы, которые показаны в таблице 2 и на схеме 2. Однако выбор буфера не ограничивается установленными системами.
| Реакция | Буфер описан в литературе |
|---|---|
| Образование ацилгидразонов 6, 24, 37 | Ацетат аммония и натрия, фосфат, трис* |
| Гидразоновая формация 45, 46 | Фосфат, Трис* |
| Дисульфид 47, 48 | Фосфат, борат |
| Тиоэфир 49 | Вода/ДМСО |
| Имине 13 | Вода |
| Сложный эфир боронатной кислоты 50, 51 | Ацетат аммония, вода |
Пример возможных буферов и диапазонов рН реакций, используемых в экспериментах DCC.
Для многих белков-мишеней стабильность при комнатной температуре и оптимальные буферные условия неизвестны. Поэтому мы рекомендуем определить эти условия до проведения экспериментов DCC. Поскольку на стабильность белка влияет несколько взаимозависимых факторов, таких как pH, буфер, ионная сила и ионы, трудно предложить пошаговую схему для определения идеального состава буфера для данного белка.28 Не только белок, но и изменение этих параметров может существенно повлиять на обменную химию.Мы предлагаем сначала измерить эффект рН, буфера и ионной силы в широком диапазоне параллельно. После этого небольшой выбор (от 2 до 5) из наиболее стабилизирующих комбинаций могут быть оценены на их долгосрочный эффект на белок. Впоследствии лучшие условия затем будут использованы для определения влияния ДМСО (раздел 2.6) и, если они представляют интерес, добавки (раздел 2.5). Выбор исходных буферов не может быть расширен, в случае, если нет подходящего условие было найдено.
Два или более буферы должны быть подвергнуты скринингу на значение рН, чтобы отличить влияние компонента буфера и величины рН на стабильность белка.Также можно использовать так называемый «супербуфер»,52 смесь трех или более компонентов буфера, позволяющая регулировать рН в широком диапазоне без изменения состава или концентрации буфера.
Влияние компонентов буфера на белок можно измерить простым способом, определив точку плавления целевого белка с помощью анализа теплового сдвига/дифференциальной сканирующей флуориметрии (TSA/DSF).28 В этом методе белок инкубируют вместе с липофильным красителем, например сипрооранжем.Краситель показывает увеличение флуоресценции после связывания с гидрофобными частями белка. Они часто располагаются внутри белка и обнажаются во время индуцированного температурой разворачивания/плавления. Зависимое от температуры увеличение флуоресценции может быть измерено в аппарате RT-PCR и дает T m белка.
Другие методы, такие как DSC, ITC и CD (дифференциальная сканирующая калориметрия, изотермическая титрационная калориметрия и спектроскопия кругового дихроизма) и определение точек плавления с помощью CD, также могут быть использованы для получения информации о взаимодействии и возможной стабилизации белка с его буфером. , но требуют большого количества белка и/или длительного времени измерения.Однако TSA предлагает высокую производительность и короткое время анализа, а также несколько уже опубликованных или коммерчески доступных наборов в 96-луночном формате.53, 54 Эти наборы изначально предназначались для скрининга оптимальных условий кристаллизации и охватывают несколько условий, влияющих на стабильность. . При проведении экспериментов с DCC может оказаться полезным разработка индивидуального макета 96-луночного планшета с учетом буферов и условий, совместимых с запланированной реакцией DCC. Это краткосрочное вложение, которое может быстро окупиться в будущем, если ptDCC будет использоваться для нескольких разных целей.
После определения стабилизирующего буфера, совместимого с DCC, белок следует проверить на его долговременную стабильность. Для проверки расщепления белкового остова анализ с помощью SDS-PAGE обладает достаточной чувствительностью (рис. 3). Чтобы определить, влияет ли сворачивание белка, TSA снова является методом выбора, поскольку сигнал напрямую зависит от процесса разворачивания белка. При длительном разложении температура плавления несколько снижается.В качестве вторичного эффекта деградации кривая флуоресценции может показывать двух- и многофазные точки плавления и общее снижение интенсивности сигнала и разрешения. Полностью денатурированный фермент будет показывать только уменьшающийся сигнал флуоресценции без пика от разворачивания белка. В качестве контроля в эксперимент должны быть включены свежий и термообработанный образец целевого белка.
12 % SDS-PAGE различных гомологов фермента 5-дезоксилулозо-5-фосфатсинтазы (DXS) после инкубации при комнатной температуре. Белок на верхнем геле не проявляет признаков деградации. Второй белок, показанный на нижнем геле, демонстрирует признаки деградации, начиная уже с первого дня с очень слабой полосы около 50 кДа. С 6-го дня также становится отчетливым уменьшение полосы основного белка. В верхнем левом углу гелевая метка была удалена с помощью программного обеспечения для обработки изображений.
Белок на верхнем геле не проявляет признаков деградации. Второй белок, показанный на нижнем геле, демонстрирует признаки деградации, начиная уже с первого дня с очень слабой полосы около 50 кДа. С 6-го дня также становится отчетливым уменьшение полосы основного белка. В верхнем левом углу гелевая метка была удалена с помощью программного обеспечения для обработки изображений.
Склонность белка к осаждению зависит от концентрации. Из-за этого анализы, определяющие стабильность белка, должны выполняться с той же концентрацией белка, которая предназначена для использования в эксперименте DCC.Если это невозможно из-за ограниченной доступности белка, первые эксперименты можно провести с меньшим количеством белка. Однако, по крайней мере, для выбранного конечного состояния оценку стабильности следует повторить с концентрацией белка, которая будет использоваться в экспериментах с DCC.
2.4. Функциональный ферментный анализ
Для ферментативных белков-мишеней можно использовать функциональный анализ вместо измерений TSA и PAGE для оценки долговременной стабильности. Анализ данных об активности функционального анализа для определения наилучших экспериментальных условий экспериментов DCC оставляет меньше возможностей для интерпретации, чем анализ результатов анализа температуры плавления. Следовательно, если доступен функциональный анализ и фермент проявляет каталитическую активность в желаемом диапазоне pH реакции DCC, анализ активности должен быть методом выбора.
Анализ данных об активности функционального анализа для определения наилучших экспериментальных условий экспериментов DCC оставляет меньше возможностей для интерпретации, чем анализ результатов анализа температуры плавления. Следовательно, если доступен функциональный анализ и фермент проявляет каталитическую активность в желаемом диапазоне pH реакции DCC, анализ активности должен быть методом выбора.
В предыдущем исследовании 2014 года мы могли отслеживать активность целевого белка эндотиапепсина, выполняя анализ на основе флуоресценции (рис. 4).Оптимум рН эндотиапепсина составляет 4,5, и ферментативная активность не изменилась даже после 20 дней инкубации при комнатной температуре и рН 4,6. Учитывая такую высокую стабильность, оптимизация буфера не потребовалась.24
Активность эндотиапепсина, пепсиноподобной аспарагиновой протеазы, в анализе на основе флуоресценции при различных временных интервалах инкубации при комнатной температуре. Адаптировано из Mondal et al.24
Адаптировано из Mondal et al.242.5. Добавки и загрязнения
Во время очистки белок может находиться в контакте с различными буферами и условиями.Некоторые компоненты буфера могут оставаться связанными с белком даже после замены буфера. Эти загрязняющие вещества могут повлиять на эксперимент. Поэтому рекомендуется критически оценить состав образца белка. Следует оценивать не только буфер для хранения белка, но и происхождение образца.
Обычными веществами, которые могут быть обнаружены в образцах белка, являются, например, имидазол в качестве остатка после этапа очистки IMAC (аффинная хроматография с иммобилизованным металлом).Образцы белка часто дополняют восстанавливающими агентами, такими как 2-ME, DTT или TCEP (2-меркаптоэтанол, дитиотреитол или трис(2-карбоксиэтил)фосфин) в концентрациях до 10 мМ, чтобы сохранить белок в восстанавливающей среде. Если образование дисульфидов является обратимой реакцией выбора, следует оценить конечную концентрацию восстановителя, чтобы убедиться, что образование дисульфидных связей не ингибируется.
Влияние добавок и загрязнений связано с объемом образца белка, используемого в отдельных экспериментах DCC.Это определяет не только конечную концентрацию белка, но и концентрацию загрязняющих веществ. Если концентрация белка от партии к партии варьируется и его объем регулируется для достижения одинаковой конечной концентрации в эксперименте DCC, следует отметить, что концентрации и эффекты добавок в эксперименте DCC могут различаться.
Соединения, которые остаются в образце белка, могут влиять на реакцию DCC или на целевой белок.Следует критически проверить каждый компонент буфера на возможное вмешательство в запланированный обменный химический процесс. Выполнение контрольного эксперимента со всеми компонентами буфера в отсутствие белка может гарантировать отсутствие побочных реакций. Если точный состав образца белка неизвестен, можно получить небольшой объем буфера путем концентрирования белка с использованием устройства для ультрафильтрации и использования проточного режима для контрольного эксперимента.
Некоторые агенты, используемые при очистке белка, такие как криопротекторы, такие как глицерин, или детергенты, такие как Tween, будут неспецифически взаимодействовать с поверхностью белка.По нашему опыту, если нет намека на то, что они могут повлиять на эксперимент, остатки криопротекторов и моющих средств можно допустить. Следует соблюдать особую осторожность, если кофакторы, коферменты или ионы добавляются в процессе очистки для стабилизации фермента. То же самое относится и к компонентам буфера, структурно связанным с этими добавками. Все, что связывается с целевым карманом связывания, конкурирует с библиотекой DCC. Если во время эксперимента присутствует естественный кофактор прочного связывания, он может препятствовать связыванию строительных блоков и, следовательно, также ингибировать их амплификацию.Однако использование плотных связующих может быть полезным в контрольных экспериментах. Если соединение с известным сайтом связывания ингибирует образование некоторых ранее наблюдаемых связывающих веществ, это может быть воспринято как указание на то, что связующие матрицы нацелены на один и тот же белковый карман.
2.6. ДМСО
Добавление небольшого количества ДМСО в реакционный раствор является обычной практикой при разработке ферментативных анализов для улучшения растворимости гидрофобных соединений.Для биохимических анализов регулярно используются концентрации ДМСО до 10 %.55
В экспериментах DCC строительные блоки библиотеки обычно растворяют в маточных растворах ДМСО, чтобы упростить сборку библиотеки. В зависимости от состава библиотеки и количества используемых соединений конечная концентрация ДМСО будет варьироваться. Чтобы условия реакции были сопоставимы, мы рекомендуем добавлять ДМСО до концентрации, которую можно поддерживать постоянной для всех экспериментов проекта.Эта фиксированная концентрация должна быть оценена и выбрана заранее, чтобы убедиться, что белок ее переносит.
ДМСО оказывает очень широкий спектр воздействия на белки, он может даже снижать растворимость и вызывать осаждение. 56 Наблюдалось как ускорение скорости, так и ингибирование ферментативно-катализируемой реакции под действием ДМСО. Влияние уже низких процентных долей ДМСО на ферментативную активность часто указывает на то, что ДМСО действует как неспецифический эффектор, взаимодействуя с активным центром фермента.57 Если ферментативная активность снижается под действием ДМСО в более высоких концентрациях (>10 % ДМСО), это часто происходит за счет влияния на общую конформацию белка за счет вытеснения молекул воды, связанных с поверхностью, и разворачивания белка.58 С другой стороны, существуют ДМСО. известны толерантные ферменты, проявляющие активность до 80 % ДМСО.57 Анализ активности ферментов является методом выбора для оценки влияния ДМСО на фермент. Если анализ активности недоступен, эффект ДМСО также можно измерить с помощью TSA, однако взаимодействие с активным центром трудно обнаружить с помощью этого метода.Мы часто наблюдаем небольшое влияние на T m белка, но сильное влияние на ферментативную активность.
56 Наблюдалось как ускорение скорости, так и ингибирование ферментативно-катализируемой реакции под действием ДМСО. Влияние уже низких процентных долей ДМСО на ферментативную активность часто указывает на то, что ДМСО действует как неспецифический эффектор, взаимодействуя с активным центром фермента.57 Если ферментативная активность снижается под действием ДМСО в более высоких концентрациях (>10 % ДМСО), это часто происходит за счет влияния на общую конформацию белка за счет вытеснения молекул воды, связанных с поверхностью, и разворачивания белка.58 С другой стороны, существуют ДМСО. известны толерантные ферменты, проявляющие активность до 80 % ДМСО.57 Анализ активности ферментов является методом выбора для оценки влияния ДМСО на фермент. Если анализ активности недоступен, эффект ДМСО также можно измерить с помощью TSA, однако взаимодействие с активным центром трудно обнаружить с помощью этого метода.Мы часто наблюдаем небольшое влияние на T m белка, но сильное влияние на ферментативную активность. В совокупности концентрация ДМСО оказывает несколько эффектов на структуру белка. Преимущества добавления ДМСО необходимо сопоставлять с риском создания искусственной ферментативной складки, которая может амплифицировать соединения, которые не будут связываться в нативных условиях. Поэтому концентрация ДМСО должна быть как можно ниже, в нашей лаборатории регулярно используется до 5 %.
В совокупности концентрация ДМСО оказывает несколько эффектов на структуру белка. Преимущества добавления ДМСО необходимо сопоставлять с риском создания искусственной ферментативной складки, которая может амплифицировать соединения, которые не будут связываться в нативных условиях. Поэтому концентрация ДМСО должна быть как можно ниже, в нашей лаборатории регулярно используется до 5 %.
2.7. Температура
Чтобы ускорить достижение равновесия DCL, эксперименты обычно проводят при комнатной температуре. Для лабильных белков может потребоваться более низкая температура реакции, что может улучшить стабильность белков. В то же время снижается скорость уравновешивания, что приводит к увеличению времени инкубации. Оптимальная температура для стабильности белка в DCC может варьироваться от фермента к ферменту и поэтому должна оцениваться в каждом отдельном случае, но в большинстве случаев используется комнатная температура.
3.
 Настройка эксперимента ptDCC
Настройка эксперимента ptDCCКогда доступны кристаллические структуры или даже сокристаллические структуры, можно применить структурный подход для разработки многообещающих строительных блоков. В этом случае в качестве управляющих элементов могут быть предусмотрены и небиндеры, которые не должны выступать в качестве хитов. Следует тщательно выбирать тип обратимой связи, поскольку он влияет на молекулярное распознавание мишенью. Например, ацилгидразоновая связь напоминает амидную функциональность и содержит доноры и акцепторы водородных связей.Мы показали, что при сочетании DCC с дизайном на основе структуры de novo риски, связанные с этим привлекательным подходом, снижаются.24
3.1. Формирование DCL
Строительные блоки, возможно, придется растворить в ДМСО, что позволит им, а также сформированным продуктам оставаться растворимыми в конечной смеси. В принципе, их можно было бы растворить и в желаемом буфере, что было бы наиболее идеально. В 2014 году мы соединили DCC с ЯМР-спектроскопией разности насыщения-переноса (STD), которая требует более низких концентраций белка, чем обычный эксперимент DCC (таблица 3).Спектроскопия STD-NMR позволяет выбрать связующие из DCL, поскольку интенсивность этих сигналов выше из-за более эффективного переноса насыщения. В результате спектры STD-NMR нельзя использовать для определения концентраций членов DCL, и, следовательно, невозможно рассчитать амплификацию. В последующих экспериментах можно определить значение K D лиганда с помощью STD-ЯМР или других биофизических анализов.59
В 2014 году мы соединили DCC с ЯМР-спектроскопией разности насыщения-переноса (STD), которая требует более низких концентраций белка, чем обычный эксперимент DCC (таблица 3).Спектроскопия STD-NMR позволяет выбрать связующие из DCL, поскольку интенсивность этих сигналов выше из-за более эффективного переноса насыщения. В результате спектры STD-NMR нельзя использовать для определения концентраций членов DCL, и, следовательно, невозможно рассчитать амплификацию. В последующих экспериментах можно определить значение K D лиганда с помощью STD-ЯМР или других биофизических анализов.59
| Конечная концентрация в целом DCC | Окончательная концентрация, используемая в DCC, в сочетании с 1 H-STD-NMR24 | |
|---|---|---|
| Альдегид | 0. 1 мм 1 мм | 0,4 мм |
| Гидразид | 0,1–0,3 мм | 1 мм (для каждого из пяти гидразидов) |
| ДМСО | 5–10 % | 5–10 % |
| Анилин* | 10 мм | – |
| Белок** | 10–100 мкм | 4 мкм |
| Буфер*** | 0. 1 м 1 м | Ацетат аммония в D 2 O (0,1 м, pH 4,6) |
| pH* | Кислотно-нейтральный | рН 4,6 |
Соотношение гидразидов иальдегиды должны допускать образование всех возможных продуктов, поэтому следует использовать по крайней мере один эквивалент каждого гидразида на альдегид. Например, если используются три альдегида, то следует добавить не менее трех эквивалентов каждого гидразида, следя за тем, чтобы был избыток гидразидов. При необходимости можно добавить нуклеофильный катализатор, такой как анилин. Наиболее часто используемая концентрация ДМСО составляет около 5–10 %.
Следует рассмотреть контрольные эксперименты, которые должны выяснить, где происходит связывание молекул с белком и является ли оно специфическим или неспецифическим. Это может быть осуществлено, например, добавлением известного ингибитора. Если наблюдаемое ранее усиление больше не наблюдается, то хитовые соединения являются конкурентными связующими. Основываясь на работе Даниэли и др., Б. Эрнст и его коллеги предлагают, чтобы использование бычьего сывороточного альбумина (БСА) в качестве шаблона отрицательного контроля, для которого не ожидается амплификации, поскольку связывающий карман отличается, не является хороший контроль, так как это может повлиять на состав библиотеки, в то время как использование конкурентного ингибитора предпочтительнее.BSA использовался в DCC, чтобы показать, что прикладная библиотека дает совпадения только с реальной мишенью и что BSA дает тот же результат, что и бланк.32, 60 BSA широко известен своей стабильностью и считалось, что он не мешает биологическим реакциям. , однако недавно эксперименты DCC даже использовались для нацеливания на BSA.61
Это может быть осуществлено, например, добавлением известного ингибитора. Если наблюдаемое ранее усиление больше не наблюдается, то хитовые соединения являются конкурентными связующими. Основываясь на работе Даниэли и др., Б. Эрнст и его коллеги предлагают, чтобы использование бычьего сывороточного альбумина (БСА) в качестве шаблона отрицательного контроля, для которого не ожидается амплификации, поскольку связывающий карман отличается, не является хороший контроль, так как это может повлиять на состав библиотеки, в то время как использование конкурентного ингибитора предпочтительнее.BSA использовался в DCC, чтобы показать, что прикладная библиотека дает совпадения только с реальной мишенью и что BSA дает тот же результат, что и бланк.32, 60 BSA широко известен своей стабильностью и считалось, что он не мешает биологическим реакциям. , однако недавно эксперименты DCC даже использовались для нацеливания на BSA.61
3.2. Анализ DCL
Различные методы, такие как флуоресцентная поляризация, SPR, ITC, MST, STD-NMR, кристаллография и другие, могут использоваться для оценки и, возможно, оптимизации полученных совпадений. Мы, Радеманн и его коллеги рассмотрели аналитические методы, используемые в динамической комбинаторной химии с белковыми матрицами для обнаружения соединений-попаданий.23, 62
Мы, Радеманн и его коллеги рассмотрели аналитические методы, используемые в динамической комбинаторной химии с белковыми матрицами для обнаружения соединений-попаданий.23, 62
Обычно применяемым методом анализа экспериментов с DCC является запись хроматограмм ВЭЖХ-МС библиотек. В качестве наглядного примера сравнительного подхода мы нарисовали хроматограммы ВЭЖХ пустой библиотеки и целевой библиотеки (рис. 5). Когда мы сравниваем обе хроматограммы, мы видим, что пик номер пять увеличился в библиотеке, содержащей мишень, тогда как пики три и шесть уменьшились.Общее количество строительных блоков остается прежним, только равновесие может быть смещено в сторону одного или нескольких продуктов.
Схематический пример хроматограмм ВЭЖХ: (а) хроматограмма пустой библиотеки, (б) хроматограмма целевой библиотеки.
Чтобы точно определить усиление или уменьшение пиков, следует сравнить их относительные площади пиков (RPA). Вымышленные RPA обеих хроматограмм на рисунке 5 приведены в таблице 4.Коэффициент усиления в процентах можно рассчитать по уравнению 1, где коэффициент усиления в «кратности» определяется уравнением 2. Используя эти два уравнения, произведение на пятом пике увеличилось на 100 % или в два раза. Фрей и др. отчет о особенно тщательном анализе DCL с использованием лектина FimH в качестве мишени с использованием анализа ВЭЖХ с оптимизированным протоколом DCC.37
(1)
(2)
Таблица 4.Пример относительных площадей пиков (RPA), полученных из хроматограмм ВЭЖХ на рисунке
Вымышленные RPA обеих хроматограмм на рисунке 5 приведены в таблице 4.Коэффициент усиления в процентах можно рассчитать по уравнению 1, где коэффициент усиления в «кратности» определяется уравнением 2. Используя эти два уравнения, произведение на пятом пике увеличилось на 100 % или в два раза. Фрей и др. отчет о особенно тщательном анализе DCL с использованием лектина FimH в качестве мишени с использованием анализа ВЭЖХ с оптимизированным протоколом DCC.37
(1)
(2)
Таблица 4.Пример относительных площадей пиков (RPA), полученных из хроматограмм ВЭЖХ на рисунке| Номер пика | Относительная площадь пика в бланке [%] | Относительная площадь пика в целевом объекте [%] | Усиление в % | Усиление в «складке» |
|---|---|---|---|---|
| 1 | 10 | 10 | – | 1 |
| 2 | 15 | 15 | – | 1 |
| 3 | 20 | 16 | –20 % | 0. 8 8 |
| 4 | 16 | 16 | – | 1 |
| 5 | 12 | 24 | 100 % | 2 |
| 6 | 27 | 19 | –30 % | 0.7 |
| Итого | 100 % | 100 % |
3.
 3. DCL, проанализированный с помощью спектроскопии STD-NMR
3. DCL, проанализированный с помощью спектроскопии STD-NMR Вдохновленные работой Рамстрема и его сотрудников,20 мы проанализировали образовавшиеся ДХЛ с помощью спектроскопии СТД-ЯМР (схема 3).Пять подбиблиотек позволили провести четкий анализ. В качестве контроля с известным связующим мы использовали саквинавир ( K i = 48 нм), мощный пептидный ингибитор, для дифференциации специфического связывания от неспецифического. Каждая подбиблиотека содержала все пять гидразидов и один из строительных блоков альдегидов, и перед добавлением мишени ей давали уравновеситься в течение 24 часов. Анализируя сигналы протонов иминного типа продуктов ацилгидразона в спектрах 1 H-STD-NMR (рис. 6), мы идентифицировали всего восемь связующих веществ.Чтобы подтвердить результаты STD-NMR, мы провели анализ ингибирования ферментов и показали, что совпадения были ингибиторами со значениями IC 50 в диапазоне от 12,8 мкм до 365 мкм. Высокий уровень совпадений в этом отчете может быть результатом мощного и синергетического сочетания разработки лекарств на основе структуры de novo и DCC. Кроме того, это связано с использованием пяти подбиблиотек, в которых обнаруживается лучший связыватель каждой библиотеки, тогда как в обычной настройке ptDCC будут обнаружены только лучшие в целом связыватели.В STD-ЯМР белок используется в качестве инструмента для анализа библиотеки, тогда как в эксперименте ptDCC белок влияет на равновесие и, следовательно, на концентрации
Высокий уровень совпадений в этом отчете может быть результатом мощного и синергетического сочетания разработки лекарств на основе структуры de novo и DCC. Кроме того, это связано с использованием пяти подбиблиотек, в которых обнаруживается лучший связыватель каждой библиотеки, тогда как в обычной настройке ptDCC будут обнаружены только лучшие в целом связыватели.В STD-ЯМР белок используется в качестве инструмента для анализа библиотеки, тогда как в эксперименте ptDCC белок влияет на равновесие и, следовательно, на концентрации
 Адаптировано из Mondal et al.24
Адаптировано из Mondal et al.244.4. Как действовать после получения хитов
Получив проверенное попадание, идентифицированное с помощью дизайна препарата на основе структуры de novo в сочетании с DCC и STD-NMR, мы использовали подход к дизайну на основе структуры для улучшения молекулярного распознавания мишенью.63 В этом конкретном случае мы посчастливилось получить рентгеновскую кристаллическую структуру целевого эндотиапепсина в комплексе с попаданием. Если это не так, оптимизация все же возможна, опираясь на отношения структура-активность.
Выводы
Существует ряд шагов, которые следует тщательно учитывать, чтобы получить активные хиты от DCC. Если информация о цели доступна, т.е. кристаллическая структура, можно было бы рассмотреть дизайн на основе структуры при выборе строительных блоков. На этом этапе можно выбрать тип обратимой связи, который будет использоваться. Условия, необходимые для уравновешивания, должны быть совместимы с целью. После создания условий, которые гарантируют, что мишень останется свернутой, можно начинать фактический эксперимент DCC.Для этого необходимо приготовить исходные растворы строительных блоков, катализатора и белка. Сформированные DCL можно анализировать с помощью различных методов, таких как STD-NMR или HPLC-MS. Соединения, выбранные мишенью, и их биохимические свойства должны быть оценены и, возможно, оптимизированы в дальнейших исследованиях.
После создания условий, которые гарантируют, что мишень останется свернутой, можно начинать фактический эксперимент DCC.Для этого необходимо приготовить исходные растворы строительных блоков, катализатора и белка. Сформированные DCL можно анализировать с помощью различных методов, таких как STD-NMR или HPLC-MS. Соединения, выбранные мишенью, и их биохимические свойства должны быть оценены и, возможно, оптимизированы в дальнейших исследованиях.
Благодарности
Финансирование Нидерландской организации научных исследований (грант VIDI: 723.014.008; грант LIFT: 731.015.414) и от Инициативного и сетевого фонда Ассоциации Гельмгольца. Мы благодарим доктора Равиндру Джумде за плодотворные обсуждения этой рукописи.
Границы химии
Frontiers in Chemistry — это авторитетный и качественный журнал, в котором публикуются тщательно рецензируемые исследования в области химических наук. Полевой главный редактор Стив Суиб из Университета Коннектикута поддерживается выдающимся редакционным советом, состоящим из международных исследователей.Этот междисциплинарный журнал с открытым доступом находится в авангарде распространения и передачи научных знаний и важных открытий ученым, лидерам отрасли и общественности во всем мире.
Полевой главный редактор Стив Суиб из Университета Коннектикута поддерживается выдающимся редакционным советом, состоящим из международных исследователей.Этот междисциплинарный журнал с открытым доступом находится в авангарде распространения и передачи научных знаний и важных открытий ученым, лидерам отрасли и общественности во всем мире.
Химия — это отрасль науки, связанная со всеми другими основными областями исследований. Вездесущность химии проявляется в нашей повседневной жизни: от электронных устройств, которые мы все используем для общения, до продуктов, которые мы едим, до нашего здоровья и благополучия, до различных форм энергии, которые мы используем.Хотя в химии существует множество подтем и специальностей, фундаментальной связью во всех этих областях является то, как атомы, ионы и молекулы объединяются и распадаются в том, что некоторые стали называть «танцем жизни».
Все специальные разделы Frontiers in Chemistry находятся в открытом доступе с целью публикации выдающихся научных публикаций, обзорных статей, комментариев и идей по различным аспектам химии. Прошлые формы публикаций часто содержали определенные поддисциплины, чаще всего аналитическую, неорганическую, органическую и физическую химию, но в наши дни эти границы и рамки довольно размыты, и разрозненность этих дисциплин, похоже, размывается.Химия важна как для фундаментальных, так и для прикладных областей исследований и производства, и действительно, очертания академических и промышленных исследований также часто бывают искусственными. Совместные исследования во всех областях химии настоятельно поощряются и поддерживаются по мере продвижения вперед. Это захватывающие времена, и область химии вносит важный и значительный вклад в наши коллективные знания.
Прошлые формы публикаций часто содержали определенные поддисциплины, чаще всего аналитическую, неорганическую, органическую и физическую химию, но в наши дни эти границы и рамки довольно размыты, и разрозненность этих дисциплин, похоже, размывается.Химия важна как для фундаментальных, так и для прикладных областей исследований и производства, и действительно, очертания академических и промышленных исследований также часто бывают искусственными. Совместные исследования во всех областях химии настоятельно поощряются и поддерживаются по мере продвижения вперед. Это захватывающие времена, и область химии вносит важный и значительный вклад в наши коллективные знания.
Все материалы, подаваемые на курс Frontiers in Chemistry , должны соответствовать рекомендациям, представленным в нашем контрольном списке.От авторов требуется сообщать данные, использованные для характеристики новых и известных соединений.
Авторам предлагается представить контрольный список характеристик вместе со своей рукописью.


 Введите свой запрос:
Введите свой запрос: