история открытия, интересные факты и байки – Москва 24, 24.10.2012
Фото: ИТАР-ТАСС
Открытие таблицы периодических химических элементов стало одной из важных вех в истории развития химии как науки. Первооткрывателем таблицы стал российский ученый Дмитрий Менделеев. Неординарный ученый с широчайшим научным кругозором сумел объединить все представления о природе химических элементов в единую стройную концепцию.
Об истории открытия таблицы периодических элементов, интересных фактах, связанных с открытием новых элементов, и народных байках, которые окружали Менделеева и созданную им таблицу химических элементов, М24.RU расскажет в этой статье.
История открытия таблицы
К середине XIX века было открыто 63 химических элемента, и ученые всего мира не раз предпринимали попытки объединить все существовавшие элементы в единую концепцию. Элементы предлагали разместить в порядке возрастания атомной массы и разбить на группы по сходству химических свойств.
В 1863 году свою теорию предложил химик и музыкант Джон Александр Ньюленд, который предложил схему размещения химических элементов, схожую с той, что открыл Менделеев, но работа ученого не была принята всерьез научным сообществом из-за того, что автор увлекся поисками гармонии и связью музыки с химией.
В 1869 году Менделеев опубликовал свою схему периодической таблицы в журнале Русского химического общества и разослал извещение об открытии ведущим ученым мира. В дальнейшем химик не раз дорабатывал и улучшал схему, пока она не приобрела привычный вид.
Суть открытия Менделеева в том, что с ростом атомной массы химические свойства элементов меняются не монотонно, а периодически. После определенного количества разных по свойствам элементов, свойства начинают повторяться. Так, калий похож на натрий, фтор – на хлор, а золото схоже с серебром и медью.
В 1871 году Менделеев окончательно объединил идеи в периодический закон. Ученые предсказал открытие нескольких новых химических элементов и описал их химические свойства. В дальнейшем расчеты химика полностью подтвердились – галлий, скандий и германий полностью соответствовали тем свойствам, которые им приписал Менделеев.
В дальнейшем расчеты химика полностью подтвердились – галлий, скандий и германий полностью соответствовали тем свойствам, которые им приписал Менделеев.
Байки о Менделееве
Гравюра, на которой изображен Менделеев. Фото: ИТАР-ТАСС
Об известном ученом и его открытиях ходило немало баек. Люди в то время слабо представляли себе химию и считали, что занятия химией – это что-то вроде поедания супа из младенцев и воровства в промышленных масштабах. Поэтому деятельность Менделеева быстро обросла массой слухов и легенд.
Одна из легенд гласит, что Менделеев открыл таблицу химических элементов во сне. Случай не единственный, точно также говорил о своем открытии Август Кекуле, которому приснилась формула бензольного кольца. Однако Менделеев только смеялся над критиками. “Я над ней, может быть, двадцать лет думал, а вы говорите: сидел и вдруг … готово!”, – как-то сказал ученый о своем открытии.
Другая байка приписывает Менделееву открытие водки. В 1865 году великий ученый защитил диссертацию на тему “Рассуждение о соединении спирта с водою”, и это сразу дало повод для новой легенды.
Посмеивались и над образом жизни ученого, а особенно над тем, что Менделеев оборудовал свою лабораторию в дупле огромного дуба.
Также современники подтрунивали над страстью Менделеева к чемоданам. Ученый в пору своего невольного бездействия в Симферополе вынужден был коротать время за плетением чемоданов. В дальнейшем он самостоятельно мастерил для нужд лаборатории картонные контейнеры. Несмотря на явно “любительский” характер этого увлечения, Менделеева часто называли “чемоданных дел мастером”.
Открытие радия
Одна из наиболее трагичных и в то же время известных страниц в истории химии и появления новых элементов в таблице Менделеева связана с открытием радия. Новый химический элемент был открыт супругами Марией и Пьером Кюри, которые обнаружили, что отходы, остающиеся после выделения урана из урановой руды, более радиоактивны, чем чистый уран.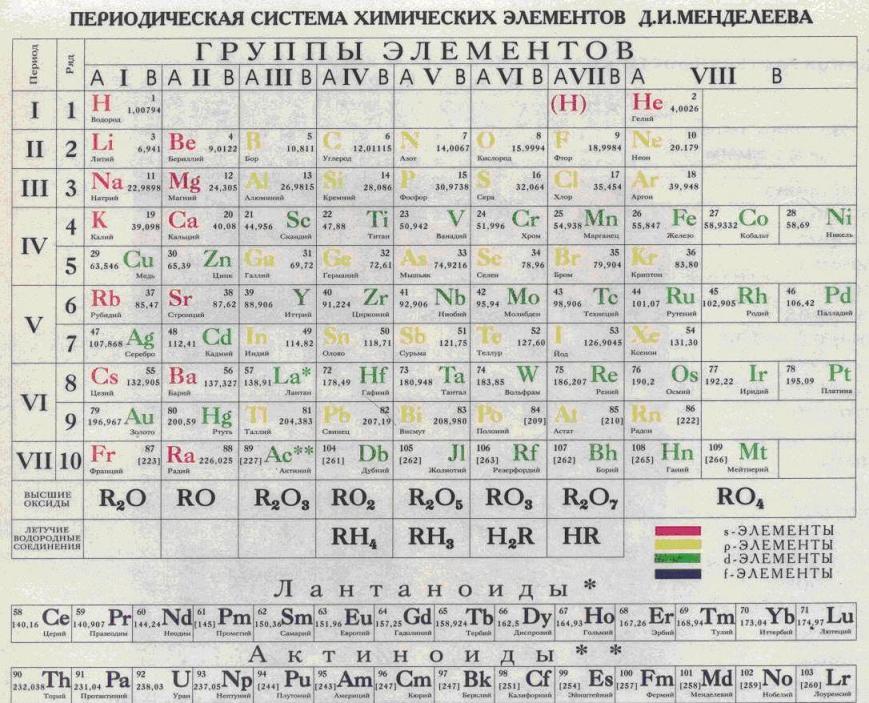
Поскольку о том, что такое радиоактивность, тогда еще никто не знал, то новому элементу молва быстро приписала целебные свойства и способность излечивать чуть ли не от всех известных науке болезней. Радий включили в состав пищевых продуктов, зубной пасты, кремов для лица. Богачи носили часы, циферблат которых был окрашен краской, содержащей радий. Радиоактивный элемент рекомендовали как средство для улучшения потенции и снятия стресса.
Подобное “производство” продолжалось целых двадцать лет – до 30-х годов двадцатого века, когда ученые открыли истинные свойства радиоактивности и выяснили насколько губительно влияние радиации на человеческий организм.
Мария Кюри умерла в 1934 году от лучевой болезни, вызванной долговременным воздействием радия на организм.
Небулий и короний
Фото: ИТАР-ТАСС
Таблица Менделеева не только упорядочила химические элементы в единую стройную систему, но и позволила предсказать многие открытия новых элементов. В то же время некоторые химические “элементы” были признаны несуществующими на основании того, что они не укладывались в концепцию периодического закона.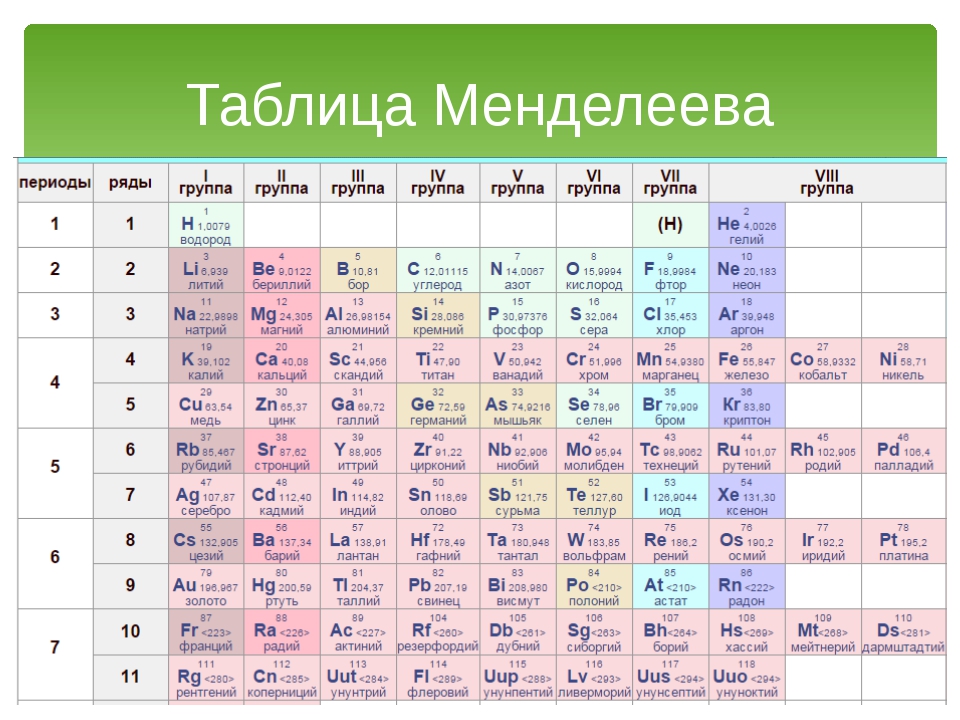 Наиболее известна история с “открытием” новых элементов небулия и корония.
Наиболее известна история с “открытием” новых элементов небулия и корония.
При исследовании солнечной атмосферы астрономы обнаружили спектральные линии, которые им не удалось отождествить ни с одним из известных на земле химических элементов. Ученые предположили, что эти линии принадлежат новому элементу, который получил название короний (потому что линии были обнаружены при исследовании “короны” Солнца – внешнего слоя атмосферы звезды).
Спустя несколько лет астрономы сделали еще одно открытие, изучая спектры газовых туманностей. Обнаруженные линии, которые снова не удалось отождествить ни с чем земным, приписали другому химическому элементу – небулию.
Открытия подверглись критике, поскольку в периодической таблице Менделеева уже не оставалось места для элементов, обладающих свойствами небулия и корония. После проверки обнаружилось, что небулий является обычным земным кислородом, а короний – сильно ионизированное железо.
Отметим, что сегодня в московском Центральном доме ученых РАН торжественно присвоят имена двум химическим элементам, открытым учеными из подмосковной Дубны.
Материал создан на основе информации из открытых источников. Подготовил Василий Макагонов @vmakagonov
Формы периодической таблицы
Наиболее распространёнными являются 3 формы таблицы Менделеева: «короткая», «длинная», «сверхдлинная».
В «короткой» форме записи четвертый и последующие периоды занимают по 2 строчки.
В «длинном» варианте лантаноиды и актиноиды вынесены из общей таблицы, делая её более компактной. В «сверхдлинном» варианте каждый период занимает одну строчку.
В качестве основного варианта IUPAC утвердил длинный вариант Периодической таблицы. Короткая форма таблицы, содержащая восемь групп элементов, официально отменена ИЮПАК еще в 1989 г.
Нильсом Бором разработана лестничная (пирамидальная) форма периодической системы.
Существует несколько сотен вариантов, редко или вовсе не используемых, но весьма оригинальных, способов графического или табличного отображения Периодического закона, при этом учёные предлагают всё новые варианты.
Познакомиться с разнообразием Периодических таблиц химических элементов, собранных со всего мира, можно на выставке, посвященной открытию Международного года Периодической таблицы, проводимой под эгидой ЮНЕСКО и Правительства Российской Федерации, при поддержке Российской Академии Наук, Московского государственного университета имени М.В. Ломоносова и Российского химико-технологического университета им. Д.И. Менделеева.
Всего предложено несколько сотен вариантов изображения периодической системы (аналитических кривых, таблиц, геометрических фигур и т. п.).
Самая большая Периодическая таблица была установлена на стенах химического факультета в Университете Мурсии в Испании. В общей сложности она занимает в общей сложности 150 м
В 2006 г. в Чикаго (США) временно была организована восьмиэтажная периодическая таблица выполненная с помощью плакатов.
Памятник Менделееву перед химическим факультетом Словацкого технологического университета в Братиславе:
В 2003 году студенты университета Уэйк Форест спроектировали стол и скамью для пикника в форме таблицы Менделеева.
На стене ВНИИ метрологии имени Д.И. Менделева в Санкт-Петербурге размещено мозаичное панно – Периодическая таблица химических элементов. В 1932 году рядом со зданием был установлен памятник великому русскому химику.
150 лет назад Дмитрий Менделеев создал свою знаменитую таблицу
150 лет назад российский ученый Дмитрий Менделеев создал Периодическую систему химических элементов. Что подтолкнуло его к открытию и к чему оно привело, рассказывает «Газета.Ru».
Поиски основы естественной классификации и систематизации химических элементов начались задолго до открытия Периодического закона. Трудности, с которыми сталкивались естествоиспытатели, которые первыми работали в этой области, были вызваны недостаточностью экспериментальных данных: в начале XIX века число известных химических элементов было мало, а принятые значения атомных масс многих элементов оказались неверны.
К середине XIX века были открыты 63 химических элемента, и попытки найти закономерности в этом наборе предпринимались неоднократно, однако их результаты не привлекали внимания научной общественности.
В 1863 году свою теорию предложил химик и музыкант Джон Александр Ньюленд, который предложил схему размещения химических элементов, схожую с той, что открыл Менделеев, но работа ученого не была принята всерьез научным сообществом из-за того, что автор увлекся поисками гармонии и связью музыки с химией.
Российского ученого Дмитрия Менделеева к созданию Периодической системы химических элементов подтолкнула работа над курсом лекций по общей химии.
В процессе работы над ним Менделеев столкнулся с трудностями, связанными с систематизацией и последовательностью изложения материала, описывающего химические элементы. На тот момент ученым уже было известно, что некоторые химические элементы имеют сходные черты, но ни одна из существовавших таблиц не охватывала все известные элементы.
Менделеев нашел связь между отдельными группами и семействами элементов, расположив все элементы в порядке возрастания атомной массы. Часами он раскладывал карточки с названиями элементов и их атомными весами, пока не обнаружил искомую закономерность.
Сам Менделеев об открытии периодического закона писал таким образом: «Заподозрив о существовании взаимосвязи между элементами еще в студенческие годы, я не уставал обдумывать эту проблему со всех сторон, собирал материалы, сравнивал и сопоставлял цифры. Наконец настало время, когда проблема созрела, когда решение, казалось, вот-вот готово было сложиться в голове. Как это всегда бывало в моей жизни, предчувствие близкого разрешения мучившего меня вопроса привело меня в возбужденное состояние. В течение нескольких недель я спал урывками, пытаясь найти тот магический принцип, который сразу привел бы в порядок всю груду накопленного за 15 лет материала.
И вот в одно прекрасное утро, проведя бессонную ночь и отчаявшись найти решение, я, не раздеваясь, прилег на диван в кабинете и заснул. И во сне мне совершенно явственно представилась таблица.
И во сне мне совершенно явственно представилась таблица.
Я тут же проснулся и набросал увиденную во сне таблицу на первом же подвернувшемся под руку клочке бумаги». Эта история позже и легла в основу легенды о том, что таблица Менделееву приснилась. Самому ученому такая интерпретация не нравилась.
«Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово», — говорил он.
13 марта 1869 года Менделеев закончил составление таблицы.
Суть открытия Менделеева заключалась в том, что с ростом атомной массы химические свойства элементов меняются не монотонно, а периодически. После определенного количества разных по свойствам элементов, свойства начинают повторяться. Так, калий похож на натрий, фтор — на хлор, а золото схоже с серебром и медью.
В 1871 году Менделеев окончательно объединил идеи в периодический закон. Ученый предсказал открытие нескольких новых химических элементов и описал их химические свойства.
Научная достоверность Периодического закона получила подтверждение очень скоро: в 1875-1886 годах были открыты галлий, скандий и германий, для которых Менделеев, пользуясь периодической системой, предсказал не только возможность их существования, но и с поразительной точностью описал целый ряд физических и химических свойств.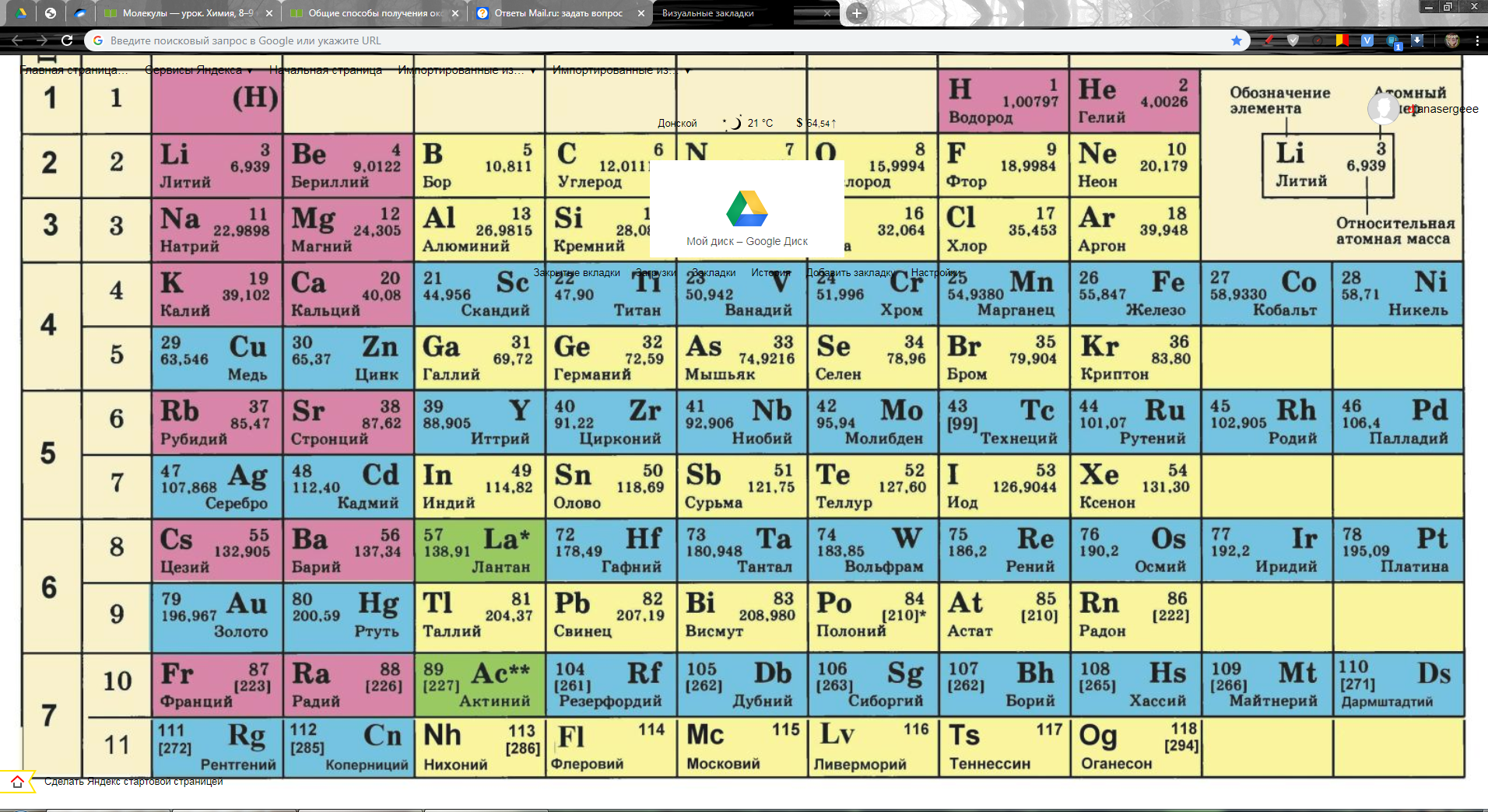
Менделеев совершенствовал таблицу несколько раз, корректируя атомные веса некоторых элементов, оставляя незаполненные клетки для новых, меняя местами группы элементов. Идеи Периодического закона определили структуру «Основ химии» и позволили систематизировать весь накопленный к этому времени материал. Труд переиздавался восемь раз и был переведен на основные европейские языки.
Один из старейших образцов таблицы недавно был найден в Великобритании, в Сент-Эндрюсском университете.
На таблицу, изготовленную в 1885 году, наткнулся во время уборки сотрудник университета, доктор Алан Айткен.
Таблица нашлась на складе университета, она лежала вместе с реактивами, оборудованием и другими лабораторными принадлежностями, скопившимися с переезда факультета химии в 1968 году. Среди вещей Айткену попался сверток плакатов для занятий, среди которых оказалась и таблица с подписями на немецком, которая от старости буквально рассыпалась в руках. Ее восстановление заняло немало времени — поверхность пришлось очистить от грязи и мусора, отделить таблицу от подкладки, на которой та была закреплена, обработать специальными растворами для выравнивания кислотно-щелочного баланса и устранить разрывы с помощью специальной бумаги из бруссонетии бумажной и пасты из пшеничного крахмала.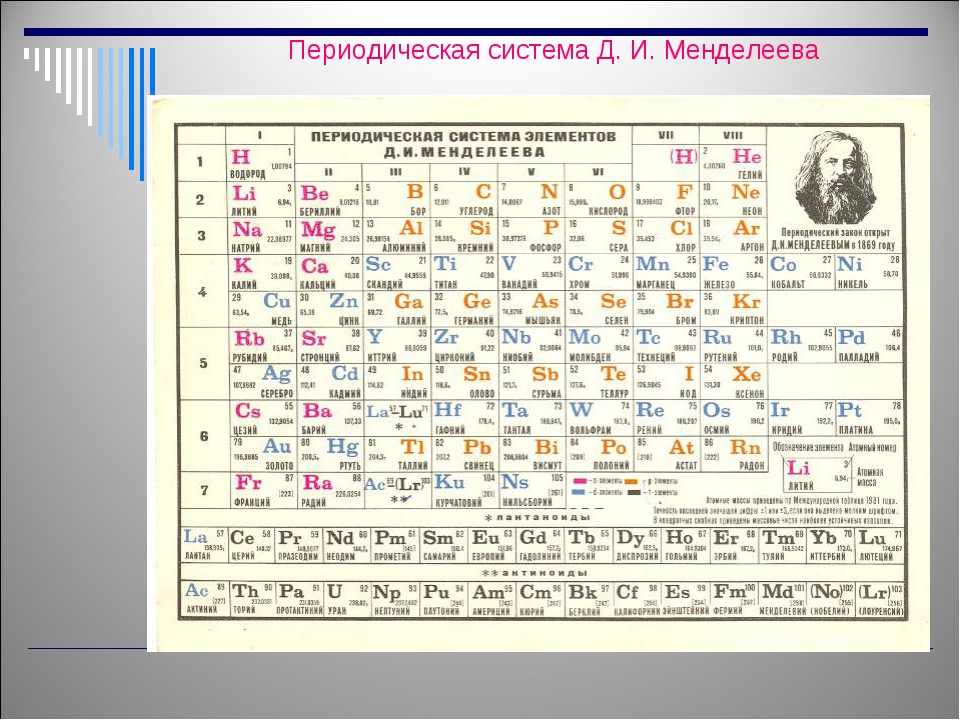
Теперь таблица будет находиться в специальном хранилище университета, где для нее будут созданы подходящие условия. На самом же факультете останется ее полномасштабная копия.
После этого сотрудники СПбГУ сообщили о новой находке — обнаруженная ими в Большой химической аудитории таблица оказалась на 9 лет старше.
По словам преподавателя СПбГУ Евгения Калинина, таблица представляет собой демонстрационный вариант, изготовленный в 1876 году. Она отличается от современных вариантов. Например, в ней нет VIII группы, в которую входят инертные газы: на момент публикации они еще не были открыты.
Периодическая система химических элементов (таблица Менделеева)
https://ria.ru/20190129/1550014194.html
Периодическая система химических элементов (таблица Менделеева)
Периодическая система химических элементов (таблица Менделеева) – РИА Новости, 29.01.2019
Периодическая система химических элементов (таблица Менделеева)
Периодическая система химических элементов – упорядоченное множество химических элементов и их естественная классификация.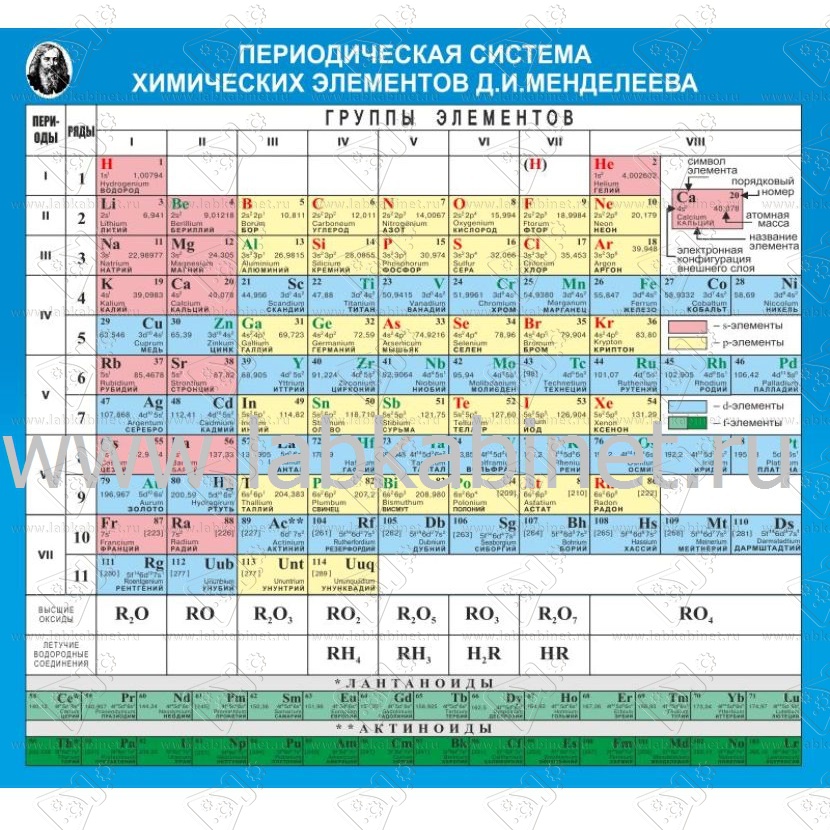 РИА Новости, 29.01.2019
РИА Новости, 29.01.2019
2019-01-29T04:51
2019-01-29T04:51
2019-01-29T04:51
справки
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdn23.img.ria.ru/images/99408/72/994087230_0:105:2000:1230_1920x0_80_0_0_b528d261d40438ab5524fc6ad7f580a3.jpg
Периодическая система химических элементов – упорядоченное множество химических элементов и их естественная классификация. Является табличным представлением периодического закона, открытого Дмитрием Менделеевым. Современная формулировка этого закона звучит так: свойства элементов находятся в периодической зависимости от заряда их атомных ядер.Прообразом Периодической системы химических элементов служит таблица “Опыт системы элементов, основанной на их атомном весе и химическом сходств”, составленная Менделеевым в 1869 году. По мере совершенствования этой таблицы он развил представления о периодах и группах элементов и о месте каждого элемента в системе. В 1871 году в книге “Основы химии” Менделеевым была включена “Естественная система элементов Д. Менделеева” – первая классическая короткая форма Периодической системы химических элементов. Современная Периодическая система химических элементов включает 118 элементов. За последние 50 лет таблица Менделеева пополнилась семнадцатью новыми элементами (102-118). Девять из них были впервые получены в российском Объединенном институте ядерных исследований в Дубне. Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали “большой гонкой”.Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры.
В 1871 году в книге “Основы химии” Менделеевым была включена “Естественная система элементов Д. Менделеева” – первая классическая короткая форма Периодической системы химических элементов. Современная Периодическая система химических элементов включает 118 элементов. За последние 50 лет таблица Менделеева пополнилась семнадцатью новыми элементами (102-118). Девять из них были впервые получены в российском Объединенном институте ядерных исследований в Дубне. Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали “большой гонкой”.Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером). Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.Номер группы элементов короткого варианта таблицы Менделеева соответствует числу валентных электронов во внешней электронной оболочке атомов. В длинном варианте таблицы номер группы в большей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы таблицы), щелочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18).
Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером). Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.Номер группы элементов короткого варианта таблицы Менделеева соответствует числу валентных электронов во внешней электронной оболочке атомов. В длинном варианте таблицы номер группы в большей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы таблицы), щелочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18). В Периодической системе химических элементов для каждого элемента указывается его символ, название, порядковый номер и значение относительной атомной массы.Первый период содержит два элемента – водород и гелий. Второй и третий периоды (литий – неон; натрий – аргон) содержат по восемь элементов. Четвертый (калий – криптон) и пятый (рубидий – ксенон) периоды содержат по 18 элементов. Шестой период (цезий – радон) содержит 32 элемента и включает особую группу элементов – лантаноиды.Седьмой период (франций – оганесон), подобно шестому, содержит 32 элемента и включает особую группу элементов – актиноиды. Лантаноиды и актиноиды помещены отдельно внизу таблицы.Периодическая система химических элементов сыграла и продолжает играть огромную роль в развитии многих естественнонаучных дисциплин. Она стала важным звеном в эволюции атомно-молекулярного учения, способствовала формулировке современного понятия “химический элемент” и уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов и возникновение понятия изотопии.
В Периодической системе химических элементов для каждого элемента указывается его символ, название, порядковый номер и значение относительной атомной массы.Первый период содержит два элемента – водород и гелий. Второй и третий периоды (литий – неон; натрий – аргон) содержат по восемь элементов. Четвертый (калий – криптон) и пятый (рубидий – ксенон) периоды содержат по 18 элементов. Шестой период (цезий – радон) содержит 32 элемента и включает особую группу элементов – лантаноиды.Седьмой период (франций – оганесон), подобно шестому, содержит 32 элемента и включает особую группу элементов – актиноиды. Лантаноиды и актиноиды помещены отдельно внизу таблицы.Периодическая система химических элементов сыграла и продолжает играть огромную роль в развитии многих естественнонаучных дисциплин. Она стала важным звеном в эволюции атомно-молекулярного учения, способствовала формулировке современного понятия “химический элемент” и уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов и возникновение понятия изотопии. С периодической системой связана строго научная постановка проблемы прогнозирования в химии, что проявилось как в предсказании существования неизвестных элементов и их свойств, так и новых особенностей химического поведения уже открытых элементов. Периодическая система – важнейшая основа неорганической химии; она служит, например, задачам синтеза веществ с заранее заданными свойствами, созданию новых материалов, подбору специфических катализаторов для различных химических процессов. Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.Материал подготовлен на основе информации РИА Новости и открытых источников
С периодической системой связана строго научная постановка проблемы прогнозирования в химии, что проявилось как в предсказании существования неизвестных элементов и их свойств, так и новых особенностей химического поведения уже открытых элементов. Периодическая система – важнейшая основа неорганической химии; она служит, например, задачам синтеза веществ с заранее заданными свойствами, созданию новых материалов, подбору специфических катализаторов для различных химических процессов. Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.Материал подготовлен на основе информации РИА Новости и открытых источников
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости
internet-group@rian. ru
ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdn23.img.ria.ru/images/99408/72/994087230_112:0:1889:1333_1920x0_80_0_0_597a34ca28aa89475eedcbd63e1a68a3.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
справки
Периодическая система химических элементов – упорядоченное множество химических элементов и их естественная классификация.
Современная Периодическая система химических элементов включает 118 элементов. За последние 50 лет таблица Менделеева пополнилась семнадцатью новыми элементами (102-118). Девять из них были впервые получены в российском Объединенном институте ядерных исследований в Дубне.
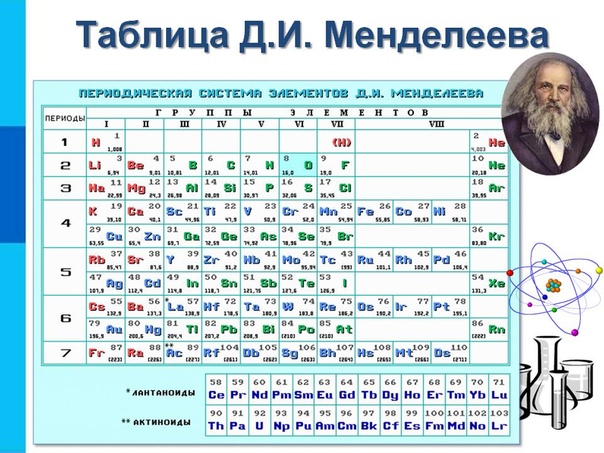 Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали “большой гонкой”.Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером).
Последнее добавление в таблицу Менделеева было сделано в 2016 году, она пополнилась четырьмя элементами с 113, 115, 117 и 118 атомными номерами, которые соответственно были названы нихоний (Nh), московий (Mc), теннессин (Ts) и оганесон (Og). Сейчас в крупнейших ядерно-физических центрах мира фактически начаты работы по синтезу 119-го, 120-го и 121-го элементов, которые назвали “большой гонкой”.Опубликовано свыше 500 вариантов Периодической системы химических элементов, что связано с попытками поиска решения некоторых частных проблем ее структуры. Наиболее распространены две табличные формы: короткая и длинная (разрабатывалась Дмитрием Менделеевым, усовершенствована в 1905 году Альфредом Вернером).Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных последовательностей элементов в соответствии с количеством валентных электронов), а короткая форма таблицы – из восьми групп.
Номер группы элементов короткого варианта таблицы Менделеева соответствует числу валентных электронов во внешней электронной оболочке атомов. В длинном варианте таблицы номер группы в большей мере формален. Группы короткого варианта включают главную (а) и побочную (б) подгруппы, в каждой из которых содержатся элементы, сходные по химическим свойствам. Элементы некоторых групп имеют собственные тривиальные названия: щелочные металлы (группа 1 длинной формы таблицы), щелочноземельные металлы (группа 2), халькогены (группа 16), галогены (группа 17), благородные газы (группа 18).
В Периодической системе химических элементов для каждого элемента указывается его символ, название, порядковый номер и значение относительной атомной массы.
Первый период содержит два элемента – водород и гелий.
Второй и третий периоды (литий – неон; натрий – аргон) содержат по восемь элементов.
Четвертый (калий – криптон) и пятый (рубидий – ксенон) периоды содержат по 18 элементов.
Шестой период (цезий – радон) содержит 32 элемента и включает особую группу элементов – лантаноиды.
Седьмой период (франций – оганесон), подобно шестому, содержит 32 элемента и включает особую группу элементов – актиноиды.
Лантаноиды и актиноиды помещены отдельно внизу таблицы.
Периодическая система химических элементов сыграла и продолжает играть огромную роль в развитии многих естественнонаучных дисциплин. Она стала важным звеном в эволюции атомно-молекулярного учения, способствовала формулировке современного понятия “химический элемент” и уточнению представлений о простых веществах и соединениях, оказала значительное влияние на разработку теории строения атомов и возникновение понятия изотопии. С периодической системой связана строго научная постановка проблемы прогнозирования в химии, что проявилось как в предсказании существования неизвестных элементов и их свойств, так и новых особенностей химического поведения уже открытых элементов. Периодическая система – важнейшая основа неорганической химии; она служит, например, задачам синтеза веществ с заранее заданными свойствами, созданию новых материалов, подбору специфических катализаторов для различных химических процессов. Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.
Периодическая система – научная база преподавания общей и неорганической химии, а также некоторых разделов атомной физики.По решению ООН 2019 год провозглашен Международным годом Периодической таблицы химических элементов.Материал подготовлен на основе информации РИА Новости и открытых источников
Таблица Менделеева: проверено временем
Этот год объявлен ЮНЕСКО Международным годом Периодической таблицы химических элементов в честь 150-летнего юбилея со дня открытия Дмитрием Ивановичем Менделеевым периодического закона, определившего дальнейшее развитие химии, физики и других наук. О том, как Периодическая таблица Менделеева помогает химикам сегодня, нам рассказали сотрудники кафедры физической химии – одной из старейших кафедр университета.
04.04.2019 3503
Первое обнародование Периодической таблицы Дмитрия Ивановича Менделеева состоялось 6 марта 1869 года на заседании Русского физико-химического общества. Множество последующих открытий и новых концепций в физике, химии и других науках опиралось на закономерности Периодической таблицы. Кафедра химии в ЛЭТИ была создана почти через три десятка лет после великого открытия Дмитрия Ивановича. Её основал в 1891 году доктор химических наук, профессор Александр Александрович Кракау. Курс «Физическая химия» ввёл основатель физико-химического анализа академик Николай Семёнович Курнаков. В разные годы здесь работали: создатель отечественной электрометаллургической промышленности проф. Максимилиан Степанович Максименко, проф. Николай Антонович Пушин, впервые получивший электролитическим способом алюминий из отечественного сырья, создатель термодинамической шкалы твёрдости профессор Борис Филиппович Ормонт, при котором кафедра была переименована в кафедру физической химии.
Множество последующих открытий и новых концепций в физике, химии и других науках опиралось на закономерности Периодической таблицы. Кафедра химии в ЛЭТИ была создана почти через три десятка лет после великого открытия Дмитрия Ивановича. Её основал в 1891 году доктор химических наук, профессор Александр Александрович Кракау. Курс «Физическая химия» ввёл основатель физико-химического анализа академик Николай Семёнович Курнаков. В разные годы здесь работали: создатель отечественной электрометаллургической промышленности проф. Максимилиан Степанович Максименко, проф. Николай Антонович Пушин, впервые получивший электролитическим способом алюминий из отечественного сырья, создатель термодинамической шкалы твёрдости профессор Борис Филиппович Ормонт, при котором кафедра была переименована в кафедру физической химии.
С приходом на заведование члена-корреспондента РАН Виктора Владимировича Гусарова кафедра после почти 80-летнего перерыва опять стала выпускающей. На ней осуществляется подготовка магистров по программе «Биосовместимые материалы» в рамках направления «Биотехнические системы и технологии», а также аспирантов по специальности «Физическая химия». Образовательную и научную деятельность осуществляют как преподаватели ЛЭТИ, так и учёные из ведущих научно-исследовательских институтов Санкт-Петербурга и Ленинградской области. Так, сотрудни- ками кафедры под руководством В.В. Гусарова в рамках совместной работы с коллективами НИТИ имени А.П. Александрова, СПб АЭП и проектно-конструкторского филиала концерна «Росэнергоатом» по разработке и обоснованию работоспособности отечественного устройства локализации расплава активной зоны ядерного реактора (ловушки расплава) был создан новый класс функциональных материалов – жертвенный материал. Он призван именно «пожертвовать собой», чтобы минимизировать последствия тяжёлых аварий на атомных станциях. Впервые в мире он был внедрён при строительстве АЭС в Китае, затем – в Индии, потом – в России.
Образовательную и научную деятельность осуществляют как преподаватели ЛЭТИ, так и учёные из ведущих научно-исследовательских институтов Санкт-Петербурга и Ленинградской области. Так, сотрудни- ками кафедры под руководством В.В. Гусарова в рамках совместной работы с коллективами НИТИ имени А.П. Александрова, СПб АЭП и проектно-конструкторского филиала концерна «Росэнергоатом» по разработке и обоснованию работоспособности отечественного устройства локализации расплава активной зоны ядерного реактора (ловушки расплава) был создан новый класс функциональных материалов – жертвенный материал. Он призван именно «пожертвовать собой», чтобы минимизировать последствия тяжёлых аварий на атомных станциях. Впервые в мире он был внедрён при строительстве АЭС в Китае, затем – в Индии, потом – в России.
На кафедре ведутся работы над созданием оксидных катализаторов (в том числе, для нужд атомной энергетики), нанокомпозиционных материалов (группа доцента А.Н. Бугрова), изучаются механизмы формирования наночастиц, свойства и области применения фуллеренов и фуллеренолов (группа профессора Н. А. Чарыкова). Об этом нам рассказала заведующая кафедрой физической химии ЛЭТИ, доктор химических наук Оксана Владимировна Альмяшева. Сама она принимала участие в разработке новых катализаторов окисления водорода для пассивной системы безопасности АЭС, позволяющих понизить вероятность образования и взрыва гремучей смеси в реакторном пространстве. В итоге разработанный научной группой химического конструирования материалов нанокомпозиционный катализатор превзошёл по ключевым параметрам более дорогие, используемые в настоящее время платино-палладиевые катализаторы.
А. Чарыкова). Об этом нам рассказала заведующая кафедрой физической химии ЛЭТИ, доктор химических наук Оксана Владимировна Альмяшева. Сама она принимала участие в разработке новых катализаторов окисления водорода для пассивной системы безопасности АЭС, позволяющих понизить вероятность образования и взрыва гремучей смеси в реакторном пространстве. В итоге разработанный научной группой химического конструирования материалов нанокомпозиционный катализатор превзошёл по ключевым параметрам более дорогие, используемые в настоящее время платино-палладиевые катализаторы.
По словам сотрудников кафедры, без использования периодического закона Д.И. Менделеева невозможно себе представить процесс конструирования новых материалов с требуемым набором свойств. Вот что рассказал начальник отдела исследований тяжёлых аварий НИТИ имени А.П. Александрова, преподаватель спецкурса для магистрантов кафедры физической химии Вячеслав Исхакович Альмяшев, принимавший непосредственное участие в разработке жертвенных материалов:
– После техногенной катастрофы на Чернобыльской АЭС стало понятно, что атомные станции помимо активных систем безопасности должны иметь такие системы, которые на уровне физико-химических процессов без участия оперативного персонала существенно понижали бы вероятность выхода радиоактивных материалов за пределы реакторного пространства, даже в случае таких серьёзных аварий, как тяжелая авария с расплавлением активной зоны. К таким системам (пассивным системам безопасности) относится и ловушка расплава, в качестве функционального наполнителя которой выступает разработанный нами жертвенный материал. Его назначение – изменить свойства поступающего в ловушку расплава таким образом, чтобы обеспечить благоприятные условия его охлаждения и кристаллизации в корпусе ловушки. Разработка любого материала начинается с выбора элементного состава, то есть с анализа Периодической системы Д.И. Менделеева. Далее осуществляется термодинамический анализ и выбор оптимальной композиции. В курсе «Физико-химическое конструирование биосовместимых материалов» я прививаю студентам навыки обоснования выбора элементного состава и структуры материалов для направленного получения совокупности свойств, требуемых для решения поставленной задачи. В иных курсах программы «Биосовместимые материалы» ребята получают опыт синтеза материалов.
К таким системам (пассивным системам безопасности) относится и ловушка расплава, в качестве функционального наполнителя которой выступает разработанный нами жертвенный материал. Его назначение – изменить свойства поступающего в ловушку расплава таким образом, чтобы обеспечить благоприятные условия его охлаждения и кристаллизации в корпусе ловушки. Разработка любого материала начинается с выбора элементного состава, то есть с анализа Периодической системы Д.И. Менделеева. Далее осуществляется термодинамический анализ и выбор оптимальной композиции. В курсе «Физико-химическое конструирование биосовместимых материалов» я прививаю студентам навыки обоснования выбора элементного состава и структуры материалов для направленного получения совокупности свойств, требуемых для решения поставленной задачи. В иных курсах программы «Биосовместимые материалы» ребята получают опыт синтеза материалов.
Сегодня происходит смена технологического уклада. Наиболее важные и заметные открытия происходят на стыке наук и опираются на использование новых материалов, конструирование которых начинается с атомного уровня. Оно немыслимо без понимания Периодической таблицы Менделеева.
Оно немыслимо без понимания Периодической таблицы Менделеева.
Лидия Березнякова
От истории химии до величайших вымыслов: вся правда о Менделееве
Как известно, в 2019 году мир отмечал 185-летие со дня рождения Д.И. Менделеева и 150-летие Периодической системы химических элементов. В честь памятных дат ведущие ученые проводили в «Сириусе» научно-популярные лекции по химии и ее истории. Подводя итоги года, мы вспоминаем самые интересные факты и вымыслы, связанные с великими открытиями.
Открытие Менделеевым таблицы химических элементов стало настоящей революцией в науке. Но история этого открытия до сих пор окутана легендами, мифами и легендами. Правда ли, что великому ученому приснился сон о том, как систематизировать знания о химических элементах? А верить ли слухам, что он торговал чемоданами в Гостином дворе в Санкт-Петербурге и придумал формулу спирта?
Развенчивает стереотипы и подтверждает догадки, а также рассказывает об истории химии – старший преподаватель кафедры радиохимии СПбГУ Евгений Калинин.
С чего начинается химия
Основа всей современной химии – наши представления об атоме. Именно на уровне атома (носителя свойств вещества) человечество может объяснить фундаментальные свойства химических элементов – электронное строение атома, масса и заряд ядра, валентность, степени окисления и многое другое.
Из школьной программы мы, конечно, помним, что:
- атом – мельчайшая частица, в состав которой входят отрицательно заряженные электроны» и «положительно заряженное» ядро. А ядро – это центр атома, который играет в его строении самую существенную роль и вокруг которого вращаются все электроны.
Но изучена ли природа мельчайшей структурной единицы досконально? Если подумать, мы в точности не знаем, как устроен атом и можем рассуждать о его строении лишь опосредованно, утверждает Евгений Калинин.
Тем не менее, история химии изучает и описывает долгий процесс накопления научных знаний, начиная с древних времен. Например, еще греческие философы были рассуждали о важных вопросах о делимости материи. Первым стал рассуждать на эту тему Левкипп, учитель Демокрита.
Первым стал рассуждать на эту тему Левкипп, учитель Демокрита.
Атомизм Левкиппа-Демокрита
Философа интересовало: можно ли каждую часть материи, которая обладает определенными свойствами, бесконечно делить на еще более мелкие части?
Например, камень, расколотый пополам или растолченный в порошок, все равно останется тем же камнем. А что, если взять каждую его крупинку и раздробить на еще меньшие частички – до какого предела можно проводить такое деление и существует ли вообще такой предел?
Левкипп пришел к выводу:
- в конечном счете это приведет к исчезновению прежних свойств и появлению новых.
Эту мысль за своим наставником стал развивать и Демокрит. Он придумал мельчайшим частицам название: «атомос», то есть «неделимые». Термин, который ввел философ, унаследовала и современная химия. Учение о том, что деление материи допустимо только до определенного предела, стало называться атомистикой, или атомистической теорией.
Таким образом, Левкипп и Демокрит обрисовали важную мысль о том, что все состоит из атомов – невидимых и неделимых сфер материи бесконечного типа и числа.
Попытка точных измерений
Тщательным экспериментальным исследованиям физических и химических явлений дал жизнь ирландский химик XVII века Роберт Бойль – автор многих фундаментальных открытий. Вы о них точно слышали:
– Бойль предпринял первые попытки точных измерений при описании изменения вещества в экспериментах по сжатию и расширению газов;
– Именно Бойль установил, что воздух под давлением ртути умеет сжиматься, правда, не бесконечно (такое свойство воздуха в 1651 году было названо упругостью). Открытая ученым обратная зависимость объема от давления получила название закона Бойля. Занимаясь изучением химических процессов, он ввел в науку понятие анализа состава тел и прославился своими взглядами на строение вещества.
Как-то охарактеризовать невидимые атомы предложил английский естествоиспытатель Джон Дальтон.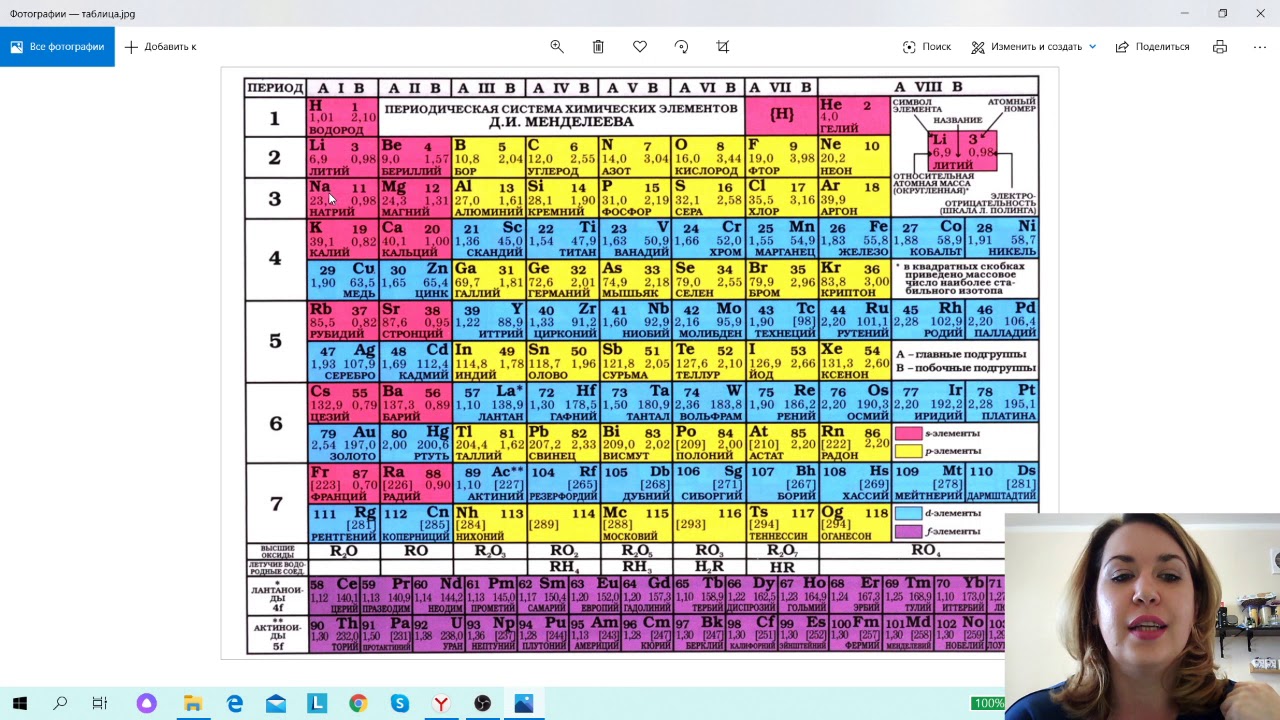 Изучая составы химических соединений, он установил:
Изучая составы химических соединений, он установил:
- Два элемента могут соединяться друг с другом в строго определенных соотношениях (соотношение малых целых чисел) и обобщил результаты своих исследований, сформулировав закон кратных отношений – важнейшее открытие в химии.
Дальтон исследовал многие распространенные бинарные соединения (гидриды и оксиды) и сгруппировал первую таблицу относительных атомных весов.
Тропинка к Менделееву
В истории развития химии важными являются и труды Йенса Якоба Берцелиуса. В попытке точно определить элементный состав различных соединений ученый провел не менее 2000 анализов и в итоге получил новую таблицу относительных атомных весов. К слову, во времена Берцелиуса было открыто уже 54 элемента.
- Метод, как их упорядочить и систематизировать, обнаружил Иоганн Деберейнер, объединивший элементы в группы. Он наблюдал за изменением их химических свойств и поведением атомного веса.
- Но впервые расположил их в порядке возрастания Джон Ньюлендс.
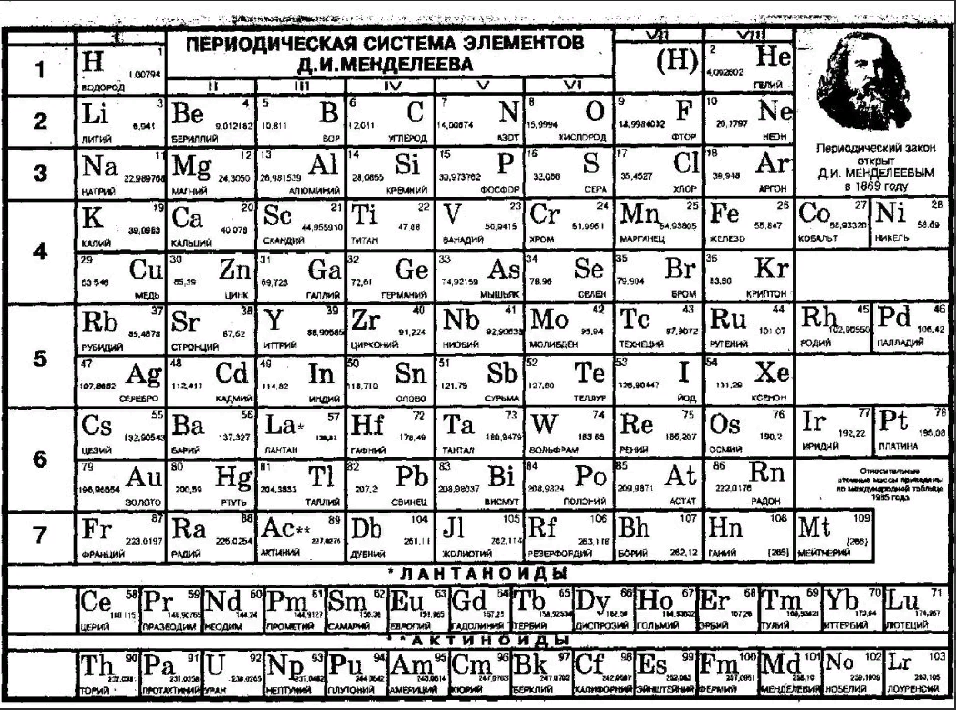 Он придумал вертикальные столбцы и вставил по семь элементов в каждый. Также ученый определил, что похожие элементы часто попадают в одни и те же горизонтальные ряды.
Он придумал вертикальные столбцы и вставил по семь элементов в каждый. Также ученый определил, что похожие элементы часто попадают в одни и те же горизонтальные ряды. - Позже немец Лотар Майер опубликовал научный труд, в котором рассматривал объемы, занимаемые весовыми количествами элемента, численно равными их атомным весам. Он первым предложил термин «периодичность».
И наконец, фундаментальный вклад в развитие науки – создание периодической системы химических элементов и формулировка Периодического закона Менделеева. К этой задаче российский ученый подошел вплотную: в 1867-1868 годах он подготовил первое издание учебника «Основы химии», где обобщал все химические свойства всех известных тогда элементов.
Спустя три года Менделеев предложил новый вариант Периодической системы, уже в известном нам виде. Особенностью этого исследования было то, что в этой системе ученый предугадал открытие новых элементов.
- По мнению Менделеева, в одном столбце должны находиться элементы с одинаковой валентностью, поэтому он решил в своей таблице оставить пустые клетки, при этом тщательно изучая динамику возрастания атомных весов.
 Потом он соотносил это с валентностями в типических соединениях и химическими свойствами элементов.
Потом он соотносил это с валентностями в типических соединениях и химическими свойствами элементов.
Интересный факт: сперва коллеги Менделеева с недоверием отнеслись к его теории о недостающих элементах, но в течение 15 лет новые элементы – галлий, скандий и германий – были открыты, их свойства в точности отвечали признакам, описанным Менделеевым. После этого сомнений в значимости Периодической системы у скептиков не осталось.
Легенды и мифы о Менделееве
Миф 1. Таблица Менделеева ученому приснилась
Историю о том, что Периодическая система элементов привиделась химику во сне, слышал чуть ли не каждый изучающий химию школьник. Эта легенда появилась благодаря товарищу Менделеева Александру Иностранцеву, русскому геологу и профессору Петербургского университета. Сам Менделеев такого не подтверждал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
Миф 2. Изобретение 40-градусной водки
Есть мнение, что Дмитрий Иванович Менделеев изобрел традиционную русскую водку. Слухи породила его революционная научная работа на тему «Рассуждение о соединении спирта с водою», и строго говоря, к алкогольному напитку эта работа имела весьма косвенное отношение – ученый в своей диссертации заложил основы гидратной теории растворов спирта с водой при различных температурах.
Слухи породила его революционная научная работа на тему «Рассуждение о соединении спирта с водою», и строго говоря, к алкогольному напитку эта работа имела весьма косвенное отношение – ученый в своей диссертации заложил основы гидратной теории растворов спирта с водой при различных температурах.
Миф 3. Чемоданных дел мастер
Еще один интересный миф говорит о том, что Менделеев изготавливал чемоданы и торговал ими в Гостином дворе в Санкт-Петербурге. Ученый действительно научился переплетному и картонажному делу еще в юности и, имея огромный архив личных и научных документов, самостоятельно переплетал их и клеил для них картонные ящики. Кроме того, он мастерски делал оригинальные рамки для фотографий. Материалы для любимого занятия Менделеев покупал в том самом петербуржском Гостином дворе.
А легенду породила одна история. Однажды, когда ученый зашел в хозяйственную лавку, он услышал за своей спиной следующий диалог:
– Кто этот почтенный господин? – спросили у лавочника.
– Неужели не знаете? – удивился тот. – Да это же известный чемоданных дел мастер Менделеев! – с уважением в голосе ответил продавец.
Так люди узнали, что Менделеев любил не только изобретать, но и заниматься «приземленными ремеслами».
Селфи на фоне Таблицы Менделеева
«Периодическая таблица – это одно из величайших достижений в науке во все времена», – заявил президент Академии наук Франции Пьер Корволь на открытии Международного года Периодической таблицы химических элементов. В Москве и в Париже дали старт длинной череде мероприятий, смысл которых очень прост – напомнить человечеству, чем оно обязано Дмитрию Менделееву, открывшему 150 лет назад Периодический закон.
«ООН намеревается таким образом донести мысль о том, как химия способна в современном мире способствовать устойчивому развитию и выдвинуть решения для вызовов планетарного масштаба в таких разных областях, как энергия, образование, сельское хозяйство или здравоохранение», – пишет портал physicsworld. com.
com.
Любопытно, что нынешний год также провозглашен Годом Леонардо в честь 500-летия со дня смерти великого флорентийца. Если иметь в виду широту научных интересов и вклад в различные области знаний, Менделеев – это и есть русский Леонардо.
Эсперанто для ученых
«Мы, ученые, высоко ценим Периодическую таблицу, потому что она представляет собой общий язык, на котором мы все говорим», – подчеркнул Нобелевский лауреат по химии 2016 г. голландец Бен Феринга. Как известно, самого Менделеева трижды выдвигали на Нобелевскую премию, но он так и не получил ее.
Первый квартал иннограда Сколково носит имя Дмитрия Менделеева. Фото: Sk.ru
В Москве на заседании комитета по проведению Международного года Периодической таблицы химических элементов глава Российской академии наук Александр Сергеев сказал: «Мы в РАН считаем, что есть три основные цели, которые страна наша должна решить в этот год. Первое, чтобы Периодическую таблицу химических элементов все стали называть таблицей Менделеева, чтобы мы получили, наконец, Нобелевскую премию в этом году, и третье – чтобы мы выиграли олимпиаду по химии в Париже», – заявил он.
«Периодическая таблица есть попытка познать природу всех вещей», – сформулировала свое отношение к открытию Менделеева генеральный секретарь ЮНЕСКО, выступая в Париже в штаб-квартире этой организации Одри Азуле. Министр науки и высшего образования РФ Михаил Котюков там же выразил мнение, что наследие Менделеева принадлежит всему человечеству. С чем участники торжественного собрания вполне согласились.
Помимо того, что Менделеев открыл Периодический закон, выходец из Тобольской губернии, 17-й сын в семье, конструировал летательные аппараты (его называют изобретателем аэростата) и занимался кораблестроением, в том числе, принимал участие в строительстве первого в мире арктического ледокола «Ермак». К числу его изобретений относят бездымный порох и нефтепровод, а на досуге ученый занимался тем, что делал чемоданы, которые сегодня назвали бы «дизайнерскими».
«Мы, ученые, высоко ценим Периодическую таблицу, потому что она представляет собой общий язык, на котором мы все говорим»
При этом сам Дмитрий Менделеев считал своей главной заслугой не Периодический закон, а введенный в России таможенный тариф, необходимость которого он сформулировал в книге «Разумный тариф». «Какой я химик, я — политэконом; что там «Основы» [химии], вот «Толковый тариф» — это другое дело», — писал он.
«Какой я химик, я — политэконом; что там «Основы» [химии], вот «Толковый тариф» — это другое дело», — писал он.
И был великий эконом
«Если говорить о широте его научных интересов, то Менделеев по большому счету был не только великим химиком, но и выдающимся экономистом, выстраивавшим тесную связь между наукой и индустрией», – считает вице-президент Фонда «Сколков» по науке и образованию Николай Суетин. – И это один из важных уроков, которые представляет для «Сколково» наследие Менделеева.
Я бы назвал его научно-экономическим гением страны. Прежде всего, он был практикующим ученым, который не сидел в башне из слоновой кости и использовал научные достижения в реальной жизни». Да и вообще был очень «приземленным» ( в лучшем смысле этого слова) человеком.
Как раз в этом и заключается смысл деятельности «Сколково». Неслучайно, первый квартал иннограда назван именем Менделеева, а фасады его зданий стилизованы под Периодическую таблицу.
Самый известный пример – когда он буквально в течение нескольких месяцев оптимизировал технологию производства керосина в Баку. «Злые языки» говорят, что это в итоге и поссорило его с семейством Нобилей, которые активно там работали, и как следствие – закрыло ему путь к Нобелевской премии.
«Злые языки» говорят, что это в итоге и поссорило его с семейством Нобилей, которые активно там работали, и как следствие – закрыло ему путь к Нобелевской премии.
Вице-президент Фонда “Сколково” по науке и образованию Николай Суетин: “Я бы назвал Менделеева научно-экономическим гением страны”. Фото: Sk.ru
Или взять введение по инициативе Менделеева таможенного тарифа. «В России все очень гордились строительством железных дорог, но при этом все железо закупали за рубежом за золото; благодаря строительству российских железных дорог в Германии металлургия получила дополнительное развитие, – напоминает вице-президент «Сколково». Благодаря введению таможенных тарифов начали развивать собственную металлургию. То же самое – с угольной промышленностью. За что ни возьмись, Менделеев всегда делал упор на связь между наукой и экономикой».
Сама история создания Периодического закона преподносит нам еще один урок, продолжает Николай Суетин: «Почему вообще появилась таблица Менделеева? В 1869 году, к тому моменту, когда Менделеев создал Периодическую таблицу, было известно только 60 элементов, причем массы ряда элементов были определены неправильно, а о существовании атома не догадывались. Не было никакой квантовой механики. Были некие вещества, которые считались фундаментальными, и из них, как полагали, состояла вся природа.
Не было никакой квантовой механики. Были некие вещества, которые считались фундаментальными, и из них, как полагали, состояла вся природа.
«Если говорить о широте его научных интересов, то Менделеев по большому счету был не только великим химиком, но и выдающимся экономистом, выстраивавшим тесную связь между наукой и индустрией»
Менделеев сформулировал свой закон, когда писал учебник «Основы химии». Он обнаружил, что если элементы выстроить по увеличению их веса, то возникает некая периодичность, которую можно представить в виде таблицы с заполненными и пустующими клетками. В ней по горизонтали выстроены элементы по возрастанию их массы, а по вертикали – с одинаковыми химическими свойствами. Были какие-то элементы, масса которых не соответствовала закономерности, в следствие чего ее впоследствии скорректировали. И были дырки, где элементов не было, но было ясно, что они должны там быть, и эти элементы потом нашли. В том числе, три – еще при жизни самого Менделеева. Т.е.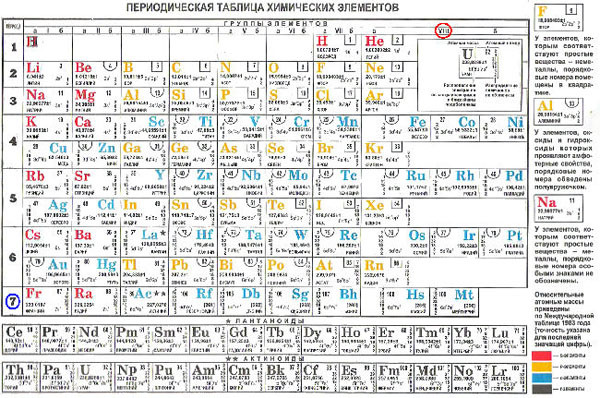 многие элементы были открыты потому, что они были предсказаны Таблицей Менделеева, и их искали целенаправленно, хотя в природе они встречаются редко.
многие элементы были открыты потому, что они были предсказаны Таблицей Менделеева, и их искали целенаправленно, хотя в природе они встречаются редко.
Вот так написание учебника, т.е. образовательная деятельность, дала выдающийся научный результат. Соединение науки и образования всегда важно, и это один из главных уроков, которые дает нам Менделеев», – считает Н.Суетин.
Сегодня в Таблице Менделеева почти в два раза больше элементов, чем 150 лет назад. Фото: Sk.ru
Судьба некоторых изобретений Менделеева тоже представляет собой определенный урок для дня сегодняшнего. Состав и метод производства бездымного пороха, разработанный Менделеевым, был запатентован не в России, а в Америке, вследствие чего Россия закупала «менделеевский порох» из-за океана. Что еще раз подчеркивает важность международной защиты, создаваемой интеллектуальной собственности.
В юбилейный год не принято вспоминать о проблемах, но Дмитрий Менделеев не был принят в Императорскую академию наук, хотя был членом множества зарубежных. Более того, когда из-за нарушения властями академических свобод ученый покинул петербургский университет, коллеги не стали его удерживать, хотя студенты и выходили на акции протеста.
Более того, когда из-за нарушения властями академических свобод ученый покинул петербургский университет, коллеги не стали его удерживать, хотя студенты и выходили на акции протеста.
«Есть такая беда: во все времена в стране было что-то неладное с признанием собственных гениев, – говорит Николай Суетин. – «Нет пророка в своем отечестве»: на Нобелевскую премию Менделеева выдвигали иностранцы, а члены Императорской академии наук при тайном голосовании неоднократно отвергали его кандидатуру. Хотя к Менделееву с очень большим уважением относились промышленники, и предприниматели, да и многие члены правительства, министры».
Тусовка длиною в год
По прошествии 150 лет Менделееву с лихвой воздают должное и на Родине, и далеко за ее пределами.
«Периодическая таблица есть попытка познать природу всех вещей»
Портал physicsworld.com в репортаже из штаб-квартиры ЮНЕСКО обращает внимание на то, что старт международного года в ЮНЕСКО был обставлен как веселая тусовка. В зале звучали музыкальные интерлюдии в исполнении знаменитой пианистки Миры Евтич. В кулуарах посетители толпились в молекулярном баре, выстраиваясь в очередь за мороженым, приготовленным с помощью жидкого азота. Можно было даже сделать селфи в интерьерах воссозданного для этой цели в Париже кабинета Менделеева.
В зале звучали музыкальные интерлюдии в исполнении знаменитой пианистки Миры Евтич. В кулуарах посетители толпились в молекулярном баре, выстраиваясь в очередь за мороженым, приготовленным с помощью жидкого азота. Можно было даже сделать селфи в интерьерах воссозданного для этой цели в Париже кабинета Менделеева.
Месседж вполне прозрачен: перефразируя Пушкина, быть можно важным в науке человеком и при этом делать селфи с Менделеевым. И, конечно, это нетривиальный способ популяризации науки.
Фото: Sk.ru.
В России наука также нуждается в творческой популяризации, и «Сколтех, как никто другой, сейчас выполняет эту роль», – считает вице-президент Фонда «Сколково» по науке и образованию. Именно здесь выпустили первый сборник комиксов, основанных на реальных научных исследованиях российских ученых. Научно-просветительский проект Сколтеха «Это точно. Чертова дюжина комиксов о науке и ученых» отмечен дипломом в специальной номинации «Прорыв года» V Всероссийской премии «За верность науке».
«Сколтех проникся идеей, что науку надо популяризировать, – утверждает Николай Суетин. – Благодаря академику Александру Кулешову профессора активно участвуют в «Сириусах», других научно-популярных мероприятиях для детей. На мой взгляд, лучший популяризатор науки в России сейчас – профессор Сколтеха Константин Северинов: никто лучше него не рассказывает о том, что такое генетика, редактирование генома».
В этом смысле стартовавший в феврале Международный год Периодической таблицы химических элементов дает хороший шанс для популяризации наследия Менделеева, о котором миллениалы знают по преимуществу то единственное, чего он никогда не делал: да, Менделеев не изобретал водку.
Периодическая таблица Дмитрия Менделеева – история
Энн Э. Робинсон
Организация Объединенных Наций объявила 2019 год Международным годом Периодической таблицы Менделеева в честь 150-летия открытия Периодического закона.
В начале 1869 года русский химик Дмитрий Менделеев находился в затруднительном положении, с которым многие люди знакомы: у него был крайний срок. Он передал издателю первый том своего учебника неорганической химии, но не мог решить, как организовать второй том.
Он передал издателю первый том своего учебника неорганической химии, но не мог решить, как организовать второй том.
Эта борьба завершится замечательным открытием – системой, которая классифицирует все химические элементы. В марте 1869 года Менделеев представил Русскому химическому обществу полный доклад, в котором излагался наиболее важный аспект его системы: характеристики элементов периодически повторяются в зависимости от их атомного веса. Это была первая итерация периодического закона.
Российский химик и педагог Дмитрий Менделеев сегодня наиболее известен своим созданием периодической таблицы элементов.
Менделеев был далеко не первым химиком, который попытался организовать элементы по атомному весу или признать, что характеристики повторялись на некоторой регулярной основе. На протяжении большей части девятнадцатого века химики работали, чтобы найти организационный принцип, который охватил бы все известные элементы и который можно было бы рассматривать как закон природы.
Система Менделеева не была совершенной, но в ней были признаки научного закона, который будет действовать через новые открытия и вопреки всем вызовам.
Одним из уникальных аспектов таблицы Менделеева были оставленные им пробелы. В этих местах он не только предсказал наличие еще неоткрытых элементов, но и предсказал их атомный вес и их характеристики. Открытие новых элементов в 1870-х годах, которые подтвердили некоторые из его предсказаний, повысило интерес к периодической системе, и она стала не только объектом изучения, но и инструментом исследования.
Сэр Уильям Рамзи, который в 1890-х годах открыл существование благородных газов, ранее не предсказанного набора элементов.
В 1890-х годах Уильям Рамзи открыл совершенно новый и непредсказуемый набор элементов – благородные газы. После открытия первых двух, аргона и гелия, он быстро обнаружил еще три элемента после использования периодической системы для предсказания их атомного веса. Благородные газы обладали необычными характеристиками – они были в значительной степени инертными и устойчивыми к соединению с другими веществами, – но весь набор легко вписывался в систему.
Благородные газы обладали необычными характеристиками – они были в значительной степени инертными и устойчивыми к соединению с другими веществами, – но весь набор легко вписывался в систему.
Открытие радиоактивности в 1896 году казалось готовым разрушить периодическую систему.Химики всегда считали элементы веществами, которые не могут распадаться на более мелкие части. Как радиоактивные элементы, распавшиеся на другие вещества, могут считаться элементами? А если да, то как такое количество могло бы уместиться в очень немногих пробелах в таблице?
Химики и физики, работая вместе, начали понимать структуру атома и вскоре смогли объяснить, как периодическая система работает на атомном уровне.
Открытие радиоактивности в 1896 году создало значительные проблемы для периодической системы.
Вместо атомного веса, атомный номер – количество протонов в ядре атома – определяет характеристики элемента. Каким-то чудом организация элементов по их атомным номерам, а не по их атомному весу не изменила структуру периодической таблицы. Фактически, понимание того, как электроны заполняют оболочки, вращающиеся вокруг ядра, объяснило некоторые аномалии, которые преследовали периодическую систему с самого начала.
Фактически, понимание того, как электроны заполняют оболочки, вращающиеся вокруг ядра, объяснило некоторые аномалии, которые преследовали периодическую систему с самого начала.
Периодическая таблица – визуальное представление периодического закона – признана одним из величайших достижений химии и объединяющей научной концепцией, имеющей отношение как к физическим наукам, так и наукам о жизни.
Но таблица Менделеева также является важным аспектом естественнонаучного образования.
Периодической таблице элементов потребовалось время, чтобы развиться в ее нынешнюю форму, и многие из ее ранних итераций, такие как эта, названная «Цветок Менделеева», сегодня были бы неузнаваемыми.
Менделеев и многие другие, кто разработал системы для организации элементов, сделали это в своей роли преподавателей химии, а не исследователей химии.Он писал учебник для своих студентов в Санкт-Петербургском университете (единственными доступными учебниками химии на русском языке были переводы), когда он разработал свой периодический закон. Возможно, самое главное, он продолжал рисовать исправленные версии таблицы Менделеева на протяжении всей своей жизни.
Возможно, самое главное, он продолжал рисовать исправленные версии таблицы Менделеева на протяжении всей своей жизни.
Ни первая попытка Менделеева построить периодическую систему, ни его самая популярная таблица 1870 года не очень похожа на таблицу Менделеева, которая сегодня висит на стене большинства кабинетов химии или появляется на обложках большинства учебников химии.Итак, существует, вероятно, 1000 различных периодических таблиц элементов.
Ранняя периодическая система Менделеева, показанная здесь в форме 1871 года, сильно отличалась от современной периодической таблицы, известной сегодняшним студентам-химикам.
Большинство этих столов выглядят фантастически по сравнению с замковыми столами, которые можно найти в классных комнатах. Изогнутые формы, такие как спирали, спирали и трехмерные восьмерки, были очень популярны среди педагогов еще в двадцатом веке.Обычно считалось, что студентам легче использовать их для изучения элементов и взаимосвязей между ними, чем плоскую двухмерную таблицу.
Особенность плоского двухмерного стола в том, что он легко умещается на одной странице или как плакат, висящий на стене. Не требует специальных раскладок или печати. Его можно легко уменьшить или расширить, чтобы при необходимости уместить его в тексте. И среди всех кривых было много таблиц.
На фотографии химического клуба Wilson College в Чемберсберге, штат Пенсильвания, около 1937 года, на заднем плане виден образец периодической таблицы компании Van Nostrand (фото любезно предоставлено сайтом ScienceHistory.org.)
Так почему именно эта таблица? Откуда это?
Было так много похожих таблиц, что в некотором смысле они просто эволюционировали с течением времени. Но химики часто указывают на таблицу, созданную Хорасом Дж. Демингом, профессором Университета Небраски, как на прародителя.Таблица Деминга впервые появилась в его учебнике Общая химия 1923 года и немного изменялась в каждом издании, пока не появилась последняя в 1952 году.
Периодическая таблица Деминга 1923 года; Химики часто считают Горация Деминга, профессора Университета Небраски, родоначальником современной таблицы Менделеева.
Преподаватели химии хвалили таблицу Деминга, но компании-поставщики научных товаров прославили ее. Merck раздал его в рамках рекламной кампании в 1920-х годах.Компания Welch Scientific продавала его в виде настенных диаграмм, а также в версиях со стандартным размером страницы и в карманных версиях.
Со временем он был включен в стандартные справочники, такие как CRC Handbook of Chemistry and Physics и Lange’s Handbook of Chemistry . К 1950-м годам версии таблицы Деминга можно было найти в большинстве учебников химии.
Сегодня изображения стола можно найти практически на любом типе потребительских товаров: на занавесках для душа, кофейных кружках, брелках, чехлах для телефонов и т. Д. Список можно продолжить.
Современная таблица Менделеева: известные, любимые и опасные для сегодняшних студентов-химиков.
История таблицы Менделеева во многом связана с учебниками, вещами, которым обычно не уделяется должного внимания. Но учтите, что Менделеев сделал себе имя в российском химическом сообществе, написав учебник (его учебник органической химии получил приз), а затем прославился, открыв закон в процессе написания другого учебника.И таблица Менделеева, которую мы видим в учебниках и в классах, берет свое начало в учебниках.
По крайней мере, история с периодическим законом должна заставить вас переосмыслить свое мнение об учебниках и их авторах. И, возможно, также следует помнить о креативности и новаторстве, которые могут возникнуть в сжатые сроки.
6.2: Периодическая таблица Менделеева – Химия LibreTexts
Один из полезных способов подготовиться к тесту – использовать карточки. Чтобы составить их, запишите словарный запас, термины на иностранном языке, математические формулы, химические реакции – все, что вы хотите выучить.Затем отсортируйте эти карточки по категориям и темам, которые подходят друг другу. Такая организация информации помогает вам увидеть закономерности в материале, чтобы вы могли связать вместе разные идеи и лучше понять их. Периодическая таблица Менделеева была впервые построена с использованием набора карточек. С помощью этой стратегии Дмитрий Менделеев, создатель таблицы Менделеева, мог систематизировать и переупорядочивать материал до тех пор, пока не возникнут закономерности.
Периодическая таблица Менделеева
В 1869 году русский химик и педагог Дмитрий Менделеев (1836–1907) опубликовал периодическую таблицу элементов.В следующем году немецкий химик Лотар Мейер независимо опубликовал очень похожую таблицу. Менделееву обычно уделяют больше внимания, чем Мейеру, потому что его таблица была опубликована первой, а также из-за нескольких ключевых идей, которые он сделал относительно таблицы.
Дмитрий Менделеев.
Менделеев писал учебник химии для своих учеников и хотел систематизировать все известные в то время элементы в соответствии с их химическими свойствами. Он классно организовал информацию для каждого элемента на отдельные карточки для заметок, которые затем можно было легко переставить по мере необходимости.Он обнаружил, что, когда он расположил их в порядке возрастания атомной массы, определенные сходства в химическом поведении повторялись через равные промежутки времени. Такой тип повторяющегося узора называется «периодическим». Маятник, который качается вперед и назад в заданный промежуток времени, является периодическим, как и движение Луны вокруг Земли.
Периодическая таблица Менделеева 1869 года.
На рисунке выше атомная масса увеличивается сверху вниз по вертикальным столбцам, а следующие друг за другом столбцы идут слева направо.В результате элементы, находящиеся в одном горизонтальном ряду, представляют собой группы элементов, которые, как известно, обладают схожими химическими свойствами. Одно из открытий Менделеева иллюстрируется элементами теллура \ (\ left (\ ce {Te} \ right) \) и йода \ (\ left (\ ce {I} \ right) \). Обратите внимание, что теллур указан перед йодом, хотя его атомная масса выше. Менделеев поменял порядок, потому что он знал, что свойства йода намного больше похожи на свойства фтора \ (\ left (\ ce {F} \ right) \), хлора \ (\ left (\ ce {Cl} \ right) \) и бром \ (\ left (\ ce {Br} \ right) \), чем они были для кислорода \ (\ left (\ ce {O} \ right) \), серы \ (\ left (\ ce { S} \ right) \) и селен \ (\ left (\ ce {Se} \ right) \).Он просто предположил, что произошла ошибка в определении одной или обеих атомных масс. Оказалось, что это не так, но Менделеев действительно правильно сгруппировал эти два элемента.
Обратите внимание, что в таблице есть несколько мест, которые не имеют химического символа, но вместо этого помечены вопросительным знаком. Между цинком \ (\ left ({Zn} \ right) \) и мышьяком \ (\ left (\ ce {As} \ right) \) два таких недостающих элемента. Менделеев считал, что элементы с атомными массами 68 и 70 в конечном итоге будут открыты и что они будут химически вписываться в каждое из этих пространств.В таблице ниже перечислены другие свойства, которые Менделеев предсказал для первого из этих двух недостающих элементов, которые он назвал «эка-алюминий», по сравнению с элементом галлием.
| Eka-Aluminium \ (\ left (\ ce {Ea} \ right) \) | Галлий \ (\ left (\ ce {Ga} \ right) \) | |
| Атомная масса | \ (68 \: \ text {amu} \) | \ (69.3 \) |
| Формула оксида | \ (\ ce {Ea_2O_3} \) | \ (\ ce {Ga_2O_3} \) |
Элемент галлий был открыт через четыре года после публикации таблицы Менделеева, и его свойства удивительно совпадали с эка-алюминием, вписываясь в таблицу именно там, где он предсказывал. То же самое было и с элементом, который последовал за галлием, который в конечном итоге был назван германием.
Периодическая таблица Менделеева получила широкое признание в научном сообществе и принесла ему признание как первооткрыватель периодического закона.Элемент номер 101, синтезированный в 1955 году, назван mendelevium в честь основателя периодической таблицы Менделеева. Однако прошло несколько лет после смерти Менделеева, прежде чем удалось объяснить несколько расхождений с атомными массами и до того, как можно было полностью объяснить причины повторения химических свойств.
Сводка
- Менделеев опубликовал свою периодическую таблицу в 1869 году.
- Его организация элементов была основана на атомной массе. Периодическая таблица
- Менделеева позволяла предсказывать свойства элементов, которые еще не были обнаружены.
Авторы и указание авторства
Фонд CK-12 Шэрон Бьюик, Ричард Парсонс, Тереза Форсайт, Шонна Робинсон и Жан Дюпон.
Дмитрий Менделеев | Изобретатель периодической таблицы элементов
8 февраля 1834 г. – 2 февраля 1907 г.
Дмитрий Менделеев придумал предсказательную версию периодической таблицы элементов
Дмитрий Менделеев придумал предсказательную версию периодической таблицы элементов
РИА Новости / Science Photo Library
17 февраля 1869 года русский химик Дмитрий Менделеев записал символы химических элементов, упорядочив их в соответствии с их атомным весом и изобрел периодическую таблицу.Он записал последовательность таким образом, чтобы они сгруппировались на странице в соответствии с известными закономерностями или «периодичностями» поведения. Возможно, это был величайший прорыв в истории химии.
Идеи Менделеева, основанные на более ранних работах французского химика Антуана Лавуазье в предыдущем столетии, полностью изменили взгляды химиков на свою дисциплину. Теперь каждый химический элемент имел свой номер и фиксированное положение в таблице, и, исходя из этого, стало возможным предсказать его поведение: как он будет реагировать с другими элементами, какие соединения он будет образовывать и какие физические свойства он будет иметь. .
Вскоре Менделеев предсказал свойства трех элементов – галлия, скандия и германия, – которые тогда еще не были открыты. Он был настолько убежден в правильности своего периодического закона, что оставил пробелы для этих элементов в своей таблице. В течение двадцати лет все трое были найдены, и их свойства почти точно подтвердили его предсказания.
Сам Менделеев был удивлен тем, насколько быстро его идеи подтвердились. В престижной лекции Фарадея в Королевском институте в Лондоне в 1889 году он признал, что не ожидал, что проживет достаточно долго, чтобы «сообщить об их открытии Химическому обществу Великобритании как подтверждение точности и универсальности периодического закона». .Когда стало распространяться известие о его выдающихся достижениях, Менделеев стал чем-то вроде героя, и интерес к таблице Менделеева резко возрос.
Всего Менделеев предсказал 10 новых элементов, из которых все, кроме двух, оказались существующими. Позже он предложил поменять местами некоторые пары соседних элементов, чтобы их свойства вписывались в периодический узор. Он предложил заменить кобальт на никель и аргон на калий, который, по его мнению, был размещен неправильно, потому что их истинный атомный вес отличался от значений, определенных химиками.Потребовалось до 1913 года, примерно через шесть лет после смерти Менделеева, чтобы прояснить эту двусмысленность. К тому времени химики получили гораздо лучшее понимание атома, и в том же году физик Генри Мозли, работавший в Манчестере, показал, что положение элемента в таблице определяется не его атомным весом, а его атомным номером. Деннис Руврей
150 лет назад периодическая таблица Менделеева началась с видения одного химика
У каждой области науки есть любимый юбилей.
Что касается физики, то это « Начала » Ньютона 1687 года, книга, которая ввела законы движения и гравитации. Биология празднует книгу Дарвина «О происхождении видов» (1859 г.) вместе с его днем рождения (1809 г.). Поклонники астрономии отмечают 1543 год, когда Коперник поместил Солнце в центр Солнечной системы.
Что касается химии, то ни один повод для торжества не превосходит происхождение периодической таблицы элементов, созданной 150 лет назад в марте этого года русским химиком Дмитрием Ивановичем Менделеевым.
Таблица Менделеева стала так же знакома студентам-химикам, как электронные таблицы – бухгалтерам. Он суммирует всю науку в примерно 100 квадратах, содержащих символы и числа. Он перечисляет элементы, из которых состоят все земные субстанции, расположенные таким образом, чтобы выявить закономерности в их свойствах, что определяет направление химических исследований как в теории, так и на практике.
Подпишитесь на последние новости
Science NewsЗаголовки и резюме последних научных новостей статей, доставленных на ваш почтовый ящик
«Периодическая таблица Менделеева, – писал химик Питер Аткинс, – возможно, является наиболее важным понятием в химии.”
Таблица Менделеева выглядела как специальная диаграмма, но он хотел, чтобы таблица выражала глубокую научную истину, которую он открыл: периодический закон. Его закон выявил глубокие семейные отношения между известными химическими элементами – они проявляли сходные свойства через равные промежутки времени (или периоды), когда они располагались в порядке их атомного веса – и позволил Менделееву предсказать существование элементов, которые еще не были обнаружены.
«До обнародования этого закона химические элементы были всего лишь отрывочными, случайными фактами в Природе», – заявил Менделеев.«Закон периодичности впервые позволил нам воспринимать неоткрытые элементы на расстоянии, которое раньше было недоступно для химического зрения».
Таблица Менделеева не только предсказывала существование новых элементов. Это подтвердило тогдашнюю спорную веру в реальность атомов. Он намекнул на существование субатомной структуры и предвосхитил математический аппарат, лежащий в основе правил, управляющих материей, которые в конечном итоге проявились в квантовой теории. Его таблица завершила трансформацию химической науки из средневекового магического мистицизма алхимии в область современной научной строгости.Таблица Менделеева символизирует не только составные части материи, но и логическую убедительность и принципиальную рациональность всей науки.
Заложить основу
Легенда гласит, что Менделеев задумал и создал свою таблицу за один день: 17 февраля 1869 года по русскому календарю (1 марта в большинстве стран мира). Но это, наверное, преувеличение. Менделеев думал о группировке элементов в течение многих лет, а другие химики несколько раз рассматривали понятие взаимосвязи между элементами в предыдущие десятилетия.
На самом деле немецкий химик Иоганн Вольфганг Доберейнер заметил особенности в группировке элементов еще в 1817 году. В те дни химики еще не полностью осознали природу атомов, как описано в атомной теории, предложенной английским школьным учителем Джоном Дальтоном в 1808 году. В своей книге «Новая система химической философии » Дальтон объяснил химические реакции, предположив, что каждое элементарное вещество состоит из определенного типа атома.
Химические реакции, предположил Дальтон, дают новые вещества, когда атомы разъединяются или соединяются.Он рассуждал, что любой данный элемент целиком состоит из одного вида атомов, отличающегося от других по весу. Атомы кислорода весили в восемь раз больше, чем атомы водорода; По мнению Дальтона, атомы углерода в шесть раз тяжелее водорода. Когда элементы объединяются, чтобы образовать новые вещества, количество, которое прореагировало, можно рассчитать, зная эти атомные веса.
Дальтон ошибался насчет некоторых весов – кислород действительно в 16 раз тяжелее водорода, а углерод в 12 раз тяжелее водорода.Но его теория сделала идею атомов полезной, что привело к революции в химии. Точное измерение атомного веса стало главной заботой химиков в последующие десятилетия.
Размышляя об этих весах, Доберейнер заметил, что определенные наборы из трех элементов (он назвал их триадами) обнаруживают своеобразную взаимосвязь. Бром, например, имел атомный вес посередине между весами хлора и йода, и все три элемента демонстрировали сходное химическое поведение.Литий, натрий и калий тоже были триадой.
Другие химики заметили связь между атомным весом и химическими свойствами, но только в 1860-х годах атомные веса были достаточно хорошо изучены и измерены для более глубокого понимания. В Англии химик Джон Ньюлендс заметил, что расположение известных элементов в порядке возрастания атомного веса приводит к повторению химических свойств каждого восьмого элемента – закономерность, которую он назвал «законом октав» в статье 1865 года.Но паттерн Ньюлендса не очень хорошо держался после первых двух октав, что побудило критика предположить, что ему следует вместо этого попытаться расположить элементы в алфавитном порядке. Очевидно, что соотношение свойств элементов и атомных весов было немного сложнее, как вскоре понял Менделеев.
Организация элементов
Менделеев родился в 1834 году в Тобольске (Сибирь) (17-й ребенок его родителей). Он жил разобщенной жизнью, преследуя множество интересов и путешествуя по запутанному пути к известности.Во время учебы в педагогическом институте в Санкт-Петербурге он чуть не умер от тяжелой болезни. После окончания школы он преподавал в средних школах (требование его стипендии в педагогическом институте) и, преподавая математику и естественные науки, проводил исследования для получения степени магистра.
Затем он работал наставником и лектором (наряду с некоторыми научно-популярными работами), пока не получил стипендию для продолжительной поездки по исследованиям в самых известных университетских химических лабораториях Европы.
Когда он вернулся в Санкт-Петербург, у него не было работы, поэтому он написал мастерское руководство по органической химии в надежде выиграть крупный денежный приз. Долгая попытка окупилась благодаря прибыльной Демидовской премии 1862 года. Он также нашел работу редактором, переводчиком и консультантом в различных отраслях химической промышленности. В конце концов он вернулся к исследованиям, получив докторскую степень. в 1865 г., а затем стал профессором Петербургского университета.
Вскоре после этого Менделеев начал преподавать неорганическую химию.Готовясь освоить эту новую (для него) область, он не был впечатлен имеющимися учебниками. Поэтому он решил написать свое собственное. Организация текста требовала систематизации элементов, поэтому он думал, как лучше их расположить.
К началу 1869 года Менделеев добился достаточного прогресса, чтобы понять, что некоторые группы подобных элементов показывают регулярное увеличение атомного веса; другие элементы с примерно равным атомным весом обладали общими свойствами. Оказалось, что упорядочение элементов по их атомному весу было ключом к их классификации.
По словам самого Менделеева, он структурировал свое мышление, записав свойства каждого из 63 известных элементов на отдельной карточке. Затем, с помощью своего рода игры в химический пасьянс, он нашел искомый паттерн. Располагая карточки в вертикальных столбцах от меньшего атомного веса к большему, в каждый горизонтальный ряд помещались элементы с аналогичными свойствами. Так родилась таблица Менделеева. 1 марта он набросал свою таблицу, отправил ее в типографию и включил в свой учебник, который скоро будет издан.Он быстро подготовил доклад для представления в Русское химическое общество.
«Элементы, расположенные в соответствии с размером их атомного веса, демонстрируют явные периодические свойства», – заявил Менделеев в своей статье. «Все сравнения, которые я сделал… привели меня к выводу, что размер атомной массы определяет природу элементов».
Тем временем немецкий химик Лотар Мейер также работал над организацией элементов. Он приготовил стол, похожий на стол Менделеева, возможно, даже раньше Менделеева.Но Менделеев опубликовал первым.
Однако важнее, чем победить Мейера в публикации, было то, что Менделеев использовал свою таблицу для смелых прогнозов относительно неоткрытых элементов. Готовя свой стол, Менделеев заметил, что пропало несколько карточек. Ему пришлось оставить пустые места, чтобы известные элементы правильно выровнялись. При его жизни три из этих пробелов были заполнены ранее неизвестными элементами галлием, скандием и германием.
Менделеев не только предсказал существование этих элементов, но и правильно подробно описал их свойства.Галлий, например, открытый в 1875 году, имел атомный вес (измеренный тогда) 69,9 и плотность в шесть раз больше плотности воды. Менделеев предсказал элемент (он назвал его эка-алюминий) именно с такой плотностью и атомным весом 68. Его предсказания для эка-кремния близко соответствовали германию (открытому в 1886 году) по атомному весу (72 предсказано, 72,3 наблюдаемых) и плотности. (5,5 против 5,469). Он также правильно предсказал плотность соединений германия с кислородом и хлором.
Стол Менделеева стал оракулом.Это было так, как если бы плитки Эрудита в конце игры раскрывали секреты вселенной. В то время как другие увидели силу периодического закона, Менделеев был мастером в использовании его.
Успешные предсказания Менделеева принесли ему легендарный статус маэстро химического волшебства. Но сегодня историки спорят, укрепило ли открытие предсказанных элементов принятие его периодического закона. Одобрение закона могло быть больше связано с его способностью объяснять установившиеся химические взаимосвязи.В любом случае точность прогнозов Менделеева, безусловно, привлекла внимание к достоинствам его таблицы.
К 1890-м годам химики широко признали его закон вехой в химических знаниях. В 1900 году будущий лауреат Нобелевской премии по химии Уильям Рамзи назвал это «величайшим обобщением, которое до сих пор было сделано в химии». И Менделеев сделал это, даже не понимая, почему это вообще работает.
Математическая карта
Во многих случаях в истории науки великие предсказания, основанные на новых уравнениях, оказывались верными.Каким-то образом математика открывает некоторые секреты природы до того, как их обнаруживают экспериментаторы. Антивещество – один пример, расширение Вселенной – другой. В случае Менделеева предсказания новых элементов возникали без какой-либо творческой математики. Но на самом деле Менделеев открыл глубокую математическую карту природы, поскольку его таблица отражала последствия квантовой механики, математических правил, управляющих атомной архитектурой.
В своем учебнике Менделеев отмечал, что «внутренние различия вещества, из которого состоят атомы», могут быть ответственны за периодически повторяющиеся свойства элементов.Но он не придерживался этой линии мысли. Фактически, на протяжении многих лет он болтал о том, насколько важна атомная теория для его таблицы.
Но другие могли прочитать сообщение в таблице. В 1888 году немецкий химик Йоханнес Вислиценус заявил, что периодичность свойств элементов при расчете по весу указывает на то, что атомы состоят из регулярного расположения более мелких частиц. Таким образом, в некотором смысле таблица Менделеева действительно предвосхищала (и предоставляла доказательства) сложную внутреннюю структуру атомов в то время, когда никто не имел ни малейшего представления о том, как на самом деле выглядит атом, и даже есть ли у него какая-либо внутренняя структура.
Ко времени смерти Менделеева в 1907 году ученые знали, что у атомов есть части: электроны, несущие отрицательный электрический заряд, плюс некоторый положительно заряженный компонент, делающий атомы электрически нейтральными. Ключ к разгадке того, как были устроены эти части, пришел в 1911 году, когда физик Эрнест Резерфорд, работающий в Манчестерском университете в Англии, открыл атомное ядро. Вскоре после этого Генри Мозли, физик, работавший с Резерфордом, продемонстрировал, что количество положительного заряда в ядре (количество протонов, которые оно содержит, или его «атомный номер») определяет правильный порядок элементов в периодической таблице.
Атомный вес был тесно связан с атомным номером Мозли – достаточно близко, чтобы элементы упорядочения по весу лишь в нескольких местах отличались от упорядочения по номерам. Менделеев настаивал на том, что эти веса были неправильными и их нужно было повторно измерить, и в некоторых случаях он был прав. Осталось несколько неточностей, но атомный номер Мозли определил положение вещей.
Примерно в то же время датский физик Нильс Бор понял, что квантовая теория управляет расположением электронов, окружающих ядро, и что самые удаленные электроны определяют химические свойства элемента.
Физик Нильс Бор пересмотрел периодическую таблицу в 1922 году. QWerk / Wikimedia CommonsПодобное расположение внешних электронов периодически повторялось, объясняя закономерности, которые изначально были обнаружены в таблице Менделеева. Бор создал свою собственную версию таблицы в 1922 году, основанную на экспериментальных измерениях энергии электронов (наряду с некоторыми рекомендациями из периодического закона).
В таблицу Бора добавлены элементы, открытые с 1869 года, но, по сути, это была периодическая структура, которую обнаружил Менделеев.Не имея ни малейшего ключа к квантовой теории, Менделеев создал таблицу, отражающую атомную архитектуру, продиктованную квантовой физикой.
Новый стол Бора не был ни первым, ни последним вариантом первоначального дизайна Менделеева. Были разработаны и опубликованы сотни версий таблицы Менделеева. Современная форма, горизонтальный дизайн в отличие от первоначальной вертикальной версии Менделеева, стала широко популярной только после Второй мировой войны, во многом благодаря работе американского химика Гленна Сиборга (давнего члена правления Science Service, первоначального издателя книги Новости науки ).
Сиборг и его сотрудники синтетическим путем получили несколько новых элементов с атомными номерами помимо урана, последнего встречающегося в природе элемента в таблице. Сиборг увидел, что эти элементы, трансурановые элементы (плюс три элемента, предшествующие урану), требуют новой строки в таблице, чего Менделеев не предвидел. В таблице Сиборга строка для этих элементов добавлена под аналогичной строкой для редкоземельных элементов, правильное место которых также никогда не было вполне ясным. «Потребовалось много смелости, чтобы противостоять Менделееву», – сказал Сиборг, умерший в 1999 году, в интервью 1997 года.
Вклад Сиборга в химию принес ему честь создать его собственный одноименный элемент, сиборгий, номер 106. Это один из немногих элементов, названных в честь известного ученого, список, который, конечно же, включает элемент 101, открытый Сиборгом и его коллегами. в 1955 году и назван менделевием – в честь химика, который прежде всего заслужил место в таблице Менделеева.
В своей редакции американский химик Гленн Сиборг повернул периодическую таблицу по горизонтали, добавив несколько синтетических элементов помимо урана.Любезно предоставлено Национальной лабораторией Лоуренса БерклиГений таблицы Менделеева
AB Наука о знаниях и трудоустройстве 10-4 (2006) 10 Блок A: Исследование свойств материи
AB Наука о знаниях и трудоустройстве 20-4 (2006) 11 Блок A: Применение материи и химических изменений
AB Наука о знаниях и возможности трудоустройства 8, 9 (пересмотрено в 2009 г.) 9 Блок B: Материя и химические изменения
AB Наука 14 (2003 г., обновлено 2014 г.) 10 Блок A: Исследование свойств материи
AB Наука 7-8-9 (2003 г., обновлено в 2014 г.) 9 Блок B: Материя и химические изменения
до н.э Химия 11 (июнь 2018) 11 Большая идея: атомы и молекулы – строительные блоки материи.
до н.э Естественные науки 9 класс (июнь 2016 г.) 9 Большая идея: электронное расположение атомов влияет на их химическую природу.
МБ Старшая 1-я наука (2000) 9 Кластер 2: атомы и элементы
NB Естественные науки 9 класс (2002) 9 Атомы и элементы
NL 9 класс естествознания 9 Раздел 2: Атомы, элементы и соединения (редакция 2011 г.)
NL Наука 3200 (2005) 12 Блок 1: Химические реакции
NS Структура результатов обучения: естественные науки 9 класс (2014 г.) 9 Атомы и элементы
NT Наука о знаниях и трудоустройстве 10-4 (Альберта, 2006 г.) 10 Блок A: Исследование свойств материи
NT Наука о знаниях и трудоустройстве 20-4 (Альберта, 2006 г.) 11 Блок A: Применение материи и химических изменений
NT Наука о знаниях и возможности трудоустройства 9 (Альберта, редакция 2009 г.) 9 Блок B: Материя и химические изменения
NT Наука 14 (Альберта, 2003 г., обновлено 2014 г.) 10 Блок A: Исследование свойств материи
NT Наука 9 (Альберта, 2003 г., обновлено в 2014 г.) 9 Блок B: Материя и химические изменения
НУ Наука о знаниях и трудоустройстве 10-4 (2006) 10 Блок A: Исследование свойств материи
НУ Наука о знаниях и трудоустройстве 20-4 (Альберта, 2006 г.) 11 Блок A: Применение материи и химических изменений
НУ Наука о знаниях и возможностях трудоустройства 9 (Альберта, редакция 2009 г.) 9 Блок B: Материя и химические изменения
НУ Наука 14 (2003 г., обновлено 2014 г.) 10 Блок A: Исследование свойств материи
НУ Наука 9 (Альберта, 2003 г., обновлено в 2014 г.) 9 Блок B: Материя и химические изменения
НА Естественные науки, 9 класс, академический (SNC1D) (2008) 9 Нить C: атомы, элементы и соединения
НА Прикладная наука 9 класс (SNC1P) 9 Строка C: исследование вопроса
PE Естественные науки 9 класс (2018) 9 Блок 2: Атомы и элементы
КК Наука и технология Секция I Материальный мир: Организация
КК Наука и технология Раздел II Материальный мир: Организация
SK Наука 9 (2009) 9 Физическая наука – атомы и элементы (AE)
YT Chemistry 11 (Британская Колумбия, июнь 2018 г.) 11 Большая идея: атомы и молекулы – строительные блоки материи.
YT Science Grade 9 (Британская Колумбия, июнь 2016 г.) 9 Большая идея: электронное расположение атомов влияет на их химическую природу.
Дмитрий Менделеев | Биография, Периодическая таблица и факты
Дмитрий Менделеев , русский полностью Дмитрий Иванович Менделеев , (родился 27 января (8 февраля по новому стилю) 1834 года, Тобольск, Сибирь, Российская Империя – умер 20 января (2 февраля) 1907 года, Санкт-Петербург, Россия), русский химик, разработавший периодическую классификацию элементов.Менделеев обнаружил, что, когда все известные химические элементы расположены в порядке возрастания атомного веса, полученная таблица показывает повторяющийся образец или периодичность свойств внутри групп элементов. В своей версии периодической таблицы 1871 года он оставил пробелы в местах, где, как он считал, найдут свое место неизвестные элементы. Он даже предсказал вероятные свойства трех потенциальных элементов. Последующее подтверждение многих его предсказаний при его жизни прославило Менделеева как основателя периодического закона.
Популярные вопросы
Чего добился Дмитрий Менделеев?
Дмитрий Менделеев разработал периодическую классификацию химических элементов, в которой элементы расположены в порядке возрастания атомного веса.
Какими были ранние годы жизни Дмитрия Менделеева?
Родителями Дмитрия Менделеева были учитель Иван Менделеев и Мария Корнилева. Иван ослеп в 1834 году, в год рождения Дмитрия, и умер в 1847 году. Мария тогда руководила стекольным заводом. Однако в 1848 году фабрика сгорела, и Дмитрий переехал в Петербург.Петербург, чтобы продолжить образование.
Чем занимался Дмитрий Менделеев?
В 1865 году Дмитрий Менделеев стал профессором химической технологии Петербургского университета. Он стал там профессором общей химии в 1867 году и преподавал до 1890 года.
Ранние годы и образование
Менделеев родился в небольшом сибирском городке Тобольске и был последним из 14 выживших детей (или 13, в зависимости от источника) Ивана. Учитель местной гимназии Павлович Менделеев и Мария Дмитриевна Корнилева.Отец Дмитрия ослеп в год рождения Дмитрия и умер в 1847 году. Чтобы поддержать семью, его мать обратилась в управление небольшой стекольной фабрикой, принадлежавшей ее семье в соседнем городе. В декабре 1848 года фабрика сгорела, и мать забрала его в Петербург, где он поступил в Главный педагогический институт. Его мать умерла вскоре после этого, и Менделеев окончил институт в 1855 году. Он получил свою первую должность преподавателя в Симферополе в Крыму. Он пробыл там всего два месяца и, недолго проучившись в одесском лицее, решил вернуться в Петербург.Петербург, чтобы продолжить образование. Он получил степень магистра в 1856 году и начал проводить исследования в области органической химии. Получив государственную стипендию, он уехал учиться за границу на два года в Гейдельбергский университет. Вместо того, чтобы тесно сотрудничать с выдающимися химиками университета, включая Роберта Бунзена, Эмиля Эрленмейера и Августа Кекуле, он открыл лабораторию в своей собственной квартире. В сентябре 1860 года он посетил Международный химический конгресс в Карлсруэ, созванный для обсуждения таких важных вопросов, как атомный вес, химические символы и химические формулы.Там он встретился и установил контакты со многими ведущими химиками Европы. В последующие годы Менделеев особенно запомнил работу итальянского химика Станислао Канниццаро, в которой разъяснялось понятие атомного веса.
В 1861 году Менделеев вернулся в Санкт-Петербург, где в 1864 году получил звание профессора Технологического института. После защиты докторской диссертации в 1865 году он был назначен профессором химической технологии Санкт-Петербургского университета.-Петербург (ныне Санкт-Петербургский государственный университет). Он стал профессором общей химии в 1867 году и продолжал преподавать там до 1890 года.
Когда он начал преподавать неорганическую химию, Менделеев не мог найти учебник, который отвечал бы его потребностям. Поскольку в 1861 году он уже издал учебник по органической химии, удостоенный престижной Демидовской премии, он задумал написать еще один. В результате получилась книга « Основы химии » (1868–71; Основы химии, ), ставшая классикой, выдержавшая множество изданий и переводов.Когда Менделеев начал составлять главу о галогеновых элементах (хлор и его аналоги) в конце первого тома, он сравнивал свойства этой группы элементов со свойствами группы щелочных металлов, таких как натрий. Внутри этих двух групп разнородных элементов он обнаружил сходство в изменении атомных весов и задался вопросом, проявляют ли другие группы элементов аналогичные свойства. Изучив щелочноземельные земли, Менделеев установил, что порядок атомных весов можно использовать не только для расположения элементов внутри каждой группы, но и для расположения самих групп.Таким образом, в своем стремлении осмыслить уже существующие обширные знания о химических и физических свойствах химических элементов и их соединений, Менделеев открыл периодический закон.
Периодическая таблица МенделееваПериодическая таблица элементов из одной из первых созданных периодических таблиц Дмитрия Менделеева Основы химии (1869; Принципы химии ).
© Photos.com/Thinkstock Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту.Подпишитесь сейчасЕго недавно сформулированный закон был объявлен Русскому химическому обществу в марте 1869 года с утверждением, что «элементы, упорядоченные в соответствии со значением их атомного веса, обладают явной периодичностью свойств». Закон Менделеева позволил ему составить систематизированную таблицу всех 70 элементов, известных на тот момент. Он настолько верил в справедливость периодического закона, что предложил изменения общепринятых значений атомного веса нескольких элементов и предсказал расположение неизвестных элементов в таблице вместе с их свойствами.Сначала периодическая система не вызывала интереса у химиков. Однако с открытием предсказанных элементов, особенно галлия в 1875 году, скандия в 1879 году и германия в 1886 году, он начал завоевывать широкое признание. Постепенно периодический закон и таблица стали основой большей части химической теории. К моменту смерти Менделеева в 1907 году он пользовался международным признанием и был награжден знаками отличия и наградами многих стран.
Дмитрий МенделеевДмитрий Менделеев, холст, масло Ивана Крамского, 1878 г.
© Архив всемирной истории / возрастной фотостокхимический элемент | Определение, происхождение, распространение и факты
Химический элемент , также называемый элементом , любое вещество, которое не может быть разложено на более простые вещества обычными химическими процессами. Элементы – это фундаментальные материалы, из которых состоит вся материя.
Британская викторина
Периодическая таблица элементов
Проверьте свою связь с периодической таблицей элементов в этой викторине по всем 118 химическим элементам и их символам.Возможно, вы знакомы с химическими символами водорода и кислорода, но можете ли вы сопоставить такие низкопрофильные элементы, как гадолиний и эрбий, с их соответствующими символами?
В этой статье рассматривается происхождение элементов и их распространенность во Вселенной. Подробно рассматривается геохимическое распределение этих элементарных веществ в земной коре и недрах, а также их присутствие в гидросфере и атмосфере. В статье также рассматривается периодический закон и табличное расположение элементов на его основе.Для получения подробной информации о соединениях элементов, см. Химическое соединение .
Редакция Британской энциклопедииОбщие наблюдения
В настоящее время известно 118 химических элементов. Около 20 процентов из них не существуют в природе (или присутствуют только в следовых количествах) и известны только потому, что были синтетически получены в лаборатории. Из известных элементов 11 (водород, азот, кислород, фтор, хлор и шесть благородных газов) являются газами при обычных условиях, два (бром и ртуть) являются жидкостями (еще два, цезий и галлий, плавятся примерно при температуре выше комнатной температуры), а остальное – твердые.Элементы могут объединяться друг с другом, образуя широкий спектр более сложных веществ, называемых соединениями. Число возможных соединений практически бесконечно; возможно, известен миллион, и каждый день открывается все больше. Когда два или более элемента объединяются в соединение, они теряют свою индивидуальность, и продукт имеет характеристики, совершенно отличные от характеристик составляющих элементов. Газообразные элементы водород и кислород, например, с совершенно разными свойствами, могут объединяться с образованием сложной воды, которая имеет совершенно другие свойства, чем кислород или водород.Очевидно, что вода не является элементом, потому что она состоит из двух веществ, водорода и кислорода, и фактически может быть химически разложена на них; эти два вещества, однако, являются элементами, потому что они не могут быть разложены на более простые вещества никаким известным химическим процессом. Большинство образцов естественного вещества представляют собой физические смеси соединений. Например, морская вода представляет собой смесь воды и большого количества других соединений, наиболее распространенным из которых является хлорид натрия или поваренная соль. Смеси отличаются от соединений тем, что их можно разделить на составные части с помощью физических процессов; например, простой процесс испарения отделяет воду от других компонентов морской воды.
Историческое развитие концепции элемента
Современная концепция элемента однозначна, поскольку она зависит от использования химических и физических процессов как средства отделения элементов от соединений и смесей. Однако существование фундаментальных веществ, из которых состоит вся материя, было основой многих теоретических предположений с самого начала истории. Древнегреческие философы Фалес, Анаксимен и Гераклит предполагали, что вся материя состоит из одного существенного принципа – элемента.Фалес считал, что этот элемент – вода; Анаксимен предложил воздух; и Гераклит, огонь. Другой греческий философ, Эмпедокл, выразил иную веру – что все вещества состоят из четырех элементов: воздуха, земли, огня и воды. Аристотель согласился и подчеркнул, что эти четыре элемента являются носителями фундаментальных свойств: сухость и тепло связаны с огнем, тепло и влага – с воздухом, влажность и холод – с водой, а холод и сухость – с землей. В мышлении этих философов все другие вещества должны были быть комбинациями четырех элементов, и считалось, что свойства веществ отражают их элементный состав.Таким образом, греческая мысль заключала в себе идею о том, что вся материя может быть понята в терминах элементарных качеств; в этом смысле сами элементы считались нематериальными. Греческое понятие элемента, которое было принято почти 2000 лет, содержало только один аспект современного определения, а именно, что элементы обладают характерными свойствами.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчасВо второй половине средневековья, когда алхимики стали более изощренными в своих знаниях о химических процессах, греческие концепции состава материи стали менее удовлетворительными.Были введены дополнительные элементарные качества, чтобы приспособиться к недавно обнаруженным химическим превращениям. Таким образом, сера стала олицетворять горючесть, ртуть – летучесть или текучесть, а соль – стойкость в огне (или негорючесть). Эти три алхимических элемента или принципа также представляют собой абстракции свойств, отражающих природу материи, а не физических субстанций.
Важное различие между смесью и химическим соединением в конце концов было понято, и в 1661 году английский химик Роберт Бойль осознал фундаментальную природу химического элемента.Он утверждал, что четыре греческих элемента не могут быть настоящими химическими элементами, потому что они не могут объединяться с образованием других веществ и не могут быть извлечены из других веществ. Бойль подчеркивал физическую природу элементов и соотносил их с соединениями, которые они образуют, современными методами.
В 1789 году французский химик Антуан-Лоран Лавуазье опубликовал то, что можно считать первым списком элементарных веществ, основанным на определении Бойля. Список элементов Лавуазье был составлен на основе тщательного количественного исследования реакций разложения и рекомбинации.Поскольку он не мог проводить эксперименты по разложению определенных веществ или формированию их из известных элементов, Лавуазье включил в свой список элементов такие вещества, как известь, глинозем и кремнезем, которые, как теперь известно, являются очень стабильными соединениями. На то, что Лавуазье все еще сохранилось влияние древнегреческой концепции элементов, указывает его включение света и тепла (калорийности) в число элементов.
Семь веществ, признанных сегодня элементами, – золото, серебро, медь, железо, свинец, олово и ртуть – были известны древним, поскольку встречаются в природе в относительно чистой форме.Они упоминаются в Библии и в раннем индуистском медицинском трактате Caraka-samhita . Шестнадцать других элементов были открыты во второй половине 18 века, когда методы отделения элементов от их соединений стали более понятными. Еще восемьдесят два последовали после внедрения количественных аналитических методов.
