Таблица Менделеева для ЕГЭ по химии 2022 📓.
Таблица Менделеева для ЕГЭ по химии 2022 📓. | Университет СИНЕРГИЯКурс подготовки к ЕГЭ и ОГЭ. Идёт набор!
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности.
Какую профессию можно получить, сдав обществознание и английский
25.10.2022
Из чего складывается проходной балл
30.06.2022
Что значит первичный балл в ЕГЭ
14.06.2022
Самые высокооплачиваемые профессии, связанные с биологией
14.06.2022
Распределение баллов ЕГЭ по русскому языку
14.04.2022
Куда можно поступить после 9 класса с обществознанием и информатикой
28.03.2022
Смотреть все
Всё нужное в твоём телефоне
Скачай приложение и узнавай самую актуальную информацию
ПОДБЕРИ КУРС ЕГЭ И ОГЭ
Ответь на пять вопросов и узнай, где будешь учиться!
Подобрать программуОбразование для карьеры
К каким профессиям вы более склонны?
ТехническимГуманитарнымТворческимМедицинским
Какой у вас уровень образования?
Без образованияШкола 9-11 классКолледжБакалавриатМагистратураАспирантура
Какой формат обучения вам подходит?
ОчноЗаочноОнлайнПо выходным дням
Вас интересуют бюджетные места?
ДаНет
И последний вопрос. Вы из Москвы?
Вы из Москвы?
ДаНет
Мы подобрали вам программу обучения
Заполните форму, чтобы узнать больше о программе и наших предложениях
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности
Уважаемый посетитель!
Если у вас есть вопрос, предложение или жалоба, пожалуйста, заполните короткую форму и изложите суть обращения в текстовом поле ниже. Мы обязательно с ним ознакомимся и в 30-дневный срок ответим на указанный вами адрес электронной почты
Статус Абитуриент Студент Родитель Соискатель Сотрудник Другое
Филиал Абакан Актобе Алагир Алматы Алушта Анапа Ангарск Архангельск Армавир Асбест Астана Астрахань Атырау Баку Балхаш Барановичи Барнаул Белая Калитва Белгород Бельцы Берлин Бишкек Благовещенск Бобров Бобруйск Борисов Боровичи Бронницы Брянск Бузулук Чехов Челябинск Череповец Черкесск Дамаск Дербент Димитровград Дмитров Долгопрудный Домодедово Дубай Дубна Душанбе Екатеринбург Электросталь Елец Элиста Ереван Евпатория Гана Гомель Гродно Грозный Хабаровск Ханты-Мансийск Хива Худжанд Иркутск Истра Иваново Ижевск Калининград Карабулак Караганда Каракол Кашира Казань Кемерово Киев Кинешма Киров Кизляр Королев Кострома Красноармейск Краснодар Красногорск Красноярск Краснознаменск Курган Курск Кызыл Липецк Лобня Магадан Махачкала Майкоп Минеральные Воды Минск Могилев Москва Моздок Мозырь Мурманск Набережные Челны Нальчик Наро-Фоминск Нижневартовск Нижний Новгород Нижний Тагил Ногинск Норильск Новокузнецк Новосибирск Новоуральск Ноябрьск Обнинск Одинцово Омск Орехово-Зуево Орел Оренбург Ош Озёры Павлодар Пенза Пермь Петропавловск Подольск Полоцк Псков Пушкино Пятигорск Радужный Ростов-на-Дону Рязань Рыбинск Ржев Сальск Самара Самарканд Санкт-Петербург Саратов Сергиев Посад Серпухов Севастополь Северодвинск Щербинка Шымкент Слоним Смоленск Солигорск Солнечногорск Ставрополь Сургут Светлогорск Сыктывкар Сызрань Тамбов Ташкент Тбилиси Терек Тихорецк Тобольск Тольятти Томск Троицк Тула Тверь Тюмень Уфа Ухта Улан-Удэ Ульяновск Ургенч Усть-Каменогорск Вёшенская Видное Владимир Владивосток Волгодонск Волгоград Волжск Воркута Воронеж Якутск Ярославль Юдино Жлобин Жуковский Златоуст Зубова Поляна Звенигород
Тип обращения Вопрос Предложение Благодарность Жалоба
Тема обращения Поступление Трудоустройство Обучение Оплата Кадровый резерв Внеучебная деятельность Работа автоматических сервисов университета Другое
* Все поля обязательны для заполнения
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности
Как периодическая таблица пережила войну, чтобы обеспечить будущее химии
- ОТ РЕДАКЦИИ
Столетие назад открытие гафния подтвердило справедливость периодической таблицы — но только благодаря ученым, которые отстаивали доказательства во времена глобальных потрясений.
Гафний — это переходный металл, названный в честь латинского названия Копенгагена (Hafnia), где этот элемент был открыт. Фото: Клаудия Килман/Alamy
Гафний не особенно примечательный элемент. Это не ваш взрывоопасный натрий, мерцающая ртуть или вонючая сера. Это сероватый металл, который обычно используется в качестве поглотителя нейтронов в управляющих стержнях атомных электростанций и атомных подводных лодок, а также в качестве изолятора в компьютерных микросхемах. Но открытие гафния, о котором сообщалось в журнале

Периодическая таблица элементов Дмитрия Менделеева, созданная в 1869 году, возникла в результате осознания того, что химические элементы, такие как кислород и водород, находятся в определенных отношениях. Вклад Менделеева и немецкого химика Юлиуса Лотара Мейера, работавших независимо друг от друга, обеспечили порядок элементов, а также критерии их классификации в четкие группы. Примечательно, что схемы Менделеева и Лотара Мейера основывались на субатомной структуре элементов — за несколько десятилетий до открытия электронов и протонов.
Когда Менделеев разработал приблизительную форму таблицы Менделеева, он начал с 63 известных элементов. Чтобы таблица работала, ему пришлось оставить пробелы, в которые могли бы быть помещены еще не обнаруженные элементы. Эти элементы вскоре начали появляться. Например, предсказанный «элемент 68», галлий, был идентифицирован несколькими годами позже, в 1875 году. К 1914 году осталось всего семь пробелов.
Прорыв произошел в 1913 году, когда Генри Мозли, британский физик, показал, что элементы можно расположить по их атомному номеру или количеству протонов.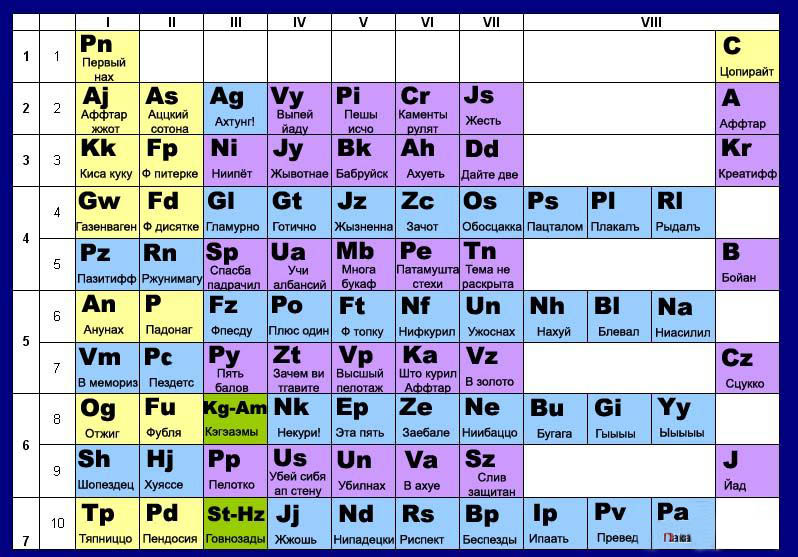 Работа Мозли предоставила как более точную «карту пробелов», так и метод идентификации элементов по спектрам, полученным путем воздействия на элементы-кандидаты рентгеновскими лучами.
Работа Мозли предоставила как более точную «карту пробелов», так и метод идентификации элементов по спектрам, полученным путем воздействия на элементы-кандидаты рентгеновскими лучами.
Битва за последние дополнения к периодической таблице
Но открытие (и название) элемента 72, гафния, было далеко не простым. Французский химик Жорж Урбен первоначально предположил в 1911 году, что 72-й элемент относится к редкоземельным элементам периодической таблицы, и назвал его кельтием. Но примерно десятилетие спустя датский физик Нильс Бор, который использовал квантовую теорию для разработки модели атома, в котором электроны вращаются вокруг ядра, предсказал, что элемент 72 будет среди переходных металлов и ближе к цирконию (элемент 40). В конце концов это подтвердили Костер и фон Хевеси, работавшие в лаборатории Бора в Копенгагене, которые искали в минералах циркония элемент 9.0017 2

Дебаты продолжались, ученые из Нидерландов, Германии и Скандинавии поддержали команду Копенгагена, в то время как ученые из Франции и Великобритании (которые поддержали бойкот немецкой науки после Первой мировой войны) выступили против встречная позиция. Гафний был принят Международным союзом теоретической и прикладной химии только в 1930, через несколько лет после официального прекращения бойкота. Во Франции кельтий продолжал занимать место 72-го элемента среди редкоземельных элементов до начала 1940-х годов
Гафний был принят Международным союзом теоретической и прикладной химии только в 1930, через несколько лет после официального прекращения бойкота. Во Франции кельтий продолжал занимать место 72-го элемента среди редкоземельных элементов до начала 1940-х годов
Спустя сто лет после открытия гафния периодическая таблица остается надежной и актуальной, даже в то время, когда к множеству данных об элементе можно получить доступ одним щелчком мыши. Таблица дает краткий обзор того, как элемент может вести себя в химической реакции, и указывает на его сходство с другими элементами в группе.
На данный момент подтверждено 118 элементов с добавлением четырех сверхтяжелых синтетических элементов в 2015 году. Но обязательно придет время, когда новых элементов не будет и периодическая таблица достигнет своего предела. Пока нет единого мнения о том, когда это может произойти или насколько большим будет последний элемент, но химики говорят, что его атомный номер может превысить 170.
Костер Д. и Хевеси Г. Nature 111 , 79 (1923).
Артикул Google Scholar
Kragh, H. Centaurus 23 , 275–301 (1980).
Артикул Google Scholar
Frederick-Frost, K.M. Chem. Междунар. 41 (2), 23–27 (2019).
Артикул Google Scholar
Урбен Г. и Довилье А. Природа 111 , 218 (1923).
Артикул Google Scholar
Костер, Д. и Хевеси, Г. Природа 111 , 462–463 (1923).
Артикул Google Scholar
Резерфорд, Э. Природа 109 , 781 (1922).
Артикул Google Scholar
Ссылки для скачивания
Учебное пособие по истории периодической таблицы химических элементов
Ключевые понятия
- Периодическая таблица элементов — очень полезный инструмент для химиков и студентов, изучающих химию.
- Периодическая таблица возникла потому, что ученые увидели закономерности в свойствах известных им элементов и попытались систематически организовать элементы в группы со сходными свойствами.
- Хронология наиболее важных событий в истории развития Периодической таблицы может выглядеть так, как показано ниже:
| Год | 1780-е | 1828 | 1829 | 1864 | 1869 | 1869 | 1894 | 1913 | 1940 |
|---|---|---|---|---|---|---|---|---|---|
| Ученый | Лавуазье | Берцелиус | Доберейнер | Ньюлендс | Мейер | Менделеев | Рамзи | Мозли | Сиборг |
| Взнос | металлы и неметаллы | символов для элементов | триады | Закон Октав | порядок атомного веса | элементов, расположенных периодически | Благородные газы | Атомный номер | Актиноиды (актиниды) |
Пожалуйста, не блокируйте рекламу на этом сайте.
Нет рекламы = нет денег для нас = нет бесплатных вещей для вас!
Историческое развитие периодической таблицы элементов
В приведенной ниже таблице показан основной вклад каждого ученого в разработку современной Периодической таблицы элементов.
| Участник | Дата | Вклад | Комментарий |
|---|---|---|---|
| Аристотель | &примерно 330 г. до н.э. | Теория четырех элементов: земля, воздух, огонь и вода | |
| Антуан Лавуазье | &приблизительно 1770-1789 | Написал первый обширный список элементов, содержащий 33 элемента. Различают металлы и неметаллы. | Позже было показано, что некоторые из элементов Лавуазье представляют собой соединения и смеси. |
| Йонс Якоб Берцелиус | 1828 | Разработал таблицу атомных весов. Введены буквы для обозначения элементов. | |
| Иоганн Доберейнер | 1829 | Разработаны «триады», группы из 3 элементов со схожими свойствами. Литий, натрий и калий образуют триаду. Кальций, стронций и барий образуют триаду. Хлор, бром и йод образуют триаду. | Предшественник понятия групп. |
| Джон Ньюлендс | 1864 | Известные элементы (> 60) были расположены в порядке атомного веса и наблюдалось сходство между первым и девятым элементами, вторым и десятым элементами и т. д. Он предложил «Закон октав». | Закон октав Ньюлендса выявил много сходства между элементами, но также требовал сходства там, где его не было. Он не оставил места для еще не открытых элементов. Предтеча понятия периодов. |
| Лотар Мейер | 1869 | Составил периодическую таблицу из 56 элементов на основе периодичности свойств, таких как молярный объем, при расположении в порядке атомного веса. | Мейер и Менделеев (см. ниже) создали свои Периодические таблицы одновременно. |
| Дмитрий Менделеев | 1869 | Создал таблицу, основанную на атомных весах, но расположенную «периодически» с элементами с похожими свойствами друг под другом. Оставлены пробелы для неизвестных в то время элементов и предсказанных их свойств (элементами были галлий, скандий и германий). Порядок элементов был изменен, если этого диктовали их свойства, например, телларий тяжелее йода, но стоит перед ним в Периодической таблице. | Периодическая таблица Менделеева была важна, потому что она позволяла предсказывать свойства элементов с помощью «периодического закона», который гласит: 90–205 свойства элементов периодически меняются в зависимости от их атомного веса. |
| Уильям Рамзи | 1894 | Открыты благородные газы. | В 1894 году Рамзи удалил кислород, азот, воду и углекислый газ из образца воздуха и получил газ в 19 раз тяжелее водорода, очень нереакционноспособный и с неизвестным спектром излучения. Он назвал этот газ аргоном. В 1895 году он открыл гелий как продукт распада урана и сопоставил его со спектром излучения неизвестного элемента на Солнце, открытого в 1868 году (гелиос по-гречески означает Солнце). Он открыл неон, криптон и ксенон и понял, что они представляют собой новую группу в Периодической таблице. Рамзи был удостоен Нобелевской премии в 1904 году. |
| Генри Мозли | 1913 | Определен атомный номер каждого из элементов. Он изменил «Периодический закон», чтобы прочесть, что свойства элементов периодически меняются в зависимости от их атомных номеров. | Модифицированный периодический закон Мозли расставляет элементы теллерий и йод в правильном порядке, как это делается для аргона и калия, кобальта и никеля. |
