Металлы в химии – формула класса, таблица (9 класс)
4
Средняя оценка: 4
Всего получено оценок: 1850.
4
Средняя оценка: 4
Всего получено оценок: 1850.
К металлам относится большая часть элементов периодической системы – 82 химических элементов. Какими свойствами они обладают, и чем отличаются от неметаллов?
Общая характеристика
Металлами называют группу элементов, в виде простых веществ, которые обладают металлическими свойствами (пластичность, ковкость, блеск, электронная проводимость и т. д.)
Основное отличие элементов-металлов – они обладают только восстановительными свойствами, а в реакциях могут только окисляться. В соединениях они могут иметь только положительные степени окисления как в элементарных положительно заряженных ионах, так и в сложных ионах, где они образуют положительные центры.
Рис. 1. Список металлов.Как правило, на внешнем уровне элементов металлов находится небольшое число электронов (1-3), значения электроотрицательности невысокие.
Физические и химические свойства
Все металлы, кроме ртути, при нормальных условиях в виде простых веществ находятся в твердом агрегатном состоянии и образуют металлическую кристаллическую решетку.
Рис. 2. Металлы в таблице Д.И. Менделеева.Таблица «Металлы»
В следующей таблицы представлены группы основных металлов:
| Группа металлов | |
| Щелочные | литий, натрий, калий и т.д. |
| Щелочноземельные | кальций, стронций, барий и т.д. |
| Переходные | уран, титан, железо, платина и т. д. д. |
| постпереходные | алюминий, свинец, олово и т.д. |
| Тугоплавкие | молибден, вольфрам |
| Цветные | медь, титан, магний и т.д. |
| Благородные | золото, серебро и т.д. |
Металлы пластичны и ковки, особенно если на внешнем электронном уровне атомов по одному электрону: слои атомов перемещаются относительно друг друга без разрушения кристаллической решетки (щелочные металлы, медь, серебро, золото). В атомах непластичных хрупких металлов хрома и марганца – большое число валентных электронов.
Плотность, твердость, температура плавления металлов изменяются в широком диапазоне и зависят от атомной массы, строения атома и геометрии кристаллической решетки. Самый легкий металл – литий (плотность 0,53 г/см3), самый тяжелый – осмий (плотность 22,5 г/см3). Металлы с плотностью больше 5 г/см3 относят к тяжелым, меньше 5 г/см3 – к легким металлам.
Самая низкая температура плавления у ртути (-39 градусов по Цельсию), самый тугоплавкий металл – вольфрам (температура плавления 3410 градусов по Цельсию.) Энергия атомизации вольфрама составляет 836 кДж/моль, а температура кипения его 5930 градусов.
Металлы вступают в реакцию как с простыми, так и со сложными веществами. Как типичные восстановители металлы реагируют почти со всеми неметаллами-окислителями (кислород, сера, азот и т. д.):
4Al+3O2=Al2O3
Также металлы реагируют с такими сложными веществами, как оксиды и гидроксиды, разбавленные растворы кислот, с растворенными в воде щелочами.
В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются; в пределах одной и той же группы (в главной подгруппе) металлические свойства усиливаются, а неметаллические ослабевают
Рис. 3. Металлы главных подгрупп.Нахождение металлов и способы их получения
Самый распространенный на земле элемент-металл – алюминий. За ним следуют железо, кальций, натрий.
За ним следуют железо, кальций, натрий.
Некоторые металлы встречаются в природе в самородном состоянии (золото, ртуть, платина), но в основном они находятся в природе в виде оксидов и солей.
Получение металлов происходит с помощью металлургии (получение из руд), пирометаллургии (получение с помощью реакции восстановления при высокой температуре), гидрометаллургии (извлечение из руд в виде растворимых соединений), электрометаллургии (получение металлов электролизом расплавов и растворов их соединений).
Что мы узнали?
Металлы – вещества, которые обладают высокой электро- и теплопроводностью, ковкостью, пластичностью и металлическим блеском. В данной статье по химии 9 класса рассматриваются их физические и химические свойства, формулы класса металлов, а также способы получения.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
Илья Васечко
10/10
10/10
Лиза Комиссарова
10/10
Софа Данилова
10/10
Наири Аракелян
10/10
Вадим Якшимбетов
10/10
Лилия Алишева
10/10
Анастасия Анисина
10/10
Влад Сергеев
9/10
Руслан Гайс
9/10
Оценка доклада
4
Средняя оценка: 4
Всего получено оценок: 1850.
А какая ваша оценка?
Металлы и неметаллы в таблице Менделеева: таблица, как определять металлические свойства и отличать элементы
Дмитрий Менделеев смог создать уникальную таблицу химических элементов, главным достоинством которой была периодичность. Металлы и неметаллы в таблице Менделеева располагаются так, что их свойства изменяются периодическим образом.
Содержание
Периодическая таблица Менделеева
Периодическая система была составлена Дмитрием Менделеевым во второй половине 19 века. Открытие не только позволило упростить работу химиков, она смогла объединить в себе как в единой системе все открытые химические вещества, а также предсказать будущие открытия.
Создание данной структурированной системы бесценно для науки и для человечества в целом. Именно это открытие дало толчок развитию всей химии на долгие годы.
Интересно знать! Существует легенда, что готовая система привиделась ученому во сне.
В интервью одному журналисту ученый объяснил, что работал над ней 25 лет и то, что она ему снилась – вполне естественно, но это не значит, что во сне пришли все ответы.
Созданная Менделеевым система делится на две части:
- периоды – столбики по горизонтали в одну или две строки (ряды),
- группы – вертикальные строчки, в один ряд.
Всего в системе 7 периодов, каждый следующий элемент отличен от предыдущего большим количеством электронов в ядре, т.е. заряд ядра каждого правого показателя больше левого на единицу. Каждый период начинается с металла, а заканчивается инертным газом – именно это и есть периодичность таблицы, ведь свойства соединений меняются внутри одного периода и повторяются в следующем. При этом, следует помнить, что 1-3 периоды неполные или малые, в них всего 2, 8 и 8 представителей. В полном периоде (т.е. оставшихся четырех) по 18 химических представителей.
В группе располагаются химические соединения с одинаковой высшей валентностью, т. е. у них одинаковое электронное строение. Всего в системе представлено 18 групп (полная версия), каждая из которых начинается щелочью и заканчивается инертным газом. Все, представленные в системе субстанции, можно разделить на две основные группы – металл или неметалл.
е. у них одинаковое электронное строение. Всего в системе представлено 18 групп (полная версия), каждая из которых начинается щелочью и заканчивается инертным газом. Все, представленные в системе субстанции, можно разделить на две основные группы – металл или неметалл.
Для облегчения поиска группы имеют свое название, а металлические свойства субстанций усиливаются с каждой нижней строчкой, т.е. чем ниже соединение, тем больше у него будет атомных орбит и тем слабее электронные связи. Также меняется и кристаллическая решетка – она становится ярко выраженной у элементов с большим количеством атомных орбит.
В химии используют три вида таблиц:
- Короткая – актиноиды и лантаноиды вынесены за границы основного поля, а 4 и все последующие периоды занимают по 2 строчки.
- Длинная – в ней актиноиды и лантаноиды вынесены за границу основного поля.
- Сверхдлинная – каждый период занимает ровно 1 строку.
Главной считается та таблица Менделеева, которая была принята и подтверждена официально, но для удобства чаще используют короткую версию.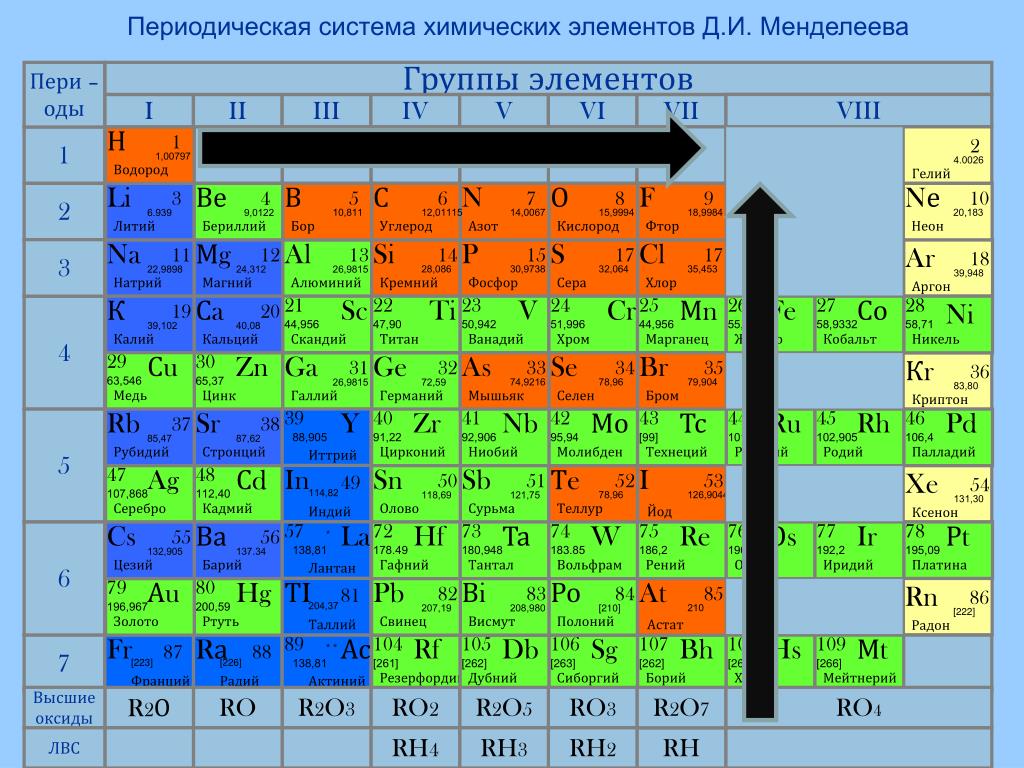 Металлы и неметаллы в таблице Менделеева располагаются согласно строгим правилам, которые облегчают работу с ней.
Металлы и неметаллы в таблице Менделеева располагаются согласно строгим правилам, которые облегчают работу с ней.
Это интересно! Уроки химии: катионы и анионы – что это такое
Металлы в таблице Менделеева
В системе Менделеева сплавы имеют преобладающее число и список их весьма велик – они начинаются с Бора (В) и заканчиваются полонием (Po) (исключением являются германий (Ge) и сурьма (Sb)). У этой группы есть характерные признаки, они разделены на группы, но их свойства при этом неоднородны. Характерные их признаки:
- пластичность,
- электропроводимость,
- блеск,
- легкая отдача электронов,
- ковкость,
- теплопроводность,
- твердость (кроме ртути).
Из-за различной химической и физической сути свойства могут существенно отличаться у двух представителей этой группы, не все они похожи на типичные природные сплавы, к примеру, ртуть – это жидкая субстанция, но относится к данной группе.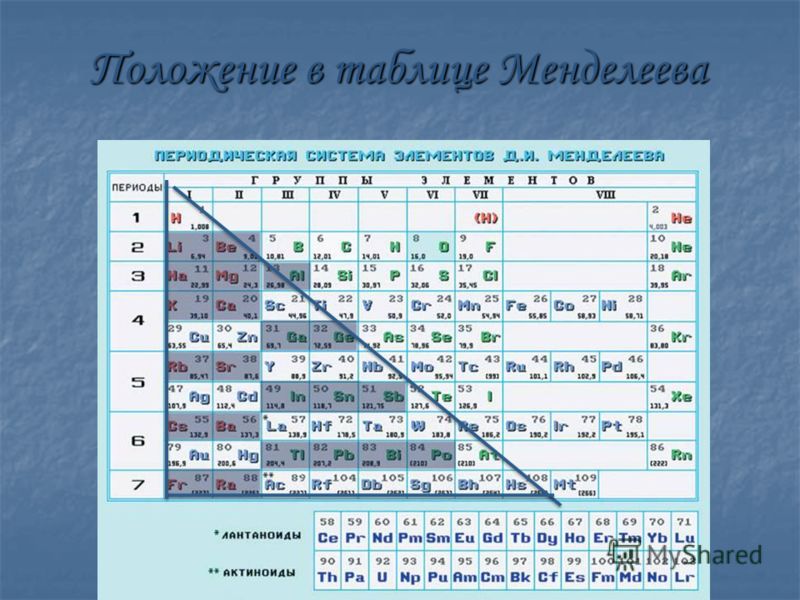
В обычном своем состоянии она жидкая и без кристаллической решетки, которая играет ключевую роль в сплавах. Только химические характеристики роднят ртуть с данной группой элементов, несмотря на условность свойств этих органических соединений. То же самое касается и цезия – самого мягкого сплава, но он не может в природе существовать в чистом виде.
Некоторые элементы такого типа могут существовать только доли секунды, а некоторые не встречаются в природе совсем – их создали в искусственных условиях лаборатории. У каждой из групп металлов в системе есть свое название и признаки, которые отличают их от других групп.
Это интересно! Уроки химии: что это такое галогены
При этом отличия у них весьма существенные. В периодической системе все металлы располагаются по количеству электронов в ядре, т.е. по увеличению атомной массы. При этом для них характерно периодическое изменение характерных свойств. Из-за этого в таблице они не размещаются аккуратно, а могут стоять неправильно.
В первой группе щелочей нет веществ, которые бы встречались в чистом виде в природе – они могут пребывать только в составе различных соединений.
Как отличить металл от неметалла?
Как определить металл в соединении? Существует простой способ определения, но для этого необходимо иметь линейку и таблицу Менделеева. Для определения надо:
- Провести условную линию по местам соединения элементов от Бора до Полония (можно до Астата).
- Все материалы, которые будут слева линии и в побочных подгруппах – металл.
- Вещества справа – другого типа.
Это интересно! Что такое алканы: строение и химические свойства
Однако у способа есть изъян – он не включает в группу Германий и Сурьму и работает только в длинной таблице. Метод можно использовать в качестве шпаргалки, но чтобы точно определить вещество, следует запомнить список всех неметаллов. Сколько их всего? Мало – всего 22 вещества.
В любом случае, для определения природы вещества необходимо рассматривать его в отдельности.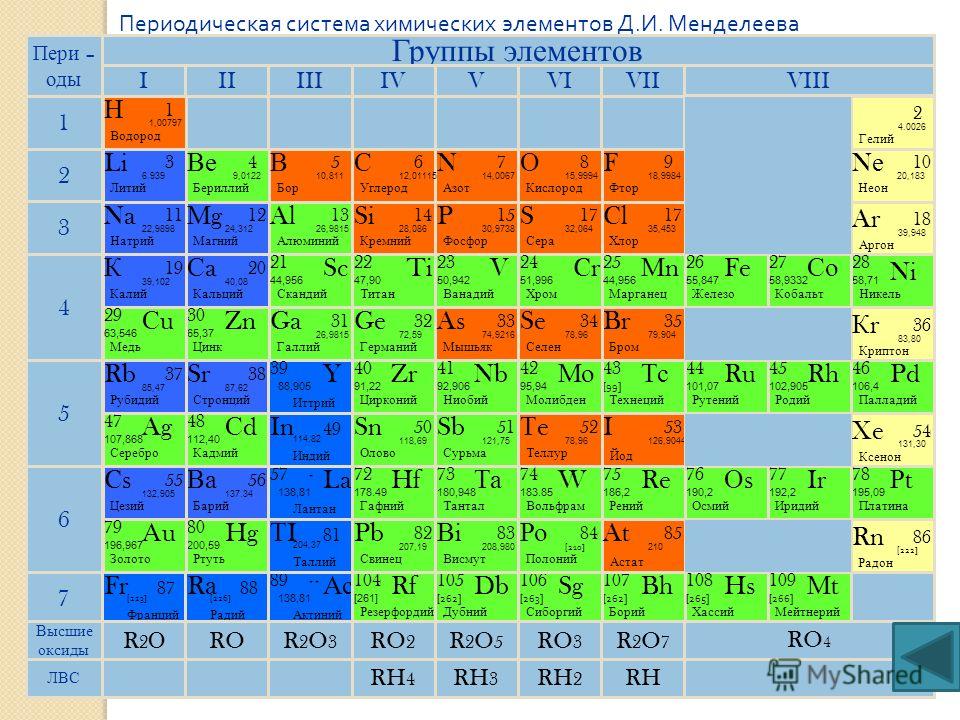 Легко будет элементы, если знать их свойства. Важно запомнить, что все металлы:
Легко будет элементы, если знать их свойства. Важно запомнить, что все металлы:
- При комнатной температуре – твердые, за исключением ртути. При этом они блестят и хорошо проводят электрический ток.
- У них на внешнем уровне ядра меньшее количество атомов.
- Состоят из кристаллической решетки (кроме ртути), а все другие элементы имеют молекулярную или ионную структуру.
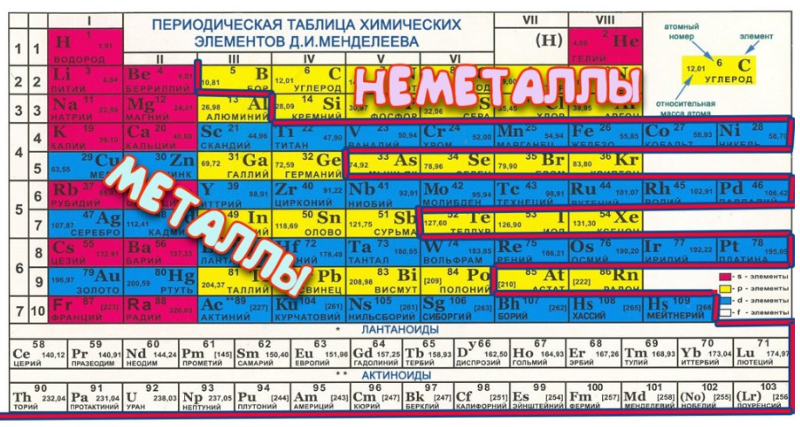
- В периодической системе все неметаллы – красного цвета, металлы – черного и зеленого.
- Если двигаться слева направо в периоде, то заряд ядра вещества будет увеличиваться.
- У некоторых веществ свойства выражены слабо, но они все равно имеют характерные признаки. Такие элементы относятся к полуметаллам, например Полоний или Сурьма, они обычно располагаются на границе двух групп.
Внимание! В левой нижней части блока в системе всегда стоят типичные металлы, а в правой верхней типичные газы и жидкости.
Важно запомнить, что при перемещении в таблице сверху вниз становятся сильнее неметаллические свойства веществ, поскольку там располагаются элементы, которые имеют отдаленные внешние оболочки. Их ядро отделено от электронов и поэтому они притягиваются слабее.
Полезное видео
Подведем итоги
Отличить элементы будет просто, если знать основные принципы формирования таблицы Менделеева и свойства металлов. Полезно будет также запомнить и список остальных 22 элементов. Но не нужно забывать, что любой элемент в соединении следует рассматривать в отдельности, не учитывая его связей с другими веществами.
II группа главная подгруппа Периодической таблицы Менделеева (щелочноземельные металлы)
1 Общая характеристка щелочноземельных металлов
2 Нахождение в природе щелочноземельных металлов
3 Способы получения щелочноземельных металлов
4 Химические свойства щелочноземельных металлов
4. 1 Взаимодействие с простыми веществами — неметаллами
1 Взаимодействие с простыми веществами — неметаллами
4.2 Взаимодействие со сложными веществами
К щелочноземельным металлам относят химические элементы: двувалентные металлы, составляющие IIА группу:
Бериллий Be
магний Mg
кальций Ca,
стронций Sr,
барий Ba и
радий Ra.
Хотя бериллий Be по свойствам больше похож на алюминий, а магний Mg проявляет некоторые свойства щелочноземельных металлов, но в целом отличается от них.
Все щелочноземельные металлы — вещества серого цвета и гораздо более твердые, чем щелочные металлы.
Бериллий Be устойчив на воздухе. Магний и кальций (Mg и Ca) устойчивы в сухом воздухе. Стронций Sr и барий Ba хранят под слоем керосина.
Общая характеристка щелочноземельных металлов
От Be к Ra (сверху вниз в периодической таблице) происходит увеличение:
- атомного радиуса,
- металлических, основных, восстановительных свойств,
- реакционной способности.
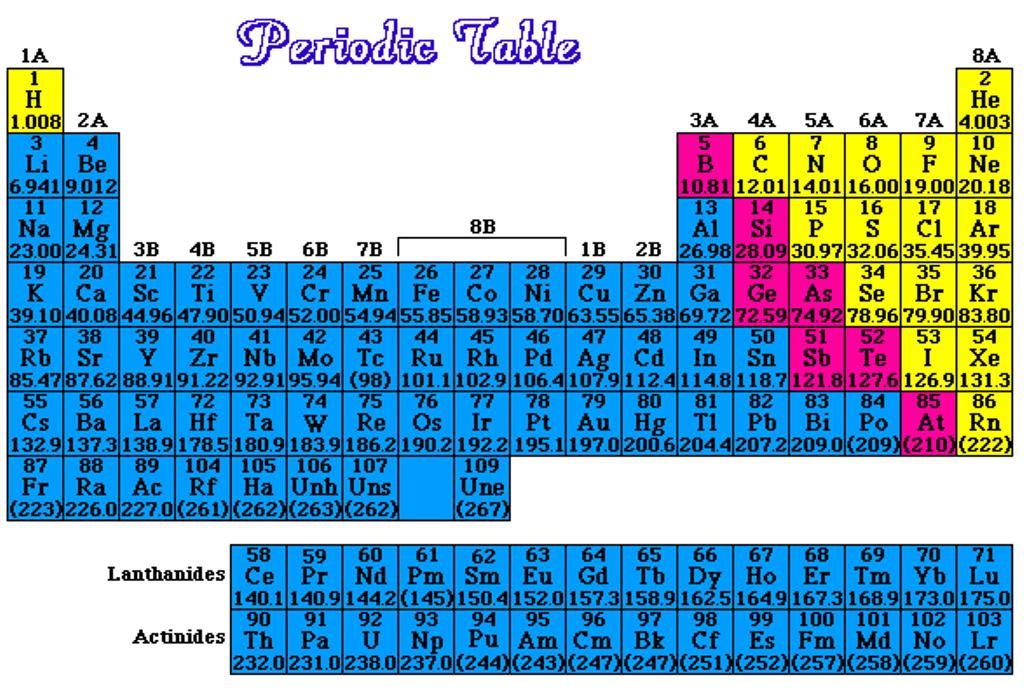
Уменьшается
- электроотрицательность,
- энергия ионизация,
- сродство к электрону.
Электронные конфигурации у данных элементов схожи, все они содержат 2 электрона на внешнем уровне ns2:
Be — 2s2
Mg —3s2
Ca — 4s2
Sr — 5s2
Ba — 6s2
Ra — 7s2
Нахождение в природе щелочноземельных металлов
Как правило, щелочноземельные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др.
Основные минералы, в которых присутствуют щелочноземельные металлы:
Способы получения щелочноземельных металлов
Магний
- Магний получают электролизом солей, чаще всего хлоридов: расплавленного карналлита (KCl·MgCl26H2O) или хлорида магния с добавками хлорида натрия при 720–750°С:
MgCl2 → Mg + Cl2
- восстановлением прокаленного доломита в электропечах при 1200–1300°С:
2(CaO · MgO) + Si → 2Mg + Ca2SiO4
Кальций
Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция:
CaCl2 → Ca + Cl2
Барий
Барий получают алюмотермическим способом — восстановление оксида бария алюминием в вакууме при 1200 °C:
4BaO+ 2Al → 3Ba + Ba(AlO2)2
Химические свойства щелочноземельных металлов
Качественные реакции
- Окрашивание пламени солями щелочных металлов
Цвет пламени:
Ca — кирпично-красный
Sr — карминово-красный (алый)
Ba — яблочно-зеленый
- Взаимодействие с веществами:
Взаимодействие с простыми веществами — неметаллами
С кислородом
С кислородом взаимодействуют при нагревании с образованием оксидов
2Сa + O2 → 2CaO
Видео Горение кальция
С галогенами
(F, Cl, Br, I)
Щелочноземельные металлы реагируют с галогенами при нагревании с образованием галогенидов .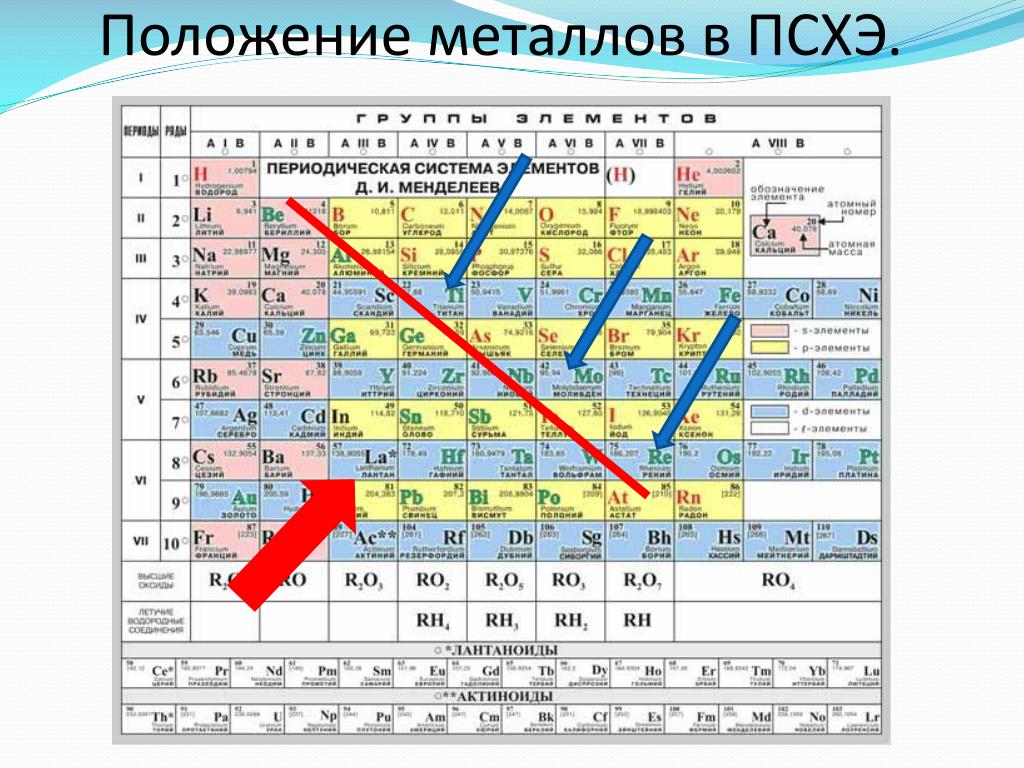
Сa + Cl2→ 2СaCl2
С водородом
Щелочноземельные металлы реагируют с водородом при нагревании с образованием гидридов:
Сa + H2 СaH2
Бериллий с водородом не взаимодействует.
Магний реагирует только при повышенном давлении:
Mg + H2 → MgH2
С серой
Щелочноземельные металлы при нагревании взаимодействуют с серой с образованием сульфидов сульфидов:
Сa + S СaS
Ca + 2C → CaC2 (карбиды)
С азотом
При комнатной температуре с азотом взаимодействует только магний с образованием нитрида:
6Mg + 2N2 → 2Mg3N2
Остальные щелочноземельные металлы реагируют с азотом при нагревании.
С углеродом
Щелочноземельные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов:
Ca + 2C → CaC2
Бериллий при нагревании с углеродом с образует карбид — метанид:
2Be + C → Be2C
С фосфором
Щелочноземельные металлы при нагревании взаимодействуют с фосфором с образованием фосфидов:
3Сa + 2P Сa3 P2
Взаимодействие со сложными веществами
С водой
Кальций, стронций и барий взаимодействуют с водой при комнатной температуре с образованием щелочи и водорода:
Sr + 2H2O → Sr(OH)2 + H2↑,
Магний реагирует с водой при кипячении, а бериллий с водой не реагирует.
С кислотами
- С растворами HCl, H2SO4, H3PO4 щелочноземельные металлы взаимодействуют с образованием соли и выделением водорода:
Са + H2SO4(разб)= СаSO4 + H2
- С кислотами-окислителями (HNO3 и конц. H2SO4):
с концентрированной серной:
4Ca + 10H2SO4(конц) → 4CaSO4 + H2S↑ + 5H2O;
с разбавленной и концентрированной азотной:
4Sr + 10HNO3(конц) → 4Sr(NO3)2 + N2O +5H2O
С водными растворами щелочей
В водных растворах щелочей растворяется только бериллий:
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
С солями
В расплаве щелочноземельные металлы могут взаимодействовать с некоторыми солями:
Ca + CuCl2 → CaCl2 + Cu
Запомните! В растворе щелочноземельные металлы взаимодействуют с водой, а не с солями других металлов.
С оксидами
Щелочноземельные металлы могут восстанавливать из оксидов такие неметаллы как кремний, бор, углерод:
2Ca + SiO2 → 2CaO + Si
Магний сгорает в атмосфере углекислого газа с образованием оксида магния и сажи (С):
2Mg + CO2 → 2MgO + C
Категории II группа (щелочноземельные металлы), НЕОРГАНИЧЕСКАЯ ХИМИЯ Метки барий, кальций, магний, щелочноземельные металлыПериодическая таблица металлов и неметаллов
Учебные пособия
- Сообщение от Доннелл Грин
12 Июль
Основные понятия
В этом уроке вы познакомитесь с металлами и неметаллами в периодической таблице элементов и их свойствами.
Темы, освещенные в других статьях
- Свойства металлов, неметаллов и металлоидов
- Ионные связи против.
 Ковалентные связи
Ковалентные связи - Сродство к электрону
- Электроотрицательность
- Металлическая связь
Металлы
Большинство элементов периодической таблицы элементов классифицируют себя как металлы. В периодической таблице металлы расположены слева от зигзагообразной линии, которая проходит между пятью элементами: бором, кремнием, мышьяком, теллуром и астатом. Элементы, попадающие на эту линию или чуть левее ее (бор, кремний, германий, мышьяк, теллур, сурьма и полоний), могут быть классифицированы как металлоиды или полуметаллы. Это означает, что они обладают свойствами как металлов, так и неметаллов.
Примеры металлов
Некоторые хорошо известные металлы периодической таблицы включают: железо, свинец, алюминий, серебро, кальций и натрий, которые находятся в твердом состоянии при комнатной температуре. Ртуть, классифицируемая как металл, является единственным металлом в периодической таблице, представленным в виде жидкости. Из ста восемнадцати металлов таблицы Менделеева золото является самым податливым. Вот почему ювелирные изделия никогда не могут быть на 100% чистым золотом, иначе они не выдержат повседневного износа.
Вот почему ювелирные изделия никогда не могут быть на 100% чистым золотом, иначе они не выдержат повседневного износа.
Свойства металлов
- Все металлы различаются по точкам плавления , но в целом все металлы имеют высокие температуры плавления и кипения.
- Большинство металлов представлены в виде твердых веществ при комнатной температуре, единственным исключением из этого правила является ртуть, поскольку она существует в жидком состоянии при комнатной температуре.
- Металлы блестящие по своей природе, то есть их поверхность блестящая. Медь — чрезвычайно блестящий металл.
- Металлы обычно более плотные, чем неметаллы.
- Как правило, металлы очень податливы , что означает, что их можно сбить в тонкие листы. Чистое золото — самый ковкий элемент.
- Металлы пластичны, это означает, что их можно раскатывать в тонкие листы.
- Наконец, металлы являются хорошими проводниками тепла и электричества.
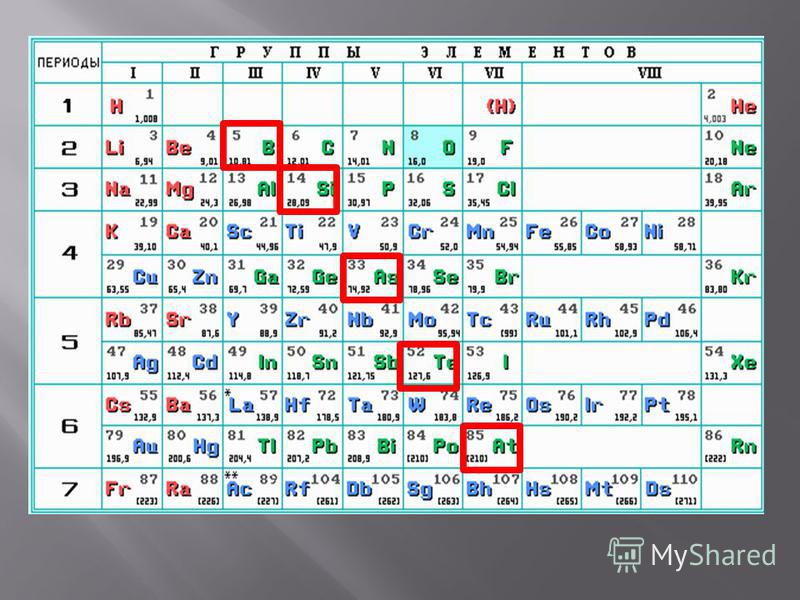
Металлы и их заряды
Поскольку металлы расположены слева от таблицы Менделеева, они часто имеют низкую энергию ионизации и низкое сродство к электрону, что означает, что они относительно легко отдают электроны, заставляя металлы становиться катионами. Металлы основной группы обычно образуют заряды, равные номеру их группы. Металлы группы 1А, такие как литий и натрий, имеют заряд +1, металлы группы 2А, такие как магний и кальций, имеют заряд +2.
Металлы, которые следуют за переходными металлами, могут терять свои s орбитальных и p орбитальных электронов и образовывать заряды, которые совпадают с номером их группы, или они могут терять свои p орбитальные электроны и сохранять свои два s орбитальных электроны; такие металлы, как олово и свинец в группе 4А, могут образовывать заряды +4 или +2. Когда эти металлы связываются с другими неметаллами, это известно как ионная связь, при которой происходит перенос электронов от одного вида к другому.
Неметаллы
Неметаллы составляют небольшую часть элементов периодической таблицы. В периодической таблице неметаллы лежат справа от зигзагообразной линии, которая проходит между элементами бором, кремнием, мышьяком, теллуром и астатом. Неметаллы также включают водород, который находится слева от металлоидов. Многие из этих элементов играют биологическую роль. Живые существа почти полностью состоят из неметаллов, таких как углерод или водород.
Это изображение не включает водород, который также является неметаллом.Примеры неметаллов
Хотя в периодической таблице всего семнадцать неметаллов, несколько распространенных примеров включают кислород и азот, которые составляют большую часть воздуха, которым мы дышим, наряду с несколькими другими газами, такими как неон или химическое вещество. сложный углекислый газ. Несвязывающие гелий, неон, радон, аргон, ксенон, криптон и оганесон, также известные как благородные газы, составляют часть неметаллов.
Свойства неметаллов
- Большинство металлов находятся в газообразное состояние, но вы можете найти некоторые в твердом или жидком состоянии.
 Как бром, который можно найти в виде жидкости.
Как бром, который можно найти в виде жидкости. - Как правило, неметаллы не блестящие или блестящие.
- Неметаллы имеют низкие температуры плавления и кипения.
- Часто присутствуют неметаллы с более низкой плотностью .
- В отличие от металлов, неметаллы часто являются очень плохими проводниками тепла и электричества.
Неметаллы и их сборы
Неметаллы обладают высокой энергией ионизации и высоким сродством к электрону, поэтому они могут легко приобретать электроны, но терять их с гораздо большими усилиями, поэтому их классифицируют как анионы. Они будут продолжать приобретать электроны до тех пор, пока их количество не станет таким же, как у ближайшего к ним инертного газа. Их сборы можно отнести к группе минус восемь. Таким образом, неметаллы в группе 7А имеют заряд -1, в группе 6А -2 заряда, а в группе 5А -3 заряда. Благородные газы в группе 8A уже имеют свой октет, поэтому они не решаются образовывать связи. Если два неметалла связаны, они образуют ковалентную связь; это происходит, когда пары электронов являются общими для атомов.
Если два неметалла связаны, они образуют ковалентную связь; это происходит, когда пары электронов являются общими для атомов.
Доннелл Грин
Доннелл Грин
Периодическая таблица – металлы, металлоиды и неметаллы
Металлы, металлоиды и неметаллы, о боже!
Трудно поверить, но мы уже прошли через огромный кусок таблицы Менделеева. До сих пор это было довольно просто: изучить столбец здесь, узнать о столбце там, при этом элементы одного и того же столбца имеют схожие свойства. Наша следующая остановка в этом химическом поезде — о веселье — р-блок. В этом разделе разделение элементов на столбцы так 2000 и поздно. Вместо этого p-блок разделен на металлы, металлоиды и неметаллы.
Металлы, металлоиды и неметаллы.
Вы когда-нибудь задумывались, что это за жирная зигзагообразная линия в правой части таблицы Менделеева? Кажется неуместным. Думайте об этом как о нулевом меридиане периодической таблицы. Он отделяет металлы в левой половине таблицы от неметаллов в правой части таблицы.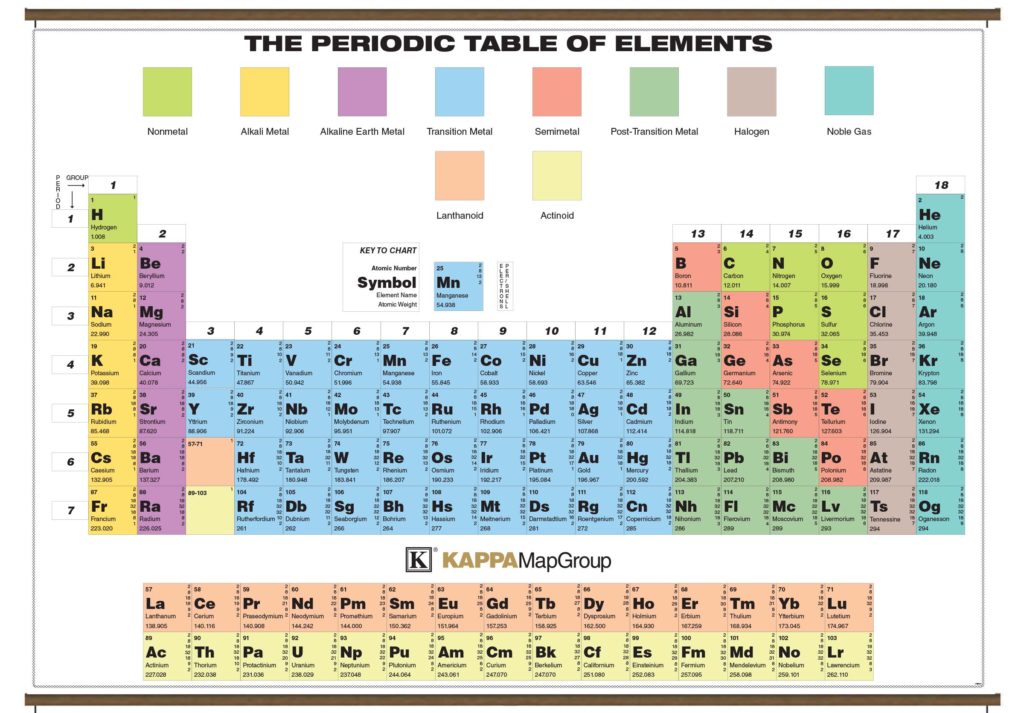 Конечно, на зигзаге есть такие надоедливые элементы, которые не совсем подходят ни к одной из категорий. Эти элементы получили название металлоидов.
Конечно, на зигзаге есть такие надоедливые элементы, которые не совсем подходят ни к одной из категорий. Эти элементы получили название металлоидов.
Элементами, удостоенными чести называться металлоидами, являются бор (B), кремний (Si), германий (Ge), мышьяк (As), сурьма (Sb), теллур (Te) и полоний (Po). Эти элементы обладают некоторыми свойствами, которые делают их похожими на металлы, и другими свойствами, которые делают их неметаллоподобными. По этой причине эти элементы типа Франкенштейна также называют полуметаллами или полупроводниками.
Значения электроотрицательности и энергии ионизации металлоидов находятся между металлами и неметаллами. По этой причине они обладают некоторыми характеристиками металлов и некоторыми характеристиками неметаллов. Возьмем, к примеру, кремний (Si). Он блестящий и серебристый, как обычный металл, но он хрупкий и плохо проводит электричество. Это так запутано.
Кремний: блестящий и серебристый, но это не металл. Это металлоид.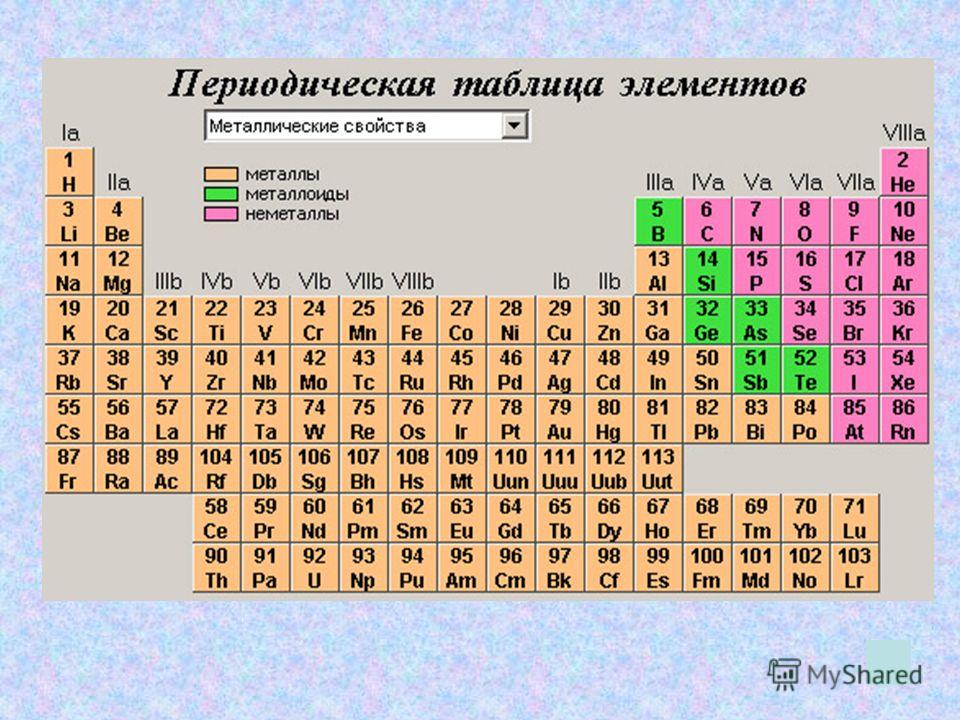
Хорошо, а реактивность? Реагируют ли металлоиды так же, как их металлические соседи или их неметаллические соседи? Правда в том, что это зависит от элемента, с которым они реагируют. Бор, например, реагирует как металл при взаимодействии с фтором, но как неметалл при взаимодействии с натрием.
Бор, металлоид, становится зеленым при попадании в пламя.
Металлоиды играют важную роль в нашей повседневной жизни. Электричество и тепло могут проходить через металлоиды, но не так легко, как через настоящие металлы. Вот почему металлоиды часто называют полупроводниками , особенно германий и кремний. Можете ли вы угадать, что является основным компонентом современной электроники, телефонов, компьютеров и радиоприемников? Правильно, полупроводники. Мы поговорим об этих модных устройствах позже.
Металлоиды (или полупроводники) являются важными компонентами электронных устройств.
Металлоиды имеют и другие применения. Например, сурьма используется в таких сплавах, как олово, и в качестве антипирена в пластмассах.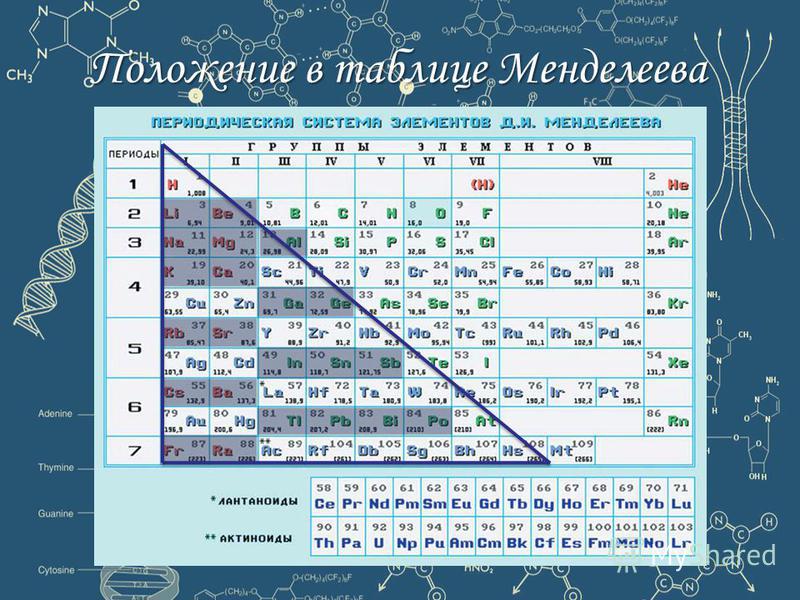 Бор используется в качестве связующего вещества в магнитах и других химических веществах. Связующее вещество? Это способ сказать, что бор помогает вещам склеиваться.
Бор используется в качестве связующего вещества в магнитах и других химических веществах. Связующее вещество? Это способ сказать, что бор помогает вещам склеиваться.
Бор используется в качестве связующего в оловянной посуде.
Хватит уже говорить о металлоидах — давайте перейдем к обсуждению их ближайших соседей — металлов. Вот так. Переходные металлы — не единственные металлы на столе. Р-блок имеет свой набор металлов, расположенных слева от металлоидов. Этими металлами являются алюминий (Al), галлий (Ga), индий (In), олово (Sn), таллий (Tl), свинец (Pb) и висмут (Bi).
Эти металлы твердые, блестящие и хорошо проводят электричество и тепло — все свойства, которые мы обычно связываем с металлами. Они также пластичны и ковки , что означает, что их можно вытягивать в тонкую проволоку и забивать в тонкие листы. Как и их аналоги из переходных металлов, эти элементы имеют тенденцию довольно легко терять (и, следовательно, проводить) электроны.
Алюминий является одним из этих металлов. Мы все знакомы со старым добрым Элом (Z = 13). Алюминиевая фольга, кто-нибудь? Он серебристо-белого цвета и очень светоотражающий. Алюминий используется для изготовления самолетов и зданий, потому что он прочно сочетается с другими элементами, образуя очень прочные и долговечные материалы. Он также довольно нетоксичен, поэтому мы можем заворачивать в него наши буррито и есть с ним, не заболевая. Мы по-прежнему не рекомендуем есть алюминий. В достаточно высоких дозах он может вас убить.
Нужен перерыв в учебе? Кошки тоже любят алюминиевую фольгу. Проверьте это. Это тоже.
Другим металлом р-блока является свинец (Pb, Z = 82). Его химический символ происходит от латинского слова plumbum , , что означает водопровод. Кажется ужасно случайным, но Pb веками использовался для изготовления водопроводных труб. Даже древние римляне использовали этот мягкий, ковкий и устойчивый к коррозии металл в своих водопроводных системах. К сожалению, свинец может накапливаться в организме человека и вызывать серьезные проблемы со здоровьем. Просто спросите Безумного Шляпника.
К сожалению, свинец может накапливаться в организме человека и вызывать серьезные проблемы со здоровьем. Просто спросите Безумного Шляпника.
Справа от металлоидной лестницы находится совершенно новая марка элементов… неметаллов . Сейчас мы обсудим только углерод (C), азот (N), кислород (O), фосфор (P), серу (S) и селен (Se). Последние две строки периодической таблицы, галогены и благородные газы , также являются неметаллами, но мы рассмотрим их в следующих двух разделах.
Свойства неметаллов противоположны свойствам металлов. Неметаллы любовь электронов, особенно те, которые у них уже есть, что означает, что они имеют высокие энергии ионизации и высокую электроотрицательность. Их большое сродство к электрону означает, что они способны легко получать электроны. Вы можете назвать их электронными свиньями.
Неметаллы обладают высоким сродством к электрону. Они электронные свиньи.
В отличие от металлов неметаллы плохо проводят тепло и электричество. Они ломкие и обычно тусклого цвета. Звучат скучно, но на самом деле они самые крутые.
Углерод (C, Z = 6) — один из наименее скучных элементов в периодической таблице. Это шестой по распространенности элемент на Земле и основа органической химии; это происходит во всех живых организмах. 11 Вы когда-нибудь задумывались, что общего между вами и слизнем? Углерод.
Элементарный углерод может существовать как одно из самых твердых веществ на Земле (алмазы), а также как одно из самых мягких веществ на Земле (графит). Человечеству известно огромное количество способов использования углерода: карандаши, смазки, средства для удаления запахов, радиоуглеродное датирование… этот список можно продолжить.
Важным неметаллом, с которым мы все знакомы, является кислород (O, Z = 8). Кислород является третьим по распространенности элементом во Вселенной и составляет 21% атмосферы Земли. 11 Это бесцветный газ без запаха и вкуса, но он необходим для жизни человека. В твердой и жидкой фазе кислород бледно-голубой, сильно парамагнитный (по сути, он магнитный…) и взрывоопасный. Кто знал, что кислород так опасен?
В твердой и жидкой фазе кислород бледно-голубой, сильно парамагнитный (по сути, он магнитный…) и взрывоопасный. Кто знал, что кислород так опасен?
Последний неметалл, о котором мы поговорим, это сера (S, Z = 16). Это бледно-желтое хрупкое твердое вещество без запаха. Однако некоторые из комплексов, которые он образует, такие как газообразный H 2 S очень вонючие. Если вам когда-нибудь представится возможность понюхать H 2 S, не делайте этого. Пахнет тухлыми яйцами.
Закуска для мозгов
Любите веселые интернет-видео? Вы тоже любите элементы? Если вы ответили утвердительно на оба этих вопроса, тогда посетите этот сайт. Он содержит забавные и информационные видеоролики о каждом элементе. Если вы ответили «нет» на любой из этих вопросов, все равно проверьте их. Обещаем, вы не пожалеете, если посмотрите их.
39.ПЕРИОДИЧЕСКАЯ ТАБЛИЦА – Металлы. – Мадоверхимия
В нашем последнем сообщении мы представили современную форму или полную форму периодического. Давайте теперь начнем изучать таблицу более подробно.
Давайте теперь начнем изучать таблицу более подробно.
Мы изучили, что периодическая таблица элементов содержит элементы. Но что такое элементы?
Элементы являются первичными составляющими материи, которые не могут быть далее разделены на другие вещества никаким физическим или химическим процессом.
В отличие от соединений , которые могут быть преобразованы в исходные элементы химическим способом.
например- Поваренная соль, т. е. NaCl, может быть преобразована в натрий (Na) и хлор (Cl) с помощью электролитического процесса. Натрий и хлор являются элементами.
Элементы можно классифицировать по их состоянию (при комнатной температуре и нормальном давлении)-
- Более 100 элементов находятся в твердом состоянии.
- Одиннадцать находятся в газообразном состоянии.
- Два в жидком состоянии – бром и ртуть.

Франций, Цезий, Галлий, Рубидий.
Далее, элементы периодической таблицы можно разделить на 3 основные категории, а именно – МЕТАЛЛЫ, НЕМЕТАЛЛЫ и металлоиды. Большинство периодической таблицы занимают металлы. Есть несколько металлоидов, а остальные не- металлы.
МЕТАЛЛЫ .
Металлы — это элементы, которые обычно являются твердыми и образуют положительные ионы, теряя электроны в химической реакции, и в которых атомы связаны друг с другом металлическими связями. Слово “металл” происходит от греческого слова “9”.0017
Сначала обсудим природу металлических связей.
Различные атомы в металле удерживаются вместе силой, известной как металлическая связь .
Как вы можете видеть на соседнем рисунке, внешние/валентные электроны металла слабо связаны с ядром и поэтому могут свободно перемещаться по металлической решетке. Эти электроны являются общими для всех атомов. электроны также называют ‘
Свойства металлов –
1) Металлы имеют сравнительно меньшее количество валентных электронов, поэтому они, как правило, являются донорами электронов .0078 склонность к образованию положительных ионов.
например,
1. Na → Na + + e – .
Na → Na + + e – .
2.Al → Al 3+ + 3e – .
2) Металлы имеют блеск т.е. они блестящие. Слово «ЛЮКС» означает «свет/сияние» на латыни. серебряные поверхности блестят. Медные сосуды тоже имеют блестящую поверхность.
Медные пломбы
Золотые блоки.
Свободные электроны в металлическом кристалле ответственны за этот блеск. Падающий свет вызывает колебания свободных электронов, которые, в свою очередь, производят свой собственный свет. Мы видим это как блеск. Некоторые металлы теряют свой блеск из-за их взаимодействия с воздух, вода или углерод. Таким образом, они образуют соединения (например, оксиды) и тускнеют или ржавеют. Когда эту ржавчину удаляют, мы получаем блестящую металлическую поверхность. Посмотрите следующее видео, чтобы узнать, как это происходит –
Ржавая поверхность не блестит, так как свободные электроны вступают в реакцию и больше не могут отражать падающий свет.
3) Металлы ковкие т.е. их можно вытягивать в листы. Мы уже изучали эксперимент Эрнеста Резерфорда с золотой фольгой. Тонкая золотая фольга может быть получена в результате этого свойства металлов. Мы даже используем алюминиевую фольгу на нашей кухне ежедневно. Можно создавать металлические листы/фольгу, поскольку они способны выдерживать давление во время процесса ковки.
Итак, металл не ломается, а гнется. Я уверен, что вы заметили вмятину на корпусе автомобиля (из металла) после удара. Металлический корпус от удара гнется, но почти не ломается.
Металлы податливы, так как слои атомов в металлической связи могут скользить друг по другу, когда металл изгибается. Это возможно, потому что металлическая связь является ненаправленной — одинаковой во всех направлениях.
4) Металлы пластичны, т.е. они могут деформироваться (но не ломаться) под действием растягивающего напряжения и могут быть вытянуты в провода.
( Примечание. Растягивающее напряжение/сила противоположны сжимающей силе. Это сила, которая растягивает вдоль оси точно так же, как люди тянут за веревку в перетягивании каната. На рисунке ниже прочность на растяжение показана бирюзовым цветом. стрелки).
Растягивающее напряжение/сила противоположны сжимающей силе. Это сила, которая растягивает вдоль оси точно так же, как люди тянут за веревку в перетягивании каната. На рисунке ниже прочность на растяжение показана бирюзовым цветом. стрелки).
Это свойство металлов также является результатом их структуры. Поскольку слои атомов скользят друг по другу, не ломаясь, металлы легко вытягиваются в провода под действием растягивающего напряжения. Это свойство очень полезно, так как металлические провода используется для проведения электричества. В основном все электроприборы, электропроводка в наших домах сделаны из металлических проводов. Эти провода имеют покрытие из ПВХ (поливинилхлорида), чтобы предотвратить поражение пользователя электрическим током.
Металлические проволоки с ПВХ покрытием. 5)Все металлы являются хорошими проводниками тепла и электричества .Свободные, делокализованные электроны в металлическом кристалле помогают эффективно проводить тепло и электричество. Поскольку эти электроны могут свободно перемещаться через металлическую структуру, электричество и тепло также могут течь через металлы без усилий.
Поскольку эти электроны могут свободно перемещаться через металлическую структуру, электричество и тепло также могут течь через металлы без усилий.
Когда металл соединяется с элементом/батареей, электроны отталкиваются от отрицательной клеммы и начинают течь к положительной клемме элемента/батареи. Это генерирует электрический ток. Серебро является лучшим проводником электричества, т.е. самая высокая электропроводность. Следующим лучшим проводником является медь, и большинство токопроводящих проводов изготовлены из меди, поскольку она намного экономичнее, чем серебро. .
Точно так же, когда тепло передается металлу на одном конце, тепло заставляет свободные электроны быстро колебаться и, таким образом, их кинетическая энергия увеличивается. Электроны передают энергию колебаний более холодному концу, таким образом проводя тепло в процесс.
6) Металлы имеют высокие температуры плавления и кипения по сравнению с неметаллами в том же ряду . Это свойство можно приписать металлам из-за высокой прочности металлической связи. Сильная сила электростатического притяжения между положительные ядра и свободные отрицательные электроны делают металлическую связь достаточно прочной, и поэтому для ее разрыва требуется большое количество энергии.
Это свойство можно приписать металлам из-за высокой прочности металлической связи. Сильная сила электростатического притяжения между положительные ядра и свободные отрицательные электроны делают металлическую связь достаточно прочной, и поэтому для ее разрыва требуется большое количество энергии.
Металл | Температура кипения | Неметалл | Температура кипения |
Натрий | 882,8 °С | Хлор | -34,04 °С |
Калий | 758,8 °С | Бром | 58,8 °С |
Висмут | 1564 °С | Астатин | 336,8 °С |
Металл | Температура плавления | Неметалл | Температура плавления |
Натрий | 97,79 °С | Хлор | -101,5 °C |
Калий | 63,5°С | Бром | -7,2°С |
Барий | 727 °С | Астатин | 301,8 °С |
Среди металлов галлий, цезий, натрий и калий имеют низкие температуры плавления -30°C, 28°C, 98°C и 64°C соответственно. Галлий и цезий могут плавиться в руках из-за температуры нашего тела.
Галлий и цезий могут плавиться в руках из-за температуры нашего тела.
7) Металлы звонкие т.е. они издают глубокий звук при ударе. Именно благодаря этому свойству металлы используются для изготовления колоколов. Колокола в Индии состоят из смеси пяти металлов (панчдхату) – свинец, медь, цинк, железо и олово в определенных пропорциях, которые создают гулкий звук, эхо которого длится 7 секунд, достаточно, чтобы коснуться семи чакр в нашем теле.
При ударе по металлу свободное облако электронов возмущается, и кинетическая энергия легко распространяется через них в виде волны из-за их делокализованной природы. Звук возникает, поскольку металлическая связь эластична по своей природе. Электроны раскачиваются из-за удара, и это раскачивающееся движение передается воздуху вокруг металла. Раскачивающееся движение воздуха вызывает звук.
8) Все металлы, кроме ртути (которая является жидкостью) являются твердыми при комнатной температуре . Они твердые, имеют высокую плотность.Хотя натрий и калий мягкие металлы и их можно резать ножом. Я уверен, что многие из вас имели дело с натрием в своих химических лабораториях — взяли кусочек натрия, который содержится в керосине, и разрезали его ножом.
Они твердые, имеют высокую плотность.Хотя натрий и калий мягкие металлы и их можно резать ножом. Я уверен, что многие из вас имели дело с натрием в своих химических лабораториях — взяли кусочек натрия, который содержится в керосине, и разрезали его ножом.
9) Металлы образуют основные оксиды в отличие от неметаллов.
например- Натрий образует гидроксид натрия (NaOH) в воде, которая является щелочной по своей природе. Оксиды металлов обычно образуют гидроксиды в воде и производят OH – ионов, что делает их основными по природе.
Na2O + h3O → 2NaOH
NaOH диссоциирует в воде с образованием ионов OH –.
В зависимости от их положения в таблице Менделеева металлы можно разделить на –
- Щелочные металлы – Группа I
- Щелочноземельные металлы – Группа II
- Переходные металлы
- Лантаниды/редкоземельные металлы
- Актиниды.
Итак, теперь у нас есть четкое представление о том, что такое металлы и их свойства.


