Мезомерный эффект
Мезомерный эффект (М-эффект)
В отличие от индуктивного эффекта, передаваемого заместителем по σ-связям, в
соединениях с сопряжёнными кратными связями основную роль играют электроны делокализованных π-связей.
Смещение электронной плотности по сопряжённой π-системе называют мезомернымOт греч. mesos — средний, промежуточный
и meros — часть. эффектом или эффектом сопряжения.
Мезомерный эффект (M-эффект) — передача электронного влияния заместителя по цепи делокализованных π-связей сопряжённой системы.
М-эффект может проявлять заместитель, если он связан с sp2– или sp-гибридизованным атомом и сам участвует в системе сопряжения, предоставляя
π-связьC=O, C=N, C=C, N=O, C≡С, C≡N и т.п. или р-орбиталь.Негибридизованная p-орбиталь sp2-атома в структуре заместителя может содержать электронную пару, один электрон или быть вакантной.
По направлению смещения электронной плотности различают положительный (+М) и отрицательный (–М) эффекты заместителей. Знак М-эффекта зависит от природы заместителя и способа его сопряжения с π-системой.
Структурные фрагменты сопряжённых систем
Примеры
Для определения направления
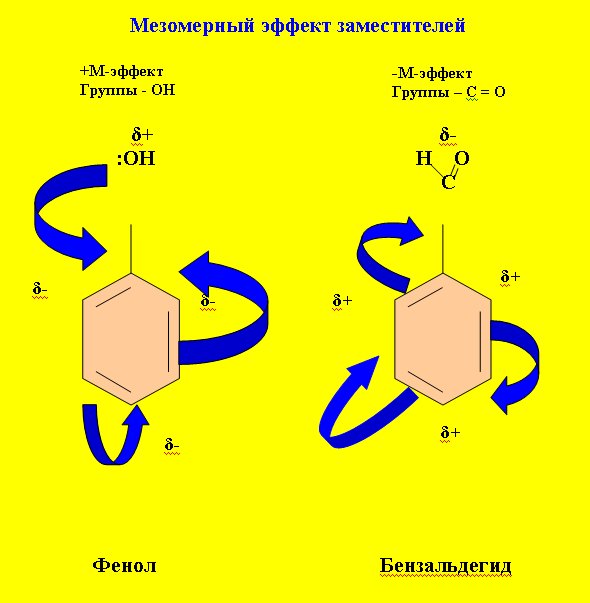
+М-эффект характерен для заместителей, повышающих электронную плотность в сопряжённой системе.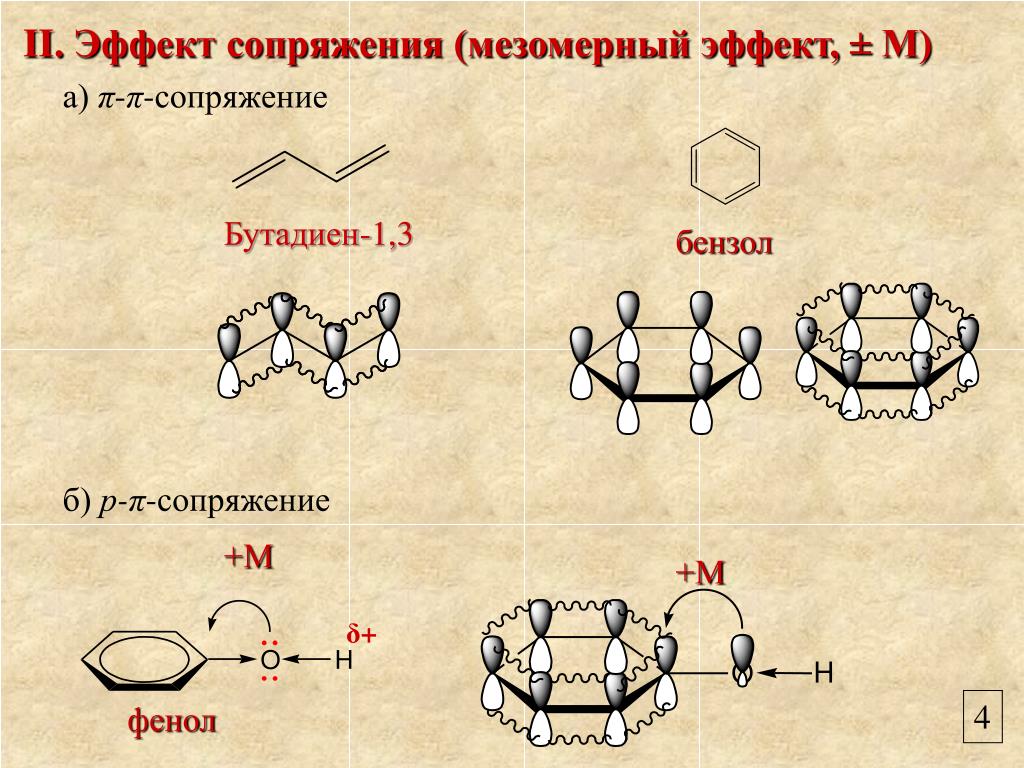 К ним относятся электронодонорные группы, которые содержат атом с неподелённой электронной парой, способный её передать в общую систему сопряжения. Такими группами являются: –OH,–OR, –NH
К ним относятся электронодонорные группы, которые содержат атом с неподелённой электронной парой, способный её передать в общую систему сопряжения. Такими группами являются: –OH,–OR, –NH
Пример. Группа –OH в молекуле фенола C6H5OH проявляет +М-эффект за счёт участия одной из неподелённых электронных пар sp2-атома кислорода в системе сопряжения. Как показано на АО-модели, это обусловлено перекрыванием негибридизованной p-орбитали атома кислорода, содержащей электронную пару, с π-системой бензольного кольца (p,π-сопряжение).
Анимация
–М-эффект проявляют заместители, содержащие электроотрицательные атомы и понижающие электронную плотность в сопряженной системе. Такими свойствами обладают
 п. В катионах типа М-эффект отсутствует, так как положительно заряженный sp3-атом азота не имеет p-орбитали (АО-модель).
п. В катионах типа М-эффект отсутствует, так как положительно заряженный sp3-атом азота не имеет p-орбитали (АО-модель).Пример. Для группы С=О в бензальдегиде C6H5CH=O характерен –М-эффект, что объясняется смещением электронов в сторону электроотрицательного атома кислорода при перекрывании π-орбитали полярной связи Cδ+=Oδ– и
Анимация
В данном случае p-орбитали атомов сопряжённой системы и sp2-орбитали атома кислорода с неподеленными парами электронов расположены взаимно перпендикулярно, то есть их π-перекрывание невозможно. Поэтому ни одна электронная пара кислорода не может передаваться в π-систему.
- Величина М-эффекта растет с увеличением заряда заместителя.
 Ионы проявляют поэтому наиболее сильный
Ионы проявляют поэтому наиболее сильный - –М-эффект заместителей тем сильнее, чем больше электроотрицательность имеющихся в заместителе элементов:
- –М-эффект заместителей тем сильнее, чем меньше их внутренняя мезомерия (делокализация электронов), например:
Группа С=О в этом случае связана с группировками, +М-эффект которых в ряду O–, NH2, OH, OR уменьшается и, наконец, для CH3 и Н – равен нулю. В хлорацильной группе -C(O)Cl атом хлора проявляет +М-эффект, однако он значительно слабее –I-эффекта (так как мезомерное взаимодействие невелико вследствие относительно малой степени перекрывания существенно различающихся орбиталей – 2 - +М-эффект заместителя тем сильнее, чем меньше электроотрицательность гетероатома, входящего в его состав:
-C≡CR < -C≡N < -NO2;
-BR2 < -AlR2.
В соответствии с указанными правилами, следующие заместители по знаку и силе мезомерного эффекта можно расположить в ряд:
| NO2 > CN > CO > COOH | H | Br < Cl < OCH3 < OH < NH2 < O– |
| (–M) акцепторы электронов | (+M) доноры электронов |
- К разновидности положительного мезомерного эффекта относят также довольно слабое электронное взаимодействие –

как понять и решать. Видео
Как понять органическую химию с нуля? Учите ее вместе с нами!
Химия… Как много в этом слове, не так ли? Не переживайте, дорогие студенты, мы сделаем все, чтобы максимально понятно донести до вас всю суть этого странного инопланетного предмета так, чтобы хотя бы сдать сессию.
И сегодня темой нашего обсуждения становится индукционный или индуктивный эффект, который довольно непонятно описывают разные книги по органической химии с нуля (даже те, что для чайников).
Карты на стол: что такое I-эффект?
Учим органическую химию с нуля – так легче!
Из школьных уроков химии мы выяснили (или должны были выяснить), что ковалентная связь возникает лишь среди атомов с разной электроотрицательностью.
Имеющаяся в молекуле полярная сигма-связь способствует поляризации ближайших 2-3-х сигма-связей, что приводит к образованию частичных зарядов дельта плюс или дельта минус на соседних атомах.
Прямые стрелки по линии связи, а также индуцируемые заместителем символы частичных зарядов показывают направление смещения электронной плотности всех сигма-связей.
Так получается, что Х(Y)-заместители способствуют поляризации не только собственной связи, но и соседних.
Данный вид влияния атомов приводит к поляризации ковалентных связей, а также к индуцированию зарядов на атомах, благодаря чему процесс и получил название индукционного (индуктивного) эффекта.
Индукционный (индуктивный) эффект – сдвижение электронной плотности по цепи сигма-связей из-за различий электроотрицательности атомов.
А так как поляризуемость сигма-связей слабая, индукционный эффект довольно быстро пропадает, постепенно удаляясь от заместителя. Так что уже к третьей-четвертой связи он становится практически нулевым.
Когда индукционный эффект называют отрицательным и положительным?
Как вы видите, индукционный эффект может быть положительным и отрицательным.
В первом случае заместитель будет увеличивать электронную плотность на атоме углерода, образуя (или вырабатывая) на нем частично отрицательный заряд. А тем временем сам он приобретает положительный заряд.
А тем временем сам он приобретает положительный заряд.
Во втором случае (то есть при индукционномэффекте со знаком минус) заместитель будет уменьшать электронную плотностьна атоме углерода, с которым наш с вами заместитель собственно и связан. В это время у заместителя образуется частичный отрицательный заряд (дельта-), а у атома углерода – частично положительный (дельта+).
Направление (то есть определяющий знак – минус или плюс) индукционного эффекта заместителя можно оценить при сравнивании с атомом водорода, чей индукционный эффект равен нулю:
- Отрицательный индукционный эффект проявляется у заместителей, чьи атомы гораздо более электроотрицательные, нежели атомы углерода
- Положительный индукционный эффект проявляется у заместителей, в которых есть атомы с низкой электроотрицательностью.
Вот, в принципе и вся органическая химия индукционного эффекта. С нуля вы можете просмотреть традиционно подобранный нами по этой теме видеоурок для «чайников»:
И совершенно не обязательно сидеть и читать днем и ночью учебник по органической химии, чтобы понять какие-то сложные понятия – мы будем помогать вам разбираться в сложных понятиях. А как понять органическую химию с нуля, если вам на днях предстоит сложнейший экзамен или контрольная? Ну и тут все просто – не надо понимать, надо обратиться за помощью к тем, кто всегда рядом – к нашим авторам, знающим о химии все! Купить недорого курсовую работу на заказ вы всегда можете обратившись в Заочник.
А как понять органическую химию с нуля, если вам на днях предстоит сложнейший экзамен или контрольная? Ну и тут все просто – не надо понимать, надо обратиться за помощью к тем, кто всегда рядом – к нашим авторам, знающим о химии все! Купить недорого курсовую работу на заказ вы всегда можете обратившись в Заочник.
Автор: Наталья
Наталья – контент-маркетолог и блогер, но все это не мешает ей оставаться адекватным человеком. Верит во все цвета радуги и не верит в теорию всемирного заговора. Увлекается «нейрохиромантией» и тайно мечтает воссоздать дома Александрийскую библиотеку.
электронных эффектов | bartleby
Что такое электронные эффекты?
Эффект электронов, находящихся в химических связях внутри атомов молекулы, называется электронным эффектом. Электронный эффект также объясняется как эффект, посредством которого реакционная способность соединения в одной части контролируется отталкиванием или притяжением электронов в другой части молекулы.
Электронный эффект также объясняется как эффект, посредством которого реакционная способность соединения в одной части контролируется отталкиванием или притяжением электронов в другой части молекулы.
Электронный эффект влияет на реакционную способность, свойства и структуру соединения. Связь между электронной структурой и геометрией соединения можно также подчеркнуть с помощью термина «стереоэлектронный эффект».
Типы электронных эффектов
Электронные эффекты делятся на четыре различных типа, включая:
- Индуктивный эффект.
- Мезомерный эффект или эффект резонанса.
- Электромерный эффект.
- Гиперконъюгация.
Индуктивный эффект
При индуктивном эффекте постоянный диполь образуется в соединении неэквивалентным распределением связывающих электронов двух атомов (разных атомов) в молекуле. Индуктивный эффект в основном возникает в сигма-связях. Поляризация, созданная в этом эффекте, постоянна.
Подразделы индуктивного эффекта
Индуктивный эффект можно разделить на два типа:
- -I эффект.
- +I эффект.
-I эффект
Если в цепь ввести электроотрицательный атом, такой как галоген, он состоит из атомов углерода, которые создадут положительный заряд из-за неравномерного распределения электронов, и этот положительный заряд передается по цепи .
Это создаст постоянный дипольный момент в соединении, где атом, богатый электронами, содержит -ve заряд. Это называется электроноакцепторным индуктивным эффектом или эффектом -I.
+I эффект
При добавлении заместителя, высвобождающего электроны, например, алкильного заместителя, к цепи, содержащей атомы C, заряд будет передаваться по цепи. Это эффект +I.
Прогнозирование основности и кислотности с помощью индукционного эффекта
Основность и кислотность молекулы можно определить с помощью индукционного эффекта. Кислотность соединения снижается за счет электронодонорного заместителя и увеличивается за счет электроноакцепторного заместителя.
Пример
Когда мы рассматриваем RCOO –, заместителем, высвобождающим электроны, считается R, тогда сопряженное основание дестабилизируется из-за межэлектронного отталкивания. Когда электроноакцепторным заместителем считается R, то сопряженное основание стабилизируется за счет делокализации образовавшегося отрицательного заряда.
Когда электроноакцепторным заместителем считается R, то сопряженное основание стабилизируется за счет делокализации образовавшегося отрицательного заряда.
Мезомерный эффект
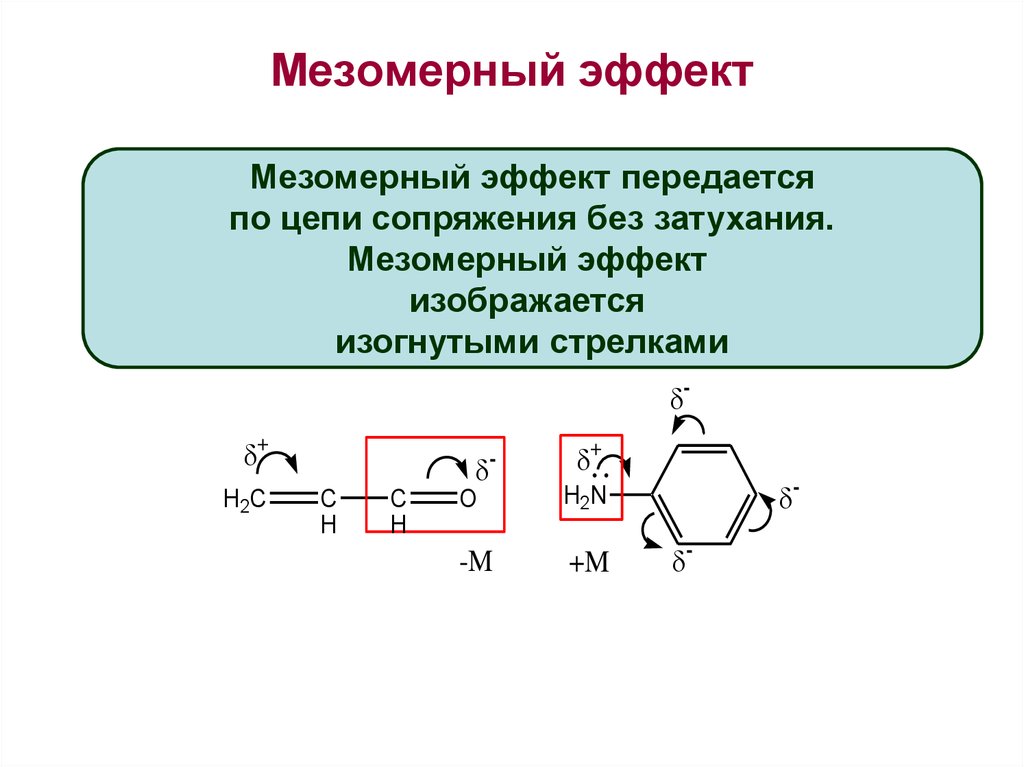
За счет переноса π электронов внутри атомов резонансной системы формируется полярность. Этот эффект называется мезомерным эффектом. Этот эффект возникает, если π-электроны удаляются или приближаются к заместителю в сопряженном орбитальном расположении. На рисунке ниже показан мезомерный эффект.
Мезомерный эффект можно классифицировать следующим образом:
- +М эффект.
- -М эффект.
+М эффект
Плотность электронов в сопряженной структуре увеличивается, когда π электронов из определенной группы направляются в сопряженную систему. Эта сопряженная система проявляет меньшую реакционную способность по отношению к нуклеофилу и большую реакционную способность по отношению к электрофилам. Это называется эффект +М. На рисунке ниже показан эффект +M.
Чтобы подвергнуться мезомерному эффекту, группа должна содержать -5 заряд или неподеленную пару электронов.
Заместители, проявляющие положительный мезомерный эффект:
-NH, -NH 2 , -NHR, -NR 2 -O, -OH, -OR, -F, -Cl, -O-COR , -NHCOR, -SH, -SR и т. д.
-M-эффект
Плотность электронов в сопряженной структуре уменьшается, когда π-электроны смещаются из сопряженной структуры в определенную группу. В эффекте –М соединение проявляет меньшую реакционную способность в присутствии электрофила и высокую реакционную способность в присутствии нуклеофила. Это называется эффектом –М. На рисунке ниже показан эффект –M.
Для осуществления мезомерного эффекта заместитель должен содержать либо положительный заряд, либо вакантную орбиталь.
Заместители, проявляющие эффект –М:
-NO 2 ,-CN,-COX,-SO и т.д.
Электромерный эффект
Электромерный эффект – это эффект, при котором происходит абсолютный сдвиг π электронной пары из-за удара нуклеофила или электрофила. Электронный эффект является обратимой реакцией. При выводе атакующего реагента этот эффект исчезнет. Этот эффект возможен только при наличии реагента удара электронов. Электромерный эффект наблюдается в органических соединениях, имеющих хотя бы одну кратную связь. Если атом, участвующий в этих множественных связях, принадлежит управляющему ударному реагенту, одна π-связывающая пара электронов полностью перемещается к одному из 2 атомов.
При выводе атакующего реагента этот эффект исчезнет. Этот эффект возможен только при наличии реагента удара электронов. Электромерный эффект наблюдается в органических соединениях, имеющих хотя бы одну кратную связь. Если атом, участвующий в этих множественных связях, принадлежит управляющему ударному реагенту, одна π-связывающая пара электронов полностью перемещается к одному из 2 атомов.
Подразделы электромерного эффекта
Электромерный эффект подразделяется на два класса, которые зависят от направления переноса электронной пары. Два типа:
- +E эффект.
- -E эффект.
+E-эффект
Если электронная пара, находящаяся в связи, переносится в сторону ударника, то это называется +E-эффектом. Эффект +Е возникает из-за присоединения кислоты к алкенам. Этот эффект обычно возникает, если ударяющий реагент является электрофилом, а π-электроны перемещаются в положительно заряженные атомы. Например, при протонировании этена будет иметь место эффект +Е, который проявляется следующим образом:
-Э Эффект
Если электронная пара, расположенная в π-связи, переносится от ударника, то это называется -Э эффектом. В случае эффекта –E ударный реагент соединяется с + сильно заряженным атомом, находящимся в соединении, то есть с атомом, который теряет пару электронов при переносе. Если ударным реагентом является нуклеофил, то будет иметь место эффект –E. Эффект –Э возникает при внедрении нуклеофилов в карбонильные соединения. На рисунке ниже показан эффект –E.
В случае эффекта –E ударный реагент соединяется с + сильно заряженным атомом, находящимся в соединении, то есть с атомом, который теряет пару электронов при переносе. Если ударным реагентом является нуклеофил, то будет иметь место эффект –E. Эффект –Э возникает при внедрении нуклеофилов в карбонильные соединения. На рисунке ниже показан эффект –E.
Гиперконъюгация
Гиперконъюгация — это эффект, при котором локализация электронов группы С-Н алкильного заместителя непосредственно связана с атомом ненасыщенного соединения. Эта гиперконъюгация в основном полезна для стабилизации карбокатиона и помогает в распределении положительного заряда. Следовательно, чем больше число алкильных заместителей, связанных с атомом углеродсодержащего положительного заряда, тем выше будет гиперсопряжение, что приведет к большей стабилизации карбокатиона. На основе гиперконъюгации стабильность карбокатиона обозначена на рисунке следующим образом:
Сравнение стерического эффекта с электронным эффектом
Стерический эффект является несвязывающей реакцией, тогда как электронный эффект представляет собой связывающее взаимодействие. Это основное различие между стерическим эффектом и электронным эффектом. Электронный эффект выражает влияние электронов, находящихся в химических связях внутри атомов молекулы, тогда как стерический эффект выражает воздействие электронов, не участвующих в химической связи, но возникающих за счет неподеленной пары электронов или несвязывающих электроны. Стерический эффект контрастирует с электронным эффектом, подразумевающим влияние таких эффектов, как соединение, индукция, электростатическое взаимодействие, орбитальная симметрия и спиновое состояние.
Это основное различие между стерическим эффектом и электронным эффектом. Электронный эффект выражает влияние электронов, находящихся в химических связях внутри атомов молекулы, тогда как стерический эффект выражает воздействие электронов, не участвующих в химической связи, но возникающих за счет неподеленной пары электронов или несвязывающих электроны. Стерический эффект контрастирует с электронным эффектом, подразумевающим влияние таких эффектов, как соединение, индукция, электростатическое взаимодействие, орбитальная симметрия и спиновое состояние.
Контекст и приложения
Эта тема важна для всех студентов и аспирантов, особенно для бакалавров и магистров химии.
Практические задачи
Вопрос 1: Среди следующих эффект, который показывает постоянное смещение электронов
A) Электромерное
B) Индуктивный
C) Индуктомерика
D) Все вышеперечисленное
40004 C) Ответ : Вариант (b) правильный.
Пояснение : Индуктивный эффект определяется как эффект, при котором в молекуле образуется постоянный диполь из-за неэквивалентного распределения связывающих электронов двух разнородных атомов в соединении. Смещение электрона, происходящее при индуктивном эффекте, является постоянным, тогда как замена электрона происходит при электромерном и индуктомерном эффекте, носит временный характер.
Вопрос 2: Какой из следующих эффектов резонанса?
1) Электромерный эффект
2) Мезомерный эффект
3)Индуктомерный эффект
4) Индуктивный эффект
Ответ: Верен вариант 2.
Пояснение: Другое название мезомерного эффекта — эффект резонанса. Это постоянный эффект, и он действует на вещества, имеющие по крайней мере 1 двойную связь.
Вопрос 3: Среди следующего, какой временный эффект возникает при необходимости атакующего реагента?
- Мезомерный эффект
- Индуктивный эффект
- Индуктометрический эффект
- Электромерный эффект
Ответ: Верен вариант 4.
Пояснение: Среди приведенных эффектов Электромерный эффект является временным эффектом, который приводится в действие при необходимости атакующего реагента. Этот эффект называется эффектом молекулярной поляризуемости, происходящим за счет внутримолекулярного смещения электронов.
Вопрос 4: Больше число гиперконъюгаций, устойчивость свободных радикалов будет
- Уменьшение
- Остается прежним
- Увеличение
- Ничего из вышеперечисленного
Пояснение: Гиперконъюгация и стабильность свободных радикалов прямо пропорциональны друг другу. Следовательно, чем больше количество гиперконъюгаций, тем выше будет стабильность свободных радикалов.
Вопрос 5: Выберите правильное утверждение из следующего,
1) –I эффект слабее, чем сопряженный эффект
2) –I эффект сильнее, чем сопряженный эффект
3) Оба эффекта одинаковы
4) Ничего из вышеперечисленного
Ответ: Верен вариант 1.
Объяснение: -I-эффект слабее, чем сопряженный эффект, потому что сопряженный эффект – это эффект, при котором МО сопряжены с новыми МО, которые сильно делокализованы и, следовательно, обычно имеют меньшую энергию.
Мезомерный эффект, эффект +М, эффект -М
Мезомерный эффект определяется как полярность, создаваемая в молекуле или сопряженной системе движением π-электронов к замещающей группе или от нее. Другими словами, атом или группа атомов, которые отдают/забирают электроны посредством резонанса, называют мезомерным эффектом. Таким образом, эффекты высвобождения электронов или электроноакцепторные эффекты возникают у заместителей за счет делокализации π- электронов. Конъюгация является необходимым критерием мезомерного эффекта. Он представлен буквой M, и такой эффект можно анализировать в различных канонических формах.
Виды мезомерного эффекта
- +М эффект (положительный мезомерный эффект)
- -М эффект (отрицательный мезомерный эффект)
+М эффект (положительный мезомер ic эффект) ic эффект) от конкретной группы к остальной части молекулы увеличивает электронную плотность молекулы/сопряженной системы. Такой эффект называется положительным мезомерным эффектом (+М эффект). Это показано заместителем, высвобождающим электроны. Некоторые из заместителей +M представляют собой -OH, -SH, -OR, -OCOR, -Nh3, -NR2, -NHCOR, Ph, -Ch4, -F, -Cl, -Br, -I и т. д.
Такой эффект называется положительным мезомерным эффектом (+М эффект). Это показано заместителем, высвобождающим электроны. Некоторые из заместителей +M представляют собой -OH, -SH, -OR, -OCOR, -Nh3, -NR2, -NHCOR, Ph, -Ch4, -F, -Cl, -Br, -I и т. д.
-М-эффект (отрицательный мезомер ic-эффект)
Когда π-электроны перемещаются из остальной части молекулы в определенную группу, электронная плотность молекулы/сопряженной системы уменьшается. Такой эффект называется отрицательным мезомерным эффектом (-М эффект). Обозначается электроноакцепторным заместителем. Некоторыми из заместителей -M являются NO2, –CN, –SO3H, –COOH, –COOR, –CONh3, –COO – , –CHO, –COR и так далее.
Мезомерный эффект определяется как полярность, создаваемая в молекуле или сопряженной системе движением π-электронов к замещающей группе или от нее. Он представлен М.
Резонансный эффект представляет собой изъятие или высвобождение электронов, связанных с определенным заместителем, посредством делокализации пи-электронов, что может быть продемонстрировано различными каноническими структурами.
Группа, демонстрирующая +R-эффект (высвобождение электронов) эквивалентна +M-эффекту, а группа показывает –R-эффект (притягивание электронов) эквивалентна –M-эффекту.
Электромерный эффект – временный эффект, при котором дипольный момент создается мгновенно в молекуле за счет полного переноса пи-электронной пары под действием атакующего реагента; электрофил или нуклеофил. Электромерный эффект бывает двух типов; Эффект +E и эффект -E. +Э эффект. Эффект +E возникает, когда π-электроны связи передаются атакующему реагенту, а эффект -E возникает, когда π -электроны связи переносятся на атом, к которому не присоединен атакующий реагент.
Мезомерный эффект определяется как полярность, создаваемая в молекуле или сопряженной системе движением π-электронов к замещающей группе или от нее. Мезомерный эффект бывает двух типов; Эффект +М и эффект -М. Эффект +M возникает, когда π-электроны перемещаются от конкретной группы к остальной части молекулы и увеличивают электронную плотность молекулы/сопряженной системы. Эффект -М возникает, когда π-электроны перемещаются из остальной части молекулы в определенную группу, электронная плотность молекулы/сопряженной системы уменьшается.
Эффект -М возникает, когда π-электроны перемещаются из остальной части молекулы в определенную группу, электронная плотность молекулы/сопряженной системы уменьшается.
| Мезомерный эффект. | Резонансный эффект. | Резонансный эффект представляет собой изъятие или высвобождение электронов, связанных с определенным заместителем, посредством делокализации пи-электронов. |
| Положительный мезомерный эффект (+М) и отрицательный мезомерный эффект (-М) представляют собой два типа мезомерного эффекта. | Эффект положительного резонанса (+M) и эффект отрицательного резонанса (-M) представляют собой два типа эффекта резонанса. | |
| Это связано с наличием заместителей, либо электроноакцепторных, либо электронодонорных в сопряженной системе. | Возникает из-за наличия неподеленных пар, примыкающих к двойной связи. |
| Мезомерный эффект | Индуктивный эффект |