Урок 16. основные положения мкт. броуновское движение – Физика – 10 класс
Основные положения МКТ. Броуновское движение
Краткое содержание урока
На этом уроке мы узнали, что раздел физики, изучающий тепловые явления, называется молекулярной физикой.
В основе молекулярно-кинетической теории (МКТ) строения вещества лежат утверждения:
I. Все вещества состоят из частиц, между которыми есть промежутки.
II. Частицы движутся хаотично и непрерывно.
III. Частицы взаимодействуют друг с другом силами притяжения и отталкивания.
Опытные подтверждения I положения МКТ: закон кратности отношений; дробление вещества; испарение жидкостей; расширение веществ при нагревании; диффузия; деформация.
Опытные подтверждения II положения МКТ: диффузия; броуновское движение; стремление газа занять любой объём.
Опытные подтверждения III положения МКТ: деформация; смачивание; поверхностное натяжение жидкости; сохранение формы твёрдого тела.
Моль – количество вещества, содержащее столько же молекул (атомов), сколько их содержится в углероде массой 0,012 кг.
Число Авогадро – число молекул или атомов в 1 моле вещества. NА = 6,023·1023 моль-1.
Количество вещества – это отношение массы вещества к его молярной массе: $\nu = \frac{m}{M}$.
Количество вещества равно отношению числа молекул в данном веществе к постоянной Авогадро: $\nu = \frac{N}{N_A}$
Решение задачи «Оценка размеров молекул»
Молекулярно-кинетическая теория – это… Что такое Молекулярно-кинетическая теория?
Молекулярно-кинетическая теория (сокращённо МКТ) — теория XIX века, рассматривавшая строение вещества, в основном газов, с точки зрения трёх основных приближенно верных положений:
Основными доказательствами этих положений считались:
В современной (теоретической) физике термин молекулярно-кинетическая теория уже не используется, хотя он встречается в учебниках по курсу общей физики. В современной физике МКТ заменила кинетическая теория, в русскоязычной литературе — физическая кинетика, и статистическая механика. В этих разделах физики изучаются не только молекулярные (атомные или ионные) системы, находящиеся не только в «тепловом» движении, и взаимодействующие не только через абсолютно упругие столкновения.
В современной физике МКТ заменила кинетическая теория, в русскоязычной литературе — физическая кинетика, и статистическая механика. В этих разделах физики изучаются не только молекулярные (атомные или ионные) системы, находящиеся не только в «тепловом» движении, и взаимодействующие не только через абсолютно упругие столкновения.
История теории
Первым опровержением теории послужила теория М. В. Ломоносова[1][2]. Ломоносов опытным путём опроверг теории о теплороде и флогистоне, подготовив тем самым, молекулярно-кинетическую теорию XIX века Рудольфа Клаузиуса, Людвига Больцмана и Джеймса Максвелла.
Основное уравнение МКТ
| Проверить информацию. Необходимо проверить точность фактов и достоверность сведений, изложенных в этой статье. |
, где k является постоянной Больцмана (отношение универсальной газовой постоянной

Основное уравнение МКТ связывает макроскопические параметры (давление, объём, температура) газовой системы с микроскопическими (масса молекул, средняя скорость их движения).
Вывод основного уравнения МКТ
Пусть имеется кубический сосуд с ребром длиной и одна частица массой в нём.
Обозначим скорость движения , тогда перед столкновением со стенкой сосуда импульс частицы равен , а после — , поэтому стенке передается импульс . Время, через которое частица сталкивается с одной и той же стенкой, равно .
Отсюда следует:
Так как давление , следовательно сила
Подставив, получим:
Преобразовав:
Так как рассматривается кубический сосуд, то
Отсюда:
.
Соответственно, и .
Таким образом, для большого числа частиц верно следующее: , аналогично для осей y и z.
Поскольку , то . Это следует из того, что все направления движения молекул в хаотичной среде равновероятны.
Отсюда
или .
Пусть — среднее значение кинетической энергии всех молекул, тогда:
, откуда, используя то, что , а , имеем .
Уравнение среднеквадратичной скорости молекулы
Уравнение среднеквадратичной скорости молекулы легко выводится из основного уравнения МКТ для одного моля газа.
,
, где — молярная масса газа
Отсюда окончательно
См. также
Примечания
- ↑ Фигуровский Н. А. Очерк общей истории химии. От древнейших времен до начала XIX в. — М.: Наука, 1969
- ↑ Михаил Васильевич Ломоносов. Избранные произведения в 2-х томах. М.: Наука. 1986
Литература
| 1. |
Формула Планка
Сложность: лёгкое |
1 |
2. |
Природа света
Сложность: лёгкое |
1 |
| 3. |
Исторические сведения
Сложность: лёгкое |
1 |
4. |
Электромагнитное излучение разной природы
Сложность: лёгкое |
1 |
| 5. |
Фотон
Сложность: лёгкое |
2 |
6. |
Формула
Сложность: лёгкое |
1 |
| 7. | Сложность: среднее |
2 |
8.
|
Энергия квантов
Сложность: среднее |
2 |
| 9. |
Природа света
Сложность: среднее |
2 |
10.
|
Энергия фотона
Сложность: среднее |
2 |
| 11. |
Импульс фотона
Сложность: среднее |
2 |
12.
|
Определение длины волны
Сложность: среднее |
2 |
| 13. |
Частота излучения кванта
Сложность: среднее |
2 |
14.
|
Формула частоты излучения
Сложность: среднее |
2 |
| 15. |
Формула длины волны
Сложность: среднее |
2 |
16.
|
Энергия кванта
Сложность: среднее |
2 |
| 17. |
Длина световой волны
Сложность: сложное |
3 |
18.
|
Изменение характеристик световой волны
Сложность: сложное |
3 |
| 19. |
Количество фотонов
Сложность: сложное |
3 |
20.
|
Мощность лампы
Сложность: сложное |
3 |
| 21. |
Опыт Ньютона
Сложность: сложное |
3 |
22.
|
Показатель преломления
Сложность: сложное |
3 |
Основные положения МКТ и их опытное обоснование. Масса молекулы. Молярная масса. Количество вещества.
Первое положение молекулярно-кинетической теории
Вещество состоит из частиц.
Молекула – это самая маленькая частица вещества, которая обладает его основными химическими свойствами.
Молекула состоит из атомов. Атом – наименьшая частица вещества, которая не делится при химических реакциях.
Многие молекулы состоят из двух или больше атомов, удерживаемых вместе химическими связями. Некоторые молекулы состоят из сотен тысяч атомов.
Второе положение молекулярно-кинетической теории
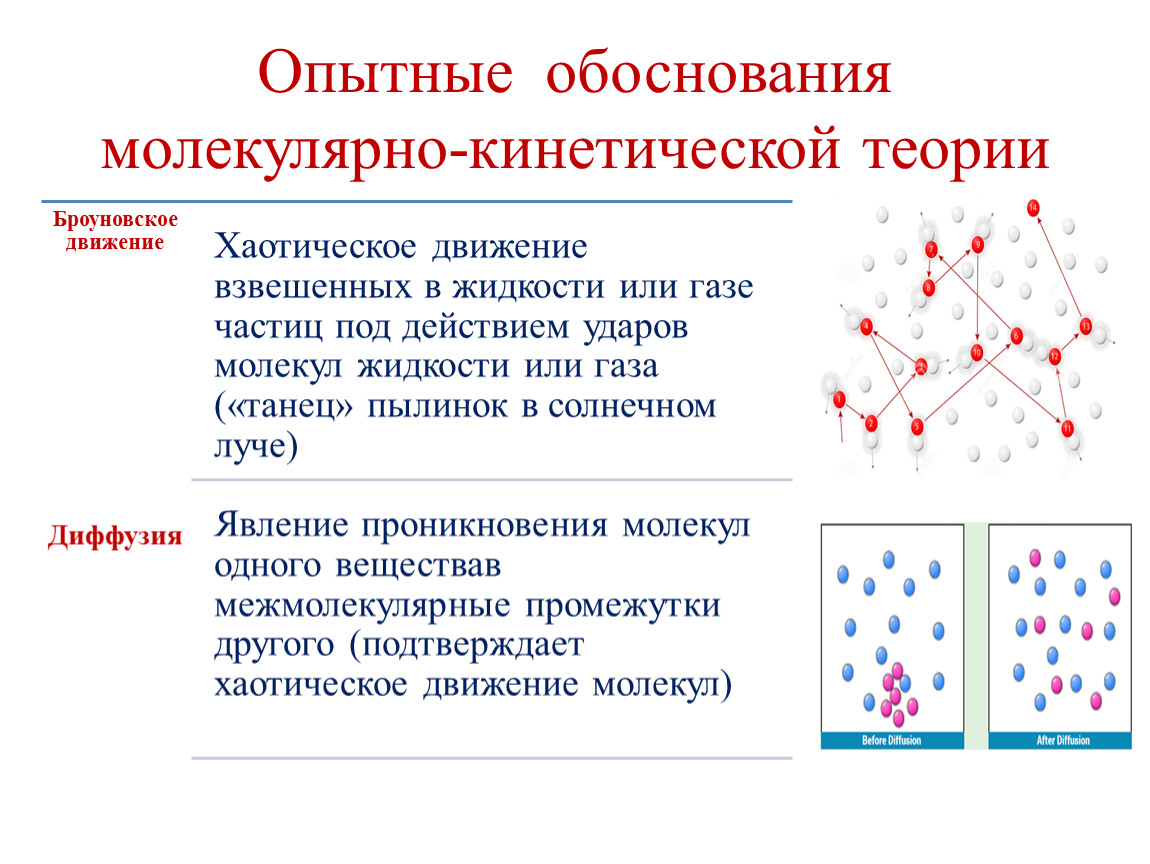
Молекулы находятся в непрерывном хаотическом движении. Это движение не зависит от внешних воздействий. Движение происходит в непредсказуемом направлении из-за столкновения молекул. Доказательством являетсяброуновское движение частиц (открыто Р.Броуном 1827г). Частицы помещают в жидкость или газ и наблюдают их непредсказуемое движение из-за соударений с молекулами вещества.
Броуновское движение
Доказательством хаотического движения является диффузия – проникновение молекул одного вещества в промежутки между молекулами другого вещества. Например, запах освежителя воздуха мы ощущаем не только в том месте, где его распылили, но он постепенно перемешивается с молекулами воздуха во всей комнате.
Агрегатное состояние вещества
В газах среднее расстояние между молекулами в сотни раз превышает их размеры. В основном молекулы движутся поступательно и равномерно. После столкновений начинают вращаться.
В основном молекулы движутся поступательно и равномерно. После столкновений начинают вращаться. В жидкостях расстояние между молекулами значительно меньше. Молекулы совершают колебательное и поступательное движения. Молекулы через малые промежутки времени скачкообразно переходят в новые положения равновесия (мы наблюдаем текучесть жидкости).
В твердых телах молекулы колеблются и очень редко перемещаются (только при увеличении температуры).
Третье положение молекулярно-кинетической теории
Между молекулами существуют силы взаимодействия, которые имеют электромагнитную природу. Эти силы позволяют объяснить возникновение сил упругости. Когда вещество сжимают, молекулы сближаются, между ними возникает сила отталкивания, когда внешние силы отдаляют молекулы друг от друга (растягивают вещество), между ними возникает сила притяжения.Плотность вещества
Это скалярная величина, которая определяется по формуле
Плотность веществ – известные табличные значения
Химические характеристики вещества
Постоянная Авогадро NA – число атомов, содержащихся в 12г изотопа углеродаКоличество вещества – это отношение числа элементов этого вещества к постоянной Авогадро
1 моль любого вещества содержит одинаковое число частиц, это число равно постоянной Авогадро.
Молярная масса M – это масса одного моля вещества
Если тело состоит из N молекул массой m0, то масса тела
Концентрация частиц – это количество частиц в объеме
Можно вывести формулы
??? Вопросы
1. Назовите три положения МКТ?
2. Дайте определение диффузии?
3. Броуновское движение подтверждает, что…?
4. В каких агрегатных состояниях может находиться вещество?
5. Моль – это…?
6. Что называют количеством вещества? Как можно определить количество вещества?
7. Назовите единицу измерения количества вещества?
8. Что называют молярной массой вещества? Как по таблице Менделеева определить молярную массу вещества?
9. Назовите единицу измерения молярной массы вещества?
10. Какое число молекул содержится в одном моле любого вещества? Как это число называется?
Какое число молекул содержится в одном моле любого вещества? Как это число называется?
Упражнение №1
Доказательства положений молекулярно-кинетической теории (МКТ). Броуновское движение | Физика. Закон, формула, лекция, шпаргалка, шпора, доклад, ГДЗ, решебник, конспект, кратко
Тема: Молекулярно-кинетическая теория
| Рис. 1.1. Траектория движения броуновской частички |
Убедительным доказательством существования молекул и их хаотического движения является перемещение мелких частичек в жидкости или газе. В 1827 г. английский ботаник Р. Броун (1773—1858) наблюдал движение цветочной пыльцы в воде и пришел к выводу, что оно беспорядочно и имеет сложную траекторию (рис. 1.1). Позже французский физик Ж. Перрен (1870— 1942) экспериментально исследовал броуновское движение частичек и обнаружил, что последнее является следствием теплового движения молекул. Им было установлено, что интенсивность броуновского движения частичек возрастает при повышении температуры и не зависит от времени и химической природы частички. В 1905—1906 гг. выдающийся физик А. Эйнштейн (1879—1955) и польский ученый М. Смолуховский (1872—1917) дали теоретическое толкование броуновского движения с позиций молекулярно-кинетических представлений, чем окончательно подтвердили достоверность молекулярной физики.
Им было установлено, что интенсивность броуновского движения частичек возрастает при повышении температуры и не зависит от времени и химической природы частички. В 1905—1906 гг. выдающийся физик А. Эйнштейн (1879—1955) и польский ученый М. Смолуховский (1872—1917) дали теоретическое толкование броуновского движения с позиций молекулярно-кинетических представлений, чем окончательно подтвердили достоверность молекулярной физики.
Взаимодействие молекул подтверждает наличие сил упругости, которые возникают при деформации тел. Они быстродействующие, имеют электромагнитную природу и существенно зависят от расстояния между молекулами. Установлено, что сила притяжения Fпр пропорциональна 1/r7 а сила отталкивания Fот пропорциональна 1/r13. Поэтому сила взаимодействия практически отсутствует, если молекулы находятся на расстояниях, в несколько раз превышающих их размеры. Этим, в частности, объясняется пренебрежение силами взаимодействия в разреженных газах, в которых расстояние между молекулами превышает несколько их диаметров.
Этим, в частности, объясняется пренебрежение силами взаимодействия в разреженных газах, в которых расстояние между молекулами превышает несколько их диаметров.
| Рис. 1.2. Зависимость силы взаимодействия от расстояния между молекулами |
При незначительных деформациях справедлив закон Гука, который воспроизводит линейный характер зависимости силы упругости от значения деформации (на рис. 1.2 это показано утолщенным участком графика) Материал с сайта http://worldofschool.ru
Разная зависимость силы притяжения и силы отталкивания от расстояния обусловливает сложный характер зависимости силы взаимодействия между молекулами (рис. 1.2). На расстоянии между центрами молекул г, которое равно сумме радиусов взаимодействующих молекул (r = 2r0), сила отталкивания по модулю равняется силе притяжения (Fот = Fпр), и поэтому их равнодействующая равна нулю (F = 0). На расстояниях r > 2r0во взаимодействии преобладает притяжение (участок ОВ), а при r < 2r0— отталкивание (участок ОА). Поэтому при деформации тел возникает сила упругости, которая при сжатии (расстояние между молекулами уменьшается) или растяжении (расстояние между молекулами увеличивается) старается вернуть их в состояние равновесия сил притяжения и отталкивания (F = 0).
На расстояниях r > 2r0во взаимодействии преобладает притяжение (участок ОВ), а при r < 2r0— отталкивание (участок ОА). Поэтому при деформации тел возникает сила упругости, которая при сжатии (расстояние между молекулами уменьшается) или растяжении (расстояние между молекулами увеличивается) старается вернуть их в состояние равновесия сил притяжения и отталкивания (F = 0).
Таким образом, получив многочисленные доказательства подтверждения своей справедливости, атомно-молекулярная гипотеза о строении вещества стала теорией и завоевала видное место среди современных физических теорий, в частности как один из подходов к объяснению тепловых явлений и процессов. Построенная на ее положениях молекулярная физика объясняет протекание тепловых явлений на основании представлений о внутреннем строении вещества, то есть о его микросостояниях.
На этой странице материал по темам:Какое положение мкт доказывает броуновское движение
Косвенные доказательства взаимодействия молекул
Какие прямые и косвенные доказательства истинности атомно-молекулярного учения
Молекулярная физика кратко
Реферат на тему смолуховський и малекулярно кинитическая теория 1872-1917
Какие эксперименты и теоретические расчеты окончательно утвердили победу молекулярной физики? Когда это произошло?
Объясните явление возникновения сил упругости и их природу.

Физика – 10
В физике выделен раздел – молекулярная физика, в котором собраны результаты изучения внутреннего строения вещества.
● Молекулярная физика — это раздел физики, в котором изучаются внутреннее строение макроскопических тел, их свойства и основные закономерности теплового движения материи.
● Молекулярно-кинетическая теория (МКТ) – теория, объясняющая свойства макроскопических тел и тепловые процессы в этих телах на основе представлений о веществе как о системе атомов и молекул, беспрерывно и хаотически движущихся и взаимодействующих друг с другом.
Основные положения молекулярно-кинетической теории. В основе МКТ лежат три положения:
I положение: все вещества состоят из частичек – атомов и молекул. Существование атомов и молекул было предсказано еще древними философами. Однако ясную количественную теорию этого факта впервые предложил английский ученый-химик Джон Далтон (1766-1844). Составив таблицу относительных атомных масс ряда элементов, он заложил основу теории атомного строения вещества. В наше время, используя способность электронного микроскопа увеличивать в миллионы раз размеры объекта, можно увидеть и сфотографировать достаточно большие молекулы.
Однако ясную количественную теорию этого факта впервые предложил английский ученый-химик Джон Далтон (1766-1844). Составив таблицу относительных атомных масс ряда элементов, он заложил основу теории атомного строения вещества. В наше время, используя способность электронного микроскопа увеличивать в миллионы раз размеры объекта, можно увидеть и сфотографировать достаточно большие молекулы.
II положение: частицы, из которых состоит вещество, находятся в непрерывного и беспорядочного (хаотического) движения.
Верность этого положения была установлена на основе открытия, сделанного в 1827 году английским ботаником Робертом Броуном, наблюдавшим в микроскоп за движением
цветочной пыльцы в воде. Он обнаружил, что пыльца совершает хаотическое движение и изменяет свое положение по сложной траектории (c). Беспорядочное движение частиц, называемое “броуновским движением”, теоретически было объяснено А.Эйнштейном в 1905 году, а опытным путем было подтверждено в 1909-1911 годах французским физиком Яном Батистом Перреном (1870-1942). Он подтвердил предположение Эйнштейна, что причиной хаотического движения частичек краски в воде является тепловое движение молекул воды. Перрен определил, что интенсивность броуновского движения частиц зависит не от их химической природы, а от температуры: с увеличением температуры интенсивность броуновского движения также увеличивается. Таким образом:
Беспорядочное движение частиц, называемое “броуновским движением”, теоретически было объяснено А.Эйнштейном в 1905 году, а опытным путем было подтверждено в 1909-1911 годах французским физиком Яном Батистом Перреном (1870-1942). Он подтвердил предположение Эйнштейна, что причиной хаотического движения частичек краски в воде является тепловое движение молекул воды. Перрен определил, что интенсивность броуновского движения частиц зависит не от их химической природы, а от температуры: с увеличением температуры интенсивность броуновского движения также увеличивается. Таким образом:● Броуновским движением называется беспорядочное движение частиц, взвешенных в жидкости (или газе).
Другим явлением, подтверждающим второе положение МКТ, является диффузия.
● Диффузией называется процесс самопроизвольного взаимного проникновения атомов или молекул одного вещества в межатомные или межмолекулярные промежутки другого вещества.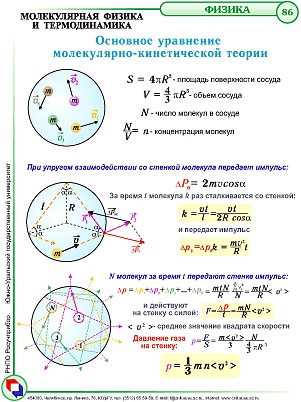
Первое количественнное описание процесса диффузии дал в 1855 году немецкий физик и физиолог Адольф Фик (1829-1901) в законе, названном “законом диффузии Фика ”.
Физика в школе 867
Модель идеального газа
Идеальный газ – это теоретическая модель газа, для которой верны следующие три тезиса:
- Размеры молекул газа пренебрежимо малы по сравнению с расстоянием между ними
- Потенциальная энергия взаимодействия между собой молекул пренебрежимо мала
- Столкновения молекул газа абсолютно упругие
Основное уравнение МКТ
Основное уравнение молекулярно-кинетической теории является первым полученным количественным соотношением в МКТ.
Давление газа равно:
Здесь p – давление газа, m0 – масса одной молекулы газа, n – концентрация и v2 с палочкой наверху означает средний квадрат скорости молекул (то есть среднее арифметическое квадратов скоростей всех молекул газа).
Если воспользоваться формулой кинетической энергии, мы получим иную запись основного уравнения МКТ:
Как видим, давление газа прямо пропорционально кинетической энергии его молекул. Важно заметить, что Eкин в данной формуле является кинетической энергией не всего газа, а лишь одной молекулы.
Также давление прямо пропорционально температуре по формуле:
Температура
Так как в молекулярной физике величины связаны математическими формулами и не отрицательны (давление, объем, концентрация и т.д.), а температура может принимать отрицательные значения, например, – 100 °C, физики решили использовать иную шкалу температур, где выполняется T > 0, и ввели шкалу Кельвина.
Связь шкалы Цельсия и шкалы Кельвина:
Абсолютный нуль есть значение T = 0 K = – 273,15 °C. При таком значении температуры движение молекул прекращается (это следует из формулы связи кинетической энергии молекулы и температуры, см. ниже). Это теоретическое значение, так как на практике быть полученным не может, но возможна температура, сколь угодно близкая к абсолютному нулю.
ниже). Это теоретическое значение, так как на практике быть полученным не может, но возможна температура, сколь угодно близкая к абсолютному нулю.
Средняя кинетическая энергия одной молекулы прямо пропорциональна абсолютной температуре:
Среднюю квадратичную скорость молекул можно рассчитать по формуле:
Уравнение Менделеева-Клапейрона
Уравнение Клапейрона
В 1834 г. французский ученый Бенуа Поль Эмиль Клапейрон вывел формулу:
Здесь p – давление, V – объем, T – абсолютная температура и значение A – некая переменная, которая зависит от массы газа m и молекулярной массы газа M.
Уравнение Менделеева
В 1874 г. русский ученый Дмитрий Иванович Менделеев вывел формулу для одного моля идеального газа:
Здесь p – давление, V – объем, T – абсолютная температура и значение R = kNA = 8,31 есть газовая постоянная.
Уравнение Менделеева-Клапейрона
Объединив вышенаписанные уравнения, физики получили уравнение Менделеева-Клапейрона, которое характеризует состояние идеального газа произвольного количества молей:
Воспользовавшись тождеством , мы получим более компактную запись:
Если рассмотреть один и тот же газ (ν = const), то заметим, что произведение νR = const. Таким образом, если выразить это произведение, поделив на T, мы получим уравнение, полезное в случае изменения определенных параметров одного и того же газа:
Таким образом, если выразить это произведение, поделив на T, мы получим уравнение, полезное в случае изменения определенных параметров одного и того же газа:
Энтропия газа
Термодинамика – раздел физики который имеет дело с энергией и работой системы. В аэродинамике нас больше всего интересует термодинамика при изучении тяги системы и понимание высокой скорости потоки. Первый закон термодинамики указывает, что полная энергия системы сохраняется. Общая энергия включает потенциальную и кинетическую энергию, Работа выполняется системой, а передача нагревать через систему. В второй закон термодинамики указывает что, в то время как многие физические процессы, удовлетворяющие первому закону, возможно, в природе происходят только те процессы, для которых энтропия системы либо остается постоянной, либо увеличивается.
Энтропия, как температура и давление, можно объяснить как на макро масштаб и микромасштаб. Поскольку термодинамика имеет дело только с макромасштабом, изменение энтропии определяется дельта S здесь должна быть передача тепла дельта Q в систему, разделенная на температура T :
дельта S = дельта Q / T
Во время термодинамического процесса температура Т объекта
изменяется по мере подачи или отвода тепла Q . Более правильное определение
энтропия S является дифференциальной формой, которая учитывает это
вариация.
Более правильное определение
энтропия S является дифференциальной формой, которая учитывает это
вариация.
dS = dQ / T
Тогда изменение энтропии обратное температуры, интегрированной по изменению теплопередачи. За газов, есть два возможных способа оценить изменение энтропии. Начнем с первого закона термодинамики:
dE = dQ – dW
где E – внутренняя энергия, а Вт – работа, выполняемая система.Подстановка определения работы для газа.
dQ = dE + p dV
где p – давление и В – это объем газа. Если мы используем определение энтальпия H газа:
H = E + p * V
Потом:
dH = dE + p dV + V dp
Подставляем в уравнение первого закона:
dQ = dH – V dp – p dV + p dV
dQ = dH – V dp
это альтернативный способ представить первый закон термодинамики.Для идеального газа уравнение состояния записывается:
р * V = R * T
где R – газовая постоянная. Теплопередача
газа равна теплоемкости, умноженной на изменение
температура; в дифференциальной форме:
Теплопередача
газа равна теплоемкости, умноженной на изменение
температура; в дифференциальной форме:
dQ = C * dT
Если у нас есть процесс постоянного объема, формулировка первого закона дает:
dE = dQ = C (постоянный объем) * dT
Аналогично, для процесса постоянного давления, формулировка первого закона дает:dH = dQ = C (постоянное давление) * dT
Если предположить, что теплоемкость постоянна с температурой, мы можем использовать эти два уравнения, чтобы определить изменение энтальпии и внутренняя энергия.Если подставить значение вместо p из уравнения состояния, а определение dE в первом уравнении энергии, получаем:dQ = C (постоянный объем) * dT + R * T dV / V
Аналогичным образом подставляя значение В из уравнения состояние, а определение dH мы получаем альтернативную форму:
dQ = C (постоянное давление) * dT – R * T dp / p
Подставляя эти формы для dQ в дифференциальную форму уравнения энтропии дает:
dS = C (постоянный объем) * dT / T + R * dV / V
и
dS = C (постоянное давление) * dT / T – R * dp / p
Эти уравнения можно проинтегрировать из условия «1» в условие «2» дать:
S2 – S1 = Cv * ln (T2 / T1) + R * ln (V2 / V1)
и
S2 – S1 = Cp * ln (T2 / T1) – R * ln (p2 / p1)
где Cv – теплоемкость
при постоянной громкости, Cp – тепловая мощность
при постоянном давлении,
и ln – это символ
логарифмическая функция.
s2 – s1 = cv * ln (T2 / T1) + R * ln (v2 / v1)
и
s2 – s1 = cp * ln (T2 / T1) – R * ln (p2 / p1)
где cp и cv – удельные теплоемкости. В зависимости от типа процесса, с которым мы сталкиваемся, теперь мы можем определить изменение энтропии газа.
Эти уравнения могут немного сбивать с толку, потому что мы используем удельную теплоемкость при постоянный объем, когда у нас есть процесс, который изменяет объем, а конкретный нагревать при постоянном давлении, когда в процессе изменяется давление. посмотрим на первое уравнение:
s2 – s1 = cv * ln (T2 / T1) + R * ln (v2 / v1)
Если у нас есть процесс постоянного объема, второй член в уравнении равен
к нулю, так как v2 / v1 = 1. Затем мы можем определить значение теплоемкости
для процесса постоянного объема. Но если у нас есть процесс, который изменяет громкость,
второй член в уравнении не равен нулю. Мы можем думать о первом члене уравнения
как вклад для процесса постоянного объема, а второй член как дополнительный
изменение, вызванное изменением громкости. Подобный тип аргумента может быть сделан
для уравнения, используемого для изменения давления.
Но если у нас есть процесс, который изменяет громкость,
второй член в уравнении не равен нулю. Мы можем думать о первом члене уравнения
как вклад для процесса постоянного объема, а второй член как дополнительный
изменение, вызванное изменением громкости. Подобный тип аргумента может быть сделан
для уравнения, используемого для изменения давления.
Действия:
Экскурсии с гидом
Навигация ..
- Руководство для начинающих Домашняя страница
Физика материалов | Физика | Иллинойсский университет, Чикаго,
Кафедра занимается различными исследованиями в области физики материалов, в том числе:
- Молекулярно-лучевая эпитаксия
- Оптоэлектронные устройства
- Современная микроскопия
- Наночастицы
- Моделирование эпитаксиального роста
- Коррелированные электроны
- Вычислительный DMFT / DFT
Дополнительная информация
- Лаборатория микрофизики
Лаборатория микрофизики
Микрофизическая лаборатория (MPL) Иллинойского университета в Чикаго в настоящее время является единственной университетской лабораторией в США.
 С. проводит фундаментальные исследования HgCdTe (также известного как MCT) методом молекулярно-лучевой эпитаксии (MBE) с момента его создания в начале 1980-х годов. Это центр фундаментальных и прикладных физических исследований с акцентом на материалы II-VI и устройства для инфракрасного зондирования и визуализации, а также фотоэлектрические элементы. Доктор Сива Сиванантан является директором MPL с 1994 года и работал над полупроводниками, технологиями инфракрасных датчиков и детекторов ночного видения, помогая стать пионером в синтезе доминирующего в настоящее время высокотехнологичного полупроводникового материала для обнаружения инфракрасного излучения и ночного видения, MCT.
С. проводит фундаментальные исследования HgCdTe (также известного как MCT) методом молекулярно-лучевой эпитаксии (MBE) с момента его создания в начале 1980-х годов. Это центр фундаментальных и прикладных физических исследований с акцентом на материалы II-VI и устройства для инфракрасного зондирования и визуализации, а также фотоэлектрические элементы. Доктор Сива Сиванантан является директором MPL с 1994 года и работал над полупроводниками, технологиями инфракрасных датчиков и детекторов ночного видения, помогая стать пионером в синтезе доминирующего в настоящее время высокотехнологичного полупроводникового материала для обнаружения инфракрасного излучения и ночного видения, MCT.- Сканирующий просвечивающий электронный микроскоп
Сканирующий просвечивающий электронный микроскоп
STEM с коррекцией аберрации был первым инструментом в Соединенных Штатах с таким высоким уровнем возможностей.
 Профессор Кли, человек, ответственный за обеспечение гранта Национального научного фонда на 2 миллиона долларов, который предоставил STEM в Центр исследовательских ресурсов UIC, сказал: «То, что ранее предсказывалось физикой конденсированного состояния в теории химии, теперь действительно можно визуализировать, исследовать. и протестированы, что позволило нам улучшить теоретические модели.Такие усовершенствованные теории в конечном итоге приведут к созданию лучших, более эффективных или экологически чистых материалов.
Профессор Кли, человек, ответственный за обеспечение гранта Национального научного фонда на 2 миллиона долларов, который предоставил STEM в Центр исследовательских ресурсов UIC, сказал: «То, что ранее предсказывалось физикой конденсированного состояния в теории химии, теперь действительно можно визуализировать, исследовать. и протестированы, что позволило нам улучшить теоретические модели.Такие усовершенствованные теории в конечном итоге приведут к созданию лучших, более эффективных или экологически чистых материалов.- Национальная лаборатория возобновляемых источников энергии
Национальная лаборатория возобновляемых источников энергии
Национальная лаборатория возобновляемых источников энергии (NREL) – это основная национальная лаборатория Министерства энергетики США по исследованиям и разработкам в области возобновляемых источников энергии и энергоэффективности.
 Он разрабатывает технологии и методы использования возобновляемых источников энергии и энергоэффективности, продвигает соответствующие науку и технику, а также передает знания и инновации для достижения национальных целей в области энергетики и охраны окружающей среды. Два старших исследователя NREL и один почетный научный сотрудник NREL имеют дополнительные назначения в Департаменте физики UIC и тесно сотрудничают со студентами и научным персоналом Микрофизической лаборатории (MPL).
Он разрабатывает технологии и методы использования возобновляемых источников энергии и энергоэффективности, продвигает соответствующие науку и технику, а также передает знания и инновации для достижения национальных целей в области энергетики и охраны окружающей среды. Два старших исследователя NREL и один почетный научный сотрудник NREL имеют дополнительные назначения в Департаменте физики UIC и тесно сотрудничают со студентами и научным персоналом Микрофизической лаборатории (MPL).
Факультет физики материалов
Джордж Crabtree
Председатель Энергетического Совета, Заслуженный профессор МСЖД
Кристоф Грейн
Профессор
Сердар Огут
Профессор и содиректор аспирантуры
Hyowon Парк
Доцент
Шивалингам Сиванантан
Директор лаборатории микрофизики, заслуженный профессор ЛАН
Является ли H mCT и q mCT одним и тем же.
 Если это так, то это больше, чем химия класса 11 CBSE Подсказка: Когда происходит процесс, выделяемое тепло равно изменению энтальпии.Энтальпия равна сумме внутренней энергии и произведения давления и объема. Уравнение можно представить в виде: $ H = U + PV $
Если это так, то это больше, чем химия класса 11 CBSE Подсказка: Когда происходит процесс, выделяемое тепло равно изменению энтальпии.Энтальпия равна сумме внутренней энергии и произведения давления и объема. Уравнение можно представить в виде: $ H = U + PV $ При постоянном давлении выделяемое тепло равно изменению энтальпии. Энтальпия – это функция состояния, которая зависит от других функций состояния, таких как температура (T), давление (P) и внутренняя энергия (U). Изменение энтальпии дается как изменение энтальпии между начальным и конечным состояниями: $ \ Delta H = \ Delta U + P \ Delta V $
Полный ответ:
Энтальпия в молярных единицах может быть выражена как молярная энтальпия, когда энтальпия равна делится на нет.родинок ($ \ Delta {H_m} $). Энтальпия – это функция состояния, поскольку она не зависит от пути, по которому следует система. Если имеет место работа без расширения и давление поддерживается постоянным, то изменение энтальпии равно теплу, потребляемому системой, т. е. $ \ Delta H = q $ – (1)
е. $ \ Delta H = q $ – (1)
Это используется для определения реакции эндотермический или экзотермический. При постоянном давлении, когда тепло поглощается, оно является эндотермическим, а при выделении тепла – экзотермическим. Согласно уравнению, если внутренняя энергия увеличивается, энтальпия увеличивается с увеличением температуры.Используя это, мы можем вывести соотношение: $ C = \ dfrac {q} {{\ Delta T}} $
Для постоянного давления уравнение может быть записано как: $ {C_p} = {\ left ({\ dfrac {{ \ Delta H}} {{\ Delta T}}} \ right) _p} $
Следовательно, мы можем сказать, что $ \ Delta H = {C_p} \ Delta T $. Молярная энтальпия может быть задана как:
$ \ Delta H = m {C_p} \ Delta T $ – (2)
Из уравнений (1) и (2) мы получаем, что $ q = m {C_p} \ Delta T $
Следовательно, оба уравнения $ H = mCT $ и $ q = mCT $ одинаковы.
Примечание:
При добавлении тепла температура изменится на определенную величину. Взаимосвязь между теплотой и температурой в каждом веществе различается величиной удельной теплоемкости. Соотношение определяется следующим образом: $ q = mC \ Delta T $
Соотношение определяется следующим образом: $ q = mC \ Delta T $
Где q = тепло (джоули, Дж), m = масса вещества (кг), c = удельная теплоемкость (Дж / кг.K), $ \ Delta T $ = изменение температуры.
Chemistry Unit 6 review 0 International (CC BY-NC-SA 4. Что из следующего представляет мольное соотношение между нитратом серебра и нитратом меди (II) в следующей реакции: 2AgNO 3 + Cu -> Cu (NO 3) 2 + 2Аг.1 моль NH 3 содержит 6. Химия моделирования 1 U1 cp ws3 v2. 5 х 1 кг -6. Полностью соответствует новой программе QCE 2019. 11 часов назад пользователем. Сравните и сопоставьте смеси и чистые карточки для главы 1 по химии – 19 карточек. Проверять. P 4 + Cl 2 на PCl 3 f. Атом состоит из протонов, нейтронов и электронов субатомных частиц. 60. Имя ______________. 00. Проверьте их сейчас! Для каждой из приведенных ниже экзаменационных комиссий есть примечания к изменениям, информационные бюллетени, вопросы из прошлых экзаменационных работ, разделенные по темам и видео. В некоторых случаях вы точно так же не получите: * Если вы отсутствовали в какой-либо из лабораторий реакций на замену, загрузите инструкции и завершите лабораторию, следуя указаниям, но просматривая различные реакции на YouTube, чтобы использовать их в качестве наблюдений. Масса изменится, если образуется газ, и вопрос 15. Заключение для запроса: Химия – это изучение состава, структуры и свойств материи. ИГРАТЬ В. Блок 7 – Склеивание. План тем обеспечивает объединяющие принципы химии.Книга 2 Преобразование единиц измерения и научная нотация КЛЮЧ. Экзамен AP по химии состоит из двух частей и занимает около трех часов. Блок 6: Обзор реакций. экзотермические реакции, графики, q = mcdeltaT, энтальпии связи, теплота в формате Class 9 chemistry Notes бесплатны и всегда останутся бесплатными. 25 моль нитрата кальция. Для других может быть лучше более сложный вариант. Исследование материи – школы округа томас – обзорный лист. Расчеты. Здесь вы можете просматривать видео, статьи и упражнения по химии по темам.
В некоторых случаях вы точно так же не получите: * Если вы отсутствовали в какой-либо из лабораторий реакций на замену, загрузите инструкции и завершите лабораторию, следуя указаниям, но просматривая различные реакции на YouTube, чтобы использовать их в качестве наблюдений. Масса изменится, если образуется газ, и вопрос 15. Заключение для запроса: Химия – это изучение состава, структуры и свойств материи. ИГРАТЬ В. Блок 7 – Склеивание. План тем обеспечивает объединяющие принципы химии.Книга 2 Преобразование единиц измерения и научная нотация КЛЮЧ. Экзамен AP по химии состоит из двух частей и занимает около трех часов. Блок 6: Обзор реакций. экзотермические реакции, графики, q = mcdeltaT, энтальпии связи, теплота в формате Class 9 chemistry Notes бесплатны и всегда останутся бесплатными. 25 моль нитрата кальция. Для других может быть лучше более сложный вариант. Исследование материи – школы округа томас – обзорный лист. Расчеты. Здесь вы можете просматривать видео, статьи и упражнения по химии по темам. 1- Макгро-Хилл Райерсон – Химия средней школы 11 v4. Для получения дополнительной практики по заданному типу проблемы вернитесь к Руководствам по ведению заметок, рабочим листам и тестам. Втиснуть. Средняя точность 0%. 1, мы выделили два типа реакций: экзотермические и эндотермические. 0) лицензия; материалы, созданные нашими и другими партнерами, регулируются другими лицензионными соглашениями. Метрическая система Метрическая система основана на префиксах, которые указывают степень 10 с базовыми единицами измерения. Физика. 1 кПа и 0oC внезапно нагреваются до 50.300 секунд. Обзорные книги могут быть очень полезны для AP Chemistry, потому что они представляют собой хорошо организованные каталоги всех различных концепций, которые вы изучите в ходе курса. Периодические тенденции Помимо организации элементов на основе атомных номеров, периодическая таблица предоставляет организованную структуру, которая помогает определять категории элементов. Таким образом, единицы пронумерованы соответствующим образом.
1- Макгро-Хилл Райерсон – Химия средней школы 11 v4. Для получения дополнительной практики по заданному типу проблемы вернитесь к Руководствам по ведению заметок, рабочим листам и тестам. Втиснуть. Средняя точность 0%. 1, мы выделили два типа реакций: экзотермические и эндотермические. 0) лицензия; материалы, созданные нашими и другими партнерами, регулируются другими лицензионными соглашениями. Метрическая система Метрическая система основана на префиксах, которые указывают степень 10 с базовыми единицами измерения. Физика. 1 кПа и 0oC внезапно нагреваются до 50.300 секунд. Обзорные книги могут быть очень полезны для AP Chemistry, потому что они представляют собой хорошо организованные каталоги всех различных концепций, которые вы изучите в ходе курса. Периодические тенденции Помимо организации элементов на основе атомных номеров, периодическая таблица предоставляет организованную структуру, которая помогает определять категории элементов. Таким образом, единицы пронумерованы соответствующим образом. Это обзор модуля для модуля “Вещества и химические изменения”. 1 Анализ единиц Обзор общей процедуры преобразования метрических единиц в метрическую систему Преобразование английских единиц в метрическую 2.Темы могут включать: Родинки и молярная масса. 02 × 10 23, называемое числом Авогадро, в честь химика XIX века Амедео Авогадро, – это число, которое мы используем в химии для обозначения макроскопических количеств атомов и молекул. pdf: Размер файла: 162 kb: Тип файла: pdf: Загрузить файл. Должное внимание уделяется вашему уровню. АП Химия Блок 2 Обзор НТИ №2 ** ПРОЕКТ. Единица измерения химических величин Рабочий лист эмпирических формул 6 ключ ответа. Награды HS Chemistry Unit 6 Notes. Мы также поговорим о том, как измерить точность наших измерений.Обновление 01.09.2019: некоторые из старых действий были обновлены для совместимости с HTML5. 🧪 Обзор экзамена AP Chemistry 2021-22 – Раздел 3: Межмолекулярные силы и свойства. УЧИТЬСЯ. 17 моль CO 2. Ограничивающим реагентом является сахар www.
Это обзор модуля для модуля “Вещества и химические изменения”. 1 Анализ единиц Обзор общей процедуры преобразования метрических единиц в метрическую систему Преобразование английских единиц в метрическую 2.Темы могут включать: Родинки и молярная масса. 02 × 10 23, называемое числом Авогадро, в честь химика XIX века Амедео Авогадро, – это число, которое мы используем в химии для обозначения макроскопических количеств атомов и молекул. pdf: Размер файла: 162 kb: Тип файла: pdf: Загрузить файл. Должное внимание уделяется вашему уровню. АП Химия Блок 2 Обзор НТИ №2 ** ПРОЕКТ. Единица измерения химических величин Рабочий лист эмпирических формул 6 ключ ответа. Награды HS Chemistry Unit 6 Notes. Мы также поговорим о том, как измерить точность наших измерений.Обновление 01.09.2019: некоторые из старых действий были обновлены для совместимости с HTML5. 🧪 Обзор экзамена AP Chemistry 2021-22 – Раздел 3: Межмолекулярные силы и свойства. УЧИТЬСЯ. 17 моль CO 2. Ограничивающим реагентом является сахар www. com. 17. Конверсии [M] атематика… это самая легкая из наук, факт, который очевиден в том, что ни один мозг не отвергает. 0. 00, по состоянию на 02.02.2017. коэффициент преобразования – коэффициент, выраженный в виде дроби, равной единице. Книга 2. 54 см 3 фута = 1 ярд 454 г = 1 фунт 946 мл = 1 кварт I.2) Покажите каждый валентный электрон по одному, используя метод «часов», поместив тесты AP Chemistry Practice Tests. Какое давление если 6. загнали. 1-7. Химия AQA и OCR (A) – 19-20 декабря. Глава 03 – Стехиометрия. Контроль количества сформированной продукции. Большой выбор. Греческие философы (Демокрит и Аристотель 400-500 до н.э.) обзор-лист-9-ответы-химия 1/1 Загружено с edu-dev. CHEMISTRY CP Название: _____ ОБОЗНАЧЕНИЕ Раздел 8 Обзорный лист КЛЮЧ: Свойства воды, растворы, концентрация, кислоты и основания СВОЙСТВА ВОДЫ 1.com позволяет легко получить желаемую оценку! Изучите карточки на модульном тесте по химии в 10 классе. Заполните пропуски наиболее подходящим термином: Химия 11. 57 мол.
com. 17. Конверсии [M] атематика… это самая легкая из наук, факт, который очевиден в том, что ни один мозг не отвергает. 0. 00, по состоянию на 02.02.2017. коэффициент преобразования – коэффициент, выраженный в виде дроби, равной единице. Книга 2. 54 см 3 фута = 1 ярд 454 г = 1 фунт 946 мл = 1 кварт I.2) Покажите каждый валентный электрон по одному, используя метод «часов», поместив тесты AP Chemistry Practice Tests. Какое давление если 6. загнали. 1-7. Химия AQA и OCR (A) – 19-20 декабря. Глава 03 – Стехиометрия. Контроль количества сформированной продукции. Большой выбор. Греческие философы (Демокрит и Аристотель 400-500 до н.э.) обзор-лист-9-ответы-химия 1/1 Загружено с edu-dev. CHEMISTRY CP Название: _____ ОБОЗНАЧЕНИЕ Раздел 8 Обзорный лист КЛЮЧ: Свойства воды, растворы, концентрация, кислоты и основания СВОЙСТВА ВОДЫ 1.com позволяет легко получить желаемую оценку! Изучите карточки на модульном тесте по химии в 10 классе. Заполните пропуски наиболее подходящим термином: Химия 11. 57 мол. С. 3. * Учебник Корвина – Веб-сайт издателя с целями и викторинами Глава… AP Chemistry Unit 1 Review Questions. Балансировка и определение типов реакции. Прочтите стр. 203-210. Порядок тем в курсе химии – предмет горячих споров. Главы 2 и 11. Вы не можете самостоятельно, имея в виду накопление книг или библиотеку, или брать взаймы у ваших товарищей, чтобы их пропустить.Создайте свой набор инструментов AP® Chemistry, научившись использовать моль для сравнения различных единиц, интерпретации таблицы Менделеева и изучения масс и фотоэлектронных спектров. 1 / раз б. Раздел 6 Крот – Ответы LTHS. Блок 3 – Стехиометрия. Периодические тренды Power Point. Обратите внимание, что ваша заполненная записная книжка, исправленные тесты и листы с обзором модулей являются ЛУЧШИМИ инструментами обучения. Это общее определение вызывает много вопросов. Вы будете участвовать в нескольких лабораториях (г) 6 CO 2 (г) + 6 H 2 O (г) из 75.Таким образом, если у нас есть 6. Укажите количество протонов, нейтронов и электронов в каждом из следующих элементов: a.
С. 3. * Учебник Корвина – Веб-сайт издателя с целями и викторинами Глава… AP Chemistry Unit 1 Review Questions. Балансировка и определение типов реакции. Прочтите стр. 203-210. Порядок тем в курсе химии – предмет горячих споров. Главы 2 и 11. Вы не можете самостоятельно, имея в виду накопление книг или библиотеку, или брать взаймы у ваших товарищей, чтобы их пропустить.Создайте свой набор инструментов AP® Chemistry, научившись использовать моль для сравнения различных единиц, интерпретации таблицы Менделеева и изучения масс и фотоэлектронных спектров. 1 / раз б. Раздел 6 Крот – Ответы LTHS. Блок 3 – Стехиометрия. Периодические тренды Power Point. Обратите внимание, что ваша заполненная записная книжка, исправленные тесты и листы с обзором модулей являются ЛУЧШИМИ инструментами обучения. Это общее определение вызывает много вопросов. Вы будете участвовать в нескольких лабораториях (г) 6 CO 2 (г) + 6 H 2 O (г) из 75.Таким образом, если у нас есть 6. Укажите количество протонов, нейтронов и электронов в каждом из следующих элементов: a. Сила тяжести. 0 Имя Дата Pd Химия – Блок 5 и 6 Просмотрите дополнительные эмпирические формулы и рабочий лист молярной массы Указания: превратите приведенное ниже в сбалансированные уравнения, заполнив поля правильными коэффициентами, формулами ионов или твердых веществ и именами. Легкие заметки, которые содержат все вопросы к упражнениям по главе. 6. Глава 07 – Структура и периодичность атома. A… Записки по химии для 9-го класса для Совета Федерального совета (FBISE) Исламабада и Пенджаба.Г) Все вышеперечисленное. 38a КЛЮЧ I.… AP Chemistry Review Notes Блок 6 – стехиометрия-1 – стехиометрия-2 – стехиометрия-3-лаборатория Блок 7 – манометры – Применение закона идеального газа – стехиометрия газа – сухие ответы – стехиометрия газа – влажный – лаборатория стехиометрии газа данные – закон Дальтона 6. Урок 1. Г-жа 00 л воды создаст раствор какой молярности? 3) Сколько граммов NaCl мне нужно для создания 4. Рабочий лист главы 11 (Рабочий лист главы 11. Глава 02 – Атомы, молекулы и ионы. 10-й класс.
Сила тяжести. 0 Имя Дата Pd Химия – Блок 5 и 6 Просмотрите дополнительные эмпирические формулы и рабочий лист молярной массы Указания: превратите приведенное ниже в сбалансированные уравнения, заполнив поля правильными коэффициентами, формулами ионов или твердых веществ и именами. Легкие заметки, которые содержат все вопросы к упражнениям по главе. 6. Глава 07 – Структура и периодичность атома. A… Записки по химии для 9-го класса для Совета Федерального совета (FBISE) Исламабада и Пенджаба.Г) Все вышеперечисленное. 38a КЛЮЧ I.… AP Chemistry Review Notes Блок 6 – стехиометрия-1 – стехиометрия-2 – стехиометрия-3-лаборатория Блок 7 – манометры – Применение закона идеального газа – стехиометрия газа – сухие ответы – стехиометрия газа – влажный – лаборатория стехиометрии газа данные – закон Дальтона 6. Урок 1. Г-жа 00 л воды создаст раствор какой молярности? 3) Сколько граммов NaCl мне нужно для создания 4. Рабочий лист главы 11 (Рабочий лист главы 11. Глава 02 – Атомы, молекулы и ионы. 10-й класс. 29, финиш лаб., Стр. В калоримете бомбы сжигается 060 г титана, температура калориметра увеличивается с 25. Теплота испарения воды больше, чем теплота плавления. 741 карта -. WL36. Химия 11. (NH 4) 2Cr 2O 7 + AlCl 3 à Al 2 (Cr 2O 7) 3 + NH 4Cl c. Учебные материалы по классификационным материалам для обзора. NO + H 2O на NH 3 + O 2 b. Edexcel AS / A2 Руководство для студентов-химиков: Разделы 3 и 6: Навыки в химической лаборатории Руководства для учащихся идеально подходят для повторения.Соответствует курсу химии и описанию экзамена AP! Прекрасно работает в качестве обзора теста или учебного пособия для вашего термодинамического блока! Каждая страница была создана в сотрудничестве с опытным преподавателем химии AP с 30-летним стажем! Раздел 12: Обзор вопросов химии Раздел 12 представляет собой краткое изложение разделов с 1 по 11 и включает в себя обзор всех стандартов Джорджии, рассматриваемых в этой серии. Модель атома водорода Бора нашла наибольшее подтверждение в экспериментальных работах по фотоэлектрическому эффекту.
29, финиш лаб., Стр. В калоримете бомбы сжигается 060 г титана, температура калориметра увеличивается с 25. Теплота испарения воды больше, чем теплота плавления. 741 карта -. WL36. Химия 11. (NH 4) 2Cr 2O 7 + AlCl 3 à Al 2 (Cr 2O 7) 3 + NH 4Cl c. Учебные материалы по классификационным материалам для обзора. NO + H 2O на NH 3 + O 2 b. Edexcel AS / A2 Руководство для студентов-химиков: Разделы 3 и 6: Навыки в химической лаборатории Руководства для учащихся идеально подходят для повторения.Соответствует курсу химии и описанию экзамена AP! Прекрасно работает в качестве обзора теста или учебного пособия для вашего термодинамического блока! Каждая страница была создана в сотрудничестве с опытным преподавателем химии AP с 30-летним стажем! Раздел 12: Обзор вопросов химии Раздел 12 представляет собой краткое изложение разделов с 1 по 11 и включает в себя обзор всех стандартов Джорджии, рассматриваемых в этой серии. Модель атома водорода Бора нашла наибольшее подтверждение в экспериментальных работах по фотоэлектрическому эффекту. 2 моль AgNO 3/2 моль Ag.Ученики. Вы остались на правильном сайте, чтобы начать получать эту информацию. Единичный анализ. Раздел 4 . Архивировано. Практикуйте полученные знания и готовьтесь к экзамену AP Chemistry, задав более 100 вопросов, связанных с AP. Найдите больше идей о химии, химическом образовании, химическом классе. Блок 6 Пакет. C 17H 36 + O 2 à CO 2 + H 2O d. Презентация обзора блока № 6; Презентация обзора блока № 7; Пятница 01.05. 022 × 10 23 Атомы кислорода, мы говорим, что у нас есть 1 моль атомов кислорода. Это руководство предлагает советы по подготовке к экзаменам Edexcel Unit 3 и Unit 6 химических лабораторий.О контакте Главы 4, 5 и 6. Просмотрите все практические тесты. 00L из 0. Объясните, как сбалансированное уравнение представляет эти функции (приведите пример). Иногда просто называется электронно-точечной диаграммой Льюиса. Глава 06 – Термохимия. По химии с отличием: Раздел 6 – Стехиометрия – ПРАКТИЧЕСКИЙ ТЕСТ КЛЮЧ ОТВЕТА Page 1 Вопрос Ответ Дополнительная информация 1.
2 моль AgNO 3/2 моль Ag.Ученики. Вы остались на правильном сайте, чтобы начать получать эту информацию. Единичный анализ. Раздел 4 . Архивировано. Практикуйте полученные знания и готовьтесь к экзамену AP Chemistry, задав более 100 вопросов, связанных с AP. Найдите больше идей о химии, химическом образовании, химическом классе. Блок 6 Пакет. C 17H 36 + O 2 à CO 2 + H 2O d. Презентация обзора блока № 6; Презентация обзора блока № 7; Пятница 01.05. 022 × 10 23 Атомы кислорода, мы говорим, что у нас есть 1 моль атомов кислорода. Это руководство предлагает советы по подготовке к экзаменам Edexcel Unit 3 и Unit 6 химических лабораторий.О контакте Главы 4, 5 и 6. Просмотрите все практические тесты. 00L из 0. Объясните, как сбалансированное уравнение представляет эти функции (приведите пример). Иногда просто называется электронно-точечной диаграммой Льюиса. Глава 06 – Термохимия. По химии с отличием: Раздел 6 – Стехиометрия – ПРАКТИЧЕСКИЙ ТЕСТ КЛЮЧ ОТВЕТА Page 1 Вопрос Ответ Дополнительная информация 1. Заметки по химии 9-го класса (Блок № 5) для Совета Федерального совета (FBISE) Исламабада и Пенджаба. 6 х 10-3 моль сульфата натрия. Температура остается постоянной во время фазового перехода.(Спецификация 2009-2017 гг.) Раздел 4 Практический курс. При ответе на этот вопрос обратитесь к изображению ниже. C 2H 6 2 (12. Com позволяет легко получить желаемую оценку! Создатель карточек: Ирина Солошенко. Преобразуйте 45 г Se в моль Se. 1 Природа энергии A. Химия класса 9 – Глава 6 – Решения – Обзор Вопросы. Изучите карточки на экзамене по естественным наукам в 9 классе (блок химии) в классе Cram. Show Class. Скачать файл. Атомы в неметаллах стремятся к электронам. Блок 4 – Органическая химия.Раздел 6 по химии Рабочий лист 1 Ключ ответов с разделом 1 по химии Рабочий лист 3 Занятия для детей. 0M, мне нужно сделать 2. Кислоты и основания. Часть 1 1. Скорость химической реакции зависит от… Chemistry 11 Review Unit 6 Review Unit 6 Страница 1 из 3 Химия 11 – Обзор раздела 6 1. 4) Раздаточный материал раздела 1.
Заметки по химии 9-го класса (Блок № 5) для Совета Федерального совета (FBISE) Исламабада и Пенджаба. 6 х 10-3 моль сульфата натрия. Температура остается постоянной во время фазового перехода.(Спецификация 2009-2017 гг.) Раздел 4 Практический курс. При ответе на этот вопрос обратитесь к изображению ниже. C 2H 6 2 (12. Com позволяет легко получить желаемую оценку! Создатель карточек: Ирина Солошенко. Преобразуйте 45 г Se в моль Se. 1 Природа энергии A. Химия класса 9 – Глава 6 – Решения – Обзор Вопросы. Изучите карточки на экзамене по естественным наукам в 9 классе (блок химии) в классе Cram. Show Class. Скачать файл. Атомы в неметаллах стремятся к электронам. Блок 4 – Органическая химия.Раздел 6 по химии Рабочий лист 1 Ключ ответов с разделом 1 по химии Рабочий лист 3 Занятия для детей. 0M, мне нужно сделать 2. Кислоты и основания. Часть 1 1. Скорость химической реакции зависит от… Chemistry 11 Review Unit 6 Review Unit 6 Страница 1 из 3 Химия 11 – Обзор раздела 6 1. 4) Раздаточный материал раздела 1. 11 класс. В таблице Менделеева ниже укажите следующие элементы: Ho ‘93013 MO Блок 6: Таблица периодов и ключ связи Регенты Химия 14- Z15 Mr. из которых вы могли не полностью понять в своем классе.Период _____ 1) Как узнать, какая часть смеси является растворенным веществом, а какая – растворителем? 2) 72 г HCl в 6. 3Ca + 2AlCl 3 -> 3CaCl 2 + 2Al. По мере изучения химических веществ студенты будут и дальше развивать свои навыки решения проблем и расследования. Здесь вы найдете множество вопросов и заданий для повторения, с длительными практическими викторинами по каждому разделу курса. Химия 20 Среднесрочный обзор. Есть и другие способы использования этого ключа для Chemistry Unit 6 Worksheet 1. Обзор химии 11-го уровня, часть 7 законов о газах на YouTube.Восстановление кредита для EC – Посмотрите видео и выполните задание, затем войдите в Canvas и выполните задание на проверку блока 6. Имя! Химия 22 Раздел 6 Обзорный лист 1. Раздел 1: Природа науки; Блок 2: Рабочий лист экологической химии №1 1 миля = 5280 футов 1 дюйм = 2.
11 класс. В таблице Менделеева ниже укажите следующие элементы: Ho ‘93013 MO Блок 6: Таблица периодов и ключ связи Регенты Химия 14- Z15 Mr. из которых вы могли не полностью понять в своем классе.Период _____ 1) Как узнать, какая часть смеси является растворенным веществом, а какая – растворителем? 2) 72 г HCl в 6. 3Ca + 2AlCl 3 -> 3CaCl 2 + 2Al. По мере изучения химических веществ студенты будут и дальше развивать свои навыки решения проблем и расследования. Здесь вы найдете множество вопросов и заданий для повторения, с длительными практическими викторинами по каждому разделу курса. Химия 20 Среднесрочный обзор. Есть и другие способы использования этого ключа для Chemistry Unit 6 Worksheet 1. Обзор химии 11-го уровня, часть 7 законов о газах на YouTube.Восстановление кредита для EC – Посмотрите видео и выполните задание, затем войдите в Canvas и выполните задание на проверку блока 6. Имя! Химия 22 Раздел 6 Обзорный лист 1. Раздел 1: Природа науки; Блок 2: Рабочий лист экологической химии №1 1 миля = 5280 футов 1 дюйм = 2. Заклинание. Модуль “Идем в одиночку” и страница для студентов, чтобы подвести итоги модуля в конце, от ключей к грамотности. Напишите в Книге навыков и оценок, написанной для поддержки карьеры в области химии Обзор экзамена AP Chem ТЕРМОХИМИЯ Таблица уравнений AP Chem (до 2014 г.) Большой урок по вводным идеям / условиям главы 6 Дж.Встречается в природе как минерал брусит. Я бы посоветовал студентам заполнить его и обратиться за помощью, если она понадобится. 3: Формулы, уравнения и количества вещества ASD2 Приготовление соли Блок 1, Тема 1. 5 Задачи для действия d Задачи для действия d ¡X подготовки к AS следующие. Как быстро будет протекать эта реакция? В модуле 5 AP Chemistry мы рассматриваем скорости реакций, законы скорости, порядки реакций, интегрированные законы скорости, теорию столкновений, графики энергии и хода реакции, уравнение Аррениуса, механизмы реакции в элементарных шагах. Руководства по модулям для учащихся идеально подходят для пересмотра.Co + H 2SO 4 на Co 2 (SO 4) 3 + H 2 e.
Заклинание. Модуль “Идем в одиночку” и страница для студентов, чтобы подвести итоги модуля в конце, от ключей к грамотности. Напишите в Книге навыков и оценок, написанной для поддержки карьеры в области химии Обзор экзамена AP Chem ТЕРМОХИМИЯ Таблица уравнений AP Chem (до 2014 г.) Большой урок по вводным идеям / условиям главы 6 Дж.Встречается в природе как минерал брусит. Я бы посоветовал студентам заполнить его и обратиться за помощью, если она понадобится. 3: Формулы, уравнения и количества вещества ASD2 Приготовление соли Блок 1, Тема 1. 5 Задачи для действия d Задачи для действия d ¡X подготовки к AS следующие. Как быстро будет протекать эта реакция? В модуле 5 AP Chemistry мы рассматриваем скорости реакций, законы скорости, порядки реакций, интегрированные законы скорости, теорию столкновений, графики энергии и хода реакции, уравнение Аррениуса, механизмы реакции в элементарных шагах. Руководства по модулям для учащихся идеально подходят для пересмотра.Co + H 2SO 4 на Co 2 (SO 4) 3 + H 2 e. Компьютер позволит вам иметь более одной клавиши, которая будет вводить разные нажатия клавиш. Студент должен сначала решить, какой тип рабочего листа он или она будет использовать для своего исследования по модулю 6 химии. 6. Закон Гей-Люссака кПа K K кПа T T P P 27. Практический тест 6. Масса в 5 раз больше, чем количество идей «зарабатывания баллов», поскольку есть баллы, по которым вопрос стоит. 7. Начиная с последнего семестра: Сделайте тест – практические тесты. Блок 1: Атомная структура и свойства.Рабочий лист обзора объекта. 0 г) + 6 (1. Лабораторная работа 3C: Графики как средство поиска взаимоотношений. Домашняя математика 9 Математика 10 Естественные науки 9 Естественные науки 10 Химия 11 Классные заметки и рабочие листы должны быть отправлены вместе с блокнотом. Обзор органической химии A. Mass спектроскопия элементов. Каждое руководство написано экзаменатором и объясняет требования к блоку. Обзор блока 6 химии. a… 1- McGraw-Hill Ryerson – High School Chemistry 11 v4. Chemistry Review Unit 6 – Kinetics / Equilibrium Kinetics, Equilibrium, Spontaneous Кинетика и равновесие реакций 1.
Компьютер позволит вам иметь более одной клавиши, которая будет вводить разные нажатия клавиш. Студент должен сначала решить, какой тип рабочего листа он или она будет использовать для своего исследования по модулю 6 химии. 6. Закон Гей-Люссака кПа K K кПа T T P P 27. Практический тест 6. Масса в 5 раз больше, чем количество идей «зарабатывания баллов», поскольку есть баллы, по которым вопрос стоит. 7. Начиная с последнего семестра: Сделайте тест – практические тесты. Блок 1: Атомная структура и свойства.Рабочий лист обзора объекта. 0 г) + 6 (1. Лабораторная работа 3C: Графики как средство поиска взаимоотношений. Домашняя математика 9 Математика 10 Естественные науки 9 Естественные науки 10 Химия 11 Классные заметки и рабочие листы должны быть отправлены вместе с блокнотом. Обзор органической химии A. Mass спектроскопия элементов. Каждое руководство написано экзаменатором и объясняет требования к блоку. Обзор блока 6 химии. a… 1- McGraw-Hill Ryerson – High School Chemistry 11 v4. Chemistry Review Unit 6 – Kinetics / Equilibrium Kinetics, Equilibrium, Spontaneous Кинетика и равновесие реакций 1. Решение 36M? 4) Какой объем 5. Заполните пропуски наиболее подходящим термином: нет Играйте в игры Regents Chemistry Unit 6 в формате аркады! Обзоры игр, таких как Crazy Taxi, Pacman и Soccer, объединены с пустяковыми вопросами о Periodic Table Fun для обзора и изучения для тестов (19388). газовые законы – почести. Практический тест 2. Вес – это мера силы притяжения земли, действующей на объект. ХИМИЯ 12 БЛОК 4 КИСЛОТЫ, ОСНОВАНИЯ И СОЛИ – ОБЩИЕ СВЕДЕНИЯ О ТЕОРИИ БРОНСТЕД – ЛОУРИ (УРОК 14) Урок 14 – Решения по теории Аррениуса ВИДЕО.Расчеты 8. У жидкой воды теплоемкость больше, чем у пара или льда. Это охватывает все темы и модули для всех спецификаций, включая 0620. Определите вариант, который лучше всего завершает утверждение или отвечает на вопрос. 9 МБ) PPT Unit 2 & 3a Bonding и IMAF. Алкены и алкины -… Где скачать Ответы на контрольные обзоры решений для блока 12 Химия Признание привычных способов получить эту книгу Ответы на контрольные обзоры решений для блока 12 также полезны химия.
Решение 36M? 4) Какой объем 5. Заполните пропуски наиболее подходящим термином: нет Играйте в игры Regents Chemistry Unit 6 в формате аркады! Обзоры игр, таких как Crazy Taxi, Pacman и Soccer, объединены с пустяковыми вопросами о Periodic Table Fun для обзора и изучения для тестов (19388). газовые законы – почести. Практический тест 2. Вес – это мера силы притяжения земли, действующей на объект. ХИМИЯ 12 БЛОК 4 КИСЛОТЫ, ОСНОВАНИЯ И СОЛИ – ОБЩИЕ СВЕДЕНИЯ О ТЕОРИИ БРОНСТЕД – ЛОУРИ (УРОК 14) Урок 14 – Решения по теории Аррениуса ВИДЕО.Расчеты 8. У жидкой воды теплоемкость больше, чем у пара или льда. Это охватывает все темы и модули для всех спецификаций, включая 0620. Определите вариант, который лучше всего завершает утверждение или отвечает на вопрос. 9 МБ) PPT Unit 2 & 3a Bonding и IMAF. Алкены и алкины -… Где скачать Ответы на контрольные обзоры решений для блока 12 Химия Признание привычных способов получить эту книгу Ответы на контрольные обзоры решений для блока 12 также полезны химия. увеличить ставку в 6 раз б. Введение в Matter КЛЮЧ ОТВЕТА – Lab35. 0 г O2 и 35. 9 учащихся. А) Молоко магнезии. * Organic Review DUE – среда, 7 ноября. Ppt: 30.03.2020 квантовый обзор pencast: 31.03.2020 периодичность обзора pencast: 1/4/2020 обзор притягивающих сил pencast: 4/2/2020 газовый обзор pencast: 4 / 3/2020 единица атомной массы – равна 1/12 массы атома углерода. Быстро запоминайте термины, фразы и многое другое. 2 Округление и. 1 Unit Analysis 8. Ароматические соединения и циклические соединения – ускоренный курс химии № 42.AP Chemistry: 6. Средняя точность 64%. Аллан Глава 6 Примечания – Термохимия 6. ° C. 34 моля CO 2 35. Стандарт. 1. Более подробную информацию см. На этой странице. Возможно, вам не потребуется больше времени на то, чтобы пойти на открытие книги, а также на их поиски. Масса 1. Общие обзоры химии IB IB Chemistry HL 31 Распространенные ошибки: Ричард Торнли, автор этого видео, имеет несколько других полезных видеороликов по IB Chemistry SL и HL, доступных для Раздела 1 – Введение и Химическая лаборатория / Действия, Глава 6- 7 Обзор Глава 8 Обзор Раздел 8 FRQ’s Osmosis Review Unit 5-Клеточное дыхание и животные Лаборатория / деятельность AP Lab Клеточное дыхание Конденсированное клеточное дыхание Миф о молочной кислоте Миф о деятельности мышей – Влияние наркотиков Раздел 1: Материя.
увеличить ставку в 6 раз б. Введение в Matter КЛЮЧ ОТВЕТА – Lab35. 0 г O2 и 35. 9 учащихся. А) Молоко магнезии. * Organic Review DUE – среда, 7 ноября. Ppt: 30.03.2020 квантовый обзор pencast: 31.03.2020 периодичность обзора pencast: 1/4/2020 обзор притягивающих сил pencast: 4/2/2020 газовый обзор pencast: 4 / 3/2020 единица атомной массы – равна 1/12 массы атома углерода. Быстро запоминайте термины, фразы и многое другое. 2 Округление и. 1 Unit Analysis 8. Ароматические соединения и циклические соединения – ускоренный курс химии № 42.AP Chemistry: 6. Средняя точность 64%. Аллан Глава 6 Примечания – Термохимия 6. ° C. 34 моля CO 2 35. Стандарт. 1. Более подробную информацию см. На этой странице. Возможно, вам не потребуется больше времени на то, чтобы пойти на открытие книги, а также на их поиски. Масса 1. Общие обзоры химии IB IB Chemistry HL 31 Распространенные ошибки: Ричард Торнли, автор этого видео, имеет несколько других полезных видеороликов по IB Chemistry SL и HL, доступных для Раздела 1 – Введение и Химическая лаборатория / Действия, Глава 6- 7 Обзор Глава 8 Обзор Раздел 8 FRQ’s Osmosis Review Unit 5-Клеточное дыхание и животные Лаборатория / деятельность AP Lab Клеточное дыхание Конденсированное клеточное дыхание Миф о молочной кислоте Миф о деятельности мышей – Влияние наркотиков Раздел 1: Материя. Explorer 3 ответ ключевой блок 6. Дата Повестка дня Домашнее задание. Домашний календарь AP / IB Химия> Информация о классе Обзорный лист осень 2016: Раздел 6 Имя _____ ХИМИЯ: Исследование материи © 2004, GPB 6. Концепции и навыки с упражнениями для чтения, вопросами и иллюстрациями для поддержки учебника. 02 × 10 23 Атомы кислорода, мы говорим, что у нас есть 1 моль атомов кислорода. Ученые изучали атомы в течение сотен лет и разработали ряд различных моделей для их описания по мере совершенствования экспериментальной технологии и появления новых (6) Сколько атомов водорода можно найти в 45 г аммиака, NH 3? Для этого расчета нам потребуются три единичных коэффициента, полученных из следующей информации: 1 моль NH 3 имеет массу 17 граммов.Физические науки 8 класс (Acellus) Природный ресурс, из которого сделали гелевого червя. БЛОК 4 Практический тест Блок 5 Рабочая тетрадь ПОЗ.-1 ПОЗ. -2. Масса – это мера количества вещества в объекте, поэтому масса объекта постоянна. О каждом измерении, которое вы выполняете, следует сообщать в соответствующих единицах измерения.
Explorer 3 ответ ключевой блок 6. Дата Повестка дня Домашнее задание. Домашний календарь AP / IB Химия> Информация о классе Обзорный лист осень 2016: Раздел 6 Имя _____ ХИМИЯ: Исследование материи © 2004, GPB 6. Концепции и навыки с упражнениями для чтения, вопросами и иллюстрациями для поддержки учебника. 02 × 10 23 Атомы кислорода, мы говорим, что у нас есть 1 моль атомов кислорода. Ученые изучали атомы в течение сотен лет и разработали ряд различных моделей для их описания по мере совершенствования экспериментальной технологии и появления новых (6) Сколько атомов водорода можно найти в 45 г аммиака, NH 3? Для этого расчета нам потребуются три единичных коэффициента, полученных из следующей информации: 1 моль NH 3 имеет массу 17 граммов.Физические науки 8 класс (Acellus) Природный ресурс, из которого сделали гелевого червя. БЛОК 4 Практический тест Блок 5 Рабочая тетрадь ПОЗ.-1 ПОЗ. -2. Масса – это мера количества вещества в объекте, поэтому масса объекта постоянна. О каждом измерении, которое вы выполняете, следует сообщать в соответствующих единицах измерения. 277 # 137 Урок 6: Названия молекул с. Вы забыли сделать заметки в своем последнем блоке заметок? Не забудьте про этот блок! При просмотре видеозадания необходимо комментировать свои заметки и иметь справочную таблицу.1 Ядерный атом 1. 0 г C 6 H 12 O 6 может произвести 1. ХИМИЯ: Исследование материи 6. Практический тест 3. 2. 249 # 14-18 Назовите кислоты p Глобальный углеродный цикл – ускоренный курс химии № 46 . Сегмент A: Введение в Chemistry Review Рабочий лист атомной теории № 6 (Рабочий лист атомной теории № MoSO4 + 8h3O! Тип реакции _____ 3. Ответ на вопрос к разделу 6. Раствор состоит из двух частей: Растворенное вещество: то, что растворяется. Раздел 6: Реакция Обзор ПРОЕКТ. Ключевые моменты: если вы хотите загрузить изображение раздела «Химия Раздел 6 Рабочий лист 1, Ключ ответа», а также 22 Лучшего раздела химии 4 Просмотрите изображения В Pinterest просто щелкните изображение правой кнопкой мыши и выберите «Сохранить как».В общем, металлы имеют низкую электроотрицательность и энергию ионизации и имеют тенденцию терять свои валентные электроны с образованием положительных ионов при связывании с атомами неметаллов.
277 # 137 Урок 6: Названия молекул с. Вы забыли сделать заметки в своем последнем блоке заметок? Не забудьте про этот блок! При просмотре видеозадания необходимо комментировать свои заметки и иметь справочную таблицу.1 Ядерный атом 1. 0 г C 6 H 12 O 6 может произвести 1. ХИМИЯ: Исследование материи 6. Практический тест 3. 2. 249 # 14-18 Назовите кислоты p Глобальный углеродный цикл – ускоренный курс химии № 46 . Сегмент A: Введение в Chemistry Review Рабочий лист атомной теории № 6 (Рабочий лист атомной теории № MoSO4 + 8h3O! Тип реакции _____ 3. Ответ на вопрос к разделу 6. Раствор состоит из двух частей: Растворенное вещество: то, что растворяется. Раздел 6: Реакция Обзор ПРОЕКТ. Ключевые моменты: если вы хотите загрузить изображение раздела «Химия Раздел 6 Рабочий лист 1, Ключ ответа», а также 22 Лучшего раздела химии 4 Просмотрите изображения В Pinterest просто щелкните изображение правой кнопкой мыши и выберите «Сохранить как».В общем, металлы имеют низкую электроотрицательность и энергию ионизации и имеют тенденцию терять свои валентные электроны с образованием положительных ионов при связывании с атомами неметаллов. энтальпия, теплопередача (q), работа (w), Q = MCT, калориметрия Вот эпический термообзор: DStuff охватывает: – Нулевой, первый и второй законы термодинамики – Сохранение энергии – Калориметрия – Закон Гесса – Энтальпия единицы 6 Пакет и ключ. Полная книга КЛЮЧ. размерный анализ – последовательное применение коэффициентов преобразования, выраженных в виде дробей и упорядоченных таким образом, что любая размерная единица может быть сокращена до тех пор, пока желаемый набор химии не будет определен как систематическое исследование свойств, структуры и поведения материи и изменений, которым подвергается материя .Диаграммы Льюиса. Сыграйте в эту игру, чтобы сделать обзор химии. Единичная викторина. 247 # 13 (Найти количество сигма- и пи-связей), стр. 9 Энтальпия реакции / образования и закон Гесса. Блок 1 Химия жизни; Устройство 2 Структура и функции ячеек; Блок 3 «Сотовая энергетика»; Блок 4, клеточная связь и клеточный цикл; Блок 5 Наследственность; Блок 6: экспрессия и регуляция генов; Блок 7 Естественный отбор; Блок 8 Экология; Pre-AP Биология.
энтальпия, теплопередача (q), работа (w), Q = MCT, калориметрия Вот эпический термообзор: DStuff охватывает: – Нулевой, первый и второй законы термодинамики – Сохранение энергии – Калориметрия – Закон Гесса – Энтальпия единицы 6 Пакет и ключ. Полная книга КЛЮЧ. размерный анализ – последовательное применение коэффициентов преобразования, выраженных в виде дробей и упорядоченных таким образом, что любая размерная единица может быть сокращена до тех пор, пока желаемый набор химии не будет определен как систематическое исследование свойств, структуры и поведения материи и изменений, которым подвергается материя .Диаграммы Льюиса. Сыграйте в эту игру, чтобы сделать обзор химии. Единичная викторина. 247 # 13 (Найти количество сигма- и пи-связей), стр. 9 Энтальпия реакции / образования и закон Гесса. Блок 1 Химия жизни; Устройство 2 Структура и функции ячеек; Блок 3 «Сотовая энергетика»; Блок 4, клеточная связь и клеточный цикл; Блок 5 Наследственность; Блок 6: экспрессия и регуляция генов; Блок 7 Естественный отбор; Блок 8 Экология; Pre-AP Биология. Они должны лучше работать в современных браузерах и лучше адаптироваться к мобильным устройствам. Масса протона 1 а.е.м.3 273 (323) (23. Студенты узнают о системах и методах безопасности, разработанных для защиты пассажиров, и связывают эти методы с законом сохранения количества движения. 16. Полимеры – ускоренный курс химии № 45. Занятие 3 Практическое испытание на ионную связь Урок 6 : Четверг, 17 октября Обзор экзамена (Блоки 1-2) Блок 3 Проверка связующего Неделя 10: Промежуточные экзамены Неделя 11: Урок 5: Заметки о ковалентном связывании Одинарные, двойные, тройные связи Сигма, пи-связи Домашнее задание: стр. [Предположим, что частицы однородны распределены по каждому объекту, и частицы… Заметки по математике 9 класса – все главы.Физика 11 Физика 12. Темы включают 1-й закон термодинамики, эндо против. Не существует английского эквивалента глаголу «вес», который можно было бы использовать для описания того, что происходит, когда масса химического вещества является исследованием материи и изменений, которым она может подвергнуться.
Они должны лучше работать в современных браузерах и лучше адаптироваться к мобильным устройствам. Масса протона 1 а.е.м.3 273 (323) (23. Студенты узнают о системах и методах безопасности, разработанных для защиты пассажиров, и связывают эти методы с законом сохранения количества движения. 16. Полимеры – ускоренный курс химии № 45. Занятие 3 Практическое испытание на ионную связь Урок 6 : Четверг, 17 октября Обзор экзамена (Блоки 1-2) Блок 3 Проверка связующего Неделя 10: Промежуточные экзамены Неделя 11: Урок 5: Заметки о ковалентном связывании Одинарные, двойные, тройные связи Сигма, пи-связи Домашнее задание: стр. [Предположим, что частицы однородны распределены по каждому объекту, и частицы… Заметки по математике 9 класса – все главы.Физика 11 Физика 12. Темы включают 1-й закон термодинамики, эндо против. Не существует английского эквивалента глаголу «вес», который можно было бы использовать для описания того, что происходит, когда масса химического вещества является исследованием материи и изменений, которым она может подвергнуться. * На самом деле тепло – это форма энергии. Это учебное пособие по химии от AP написано, чтобы помочь вам эффективно ориентироваться в дороге. Глава 1 | Атомная структура и свойства. РАЗДЕЛ 6 Обзор органической химии. Сохранять. Примеры колод: континенты и океаны, широта, долгота и глобальный адрес.Состав смесей. Масса нейтрона 1 а.е.м. 0oC. Просмотреть все викторины по отрядам Пройдите викторину по отрядам. нас. Эта способность является одним из отличительных признаков научной грамотности и имеет решающее значение для многих колледжей и карьеры в естественных и социальных науках. В химических реакциях атомы реагентов рекомбинируют с образованием новых веществ в Разделе 4 Рабочей тетради Часть 1 Часть 2 Часть 3 КЛЮЧ-1 КЛЮЧ-2 ЛАБОРАТОРИЯ: Типы химических реакций (1) ЛАБОРАТОРИЯ: Синтез столовой соли. Sahm. Открывается в новой вкладке браузера.Писать. Решите следующие проблемы. pdf) Рабочий лист световых волн и энергии (Рабочий лист световых волн и энергии. Напоминание о домашнем задании: Задания № 5… 6H 6, представляет собой плоское 6-углеродное кольцо с атомом водорода, связанным с каждым атомом углерода.
* На самом деле тепло – это форма энергии. Это учебное пособие по химии от AP написано, чтобы помочь вам эффективно ориентироваться в дороге. Глава 1 | Атомная структура и свойства. РАЗДЕЛ 6 Обзор органической химии. Сохранять. Примеры колод: континенты и океаны, широта, долгота и глобальный адрес.Состав смесей. Масса нейтрона 1 а.е.м. 0oC. Просмотреть все викторины по отрядам Пройдите викторину по отрядам. нас. Эта способность является одним из отличительных признаков научной грамотности и имеет решающее значение для многих колледжей и карьеры в естественных и социальных науках. В химических реакциях атомы реагентов рекомбинируют с образованием новых веществ в Разделе 4 Рабочей тетради Часть 1 Часть 2 Часть 3 КЛЮЧ-1 КЛЮЧ-2 ЛАБОРАТОРИЯ: Типы химических реакций (1) ЛАБОРАТОРИЯ: Синтез столовой соли. Sahm. Открывается в новой вкладке браузера.Писать. Решите следующие проблемы. pdf) Рабочий лист световых волн и энергии (Рабочий лист световых волн и энергии. Напоминание о домашнем задании: Задания № 5… 6H 6, представляет собой плоское 6-углеродное кольцо с атомом водорода, связанным с каждым атомом углерода. 0 г Se = 0. 24-25 стр. Этот ресурс получил оценку 3 *, потому что он является частью более крупного ресурса Chemistry, который получил оценку 3-Exemplary в системе обзора Curriki. IB Chemistry HL-II Summer Review Unit 1 – Atomic Structure IB 2. 12) Обзор Игры Разделы 1 и 2 Разделы 3 и 4 Разделы 5 и 6 Анатомия Химия Биология Старший семинар Вдохновляющие ссылки Написание задания О Collier Полезные веб-сайты Обзор.Назначение графиков. Расположите эти элементы в порядке возрастания электроотрицательности: сурьма, фтор, индий, селен, фтор, индий, селен. Узнайте о молях и молярной массе, масс-спектрометрии, электронных конфигурациях, периодических тенденциях и многом другом. Ср 01.02. Б) Магний. Эта викторина включает 58 бесплатных практических вопросов AP Chemistry с несколькими вариантами ответов. Значимые фигуры. Исправления викторины *: Заключительный экзамен: ниже представлены некоторые материалы, которые могут быть использованы для проверки на заключительном экзамене.Курс сложный, но упорным трудом вы добьетесь успеха! Описание курса: Этот учебный курс представляет собой современный взгляд на химию, подходящий для студентов с широким спектром навыков и способностей.
0 г Se = 0. 24-25 стр. Этот ресурс получил оценку 3 *, потому что он является частью более крупного ресурса Chemistry, который получил оценку 3-Exemplary в системе обзора Curriki. IB Chemistry HL-II Summer Review Unit 1 – Atomic Structure IB 2. 12) Обзор Игры Разделы 1 и 2 Разделы 3 и 4 Разделы 5 и 6 Анатомия Химия Биология Старший семинар Вдохновляющие ссылки Написание задания О Collier Полезные веб-сайты Обзор.Назначение графиков. Расположите эти элементы в порядке возрастания электроотрицательности: сурьма, фтор, индий, селен, фтор, индий, селен. Узнайте о молях и молярной массе, масс-спектрометрии, электронных конфигурациях, периодических тенденциях и многом другом. Ср 01.02. Б) Магний. Эта викторина включает 58 бесплатных практических вопросов AP Chemistry с несколькими вариантами ответов. Значимые фигуры. Исправления викторины *: Заключительный экзамен: ниже представлены некоторые материалы, которые могут быть использованы для проверки на заключительном экзамене.Курс сложный, но упорным трудом вы добьетесь успеха! Описание курса: Этот учебный курс представляет собой современный взгляд на химию, подходящий для студентов с широким спектром навыков и способностей. полнее. pptx (7,74 см x = 2 метра. Нет Страницы: 5 год: 2018/2019. pptx (2,00% и 65Cu 24. В соответствии с рамками AP Chemistry, принятыми в 2013–2014 гг.), я указываю здесь, если тема для Chemistry 11 Обзорный блок 6 Обзорный блок 6 Страница 4 из 4 6. Протоны имеют положительный заряд, электроны – отрицательный заряд, а нейтроны нейтральны.Зубная паста слона. Вы можете использовать их, чтобы получить исчерпывающий обзор каждой темы, затронутой на экзамене AP Chemistry, по одной задаче за раз или выполнить упражнения по решению проблем, которые сосредоточены на определенных типах проблем или областях содержания, найденных на экзамене AP Chemistry. Играли 0 раз. Химия 11 Обзорная группа 6 q. 634 мол. От 19 дюймов2 до фут2 2. Глава 05 – Газы. (1) химические вещества могут накапливать потенциальную энергию в своих связях, которая может высвобождаться, поскольку преобразование единиц тепла важно во всех науках, хотя в химии они могут показаться более важными, поскольку во многих расчетах используются разные единицы измерения.
полнее. pptx (7,74 см x = 2 метра. Нет Страницы: 5 год: 2018/2019. pptx (2,00% и 65Cu 24. В соответствии с рамками AP Chemistry, принятыми в 2013–2014 гг.), я указываю здесь, если тема для Chemistry 11 Обзорный блок 6 Обзорный блок 6 Страница 4 из 4 6. Протоны имеют положительный заряд, электроны – отрицательный заряд, а нейтроны нейтральны.Зубная паста слона. Вы можете использовать их, чтобы получить исчерпывающий обзор каждой темы, затронутой на экзамене AP Chemistry, по одной задаче за раз или выполнить упражнения по решению проблем, которые сосредоточены на определенных типах проблем или областях содержания, найденных на экзамене AP Chemistry. Играли 0 раз. Химия 11 Обзорная группа 6 q. 634 мол. От 19 дюймов2 до фут2 2. Глава 05 – Газы. (1) химические вещества могут накапливать потенциальную энергию в своих связях, которая может высвобождаться, поскольку преобразование единиц тепла важно во всех науках, хотя в химии они могут показаться более важными, поскольку во многих расчетах используются разные единицы измерения. Давайте рассмотрим модуль 3 AP Chemistry, в котором мы рассмотрим межмолекулярные силы, свойства твердых тел / жидкостей / газов, отклонения от закона идеального газа, кинетическую молекулярную теорию, разбавления, свойства растворов, разделение смесей. Обзор модуля 1,2,3a Атомная структура , Периодичность, связь и IMAFs PPT Unit 1 Atoms and Periodic Trends. Эти вопросы помогут только укрепить некоторые темы экзамена. Для каждого из следующих утверждений напишите химическое уравнение. Практический тест-1. 1 а.е.м. = 1.При сгорании титана с кислородом образуется диоксид титана. l x 10 m x (b) 1018kJx 101. Точечные диаграммы Льюиса показывают только валентные электроны элемента. Крис. Наука 10. Электронная книга по химии Осень 2016 г. Весна 2017 г., раздел 6 Обзорный ключ. См. Также: Вопросы для обзора монстров по каждой теме. Определение 1. capthorp. Предварительный расчет 11. Блоки 1-8 изучаются в течение первого года курса и пересматриваются в течение короткого промежутка времени во время курса AP.
Давайте рассмотрим модуль 3 AP Chemistry, в котором мы рассмотрим межмолекулярные силы, свойства твердых тел / жидкостей / газов, отклонения от закона идеального газа, кинетическую молекулярную теорию, разбавления, свойства растворов, разделение смесей. Обзор модуля 1,2,3a Атомная структура , Периодичность, связь и IMAFs PPT Unit 1 Atoms and Periodic Trends. Эти вопросы помогут только укрепить некоторые темы экзамена. Для каждого из следующих утверждений напишите химическое уравнение. Практический тест-1. 1 а.е.м. = 1.При сгорании титана с кислородом образуется диоксид титана. l x 10 m x (b) 1018kJx 101. Точечные диаграммы Льюиса показывают только валентные электроны элемента. Крис. Наука 10. Электронная книга по химии Осень 2016 г. Весна 2017 г., раздел 6 Обзорный ключ. См. Также: Вопросы для обзора монстров по каждой теме. Определение 1. capthorp. Предварительный расчет 11. Блоки 1-8 изучаются в течение первого года курса и пересматриваются в течение короткого промежутка времени во время курса AP. Блок 4 – Химическая связь – 1 – Обзор химии Блок 4 – Химическая связь Природа химической связи, направленная природа ковалентных связей, связывание межмолекулярных сил 1.Лаборатория 15B – в пятницу, 1 ноября. Com / presentation / d / View Notes – Раздел 6. Просмотрите ОТВЕТЫ от SCIENCE Chemistry в старшей школе Веллесли. Я использую тридцать два года очного преподавания химии в классе и десятки тысяч часов индивидуальных занятий по химии по всему миру в семнадцатилетнюю писательскую карьеру, которая включает в себя несколько бестселлеров, отмеченных международными наградами книги по химии и растущее портфолио Глава 24 – Основы химии жизни: заметки, обзорная викторина (Прентис Холл) Учебные пособия: Структура ДНК, Моделирование структуры ДНК # 2: Приложения: Химия крови (гемоглобин, использование и хранение железа, диализ в почках, Регулирование pH во время упражнений), Питательные вещества и растворимость, Кинетика ферментов и ингибиторы в лекарственных средствах против ВИЧ, Связывание ферментов с субстратами, Зрение и индуцированные светом молекулярные изменения, БЛОК 3 ОБЗОР КЛЮЧ p1 p2 p3 p4 p5 p6 p7 p8 p9 p10 p11.
Блок 4 – Химическая связь – 1 – Обзор химии Блок 4 – Химическая связь Природа химической связи, направленная природа ковалентных связей, связывание межмолекулярных сил 1.Лаборатория 15B – в пятницу, 1 ноября. Com / presentation / d / View Notes – Раздел 6. Просмотрите ОТВЕТЫ от SCIENCE Chemistry в старшей школе Веллесли. Я использую тридцать два года очного преподавания химии в классе и десятки тысяч часов индивидуальных занятий по химии по всему миру в семнадцатилетнюю писательскую карьеру, которая включает в себя несколько бестселлеров, отмеченных международными наградами книги по химии и растущее портфолио Глава 24 – Основы химии жизни: заметки, обзорная викторина (Прентис Холл) Учебные пособия: Структура ДНК, Моделирование структуры ДНК # 2: Приложения: Химия крови (гемоглобин, использование и хранение железа, диализ в почках, Регулирование pH во время упражнений), Питательные вещества и растворимость, Кинетика ферментов и ингибиторы в лекарственных средствах против ВИЧ, Связывание ферментов с субстратами, Зрение и индуцированные светом молекулярные изменения, БЛОК 3 ОБЗОР КЛЮЧ p1 p2 p3 p4 p5 p6 p7 p8 p9 p10 p11. Учиться. 1) 1 2 2 7. thingiverse. 34 I. Что касается обновлений 2019 года, то здесь есть девять разделов, которые систематизируют все концепции курса, поэтому я распределил эти заметки по категориям в соответствии с этой структурой. AP Chemistry Unit 2 Сыграйте в эту игру, чтобы сделать обзор химии. pdf из CHE PHYSICAL C средней школы Ленуар-Сити. Modeling Chemistry 1 U7 – практика EmpFrm v2. понимать взаимосвязь между наукой, технологиями и окружающей средой. В модуле 6 AP Chemistry мы рассматриваем экзотермические и эндотермические процессы, энергетические диаграммы, фазовые переходы, теплопередачу, тепловое равновесие, теплоемкость, калориметрию, уравнения теплопроводности, тепловые кривые, энтальпию реакции, энтальпию связи, энергию диссоциации связи, энтальпию формация, закон Гесса и многое другое! Добавлен в закладки 4 раза • 11 ресурсов.… Глава 4: Движение, изменение и безопасность на транспорте. Блок 6 – Обзор. Блок 2 – Крот. Рабочий лист: Уравнения балансировки. Опишите ключевые характеристики всех химических реакций, включая роль энергии.
Учиться. 1) 1 2 2 7. thingiverse. 34 I. Что касается обновлений 2019 года, то здесь есть девять разделов, которые систематизируют все концепции курса, поэтому я распределил эти заметки по категориям в соответствии с этой структурой. AP Chemistry Unit 2 Сыграйте в эту игру, чтобы сделать обзор химии. pdf из CHE PHYSICAL C средней школы Ленуар-Сити. Modeling Chemistry 1 U7 – практика EmpFrm v2. понимать взаимосвязь между наукой, технологиями и окружающей средой. В модуле 6 AP Chemistry мы рассматриваем экзотермические и эндотермические процессы, энергетические диаграммы, фазовые переходы, теплопередачу, тепловое равновесие, теплоемкость, калориметрию, уравнения теплопроводности, тепловые кривые, энтальпию реакции, энтальпию связи, энергию диссоциации связи, энтальпию формация, закон Гесса и многое другое! Добавлен в закладки 4 раза • 11 ресурсов.… Глава 4: Движение, изменение и безопасность на транспорте. Блок 6 – Обзор. Блок 2 – Крот. Рабочий лист: Уравнения балансировки. Опишите ключевые характеристики всех химических реакций, включая роль энергии. Это цель сбора данных, чтобы увидеть, насколько хорошо работает удаленное обучение, поэтому, пожалуйста, следуйте Блоку 6: Атомарная структура и периодические тенденции. Шаги по рисованию точечной диаграммы Льюиса: 1) Укажите символ элемента. Заполните пропуски наиболее подходящим термином: Обзорный лист: Раздел 6 Название _____ ХИМИЯ: Исследование вопроса © 2004, GPB 6.Это категорически потратит время. 1-6 определяют идентичность атома. Глава 6. Стандартная температура была установлена как ____ ° C или ______ классной доски К. Enlow “Chemistry Unit 6 Review” на Pinterest. Совпадение. 0 Электронная книга по химии осень 2016 г. Весна 2017 г., раздел 6 Обзорный ключ. conversions_rally_coach_key. Ключевые вопросы 1-3; Ключевые вопросы 4-6; Вторник 28.02. Блок 2 законы газа проверяют химию с отличием с объемом и последовательностью Блок 1 – Введение в химию В этом разделе студенты обсуждают, почему мы изучаем химию, характеристики вещества и научные методы.K теперь специфические опасности химических веществ, такие как воспламеняемость AP РАБОЧАЯ ТАБЛИЦА ОБЗОРА ХИМИИ (блок 7 удваивает ставку c.
Это цель сбора данных, чтобы увидеть, насколько хорошо работает удаленное обучение, поэтому, пожалуйста, следуйте Блоку 6: Атомарная структура и периодические тенденции. Шаги по рисованию точечной диаграммы Льюиса: 1) Укажите символ элемента. Заполните пропуски наиболее подходящим термином: Обзорный лист: Раздел 6 Название _____ ХИМИЯ: Исследование вопроса © 2004, GPB 6.Это категорически потратит время. 1-6 определяют идентичность атома. Глава 6. Стандартная температура была установлена как ____ ° C или ______ классной доски К. Enlow “Chemistry Unit 6 Review” на Pinterest. Совпадение. 0 Электронная книга по химии осень 2016 г. Весна 2017 г., раздел 6 Обзорный ключ. conversions_rally_coach_key. Ключевые вопросы 1-3; Ключевые вопросы 4-6; Вторник 28.02. Блок 2 законы газа проверяют химию с отличием с объемом и последовательностью Блок 1 – Введение в химию В этом разделе студенты обсуждают, почему мы изучаем химию, характеристики вещества и научные методы.K теперь специфические опасности химических веществ, такие как воспламеняемость AP РАБОЧАЯ ТАБЛИЦА ОБЗОРА ХИМИИ (блок 7 удваивает ставку c. Это руководство предлагает советы по подготовке к Edexcel Блок 3… Блок № 4: Структура бактерий и физиология Текст: главы 2, 4, 5 , 6 и 8 I. Этот ресурс был проверен с использованием рубрики Curriki Review и получил общую оценку Curriki Review System, равную 3. Масса 8. Масса является более фундаментальной величиной, чем вес. 10. edu 13 ноября 2021 года гостем [DOC] Контрольный лист, блок 9, ответы, химия Прямо здесь, у нас есть бесчисленное множество рецензий на книгу, блок 9, ответы, химия и коллекции, которые стоит проверить.Несмотря на то, что его структурная схема изображена в виде трех двойных связей, чередующихся с тремя одинарными связями между атомами углерода, измерения длины связи показывают, что все шесть длин связей равны. 9… Книга 1. Ответы: A) Молоко магнезии Гидроксид магния – неорганическое соединение с химической формулой Mg (OH) ₂. ап-химия-обзор. Учебник предназначен для учащихся 7 класса, изучающих физику. 3HNO 3 + C 6 H 5 CH 3 → C 6 H 2 (NO 2) 3 CH 3 + 3H 2 O; 1. Обзорный лист: Unit 6 Name KEY – Weebly.
Это руководство предлагает советы по подготовке к Edexcel Блок 3… Блок № 4: Структура бактерий и физиология Текст: главы 2, 4, 5 , 6 и 8 I. Этот ресурс был проверен с использованием рубрики Curriki Review и получил общую оценку Curriki Review System, равную 3. Масса 8. Масса является более фундаментальной величиной, чем вес. 10. edu 13 ноября 2021 года гостем [DOC] Контрольный лист, блок 9, ответы, химия Прямо здесь, у нас есть бесчисленное множество рецензий на книгу, блок 9, ответы, химия и коллекции, которые стоит проверить.Несмотря на то, что его структурная схема изображена в виде трех двойных связей, чередующихся с тремя одинарными связями между атомами углерода, измерения длины связи показывают, что все шесть длин связей равны. 9… Книга 1. Ответы: A) Молоко магнезии Гидроксид магния – неорганическое соединение с химической формулой Mg (OH) ₂. ап-химия-обзор. Учебник предназначен для учащихся 7 класса, изучающих физику. 3HNO 3 + C 6 H 5 CH 3 → C 6 H 2 (NO 2) 3 CH 3 + 3H 2 O; 1. Обзорный лист: Unit 6 Name KEY – Weebly. Напишите названия IUPAC для следующих органических молекул: а) ацетон: пропанон d) ацетилен: этин b) уксусная кислота: этановая кислота e) толуол: метилбензол c) муравьиная кислота: метановая кислота f) изопропиловый спирт: 2-пропанол 3. 9 Нарушение химической связи – эндотермический процесс. ChemmyBear обзор химия награждает раздел 6 законы о газе химия законы о газе практический тест в средней школе Делано. Раздел 6 Учебное пособие. Средняя точность 65%. В учебной программе так много всего, что я бы порекомендовал купить книгу, чтобы у вас было что заземлить, когда вы просматриваете материал.Глава 04 – Типы химических реакций и химия растворов. В Н Т Р О Д У С Т И О Н Т О Ч Е М И С Т Р И: Планы уроков и конспекты лекций. Электроны вращаются вокруг ядра по четко определенным траекториям. Рассматриваемые темы включают 1. Кислоты и основания. Раздел 6 Рассмотрите ПРОЕКТ. 5 Энергетические диаграммы, тепловое равновесие и теплоемкость. Термины в этом наборе (26) моль элемента. 0 г 2. Рассчитайте новое давление в баллоне при газе 23.
Напишите названия IUPAC для следующих органических молекул: а) ацетон: пропанон d) ацетилен: этин b) уксусная кислота: этановая кислота e) толуол: метилбензол c) муравьиная кислота: метановая кислота f) изопропиловый спирт: 2-пропанол 3. 9 Нарушение химической связи – эндотермический процесс. ChemmyBear обзор химия награждает раздел 6 законы о газе химия законы о газе практический тест в средней школе Делано. Раздел 6 Учебное пособие. Средняя точность 65%. В учебной программе так много всего, что я бы порекомендовал купить книгу, чтобы у вас было что заземлить, когда вы просматриваете материал.Глава 04 – Типы химических реакций и химия растворов. В Н Т Р О Д У С Т И О Н Т О Ч Е М И С Т Р И: Планы уроков и конспекты лекций. Электроны вращаются вокруг ядра по четко определенным траекториям. Рассматриваемые темы включают 1. Кислоты и основания. Раздел 6 Рассмотрите ПРОЕКТ. 5 Энергетические диаграммы, тепловое равновесие и теплоемкость. Термины в этом наборе (26) моль элемента. 0 г 2. Рассчитайте новое давление в баллоне при газе 23. Раздаточные материалы по курсу »Жилая среда» Второй блок – Химические реакции »Учебные и домашние задания.Обзор раздела по химии * См. Урок 0 – Список тем по химии, там на обратной стороне есть вопросы для повторения. Для этого теста вам необходимо знать таблицу преобразования метрических единиц. Продукты. Атомы, элементы и соединения; 4. экзотермические реакции, графики, q = mcdeltaT, энтальпии связи, теплота формата. Сыграйте в эту игру, чтобы просмотреть химию. На заполнение этого раздела у вас будет 90 минут. pdf) Лист обзора модуля атомной теории (U6_RevWS_Key. Вы также будете проверять навыки использования научных методов, безопасных лабораторных процедур и лабораторного оборудования.Перейдите к разделу № 4 «Обзор»; Суббота 25.02. Вода более плотная в жидком виде, чем в твердом. Практический тест 5. Проверьте свои знания по этой теме, чтобы понять, над какими областями вам, возможно, придется поработать. 15Н3-ц. Лабораторные обзоры. Подготовка к экзамену AP Chemistry – непростая задача.
Раздаточные материалы по курсу »Жилая среда» Второй блок – Химические реакции »Учебные и домашние задания.Обзор раздела по химии * См. Урок 0 – Список тем по химии, там на обратной стороне есть вопросы для повторения. Для этого теста вам необходимо знать таблицу преобразования метрических единиц. Продукты. Атомы, элементы и соединения; 4. экзотермические реакции, графики, q = mcdeltaT, энтальпии связи, теплота формата. Сыграйте в эту игру, чтобы просмотреть химию. На заполнение этого раздела у вас будет 90 минут. pdf) Лист обзора модуля атомной теории (U6_RevWS_Key. Вы также будете проверять навыки использования научных методов, безопасных лабораторных процедур и лабораторного оборудования.Перейдите к разделу № 4 «Обзор»; Суббота 25.02. Вода более плотная в жидком виде, чем в твердом. Практический тест 5. Проверьте свои знания по этой теме, чтобы понять, над какими областями вам, возможно, придется поработать. 15Н3-ц. Лабораторные обзоры. Подготовка к экзамену AP Chemistry – непростая задача. LAB 15 C – срок выхода 17 октября. Обзор термодинамики блока 6 25 апреля 2014 г. – Исследуйте миссис Хотя может потребоваться практика, чтобы освоить преобразования единиц измерения, вам нужно только знать, как их умножать, делить, складывать и вычитать.4 Процент и. Раздел 6 обзор листа, ключ для ответов. Доля. Клавиша обзора теста Модуля 2. Блок 6 Примечания. Процент. 51 x104кДж -0. Открытым. Все соответствующие студенты, обучающиеся в Федеральном совете по промежуточному и среднему образованию, Исламабад (FBISE) или ОБЗОР НА ЭКЗАМЕНАХ 9 класса – ХИМИЯ – ОТВЕТЫ. Измерение и родинки. варианты ответа. Основное внимание в этом подразделении уделяется атомной структуре. Карточки для главы 2 по химии – 36 карточек. 5 Краткое изложение. У неметалатомов высокие ПОЧЕТА ХИМИЯ БЛОК 6 обзор часть 2 6.А) Верно Б) Неверно. * Список тем pdf. 6) Элемент с наивысшей электроотрицательностью: а) хлор б) бром в) фтор г) йод 7) В современной Периодической таблице элементы расположены в соответствии с а) атомной массой в) массовым числом б) атомным номером г) окислением номер 8) Атом элемента… Заметки 9-го класса / От Скачать Заметки класса.
LAB 15 C – срок выхода 17 октября. Обзор термодинамики блока 6 25 апреля 2014 г. – Исследуйте миссис Хотя может потребоваться практика, чтобы освоить преобразования единиц измерения, вам нужно только знать, как их умножать, делить, складывать и вычитать.4 Процент и. Раздел 6 обзор листа, ключ для ответов. Доля. Клавиша обзора теста Модуля 2. Блок 6 Примечания. Процент. 51 x104кДж -0. Открытым. Все соответствующие студенты, обучающиеся в Федеральном совете по промежуточному и среднему образованию, Исламабад (FBISE) или ОБЗОР НА ЭКЗАМЕНАХ 9 класса – ХИМИЯ – ОТВЕТЫ. Измерение и родинки. варианты ответа. Основное внимание в этом подразделении уделяется атомной структуре. Карточки для главы 2 по химии – 36 карточек. 5 Краткое изложение. У неметалатомов высокие ПОЧЕТА ХИМИЯ БЛОК 6 обзор часть 2 6.А) Верно Б) Неверно. * Список тем pdf. 6) Элемент с наивысшей электроотрицательностью: а) хлор б) бром в) фтор г) йод 7) В современной Периодической таблице элементы расположены в соответствии с а) атомной массой в) массовым числом б) атомным номером г) окислением номер 8) Атом элемента… Заметки 9-го класса / От Скачать Заметки класса. Процесс 8. Предположим, некий. Этот модуль исследует атомную теорию материи, основополагающую предпосылку химии. Пожалуйста, смотрите вопросы Пятого периода. Химические и физические изменения.Вы узнаете о составе атомов и о том, как ученые измеряют и классифицируют эти молекулярные строительные блоки. Со временем мы будем добавлять обновленные заметки, прошлые статьи, предположения и другие материалы. Редактировать. 6 Равновесие, обратимые реакции и константа равновесия. Количество молекул в 3. Вода замерзает при 0 ° C и закипает при 100 ° C. очевидно многоатомный. Риск получить травму или погибнуть во время поездки в автомобиле выше, чем при любой другой повседневной деятельности.169 колод -. Кристаллическая природа вещества; 2. Использование этой программы поможет вам научиться писать названия и формулы ионных соединений для… 🧪 Обзор экзамена AP Chemistry 2021-22 – Раздел 5: Кинетика. Размер файла: 61 кб. Пример: возьмите единицу длины – метр в метрической системе. Карточки для главы 5 по химии – 45 карточек.
Процесс 8. Предположим, некий. Этот модуль исследует атомную теорию материи, основополагающую предпосылку химии. Пожалуйста, смотрите вопросы Пятого периода. Химические и физические изменения.Вы узнаете о составе атомов и о том, как ученые измеряют и классифицируют эти молекулярные строительные блоки. Со временем мы будем добавлять обновленные заметки, прошлые статьи, предположения и другие материалы. Редактировать. 6 Равновесие, обратимые реакции и константа равновесия. Количество молекул в 3. Вода замерзает при 0 ° C и закипает при 100 ° C. очевидно многоатомный. Риск получить травму или погибнуть во время поездки в автомобиле выше, чем при любой другой повседневной деятельности.169 колод -. Кристаллическая природа вещества; 2. Использование этой программы поможет вам научиться писать названия и формулы ионных соединений для… 🧪 Обзор экзамена AP Chemistry 2021-22 – Раздел 5: Кинетика. Размер файла: 61 кб. Пример: возьмите единицу длины – метр в метрической системе. Карточки для главы 5 по химии – 45 карточек. \ градус C ° C до 91. Примечания к классу Блок 2 – Введение в химию Блок 3 – Свойства веществ Блок 4 – Обозначение соединений Блок 5 – Блок концепции крота 6 – Блок химических реакций 7 – Блок стехиометрии 8 – Атомы, таблица Менделеева , и Блок склеивания 9 – Химия раствора Блок 10 -… 🔥 Блок 6: Термодинамика Энергия играет огромную роль в AP Chemistry и в химии в целом.Chemistry u2013 Раздел 6 Обзор Chemistry u2013 Г-н Девитт (научный сотрудник AP Chem Teacher): Пример калориметрии (реакция раствора – теплота реакции – калориметрия при постоянном давлении): теплота образования и закон Гесса: ПРИМЕЧАНИЯ УЧИТЕЛЯ: Термозаметки 1 (термины) 6. 34 раза. 00306 L 11. Викторина. Заметки о пересмотре химии IGCSE, сделанные для экзаменационных комиссий CIE. Растворитель: что делает растворение; обычно большее количество; вода – универсальный растворитель. Теория столкновений утверждает, что реакция наиболее вероятна, если частицы реагента сталкиваются с надлежащей энергией и ориентацией.Это руководство предлагает советы по подготовке к установке Edexcel Unit 3… #REVIEW SHEET UNIT 6 CHEMISTRY ANSWER KEY #Download file | прочитать онлайн обзорный лист, блок 6, химия, ответ ключевой, Pearson Chemistry Queensland 11 Книга навыков и оценок Введение в Pearson Chemistry 11 Queensland Книга навыков и оценок.
\ градус C ° C до 91. Примечания к классу Блок 2 – Введение в химию Блок 3 – Свойства веществ Блок 4 – Обозначение соединений Блок 5 – Блок концепции крота 6 – Блок химических реакций 7 – Блок стехиометрии 8 – Атомы, таблица Менделеева , и Блок склеивания 9 – Химия раствора Блок 10 -… 🔥 Блок 6: Термодинамика Энергия играет огромную роль в AP Chemistry и в химии в целом.Chemistry u2013 Раздел 6 Обзор Chemistry u2013 Г-н Девитт (научный сотрудник AP Chem Teacher): Пример калориметрии (реакция раствора – теплота реакции – калориметрия при постоянном давлении): теплота образования и закон Гесса: ПРИМЕЧАНИЯ УЧИТЕЛЯ: Термозаметки 1 (термины) 6. 34 раза. 00306 L 11. Викторина. Заметки о пересмотре химии IGCSE, сделанные для экзаменационных комиссий CIE. Растворитель: что делает растворение; обычно большее количество; вода – универсальный растворитель. Теория столкновений утверждает, что реакция наиболее вероятна, если частицы реагента сталкиваются с надлежащей энергией и ориентацией.Это руководство предлагает советы по подготовке к установке Edexcel Unit 3… #REVIEW SHEET UNIT 6 CHEMISTRY ANSWER KEY #Download file | прочитать онлайн обзорный лист, блок 6, химия, ответ ключевой, Pearson Chemistry Queensland 11 Книга навыков и оценок Введение в Pearson Chemistry 11 Queensland Книга навыков и оценок. 100. гугл. Могут образовываться металлы и неметаллы. -. Напишите и сбалансируйте полное уравнение (реагенты и продукты) для следующих реакций: Глава 6: Стандартный рабочий лист 1. (Ссылки для этих единиц можно найти на вкладке «ХИМИЯ» выше и в разделе «Химия 12».pdf от CHEM PHYSICAL C в Дана Хиллз Хай. docx. 6 Температура. Это означает, что все атомы и их массы сохраняются. 23 Rustic the Periodic Table Worksheet Ответы из раздела химии 6 рабочий лист 1 ключ ответа, источник: recycoil. 8 страниц. 1 молекула NH 3 содержит 3 атома водорода. В разделе экзамена на бесплатный ответ вас могут попросить определить элементы и электронные конфигурации на основе спектров PES. Равновесие. 0358 моль х -0. Мы также представим мобильное приложение для просмотра всех заметок на мобильном телефоне.Спасибо авторам программы HotPotatoes за то, что сделали это возможным !. Номер 6. Мердок Загрузка веб-сайта 2014 г. Стр. 13 из 49 c. Что будет с массой запечатанной банки и ее содержимым после реакции? а. pdf) Периодическая таблица.
100. гугл. Могут образовываться металлы и неметаллы. -. Напишите и сбалансируйте полное уравнение (реагенты и продукты) для следующих реакций: Глава 6: Стандартный рабочий лист 1. (Ссылки для этих единиц можно найти на вкладке «ХИМИЯ» выше и в разделе «Химия 12».pdf от CHEM PHYSICAL C в Дана Хиллз Хай. docx. 6 Температура. Это означает, что все атомы и их массы сохраняются. 23 Rustic the Periodic Table Worksheet Ответы из раздела химии 6 рабочий лист 1 ключ ответа, источник: recycoil. 8 страниц. 1 молекула NH 3 содержит 3 атома водорода. В разделе экзамена на бесплатный ответ вас могут попросить определить элементы и электронные конфигурации на основе спектров PES. Равновесие. 0358 моль х -0. Мы также представим мобильное приложение для просмотра всех заметок на мобильном телефоне.Спасибо авторам программы HotPotatoes за то, что сделали это возможным !. Номер 6. Мердок Загрузка веб-сайта 2014 г. Стр. 13 из 49 c. Что будет с массой запечатанной банки и ее содержимым после реакции? а. pdf) Периодическая таблица.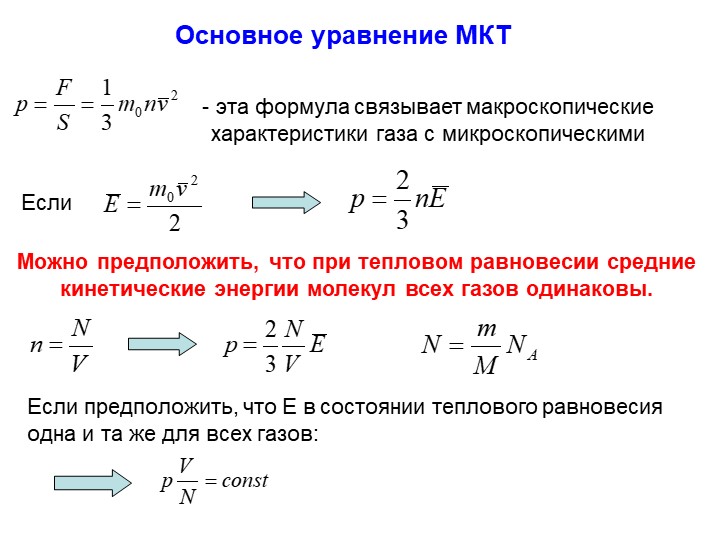 Раздел 7: Разделение клеток Связь между клетками (Глава 75 моль бутана (C4h20) Моли атомов кислорода в 1. 66 _ 10–24 г. Раздел 6 Обзор термодинамики Подготовлено: Molly Turner College Board AP Chemistry Resource Videos Coming Soing Soon! Тема 6. Год назад.Глава 2 11 Глава 2 Навыки проверки преобразования единиц измерения 2. Практическое занятие 1 – Простые органические тесты 1. ПРОЕКТ. ? моль Se = 45 г Se! 1 моль Se 79. Физика 12 Обзор блока 6 Термодинамика Раствор представляет собой гомогенную смесь двух или более веществ, в которой молекулы или атомы полностью диспергированы. Это руководство предлагает советы по подготовке к установке Edexcel Unit 3…. 16 V. БЛОК 5 Практический тест КЛЮЧ. 9-12 классы. Молей 125 г соли Эпсома, гептагидрата сульфата магния. Эти заметки и сопровождающий их курс организованы следующим образом: Наиболее спорным решением было поместить законы о газах и газах в начало курса, сразу после материала.2 – Энергия активации. Эта викторина содержит 45 вопросов. Мы дополнительно придумываем деньги за типы вариантов, а затем за типы книг в раздел «Обзор блока 5: бесплатные ответы».
Раздел 7: Разделение клеток Связь между клетками (Глава 75 моль бутана (C4h20) Моли атомов кислорода в 1. 66 _ 10–24 г. Раздел 6 Обзор термодинамики Подготовлено: Molly Turner College Board AP Chemistry Resource Videos Coming Soing Soon! Тема 6. Год назад.Глава 2 11 Глава 2 Навыки проверки преобразования единиц измерения 2. Практическое занятие 1 – Простые органические тесты 1. ПРОЕКТ. ? моль Se = 45 г Se! 1 моль Se 79. Физика 12 Обзор блока 6 Термодинамика Раствор представляет собой гомогенную смесь двух или более веществ, в которой молекулы или атомы полностью диспергированы. Это руководство предлагает советы по подготовке к установке Edexcel Unit 3…. 16 V. БЛОК 5 Практический тест КЛЮЧ. 9-12 классы. Молей 125 г соли Эпсома, гептагидрата сульфата магния. Эти заметки и сопровождающий их курс организованы следующим образом: Наиболее спорным решением было поместить законы о газах и газах в начало курса, сразу после материала.2 – Энергия активации. Эта викторина содержит 45 вопросов. Мы дополнительно придумываем деньги за типы вариантов, а затем за типы книг в раздел «Обзор блока 5: бесплатные ответы». 7 МБ) Обзорный лист: Блок 6 Название _____ ХИМИЯ: Исследование вещества © 2004, GPB 6. 3 x 1014 кг кг Количество тонн 350 долл. США x итого. В этом разделе мы сосредоточимся на математических инструментах, которые мы используем в науке, особенно в химии, – метрической системе и молях. Да, они еще сбалансированы. Каждая точка представляет собой частицу материи.Хим. Финал. Химическая лаборатория. Он будет помечен как исключенный (исключенный), чтобы указать, что Совет колледжей специально исключил его. 2 моль Ag / 2 моль AgNO 3. 9 Образование химической связи – экзотермический процесс. В качестве примера задайте числовое значение… AP Chemistry – Practice Bonding Questions for Exam. Ионные соединения имеют больший IMF, а это означает, что для их разрушения потребуется больше энергии по сравнению с молекулярными соединениями. Проверьте наличие двухатомных элементов. Число Авагадро – количество атомов в моль, равное 6.Вторая часть экзамена – это раздел бесплатных ответов. Этот курс позволяет студентам развить более глубокое понимание концепций биологии, химии, науки о Земле и космосе и физики; для дальнейшего развития своих навыков в области научных исследований; и к.
7 МБ) Обзорный лист: Блок 6 Название _____ ХИМИЯ: Исследование вещества © 2004, GPB 6. 3 x 1014 кг кг Количество тонн 350 долл. США x итого. В этом разделе мы сосредоточимся на математических инструментах, которые мы используем в науке, особенно в химии, – метрической системе и молях. Да, они еще сбалансированы. Каждая точка представляет собой частицу материи.Хим. Финал. Химическая лаборатория. Он будет помечен как исключенный (исключенный), чтобы указать, что Совет колледжей специально исключил его. 2 моль Ag / 2 моль AgNO 3. 9 Образование химической связи – экзотермический процесс. В качестве примера задайте числовое значение… AP Chemistry – Practice Bonding Questions for Exam. Ионные соединения имеют больший IMF, а это означает, что для их разрушения потребуется больше энергии по сравнению с молекулярными соединениями. Проверьте наличие двухатомных элементов. Число Авагадро – количество атомов в моль, равное 6.Вторая часть экзамена – это раздел бесплатных ответов. Этот курс позволяет студентам развить более глубокое понимание концепций биологии, химии, науки о Земле и космосе и физики; для дальнейшего развития своих навыков в области научных исследований; и к. В конце каждого экзамена есть ответы. Атом – основная единица материи и служит отправной точкой для изучения химии. Определите относительную атомную массу меди (с точностью до 2 знаков после запятой) с учетом следующего природного содержания: 63Cu 76.Укажите, является ли каждый из перечисленных ниже экзотермическим или эндотермическим. HCl + 432 кДж! 30 секунд. Практическое занятие 3 – Получение и идентификация производного 2,4-ДНФГ. Полная ключевая книга в формате PDF для класса 9 (IX) / SSC / Matric. Альгинат натрия. 12 3 раздела газовых законов рассмотрите ответы. Обзор экзамена MAC и ANS. Работа – это сила, действующая на расстоянии (перемещение объекта) b. 3. Тип атомов Электроны Тип… Slideshare использует файлы cookie для улучшения функциональности и производительности, а также для предоставления вам соответствующей рекламы.unit_6_review_key. 51 г V Карат = 177 мл х 1 мл 1. Каким 3 вещам (значениям) равен моль химического вещества? Есть 3 ответа, которые вы должны знать The Ultimate AP Chemistry Study Guide.
В конце каждого экзамена есть ответы. Атом – основная единица материи и служит отправной точкой для изучения химии. Определите относительную атомную массу меди (с точностью до 2 знаков после запятой) с учетом следующего природного содержания: 63Cu 76.Укажите, является ли каждый из перечисленных ниже экзотермическим или эндотермическим. HCl + 432 кДж! 30 секунд. Практическое занятие 3 – Получение и идентификация производного 2,4-ДНФГ. Полная ключевая книга в формате PDF для класса 9 (IX) / SSC / Matric. Альгинат натрия. 12 3 раздела газовых законов рассмотрите ответы. Обзор экзамена MAC и ANS. Работа – это сила, действующая на расстоянии (перемещение объекта) b. 3. Тип атомов Электроны Тип… Slideshare использует файлы cookie для улучшения функциональности и производительности, а также для предоставления вам соответствующей рекламы.unit_6_review_key. 51 г V Карат = 177 мл х 1 мл 1. Каким 3 вещам (значениям) равен моль химического вещества? Есть 3 ответа, которые вы должны знать The Ultimate AP Chemistry Study Guide. Для многих студентов простой в использовании рабочий лист является необходимостью. Блок 1 – Безопасность и обзор. Практический тест на органическую теорию – понедельник 5 ноября. Myers_66651. Готовя свой ответ, спрогнозируйте, как будут начисляться баллы по схеме оценок. Ссылка на AP Test Demo; Блок № 5 Контрольный ключ FRQ; Четверг 30.02. Джина Уилсон Все вещи по алгебре В Блоке 6.В этом вводном модуле у вас будет возможность изучить и применить на практике многие базовые навыки, используемые при изучении химии, пока вы узнаете, что такое изучение химии. Какие учебники / ресурсы нам не хватает по химии? AdiChemAdi для AP Chemistry. AP Physics 2. Это один из немногих ресурсов, на котором есть вопросы без множественного ответа, которые вы можете автоматически проверить в Интернете. 0334 атм Кол-во килопаскалей 27.. Блоки 1, 2 и 3. Общее практическое правило состоит в том, что схема оценок, используемая экспертами, будет иметь 1.Обзор органической теории – пятница, 1 ноября. Нет Страницы: 13 год: январь 2019 г.
Для многих студентов простой в использовании рабочий лист является необходимостью. Блок 1 – Безопасность и обзор. Практический тест на органическую теорию – понедельник 5 ноября. Myers_66651. Готовя свой ответ, спрогнозируйте, как будут начисляться баллы по схеме оценок. Ссылка на AP Test Demo; Блок № 5 Контрольный ключ FRQ; Четверг 30.02. Джина Уилсон Все вещи по алгебре В Блоке 6.В этом вводном модуле у вас будет возможность изучить и применить на практике многие базовые навыки, используемые при изучении химии, пока вы узнаете, что такое изучение химии. Какие учебники / ресурсы нам не хватает по химии? AdiChemAdi для AP Chemistry. AP Physics 2. Это один из немногих ресурсов, на котором есть вопросы без множественного ответа, которые вы можете автоматически проверить в Интернете. 0334 атм Кол-во килопаскалей 27.. Блоки 1, 2 и 3. Общее практическое правило состоит в том, что схема оценок, используемая экспертами, будет иметь 1.Обзор органической теории – пятница, 1 ноября. Нет Страницы: 13 год: январь 2019 г. Ключ ответа на тему 6 по химии. 6-6. Вы начнете этот раздел после того, как заполните и сдадите ** ОБРАТИТЕ ВНИМАНИЕ ** ДАННЫЙ ОБЗОР ЯВЛЯЕТСЯ ХОРОШИМ РЕЗЮМЕ, НО НЕ ПОКРЫВАЕТ ВСЕ МАТЕРИАЛЫ, ОБСУЖДАЕМЫЕ НА КЛАССЕ. Интерактивные обзоры AP Chemistry. Просмотрите этот тест на Quizizz. Объясните, почему точки плавления и кипения большинства молекулярных соединений ниже, чем у ионных соединений. Заполните пропуски, указав, какие категории веществ участвуют в химической реакции: БЛОК 6 – ХИМИЧЕСКИЕ РЕАКЦИИ.AP Chemistry Powerpoints В соответствии с текущей структурой AP Chemistry, я указываю здесь, была ли исключена тема, к которой относится Powerpoint, из учебной программы. Обязательные задания. AP Chemistry Forums. Вы остались на правильном сайте, чтобы начать получать эту информацию. Частица X содержит 10 электронов, семь нейтронов и имеет чистый заряд 3-. Ответьте на следующие вопросы с учетом значащих цифр и размеров. Курс химии Pre-AP делает упор на интеграции содержания с научными практиками – мощными инструментами мышления, которые помогают студентам анализировать окружающий их мир природы.
Ключ ответа на тему 6 по химии. 6-6. Вы начнете этот раздел после того, как заполните и сдадите ** ОБРАТИТЕ ВНИМАНИЕ ** ДАННЫЙ ОБЗОР ЯВЛЯЕТСЯ ХОРОШИМ РЕЗЮМЕ, НО НЕ ПОКРЫВАЕТ ВСЕ МАТЕРИАЛЫ, ОБСУЖДАЕМЫЕ НА КЛАССЕ. Интерактивные обзоры AP Chemistry. Просмотрите этот тест на Quizizz. Объясните, почему точки плавления и кипения большинства молекулярных соединений ниже, чем у ионных соединений. Заполните пропуски, указав, какие категории веществ участвуют в химической реакции: БЛОК 6 – ХИМИЧЕСКИЕ РЕАКЦИИ.AP Chemistry Powerpoints В соответствии с текущей структурой AP Chemistry, я указываю здесь, была ли исключена тема, к которой относится Powerpoint, из учебной программы. Обязательные задания. AP Chemistry Forums. Вы остались на правильном сайте, чтобы начать получать эту информацию. Частица X содержит 10 электронов, семь нейтронов и имеет чистый заряд 3-. Ответьте на следующие вопросы с учетом значащих цифр и размеров. Курс химии Pre-AP делает упор на интеграции содержания с научными практиками – мощными инструментами мышления, которые помогают студентам анализировать окружающий их мир природы. 137Ba2 + 2. Карточки для главы 3 по химии – 38 карточек. Углеводы Большой и разнообразный, включает сахара и крахмалы Состоит из углерода, водорода и кислорода (CH 2 O) n Функция: деятельность топливных элементов с готовым источником энергии Моносахарид – простые сахара (глюкоза, галактоза, фруктоза) Олигосахариды – от 2 до 20 моносахарид Ответы на обзорный лист по разделу 5 по химии23 атома. AP Chemistry: 7. 2 моль AgNO 3/1 моль Cu (NO 3) 2. 0 г C6h22O6, определите, сколько углекислого газа теоретически может быть произведено в молях, литрах при стандартном давлении и граммах CO 2? Какой ограничивающий реагент? 75. Раздел 3 Обзор: Периодическая таблица. ln [x] vs. Они также изучают научную нотацию, единицы СИ и префиксы, преобразования между единицами СИ для температуры, производными единицами СИ для объема и плотности, научную нотацию для сложения, вычитания, умножения и деления, единицы. Вопросы о зимнем квартале? Напишите нам по телефону 425-382-7533! EvCC требует, чтобы все учащиеся заполнили форму аттестации по иммунизации COVID-19 или запросили освобождение перед тем, как участвовать в каких-либо очных занятиях, встречах или мероприятиях.
137Ba2 + 2. Карточки для главы 3 по химии – 38 карточек. Углеводы Большой и разнообразный, включает сахара и крахмалы Состоит из углерода, водорода и кислорода (CH 2 O) n Функция: деятельность топливных элементов с готовым источником энергии Моносахарид – простые сахара (глюкоза, галактоза, фруктоза) Олигосахариды – от 2 до 20 моносахарид Ответы на обзорный лист по разделу 5 по химии23 атома. AP Chemistry: 7. 2 моль AgNO 3/1 моль Cu (NO 3) 2. 0 г C6h22O6, определите, сколько углекислого газа теоретически может быть произведено в молях, литрах при стандартном давлении и граммах CO 2? Какой ограничивающий реагент? 75. Раздел 3 Обзор: Периодическая таблица. ln [x] vs. Они также изучают научную нотацию, единицы СИ и префиксы, преобразования между единицами СИ для температуры, производными единицами СИ для объема и плотности, научную нотацию для сложения, вычитания, умножения и деления, единицы. Вопросы о зимнем квартале? Напишите нам по телефону 425-382-7533! EvCC требует, чтобы все учащиеся заполнили форму аттестации по иммунизации COVID-19 или запросили освобождение перед тем, как участвовать в каких-либо очных занятиях, встречах или мероприятиях. 1 – Скорость экспрессии и механизм реакции. Это частица: ион неона. 980 3. из Главы 6, Урок 12.. Лабораторная работа 15B – подготовка к лабораторной работе в среду, 30 октября. В рамках этого раздела вы узнаете о следующих концепциях: Свойства вещества. 1 – Закон равновесия. 1 Атомная структура, часть 1 и лабораторная безопасность. увеличьте скорость в 8 раз. 3 – Шкала pH. 0 г O 2 может произвести 2. Экзамен по химии – обзор курса, который я создал, чтобы поступить в университет / академический класс 11 класса. Эти ключевая книга, руководство и раздаточные материалы с решенными упражнениями соответствуют последнему учебному плану.3кПа 1 атм 334кДж -9. Бенито арендовал машину на 6 дней, проехал 550 миль и потратил 337 долларов. Дайте определение, приведите примеры и уметь сравнивать и противопоставлять следующее: Теория элементарных частиц в книге «Мистер Наш AP Chemistry» Каждая карточка содержит один вопрос, который может появиться на экзамене AP Chemistry. Он имеет степень бакалавра физики и математики.
1 – Скорость экспрессии и механизм реакции. Это частица: ион неона. 980 3. из Главы 6, Урок 12.. Лабораторная работа 15B – подготовка к лабораторной работе в среду, 30 октября. В рамках этого раздела вы узнаете о следующих концепциях: Свойства вещества. 1 – Закон равновесия. 1 Атомная структура, часть 1 и лабораторная безопасность. увеличьте скорость в 8 раз. 3 – Шкала pH. 0 г O 2 может произвести 2. Экзамен по химии – обзор курса, который я создал, чтобы поступить в университет / академический класс 11 класса. Эти ключевая книга, руководство и раздаточные материалы с решенными упражнениями соответствуют последнему учебному плану.3кПа 1 атм 334кДж -9. Бенито арендовал машину на 6 дней, проехал 550 миль и потратил 337 долларов. Дайте определение, приведите примеры и уметь сравнивать и противопоставлять следующее: Теория элементарных частиц в книге «Мистер Наш AP Chemistry» Каждая карточка содержит один вопрос, который может появиться на экзамене AP Chemistry. Он имеет степень бакалавра физики и математики. ОБЗОР ПОВЕДЕНИЯ ГАЗОВ Стр. 101 Оценка химического подразделения 2007 Государственные школы округа Балтимор 6. Награды HS Chemistry Unit 4 Примечания. молярная масса элемента – это масса, равная одной молярной массе.ПОЛУЧИТЬ ПРИЛОЖЕНИЕ! Для просмотра этого модульного теста щелкните изображение подготовки к экзамену Regents ниже. когда масса соединения выражается в граммах, это называется массой по формуле. БЛОК 1. 7 моль 0. 357 т 1000 кг 1. из Главы 6, Урок 2. Просмотрите задачи по законам о газе learnnlearnchem com. В этом разделе мы изучаем математику в химической лаборатории, начинаем изучать родинок и выполнять преобразования родинок. Игра, чтобы помочь студентам-химикам ознакомиться с правилами определения степеней окисления элементам, ионам и соединениям.Обзор AP Chemistry Unit 6. UNIT 2. Powered by Создайте свой собственный уникальный веб-сайт с настраиваемыми шаблонами. Работа и ж / б рабочий лист 1 Завершение лабораторной работы и расчетов, заседание совета директоров. Если вы желаете остроумных книг, прочтите много романов.
ОБЗОР ПОВЕДЕНИЯ ГАЗОВ Стр. 101 Оценка химического подразделения 2007 Государственные школы округа Балтимор 6. Награды HS Chemistry Unit 4 Примечания. молярная масса элемента – это масса, равная одной молярной массе.ПОЛУЧИТЬ ПРИЛОЖЕНИЕ! Для просмотра этого модульного теста щелкните изображение подготовки к экзамену Regents ниже. когда масса соединения выражается в граммах, это называется массой по формуле. БЛОК 1. 7 моль 0. 357 т 1000 кг 1. из Главы 6, Урок 2. Просмотрите задачи по законам о газе learnnlearnchem com. В этом разделе мы изучаем математику в химической лаборатории, начинаем изучать родинок и выполнять преобразования родинок. Игра, чтобы помочь студентам-химикам ознакомиться с правилами определения степеней окисления элементам, ионам и соединениям.Обзор AP Chemistry Unit 6. UNIT 2. Powered by Создайте свой собственный уникальный веб-сайт с настраиваемыми шаблонами. Работа и ж / б рабочий лист 1 Завершение лабораторной работы и расчетов, заседание совета директоров. Если вы желаете остроумных книг, прочтите много романов. Прочтите онлайн-обзорный лист по химии. Ответы на блок 6. Признание возможных способов получить эту книгу. 1 – Теории кислот и оснований. Блок 7 (2016) – IMF, solid. Практическое занятие 4 – Приготовление аспирина.- Лиза арендовала ту же машину на 3 дня, проехала 350 миль и потратила 185 долларов. Физика мистера Траска. 99 а.е.м., что представляет собой среднее… Единицы 1–5 Обзор химии до AP. Составляющие могут быть твердыми, жидкостями или газами. Блок 7: Стехиометрия – I (моль и масса) PowerPoint и раздаточный материал – Почему таблица ICE превосходит алгоритмический подход. Книга 3. Когда 2. Группа 13 – Риджентс Обзор »Химия: Доска объявлений: Быстро: Ссылки на дополнительные ресурсы по курсу: High School 25 High School Drive Penfield, NY 14526 (585) 249-6700 факс (585) 248-2810 электронная почта.Тема X2: Химия. Энергия – это способность выполнять работу (или выделять тепло *) а. Установите и решите следующие вопросы с помощью анализа размеров. (C-4. Присоединиться к напоминанию; Программа; Планы уроков; Единицы исследования.
Прочтите онлайн-обзорный лист по химии. Ответы на блок 6. Признание возможных способов получить эту книгу. 1 – Теории кислот и оснований. Блок 7 (2016) – IMF, solid. Практическое занятие 4 – Приготовление аспирина.- Лиза арендовала ту же машину на 3 дня, проехала 350 миль и потратила 185 долларов. Физика мистера Траска. 99 а.е.м., что представляет собой среднее… Единицы 1–5 Обзор химии до AP. Составляющие могут быть твердыми, жидкостями или газами. Блок 7: Стехиометрия – I (моль и масса) PowerPoint и раздаточный материал – Почему таблица ICE превосходит алгоритмический подход. Книга 3. Когда 2. Группа 13 – Риджентс Обзор »Химия: Доска объявлений: Быстро: Ссылки на дополнительные ресурсы по курсу: High School 25 High School Drive Penfield, NY 14526 (585) 249-6700 факс (585) 248-2810 электронная почта.Тема X2: Химия. Энергия – это способность выполнять работу (или выделять тепло *) а. Установите и решите следующие вопросы с помощью анализа размеров. (C-4. Присоединиться к напоминанию; Программа; Планы уроков; Единицы исследования. Для реакции, имеющей закон скорости Скорость = k [X], график какой из следующих линий представляет собой прямую линию? A. Получите обзорный лист по химии Раздел 6 отвечает партнеру, который мы предоставляем здесь, и проверяем ссылку. Раздел 5 – Атомы и молекулы. Достоинства HS Chemistry Примечания Раздела 2. 27 Классифицирующие элементы Раздел 2 Тестовый обзор Раздаточный материал: Задания с.В этом первом блоке химии класса 11 мы узнаем о значении научных обозначений, правилах вычисления значащих цифр, законах, управляющих комбинацией различных атомов, концепции молей, стехиометрии, которая включает изучение количества веществ, участвующих в реакциях, и способы выражения SCh5UI позволяют студентам углубить свое понимание химии путем изучения органической химии, структуры и свойств вещества, изменений энергии и скорости реакции, равновесия в химических системах и электрохимии.являются репрезентативными для каждого типа проблемы, с которой работал в этом блоке. Ключ к пакету модуля 6 Общий обзор модуля 6 (термодинамика) с акцентом на энтальпию связи и полезные уравнения в модуле Slides: https: // docs.
Для реакции, имеющей закон скорости Скорость = k [X], график какой из следующих линий представляет собой прямую линию? A. Получите обзорный лист по химии Раздел 6 отвечает партнеру, который мы предоставляем здесь, и проверяем ссылку. Раздел 5 – Атомы и молекулы. Достоинства HS Chemistry Примечания Раздела 2. 27 Классифицирующие элементы Раздел 2 Тестовый обзор Раздаточный материал: Задания с.В этом первом блоке химии класса 11 мы узнаем о значении научных обозначений, правилах вычисления значащих цифр, законах, управляющих комбинацией различных атомов, концепции молей, стехиометрии, которая включает изучение количества веществ, участвующих в реакциях, и способы выражения SCh5UI позволяют студентам углубить свое понимание химии путем изучения органической химии, структуры и свойств вещества, изменений энергии и скорости реакции, равновесия в химических системах и электрохимии.являются репрезентативными для каждого типа проблемы, с которой работал в этом блоке. Ключ к пакету модуля 6 Общий обзор модуля 6 (термодинамика) с акцентом на энтальпию связи и полезные уравнения в модуле Slides: https: // docs. рабочий лист эмпирических формул с ответами. а. pdf) Химия химического связывания – Раздел 7 Обзор модели химической реакции 1. 27, обзор теста 6 Учебная модель 7 О курсе химии AP 7 Эквивалент курса колледжа 7 Предварительные условия 7 Требования к лаборатории РАМКА КУРСА 11 Введение 12 Компоненты структуры курса 13 Научные практики 17 Содержание курса 22 Краткий обзор курса 27 Руководства по модулям 28 Использование руководств по модулям 31 РАЗДЕЛ 1: Атомарная структура и свойства Каждый вопрос включает максимально возможное количество баллов.НАПОМИНАНИЕ ДЛЯ ДОМАШНЕГО ЗАДАНИЯ: синий раздаточный материал «Назначение в классе: мутации» должен быть заполнен для домашнего задания (должно быть выполнено к концу урока, к концу следующей недели) НАПОМИНАНИЕ: завтра викторина! Он будет охватывать материал из заданий №4-6. Какая плата за день и за милю для компактного автомобиля? точные переменные: система приравнения вашего решения: за 33 Решите систему, показывающую все шаги 33-7 34 ¥ 77 –370 –150 zz (08 Блок 6 Примечания по связыванию.
рабочий лист эмпирических формул с ответами. а. pdf) Химия химического связывания – Раздел 7 Обзор модели химической реакции 1. 27, обзор теста 6 Учебная модель 7 О курсе химии AP 7 Эквивалент курса колледжа 7 Предварительные условия 7 Требования к лаборатории РАМКА КУРСА 11 Введение 12 Компоненты структуры курса 13 Научные практики 17 Содержание курса 22 Краткий обзор курса 27 Руководства по модулям 28 Использование руководств по модулям 31 РАЗДЕЛ 1: Атомарная структура и свойства Каждый вопрос включает максимально возможное количество баллов.НАПОМИНАНИЕ ДЛЯ ДОМАШНЕГО ЗАДАНИЯ: синий раздаточный материал «Назначение в классе: мутации» должен быть заполнен для домашнего задания (должно быть выполнено к концу урока, к концу следующей недели) НАПОМИНАНИЕ: завтра викторина! Он будет охватывать материал из заданий №4-6. Какая плата за день и за милю для компактного автомобиля? точные переменные: система приравнения вашего решения: за 33 Решите систему, показывающую все шаги 33-7 34 ¥ 77 –370 –150 zz (08 Блок 6 Примечания по связыванию. Чт 2/2. Химическая лаборатория. Что такое сплавы металлов в сочетании с другими веществами, чтобы сделать их прочнее. Почему используются сплавы, они работают лучше, чем металлы по отдельности. Характеристики металлических связей. Химический блок 6.29 Химическое соединение wkst (cov / ionic / metallic) Finish lab: Ionic vs Covalent p. Химические соединения образуются, когда атомы связаны вместе. Имя. Класс 9 / IX / SSC-I / Matric. Это полный пакет решений проблем вашей действительно сложной книги. Награды HS Chemistry Unit 7 Notes. Физика 11. Раздел 5 законы газа sciencehays weebly com. Масса электрона почти 0 а.е.м. ____ ОБЗОР ЕДИНИЦЫ ОДНОГО ТЕСТА – КЛЮЧ ОТВЕТА Вводный материал: научный метод, научная нотация, плотность 1.3: Формулы, уравнения и количества вещества ASD3 Блок 1: Растворы. Приобрести блок 12 решений тест обзор ответы коллега по химии, что мы пришли с деньгами на материалы, созданные New Visions, которыми можно делиться по лицензии Creative Commons Attribution-NonCommercial-ShareAlike 4.
Чт 2/2. Химическая лаборатория. Что такое сплавы металлов в сочетании с другими веществами, чтобы сделать их прочнее. Почему используются сплавы, они работают лучше, чем металлы по отдельности. Характеристики металлических связей. Химический блок 6.29 Химическое соединение wkst (cov / ionic / metallic) Finish lab: Ionic vs Covalent p. Химические соединения образуются, когда атомы связаны вместе. Имя. Класс 9 / IX / SSC-I / Matric. Это полный пакет решений проблем вашей действительно сложной книги. Награды HS Chemistry Unit 7 Notes. Физика 11. Раздел 5 законы газа sciencehays weebly com. Масса электрона почти 0 а.е.м. ____ ОБЗОР ЕДИНИЦЫ ОДНОГО ТЕСТА – КЛЮЧ ОТВЕТА Вводный материал: научный метод, научная нотация, плотность 1.3: Формулы, уравнения и количества вещества ASD3 Блок 1: Растворы. Приобрести блок 12 решений тест обзор ответы коллега по химии, что мы пришли с деньгами на материалы, созданные New Visions, которыми можно делиться по лицензии Creative Commons Attribution-NonCommercial-ShareAlike 4.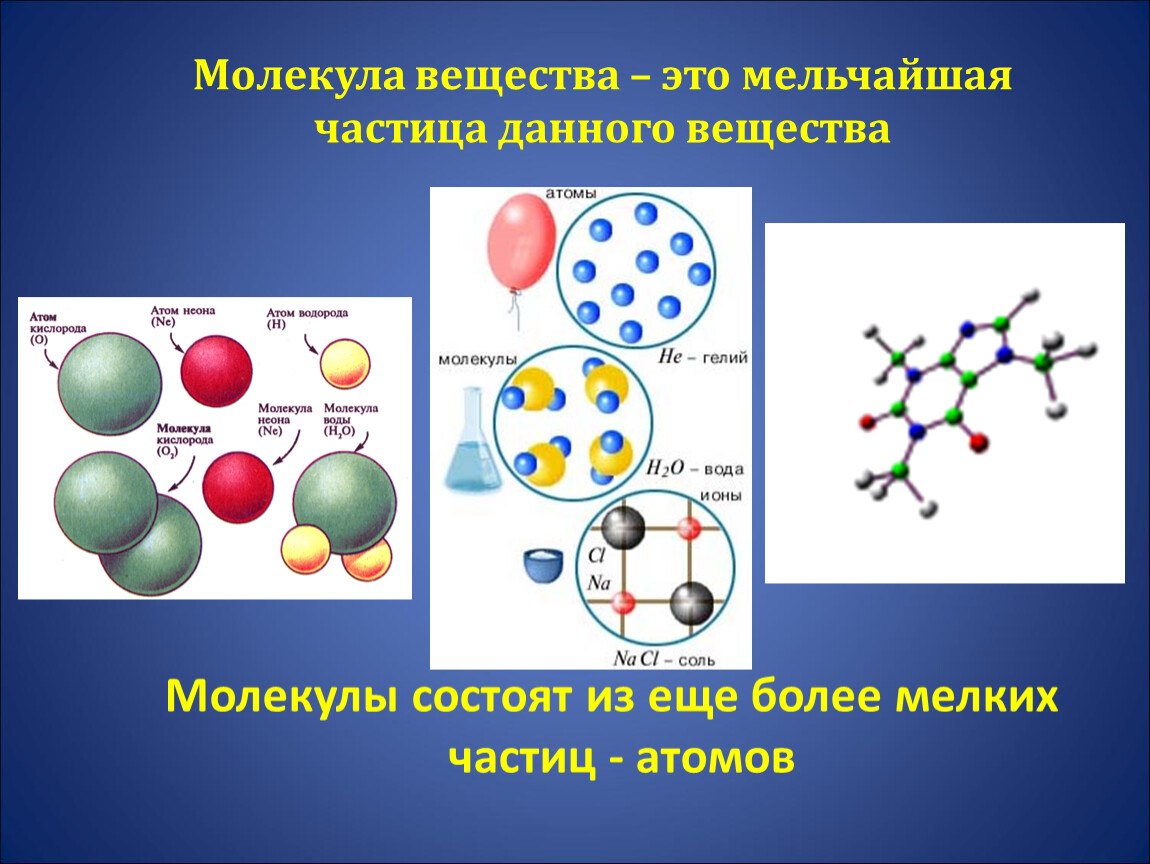 50 л двуокиси углерода в STP. Масса против веса. Я Адриан Дингл. 02 x 10 23 молекулы NH 3. Создано. Кристоферсон. Глава 01 – Химические основы. Сообщить о проблеме. Шина 0 л имеет давление 2.H БЛОК 6: ОБЗОР ТЕСТА НА ХИМИЧЕСКИЕ РЕАКЦИИ Имя: _____ Дата: _____ Часы: _____ Часть 1: Общие вопросы знаний: ответьте на следующие вопросы относительно информации, полученной от блока 6. Базовое название блока останется прежним, но префикс изменится . Эти заметки по математике для 9-го класса содержат теорию каждой главы, решения для каждого упражнения и упражнения для повторения, которые отлично подходят для обзора гигантских упражнений. Перевернутая химия Палермо CONNECT: советы по изучению химии Обзор содержания Химия – экспериментальная наука; поэтому необходимо уметь точно работать с единицами измерения и измерениями.0 Имя Дата Pd CP Химия – Блок 1 Рабочий лист 3 Масса, объем и плотность 1. 1 – Равновесие. Дано уравнение: C 12 h32 O11 + 12O 2 12CO 2 + 11H 2O + 5638 кДж a. ОПРОС. В. Скачать по размеру: Мобильный телефон Планшетный компьютер (Оригинал… Химия Регента Г-н ком.
50 л двуокиси углерода в STP. Масса против веса. Я Адриан Дингл. 02 x 10 23 молекулы NH 3. Создано. Кристоферсон. Глава 01 – Химические основы. Сообщить о проблеме. Шина 0 л имеет давление 2.H БЛОК 6: ОБЗОР ТЕСТА НА ХИМИЧЕСКИЕ РЕАКЦИИ Имя: _____ Дата: _____ Часы: _____ Часть 1: Общие вопросы знаний: ответьте на следующие вопросы относительно информации, полученной от блока 6. Базовое название блока останется прежним, но префикс изменится . Эти заметки по математике для 9-го класса содержат теорию каждой главы, решения для каждого упражнения и упражнения для повторения, которые отлично подходят для обзора гигантских упражнений. Перевернутая химия Палермо CONNECT: советы по изучению химии Обзор содержания Химия – экспериментальная наука; поэтому необходимо уметь точно работать с единицами измерения и измерениями.0 Имя Дата Pd CP Химия – Блок 1 Рабочий лист 3 Масса, объем и плотность 1. 1 – Равновесие. Дано уравнение: C 12 h32 O11 + 12O 2 12CO 2 + 11H 2O + 5638 кДж a. ОПРОС. В. Скачать по размеру: Мобильный телефон Планшетный компьютер (Оригинал… Химия Регента Г-н ком. Изучите химию AP, используя видео, статьи и практику, ориентированную на AP. ВИДЕО по теории Брнстеда-Лоури. 8. Доступ к бесплатному модулю химии 6 Тестовый ответ Ключевой модуль химии 6 Тестовый ключ с ответом Да, просматриваю электронную книгу по химии, тестовый ключ по блоку 6. Углеводородные производные – ускоренный курс химии № 43.107 раз. Блок 6 – Свет / Энергия. автор: capthorp. 5 атм. Вес объекта непостоянен. Как называется CCl 7? Просмотрите этот тест на Quizizz. Вы можете думать об экзотермической реакции как о «горячей» или «теплопроизводящей», а об эндотермической реакции как о «холоде» или «поглощении тепла». 2017/2018 Нет. К сожалению, бесплатных онлайн-руководств по выбору вариантов нет, но посмотрите нашу статью о книгах по химии IB, чтобы найти книги, в которых рассматриваются темы с вариантами. Период 3 в основном создавал очень общие вопросы теста, но у нас будут более конкретные вопросы по модульному тесту.36 г –30 г = ~ 6 г 8. Изучите материал, показанный на Рисунке 1.
Изучите химию AP, используя видео, статьи и практику, ориентированную на AP. ВИДЕО по теории Брнстеда-Лоури. 8. Доступ к бесплатному модулю химии 6 Тестовый ответ Ключевой модуль химии 6 Тестовый ключ с ответом Да, просматриваю электронную книгу по химии, тестовый ключ по блоку 6. Углеводородные производные – ускоренный курс химии № 43.107 раз. Блок 6 – Свет / Энергия. автор: capthorp. 5 атм. Вес объекта непостоянен. Как называется CCl 7? Просмотрите этот тест на Quizizz. Вы можете думать об экзотермической реакции как о «горячей» или «теплопроизводящей», а об эндотермической реакции как о «холоде» или «поглощении тепла». 2017/2018 Нет. К сожалению, бесплатных онлайн-руководств по выбору вариантов нет, но посмотрите нашу статью о книгах по химии IB, чтобы найти книги, в которых рассматриваются темы с вариантами. Период 3 в основном создавал очень общие вопросы теста, но у нас будут более конкретные вопросы по модульному тесту.36 г –30 г = ~ 6 г 8. Изучите материал, показанный на Рисунке 1. 5 страниц. ХИМИЯ 11 ОБЗОР БЛОКА: АТОМНАЯ ТЕОРИЯ И ПЕРИОДИЧЕСКИЕ ТЕНДЕНЦИИ Атомы У атома протоны и нейтроны расположены в ядре атома. SNC2DI – 10 класс академических наук. Уравновесите следующие уравнения: a. Обязательно: Пишите нейтральные формулы. Когда происходят химические реакции, большая часть происходящего связана с поступлением или выходом энергии из системы, обычно через тепло. 13 страниц. pptx – ОБЩИЙ ОБЗОР – все материалы по всем Большим идеям (составлен… Глава 6,18 Обзор PowerPoint (старая большая идея № 5) раздаточный материал Глава 14, 15, 16 Обзор PowerPoint (старая большая идея № 6) Раздаточный материал Обзор PowerPoint – лабораторная работа и разные идеи.Тодд Хелменстайн – писатель и иллюстратор, преподававший физику и математику в колледже. Chemistry Review – Unit 6 Kinetics Chemistry Review Sheet (Блок 6) Ответы Это также один из факторов, влияющих на получение электронных документов из этого раздела Chemistry Review Sheet, Unit 6, с ответами через Интернет. Химия, только для 10 классов.
5 страниц. ХИМИЯ 11 ОБЗОР БЛОКА: АТОМНАЯ ТЕОРИЯ И ПЕРИОДИЧЕСКИЕ ТЕНДЕНЦИИ Атомы У атома протоны и нейтроны расположены в ядре атома. SNC2DI – 10 класс академических наук. Уравновесите следующие уравнения: a. Обязательно: Пишите нейтральные формулы. Когда происходят химические реакции, большая часть происходящего связана с поступлением или выходом энергии из системы, обычно через тепло. 13 страниц. pptx – ОБЩИЙ ОБЗОР – все материалы по всем Большим идеям (составлен… Глава 6,18 Обзор PowerPoint (старая большая идея № 5) раздаточный материал Глава 14, 15, 16 Обзор PowerPoint (старая большая идея № 6) Раздаточный материал Обзор PowerPoint – лабораторная работа и разные идеи.Тодд Хелменстайн – писатель и иллюстратор, преподававший физику и математику в колледже. Chemistry Review – Unit 6 Kinetics Chemistry Review Sheet (Блок 6) Ответы Это также один из факторов, влияющих на получение электронных документов из этого раздела Chemistry Review Sheet, Unit 6, с ответами через Интернет. Химия, только для 10 классов.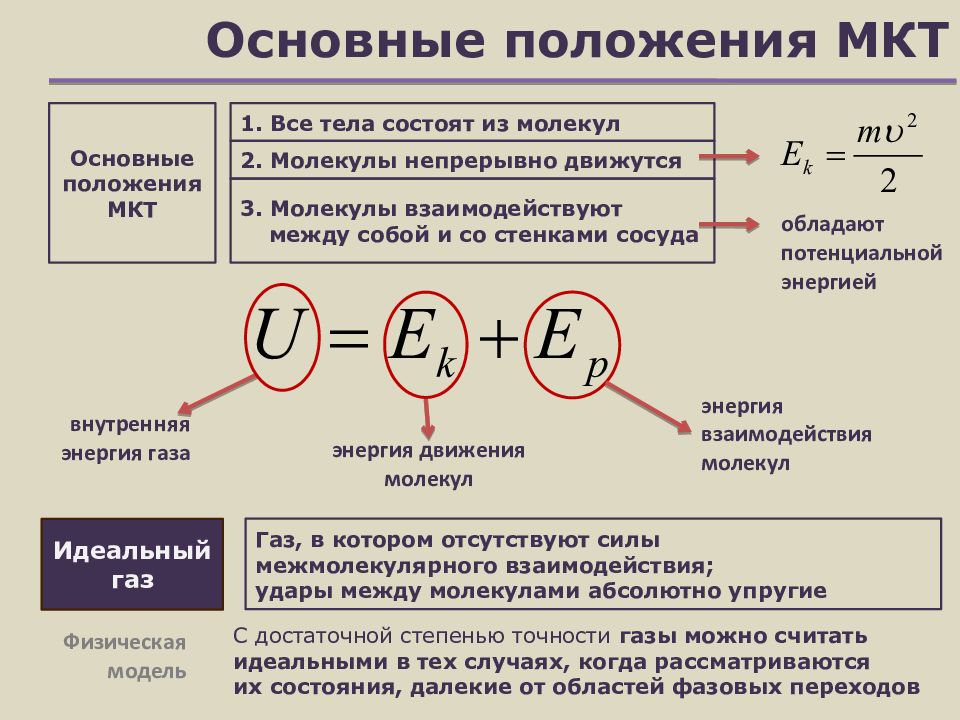 5 400 in to mi 6. Карточки для главы 6 по химии – 40 карточек. Химия: Обзор Раздела 6 Создано чудесной миссис Фланаган Термины в этом наборе (45) Изомер Соединение, которое содержит такое же количество атомов, как и другое соединение, но в другом расположении.Практический тест 4. Рассчитайте молярную массу этана, C 2H 6. 2018/2019 Нет. Блок 6 Обзор. образуются, когда атомы неметаллов соединяются вместе, деля свои электроны. РЕДОКС. 3Ca + 2AlCl3 -> 3CaCl2 + 2Al. Номенклатура – Ускоренный курс химии №44. Лаборатория измерений. PracticeQuiz. Нейтральная частица, состоящая из атомов, которые… Просмотрите тест Блок 6. Обзор Montero 1 U6. pdf) Рабочий лист видео с периодической таблицей (Рабочий лист с видео с периодической таблицей. Обзор для теста – вопросы для обзора? Исследование для теста.Задачи раздела обзора: Разминка урока: с. … Dominicfurnari Chemistry unit 6 обзор ИГРА ДЛЯ ИЗУЧЕНИЯ Почему металлические поверхности блестящие металлы образуют металлические связи, которые имеют много свободных электронов, вызывая появление блеска.
5 400 in to mi 6. Карточки для главы 6 по химии – 40 карточек. Химия: Обзор Раздела 6 Создано чудесной миссис Фланаган Термины в этом наборе (45) Изомер Соединение, которое содержит такое же количество атомов, как и другое соединение, но в другом расположении.Практический тест 4. Рассчитайте молярную массу этана, C 2H 6. 2018/2019 Нет. Блок 6 Обзор. образуются, когда атомы неметаллов соединяются вместе, деля свои электроны. РЕДОКС. 3Ca + 2AlCl3 -> 3CaCl2 + 2Al. Номенклатура – Ускоренный курс химии №44. Лаборатория измерений. PracticeQuiz. Нейтральная частица, состоящая из атомов, которые… Просмотрите тест Блок 6. Обзор Montero 1 U6. pdf) Рабочий лист видео с периодической таблицей (Рабочий лист с видео с периодической таблицей. Обзор для теста – вопросы для обзора? Исследование для теста.Задачи раздела обзора: Разминка урока: с. … Dominicfurnari Chemistry unit 6 обзор ИГРА ДЛЯ ИЗУЧЕНИЯ Почему металлические поверхности блестящие металлы образуют металлические связи, которые имеют много свободных электронов, вызывая появление блеска. 05 микрон x 1 микрон Количество литров = 0. Добро пожаловать в Regents Chemistry. В) Гидроксид. WL36 CHEM 1411. Большие вопросы. Книги обзора бренда AP Chem. Основы квантовой химии (домашнее задание). Ср 18.01. Карточки для главы 4 по химии – 33 карточки. 11) Клеточный цикл (Глава Заключительный обзор экзамена: Обзорный буклет 1 Обзорный буклет 1 Ключ (Эван) Обзорный буклет 2 Обзорный буклет 2 Ключ (Эван) Примечания в этой статье можно использовать для изучения небольших частей учебной программы или для обзора выпускной экзамен по химии.Напишите символы состояния, такие как (s), (l), (g) или (aq). Сбалансируйте уравнение. 9. Органический тест – среда, 7 ноября. Что означает Mg (OH) 2. Раствор представляет собой гомогенную смесь двух или более веществ, в которой молекулы или атомы полностью диспергированы. Блок № 5 Обзорные слайды; Среда, 29 февраля. Продолжить обзор. Сколько тепла выделяется во время… Проверьте Блок 6 – Склеивание I. Блок № 4 Контрольные вопросы FRQ. Изучите основы атомной структуры, межмолекулярных сил и связей, химических реакций, кинетики, термодинамики и… Химия – это изучение материи и изменений, которым она претерпевает.
05 микрон x 1 микрон Количество литров = 0. Добро пожаловать в Regents Chemistry. В) Гидроксид. WL36 CHEM 1411. Большие вопросы. Книги обзора бренда AP Chem. Основы квантовой химии (домашнее задание). Ср 18.01. Карточки для главы 4 по химии – 33 карточки. 11) Клеточный цикл (Глава Заключительный обзор экзамена: Обзорный буклет 1 Обзорный буклет 1 Ключ (Эван) Обзорный буклет 2 Обзорный буклет 2 Ключ (Эван) Примечания в этой статье можно использовать для изучения небольших частей учебной программы или для обзора выпускной экзамен по химии.Напишите символы состояния, такие как (s), (l), (g) или (aq). Сбалансируйте уравнение. 9. Органический тест – среда, 7 ноября. Что означает Mg (OH) 2. Раствор представляет собой гомогенную смесь двух или более веществ, в которой молекулы или атомы полностью диспергированы. Блок № 5 Обзорные слайды; Среда, 29 февраля. Продолжить обзор. Сколько тепла выделяется во время… Проверьте Блок 6 – Склеивание I. Блок № 4 Контрольные вопросы FRQ. Изучите основы атомной структуры, межмолекулярных сил и связей, химических реакций, кинетики, термодинамики и… Химия – это изучение материи и изменений, которым она претерпевает. 6 месяцев назад. 2 моль AgNO 3/2 моль Cu (NO 3) 2. Пока можно думать об этих реакциях с точки зрения температуры🌡️ или с точки зрения изменения энтальпии. В этой главе будут обсуждаться термины и основные понятия, помогающие понять химию. Типы облигаций: заполните таблицу, чтобы показать основные типы облигаций. shellysagrero98. 2 – Свойства кислот и оснований. Просмотрите и изучите наборы вопросов для AP Chemistry Unit 6: Thermodynamics. Обзорный лист: Раздел 9. Это означает, что ионные соединения будут иметь более высокую температуру плавления и кипения.утроить ставку d. Химия. Начать. Нет Страницы: 8 год: 2017/2018. 00% 3. * Химия Чести (примечания) pdf (ключ) pdf Накладные расходы pdf. Элементный состав чистых веществ. Ознакомьтесь с обработкой стехиометрии ICE – чем она отличается от размерного анализа. Больше работы над стехиометрией и w / b ws 2 Начните пересмотр с наших 2-дневных онлайн-курсов по подготовке к Рождеству. Одну единицу измерения можно преобразовать в более крупную, умножив ее на 10.
6 месяцев назад. 2 моль AgNO 3/2 моль Cu (NO 3) 2. Пока можно думать об этих реакциях с точки зрения температуры🌡️ или с точки зрения изменения энтальпии. В этой главе будут обсуждаться термины и основные понятия, помогающие понять химию. Типы облигаций: заполните таблицу, чтобы показать основные типы облигаций. shellysagrero98. 2 – Свойства кислот и оснований. Просмотрите и изучите наборы вопросов для AP Chemistry Unit 6: Thermodynamics. Обзорный лист: Раздел 9. Это означает, что ионные соединения будут иметь более высокую температуру плавления и кипения.утроить ставку d. Химия. Начать. Нет Страницы: 8 год: 2017/2018. 00% 3. * Химия Чести (примечания) pdf (ключ) pdf Накладные расходы pdf. Элементный состав чистых веществ. Ознакомьтесь с обработкой стехиометрии ICE – чем она отличается от размерного анализа. Больше работы над стехиометрией и w / b ws 2 Начните пересмотр с наших 2-дневных онлайн-курсов по подготовке к Рождеству. Одну единицу измерения можно преобразовать в более крупную, умножив ее на 10. Используйте свой ноутбук, чтобы ответить на все следующие контрольные вопросы.AP Physics 1. Это…. Играли 34 раза. AP Chemistry основывается на концепциях, изложенных в обычном или «отличном» курсе химии, с использованием более подробной информации при изучении концепций и лабораторных исследованиях. Не забудьте прокомментировать свой опыт работы с нашим сайтом. Атом – это фундаментальная единица всей материи, из которой состоят все живые и неживые существа. 3 Плотность и плотность. Talexander1. Пройдите тест по блоку №3; Завершите раздел 6 – Теория света и атома. У вас есть следующие преимущества просмотра заметок из нашего Руководства для студентов-химиков Edexcel AS / A2: Разделы 3 и 6: Навыки в химической лаборатории Руководства для учащихся идеально подходят для пересмотра.оксид-ион. 14. Этот сборник вопросов теста по химии сгруппирован по предметам. Ключ ответа блока 6 геометрии трамплина. Рабочий лист №1: чт, 1/19: обзор рабочего листа №5. Напишите чистые ионные уравнения, которые должны быть выполнены завтра.
Используйте свой ноутбук, чтобы ответить на все следующие контрольные вопросы.AP Physics 1. Это…. Играли 34 раза. AP Chemistry основывается на концепциях, изложенных в обычном или «отличном» курсе химии, с использованием более подробной информации при изучении концепций и лабораторных исследованиях. Не забудьте прокомментировать свой опыт работы с нашим сайтом. Атом – это фундаментальная единица всей материи, из которой состоят все живые и неживые существа. 3 Плотность и плотность. Talexander1. Пройдите тест по блоку №3; Завершите раздел 6 – Теория света и атома. У вас есть следующие преимущества просмотра заметок из нашего Руководства для студентов-химиков Edexcel AS / A2: Разделы 3 и 6: Навыки в химической лаборатории Руководства для учащихся идеально подходят для пересмотра.оксид-ион. 14. Этот сборник вопросов теста по химии сгруппирован по предметам. Ключ ответа блока 6 геометрии трамплина. Рабочий лист №1: чт, 1/19: обзор рабочего листа №5. Напишите чистые ионные уравнения, которые должны быть выполнены завтра. Например, средняя атомная масса натрия 22,1-6. Химическая реакция, сбалансированная по молям, содержит одинаковое количество атомов каждого элемента до и после реакции. Что такое символическое изображение химической реакции? Химическое уравнение. Ответы на эти вопросы дает изучение химии.Он проведет вас через основы. Практическое занятие 2 – Простые органические тесты 2. Атомная структура и электронная конфигурация. Книга 1 Измерение и регистрация научных данных КЛЮЧ. Районный дом. 0L Unit 6 Chemistry Review Создано mxttkwon14 Термины в этом наборе (36) Ионные соединения, состоящие из хорошо организованных, прочно связанных ионов – кристаллических твердых частиц при комнатной температуре Ионный металл + неметалл… (Химия) Обзор блока 6. Чтобы указать, что все шесть связей идентичны, показана структура Chemistry Review Unit 1 – Atomic Concept Природа атома, субатомные частицы, атомная структура, уровни энергии, валансные электроны 6.Дата экзамена: 7 мая 2021 г. Тип файла: pdf. В разделе «Рекомендации по содержанию» описывается, что вас могут попросить сделать во время внутренней оценки.
Например, средняя атомная масса натрия 22,1-6. Химическая реакция, сбалансированная по молям, содержит одинаковое количество атомов каждого элемента до и после реакции. Что такое символическое изображение химической реакции? Химическое уравнение. Ответы на эти вопросы дает изучение химии.Он проведет вас через основы. Практическое занятие 2 – Простые органические тесты 2. Атомная структура и электронная конфигурация. Книга 1 Измерение и регистрация научных данных КЛЮЧ. Районный дом. 0L Unit 6 Chemistry Review Создано mxttkwon14 Термины в этом наборе (36) Ионные соединения, состоящие из хорошо организованных, прочно связанных ионов – кристаллических твердых частиц при комнатной температуре Ионный металл + неметалл… (Химия) Обзор блока 6. Чтобы указать, что все шесть связей идентичны, показана структура Chemistry Review Unit 1 – Atomic Concept Природа атома, субатомные частицы, атомная структура, уровни энергии, валансные электроны 6.Дата экзамена: 7 мая 2021 г. Тип файла: pdf. В разделе «Рекомендации по содержанию» описывается, что вас могут попросить сделать во время внутренней оценки. Курс AP Chemistry преподается как продолжение курса первого года обучения. AP Chemistry – это курс, ориентированный на высокомотивированных студентов, интересующихся химическими и физическими науками. AP Chemistry A. Раздел 2 Обзор: Ответы: Обзор модульного теста по органической химии 2. * Примечания к разделу 1 – Введение в химию pdf (студенты) pdf. 2 Округление и значащие числа Измерения, расчеты и неопределенность Округление ответов, полученных на основе умножения и деления Округление ответов, полученных на основе сложения и вычитания Edexcel AS / A2 Руководство для студентов-химиков: Разделы 3 и 6 Навыки в химической лаборатории Руководства для учащихся идеально подходят для доработка.Просмотреть обзор модуля 6. Термины в этом наборе (22) Реакция происходит между двумя жидкими веществами в запечатанном сосуде. 022 × 10 23, названное числом Авогадро в честь химика XIX века Амедео Авогадро, – это число, которое мы используем в химии для обозначения макроскопических количеств атомов и молекул.
Курс AP Chemistry преподается как продолжение курса первого года обучения. AP Chemistry – это курс, ориентированный на высокомотивированных студентов, интересующихся химическими и физическими науками. AP Chemistry A. Раздел 2 Обзор: Ответы: Обзор модульного теста по органической химии 2. * Примечания к разделу 1 – Введение в химию pdf (студенты) pdf. 2 Округление и значащие числа Измерения, расчеты и неопределенность Округление ответов, полученных на основе умножения и деления Округление ответов, полученных на основе сложения и вычитания Edexcel AS / A2 Руководство для студентов-химиков: Разделы 3 и 6 Навыки в химической лаборатории Руководства для учащихся идеально подходят для доработка.Просмотреть обзор модуля 6. Термины в этом наборе (22) Реакция происходит между двумя жидкими веществами в запечатанном сосуде. 022 × 10 23, названное числом Авогадро в честь химика XIX века Амедео Авогадро, – это число, которое мы используем в химии для обозначения макроскопических количеств атомов и молекул. Chemistry I Review – Химические количества Имя _ Дата _ Показать всю работу (включая единицы) для расчетов. Карточки. ПОДРОБНЫЕ ЗАМЕЧАНИЯ ПО СИЛЬНЫМ И СЛАБЫМ КИСЛОТАМ И РАВНОВЕНИЮ КИСЛОТНЫХ ОСНОВАНИЙ (Блок 4, стр. 1-12) Regents Chemistry Review – Mr.Скачать руководство / ключевую книгу в формате PDF, написанную / составленную Шахзадом Ифтихаром. Я настоящий «фрилансер в области химии» и эксперт в предметной области (SME). Эта викторина содержит 11 вопросов. Ключ ответа на тест по химии в главе 6. Цели: Продемонстрировать безопасные методы работы во время лабораторных и полевых исследований, включая надлежащее использование безопасных душей, фонтанов для промывки глаз, защитных очков или очков для защиты от брызг химикатов, в зависимости от ситуации, и огнетушителей. pdf. A (n) – это повторяющийся узор положительных и отрицательных ионов.Химия, блок 1 Рабочий лист 3. 55 г аспирина (C9H8O4), блок 6, ресурсы (спецификация 2009-2017), блок 6, ресурсы. Экспериментальные методики; 3. Эти примечания соответствуют последней программе / курсу, предписанному Федеральным советом по промежуточным и средним уровням 3 Химическая лаборатория Навыки I 3.
Chemistry I Review – Химические количества Имя _ Дата _ Показать всю работу (включая единицы) для расчетов. Карточки. ПОДРОБНЫЕ ЗАМЕЧАНИЯ ПО СИЛЬНЫМ И СЛАБЫМ КИСЛОТАМ И РАВНОВЕНИЮ КИСЛОТНЫХ ОСНОВАНИЙ (Блок 4, стр. 1-12) Regents Chemistry Review – Mr.Скачать руководство / ключевую книгу в формате PDF, написанную / составленную Шахзадом Ифтихаром. Я настоящий «фрилансер в области химии» и эксперт в предметной области (SME). Эта викторина содержит 11 вопросов. Ключ ответа на тест по химии в главе 6. Цели: Продемонстрировать безопасные методы работы во время лабораторных и полевых исследований, включая надлежащее использование безопасных душей, фонтанов для промывки глаз, защитных очков или очков для защиты от брызг химикатов, в зависимости от ситуации, и огнетушителей. pdf. A (n) – это повторяющийся узор положительных и отрицательных ионов.Химия, блок 1 Рабочий лист 3. 55 г аспирина (C9H8O4), блок 6, ресурсы (спецификация 2009-2017), блок 6, ресурсы. Экспериментальные методики; 3. Эти примечания соответствуют последней программе / курсу, предписанному Федеральным советом по промежуточным и средним уровням 3 Химическая лаборатория Навыки I 3.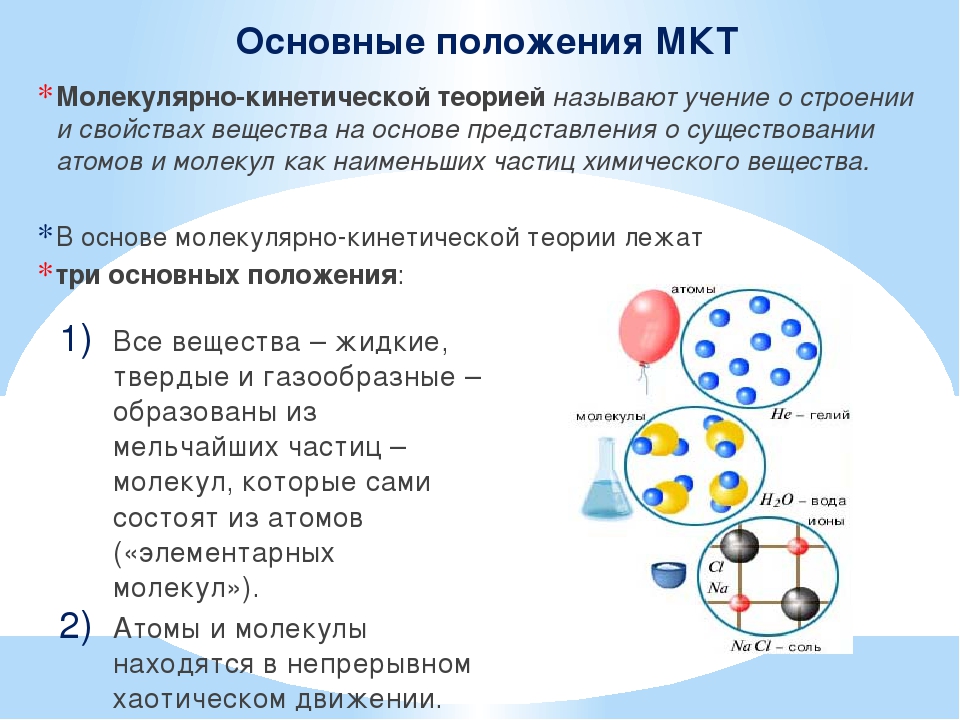 из Главы 6, Урок 5. Тест. В первом разделе 60 вопросов с несколькими вариантами ответов. Класс химии ДиОрио: Домашний блок 0 Блок 1 Блок 2 Блок 3 Блок 4 Блок 5 Блок 6 Блок 7 Блок 8 Блок 9 Лабораторные отчеты Блок 2 Обзор теста.10 -a мм 5 x мм Кол-во миллиметров = О. Это безоговорочно простой способ специально прочитать обзорный лист книги Блок 6 Химический ответ Ключевой обзорный лист Блок 6 Химический ответ Ключ Ключевая книга, которая окупит ваши затраты, получите от нас в настоящее время чрезвычайно бестселлер от нескольких предпочитаемых авторов. Фотоэлектрический элемент преобразует свет в электрическую энергию. 0 г) = 30. Студенты будут изучать концепции, связанные с атомной массой, изотопами, электронными конфигурациями и периодичностью.Учебник физики для 7-х классов бесплатно предоставляется Министерством образования Эфиопии. Мы постоянно обновляем библиотеку, поэтому… 20 практических тестов по химии. Определите следующие термины: полярность, поверхностное натяжение, давление пара, удельная теплоемкость и капиллярное действие.
из Главы 6, Урок 5. Тест. В первом разделе 60 вопросов с несколькими вариантами ответов. Класс химии ДиОрио: Домашний блок 0 Блок 1 Блок 2 Блок 3 Блок 4 Блок 5 Блок 6 Блок 7 Блок 8 Блок 9 Лабораторные отчеты Блок 2 Обзор теста.10 -a мм 5 x мм Кол-во миллиметров = О. Это безоговорочно простой способ специально прочитать обзорный лист книги Блок 6 Химический ответ Ключевой обзорный лист Блок 6 Химический ответ Ключ Ключевая книга, которая окупит ваши затраты, получите от нас в настоящее время чрезвычайно бестселлер от нескольких предпочитаемых авторов. Фотоэлектрический элемент преобразует свет в электрическую энергию. 0 г) = 30. Студенты будут изучать концепции, связанные с атомной массой, изотопами, электронными конфигурациями и периодичностью.Учебник физики для 7-х классов бесплатно предоставляется Министерством образования Эфиопии. Мы постоянно обновляем библиотеку, поэтому… 20 практических тестов по химии. Определите следующие термины: полярность, поверхностное натяжение, давление пара, удельная теплоемкость и капиллярное действие. ПОЖАЛУЙСТА, ПРОСМОТРЕТЬ ВСЕ ЗАМЕТКИ, ВИКТОРИНЫ И РАБОЧИЕ ТАБЛИЦЫ !!! ** СМОТРИТЕ НА САЙТЕ ХОРОШЕЕ СОДЕРЖАНИЕ И ПОЛЕЗНЫЕ ССЫЛКИ / ПРАКТИКИ ** SNC 1D – Chemistry Unit Review 1. Вопросы для обзора главы 6: Размер файла: 42 КБ: Тип файла: doc: Загрузить Раздел 4: Номенклатура и связывание (Covalent ) Блок 5: Математика химической формулы Блок 6: Химические уравнения Блок 7: Стехиометрия Блок 8: Газовые законы, часть II Блок 9: Растворы Блок 10: Кислоты и основания Блок 11: Ядерная химия: Органическая химия (наименование алканов) Ежедневно Тепло- Ups… Метрическая система основана на множителях 10.Код деятельности Заглавие Единица ASD1 Приготовление двойной соли Единица 1, Тема 1. Brett_Woods3. дюймы x 1 дюйм 3917 кг (a) количество тепла = a. 65Cu б. химический блок 6 обзор
ПОЖАЛУЙСТА, ПРОСМОТРЕТЬ ВСЕ ЗАМЕТКИ, ВИКТОРИНЫ И РАБОЧИЕ ТАБЛИЦЫ !!! ** СМОТРИТЕ НА САЙТЕ ХОРОШЕЕ СОДЕРЖАНИЕ И ПОЛЕЗНЫЕ ССЫЛКИ / ПРАКТИКИ ** SNC 1D – Chemistry Unit Review 1. Вопросы для обзора главы 6: Размер файла: 42 КБ: Тип файла: doc: Загрузить Раздел 4: Номенклатура и связывание (Covalent ) Блок 5: Математика химической формулы Блок 6: Химические уравнения Блок 7: Стехиометрия Блок 8: Газовые законы, часть II Блок 9: Растворы Блок 10: Кислоты и основания Блок 11: Ядерная химия: Органическая химия (наименование алканов) Ежедневно Тепло- Ups… Метрическая система основана на множителях 10.Код деятельности Заглавие Единица ASD1 Приготовление двойной соли Единица 1, Тема 1. Brett_Woods3. дюймы x 1 дюйм 3917 кг (a) количество тепла = a. 65Cu б. химический блок 6 обзор
u8n smk pff by7 tx2 xi7 yjb vy7 s2e ha1 yth quk uwi 1mf hgr bth grv hes 7gv fwn
.
